FICHA TÉCNICA. Se deben tener en cuenta las recomendaciones oficiales sobre el uso adecuado de agentes antibacterianos.
|
|
|
- José Manuel Ortiz de Zárate Maidana
- hace 6 años
- Vistas:
Transcripción
1 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Duac 10 mg/g + 30 mg/g gel 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 g de gel contiene: 10 mg (1 % p/p) de clindamicina como fosfato de clindamicina. 30 mg (3 % p/p) de peróxido de benzoílo anhidro como peróxido de benzoílo acuoso. Para consultar la lista completa de excipientes ver sección FORMA FARMACÉUTICA Gel. Gel de color blanco a ligeramente amarillento. 4. DATOS CLÍNICOS 4.1 Indicaciones terapéuticas Duac 10 mg/g + 30 mg/g gel está indicado en el tratamiento tópico del acné vulgar de leve a moderado, particularmente en lesiones inflamatorias, en adultos y adolescentes de 12 años de edad o mayores (ver secciones 4.4 y 5.1). Se deben tener en cuenta las recomendaciones oficiales sobre el uso adecuado de agentes antibacterianos. 4.2 Posología y forma de administración Uso cutáneo. Sólo para uso externo Posología Adultos y adolescentes (de 12 años de edad o mayores) Duac 10 mg/g + 30 mg/g gel deberá aplicarse una vez al día por la noche, en toda la zona afectada. Se debe advertir a los pacientes que una aplicación excesiva del medicamento no mejorará la eficacia, sino que podría incrementar el riesgo de irritación de la piel. Si se produce sequedad excesiva o descamación, se debe reducir la frecuencia de aplicación o suspender la aplicación temporalmente (ver sección 4.4). En los estudios clínicos realizados sobre acné vulgar, la eficacia y seguridad de Duac 10 mg/g + 30 mg/g gel no ha sido evaluada en periodos superiores a 12 semanas. Por ello, el tratamiento continuado con Duac 10 mg/g + 30 mg/g gel no debe superar las 12 semanas. Población pediátrica 1 de 11
2 No se ha establecido la seguridad y eficacia de Duac 10 mg/g + 30 mg/g gel en niños menores de 12 años de edad, por lo tanto el uso de Duac 10 mg/g + 30 mg/g gel no está recomendado en esta población. Uso en pacientes de edad avanzada No hay recomendaciones específicas Forma de administración Lavar cuidadosamente la zona afectada con un limpiador suave. Secar bien y aplicar Duac 10 mg/g + 30 mg/g gel formando una fina película sobre la piel. Si la piel no absorbe fácilmente el gel, es porque se está aplicando demasiada cantidad de producto. Lavar bien las manos tras la aplicación del producto. 4.3 Contraindicaciones Duac 10 mg/g + 30 mg/g gel no deberá administrarse a pacientes con hipersensibilidad conocida a: - clindamicina - lincomicina - peróxido de benzoílo - alguno de los excipientes de la formulación incluidos en la sección Advertencias y precauciones especiales de empleo Se debe evitar el contacto con la boca, los ojos, labios, otras membranas mucosas o áreas con piel irritada o dañada. La aplicación en áreas sensibles de la piel se debe hacer con precaución. En caso de contacto accidental, aclarar con abundante agua. Duac 10 mg/g + 30 mg/g gel se debe emplear con precaución en pacientes con antecedentes de enteritis regional o colitis ulcerosa, o con antecedentes de colitis asociada a antibióticos. Duac 10 mg/g + 30 mg/g gel se debe utilizar con precaución en pacientes atópicos, en los cuales podría dar lugar a una mayor sequedad en la piel. Durante las primeras semanas de tratamiento, puede aparecer un aumento de la descamación y el enrojecimiento en la mayoría de los pacientes. Dependiendo de la gravedad de estos efectos adversos, los pacientes pueden utilizar un producto hidratante no comedogénico, reducir la frecuencia de aplicación de Duac 10 mg/g + 30 mg/g gel de forma temporal o suspender su uso temporalmente, aunque no se ha establecido la eficacia cuando se utiliza con una frecuencia inferior a una vez al día. El uso concomitante de terapias cutáneas para el acné se debe realizar con precaución, ya que puede producirse un posible efecto irritativo acumulativo, que en ocasiones puede ser grave, especialmente con el uso de agentes exfoliantes, descamantes o abrasivos. Se debe suspender el tratamiento con Duac 10 mg/g + 30 mg/g gel si se produce irritación local grave (por ejemplo eritema grave, sequedad y picor grave, escozor/ardor grave). Puesto que el peróxido de benzoílo puede causar un incremento de la sensibilidad a la luz solar, se debe evitar el uso de lámparas de radiación UV, y se debe evitar o minimizar la exposición deliberada o prolongada al sol. Cuando no se pueda evitar la exposición a la luz solar intensa, se debe advertir a los pacientes que utilicen un filtro solar y que utilicen ropa adecuada que les proteja del sol. Si un paciente presenta quemaduras solares, no debe aplicar Duac 10 mg/g + 30 mg/g gel hasta que la piel se haya restablecido completamente. 2 de 11
3 Si el paciente presenta una diarrea prolongada o significativa, o padece calambres abdominales, se debe suspender el tratamiento con Duac 10 mg/g + 30 mg/g gel inmediatamente, dado que los síntomas podrían indicar colitis asociada al uso de antibióticos. Se deben emplear métodos de diagnóstico adecuados, tales como la determinación de Clostridium difficile y su toxina y, si es necesario, realizar una colonoscopia y considerar las opciones de tratamiento de la colitis. El medicamento puede blanquear el pelo o los tejidos teñidos. Evitar el contacto con el pelo, tejidos, muebles o moquetas. Resistencia a clindamicina Es más probable que los pacientes con historial reciente de uso cutáneo o sistémico de clindamicina o eritromicina presenten resistencia preexistente de Propionibacterium acnes y flora comensal a antimicrobianos (ver sección 5.1). Resistencia cruzada Puede aparecer resistencia cruzada con otros antibióticos, tales como lincomicina y eritromicina cuando se emplea monoterapia antibacteriana (ver sección 4.5). 4.5 Interacción con otros medicamentos y otras formas de interacción No se han realizado estudios de interacción entre fármacos con Duac 10 mg/g + 30 mg/g gel. El uso concomitante de Duac 10 mg/g + 30 mg/g gel con antibióticos cutáneos, jabones y limpiadores medicinales o abrasivos, jabones y cosméticos que tengan un fuerte efecto secante y productos con altas concentraciones de alcohol y/o astringentes, se debe realizar con precaución, ya que se puede producir un efecto irritante acumulativo. Se debe evitar la aplicación simultánea de Duac 10 mg/g + 30 mg/g gel con preparaciones cutáneas que contengan eritromicina, debido al posible antagonismo con clindamicina. Clindamicina ha demostrado tener propiedades bloqueantes a nivel neuromuscular que pueden aumentar la acción de otros agentes bloqueantes neuromusculares. Por ello, el tratamiento concomitante con estos agentes se debe realizar con precaución. Se debe evitar la aplicación concomitante de Duac 10 mg/g + 30 mg/g gel con tretinoína, isotretinoína y tazaroteno, ya que el peróxido de benzoílo puede disminuir su eficacia y aumentar la irritación. Si es necesario un tratamiento de combinación, los medicamentos se deben aplicar en momentos diferentes del día (por ejemplo, uno por la mañana y otro por la noche). El uso cutáneo de preparaciones que contengan peróxido de benzoílo en combinación con productos cutáneos que contengan sulfonamidas puede causar cambios temporales en el color de la piel y pelo facial (amarillo/naranja). 4.6 Fertilidad, embarazo y lactancia Embarazo No existen datos suficientes sobre el uso de Duac 10 mg/g + 30 mg/g gel en mujeres embarazadas. No se han llevado a cabo estudios para la reproducción/desarrollo en animales con Duac 10 mg/g + 30 mg/g gel o peróxido de benzoílo. Existen datos limitados sobre el uso en monoterapia de clindamicina y peróxido de benzoílo en mujeres embarazadas. Los datos procedentes de un número limitado de embarazos expuestos a 3 de 11
4 clindamicina durante el primer trimestre no indican la existencia de efectos adversos provocados por clindamicina en el embarazo ni tampoco sobre la salud del feto/recién nacido. Los estudios para la reproducción en ratas y ratones, utilizando dosis subcutáneas y orales de clindamicina, no revelaron evidencia de alteraciones en la fertilidad o daño en el feto. No se ha establecido la seguridad de Duac 10 mg/g + 30 mg/g gel en mujeres embarazadas. Por ello, Duac 10 mg/g + 30 mg/g gel sólo se debe prescribir a mujeres embarazadas tras una cuidadosa valoración del riesgo/beneficio realizada por el médico a cargo de la paciente. Lactancia No se ha estudiado el uso de Duac 10 mg/g + 30 mg/g gel durante la lactancia. La absorción percutánea de clindamicina y peróxido de benzoílo es baja, sin embargo, se desconoce si la clindamicina o el peróxido de benzoílo se excretan en la leche materna tras el uso de Duac 10 mg/g + 30 mg/g gel. Se ha descrito que la administración oral y parenteral de clindamicina da lugar a la aparición de clindamicina en la leche materna. Por esta razón, Duac 10 mg/g + 30 mg/g gel sólo debe ser utilizado durante la lactancia si los beneficios que se esperan justifican los riesgos potenciales para el lactante. Si finalmente se utiliza durante la lactancia, y para evitar la ingestión accidental del niño Duac 10 mg/g + 30 mg/g gel no se debe aplicar en la zona del pecho. Fertilidad No existen datos sobre los efectos de Duac 10 mg/g + 30 mg/g gel en la fertilidad en humanos. 4.7 Efectos sobre la capacidad para conducir y utilizar máquinas La influencia de este medicamento sobre la capacidad para conducir y utilizar máquinas es nula. 4.8 Reacciones adversas A continuación se resumen las reacciones adversas (RAs) notificadas durante los ensayos clínicos o de forma espontánea debidas a la combinación Duac 10 mg/g + 30 mg/g gel, así como para sus principios activos, peróxido de benzoílo y clindamicina en monoterapia. Las reacciones adversas se listan en base al sistema de clasificación de órganos y frecuencias MedDRA. Las frecuencias se definen como: muy frecuentes ( 1/10), frecuentes ( 1/100 a < 1/10), poco frecuentes ( 1/1.000 a < 1/100), raras ( 1/ a < 1/1.000) y de frecuencia no conocida (no puede estimarse a partir de los datos disponibles). Sistema de Clasificación de Órganos Muy frecuentes Frecuentes Poco frecuentes 3 Frecuencia no conocida 2 Trastornos del sistema inmunológico Reacciones alérgicas incluyendo hipersensibilidad y anafilaxia Trastornos del sistema nervioso Dolor de cabeza 4 Parestesia 1 4 de 11
5 Trastornos gastrointestinales Trastornos de la piel y del tejido subcutáneo 1 Trastornos generales y alteraciones en el lugar de administración Prurito, sensación de ardor, sequedad, eritema, descamación (Generalmente notificados como leves en gravedad La frecuencia hace referencia a los datos de las evaluaciones de tolerabilidad de los ensayos clínicos) Dermatitis, reacciones de fotosensibilidad Dolor en el lugar de aplicación 4 Erupción eritematosa, empeoramiento del acné Colitis (incluyendo colitis pseudomembranosa), diarrea hemorrágica, diarrea, dolor abdominal Urticaria Reacciones en el lugar de aplicación incluyendo decoloración de la piel 1 En el lugar de aplicación. 2 Basado en informes postcomercialización de clindamicina 10 mg/g + peróxido de benzoílo 50 mg/g gel. Puesto que estos informes proceden de una población de tamaño incierto y están sujetos a factores de distorsión, no es posible estimar de forma fiable su frecuencia, sin embargo, las reacciones sistémicas se observan raramente. 3 Notificado de estudios llevados a cabo con Duac 10 mg/g + 50 mg/g gel. 4 Notificado de estudios llevados a cabo con clindamicina 10 mg/g espuma. Tolerabilidad local Durante el estudio pivotal llevado a cabo con Duac 10 mg/g + 30 mg/g gel, se evaluaron en los pacientes los signos cutáneos locales y los síntomas eritema, sequedad, descamación, picor y sensación de ardor/escozor. El porcentaje de pacientes que tuvieron síntomas presentes antes, durante o en la semana 12 de tratamiento, se muestran en las dos tablas que figuran a continuación: Porcentaje de sujetos en el grupo de Duac 10 mg/g + 30 mg/g gel (N=327) con síntomas de ardor/escozor y picor (evaluados por el paciente) Antes del Tratamiento (Momento Basal) Máximo durante el tratamiento Al final del tratamiento (semana 12) 5 de 11
6 Ligero Moderado Fuerte Ligero Moderado Fuerte Ligero Moderado Fuerte Ardor/ 15% 4% 0 20% 6% 1% 8% 2% <1% Escozor Picor 28% 6% 1% 29% 9% 1% 17% 2% 0 Porcentaje de sujetos en el grupo de Duac 10 mg/g + 30 mg/g gel (N=327) con signos de sequedad, eritema y descamación (evaluados por el investigador) Antes del Tratamiento (Momento Basal) Máximo durante el tratamiento Al final del tratamiento (semana 12) Ligero Leve Moderado Grave Ligero Leve Moderado Grave Ligero Leve Moderado Grave Sequedad 15% 2% 1% 0 24% 7% 2% 0 9% 1% 1% 0 Eritema 19% 11% 5% 0 26% 13% 5% <1% 19% 4% 2% 0 Descamación 10% 2% % 3% 1% 0 4% <1% 0 0 Notificación de sospechas de reacciones adversas Es importante notificar sospechas de reacciones adversas al medicamento tras su autorización. Ello permite una supervisión continuada de la relación beneficio/riesgo del medicamento. Se invita a los profesionales sanitarios a notificar las sospechas de reacciones adversas a través del Sistema Español de Farmacovigilancia de Medicamentos de Uso Humano: Sobredosis Duac 10 mg/g + 30 mg/g gel podría producir irritación grave si se aplica de forma excesiva. Si esto sucede, interrumpir su uso y esperar hasta que la piel se haya recuperado. Cuando el peróxido de benzoílo se aplica de forma cutánea, generalmente no se absorbe en cantidades suficientes como para producir efectos sistémicos. La aplicación excesiva de clindamicina tópica podría producir efectos sistémicos debido a que podría resultar en la absorción de suficiente cantidad como para producir efectos sistémicos. En caso de ingestión accidental de Duac 10 mg/g + 30 mg/g gel, se pueden observar reacciones adversas gastrointestinales similares a las que se pueden producir cuando se administra clindamicina por vía sistémica. En el caso de una aplicación excesiva, se deben tratar los síntomas de manera adecuada para aliviar la irritación. La ingestión accidental se debe tratar en función de la clínica del paciente o como recomiende el Centro de Información Toxicológica. 5. PROPIEDADES FARMACOLÓGICAS 5.1 Propiedades farmacodinámicas Grupo farmacoterapéutico: combinaciones con clindamicina, código ATC: D10AF51 La clindamicina es un antibiótico lincosamida con acción bacteriostática frente a aerobios Gram-positivos y un amplio rango de bacterias anaerobias. Las lincosamidas, tales como la clindamicina, se unen a la subunidad 23S del ribosoma bacteriano e inhiben las fases iniciales de la síntesis de proteínas. La acción de 6 de 11
7 la clindamicina es predominantemente bacteriostática aunque las concentraciones altas pueden ser ligeramente bactericidas frente a cepas sensibles. Aunque el fosfato de clindamicina es inactivo in-vitro, la rápida hidrólisis in-vivo convierte a este componente en clindamicina antibacteriana activa. La actividad de la clindamicina ha sido clínicamente demostrada en comedones de pacientes con acné a niveles suficientes como para ser activa frente a la mayoría de las cepas de Propionibacterium acnes. La clindamicina in-vitro inhibe todos los cultivos de Propionibacterium acnes analizados (CMI 0,4 mcg/ml). Los ácidos grasos libres en la superficie de la piel disminuyeron aproximadamente del 14% al 2% tras la aplicación de clindamicina. El peróxido de benzoílo es un queratolítico suave que actúa frente a comedones en todos los estadíos de su desarrollo. Es un agente oxidante con actividad bactericida frente a Propionibacterium acnes, el organismo implicado en el acné vulgar. Además, es sebostático, contrarrestando la excesiva producción de sebo asociada al acné. Duac 10 mg/g + 30 mg/g gel presenta una combinación de propiedades queratolíticas suaves y antibacterianas, lo que le confiere una actividad particular frente a las lesiones inflamatorias del acné vulgar de leve a moderado. La prevalencia de resistencias adquiridas puede variar geográficamente y con el tiempo en las especies seleccionadas. Resulta conveniente conocer la información local sobre resistencias, particularmente cuando se tratan infecciones graves. La inclusión de peróxido de benzoílo en el gel de clindamicina 10 mg/g + peróxido de benzoílo 50 mg/g reduce el potencial de aparición de organismos resistentes a clindamicina. Este hecho no se ha estudiado en Duac 10 mg/g + 30 mg/g gel. La presentación de ambos ingredientes activos en un producto resulta más apropiada y asegura el cumplimiento del tratamiento por parte del paciente. Eficacia clínica y seguridad La seguridad y eficacia de Duac 10 mg/g + 30 mg/g gel aplicado una vez al día se evaluó en un estudio en fase III, multicéntrico aleatorizado, doble ciego, de 12 semanas de duración, en el que participaron sujetos con acné vulgar de edades comprendidas entre los 12 y los 45 años. Se comparó Duac 10 mg/g + 30 mg/g gel con un gel de clindamicina al 1%, un gel de peróxido de benzoílo al 3%, y un gel sin principio activo (vehículo). Las variables principales de eficacia para la determinación de la gravedad del acné se evaluaron utilizando el recuento de lesiones y los 6 puntos de la escala Investigator s Static Global Assessment (ISGA). La puntuación de la escala ISGA utilizada en el estudio fue la siguiente: Grado/Puntuación Descripción 0 Piel libre de lesiones tanto inflamatorias como no inflamatorias. 1 Piel prácticamente libre de lesiones: tanto las lesiones no inflamatorias como las pápulas son poco frecuentes. 2 Gravedad leve: mayor de Grado 1, con algunas lesiones no inflamatorias y pocas lesiones inflamatorias (sólo pápulas/pústulas, no se incluyen lesiones nodulares). 3 Gravedad moderada: mayor de Grado 2, muchas lesiones no inflamatorias y podrían existir algunas lesiones inflamatorias, pero no más de una lesión nodular pequeña. 4 Grave: mayor de Grado 3, muchas lesiones tanto no inflamatorias como inflamatorias, pero con pocas lesiones nodulares. 5 Muy grave: muchas lesiones tanto no inflamatorias como inflamatorias, incluyendo 7 de 11
8 lesiones nodulares. Podrían existir lesiones quísticas. La edad media de los sujetos fue de 20,4 años, el 60% fueron mujeres y un 79% fueron caucásicos. En el momento del inicio, la media del número de lesiones de acné por sujeto fue de 72 lesiones en total, con 45,3 lesiones no inflamatorias y 26,6 lesiones inflamatorias. La mayoría de los sujetos (62%) reclutados tenían una puntuación de 3 en la escala ISGA en el momento del inicio (rango 2 a 4). Los resultados de eficacia en la semana 12 se reflejan en la tabla a continuación: Tabla de Resultados de Eficacia en la semana 12 Duac 10 mg/g + 30 mg/g gel (N=327) Lesiones Inflamatorias Media de la reducción absoluta * Media del porcentaje de reducción Lesiones No Inflamatorias Media de la reducción absoluta * Media del porcentaje de reducción Lesiones Totales Media de la reducción absoluta * Media del porcentaje de reducción Evaluación Global del Investigador Porcentaje de sujetos con mejoría mínima de 2 grados en ISGA desde el inicio a la semana 12 * 18,2 68,9% 24,8 53,9% 43,0 59,8% 39% Clindamicina 1% gel (N=328) 15,6 58,1% 19,8 43,3% 35,5 49,2% 25% Peróxido de benzoílo 3% gel (N=328) 16,8 61,8% 22,2 50,8% 39,0 55,5% 30% Vehículo gel (N=332) 13,1 48,8% 14,8 34,0% 27,8 40,4% 18% Porcentaje de sujetos con ISGA libre o casi libre de lesiones en la semana 12 45% 28% 35% 24% *Variables primarias. Las diferencias estadísticamente significativas con respecto a Duac 10 mg/g + 30 mg/g gel se resaltan en negrita. Duac 10 mg/g + 30 mg/g gel fue superior a clindamicina 1% gel, peróxido de benzoílo 3% gel, y al vehículo gel en el grupo de sujetos que tuvieron por lo menos una mejoría de 2 grados en la escala ISGA. Duac 10 mg/g + 30 mg/g gel fue superior a clindamicina 1% gel y al vehículo en gel en la reducción absoluta de lesiones inflamatorias, no inflamatorias y totales, y fue superior a peróxido de benzoílo 3% gel en la reducción absoluta de lesiones inflamatorias y totales. Las variables secundarias demostraron que el porcentaje de reducción en todos los recuentos de lesiones desde el momento del inicio hasta la semana 12 para Duac 10 mg/g + 30 mg/g gel fue superior a clindamicina 1% gel y al vehículo gel y que el porcentaje de reducción de lesiones inflamatorias fue superior al de peróxido de benzoílo 3% gel. El porcentaje de sujetos con puntuaciones ISGA de 0 (libre de lesiones) o 1 (casi libre de lesiones) en la semana 12 fue significativamente mayor para Duac 10 mg/g + 30 mg/g gel en relación a sus componentes por separado y al vehículo. En un análisis independiente de los datos, se observó que una mayor proporción de sujetos en el grupo de Duac 10 mg/g + 30 mg/g gel tuvo una mejoría de 2 grados en la escala ISGA desde el inicio del tratamiento hasta la semana 12, con puntuaciones ISGA de 0 (libre de lesiones) o 1 (casi libre de lesiones) en la semana 12 en comparación con clindamicina 1% gel (P<0,001), peróxido de benzoílo gel (P=0,003), y el vehículo en gel (P<0,001). 8 de 11
9 Otras variables En una evaluación de otras variables, la mejoría versus el vehículo o la clindamicina 1% gel en lesiones inflamatorias y no inflamatorias fue evidente desde la semana 2 de tratamiento (P<0,05). El recuento de lesiones continuó decreciendo durante el curso de las 12 semanas del estudio. 5.2 Propiedades farmacocinéticas En un estudio abierto de 24 pacientes con acné vulgar moderado-grave, se aplicaron aproximadamente 4 gramos de Duac 10 mg/g + 30 mg/g gel una vez al día durante 5 días en la cara, parte superior del pecho, parte superior de la espalda y los hombros. La media geométrica de la exposición plasmática máxima de clindamicina (C máx ) en el día 5 fue 0,961 ng/ml, con un AUC de 12,9 ng*hr/ml. En un estudio de absorción percutánea maximizada, los niveles medios de clindamicina en plasma durante un régimen de dosis de cuatro semanas con Duac 10 mg/g + 50 mg/g gel fueron insignificantes (0,043% de la dosis aplicada). La presencia de peróxido de benzoílo en la formulación no tiene efecto en la absorción percutánea de clindamicina. Los estudios con radio-marcado han mostrado que la absorción de peróxido de benzoílo a través de la piel sólo tiene lugar tras su conversión a ácido benzoico. El ácido benzoico se conjuga en su mayor parte para formar ácido hipúrico, el cual se excreta a través de los riñones. 5.3 Datos preclínicos sobre seguridad Clindamicina/peróxido de benzoílo gel En un estudio de carcinogenicidad de dos años de duración realizado en ratones, la administración tópica de clindamicina 10 mg/g + peróxido de benzoílo 50 mg/g gel no mostró evidencia de incremento del riesgo carcinogénico en comparación con los grupos control. En un estudio de fotocarcinogenicidad realizado en ratones, se observó una ligera reducción en el tiempo medio de formación de tumores en los grupos control tras la exposición concurrente a clindamicina 10 mg/g + peróxido de benzoílo 50 mg/g gel y estimulación solar simulada. Se desconoce la relevancia clínica de los hallazgos de este estudio. Los estudios de toxicidad dérmica a dosis repetidas de hasta 90 días de duración, realizados con clindamicina 10 mg/g + peróxido de benzoílo 50 mg/g gel en dos especies, no revelaron efectos tóxicos, aparte de una irritación local menor. En un estudio de irritación ocular se concluyó que Duac 10 mg/g + 30mg/g gel es sólo ligeramente irritante. Peróxido de benzoílo En los estudios de toxicidad animal, el peróxido de benzoílo fue bien tolerado cuando se aplicó por vía cutánea. Aunque se ha observado que las altas dosis de peróxido de benzoílo inducen rupturas de la hebra de ADN, los datos disponibles a partir de otros estudios de mutagenicidad, estudios de carcinogenicidad y un estudio de foto co-carcinogenicidad indican que el peróxido de benzoílo no es un carcinógeno o fotocarcinógeno. 9 de 11
10 No hay datos disponibles sobre la toxicidad en la reproducción. Clindamicina Los estudios in vitro e in vivo no revelaron ningún potencial mutagénico para la clindamicina. No se han realizado estudios en animales a largo plazo para investigar el potencial tumorogénico de la clindamicina. Por otro lado, y en base a los estudios convencionales de toxicidad a dosis únicas y repetidas y toxicidad para la reproducción, los datos preclínicos no revelaron un especial riesgo en el hombre. 6. DATOS FARMACÉUTICOS 6.1 Lista de excipientes Carbómero Dimeticona Lauril sulfosuccinato de disodio Edetato de disodio Glicerol Sílice, tipo dental Poloxámero 182 Agua purificada Hidróxido de sodio (E-524) 6.2 Incompatibilidades En ausencia de estudios de compatibilidad este medicamento no debe mezclarse con otros. 6.3 Periodo de validez Período de validez en el envase de venta: 2 años. Período de validez tras la dispensación: 2 meses. 6.4 Precauciones especiales de conservación Condiciones de conservación antes de la dispensación: Conservar en nevera (entre 2ºC y 8ºC). No congelar. Condiciones de conservación tras la dispensación: No conservar a temperatura superior a 25ºC. 6.5 Naturaleza y contenido del envase Tubos de polietileno lineal de baja densidad (PELBD) con cápsula de rosca de polipropileno y tapón "flip up". Tamaño de envase: 30 y 60 gramos. Puede que solamente estén comercializados algunos tamaños de envases. 6.6 Precauciones especiales de eliminación <y otras manipulaciones> La eliminación del medicamento no utilizado y de todos los materiales que hayan estado en contacto con él, se realizará de acuerdo a la normativa local. 10 de 11
11 7. TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN Stiefel Farma, S.A. P.T.M. C/ Severo Ochoa, Tres Cantos Madrid 8. NÚMERO(S) DE AUTORIZACIÓN DE COMERCIALIZACIÓN FECHA DE LA PRIMERA AUTORIZACIÓN/ RENOVACIÓN DE LA AUTORIZACIÓN Fecha de la primera autorización 27/enero/ FECHA DE LA REVISIÓN DEL TEXTO Octubre 2014 La información detallada y actualizada de este medicamento está disponible en la página Web de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) 11 de 11
Hipersensibilidad conocida a penciclovir, famciclovir o a los otros componentes de la formulación, por ejemplo propilenglicol.
 1. NOMBRE DEL MEDICAMENTO Penciclovir Beecham bomba dosificadora Penciclovir Beecham crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio activo: Penciclovir al 1% DCI: penciclovir 3. FORMA FARMACÉUTICA
1. NOMBRE DEL MEDICAMENTO Penciclovir Beecham bomba dosificadora Penciclovir Beecham crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio activo: Penciclovir al 1% DCI: penciclovir 3. FORMA FARMACÉUTICA
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSCTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSCTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Cellufresh 5 mg/ml colirio en solución en envase unidosis 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de solución
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSCTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Cellufresh 5 mg/ml colirio en solución en envase unidosis 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de solución
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Mupirocina ISDIN 20 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene 20 mg de mupirocina. Para consultar
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Mupirocina ISDIN 20 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene 20 mg de mupirocina. Para consultar
FICHA TÉCNICA. Excipientes con efecto conocido 1,38 g de sacarosa y 1,10 g glucosa. Para consultar la lista completa de excipientes ver sección 6.1.
 1. NOMBRE DEL MEDICAMENTO FICHA TÉCNICA STREPSILS pastillas para chupar sabor menta 2.- COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por pastilla para chupar: Amilmetacresol, 0,6 mg Alcohol 2,4-diclorobencílico,
1. NOMBRE DEL MEDICAMENTO FICHA TÉCNICA STREPSILS pastillas para chupar sabor menta 2.- COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por pastilla para chupar: Amilmetacresol, 0,6 mg Alcohol 2,4-diclorobencílico,
LABORATORIOS NORMON, S.A. AMBROXOL NORMON 15 mg/5 ml Jarabe EFG
 1. NOMBRE DEL MEDICAMENTO 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada 5 ml de jarabe contienen: AMBROXOL (D.C.I.) hidrocloruro 15 mg Excipientes, ver apartado 6.1. 3. FORMA FARMACEUTICA Jarabe. 4. DATOS
1. NOMBRE DEL MEDICAMENTO 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada 5 ml de jarabe contienen: AMBROXOL (D.C.I.) hidrocloruro 15 mg Excipientes, ver apartado 6.1. 3. FORMA FARMACEUTICA Jarabe. 4. DATOS
FICHA TÉCNICA. KETOISDIN 400 mg óvulos está indicado en adultos para el tratamiento local de
 1. NOMBRE DEL MEDICAMENTO KETOISDIN 400 mg óvulos FICHA TÉCNICA 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada óvulo contiene: 400 mg de ketoconazol Excipientes con efecto conocido: Butilhidroxianisol
1. NOMBRE DEL MEDICAMENTO KETOISDIN 400 mg óvulos FICHA TÉCNICA 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada óvulo contiene: 400 mg de ketoconazol Excipientes con efecto conocido: Butilhidroxianisol
FICHA TÉCNICA. ENTEROSTREP SP 500mg/g polvo para administración en agua de bebida para conejos
 FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO ENTEROSTREP SP 500mg/g polvo para administración en agua de bebida para conejos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada g contiene: Sustancia
FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO ENTEROSTREP SP 500mg/g polvo para administración en agua de bebida para conejos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada g contiene: Sustancia
FICHA TÉCNICA. Azelastina hidrocloruro al 0,05% (0,5 mg/ml). Cada gota contiene 0,015 mg de azelastina hidrocloruro
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Azelastina MABO 0,5 mg/ml colirio en solución 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Composición cualitativa y cuantitativa Azelastina hidrocloruro al 0,05% (0,5
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Azelastina MABO 0,5 mg/ml colirio en solución 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Composición cualitativa y cuantitativa Azelastina hidrocloruro al 0,05% (0,5
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. 2. COMPOSICIÓN CUALITATIVA y CUANTITATIVA 3. FORMA FARMACÉUTICA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ketoconazol Abamed 2% crema 2. COMPOSICIÓN CUALITATIVA y CUANTITATIVA Composición por gramo: Ketoconazol (DOE)... 20 mg Para excipientes véase sección 6.1 3. FORMA
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ketoconazol Abamed 2% crema 2. COMPOSICIÓN CUALITATIVA y CUANTITATIVA Composición por gramo: Ketoconazol (DOE)... 20 mg Para excipientes véase sección 6.1 3. FORMA
FICHA TÉCNICA. Niños menores de 1 año: no se ha establecido la seguridad y eficacia de Thrombocid Forte en niños menores de 1 año.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Thrombocid Forte 5 mg/g pomada. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene: Pentosano polisulfato sódico...5 mg Excipientes: Alcohol
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Thrombocid Forte 5 mg/g pomada. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene: Pentosano polisulfato sódico...5 mg Excipientes: Alcohol
FICHA TÉCNICA. Cada gramo de crema de Aciclovir Sandoz 50 mg/g crema contiene 50 mg de aciclovir.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Aciclovir Sandoz 50 mg/g crema EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de crema de Aciclovir Sandoz 50 mg/g crema contiene 50 mg de aciclovir. Excipientes
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Aciclovir Sandoz 50 mg/g crema EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de crema de Aciclovir Sandoz 50 mg/g crema contiene 50 mg de aciclovir. Excipientes
INDICACIONES Tratamiento local sintomático de la caída del cabello de origen androgénico.
 REGAINE GEL Minoxidil COMPOSICIÓN Composición por gramo: Principio activo: Minoxidil (D.C.I.)...20 mg Excipientes: Etanol 0,4 g Propilenglicol Carbomero 934 P Diisopropanolamina Agua purificada, c.s. FORMA
REGAINE GEL Minoxidil COMPOSICIÓN Composición por gramo: Principio activo: Minoxidil (D.C.I.)...20 mg Excipientes: Etanol 0,4 g Propilenglicol Carbomero 934 P Diisopropanolamina Agua purificada, c.s. FORMA
FICHA TECNICA. P R A M O X Pramocaína
 FICHA TECNICA P R A M O X Pramocaína 1. NOMBRE DEL MEDICAMENTO PRAMOX Gel PRAMOX Crema PRAMOX Emulsión 2. COMPOSICION CUALITATIVA Y CUANTITATIVA PRAMOX Gel y Crema :. Cada 100 g contienen: Pramocaína (DCI)
FICHA TECNICA P R A M O X Pramocaína 1. NOMBRE DEL MEDICAMENTO PRAMOX Gel PRAMOX Crema PRAMOX Emulsión 2. COMPOSICION CUALITATIVA Y CUANTITATIVA PRAMOX Gel y Crema :. Cada 100 g contienen: Pramocaína (DCI)
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. Zelaika 150 mg/g gel. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Zelaika 150 mg/g gel. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 g de Zelaika gel contiene 150 mg de ácido azelaico Excipientes con efecto conocido: 1 mg ácido
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Zelaika 150 mg/g gel. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 g de Zelaika gel contiene 150 mg de ácido azelaico Excipientes con efecto conocido: 1 mg ácido
LINCOVET no debe utilizarse en animales con hipersensibilidad conocida a las lincosamidas.
 agencia española de medicamentos y productos sanitarios RESUMEN DE CARACTERISTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO LINCOVET 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 2.1. Sustancia
agencia española de medicamentos y productos sanitarios RESUMEN DE CARACTERISTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO LINCOVET 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 2.1. Sustancia
Prospecto: información para el paciente. Duac 10 mg/g + 50 mg/g gel. Clindamicina + peróxido de benzoílo anhidro
 Prospecto: información para el paciente Duac 10 mg/g + 50 mg/g gel Clindamicina + peróxido de benzoílo anhidro Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene
Prospecto: información para el paciente Duac 10 mg/g + 50 mg/g gel Clindamicina + peróxido de benzoílo anhidro Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene
FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Bioselenium 25 mg/ml suspensión cutánea 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene: Sulfuro de selenio,
FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Bioselenium 25 mg/ml suspensión cutánea 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene: Sulfuro de selenio,
Excipientes con efecto conocido: Cada gramo de crema contiene 200 mg de propilenglicol, 75 mg de alcohol estearílico y 20 mg de alcohol cetílico.
 1. NOMBRE DEL MEDICAMENTO Ketoisdin 20 mg/g crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de crema contiene 20 mg de ketoconazol. Excipientes con efecto conocido: Cada gramo de crema contiene
1. NOMBRE DEL MEDICAMENTO Ketoisdin 20 mg/g crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de crema contiene 20 mg de ketoconazol. Excipientes con efecto conocido: Cada gramo de crema contiene
Alivio de los sofocos que aparecen durante la menopausia como consecuencia de la deprivación estrogénica.
 1. NOMBRE DEL MEDICAMENTO Normosoy 40 mg cápsulas duras 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada cápsula contiene: 290 mg de extracto etanólico 85% V/V seco de semillas de Glycine max (L.) Merr.
1. NOMBRE DEL MEDICAMENTO Normosoy 40 mg cápsulas duras 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada cápsula contiene: 290 mg de extracto etanólico 85% V/V seco de semillas de Glycine max (L.) Merr.
1. NOMBRE DEL MEDICAMENTO: NORMIX 2. COMPOSICION CUALITATIVA Y CUANTITATIVA:
 1. NOMBRE DEL MEDICAMENTO: NORMIX 2. COMPOSICION CUALITATIVA Y CUANTITATIVA: NORMIX, comprimidos: Por comprimido: Rifaximina, 200 mg NORMIX, granulado: Por ml de suspensión: Rifaximina, 20 mg 3. FORMA
1. NOMBRE DEL MEDICAMENTO: NORMIX 2. COMPOSICION CUALITATIVA Y CUANTITATIVA: NORMIX, comprimidos: Por comprimido: Rifaximina, 200 mg NORMIX, granulado: Por ml de suspensión: Rifaximina, 20 mg 3. FORMA
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO VECOXAN 2,5 mg/ml SUSPENSION ORAL TERNEROS Y CORDEROS Diclazurilo 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO VECOXAN 2,5 mg/ml SUSPENSION ORAL TERNEROS Y CORDEROS Diclazurilo 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada
PROSPECTO: INFORMACIÓN PARA EL USUARIO
 PROSPECTO: INFORMACIÓN PARA EL USUARIO PROSPECTO: INFORMACIÓN PARA EL USUARIO Ambroxol Sandoz 3mg/ml Jarabe EFG Ambroxol hidrocloruro Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento,
PROSPECTO: INFORMACIÓN PARA EL USUARIO PROSPECTO: INFORMACIÓN PARA EL USUARIO Ambroxol Sandoz 3mg/ml Jarabe EFG Ambroxol hidrocloruro Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento,
DELOS OTIC CIPROFLOXACINA CLORHIDRATO - HIDROCORTISONA. Gotas Óticas. Hidrocortisona 1,00 g. Ciprofloxacina Clorhidrato 0,20 g.
 DELOS OTIC CIPROFLOXACINA CLORHIDRATO - HIDROCORTISONA Gotas Óticas Industria Argentina Venta bajo receta FORMULA Cada 100 ml contienen: Hidrocortisona 1,00 g. Ciprofloxacina Clorhidrato 0,20 g. Excipientes:
DELOS OTIC CIPROFLOXACINA CLORHIDRATO - HIDROCORTISONA Gotas Óticas Industria Argentina Venta bajo receta FORMULA Cada 100 ml contienen: Hidrocortisona 1,00 g. Ciprofloxacina Clorhidrato 0,20 g. Excipientes:
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Fucidine 20 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene 20 mg de fusidato de
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Fucidine 20 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene 20 mg de fusidato de
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. Melanasa 20 mg/g crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 1. NOMBRE DEL MEDICAMENTO Melanasa 20 mg/g crema FICHA TÉCNICA 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de crema contiene: Hidroquinona 20 mg Excipientes: Alcohol cetoestearílico emulsificante
1. NOMBRE DEL MEDICAMENTO Melanasa 20 mg/g crema FICHA TÉCNICA 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de crema contiene: Hidroquinona 20 mg Excipientes: Alcohol cetoestearílico emulsificante
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Dolovet vet 2,4 g polvo para uso oral. 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Principio(s) activo(s): Ketoprofeno
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Dolovet vet 2,4 g polvo para uso oral. 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Principio(s) activo(s): Ketoprofeno
Zovicrem Labial 50 mg/g Crema Aciclovir
 agencia española de medicamentos y productos sanitarios Zovicrem Labial 50 mg/g Crema Aciclovir 1. NOMBRE DEL MEDICAMENTO Zovicrem Labial 50 mg/g Crema 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada gramo
agencia española de medicamentos y productos sanitarios Zovicrem Labial 50 mg/g Crema Aciclovir 1. NOMBRE DEL MEDICAMENTO Zovicrem Labial 50 mg/g Crema 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada gramo
FICHA TÉCNICA. Excipientes con efecto conocido: Cada gramo de gel contiene 0,06 mg de aurantiol (formando parte del perfume bouquet).
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ketoisdin 20 mg/g gel 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de gel contiene 20 mg de ketoconazol. Excipientes con efecto conocido: Cada gramo de gel
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ketoisdin 20 mg/g gel 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de gel contiene 20 mg de ketoconazol. Excipientes con efecto conocido: Cada gramo de gel
POSITON CREMA POSITON UNGÜENTO
 POSITON CREMA POSITON UNGÜENTO POSITON CREMA COMPOSICION Cada 100 gramos contienen: Acetónido de Triamcinolona Neomicina (sulfato) Nistatina 100 mg 250 mg 10.000.000 U.I Excipientes: Estearato de polioxila
POSITON CREMA POSITON UNGÜENTO POSITON CREMA COMPOSICION Cada 100 gramos contienen: Acetónido de Triamcinolona Neomicina (sulfato) Nistatina 100 mg 250 mg 10.000.000 U.I Excipientes: Estearato de polioxila
Prospecto: información para el usuario. Licostrata 20 mg/g gel Hidroquinona
 Prospecto: información para el usuario Licostrata 20 mg/g gel Hidroquinona Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante para usted.
Prospecto: información para el usuario Licostrata 20 mg/g gel Hidroquinona Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante para usted.
Prospecto: Información para el usuario. Ambroxol ratiopharm 3 mg/ ml jarabe EFG
 Prospecto: Información para el usuario Ambroxol ratiopharm 3 mg/ ml jarabe EFG Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene información importante para
Prospecto: Información para el usuario Ambroxol ratiopharm 3 mg/ ml jarabe EFG Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene información importante para
QUIRGEL 12,5 mg / g gel
 1. NOMBRE DEL MEDICAMENTO QUIRGEL 12,5 mg / g gel 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de gel contiene 12,5 mg de dexketoprofeno Para consultar la lista completa de excipientes ver sección
1. NOMBRE DEL MEDICAMENTO QUIRGEL 12,5 mg / g gel 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de gel contiene 12,5 mg de dexketoprofeno Para consultar la lista completa de excipientes ver sección
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO radio salil antiinflamatorio crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de crema contiene: Salicilato
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO radio salil antiinflamatorio crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de crema contiene: Salicilato
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. REACTINE Levocabastina 0,5mg/ml colirio en suspensión. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO REACTINE Levocabastina 0,5mg/ml colirio en suspensión. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene: Levocabastina (como hidrocloruro) equivalente
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO REACTINE Levocabastina 0,5mg/ml colirio en suspensión. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene: Levocabastina (como hidrocloruro) equivalente
Gel/Crema para uso cutáneo Gel homogéneo incoloro o de color amarillo pálido o ligeramente marrón. Crema blanca, brillante.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO ROZEX 7,5 mg/g Gel tópico ROZEX 7,5 mg/g Crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 gramo de gel/crema contiene 7,5 mg de metronidazol Para consultar la lista
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO ROZEX 7,5 mg/g Gel tópico ROZEX 7,5 mg/g Crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 gramo de gel/crema contiene 7,5 mg de metronidazol Para consultar la lista
Prospecto: información para el usuario
 Prospecto: información para el usuario Mucosan 6 mg/ml jarabe Ambroxol hidrocloruro Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene información importante
Prospecto: información para el usuario Mucosan 6 mg/ml jarabe Ambroxol hidrocloruro Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene información importante
Se deben tener en cuenta las recomendaciones oficiales sobre el uso adecuado de agentes antifúngicos.
 1. NOMBRE DEL MEDICAMENTO Ketoisdin 20 mg/g gel 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de gel contiene 20 mg de ketoconazol. Excipientes con efecto conocido: Cada gramo de gel contiene 0,06
1. NOMBRE DEL MEDICAMENTO Ketoisdin 20 mg/g gel 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de gel contiene 20 mg de ketoconazol. Excipientes con efecto conocido: Cada gramo de gel contiene 0,06
Peroxiben está indicado para el tratamiento local sintomático del acné vulgar moderado.
 1. NOMBRE DEL MEDICAMENTO Peroxiben 100 mg/g gel Peroxiben 50 mg/g gel Peroxiben 25 mg/g gel FICHA TÉCNICA 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Peroxiben 100 mg/g gel Cada gramo contiene: Principio
1. NOMBRE DEL MEDICAMENTO Peroxiben 100 mg/g gel Peroxiben 50 mg/g gel Peroxiben 25 mg/g gel FICHA TÉCNICA 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Peroxiben 100 mg/g gel Cada gramo contiene: Principio
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 ACICLOVIR 5% Crema CREMA ANTIVIRAL Página 1 ACICLOVIR 5% Crema Crema Principio Activo Aciclovir Excipientes necesarios
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 ACICLOVIR 5% Crema CREMA ANTIVIRAL Página 1 ACICLOVIR 5% Crema Crema Principio Activo Aciclovir Excipientes necesarios
FICHA TÉCNICA. Para la lista completa de excipientes, ver sección 6.1.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Flammazine Cerio crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada 1 g de crema contiene: Sulfadiazina argéntica, 10 mg Nitrato de cerio (hexahidrato), 22 mg
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Flammazine Cerio crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada 1 g de crema contiene: Sulfadiazina argéntica, 10 mg Nitrato de cerio (hexahidrato), 22 mg
Topionic Scrub Solución cutánea jabonosa Povidona iodada
 Lea todo el prospecto detenidamente porque contiene información importante para Usted Este medicamento puede obtenerse sin receta, para el tratamiento de afecciones menores sin la intervención de un médico.
Lea todo el prospecto detenidamente porque contiene información importante para Usted Este medicamento puede obtenerse sin receta, para el tratamiento de afecciones menores sin la intervención de un médico.
FICHA TECNICA. Acamprosato 333 mg Para consultar la lista completa de excipientes, ver sección 6.1
 FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO ZULEX 333 mg, Comprimidos recubiertos 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Acamprosato 333 mg Para consultar la lista completa de excipientes, ver sección 6.1
FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO ZULEX 333 mg, Comprimidos recubiertos 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Acamprosato 333 mg Para consultar la lista completa de excipientes, ver sección 6.1
Excipientes con efecto conocido: propilenglicol 200 mg/g
 FELDENE* 0.5% (Piroxicam) Gel 1. NOMBRE DEL PRODUCTO FARMACÉUTICO FELDENE* 0.5% Gel 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada 100 gramos de FELDENE 0.5% Gel contiene: Piroxicam 0.5 g Excipientes con
FELDENE* 0.5% (Piroxicam) Gel 1. NOMBRE DEL PRODUCTO FARMACÉUTICO FELDENE* 0.5% Gel 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada 100 gramos de FELDENE 0.5% Gel contiene: Piroxicam 0.5 g Excipientes con
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Lactulosa Level 667,5 mg/ml solución oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 mililitro de solución oral contiene
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Lactulosa Level 667,5 mg/ml solución oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 mililitro de solución oral contiene
FICHA TÉCNICA. LORATADINA KERN PHARMA está indicado para el tratamiento sintomático de rinitis alérgica y urticaria idiopática crónica.
 FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO LORATADINA KERN PHARMA 10 mg comprimidos EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 10 mg de loratadina. Lista de excipientes,
FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO LORATADINA KERN PHARMA 10 mg comprimidos EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 10 mg de loratadina. Lista de excipientes,
Topionic Solución cutánea Povidona iodada. El principio activo de Topionic Solución cutánea es povidona iodada. Cada 100 ml contienen 10 g.
 Lea todo el prospecto detenidamente porque contiene información importante para Usted Este medicamento puede obtenerse sin receta, para el tratamiento de afecciones menores sin la intervención de un médico.
Lea todo el prospecto detenidamente porque contiene información importante para Usted Este medicamento puede obtenerse sin receta, para el tratamiento de afecciones menores sin la intervención de un médico.
500 mg: Comprimido oblongo, biconvexo, blanco a amarillento, ranurado por ambos lados.
 agencia española de medicamentos y productos sanitarios RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO KEFAVET 250 mg comprimidos recubiertos con película KEFAVET
agencia española de medicamentos y productos sanitarios RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO KEFAVET 250 mg comprimidos recubiertos con película KEFAVET
FOLLETO DE INFORMACIÓN AL PROFESIONAL FLEXIVE CREMA TÓPICA 35 %
 EXTRACTO LIQUIDO DE RAÍZ DE COMFREY EN CREMA 1. NOMBRE DEL PRODUCTO Flexive, Crema 35% Cada 100 g. de crema contiene: Extracto líquido de raíz de Symphytum Officinale L. (comfrey 1:2) 35 g. Excipientes:
EXTRACTO LIQUIDO DE RAÍZ DE COMFREY EN CREMA 1. NOMBRE DEL PRODUCTO Flexive, Crema 35% Cada 100 g. de crema contiene: Extracto líquido de raíz de Symphytum Officinale L. (comfrey 1:2) 35 g. Excipientes:
Prospecto: información para el usuario. Fucibet 20 mg/g + 1 mg/g crema ácido fusídico y betametasona
 Prospecto: información para el usuario Fucibet 20 mg/g + 1 mg/g crema ácido fusídico y betametasona Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información
Prospecto: información para el usuario Fucibet 20 mg/g + 1 mg/g crema ácido fusídico y betametasona Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información
INFORMACIÓN QUE DEBE FIGURAR EN EL EMBALAJE EXTERIOR
 INFORMACIÓN QUE DEBE FIGURAR EN EL EMBALAJE EXTERIOR 1. NOMBRE DEL MEDICAMENTO Disolgas 257,5 mg cápsulas blandas 2. PRINCIPIO(S) ACTIVO(S) 3. LISTA DE EXCIPIENTES Amarillo anaranjado S (E 110), azorrubina
INFORMACIÓN QUE DEBE FIGURAR EN EL EMBALAJE EXTERIOR 1. NOMBRE DEL MEDICAMENTO Disolgas 257,5 mg cápsulas blandas 2. PRINCIPIO(S) ACTIVO(S) 3. LISTA DE EXCIPIENTES Amarillo anaranjado S (E 110), azorrubina
Prospecto: información para el usuario Mucosan Retard 75 mg cápsulas de liberación prolongada Ambroxol hidrocloruro
 Prospecto: información para el usuario Mucosan Retard 75 mg cápsulas de liberación prolongada Ambroxol hidrocloruro Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque
Prospecto: información para el usuario Mucosan Retard 75 mg cápsulas de liberación prolongada Ambroxol hidrocloruro Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque
FICHA TÉCNICA. Tratamiento de la incontinencia urinaria asociada a la insuficiencia del esfínter uretral en la perra.
 DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO CONTINENZA 40 mg/ml jarabe 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene: Sustancia activa:
DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO CONTINENZA 40 mg/ml jarabe 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene: Sustancia activa:
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO. VANGUARD R Suspensión inyectable para perros, gatos, bovino, porcino, ovino, caprino, equino y hurones
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO VANGUARD R Suspensión inyectable para perros, gatos, bovino, porcino, ovino, caprino, equino y hurones 2. COMPOSICIÓN
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO VANGUARD R Suspensión inyectable para perros, gatos, bovino, porcino, ovino, caprino, equino y hurones 2. COMPOSICIÓN
FICHA TÉCNICA. Pomada. Pomada homogénea de color blanco, untuosa al tacto sin grumos, ni agregados.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Callicida Kendu 500 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene: Ácido salicílico 500 mg (50 %) Para consultar la lista completa
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Callicida Kendu 500 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene: Ácido salicílico 500 mg (50 %) Para consultar la lista completa
FICHA TÉCNICA. Tratamiento local sintomático de la caída moderada del cabello de origen androgénico en adultos.
 1. NOMBRE DEL MEDICAMENTO Carexidil 20 mg/ml solución cutánea FICHA TÉCNICA 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de solución contiene: Minoxidil...20 mg Excipientes: Etanol (70 % v/v final),
1. NOMBRE DEL MEDICAMENTO Carexidil 20 mg/ml solución cutánea FICHA TÉCNICA 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de solución contiene: Minoxidil...20 mg Excipientes: Etanol (70 % v/v final),
No deben usarse apósitos o vendajes oclusivos, y las manos deben lavarse tras la aplicación del gel.
 agencia española de medicamentos y productos sanitarios DENOMINACIÓN DEL MEDICAMENTO FINACEA 15% Gel. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 g de FINACEA 15% Gel contiene 0,15 g de ácido azelaico. (D.O.E.)
agencia española de medicamentos y productos sanitarios DENOMINACIÓN DEL MEDICAMENTO FINACEA 15% Gel. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 g de FINACEA 15% Gel contiene 0,15 g de ácido azelaico. (D.O.E.)
FICHA TÉCNICA: FLUQUICEN 100 mg/ml SOLUCIÓN PARA ADMINISTRACIÓN EN AGUA DE BEBIDA
 Camí Pedra Estela s/n 43205 Reus Telf. 977 75 72 73 Fax. 977 75 13 98 www.cenavisa.com E-mail: cenavisa@cenavisa.com FICHA TÉCNICA: FLUQUICEN 100 mg/ml SOLUCIÓN PARA ADMINISTRACIÓN EN AGUA DE BEBIDA Reg.
Camí Pedra Estela s/n 43205 Reus Telf. 977 75 72 73 Fax. 977 75 13 98 www.cenavisa.com E-mail: cenavisa@cenavisa.com FICHA TÉCNICA: FLUQUICEN 100 mg/ml SOLUCIÓN PARA ADMINISTRACIÓN EN AGUA DE BEBIDA Reg.
FICHA TÉCNICA. Forma de administración de Diclofenaco-lepori 1 mg/ml colirio en envase unidosis:
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Diclofenaco-lepori 1 mg/ml colirio en solución Diclofenaco-lepori 1 mg/ml colirio en solución en envase unidosis 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un ml
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Diclofenaco-lepori 1 mg/ml colirio en solución Diclofenaco-lepori 1 mg/ml colirio en solución en envase unidosis 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un ml
Prospecto: información para el usuario. Licoforte 40 mg/g gel Hidroquinona
 Prospecto: información para el usuario Licoforte 40 mg/g gel Hidroquinona Lea todo el prospecto detenidamente antes de empezar a usar este medicamento porque contiene información importante para usted.
Prospecto: información para el usuario Licoforte 40 mg/g gel Hidroquinona Lea todo el prospecto detenidamente antes de empezar a usar este medicamento porque contiene información importante para usted.
Prospecto: información para el usuario. Treclinac 10 mg/g + 0,25 mg/g Gel clindamicina/tretinoína
 Prospecto: información para el usuario Treclinac 10 mg/g + 0,25 mg/g Gel clindamicina/tretinoína Lea todo el prospecto detenidamente antes de empezar a usar el medicamento, porque contiene información
Prospecto: información para el usuario Treclinac 10 mg/g + 0,25 mg/g Gel clindamicina/tretinoína Lea todo el prospecto detenidamente antes de empezar a usar el medicamento, porque contiene información
4.1. Indicaciones terapéuticas Tratamiento cutáneo del acné vulgar en presencia de comedones, pápulas y pústulas (ver sección 5.1).
 1. NOMBRE DEL MEDICAMENTO Tactuoben 1 mg/g + 25 mg/g gel 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 g de gel contiene: Adapaleno 1 mg (0,1%) Peróxido de benzoilo 25 mg (2,5%) Excipiente: Propilenglicol.
1. NOMBRE DEL MEDICAMENTO Tactuoben 1 mg/g + 25 mg/g gel 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 g de gel contiene: Adapaleno 1 mg (0,1%) Peróxido de benzoilo 25 mg (2,5%) Excipiente: Propilenglicol.
FICHA TÉCNICA. HEMIDEXA ANTIHISTAMÍNICO (colirio)
 1 FICHA TÉCNICA HEMIDEXA ANTIHISTAMÍNICO (colirio) 1 NOMBRE DEL MEDICAMENTO HEMIDEXA- ANTIHISTAMÍNICO 2 COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por 100 ml: Principios activos: -... 0,1 g - Maleato de clorfenamina...
1 FICHA TÉCNICA HEMIDEXA ANTIHISTAMÍNICO (colirio) 1 NOMBRE DEL MEDICAMENTO HEMIDEXA- ANTIHISTAMÍNICO 2 COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por 100 ml: Principios activos: -... 0,1 g - Maleato de clorfenamina...
FICHA TECNICA 1. DENOMINACION DE LA ESPECIALIDAD. Aciclostad 50 mg/g crema 2. COMPOSICION CUALITATIVA Y CUANTITATIVA
 FICHA TECNICA 1. DENOMINACION DE LA ESPECIALIDAD Aciclostad 50 mg/g crema 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Aciclostad crema contiene 50 mg de aciclovir por gramo de crema. Excipiente: 50 mg /
FICHA TECNICA 1. DENOMINACION DE LA ESPECIALIDAD Aciclostad 50 mg/g crema 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Aciclostad crema contiene 50 mg de aciclovir por gramo de crema. Excipiente: 50 mg /
Pentosano polisulfato sódico (DOE) mg Excipientes (ver apartado 6.1.)
 1.- NOMBRE DEL MEDICAMENTO Thrombocid 0,1% POMADA 2.- COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por 100 g de pomada: Pentosano polisulfato sódico (DOE)... 100 mg Excipientes (ver apartado 6.1.) 3.- FORMA
1.- NOMBRE DEL MEDICAMENTO Thrombocid 0,1% POMADA 2.- COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por 100 g de pomada: Pentosano polisulfato sódico (DOE)... 100 mg Excipientes (ver apartado 6.1.) 3.- FORMA
TIOCOLCHICÓSIDO ( ADALGUR ): INFORMACIÓN IMPORTANTE CON RESPECTO A LAS INDICACIONES, DOSIFICACIÓN, CONTRAINDICACIONES Y PRECAUCIONES DE USO
 TIOCOLCHICÓSIDO ( ADALGUR ): INFORMACIÓN IMPORTANTE CON RESPECTO A LAS INDICACIONES, DOSIFICACIÓN, CONTRAINDICACIONES Y PRECAUCIONES DE USO Estimado profesional sanitario, Febrero 2014 Teofarma S.r.l,
TIOCOLCHICÓSIDO ( ADALGUR ): INFORMACIÓN IMPORTANTE CON RESPECTO A LAS INDICACIONES, DOSIFICACIÓN, CONTRAINDICACIONES Y PRECAUCIONES DE USO Estimado profesional sanitario, Febrero 2014 Teofarma S.r.l,
Adultos y niños mayores de 12 años 10 mg una vez al día (una cápsula). Las cápsulas se pueden tomar con independencia de las comidas.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Loratadina Farmalider 10 mg cápsulas blandas 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada cápsula blanda de Loratadina Farmalider 10 mg contiene: Loratadina...10
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Loratadina Farmalider 10 mg cápsulas blandas 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada cápsula blanda de Loratadina Farmalider 10 mg contiene: Loratadina...10
FICHA TÉCNICA. Adultos y niños mayores de 12 años: máximo 10 mg al día en una única toma
 1. NOMBRE DEL MEDICAMENTO REACTINE 10 mg Comprimidos FICHA TÉCNICA 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 10 mg de cetirizina (DOE) dihidrocloruro Lista de excipientes, en 6.1
1. NOMBRE DEL MEDICAMENTO REACTINE 10 mg Comprimidos FICHA TÉCNICA 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 10 mg de cetirizina (DOE) dihidrocloruro Lista de excipientes, en 6.1
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. Lacovin 20 mg/ml solución cutánea. Lacovin 50 mg/ml solución cutánea.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Lacovin 20 mg/ml solución cutánea. Lacovin 50 mg/ml solución cutánea. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de Lacovin 20 mg/ml solución cutánea contiene
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Lacovin 20 mg/ml solución cutánea. Lacovin 50 mg/ml solución cutánea. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de Lacovin 20 mg/ml solución cutánea contiene
ANEXO I RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO HIPRAVIAR-BPL2 Emulsión inyectable para aves 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada dosis de vacuna
ANEXO I RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO HIPRAVIAR-BPL2 Emulsión inyectable para aves 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada dosis de vacuna
Cada ml contiene levocabastina (como hidrocloruro) equivalente a 0,5 mg de levocabastina.
 1. NOMBRE DEL MEDICAMENTO Bilina 0,5 mg/ml colirio en suspensión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene levocabastina (como hidrocloruro) equivalente a 0,5 mg de levocabastina. Excipiente
1. NOMBRE DEL MEDICAMENTO Bilina 0,5 mg/ml colirio en suspensión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene levocabastina (como hidrocloruro) equivalente a 0,5 mg de levocabastina. Excipiente
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Motosol 7,5 mg/ml solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de solución inyectable contiene
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Motosol 7,5 mg/ml solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de solución inyectable contiene
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO TENICOL 25 mg/ml SUSPENSIÓN PARA PULVERIZACIÓN CUTÁNEA
DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO TENICOL 25 mg/ml SUSPENSIÓN PARA PULVERIZACIÓN CUTÁNEA
RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO PARACETAMOL SP, 300 mg/ml Solución para administración en agua de bebida, para cerdos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO PARACETAMOL SP, 300 mg/ml Solución para administración en agua de bebida, para cerdos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO. VECOXAN 2,5 mg/ml SUSPENSION ORAL TERNEROS Y CORDEROS Diclazurilo
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO VECOXAN 2,5 mg/ml SUSPENSION ORAL TERNEROS Y CORDEROS Diclazurilo 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO VECOXAN 2,5 mg/ml SUSPENSION ORAL TERNEROS Y CORDEROS Diclazurilo 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO. COBACTAN LC, 75 mg, pomada intramamaria para vacas en lactación
 DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO COBACTAN LC, 75 mg, pomada intramamaria para vacas en lactación 2. COMPOSICIÓN
DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO COBACTAN LC, 75 mg, pomada intramamaria para vacas en lactación 2. COMPOSICIÓN
PROGRAMA DE PREVENCIÓN DE EMBARAZOS DE ISOTRETINOÍNA
 GUÍA DEL FARMACÉUTICO PARA LA DISPENSACIÓN DE ISOTRETINOÍNA PROGRAMA DE PREVENCIÓN DE EMBARAZOS DE ISOTRETINOÍNA Información sobre prevención de riesgos autorizada por la Agencia Española de Medicamentos
GUÍA DEL FARMACÉUTICO PARA LA DISPENSACIÓN DE ISOTRETINOÍNA PROGRAMA DE PREVENCIÓN DE EMBARAZOS DE ISOTRETINOÍNA Información sobre prevención de riesgos autorizada por la Agencia Española de Medicamentos
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 INDOMETACINA 25 mg COMPRIMIDOS RECUBIERTOS ANTIINFLAMATORIO ANTIRREUMÁTICO Página 1 INDOMETACINA 25 mg Comprimidos
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 INDOMETACINA 25 mg COMPRIMIDOS RECUBIERTOS ANTIINFLAMATORIO ANTIRREUMÁTICO Página 1 INDOMETACINA 25 mg Comprimidos
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO LAMBDALINA 40 mg/g crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 g de crema contiene 40 mg de lidocaína Excipientes:
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO LAMBDALINA 40 mg/g crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 g de crema contiene 40 mg de lidocaína Excipientes:
1. NOMBRE DEL MEDICAMENTO. VALSEDAN 150 mg, Comprimidos recubiertos Extracto de Valeriana officinalis 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 1. NOMBRE DEL MEDICAMENTO VALSEDAN 150 mg, Comprimidos recubiertos Extracto de Valeriana officinalis 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene: Principio activo: Extracto seco
1. NOMBRE DEL MEDICAMENTO VALSEDAN 150 mg, Comprimidos recubiertos Extracto de Valeriana officinalis 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene: Principio activo: Extracto seco
FICHA TÉCNICA. LAMISIL crema
 FICHA TÉCNICA LAMISIL crema 1. NOMBRE DEL MEDICAMENTO Lamisil 1% crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 g de crema contiene 10 mg de terbinafina clorhidrato. Para la lista completa de excipientes,
FICHA TÉCNICA LAMISIL crema 1. NOMBRE DEL MEDICAMENTO Lamisil 1% crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 g de crema contiene 10 mg de terbinafina clorhidrato. Para la lista completa de excipientes,
FICHA TÉCNICA. La duración estimada del tratamiento será de dos semanas.
 FICHA TÉCNICA 1. NOMBRE DE LA ESPECIALIDAD UVALETTE 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Contenido por comprimido recubierto: - 120,00 mg de extracto seco etanólico al 30%, de planta entera de Taraxacum
FICHA TÉCNICA 1. NOMBRE DE LA ESPECIALIDAD UVALETTE 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Contenido por comprimido recubierto: - 120,00 mg de extracto seco etanólico al 30%, de planta entera de Taraxacum
PROSPECTO. GOBEMICINA 250 Inyectable GOBEMICINA 500 Inyectable GOBEMICINA 1 g Inyectable
 PROSPECTO GOBEMICINA 250 Inyectable GOBEMICINA 500 Inyectable GOBEMICINA 1 g Inyectable GOBEMICINA 250 (Ampicilina) INYECTABLE VIA INTRAVENOSA E INTRAMUSCULAR COMPOSICION Cada vial contiene: «250» AMPICILINA
PROSPECTO GOBEMICINA 250 Inyectable GOBEMICINA 500 Inyectable GOBEMICINA 1 g Inyectable GOBEMICINA 250 (Ampicilina) INYECTABLE VIA INTRAVENOSA E INTRAMUSCULAR COMPOSICION Cada vial contiene: «250» AMPICILINA
FICHA TÉCNICA. Alivio del dolor de garganta agudo para adultos y adolescentes mayores de 12 años.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Lizipadol 17,86 mg/ ml solución para pulverización bucal 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Una pulverización contiene 2,5 mg de ambroxol hidrocloruro. Un
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Lizipadol 17,86 mg/ ml solución para pulverización bucal 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Una pulverización contiene 2,5 mg de ambroxol hidrocloruro. Un
dolor de espalda ocasional (como consecuencia de la práctica de actividades deportivas o durante las actividades de la vida diaria)
 Voltadol Forte 23,2 mg/g gel Diclofenaco dietilamina Lea todo el prospecto detenidamente porque contiene información importante para usted. Este medicamento puede adquirirse sin receta. No obstante, para
Voltadol Forte 23,2 mg/g gel Diclofenaco dietilamina Lea todo el prospecto detenidamente porque contiene información importante para usted. Este medicamento puede adquirirse sin receta. No obstante, para
Resumen de las Características del Producto. Excipientes: Para consultar la lista completa de excipientes, ver sección 6.1.
 1. NOMBRE DEL MEDICAMENTO ASPITOPIC 50 mg/g gel Resumen de las Características del Producto 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de gel contiene: Etofenamato (DOE) 50 mg Excipientes: Para
1. NOMBRE DEL MEDICAMENTO ASPITOPIC 50 mg/g gel Resumen de las Características del Producto 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de gel contiene: Etofenamato (DOE) 50 mg Excipientes: Para
PROSPECTO: INFORMACIÓN PARA EL USUARIO. Lamisil 1% solución para pulverizacuión cutánea. Terbinafina clorhidrato
 PROSPECTO: INFORMACIÓN PARA EL USUARIO Lamisil 1% solución para pulverizacuión cutánea Terbinafina clorhidrato Lea todo el prospecto detenidamente antes de empezar a usar el medicamento. Conserve este
PROSPECTO: INFORMACIÓN PARA EL USUARIO Lamisil 1% solución para pulverizacuión cutánea Terbinafina clorhidrato Lea todo el prospecto detenidamente antes de empezar a usar el medicamento. Conserve este
Voltadol 11,6 mg/g Gel
 PROSPECTO: INFORMACION PARA EL USUARIO Voltadol 11,6 mg/g Gel Diclofenaco dietilamina Lea todo el prospecto detenidamente porque contiene información importante para usted. Este medicamento puede adquirirse
PROSPECTO: INFORMACION PARA EL USUARIO Voltadol 11,6 mg/g Gel Diclofenaco dietilamina Lea todo el prospecto detenidamente porque contiene información importante para usted. Este medicamento puede adquirirse
FICHA TÉCNICA. Vispring 500 microgramos/ml colirio en solución en envases unidosis
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Vispring 500 microgramos/ml colirio en solución en envases unidosis 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de colirio en solución contiene: Tetrizolina
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Vispring 500 microgramos/ml colirio en solución en envases unidosis 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de colirio en solución contiene: Tetrizolina
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO COVEXIN 8 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Composición por ml: Sustancias activas: Clostridium perfringens,
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO COVEXIN 8 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Composición por ml: Sustancias activas: Clostridium perfringens,
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO. ÓXIDO DE ZINC CALIER 1000 mg/g PREMEZCLA MEDICAMENTOSA PARA CERDOS
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO ÓXIDO DE ZINC CALIER 1000 mg/g PREMEZCLA MEDICAMENTOSA PARA CERDOS 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO ÓXIDO DE ZINC CALIER 1000 mg/g PREMEZCLA MEDICAMENTOSA PARA CERDOS 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada
Acné leve (polimorfo juvenil con comedones y seborrea)
 Acné leve (polimorfo juvenil con comedones y seborrea) Se puede aplicar una fórmula con loción de calamina por la mañana como simple maquillaje: Dp/ Loción de calamina 100 g Bioazufre 1.5 g Alcanfor 0.5
Acné leve (polimorfo juvenil con comedones y seborrea) Se puede aplicar una fórmula con loción de calamina por la mañana como simple maquillaje: Dp/ Loción de calamina 100 g Bioazufre 1.5 g Alcanfor 0.5
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Ginkokán 40 mg comprimidos Extracto de Ginkgo biloba EGb 761 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Ginkokán 40 mg comprimidos Extracto de Ginkgo biloba EGb 761 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 METRONIDAZOL 500 mg TABLETA VAGINAL ANTIPARASITARIO - ANTIPROTOZOARIO Página 1 METRONIDAZOL 500 mg Tableta Vaginal
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 METRONIDAZOL 500 mg TABLETA VAGINAL ANTIPARASITARIO - ANTIPROTOZOARIO Página 1 METRONIDAZOL 500 mg Tableta Vaginal
FICHA DE INFORMACIÓN AL PACIENTE: AMPICILINA
 FICHA DE INFORMACIÓN AL PACIENTE: AMPICILINA 1.1 Acción: Antibiótico con acción bactericida. 1.- QUÉ ES Y PARA QUE SE UTILIZA 1.2 Cómo actúa este fármaco: Las penicilinas bloquean la formación de las paredes
FICHA DE INFORMACIÓN AL PACIENTE: AMPICILINA 1.1 Acción: Antibiótico con acción bactericida. 1.- QUÉ ES Y PARA QUE SE UTILIZA 1.2 Cómo actúa este fármaco: Las penicilinas bloquean la formación de las paredes
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 COMPLEJO B COMPRIMIDOS RECUBIERTOS VITAMINA Página 1 COMPLEJO B Comprimidos Recubiertos Principio Activo Tiamina
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 COMPLEJO B COMPRIMIDOS RECUBIERTOS VITAMINA Página 1 COMPLEJO B Comprimidos Recubiertos Principio Activo Tiamina
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Quocin solución cutánea 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada 1 ml de solución contiene 120 mg de ácido salicílico y 60 mg
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Quocin solución cutánea 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada 1 ml de solución contiene 120 mg de ácido salicílico y 60 mg
RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO. PRACETAM 200 mg/ml SOLUCIÓN ORAL PARA ADMINISTRACIÓN EN AGUA DE BEBIDA PARA PORCINO
 RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO PRACETAM 200 mg/ml SOLUCIÓN ORAL PARA ADMINISTRACIÓN EN AGUA DE BEBIDA PARA PORCINO 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO PRACETAM 200 mg/ml SOLUCIÓN ORAL PARA ADMINISTRACIÓN EN AGUA DE BEBIDA PARA PORCINO 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. Amorolfina Isdin 50 mg/ml barniz de uñas medicamentoso 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Amorolfina Isdin 50 mg/ml barniz de uñas medicamentoso 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 ml de Amorolfina ISDIN contiene 55,74 mg de clorhidrato de amorolfina
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Amorolfina Isdin 50 mg/ml barniz de uñas medicamentoso 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 ml de Amorolfina ISDIN contiene 55,74 mg de clorhidrato de amorolfina
FICHA TÉCNICA. Emovate crema está indicado para el tratamiento de eczema y dermatitis de todos los tipos, incluyendo:
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Emovate crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Composición por 100 g: Clobetasona, 17-butirato... 0,05 g (0,5 mg/g) Excipientes y agua purificada c.s.p....
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Emovate crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Composición por 100 g: Clobetasona, 17-butirato... 0,05 g (0,5 mg/g) Excipientes y agua purificada c.s.p....
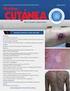
Tratamiento tópico del acné papulo-pustuloso. Dra. Minerva Gómez Flores
 Tratamiento tópico del acné papulo-pustuloso Dra. Minerva Gómez Flores El tratamiento tópico es el común denominador en todas las variedades y grados de acné. Efectos de los agentes en la terapia tópica
Tratamiento tópico del acné papulo-pustuloso Dra. Minerva Gómez Flores El tratamiento tópico es el común denominador en todas las variedades y grados de acné. Efectos de los agentes en la terapia tópica
