MAXIMILIANO MÉNDEZ, OSCAR JULIO, HÉCTOR ESPITIA
|
|
|
- Francisco José Silva Mora
- hace 6 años
- Vistas:
Transcripción
1 EFECTO DE LA TEMPERATURA SOBRE LAS PROPIEDADES VISCOSIMÉTRICAS DE LAS SOLUCIONES ACUOSAS DE HEXANO-1,2-DIOL, HEXANO-1,5-DIOL, HEXANO-1,6-DIOL Y HEXANO-2,5-DIOL EN FUNCIÓN DE LA COMPOSICIÓN RESUMEN MAXIMILIANO MÉNDEZ, OSCAR JULIO, HÉCTOR ESPITIA hmes83@latinmail.com Las viscosidades de las soluciones acuosas de hexano-1,2-diol (1,2-HD), hexano-1,5-diol (1,5- HD), hexano-1,6-diol (1,6-HD) y hexano-2,5-diol (2,5-HD) fueron medidas en el rango de composición: en la escala de fracción molar del alcohol, a las temperaturas de , , , , y K. Las viscosidades relativas, / 0, de estas soluciones fueron expresadas en función de la molalidad, de acuerdo con la ecuación propuesta por Tsangaris-Martin, a partir de la cual se obtuvieron los coeficientes B de viscosidad. Estos coeficientes informan acerca de los fenómenos estructurales y de las interacciones predominantes en la solución. La magnitud y el signo de estos coeficientes indican que el grado de hidrofobicidad de estos alcoholes sigue el orden: 1,2-HD > 1,5-HD > 2,5-HD >1,6-HD. Adicionalmente, también se presentan las tendencias E (X 2 )y G (X 2 ) la cual esta de acuerdo con los resultados obtenidos por otros autores para otros tipos de dioles[1,2]. INTRODUCCIÓN En los últimos años se ha dado gran importancia al estudio de las soluciones acuosas de alcoholes debido en gran parte a que la estabilidad de las proteínas es altamente afectada por la presencia de soluciones acuosas concentradas de estos solutos, los cuales tienen diferentes efectos sobre la estructura del agua[3]; es importante mencionar que los alcoholes son bien conocidos como agentes desnaturalizantes[4]. En este articulo se reportan datos novedosos respecto a los sistemas alcohol agua, en cuanto a propiedades viscosimétricas para los isómeros de hexanodiol en soluciones acuosas. En la actualidad no se encontró información para estos sistemas. Adicionalmente también se reportan datos de densidad de soluciones acuosas de hexano-1,2-diol (1,2-HD), hexano-1,5-diol (1,5-HD), hexano-1,6-diol (1,6-HD) y hexano-2,5-diol (2,5-HD) en un rango de composición de: en la escala de fracción molar a las temperaturas de K, con intervalos de 5 K., obtenidas por el método picnómetrico. Las propiedades viscosimétricas de dioles de cadena larga son influenciadas principalmente por los fenómenos de hidratación hidrofóbica, particularmente en la región rica en agua[5]. El estudio de isómeros de hexanodioles es importante porque permite examinar en detalle la influencia de la posición relativa de los grupos OH sobre las propiedades termodinámicas de estos alcoholes. OBJETIVOS OBJETIVO GENERAL Estudiar el efecto de la temperatura sobre las propiedades viscosimétricas de las soluciones acuosas de hexano-1,2-diol, hexano-1,6-diol y hexano-2,5-diol en función de la composición.
2 OBJETIVOS ESPECÍFICOS 1. Determinar la viscosidad dinámica de las soluciones antes mencionadas, en un rango de temperatura de 10,00 35, 00 ºC, en la región diluida. 2. Examinar como la viscosidad de las soluciones acuosas de hexanodioles son influenciadas por la posición relativa de sus grupos hidroxilos. 3. Determinar la naturaleza hidrofílica o hidrofóbica de estos alcoholes a las temperaturas de 10,00-35,00 ºC. JUSTIFICACIÓN La determinación y el análisis de la viscosidad una propiedad fisicoquímica, es de gran importancia debido a que permite el cálculo de las propiedades termodinámicas de activación ( H*, G* y S*). Además los coeficientes B de viscosidad brindan importante información que conlleva a caracterizar los solutos bien como hidrofóbicos o bien como hidrofílicos, pero este no es el único aspecto importante del estudio de la viscosidad, ya que teniendo en cuenta su dependencia con la temperatura es posible determinar el efecto del soluto sobre la estructura del solvente. Conociendo la importancia de la viscosidad es interesante resaltar que para nuestros sistemas constituidos por los alcoholes: hexano-1,2-diol, hexano-1,6-diol y hexano-2,5-diol en solución acuosa, no hay muchos estudios acerca del comportamiento fisicoquímico y termodinámico, que ayuden a comprender las interacciones soluto-soluto y soluto - solvente en función de la composición y de la temperatura. Otro aspecto a destacar es que este tipo de alcoholes presenta grandes similitudes en cuanto a estructura y comportamiento con aminoácidos, por lo cual el estudio de éstos en soluciones acuosas permitirá analizar, entender y comprender mejor aún como se dan las interacciones en sistemas biológicos. Algunas de estas son la interacción hidrofílica la cual esta ligada al hecho que los grupos hidroxilos de algunos aminoácidos y moléculas de agua forman puentes de hidrógeno; el carácter hidrofóbico, es decir, el hecho de que los grupos hibrocarbonados tienden a ser repelidos por las moléculas de agua, este efecto es responsable, en parte al menos, de las complejas estructuras espaciales que presentan las proteínas, el ADN y las bicapas lipidicas de las membranas celulares. En la actualidad no existe una teoría general para las soluciones y mucho menos para el agua como solvente que de cuenta de su comportamiento, por lo cual se contribuirá en parte con el entendimiento de estos hechos, además se escogieron los isómeros comerciales del hexanodiol para examinar como afectan las posiciones de los grupos hidroxilos (OH) a las propiedades termodinámicas y fisicoquímicas de estos sistemas. SECCIÓN EXPERIMENTAL Materiales. Todos los reactivos usados en este trabajo fueron suministrados por Aldrich Chemical Co., Inc., con una pureza del 99%. El agua empleada para la calibración de los equipos y la preparación de las soluciones fue doblemente destilada, con una conductividad menor que 2 µs-cm -1. Todas las soluciones fueron preparadas por el método de pesada usando una balanza Ohaus con una sensibilidad de 10-4 g. Medidas de densidad.
3 Para determinar las densidades de alcoholes, se usaron picnómetros de cuello capilar, tipo Wood y Brusie con capacidad aproximada de 50 cm 3 los cuales fueron calibrados con agua a las temperaturas de trabajo. Las densidades así obtenidas presentan una incertidumbre de ± 1X10-5 g- cm -3. Medidas de viscosidad. Las viscosidades fueron determinadas usando un viscosímetro de Ubbelohde de nivel suspendido [6], con tiempos de flujo entre 300 y 500 s, previamente calibrados según las recomendaciones de la literatura. Los tiempos de flujo fueron medidos usando un cronómetro Casio que permite leer 0.01s. Las viscosidades obtenidas presentan una incertidumbre de ± cp. Tanto las mediciones de la viscosidad de las soluciones como las densidades se realizaron en un baño termostatado a temperatura controlada con un termómetro Beckmann de 5ºC que tiene una división mínima de 0.01ºC, durante este proceso los viscosímetros y picnómetros fueron mantenidos en posición vertical soportados mediante un montaje rígido. RESULTADOS Y DISCUSIÓN Las densidades y viscosidades experimentales para los alcoholes hexano-1,2-diol y hexano-2,5- diol en su estado puro a las diferentes temperaturas, fueron determinados, exceptuando el hexano-1,6-diol y hexano-1,5-diol, por ser el primero un sólido y el segundo por carecer de las cantidades suficientes. Los valores aquí mostrados son el resultado de un trabajo novedoso con los isómeros de hexanodiol en solución acuosa ya que en la actualidad no se encontró información para estos sistemas. Los valores en cuanto a propiedades viscosimétricas son bastante altos en comparación con los conocidos para el agua y otros dioles[1,2]. El hexano-2,5-diol mostró mayores viscosidades que el hexano-1,2-diol a todas las temperaturas, lo cual es posible explicar por la posición de los grupos OH en la cadena carbonada. Estos grupos en el hexano-2,5-diol se encuentran en una posición tal, que cuando se dan los puentes de hidrógeno estas moléculas quedan con poca libertad de movimiento y más compactadas a diferencia del hexano-1,2-diol en donde la parte apolar queda libre por lo cual se hacen menos compactas y así menos densa. Además el gran tamaño de estas moléculas favorece a las altas viscosidades. En cuanto a la temperatura, a medida que esta aumenta la viscosidad de ambos alcoholes disminuye debido a que las fuerzas intermolecular e intramolecular se hacen más débiles haciendo que los dioles muestren menos resistencia al fluir. Las densidades, viscosidades y viscosidades relativas para cada una de las soluciones de los dioles a diferentes temperaturas en función de la composición fueron también calculadas. La viscosidad, para las distintas mezclas binarias acuosas de los isómeros de hexanodiol fue calculada a partir de la densidad ρ y los tiempos de flujo t de cada sistema acuoso usando la siguiente expresión: αρ t β ρ / t 1 Donde α y β son las constantes especificas de los viscosímetros. La viscosidad relativa r, fue calculada como la razón de la viscosidad de la solución respecto a la viscosidad del agua a cada una de las temperaturas, la que a su vez fue relacionada con la molalidad m, a través de una ecuación de segundo orden como sugiere Tsangaris-Martin[7]. 2 r = / 0 = 1+ Bm + Dm ( 2 ) = ( )
4 Donde 0 es la viscosidad del solvente, B y D son constantes empíricas características de cada sistema. Esta ecuación es empleada para soluciones con solutos moderadamente concentrados[8]. La Figura 1 muestra a r en función de la composición de hexano-2,5-diol en solución acuosa a diferentes temperaturas. Los otros isómeros estudiados siguen una tendencia similar. En ella se puede observar un aumento en la viscosidad relativa al incrementar la concentración del alcohol a todas las temperaturas, pero esta propiedad disminuye con el incremento de la temperatura. Este comportamiento es análogo para los demás isómeros. Todos los sistemas aquí estudiados presentan viscosidades mayores que la del agua pura (solvente), por lo que es posible que el soluto ayude a la formación de la estructura del agua[9] r m / mol-kg-1 Fig. 1. Grafica de r vs molalidad de hexano-2,5-diol a diferentes temperaturas. 10ºC, 15ºC, 20ºC, 25ºC, 30ºC y 35ºC Los valores de los coeficientes B de viscosidad para todos los alcoholes aquí estudiados son positivos y de magnitud relativamente alta en comparación con otros alcoholes[8]. Estos coeficiente brinda información acerca del tamaño y forma del soluto, a demás de reflejar el efecto de ellos sobre la estructura del solvente, siendo formadores o dirruptores de está. En la Tabla 6 se observa que la magnitud de los coeficiente B sigue el siguiente orden: hexano-1,2-diol > hexano- 1,5-diol > hexano-2,5-diol > hexano-1,6-diol; este comportamiento fue el mismo a todas las temperaturas de trabajo. También se encontró que a medida que aumenta la temperatura los coeficiente B de viscosidad disminuyen para todos los alcoholes ( db/dt < 0 ) como se observa en la Figura 2.
5 Fig. 2. Grafica de coeficientes B de viscosidad vs temperatura para soluciones acuosas de: Hexano-2,5-diol Hexano-1,6-diol Hexano-1,2-diol Hexano-1,5-diol. Coeficiente B / kg-mol T / ºC Como se mencionó anteriormente el db/dt es negativo por lo que se propone que estos hexanodioles son formadores de la estructura del agua como sugiere Tsangaris Martín[7] y que el efecto predominante es el hidrofóbico; este hecho es bastante importante teniendo en cuenta que estos alcoholes poseen un dominio hidrofóbico y uno hidrofílico, es decir, poseen grupos polares (- OH) y apolares (-CH 2 - y -CH 3 ) los cuales compiten por imponer su sello sobre las propiedades de la solución. Se piensa que este efecto predomina debido en parte a que los grupos apolares vecinos a grupos polares tienden a neutralizarlos, siendo ellos los prevalecientes. E Las viscosidades de exceso,, fueron determinadas por la ecuación (3), la cual ha sido usada por varios autores en soluciones acuosas de dioles[1,2]. E = exp( X ln + X ) ( 3 ) ln 2 Donde X 1 y X 2 son las fracciones molares del soluto y del solvente, 1 y 2 son las viscosidades del soluto y el solvente puro respectivamente. Las tendencias mostrada en la anterior figura es semejante a las presentada por otros autores para dioles diferentes[1,2]. Las valores encontrados para la viscosidad de exceso de hexano-2,5-diol y hexano-1,2-diol fueron positivos, lo cual nos indica que existen fuertes interacciones entre estos alcoholes y el agua. Las altas magnitudes indican que las soluciones son altamente no ideales y que las interacciones entre los componentes de la mezcla son bastante fuertes[10]. Esta propiedad decrece con el incremento de la temperatura para ambos alcoholes. La entalpía y entropía de activación, H y S, para el flujo viscoso fueron calculados por la ecuación de Eyring[11], que se expresa de la siguiente forma: V m hn H = RT S R ln ( 4 ) Donde V m, es el volumen molar de la solución, h la constante de Planck, N el número de Avogadro y R la constante de los gases. En todos los casos los datos obtenidos se ajustaron correctamente a una línea recta al graficar ln V m / hn vs 1 / T. Para el cálculo de la energía libre de Gibbs de activación, G, se empleó la siguiente expresión:
6 G = H T S ( 5 ) REFERENCIAS 1. B. Haweylak, S. Andrecyk, C. Gabriel, K. Gracie, R. Palepu. J. S. Chem. 27 (1998) M. A. Saleh, S. Begum, S. K. Begum, B. A. Begum. Phys. Chem. Liq. 37 (1999) G. Castronuovo, V. Elia, V. Moiello, F. Velleca, S. Perez. Phys. Chem. Chem. Phys. 1 (1999) C. M. Romero, J. L. Rojas. Phys. Chem. Liq. 38 (2000) R. Badarayani, A. Kumar. J. Chem. Thermodynamics. 36 (2004) L. Korson, W. Drost-Hansen, F. Millero. J. Phys. Chem. 73 (1969) J. Tsangaris, R. Martín. Biochem. Biophys. 112 (1965) T. Herskovits, T. Kelly. J. Phys. Chem. 77 (1973) S. Aznarez, A. Amid, M. Holgado, E. Arancibia. J. Mol. Liq. 115 (2004) M. Saleh, O. Ahmed, M. Ahmed. J. Mol. Liq. 115 (2004) Glasstone, K. Laidler, H. Eyring. The theory of Rate Processes, McGraw Hill, New York, 1941 p. 447.
Efecto de la Temperatura sobre la Viscosidad de Soluciones Acuosas Diluidas de 1,2-Pentanodiol
 Información Tecnológica Efecto Vol. 20(2), de la 55-60 Temperatura (2009) sobre la Viscosidad de Soluciones Acuosas Diluidas doi:10.1612/inf.tecnol.4030dit.08 Efecto de la Temperatura sobre la Viscosidad
Información Tecnológica Efecto Vol. 20(2), de la 55-60 Temperatura (2009) sobre la Viscosidad de Soluciones Acuosas Diluidas doi:10.1612/inf.tecnol.4030dit.08 Efecto de la Temperatura sobre la Viscosidad
Fundamentos de Química. Horario de Tutorías
 Fundamentos de Química Segundo Cuatrimestre Horario de Tutorías Martes 12:00-14:00 16:00-19:00 Edificio 24B.Tercera Planta 14/02/2006 Tema 11: Propiedades de las disoluciones 11.1 Definición de disolución
Fundamentos de Química Segundo Cuatrimestre Horario de Tutorías Martes 12:00-14:00 16:00-19:00 Edificio 24B.Tercera Planta 14/02/2006 Tema 11: Propiedades de las disoluciones 11.1 Definición de disolución
DEPARTAMENTO DE INGENIERIA QUÍMICA CÁTEDRA DE FISICOQUÍMICA TRABAJO PRÁCTICO DE LABORATORIO Nº 4
 Universidad Tecnológica Nacional Facultad Regional La Plata DEPARTAMENTO DE INGENIERIA QUÍMICA CÁTEDRA DE FISICOQUÍMICA TRABAJO PRÁCTICO DE LABORATORIO Nº 4 Descenso crioscópico Objeto de la experiencia:
Universidad Tecnológica Nacional Facultad Regional La Plata DEPARTAMENTO DE INGENIERIA QUÍMICA CÁTEDRA DE FISICOQUÍMICA TRABAJO PRÁCTICO DE LABORATORIO Nº 4 Descenso crioscópico Objeto de la experiencia:
A continuación se detallan cada una de las propiedades coligativas:
 PREGUNTA (Técnico Profesional) Se prepara una solución con 2 mol de agua y 0,5 mol de un electrolito no volátil. Al respecto, cuál es la presión de vapor a 25 ºC de esta solución, si la presión del agua
PREGUNTA (Técnico Profesional) Se prepara una solución con 2 mol de agua y 0,5 mol de un electrolito no volátil. Al respecto, cuál es la presión de vapor a 25 ºC de esta solución, si la presión del agua
VOLUMEN MOLAR PARCIAL DE UNA MEZCLA BINARIA
 Práctica VOLUMEN MOLAR PARCIAL DE UNA MEZCLA BINARIA. INTRODUCCIÓN Las magnitudes termodinámicas como la entropía S, energía interna E, volumen V ó entalpía H son magnitudes extensivas, que dependen de
Práctica VOLUMEN MOLAR PARCIAL DE UNA MEZCLA BINARIA. INTRODUCCIÓN Las magnitudes termodinámicas como la entropía S, energía interna E, volumen V ó entalpía H son magnitudes extensivas, que dependen de
UNIVERSIDAD DE ANTIOQUIA FACULTAD DE QUÍMICA FARMACÉUTICA LABORATORIO DE QUÍMICA GENERAL Profesor: Jaime O. Pérez
 UNIVERSIDAD DE ANTIOQUIA FACULTAD DE QUÍMICA FARMACÉUTICA LABORATORIO DE QUÍMICA GENERAL Profesor: Jaime O. Pérez Práctica: Determinación de Densidades. Fecha: 24 de noviembre de 2009 DEYMER GÓMEZ CORREA:
UNIVERSIDAD DE ANTIOQUIA FACULTAD DE QUÍMICA FARMACÉUTICA LABORATORIO DE QUÍMICA GENERAL Profesor: Jaime O. Pérez Práctica: Determinación de Densidades. Fecha: 24 de noviembre de 2009 DEYMER GÓMEZ CORREA:
DISOLUCIONES UNIDAD IV. Licda. Miriam Marroquín Leiva
 DISOLUCIONES UNIDAD IV 1 DISOLUCIÓN Es una mezcla homogénea de dos o más sustancias; el soluto y el disolvente. Es un término utilizado para describir un sistema en el cual una o más sustancias están mezcladas
DISOLUCIONES UNIDAD IV 1 DISOLUCIÓN Es una mezcla homogénea de dos o más sustancias; el soluto y el disolvente. Es un término utilizado para describir un sistema en el cual una o más sustancias están mezcladas
PRÁCTICA Nº 3 PROPIEDADES COLIGATIVAS: DETERMINACIÓN DE LA MASA MOLECULAR DE UN SOLUTO PROBLEMA POR CRIOSCOPIA
 PRÁCTICA Nº 3 PROPIEDADES COLIGATIVAS: DETERINACIÓN DE LA ASA OLECULAR DE UN SOLUTO PROBLEA POR CRIOSCOPIA OBJETIVOS: El objetivo de la práctica es el estudio del efecto que produce la adición de un soluto
PRÁCTICA Nº 3 PROPIEDADES COLIGATIVAS: DETERINACIÓN DE LA ASA OLECULAR DE UN SOLUTO PROBLEA POR CRIOSCOPIA OBJETIVOS: El objetivo de la práctica es el estudio del efecto que produce la adición de un soluto
FÍSICA APLICADA Y FISICOQUÍMICA I. Tema 2. El Primer Principio de la Termodinámica
 María del Pilar García Santos GRADO EN FARMACIA FÍSICA APLICADA Y FISICOQUÍMICA I Tema 2 El Primer Principio de la Termodinámica Esquema Tema 2. Primer Principio de la Termodinámica 2.1 Primer Principio
María del Pilar García Santos GRADO EN FARMACIA FÍSICA APLICADA Y FISICOQUÍMICA I Tema 2 El Primer Principio de la Termodinámica Esquema Tema 2. Primer Principio de la Termodinámica 2.1 Primer Principio
SUSTANCIA QUÍMICA mercurio oxígeno
 ELEMENTO O SUSTANCIA ELEMENTAL: Sustancia formada por un mismo tipo de átomos, por ejemplo: Hg, H 2, Cu, O 2 SUSTANCIA QUÍMICA mercurio oxígeno COMPUESTO O SUSTANCIA COMPUESTA: Sustancia formada por dos
ELEMENTO O SUSTANCIA ELEMENTAL: Sustancia formada por un mismo tipo de átomos, por ejemplo: Hg, H 2, Cu, O 2 SUSTANCIA QUÍMICA mercurio oxígeno COMPUESTO O SUSTANCIA COMPUESTA: Sustancia formada por dos
CINÉTICA QUÍMICA. Dr. Hugo Cerecetto. Prof. Titular de Química
 CINÉTICA QUÍMICA Dr. Hugo Cerecetto Prof. Titular de Química Temario 2) La reacción química: - Nociones de Termoquímica y Termodinámica. Conceptos de entalpía y entropía de reacción. Energía libre. Espontaneidad
CINÉTICA QUÍMICA Dr. Hugo Cerecetto Prof. Titular de Química Temario 2) La reacción química: - Nociones de Termoquímica y Termodinámica. Conceptos de entalpía y entropía de reacción. Energía libre. Espontaneidad
FÍSICA Y QUÍMICA 3º ESO. OBJETIVOS, CONTENIDOS Y CRITERIOS DE EVALUACIÓN 1ª Evaluación: Unidad 1. La medida y el método científico.
 FÍSICA Y QUÍMICA 3º ESO. OBJETIVOS, CONTENIDOS Y CRITERIOS DE EVALUACIÓN 1ª Evaluación: Unidad 1. La medida y el método científico. OBJETIVOS 1. Reconocer las etapas del trabajo científico y elaborar informes
FÍSICA Y QUÍMICA 3º ESO. OBJETIVOS, CONTENIDOS Y CRITERIOS DE EVALUACIÓN 1ª Evaluación: Unidad 1. La medida y el método científico. OBJETIVOS 1. Reconocer las etapas del trabajo científico y elaborar informes
Química Biológica TP 1: ESPECTROFOTOMETRIA.
 TP 1: ESPECTROFOTOMETRIA. Introducción Al observar una solución acuosa de un colorante a trasluz, observamos una leve coloración, la cual se debe a la interacción entre las moléculas del colorante y la
TP 1: ESPECTROFOTOMETRIA. Introducción Al observar una solución acuosa de un colorante a trasluz, observamos una leve coloración, la cual se debe a la interacción entre las moléculas del colorante y la
Investigación Espectrofométrica de la interacción de Yodo con Hidrocarburos A romáticos
 Investigación Espectrofométrica de la interacción de Yodo con Hidrocarburos A romáticos Alicia Castro (200718024), Carlos García (200911158), Byron Pérez (201013499) Departamento de Fisicoquímica, Facultad
Investigación Espectrofométrica de la interacción de Yodo con Hidrocarburos A romáticos Alicia Castro (200718024), Carlos García (200911158), Byron Pérez (201013499) Departamento de Fisicoquímica, Facultad
UNIVERSIDAD TECNOLÓGICA DE PUEBLA
 TÉRMICA. PRÁCTICA NÚMERO 1 TEMPERATURA OBJETIVO: 1. Comprender el fundamento termodinámico de la medición de la temperatura. 2. Construirla curva de calentamiento del agua. 3. Obtener mediciones de temperatura
TÉRMICA. PRÁCTICA NÚMERO 1 TEMPERATURA OBJETIVO: 1. Comprender el fundamento termodinámico de la medición de la temperatura. 2. Construirla curva de calentamiento del agua. 3. Obtener mediciones de temperatura
PROPIEDADES COLIGATIVAS DE LAS SOLUCIONES
 PROPIEDADES COLIGATIVAS DE LAS SOLUCIONES Los estudios teóricos y experimentales han permitido establecer, que los líquidos poseen propiedades físicas características. Entre ellas cabe mencionar: la densidad,
PROPIEDADES COLIGATIVAS DE LAS SOLUCIONES Los estudios teóricos y experimentales han permitido establecer, que los líquidos poseen propiedades físicas características. Entre ellas cabe mencionar: la densidad,
5. Equilibrio químico
 5. Equilibrio químico Química (1S, Grado Biología) UAM 5. Equilibrio químico Contenidos Equilibrio químico Concepto Condición de uilibro químico Energía libre de Gibbs de reacción Cociente de reacción
5. Equilibrio químico Química (1S, Grado Biología) UAM 5. Equilibrio químico Contenidos Equilibrio químico Concepto Condición de uilibro químico Energía libre de Gibbs de reacción Cociente de reacción
Práctica No 12. Determinación experimental de la Presión de vapor de un líquido puro
 Práctica No 12 Determinación experimental de la Presión de vapor de un líquido puro 1. Objetivo general: Evaluar la entalpía de vaporización mediante el modelo de Clausius y Clapeyron. 2. Marco teórico:
Práctica No 12 Determinación experimental de la Presión de vapor de un líquido puro 1. Objetivo general: Evaluar la entalpía de vaporización mediante el modelo de Clausius y Clapeyron. 2. Marco teórico:
Actividad introductoria: Aplicación en la industria de las fuerzas intermoleculares.
 Grado 10 Ciencias - Unidad 3 Cómo se relacionan los componentes del mundo? Tema Cómo afectan las fuerzas intermoleculares las propiedades de los compuestos? Curso: Nombre: Actividad introductoria: Aplicación
Grado 10 Ciencias - Unidad 3 Cómo se relacionan los componentes del mundo? Tema Cómo afectan las fuerzas intermoleculares las propiedades de los compuestos? Curso: Nombre: Actividad introductoria: Aplicación
UNIVERSIDAD AUTONOMA DE ZACATECAS Francisco García Salinas UNIDAD ACADÉMICA DE CIENCIAS QUÍMICAS Químico Farmacéutico Biólogo
 UNIVERSIDAD AUTONOMA DE ZACATECAS Francisco García Salinas UNIDAD ACADÉMICA DE CIENCIAS QUÍMICAS Químico Farmacéutico Biólogo PROGRAMA: ACADEMIA DE FISICOQUÍMICA JUNIO 2010 PROPUESTA ELABORADA POR: ACADEMIA
UNIVERSIDAD AUTONOMA DE ZACATECAS Francisco García Salinas UNIDAD ACADÉMICA DE CIENCIAS QUÍMICAS Químico Farmacéutico Biólogo PROGRAMA: ACADEMIA DE FISICOQUÍMICA JUNIO 2010 PROPUESTA ELABORADA POR: ACADEMIA
Aplicación de los criterios de espontaneidad a una reacción química completa
 Algunas reflexiones sobre el equilibrio químico a partir de consideraciones termodinámicas Prof. Marisa García Dra. María Antonia Grompone 1 Introducción En los programas de Química del Bachillerato Diversificado
Algunas reflexiones sobre el equilibrio químico a partir de consideraciones termodinámicas Prof. Marisa García Dra. María Antonia Grompone 1 Introducción En los programas de Química del Bachillerato Diversificado
Tema 4. Fuerzas intermoleculares
 Tema 4: Fuerzas intermoleculares Química para biólogos Slide 1 of 35 Contenidos 4-1 Electronegatividad 4-2 Polaridad de enlace y molécula: momento dipolar 4-3 Fuerzas intermoleclares 4-4 Puentes de hidrógeno
Tema 4: Fuerzas intermoleculares Química para biólogos Slide 1 of 35 Contenidos 4-1 Electronegatividad 4-2 Polaridad de enlace y molécula: momento dipolar 4-3 Fuerzas intermoleclares 4-4 Puentes de hidrógeno
Conductividad en presencia de campo eléctrico
 6. Fenómenos de transporte Fenómenos de transporte Conductividad térmicat Viscosidad Difusión n sedimentación Conductividad en presencia de campo eléctrico UAM 01-13. Química Física. Transporte CT V 1
6. Fenómenos de transporte Fenómenos de transporte Conductividad térmicat Viscosidad Difusión n sedimentación Conductividad en presencia de campo eléctrico UAM 01-13. Química Física. Transporte CT V 1
Bioquímica Tema 2: Soluciones. Unidades Año: 2013
 TEMA 2: SOLUCIONES Al estudio de las soluciones se le asigna gran importancia, teniendo en cuenta que la mayoría de las reacciones químicas ocurren entre soluciones, particularmente en medios acuosos.
TEMA 2: SOLUCIONES Al estudio de las soluciones se le asigna gran importancia, teniendo en cuenta que la mayoría de las reacciones químicas ocurren entre soluciones, particularmente en medios acuosos.
SEGUNDO DE BACHILLERATO QUÍMICA. a A + b B c C + d D
 TEMA 5. CINÉTICA QUÍMICA a A + b B c C + d D 1 d[a] 1 d[b] 1 d[c] 1 d[d] mol v = = = + = + a dt b dt c dt d dt L s El signo negativo en la expresión de velocidad es debido a que los reactivos desaparecen,
TEMA 5. CINÉTICA QUÍMICA a A + b B c C + d D 1 d[a] 1 d[b] 1 d[c] 1 d[d] mol v = = = + = + a dt b dt c dt d dt L s El signo negativo en la expresión de velocidad es debido a que los reactivos desaparecen,
Disoluciones. Química General II 2011
 Disoluciones Química General II 2011 Disolución Es una mezcla homogénea de dos o mas sustancias. Componentes: Soluto: Sustancia (s) presente (s) en menor cantidad en una disolución, son las sustancias
Disoluciones Química General II 2011 Disolución Es una mezcla homogénea de dos o mas sustancias. Componentes: Soluto: Sustancia (s) presente (s) en menor cantidad en una disolución, son las sustancias
DISOLUCIONES. Las disoluciones son mezclas homogéneas de dos o más sustancias (componentes) en proporciones variables.
 DISOLUCIONES Las disoluciones son mezclas homogéneas de dos o más sustancias (componentes) en proporciones variables. Soluto es la sustancia que se encuentra en menor proporción. Disolvente es la sustancia
DISOLUCIONES Las disoluciones son mezclas homogéneas de dos o más sustancias (componentes) en proporciones variables. Soluto es la sustancia que se encuentra en menor proporción. Disolvente es la sustancia
UNIVERSIDAD AUTONOMA DE BAJA CALIFORNIA
 UNIVERSIDAD AUTONOMA DE BAJA CALIFORNIA CARTA DESCRIPTIVA Carrera: Licenciado en Biología I. DATOS DE IDENTIFICACION. Nombre de la Asignatura Fisicoquímica Clave No. de Horas Teóricas 3 Prácticas 3 Teórico-Prácticas
UNIVERSIDAD AUTONOMA DE BAJA CALIFORNIA CARTA DESCRIPTIVA Carrera: Licenciado en Biología I. DATOS DE IDENTIFICACION. Nombre de la Asignatura Fisicoquímica Clave No. de Horas Teóricas 3 Prácticas 3 Teórico-Prácticas
EQUILIBRIO LÍQUIDO-VAPOR PRESIÓN DE VAPOR Y ENTALPÍA DE VAPORIZACIÓN DEL AGUA
 EQUILIBRIO LÍQUIDO-VAPOR PRESIÓN DE VAPOR Y ENTALPÍA DE VAPORIZACIÓN DEL AGUA I. OBJETIVO GENERAL Comprender e interpretar el significado de las variables termodinámicas involucradas en la ecuación de
EQUILIBRIO LÍQUIDO-VAPOR PRESIÓN DE VAPOR Y ENTALPÍA DE VAPORIZACIÓN DEL AGUA I. OBJETIVO GENERAL Comprender e interpretar el significado de las variables termodinámicas involucradas en la ecuación de
LOS GASES Y LAS DISOLUCIONES. Departamento de Física y Química 3º ESO
 LOS GASES Y LAS DISOLUCIONES Departamento de Física y Química 3º ESO 0. Mapa conceptual SÓLIDO ESTADOS DE LA MATERIA LÍQUIDO Presión atmosférica GAS Solubilidad Disolución saturada Disoluciones Soluto
LOS GASES Y LAS DISOLUCIONES Departamento de Física y Química 3º ESO 0. Mapa conceptual SÓLIDO ESTADOS DE LA MATERIA LÍQUIDO Presión atmosférica GAS Solubilidad Disolución saturada Disoluciones Soluto
EJERCICIOS DE TERMOQUÍMICA
 EJERCICIOS DE TERMOQUÍMICA En los exámenes de Acceso a la Universidad se proponen una serie de cuestiones (más teóricas) y problemas (prácticos) para resolver. En estos apuntes vamos a resolver ambos tipos
EJERCICIOS DE TERMOQUÍMICA En los exámenes de Acceso a la Universidad se proponen una serie de cuestiones (más teóricas) y problemas (prácticos) para resolver. En estos apuntes vamos a resolver ambos tipos
INGENIERO. JOSMERY SÁNCHEZ
 UNIVERSIDAD NACIONAL EXPERIMENTAL FRANCISCO DE MIRANDA COMPLEJO ACADÉMICO "EL SABINO" PROGRAMA DE INGENIERÍA MECÁNICA AREA DE TECNOLOGÍA UNIDAD CURRICULAR: TERMODINÁMICA APLICADA REALIZADO POR: INGENIERO.
UNIVERSIDAD NACIONAL EXPERIMENTAL FRANCISCO DE MIRANDA COMPLEJO ACADÉMICO "EL SABINO" PROGRAMA DE INGENIERÍA MECÁNICA AREA DE TECNOLOGÍA UNIDAD CURRICULAR: TERMODINÁMICA APLICADA REALIZADO POR: INGENIERO.
Determinar de forma cuantitativa el calor que se absorbe o desprende en una reacción de neutralización en medio acuoso -NaOH+HCl- que evoluciona a
 Determinar de forma cuantitativa el calor que se absorbe o desprende en una reacción de neutralización en medio acuoso -NaOH+HCl- que evoluciona a presión constante, interpretando los resultados obtenidos
Determinar de forma cuantitativa el calor que se absorbe o desprende en una reacción de neutralización en medio acuoso -NaOH+HCl- que evoluciona a presión constante, interpretando los resultados obtenidos
Un sistema se encuentra en un estado de equilibrio químico cuando su composición no varía con el tiempo.
 Un sistema se encuentra en un estado de equilibrio químico cuando su composición no varía con el tiempo. N 2 g 3 H 2 g 2 NH 3 g 2 NH 3 g N 2 g 3 H 2 g concentración H 2 N 2 NH 3 concentración NH 3 H 2
Un sistema se encuentra en un estado de equilibrio químico cuando su composición no varía con el tiempo. N 2 g 3 H 2 g 2 NH 3 g 2 NH 3 g N 2 g 3 H 2 g concentración H 2 N 2 NH 3 concentración NH 3 H 2
PREPARACIÓN DE SOLUCIONES
 PRÁCTICA 4 PREPARACIÓN DE SOLUCIONES OBJETIVOS: Determinar las concentraciones físicas y químicas de las soluciones Preparar soluciones a partir de reactivos sólidos y líquidos I. FUNDAMENTO TEÓRICO. Las
PRÁCTICA 4 PREPARACIÓN DE SOLUCIONES OBJETIVOS: Determinar las concentraciones físicas y químicas de las soluciones Preparar soluciones a partir de reactivos sólidos y líquidos I. FUNDAMENTO TEÓRICO. Las
MATERIA: ES TODO LO QUE TIENE MASA Y VOLUMEN.
 MATERIA: ES TODO LO QUE TIENE MASA Y VOLUMEN. CLASIFICACIÓN DE LA MATERIA: SEGÚN: A. ESTADO DE AGREGACIÓN. B. COMPOSICIÓN. A. ESTADO DE AGREGACIÓN. SE REFIERE A LA FORMA DE INTERACCIÓN ENTRE LAS MOLÉCULAS
MATERIA: ES TODO LO QUE TIENE MASA Y VOLUMEN. CLASIFICACIÓN DE LA MATERIA: SEGÚN: A. ESTADO DE AGREGACIÓN. B. COMPOSICIÓN. A. ESTADO DE AGREGACIÓN. SE REFIERE A LA FORMA DE INTERACCIÓN ENTRE LAS MOLÉCULAS
Derivación por Equilibrio de Complejo Activado
 1/3/14 Energía Libre de Gibbs reactivos G Estado de transición Productos Coordenada de reacción Reacción: HO + CH 3 r [HO --- CH 3 --- r] + CH 3 OH + r http://upload.wikimedia.org/wikipedia/commons/thumb/9/99/rxn_coordinate_diagram_5.pg/4px-rxn_coordinate_diagram_5.pg
1/3/14 Energía Libre de Gibbs reactivos G Estado de transición Productos Coordenada de reacción Reacción: HO + CH 3 r [HO --- CH 3 --- r] + CH 3 OH + r http://upload.wikimedia.org/wikipedia/commons/thumb/9/99/rxn_coordinate_diagram_5.pg/4px-rxn_coordinate_diagram_5.pg
DISOLUCIONES DILUIDAS IDEALES. LEY DE HENRY. MODELO DE LA DISOLUCIÓN DILUIDA IDEAL
 DISOLUCIONES DILUIDAS IDEALES. LEY DE HENRY. Muchas disoluciones se desvían bastante del modelo de disolución ideal. or ello resulta útil definir otro modelo: MODELO DE LA DISOLUCIÓN DILUIDA IDEAL 1) Descripción
DISOLUCIONES DILUIDAS IDEALES. LEY DE HENRY. Muchas disoluciones se desvían bastante del modelo de disolución ideal. or ello resulta útil definir otro modelo: MODELO DE LA DISOLUCIÓN DILUIDA IDEAL 1) Descripción
Determinación de la Masa Molar del Magnesio
 Determinación de la Masa Molar del Magnesio Introducción teórica Como en muchas reacciones químicas, los reactivos o sus productos o ambos son gases, es más común medir éstos en función del volumen usando
Determinación de la Masa Molar del Magnesio Introducción teórica Como en muchas reacciones químicas, los reactivos o sus productos o ambos son gases, es más común medir éstos en función del volumen usando
Unidad 0 CÁLCULOS QUÍMICOS. Unidad 0. Cálculos químicos
 Unidad 0 CÁLCULOS QUÍMICOS Unidad 0. Cálculos químicos 1 0. Leyes ponderales Leyes que rigen las combinaciones químicas. Se basan en la experimentación y miden cuantitativamente la cantidad de materia
Unidad 0 CÁLCULOS QUÍMICOS Unidad 0. Cálculos químicos 1 0. Leyes ponderales Leyes que rigen las combinaciones químicas. Se basan en la experimentación y miden cuantitativamente la cantidad de materia
Conceptos basicos del equilibrio de quimico en medio acuoso
 Conceptos basicos del equilibrio de quimico en medio acuoso Elaborado por: Gustavo Gomez Sosa Facultad de Quimica UNAM QU ÍM IC A A N A LÍTIC A I C LAV E 1402 G rupo 4, s em es tre 2010-2 CONCEPTOS BASICOS
Conceptos basicos del equilibrio de quimico en medio acuoso Elaborado por: Gustavo Gomez Sosa Facultad de Quimica UNAM QU ÍM IC A A N A LÍTIC A I C LAV E 1402 G rupo 4, s em es tre 2010-2 CONCEPTOS BASICOS
DISCUSION DE RESULTADOS. Los resultados reportados para los catalizadores por la técnica de
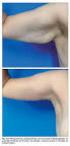 DISCUSION DE RESULTADOS Los resultados reportados para los catalizadores por la técnica de Absorción Atómica indica que los contenidos metálicos de las muestras preparadas son similares a los valores nominales,
DISCUSION DE RESULTADOS Los resultados reportados para los catalizadores por la técnica de Absorción Atómica indica que los contenidos metálicos de las muestras preparadas son similares a los valores nominales,
- Leyes ponderales: Las leyes ponderales relacionan las masas de las sustancias que intervienen en una reacción química.
 FÍSICA Y QUÍMICA 4ºESO COLEGIO GIBRALJAIRE CÁLCULOS QUÍMICOS 1.- LA REACCIÓN QUÍMICA. LEYES PONDERALES Una reacción química es el proceso en el que, mediante una reorganización de enlaces y átomos, una
FÍSICA Y QUÍMICA 4ºESO COLEGIO GIBRALJAIRE CÁLCULOS QUÍMICOS 1.- LA REACCIÓN QUÍMICA. LEYES PONDERALES Una reacción química es el proceso en el que, mediante una reorganización de enlaces y átomos, una
TRABAJO PRÁCTICO N 0 3 TERMOQUÍMICA
 TRABAJO PRÁCTICO N 0 3 TERMOQUÍMICA OBJETIVOS Determinación de la variación de entalpía asociada a procesos químicos. Aplicación de conceptos termodinámicos: temperatura, calor, entalpía. Verificación
TRABAJO PRÁCTICO N 0 3 TERMOQUÍMICA OBJETIVOS Determinación de la variación de entalpía asociada a procesos químicos. Aplicación de conceptos termodinámicos: temperatura, calor, entalpía. Verificación
CINÉTICA QUÍMICA DETERMINACIÓN DEL ORDEN DE REACCIÓN Y ENERGÍA DE ACTIVACIÓN
 II PRÁCTICA 2 CINÉTICA QUÍMICA DETERMINACIÓN DEL ORDEN DE REACCIÓN Y ENERGÍA DE ACTIVACIÓN En esta experiencia comprobaremos la influencia de la concentración de los reactivos, de la temperatura, y de
II PRÁCTICA 2 CINÉTICA QUÍMICA DETERMINACIÓN DEL ORDEN DE REACCIÓN Y ENERGÍA DE ACTIVACIÓN En esta experiencia comprobaremos la influencia de la concentración de los reactivos, de la temperatura, y de
Área Académica de: Química
 Área Académica de: Química Línea de Investigación: Química-física teórica de soluciones y superficies: Síntesis, caracterización y evaluación de catalizadores de hidrotratamiento de petróleo y abatimiento
Área Académica de: Química Línea de Investigación: Química-física teórica de soluciones y superficies: Síntesis, caracterización y evaluación de catalizadores de hidrotratamiento de petróleo y abatimiento
Unidad 16: Temperatura y gases ideales
 Apoyo para la preparación de los estudios de Ingeniería y Arquitectura Física (Preparación a la Universidad) Unidad 16: Temperatura y gases ideales Universidad Politécnica de Madrid 14 de abril de 2010
Apoyo para la preparación de los estudios de Ingeniería y Arquitectura Física (Preparación a la Universidad) Unidad 16: Temperatura y gases ideales Universidad Politécnica de Madrid 14 de abril de 2010
Maestría en Ciencia y Tecnología Ambiental
 Maestría en Ciencia y Tecnología Ambiental Temario: Química Propósito general: Proporcionar y estandarizar el conocimiento básico de química a los candidatos para ingresar al programa de Maestría en Ciencia
Maestría en Ciencia y Tecnología Ambiental Temario: Química Propósito general: Proporcionar y estandarizar el conocimiento básico de química a los candidatos para ingresar al programa de Maestría en Ciencia
Determinación de la concentración micelar crítica (cmc) y grado de disociación (α) de un tensioactivo iónico mediante medidas de conductividad
 Determinación de la concentración micelar crítica (cmc) y grado de disociación (α) de un tensioactivo iónico mediante medidas de conductividad OBJETIVO: Determinación de la concentración micelar crítica
Determinación de la concentración micelar crítica (cmc) y grado de disociación (α) de un tensioactivo iónico mediante medidas de conductividad OBJETIVO: Determinación de la concentración micelar crítica
Composición química de los seres vivos
 Composición química de los seres vivos Elementos químicos de la materia viva BIOELEMENTOS Se clasifican por su abundancia En proporcion superior al 96% PRIMARIOS En una proporción aprox. 3,9% SECUNDARIOS
Composición química de los seres vivos Elementos químicos de la materia viva BIOELEMENTOS Se clasifican por su abundancia En proporcion superior al 96% PRIMARIOS En una proporción aprox. 3,9% SECUNDARIOS
2. Disoluciones. Química (1S, Grado Biología) UAM
 2. Disoluciones Química (1S, Grado Biología) UAM 2. Disoluciones Contenidos Tipos de disoluciones Expresiones de la concentración Dilución ropiedades coligativas de las disoluciones resión de vapor [de
2. Disoluciones Química (1S, Grado Biología) UAM 2. Disoluciones Contenidos Tipos de disoluciones Expresiones de la concentración Dilución ropiedades coligativas de las disoluciones resión de vapor [de
QUÉ ES LA TEMPERATURA?
 1 QUÉ ES LA TEMPERATURA? Nosotros experimentamos la temperatura todos los días. Cuando estamos en verano, generalmente decimos Hace calor! y en invierno Hace mucho frío!. Los términos que frecuentemente
1 QUÉ ES LA TEMPERATURA? Nosotros experimentamos la temperatura todos los días. Cuando estamos en verano, generalmente decimos Hace calor! y en invierno Hace mucho frío!. Los términos que frecuentemente
Mediciones Confiables con Termómetros de Resistencia i de Platino. Edgar Méndez Lango
 Mediciones Confiables con Termómetros de Resistencia i de Platino Edgar Méndez Lango Termometría, Metrología Eléctrica, CENAM Noviembre 2009 Contenido 2 1. Concepto de temperatura 2. La Escala Internacional
Mediciones Confiables con Termómetros de Resistencia i de Platino Edgar Méndez Lango Termometría, Metrología Eléctrica, CENAM Noviembre 2009 Contenido 2 1. Concepto de temperatura 2. La Escala Internacional
Bioenergética e introducción al metabolismo Departamento de Bioquímica Noviembre de 2005
 U.T.I. Biología Celular Bioenergética e introducción al metabolismo Departamento de Bioquímica Noviembre de 2005 Definiciones LA TERMODINAMICA ES LA CIENCIA QUE ESTUDIA LA ENERGIA Y SUS TRANSFORMACIONES
U.T.I. Biología Celular Bioenergética e introducción al metabolismo Departamento de Bioquímica Noviembre de 2005 Definiciones LA TERMODINAMICA ES LA CIENCIA QUE ESTUDIA LA ENERGIA Y SUS TRANSFORMACIONES
6 APENDICE. A. Curvas de Calibración
 6 APENDICE A. Curvas de Calibración Las muestras colectadas en las hidrólisis contenían básicamente carbohidratos como, glucosa, xilosa y arabinosa, entre otros. Se realizaron curvas de calibración para
6 APENDICE A. Curvas de Calibración Las muestras colectadas en las hidrólisis contenían básicamente carbohidratos como, glucosa, xilosa y arabinosa, entre otros. Se realizaron curvas de calibración para
QUÍMICA FÍSICA II Grupo A. Tercer control, 10 de mayo de Escoged 2 de las 3 preguntas que os propongo, cada una de las preguntas vale 5 puntos.
 QUÍMICA FÍSICA II Grupo A. Tercer control, 10 de mayo de 2011 Escoged 2 de las 3 preguntas que os propongo, cada una de las preguntas vale 5 puntos. 1. Qué significado tienen los parámetros termodinámicos
QUÍMICA FÍSICA II Grupo A. Tercer control, 10 de mayo de 2011 Escoged 2 de las 3 preguntas que os propongo, cada una de las preguntas vale 5 puntos. 1. Qué significado tienen los parámetros termodinámicos
QUÍMICA. La MATERIA REPRESENTACIÓN. Observación Datos Ley Hipótesis Teoría DEFINICIONES BÁSICAS. Propiedades
 QUÍMICA La MATERIA Relación constante TEORÍA EXPERIMENTACIÓN Ciencia básica - Estructura - Composición - Propiedades - Transformaciones REPRESENTACIÓN OBSERVACIÓN mundo macroscópico Técnica sistemática
QUÍMICA La MATERIA Relación constante TEORÍA EXPERIMENTACIÓN Ciencia básica - Estructura - Composición - Propiedades - Transformaciones REPRESENTACIÓN OBSERVACIÓN mundo macroscópico Técnica sistemática
Balance de masa con reacción química. Balances de masa con reacción química en reactores discontinuos y continuos.
 Balance de masa con química. Balances de masa con química en reactores discontinuos y continuos. La aparición de una química en un proceso impone las restricciones adicionales dadas por la ecuación estequiométrica
Balance de masa con química. Balances de masa con química en reactores discontinuos y continuos. La aparición de una química en un proceso impone las restricciones adicionales dadas por la ecuación estequiométrica
UNIDAD 1 La materia y sus cambios
 UNIDAD 1 La materia y sus cambios Tema 1.3 Propiedades características de las sustancias: físicas, organolépticas, químicas; intensivas y extensivas. NMLV 1 Propiedades de las sustancias Organolépticas
UNIDAD 1 La materia y sus cambios Tema 1.3 Propiedades características de las sustancias: físicas, organolépticas, químicas; intensivas y extensivas. NMLV 1 Propiedades de las sustancias Organolépticas
TRAZABILIDAD DE LAS MEDICIONES DE VISCOSIDAD
 TRAZABILIDAD DE LAS MEDICIONES DE VISCOSIDAD Sonia Trujillo Juárez, Raul Molina Mercado Centro Nacional de Metrología km 4,5 carr. a los Cués, Mpio del Marqués, Qro (44) -05-00, sonia.trujillo@cenam.mx,
TRAZABILIDAD DE LAS MEDICIONES DE VISCOSIDAD Sonia Trujillo Juárez, Raul Molina Mercado Centro Nacional de Metrología km 4,5 carr. a los Cués, Mpio del Marqués, Qro (44) -05-00, sonia.trujillo@cenam.mx,
FORMAS MÁS COMUNES DE EXPRESAR LA CONCENTRACIÓN:
 CÁTEDRA: QUÍMICA GUÍA DE PROBLEMAS Nº 4 TEMA: ESTEQUIOMETRÍA DE SOLUCIONES OBJETIVOS: Resolver problemas basados en la estequiometría de las soluciones, ampliando los conocimientos para ser aplicados criteriosamente
CÁTEDRA: QUÍMICA GUÍA DE PROBLEMAS Nº 4 TEMA: ESTEQUIOMETRÍA DE SOLUCIONES OBJETIVOS: Resolver problemas basados en la estequiometría de las soluciones, ampliando los conocimientos para ser aplicados criteriosamente
Contenidos mínimos Física y Química 3º ESO
 Contenidos mínimos Física y Química 3º ESO EL TRABAJO CIENTÍFICO Etapas del método científico. Magnitudes y unidades. Cambio de unidades. Sistema Internacional de Unidades (SI). Representación de gráficas
Contenidos mínimos Física y Química 3º ESO EL TRABAJO CIENTÍFICO Etapas del método científico. Magnitudes y unidades. Cambio de unidades. Sistema Internacional de Unidades (SI). Representación de gráficas
MAGNITUDES MOLARES COMPOSICIÓN DE LAS DISOLUCIONES. Actividad 7. Actividad 1. Actividad 8. Actividad 2. Actividad 9. Actividad 3.
 MAGNITUDES MOLARES {Respuesta: [a] 0, mol; [b] 0,82 mol; [c] 0,56 mol} Actividad [a] En qué se parecen y en qué se diferencian las siguientes magnitudes: masa molecular relativa y masa molar? [b] Calcula
MAGNITUDES MOLARES {Respuesta: [a] 0, mol; [b] 0,82 mol; [c] 0,56 mol} Actividad [a] En qué se parecen y en qué se diferencian las siguientes magnitudes: masa molecular relativa y masa molar? [b] Calcula
DETERMINACIÓN DE LA CONSTANTE UNIVERSAL DE LOS GASES
 DETERMINACIÓN DE LA CONSTANTE UNIERSAL DE LOS GASES La ley general de los gases relaciona la presión P, el volumen, la temperatura T, el número de moles n, y la constante universal de los gases R, como
DETERMINACIÓN DE LA CONSTANTE UNIERSAL DE LOS GASES La ley general de los gases relaciona la presión P, el volumen, la temperatura T, el número de moles n, y la constante universal de los gases R, como
Problemas resueltos de disoluciones y sus diferentes medidas de concentración.
 UNIVERSIDAD CENTRAL DE VENEZUELA FACULTAD DE CIENCIAS ESCUELA DE QUÍMICA Problemas resueltos de disoluciones y sus diferentes medidas de concentración. 1. Qué es una disolución? Una disolución consiste
UNIVERSIDAD CENTRAL DE VENEZUELA FACULTAD DE CIENCIAS ESCUELA DE QUÍMICA Problemas resueltos de disoluciones y sus diferentes medidas de concentración. 1. Qué es una disolución? Una disolución consiste
La Química Analítica nos permite medir, monitorear o caracterizar una, varias especies o procesos químicos para la resolución de diversos problemas:
 QUÍMICA ANALÍTICA I Documento de apoyo (1) : Formación de soluciones analíticas. Dr. Alejandro Baeza. Semestre 2010-II. Antecedentes La Química Analítica nos permite medir, monitorear o caracterizar una,
QUÍMICA ANALÍTICA I Documento de apoyo (1) : Formación de soluciones analíticas. Dr. Alejandro Baeza. Semestre 2010-II. Antecedentes La Química Analítica nos permite medir, monitorear o caracterizar una,
Profesora: Teresa Esparza Araña ASPECTOS CUANTITATIVOS DE LA QUÍMICA. UNIDAD 2: Los gases ideales
 Departamento de Física y Química Profesora: Teresa Esparza Araña CEAD P. Félix Pérez Parrilla ASPECTOS CUANTITATIVOS DE LA QUÍMICA UNIDAD 2: Los gases ideales ÍNDICE 1. LOS GASES SEGÚN LA TEORÍA CINÉTICA
Departamento de Física y Química Profesora: Teresa Esparza Araña CEAD P. Félix Pérez Parrilla ASPECTOS CUANTITATIVOS DE LA QUÍMICA UNIDAD 2: Los gases ideales ÍNDICE 1. LOS GASES SEGÚN LA TEORÍA CINÉTICA
CAPÍTULO 4 RESULTADOS Y DISCUSIÓN
 CAPÍTULO 4 RESULTADOS Y DISCUSIÓN 4.1 Verificación del código numérico Para verificar el código numérico, el cual simula la convección natural en una cavidad abierta considerando propiedades variables,
CAPÍTULO 4 RESULTADOS Y DISCUSIÓN 4.1 Verificación del código numérico Para verificar el código numérico, el cual simula la convección natural en una cavidad abierta considerando propiedades variables,
CRITERIOS DE ESPONTANEIDAD
 CRITERIOS DE ESPONTANEIDAD Con ayuda de la Primera Ley de la Termodinámica podemos considerar el equilibrio de la energía y con La Segunda Ley podemos decidir que procesos pueden ocurrir de manera espontanea,
CRITERIOS DE ESPONTANEIDAD Con ayuda de la Primera Ley de la Termodinámica podemos considerar el equilibrio de la energía y con La Segunda Ley podemos decidir que procesos pueden ocurrir de manera espontanea,
Profesora: Teresa Esparza Araña LA CANTIDAD DE SUSTANCIA EN QUÍMICA. UNIDAD 6: Los gases ideales
 Departamento de Física y Química Profesora: Teresa Esparza Araña CEAD P. Félix Pérez Parrilla LA CANTIDAD DE SUSTANCIA EN QUÍMICA UNIDAD 6: Los gases ideales 1. LOS GASES SEGÚN LA TEORÍA CINÉTICA DE LA
Departamento de Física y Química Profesora: Teresa Esparza Araña CEAD P. Félix Pérez Parrilla LA CANTIDAD DE SUSTANCIA EN QUÍMICA UNIDAD 6: Los gases ideales 1. LOS GASES SEGÚN LA TEORÍA CINÉTICA DE LA
Ley de enfriamiento de Newton considerando reservorios finitos
 Ley de enfriamiento de Newton considerando reservorios finitos María ecilia Molas, Florencia Rodriguez Riou y Débora Leibovich Facultad de Ingeniería, iencias Exactas y Naturales Universidad Favaloro,.
Ley de enfriamiento de Newton considerando reservorios finitos María ecilia Molas, Florencia Rodriguez Riou y Débora Leibovich Facultad de Ingeniería, iencias Exactas y Naturales Universidad Favaloro,.
DESARROLLO DE UN PROGRAMA DE CÁLCULO PARA PROPIEDADES FÍSICAS DEL AIRE RELACIONADAS CON LA HUMEDAD
 DESARROLLO DE UN PROGRAMA DE CÁLCULO PARA PROPIEDADES FÍSICAS DEL AIRE RELACIONADAS CON LA HUMEDAD 1 Enrique Martines López, 2 Israel E. Alvarado Ramírez 1 Centro Nacional de Metrología, División de Termometría
DESARROLLO DE UN PROGRAMA DE CÁLCULO PARA PROPIEDADES FÍSICAS DEL AIRE RELACIONADAS CON LA HUMEDAD 1 Enrique Martines López, 2 Israel E. Alvarado Ramírez 1 Centro Nacional de Metrología, División de Termometría
Actividad: Cómo ocurren las reacciones químicas?
 Cinética química Cómo ocurren las reacciones químicas? Nivel: 3º Medio Subsector: Ciencias químicas Unidad temática: Cinética Actividad: Cómo ocurren las reacciones químicas? Qué es la cinética de una
Cinética química Cómo ocurren las reacciones químicas? Nivel: 3º Medio Subsector: Ciencias químicas Unidad temática: Cinética Actividad: Cómo ocurren las reacciones químicas? Qué es la cinética de una
TEMA 6 MEZCLAS Y DISOLUCIONES
 TEMA 6 MEZCLAS Y DISOLUCIONES 1 Contenidos: 1. Tipos de disoluciones 2. El proceso de disolución 3. Formas de expresar la concentración. 4. Solubilidad. Factores que afectan a la solubilidad 5. Propiedades
TEMA 6 MEZCLAS Y DISOLUCIONES 1 Contenidos: 1. Tipos de disoluciones 2. El proceso de disolución 3. Formas de expresar la concentración. 4. Solubilidad. Factores que afectan a la solubilidad 5. Propiedades
PRÁCTICO 3: SOLUCIONES
 Curso de Laboratorio Página: 1/6 DEPARTAMENTO ESTRELLA CAMPOS PRÁCTICO 3: SOLUCIONES Bibliografía: Química, La Ciencia Central, T.L. Brown, H.E.LeMay, Jr., B.Bursten; Ed. Prentice-Hall Hispanoamericana,
Curso de Laboratorio Página: 1/6 DEPARTAMENTO ESTRELLA CAMPOS PRÁCTICO 3: SOLUCIONES Bibliografía: Química, La Ciencia Central, T.L. Brown, H.E.LeMay, Jr., B.Bursten; Ed. Prentice-Hall Hispanoamericana,
ESTRUCTURA DE COMPUESTOS ORGÁNICOS
 ESTRUCTURA DE COMPUESTOS ORGÁNICOS La Química orgánica es el estudio de los compuestos que contienen carbono, en química inorgánica se estudian todos los demás elementos y compuestos. La cantidad de compuestos
ESTRUCTURA DE COMPUESTOS ORGÁNICOS La Química orgánica es el estudio de los compuestos que contienen carbono, en química inorgánica se estudian todos los demás elementos y compuestos. La cantidad de compuestos
[ A ], [ B ]...: concentraciones molares de los reactivos en un momento dado.
![[ A ], [ B ]...: concentraciones molares de los reactivos en un momento dado. [ A ], [ B ]...: concentraciones molares de los reactivos en un momento dado.](/thumbs/49/25484895.jpg) VELOCIDAD MEDIA DE UNA REACCIÓN aa + b B c C + d D [ A] [ B] [ C] [ D] Vmedia = = = = a b c d A Velocidad de disminución de los reactivos: a Velocidad de aumento de los productos: ECUACIÓN DE VELOCIDAD
VELOCIDAD MEDIA DE UNA REACCIÓN aa + b B c C + d D [ A] [ B] [ C] [ D] Vmedia = = = = a b c d A Velocidad de disminución de los reactivos: a Velocidad de aumento de los productos: ECUACIÓN DE VELOCIDAD
PLANEACIÓN DEL CONTENIDO DE CURSO
 FACULTAD DE CIENCIAS BÁSICAS PROGRAMA DE QUÍMICA PÁGINA: 1 de 5 PLANEACIÓN DEL CONTENIDO DE CURSO 1. IDENTIFICACIÓN DEL CURSO NOMBRE : FISICOQUÍMICA I CÓDIGO : 23409 SEMESTRE : 5 NUMERO DE CRÉDITOS : 5
FACULTAD DE CIENCIAS BÁSICAS PROGRAMA DE QUÍMICA PÁGINA: 1 de 5 PLANEACIÓN DEL CONTENIDO DE CURSO 1. IDENTIFICACIÓN DEL CURSO NOMBRE : FISICOQUÍMICA I CÓDIGO : 23409 SEMESTRE : 5 NUMERO DE CRÉDITOS : 5
PREPARACIÓN Y CONDUCTIVIDAD DE DISOLUCIONES
 PREPARACIÓN Y CONDUCTIVIDAD DE DISOLUCIONES M. C. Q. Alfredo Velásquez Márquez Objetivos de la práctica El alumno: 1. Preparará disoluciones de diferentes concentraciones mediante el manejo del material
PREPARACIÓN Y CONDUCTIVIDAD DE DISOLUCIONES M. C. Q. Alfredo Velásquez Márquez Objetivos de la práctica El alumno: 1. Preparará disoluciones de diferentes concentraciones mediante el manejo del material
CONDUCTIVIDAD. Definición:
 CONDUCTIVIDAD Definición: La conductividad es la capacidad de una solución acuosa para conducir una corriente eléctrica. Es igual al recíproco de la resistividad de la solución. Las medidas de conductividad
CONDUCTIVIDAD Definición: La conductividad es la capacidad de una solución acuosa para conducir una corriente eléctrica. Es igual al recíproco de la resistividad de la solución. Las medidas de conductividad
Física y Química 1º Bach.
 Física y Química 1º Bach. Leyes de los gases. Teoría cinético-molecular 05/11/10 DEPARTAMENTO FÍSICA E QUÍMICA Nombre: OPCIÓN 1 1. Observa el aparato de la Figura. Si la temperatura del aceite se eleva
Física y Química 1º Bach. Leyes de los gases. Teoría cinético-molecular 05/11/10 DEPARTAMENTO FÍSICA E QUÍMICA Nombre: OPCIÓN 1 1. Observa el aparato de la Figura. Si la temperatura del aceite se eleva
CLASIFICACIÓN DE LA MATERIA
 1. Clasificación de la materia por su aspecto CLASIFICACIÓN DE LA MATERIA La materia homogénea es la que presenta un aspecto uniforme, en la cual no se pueden distinguir a simple vista sus componentes.
1. Clasificación de la materia por su aspecto CLASIFICACIÓN DE LA MATERIA La materia homogénea es la que presenta un aspecto uniforme, en la cual no se pueden distinguir a simple vista sus componentes.
3. PROPIEDADES Y ESTADOS
 3. PROPIEDADES Y ESTADOS 3.1 LOS CONCEPTOS DE PROPIEDAD Y ESTADO La propiedad es cualquier característica o atributo que se puede evaluar cuantitativamente El volumen La masa La energía La temperatura
3. PROPIEDADES Y ESTADOS 3.1 LOS CONCEPTOS DE PROPIEDAD Y ESTADO La propiedad es cualquier característica o atributo que se puede evaluar cuantitativamente El volumen La masa La energía La temperatura
TRANSPORTE A TRAVÉS DE LA MEMBRANA CELULAR
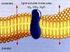 TRANSPORTE A TRAVÉS DE LA MEMBRANA CELULAR Introducción Compartimientos Acuosos separados por Barreras Biológicas Organelos selectivos, autocatalíticos, autoreproductivos, competitivos, adaptativos...
TRANSPORTE A TRAVÉS DE LA MEMBRANA CELULAR Introducción Compartimientos Acuosos separados por Barreras Biológicas Organelos selectivos, autocatalíticos, autoreproductivos, competitivos, adaptativos...
TEMA 2: LEYES Y CONCEPTOS BÁSICOS EN QUÍMICA
 1. SUSTANCIAS PURAS Y MEZCLAS 2. LEYES PONDERALES DE LAS COMBINACIONES QUÍMICAS 2.1. LEY DE CONSERVACIÓN DE LA MATERIA Enunciada en 1783 por Lavoisier: La materia ni se crea ni se destruye, únicamente
1. SUSTANCIAS PURAS Y MEZCLAS 2. LEYES PONDERALES DE LAS COMBINACIONES QUÍMICAS 2.1. LEY DE CONSERVACIÓN DE LA MATERIA Enunciada en 1783 por Lavoisier: La materia ni se crea ni se destruye, únicamente
Objetivos: Principal: Investigar las propiedades de un gas a presión constante. Secundario: Determinar la tasa de enfriamiento de un cuerpo.
 ! " # $ %& ' () ) Objetivos: Principal: Investigar las propiedades de un gas a presión constante. Secundario: Determinar la tasa de enfriamiento de un cuerpo. Conceptos a afianzar: Descripción termodinámica
! " # $ %& ' () ) Objetivos: Principal: Investigar las propiedades de un gas a presión constante. Secundario: Determinar la tasa de enfriamiento de un cuerpo. Conceptos a afianzar: Descripción termodinámica
LEYES DE LOS GASES. Leyes de los gases. Leyes de los gases
 LEYES DE LOS GASES Estado gaseoso Medidas en gases Ley de Avogadro Ley de Boyle y Mariotte Ley de Charles y Gay-Lussac (1ª) Ley de Charles y Gay-Lussac (2ª) Ecuación n general de los gases ideales Teoría
LEYES DE LOS GASES Estado gaseoso Medidas en gases Ley de Avogadro Ley de Boyle y Mariotte Ley de Charles y Gay-Lussac (1ª) Ley de Charles y Gay-Lussac (2ª) Ecuación n general de los gases ideales Teoría
DESARROLLO COGNOSCITIVO Y APRENDIZAJE
 Prof. Jhonis Valbuena Cátedra: Análisis Instrumental La Electrofóresis es un método de la Química Analítica que utiliza corriente eléctrica controlada con la finalidad de separar biomolèculas según su
Prof. Jhonis Valbuena Cátedra: Análisis Instrumental La Electrofóresis es un método de la Química Analítica que utiliza corriente eléctrica controlada con la finalidad de separar biomolèculas según su
Colegio San Lorenzo - Copiapó - Región de Atacama Per Laborem ad Lucem
 TEMARIO EXAMENES QUIMICA 2012 7º BASICO Descubrimiento del átomo: Quién lo descubrió y su significado Estructura atómica: Partes del átomo, características del núcleo y la corteza, cálculo del protón,
TEMARIO EXAMENES QUIMICA 2012 7º BASICO Descubrimiento del átomo: Quién lo descubrió y su significado Estructura atómica: Partes del átomo, características del núcleo y la corteza, cálculo del protón,
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2007 QUÍMICA TEMA 1: LA TRANSFORMACIÓN QUÍMICA
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 007 QUÍMICA TEMA 1: LA TRANSFORMACIÓN QUÍMICA Junio, Ejercicio 4, Opción A Junio, Ejercicio 5, Opción B Reserva 1, Ejercicio, Opción B Reserva, Ejercicio 5, Opción
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 007 QUÍMICA TEMA 1: LA TRANSFORMACIÓN QUÍMICA Junio, Ejercicio 4, Opción A Junio, Ejercicio 5, Opción B Reserva 1, Ejercicio, Opción B Reserva, Ejercicio 5, Opción
PREGUNTAS DE SELECCIÓN MÚLTIPLE CON ÚNICA RESPUESTA (TIPO 1)
 PREGUNTAS DE SELECCIÓN MÚLTIPLE CON ÚNICA RESPUESTA (TIPO 1) Un gas es sometido a tres procesos identificados con las letras X, Y y Z. Estos procesos son esquematizados en los gráficos que se presentan
PREGUNTAS DE SELECCIÓN MÚLTIPLE CON ÚNICA RESPUESTA (TIPO 1) Un gas es sometido a tres procesos identificados con las letras X, Y y Z. Estos procesos son esquematizados en los gráficos que se presentan
QUÍMICA de 2º de BACHILLERATO EL EQUILIBRIO QUÍMICO
 QUÍMICA de 2º de BACHILLERATO EL EQUILIBRIO QUÍMICO PROBLEMAS RESUELTOS QUE HAN SIDO PROPUESTOS EN LOS EXÁMENES DE LAS PRUEBAS DE ACCESO A ESTUDIOS UNIVERSITARIOS EN LA COMUNIDAD DE MADRID (1996 2010)
QUÍMICA de 2º de BACHILLERATO EL EQUILIBRIO QUÍMICO PROBLEMAS RESUELTOS QUE HAN SIDO PROPUESTOS EN LOS EXÁMENES DE LAS PRUEBAS DE ACCESO A ESTUDIOS UNIVERSITARIOS EN LA COMUNIDAD DE MADRID (1996 2010)
ANÁLISIS CUANTITATIVO POR WDFRX
 ANÁLISIS CUANTITATIVO POR WDFRX El análisis cuantitativo se obtiene mediante la medida de las intensidades de las energías emitidas por la muestra. Siendo la intensidad de la emisión (número de fotones)
ANÁLISIS CUANTITATIVO POR WDFRX El análisis cuantitativo se obtiene mediante la medida de las intensidades de las energías emitidas por la muestra. Siendo la intensidad de la emisión (número de fotones)
Diagrama de fases Sn-Pb
 Práctica 4 Diagrama de fases Sn-Pb Objetivo Determinación del diagrama de fases Temperatura vs. Composición, a presión atmosférica, de la aleación Estaño - Plomo. Fundamento teórico Casi todos los metales
Práctica 4 Diagrama de fases Sn-Pb Objetivo Determinación del diagrama de fases Temperatura vs. Composición, a presión atmosférica, de la aleación Estaño - Plomo. Fundamento teórico Casi todos los metales
Ejercicios relacionados con líquidos y sólidos
 Ejercicios relacionados con líquidos y sólidos. La presión de vapor del etanol es de 35,3 mmhg a 40 o C y 542,5 mmhg a 70 o C. Calcular el calor molar de vaporización y la presión del etanol a 50 o C.
Ejercicios relacionados con líquidos y sólidos. La presión de vapor del etanol es de 35,3 mmhg a 40 o C y 542,5 mmhg a 70 o C. Calcular el calor molar de vaporización y la presión del etanol a 50 o C.
13. REACTOR CSTR. X r
 13. REACTOR CSTR 1. OBJETIVOS 1.1. Definir paquetes fluidos que incluyan reacciones de tipo cinético 1.2. Determinar los grados de libertad requeridos para simular un reactor CSTR de tipo cinético 1.3.
13. REACTOR CSTR 1. OBJETIVOS 1.1. Definir paquetes fluidos que incluyan reacciones de tipo cinético 1.2. Determinar los grados de libertad requeridos para simular un reactor CSTR de tipo cinético 1.3.
Teoría Disoluciones Fórmula empírica y molecular Física y Química. 1º bachiller DISOLUCIONES
 Teoría Disoluciones Fórmula empírica y molecular Física y Química. 1º bachiller 18-1-2015 CONCEPTO DE DISOLUCIÓN DISOLUCIONES Una disolución es una mezcla homogénea de sustancias en igual o distintos estados
Teoría Disoluciones Fórmula empírica y molecular Física y Química. 1º bachiller 18-1-2015 CONCEPTO DE DISOLUCIÓN DISOLUCIONES Una disolución es una mezcla homogénea de sustancias en igual o distintos estados
Molaridad y molalidad
 Molaridad y molalidad Apellidos, nombre Atarés Huerta, Lorena (loathue@tal.upv.es) Departamento Centro Departamento de Tecnología de Alimentos ETSIAMN (Universidad Politécnica de Valencia) 1 Resumen de
Molaridad y molalidad Apellidos, nombre Atarés Huerta, Lorena (loathue@tal.upv.es) Departamento Centro Departamento de Tecnología de Alimentos ETSIAMN (Universidad Politécnica de Valencia) 1 Resumen de
Resultado de aprendizaje:
 Objetivo: Describir composición y arquitectura de las membranas biológicas Resultado de aprendizaje: Explicar la dinámica de las membranas biologicas y su implicación funcional. INTRODUCCION La mayoría
Objetivo: Describir composición y arquitectura de las membranas biológicas Resultado de aprendizaje: Explicar la dinámica de las membranas biologicas y su implicación funcional. INTRODUCCION La mayoría
Manual de Prácticas. Práctica número 2 Propiedades de las sustancias
 Práctica número 2 Propiedades de las sustancias Tema Correspondiente: Conceptos básicos Nombre del Profesor: Nombre completo del alumno Firma N de brigada: Fecha de elaboración: Grupo: Elaborado por: Revisado
Práctica número 2 Propiedades de las sustancias Tema Correspondiente: Conceptos básicos Nombre del Profesor: Nombre completo del alumno Firma N de brigada: Fecha de elaboración: Grupo: Elaborado por: Revisado
