Fisiología y farmacología neuromusculares
|
|
|
- Felisa Pereyra Castellanos
- hace 6 años
- Vistas:
Transcripción
1 Capítulo 18 Fisiología y farmacología neuromusculares J. A. JEEVENDRA MARTYN P u n t o s c l a v e La unión neuromuscular está formada por la terminación nerviosa distal, la hendidura sináptica y la placa terminal muscular, y tiene una disposición ordenada de receptores y sustratos para la acción de los fármacos. La transmisión neuromuscular depende predominantemente de la acetilcolina como transmisor natural. Cuando se libera en la terminación nerviosa presináptica, la acetilcolina se une a los receptores característicos de acetilcolina (RACh) dispuestos a nivel presináptico o postsináptico en la unión neuromuscular, y dependiendo de su composición estructural, se clasifican en subtipo de RACh muscular o una variedad del subtipo de RACh neuronal. Los relajantes musculares tienen múltiples zonas de acción. Aunque en el caso de los relajantes musculares despolarizantes y no despolarizantes (RMND) sus principales acciones se producen por mecanismos y en localizaciones descritas como agonistas y antagonistas sobre los receptores postsinápticos, esta descripción de la acción farmacológica neuromuscular es simplista. Los RMND impiden la transmisión neuromuscular porque impiden el acceso de acetilcolina a su zona de reconocimiento preferible en los RACh nicotínicos postsinápticos. Cuando aumentan las concentraciones de RMND, se superpone otra acción no competitiva el bloqueo de canales iónicos. Los efectos paralizantes postsinápticos de los relajantes musculares pueden intensificarse por su acción sobre los RACh presinápticos que modulan la liberación de acetilcolina. Esto último puede demostrarse como la atenuación que aparece al aumentar la frecuencia de estimulación. La atenuación también puede verse cuando se bloquean funcionalmente solo los RACh postsinápticos (p. ej., por bungarotoxina) o cuando el número de RACh está disminuido (p. ej., en la miastenia grave). Por tanto, la unión neuromuscular es un sistema complejo y dinámico en el cual los fenómenos producidos por los fármacos son acciones combinadas que varían con el fármaco, la dosis, la actividad en la terminación nerviosa y el músculo, el tiempo tras la administración, la presencia de anestésicos u otros fármacos, y la edad y el estado del paciente. La inhibición de la enzima muscular acetilcolinesterasa por anticolinesterásicos (p. ej., neostigmina) aumenta la concentración de acetilcolina, que puede competir con los RMND y desplazarlos, revirtiendo así la parálisis. Estos fármacos anticolinesterásicos (p. ej., neostigmina) tienen también otros efectos sobre las terminaciones nerviosas y sobre el receptor, mediante un mecanismo alostérico. La administración en bolo o prolongada de anticolinesterásicos puede tener efectos perjudiciales sobre la función neuromuscular en pacientes por lo demás sanos. Una clase nueva e innovadora de compuestos que revierte la parálisis solo de los relajantes musculares esteroideos es una ciclodextrina modificada, sugammadex, que actúa encapsulando este tipo de compuestos. Los compuestos despolarizantes (p. ej., succinilcolina) reaccionan inicialmente con la zona de reconocimiento de acetilcolina y, al igual que el transmisor, abren los canales iónicos del RACh durante la despolarización de la membrana de la placa terminal. Al contrario que el transmisor, no son objeto de hidrólisis por acetilcolinesterasa y por ello permanecen en la unión. Poco después de la administración de succinilcolina, algunos receptores se desensibilizan y, aunque estén ocupados por el agonista, no se abren ni permiten el flujo de corriente para despolarizar el área de la membrana muscular. Si el relajante despolarizante se administra en una concentración superior a la habitual o se permite que permanezca en la unión por mucho tiempo, entonces Elsevier España, S.L.U. Reservados todos los derechos 423
2 424 PARTE II: Fisiología anestésica P u n t o s c l a v e ( cont.) aparecen otros efectos. Los relajantes despolarizantes tienen efectos sobre las estructuras presinápticas, y la combinación de efectos presinápticos y postsinápticos más los efectos secundarios sobre la homeostasis del músculo y el nervio da lugar a un fenómeno complejo conocido como bloqueo de fase II. La intensa investigación en el campo de la transmisión neuromuscular continúa a un ritmo rápido. Las observaciones más novedosas sobre los tipos musculares y neuronales de RACh, los canales iónicos, las membranas y la función presináptica revelan un alcance mucho más amplio de las zonas y mecanismos de acción de los agonistas y antagonistas. Algunos otros fármacos usados clínicamente (p. ej., toxina botulínica) tienen efectos sobre el nervio y, por tanto, indirectamente sobre el músculo. La infección sistémica por toxinas de Clostridium (C. botulinum, gangrena gaseosa) puede producir parálisis sistémica como consecuencia de la disminución de liberación de acetilcolina en la terminación nerviosa. Los RMND administrados incluso durante 12 h o por períodos prolongados pueden tener efectos sobre el receptor postsináptico y simular una desnervación (desnervación química). El magnesio administrado a mujeres con preeclampsia disminuye la liberación de acetilcolina, con la posibilidad de debilidad muscular en la madre o el recién nacido. Al reconocer estas localizaciones y mecanismos, empezamos a tener un conocimiento teórico más próximo que nos permite explicar los fenómenos observados cuando el ser humano vivo se expone a estos fármacos. Los trabajos actuales de investigación se han centrado en el control de la expresión del RACh en la membrana postsináptica en estado normal y patológico. La presencia o ausencia de isoformas maduras e inmaduras parece complicar más el asunto. En ciertos estados patológicos (p. ej., desnervación, ictus, sepsis, quemaduras, inmovilización, uso crónico de RMND) los RACh están regulados al alza, con un aumento de expresión de la isoforma inmadura. Más recientemente se ha identificado otra isoforma del RACh nicotínico en el músculo, el RACh neuronal a7, previamente descrito solo en tejidos neuronales. Estos receptores tienen diferentes propiedades funcionales y farmacológicas que los receptores postsinápticos musculares convencionales. Las características funcionales y farmacológicas alteradas de los receptores inmaduros (subunidad g) y neuronales (subunidad a7) dan lugar a una mayor sensibilidad a la succinilcolina con hiperpotasemia y resistencia a los RMND. Un área de interés creciente es el control de expresión de las isoformas maduras del receptor frente a las otras dos isoformas (inmadura g y con subunidades a7). La expresión repetida de receptores inmaduros g y con subunidad a7 probablemente se relacione con señales aberrantes del factor de crecimiento. Las mutaciones genéticas del RACh que producen una apertura prolongada o rápida del canal pueden conducir a un estado de tipo miastenia, incluso en presencia de un número normal de receptores. La debilidad generalmente se relaciona con una despolarización ineficaz, con alteración del tiempo de apertura del canal, o con ambos. A pesar de que la neurotransmisión colinérgica a nivel de la unión neuromuscular es la sinapsis más ampliamente estudiada del sistema nervioso, todavía no se ha alcanzado un conocimiento completo de su funcionamiento. Esta es un área de continuo interés para muchos investigadores de todo el mundo. La fisiología de la transmisión neuromuscular se puede analizar y comprender de la manera más simple utilizando el modelo clásico de estimulación del nervio al músculo a través del receptor de acetilcolina (RACh). La unión neuromuscular del mamífero es la sinapsis prototipo y la que más se ha estudiado. Las investigaciones han proporcionado más información detallada sobre el proceso que, dentro del esquema clásico, puede modificar la neurotransmisión y la respuesta a los fármacos. Como ejemplo se puede señalar el papel de los cambios cuantitativos o cualitativos en los receptores de acetilcolina que modifican la neurotransmisión y la respuesta a los fármacos 1-3. En el caso de la miastenia grave, la disminución de receptores de acetilcolina produce un descenso en la eficacia de la neurotransmisión (y, por consiguiente, debilidad muscular) 4 y una sensibilidad alterada a los relajantes neuromusculares 3. Otro ejemplo es la importancia de los cambios relacionados con el nervio (presinápticos) que alteran la neurotransmisión y la respuesta a los fármacos anestésicos 5-7. Además, los relajantes musculares actúan de modos que no se enmarcan dentro del esquema clásico de un sitio de acción unitario. La observación de que los relajantes musculares pueden tener efectos presinápticos 5 o que algunos relajantes musculares no despolarizantes (RMND) pueden presentar también acciones estimulantes sobre el receptor 8 similares a los agonistas, mientras que otros poseen efectos no explicables por acciones de los músculos postsinápticas puras 9-11, ha proporcionado nuevas perspectivas a algunas observaciones que
3 Capítulo 18: Fisiología y farmacología neuromusculares 425 Elsevier. Fotocopiar sin autorización es un delito. hasta ese momento no se habían podido explicar. Aunque se sabe que los relajantes musculares tienen efectos sobre los receptores pre- y postsinápticos de la unión neuromuscular, la evidencia reciente indica que pueden reaccionar con otros receptores nicotínicos y muscarínicos distintos a los del músculo, como los receptores del seno carotídeo, del nervio vago en el corazón, o del músculo liso bronquial Aunque este esquema multifactorial de acción-respuesta complica la fisiología y la farmacología de la neurotransmisión, también aporta un conocimiento derivado de la experimentación que se acerca más a las observaciones clínicas. La introducción de técnicas potentes y contemporáneas en biología molecular, inmunología y electrofisiología, así como de técnicas más refinadas para la observación de la unión neuromuscular in vivo, es crucial para los conceptos básicos que se han desarrollado con relación a la transmisión neuromuscular 14. Estas técnicas han mejorado las aproximaciones farmacológica, química proteica, morfológica y citológica más tradicionales Los trabajos de investigación han aclarado el modo en el que la terminación nerviosa regula la síntesis y liberación del transmisor y la liberación de factores tróficos procesos ambos que controlan la función muscular y cómo estos procesos están influidos por sustancias exógenas y endógenas Se sigue investigando sobre cómo se sintetizan y anclan los receptores en la placa terminal, sobre qué papel tiene la terminación nerviosa en el proceso de maduración, y sobre la síntesis y control de la acetilcolinesterasa, la enzima que fragmenta la acetilcolina. Existen varias revisiones que aportan información detallada sobre estas áreas TRANSMISIÓN NEUROMUSCULAR La transmisión neuromuscular se produce por medio de un mecanismo bastante simple y directo. El nervio sintetiza acetilcolina y la acumula en paquetes pequeños de tamaño uniforme, denominados vesículas. La estimulación del nervio hace que estas vesículas migren a la superficie del nervio, se rompan y liberen la acetilcolina al interior de la hendidura que separa el nervio del músculo. Los receptores de acetilcolina en la placa terminal del músculo responden mediante la apertura de sus canales para la entrada de iones de sodio dentro del músculo para despolarizarlo. El potencial de placa terminal creado se prolonga a lo largo de la membrana muscular mediante la apertura de los canales de sodio que están presentes por toda la membrana muscular, para iniciar una contracción 16,17. La acetilcolina se despega inmediatamente del receptor y es destruida por la enzima acetilcolinesterasa, que se encuentra también en la hendidura. Sustancias como los relajantes despolarizantes o la nicotina y el carbacol (un análogo sintético de la acetilcolina que no se destruye por la acetilcolinesterasa) también pueden actuar sobre estos receptores, mimetizando el efecto de la acetilcolina, y causar despolarización de la placa terminal. Por consiguiente, a estos fármacos se hace referencia como agonistas del receptor, porque, al menos inicialmente, llevan al receptor a un estado activo. Los RMND también actúan sobre los receptores, aunque impiden la unión de la acetilcolina con el receptor, y de este modo evitan la despolarización por agonistas. Puesto que los RMND previenen la acción de los agonistas (p. ej., acetilcolina, carbacol y succinilcolina), pertenecen a la clase de compuestos conocidos como antagonistas de los RACh musculares. Otros compuestos, frecuentemente denominados fármacos que revierten o que son antagonistas de parálisis neuromuscular (p. ej., neostigmina y prostigmina), inhiben la enzima acetilcolinesterasa, impidiendo así la hidrólisis de la acetilcolina. La acumulación progresiva de acetilcolina sin degradar puede competir de forma efectiva con los RMND al desplazar a los últimos del receptor (es decir, por la ley de acción de masas) y antagonizar el efecto de los RMND. MORFOLOGÍA La unión neuromuscular está especializada en el lado nervioso y muscular para transmitir y recibir mensajes químicos Cada motoneurona discurre sin interrupción desde el asta anterior de la médula espinal hasta la unión neuromuscular como un axón largo mielinizado (fig. 18-1, A). Conforme se aproxima al músculo, se ramifica repetidamente para contactar con muchas células musculares, uniéndose a ellas en un grupo funcional conocido como unidad motora (fig. 18-1, B). La arquitectura de la terminación nerviosa es bastante diferente de la del resto del axón. Cuando la terminal alcanza la fibra muscular pierde su capa de mielina para formar una película de ramas terminales contra la superficie muscular y se cubre de células de Schwann. Esta disposición se ajusta a la arquitectura en el área sináptica de la membrana muscular (fig. 18-1, C). El nervio está separado de la superficie del músculo por un hueco de unos 20 nm, llamado hendidura sináptica o hendidura de la unión. El nervio y el músculo están sujetos en una alineación rígida por filamentos proteicos denominados lámina basal, los cuales abarcan la hendidura entre el nervio y la placa terminal. La superficie muscular tiene grandes ondulaciones, con invaginaciones profundas de la hendidura de la unión las hendiduras primarias y secundarias entre los pliegues en la membrana muscular; por tanto, la superficie total del área de la placa terminal es muy extensa. Las profundidades de los pliegues también varían según los tipos de músculos y especies. Las uniones neuromusculares humanas, en relación con el tamaño del músculo, son más pequeñas que las del ratón, aunque las uniones están localizadas sobre fibras musculares que son mucho mayores. Las uniones humanas tienen pliegues funcionales más largos y huecos más profundos 14,17. Los canales de sodio, que propagan la onda de despolarización, se localizan en la profundidad de los pliegues (fig. 18-1, D). Las crestas de los pliegues están densamente pobladas de RACh, aproximadamente 5 millones en cada unión. Los RACh son escasos en las profundidades entre los pliegues. La función trófica del nervio es vital para el desarrollo y mantenimiento de una función neuromuscular adecuada. Antes del nacimiento, cada célula muscular mantiene normalmente contactos con varios nervios y tiene varias uniones neuromusculares 14,19. En el nacimiento, todos los nervios, salvo uno, se retraen y permanece una única placa terminal (v. «Unión neuromuscular en edades extremas», más adelante). Una vez formado, el contacto entre nervio y músculo, especialmente la placa terminal, es duradero. Incluso aunque el nervio originario muera, el que lo reemplaza inerva exactamente la misma región del músculo. Las terminaciones nerviosas sobre músculos rápidos son mayores y más complicadas que las terminaciones nerviosas sobre músculos lentos. La razón no está clara. Estas diferencias en las terminaciones nerviosas sobre la superficie muscular pueden tener algo que ver con las diferencias en la respuesta de los músculos rápidos y lentos a los relajantes musculares. Puesto que todas las células musculares en una unidad son excitadas por una sola neurona, la estimulación eléctrica del nervio o por un potencial de acción originado desde el asta anterior o por cualquier agonista, incluidos los relajantes
4 426 PARTE II: Fisiología anestésica Figura Estructura de la unión neuromuscular adulta que muestra las tres células que constituyen la sinapsis: la motoneurona (es decir, la terminación nerviosa), la fibra muscular y la célula de Schwann. A. El nervio motor se origina en el asta anterior de la médula espinal o en el tronco del encéfalo. B. Conforme se aproxima a sus fibras musculares, y antes de fijarse a la superficie de la fibra muscular, el nervio se divide en ramas que inervan muchas fibras musculares individuales. C. Cada músculo recibe únicamente una sinapsis. El nervio motor pierde su mielina y luego se subdivide en muchos botones presinápticos para terminar sobre la superficie de la fibra muscular. D. La terminación nerviosa, cubierta por una célula de Schwann, posee vesículas agrupadas alrededor de los engrosamientos de la membrana, que son las zonas activas, hacia su lado sináptico, y mitocondrias y microtúbulos hacia su otro lado. Un canal, o hendidura, sináptico, formado por muchas hendiduras primarias y secundarias, separa el nervio del músculo. La superficie muscular está ondulada y áreas densas sobre las crestas de cada pliegue contienen receptores de acetilcolina. Los canales de sodio (Na + ) están presentes en el fondo de las hendiduras y a lo largo de toda la membrana muscular. En las hendiduras sinápticas se hallan la acetilcolinesterasa, proteínas y proteoglucanos que estabilizan la unión neuromuscular. despolarizantes (como la succinilcolina), hace que todas las células musculares de la unidad motora se contraigan al mismo tiempo. La contracción simultánea de las células en una unidad motora se denomina fasciculación, y con frecuencia es lo suficientemente vigorosa como para que se pueda observar a través de la piel. Aunque la mayoría de las células musculares adultas solo poseen una unión neuromuscular por célula, una importante excepción son algunas de las células de los músculos extraoculares. Estos músculos son tónicos y, a diferencia de otros músculos estriados de mamíferos, tienen inervación múltiple, con varias uniones neuromusculares alineadas a lo largo de la superficie de cada fibra muscular Como contrapunto a otros músculos, incluso el músculo ocular del adulto contiene receptores maduros e inmaduros fetales segregados en sinapsis distintas en fibras diferentes (v. «Biología de los receptores nicotínicos de acetilcolina prey postsinápticos», más adelante) 20,22. Los músculos oculares se contraen y relajan más bien despacio, y no rápidamente como lo hacen otros músculos estriados; pueden mantener una contracción continuada o contractura, con una fuerza proporcional al estímulo recibido. Fisiológicamente, esta especialización sujeta firmemente el ojo en su posición. Los músculos oculares son importantes para un anestesiólogo porque los relajantes musculares despolarizantes (p. ej., succinilcolina) los afectan de forma distinta a como afecta a otros músculos esqueléticos. En vez de producir una contracción
5 Capítulo 18: Fisiología y farmacología neuromusculares 427 breve seguida de parálisis, los fármacos pueden dar lugar a una respuesta en contractura de larga duración, que presiona al ojo contra la órbita y contribuye a un incremento en la presión del líquido intraocular 22,23. Se ha cuestionado el significado clínico del aumento de la presión intraocular inducido por succinilcolina. A pesar de que bastantes libros de texto aluden a la señalada extrusión del contenido ocular con succinilcolina, la base para este efecto parece ser anecdótica 24. Los estudios clínicos, sin embargo, han indicado que las contracciones de los músculos extraoculares inducidas por succinilcolina pueden durar hasta 1-2 min, y que puede desarrollarse una tensión isométrica mayor de 12 g para cada músculo extraocular 23. Por ello, probablemente no deba administrarse succinilcolina a pacientes con lesiones oculares abiertas (v. también capítulos 34 y 84). La zona perisináptica es el área del músculo adyacente al área de unión, y resulta crítica para el funcionamiento de la unión neuromuscular. La zona perisináptica contiene una mezcla de receptores, que incluye una menor densidad de receptores de acetilcolina y una alta densidad de canales de sodio (v. fig. 18-1, D). La mezcla favorece la capacidad de la zona perisináptica para responder a la despolarización (es decir, el potencial de placa terminal) producida por los RACh y trasladarla a la ola de despolarización que viaja a lo largo del músculo para iniciar la contracción muscular. La densidad de canales de sodio en el área perisináptica es más rica que en partes más distales de la membrana muscular 25,26. La zona perisináptica está lo suficientemente cerca de la terminación nerviosa como para ser influida por los transmisores que han sido liberados desde la misma. Por otra parte, en esta área pueden aparecer variantes especiales (es decir, isoformas) de receptores y de canales de sodio en diferentes etapas de la vida y como respuesta a los descensos anómalos en la actividad nerviosa (v. «Biología de los receptores nicotínicos de acetilcolina pre- y postsinápticos», más adelante). También se conocen anomalías congénitas en el RACh o en el canal de sodio (es decir, mutaciones) Estas variabilidades parecen contribuir a las diferencias en la respuesta a los relajantes que se observan en pacientes con distintas edades y condiciones patológicas 17,27. TEORÍA DE LOS CUANTOS Los contenidos de la terminación nerviosa no son homogéneos. Como se puede ver en las figuras 18-1 y 18-2, las vesículas se congregan en la porción hacia la superficie de la unión, mientras que los microtúbulos, mitocondrias y otras estructuras de apoyo se localizan hacia el lado opuesto. Las Elsevier. Fotocopiar sin autorización es un delito. Figura Funcionamiento de una sinapsis química: terminación nerviosa motora, incluida una parte del aparato para la síntesis del transmisor. Las grandes estructuras intracelulares son mitocondrias. La acetilcolina (ACh), sintetizada a partir de colina y de acetato por la acetil coenzima A (CoA), es transportada al interior de vesículas recubiertas, las cuales son trasladadas a los sitios de liberación. Un potencial de acción presináptico, que dispara el influjo de calcio a través de proteínas especializadas (es decir, canales de Ca 2+ ), provoca la fusión de las vesículas con la membrana y la liberación del transmisor. La membrana de la vesícula es retirada de la membrana del nervio y reciclada. Cada vesícula puede sufrir varios grados de liberación de contenidos desde un grado incompleto hasta uno completo. El transmisor es inactivado por difusión, catabolismo o recaptación. El contenido del círculo representa una vista magnificada de una vesícula sináptica. Los cuantos de ACh junto con trifosfato de adenosina (ATP) son almacenados en la vesícula y cubiertos por proteínas de membrana vesicular. La sinaptofisina es una glucoproteína que forma parte de la membrana vesicular. La sinaptotagmina es el sensor de calcio de la vesícula. La fosforilación de otra proteína de membrana, la sinapsina, facilita el tráfico vesicular hasta el sitio de liberación. La sinaptobrevina (proteína de membrana asociada a la vesícula [VAMP]) es una proteína SNARE involucrada en la adhesión de la vesícula al sitio de liberación (v. también fig. 18-3). CAT, colina acetiltransferasa; K +, potasio; Na +, sodio.
6 428 PARTE II: Fisiología anestésica vesículas que contienen el transmisor están ordenadas en conjuntos repetidos a lo largo de pequeñas zonas engrosadas, parches electrón-densos de la membrana a los que se hace referencia como zonas activas o sitios de liberación. Esta área engrosada es una sección cortada de una banda que discurre a través de la anchura de la superficie sináptica de la terminación nerviosa, que está considerada como la estructura a la cual se fusionan las vesículas (zonas activas) antes de que se rompan hacia la hendidura de la unión (v. «Proceso de exocitosis», más adelante). Las microfotografías de alta resolución mediante microscopio electrónico de barrido revelan pequeñas partículas proteicas colocadas a lo largo de la zona activa entre las vesículas. Se cree que estas partículas son canales especiales, los canales de calcio dependientes de voltaje que permiten al calcio entrar en el nervio y provocar la liberación de las vesículas 28,29. La rapidez con la que es liberado el neurotransmisor (200 ms) sugiere que los canales de calcio dependientes de voltaje están cerca de los sitios de liberación. Los estudios proteómicos sugieren que al menos 26 genes codifican proteínas presinápticas y las mutaciones en 12 de ellos causan defectos en las estructuras presinápticas que pueden conducir a una disminución en la liberación de acetilcolina y a debilidad muscular 30. Estos defectos pueden estar relacionados con la exocitosis, la endocitosis, la formación de las zonas activas y periactivas, el transporte vesicular y la modulación del neuropéptido 30. Cuando se observa la actividad electrofisiológica de un músculo esquelético, pueden verse potenciales de despolarización pequeños y espontáneos en la unión neuromuscular. Estos potenciales solo tienen una centésima de la amplitud del potencial evocado en la placa terminal que se produce al ser estimulado el nervio motor. Salvo por la amplitud, estos potenciales son similares al potencial de la placa terminal en su curso temporal y en el modo en el que son afectados por los fármacos. A estos potenciales de amplitud pequeña se los llama potenciales miniatura de placa terminal (PMPT). El análisis estadístico llevó a concluir que son respuestas unitarias; es decir, existe un tamaño mínimo para el PMPT y los tamaños de todos los PMPT son iguales o múltiplos de ese tamaño mínimo. Puesto que los PMPT son demasiado grandes para ser generados por una sola molécula de acetilcolina, se dedujo que están producidos por paquetes de tamaño uniforme o cuantos de transmisor liberados desde el nervio (en ausencia de estimulación). El potencial de placa terminal evocado por estímulo es la despolarización aditiva que se produce por la descarga síncrona de cuantos que proceden de varios cientos de vesículas. El potencial de acción que se propaga hasta el terminal del nervio permite la entrada de calcio al interior del nervio a través de los canales de calcio dependientes de voltaje; esto hace que las vesículas migren a la zona activa, se fusionen con la membrana neuronal y descarguen la acetilcolina contenida en el interior de la hendidura sináptica 28,29. Puesto que los sitios de liberación se localizan en lugares opuestos a los receptores sobre la superficie de la membrana postsináptica, se desaprovechan pocos transmisores y la respuesta del músculo se acopla directamente a la señal que proviene del nervio 17,28. El alineamiento del lugar del receptor presináptico se consigue mediante moléculas de adhesión o proteínas específicas de la superficie celular localizadas a ambos lados de la sinapsis que se acoplan entre sí a través de la hendidura sináptica y mantienen cohesionados los aparatos pre- y postsinápticos 14,19,31. Una de las proteínas implicadas en la adhesión sináptica es la neurexina, que se une a las neuroliginas sobre la membrana postsináptica. La cantidad de acetilcolina liberada por cada impulso nervioso es grande, al menos 200 cuantos con cerca de moléculas cada uno, y el número de receptores de acetilcolina activados por el transmisor liberado también es grande, alrededor de Los iones (sobre todo de sodio y algunos de calcio) que fluyen a través de los canales de los RACh activados provocan una despolarización máxima sobre la placa terminal, que produce un potencial de la placa terminal mayor que el umbral necesario para la estimulación del músculo. Este sistema es muy vigoroso. La señal es conducida por más moléculas de transmisor de las que se requieren y estas evocan una respuesta mayor de la necesaria. Al mismo tiempo, solo se emplea una pequeña fracción de las vesículas disponibles y de receptores o canales para enviar cada señal. Por consiguiente, la transmisión tiene un considerable margen de seguridad y, al mismo tiempo, el sistema tiene una capacidad sustancial en la reserva 16-18,32. UNIÓN NEUROMUSCULAR FORMACIÓN DEL NEUROTRANSMISOR EN LAS TERMINACIONES NERVIOSAS MOTORAS El axón del nervio motor transporta las señales eléctricas desde la médula espinal hasta los músculos, y posee todo el aparato bioquímico necesario para transformar la señal eléctrica en una señal química. Todos los canales iónicos, enzimas, otras proteínas, macromoléculas y componentes de la membrana que necesita la terminación nerviosa para sintetizar, almacenar y liberar acetilcolina y otros factores tróficos, se fabrican en el soma celular y son transmitidos a la terminación nerviosa mediante transporte axónico (v. fig. 18-2) 15,28,29. Las moléculas simples, colina y acetato, se obtienen del entorno de la terminación nerviosa, donde la colina es transportada por un sistema especial desde el líquido extracelular hasta el citoplasma, y el acetato en la forma de acetil coenzima A desde las mitocondrias. La enzima colina acetiltransferasa cataliza la reacción entre la colina y el acetato para formar acetilcolina. Después de la síntesis, la acetilcolina se almacena en el citoplasma hasta que es transportada al interior de las vesículas e incorporada a ellas, y estas se sitúan adecuadamente para su liberación cuando un potencial de acción alcanza la terminación nerviosa. POTENCIAL DE ACCIÓN NERVIOSO Durante un potencial de acción nervioso, el sodio del exterior fluye a través de la membrana y el voltaje resultante de la despolarización abre los canales de calcio, los cuales permiten la entrada de iones calcio al interior del nervio y provocan la liberación de acetilcolina. Un potencial de acción nervioso es el activador normal que libera acetilcolina al transmisor. El número de cuantos liberados por un nervio estimulado depende en gran parte de la concentración de calcio ionizado en el fluido extracelular. Si no hay presencia de calcio, la despolarización del nervio, incluso mediante la estimulación eléctrica, no provocará la liberación del transmisor. Si se duplica el calcio extracelular se produce un incremento en 16 veces del contenido de cuantos de un potencial de placa terminal 33. La corriente de calcio se mantiene hasta que el potencial de membrana regresa al valor normal, mediante el flujo de potasio desde el interior de la célula nerviosa hacia el exterior. Junto con los canales de
7 Capítulo 18: Fisiología y farmacología neuromusculares 429 Elsevier. Fotocopiar sin autorización es un delito. calcio sobre la terminación nerviosa están los canales de potasio, incluidos los canales de potasio dependientes de voltaje y los activados por calcio, cuya función es limitar la entrada de calcio al interior del nervio y, por tanto, la despolarización 26,32. La corriente de calcio puede prolongarse mediante bloqueantes de los canales de potasio (p. ej., 4-aminopiridina tetraetilamonio), que ralentizan o impiden el flujo de potasio fuera del nervio. El aumento en el contenido de cuantos así provocado puede llegar a proporciones asombrosas 17,34. También se observa en la práctica clínica un efecto del incremento de calcio, como la denominada potenciación postetánica, que se produce después de que un nervio de un paciente paralizado con un relajante no despolarizante es estimulado a altas frecuencias tetánicas. El calcio penetra en el nervio con cada estímulo, pero se acumula durante el período tetánico ya que no puede excretarse con la misma rapidez con la que el nervio es estimulado. Dado que la terminación nerviosa contiene una cantidad de calcio mayor de la normal durante algún tiempo después de la tetania, un estímulo aplicado en ese momento al nervio provoca la liberación de cantidades de acetilcolina superiores a las normales. Las cantidades anómalamente elevadas de acetilcolina antagonizan al relajante y producen el aumento característico en la magnitud de la contracción. El calcio entra en el nervio a través de proteínas especializadas, denominadas canales de calcio 15,32. De los diversos tipos de canales de calcio, dos parecen ser importantes para la liberación del transmisor: los canales P y los canales L, más lentos. Los canales P, probablemente el tipo responsable de la liberación normal del transmisor, solo se encuentran en las terminaciones nerviosas 13,35. En las terminaciones nerviosas motoras, se localizan inmediatamente adyacentes a las zonas activas (v. fig. 18-2). Son dependientes de voltaje y se abren y cierran mediante los cambios en el voltaje de la membrana causados por el potencial de acción nervioso. Además de los canales de calcio, hay varias formas de canales de potasio en la terminación nerviosa, incluidos los canales de potasio activados por voltaje y por calcio. Los canales de potasio limitan la duración de la despolarización de la terminación nerviosa y de ahí la entrada de calcio y la liberación del transmisor 26. Las alteraciones en la entrada de calcio al interior de la terminación nerviosa también pueden alterar la liberación del transmisor. El síndrome miasténico de Eaton-Lambert, que no debe confundirse con la miastenia grave, es una enfermedad autoinmune adquirida en la que los anticuerpos se dirigen contra los canales de calcio dependientes de voltaje de las terminaciones nerviosas 36. En este síndrome, la función disminuida del canal de calcio provoca un descenso en la liberación del transmisor, lo que produce una despolarización inadecuada y debilidad muscular. Los pacientes con síndrome de Eaton-Lambert tienen una sensibilidad aumentada a los relajantes despolarizantes y no despolarizantes 37. Concentraciones superiores a las normales de cationes inorgánicos bivalentes (p. ej., magnesio, cadmio y manganeso) también pueden bloquear la entrada de calcio a través de los canales P y alterar profundamente la transmisión neuromuscular. Este es el mecanismo subyacente a la debilidad muscular característica y a la potenciación del efecto de los relajantes musculares en la madre y el feto cuando se administra sulfato de magnesio para tratar la preeclampsia. Sin embargo, los canales P no están afectados por los fármacos bloqueantes de la entrada de calcio, como el verapamilo, el diltiacem y el nifedipino. Estas sustancias tienen efectos profundos sobre los canales L, más lentos, que están presentes en el sistema cardiovascular. En consecuencia, los bloqueantes del canal de calcio tipo L no tienen, en dosis terapéuticas, un efecto significativo sobre la liberación normal de acetilcolina ni sobre la potencia de la transmisión neuromuscular normal. No obstante, los fármacos bloqueantes de la entrada de calcio pueden aumentar el bloqueo en la transmisión neuromuscular inducido por RMND. El efecto es pequeño, y no todos los investigadores han sido capaces de observarlo. La explicación puede subyacer en el hecho de que las terminaciones nerviosas también pueden contener canales de calcio de tipo L. VESÍCULAS SINÁPTICAS Y RECICLAJE Al parecer hay dos grupos de vesículas que liberan acetilcolina: un depósito fácilmente liberable y un depósito de reserva, algunas veces denominados VP2 y VP1, respectivamente 38,39. Las vesículas del primer grupo son un poco más pequeñas y están limitadas a un área muy cercana a la membrana nerviosa, donde se unen a las zonas activas. Estas vesículas son las que por lo general liberan el transmisor. Los estudios realizados mediante microscopía electrónica han demostrado que la mayoría de las vesículas sinápticas (VP1) están secuestradas en el depósito de reserva y ancladas al citoesqueleto en una red filamentosa compuesta principalmente por actina, sinapsina (una proteína de unión a la actina), sinaptotagmina y espectrina 38,39. La liberación parece ocurrir cuando el ión calcio entra en el nervio a través de los canales P alineados sobre los lados de las zonas activas mediante las proteínas solubles de anclaje a receptores sensibles a N-etilmaleimida (SNARE) 38,39. Las proteínas SNARE están involucradas en la fusión, atraque y liberación de acetilcolina en la zona activa. El calcio tan solo necesita moverse una distancia muy corta (es decir, unos pocos radios atómicos) para encontrar una vesícula y activar las proteínas en la pared involucradas en un proceso conocido como atraque (v. «Proceso de exocitosis», más adelante) 39. La proteína activada parece reaccionar con la membrana nerviosa para formar un poro, a través del cual la vesícula descarga su acetilcolina dentro de la hendidura sináptica. Los estudios que han utilizado proteínas fluorescentes han observado cómo se fusionan las vesículas sinápticas con los sitios de liberación y liberan sus contenidos, los cuales son entonces recuperados. Algunas vesículas permanecen abiertas durante un breve período antes de su recuperación y no se colapsan completamente dentro de la superficie de la membrana (modelo «besa y corre»). Otras permanecen abiertas más tiempo y probablemente no se colapsan por completo (modelo «compensatorio»). Otras incluso se colapsan completamente y no son recuperadas hasta que se desencadena otro estímulo («encallado») 38,39. Las vesículas de reserva más grandes (VP1), desde su posición más profunda en la terminación nerviosa y firmemente ancladas al citoesqueleto por muchas proteínas, incluidas la actina, la sinapsina (una proteína fijadora de actina) y la espectrina 37,38, pueden ser movidas hacia los depósitos fácilmente trasladables para reemplazar a las vesículas gastadas o para participar en la transmisión cuando se requiere que el nervio funcione de manera intensiva (p. ej., cuando es estimulado a frecuencias muy altas o durante un período muy largo). En esas agotadoras circunstancias, el calcio puede penetrar más profundamente de lo normal dentro del nervio o puede entrar a través de los canales L para activar las enzimas dependientes de calcio, las cuales producen la rotura de los puentes de sinapsina que sujetan las vesículas
8 430 PARTE II: Fisiología anestésica al citoesqueleto, y por tanto permiten que las vesículas sean trasladadas a los sitios de liberación. La estimulación repetida requiere que la terminación nerviosa reponga sus depósitos de vesículas llenos de transmisor, un proceso conocido como movilización. El término se suele aplicar a la suma de todos los pasos que están involucrados en el mantenimiento de la capacidad de la terminación nerviosa para liberar el transmisor: cada paso desde la adquisición de colina y la síntesis de acetato hasta el movimiento de las vesículas rellenas hacia los lugares de liberación. La captación de colina y la actividad de la colina acetiltransferasa, la enzima que sintetiza acetilcolina, sean probablemente los pasos limitantes de la velocidad 15,29. PROCESO DE EXOCITOSIS El depósito de vesículas fácilmente liberables está constituido por aquellas vesículas que están directamente disponibles para su liberación. Durante un potencial de acción y el influjo de calcio se libera el neurotransmisor. Algunos estudios han aclarado un poco el funcionamiento íntimo por el cual la vesícula libera sus contenidos. El proceso completo se denomina exocitosis. Las proteínas SNARE incluyen la proteína de la vesícula sináptica, sinaptobrevina; la proteína asociada a la plasmolema, sintaxina; y la proteína de 25 kda asociada al sinaptosoma, SNAP-25 38,39. El modelo actual de la fusión mediada por proteínas de membrana en la exocitosis es el siguiente. Cuando existe un potencial de acción y entran iones calcio, la sinapsina se fosforila, lo que libera la vesícula de su inserción en el citoesqueleto. La sintaxina y la SNAP-25 son complejos adheridos a la membrana plasmática. Después del contacto inicial, la sinaptobrevina sobre la vesícula forma un complejo ternario con la sintaxina y el SNAP-25. La sinaptotagmina es la proteína sobre la membrana vesicular que actúa como sensor de calcio y guía a las vesículas hacia las zonas sinápticas ricas en canales de calcio, estabilizando las vesículas en la situación de atraque 38. El ensamblaje de los complejos ternarios fuerza a la vesícula a moverse cerca de la membrana subyacente de la terminación nerviosa (es decir, la zona activa) y la vesícula está entonces preparada para la liberación (fig. 18-3). La estrecha proximidad de los lugares de liberación, los canales de calcio y las vesículas sinápticas, así como el uso del sensor de calcio conduce a una descarga de liberación de nuevo transmisor de forma síncrona con el estímulo La vesícula puede liberar parte de, o todo, su contenido, parte del cual puede reciclarse para formar nuevas vesículas como se ha descrito anteriormente (modelos «besa y corre», «compensatorio», «encallado») La neurotoxina botulínica digiere selectivamente una o todas estas tres proteínas SNARE, y bloquea la exocitosis de las vesículas ; el resultado final es la debilidad muscular o parálisis muscular más intensa. Esta toxina puede producir una desnervación química parcial o completa. La toxina botulínica se usa terapéuticamente para tratar la espasticidad o espasmos en varias enfermedades neurológicas y quirúrgicas, para prevenir la hiperhidrosis en pacientes con sudoración excesiva, y para corregir arrugas como Figura Modelo para la fusión de membrana mediada por proteínas y exocitosis. A. La liberación de acetilcolina desde las vesículas es mediada por una serie de proteínas denominadas colectivamente proteínas SNARE. La sinaptotagmina es el receptor de calcio neuronal que detecta la entrada de calcio. La sinaptobrevina (es decir, una proteína de membrana asociada a las vesículas [VAMP]) es una proteína de tipo filamentoso ubicada sobre la vesícula. B. Durante la despolarización y la entrada de calcio, la sinapsina también está presente en la membrana de la vesícula. La sinaptobrevina de la vesícula se despliega y forma un complejo ternario con sintaxina/snap-25 en la membrana de la terminación nerviosa. C. El ensamblaje del complejo ternario fuerza a la vesícula en una aproximación estrecha a la membrana nerviosa en la zona activa con la liberación de su contenido, la acetilcolina. La fusión queda desensamblada y la vesícula es reciclada. D. Las toxinas de clostridios, incluida la botulínica, inhiben la liberación de acetilcolina y provocan parálisis de los músculos. La toxina consta de una cadena ligera (L C ) y una cadena pesada (H C ). La primera fase de la intoxicación es la interacción de la toxina con un receptor aún no identificado. E. Le siguen la internalización de la toxina dentro de la vesícula y la liberación de la L C de la vesícula. F. La L C liberada fragmenta diversas proteínas SNARE, en función del tipo de toxina liberada, y, por tanto, se impide el ensamblaje del complejo de fusión y se bloquea la liberación de acetilcolina. ATP, trifosfato de adenosina; SNAP-25, proteína de 25 kda asociada al sinaptosoma.
9 Capítulo 18: Fisiología y farmacología neuromusculares 431 Figura Esquema de los canales del receptor de acetilcolina (RACh) (derecha) y de los trazados de registros de muestras celulares de la apertura de los canales de los receptores (izquierda). El receptor maduro, o de la sinapsis, está formado por dos subunidades a1 y por una subunidad b1, d, y ε, respectivamente. La forma inmadura, fetal o extrasináptica, está constituida por dos subunidades a1 y por una subunidad b1, d y g. Por tanto, el último se denomina receptor de subunidad g. Recientemente se ha descrito en el músculo un receptor neuronal que consta de cinco subunidades a7. Estas subunidades están dispuestas alrededor del canal catiónico central. La isoforma inmadura que contiene la subunidad g muestra tiempos de apertura prolongados y corrientes del canal de amplitud baja. La isoforma madura que contiene la subunidad ε muestra tiempos de apertura más cortos y unas corrientes del canal elevadas durante la despolarización. La sustitución de la subunidad ε por la subunidad g produce el tipo de canal de apertura rápida y conductancia elevada. Como era de esperar, la aplicación de acetilcolina al RACh a7 también provoca una corriente rápida interior con un descenso acelerado. Todos estos acontecimientos despolarizantes son insensibles al tratamiento con atropina, aunque son sensibles al tratamiento con a-bungarotoxina o con relajantes musculares, los cuales bloquean el flujo de corriente. La afinidad de los relajantes musculares a cada isoforma puede ser diferente, y la del RACh a7 es la menos sensible al bloqueo. Elsevier. Fotocopiar sin autorización es un delito. tratamiento estético 43,44. La toxina botulínica consta de dos segmentos de proteínas, conocidos como cadenas pesada y ligera. La cadena pesada interactúa con las moléculas lipídicas denominadas polisialogangliósidos en la membrana celular y la sinaptotagmina para entrar en la vesícula. Una vez dentro de la vesícula, la cadena ligera inactiva la transmisión neuromuscular por rotura y, por tanto, inhibe la función de las proteínas SNARE (fig. 18-4). Algunos estudios indican que hay una incidencia elevada de infecciones por clostridios tanto en Canadá como en EE. UU., siendo la infección por Clostridium botulinum especialmente común después de lesiones traumáticas, en drogodependientes, y después de aloinjertos musculoesqueléticos 6,7. Por tanto, puede producirse una parálisis sistémica después de una infección por clostridios. La inyección local con fines terapéuticos suele provocar una parálisis localizada, aunque se han comunicado efectos sistémicos 7,45. ACETILCOLINESTERASA La acetilcolina liberada desde el nervio se difunde a través de la hendidura sináptica y reacciona con proteínas receptoras especializadas en la placa terminal para iniciar la contracción muscular. Las moléculas de transmisor que no reaccionan inmediatamente con un receptor o las que son liberadas después de la unión al receptor son destruidas casi instantáneamente por la acetilcolinesterasa en la hendidura sináptica. La acetilcolinesterasa de la unión es la forma proteica A12 o asimétrica, sintetizada en el músculo bajo la placa terminal. La acetilcolinesterasa (clasificación de enzimas ) es el tipo B de enzima carboxilesterasa. Hay una concentración menor de la misma en la zona externa a la unión sináptica. La enzima se excreta desde el músculo pero permanece adherida al mismo mediante filamentos finos de colágeno que están enganchados a la membrana basal 15,37. La mayoría de las moléculas de acetilcolina liberadas desde el nervio pasan inicialmente entre las enzimas para alcanzar los receptores postsinápticos, aunque conforme son liberadas del receptor, se topan invariablemente con la acetilcolinesterasa y son destruidas. En circunstancias normales, una molécula de acetilcolina reacciona solo con un receptor antes de ser hidrolizada. La acetilcolina es un potente mensajero, pero su acción dura muy poco tiempo porque es destruida en menos de 1 milisegundo después de ser liberada. Existen enfermedades congénitas y adquiridas que están relacionadas con una actividad alterada de la enzima acetilcolinesterasa. La ausencia congénita de la enzima excretada (en ratones knock-out, es decir, defectivos para un gen) conlleva una alteración en el mantenimiento del sistema neuronal motor y en la organización de las ramas nerviosas terminales 46. Hay muchos síndromes que se deben a anomalías congénitas de la función de la colinesterasa y que provocan enfermedades neuromusculares cuyos signos y síntomas habitualmente se asemejan a los de la miastenia grave o síndromes miasténicos 27,47. La desnervación disminuye la acetilcolinesterasa en las zonas sináptica y extrasináptica 37. Otras enfermedades adquiridas que afectan a las colinesterasas tienen que ver con la inhibición crónica de la acetilcolinesterasa por pesticidas organofosforados o gases nerviosos (p. ej., sarín) o con el tratamiento crónico con piridostigmina administrado como profilaxis contra el envenenamiento por gas nervioso 48,49. Los síntomas, que van desde la fatiga crónica hasta la debilidad muscular, se han atribuido a la inhibición crónica de la colinesterasa, por tanto se ha infravalorado la importancia de la acetilcolinesterasa en la función neuromuscular normal y anómala. Un estudio reciente en roedores confirma que la debilidad muscular asociada al tratamiento crónico con piridostigmina se relaciona tanto con una regulación a la baja de los RACh como con factores independientes del receptor 50.
10 432 PARTE II: Fisiología anestésica RECEPTORES POSTSINÁPTICOS DE ACETILCOLINA La similitud entre los RACh de bastantes especies y la abundancia de receptores de acetilcolina en el pez eléctrico Torpedo han facilitado mucho la investigación en esta área. La disponibilidad del ARN mensajero de seres humanos y de otras especies, así como la del ADN ha posibilitado el estudio del receptor en sistemas artificiales como los ovocitos de ranas y en células de mamíferos que no expresan el receptor, como COS o fibroblastos. También puede hacerse mutar a los receptores mediante técnicas moleculares que simulan estados patológicos; después puede estudiarse la función del receptor en estos sistemas artificiales. Con el uso de estas técnicas y de otras relacionadas se ha avanzado en el conocimiento de la síntesis, composición, función biológica y mecanismos que subyacen en las respuestas fisiológicas y farmacológicas de los RACh Existen tres isoformas de receptores postsinápticos: una forma sináptica o madura, un receptor extrasináptico o inmaduro (fetal), y el receptor neuronal a7 descrito más recientemente 2,16,18 (v. «Biología de los receptores nicotínicos de acetilcolina pre- y postsinápticos», más adelante). Sin embargo, las diferencias entre los subtipos de receptores pueden obviarse en una explicación general sobre la función de los receptores en la transmisión neuromuscular. Los RACh son sintetizados en las células musculares y se almacenan en la membrana de la placa terminal mediante una proteína especial de 43 kda conocida como rapsina. Esta proteína citoplásmica se asocia al receptor de acetilcolina en una proporción de 1: Los receptores, formados por cinco subunidades proteicas, están dispuestos como las cuadernas de un barril dentro de un receptor cilíndrico con un poro central para el canal iónico (en la figura 18-4 se puede ver un esquema de los factores fundamentales). La proteína receptora tiene un peso molecular de unos Da. Cada receptor tiene cinco subunidades. El receptor maduro consta de las subunidades a1, b1, d y ε, y el receptor fetal (inmaduro y extrasináptico) de las a1, b1, d y g; existen dos subunidades a y una subunidad de cada una de las otras. El RACh neuronal a7 consta de cinco subunidades a7 16,18. Cada una de las subunidades de todos los receptores está compuesta aproximadamente por aminoácidos. El complejo proteico del receptor atraviesa por completo la membrana y protruye más allá de la superficie extracelular de la misma y en el interior del citoplasma. El sitio de unión para la acetilcolina está en cada una de las subunidades a1, se localiza en el componente extracelular y en la subunidad a1, y constituye la zona competitiva entre los agonistas y los antagonistas del receptor. Los agonistas y antagonistas son atraídos hacia el sitio de unión y pueden ocupar el lugar, que se localiza cerca del residuo de cisteína (exclusivo de la cadena a) en la posición de la cadena de aminoácidos de la subunidad a 16,18. La a-bungarotoxina radiomarcada procedente de la cobra, usada para la cuantificación o tinción fluorescente del receptor, se une a la región heptapeptídica de la subunidad a 54 La neurregulina-1b (NRb-1) derivada de la motoneurona, descrita inicialmente con actividad inductora del receptor de acetilcolina (AIRA), induce la transcripción del gen del RACh en los mionúcleos subsinápticos mediante la activación de receptores ErbB SÍNTESIS Y ESTABILIZACIÓN DE LOS RECEPTORES POSTSINÁPTICOS El tejido muscular está formado a partir del mesodermo, y al principio aparece como mioblastos. Los mioblastos se fusionan para producir miotubos, los cuales tienen, por tanto, múltiples núcleos. Conforme los miotubos van madurando, se desarrolla el sarcómero, que es el elemento contráctil del músculo, compuesto por actina y miosina 55. La proteína b-integrina parece esencial para la fusión de mioblastos y para el ensamblaje del sarcómero 55. Poco tiempo después, los axones de los nervios motores crecen en el interior del músculo en desarrollo, y estos axones aportan señales derivadas del nervio (es decir, factores de crecimiento), incluidas agrina y neurregulinas (NRb-1 y NRb-2), que son fundamentales para la maduración de los miotubos hacia el músculo 19. La agrina es una proteína del nervio que estimula la diferenciación postsináptica mediante la activación de una cinasa muscular específica (MuSK), una tirosina cinasa expresada de forma selectiva en el músculo. Con la señalización por la agrina, los receptores de acetilcolina, que han estado dispersos por toda la membrana muscular, se agrupan en el área inmediatamente por debajo del nervio. La agrina, junto a neurregulinas y otros factores de crecimiento, induce también el agrupamiento de otras proteínas críticas derivadas del músculo, incluidas MuSK, rapsina y proteínas ErbB, todas ellas necesarias para la maduración y estabilización de los receptores de acetilcolina en la unión. Además de los efectos sobre la diferenciación postsináptica, la agrina y la MuSK también exhiben efectos en la diferenciación presináptica. La agrina y MuSK inducen señales retrógradas que instruyen a los axones para provocar el crecimiento neuronal y la diferenciación terminal 19. Sin embargo, a día de hoy se conoce menos el desarrollo presináptico de la unión neuromuscular que el desarrollo postsináptico. Justo antes y un poco después del nacimiento, los RACh que contienen la subunidad g inmadura son convertidos en los receptores maduros que contienen la subunidad ε. Aunque no se conoce con exactitud el mecanismo de este cambio, parece que está involucrada la neurregulina NRb-1, también llamada AIRA, que se une a uno de los receptores ErbB 19,56. ELECTROFISIOLOGÍA BÁSICA DE LA NEUROTRANSMISIÓN El conocimiento de las técnicas de electrofisiología ha progresado al mismo ritmo que los avances en la aproximación molecular para el estudio de los receptores presinápticos y postsinápticos. La fijación de membrana es una técnica que emplea una micropipeta de cristal para sondear la superficie de la membrana hasta que se localiza un único receptor funcional. Se presiona la punta de la pipeta en el interior de los lípidos de la membrana y se dispone el aparato electrónico para mantener el potencial de membrana pinzado (es decir, fijo) y medir la corriente que fluye a través del canal del receptor. La solución en la pipeta puede contener acetilcolina, un relajante muscular, otra sustancia, o una mezcla de fármacos. Pueden monitorizarse los cambios eléctricos mediante la aplicación de estas sustancias al receptor a través de la micropipeta. La figura 18-5 ilustra el resultado de la acción clásica despolarizadora de la acetilcolina sobre los receptores de la placa terminal. Normalmente, el poro del canal está cerrado por la aproximación de los cilindros (es decir, subunidades). Cuando un agonista ocupa los sitios de ambas subunidades a, la macromolécula proteica sufre un cambio de conformación con un movimiento de torsión a lo largo del eje central del receptor que da lugar a la apertura del canal central, a través del cual pasan los iones que pueden fluir a favor de un gradiente de concentración. Cuando el canal central está abierto, se produce un flujo de sodio y calcio desde el
11 Capítulo 18: Fisiología y farmacología neuromusculares 433 Figura Acciones de la acetilcolina o el curare sobre los receptores de la placa terminal. A. El canal iónico está inactivo y no se abre en ausencia de acetilcolina. B. Ni siquiera la unión de una molécula de acetilcolina (círculo relleno) a uno de los dos sitios de unión abre el canal. C. Cuando la acetilcolina se une a los sitios de reconocimiento de ambas subunidades a simultáneamente (círculos rellenos) desencadena un cambio de conformación que abre el canal y permite que los iones fluyan a través de la membrana. D. Acción de antagonistas como el curare (cuadrado relleno). La acetilcolina compite con la tubocurarina por el reconocimiento del lugar del receptor, pero también puede reaccionar con la acetilcolinesterasa. La tubocurarina es un prototipo de relajante muscular no despolarizante. La inhibición de la enzima acetilcolinesterasa aumenta la vida de la acetilcolina y la probabilidad de que reaccione con un receptor. Cuando uno de los dos sitios de unión (reconocimiento) esté ocupado por curare, el receptor no se abrirá, ni siquiera aunque el otro lugar esté ocupado por acetilcolina. Ca ++, ión de calcio; K +, ión de potasio; Na +, ión de sodio. Elsevier. Fotocopiar sin autorización es un delito. exterior de la célula hacia el interior, y un flujo de potasio desde el interior hacia el exterior. El canal dentro del tubo es lo suficientemente largo como para acomodar bastantes cationes y moléculas eléctricamente neutras, pero excluye los aniones (p. ej., cloro). La corriente transportada por los iones despolariza la membrana adyacente. La corriente neta es despolarizante y crea el potencial de placa terminal que estimula al músculo para contraerse. En esta situación, pueden registrarse pulsos rectangulares descendentes (es decir, despolarizantes) mediante la técnica electrofisiológica denominada fijación de membrana antes descrita (v. fig. 18-4). El pulso se detiene cuando se cierra el canal mediante inversión de la conformación mecánica (v. anteriormente), que se inicia característicamente cuando una o ambas moléculas agonistas se separan del receptor. En el estado activado, la corriente que pasa a través de cada canal abierto es minúscula, tan solo de unos pocos picoamperios (alrededor de 10 4 iones/ms). Sin embargo, cada descarga de acetilcolina desde el nervio abre aproximadamente canales y la corriente total es más que suficiente para producir la despolarización de la placa terminal y la contracción del músculo. La apertura de un canal produce la conversión de las señales químicas del nervio en flujo de corriente en la unión neuromuscular como potenciales de placa terminal, lo que conduce a la contracción muscular. El potencial de placa terminal se ha visto como un fenómeno graduado, que puede ser reducido de magnitud o prolongado en el tiempo con fármacos, pero en realidad el potencial de placa terminal es la suma de muchos fenómenos de todo o nada que se producen simultáneamente en multitud de canales iónicos. Son estos minúsculos fenómenos los que se ven afectados por los fármacos. Los receptores que no tienen dos moléculas de agonistas (p. ej., acetilcolina) unidos permanecen cerrados. Ambas subunidades a deben estar ocupadas simultáneamente por agonistas; si solo una está ocupada, el canal permanece cerrado (v. fig. 18-5). Esta es la base para la prevención de la despolarización por antagonistas. Los RMND actúan mediante unión a una o a ambas subunidades a y, por tanto, evitan que la acetilcolina se una y abra el canal. Esta interacción entre agonistas y antagonistas es competitiva, y el resultado transmisión o bloqueo depende de la concentración relativa y de las características de la unión de los fármacos involucrados (v. «Efectos de los fármacos sobre los receptores postsinápticos»). Los canales individuales también pueden tener una amplia variedad de conformaciones 17,57. Pueden permanecer abiertos o cerrados, afectando por tanto al flujo total de corriente a través de la membrana, pero pueden hacer más. Pueden abrirse durante un período de tiempo mayor o menor del normal, abrirse o cerrarse de forma más gradual de lo normal, abrirse de forma breve y repetida (es decir, castañeteo), o dejar pasar más o menos iones por apertura de lo que suelen permitir. Su función también está influida por fármacos, cambios en la fluidez de la membrana, temperatura, equilibrio electrolítico en el medio, y otros factores físico-químicos 38,39. Los canales del receptor son estructuras dinámicas que pueden establecer una amplia variedad de interacciones con fármacos y atravesar muchas situaciones de paso de corriente. Todas estas influencias sobre la actividad del canal se reflejan finalmente en la intensidad o debilidad de la transmisión neuromuscular y en la contracción muscular. EFECTOS DE LOS FÁRMACOS SOBRE LOS RECEPTORES POSTSINÁPTICOS ACCIONES CLÁSICAS DE LOS RELAJANTES MUSCULARES NO DESPOLARIZANTES La neurotransmisión se produce cuando el potencial de acción libera acetilcolina y esta se une a los RACh nicotínicos. Todos los relajantes no despolarizantes impiden o bloquean la neurotransmisión al evitar de modo competitivo la unión de la acetilcolina al RACh muscular. El resultado final bloqueo o transmisión depende de la concentración relativa de las sustancias químicas y de sus afinidades comparativas para el receptor. La figura 18-5 muestra un sistema expuesto a la acetilcolina y al bloqueante neuromuscular no despolarizante tubocurarina. Todos los demás relajantes musculares (p. ej., pancuronio, vecuronio) (v. también capítulo 34) tienen acciones similares a la tubocurarina. Un
12 434 PARTE II: Fisiología anestésica receptor ha atraído dos moléculas de acetilcolina y ha abierto su canal, por donde fluirá la corriente para despolarizar ese segmento de la membrana. Otro ha atraído una molécula de tubocurarina; su canal no se abrirá, y no fluirá corriente incluso si otra molécula de acetilcolina se une en el otro lugar. El tercer receptor tiene acetilcolina sobre una subunidad a y nada sobre la otra. Lo que ocurra depende de qué molécula se una. Si se une la acetilcolina, el canal se abrirá y la membrana se despolarizará; si se une la tubocurarina, el canal permanecerá cerrado y la membrana no se despolarizará. En otras ocasiones, una o dos moléculas de tubocurarina pueden adherirse al receptor, en cuyo caso el receptor no está disponible para los agonistas; no se registrará flujo de corriente. En presencia de concentraciones moderadas de tubocurarina, la cantidad de corriente que fluye a través de la totalidad de la placa terminal en cualquier instante será menor de la normal, lo que producirá un menor potencial de placa terminal y, llevada a proporciones mayores, un bloqueo en la neurotransmisión o parálisis neuromuscular. Normalmente la enzima acetilcolinesterasa destruye la acetilcolina y la retira para competir con el receptor, por lo que la tubocurarina tiene mejores oportunidades para inhibir la transmisión. Sin embargo, si se añade un inhibidor de la acetilcolinesterasa, como la neostigmina, la colinesterasa no puede destruir la acetilcolina. La concentración de agonista en la hendidura se mantiene elevada, y esta alta concentración desplaza la competición entre la acetilcolina y la tubocurarina a favor de la primera, mejorando así las posibilidades de que dos moléculas de acetilcolina se unan a un receptor, incluso aunque la tubocurarina siga permaneciendo en el entorno. Los inhibidores de la colinesterasa revierten la parálisis neuromuscular producida por RMND a través de este mecanismo. El canal solo se abre cuando la acetilcolina se adhiere a ambos sitios de reconocimiento. Sin embargo, una sola molécula de antagonista es suficiente para impedir la despolarización de ese receptor. Esto modifica la competición, sesgándola fuertemente a favor del antagonista (relajante). Matemáticamente, si se duplica la concentración de tubocurarina, la concentración de acetilcolina debe ser incrementada cuatro veces para que esta siga siendo competitiva. Las parálisis producidas por concentraciones elevadas de relajantes musculares (antagonista) son más difíciles de revertir con inhibidores de la colinesterasa que las que se generan por concentraciones bajas. Después de dosis elevadas de RMND, los inhibidores de la colinesterasa pueden ser ineficaces hasta que la concentración del relajante en el área perisináptica disminuya a un nivel más bajo mediante redistribución o eliminación del fármaco. Al contrario que los inhibidores de colinesterasa, la ciclodextrina revierte la acción de los relajantes mediante una encapsulación que tiene lugar a cualquier concentración si el compuesto es esteroideo, como vecuronio o rocuronio, y por ello este novedoso mecanismo puede revertir la relajación a cualquier nivel de bloqueo neuromuscular siempre que la cantidad de ciclodextrina (sugammadex) sea lo suficientemente grande (v. también capítulo 35 para más detalles). ACCIONES CLÁSICAS DE LOS RELAJANTES MUSCULARES DESPOLARIZANTES Al menos al principio, los relajantes musculares despolarizantes (p. ej., succinilcolina, decametonio) simulan el efecto de la acetilcolina, y por tanto se les puede considerar agonistas a pesar del hecho de que bloqueen la neurotransmisión después de una estimulación inicial. Desde el punto de vista estructural, la succinilcolina es muy similar al ligando natural acetilcolina y consiste en dos moléculas de acetilcolina unidas a través de su columna principal. Por tanto, no es sorprendente que la succinilcolina pueda mimetizar los efectos de la acetilcolina. La succinilcolina o el decametonio pueden unirse al receptor, abrir el canal, hacer pasar corriente y despolarizar la placa terminal. Estos agonistas, similares a la acetilcolina, se adhieren solo brevemente; cada apertura de un canal tiene una duración muy corta 1 ms o menos. Sin embargo, la respuesta a la acetilcolina es del orden de milisegundos debido a su rápida degradación por la acetilcolinesterasa, y la placa terminal vuelve a su estado de reposo durante un tiempo prolongado antes de que llegue otro impulso nervioso. En cambio, los relajantes despolarizantes tienen de manera característica una acción bifásica sobre el músculo una contracción inicial, seguida de una relajación que puede durar minutos u horas. Los relajantes despolarizantes, puesto que no son susceptibles a la hidrólisis por acetilcolinesterasa, no se eliminan de la hendidura sináptica hasta que son aclarados del plasma. El tiempo necesario para aclarar el fármaco del organismo es el principal determinante de la duración del efecto del fármaco. El aclaramiento corporal total del relajante es muy lento en comparación con la acetilcolina, especialmente cuando la (seudo)colinesterasa plasmática es anómala. Puesto que las moléculas de relajante no se eliminan rápidamente de la hendidura en comparación con acetilcolina, reaccionan repetidamente con los receptores incluso con niveles normales de colinesterasa plasmática, se unen casi inmediatamente a un receptor tras separarse de otro y despolarizan así la placa motora y abren los canales repetidamente. Para más detalles sobre el efecto de succinilcolina en los pacientes con deficiencia de colinesterasa, véase también el capítulo 34. El desplazamiento rápido desde la excitación de la contracción muscular hasta el bloqueo de la transmisión por los relajantes despolarizantes se produce porque la placa terminal está continuamente despolarizada. Esto ocurre por la yuxtaposición del borde de la placa terminal sobre una clase distinta de canal iónico: el canal de sodio, que no responde a agentes químicos, aunque se abre cuando se expone a un cambio del voltaje transmembranoso. El canal de sodio también es una proteína cilíndrica transmembranosa a través de la cual pueden fluir los iones de sodio. Dos partes de su estructura actúan como puertas que permiten o detienen el flujo de iones de sodio 58 Ambas puertas deben estar abiertas para que el sodio fluya a través del canal; el cierre de una de ellas corta el flujo. Puesto que estas dos puertas actúan secuencialmente, un canal de sodio tiene tres estados conformacionales funcionales y puede moverse de manera progresiva de un estado a otro (fig. 18-6). Cuando el canal de sodio se encuentra en situación de reposo, la puerta inferior (es decir, la puerta de inactivación o dependiente de tiempo) está abierta, pero la puerta superior (es decir, la puerta dependiente de voltaje) está cerrada, y los iones de sodio no pueden pasar. Cuando la molécula está sujeta a un cambio brusco de voltaje por despolarización de la membrana adyacente se abre la puerta superior; puesto que la puerta inferior (dependiente de tiempo) sigue abierta, el sodio fluye a través del canal. La puerta dependiente de voltaje permanece abierta tanto tiempo como la molécula esté sujeta a la influencia despolarizadora de la membrana de alrededor; no se cerrará hasta que desaparezca la despolarización. Sin embargo, poco tiempo después de que la puerta dependiente de voltaje se abre, la puerta inferior se cierra y corta de nuevo el flujo de iones. No puede abrirse de nuevo hasta que la puerta dependiente de voltaje se cierre. Cuando
13 Capítulo 18: Fisiología y farmacología neuromusculares 435 Elsevier. Fotocopiar sin autorización es un delito. Figura Esquema del canal de sodio (Na + ). Las barras representan partes de la molécula que actúan como puertas. La barra superior es dependiente del voltaje; la barra inferior es dependiente del tiempo. El lado izquierdo del dibujo representa la situación de reposo. Una vez activada por un cambio de voltaje, la molécula y sus puertas progresan como se ilustra (de izquierda a derecha). Véase el texto para los detalles. cesa la despolarización de la placa terminal, se cierra la puerta dependiente de voltaje; la puerta dependiente de tiempo se abre y el canal de sodio vuelve a su situación de reposo. El proceso completo es breve cuando la despolarización se produce con acetilcolina 58. La respuesta inicial de un relajante muscular despolarizante se parece a la de la acetilcolina, pero, dado que el relajante muscular no se hidroliza fácilmente, la despolarización de la placa terminal no es breve. La despolarización de la placa terminal por el relajante determina al principio la apertura de la puerta mediada por voltaje en los canales de sodio adyacentes, lo que produce una onda de despolarización que barre a lo largo del músculo, provocando la contracción muscular. Poco tiempo después de abrirse la puerta dependiente de voltaje, se cierra la puerta dependiente de tiempo. Puesto que el relajante no es retirado de la hendidura, la placa terminal sigue despolarizándose. Como los canales de sodio inmediatamente adyacentes a la placa terminal están influidos por la despolarización de la misma, sus puertas dependientes de voltaje permanecen abiertas y sus puertas inactivadoras, cerradas. Dado que el sodio no puede fluir a través de un canal que tiene cerrada una puerta inactivadora, la membrana muscular perisináptica no se despolariza. Cuando se detiene el flujo de iones a través de los canales de sodio de la zona perisináptica porque se han cerrado las puertas inactivadoras, los canales que se encuentran más abajo (más allá de la región perisináptica) se liberan de la influencia despolarizadora. En efecto, la zona perisináptica se convierte en un tampón que protege al resto del músculo de los episodios que se producen en la placa terminal. Por consiguiente, la membrana muscular está separada en tres zonas: 1) la placa terminal, que se despolariza por la succinilcolina; 2) la zona perisináptica, en la cual los canales de sodio están congelados en un estado inactivo, y 3) el resto de la membrana muscular, en la que los canales de sodio están en una situación de reposo. Dado que una descarga de acetilcolina del nervio no puede sobrepasar los canales de sodio inactivados en la zona perisináptica, la transmisión neuromuscular está bloqueada. Este fenómeno también se denomina acomodación. Durante la acomodación, cuando la sinapsis no es excitable a través del nervio (transmisor), la estimulación eléctrica directa del músculo causa una contracción muscular porque los canales de sodio más allá de la zona sináptica están en situación de reposo excitable. Los músculos extraoculares son músculo tónicos, con inervación múltiple y químicamente excitables a lo largo de la mayoría de su superficie A pesar de su inervación, los músculos oculares expresan tanto receptores maduros como inmaduros 20,22. No se produce la acomodación, por lo que estos músculos pueden sufrir una contractura sostenida en presencia de succinilcolina. La tensión así desarrollada fuerza al ojo contra la órbita y provoca, en parte, el aumento de la presión intraocular producida por relajantes despolarizantes (v. también capítulo 34). Los músculos extraoculares contienen un tipo especial de receptor que no se desensibiliza con la presencia continuada de acetilcolina u otros agonistas (v. comentario más adelante) 21,23. Una única dosis de succinilcolina puede causar una contractura que dure varios minutos 23. Se desconoce si es la subunidad g inmadura del RACh o la subunidad a7 del RACh la que desempeña una función en esta resistencia a la desensibilización en los músculos oculares. ACCIONES NO CLÁSICAS Y NO COMPETITIVAS DE LOS FÁRMACOS NEUROMUSCULARES Varios fármacos pueden interferir en el receptor para cambiar la transmisión, directamente o a través de su entorno lipídico. Estas sustancias reaccionan con el receptor neuromuscular para cambiar su función e impedir la transmisión, pero no actúan a través del sitio de unión a la acetilcolina. Estas reacciones provocan cambios en la dinámica del receptor inducidos por los fármacos y, en vez de abrirse o cerrarse rápidamente, los canales modificados son perezosos. Se abren más despacio y permanecen abiertos más tiempo o se cierran de forma lenta y en varios pasos; también pueden existir ambas situaciones. Estos efectos sobre los canales producen los correspondientes cambios en el flujo de iones y distorsiones del potencial de placa terminal. El efecto clínico depende de los fenómenos moleculares. Por ejemplo, la procaína, la ketamina, los anestésicos volátiles u otros fármacos que se disuelven en los lípidos de la membrana pueden cambiar las características de apertura o de cierre del canal 57,59. Si se impide que el canal se abra, la transmisión se debilita. Sin embargo, si se impide que el canal se cierre de forma lenta o completa, la transmisión puede resultar potenciada. Estos fármacos no encajan en el modelo clásico y la función neuromuscular alterada no está antagonizada por concentraciones aumentadas de acetilcolina en la zona perisináptica. Tales fármacos pueden estar involucrados en dos reacciones clínicamente importantes: la desensibilización del receptor y el bloqueo del canal. La primera se produce en la molécula del receptor, mientras que la última sucede en el canal iónico. BLOQUEO POR DESENSIBILIZACIÓN El RACh, debido a su flexibilidad y a la fluidez de los lípidos de alrededor, es capaz de existir en diferentes estados conformacionales Puesto que el receptor en reposo se encuentra libre de agonista, su canal está cerrado. El segundo estado se produce cuando dos moléculas de agonistas están unidas a la subunidad a del receptor y este ha sufrido el cambio de conformación que abre el canal y permite el flujo de iones. Estas reacciones son las bases de la transmisión neuromuscular normal. Sin embargo, algunos receptores a los que se unen agonistas no experimentan el cambio conformacional para abrir el canal. A los receptores que se encuentran en este estado se les denomina desensibilizados (es decir, que no son sensibles a las acciones de apertura del canal de los agonistas). Se unen a los agonistas con una avidez excepcional, pero la unión no produce la apertura del canal. Se desconocen los mecanismos por los cuales se produce la desensibilización. La macromolécula del receptor, con un peso veces
14 436 PARTE II: Fisiología anestésica mayor que la mayoría de fármacos o gases, tiene muchos lugares donde pueden actuar moléculas más pequeñas. La interfase entre lípidos y proteínas del receptor es otro sitio de reacción potencial. Se conocen varias conformaciones distintas de la proteína y, puesto que la acetilcolina no puede provocar la apertura del canal en ninguna de ellas, todas están incluidas bajo el término funcional de desensibilización. La desensibilización se acompaña de la fosforilación de un residuo de tirosina en la proteína del receptor 61,62. Aunque los agonistas (p. ej., succinilcolina) inducen desensibilización, los receptores se encuentran en un estado constante de transición entre situaciones de reposo y de desensibilización, haya o no agonistas. Los agonistas promueven la transición a un estado desensibilizado o, puesto que se unen muy estrechamente a receptores desensibilizados, atrapan al receptor en un estado desensibilizado. Los antagonistas también se unen estrechamente a los receptores desensibilizados y pueden atrapar moléculas en estos estados. Esta acción de los antagonistas no compite con la de la acetilcolina; puede ser aumentada por la acetilcolina si la última promueve el cambio a un estado desensibilizado. La desensibilización puede conducir a que se interpreten los datos de forma errónea. Superficialmente, la preparación parece normal, pero su respuesta a los agonistas o antagonistas está alterada. Una variedad aparece muy rápidamente, pocos milisegundos después de la aplicación de un agonista, lo que puede explicar el aumento de sensibilidad a un relajante no despolarizante después de la administración previa de succinilcolina. La desensibilización también puede formar parte del fenómeno conocido como bloqueo de fase II (v. «Bloqueo de fase II», más adelante en este capítulo), que está causado por una administración prolongada de relajantes despolarizantes. El bloqueo de fase II se denomina frecuentemente bloqueo por desensibilización, pero no debería, porque la desensibilización de los receptores solo es uno de los muchos fenómenos que contribuyen al proceso. Muchos otros fármacos que utilizan los anestesiólogos también promueven el cambio de los receptores desde un estado normal hasta un estado desensibilizado Estas sustancias, algunas de las cuales se enumeran en el cuadro 18-1, pueden debilitar la transmisión neuromuscular al reducir el margen de seguridad que existe normalmente en la unión neuromuscular, o pueden provocar un aumento aparente en la capacidad de los agentes no despolarizantes para bloquear la transmisión. Estas acciones son independientes de los efectos clásicos basados en la inhibición competitiva de la acetilcolina. La presencia de receptores desensibilizados significa que hay disponibles menos canales de receptores de lo habitual para transportar la corriente transmembranosa. La producción de receptores desensibilizados disminuye la eficacia de la transmisión neuromuscular. Si existen muchos receptores desensibilizados, los normales, que son insuficientes, son los únicos disponibles para despolarizar la placa terminal, por lo que no se producirá la transmisión neuromuscular. Incluso si solo algunos receptores están desensibilizados, la transmisión neuromuscular se verá alterada y el sistema será más susceptible al bloqueo por antagonistas convencionales, como el atracurio o el rocuronio. BLOQUEO DEL CANAL Los anestésicos locales y los bloqueantes de la entrada de calcio impiden el flujo de sodio o calcio a través de sus canales respectivos, lo que explica el término fármaco bloqueante del canal. De manera similar, puede producirse un bloqueo en el CUADRO 18-1 Fármacos que pueden causar o promover la desensibilización de los receptores colinérgicos nicotínicos Anestésicos volátiles Halotano Sevoflurano Isoflurano Antibióticos Polimixina B Cocaína Alcoholes Etanol Butanol Propanol Octanol Barbitúricos Tiopental Pentobarbital Agonistas Acetilcolina Decametonio Carbacol Succinilcolina Inhibidores de la acetilcolinesterasa Neostigmina Piridostigmina Difluorofosfato Edrofonio Anestésicos locales Dibucaína Lidocaína Prilocaína Etidocaína Fenotiacinas Clorpromacina Trifluoperacina Proclorperacina Fenciclidina Bloqueantes de los canales de calcio Verapamilo flujo de iones en el RACh con concentraciones de fármacos que se utilizan en la práctica clínica, y esto puede contribuir a alguno de los fenómenos e interacciones farmacológicas observados en el receptor. Pueden producirse fundamentalmente dos tipos de bloqueo, el del canal abierto y el del canal cerrado 60,63,64. En un bloqueo del canal cerrado, ciertas sustancias pueden ocupar la boca del canal, impidiendo el paso de iones a través del mismo para despolarizar la placa terminal. El proceso puede tener lugar incluso aunque el canal no esté abierto. En un bloqueo de canal abierto, una molécula del fármaco entra en el canal que ha sido abierto mediante reacción con la acetilcolina pero no penetra necesariamente por todo el recorrido. El bloqueo del canal abierto es un tipo de bloqueo dependiente del uso, lo que quiere decir que las moléculas solo pueden entrar en el canal cuando este se encuentra abierto. En los bloqueos del canal abierto y cerrado, el flujo normal de iones a través del receptor está alterado, lo que da lugar a una prevención de la despolarización de la placa terminal y a una transmisión neuromuscular más débil o bloqueada. Sin embargo, puesto que la acción no se produce en el sitio de reconocimiento de la acetilcolina, no se trata de un antagonismo competitivo de la acetilcolina y no se revierte por anticolinesterásicos que aumenten la concentración de acetilcolina. El incremento en
15 Capítulo 18: Fisiología y farmacología neuromusculares 437 Elsevier. Fotocopiar sin autorización es un delito. la concentración de acetilcolina puede provocar la apertura de los canales con más frecuencia y, por tanto, hacer que se vuelvan más susceptibles al bloqueo por compuestos dependientes del uso. Hay evidencias de que la neostigmina y los inhibidores de la colinesterasa relacionados pueden actuar como fármacos bloqueantes de canales 17,63. El bloqueo del canal está involucrado en las alteraciones de la función neuromuscular inducidas por algunos antibióticos, cocaína, quinidina, piperocaína, antidepresivos tricíclicos, naltrexona, naloxona e histrionicotoxina. Por el contrario, los relajantes musculares pueden unirse al sitio de acción de la acetilcolina del receptor y ocupar el canal. El pancuronio se une preferentemente al sitio de reconocimiento. La galamina parece actuar por igual en ambos sitios (bloqueo de canales y bloqueo de zonas de reconocimiento de acetilcolina). La tubocurarina ocupa un lugar intermedio; en dosis bajas, las que clínicamente producen un bloqueo mínimo de la transmisión, el fármaco es, ante todo, un antagonista puro en el sitio de reconocimiento; en dosis mayores, también penetra en el canal y lo bloquea. El decametonio y la succinilcolina, como agonistas, pueden abrir los canales y, como moléculas sinuosas, también penetrar y bloquearlos. El decametonio y algunas otras moléculas largas y finas pueden penetrar en todo el trayecto del canal abierto y entrar en el sarcoplasma. Se desconoce si en situaciones de administración prolongada de RMND, como en un contexto de cuidados intensivos, puede producirse la entrada del RMND, la ocupación del canal y el paso del fármaco al citosol. BLOQUEO DE FASE II El bloqueo de fase II es un fenómeno complejo que se produce lentamente en las uniones que están expuestas de forma continuada a agentes despolarizantes. Este fenómeno de atenuación se debe probablemente a la interacción de la acción despolarizante de la succinilcolina a nivel de varios RACh neuronales (presinápticos); estos receptores presinápticos están bloqueados por concentraciones de succinilcolina más elevadas que las habituales. Esta atenuación tras la administración de succinilcolina depende, al menos en parte, de una interacción presináptica y de importancia para la movilización y la liberación de neurotransmisores. Sin embargo, la atenuación en el músculo durante la estimulación nerviosa repetitiva también puede ser atribuible a un bloqueo RACh postsináptico 65. Varios factores están involucrados en este fenómeno. La apertura repetida de canales permite una afluencia continua de potasio y un influjo de sodio, y el desequilibrio electrolítico resultante altera la función de la membrana sináptica. El calcio que penetra en el músculo a través de los canales abiertos puede provocar un trastorno en los propios receptores y en los elementos subyacentes de la placa terminal. La actividad de una bomba de sodio-potasio ATPasa en la membrana aumenta con el incremento de sodio intracelular y, al bombear sodio fuera de la célula y potasio dentro de ella, trabaja para restaurar el balance iónico y el potencial de membrana hacia la normalidad. Durante el tiempo que está presente la sustancia despolarizante, los canales del receptor permanecen abiertos y el flujo de iones a través de ellos se mantiene alto 66. Los factores que influyen en el desarrollo del bloqueo de fase II son la duración de la exposición al fármaco, la sustancia utilizada y su concentración, e incluso el tipo de músculo (es decir, rápido o lento). Las interacciones con anestésicos y otros agentes también afectan al proceso. Todas estas sustancias pueden tener también efectos presinápticos sobre la proporción y la cantidad de liberación y movilización del transmisor. Con tantas variables involucradas en la interferencia en la transmisión neuromuscular, el bloqueo de fase II es un fenómeno complejo y de notable variabilidad. Es difícil predecir la reversión de la respuesta a un bloqueo de fase II producido por un relajante muscular despolarizante a la administración de inhibidores de la colinesterasa. Por tanto, es mejor que no se intente revertir mediante inhibidores de la colinesterasa, aunque la respuesta a la tetania o a la estimulación en tren de cuatro se parece a la que es producida por los RMND. BIOLOGÍA DE LOS RECEPTORES NICOTÍNICOS DE ACETILCOLINA PRE- Y POSTSINÁPTICOS RECEPTORES CONVENCIONALES POSTSINÁPTICOS DE ACETILCOLINA EN EL MÚSCULO FRENTE A RECEPTORES NEURONALES MADUROS EN EL MÚSCULO A día de hoy se han identificado tres variantes de RACh postsinápticos. La isoforma de RACh que está presente en la unión neuromuscular adulta inervada se denomina receptor adulto, maduro o sináptico. Se expresa otra isoforma de RACh, descrita hace más de cuatro décadas, cuando hay un descenso de la actividad muscular, como se observa en el feto antes de la inervación, después de una lesión de motoneurona superior o inferior, quemaduras o sepsis, o después de otros acontecimientos que provocan un incremento del catabolismo proteico muscular, incluidas sepsis o inflamación generalizada 1-3. Para diferenciarlos de los receptores maduros o sinápticos, la otra isoforma se denomina receptor de acetilcolina inmaduro, extrasináptico o fetal. Alguna evidencia sugiere que la isoforma inmadura no se observa en el catabolismo muscular proteico ni en la atrofia que aparece en la malnutrición 67. Pueden aparecer diferencias cualitativas de la isoforma madura como consecuencia de mutaciones genéticas que alteran la estructura proteica de las subunidades. Estos cambios cualitativos del RACh también pueden causar anomalías de la neurotransmisión (p. ej., síndrome de canal lento o rápido) 27,47 y, por tanto, de la respuesta a los relajantes musculares. A nivel molecular, los receptores maduros e inmaduros están formados por cinco subunidades (v. fig. 18-4) 1-3. El receptor sináptico maduro es un pentámero de dos subunidades a1 y una subunidad b1, d7 y ε. El receptor inmaduro está formado por dos subunidades a y una subunidad b7, d7 y g; es decir que en el receptor inmaduro está presente la subunidad g en vez de la subunidad ε. Las subunidades g y ε difieren muy poco en su homología de aminoácidos pero las diferencias son lo suficientemente grandes como para afectar a la fisiología y farmacología del receptor y de su canal iónico. Los receptores sinápticos están siempre confinados a la región de la placa terminal de la membrana muscular. El receptor inmaduro o extrasináptico puede expresarse en cualquier lugar de la membrana muscular aunque su expresión en la unión neuromuscular parece mínima 16. Durante el desarrollo y en determinadas situaciones patológicas, los receptores sinápticos y extrasinápticos pueden coexistir en el área perisináptica de la membrana muscular (fig. 18-7). A diferencia de los RACh del músculo convencional, que constan de las subunidades a1, b1, d y ε/g descritas anteriormente, RACh formados por unidades a7 han sido hallados recientemente en el músculo esquelético durante la inmovilización, la sepsis, el desarrollo y la desnervación 68,69.
16 438 PARTE II: Fisiología anestésica Figura Distribución de los receptores de acetilcolina en el músculo adulto en desarrollo, maduro, desnervado, o en el músculo inmovilizado o sujeto a catabolismo por inflamación. A y B. En la etapa fetal precoz, los mioblastos mononucleados, derivados del mesodermo, se fusionan para formar miotubos multinucleados. Los receptores de acetilcolina inmaduros que contienen la subunidad g y los receptores de acetilcolina (RACh) a7 neuronales están diseminados por toda la membrana muscular antes de la inervación. C. Cuando el nervio contacta con el músculo, se produce el agrupamiento de los receptores en la sinapsis y se asocia a la pérdida de algunos receptores extrasinápticos. D. Se dice que se produce la maduración de la unión cuando los receptores que contienen la subunidad ε reemplazan a los RACh que contienen las subunidades g y a7. Incluso el miocito maduro es multinucleado, aunque carece de RACh extrasinápticos. E. La desnervación y algunos otros estados patológicos incluso sin desnervación anatómica (p. ej., quemaduras, inmovilización, tratamiento crónico con relajantes musculares, ictus y sepsis) llevan a la reexpresión de los RACh con subunidad g principalmente en las áreas extrasinápticas. Los RACh con subunidad a7 se expresan en las áreas de la unión neuromuscular y también con más probabilidad en las áreas externas a ella. Estos cambios del receptor son potencialmente reversibles si la inmovilización, el catabolismo y la inflamación muscular cesan y se restablecen las condiciones normales. Dos estudios recientes han probado un aumento de expresión de las subunidades a7 del RACh en el músculo, mediante Western blot, unión de ligandos o técnicas genéticas después de sepsis, quemaduras o inmovilización, en las cuales no se produce desnervación manifiesta 16,70. Estos RACh a7 son canales homoméricos (es decir, formados por las mismas subunidades) dispuestos como pentámeros (v. fig. 18-4). Se piensa que los bolsillos de unión al ligando (fármaco) están formados por caras negativas y positivas de las interfases de unión de la subunidad a7. Como se esperaba, el agonista endógeno de la acetilcolina se une al RACh a7, y cada una de las cinco subunidades tiene el potencial de unir moléculas de acetilcolina o de succinilcolina 18,69. Otros agonistas, como la nicotina y la colina, y antagonistas, incluidos los relajantes musculares, pancuronio, toxina de cobra y a-bungarotoxina, también se unen al RACh a7 18,69. Los RACh a7 en el músculo presentan unas características funcionales y farmacológicas inusuales cuando se los compara con los RACh musculares convencionales (a1, b1, d, ε/g) o los RACh a7 neuronales en el cerebro. La colina, un precursor y metabolito de la acetilcolina (y de la succinilcolina), es un agonista extremadamente débil del RACh muscular convencional aunque es un agonista completo del RACh a7 muscular; es decir, concentraciones de colina que no abran canales del RACh convencional abrirán canales del RACh a7 69. Es más, no se produce una desensibilización del RACh a7 incluso durante la presencia continua de colina 69, lo que aumenta la posibilidad de que el potasio fluya (145 meq/l, aproximadamente) desde el interior de la célula hacia el espacio extracelular, incluido el plasma (4,5 meq/l), por su gradiente de concentración. La a-conotoxina GI química inhibe específicamente a los RACh convencionales del músculo (maduros e inmaduros) pero no inhibe a los RACh a7. La importante función de los RACh a7 en la resistencia a los RMND se demuestra por la presencia de resistencia inducida por la inmovilización en ratones salvajes y por la ausencia de resistencia en ratones deficitarios del gen 73. Los RACh a7 que se expresan en el tejido neuronal también se desensibilizan inmediatamente con colina, una característica que contrasta con los RACh a7 musculares que no se desensibilizan con colina 69. Los RACh a7 del músculo también tienen menor afinidad por sus antagonistas, como pancuronio, rocuronio, atracurio o a-bungarotoxina; por ello, para bloquear la despolarización inducida por agonistas en los RACh a7 in vitro o para causar parálisis neuromuscular in vivo o ex vivo cuando los RACh a7 están regulados al alza, se requieren concentraciones más altas de estos fármacos En los RACh convencionales del músculo, la unión incluso de una de las subunidades a1 del RACh a un antagonista da lugar a inactivación de ese receptor porque la acetilcolina necesita ambas subunidades a1 para su activación. Sin embargo, en los RACh a7, incluso aunque estén unidas tres subunidades al antagonista (p. ej., relajante muscular), todavía están disponibles otras dos subunidades para la unión de un agonista que cause despolarización. Esta característica puede justificar en parte la resistencia a los relajantes musculares cuando los RACh a7 se expresan en el músculo y en otros tejidos en estados patológicos Todavía no se ha estudiado la farmacología clínica del RACh a7 muscular, aunque su farmacología básica ayuda a comprender la hiperpotasemia relacionada con la succinilcolina. La desnervación química o física del músculo no solo provoca una regulación al alza y cambios cualitativos (subunidad ε subunidad g) en los RACh sino también una regulación al alza de los RACh a7 en el músculo. La succinilcolina, un análogo sintético de la acetilcolina que consiste en la unión de dos moléculas de acetilcolina, es capaz de despolarizar no solo los RACh convencionales sino también
17 Capítulo 18: Fisiología y farmacología neuromusculares 439 los RACh a7 en el músculo 72. Además, el metabolito de la succinilcolina, la colina, puede despolarizar los RACh a7 con poca desensibilización. Los efectos despolarizantes de la succinilcolina y de la colina sobre los RACh a7 regulados al alza pueden producir una fuga continua de potasio intracelular y el anegamiento del líquido extracelular, incluido el plasma, lo cual conduce a una hiperpotasemia. Por ello, las diferencias en la composición de subunidades y en el número de las tres isoformas que se expresan en la unión neuromuscular y fuera de ella pueden justificar las respuestas clínicas aberrantes a los relajantes musculares, como la resistencia aislada a los RMND y la respuesta hiperpotasémica a la succinilcolina 2,72,73. Elsevier. Fotocopiar sin autorización es un delito. MANTENIMIENTO DE LAS UNIONES NEUROMUSCULARES MADURAS A diferencia de otras células, las células musculares son poco corrientes en el sentido de que tienen gran cantidad generalmente cientos de núcleos por célula. Cada núcleo tiene los genes que producen las tres isoformas de receptores. Múltiples factores, como la actividad eléctrica, la señalización por factor de crecimiento (p. ej., insulina, agrina y neurregulinas) y la presencia o ausencia de inervación, controlan la expresión de los tres tipos de isoformas del receptor 19,37. Este control se aprecia con mayor claridad en el embrión en desarrollo conforme se forma la unión neuromuscular. Antes de que sean inervadas, las células musculares de un feto solo sintetizan los receptores inmaduros y los RACh a7 de ahí el término isoforma fetal para el primer receptor. La síntesis está dirigida por prácticamente todos los núcleos en la célula, y los receptores se expresan por toda la membrana de la célula muscular (fig. 18-8). Conforme el feto se desarrolla y el músculo es inervado, las células musculares comienzan a sintetizar la isoforma madura de los receptores, los cuales son insertados exclusivamente dentro del área de la (futura) placa en desarrollo El nervio libera varios factores de crecimiento que influyen sobre el aparato sintetizador de los núcleos próximos. En primer lugar, los factores inducidos por el nervio hacen que los núcleos subsinápticos incrementen la síntesis de RACh. Luego, la actividad eléctrica inducida por el nervio provoca una represión de los receptores en el área extrasináptica. Los factores de crecimiento derivados del nervio, como agrina y AIRA/neurorregulina, hacen que los receptores se acumulen en el área subsináptica y se acelere la expresión de la isoforma madura (v. fig. 18-8) 19,37. Varias líneas de evidencia indican que el agrupamiento, la expresión y la estabilización de los receptores maduros están desencadenados por al menos tres factores de crecimiento: la agrina, la AIRA y, posiblemente, el gen del péptido relacionado con la calcitonina 56,74,75. La neurregulina y la agrina también se liberan desde el músculo, aunque la agrina de origen muscular no parece ser tan importante en el agrupamiento y la maduración del receptor. La AIRA se sintetiza en el nervio y parece desempeñar un papel en la maduración del ordenamiento vesicular y en la conversión del cambio de g a ε 75. Todos estos factores de crecimiento interactúan con distintas proteínas de membrana y con receptores del citosol, produciendo la fosforilación y activación de los sistemas de transcripción nuclear (genes). La agrina señaliza a través de MuSK, y las neurregulinas lo hacen a través de receptores ErbB (v. fig. 18-8). Estos receptores controlan los cambios cualitativos y cuantitativos de la unión. Una vez comenzado, el proceso es muy estable y los núcleos del área sináptica siguen expresando los receptores maduros. En ciertos estados patológicos que inducen una resistencia a la insulina parece producirse una proliferación concomitante de RACh más allá de la unión Figura Diagrama de los acontecimientos dependientes de la agrina y de la actividad inductora del receptor de acetilcolina (AIRA) durante la maduración de la unión neuromuscular. Después del establecimiento de un nervio sobre el músculo, se liberan los factores de crecimiento, incluidas la agrina y las neurregulinas. La señalización por neurregulina es esencial para la supervivencia de la célula de Schwann, y las células de Schwann son fundamentales para el mantenimiento de los axones. La interacción de la agrina con su receptor de tirosina cinasa específica del músculo (MuSK) favorece el agrupamiento de proteínas sinápticas, incluidos los receptores de acetilcolina (RACh), la rapsina y los receptores ErbB. La AIRA/neurregulina es el mejor candidato para la implicación en la conversión del receptor inmaduro que contiene la subunidad g en el receptor maduro (inervado) que contiene la subunidad ε, que es específico de la sinapsis y, por tanto, no está insertado en el área extrasináptica. neuromuscular. Los trastornos en los que se ha observado esta forma de resistencia a la insulina (es decir, disminución de la señal de factor de crecimiento) son inmovilización, quemaduras y desnervación ; en estos casos, no solo existe una regulación al alza de los RACh totales, sino que también se observa una regulación al alza de novo de las isoformas inmaduras y de los RACh a Esta regulación al alza puede relacionarse con el hecho de que la agrina y posiblemente la neurorregulina envían la señal a través de la misma cascada de proteínas que la insulina (p. ej., fosfatidilinositol 3-cinasa [PI3K]) 56, Por tanto, la señal de agrina y neurorregulina puede ser importante para la supresión de los RACh a7 y los RACh inmaduros en la unión neuromuscular normal. Antes de la inervación, como en el feto, los RACh están presentes por toda la membrana muscular. Después de la inervación, los RACh se concentran cada vez más en la membrana postsináptica y en el momento del nacimiento llegan a estar prácticamente ausentes en el área extrasináptica. El proceso de inervación progresa algo lentamente durante la vida fetal y madura durante la lactancia y el inicio de la infancia Con el tiempo, los receptores inmaduros disminuyen de concentración y desaparecen de la parte periférica del músculo. En el músculo inervado normal de un adulto activo, los núcleos localizados inmediatamente debajo de la placa terminal y muy próximos a ella dirigen la síntesis del receptor; solo están activos los genes para la expresión de receptores maduros. Los núcleos más allá de la unión neuromuscular no están
18 440 PARTE II: Fisiología anestésica activos, y por ello en las células más allá de esta área no se expresan receptores. Después del nacimiento, sigue teniendo lugar la conversión de todos los receptores con subunidades g a subunidades ε en toda la zona alrededor de la unión. En roedores, la conversión supone aproximadamente 2 semanas En el ser humano, este proceso tarda más tiempo. El período de tiempo para la desaparición de los RACh a7 en el feto o recién nacido también es desconocido. Algunas de las proteínas implicadas en la unión de los receptores maduros al citoesqueleto son integrina, sintrofina, utrofina, a- y b-distroglucano y rapsina, por citar algunas de ellas REEXPRESIÓN DE LAS SUBUNIDADES g INMADURA (FETAL) Y a7 DE LOS RACH EN LA VIDA ADULTA Los receptores extrasinápticos pueden reaparecer poco después de una desnervación de la motoneurona superior e inferior y en ciertos estados patológicos (p. ej., quemaduras, sepsis, inmovilización, tratamiento crónico con relajantes musculares o botulismo, pérdida de la actividad eléctrica). La estimulación de un músculo desnervado con un estímulo eléctrico externo puede impedir la aparición de receptores inmaduros. Se ha sugerido que el calcio que penetra en el músculo durante la actividad es importante para el proceso de supresión 16,17. En los estados patológicos antes mencionados, si el proceso es grave y prolongado, los receptores extrasinápticos aparecen a lo largo de toda la superficie del músculo, incluida el área perisináptica (v. fig. 18-7). Los núcleos de la unión también continúan produciendo receptores maduros. La síntesis de receptores inmaduros se inicia a las pocas horas de la inactividad, pero se requieren varios días para que la totalidad de la membrana esté cubierta con receptores. Esta regulación al alza de los receptores tiene implicaciones para el uso de los relajantes despolarizantes y posiblemente RMND. Los cambios en los RACh a7 parecen ir paralelos a la expresión de receptores inmaduros, aunque esto no se ha estudiado bien. Los cambios en la composición de las subunidades (g frente a ε) en el receptor confieren ciertos cambios en las características electrofisiológicas (funcionales), farmacológicas y metabólicas Los receptores maduros son metabólicamente estables, con una semivida aproximada de 2 semanas, mientras que los receptores inmaduros tienen una semivida de menos de 24 h. Los receptores inmaduros tienen una conductancia unitaria por canal menor y un tiempo medio de apertura del canal de 2 a 10 veces más largo que los receptores maduros (v. fig. 18-4). Los cambios en la composición de las subunidades pueden también alterar la sensibilidad o la afinidad del receptor, o ambas, para ligandos específicos. Los fármacos despolarizantes o agonistas, como la succinilcolina y la acetilcolina, despolarizan más fácilmente los receptores inmaduros, lo que da lugar a flujos de cationes; dosis de una décima a una centésima de la necesaria para que los receptores maduros puedan efectuar la despolarización 2. La potencia de los fármacos no despolarizantes también está disminuida, como demuestra la resistencia a los no despolarizantes que se ha documentado en pacientes con quemaduras, desnervación e inmovilización 1,3. A la luz de las últimas investigaciones, sin embargo, parece que la resistencia a los fármacos no despolarizantes es debida más probablemente a la expresión de RACh a7 en la unión neuromuscular, los cuales tienen una menor afinidad por los RMND 16, Algunos RMND también pueden causar una respuesta agonista parcial a nivel de receptores inmaduros, lo que explicaría la disminución de potencia en procesos en los que aparece una regulación al alza de los RACh 8. La regulación al alza de los RACh inmaduros en el área de la unión y fuera de ella puede tener un efecto amortiguador para la difusión de los relajantes y contribuir a la resistencia a los RMND 80. La sensibilidad alterada a los relajantes musculares puede ocurrir solo en determinadas partes del organismo o en determinados músculos si únicamente algunos músculos están afectados por una disminución de la actividad nerviosa (p. ej., tras un ictus). La sensibilidad a los relajantes musculares puede empezar a cambiar entre 48 y 72 h después de una lesión u hospitalización. La hiperpotasemia es el efecto adverso más serio que se puede producir con el uso de succinilcolina en presencia de una regulación al alza de los receptores en el área perisináptica en uno o más músculos 1-3. En estos pacientes, los receptores pueden estar desperdigados sobre una gran superficie del músculo. Los canales de los RACh abiertos por el agonista (succinilcolina) permiten que el potasio salga del músculo y penetre en la sangre (fig. 18-9) 2,3. Si una parte importante de la superficie muscular contiene canales de receptores regulados al alza (inmaduros), cada uno de los cuales permanece abierto durante más tiempo, la cantidad de potasio que es trasladada desde el músculo hasta el torrente sanguíneo puede ser considerable. La hiperpotasemia resultante puede provocar trastornos graves del ritmo cardíaco, incluso fibrilación ventricular. Además, la hiperpotasemia probablemente no pueda prevenirse con la administración previa de RMND, porque las grandes dosis requeridas para bloquear los RACh causarían parálisis por sí mismas, obviando la necesidad de administrar succinilcolina 3. Dosis de RMND superiores a las normales pueden atenuar el aumento de concentración de potasio en sangre, pero no pueden prevenirlo completamente. Sin embargo, tras la administración de succinilcolina pueden aparecer hiperpotasemia y parada cardíaca, incluso en ausencia de desnervación. Estos efectos se observan en ciertas distrofias musculares congénitas en las que la membrana muscular es propensa a la lesión por la despolarización producida por succinilcolina y da lugar a la liberación de potasio a través de la lesión en la membrana 81. RECEPTORES PRESINÁPTICOS DE ACETILCOLINA Los RACh nicotínicos existen en diversas formas aparte de la que se observa en el músculo 16,18. El RACh nicotínico clásico de tipo muscular se encuentra a nivel postsináptico, mientras que los receptores de subtipo neuronal pueden estar a nivel presináptico y postsináptico. Los RACh nicotínicos de subtipo neuronal que se expresan a nivel presináptico generalmente son heteroméricos y están constituidos por una sola subunidad a y subunidades b. Esta familia de RACh nicotínicos se expresa extensamente en el sistema nervioso central y periférico, en los nervios autónomos y en los ganglios a nivel de las células sensibles al oxígeno de los cuerpos carotídeos. En las células inmunocompetentes, como macrófagos, linfocitos y granulocitos, así como en los fibroblastos y condrocitos, también existen RACh a7 16,18. Diversos genes codifican los RACh heterogéneos, y el canal iónico está formado por múltiples subunidades (multímeros). En los vertebrados se han clonado diecisiete genes del RACh. Estos incluyen varias combinaciones de subunidades a (desde a1 hasta a10) y subunidades b (desde b1 hasta b4) y una subunidad g, d, y ε, respectivamente. Las subunidades g, d, y ε solo se encuentran en el músculo Los receptores colinérgicos presinápticos o asociados a la terminación nerviosa han sido demostrados mediante
19 Capítulo 18: Fisiología y farmacología neuromusculares 441 Figura Esquema de la liberación de potasio (K + ) inducida por succinilcolina (SCh) en un músculo inervado (arriba) y desnervado (abajo). En el músculo inervado, la SCh administrada sistémicamente alcanza toda la membrana muscular, pero solo despolariza los receptores de la unión neuromuscular (a1, b1, d/ε) porque los receptores de acetilcolina (RACh) se localizan solo en esta zona. Con la desnervación, los núcleos del músculo no solo expresan RACh fuera de la unión (a1, b1 y d/g) sino también RACh nicotínicos a7 a través de la membrana muscular. La SCh sistémica, al contrario que la acetilcolina liberada localmente, puede despolarizar todos los RACh con regulación al alza, lo que lleva a una salida masiva del K + intracelular a la circulación e hiperpotasemia. El metabolito de SCh, la colina, y posiblemente la succinilmonocolina pueden mantener esta despolarización a través de los RACh nicotínicos a7 e intensificar la liberación de K + y mantener la hiperpotasemia. (Tomado de Martyn JAJ, Richtsfeld M: Succinylcholine-induced hyperkalemia in acquired pathologic states: etiologic factors and molecular mechanisms, Anesthesiology 104: , 2006.) Elsevier. Fotocopiar sin autorización es un delito. técnicas morfológicas, farmacológicas y de biología molecular, pero su forma y funciones no se conocen con exactitud en comparación con las de los receptores del área postsináptica. Muchos fármacos con abundantes dianas potenciales para su acción farmacológica pueden afectar a la capacidad de la terminación nerviosa para llevar a cabo sus funciones. La función trófica de mantenimiento del contacto entre nervio y músculo implica la liberación y el relleno de acetilcolina junto con factores tróficos que requieren la señalización a través de bastantes receptores, de los cuales el RACh presináptico nicotínico solo es uno de ellos. La succinilcolina produce fasciculaciones que pueden evitarse con RMND. Puesto que una fasciculación es, por definición, la contracción simultánea de multitud de células musculares de una única unidad motora, y dado que solo el nervio puede sincronizar todos los músculos en su unidad motora, parece que la succinilcolina debe actuar sobre las terminaciones nerviosas. Como los RMND previenen las fasciculaciones, se ha concluido que estos actúan sobre el mismo receptor presináptico. Dosis muy pequeñas de agonistas colinérgicos (p. ej., succinilcolina) y antagonistas (p. ej., RMND) afectan a los receptores nicotínicos sobre la terminación nerviosa, el primero al despolarizar la terminación y algunas veces induciendo descargas repetitivas del nervio, y el último previniendo la acción de los agonistas 5. Con ayuda de anticuerpos monoclonales específicos se ha logrado demostrar la presencia de subunidades a3 nicotínicas en la terminación nerviosa 82. Otra clave para diferenciar los RACh presinápticos de los postsinápticos fue el hallazgo de que algunos fármacos (p. ej., dihidro-b-eritroidina) se unen solo a los RACh presinápticos, mientras que otros (p. ej., a-bungarotoxina) solo se unen a los receptores postsinápticos 65. Se han encontrado pistas adicionales en numerosas demostraciones acerca de las diferencias cuantitativas en la reacción de los receptores nicotínicos presinápticos y postsinápticos a los agonistas y antagonistas 65, Por ejemplo, se sabía que la tubocurarina se une muy poco a los sitios de reconocimiento de los receptores colinérgicos nicotínicos ganglionares y que no es un antagonista competitivo de la acetilcolina en ese lugar. El decametonio (un relajante muscular despolarizante que ya no se usa) es un inhibidor selectivo del receptor muscular, y el hexametonio es un inhibidor selectivo de los receptores nicotínicos en los ganglios autónomos Sin embargo, la d-tubocurarina y el hexametonio pueden bloquear los canales abiertos de estos receptores y deben su habilidad para bloquear la transmisión ganglionar a esta propiedad. Las características funcionales de los canales de los receptores presinápticos también pueden ser diferentes. Por ejemplo, la despolarización de las terminaciones nerviosas motoras iniciada por la administración de acetilcolina puede prevenirse con tetrodotoxina, un bloqueante específico del flujo de sodio sin efecto sobre la placa terminal. No se dispone de información específica sobre la estructura molecular de los receptores neuronales nicotínicos de la motoneurona terminal. Parte de la composición de
20 442 PARTE II: Fisiología anestésica las subunidades es similar, pero otras subunidades no se parecen a las del receptor postsináptico. De los 16 productos identificados de los genes del RACh nicotínico, se piensa que solo 12 (a1 hasta a10 y b2 hasta b4) contribuyen a los receptores nicotínicos expresados sobre las neuronas. Mucho más llamativo es el hecho de que el tejido nervioso no exprese las subunidades g, d o ε del receptor; solo contiene genes para las subunidades a y b. Los genes para las subunidades a y b en el nervio y en el músculo no son exactamente los mismos; existen variantes. Para enfatizar la diferencia entre los receptores nicotínicos neuronales y musculares, a veces a los primeros se les denomina Nn y a los últimos Nm. Con tal cantidad de subunidades disponibles existen muchas combinaciones posibles y no se sabe qué combinaciones se encuentran en los nervios motores. Sus papeles fisiológicos tampoco han sido caracterizados por completo. La expresión de los RACh neuronales nicotínicos de acetilcolina en sistemas in vitro ha confirmado que los relajantes musculares y sus metabolitos pueden unirse a algunos de estos RACh 53, El receptor nicotínico sobre la superficie sináptica del nervio (terminación nerviosa) sondea al transmisor en la hendidura y, mediante un sistema de retroalimentación positiva, provoca la liberación de más transmisor. En otras partes del sistema nervioso, esta retroalimentación positiva se complementa mediante un sistema de retroalimentación negativa, que sondea cuándo la concentración del transmisor en la hendidura sináptica se ha incrementado apropiadamente e interrumpe el sistema de liberación. Se cree que la amortiguación tetánica y del tren de cuatro durante el bloqueo neuromuscular con RMND surge de autorreceptores colinérgicos presinápticos en la terminación nerviosa motora 5,52. El subtipo de RACh neuronal que está implicado de forma crítica en la liberación de acetilcolina y el consiguiente fenómeno de atenuación (como el que se observa en el patrón de estímulo tetánico y en el de tren de cuatro) se ha identificado como el subtipo a3b2 de RACh nicotínico 10,84. Cuando se bloquea específicamente este receptor presináptico por un relajante no despolarizante como tubocurarina, se produce una reducción de la liberación del neurotransmisor con la estimulación repetida y el consiguiente fenómeno de atenuación. Sin embargo, debería tenerse en cuenta que el bloqueo aislado del RACh presináptico no es necesario ni suficiente para inducir la atenuación; para que sea detectable debe estar presente una reducción concomitante de seguridad de la neurotransmisión presináptica o postsináptica 65. Aunque todos los fármacos bloqueantes neuromusculares despolarizantes que se utilizan clínicamente inhiben este RACh nicotínico presináptico, así como varios RACh nicotínicos neuronales más, en el intervalo de concentración clínicamente relevante, la succinilcolina no activa ni inhibe el autorreceptor presináptico a3b2 a concentraciones clínicamente importantes 53,85. Esta observación puede ser la razón de la característica ausencia de atenuación durante el bloqueo neuromuscular inducido por la succinilcolina. Sin embargo, la succinilcolina no interactúa con el RACh a3b4 que se encuentra en los ganglios autónomos 53. También se ha mostrado que los RMND reducen la respuesta hipóxica ventilatoria en seres humanos que están parcialmente paralizados 86, y el mecanismo que subyace tras la depresión puede estar relacionado con la inhibición de receptores nicotínicos en el cuerpo carotídeo 11. Los RACh nicotínicos a3, a7 y b2 se han demostrado últimamente en el cuerpo carotídeo humano 87. Se necesita investigación adicional para determinar si la inhibición de estos receptores tiene algún papel en la respuesta atenuada a la hipoxia. Se sabe, asimismo, que la terminación nerviosa motora comparte otros tipos de receptores, como opioides, adrenérgicos, dopaminérgicos, de purina y de adenosina, así como receptores para hormonas endógenas, neuropéptidos y una variedad de proteínas 88,89. Se desconocen cuáles son las funciones fisiológicas de estos receptores y los efectos de los anestésicos sobre los mismos. UNIÓN NEUROMUSCULAR EN EDADES EXTREMAS RECIÉN NACIDO Inmediatamente antes del nacimiento, los RACh se encuentran agrupados alrededor del nervio en la unión Figura Maduración del aparato postsináptico. Día 0 posnatal (P0): en el momento del nacimiento, los agregados de RACh se han consolidado hasta formar una placa ovalada con bordes irregulares. En este momento, cada unión neuromuscular puede tener más de una terminación nerviosa e inervarla. Día 5 posnatal (P5): aproximadamente 5 días después del nacimiento, la membrana postsináptica se invagina y forma un canal, y se desarrollan pequeñas perforaciones en la placa. Día 14 posnatal (P14): aproximadamente 14 días después del nacimiento, los receptores de acetilcolina (RACh) que contienen la subunidad g inmadura son completamente sustituidos por RACh maduros que presentan subunidad a. Las invaginaciones o hendiduras aumentan en número y producen más perforaciones en la unión con forma de pretzel (galleta salada en forma de lazo). Las perforaciones se corresponden con las hendiduras o pliegues sinápticos. Día 30 posnatal (P30): la unión neuromuscular está completamente desarrollada a los 30 días del nacimiento. Los RACh tienen su máxima densidad. En el área subsináptica se transcribe selectivamente un conjunto distintivo de proteínas postsinápticas y moléculas de señal, lo que aporta integridad a la unión neuromuscular y una neurotransmisión eficaz. (Modificado de Shi L, Fu AK, Ip NY: Molecular mechanisms underlying maturation and maintenance of the vertebrate neuromuscular junction, Trends Neurosci 35: , 2012; and Sanes JR, Lichtman JW: Induction, assembly, maturation and maintenance of a postsynaptic apparatus, Nat Rev Neurosci 2: , 2001.)
FUNCION NEURAL. Prof. Alexander Bravo Ovarett Kinesiólogo Magister Neurehabilitacion
 FUNCION NEURAL Prof. Alexander Bravo Ovarett Kinesiólogo Magister Neurehabilitacion 1 CONTINUO CONTACTO 3 4 5 PRINCIPIOS DE LA NEURONA POLARIZACION DINAMINCA ESPECIFICAD DE CONEXIÓN PLASTICIDAD 6 POLARIZACION
FUNCION NEURAL Prof. Alexander Bravo Ovarett Kinesiólogo Magister Neurehabilitacion 1 CONTINUO CONTACTO 3 4 5 PRINCIPIOS DE LA NEURONA POLARIZACION DINAMINCA ESPECIFICAD DE CONEXIÓN PLASTICIDAD 6 POLARIZACION
Soluciones de la serie de ejercicios 8 (7.012)
 Nombre AT Grupo Soluciones de la serie de ejercicios 8 (7.012) Pregunta 1 a) A continuación se muestra un esquema básico de la estructura de una neurona. Nombre las partes. 1= dendritas, 2= cuerpo celular
Nombre AT Grupo Soluciones de la serie de ejercicios 8 (7.012) Pregunta 1 a) A continuación se muestra un esquema básico de la estructura de una neurona. Nombre las partes. 1= dendritas, 2= cuerpo celular
Unidad 2. Neurona y Transmisión Sináptica. Estudio Anatomo-Funcional del Sistema Nervioso
 Unidad 2. Neurona y Transmisión Sináptica Estudio Anatomo-Funcional del Sistema Nervioso Objetivos Conocer los principales tipos de células nerviosas. Conocer la estructura externa e interna de la neurona.
Unidad 2. Neurona y Transmisión Sináptica Estudio Anatomo-Funcional del Sistema Nervioso Objetivos Conocer los principales tipos de células nerviosas. Conocer la estructura externa e interna de la neurona.
LA UNIDAD NEUROMUSCULAR
 LA UNIDAD NEUROMUSCULAR UNIÓN NEUROMUSCULAR o PLACA MOTORA : es la sinapsis entre axones de motoneuronas y fibras musculares esqueléticas. * El cuerpo celular de las motoneuronas está dentro del asta ventral
LA UNIDAD NEUROMUSCULAR UNIÓN NEUROMUSCULAR o PLACA MOTORA : es la sinapsis entre axones de motoneuronas y fibras musculares esqueléticas. * El cuerpo celular de las motoneuronas está dentro del asta ventral
TEMA: RELAJANTES NEUROMUSCULARES, SU USO EN LA PRACTICA MÉDICA. Funcionamiento del Sistema Nervioso Autónomo; cuales son sus neurotransmisores
 TEMA: RELAJANTES NEUROMUSCULARES, SU USO EN LA PRACTICA MÉDICA. CONOCIMIENTOS PREVIOS Funcionamiento del Sistema Nervioso Autónomo; cuales son sus neurotransmisores Anatomía básica del músculo estriado
TEMA: RELAJANTES NEUROMUSCULARES, SU USO EN LA PRACTICA MÉDICA. CONOCIMIENTOS PREVIOS Funcionamiento del Sistema Nervioso Autónomo; cuales son sus neurotransmisores Anatomía básica del músculo estriado
Tema 24 Sistema cardiovascular. Ciclo cardiaco. Sístole y diástole. Fases.
 Tema 24 Sistema cardiovascular. Ciclo cardiaco. Sístole y diástole. Fases. 1. Músculo cardiaco. 1.1. Anatomía del músculo cardiaco. 2. Actividad eléctrica del corazón. 2.1.Potencial de acción en el miocardio.
Tema 24 Sistema cardiovascular. Ciclo cardiaco. Sístole y diástole. Fases. 1. Músculo cardiaco. 1.1. Anatomía del músculo cardiaco. 2. Actividad eléctrica del corazón. 2.1.Potencial de acción en el miocardio.
Fisiología del Músculo. Dr. Ricardo Curcó
 Fisiología del Músculo Dr. Ricardo Curcó Músculo Estriado Liso Esquelético Cardíaco Músculo Liso Músculo esquelético Es el músculo bajo control voluntario. Cada fibra muscular se encuentra inervado por
Fisiología del Músculo Dr. Ricardo Curcó Músculo Estriado Liso Esquelético Cardíaco Músculo Liso Músculo esquelético Es el músculo bajo control voluntario. Cada fibra muscular se encuentra inervado por
Funcionalmente las neuronas se pueden clasificar en tres tipos: Neuronas sensitivas: aisladas o localizadas en órganos sensoriales o en zonas del
 LA NEURONA La neurona es considerada la unidad estructural y funcional fundamental del sistema nervioso. Esto quiere decir que las diferentes estructuras del sistema nervioso tienen como base grupos de
LA NEURONA La neurona es considerada la unidad estructural y funcional fundamental del sistema nervioso. Esto quiere decir que las diferentes estructuras del sistema nervioso tienen como base grupos de
CELULAS DEL SISTEMA NERVIOSO CENTRAL. Universidad Intercontinental UIC
 CELULAS DEL SISTEMA NERVIOSO CENTRAL Universidad Intercontinental UIC Área de la Salud Facultad de Psicología Mtro. Gabriel Perea UNIDAD ELEMENTAL DEL SISTEMA NERVIOSO 2 Neuronas y neuroglia EL TEJIDO
CELULAS DEL SISTEMA NERVIOSO CENTRAL Universidad Intercontinental UIC Área de la Salud Facultad de Psicología Mtro. Gabriel Perea UNIDAD ELEMENTAL DEL SISTEMA NERVIOSO 2 Neuronas y neuroglia EL TEJIDO
En el estudio de los mecanismos de acción farmacológica hay que distinguir.
 TEMA : ASPECTOS MOLECULARES DEL MECANISMO DE ACCIÓN DE LOS FÁRMACOS En el estudio de los mecanismos de acción farmacológica hay que distinguir. Fármacos de Acción Específica: son aquellos que han de interaccionar
TEMA : ASPECTOS MOLECULARES DEL MECANISMO DE ACCIÓN DE LOS FÁRMACOS En el estudio de los mecanismos de acción farmacológica hay que distinguir. Fármacos de Acción Específica: son aquellos que han de interaccionar
Trabajo Final: Curso de Neurobiología y Plasticidad Neuronal
 Trabajo Final: Curso de Neurobiología y Plasticidad Neuronal Alumno: Horacio Hernández www.asociacioneducar.com Mail: informacion@asociacioneducar.com Facebook: www.facebook.com/neurocienciasasociacioneducar
Trabajo Final: Curso de Neurobiología y Plasticidad Neuronal Alumno: Horacio Hernández www.asociacioneducar.com Mail: informacion@asociacioneducar.com Facebook: www.facebook.com/neurocienciasasociacioneducar
Experimentos: [Ca 2+ ] media de la tensión desarrollada y representarla frente al logaritmo de [Ca 2+ ]. Determinar la EC 50.
![Experimentos: [Ca 2+ ] media de la tensión desarrollada y representarla frente al logaritmo de [Ca 2+ ]. Determinar la EC 50. Experimentos: [Ca 2+ ] media de la tensión desarrollada y representarla frente al logaritmo de [Ca 2+ ]. Determinar la EC 50.](/thumbs/52/28982569.jpg) Fisiol Hum Farmacia. (2008-2009) Dr. Guadalberto Hernández Dr. Juan Vicente.Sánchez Fisiología del músculo liso. Motilidad intrínseca. Influencia del sistema nervioso autónomo: efecto de drogas simpático
Fisiol Hum Farmacia. (2008-2009) Dr. Guadalberto Hernández Dr. Juan Vicente.Sánchez Fisiología del músculo liso. Motilidad intrínseca. Influencia del sistema nervioso autónomo: efecto de drogas simpático
EL GUSTO EN LOS VERTEBRADOS.
 EL GUSTO EN LOS VERTEBRADOS. Como los insectos, muchos vertebrados tienen receptores gustativos sobre la superficie corporal. Algunos peces que habitan en el fondo marino tienen aletas pectorales modificadas
EL GUSTO EN LOS VERTEBRADOS. Como los insectos, muchos vertebrados tienen receptores gustativos sobre la superficie corporal. Algunos peces que habitan en el fondo marino tienen aletas pectorales modificadas
Electroestimulación n algo mas que Gimnasia Pasiva
 Electroestimulación n algo mas que Gimnasia Pasiva Gimnasia pasiva o electroestimulación? Fisiología a de la contracción n muscular Que debemos saber de los equipos de electroestimulación Energía-Ejercicio-Adelgazamiento
Electroestimulación n algo mas que Gimnasia Pasiva Gimnasia pasiva o electroestimulación? Fisiología a de la contracción n muscular Que debemos saber de los equipos de electroestimulación Energía-Ejercicio-Adelgazamiento
TEMA 7: LA MEMBRANA PLASMÁTICA.
 TEMA 7: LA MEMBRANA PLASMÁTICA. 1.-La membrana plasmática como unidad estructural. 2.- Características de la membrana plasmática. 2.1. Estructura y composición. 2.2. Propiedades de la membrana plasmática.
TEMA 7: LA MEMBRANA PLASMÁTICA. 1.-La membrana plasmática como unidad estructural. 2.- Características de la membrana plasmática. 2.1. Estructura y composición. 2.2. Propiedades de la membrana plasmática.
Características de la preparación que se usará en los experimentos. Experimento 1: Relación entre intensidad del estímulo y tensión.
 1 Fisiol Hum Farmacia. (2008-2009) Dr. Guadalberto Hernández Dr. Juan Vicente.Sánchez Práctica: Fisiología del Músculo Estriado Características de la preparación que se usará en los experimentos. 1. Se
1 Fisiol Hum Farmacia. (2008-2009) Dr. Guadalberto Hernández Dr. Juan Vicente.Sánchez Práctica: Fisiología del Músculo Estriado Características de la preparación que se usará en los experimentos. 1. Se
Tejido Muscular. La célula o fibra muscular es la unidad estructural y funcional del tejido muscular
 Tejido Muscular La célula o fibra muscular es la unidad estructural y funcional del tejido muscular Cuando decimos fibra muscular no nos estamos refiriendo a un tipo de fibra extracelular, como es el caso
Tejido Muscular La célula o fibra muscular es la unidad estructural y funcional del tejido muscular Cuando decimos fibra muscular no nos estamos refiriendo a un tipo de fibra extracelular, como es el caso
Capítulo 12 REGULACIÓN DE LA EXPRESIÓN GÉNICA. Factores de Transcripción. Metilación. Procesamiento del ARN. Post-traduccional
 REGULACIÓN DE LA EXPRESIÓN GÉNICA - Mecanismos de Regulación Regulación Procariontes Eucariontes Operón Lactosa Operón Triptofano Transcripcional Procesamiento del ARN Traduccional Post-traduccional Factores
REGULACIÓN DE LA EXPRESIÓN GÉNICA - Mecanismos de Regulación Regulación Procariontes Eucariontes Operón Lactosa Operón Triptofano Transcripcional Procesamiento del ARN Traduccional Post-traduccional Factores
Aspectos generales de farmacodinamia Parte I. Dr. Mario Acosta Mejía
 Aspectos generales de farmacodinamia Parte I Dr. Mario Acosta Mejía Objetivos Analizar el concepto general y actualizado de farmacodinamia Entender los mecanismos de acción por los cuales actúan los fármacos
Aspectos generales de farmacodinamia Parte I Dr. Mario Acosta Mejía Objetivos Analizar el concepto general y actualizado de farmacodinamia Entender los mecanismos de acción por los cuales actúan los fármacos
La Contracción Muscular
 La Contracción Muscular El 40 % del cuerpo está formado por músculo esquelético y el 10 % por músculo liso y cardiaco. El músculo esquelético está formado por fibras musculares, cada una contiene cientos
La Contracción Muscular El 40 % del cuerpo está formado por músculo esquelético y el 10 % por músculo liso y cardiaco. El músculo esquelético está formado por fibras musculares, cada una contiene cientos
EL CONTROL DE LAS ACTIVIDADES CELULARES
 EL CONTROL DE LAS ACTIVIDADES CELULARES LAS REACCIONES CELULARES BÁSICAS Todas las células llevan a cabo funciones vitales: Ingestión de nutrientes Eliminación de desperdicios Crecimiento Reproducción
EL CONTROL DE LAS ACTIVIDADES CELULARES LAS REACCIONES CELULARES BÁSICAS Todas las células llevan a cabo funciones vitales: Ingestión de nutrientes Eliminación de desperdicios Crecimiento Reproducción
FISIOLOGÍA LICENCIATURA EN ENFERMERÍA
 UNIDAD TEMÁTICA N 2: FISIOLOGÍA DE LOS TEJIDOS EXCITABLES MÚSCULO Y NERVIO PERIFÉRICO. OBJETIVOS ESPECÍFICOS: Conocer las particularidades de la membrana celular que permiten el pasaje a través de ella.
UNIDAD TEMÁTICA N 2: FISIOLOGÍA DE LOS TEJIDOS EXCITABLES MÚSCULO Y NERVIO PERIFÉRICO. OBJETIVOS ESPECÍFICOS: Conocer las particularidades de la membrana celular que permiten el pasaje a través de ella.
SISTEMA NERVIOSO: MORFOFISIOLOGÍA
 SISTEMA NERVIOSO: MORFOFISIOLOGÍA SISTEMA NERVIOSO El sistema nervioso permite que el organismo responda a los cambios del medio externo e interno. Este controla e integra las actividades funcionales de
SISTEMA NERVIOSO: MORFOFISIOLOGÍA SISTEMA NERVIOSO El sistema nervioso permite que el organismo responda a los cambios del medio externo e interno. Este controla e integra las actividades funcionales de
Tiene a su cargo el movimiento del cuerpo y el cambio de tamaño y forma de los órganos internos.
 Tejido muscular Tiene a su cargo el movimiento del cuerpo y el cambio de tamaño y forma de los órganos internos. Este tejido se caracteriza por poseer conjuntos de células especializadas largas, cuya función
Tejido muscular Tiene a su cargo el movimiento del cuerpo y el cambio de tamaño y forma de los órganos internos. Este tejido se caracteriza por poseer conjuntos de células especializadas largas, cuya función
TRANSPORTE A TRAVÉS DE MEMBRANA
 Cómo la célula moviliza sustancias? TRANSPORTE A TRAVÉS DE MEMBRANA PRUEBA DE CIENCIAS-BIOLOGÍA Profesora: Daniela Marchant Cantillana dmarchantcan@veterinaria.uchile.cl Antes de empezar, recordemos algo
Cómo la célula moviliza sustancias? TRANSPORTE A TRAVÉS DE MEMBRANA PRUEBA DE CIENCIAS-BIOLOGÍA Profesora: Daniela Marchant Cantillana dmarchantcan@veterinaria.uchile.cl Antes de empezar, recordemos algo
Actividad: Cómo controlamos el dolor?
 Nivel: 3º medio Subsector: Biología Unidad temática: Control nervioso y comportamiento Actividad: Cómo controlamos el dolor? A qué le llamamos dolor? El dolor corresponde a una serie de impulsos nerviosos
Nivel: 3º medio Subsector: Biología Unidad temática: Control nervioso y comportamiento Actividad: Cómo controlamos el dolor? A qué le llamamos dolor? El dolor corresponde a una serie de impulsos nerviosos
Selectividad: ANATOMÍA CELULAR
 Selectividad: ANATOMÍA CELULAR Jun09.3.- La figura siguiente muestra un orgánulo celular importante. a.- Cómo se llama este orgánulo? b.- En qué tipo de células se encuentra? c.- Indica qué estructura
Selectividad: ANATOMÍA CELULAR Jun09.3.- La figura siguiente muestra un orgánulo celular importante. a.- Cómo se llama este orgánulo? b.- En qué tipo de células se encuentra? c.- Indica qué estructura
Unidad básica estructural y funcional de todos los seres vivos.
 Unidad básica estructural y funcional de todos los seres vivos. Robert Hooke Siglo XVII Observó que el corcho y otras materias vegetales aparecían constituidas por celdillas. De allí viene el nombre de
Unidad básica estructural y funcional de todos los seres vivos. Robert Hooke Siglo XVII Observó que el corcho y otras materias vegetales aparecían constituidas por celdillas. De allí viene el nombre de
Generación y Transmisión de señales en las Neuronas
 Generación y Transmisión de señales en las Neuronas Los detalle de la transmisión sináptica (comunicación entre neuronas) se explicará en el siguiente capítulo. En éste trataremos de los cambios intraneuronal:
Generación y Transmisión de señales en las Neuronas Los detalle de la transmisión sináptica (comunicación entre neuronas) se explicará en el siguiente capítulo. En éste trataremos de los cambios intraneuronal:
Cristina Santiago Fernández Neurofisiología Clínica. H. U. Río Hortega
 Cristina Santiago Fernández Neurofisiología Clínica. H. U. Río Hortega Diagnóstico Neurofisiológico Confirmar o no el diagnóstico clínico. Excluir otras enfermedades neuromusculares. Determinar si el proceso
Cristina Santiago Fernández Neurofisiología Clínica. H. U. Río Hortega Diagnóstico Neurofisiológico Confirmar o no el diagnóstico clínico. Excluir otras enfermedades neuromusculares. Determinar si el proceso
SISTEMA NERVIOSO Y ENDOCRINO. martes, 19 de marzo de 13
 SISTEMA NERVIOSO Y ENDOCRINO El SISTEMA NERVIOSO se encarga de recibir la información y elaborar las respuestas adecuadas. E s e l procesador de información: coordina y relaciona todas las funciones corporales.
SISTEMA NERVIOSO Y ENDOCRINO El SISTEMA NERVIOSO se encarga de recibir la información y elaborar las respuestas adecuadas. E s e l procesador de información: coordina y relaciona todas las funciones corporales.
UNIDAD II. MECANISMOS CELULARES DE TRANSPORTE E INTEGRACIÓN DE SUSTANCIAS EXTRACELULARES
 UNIDAD II. MECANISMOS CELULARES DE TRANSPORTE E INTEGRACIÓN DE SUSTANCIAS EXTRACELULARES La membrana plasmática: Se encuentra rodeando a la célulac Delimita el territorio de la célula c y controla el
UNIDAD II. MECANISMOS CELULARES DE TRANSPORTE E INTEGRACIÓN DE SUSTANCIAS EXTRACELULARES La membrana plasmática: Se encuentra rodeando a la célulac Delimita el territorio de la célula c y controla el
- Microtúbulos - Microfilamentos - Filamentos intermedios
 Citoesqueleto Cómo se mantiene la forma de una célula? Cómo se transportan proteínas y otras sustancias a través del citoplasma? Cómo se ubican las distintas organelas? La respuesta a estas y otras preguntas
Citoesqueleto Cómo se mantiene la forma de una célula? Cómo se transportan proteínas y otras sustancias a través del citoplasma? Cómo se ubican las distintas organelas? La respuesta a estas y otras preguntas
INTRODUCCIÓN N A LA FISIOLOGIA Versión n alumnos. Dra. Cristina León n de Velasco
 INTRODUCCIÓN N A LA FISIOLOGIA Versión n alumnos Dra. Cristina León n de Velasco FI-UNAM 2007-2 Fisiología: conceptos importantes Proceso fisiológico: gico: sucesión n de fases o estados diferentes. Lo
INTRODUCCIÓN N A LA FISIOLOGIA Versión n alumnos Dra. Cristina León n de Velasco FI-UNAM 2007-2 Fisiología: conceptos importantes Proceso fisiológico: gico: sucesión n de fases o estados diferentes. Lo
SISTEMA NERVIOSO AUTONOMO
 SISTEMA NERVIOSO AUTONOMO OBJETIVOS Revisar organización del SNA Describir respuesta de los efectores en cada tipo (Adrenérgico y Colinérgico) Reconocer modificaciones de las respuestas autónomas con el
SISTEMA NERVIOSO AUTONOMO OBJETIVOS Revisar organización del SNA Describir respuesta de los efectores en cada tipo (Adrenérgico y Colinérgico) Reconocer modificaciones de las respuestas autónomas con el
Evaluación neurofisiológica de las enfermedades de la unión neuromuscular
 Evaluación neurofisiológica de las enfermedades de la unión neuromuscular Lidia Cabañes Martínez Servicio de Neurofisiología Clínica Enfermedades Musculares en la Infancia y Adolescencia (XI) UNIDAD MOTORA
Evaluación neurofisiológica de las enfermedades de la unión neuromuscular Lidia Cabañes Martínez Servicio de Neurofisiología Clínica Enfermedades Musculares en la Infancia y Adolescencia (XI) UNIDAD MOTORA
FISIOLOGÍA DEL CUERPO HUMANO
 FISIOLOGÍA DEL CUERPO HUMANO FUNCIONES VITALES NUTRICIÓN RELACIÓN REPRODUCCIÓN LA FUNCIÓN DE RELACIÓN La función de relación permite a los seres vivos captar los cambios (estímulos) que se producen fuera
FISIOLOGÍA DEL CUERPO HUMANO FUNCIONES VITALES NUTRICIÓN RELACIÓN REPRODUCCIÓN LA FUNCIÓN DE RELACIÓN La función de relación permite a los seres vivos captar los cambios (estímulos) que se producen fuera
FUNCIONES DEL SISTEMA NERVIOSO: CONTROL ESPINAL DEL MOVIMIENTO
 FUNCIONES DEL SISTEMA NERVIOSO: CONTROL ESPINAL DEL MOVIMIENTO FUNCIONES DEL SISTEMA NERVIOSO SISTEMA SENSORIAL : Capta la información. SISTEMA INTEGRADOR : Analiza los estímulos recibidos y decide las
FUNCIONES DEL SISTEMA NERVIOSO: CONTROL ESPINAL DEL MOVIMIENTO FUNCIONES DEL SISTEMA NERVIOSO SISTEMA SENSORIAL : Capta la información. SISTEMA INTEGRADOR : Analiza los estímulos recibidos y decide las
Diferencia entre el sistema nervioso simpático y parasimpático
 Diferencia entre el sistema nervioso simpático y parasimpático Característica Simpático Parasimpático Ganglios Origen Longitud de las Neuronas Neurotransmisor Están ubicados o localizados cerca de la medula
Diferencia entre el sistema nervioso simpático y parasimpático Característica Simpático Parasimpático Ganglios Origen Longitud de las Neuronas Neurotransmisor Están ubicados o localizados cerca de la medula
SISTEMA NERVIOSO AUTONOMO Q. F. N I D I A J. H E R N Á N D E Z Z A M B R A N O
 SISTEMA NERVIOSO AUTONOMO Q. F. N I D I A J. H E R N Á N D E Z Z A M B R A N O SISTEMA NERVIOSO El funcionamiento coordinado de las células de un organismo depende de la comunicación entre ellas Esta comunicación
SISTEMA NERVIOSO AUTONOMO Q. F. N I D I A J. H E R N Á N D E Z Z A M B R A N O SISTEMA NERVIOSO El funcionamiento coordinado de las células de un organismo depende de la comunicación entre ellas Esta comunicación
Es considerada como una de las características funcionales principales de las células.
 DIVISIÓN CELULAR Es considerada como una de las características funcionales principales de las células. El crecimiento y desarrollo adecuados de los organismos vivos depende del crecimiento y multiplicación
DIVISIÓN CELULAR Es considerada como una de las características funcionales principales de las células. El crecimiento y desarrollo adecuados de los organismos vivos depende del crecimiento y multiplicación
PLAN DE NIVELACION DE CIENCIAS NATURALES DEL SEGUNDO PERIODO OCTAVO GRADO 2016
 PLAN DE NIVELACION DE CIENCIAS NATURALES DEL SEGUNDO PERIODO OCTAVO GRADO 2016 1. Las siguientes son funciones de la neurona EXCEPTO: A. Conducir la señal eléctrica B. Recibir información externa interna
PLAN DE NIVELACION DE CIENCIAS NATURALES DEL SEGUNDO PERIODO OCTAVO GRADO 2016 1. Las siguientes son funciones de la neurona EXCEPTO: A. Conducir la señal eléctrica B. Recibir información externa interna
Esclerosis Múltiple. Enfermedad autoinmune dirigida contra componentes de la mielina - glucoproteína mielínica - proteína básica mielina
 Esclerosis Múltiple Esclerosis Múltiple Enfermedad autoinmune dirigida contra componentes de la mielina - glucoproteína mielínica - proteína básica mielina Se caracteriza por la triada: inflamación, desmielinización
Esclerosis Múltiple Esclerosis Múltiple Enfermedad autoinmune dirigida contra componentes de la mielina - glucoproteína mielínica - proteína básica mielina Se caracteriza por la triada: inflamación, desmielinización
II PRÁCTICA DE FISIOLOGIA ANIMAL ELECTROCARDIOGRAMA
 II PRÁCTICA DE FISIOLOGIA ANIMAL ELECTROCARDIOGRAMA 3º CURSO INTRODUCCIÓN A medida que los impulsos cardíacos pasan a través del corazón, las corrientes eléctricas difunden a los tejidos circundantes y
II PRÁCTICA DE FISIOLOGIA ANIMAL ELECTROCARDIOGRAMA 3º CURSO INTRODUCCIÓN A medida que los impulsos cardíacos pasan a través del corazón, las corrientes eléctricas difunden a los tejidos circundantes y
Las funciones de los seres vivos. Fisiología celular
 Las funciones de los seres vivos Fisiología celular La célula, como unidad funcional de los seres vivos, está capacitada para llevar a cabo las funciones características de éstos: nutrición, reproducción
Las funciones de los seres vivos Fisiología celular La célula, como unidad funcional de los seres vivos, está capacitada para llevar a cabo las funciones características de éstos: nutrición, reproducción
LA ORGANIZACIÓN DEL CUERPO HUMANO
 LA ORGANIZACIÓN DEL CUERPO HUMANO RICARDO, ALBERTO, PABLO Y JORGE 1º Los niveles de organización Todos los seres vivos estamos dotados de un conjunto de estructuras con sus funciones específicas. Ordenados
LA ORGANIZACIÓN DEL CUERPO HUMANO RICARDO, ALBERTO, PABLO Y JORGE 1º Los niveles de organización Todos los seres vivos estamos dotados de un conjunto de estructuras con sus funciones específicas. Ordenados
Material del Dpto. de Fisiología- Facultad de Medicina- Universidad de la República Material de uso interno.
 Algunos comentarios previos a modo de instructivo. Cada pregunta consta de 5 opciones entre las que al menos una es incorrecta. En todos los casos es muy importante leer con atención el encabezado; todas
Algunos comentarios previos a modo de instructivo. Cada pregunta consta de 5 opciones entre las que al menos una es incorrecta. En todos los casos es muy importante leer con atención el encabezado; todas
M/E Lámina con tres bandas: dos oscuras (20 30 Å) separada por una banda clara (30 25Å)
 MEMBRANAS CELULARES MEMBRANA CELULAR: Elemento extraordinariamente dinámico y activo que aisla y relaciona a la célula con su entorno. En ella tienen lugar los mas sofisticados procesos de transporte y
MEMBRANAS CELULARES MEMBRANA CELULAR: Elemento extraordinariamente dinámico y activo que aisla y relaciona a la célula con su entorno. En ella tienen lugar los mas sofisticados procesos de transporte y
30/04/2010. SN1: Estructura del sistema nervioso. Anatomía y propiedades de las neuronas.
 SN1: Estructura del sistema nervioso. Anatomía y propiedades de las neuronas. SN2 Potencial de membrana o de reposo. Potencial de acción. Canales iónicos. SN3 Potencial de membrana o de reposo. Potencial
SN1: Estructura del sistema nervioso. Anatomía y propiedades de las neuronas. SN2 Potencial de membrana o de reposo. Potencial de acción. Canales iónicos. SN3 Potencial de membrana o de reposo. Potencial
GUIA DE ESTUDIO PARA PRUEBA DE RELEVANCIA BIOLOGÍA PRIMERO MEDIO GUIA DE APOYO
 Royal American School Subsector Biología Profesor Mario Navarrete GUIA DE ESTUDIO PARA PRUEBA DE RELEVANCIA BIOLOGÍA PRIMERO MEDIO 1.- Complete el siguiente diagrama anotando los organelos y estructuras
Royal American School Subsector Biología Profesor Mario Navarrete GUIA DE ESTUDIO PARA PRUEBA DE RELEVANCIA BIOLOGÍA PRIMERO MEDIO 1.- Complete el siguiente diagrama anotando los organelos y estructuras
2.5 - Tejido nervioso
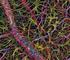 2.5 - Tejido nervioso Tejido especializado en la transmisión de información Se basa en una células llamadas Células nerviosas o Neuronas Estas células necesitan la ayuda de células auxiliares: células
2.5 - Tejido nervioso Tejido especializado en la transmisión de información Se basa en una células llamadas Células nerviosas o Neuronas Estas células necesitan la ayuda de células auxiliares: células
Resultado de aprendizaje:
 Objetivo: Describir composición y arquitectura de las membranas biológicas Resultado de aprendizaje: Explicar la dinámica de las membranas biologicas y su implicación funcional. INTRODUCCION La mayoría
Objetivo: Describir composición y arquitectura de las membranas biológicas Resultado de aprendizaje: Explicar la dinámica de las membranas biologicas y su implicación funcional. INTRODUCCION La mayoría
LA CÉLULA Y LA BASE FÍSICO-QUÍMICA DE LA VIDA
 LA CÉLULA Y LA BASE FÍSICO-QUÍMICA DE LA VIDA 7. PAREDES CELULARES Y MEMBRANA PLASMÁTICA. ORGÁNULOS MICROTUBULARES 1. Membrana plasmática: (jun 97 B4) a) Dibuja un diagrama rotulado de la membrana plasmática
LA CÉLULA Y LA BASE FÍSICO-QUÍMICA DE LA VIDA 7. PAREDES CELULARES Y MEMBRANA PLASMÁTICA. ORGÁNULOS MICROTUBULARES 1. Membrana plasmática: (jun 97 B4) a) Dibuja un diagrama rotulado de la membrana plasmática
FISIOLOGÍA GENERAL Jesús Merino Pérez y María José Noriega Borge
 FISIOLOGÍA DEL MÚSCULO Una de las características de los animales es su capacidad para realizar movimientos coordinados que le permitan la exploración y el aprovechamiento de su entorno. Este movimiento
FISIOLOGÍA DEL MÚSCULO Una de las características de los animales es su capacidad para realizar movimientos coordinados que le permitan la exploración y el aprovechamiento de su entorno. Este movimiento
Nutrición Vegetal. Absorción de sales minerales
 Nutrición Vegetal Absorción de sales minerales Absorción - Es el proceso mediante el cual un ión o molécula ingresa a una célula o un cuerpo a través de una membrana. No intervienen fuerzas intermoleculares.
Nutrición Vegetal Absorción de sales minerales Absorción - Es el proceso mediante el cual un ión o molécula ingresa a una célula o un cuerpo a través de una membrana. No intervienen fuerzas intermoleculares.
La Célula. Membrana celular. UNIVERSIDAD NACIONAL DE GRAL. SAN MARTÍN ECyT BIOLOGÍA. Biología I
 La Célula. Membrana celular UNIVERSIDAD NACIONAL DE GRAL. SAN MARTÍN ECyT BIOLOGÍA Biología I Los seres vivos están formados por células Organismos unicelulares: bacterias, plantas (algas unicelulares),
La Célula. Membrana celular UNIVERSIDAD NACIONAL DE GRAL. SAN MARTÍN ECyT BIOLOGÍA Biología I Los seres vivos están formados por células Organismos unicelulares: bacterias, plantas (algas unicelulares),
BASES BIOFÍSICAS DE LA EXCITABILIDAD
 BASES BIOFÍSICAS DE LA EXCITABILIDAD Depto. Biofísica Facultad de Medicina ESFUNO Escuelas UTI: Biología Celular y Tisular Importancia del estudio de la membrana celular Funciones de la membrana: -Barrera
BASES BIOFÍSICAS DE LA EXCITABILIDAD Depto. Biofísica Facultad de Medicina ESFUNO Escuelas UTI: Biología Celular y Tisular Importancia del estudio de la membrana celular Funciones de la membrana: -Barrera
FISIOLOGÍA DEL CUERPO HUMANO
 FISIOLOGÍA DEL CUERPO HUMANO FUNCIONES VITALES NUTRICIÓN RELACIÓN REPRODUCCIÓN LA FUNCIÓN DE RELACIÓN La función de relación permite a los seres vivos captar los cambios (estímulos) que se producen fuera
FISIOLOGÍA DEL CUERPO HUMANO FUNCIONES VITALES NUTRICIÓN RELACIÓN REPRODUCCIÓN LA FUNCIÓN DE RELACIÓN La función de relación permite a los seres vivos captar los cambios (estímulos) que se producen fuera
Profesor Mauricio Hernández F Biología 3 Medio
 Acción Hormonal Introducción Las hormonas son moléculas o macromoléculas químicas, que participan de la regulación de numerosos procesos, manteniendo la homeostasis. Las hormonas son mensajeros químicos,
Acción Hormonal Introducción Las hormonas son moléculas o macromoléculas químicas, que participan de la regulación de numerosos procesos, manteniendo la homeostasis. Las hormonas son mensajeros químicos,
CMUCH. TERAPIA FÍSICA
 LA NEURONA M-BOOK #5 El hecho de que las células constituyen los elementos básicos de los organismos vivíos fue reconocido en un periodo temprano en el siglo XX en que los neurocientificos concordaron
LA NEURONA M-BOOK #5 El hecho de que las células constituyen los elementos básicos de los organismos vivíos fue reconocido en un periodo temprano en el siglo XX en que los neurocientificos concordaron
Repaso: Química celular (biomoléculas)
 Repaso: Química celular (biomoléculas) Hay 4 tipos principales de biomoléculas: 1) glúcidos o hidratos de carbono, 2) lípidos o grasas, 3) proteínas y 4) ácidos nucleicos. Las biomoléculas más grandes,
Repaso: Química celular (biomoléculas) Hay 4 tipos principales de biomoléculas: 1) glúcidos o hidratos de carbono, 2) lípidos o grasas, 3) proteínas y 4) ácidos nucleicos. Las biomoléculas más grandes,
Organización Funcional y el Medio Interno
 Organización Funcional y el Medio Interno Aproximadamente el 50 % del cuerpo humano es líquido y la mayor parte es intracelular, la tercera parte es extracelular, la misma que se encuentra en movimiento
Organización Funcional y el Medio Interno Aproximadamente el 50 % del cuerpo humano es líquido y la mayor parte es intracelular, la tercera parte es extracelular, la misma que se encuentra en movimiento
LA NEURONA Historia. Concepto
 LA NEURONA Historia A fines del siglo XIX, Santiago Ramón y Cajal situó por vez primera las neuronas como elementos funcionales del sistema nervioso.4 Cajal propuso que actuaban como entidades discretas
LA NEURONA Historia A fines del siglo XIX, Santiago Ramón y Cajal situó por vez primera las neuronas como elementos funcionales del sistema nervioso.4 Cajal propuso que actuaban como entidades discretas
TEMA 1: CELULAS DEL SISTEMA NERVIOSO
 TEMA 1: CELULAS DEL SISTEMA NERVIOSO Dos son los tipos fundamentales de células cerebrales: Las neuronas, principales portadoras de información y las células de la glía, con misión auxiliar. Página 2 Cuántas
TEMA 1: CELULAS DEL SISTEMA NERVIOSO Dos son los tipos fundamentales de células cerebrales: Las neuronas, principales portadoras de información y las células de la glía, con misión auxiliar. Página 2 Cuántas
Tema 16. Señalización celular I.
 Tema 16. Señalización celular I. 1.Organismos pluricelulares y homeostasis. 2.Sistema endocrino. Hormonas 3. El sistema nervioso. 3.1. Estructura de una neurona. 3.2. Transmisión sináptica: tipos de sinapsis.
Tema 16. Señalización celular I. 1.Organismos pluricelulares y homeostasis. 2.Sistema endocrino. Hormonas 3. El sistema nervioso. 3.1. Estructura de una neurona. 3.2. Transmisión sináptica: tipos de sinapsis.
Tema VI: Transporte Celular
 República Bolivariana de Venezuela Ministerio del Poder Popular para la Educación U.E. Colegio Santo Tomás de Villanueva Departamento de Ciencias Cátedra: Ciencias Biológicas 3 Año Tema VI: Transporte
República Bolivariana de Venezuela Ministerio del Poder Popular para la Educación U.E. Colegio Santo Tomás de Villanueva Departamento de Ciencias Cátedra: Ciencias Biológicas 3 Año Tema VI: Transporte
Cómo ocurre la fecundación en los mamíferos?
 Cómo ocurre la fecundación en los mamíferos? Aparato reproductor femenino La fecundación, también llamada fertilización, es la penetración del espermatozoide en el interior del óvulo con la unión de los
Cómo ocurre la fecundación en los mamíferos? Aparato reproductor femenino La fecundación, también llamada fertilización, es la penetración del espermatozoide en el interior del óvulo con la unión de los
BLOQUE II. ORGANIZACIÓN Y FISIOLOGÍA CELULAR
 I.E.S. Flavio Irnitano El Saucejo (Sevilla) Curso 2.015 2.016 Departamento de Biología y Geología NIVEL: 2º Bachillerato MATERIA: BIOLOGÍA BLOQUE II. ORGANIZACIÓN Y FISIOLOGÍA CELULAR 3. CÉLULA EUCARIÓTICA.
I.E.S. Flavio Irnitano El Saucejo (Sevilla) Curso 2.015 2.016 Departamento de Biología y Geología NIVEL: 2º Bachillerato MATERIA: BIOLOGÍA BLOQUE II. ORGANIZACIÓN Y FISIOLOGÍA CELULAR 3. CÉLULA EUCARIÓTICA.
La célula animal y vegetal. Miller & Levine Pags
 La célula animal y vegetal Miller & Levine Pags. 196-205 Célula animal Membrana celular: fina capa de proteína y grasa que rodea la célula. La membrana celular es semipermeable, permitiendo que algunas
La célula animal y vegetal Miller & Levine Pags. 196-205 Célula animal Membrana celular: fina capa de proteína y grasa que rodea la célula. La membrana celular es semipermeable, permitiendo que algunas
UNIDAD II ANATOMÍA Y FISIOLOGÍA DE LA CÉLULA. Prof. Glamil Acevedo Anatomía y Fisiología
 UNIDAD II ANATOMÍA Y FISIOLOGÍA DE LA CÉLULA Prof. Glamil Acevedo Anatomía y Fisiología La Célula Es la unidad funcional y estructural más pequeña de los organismos vivos. Se compone de partes características,
UNIDAD II ANATOMÍA Y FISIOLOGÍA DE LA CÉLULA Prof. Glamil Acevedo Anatomía y Fisiología La Célula Es la unidad funcional y estructural más pequeña de los organismos vivos. Se compone de partes características,
Es la capacidad de realizar un trabajo. A pesar que existen varias formas de energía: química, luminosa, mecánica, etc., solo hay dos tipos básicos:
 Es la capacidad de realizar un trabajo. A pesar que existen varias formas de energía: química, luminosa, mecánica, etc., solo hay dos tipos básicos: Potencial: es la capacidad de realizar trabajo como
Es la capacidad de realizar un trabajo. A pesar que existen varias formas de energía: química, luminosa, mecánica, etc., solo hay dos tipos básicos: Potencial: es la capacidad de realizar trabajo como
1. TEORÍA CELULAR 2. ORGANIZACIÓN CELULAR PROCARIOTA 3. ORGANIZACIÓN CELULAR EUCARIOTA: ANIMAL Y VEGETAL
 LAS CÉLULAS INDICE: 1. TEORÍA CELULAR 2. ORGANIZACIÓN CELULAR PROCARIOTA 3. ORGANIZACIÓN CELULAR EUCARIOTA: ANIMAL Y VEGETAL 1º.- TEORÍA CELULAR Los principios básicos de la teoría celular son: La célula
LAS CÉLULAS INDICE: 1. TEORÍA CELULAR 2. ORGANIZACIÓN CELULAR PROCARIOTA 3. ORGANIZACIÓN CELULAR EUCARIOTA: ANIMAL Y VEGETAL 1º.- TEORÍA CELULAR Los principios básicos de la teoría celular son: La célula
Unidad Didáctica I. Tema 1. Conceptos generales de Fisiología y Fisiopatología. Tema 1. Conceptos generales de Fisiología y Fisiopatología.
 Unidad Didáctica I. It Introducción a la Fiil Fisiología. Concepto de Homeostasis. Conceptos Fisiopatológicos Básicos.... 1. Concepto de Fisiología. 1.1.Regulación 1 fisiológica y concepto de homeostasis.
Unidad Didáctica I. It Introducción a la Fiil Fisiología. Concepto de Homeostasis. Conceptos Fisiopatológicos Básicos.... 1. Concepto de Fisiología. 1.1.Regulación 1 fisiológica y concepto de homeostasis.
Lección 22. Mecanismos de transporte a través de membranas
 Lección 22. Mecanismos de transporte a través de membranas Objetivos: 1. Diferenciar los mecanismos de transporte de solutos apolares y de solutos polares a través de las membranas 2. Clasificar los diferentes
Lección 22. Mecanismos de transporte a través de membranas Objetivos: 1. Diferenciar los mecanismos de transporte de solutos apolares y de solutos polares a través de las membranas 2. Clasificar los diferentes
Estructura celular. Teoría Celular. Cap. 4. Los organismos se componen de una o más células. La célula es la unidad más pequeña de la vida.
 Estructura celular Cap. 4 Teoría Celular Los organismos se componen de una o más células. Procesos metabólicos y de la herencia ocurren dentro de la célula. La célula es la unidad más pequeña de la vida.
Estructura celular Cap. 4 Teoría Celular Los organismos se componen de una o más células. Procesos metabólicos y de la herencia ocurren dentro de la célula. La célula es la unidad más pequeña de la vida.
ESTRUCTURA
 ESTRUCTURA Las células poseen diferentes membranas, como por ejemplo, la membrana plasmática, las membranas de organoides como ser el R.E., el complejo de Golgi, los endosomas, los lisosomas, las vesículas,
ESTRUCTURA Las células poseen diferentes membranas, como por ejemplo, la membrana plasmática, las membranas de organoides como ser el R.E., el complejo de Golgi, los endosomas, los lisosomas, las vesículas,
Teoría celular (1) Idea: la célula es la unidad básica de la vida
 LA CÉLULA Tema 2 Teoría celular (1) Idea: la célula es la unidad básica de la vida Primeras células observadas. Celdillas de corcho (R. Hooke, 1665) Animales microscópicos (A. Van Leeuwenhoek,1675) todos
LA CÉLULA Tema 2 Teoría celular (1) Idea: la célula es la unidad básica de la vida Primeras células observadas. Celdillas de corcho (R. Hooke, 1665) Animales microscópicos (A. Van Leeuwenhoek,1675) todos
Usos de fármacos durante el embarazo y la lactancia
 Usos de fármacos durante el embarazo y la lactancia -Son situaciones farmacocinéticas especiales. -En estos estados fisiológicos los fármacos actúan de diferente manera. *Fármacos administrados a la madre
Usos de fármacos durante el embarazo y la lactancia -Son situaciones farmacocinéticas especiales. -En estos estados fisiológicos los fármacos actúan de diferente manera. *Fármacos administrados a la madre
Tejido Nervioso Las neuronas Las células gliales
 Tejido Nervioso Está formado por células y escasa sustancia extracelular. El material interpuesto entre las células no es un material predominante extracelular fibroso o amorfo como en el tejido conectivo,
Tejido Nervioso Está formado por células y escasa sustancia extracelular. El material interpuesto entre las células no es un material predominante extracelular fibroso o amorfo como en el tejido conectivo,
CAPÍTULO 2 FLUJO DE LA INFORMACIÓN BIOLÓGICA FACULTAD DE AGRONOMÍA CURSO DE BIOQUÍMICA
 CAPÍTULO 2 FLUJO DE LA INFORMACIÓN BIOLÓGICA FACULTAD DE AGRONOMÍA CURSO DE BIOQUÍMICA Contenido 2.1 Información biológica e interacciones no covalentes. 2.2 Almacenamiento de la información biológica
CAPÍTULO 2 FLUJO DE LA INFORMACIÓN BIOLÓGICA FACULTAD DE AGRONOMÍA CURSO DE BIOQUÍMICA Contenido 2.1 Información biológica e interacciones no covalentes. 2.2 Almacenamiento de la información biológica
UNIDAD 1. D. Borja Blanco Vives. Profesor de Biología y Geología 4ºESO
 UNIDAD 1. D. Borja Blanco Vives. Profesor de Biología y Geología 4ºESO 1. LA COMPOSICIÓN DE LOS SERES VIVOS. Todos los seres vivos están formados por: - materia inorgánica: agua y sales minerales - materia
UNIDAD 1. D. Borja Blanco Vives. Profesor de Biología y Geología 4ºESO 1. LA COMPOSICIÓN DE LOS SERES VIVOS. Todos los seres vivos están formados por: - materia inorgánica: agua y sales minerales - materia
GUIA DE COMPLEMENTACION DE CONTENIDOS 3º Medio Común MUSCULOS COMO EFECTORES
 GUIA DE COMPLEMENTACION DE CONTENIDOS 3º Medio Común MUSCULOS COMO EFECTORES Vías Eferentes Estructuras de respuestas: los efectores El sistema nervioso es capaz de elaborar respuestas frente a los cambios
GUIA DE COMPLEMENTACION DE CONTENIDOS 3º Medio Común MUSCULOS COMO EFECTORES Vías Eferentes Estructuras de respuestas: los efectores El sistema nervioso es capaz de elaborar respuestas frente a los cambios
TEMA 1. ORGANIZACIÓN DEL CUERPO HUMANO
 TEMA 1. ORGANIZACIÓN DEL CUERPO HUMANO I.- NIVELES DE ORGANIZACIÓN DE LOS SERES HUMANOS. Elementos o átomos C H O N P S Moléculas sencillas H 2 O O 2 Aminoácido Monosacárido Moléculas complejas Células
TEMA 1. ORGANIZACIÓN DEL CUERPO HUMANO I.- NIVELES DE ORGANIZACIÓN DE LOS SERES HUMANOS. Elementos o átomos C H O N P S Moléculas sencillas H 2 O O 2 Aminoácido Monosacárido Moléculas complejas Células
Seminario Práctico Nº 4 FARMACOLOGÍA DEL SISTEMA NERVIOSO AUTÓNOMO (I) EL EJEMPLO DEL OJO.-
 Facultad de Medicina Departamento de Farmacología y Terapéutica Seminario Práctico Nº 4 FARMACOLOGÍA DEL SISTEMA NERVIOSO AUTÓNOMO (I) EL EJEMPLO DEL OJO.- 1.- Control autonómico del diámetro pupilar La
Facultad de Medicina Departamento de Farmacología y Terapéutica Seminario Práctico Nº 4 FARMACOLOGÍA DEL SISTEMA NERVIOSO AUTÓNOMO (I) EL EJEMPLO DEL OJO.- 1.- Control autonómico del diámetro pupilar La
Niveles de organización biológica. La composición de los seres vivos
 Niveles de organización biológica. La composición de los seres vivos Imagen de Fondo bajo licencia Creative Commons, autor: René Ehrtardt. Animación ADN de dominio público, fuente:wikipedia Con este tema
Niveles de organización biológica. La composición de los seres vivos Imagen de Fondo bajo licencia Creative Commons, autor: René Ehrtardt. Animación ADN de dominio público, fuente:wikipedia Con este tema
Diferenciaciones de la membrana plasmática. Microvellosidades
 Diferenciaciones de la membrana plasmática Son regiones de la membrana plasmática que presentan modificaciones estructurales especializadas para cumplir diferentes funciones. Un típico ejemplo lo ofrecen
Diferenciaciones de la membrana plasmática Son regiones de la membrana plasmática que presentan modificaciones estructurales especializadas para cumplir diferentes funciones. Un típico ejemplo lo ofrecen
ESTRUCTURA Y FUNCION CELULAR
 ESTRUCTURA Y FUNCION CELULAR Sumario Historia de la teoría celular Estructura y función celular 1. El núcleo 2. Los organelos citoplásmicos 3. Los organelos de células vegetales Transporte celular Métodos
ESTRUCTURA Y FUNCION CELULAR Sumario Historia de la teoría celular Estructura y función celular 1. El núcleo 2. Los organelos citoplásmicos 3. Los organelos de células vegetales Transporte celular Métodos
La organización del cuerpo humano. Punto 1: Los niveles de organización.
 La organización del cuerpo humano Punto 1: Los niveles de organización. ATOMO MOLECULA Unidad constituyente más pequeña de la materia ordinaria. Conjunto de al menos dos átomos enlazados covalentes que
La organización del cuerpo humano Punto 1: Los niveles de organización. ATOMO MOLECULA Unidad constituyente más pequeña de la materia ordinaria. Conjunto de al menos dos átomos enlazados covalentes que
Proteínas y Ácidos Nucleicos
 Proteínas y Ácidos Nucleicos Mapa conceptual Biomoléculas. Biomoléculas inorgánicas: Moléculas que no presentan carbono en su estructura. Biomoléculas orgánicas: Moléculas que presentan carbono en su estructura.
Proteínas y Ácidos Nucleicos Mapa conceptual Biomoléculas. Biomoléculas inorgánicas: Moléculas que no presentan carbono en su estructura. Biomoléculas orgánicas: Moléculas que presentan carbono en su estructura.
Revisión- Opción Múltiple Procesamiento de energía
 Revisión- Opción Múltiple Procesamiento de energía 1. El mmetabolismo es considerado como las "reacciones químicas totales que ocurren dentro de un organismo". Estas reacciones químicas pueden estar vinculados
Revisión- Opción Múltiple Procesamiento de energía 1. El mmetabolismo es considerado como las "reacciones químicas totales que ocurren dentro de un organismo". Estas reacciones químicas pueden estar vinculados
2.4 - Tejido muscular
 2.4 - Tejido muscular Los animales poseemos un tejido contráctil especializado: el tejido muscular Está formado por células con gran cantidad de fibras contráctiles internas Estas fibras están formadas
2.4 - Tejido muscular Los animales poseemos un tejido contráctil especializado: el tejido muscular Está formado por células con gran cantidad de fibras contráctiles internas Estas fibras están formadas
los MÚSCULOS, ÓRGANOS ACTIVOS DEL APARATO LOCOMOTOR
 los MÚSCULOS, ÓRGANOS ACTIVOS DEL APARATO LOCOMOTOR ESTRUCTURA Y COMPOSICIÓN PROPIEDADES DEL TEJIDO MUSCULAR Excitabilidad Las células musculares responden a estímulos eléctricos. Contractibilidad Las
los MÚSCULOS, ÓRGANOS ACTIVOS DEL APARATO LOCOMOTOR ESTRUCTURA Y COMPOSICIÓN PROPIEDADES DEL TEJIDO MUSCULAR Excitabilidad Las células musculares responden a estímulos eléctricos. Contractibilidad Las
Bloque II: Estructura y fisiología de la célula TEMA 10: LA CÉLULA EUCARIOTA: ESTRUCTURAS Y ORGÁNULOS NO MEMBRANOSOS.
 Bloque II: Estructura y fisiología de la célula TEMA 10: LA CÉLULA EUCARIOTA: ESTRUCTURAS Y ORGÁNULOS NO MEMBRANOSOS. PARED CELULAR Envoltura gruesa y rígida. En plantas, hongos, algas y bacterias. LA
Bloque II: Estructura y fisiología de la célula TEMA 10: LA CÉLULA EUCARIOTA: ESTRUCTURAS Y ORGÁNULOS NO MEMBRANOSOS. PARED CELULAR Envoltura gruesa y rígida. En plantas, hongos, algas y bacterias. LA
Fisiología y Envejecimiento Sistema muscular. Tema 7
 Tema 7 * Clasificación. * Funciones. * Anatomofisiología del músculo esquelético. * Mecanismo general de la contracción muscular. Clasificación Los músculos se pueden clasificar según 3 criterios: 1. Anatómicamente:
Tema 7 * Clasificación. * Funciones. * Anatomofisiología del músculo esquelético. * Mecanismo general de la contracción muscular. Clasificación Los músculos se pueden clasificar según 3 criterios: 1. Anatómicamente:
LA RESPIRACIÓN CELULAR
 LA RESPIRACIÓN CELULAR Respiración celular La degradación de la glucosa mediante el uso de oxígeno o alguna otra sustancia inorgánica, se conoce como respiración celular. La respiración celular que necesita
LA RESPIRACIÓN CELULAR Respiración celular La degradación de la glucosa mediante el uso de oxígeno o alguna otra sustancia inorgánica, se conoce como respiración celular. La respiración celular que necesita
Células. 2ª Parte: Células procariotas. Tema 13 de Biología NS Diploma BI Curso
 Células 2ª Parte: Células procariotas Tema 13 de Biología NS Diploma BI Curso 2012-2014 Estructura de la célula procariota: Escherichia coli Las bacterias son las células procariotas típicas. Tienen pequeño
Células 2ª Parte: Células procariotas Tema 13 de Biología NS Diploma BI Curso 2012-2014 Estructura de la célula procariota: Escherichia coli Las bacterias son las células procariotas típicas. Tienen pequeño
Control de Expresión Génica Procariota. Profesor: Javier Cabello Schomburg, MS
 Control de Expresión Génica Procariota Profesor: Javier Cabello Schomburg, MS Qué es un gen? Es una secuencia de nucleótidos en la molécula de ADN, equivalente a una unidad de transcripción. Contiene la
Control de Expresión Génica Procariota Profesor: Javier Cabello Schomburg, MS Qué es un gen? Es una secuencia de nucleótidos en la molécula de ADN, equivalente a una unidad de transcripción. Contiene la
Comunicación y Mecanismos de Señalización Celular
 Comunicación y Mecanismos de Señalización Celular Qué le dijo una célula a otra célula? Figure 15-8 Molecular Biology of the Cell ( Garland Science 2008) Qué le dijo una célula a otra célula? Figure 15-8
Comunicación y Mecanismos de Señalización Celular Qué le dijo una célula a otra célula? Figure 15-8 Molecular Biology of the Cell ( Garland Science 2008) Qué le dijo una célula a otra célula? Figure 15-8
RECOMENDACIONES DE SELECTIVIDAD
 RECOMENDACIONES DE SELECTIVIDAD 1. Se recomienda que los procesos de replicación del ADN, transcripción y traducción se expliquen tomando como referencia lo que acontece en una célula procariótica sin
RECOMENDACIONES DE SELECTIVIDAD 1. Se recomienda que los procesos de replicación del ADN, transcripción y traducción se expliquen tomando como referencia lo que acontece en una célula procariótica sin
