PARTE 1 (DECISIÓN DEL CONSEJO 2002/813/CE)
|
|
|
- Montserrat Valdéz Benítez
- hace 6 años
- Vistas:
Transcripción
1 PARTE 1 (DECISIÓN DEL CONSEJO 2002/813/CE) MODELO DE RESUMEN DE LA NOTIFICACIÓN DE LA LIBERACIÓN DE ORGANISMOS MODIFICADOS GENÉTICAMENTE DISTINTOS DE LAS PLANTAS SUPERIORES DE ACUERDO CON EL ARTÍCULO 11 DE LA DIRECTIVA 2001/18/CE A. Información de carácter general: 1. Detalles de la notificación a) Estado miembro de la notificación: España b) Número de la notificación: B/ES/18/05 c) Fecha del acuse de recibo de la notificación: 26-Mar-2018 d) Título del proyecto: Ensayo clínico 19429, Ensayo de fase I/II, abierto, de seguridad y de búsqueda de dosis de BAY (DTX201), una transferencia génica del factor VIII humano con el dominio B eliminado -mediada por el virus adenoasociado (VAA) del serotipo hu37- en adultos con hemofilia A grave e) Período propuesto para la liberación: Agosto 2018 Marzo Notificador Nombre de la institución o empresa: Bayer AG D Leverkusen Alemania 3. Definición de la OMG a) Indíquese si el OMG es: Viroide Virus ARN Virus ADN Bacteria Hongo Animal - mamíferos - insectos - peces - otro animal especifique el phylum y la clase Otro, especifíquese (reino, phylum y clase) Página 1 de 28
2 b) Identidad del OMG (género y especie) Género: Dependoparvovirus Especie: Virus adenoasociado de serotipo humano 37 (AAVhu37) c) Estabilidad genética, de acuerdo con el punto 10 de la letra A de la sección II del anexo III A: El AAV es un virus ADN monocatenario con una gran estabilidad genética, según pone de manifiesto la estrecha relación existente entre los genes rep y cap de distintos serotipos y genomovares del AAV. En relación con estos datos sobre homologías de secuencias, está el hecho de que el AAV utiliza una ADN polimerasa del huésped para la replicación viral que no muestra propensión a errores en comparación con las ARN polimerasas que emplean los virus ARN. En relación con la estabilidad genética, está la observación de que los episomas de ADN proviral de AAV aislados de diferentes muestras de tejidos humanos poseen sistemáticamente la secuencia rep y cap canónica esperada de AAV2. En base a estas características del AAV natural, también cabe esperar que BAY (DTX201) sea genéticamente muy estable. La secuencia del genoma del vector de BAY (DTX201) se verifica mediante secuenciación directa. 4. Tiene previsto el mismo notificador la liberación de ese mismo OMG en algún otro lugar de la Comunidad (de acuerdo con el apartado 1 del artículo 6)? Sí En caso afirmativo, indique el código del país: BG, DE, FR, GB, NL No 5. Ha notificado ese mismo notificador la liberación de ese mismo OMG en algún otro lugar de la Comunidad? Sí En caso afirmativo: - Estado miembro de la notificación: - Número de la notificación: No Utilice los siguientes códigos nacionales: Austria AT; Bélgica BE; Alemania DE; Dinamarca DK; España ES; Finlandia FI; Francia FR; Reino Unido GB; Grecia GR; Irlanda IE; Islandia IS; Italia IT; Luxemburgo LU; Países Bajos NL; Noruega NO; Portugal PT; Suecia SE. Página 2 de 28
3 6. Ha notificado el mismo notificador u otro la liberación o comercialización de ese mismo OMG fuera de la Comunidad? Sí No En caso afirmativo: - Estado miembro de la notificación: EE.UU. - Número de la notificación: Protocolo n.º del NIH 7. Resumen del impacto ambiental potencial de la liberación de los OMG BAY (DTX201), el producto del ensayo, es un AAVhu37FVIII, es decir, un vector de AAVhu37 recombinante sin capacidad de replicación que contiene un genoma de ADN monocatenario que codifica una forma de FVIII humano bajo el control del promotor específico del hígado para el tratamiento de los pacientes con hemofilia A. No cabe esperar que la liberación de BAY (DTX201), tal como se describe en esta solicitud, tenga un impacto ambiental adverso, por las siguientes razones: Ausencia de patogenicidad del virus parental: A pesar de una seroprevalencia estimada de hasta el 90% de algunos serotipos humanos frecuentes, no se han identificado efectos patógenos del AAV. OMG sin capacidad de replicación: BAY (DTX201) es un vector de AAV recombinante no infeccioso que carece de todos los genes virales del AAV y no puede replicarse sin funciones auxiliares específicas del AAV y sin la actividad de un virus auxiliar. La replicación de BAY (DTX201) solo podría tener lugar en el caso extraordinariamente improbable de que una célula huésped resultara infectada por tres virus distintos (BAY (DTX201), AAV natural y un virus auxiliar, como adenovirus humano o virus del herpes simple). El riesgo de que esto ocurra es insignificante. Riesgo mínimo de transmisión por diseminación del virus: Se ha comprobado que el ADN del vector de AAV se disemina en la saliva, orina, heces y semen de primates no humanos después de su administración sistémica. En general, se observó diseminación en los pacientes que recibieron una dosis única de a CG/kg de un vector de AAV recombinante en las heces, orina, saliva y semen durante un máximo de 10 a 50 días después de la administración del vector, con concentraciones máximas obtenidas en torno a dos días después de la administración (Nathwani 2011, Nathwani 2012, Nathwani 2014). La magnitud y la duración de la diseminación de BAY (DTX201) se controlarán como parte del ensayo clínico propuesto. Sin embargo, dado que BAY (DTX201) carece de capacidad de replicación, las partículas virales diseminadas no pueden multiplicarse y, por consiguiente, su dispersión se encuentra limitada de manera inherente. Además, los posibles riesgos de exposición a BAY (DTX201) para los seres humanos están basados en la administración sistémica de BAY (DTX201). Una exposición mínima, como la exposición ambiental, de personas distintas de los sujetos que reciban BAY (DTX201) como parte del ensayo no sería una dosis suficiente para representar una expresión génica significativa ni problemas de seguridad para los seres humanos. Cabe esperar que la carga viral en orina y heces sea baja. Aparte de los posibles huéspedes humanos, no cabe esperar que la exposición a Página 3 de 28
4 BAY (DTX201) afecte a organismos no diana, ya sea de manera directa o indirecta. Así pues, el riesgo para los seres humanos y el medio ambiente asociado a la diseminación viral de BAY (DTX201) es bajo o insignificante. Riesgo mínimo de mutagénesis por inserción: El riesgo de mutagénesis por inserción se considera bajo o insignificante, ya que la inmensa mayoría del ADN del vector de AAVr persiste en forma de episoma ( 99,5%) en lugar de como ADN integrado. En ningún ensayo clínico de AAV hasta la fecha se han descrito casos de mutagénesis por inserción. Expresión del transgén específica del hígado: El estudio de toxicidad/biodistribución conforme a la BPL confirma el tropismo esperado del vector AAVhu37 por el hígado. BAY (DTX201) codifica el gen del factor VIII cuya expresión se ve estimulada por un promotor específico del hígado encapsidado en un vector de AAVhu37. Por tanto, se considera que la expresión del transgén en células diferentes de los hepatocitos humanos es improbable. Riesgo mínimo asociado al transgén: El vector AAV codifica el gen del factor VIII humano. En el OMG no se han introducido genes que codifican toxinas, posibles oncogenes, factores de crecimiento ni otros genes que podrían ser potencialmente perjudiciales. B. Información sobre el organismo receptor o sobre los organismos parentales de los que se deriva el OMG 1. Identificación del organismo receptor o parental a) Indíquese si el organismo receptor o parental es: Viroide Virus ARN Virus ADN Bacteria Hongo Animal - mamíferos - insectos - peces - otro animal (especifique el phylum y la clase) Otros, (especifíquense): Página 4 de 28
5 2. Nombre i) Orden y taxón superior (animales): Virus ADN monocatenario ii) Género: Dependoparvovirus iii) Especie: Virus adenoasociado iv) Subespecie: No procede v) Cepa: serotipo hu37 vi) Patovar (biotipo, ecotipo, raza, etc.): No procede vii) Nombre vulgar: No procede 3. Distribución geográfica del organismo a) Autóctono del país que notifica o establecido en él: Sí No No se sabe b) Autóctono de otros países de la Comunidad o establecido en ellos: i) Sí En caso afirmativo, indíquese el tipo de ecosistema en que se encuentra: ii) No Atlántico Mediterráneo Boreal Alpino Continental Macaronésico iii) No se sabe Página 5 de 28
6 c) Se usa frecuentemente en el país que notifica? Sí No d) Es frecuente su tenencia en el país que notifica? Sí No 4. Hábitat natural del organismo a) Si es un microorganismo: Agua Suelo, en libertad Suelo, en simobiosis radiculares de plantas En simbiosis con sistemas foliares o caulinares de plantas En simbiosis con animales Otros, (especifíquense): En asociación con animales (huéspedes primates) b) Si es un animal, hábitat natural o ecosistema agrícola habitual: No procede. 5.a) Técnicas de detección El AAV puede detectarse mediante reacción en cadena de la polimerasa cuantitativa (qpcr) con cebadores específicos del genoma viral. 5.b) Técnicas de identificación El AAV puede identificarse mediante reacción en cadena de la polimerasa cuantitativa (qpcr) con cebadores específicos del genoma viral. Página 6 de 28
7 6. Está clasificado el organismo receptor con arreglo a las normas comunitarias vigentes en relación con la protección de la salud humana y el medio ambiente? Sí No En caso afirmativo, especifíquese: El AAV natural no es patógeno y no se ha clasificado según la Directiva 2000/54/CE del Parlamento Europeo y del Consejo de 18 de septiembre de 2000 sobre la protección de los trabajadores contra los riesgos relacionados con la exposición a agentes biológicos durante el trabajo. El AAV carece de efectos patógenos conocidos, a pesar de que la seroprevalencia estimada de algunos serotipos humanos frecuentes es del 90%. En consecuencia, el AAV cumple la definición de agente biológico del grupo 1 según la Directiva 2000/54/CE (un agente biológico con pocas probabilidades de causar enfermedad en los seres humanos). 7. Es el organismo receptor, vivo o muerto (incluidos sus productos extracelulares), apreciablemente patógeno o nocivo de cualquier otra forma? Sí No No se sabe En caso afirmativo a) Para cuál de los organismos siguientes?: humanos animales plantas otros b) Aporte la información pertinente especificada en la letra d) del punto 11 de la letra A de la sección 11 del anexo III A de la Directiva 2001/18/CE. Página 7 de 28
8 8. Información sobre reproducción a) Tiempo de generación en ecosistemas naturales: El AAV carece de capacidad de replicación, por lo que el tiempo de generación es variable en función de la presencia o ausencia de un virus auxiliar. b) Tiempo de generación en el ecosistema en el que vaya a ser liberado: El AAV carece de capacidad de replicación, por lo que el tiempo de generación es variable en función de la presencia o ausencia de un virus auxiliar. c) Modo de reproducción Sexual No procede Asexual No procede d) Factores que afectan a la reproducción: La presencia de un virus auxiliar, como adenovirus o virus del herpes simple, favorece la expresión génica del AAV, la replicación del genoma y la producción de viriones. En ausencia de un virus auxiliar, el AAV natural carece de capacidad de replicación. Hay que señalar que el OMG final, BAY (DTX201), no tiene capacidad de replicación ni siquiera en presencia de un virus auxiliar debido a la eliminación de los genes virales rep y cap. 9. Capacidad de supervivencia a) Capacidad de formar estructuras que favorezcan la supervivencia o el letargo (i) endosporas (ii) quistes (iii) esclerocios (iv) esporas asexuales(hongos) (v) esporas sexuales (hongos) (vi) huevos (vii) pupas (viii) larvas (ix) otras (especifíquense) El AAV no forma estructuras de supervivencia. b) Factores pertinentes que afectan a la capacidad de supervivencia: Los miembros de la familia de los parvovirus, como el AAV, son virus estables que pueden persistir en el ambiente durante períodos prolongados (del orden de varias semanas). Las partículas de AAV son resistentes a una amplia variedad de ph (ph 3-9) y soportan temperaturas elevadas (55 C durante 1 hora). El AAV no forma estructuras de supervivencia. Sin embargo, al igual que todos los virus, la replicación del AAV no puede ocurrir fuera de una célula huésped. Página 8 de 28
9 10.a) Vías de diseminación El AAV podría transmitirse por contacto directo o indirecto. El AAV podría transmitirse por inhalación, ingestión y, posiblemente, transmisión sexual. 10.b) Factores que afectan a la diseminación La replicación del virus solo es posible en células huésped que hayan sido coinfectadas por un virus auxiliar (p. ej., adenovirus o virus del herpes simple). 11. Modificaciones genéticas previas del organismo receptor o parental de las que ya se ha notificado la liberación en el país notificador (se darán los números de la notificación) El promotor, Bayer AG, no ha notificado modificaciones genéticas previas del virus parental (AAVhu37) en relación con su liberación en España. C. Información sobre la modificación genética 1. Tipo de modificación genética: i) Inserción de material genético ii) Eliminación de material genético iii) Sustitución de una base iv) Fusión celular v) Otro (especifíquese) Página 9 de 28
10 2. Resultado que se pretende obtener mediante la modificación genética El resultado pretendido de la modificación genética era generar un vector de AAV recombinante que contuviese un casete de expresión de FVIII humano para el tratamiento de pacientes con hemofilia A. BAY (DTX201) contiene un ADN que codifica la proteína del FVIII humano. La expresión está inducida por un elemento potenciador específico del hígado y un promotor específico del hígado encapsulado en un vector de AAVhu37 sin capacidad de replicación. El estudio de toxicidad/biodistribución conforme a la BPL confirma el tropismo esperado del vector AAVhu37 por el hígado. Así pues, cabe esperar que la administración de BAY (DTX201) dé lugar a la expresión del gen de hfviii en el hígado de los sujetos del ensayo. 3.a) Se ha usado un vector en el proceso de modificación? Sí En caso negativo, pase a la pregunta 5. No 3.b) En caso afirmativo, está presente el vector, total o parcialmente, en el organismo modificado? Sí En caso negativo, pase a la pregunta 5 No Página 10 de 28
11 4. Si ha contestado afirmativamente a la pregunta 3 b), aporte la información siguiente a) Tipo de vector plásmido bacteriófago virus cósmido Elemento de transposición Otros (especifíquense): b) Identidad del vector: pdtx.hfviiico SQ.201 c) Gama de organismos huéspedes del vector: Bacterias, células de mamífero d) Presencia en el vector de secuencias que den un fenotipo seleccionable o identificable Sí No Resistencia a los antibióticos Otras, (especifíquense) Indique qué gen de resistencia a los antibióticos se inserta: Kanamicina, puromicina e) Fragmentos constituyentes del vector El casete de expresión consta de un promotor y un potenciador específicos del hígado, un transgén de hfviii flanqueado por repeticiones terminales invertidas (RTI) de AAV. Únicamente el casete de expresión de hfviii está presente en el OMG final. Además, el vector contiene un origen bacteriano de replicación, el gen de la resistencia a kanamicina para permitir la propagación del plásmido en E. coli, y los genes de rep y cap de AAV para la amplificación y acondicionamiento del ADN del vector. f) Método de introducción del vector en el organismo receptor i) transformación ii) electroporación Página 11 de 28
12 iii) macroinyección iv) microinyección v) infección vi) otros, (especifíquense) Transfección de la estirpe celular estable productora con plásmido de expresión e infección por el adenovirus natural para inducir la producción de partículas de AAV recombinantes. 5. Si las repuestas a C. 3) a) y b) son negativas, qué método se siguió en el proceso de modificación? i) transformación ii) microinyección iii) macroencapsulación iv) macroinyección v) otros, (especifíquense) 6. Información sobre el fragmento de inserción: a) Composición del fragmento de inserción: El fragmento de inserción consta de un promotor y un potenciador específicos del hígado, un transgén de hfviii y una señal de poliadenilación, flanqueada por repeticiones terminales invertidas (RTI) de AAV. b) Fuente de cada parte constitutiva del fragmento de inserción: Gen del factor VIII humano: homo sapiens Señal de poliadenilación: homo sapiens Promotor/potenciador específico del hígado: murino/ homo sapiens RTI: AAV Página 12 de 28
13 c) Función prevista de cada parte constitutiva del fragmento de inserción en el OMG Promotor y potenciador específicos del hígado: Incorporados con la intención de estimular una expresión del gen del hfviii específica del hígado y de alto nivel. Gen del hfviii: Cabe esperar que la transferencia del gen del hfviii resulte eficaz para tratar la hemofilia A, dado que dicha enfermedad está causada por mutaciones en este gen que afectan a la expresión o actividad de la proteína del factor VIII. Señal de poliadenilación: Incorporada con la intención de proporcionar secuencias cis para una poliadenilación eficiente del ARNm del hfviii. Este elemento actúa a modo de señal para un fenómeno de escisión específico en el extremo 3 del transcrito incipiente y la adición de una cola larga de poliadenilo. RTI: Necesarias para la replicación y el acondicionamiento del genoma del vector en presencia de rep y cap. d) Localización del fragmento de inserción en el organismo receptor: - en un plásmido libre - integrado en el cromosoma - Otros especifíquense): Genoma de virus ADN monocatenario e) Contiene el fragmento de inserción partes cuyo producto o función no se conozcan? Sí No En caso afirmativo, especifíquese: D. Información sobre el organismo u organismos de los que se deriva el fragmento de inserción (donante) 1. Indíquese si es: Viroide Virus ARN Virus ADN Bacteria Hongo Animal Página 13 de 28
14 - mamíferos - insectos - peces - otro animal (especifique el phylum y la clase): Otros (especifíquense) 2. Nombre completo i) Orden y taxón superior (animales): Primates ii) Familia (plantas): No procede iii) Género: homo iv) Especie: sapiens v) Subespecie: No procede vi) Cepa: No procede vii) Cultivar/línea de reproducción: No procede viii) Patovar: No procede ix) Nombre vulgar: Ser humano 3. Es el organismo vivo o muerto (incluidos sus productos extracelulares), apreciablemente patógeno o nocivo de cualquier otra forma? Sí No No se sabe En caso afirmativo, especifíquese (a) para cuál de los organismos siguientes? humanos animales plantas otros (b) están implicadas de alguna forma las secuencias donadas en las propiedades patógenas o nocivas del organismo? Sí No No se sabe Página 14 de 28
15 En caso afirmativo, proporcione la información pertinente de conformidad con la letra d) del punto 11 de la letra A de la sección II del Anexo III A: No procede 4. Está clasificado el organismo donante con arreglo a normas comunitarias vigentes en relación con la protección de la salud humana y el medio ambiente como, por ejemplo, la Directiva 90/679/ CEE sobre la protección de los trabajadores contra los riesgos relacionados con la exposición a agentes biológicos durante el trabajo? Sí En caso afirmativo, especifíquese: No 5. Intercambian los organismos donante y receptor material genético de forma natural? Sí No No se sabe E. Información sobre el organismo modificado genéticamente 1. Rasgos genéticos y características fenotípicas del organismo receptor o parental que hayan sufrido algún cambio como resultado de la modificación genética a) Se diferencia el OMG del receptor en lo que a capacidad de supervivencia se refiere? Sí No No se sabe Especifíquese b) Se diferencia en algo el OMG del receptor en lo que respecta al modo o índice de reproducción? Sí No No se sabe Especifíquese: El genoma viral de BAY (DTX201) se ha modificado significativamente en comparación con el virus parental para que carezca de capacidad de replicación. Los genes rep y cap del AAV se han sustituido por un casete de expresión eucariótico y únicamente se han mantenido las secuencias RTI virales, que son secuencias de ADN no codificadoras (< 300 pb). Por tanto, BAY (DTX201) no contiene genes virales naturales. El AAV natural requiere la presencia de un virus auxiliar, como adenovirus humano o virus del herpes simple, para replicarse. La replicación de BAY (DTX201) requeriría la presencia del AAV natural además de la de un virus auxiliar. La probabilidad de que esto ocurra es extremadamente baja. Página 15 de 28
16 c) Se diferencia en algo el OMG del receptor en lo que respecta a la diseminación? Sí No No se sabe Especifíquese: Como la replicación de BAY (DTX201) solo podría tener lugar en el caso extraordinariamente improbable de que una célula huésped resultara infectada por tres virus distintos (BAY (DTX201), AAV natural y un virus auxiliar, como adenovirus humano o virus del herpes simple), la probabilidad de diseminación es menor que la del AAV natural. d) Se diferencia en algo el OMG del receptor en lo que respecta a la patogenicidad? Sí No No se sabe Especifíquese: No se conocen efectos patógenos del AAV natural en seres humanos. No cabe esperar que la introducción del casete de expresión de hfviii favorezca la aparición de patogenicidad. Por tanto, ni el AAV natural ni BAY (DTX201) son patógenos ni se espera que lo sean. 2. Estabilidad genética del organismo modificado genéticamente AAV es un virus ADN monocatenario que tiene gran estabilidad genética; basándose en ello, también se espera que BAY (DTX201) sea genéticamente estable. La integridad del casete de expresión de hfviii se confirmará mediante secuenciación directa. 3. Es el OMG, vivo o muerto (incluidos sus productos extracelulares), apreciablemente patógeno o nocivo de cualquier forma? En caso afirmativo: Sí No No se sabe a) Para cuál de los organismos siguientes? humanos animales plantas otros b) Aporte la información pertinente especificada en la letra d) del punto 11 de la letra A de la sección II y en el inciso i) del punto 2 de la letra C de la sección II del anexo III A 4. Descripción de los métodos de identificación y detección a) Técnicas utilizadas para detectar el OMG en el medio ambiente: Página 16 de 28
17 BAY (DTX201) puede detectarse mediante reacción en cadena de la polimerasa cuantitativa (qpcr). b) Técnicas utilizadas para identificar el OMG: BAY (DTX201) se puede identificar mediante qpcr. F. Información sobre la liberación 1. Finalidad de la liberación (incluido todo beneficio ambiental potencial significativo esperado) La finalidad de la liberación es llevar a cabo el ensayo clínico (EudraCT ), un ensayo de fase I/II, abierto, de seguridad y de búsqueda de dosis de BAY (DTX201), una transferencia génica del factor VIII humano con el dominio B eliminado -mediada por el virus adenoasociado (VAA) del serotipo hu37- en adultos con hemofilia A grave. 2. Es diferente el lugar de liberación del hábitat natural o del ecosistema en el que se utiliza, se mantiene o se encuentra regularmente el organismo receptor o parental? Sí No En caso afirmativo, especifíquese: El hábitat natural del AAV serotipo hu37 natural son células huésped de primates. BAY (DTX201) se administrará a seres humanos en el contexto del ensayo clínico Información relativa a la liberación y a la zona circundante a) Localización geográfica (región administrativa y coordenadas de referencia cuando proceda): Centro 1: Complejo Hospitalario Regional de Málaga Avenida de Carlos Haya, s/n Málaga Centro 2: Hospital Universitario Central de Asturias Avenida Roma, s/n Oviedo Asturias Centro 3: Hospital de la Santa Creu I Sant Pau C/ Mas Casanovas, Barcelona Página 17 de 28
18 Centro 4: Hospital Universitari Vall d Hebrón Pg. Vall d'hebron, Barcelona Centro 5: Hospital Universitario La Paz Paseo de la Castellana, Madrid Centro 6: Hospital Universitari I Politècnic La Fe Avenida de Fernando Abril Martorell, Valencia b) Área del lugar (m 2 ): (i) lugar real de la liberación (m 2 ): No procede. No puede definirse un tamaño específico del lugar de liberación porque BAY (DTX201) se administrará a pacientes como parte de un ensayo clínico. (ii) área de liberación más amplia (m 2 ) No procede. No puede definirse un tamaño específico del lugar de liberación porque BAY (DTX201) se administrará a pacientes como parte de un ensayo clínico. c) Proximidad a biotipos reconocidos internacionalmente o zonas protegidas (incluidos depósitos de agua potable) que pudieran verse afectados: No procede. BAY (DTX201) se administrará en una única infusión intravenosa en un entorno hospitalario. Por tanto, no cabe prever que entre en contacto con biotipos reconocidos ni zonas protegidas. d) Flora y fauna, incluidos cultivos, ganado y especies migratorias que pueden potencialmente interactuar con el OMG: La administración de BAY (DTX201) tendrá lugar únicamente en un entorno hospitalario controlado; por consiguiente, no cabe prever que entre en contacto con flora, fauna ni cultivos. 4. Método y amplitud de la liberación a) Cantidad de OMG que vaya a liberarse: La dosis se basará en el peso corporal del paciente. Dependiendo de la cohorte de dosis, se calcula que podrá administrarse una cantidad total aproximada de 4 x ,6 x CG de BAY (DTX201) a cada paciente de España (cálculo basado en la suposición de un peso corporal de 80 kg en un paciente varón medio). b) Duración de la operación: La duración del ensayo en cada sujeto se define como el tiempo transcurrido entre la fecha de obtención del consentimiento informado por escrito firmado y la visita de la semana 52. Página 18 de 28
19 (c) Métodos y procedimientos para evitar o reducir al mínimo la propagación de los OMG más allá del lugar de liberación: BAY (DTX201) será conservado, preparado y administrado por profesionales médicos cualificados, en un entorno hospitalario y únicamente a pacientes que cumplan los criterios de inclusión en el ensayo clínico Una vez finalizado el recuento de la medicación del ensayo, los viales tendrán que descontaminarse conforme a la práctica del centro. Los viales usados y sin usar de BAY (DTX201) se conservarán en el centro del ensayo hasta que el monitor de investigación clínica (CRA) proceda al recuento de la medicación del ensayo. Todos los viales no utilizados tendrán que conservarse en las condiciones de conservación exigidas ( -60 C); los viales usados/parcialmente usados se podrán conservar a temperatura ambiente. Los viales no utilizados y utilizados/parcialmente utilizados se podrán desechar en el centro siguiendo las normas locales solo después de que el CRA realice el recuento y dé su aprobación. BAY (DTX201) es un producto en investigación (PEI) fabricado y distribuido por una persona cualificada (PC) ubicada en un Estado miembro de la Unión Europea, para uso en ensayos clínicos, tras haber cumplido las especificaciones definidas en cuanto a calidad y seguridad del producto para administración a seres humanos de acuerdo con el protocolo del ensayo clínico. Además, se utilizará conforme al protocolo del ensayo clínico aprobado por las autoridades sanitarias y comités de ética del país en el que vaya a realizarse el ensayo. Por este motivo, la cadena de suministro del PEI y su gestión en el centro están reguladas en el contexto de las normativas sobre ensayos clínicos, las leyes locales y las directrices aplicables en cuanto a recepción, conservación, manipulación, dispensación, contabilidad y destrucción del PEI. En el Manual de Farmacia del ensayo y el material de formación facilitado a los centros se proporcionan instrucciones sobre el uso, conservación y destrucción del PEI al personal de farmacia y clínico. También incluirán instrucciones para documentar el control del PEI desde el momento de su recepción en el centro del ensayo hasta la contabilidad final y su destrucción. Además, se describen los procesos necesarios para gestionar y documentar las desviaciones, como las desviaciones de la temperatura, y se transfiere, al personal cualificado del centro en el envío de medicamentos, las reclamaciones técnicas notificadas para el producto. Los riesgos relacionados con la liberación al medio ambiente del OMG y los riesgos para el personal, en caso de que se produzca una alteración de la integridad del envase y/o la conservación o un vertido accidental en el centro o durante el transporte o conservación, se consideran insignificantes. El OMG será manipulado exclusivamente por el personal cualificado designado y, en caso de que se produzca un derrame, el producto no es patógeno y carece de capacidad de replicación, lo que limita la dispersión y los riesgos para el ambiente o el personal. Los vectores de AAV recombinantes carecen de capacidad de replicación y no cabe esperar que supongan un riesgo de transmisión. Sin embargo, a fin de evitar una posible exposición de las parejas sexuales, los pacientes que participen en el ensayo clínico tendrán que utilizar métodos anticonceptivos de barrera desde el momento de la administración del fármaco del ensayo hasta la visita de seguimiento 12 semanas después de dicha administración. Las muestras de semen se obtendrán como se detalla en el protocolo clínico, y se exigirá a los pacientes que usen métodos anticonceptivos de doble barrera hasta que se lo indiquen los investigadores principales. Página 19 de 28
20 Las terapias génicas basadas en virus pueden obtenerse a partir de virus o bacterias infecciosos. Aunque los AAVr no son infecciosos, son eliminados por las personas mediante diseminación. Para reducir al mínimo el riesgo de exposición al virus diseminado, los pacientes recibirán BAY (DTX201) mediante una única infusión IV en un entorno ambulatorio y solo serán dados de alta al menos 8 horas después de la administración de BAY (DTX201), lo que limita la probabilidad de exposición de familiares. Se obtendrán muestras de heces, saliva, orina, plasma y semen con los intervalos de tiempo especificados, hasta la desaparición del virus, y los pacientes tendrán que utilizar métodos anticonceptivos de doble barrera desde el momento de la administración del fármaco del ensayo hasta que se lo indiquen los investigadores. 5. Descripción resumida de las condiciones ambientales medias (clima, temperatura, etc.) No procede. La administración de BAY (DTX201) se realizará exclusivamente en un entorno hospitalario controlado. 6. Datos pertinentes sobre liberaciones anteriores del mismo OMG, si los hubiera, específicamente relacionados a las repercusiones potenciales de la liberación en el medio ambiente y la salud humana BAY (DTX201) no se ha liberado al ambiente con anterioridad. G. Interacciones del OMG con el medio ambiente y repercusiones potenciales sobre este, si es apreciablemente diferente del organismo receptor o parental 1. Nombre del organismo objeto de investigación (si procede) i) Orden y taxón superior (animales): Primates ii) Familia (plantas): No procede iii) Género: Homo iv) Especie: sapiens v) Subespecies: No procede vi) Cepa: No procede vii) Cultivar/Línea de reproducción: No procede viii) Patovar: No procede Página 20 de 28
21 ix) Nombre vulgar: Ser humano 2. Mecanismo previsto y resultado de la interacción entre los OMG liberados y el organismo diana (si procede) BAY (DTX201) codifica el gen del factor VIII humano cuya expresión se ve estimulada por un potenciador y un promotor específicos del hígado encapsidados en un vector de AAVhu37. El estudio de toxicidad/biodistribución conforme a la BPL confirma el tropismo esperado del vector AAVhu37 por el hígado. Así pues, cabe esperar que la administración de BAY (DTX201) dé lugar a la expresión del gen de hfviii en el hígado de los sujetos del ensayo. Cabe esperar que la transferencia del gen del hfviii resulte eficaz para tratar la hemofilia A, dado que dicha enfermedad está causada por mutaciones en este gen que afectan a la expresión o actividad de la proteína del factor VIII. 3. Otras interacciones potencialmente significativas con otros organismos en el medio ambiente No se expondrá a personas distintas de los sujetos tratados con el medicamento a concentraciones de BAY (DTX201) que puedan representar un posible riesgo. Los posibles riesgos de exposición a BAY (DTX201) están basados en la administración sistémica de BAY (DTX201). Una exposición mínima, como la exposición ambiental, de personas distintas de los sujetos que reciban BAY (DTX201) como parte del ensayo no sería una dosis suficiente para representar una expresión génica significativa ni posibles riesgos de seguridad para los seres humanos. Dado que BAY (DTX201) también carece de capacidad de replicación, cabe esperar una eliminación rápida del vector de cualquier organismo no diana sin causar ningún efecto perjudicial. Además, la expresión del transgén se ha diseñado para que tenga lugar exclusivamente en los hepatocitos. Aparte de los posibles huéspedes humanos, no cabe esperar que la exposición a BAY (DTX201) afecte a organismos no diana, ya sea de manera directa o indirecta. 4. Es probable que se dé una selección posterior a la liberación del OMG como, por ejemplo, una competencia mayor, un carácter más invasivo, etc.? Sí No No se sabe Especifíquese: Dado que BAY (DTX201) es incapaz de replicarse, no puede producirse selección posterior a la liberación. 5. Tipos de ecosistemas a los que puede extenderse el OMG desde el lugar de liberación y en los cuales puede quedar establecido Página 21 de 28
22 Dado que BAY (DTX201) es incapaz de replicarse, no cabe esperar que se disemine al ambiente en un grado significativo ni que se establezca en ningún ecosistema. 6. Nombre completo de los organismos que no son el organismo diana, pero que (teniendo en cuenta la naturaleza del medio ambiente receptor) pueden sufrir accidentalmente daños importantes por la liberación del OMG No procede i) Orden y taxón superior (animales): No procede ii) Familia (plantas): No procede iii) Género: No procede iv) Especie: No procede v) Subespecie: No procede vi) Cepa: No procede vii) Cultivar/línea de reproducción: No procede viii) Patovar: No procede ix) Nombre vulgar: No procede 7. Probabilidad de intercambio genético en vivo a) Del OMG a otros organismos del ecosistema de liberación: Cabe esperar que el genoma viral de BAY (DTX201) se transfiera a los hepatocitos presentes en el hígado de los pacientes incluidos en el ensayo Cabe prever que la inmensa mayoría de los genomas de vector BAY (DTX201) presentes en el interior de las células de los sujetos sean episómicos, en lugar de quedar integrados en el ADN de las células huésped. Dado que BAY (DTX201) carece de capacidad de replicación, y únicamente cabe prever que se disemine a los fluidos corporales de los sujetos del ensayo en un grado limitado, se considera improbable la transmisión y transferencia génica a organismos distintos de los sujetos del ensayo. b) De otros organismos al OMG: La eliminación del 94% del ADN viral disminuye la probabilidad de recombinación homóloga con virus relacionados que podría dar lugar a variantes del OMG. Página 22 de 28
23 c) Consecuencias probables de la transferencia de genes: Aunque la recombinación entre BAY (DTX201) y un AAV natural para generar un genoma de vector híbrido que contenga el casete de expresión de hfviii y los genes rep y cap de AAV sigue siendo una posibilidad teórica, una molécula de este tipo, aunque se generara en una célula, no podría replicarse a menos que también hubiera presencia de un adenovirus o virus herpes auxiliar. Por otro lado, este genoma híbrido sería demasiado grande para acondicionar el ADN híbrido en una partícula de AAV. Se sabe que el AAV posee un límite de acondicionamiento de unas 5 kb (Wu 2010) y sería previsible que una molécula híbrida que contuviera los genes rep-cap más el casete de expresión de hfviii superara este límite. Por tal motivo, los riesgos asociados a la transferencia génica de AAV natural a BAY (DTX201) se consideran insignificantes. 8. Referencias de los resultados pertinentes (si los hay) de estudios sobre el comportamiento y las características del OMG sobre su repercusión ecológica llevados a cabo en ambientes naturales simulados (por ejemplo, microcosmos, etc.) No se han realizado estudios de este tipo con BAY (DTX201). 9. Posibles interacciones ambientalmente significativas con procesos biogeoquímicos (si son diferentes del organismo receptor o parental) No se conoce ni cabe prever que BAY (DTX201) pueda influir en procesos biogeoquímicos. H. Información sobre el seguimiento 1. Métodos de seguimiento de los OMG La diseminación del virus se vigilará estrechamente en el ensayo Otros métodos para vigilar los efectos de BAY (DTX201) consisten en evaluaciones de la seguridad y la eficacia. 2. Métodos de seguimiento de las repercusiones en el ecosistema La presencia de BAY (DTX201) en fluidos corporales tras la administración de BAY (DTX201) se determinará mediante reacción en cadena de la polimerasa cuantitativa (qpcr). 3. Métodos de detección de la transferencia del material genético donado del OMG a otros organismos Página 23 de 28
24 La transferencia del casete de expresión del factor VIII a los sujetos del ensayo se detectará evaluando la actividad del factor VIII, para lo cual se utilizarán interpretaciones clínicas adecuadas. 4. Tamaño del área de seguimiento (m2) No procede; únicamente se utilizarán técnicas de vigilancia en relación con la diseminación del virus a fluidos corporales de los pacientes. 5. Duración del seguimiento La diseminación del virus se evaluará hasta que se obtengan resultados negativos o por debajo del límite de cuantificación en al menos tres ocasiones consecutivas. Se realizarán evaluaciones de la seguridad y eficacia durante todo el ensayo según se describe en el protocolo del ensayo. 6. Frecuencia del seguimiento La diseminación del virus se evaluará hasta que se obtengan resultados negativos o por debajo del límite de cuantificación en al menos tres ocasiones consecutivas. Se realizarán evaluaciones de la seguridad y eficacia durante todo el ensayo según se describe en el protocolo del ensayo. I. Información sobre el tratamiento posliberación y el tratamiento de residuos 1. Tratamiento del lugar tras la liberación Todas las superficies contaminadas con BAY (DTX201) se desinfectarán de acuerdo con las normas locales y los procedimientos del centro relacionados con el tratamiento de sustancias biológicas peligrosas y utilizando un desinfectante eficaz contra AAV (p. ej., hipoclorito sódico al 1%, glutaraldehído al 2% o dodecilsulfato sódico al 0,25%). 2. Tratamiento del OMG tras la liberación Todos los materiales desechables que entren en contacto con BAY (DTX201) deberán desecharse de acuerdo con las prácticas y normas de cada centro en materia de eliminación y descontaminación de residuos biológicos peligrosos. En general, los materiales desechables se desecharán en recipientes para objetos punzantes o bolsas para materiales biológicos peligrosos y se descontaminarán mediante autoclave, incineración o ambos. El material no desechable se descontaminará de acuerdo con las prácticas y procedimientos del centro, por ejemplo, mediante tratamiento con un desinfectante adecuado y/o con autoclave. Los viales usados y sin usar de BAY (DTX201) se conservarán en el centro del ensayo hasta que el CRA proceda al recuento de la medicación del ensayo. Todos los viales no utilizados tendrán que conservarse en las condiciones Página 24 de 28
25 de conservación exigidas ( -60 C); los viales usados/parcialmente usados se podrán conservar a temperatura ambiente. Los viales no utilizados y utilizados/parcialmente utilizados se podrán desechar en el centro siguiendo las normas locales sólo después de que el CRA realice el recuento y de su aprobación. 3(a) Tipo y cantidad de residuos producidos Se prevén los siguientes tipos de residuos: Viales de vidrio que contengan BAY (DTX201). El número de viales de BAY (DTX201) necesarios por paciente dependerá de la cohorte de dosis y del peso corporal del paciente. Materiales utilizados en la preparación y administración del fármaco del ensayo, por ejemplo, bolsa de solución salina, equipo de administración IV, jeringas y agujas. Equipo de protección personal, por ejemplo, guantes. 3(b) Tratamiento de residuos Todos los materiales desechables que entren en contacto con BAY (DTX201) deberán desecharse de acuerdo con las prácticas y normas de cada centro. Por ejemplo, estos materiales se desecharán en recipientes para objetos punzantes o bolsas para materiales biológicos peligrosos y se descontaminarán mediante autoclave, incineración o ambos. Los residuos líquidos se descontaminarán y desecharán según las prácticas del centro. J. Información sobre planes de actuación en caso de emergencia 1. Métodos y procedimientos de control de la diseminación del OMG o de los OMG en caso de dispersión imprevista En caso de que se libere accidentalmente el contenido de un vial/viales de BAY (DTX201) o del producto para infusión diluido y que entre en contacto con materiales de transporte o superficies de la farmacia u hospital, el vertido deberá descontaminarse y eliminarse de acuerdo con a las prácticas del centro. Los desinfectantes eficaces contra el AAV son hipoclorito sódico al 1%, glutaraldehído al 2% y dodecilsulfato sódico al 0,25%. BAY (DTX201) se conserva en viales de vidrio. Se advertirá al personal de que tenga precaución al manipular los viales y de que reduzca al mínimo el uso de agujas. En caso de lesión, el personal seguirá los procedimientos de cada centro. En caso de contacto accidental de BAY (DTX201) con la piel, los ojos o la ropa, la zona afectada se lavará con una cantidad abundante de agua y el personal seguirá los procedimientos del centro para la gestión de material biológico peligroso. Página 25 de 28
26 2. Métodos de eliminación del OMG o de los OMG de las áreas potencialmente afectadas Toda superficie expuesta al OMG se desinfectará con un desinfectante adecuado de acuerdo con las leyes locales y las políticas y procedimientos del centro. Los desinfectantes eficaces contra el AAV son hipoclorito sódico al 1%, glutaraldehído al 2% y dodecilsulfato sódico al 0,25%. Página 26 de 28
27 3. Métodos de eliminación o saneamiento de plantas, animales, suelos, etc. que pudieran ser expuestos al organismo durante la dispersión o después de la misma La administración de BAY (DTX201) tendrá lugar únicamente en un entorno hospitalario controlado; por consiguiente, no cabe prever que entre en contacto con flora, fauna ni cultivos. Además, BAY (DTX201) no es capaz de infectar a plantas ni microbios. 4. Planes de protección de la salud humana y del medio ambiente en caso de que se produzca un efecto no deseable El personal respetará la legislación local y los procedimientos del centro en materia de manipulación y eliminación de organismos modificados genéticamente. Además, se facilitan recomendaciones de seguridad y orientación sobre el tratamiento de los incidentes relacionados con BAY (DTX201) en las instrucciones de seguridad para los investigadores y el personal incluidas en esta presentación. Se vigilará estrechamente a todos los pacientes para detectar reacciones adversas durante el ensayo. Un comité de vigilancia de los datos (CVD) independiente se encargará de vigilar los datos de seguridad de este ensayo. El CVD podrá recomendar, en cualquier momento, que se modifique o interrumpa el ensayo prematuramente por problemas de seguridad basándose en los análisis de los datos. Página 27 de 28
28 Bibliografía Directiva 2001/18/CE del Parlamento Europeo y del Consejo Europeo sobre la liberación deliberada en el ambiente de organismos modificados genéticamente. Directiva del Consejo Europeo 90/679/CEE de 26 de noviembre de 1990 sobre la protección de los trabajadores frente a los riesgos relacionados con la exposición a agentes biológicos en el trabajo. Nathwani AC, Rosales C, McIntosh J, et al. Long-term safety and efficacy following systemic administration of a self-complementary AAV vector encoding human FIX pseudotyped with serotype 5 and 8 capsid proteins. Mol Ther. 2011;19(5): Nathwani AC, Tuddenham EG, Ranqarajan S, et al. Adenovirus-associated virus vector mediated gene transfer in hemophilia B. N Engl J Med. 2012;365(25): Nathwani ACV, Reiss UM, Tuddenham EG, et al. Long-term safety and efficacy of factor IX gene therapy in hemophilia B. N Engl J Med. 2014;371(21) Wu Z, Yang H, Colosi P. Effect of genome size on AAV vector packaging. Mol Ther Jan;18(1):80-6. Página 28 de 28
PRIMERA PARTE. Nombre de la institución o empresa: Laboratorios SYVA, S.A. León (España).
 PRIMERA PARTE MODELO DE RESUMEN DE LA LIBERACIÓN DE ORGANISMOS MODIFICADOS GENÉTICAMENTE DISTINTOS DE LAS PLANTAS SUPERIORES DE ACUERDO CON EL ARTÍCULO 11 DE LA DIRECTIVA 2001/18/CE A. Información de carácter
PRIMERA PARTE MODELO DE RESUMEN DE LA LIBERACIÓN DE ORGANISMOS MODIFICADOS GENÉTICAMENTE DISTINTOS DE LAS PLANTAS SUPERIORES DE ACUERDO CON EL ARTÍCULO 11 DE LA DIRECTIVA 2001/18/CE A. Información de carácter
Nombre de la institución o empresa: Digna Biotech SL Avda. Pio XII, 22 - Oficina Pamplona (Navarra) Viroide Virus ADN
 MODELO DE RESUMEN DE LA NOTIFICACIÓN DE LA LIBERACIÓN DE ORGANISMOS MODIFICADOS GENÉTICAMENTE DISTINTOS DE LAS PLANTAS SUPERIORES DE ACUERDO CON EL ARTÍCULO 11 DE LA DIRECTIVA 2001/18/CE A. Información
MODELO DE RESUMEN DE LA NOTIFICACIÓN DE LA LIBERACIÓN DE ORGANISMOS MODIFICADOS GENÉTICAMENTE DISTINTOS DE LAS PLANTAS SUPERIORES DE ACUERDO CON EL ARTÍCULO 11 DE LA DIRECTIVA 2001/18/CE A. Información
Evento de Transformación 56c
 MODELO DE RESUMEN DE LA NOTIFICACIÓN DE LA LIBERACIÓN DE PLANTAS SUPERIORES MODIFICADAS GENÉTICAMENTE (ANGIOSPERMAS Y GYMNOSPERMAS) Modelo establecido por la Decisión 2002/813/CE del Consejo, de 3 de octubre
MODELO DE RESUMEN DE LA NOTIFICACIÓN DE LA LIBERACIÓN DE PLANTAS SUPERIORES MODIFICADAS GENÉTICAMENTE (ANGIOSPERMAS Y GYMNOSPERMAS) Modelo establecido por la Decisión 2002/813/CE del Consejo, de 3 de octubre
AAV9-CAG-coh-SGSH Modelo resumen
 MODELO DE RESUMEN DE LA NOTIFICACIÓN DE LA LIBERACIÓN DE ORGANISMOS MODIFICADOS GENÉTICAMENTE DISTINTOS DE LAS PLANTAS SUPERIORES DE ACUERDO CON EL ARTÍCULO 11 DE LA DIRECTIVA 2001/18/CE Laboratorios del
MODELO DE RESUMEN DE LA NOTIFICACIÓN DE LA LIBERACIÓN DE ORGANISMOS MODIFICADOS GENÉTICAMENTE DISTINTOS DE LAS PLANTAS SUPERIORES DE ACUERDO CON EL ARTÍCULO 11 DE LA DIRECTIVA 2001/18/CE Laboratorios del
Nombre de la institución o empresa: Novartis Farmacéutica SA
 MODELO DE RESUMEN DE LA NOTIFICACIÓN DE LA LIBERACIÓN DE ORGANISMOS MODIFICADOS GENÉTICAMENTE DISTINTOS DE LAS PLANTAS SUPERIORES DE ACUERDO CON EL ARTÍCULO 11 DE LA DIRECTIVA 2001/18/CE A. Información
MODELO DE RESUMEN DE LA NOTIFICACIÓN DE LA LIBERACIÓN DE ORGANISMOS MODIFICADOS GENÉTICAMENTE DISTINTOS DE LAS PLANTAS SUPERIORES DE ACUERDO CON EL ARTÍCULO 11 DE LA DIRECTIVA 2001/18/CE A. Información
LA NUEVA BIOTECNOLOGÍA
 LA NUEVA BIOTECNOLOGÍA Ingeniería genética: técnicas que permiten manipular la información genética de un ser vivo. TECNOLOGÍA TRADICIONAL DEL ADN RECOMBINANTE CLONACIÓN DE GENES: Obtención de muchas copias
LA NUEVA BIOTECNOLOGÍA Ingeniería genética: técnicas que permiten manipular la información genética de un ser vivo. TECNOLOGÍA TRADICIONAL DEL ADN RECOMBINANTE CLONACIÓN DE GENES: Obtención de muchas copias
A. Información de carácter general: 1. Detalles de la notificación
 MODELO DE RESUMEN DE LA NOTIFICACIÓN DE LA LIBERACIÓN DE ORGANISMOS MODIFICADOS GENÉTICAMENTE DISTINTOS DE LAS PLANTAS SUPERIORES DE ACUERDO CON EL ARTÍCULO 11 DE LA DIRECTIVA 2001/18/CE A. Información
MODELO DE RESUMEN DE LA NOTIFICACIÓN DE LA LIBERACIÓN DE ORGANISMOS MODIFICADOS GENÉTICAMENTE DISTINTOS DE LAS PLANTAS SUPERIORES DE ACUERDO CON EL ARTÍCULO 11 DE LA DIRECTIVA 2001/18/CE A. Información
PARTE 1 (DECISIÓN DEL CONSEJO 2002/813/CE)
 PARTE 1 (DECISIÓN DEL CONSEJO 2002/813/CE) MODELO DE RESUMEN DE LA LIBERACIÓN DE ORGANISMOS MODIFICADOS GENÉTICAMENTE DISTINTOS DE LAS PLANTAS SUPERIORES DE ACUERDO CON EL ARTÍCULO 11 DE LA DIRECTIVA 2001/18/CE
PARTE 1 (DECISIÓN DEL CONSEJO 2002/813/CE) MODELO DE RESUMEN DE LA LIBERACIÓN DE ORGANISMOS MODIFICADOS GENÉTICAMENTE DISTINTOS DE LAS PLANTAS SUPERIORES DE ACUERDO CON EL ARTÍCULO 11 DE LA DIRECTIVA 2001/18/CE
EVALUACIÓN DEL RIESGO ASOCIADO A LA RESISTENCIA A LOS ANTIMICROBIANOS COMO CONSECUENCIA DEL USO DE ANTIMICROBIANOS
 CAPÍTULO 6.10. EVALUACIÓN DEL RIESGO ASOCIADO A LA RESISTENCIA A LOS ANTIMICROBIANOS COMO CONSECUENCIA DEL USO DE ANTIMICROBIANOS Artículo 6.10.1. Recomendaciones para analizar los riesgos que entrañan
CAPÍTULO 6.10. EVALUACIÓN DEL RIESGO ASOCIADO A LA RESISTENCIA A LOS ANTIMICROBIANOS COMO CONSECUENCIA DEL USO DE ANTIMICROBIANOS Artículo 6.10.1. Recomendaciones para analizar los riesgos que entrañan
LIBERACIÓN VOLUNTARIA DE ORGANISMOS MODIFICADOS GENÉTICAMENTE CON FINES DISTINTOS A SU COMERCIALIZACIÓN
 LIBERACIÓN VOLUNTARIA DE ORGANISMOS MODIFICADOS GENÉTICAMENTE CON FINES DISTINTOS A SU COMERCIALIZACIÓN SOLICITUD DE AUTORIZACIÓN (1) Nº DE EXPEDIENTE REGISTRO PRESENTACIÓN EN LA ADMINISTRACIÓN REGISTRO
LIBERACIÓN VOLUNTARIA DE ORGANISMOS MODIFICADOS GENÉTICAMENTE CON FINES DISTINTOS A SU COMERCIALIZACIÓN SOLICITUD DE AUTORIZACIÓN (1) Nº DE EXPEDIENTE REGISTRO PRESENTACIÓN EN LA ADMINISTRACIÓN REGISTRO
Genética microbiana. Sergio Abate, Vet., Mag. Dr. Profesor Adjunto Microbiología Universidad Nacional de Rio Negro - Sede Atlántica
 Sergio Abate, Vet., Mag. Dr. Profesor Adjunto Microbiología Universidad Nacional de Rio Negro - Sede Atlántica Por que razón los microorganismos han sido los principales modelos para el estudio de la genética?
Sergio Abate, Vet., Mag. Dr. Profesor Adjunto Microbiología Universidad Nacional de Rio Negro - Sede Atlántica Por que razón los microorganismos han sido los principales modelos para el estudio de la genética?
Vectormune FP-LT Liofilizado para suspensión inyectable para pollos
 Fecha: 16 de septiembre de 2013 Referencia Nº: VCTE FP-LT SNIF 201309 ES Número de páginas: 26 Vectormune FP-LT Liofilizado para suspensión inyectable para pollos RESUMEN DE LA NOTIFICACIÓN DE LA LIBERACIÓN
Fecha: 16 de septiembre de 2013 Referencia Nº: VCTE FP-LT SNIF 201309 ES Número de páginas: 26 Vectormune FP-LT Liofilizado para suspensión inyectable para pollos RESUMEN DE LA NOTIFICACIÓN DE LA LIBERACIÓN
a) Estado miembro de la notificación: España b) Número de la notificación: B/ES/15/13 c) Fecha del acuse de recibo de la 16-Oct-2015
 MODELO DE RESUMEN DE LA NOTIFICACIÓN DE LA LIBERACIÓN DE ORGANISMOS MODIFICADOS GENÉTICAMENTE DISTINTOS DE LAS PLANTAS SUPERIORES DE ACUERDO CON EL ARTÍCULO 11 DE LA DIRECTIVA 2001/18/CE A. Información
MODELO DE RESUMEN DE LA NOTIFICACIÓN DE LA LIBERACIÓN DE ORGANISMOS MODIFICADOS GENÉTICAMENTE DISTINTOS DE LAS PLANTAS SUPERIORES DE ACUERDO CON EL ARTÍCULO 11 DE LA DIRECTIVA 2001/18/CE A. Información
A. Información de carácter general: 1. Detalles de la notificación
 MODELO DE RESUMEN DE LA NOTIFICACIÓN DE LA LIBERACIÓN DE ORGANISMOS MODIFICADOS GENÉTICAMENTE DISTINTOS DE LAS PLANTAS SUPERIORES DE ACUERDO CON EL ARTÍCULO 11 DE LA DIRECTIVA 2001/18/CE A. Información
MODELO DE RESUMEN DE LA NOTIFICACIÓN DE LA LIBERACIÓN DE ORGANISMOS MODIFICADOS GENÉTICAMENTE DISTINTOS DE LAS PLANTAS SUPERIORES DE ACUERDO CON EL ARTÍCULO 11 DE LA DIRECTIVA 2001/18/CE A. Información
Clonación. Producción de un gran número de copias de una región de ADN (fragmentos o
 CLONACIÓN Clonación Producción de un gran número de copias de una región de ADN (fragmentos o genes) o de ADNc Clonación Celular Acelular Célula anfitriona PCR Secuenciación Estudio de estructura de ácido
CLONACIÓN Clonación Producción de un gran número de copias de una región de ADN (fragmentos o genes) o de ADNc Clonación Celular Acelular Célula anfitriona PCR Secuenciación Estudio de estructura de ácido
UNIDAD V GENETICA BACTERIANA. Microbiología Prof. Glamil Acevedo
 UNIDAD V GENETICA BACTERIANA Microbiología Prof. Glamil Acevedo CROMOSOMA BACTERIANO Cromosomas son las estructuras físicas de las células donde se sitúa y almacena la in formación transmitida por herencia
UNIDAD V GENETICA BACTERIANA Microbiología Prof. Glamil Acevedo CROMOSOMA BACTERIANO Cromosomas son las estructuras físicas de las células donde se sitúa y almacena la in formación transmitida por herencia
PARTE 1 (DECISIÓN DEL CONSEJO 2002/813/CE)
 PARTE 1 (DECISIÓN DEL CONSEJO 2002/813/CE) MODELO DE RESUMEN DE LA LIBERACIÓN DE ORGANISMOS MODIFICADOS GENÉTICAMENTE DISTINTOS DE LAS PLANTAS SUPERIORES DE ACUERDO CON EL ARTÍCULO 11 DE LA DIRECTIVA 2001/18/CE
PARTE 1 (DECISIÓN DEL CONSEJO 2002/813/CE) MODELO DE RESUMEN DE LA LIBERACIÓN DE ORGANISMOS MODIFICADOS GENÉTICAMENTE DISTINTOS DE LAS PLANTAS SUPERIORES DE ACUERDO CON EL ARTÍCULO 11 DE LA DIRECTIVA 2001/18/CE
REQUISITOS PARA EL REGISTRO DE BIOFERTILIZANTES
 REQUISITOS PARA EL REGISTRO DE BIOFERTILIZANTES 1.-PLANILLA DE SOLICITUD DE REGISTRO DE PRODUCTO 2.-PLANILLA DE DEPÓSITO BANCARIO 3.-CARTA DE SOLICITUD DE REGISTRO DEL PRODUCTO 4.-CERTIFICADOS: - CERTIFICADO
REQUISITOS PARA EL REGISTRO DE BIOFERTILIZANTES 1.-PLANILLA DE SOLICITUD DE REGISTRO DE PRODUCTO 2.-PLANILLA DE DEPÓSITO BANCARIO 3.-CARTA DE SOLICITUD DE REGISTRO DEL PRODUCTO 4.-CERTIFICADOS: - CERTIFICADO
AGENTES BIOLÓGICOS Antonio Lobato Gutiérrez
 AGENTES BIOLÓGICOS Antonio Lobato Gutiérrez Introducción Contaminantes biológicos Son organismos con un determinado ciclo de vida que al penetrar en el hombre, determinan en él un efecto adverso para su
AGENTES BIOLÓGICOS Antonio Lobato Gutiérrez Introducción Contaminantes biológicos Son organismos con un determinado ciclo de vida que al penetrar en el hombre, determinan en él un efecto adverso para su
FORMATO DE INFORMACIÓN DEL RESUMEN DE LA NOTIFICACIÓN (SNIF) PARA LA LIBERACIÓN DE PLANTAS SUPERIORES MODIFICADAS GENÉTICAMENTE (PSMG)
 FORMATO DE INFORMACIÓN DEL RESUMEN DE LA NOTIFICACIÓN (SNIF) PARA LA LIBERACIÓN DE PLANTAS SUPERIORES MODIFICADAS GENÉTICAMENTE (PSMG) REMOLACHA H7-1 (7 DE SEPTIEMBRE DE 2009) A. INFORMACIÓN GENERAL 1.
FORMATO DE INFORMACIÓN DEL RESUMEN DE LA NOTIFICACIÓN (SNIF) PARA LA LIBERACIÓN DE PLANTAS SUPERIORES MODIFICADAS GENÉTICAMENTE (PSMG) REMOLACHA H7-1 (7 DE SEPTIEMBRE DE 2009) A. INFORMACIÓN GENERAL 1.
VARIABILIDAD Y HERENCIA DE LAS CARACTERISTICAS
 GENÉTICA BACTERIANA VARIABILIDAD Y HERENCIA DE LAS CARACTERISTICAS Células como maquinarias químicas y dispositivos codificadores (almacenan, procesan y utilizan los genes) Gen Unidad funcional de información
GENÉTICA BACTERIANA VARIABILIDAD Y HERENCIA DE LAS CARACTERISTICAS Células como maquinarias químicas y dispositivos codificadores (almacenan, procesan y utilizan los genes) Gen Unidad funcional de información
RESUMEN DE LA NOTIFICACION DE LA LIBERACION DE PLANTAS SUPERIORES MODIFICADAS GENETICAMENTE (Angiospermas y Gimnospermas)
 RESUMEN DE LA NOTIFICACION DE LA LIBERACION DE PLANTAS SUPERIORES MODIFICADAS GENETICAMENTE (Angiospermas y Gimnospermas) A. INFORMACIÓN DE CARÁCTER GENERAL 1- Detalles de la notificación (a) Número de
RESUMEN DE LA NOTIFICACION DE LA LIBERACION DE PLANTAS SUPERIORES MODIFICADAS GENETICAMENTE (Angiospermas y Gimnospermas) A. INFORMACIÓN DE CARÁCTER GENERAL 1- Detalles de la notificación (a) Número de
BIOQUIMICA Y GENETICA MOLECULAR APLICADA A LA VETERINARIA
 BIOQUIMICA Y GENETICA MOLECULAR APLICADA A LA VETERINARIA PROFESORADO CURSO 1994-1995: Dr. J. Ariño (Unidad de Bioquímica) Dra. F. Bosch (Unidad de Bioquímica) Dr. A. Sánchez (Unidad de Genética y Mejora)
BIOQUIMICA Y GENETICA MOLECULAR APLICADA A LA VETERINARIA PROFESORADO CURSO 1994-1995: Dr. J. Ariño (Unidad de Bioquímica) Dra. F. Bosch (Unidad de Bioquímica) Dr. A. Sánchez (Unidad de Genética y Mejora)
Genética microbiana. Sergio Abate, Vet., Mag. Dr. Profesor Adjunto Microbiología Universidad Nacional de Rio Negro - Sede Atlántica
 Sergio Abate, Vet., Mag. Dr. Profesor Adjunto Microbiología Universidad Nacional de Rio Negro - Sede Atlántica Por que razón los microorganismos han sido los principales modelos para el estudio de la genética?
Sergio Abate, Vet., Mag. Dr. Profesor Adjunto Microbiología Universidad Nacional de Rio Negro - Sede Atlántica Por que razón los microorganismos han sido los principales modelos para el estudio de la genética?
Estructura y función del genoma bacteriano
 GENETICA BACTERIANA Estructura y función del genoma bacteriano! El material genético de las bacterias se encuentra en el citoplasma, se le denomina como nucleoide, cuerpo nuclear, región nuclear.! Esta
GENETICA BACTERIANA Estructura y función del genoma bacteriano! El material genético de las bacterias se encuentra en el citoplasma, se le denomina como nucleoide, cuerpo nuclear, región nuclear.! Esta
COMISIÓN FEDERAL PARA LA PROTECCIÓN CONTRA RIESGOS SANITARIOS
 COMISIÓN FEDERAL PARA LA PROTECCIÓN CONTRA RIESGOS SANITARIOS MANUAL DE PROTOCOLOS RESUMIDOS DE FABRICACION PROTOCOLO RESUMIDO DE FABRICACIÓN PARA VACUNA HEPATITIS B 1. CONTROL FINAL Nombre Internacional
COMISIÓN FEDERAL PARA LA PROTECCIÓN CONTRA RIESGOS SANITARIOS MANUAL DE PROTOCOLOS RESUMIDOS DE FABRICACION PROTOCOLO RESUMIDO DE FABRICACIÓN PARA VACUNA HEPATITIS B 1. CONTROL FINAL Nombre Internacional
NOTIFICACIÓN B/ES/10/18
 RESUMEN DE LA NOTIFICACION DE LA LIBERACION DE PLANTAS SUPERIORES MODIFICADAS GENETICAMENTE (ANGIOSPERMAS Y GIMNOSPERMAS) RESUMEN DE LA NOTIFICACIÓN DE LA LIBERACIÓN EXPERIMENTAL AL MEDIO AMBIENTE DEL
RESUMEN DE LA NOTIFICACION DE LA LIBERACION DE PLANTAS SUPERIORES MODIFICADAS GENETICAMENTE (ANGIOSPERMAS Y GIMNOSPERMAS) RESUMEN DE LA NOTIFICACIÓN DE LA LIBERACIÓN EXPERIMENTAL AL MEDIO AMBIENTE DEL
EVALUACIÓN DE RIESGO DE LA LIBERACIÓN AL MEDIO AMBIENTE DE UN ADENOVIRUS MODIFICADO GENÉTICAMENTE (Notificación B/ES/13/05)
 MINISTERIO DE AGRICULTURA, ALIMENTACIÓN Y MEDIO AMBIENTE DIRECCION GENERAL DE CALIDAD Y EVALUACION AMBIENTAL Y MEDIO AMBIENTE COMISIÓN NACIONAL DE BIOSEGURIDAD EVALUACIÓN DE RIESGO DE LA LIBERACIÓN AL
MINISTERIO DE AGRICULTURA, ALIMENTACIÓN Y MEDIO AMBIENTE DIRECCION GENERAL DE CALIDAD Y EVALUACION AMBIENTAL Y MEDIO AMBIENTE COMISIÓN NACIONAL DE BIOSEGURIDAD EVALUACIÓN DE RIESGO DE LA LIBERACIÓN AL
EVALUACIÓN DE RIESGO DE LA LIBERACIÓN AL MEDIO AMBIENTE DE UN VECTOR DE TERAPIA GÉNICA MODIFICADO GENÉTICAMENTE (Notificación B/ES/12/35)
 MINISTERIO DE AGRICULTURA, ALIMENTACIÓN Y MEDIO AMBIENTE DIRECCION GENERAL DE CALIDAD Y EVALUACION AMBIENTAL Y MEDIO NATURAL COMISIÓN NACIONAL DE BIOSEGURIDAD EVALUACIÓN DE RIESGO DE LA LIBERACIÓN AL MEDIO
MINISTERIO DE AGRICULTURA, ALIMENTACIÓN Y MEDIO AMBIENTE DIRECCION GENERAL DE CALIDAD Y EVALUACION AMBIENTAL Y MEDIO NATURAL COMISIÓN NACIONAL DE BIOSEGURIDAD EVALUACIÓN DE RIESGO DE LA LIBERACIÓN AL MEDIO
Comité de Ética de Experimentación Animal del Hospital Clínico San Carlos (CEEA)
 Comité de Ética de Experimentación Animal del Hospital Clínico San Carlos (CEEA) SOLICITUD DE INFORME DE AUTORIZACIÓN DE PROCEDIMIENTO EXPERIMENTAL DE ORGANISMOS GENETICAMENTE MODIFICADOS AL COMITÉ DE
Comité de Ética de Experimentación Animal del Hospital Clínico San Carlos (CEEA) SOLICITUD DE INFORME DE AUTORIZACIÓN DE PROCEDIMIENTO EXPERIMENTAL DE ORGANISMOS GENETICAMENTE MODIFICADOS AL COMITÉ DE
Resistencia de Microorganismos a Agentes Antimicrobianos. Mecanismos de Transmisión de Resistencia. Orígenes de la resistencia
 Resistencia de Microorganismos a Agentes Antimicrobianos Mecanismos de Transmisión de Resistencia Orígenes de la resistencia Por definición un antibiótico es un metabolito producido por una bacteria o
Resistencia de Microorganismos a Agentes Antimicrobianos Mecanismos de Transmisión de Resistencia Orígenes de la resistencia Por definición un antibiótico es un metabolito producido por una bacteria o
Sanidad - Enfermedades Virales Los virus son parásitos intracelulares obligados
 Sanidad - Enfermedades Virales Los virus son parásitos intracelulares obligados Están formados por un núcleo o genoma de ADN o ARN, una cápside proteica que los recubre (nucleocápside) y algunos poseen
Sanidad - Enfermedades Virales Los virus son parásitos intracelulares obligados Están formados por un núcleo o genoma de ADN o ARN, una cápside proteica que los recubre (nucleocápside) y algunos poseen
Julio 2008 LOS TRANSGENICOS EN LA AGRICULTURA
 Julio 2008 LOS TRANSGENICOS EN LA AGRICULTURA EL ROL DE LA BIOTECNOLOGIA MODERNA EN EL DESARROLLO DE TRANSGENICOS Gen LA BIOTECNOLOGIA MODERNA Se entiende como tal a la aplicación de técnicas in vitro
Julio 2008 LOS TRANSGENICOS EN LA AGRICULTURA EL ROL DE LA BIOTECNOLOGIA MODERNA EN EL DESARROLLO DE TRANSGENICOS Gen LA BIOTECNOLOGIA MODERNA Se entiende como tal a la aplicación de técnicas in vitro
Plan de formación 2015
 Plan de formación 2015 Jornada técnica Actualización de la guía técnica para la evaluación y prevención de los riesgos relacionados con la exposición a agentes biológicos Ponencia Biogaval Ponente Andrea
Plan de formación 2015 Jornada técnica Actualización de la guía técnica para la evaluación y prevención de los riesgos relacionados con la exposición a agentes biológicos Ponencia Biogaval Ponente Andrea
REGULACIÓN DE LA EXPRESIÓN GÉNICA EN PROCARIOTAS ANÁLISIS DE LA EXPRESIÓN DE LACZ
 REGULACIÓN DE LA EXPRESIÓN GÉNICA EN PROCARIOTAS ANÁLISIS DE LA EXPRESIÓN DE LACZ Para conocer la organización del ADN se desarrollaron métodos que permitieron conocer la secuencia exacta de nucleótidos,
REGULACIÓN DE LA EXPRESIÓN GÉNICA EN PROCARIOTAS ANÁLISIS DE LA EXPRESIÓN DE LACZ Para conocer la organización del ADN se desarrollaron métodos que permitieron conocer la secuencia exacta de nucleótidos,
FICHA TECNICA DE PRODUCTO
 FICHA TECNICA DE PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO KARITIL ORAL Reg. SAGARPA: Q-0265-003 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada 1000 ml contiene: Tilmicosina (fosfato)... 250
FICHA TECNICA DE PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO KARITIL ORAL Reg. SAGARPA: Q-0265-003 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada 1000 ml contiene: Tilmicosina (fosfato)... 250
PROCEDIMIENTO PARA LA DECLARACIÓN DE SUBPRODUCTO SEGÚN LA LEY 22/2011, DE RESIDUOS y SUELOS CONTAMINADOS
 PROCEDIMIENTO PARA LA DECLARACIÓN DE SUBPRODUCTO SEGÚN LA LEY 22/2011, DE RESIDUOS y SUELOS CONTAMINADOS Barcelona, 26 de mayo de 2015 Margarita Ruiz Saiz-Aja Subdirectora General Adjunta de Residuos MAGRAMA
PROCEDIMIENTO PARA LA DECLARACIÓN DE SUBPRODUCTO SEGÚN LA LEY 22/2011, DE RESIDUOS y SUELOS CONTAMINADOS Barcelona, 26 de mayo de 2015 Margarita Ruiz Saiz-Aja Subdirectora General Adjunta de Residuos MAGRAMA
2. ESTRATEGIA PARA EFECTUAR LA CLONACION Y EXPRESION DEL GEN
 1. CONTROL FINAL Nombre Internacional y nombre de la vacuna Nombre del propietario Nombre y dirección del fabricante Número de Lote Fecha de fabricación Fecha de caducidad Temperatura de almacenamiento
1. CONTROL FINAL Nombre Internacional y nombre de la vacuna Nombre del propietario Nombre y dirección del fabricante Número de Lote Fecha de fabricación Fecha de caducidad Temperatura de almacenamiento
Frecuencia de mutaciones espontáneas en un gen típico de 1000 pb: 10-6 y 10-9 por generación ó 10-6 y 10-9 Kpb durante un sólo ciclo de replicación.
 MUTACIÓN: modificación heredable en la secuencias de bases de un genoma (pequeños cambios en la célula) Frecuencia de mutaciones espontáneas en un gen típico de 1000 pb: 10-6 y 10-9 por generación ó 10-6
MUTACIÓN: modificación heredable en la secuencias de bases de un genoma (pequeños cambios en la célula) Frecuencia de mutaciones espontáneas en un gen típico de 1000 pb: 10-6 y 10-9 por generación ó 10-6
FICHA TÉCNICA Sepiolita 15-30
 FICHA TÉCNICA CARACTERÍSTICAS DEL ABSORBENTE: Análisis mineralógico (DRX): - Sepiolita 75% (Mín 65%) Densidad (BS 1460): 0.64 g/cc (Máx 0.71 g/cc) ph: 8.5 ± 1.0 Absorción Westinghouse: - Agua 130% (Mín
FICHA TÉCNICA CARACTERÍSTICAS DEL ABSORBENTE: Análisis mineralógico (DRX): - Sepiolita 75% (Mín 65%) Densidad (BS 1460): 0.64 g/cc (Máx 0.71 g/cc) ph: 8.5 ± 1.0 Absorción Westinghouse: - Agua 130% (Mín
Brucella melitensis, viva atenuada, cepa Rev-1 (fase lisa) x 10 9 ufc* *ufc: Unidades formadoras de colonias
 DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO CZV Rev-1 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada dosis (1 ml) de
DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO CZV Rev-1 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada dosis (1 ml) de
Thais Salazar C O LE G I O C HAM PAG N AT
 Thais Salazar COLEGIO CHAMPAGNAT ALGUNOS DE SUS PRODUCTOS Fabricación de Insulina Elaboración del factor de coagulación Procedimiento utilizado Se usa un plásmido cuya función es introducir el gen de la
Thais Salazar COLEGIO CHAMPAGNAT ALGUNOS DE SUS PRODUCTOS Fabricación de Insulina Elaboración del factor de coagulación Procedimiento utilizado Se usa un plásmido cuya función es introducir el gen de la
FICHA TÉCNICA Sepiolita 15 30
 FICHA TÉCNICA Sepiolita 15 30 CARACTERÍSTICAS DEL ABSORBENTE: Análisis mineralógico (DRX): Sepiolita 75% (Mín 65%) Densidad (BS 1460): 0,64 g/cc (Máx 0,71 g/cc) PH: 8.5 + 1.0 Absorción Westinghouse: Agua
FICHA TÉCNICA Sepiolita 15 30 CARACTERÍSTICAS DEL ABSORBENTE: Análisis mineralógico (DRX): Sepiolita 75% (Mín 65%) Densidad (BS 1460): 0,64 g/cc (Máx 0,71 g/cc) PH: 8.5 + 1.0 Absorción Westinghouse: Agua
. Absorbente para carreteras homologado por Le Ministére de l Équipement des Transports et du Logement, con número de autorización ABS.2002.
 SEPIOLITA 15-30 CALCINADA CARACTERÍSTICAS Edición nº 1 Aplicación. Absorbente para carreteras homologado por Le Ministére de l Équipement des Transports et du Logement, con número de autorización ABS.2002.17.
SEPIOLITA 15-30 CALCINADA CARACTERÍSTICAS Edición nº 1 Aplicación. Absorbente para carreteras homologado por Le Ministére de l Équipement des Transports et du Logement, con número de autorización ABS.2002.17.
Expresión de proteínas recombinantes en plantas mediante el uso de vectores virales
 Expresión de proteínas recombinantes en plantas mediante el uso de vectores virales Apellidos, nombre Departamento Centro Carmelo López del Rincón 1 (clopez@upvnet.upv.es) María Ferriol Molina 2 (mafermo@upvnet.upv.es)
Expresión de proteínas recombinantes en plantas mediante el uso de vectores virales Apellidos, nombre Departamento Centro Carmelo López del Rincón 1 (clopez@upvnet.upv.es) María Ferriol Molina 2 (mafermo@upvnet.upv.es)
CONSEJO DE LA UNIÓN EUROPEA. Bruselas, 13 de enero de 2012 (16.01) (OR. en) 5313/12 TRANS 9
 CONSEJO DE LA UNIÓN EUROPEA Bruselas, 13 de enero de 2012 (16.01) (OR. en) 5313/12 TRANS 9 NOTA DE TRANSMISIÓN Emisor: Comisión Europea Fecha de recepción: 9 de enero de 2012 Destinatario: Secretaría General
CONSEJO DE LA UNIÓN EUROPEA Bruselas, 13 de enero de 2012 (16.01) (OR. en) 5313/12 TRANS 9 NOTA DE TRANSMISIÓN Emisor: Comisión Europea Fecha de recepción: 9 de enero de 2012 Destinatario: Secretaría General
Recombinación. El éxito de la transferencia horizontal de gene se basa en la habilidad de una bacteria de integrar el DNA del donador a su genoma.
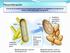 Recombinación El éxito de la transferencia horizontal de gene se basa en la habilidad de una bacteria de integrar el DNA del donador a su genoma. Recombinantes no estables Población de recombinantes estables
Recombinación El éxito de la transferencia horizontal de gene se basa en la habilidad de una bacteria de integrar el DNA del donador a su genoma. Recombinantes no estables Población de recombinantes estables
TEMA 4: ADN Y PROTEÍNAS. LA BIOTECNOLOGÍA
 TEMA 4: ADN Y PROTEÍNAS. LA BIOTECNOLOGÍA ADN e información genética Genes y control celular Mutaciones y su importancia biológica La biotecnología y sus aplicaciones La ingeniería genética Modificación
TEMA 4: ADN Y PROTEÍNAS. LA BIOTECNOLOGÍA ADN e información genética Genes y control celular Mutaciones y su importancia biológica La biotecnología y sus aplicaciones La ingeniería genética Modificación
Limagrain Ibérica S.A.
 MODELO PARA LA PRESENTACIÓN DE LOS RESULTADOS DE LOS ENSAYOS DE LIBERACIÓN INTENCIONAL EN EL MEDIO AMBIENTE DE PLANTAS SUPERIORES MODIFICADAS GENÉTICAMENTE CON ARREGLO AL ARTÍCULO 10 DE LA DIRECTIVA 2001/18/CE
MODELO PARA LA PRESENTACIÓN DE LOS RESULTADOS DE LOS ENSAYOS DE LIBERACIÓN INTENCIONAL EN EL MEDIO AMBIENTE DE PLANTAS SUPERIORES MODIFICADAS GENÉTICAMENTE CON ARREGLO AL ARTÍCULO 10 DE LA DIRECTIVA 2001/18/CE
Tratamiento del herpes genital inicial y recurrente, herpes labial y de infecciones mucocutáneas localizadas, producidas por virus de herpes simple
 1. NOMBRE DEL MEDICAMENTO ACICLOVIR DEXTER Crema E.F.G. 2. COMPOSICION CUALITATIVA Y CUANTITATIVA ACICLOVIR DEXTER Crema E.F.G. Cada gramo contiene: Aciclovir (DCI)... 50 mg Excipientes, c.s. 3. FORMA
1. NOMBRE DEL MEDICAMENTO ACICLOVIR DEXTER Crema E.F.G. 2. COMPOSICION CUALITATIVA Y CUANTITATIVA ACICLOVIR DEXTER Crema E.F.G. Cada gramo contiene: Aciclovir (DCI)... 50 mg Excipientes, c.s. 3. FORMA
EVALUACIÓN DE RIESGO DE LA LIBERACIÓN AL MEDIO AMBIENTE DE UNA VACUNA MODIFICADA GENÉTICAMENTE (Notificación B/ES/12/11)
 MINISTERIO DE MEDIO AMBIENTE, Y MEDIO RURAL Y MARINO DIRECCION GENERAL DE CALIDAD Y EVALUACION AMBIENTAL COMISIÓN NACIONAL DE BIOSEGURIDAD EVALUACIÓN DE RIESGO DE LA LIBERACIÓN AL MEDIO AMBIENTE DE UNA
MINISTERIO DE MEDIO AMBIENTE, Y MEDIO RURAL Y MARINO DIRECCION GENERAL DE CALIDAD Y EVALUACION AMBIENTAL COMISIÓN NACIONAL DE BIOSEGURIDAD EVALUACIÓN DE RIESGO DE LA LIBERACIÓN AL MEDIO AMBIENTE DE UNA
Universidad de Chile Facultad de Odontología Marzo de Genética Bacteriana. Prof. Carla Lozano M.
 Universidad de Chile Facultad de Odontología Marzo de 2011 Genética Bacteriana Prof. Carla Lozano M. Qué es la Genética? Disciplina científica que estudia la Herencia Gregor Mendel GENES Unidad básica,
Universidad de Chile Facultad de Odontología Marzo de 2011 Genética Bacteriana Prof. Carla Lozano M. Qué es la Genética? Disciplina científica que estudia la Herencia Gregor Mendel GENES Unidad básica,
Hipersensibilidad conocida a penciclovir, famciclovir o a los otros componentes de la formulación, por ejemplo propilenglicol.
 1. NOMBRE DEL MEDICAMENTO Penciclovir Beecham bomba dosificadora Penciclovir Beecham crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio activo: Penciclovir al 1% DCI: penciclovir 3. FORMA FARMACÉUTICA
1. NOMBRE DEL MEDICAMENTO Penciclovir Beecham bomba dosificadora Penciclovir Beecham crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio activo: Penciclovir al 1% DCI: penciclovir 3. FORMA FARMACÉUTICA
CUESTIONES SELECTIVIDAD: MICROBIOLOGÍA. 1) Qué es un virus?(0,5).describa el ciclo lítico de un bacteriófago. (JUNIO 2007)
 CUESTIONES SELECTIVIDAD: MICROBIOLOGÍA 1) Qué es un virus?(0,5).describa el ciclo lítico de un bacteriófago. (JUNIO 2007) ) Realice una clasificación de los cinco tipos principales de microorganismos indicando
CUESTIONES SELECTIVIDAD: MICROBIOLOGÍA 1) Qué es un virus?(0,5).describa el ciclo lítico de un bacteriófago. (JUNIO 2007) ) Realice una clasificación de los cinco tipos principales de microorganismos indicando
06. VIRUS, VIROIDES Y PRIONES
 06. VIRUS, VIROIDES Y PRIONES 1 6.1 Características generales de virus, viroides y priones. Agente Replicación Composición Química Imagen Virus En célula toma el control genético al insertar su ácido nucléico.
06. VIRUS, VIROIDES Y PRIONES 1 6.1 Características generales de virus, viroides y priones. Agente Replicación Composición Química Imagen Virus En célula toma el control genético al insertar su ácido nucléico.
Antibióticos ticos y cultivos transgénicos. nicos. Congreso Latinoamericana de Salud Socioambiental Rosario, Argentina. Abril 2011
 Antibióticos ticos y cultivos transgé Congreso Latinoamericana de Salud Socioambiental Rosario, Argentina Abril 2011 Dr. Medardo Avila Vazquez Red Universitaria de Ambiente y Salud/Médicos dicos de Pueblos
Antibióticos ticos y cultivos transgé Congreso Latinoamericana de Salud Socioambiental Rosario, Argentina Abril 2011 Dr. Medardo Avila Vazquez Red Universitaria de Ambiente y Salud/Médicos dicos de Pueblos
OFTALMOCAN IVEN COLIRIO EN SOLUCIÓN
 PROSPECTO TEXTO PROSPECTO 10 ml: C1- Fabricante: Laboratorios Maymó S.A. OFTALMOCAN IVEN COLIRIO EN SOLUCIÓN Cloranfenicol /ml +Fosfato sódico de prednisolona /ml + Lidocaína 5 mg/ml Colirio en solución.
PROSPECTO TEXTO PROSPECTO 10 ml: C1- Fabricante: Laboratorios Maymó S.A. OFTALMOCAN IVEN COLIRIO EN SOLUCIÓN Cloranfenicol /ml +Fosfato sódico de prednisolona /ml + Lidocaína 5 mg/ml Colirio en solución.
TALLER (Evaluación 20 de abril). C E R T A A P R I N C I P I O D E S E G R E G A C I O N I
 I. SOPA DE LETRAS TALLER (Evaluación 20 de abril). C E R T A A P R I N C I P I O D E S E G R E G A C I O N I A R D C Z F J Ñ V H I R A J V U B W L G B A C O R P I X P C D G N Z Q E H U L M F A F J A C
I. SOPA DE LETRAS TALLER (Evaluación 20 de abril). C E R T A A P R I N C I P I O D E S E G R E G A C I O N I A R D C Z F J Ñ V H I R A J V U B W L G B A C O R P I X P C D G N Z Q E H U L M F A F J A C
AUTOEVALUACIÓN CUESTIONARIO del SEMINARIO 12 Generalidades de virus, respuesta inmune antiviral e introducción a la patogénesis viral
 AUTOEVALUACIÓN CUESTIONARIO del SEMINARIO 12 Generalidades de virus, respuesta inmune antiviral e introducción a la patogénesis viral En todos los casos, señale la opción CORRECTA. Puede haber más de una
AUTOEVALUACIÓN CUESTIONARIO del SEMINARIO 12 Generalidades de virus, respuesta inmune antiviral e introducción a la patogénesis viral En todos los casos, señale la opción CORRECTA. Puede haber más de una
Para la revisión de los Proyectos, se requiere que el Investigador Responsable envíe:
 Estimada Comunidad Científica y Docente: Según la normativa actual, el desarrollo de cualquier proyecto (docencia y/ o investigación básica/aplicada) que incluya el uso de microorganismos patógenos, sustancias
Estimada Comunidad Científica y Docente: Según la normativa actual, el desarrollo de cualquier proyecto (docencia y/ o investigación básica/aplicada) que incluya el uso de microorganismos patógenos, sustancias
DNA RECOMBINANTE E INGENIERÍA GENÉTICA
 DNA RECOMBINANTE E INGENIERÍA GENÉTICA INGENIERÍA GENÉTICA M A N I P U L A C I Ó N D E L D N A D E L O S ORGANISMOS VIVOS 1) INVESTIGACIÓN BÁSICA (ESTUDIO DE LA ORGANIZACIÓN, EXPRESIÓN Y FUNCIÓN DE GENES
DNA RECOMBINANTE E INGENIERÍA GENÉTICA INGENIERÍA GENÉTICA M A N I P U L A C I Ó N D E L D N A D E L O S ORGANISMOS VIVOS 1) INVESTIGACIÓN BÁSICA (ESTUDIO DE LA ORGANIZACIÓN, EXPRESIÓN Y FUNCIÓN DE GENES
NOTIFICACIÓN B/ES/09/44
 SNIF B/ES/09/44 RESUMEN DE LA NOTIFICACION DE LA LIBERACION DE PLANTAS SUPERIORES MODIFICADAS GENETICAMENTE (ANGIOSPERMAS Y GIMNOSPERMAS) NOTIFICACIÓN DE LA LIBERACIÓN EXPERIMENTAL AL MEDIO AMBIENTE DE
SNIF B/ES/09/44 RESUMEN DE LA NOTIFICACION DE LA LIBERACION DE PLANTAS SUPERIORES MODIFICADAS GENETICAMENTE (ANGIOSPERMAS Y GIMNOSPERMAS) NOTIFICACIÓN DE LA LIBERACIÓN EXPERIMENTAL AL MEDIO AMBIENTE DE
El uso del análisis de riesgo en peces genéticamente modificados
 El uso del análisis de riesgo en peces genéticamente modificados Dr. Assad Heneidi Zeckua Departamento de Medicina Preventiva Facultad de Medicina Veterinaria y Zootecnia, UNAM Que son los organismos genéticamente
El uso del análisis de riesgo en peces genéticamente modificados Dr. Assad Heneidi Zeckua Departamento de Medicina Preventiva Facultad de Medicina Veterinaria y Zootecnia, UNAM Que son los organismos genéticamente
Ingeniería Genética en Eucariontes
 Universidad de Chile Facultad de Ciencias Químicas y Farmacéuticas Departamento de Bioquímica y Biología Molecular l Ingeniería Genética en Eucariontes Bibliografía : Recombinant DNA, Third Edition: Genes
Universidad de Chile Facultad de Ciencias Químicas y Farmacéuticas Departamento de Bioquímica y Biología Molecular l Ingeniería Genética en Eucariontes Bibliografía : Recombinant DNA, Third Edition: Genes
3. Aprendizajes esperados de esta actividad: Los alumnos y alumnas saben y entienden que:
 Guía del docente 1. Descripción curricular: Nivel: 4º medio. Subsector: Biología. Unidad temática: Microbios y sistema de defensas, microorganismos. Palabras claves: sistema inmune, bacterias, virus, protozoos,
Guía del docente 1. Descripción curricular: Nivel: 4º medio. Subsector: Biología. Unidad temática: Microbios y sistema de defensas, microorganismos. Palabras claves: sistema inmune, bacterias, virus, protozoos,
Ficha de Seguridad. MELACIDE SC 20 Página 1 de 5
 MELACIDE SC 20 Página 1 de 5 1: IDENTIFICACION DEL PREPARADO Y DE LA EMPRESA 1.1 Nombre del producto : MELACIDE SC 20 1.2 Uso del preparado : Aditivo antioxidante, antimelanósico, estabilizante del color
MELACIDE SC 20 Página 1 de 5 1: IDENTIFICACION DEL PREPARADO Y DE LA EMPRESA 1.1 Nombre del producto : MELACIDE SC 20 1.2 Uso del preparado : Aditivo antioxidante, antimelanósico, estabilizante del color
Bacteriófagos. Transducción
 Bacteriófagos. Transducción Virus: elemento genético que contiene ADN o ARN rodeado por una cápside proteica y que sólo se replica dentro de la célula huésped. Explotan la maquinaria metabólica de la célula.
Bacteriófagos. Transducción Virus: elemento genético que contiene ADN o ARN rodeado por una cápside proteica y que sólo se replica dentro de la célula huésped. Explotan la maquinaria metabólica de la célula.
INGENIERÍA GENÉTICA Apuntes de biología
 INGENIERÍA GENÉTICA Son técnicas para la manipulación del genoma; entre ellas, las principales: - Técnicas de ADN recombinante - Clonación de genes - Hibridación de ácidos nucleicos Técnica del ADN Recombinante:
INGENIERÍA GENÉTICA Son técnicas para la manipulación del genoma; entre ellas, las principales: - Técnicas de ADN recombinante - Clonación de genes - Hibridación de ácidos nucleicos Técnica del ADN Recombinante:
Modelo resumen EudraCT: Talimogene laherparepvec Página 1. Talimogene laherparepvec
 Talimogene laherparepvec Página 1 Talimogene laherparepvec MODELO DE RESUMEN DE LA NOTIFICACIÓN DE LA LIBERACIÓN DE ORGANISMOS MODIFICADOS GENÉTICAMENTE DISTINTOS DE LAS PLANTAS SUPERIORES DE ACUERDO CON
Talimogene laherparepvec Página 1 Talimogene laherparepvec MODELO DE RESUMEN DE LA NOTIFICACIÓN DE LA LIBERACIÓN DE ORGANISMOS MODIFICADOS GENÉTICAMENTE DISTINTOS DE LAS PLANTAS SUPERIORES DE ACUERDO CON
CONTAMINACIÓN CRUZADA DE MUESTRAS CONTROL POR PRODUCTO DE ENSAYO EN ESTUDIOS CON ANIMALES
 CONTAMINACIÓN CRUZADA DE MUESTRAS CONTROL POR PRODUCTO DE ENSAYO EN ESTUDIOS CON ANIMALES DOCUMENTO Nº 11 Octubre 2010 Este documento ha sido aprobado por el Comité Técnico de Inspección (CTI), integrado
CONTAMINACIÓN CRUZADA DE MUESTRAS CONTROL POR PRODUCTO DE ENSAYO EN ESTUDIOS CON ANIMALES DOCUMENTO Nº 11 Octubre 2010 Este documento ha sido aprobado por el Comité Técnico de Inspección (CTI), integrado
INFORMACIÓN VOLUNTARIA DE PRODUCTO basada en el formato de la hoja de seguridad para abrasivos flexibles
 Página 1 de 6 INFORMACIÓN VOLUNTARIA DE PRODUCTO basada en el formato de la hoja de seguridad para abrasivos flexibles 1. Identificación de la sustancia o la mezcla y de la sociedad o la empresa 1.1. Identificaciór
Página 1 de 6 INFORMACIÓN VOLUNTARIA DE PRODUCTO basada en el formato de la hoja de seguridad para abrasivos flexibles 1. Identificación de la sustancia o la mezcla y de la sociedad o la empresa 1.1. Identificaciór
SECCION 1. Producto e identificación de la compañía. Nombre del producto BIOSTAT WP. polvo mojable
 Standard: HTAG 2004 BIOSTAT WP HOJA DE SEGURIDAD Version : Pagina 1 de 5 Revisado: 2010-07-12 SECCION 1. Producto e identificación de la compañía Nombre del producto BIOSTAT WP Nombre químico Producido
Standard: HTAG 2004 BIOSTAT WP HOJA DE SEGURIDAD Version : Pagina 1 de 5 Revisado: 2010-07-12 SECCION 1. Producto e identificación de la compañía Nombre del producto BIOSTAT WP Nombre químico Producido
Limagrain Ibérica S.A.
 MODELO PARA LA PRESENTACIÓN DE LOS RESULTADOS DE LOS ENSAYOS DE LIBERACIÓN INTENCIONAL EN EL MEDIO AMBIENTE DE PLANTAS SUPERIORES MODIFICADAS GENÉTICAMENTE CON ARREGLO AL ARTÍCULO 10 DE LA DIRECTIVA 2001/18/CE
MODELO PARA LA PRESENTACIÓN DE LOS RESULTADOS DE LOS ENSAYOS DE LIBERACIÓN INTENCIONAL EN EL MEDIO AMBIENTE DE PLANTAS SUPERIORES MODIFICADAS GENÉTICAMENTE CON ARREGLO AL ARTÍCULO 10 DE LA DIRECTIVA 2001/18/CE
RESUMEN DE LA NOTIFICACION DE LA LIBERACION DE PLANTAS SUPERIORES MODIFICADAS GENETICAMENTE (Angiospermas y Gimnospermas)
 RESUMEN DE LA NOTIFICACION DE LA LIBERACION DE PLANTAS SUPERIORES MODIFICADAS GENETICAMENTE (Angiospermas y Gimnospermas) A. INFORMACIÓN DE CARÁCTER GENERAL 1- Detalles de la notificación (a) Número de
RESUMEN DE LA NOTIFICACION DE LA LIBERACION DE PLANTAS SUPERIORES MODIFICADAS GENETICAMENTE (Angiospermas y Gimnospermas) A. INFORMACIÓN DE CARÁCTER GENERAL 1- Detalles de la notificación (a) Número de
HOJA DE DATOS DE SEGURIDAD MicroINR
 Rev A-2011-10-ES HOJA DE DATOS DE SEGURIDAD MicroINR 1. IDENTIFICACION DEL PRODUCTOO / IDENTIFICACION DE LA EMPRESA Nombre del producto Referencia Proveedor Número de teléfono Teléfono de emergencia micro
Rev A-2011-10-ES HOJA DE DATOS DE SEGURIDAD MicroINR 1. IDENTIFICACION DEL PRODUCTOO / IDENTIFICACION DE LA EMPRESA Nombre del producto Referencia Proveedor Número de teléfono Teléfono de emergencia micro
Introduccion a la Virología Médica. Dra Guadalupe Carballal 2013
 Introduccion a la Virología Médica Dra Guadalupe Carballal 2013 Que es un virus? DEFINICIONES PATÓGENOS INERTES VIRUS ES UN VENENO (Latín) ES UN COMPLEJO MACROMOLECULAR INFORMACIONAL ES UN PROGRAMA VIROIDES
Introduccion a la Virología Médica Dra Guadalupe Carballal 2013 Que es un virus? DEFINICIONES PATÓGENOS INERTES VIRUS ES UN VENENO (Latín) ES UN COMPLEJO MACROMOLECULAR INFORMACIONAL ES UN PROGRAMA VIROIDES
NOTIFICACIÓN SOBRE OPERACIONES DE UTILIZACIÓN CONFINADA DE ORGANISMOS MODIFICADOS GENETICAMENTE
 MINISTERIO DE MEDIO AMBIENTE PARTE A Tipos 2, 3 y 4 SECRETARIA GENERAL DE MEDIO AMBIENTE DIRECCION GENERAL DE CALIDAD Y EVALUACION AMBIENTAL NOTIFICACIÓN SOBRE OPERACIONES DE UTILIZACIÓN CONFINADA DE ORGANISMOS
MINISTERIO DE MEDIO AMBIENTE PARTE A Tipos 2, 3 y 4 SECRETARIA GENERAL DE MEDIO AMBIENTE DIRECCION GENERAL DE CALIDAD Y EVALUACION AMBIENTAL NOTIFICACIÓN SOBRE OPERACIONES DE UTILIZACIÓN CONFINADA DE ORGANISMOS
DECISIÓN DE LA COMISIÓN
 22.4.2009 Diario Oficial de la Unión Europea L 102/7 II (Actos adoptados en aplicación de los Tratados CE/Euratom cuya publicación no es obligatoria) DECISIONES COMISIÓN DECISIÓN DE LA COMISIÓN de 20 de
22.4.2009 Diario Oficial de la Unión Europea L 102/7 II (Actos adoptados en aplicación de los Tratados CE/Euratom cuya publicación no es obligatoria) DECISIONES COMISIÓN DECISIÓN DE LA COMISIÓN de 20 de
SISTEMA DE PRECAUCIONES UNIVERSALES Este sistema fué establecido por el Centro de Control de Enfermedades (C.D.C) de Atlanta, en 1987, a través de un
 SISTEMA DE PRECAUCIONES UNIVERSALES Este sistema fué establecido por el Centro de Control de Enfermedades (C.D.C) de Atlanta, en 1987, a través de un grupo de expertos quienes desarrollaron guías para
SISTEMA DE PRECAUCIONES UNIVERSALES Este sistema fué establecido por el Centro de Control de Enfermedades (C.D.C) de Atlanta, en 1987, a través de un grupo de expertos quienes desarrollaron guías para
Ingeniería genética y biotecnología. Ing. MBtA Kevin Estévez Ramírez Departamento de Agroindustria UNAH-CUROC
 Ingeniería genética y biotecnología. Ing. Departamento de Agroindustria Los organismos involucrados. Virus: bacteriófagos, virus animales. Los organismos involucrados. Bacterias: Seres vivos más utilizados
Ingeniería genética y biotecnología. Ing. Departamento de Agroindustria Los organismos involucrados. Virus: bacteriófagos, virus animales. Los organismos involucrados. Bacterias: Seres vivos más utilizados
TEMA 2 LA INFORMACIÓN GENÉTICA COLEGIO LEONARDO DA VINCI BIOLOGÍA Y GEOLOGÍA 4º ESO CURSO 2014/15
 TEMA 2 LA INFORMACIÓN GENÉTICA COLEGIO LEONARDO DA VINCI BIOLOGÍA Y GEOLOGÍA 4º ESO CURSO 2014/15 OBJETIVOS DEL TEMA * Ácidos nucleicos. Composición. Estructura. Tipos. Funciones. * Procesos del dogma
TEMA 2 LA INFORMACIÓN GENÉTICA COLEGIO LEONARDO DA VINCI BIOLOGÍA Y GEOLOGÍA 4º ESO CURSO 2014/15 OBJETIVOS DEL TEMA * Ácidos nucleicos. Composición. Estructura. Tipos. Funciones. * Procesos del dogma
FICHA DE DATOS DE SEGURIDAD
 FICHA DE DATOS DE SEGURIDAD (Conforme a la directiva 93/112/CE). RECUBRIMIENTO IMPERMEABILIZANTE ChovATEC FECHA DE EDICIÓN: Página 1 de 5 PRODUCTOS: 1. IDENTIFICACIÓN DEL PRODUCTO RECUBRIMIENTOS IMPERMEABILIZANTES.
FICHA DE DATOS DE SEGURIDAD (Conforme a la directiva 93/112/CE). RECUBRIMIENTO IMPERMEABILIZANTE ChovATEC FECHA DE EDICIÓN: Página 1 de 5 PRODUCTOS: 1. IDENTIFICACIÓN DEL PRODUCTO RECUBRIMIENTOS IMPERMEABILIZANTES.
Hoja de datos de seguridad
 Hoja de datos de seguridad 1. Identificación de la sustancia o el preparado y de la sociedad o empresa Identificación de la sustancia o del preparado Nombre del producto o Nombre comercial: Sika Fiber
Hoja de datos de seguridad 1. Identificación de la sustancia o el preparado y de la sociedad o empresa Identificación de la sustancia o del preparado Nombre del producto o Nombre comercial: Sika Fiber
Plan de formación 2015
 Plan de formación 2015 Jornada técnica Actualización de la guía técnica para la evaluación y prevención de los riesgos relacionados con la exposición a agentes biológicos Ponencia Guía técnica para la
Plan de formación 2015 Jornada técnica Actualización de la guía técnica para la evaluación y prevención de los riesgos relacionados con la exposición a agentes biológicos Ponencia Guía técnica para la
PROTOCOLO MANEJO INFECCIONES NOSOCOMIALES
 ÍNDICE 1) Objeto. 2 2) Profesionales implicados. 2 3) Población diana. 2 4) Desarrollo. 2 5) Indicadores de evaluación. 6 6) Control de cambio de protocolo. 6 ELABORADO POR: REVISADO POR: APROBADO POR:
ÍNDICE 1) Objeto. 2 2) Profesionales implicados. 2 3) Población diana. 2 4) Desarrollo. 2 5) Indicadores de evaluación. 6 6) Control de cambio de protocolo. 6 ELABORADO POR: REVISADO POR: APROBADO POR:
Slide 1 / Cuáles son los organismos más simples que se ajustan a la definición de la vida?
 Slide 1 / 105 1 Cuáles son los organismos más simples que se ajustan a la definición de la vida? Slide 2 / 105 2 Identifica un tipo de células procariotas de la que dependen los seres humanos. Slide 3
Slide 1 / 105 1 Cuáles son los organismos más simples que se ajustan a la definición de la vida? Slide 2 / 105 2 Identifica un tipo de células procariotas de la que dependen los seres humanos. Slide 3
GENÉTICA Y BIOSEGURIDAD
 Mª Jesús Marcos Donostia, junio 2015 www.ehu.es/ceid INTRODUCCIÓN GENÉTICA Manipulación de muestras biológicas de origen humano o animal Generación y mantenimiento de líneas celulares. Modelo in vitro
Mª Jesús Marcos Donostia, junio 2015 www.ehu.es/ceid INTRODUCCIÓN GENÉTICA Manipulación de muestras biológicas de origen humano o animal Generación y mantenimiento de líneas celulares. Modelo in vitro
Nombre de la institución o empresa: Centro de Investigaciones Energéticas Medioambientales y Tecnológicas (CIEMAT)
 MODELO DE RESUMEN DE LA NOTIFICACIÓN DE LA LIBERACIÓN DE ORGANISMOS MODIFICADOS GENÉTICAMENTE DISTINTOS DE LAS PLANTAS SUPERIORES DE ACUERDO CON EL ARTÍCULO 11 DE LA DIRECTIVA 2001/18/CE A. Información
MODELO DE RESUMEN DE LA NOTIFICACIÓN DE LA LIBERACIÓN DE ORGANISMOS MODIFICADOS GENÉTICAMENTE DISTINTOS DE LAS PLANTAS SUPERIORES DE ACUERDO CON EL ARTÍCULO 11 DE LA DIRECTIVA 2001/18/CE A. Información
Técnicas del ADN recombinante Introducción
 Técnicas del ADN recombinante Introducción Estructura primaria del ADN Enzimas de restricción (ER) Son enzimas (endonucleasas) de origen bacteriano que reconocen y cortan secuencias específicas (4-8 pb)
Técnicas del ADN recombinante Introducción Estructura primaria del ADN Enzimas de restricción (ER) Son enzimas (endonucleasas) de origen bacteriano que reconocen y cortan secuencias específicas (4-8 pb)
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Mupirocina ISDIN 20 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene 20 mg de mupirocina. Para consultar
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Mupirocina ISDIN 20 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene 20 mg de mupirocina. Para consultar
Herramientas básicas de clonación molecular. Plasmidos como vectores de clonación. Métodos de transformación de bacteria
 Herramientas básicas de clonación molecular Estirpes de Escherichia coli para propagar el DNA Plasmidos como vectores de clonación Métodos de transformación de bacteria Bacteriófagos para clonación Estirpes
Herramientas básicas de clonación molecular Estirpes de Escherichia coli para propagar el DNA Plasmidos como vectores de clonación Métodos de transformación de bacteria Bacteriófagos para clonación Estirpes
ANEXO 2 GLOSARIO DE TÉRMINOS EN MATERIA DE BIOTECNOLOGÍA. representa el soporte químico de la herencia: Está presente en los cromosomas, así
 ANEXO 2 GLOSARIO DE TÉRMINOS EN MATERIA DE BIOTECNOLOGÍA ADN: Ácido desoxirribonucleico, molécula con una estructura en doble hélice y que representa el soporte químico de la herencia: Está presente en
ANEXO 2 GLOSARIO DE TÉRMINOS EN MATERIA DE BIOTECNOLOGÍA ADN: Ácido desoxirribonucleico, molécula con una estructura en doble hélice y que representa el soporte químico de la herencia: Está presente en
VIRUS. En la frontera de la vida
 VIRUS En la frontera de la vida Los virus Son los seres más simples y pequeños que se conocen. Básicamente son moléculas de ácido nucleico envueltas por una cubierta proteica. Son acelulares, (no tienen
VIRUS En la frontera de la vida Los virus Son los seres más simples y pequeños que se conocen. Básicamente son moléculas de ácido nucleico envueltas por una cubierta proteica. Son acelulares, (no tienen
DISTRIBUCIÓN HORARIA DE LA ASIGNATURA SEGÚN NORMATIVA
 GUÍA DOCENTE CURSO: 2017-18 DATOS BÁSICOS DE LA ASIGNATURA Asignatura: Ingeniería Genética Código de asignatura: 49152202 Plan: Grado en Biotecnología (Plan 2015) Año académico: 2017-18 Ciclo formativo:
GUÍA DOCENTE CURSO: 2017-18 DATOS BÁSICOS DE LA ASIGNATURA Asignatura: Ingeniería Genética Código de asignatura: 49152202 Plan: Grado en Biotecnología (Plan 2015) Año académico: 2017-18 Ciclo formativo:
TRANSFERENCIA DE MATERIAL GENÉTICO II: TRANSFORMACIÓN
 TRANSFERENCIA DE MATERIAL GENÉTICO II: TRANSFORMACIÓN Nucleína Johan F. Miescher (1868) aisló de núcleos de leucocitos una sustancia que contenía fósforo con una fracción ácida (DNA) y una básica (proteína)
TRANSFERENCIA DE MATERIAL GENÉTICO II: TRANSFORMACIÓN Nucleína Johan F. Miescher (1868) aisló de núcleos de leucocitos una sustancia que contenía fósforo con una fracción ácida (DNA) y una básica (proteína)
PREGUNTAS DE EXÁMENES DE SELECTIVIDAD DE BIOLOGÍA. Tema 7: Microbiología y biotecnología
 PREGUNTAS DE EXÁMENES DE SELECTIVIDAD DE BIOLOGÍA Tema 7: Microbiología y biotecnología 1.- Cite dos diferencias que distingan a los virus del resto de microorganismos [0,5]. Describa el ciclo lítico de
PREGUNTAS DE EXÁMENES DE SELECTIVIDAD DE BIOLOGÍA Tema 7: Microbiología y biotecnología 1.- Cite dos diferencias que distingan a los virus del resto de microorganismos [0,5]. Describa el ciclo lítico de
1.- IDENTIFICACION DE LA SUSTANCIA O PREPARADO Y DE LA EMPRESA. Identificación de la Sustancia o Preparado: VAMEL AUT
 1.- IDENTIFICACION DE LA SUSTANCIA O PREPARADO Y DE LA EMPRESA Identificación de la Sustancia o Preparado: VAMEL AUT Uso de la Sustancia o Preparado: Vajillas Automáticas universal Identificación de la
1.- IDENTIFICACION DE LA SUSTANCIA O PREPARADO Y DE LA EMPRESA Identificación de la Sustancia o Preparado: VAMEL AUT Uso de la Sustancia o Preparado: Vajillas Automáticas universal Identificación de la
Ficha de Seguridad. MELACIDE FRESH Página 1 de 5
 MELACIDE FRESH Página 1 de 5 1: IDENTIFICACION DEL PREPARADO Y DE LA EMPRESA 1.1 Nombre del producto : MELACIDE FRESH 1.2 Uso del preparado : Aditivo antioxidante-antimelanósico y estabilizante del color
MELACIDE FRESH Página 1 de 5 1: IDENTIFICACION DEL PREPARADO Y DE LA EMPRESA 1.1 Nombre del producto : MELACIDE FRESH 1.2 Uso del preparado : Aditivo antioxidante-antimelanósico y estabilizante del color
Investigación en genes
 Investigación en genes Conocer el genóma de los organismos Modificar la dotación génica natural Tecnología a del ADN recombinante Conocimientos básicos que posibilitaron el desarrollo de la Tecnología
Investigación en genes Conocer el genóma de los organismos Modificar la dotación génica natural Tecnología a del ADN recombinante Conocimientos básicos que posibilitaron el desarrollo de la Tecnología
