INTRODUCCIÓN DIDÁCTICA A LAS REACCIONES DE PRECIPITACIÓN Y A LAS DE FORMACIÓN DE COMPLEJOS
|
|
|
- Mariano Ramos Naranjo
- hace 5 años
- Vistas:
Transcripción
1 INTRODUCCIÓN DIDÁCTICA A LAS REACCIONES DE PRECIPITACIÓN Y A LAS DE FORMACIÓN DE COMPLEJOS AUTOR JAVIER RUIZ HIDALGO TEMÁTICA REACCIONES QUÍMICAS DE PRECIPITACIÓN Y FORMACIÓN DE COMPLEJOS ETAPA BACHILLERATO Resumen En el presente trabajo muestro una práctica para realizar con el alumnado de 2º de Bachillerato para introducirlos en las reacciones de precipitación así como en la formación de iones complejos. Esta práctica la podemos realizar en el laboratorio, pero por su simplicidad procedimental, así como por la utilización de sustancias fáciles de conseguir en una droguería, podemos también proponérsela para que la realicen en sus casas. Palabras clave Iones complejos, tetramíncobre (II), sulfato de cobre pentahidratado e ion cuprato. 1. INTRODUCCIÓN En el presente artículo, vamos a tratar de mostrarle al alumnado, que son los iones complejos, dado que este tema no está contenido dentro del temario de segundo de bachillerato en la materia de Química, es un complemento que podemos hacer a dicha materia que en principio podríamos incluir en el proyecto integrado de dicho curso. Los iones complejos son unos iones que sólo existen en disolución, que se caracterizan por tener un ion metálico central y alrededor de el se agrupan átomos o iones para dar lugar al ion complejo. Por otro lado, en este artículo también repasamos algunas reacciones de precipitación, y de disolución de precipitados, que igualmente no se estudian como tema independiente en el temario de Química de segundo de bachillerato, pero que tiene una relevancia analítica importante, por lo que considero que es un buen complemento al temario de dicha materia, y que igual que antes he indicado podemos tratarlo bien en el proyecto integrado de segundo de bachillerato.
2 2. PROPUESTA Se va a proponer que el alumnado realice una práctica de forma cualitativa, que podemos realizarla en el laboratorio del centro o incluso si trabajamos con materiales caseros, podemos indicarles que la pueden realizar en sus propias casas, dependiendo de la disponibilidad que del laboratorio tengamos, del tiempo, etc. Debemos tener en cuenta por tanto que los reactivos con los que vamos a trabajar deben ser fáciles de conseguir de forma cotidiana, y el material de laboratorio debe ser fácilmente intercambiable por material habitual de nuestras casas. 3. MATERIALES Para la realización de esta práctica, podemos emplear el siguiente material, si bien detallo como podemos trabajar en casa, y como podemos trabajar en el laboratorio. - 5 botes de cristal pequeños, o 5 vasos de precipitados pequeños. - Uno bote de cristal más grande o un vaso de precipitados más grande. - Una cucharilla o una varilla para agitar las disoluciones. - Una jeringa o una bureta 4. REACTIVOS Para la realización de esta práctica vamos a emplear los siguientes reactivos, todo ellos fáciles de conseguir en las casas de los/as alumnos/as. - Agua. - Sulfato de cobre pentahidratado. - Amoniaco - Sosa cáustica (hidróxido de sodio) 5. METODOLOGÍA Y FUNDAMENTO TEÓRICO Vamos a proponer al alumnado que hagan una serie de disoluciones, para poder acercarnos a la formación de iones complejos, así como a las reacciones de precipitación. Para eso tomamos de partida una disolución que haremos disolviendo en un recipiente una cucharada aproximadamente de sulfato de cobre pentahidratado en unos 200 ml de agua. Distribuimos este volumen en 5 recipientes añadiendo a cada uno más o menos el mismo volumen de disolución. Procedemos también a disolver una cucharadita de sosa cáustica en unos 200 ml de agua, consideremos que este proceso de disolución es fuertemente exotérmico.
3 5.1. Recipiente 1 (Nada) Un recipientelo tomamos como referencia y no le echamos ningún aditivo, para poder ver el color original de la disolución acuosa del sulfato de cobre pentahidratado y poder así poner de manifiesto los cambios de color en los otros recipientes a añadirle los aditivos indicados y en las cantidades especificadas (si bien el estudio es cualitativo no cuantitativo) Recipiente 2 (Poco hidróxido sódico) Sobre uno de los recipientes, con la disolución acuosa del sulfato de cobre pentahiodratado, echamos un poco de disolución de sosa cáustica (hidróxido de sodio) en agua (con una jeringa), que previamente hemos preparado. Al añadir un poco de la disolución de hidróxido de sodio sobre la disolución de sulfato de cobre pentahidratado, tiene lugar la siguiente reacción:
4 2NaOH + CuSO4 Na2SO4 + Cu(OH)2 (s) Recordemos que el sulfato de cobre pentahidratado en disolución aparece sólo con sulfato de cobre. El Hidróxido de cobre (II) es un sólido azul de aspecto gelatinoso Recipiente 3 (Exceso de hidróxido sódico) Sobre otro de los recipientes, con la disolución acuosa del sulfato de cobre pentahiodratado, echamos un exceso de disolución de sosa cáustica (hidróxido de sodio) en agua (con una jeringa), que previamente hemos preparado. Si sobre la reacción anterior seguimos echando más hidróxido sódico, se empieza a formar el ion cuprato (CuO2² ) que tiene un color azul más fuerte que el de la disolución del sulfato de cobre pentahidratado.
5 Observando los tres a la vez para ver el contraste quedaría: 5.4. Recipiente 4 (Poco amoniaco)
6 Sobre otro de los recipientes, con la disolución acuosa del sulfato de cobre pentahiodratado, echamos un poco de disolución de amoniaco en agua (con una jeringa), esta disolución no es otra cosa que el amoniaco comercial. Al añadir una pequeña cantidad de amoniaco vemos un nuevo sólido de tono verdeazulado. 2Cu² + + SO NH 3 + H 2 O Cu 2 SO 4 (OH) 2 (s) + 2NH 4 + El Cu 2 SO 4 (OH) 2 es el sólido verdeazulado Recipiente 5 (Exceso de amoniaco) Sobre otro de los recipientes, con la disolución acuosa del sulfato de cobre pentahiodratado, echamos un exceso de disolución de amoniaco en agua (con una jeringa), esta disolución no es otra cosa que el amoniaco comercial. Si se añade más amoniaco desaparece el sólido y aparece un fuerte color azul debido a la formación del ion complejo tetramíncobre (II) Cu 2 SO 4 (OH) 2 (s) + 8NH 3 2Cu(NH 3 ) SO OH -
7 Observando los tres a la vez, para ver el contraste de color queda: BIBLIOGRAFIA - Lozano, J.J: (1983). Fundamentos de Química General. Barcelona: Editorial Alambra.
8 - Morcillo, Jesús (1976). Química General. Madrid: Editorial U.N.E.D. - Romero, M (2002). Enlace Químico y Estructura Molecular. Barcelona: Editorial Calamo Producciones. - Gutiérrez Ríos, Enrique (1998). Química Inorgánica. Madrid: Reverte - Álvarez, J. M. (1988). Didáctica, Currículo y Evaluación: Ensayos sobre cuestiones didácticas. Barcelona: Alamex, S.A. - Estebaranz García, A. (1994). Didáctica e innovación curricular. Sevilla: Publicaciones Universidad de Sevilla. - López Ruiz, Juan Ignacio (2000). Aprendizaje docente e innovación curricular. Dos estudios de caso sobre el constructivismo en la escuela. Granada: Aljibe. - MENA Merchán, B. (1998). Didáctica y currículum escolar. Salamanca: Anthema. - Román M. y Diez E. (1994). Currículum y Enseñanza: una Didáctica centrada en procesos. Madrid: EOS. Autoría Nombre y Apellidos: Javier Ruiz Hidalgo Centro, localidad, provincia: IES Diego de Siloé, Íllora, Granada javierruizh@hotmail.com
SUSTANCIAS NATURALES CON ENLACE QUÍMICO IÓNICO
 SUSTANCIAS NATURALES CON ENLACE QUÍMICO IÓNICO AUTOR JAVIER RUIZ HIDALGO TEMÁTICA ENLACE QUÍMICO ETAPA BACHILLERATO Resumen En este trabajo he querido buscar imágenes de minerales, para poder utilizarlas
SUSTANCIAS NATURALES CON ENLACE QUÍMICO IÓNICO AUTOR JAVIER RUIZ HIDALGO TEMÁTICA ENLACE QUÍMICO ETAPA BACHILLERATO Resumen En este trabajo he querido buscar imágenes de minerales, para poder utilizarlas
PREPARACIÓN DE MATERIALES DIDÁCTICOS EN QUÍMICA PARA EXPLICAR LA GEOMETRÍA DE LAS MOLÉCULAS
 PREPARACIÓN DE MATERIALES DIDÁCTICOS EN QUÍMICA PARA EXPLICAR LA GEOMETRÍA DE LAS MOLÉCULAS AUTOR JAVIER RUIZ HIDALGO TEMÁTICA DIDÁCTICA DE LA QUÍMICA ETAPA BACHILLERATO Resumen En el siguiente trabajo
PREPARACIÓN DE MATERIALES DIDÁCTICOS EN QUÍMICA PARA EXPLICAR LA GEOMETRÍA DE LAS MOLÉCULAS AUTOR JAVIER RUIZ HIDALGO TEMÁTICA DIDÁCTICA DE LA QUÍMICA ETAPA BACHILLERATO Resumen En el siguiente trabajo
PREPARACIÓN DE MATERIALES DIDÁCTICOS PARA QUÍMICA POR PARTE DEL ALUMNADO DE LA EDUCACIÓN SECUNDARIA OBLIGATORIA
 PREPARACIÓN DE MATERIALES DIDÁCTICOS PARA QUÍMICA POR PARTE DEL ALUMNADO DE LA EDUCACIÓN SECUNDARIA OBLIGATORIA AUTOR JAVIER RUIZ HIDALGO TEMÁTICA DIDÁCIRTICA DE LA QUÍMICA ETAPA EDUCACIÓN SECUNDARIA OBLIGATORIA
PREPARACIÓN DE MATERIALES DIDÁCTICOS PARA QUÍMICA POR PARTE DEL ALUMNADO DE LA EDUCACIÓN SECUNDARIA OBLIGATORIA AUTOR JAVIER RUIZ HIDALGO TEMÁTICA DIDÁCIRTICA DE LA QUÍMICA ETAPA EDUCACIÓN SECUNDARIA OBLIGATORIA
MATERIAL DIDÁCTICO DE LOS HIDROCARBUROS AROMÁTICOS
 MATERIAL DIDÁCTICO DE LOS HIDROCARBUROS AROMÁTICOS AUTOR JAVIER RUIZ HIDALGO TEMÁTICA QUÍMICA ORGÁNICA ETAPA BACHILLERATO Resumen En el presente artículo vamos a ver una serie de fotos de representaciones
MATERIAL DIDÁCTICO DE LOS HIDROCARBUROS AROMÁTICOS AUTOR JAVIER RUIZ HIDALGO TEMÁTICA QUÍMICA ORGÁNICA ETAPA BACHILLERATO Resumen En el presente artículo vamos a ver una serie de fotos de representaciones
DETERMINACIÓN EXPERIMENTAL DEL ORDEN DE UNA REACCIÓN QUÍMICA PARA SEGUNDO DE BACHILLERATO
 DETERMINACIÓN EXPERIMENTAL DEL ORDEN DE UNA REACCIÓN QUÍMICA PARA SEGUNDO DE BACHILLERATO AUTOR JAVIER RUIZ HIDALGO TEMÁTICA CINÉTICA QUÍMICA ETAPA BACHILLERATO Resumen En el presente artículo vamos a
DETERMINACIÓN EXPERIMENTAL DEL ORDEN DE UNA REACCIÓN QUÍMICA PARA SEGUNDO DE BACHILLERATO AUTOR JAVIER RUIZ HIDALGO TEMÁTICA CINÉTICA QUÍMICA ETAPA BACHILLERATO Resumen En el presente artículo vamos a
CONTRIBUCIÓN DE LA FÍSICA Y QUÍMICA AL DESARROLLO DE LA COMPETENCIA BÁSICA MATEMÁTICA EN LA EDUCACIÓN SECUNDARIA OBLIGATORIA y BACHILLERATO
 CONTRIBUCIÓN DE LA FÍSICA Y QUÍMICA AL DESARROLLO DE LA COMPETENCIA BÁSICA MATEMÁTICA EN LA EDUCACIÓN SECUNDARIA OBLIGATORIA y BACHILLERATO AUTOR JAVIER RUIZ HIDALGO TEMÁTICA COMPETENCIAS BÁSICAS Y FÍSICA
CONTRIBUCIÓN DE LA FÍSICA Y QUÍMICA AL DESARROLLO DE LA COMPETENCIA BÁSICA MATEMÁTICA EN LA EDUCACIÓN SECUNDARIA OBLIGATORIA y BACHILLERATO AUTOR JAVIER RUIZ HIDALGO TEMÁTICA COMPETENCIAS BÁSICAS Y FÍSICA
ESTUDIO SOBRE LA DESNATURALIZACIÓN DE PROTEÍNAS Y DETERMINACIÓN DE ALGUNAS PROPIEDADES DE LAS PROTEÍNAS CON SEGUNDO DE BACHILLERARO
 ESTUDIO SOBRE LA DESNATURALIZACIÓN DE PROTEÍNAS Y DETERMINACIÓN DE ALGUNAS PROPIEDADES DE LAS PROTEÍNAS CON SEGUNDO DE BACHILLERARO AUTOR JAVIER RUIZ HIDALGO TEMÁTICA PROTEINAS ETAPA BACHILLERATO Resumen
ESTUDIO SOBRE LA DESNATURALIZACIÓN DE PROTEÍNAS Y DETERMINACIÓN DE ALGUNAS PROPIEDADES DE LAS PROTEÍNAS CON SEGUNDO DE BACHILLERARO AUTOR JAVIER RUIZ HIDALGO TEMÁTICA PROTEINAS ETAPA BACHILLERATO Resumen
UTILIZACIÓN DE SEMEJANZAS Y SIMILITUDES COMO RECURSO DIDÁCTICO PARA QUÍMICA EN EL BACHILLERATO Y EN LA EDUCACIÓN SECUNDARIA OBLIGATORIA
 UTILIZACIÓN DE SEMEJANZAS Y SIMILITUDES COMO RECURSO DIDÁCTICO PARA QUÍMICA EN EL BACHILLERATO Y EN LA EDUCACIÓN SECUNDARIA OBLIGATORIA AUTOR JAVIER RUIZ HIDALGO TEMÁTICA DIDÁCTICA DE LA QUÍMICA ETAPA
UTILIZACIÓN DE SEMEJANZAS Y SIMILITUDES COMO RECURSO DIDÁCTICO PARA QUÍMICA EN EL BACHILLERATO Y EN LA EDUCACIÓN SECUNDARIA OBLIGATORIA AUTOR JAVIER RUIZ HIDALGO TEMÁTICA DIDÁCTICA DE LA QUÍMICA ETAPA
CONCURSO DIDÁCTICO: VAMOS A OBTENER UN CRISTAL IÓNICO DE GRAN TAMAÑO
 CONCURSO DIDÁCTICO: VAMOS A OBTENER UN CRISTAL IÓNICO DE GRAN TAMAÑO AUTOR JAVIER RUIZ HIDALGO TEMÁTICA CRISTALIZACIÓN DE COMPUESTOS IÓNICOS ETAPA EDUCACIÓN SECUNDARIA OBLIGATORIO Resumen En el presente
CONCURSO DIDÁCTICO: VAMOS A OBTENER UN CRISTAL IÓNICO DE GRAN TAMAÑO AUTOR JAVIER RUIZ HIDALGO TEMÁTICA CRISTALIZACIÓN DE COMPUESTOS IÓNICOS ETAPA EDUCACIÓN SECUNDARIA OBLIGATORIO Resumen En el presente
ESTRUCTURA QUÍMICA DE LOS METALES NATIVOS
 ESTRUCTURA QUÍMICA DE LOS METALES NATIVOS AUTOR JAVIER RUIZ HIDALGO TEMÁTICA ESTRUCTURA DE LA MATERIA ETAPA BACHILLERATO Resumen En el presente trabajo vamos a proponer una serie de imágenes de metales,
ESTRUCTURA QUÍMICA DE LOS METALES NATIVOS AUTOR JAVIER RUIZ HIDALGO TEMÁTICA ESTRUCTURA DE LA MATERIA ETAPA BACHILLERATO Resumen En el presente trabajo vamos a proponer una serie de imágenes de metales,
Práctica 11 Equilibrios de Solubilidad
 UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE QUÍMICA LABORATORIO DE QUÍMICA GENERAL II Grupo: Equipo: Nombre: Nombre: Nombre: Nombre: Nombre: 1 PROBLEMAS: Práctica 11 Equilibrios de Solubilidad
UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE QUÍMICA LABORATORIO DE QUÍMICA GENERAL II Grupo: Equipo: Nombre: Nombre: Nombre: Nombre: Nombre: 1 PROBLEMAS: Práctica 11 Equilibrios de Solubilidad
SUSTANCIAS NATURALES CON ENLACE QUÍMICO COVALENTE
 SUSTANCIAS NATURALES CON ENLACE QUÍMICO COVALENTE AUTOR JAVIER RUIZ HIDALGO TEMÁTICA ENLACE QUÍMICO ETAPA BACHILLERATO Resumen En el presente trabajo recopilo imágenes de sustancias sólidas naturales,
SUSTANCIAS NATURALES CON ENLACE QUÍMICO COVALENTE AUTOR JAVIER RUIZ HIDALGO TEMÁTICA ENLACE QUÍMICO ETAPA BACHILLERATO Resumen En el presente trabajo recopilo imágenes de sustancias sólidas naturales,
PROCEDIMIENTO DIDÁCTICO PARA LA REALIZACIÓN DE VALORACIONES ÁCIDO-BASE (CÁLCULO DE LA ACIDEZ DE UN ACEITE DE OLIVA)
 PROCEDIMIENTO DIDÁCTICO PARA LA REALIZACIÓN DE VALORACIONES ÁCIDO-BASE (CÁLCULO DE LA ACIDEZ DE UN ACEITE DE OLIVA) AUTOR JAVIER RUIZ HIDALGO TEMÁTICA REACCIONES DE TRANSFERENCIA DE PROTONES ETAPA BACHILLERATO
PROCEDIMIENTO DIDÁCTICO PARA LA REALIZACIÓN DE VALORACIONES ÁCIDO-BASE (CÁLCULO DE LA ACIDEZ DE UN ACEITE DE OLIVA) AUTOR JAVIER RUIZ HIDALGO TEMÁTICA REACCIONES DE TRANSFERENCIA DE PROTONES ETAPA BACHILLERATO
Nombres de los integrantes: Práctica 13 Ley de la conservación de la materia. Transformaciones sucesivas del cobre
 Nombres de los integrantes: 1 Universidad Nacional Autónoma de México Facultad de Química Laboratorio de Química General I Grupo Equipo Práctica 13 Ley de la conservación de la materia. Problema Qué masa
Nombres de los integrantes: 1 Universidad Nacional Autónoma de México Facultad de Química Laboratorio de Química General I Grupo Equipo Práctica 13 Ley de la conservación de la materia. Problema Qué masa
OBTENCIÓN DE UN PAPEL INDICADOR PARTIENDO DE PÉTALOS DE ROSAS, LOMBARDA Y CURRY
 OBTENCIÓN DE UN PAPEL INDICADOR PARTIENDO DE PÉTALOS DE ROSAS, LOMBARDA Y CURRY AUTOR JAVIER RUIZ HIDALGO TEMÁTICA QUÍMICA GENERAL ETAPA BACHILLERATO Resumen En el presente artículo vamos a intentar demostrar
OBTENCIÓN DE UN PAPEL INDICADOR PARTIENDO DE PÉTALOS DE ROSAS, LOMBARDA Y CURRY AUTOR JAVIER RUIZ HIDALGO TEMÁTICA QUÍMICA GENERAL ETAPA BACHILLERATO Resumen En el presente artículo vamos a intentar demostrar
Práctica 11: Equilibrios de Solubilidad
 Equipo: Nombre: Nombre: Nombre: Práctica 11: Equilibrios de Solubilidad PROBLEMAS: Ordenar, de menor a mayor solubilidad, los siguientes compuestos de cobre: Cu(OH) 2, CuCO 3, CuSO 4, Cu (S) y Cu 2 [Fe(CN)
Equipo: Nombre: Nombre: Nombre: Práctica 11: Equilibrios de Solubilidad PROBLEMAS: Ordenar, de menor a mayor solubilidad, los siguientes compuestos de cobre: Cu(OH) 2, CuCO 3, CuSO 4, Cu (S) y Cu 2 [Fe(CN)
PRÁCTICA 18 EQUILIBRIOS DE SOLUBILIDAD. ESTIMACIÓN DEL PRODUCTO DE SOLUBILIDAD DEL HIDRÓXIDO DE ZINC.
 PRÁCTICA 18 EQUILIBRIOS DE SOLUBILIDAD. ESTIMACIÓN DEL PRODUCTO DE SOLUBILIDAD DEL HIDRÓXIDO DE ZINC. OBJETIVOS Determinar experimentalmente si se forma o no un determinado compuesto insoluble. Determinar
PRÁCTICA 18 EQUILIBRIOS DE SOLUBILIDAD. ESTIMACIÓN DEL PRODUCTO DE SOLUBILIDAD DEL HIDRÓXIDO DE ZINC. OBJETIVOS Determinar experimentalmente si se forma o no un determinado compuesto insoluble. Determinar
Ordenar, de menor a mayor solubilidad, los siguientes compuestos de cobre: Cu(OH) 2, CuCO 3, CuSO 4, CuS y Cu 2 [Fe(CN) 6 ].
![Ordenar, de menor a mayor solubilidad, los siguientes compuestos de cobre: Cu(OH) 2, CuCO 3, CuSO 4, CuS y Cu 2 [Fe(CN) 6 ]. Ordenar, de menor a mayor solubilidad, los siguientes compuestos de cobre: Cu(OH) 2, CuCO 3, CuSO 4, CuS y Cu 2 [Fe(CN) 6 ].](/thumbs/87/95356961.jpg) 13. Equilibrios de Solubilidad Elaborada por: Dr. Ruy Cervantes Díaz de Guzmán Pregunta a responder al final de la sesión Ordenar, de menor a mayor solubilidad, los siguientes compuestos de cobre: Cu(OH)
13. Equilibrios de Solubilidad Elaborada por: Dr. Ruy Cervantes Díaz de Guzmán Pregunta a responder al final de la sesión Ordenar, de menor a mayor solubilidad, los siguientes compuestos de cobre: Cu(OH)
PVQ28-1.**. Mezcla de Fe/S con ácido sulfúrico reaccionando sobre sulfato de cobre(ii)
 PROBLEMAS VISUALES DE QUÍMICA PVQ8-1.**. Mezcla de Fe/S con ácido sulfúrico reaccionando sobre sulfato de cobre(ii) En A se disponen 5,6 de Fe y 3,g de azufre,y 10mL de ácido sulfúrico 6N,y en B, 30mL
PROBLEMAS VISUALES DE QUÍMICA PVQ8-1.**. Mezcla de Fe/S con ácido sulfúrico reaccionando sobre sulfato de cobre(ii) En A se disponen 5,6 de Fe y 3,g de azufre,y 10mL de ácido sulfúrico 6N,y en B, 30mL
CuO (s) + H 2 SO 4(aq) CuSO 4(aq) +H 2 O (aq)
 Relación de problemas Química 4º ESO CDP. NTRA. SRA. DE LORETO 1. El trióxido de azufre se sintetiza a partir de dióxido de azufre y oxígeno molecular. Calcula la masa y el volumen de los reactivos que
Relación de problemas Química 4º ESO CDP. NTRA. SRA. DE LORETO 1. El trióxido de azufre se sintetiza a partir de dióxido de azufre y oxígeno molecular. Calcula la masa y el volumen de los reactivos que
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2002 QUÍMICA TEMA 1: LA TRANSFORMACIÓN QUÍMICA
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 00 QUÍMICA TEMA 1: LA TRANSFORMACIÓN QUÍMICA Junio, Ejercicio, Opción B Junio, Ejercicio 6, Opción A Reserva 1, Ejercicio, Opción B Reserva 1, Ejercicio 4, Opción
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 00 QUÍMICA TEMA 1: LA TRANSFORMACIÓN QUÍMICA Junio, Ejercicio, Opción B Junio, Ejercicio 6, Opción A Reserva 1, Ejercicio, Opción B Reserva 1, Ejercicio 4, Opción
ANÁLISIS CUALITATIVO DE CATIONES Y ANIONES
 VII 1 PRÁCTICA 7 ANÁLISIS CUALITATIVO DE CATIONES Y ANIONES FORMACIÓN DE PRECIPITADOS Y DISOLUCIÓN DE LOS MISMOS POR FORMACIÓN DE COMPLEJOS FUNDAMENTO DE LA PRÁCTICA En esta práctica llevaremos a cabo
VII 1 PRÁCTICA 7 ANÁLISIS CUALITATIVO DE CATIONES Y ANIONES FORMACIÓN DE PRECIPITADOS Y DISOLUCIÓN DE LOS MISMOS POR FORMACIÓN DE COMPLEJOS FUNDAMENTO DE LA PRÁCTICA En esta práctica llevaremos a cabo
DETERMINACIÓN EXPERIMENTAL DEL CONTENIDO DE ÁCIDO ASCÓRBICO (VITAMINA C) EN UN ZUMO DE NARANJA
 DETERMINACIÓN EXPERIMENTAL DEL CONTENIDO DE ÁCIDO ASCÓRBICO (VITAMINA C) EN UN ZUMO DE NARANJA AUTOR JAVIER RUIZ HIDALGO TEMÁTICA REACCIONES DE OXIDACIÓN-REDUCCIÓN ETAPA BACHILLERATO Resumen En el presente
DETERMINACIÓN EXPERIMENTAL DEL CONTENIDO DE ÁCIDO ASCÓRBICO (VITAMINA C) EN UN ZUMO DE NARANJA AUTOR JAVIER RUIZ HIDALGO TEMÁTICA REACCIONES DE OXIDACIÓN-REDUCCIÓN ETAPA BACHILLERATO Resumen En el presente
Comprobar la reversibilidad de algunas reacciones químicas, por medio de la modificación de las condiciones de equilibrio.
 Laboratorio de Análisis Cuantitativo Hoja 1 de 5 Elaboró: M.C. Yolanda Ángeles Cruz 1. OBJETIVOS. Demostrar que un estado de equilibrio puede alcanzarse haciendo reaccionar a los reactivos para formar
Laboratorio de Análisis Cuantitativo Hoja 1 de 5 Elaboró: M.C. Yolanda Ángeles Cruz 1. OBJETIVOS. Demostrar que un estado de equilibrio puede alcanzarse haciendo reaccionar a los reactivos para formar
Práctica 11: Equilibrios de Solubilidad
 Equipo: PROBLEMAS: Nombre: Nombre: Nombre: Práctica 11: Equilibrios de Solubilidad Ordenar, de menor a mayor solubilidad, los siguientes compuestos de cobre: Cu(OH) 2, CuCO 3, CuSO 4, Cu (S) y Cu 2 [Fe(CN)
Equipo: PROBLEMAS: Nombre: Nombre: Nombre: Práctica 11: Equilibrios de Solubilidad Ordenar, de menor a mayor solubilidad, los siguientes compuestos de cobre: Cu(OH) 2, CuCO 3, CuSO 4, Cu (S) y Cu 2 [Fe(CN)
ISSN DEP. LEGAL: GR 2922/2007 Nº 21 AGOSTO DE 2009
 ACTIVIDADES DE MOTIVACIÓN PARTICIPACIÓN COMO APLICACIÓN DIDÁCTICA EN FÍSICA Y QUÍMICA Y CIENCIAS DE LA NATURALEZA PARA LA EDUCACIÓN SECUNDARIA OBLIGATORIA AUTOR JAVIER RUIZ HIDALGO TEMÁTICA DIDÁCTICA DE
ACTIVIDADES DE MOTIVACIÓN PARTICIPACIÓN COMO APLICACIÓN DIDÁCTICA EN FÍSICA Y QUÍMICA Y CIENCIAS DE LA NATURALEZA PARA LA EDUCACIÓN SECUNDARIA OBLIGATORIA AUTOR JAVIER RUIZ HIDALGO TEMÁTICA DIDÁCTICA DE
Experimentación en Química Inorgánica 1 PRÁCTICA X. HIERRO
 Experimentación en Química Inorgánica 1 PRÁCTICA X. HIERRO Reacciones del hierro Material Reactivos Gradilla de tubos de ensayo Sulfato de hierro(ii) 0.1M Cloruro de hierro(ii) (s) Cuentagotas Cloruro
Experimentación en Química Inorgánica 1 PRÁCTICA X. HIERRO Reacciones del hierro Material Reactivos Gradilla de tubos de ensayo Sulfato de hierro(ii) 0.1M Cloruro de hierro(ii) (s) Cuentagotas Cloruro
INFORME DE LABORATORIO N 5 ESTEQUIOMETRÌA I
 UNIVERSIDAD DE CIENCIAS E INFORMATICA FACULTAD DE CIENCIAS DE LA SALUD ESCUELA DE KINESIOLOGIA INFORME DE LABORATORIO N 5 ESTEQUIOMETRÌA I Asignatura Profesor Alumno :Química general : José Gabriel Martínez
UNIVERSIDAD DE CIENCIAS E INFORMATICA FACULTAD DE CIENCIAS DE LA SALUD ESCUELA DE KINESIOLOGIA INFORME DE LABORATORIO N 5 ESTEQUIOMETRÌA I Asignatura Profesor Alumno :Química general : José Gabriel Martínez
Ácido + Base -----> Sal + Agua
 - REACCIÓN DE NEUTRALIZACIÓN - Objetivos: A).- Realización de cálculos en la reacción de neutralización (o valoración) entre una base, la sosa cáustica NaOH, y un ácido, el ácido clorhídrico HCl. La ecuación
- REACCIÓN DE NEUTRALIZACIÓN - Objetivos: A).- Realización de cálculos en la reacción de neutralización (o valoración) entre una base, la sosa cáustica NaOH, y un ácido, el ácido clorhídrico HCl. La ecuación
Problemas disoluciones
 Problemas disoluciones Determinar la concentración de una disolución expresada de diferentes formas: g/l, % en masa y en volumen, Molaridad y fracción molar Preparar disoluciones a partir de solutos sólidos
Problemas disoluciones Determinar la concentración de una disolución expresada de diferentes formas: g/l, % en masa y en volumen, Molaridad y fracción molar Preparar disoluciones a partir de solutos sólidos
ESTEQUIOMETRÍA. cobre(ii) y se descompone, cuántas moles de dióxido de nitrógeno se formarán? A moles B moles C moles D. 0.
 ESTEQUIOMETRÍA 1 Al calentarse fuertemente, el nitrato de cobre(ii) se descompone en óxido de cobre(ii), dióxido de nitrógeno y oxígeno elemental (O 2 ). Si calentamos 0.10 moles de nitrato de cobre(ii)
ESTEQUIOMETRÍA 1 Al calentarse fuertemente, el nitrato de cobre(ii) se descompone en óxido de cobre(ii), dióxido de nitrógeno y oxígeno elemental (O 2 ). Si calentamos 0.10 moles de nitrato de cobre(ii)
Vamos a reaccionar una solución de lactosa 5%, solución de fehling A, solución de fehling B.
 RECONOCIMIENTO DE LOS HIDRATOS DE CARBONO. Los monosacáridos son el grupo funcional más simple de los hidratos de carbono y se clasifican según estén formados por un aldehído o por una cetona. Una de las
RECONOCIMIENTO DE LOS HIDRATOS DE CARBONO. Los monosacáridos son el grupo funcional más simple de los hidratos de carbono y se clasifican según estén formados por un aldehído o por una cetona. Una de las
Problemas de Química. 1º de Grado en Ingeniería Química. Tema 17
 Problemas de Química. 1º de Grado en Ingeniería Química. Tema 17 Si cree que necesita datos adicionales para resolver los problemas búsquelos en las tablas de los libros. EQUILIBRIO ÁCIDO-BASE 1. a) Cuál
Problemas de Química. 1º de Grado en Ingeniería Química. Tema 17 Si cree que necesita datos adicionales para resolver los problemas búsquelos en las tablas de los libros. EQUILIBRIO ÁCIDO-BASE 1. a) Cuál
QUÍMICA.SEPTIEMBRE (FE). OPCIÓN A
 1. (2,5 puntos) QUÍMICA.SEPTIEMBRE (FE). OPCIÓN A Las entalpías estándar de combustión del C(s), H 2 (g) y propano gas, C 3 H 8 (g), son -394, -286 y -2220 kj/mol, respectivamente: i. Calcule la entalpía
1. (2,5 puntos) QUÍMICA.SEPTIEMBRE (FE). OPCIÓN A Las entalpías estándar de combustión del C(s), H 2 (g) y propano gas, C 3 H 8 (g), son -394, -286 y -2220 kj/mol, respectivamente: i. Calcule la entalpía
PIP 4º ESO IES SÉNECA TRABAJO EXPERIMENTAL EN FÍSICA Y QUÍMICA
 1. REACCIÓN REDOX Una reacción redox muy conocida es la reducción del permanganato. Si dicho proceso se lleva a cabo en medio ácido, el ion permanganato (MnO4 - ), de color violeta intenso en disolución,
1. REACCIÓN REDOX Una reacción redox muy conocida es la reducción del permanganato. Si dicho proceso se lleva a cabo en medio ácido, el ion permanganato (MnO4 - ), de color violeta intenso en disolución,
Una reacción redox con cambios de color (tartrato+ agua oxigenada + sulfato de cobre)
 Una reacción redox con cambios de color (tartrato+ agua oxigenada + sulfato de cobre) Material Agitador magnético Vasos de precipitados Probetas Termómetro Base y varilla soporte Disolución de tartrato
Una reacción redox con cambios de color (tartrato+ agua oxigenada + sulfato de cobre) Material Agitador magnético Vasos de precipitados Probetas Termómetro Base y varilla soporte Disolución de tartrato
XX OLIMPIADA DE QUÍMICA CUESTIONES
 XX OLIMPIADA DE QUÍMICA CUESTIONES 1º) Se quema con una cerilla un poco de alcohol en un plato hasta que no quede nada de líquido. Indica cual de las siguientes proposiciones es la correcta: a) Los gases
XX OLIMPIADA DE QUÍMICA CUESTIONES 1º) Se quema con una cerilla un poco de alcohol en un plato hasta que no quede nada de líquido. Indica cual de las siguientes proposiciones es la correcta: a) Los gases
Una introducción al laboratorio de Química
 Mina de Naica (México). Cristales de selenita (CaSO 4.2H 2 O) Imagen http://www.taringa.net/posts/info/13526031/proyecto-naica.html Una introducción al laboratorio de Química 1. INTRODUCCIÓN La gente joven
Mina de Naica (México). Cristales de selenita (CaSO 4.2H 2 O) Imagen http://www.taringa.net/posts/info/13526031/proyecto-naica.html Una introducción al laboratorio de Química 1. INTRODUCCIÓN La gente joven
2º CUADERNILLO DE FÍSICA Y QUÍMICA
 2º CUADERNILLO DE FÍSICA Y QUÍMICA Alumnos de 4º ESO con la asignatura de Física y Química de 3º ESO suspensa NOMBRE CURSO ENLACES 1. Representa mediante un diagrama de Lewis las siguientes moléculas:
2º CUADERNILLO DE FÍSICA Y QUÍMICA Alumnos de 4º ESO con la asignatura de Física y Química de 3º ESO suspensa NOMBRE CURSO ENLACES 1. Representa mediante un diagrama de Lewis las siguientes moléculas:
CONTRIBUCIÓN DE LA FÍSICA Y QUÍMICA A LA ADQUISICIÓN DE LA COMPETENCIA BÁSICA LINGÜÍSTICA EN LA EDUCACIÓN SECUNDARIA OBLIGATORIA y BACHILLERATO
 CONTRIBUCIÓN DE LA FÍSICA Y QUÍMICA A LA ADQUISICIÓN DE LA COMPETENCIA BÁSICA LINGÜÍSTICA EN LA EDUCACIÓN SECUNDARIA OBLIGATORIA y BACHILLERATO AUTOR JAVIER RUIZ HIDALGO TEMÁTICA FISICA Y QUIMICA ETAPA
CONTRIBUCIÓN DE LA FÍSICA Y QUÍMICA A LA ADQUISICIÓN DE LA COMPETENCIA BÁSICA LINGÜÍSTICA EN LA EDUCACIÓN SECUNDARIA OBLIGATORIA y BACHILLERATO AUTOR JAVIER RUIZ HIDALGO TEMÁTICA FISICA Y QUIMICA ETAPA
Química. Equilibrio ácido-base Nombre:
 Química DEPARTAMENTO DE FÍSICA E QUÍMICA Equilibrio ácido-base 25-02-08 Nombre: Cuestiones y problemas 1. a) Qué concentración tiene una disolución de amoníaco de ph =10,35? [1½ PUNTO] b) Qué es una disolución
Química DEPARTAMENTO DE FÍSICA E QUÍMICA Equilibrio ácido-base 25-02-08 Nombre: Cuestiones y problemas 1. a) Qué concentración tiene una disolución de amoníaco de ph =10,35? [1½ PUNTO] b) Qué es una disolución
Reacciones de transferencia de protones
 Reacciones de transferencia de protones 4. Aplicar la teoría de Brönsted para reconocer las sustancias que pueden actuar como ácidos o bases, saber determinar el ph de sus disoluciones, explicar las reacciones
Reacciones de transferencia de protones 4. Aplicar la teoría de Brönsted para reconocer las sustancias que pueden actuar como ácidos o bases, saber determinar el ph de sus disoluciones, explicar las reacciones
Electroquímic a a tu alcance
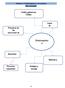 Práctica 2. Electroquímica a tu alcance Mapa conceptual Celdas galvánicas Celdas electroquímicas Principios de las reacciones de óxido reducción Leyes de Faraday Electroquímic a a tu alcance Electrólisi
Práctica 2. Electroquímica a tu alcance Mapa conceptual Celdas galvánicas Celdas electroquímicas Principios de las reacciones de óxido reducción Leyes de Faraday Electroquímic a a tu alcance Electrólisi
2º de Bachillerato EQUILIBRIOS DE SOLUBILIDAD
 º de Bachillerato EQUILIBRIOS DE SOLUBILIDAD Indice 1. Equilibrios heterogéneos.. Solubilidad. Reglas de solubilidad. 3. Reacciones de precipitación. 4. Producto de solubilidad. 5. Factores que modifican
º de Bachillerato EQUILIBRIOS DE SOLUBILIDAD Indice 1. Equilibrios heterogéneos.. Solubilidad. Reglas de solubilidad. 3. Reacciones de precipitación. 4. Producto de solubilidad. 5. Factores que modifican
PROPIEDADES ÁCIDO-BASE DE LAS SALES: HIDRÓLISIS
 IV-1 PRÁCTICA- PROPIEDADES ÁCIDO-BASE DE LAS SALES: HIDRÓLISIS En esta práctica mediremos el ph (carácter ácido, básico o neutro de disoluciones acuosas de diversas sales, y comprobaremos que estas disoluciones
IV-1 PRÁCTICA- PROPIEDADES ÁCIDO-BASE DE LAS SALES: HIDRÓLISIS En esta práctica mediremos el ph (carácter ácido, básico o neutro de disoluciones acuosas de diversas sales, y comprobaremos que estas disoluciones
1. Se dispone de una disolución acuosa de ácido sulfúrico del 98% de riqueza en masa y densidad 1,84 g/ml.
 ESTEQUIOMETRÍA,DISOLUCIONES: ACTIVIDADES DE SELECTIVIDAD. 1. Se dispone de una disolución acuosa de ácido sulfúrico del 98% de riqueza en masa y densidad 1,84 g/ml. a) Qué volumen de esta disolución se
ESTEQUIOMETRÍA,DISOLUCIONES: ACTIVIDADES DE SELECTIVIDAD. 1. Se dispone de una disolución acuosa de ácido sulfúrico del 98% de riqueza en masa y densidad 1,84 g/ml. a) Qué volumen de esta disolución se
LABORATORIO GRUPO 15. NaOH NH 3
 Química Inorgánica Laboratorio Grupo 15 1 A) OBTENCIÓN DE AMONÍACO LABORATORIO GRUPO 15 Materiales: balanza granataria, un tubo de ensayos con tapón con un tubo de vidrio doblado 90,... Reactivos: cloruro
Química Inorgánica Laboratorio Grupo 15 1 A) OBTENCIÓN DE AMONÍACO LABORATORIO GRUPO 15 Materiales: balanza granataria, un tubo de ensayos con tapón con un tubo de vidrio doblado 90,... Reactivos: cloruro
LABORATORIO # 5 TITULO : ANALISIS CUALITATIVO DE CATIONES Y ANIONES.
 LABORATORIO # 5 TITULO : ANALISIS CUALITATIVO DE CATIONES Y ANIONES. OBJETIVO: Mostrar al estudiante como los iones metálicos y algunos aniones pueden separarse e identificarse, en base a reacciones químicas
LABORATORIO # 5 TITULO : ANALISIS CUALITATIVO DE CATIONES Y ANIONES. OBJETIVO: Mostrar al estudiante como los iones metálicos y algunos aniones pueden separarse e identificarse, en base a reacciones químicas
QUÍMICA 2º Bachillerato Ejercicios: Reacciones Ácido Base
 1(8) Ejercicio nº 1 Completa las siguientes reacciones ácido-base, indicando qué especies químicas son el ácido y la base, y cuáles sus conjugados: a) HA + B b) HCl + NH 3 c) HNO 3 + H 2 O Ejercicio nº
1(8) Ejercicio nº 1 Completa las siguientes reacciones ácido-base, indicando qué especies químicas son el ácido y la base, y cuáles sus conjugados: a) HA + B b) HCl + NH 3 c) HNO 3 + H 2 O Ejercicio nº
DETERMINACIÓN DE LA ALCALINIDAD DE UN DESATASCADOR COMERCIAL
 DETERMINACIÓN DE LA ALCALINIDAD DE UN DESATASCADOR COMERCIAL AUTORÍA JOAQUÍN RUIZ MOLINA TEMÁTICA CIENCIAS EXPERIMENTALES, QUÍMICA ETAPA BACHILLERATO, FORMACIÓN PROFESIONAL Resumen En las asignaturas como
DETERMINACIÓN DE LA ALCALINIDAD DE UN DESATASCADOR COMERCIAL AUTORÍA JOAQUÍN RUIZ MOLINA TEMÁTICA CIENCIAS EXPERIMENTALES, QUÍMICA ETAPA BACHILLERATO, FORMACIÓN PROFESIONAL Resumen En las asignaturas como
5) En 20 g de Ni 2 (CO 3 ) 3 : a) Cuántos moles hay de dicha sal? b) Cuántos átomos hay de oxígeno? c) Cuántos moles hay de iones carbonato?
 QUÍMICA 2º BACH. SELECTIVIDAD: MOL-N A 1) Para un mol de agua, justifique la veracidad o falsedad de las siguientes afirmaciones: a) En condiciones normales de presión y temperatura, ocupa un volumen de
QUÍMICA 2º BACH. SELECTIVIDAD: MOL-N A 1) Para un mol de agua, justifique la veracidad o falsedad de las siguientes afirmaciones: a) En condiciones normales de presión y temperatura, ocupa un volumen de
UNIDADES QUIMICAS. ING Roxsana M Romero A. Valencia, Febrero 2012
 UNIDADES QUIMICAS ING Roxsana M Romero A Valencia, Febrero 2012 1 UNIDADES QUIMICAS Otra forma de expresar las concentraciones es por métodos químicos, estos se diferencian de los métodos FÍSICOS porque
UNIDADES QUIMICAS ING Roxsana M Romero A Valencia, Febrero 2012 1 UNIDADES QUIMICAS Otra forma de expresar las concentraciones es por métodos químicos, estos se diferencian de los métodos FÍSICOS porque
DETERMINACIÓN EXPERIMENTAL DE LA DUREZA DEL AGUA DE ARMILLA UTILIZANDO UNA VALORACIÓN CON LA FORMACIÓN DE COMPLEJOS PARA 2º DE BACHILERATO
 DETERMINACIÓN EXPERIMENTAL DE LA DUREZA DEL AGUA DE ARMILLA UTILIZANDO UNA VALORACIÓN CON LA FORMACIÓN DE COMPLEJOS PARA 2º DE BACHILERATO AUTOR JAVIER RUIZ HIDALGO TEMÁTICA REACCIONES DE FORMACIÓN DE
DETERMINACIÓN EXPERIMENTAL DE LA DUREZA DEL AGUA DE ARMILLA UTILIZANDO UNA VALORACIÓN CON LA FORMACIÓN DE COMPLEJOS PARA 2º DE BACHILERATO AUTOR JAVIER RUIZ HIDALGO TEMÁTICA REACCIONES DE FORMACIÓN DE
GUÍA N 3 CONDUCTIVIDAD DE LAS DISOLUCIONES ELECTROLÍTICAS 2018-I
 GUÍA N 3 CONDUCTIVIDAD DE LAS DISOLUCIONES ELECTROLÍTICAS 2018-I Laboratorio N 3: Conductividad de las disoluciones electrolíticas. LABORATORIO DE FISICOQUÍMICA - UNIVERSIDAD TECNOLÓGICA DEL PERÚ LABORATORIO
GUÍA N 3 CONDUCTIVIDAD DE LAS DISOLUCIONES ELECTROLÍTICAS 2018-I Laboratorio N 3: Conductividad de las disoluciones electrolíticas. LABORATORIO DE FISICOQUÍMICA - UNIVERSIDAD TECNOLÓGICA DEL PERÚ LABORATORIO
Práctica 13. Equilibrios de solubilidad
 Práctica 13. Equilibrios de solubilidad ELABORADO POR: LAURA GASQUE SILVA ENUNCIADO A RESPONDER AL FINAL DE LA PRÁCTICA En sales poco solubles cuando el valor de (K ps /pk ps ), se (incrementa/disminuye),
Práctica 13. Equilibrios de solubilidad ELABORADO POR: LAURA GASQUE SILVA ENUNCIADO A RESPONDER AL FINAL DE LA PRÁCTICA En sales poco solubles cuando el valor de (K ps /pk ps ), se (incrementa/disminuye),
4.4. MOLES Y MOLÉCULAS.
 4.4. MOLES Y MOLÉCULAS. 4.4.1. MASA ATÓMICA Y MASA MOLECULAR Las moléculas están formadas por la unión de átomos que se unen mediante enlace químico. Esto significa que los átomos son difíciles de separar
4.4. MOLES Y MOLÉCULAS. 4.4.1. MASA ATÓMICA Y MASA MOLECULAR Las moléculas están formadas por la unión de átomos que se unen mediante enlace químico. Esto significa que los átomos son difíciles de separar
1. Ajusta la siguiente reacción: El cloro diatómico reacciona con el hidrógeno diatómico para formar cloruro de hidrógeno
 TEMA 4. CÁLCULOS QUÍMICOS ACTIVIDADES 1. Ajuste de ecuaciones químicas 1. Ajusta la siguiente reacción: El cloro diatómico reacciona con el hidrógeno diatómico para formar cloruro de hidrógeno 2. Ajusta
TEMA 4. CÁLCULOS QUÍMICOS ACTIVIDADES 1. Ajuste de ecuaciones químicas 1. Ajusta la siguiente reacción: El cloro diatómico reacciona con el hidrógeno diatómico para formar cloruro de hidrógeno 2. Ajusta
Universidad Iberoamericana
 Universidad Iberoamericana Ingeniería Química Laboratorio de Química General Grupo R Equipo 1 : Soluciones por Arlette Mayela Canut Noval y Francisco José Guerra Millán Prof. Celia Margarita del Valle
Universidad Iberoamericana Ingeniería Química Laboratorio de Química General Grupo R Equipo 1 : Soluciones por Arlette Mayela Canut Noval y Francisco José Guerra Millán Prof. Celia Margarita del Valle
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2000 QUÍMICA TEMA 1: LA TRANSFORMACIÓN QUÍMICA
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 000 QUÍMICA TEMA 1: LA TRANSFORMACIÓN QUÍMICA Junio, Ejercicio, Opción A Junio, Ejercicio 5, Opción A Reserva 1, Ejercicio, Opción A Reserva 1, Ejercicio 6, Opción
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 000 QUÍMICA TEMA 1: LA TRANSFORMACIÓN QUÍMICA Junio, Ejercicio, Opción A Junio, Ejercicio 5, Opción A Reserva 1, Ejercicio, Opción A Reserva 1, Ejercicio 6, Opción
1º Control 2ª Evaluación. Física y Química 1º Bachillerato D. 1.- (2 puntos) Formula o nombra los siguientes compuestos químicos:
 1º Control 2ª Evaluación Física y Química 1º Bachillerato D a) Seleniuro de hidrógeno; b) Yodato de cobre (II); c) Li 2 O 2; d) K 2 S; e) Na 3 PO 4 2. (2 puntos) a) Calcula los gramos de hidróxido potásico
1º Control 2ª Evaluación Física y Química 1º Bachillerato D a) Seleniuro de hidrógeno; b) Yodato de cobre (II); c) Li 2 O 2; d) K 2 S; e) Na 3 PO 4 2. (2 puntos) a) Calcula los gramos de hidróxido potásico
RECOPILADO POR: EL PROGRAMA UNIVERSITARIO DE ALIMENTOS
 NMX-F-321-S-1978. DETERMINACIÓN DE FÉCULA POR HIDRÓLISIS ÁCIDA EN EMBUTIDOS. DETERMINATION OF STARCH IN SAUSAGES BY ACID HIDROLISIS. NORMAS MEXICANAS. DIRECCIÓN GENERAL DE NORMAS. PREFACIO En la elaboración
NMX-F-321-S-1978. DETERMINACIÓN DE FÉCULA POR HIDRÓLISIS ÁCIDA EN EMBUTIDOS. DETERMINATION OF STARCH IN SAUSAGES BY ACID HIDROLISIS. NORMAS MEXICANAS. DIRECCIÓN GENERAL DE NORMAS. PREFACIO En la elaboración
Nombres de los integrantes: Práctica 6 Propiedades Físicas y Enlace Químico en Sólidos
 1 Nombres de los integrantes: Universidad Nacional Autónoma de México Facultad de Química Laboratorio de Química General I Grupo Equipo Práctica 6 Propiedades Físicas y Enlace Químico en Sólidos Problema
1 Nombres de los integrantes: Universidad Nacional Autónoma de México Facultad de Química Laboratorio de Química General I Grupo Equipo Práctica 6 Propiedades Físicas y Enlace Químico en Sólidos Problema
1atm OPCIÓN A. Solución:
 OPCIÓN A CUESTIÓN.- Si se preparan disoluciones 0,5 M de NH 3, NaCl, NaOH y NH Cl: a) Justifica de forma cualitativa cuál de ellas tendrá el ph más bajo. b) Elige de forma razonada una pareja que forme
OPCIÓN A CUESTIÓN.- Si se preparan disoluciones 0,5 M de NH 3, NaCl, NaOH y NH Cl: a) Justifica de forma cualitativa cuál de ellas tendrá el ph más bajo. b) Elige de forma razonada una pareja que forme
PRÁCTICA 2. PURIFICACIÓN DEL CLORURO DE SODIO (NaCl), POR EFECTO DEL ION COMÚN
 11 PRÁCTICA 2 PURIFICACIÓN DEL CLORURO DE SODIO (NaCl), POR EFECTO DEL ION COMÚN PROPÓSITO GENERAL I. El propósito general de esta práctica es ampliar en el estudiante sus conocimientos acerca de algunos
11 PRÁCTICA 2 PURIFICACIÓN DEL CLORURO DE SODIO (NaCl), POR EFECTO DEL ION COMÚN PROPÓSITO GENERAL I. El propósito general de esta práctica es ampliar en el estudiante sus conocimientos acerca de algunos
PRÁCTICA 15 CÁLCULO TEÓRICO Y EXPERIMENTAL DE ph DE DISOLUCIONES DE ÁCIDOS, BASES Y SALES. DISOLUCIONES REGULADORAS.
 PRÁCTICA 15 CÁLCULO TEÓRICO Y EXPERIMENTAL DE ph DE DISOLUCIONES DE ÁCIDOS, BASES Y SALES. DISOLUCIONES REGULADORAS. OBJETIVOS En esta práctica se tratarán aspectos de interés relacionados con los equilibrios
PRÁCTICA 15 CÁLCULO TEÓRICO Y EXPERIMENTAL DE ph DE DISOLUCIONES DE ÁCIDOS, BASES Y SALES. DISOLUCIONES REGULADORAS. OBJETIVOS En esta práctica se tratarán aspectos de interés relacionados con los equilibrios
DIVISIÓN DE INGENIERÍA MECATRÓNICA
 DIRECCIÓN ACADÉMICA DIVISIÓN DE INGENIERÍA MECATRÓNICA QUIMICA PRACTICA NO. NOMBRE DE LA RÁCTICA. GRUPO: EQUIPO: ALUMNOS: PRACTICA No. 4 REACCIONES QUÍMICA COMPETENCIA ESPECÍFICA: Diferenciar prácticamente
DIRECCIÓN ACADÉMICA DIVISIÓN DE INGENIERÍA MECATRÓNICA QUIMICA PRACTICA NO. NOMBRE DE LA RÁCTICA. GRUPO: EQUIPO: ALUMNOS: PRACTICA No. 4 REACCIONES QUÍMICA COMPETENCIA ESPECÍFICA: Diferenciar prácticamente
FÍSICA Y QUÍMICA Solucionario ÁCIDOS Y BASES
 FÍSICA Y QUÍMICA Solucionario ÁCIDOS Y BASES 1.* Calculad la molaridad de las siguientes disoluciones. a) Añadimos 3,6 moles de NaCl a 0,5 l de agua. 7 M b) Añadimos 2,5 moles de NaCl a 0,4 l de agua.
FÍSICA Y QUÍMICA Solucionario ÁCIDOS Y BASES 1.* Calculad la molaridad de las siguientes disoluciones. a) Añadimos 3,6 moles de NaCl a 0,5 l de agua. 7 M b) Añadimos 2,5 moles de NaCl a 0,4 l de agua.
PRACTICA No.8 ENLACE QUIMICO PROPIEDADES QUE GENERA
 ESCUELA DE QUÍMICA DEPARTAMENTO DE QUÍMICA GENERAL QUÍMICA GENERAL I PRACTICA No.8 ENLACE QUIMICO PROPIEDADES QUE GENERA 1. INTRODUCCION: Los elementos se enlazan para formar compuestos, este enlace se
ESCUELA DE QUÍMICA DEPARTAMENTO DE QUÍMICA GENERAL QUÍMICA GENERAL I PRACTICA No.8 ENLACE QUIMICO PROPIEDADES QUE GENERA 1. INTRODUCCION: Los elementos se enlazan para formar compuestos, este enlace se
OBTENCIÓN EXPERIMENTAL DEL NÚMERO DE AVOGADRO EMPLEANDO EL MÉTODO DE ELECTRODEPOSICIÓN CON PRIMERO DE BACHILLERATO
 OBTENCIÓN EXPERIMENTAL DEL NÚMERO DE AVOGADRO EMPLEANDO EL MÉTODO DE ELECTRODEPOSICIÓN CON PRIMERO DE BACHILLERATO AUTOR JAVIER RUIZ HIDALGO TEMÁTICA QUÍMICA GENERAL ETAPA BACHILLERATO Resumen En el presente
OBTENCIÓN EXPERIMENTAL DEL NÚMERO DE AVOGADRO EMPLEANDO EL MÉTODO DE ELECTRODEPOSICIÓN CON PRIMERO DE BACHILLERATO AUTOR JAVIER RUIZ HIDALGO TEMÁTICA QUÍMICA GENERAL ETAPA BACHILLERATO Resumen En el presente
FÍSICA Y QUÍMICA UNIDAD 4: LAS REACCIONES QUÍMICAS
 Física y Química 3º Curso Educación Secundaria Obligatoria Curso académico 2017/2018 1 FÍSICA Y QUÍMICA UNIDAD 4: LAS REACCIONES QUÍMICAS Física y Química 3º Curso Educación Secundaria Obligatoria Curso
Física y Química 3º Curso Educación Secundaria Obligatoria Curso académico 2017/2018 1 FÍSICA Y QUÍMICA UNIDAD 4: LAS REACCIONES QUÍMICAS Física y Química 3º Curso Educación Secundaria Obligatoria Curso
Estudia un día en la U.M.H.
 Estudia un día en la U.M.H. Buscando respuestas, resolviendo enigmas cuáles son las leyes que rigen los cambios de la Naturaleza? La Química en acción II Acerca del calor y del color: cambios que acompañan
Estudia un día en la U.M.H. Buscando respuestas, resolviendo enigmas cuáles son las leyes que rigen los cambios de la Naturaleza? La Química en acción II Acerca del calor y del color: cambios que acompañan
PRACTICA No.8 ENLACE QUIMICO PROPIEDADES QUE GENERA
 PRACTICA No.8 ENLACE QUIMICO PROPIEDADES QUE GENERA INTRODUCCION: Los elementos se enlazan para formar compuestos, este enlace se clasifica como: IONICO O ELECTROVALENTE, COVALENTE Y METALICO. La clase
PRACTICA No.8 ENLACE QUIMICO PROPIEDADES QUE GENERA INTRODUCCION: Los elementos se enlazan para formar compuestos, este enlace se clasifica como: IONICO O ELECTROVALENTE, COVALENTE Y METALICO. La clase
Reacciones Químicas. Que es una reacción química?
 Reacciones Químicas Tema 11 Química General Que es una reacción química? proceso en el cual un grupo de sustancias denominadas reactivos se trasforman en otro grupo denominados productos. Evidencia para
Reacciones Químicas Tema 11 Química General Que es una reacción química? proceso en el cual un grupo de sustancias denominadas reactivos se trasforman en otro grupo denominados productos. Evidencia para
Materia: es aquello que ocupa un lugar en el espacio y cuyas propiedades percibimos por los sentidos. Es diversa y discontinua.
 Sistemas materiales Materia: es aquello que ocupa un lugar en el espacio y cuyas propiedades percibimos por los sentidos. Es diversa y discontinua. Mezcla Heterogénea: unión de dos o más sustancias de
Sistemas materiales Materia: es aquello que ocupa un lugar en el espacio y cuyas propiedades percibimos por los sentidos. Es diversa y discontinua. Mezcla Heterogénea: unión de dos o más sustancias de
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2006 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2006 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE Junio, Ejercicio 4, Opción A Reserva 1, Ejercicio 6, Opción A Reserva 1, Ejercicio 4, Opción B Reserva 2, Ejercicio
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2006 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE Junio, Ejercicio 4, Opción A Reserva 1, Ejercicio 6, Opción A Reserva 1, Ejercicio 4, Opción B Reserva 2, Ejercicio
PRACTICA Nº 2 REACCIONES QUÍMICAS
 UNIVERSIDAD DR. RAFAEL BELLOSO CHACÍN FACULTAD DE INGENIERÍA LABORATORIO DE QUÍMICA Objetivo PRACTICA Nº 2 REACCIONES QUÍMICAS 1. Diferenciar los diversos tipos de reacciones químicas 2. Identificar el
UNIVERSIDAD DR. RAFAEL BELLOSO CHACÍN FACULTAD DE INGENIERÍA LABORATORIO DE QUÍMICA Objetivo PRACTICA Nº 2 REACCIONES QUÍMICAS 1. Diferenciar los diversos tipos de reacciones químicas 2. Identificar el
EJEMPLO DE ANÁLISIS POR RETROCESO: DETERMINACIÓN DEL SULFATO DE AMONIO PRESENTE EN UNA MUESTRA COMERCIAL
 ISSN 1988-607 DEP. EGA: GR 9/007 Nº 1 ENERO DE 008 EJEMPO DE ANÁISIS POR RETROCESO: DETERMINACIÓN DE SUFATO DE AMONIO PRESENTE EN UNA MUESTRA COMERCIA AUTORÍA JOAQUÍN RUIZ MOINA TEMÁTICA CIENCIAS EXPERIMENTAES,
ISSN 1988-607 DEP. EGA: GR 9/007 Nº 1 ENERO DE 008 EJEMPO DE ANÁISIS POR RETROCESO: DETERMINACIÓN DE SUFATO DE AMONIO PRESENTE EN UNA MUESTRA COMERCIA AUTORÍA JOAQUÍN RUIZ MOINA TEMÁTICA CIENCIAS EXPERIMENTAES,
Práctica 13. Equilibrios de solubilidad
 Práctica 13. Equilibrios de solubilidad ELABORADO POR: LAURA GASQUE SILVA ENUNCIADO A RESPONDER AL FINAL DE LA PRÁCTICA En sales poco solubles cuando el valor de (K ps /pk ps ), se (incrementa/disminuye),
Práctica 13. Equilibrios de solubilidad ELABORADO POR: LAURA GASQUE SILVA ENUNCIADO A RESPONDER AL FINAL DE LA PRÁCTICA En sales poco solubles cuando el valor de (K ps /pk ps ), se (incrementa/disminuye),
PROBLEMAS TIPO DE CÁLCULOS QUÍMICOS
 PROBLEMAS TIPO DE CÁLCULOS QUÍMICOS Átomos, moléculas y moles 1) Un tubo de ensayo contiene 25 ml de agua. Calcula: a) El número de moles de agua. b) El número total de átomos de hidrógeno. c) La masa
PROBLEMAS TIPO DE CÁLCULOS QUÍMICOS Átomos, moléculas y moles 1) Un tubo de ensayo contiene 25 ml de agua. Calcula: a) El número de moles de agua. b) El número total de átomos de hidrógeno. c) La masa
GUÍA DE EJERCICIOS DISOLUCIONES
 GUÍA DE EJERCICIOS DISOLUCIONES Área Química Resultados de aprendizaje Conocer el concepto de disolución y calcular la concentración de esta en ejercicios, de forma lógica. Contenidos 1. Definición de
GUÍA DE EJERCICIOS DISOLUCIONES Área Química Resultados de aprendizaje Conocer el concepto de disolución y calcular la concentración de esta en ejercicios, de forma lógica. Contenidos 1. Definición de
Nombre Grupo. Unidad 6 Ácido-base
 Nombre Grupo OPCIÓN A Unidad 6 Ácido-base 1. (2 p) a) Calcule el ph de una disolución 0.1 M de hidróxido potásico. El hidróxido potásico, como base fuerte que es, está completamente disociada en disolución
Nombre Grupo OPCIÓN A Unidad 6 Ácido-base 1. (2 p) a) Calcule el ph de una disolución 0.1 M de hidróxido potásico. El hidróxido potásico, como base fuerte que es, está completamente disociada en disolución
INSTITUTO SUPERIOR DE CIENCIA Y TECNOLOGÍA ISCYT PROGRAMA DE ASIGNATURA POR COMPETENCIA FUNDAMENTO DEL CURRÍCULUM
 INSTITUTO SUPERIOR DE CIENCIA Y TECNOLOGÍA ISCYT PROGRAMA DE ASIGNATURA POR COMPETENCIA FUNDAMENTO DEL CURRÍCULUM FUNDAMENTACIÓN La asignatura se centra en el estudio del currículo escolar, entendiendo
INSTITUTO SUPERIOR DE CIENCIA Y TECNOLOGÍA ISCYT PROGRAMA DE ASIGNATURA POR COMPETENCIA FUNDAMENTO DEL CURRÍCULUM FUNDAMENTACIÓN La asignatura se centra en el estudio del currículo escolar, entendiendo
La reacción química (Segunda parte)
 La reacción química (Segunda parte) Problemas 1. Cuáles son los productos de las reacciones químicas involucradas? 2. Cómo se expresan estos procesos mediante ecuaciones químicas? 3. Cómo se pueden clasificar
La reacción química (Segunda parte) Problemas 1. Cuáles son los productos de las reacciones químicas involucradas? 2. Cómo se expresan estos procesos mediante ecuaciones químicas? 3. Cómo se pueden clasificar
Tarea Previa 1. Qué es un enlace químico? 2. Investiga las características de los siguientes tipos de enlace químico: Iónico. Covalente molecular
 Equipo: Nombre: Nombre: Nombre: Práctica 6: Propiedades Físicas y Enlace Químico en Sólidos Problema 1 Cómo son los puntos de fusión y la solubilidad de sustancias cuya estructura se mantiene por diferentes
Equipo: Nombre: Nombre: Nombre: Práctica 6: Propiedades Físicas y Enlace Químico en Sólidos Problema 1 Cómo son los puntos de fusión y la solubilidad de sustancias cuya estructura se mantiene por diferentes
TRANSFERENCIA DE PROTONES. CUESTIONES Y PROBLEMAS. E1B.S2009 Para las especies CN, HF y CO 3
 TRANSFERENCIA DE PROTONES. CUESTIONES Y PROBLEMAS. E1B.S2009 Para las especies CN, HF y CO 3 2, en disolución acuosa: a.- Escriba, según corresponda, la fórmula del ácido o de la base conjugados. b.- Justifique,
TRANSFERENCIA DE PROTONES. CUESTIONES Y PROBLEMAS. E1B.S2009 Para las especies CN, HF y CO 3 2, en disolución acuosa: a.- Escriba, según corresponda, la fórmula del ácido o de la base conjugados. b.- Justifique,
JUNIO FASE GENERAL QUÍMICA. OPCIÓN A
 JUNIO 2011. FASE GENERAL 1. (2,5 puntos) QUÍMICA. OPCIÓN A La nitroglicerina, C 3 H 5 N 3 O 9 (l), descompone a 1 atm y 25 ºC para formar N 2 (g), CO 2 (g), H 2 O(l) y O 2 (g), desprendiendo 1541,4 kj/mol
JUNIO 2011. FASE GENERAL 1. (2,5 puntos) QUÍMICA. OPCIÓN A La nitroglicerina, C 3 H 5 N 3 O 9 (l), descompone a 1 atm y 25 ºC para formar N 2 (g), CO 2 (g), H 2 O(l) y O 2 (g), desprendiendo 1541,4 kj/mol
QUÍMICA. Br (g) [ΔH afinidad Br(g)] = - 324,6 kj mol - (0,25 puntos) ½ [ΔH D Br 2 (g)] = 1 96,5 kj mol -1 Na + (g) + Br - (g)
![QUÍMICA. Br (g) [ΔH afinidad Br(g)] = - 324,6 kj mol - (0,25 puntos) ½ [ΔH D Br 2 (g)] = 1 96,5 kj mol -1 Na + (g) + Br - (g) QUÍMICA. Br (g) [ΔH afinidad Br(g)] = - 324,6 kj mol - (0,25 puntos) ½ [ΔH D Br 2 (g)] = 1 96,5 kj mol -1 Na + (g) + Br - (g)](/thumbs/76/73887985.jpg) OPCIÓN A QUÍMICA 1. (2,5 puntos) Construya el ciclo de Born-Haber para la formación del NaBr(s), a partir de bromo líquido y sodio metálico, y calcule la energía de red (ΔH red ) del compuesto, a partir
OPCIÓN A QUÍMICA 1. (2,5 puntos) Construya el ciclo de Born-Haber para la formación del NaBr(s), a partir de bromo líquido y sodio metálico, y calcule la energía de red (ΔH red ) del compuesto, a partir
PROPIEDADES ÁCIDO BASE DE LAS SALES: HIDRÓLISIS
 IV 1 PRÁCTICA 4 PROPIEDADES ÁCIDO BASE DE LAS SALES: HIDRÓLISIS En esta práctica mediremos el ph (carácter ácido, básico o neutro de disoluciones acuosas de diversas sales, y comprobaremos que estas disoluciones
IV 1 PRÁCTICA 4 PROPIEDADES ÁCIDO BASE DE LAS SALES: HIDRÓLISIS En esta práctica mediremos el ph (carácter ácido, básico o neutro de disoluciones acuosas de diversas sales, y comprobaremos que estas disoluciones
PROBLEMARIO (Solubilidad)
 PROBLEMARIO (Solubilidad) 1. Una disolución saturada de fosfato de plata, Ag 3 PO 4, contiene 3.4X10 5 moles por litro de ion fosfato (s de PO 4 3- = 3.4X10 5 ). Calcula el producto de solubilidad de dicha
PROBLEMARIO (Solubilidad) 1. Una disolución saturada de fosfato de plata, Ag 3 PO 4, contiene 3.4X10 5 moles por litro de ion fosfato (s de PO 4 3- = 3.4X10 5 ). Calcula el producto de solubilidad de dicha
Método de las tangentes para la determinación del punto final en valoraciones potenciométricas
 Método de las tangentes para la determinación del punto final en valoraciones potenciométricas Apellidos, nombre Muñoz Portero, María José (mjmunoz@iqn.upv.es) Departamento Centro Ingeniería Química y
Método de las tangentes para la determinación del punto final en valoraciones potenciométricas Apellidos, nombre Muñoz Portero, María José (mjmunoz@iqn.upv.es) Departamento Centro Ingeniería Química y
FACULTAD DE CIENCIAS NATURALES EXACTAS Y DE LA EDUCACIÓN DEPARTAMENTO DE QUÍMICA BIORGÁNICA
 FACULTAD DE CIENCIAS NATURALES EXACTAS Y DE LA EDUCACIÓN DEPARTAMENTO DE QUÍMICA BIORGÁNICA PRÁCTICA 3: PRUEBAS GENERALES PARA AMINOÁCIDOS Los aminoácidos constituyentes de las proteínas, contienen además
FACULTAD DE CIENCIAS NATURALES EXACTAS Y DE LA EDUCACIÓN DEPARTAMENTO DE QUÍMICA BIORGÁNICA PRÁCTICA 3: PRUEBAS GENERALES PARA AMINOÁCIDOS Los aminoácidos constituyentes de las proteínas, contienen además
Determinación del contenido de carbonato de calcio (CaCO 3 ) en una muestra comercial
 Determinación del contenido de carbonato de calcio (CaCO 3 ) en una muestra comercial Autores: Olivia Zamora Martínez y Alberto Colín Segundo Revisores 1. INTRODUCCIÓN Los equilibrios ácido-base son bastante
Determinación del contenido de carbonato de calcio (CaCO 3 ) en una muestra comercial Autores: Olivia Zamora Martínez y Alberto Colín Segundo Revisores 1. INTRODUCCIÓN Los equilibrios ácido-base son bastante
CH 4 (g) + 2O 2 (g) CO 2 (g) + 2H 2 O(g)
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS, CUM UNIDAD DIDÁCTICA DE QUÍMICA, PRIMER AÑO PRÁCTICAS DE LABORATORIO 2014 SEMANA 4 REACCIONES QUÍMICAS Elaborado por: Licda. Bárbara
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS, CUM UNIDAD DIDÁCTICA DE QUÍMICA, PRIMER AÑO PRÁCTICAS DE LABORATORIO 2014 SEMANA 4 REACCIONES QUÍMICAS Elaborado por: Licda. Bárbara
Nombres de los integrantes: Práctica 12 Preparación de disoluciones
 Nombres de los integrantes: 1 Universidad Nacional Autónoma de México Facultad de Química Laboratorio de Química General I Grupo Equipo Práctica 12 Preparación de disoluciones Problemas: 1. Preparar 50mL
Nombres de los integrantes: 1 Universidad Nacional Autónoma de México Facultad de Química Laboratorio de Química General I Grupo Equipo Práctica 12 Preparación de disoluciones Problemas: 1. Preparar 50mL
ESTRUCTURA QUÍMICA DE LAS ZEOLITAS ASÍ COMO SUS APLICACIONES INDUSTRIALES
 ESTRUCTURA QUÍMICA DE LAS ZEOLITAS ASÍ COMO SUS APLICACIONES INDUSTRIALES AUTOR JAVIER RUIZ HIDALGO TEMÁTICA ENLACE QUÍMICO ETAPA BACHILLERATO Resumen En este trabajo pretendo mostrar una serie de estructuras
ESTRUCTURA QUÍMICA DE LAS ZEOLITAS ASÍ COMO SUS APLICACIONES INDUSTRIALES AUTOR JAVIER RUIZ HIDALGO TEMÁTICA ENLACE QUÍMICO ETAPA BACHILLERATO Resumen En este trabajo pretendo mostrar una serie de estructuras
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2009 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 009 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE Junio, Ejercicio, Opción A Junio, Ejercicio 5, Opción B Reserva 1, Ejercicio 5, Opción A Reserva 1, Ejercicio 4, Opción
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 009 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE Junio, Ejercicio, Opción A Junio, Ejercicio 5, Opción B Reserva 1, Ejercicio 5, Opción A Reserva 1, Ejercicio 4, Opción
 REACCIONES DE TRANSFERENCIA DE PROTONES 1.-junio 1997 a) El ph de una disolución 0.2 M de ácido fórmico (ácido metanoico) cuya K a = 10-4 b) El ph y el grado de disociación del ácido fórmico cuando a 40
REACCIONES DE TRANSFERENCIA DE PROTONES 1.-junio 1997 a) El ph de una disolución 0.2 M de ácido fórmico (ácido metanoico) cuya K a = 10-4 b) El ph y el grado de disociación del ácido fórmico cuando a 40
