oluciones del apartado «Resuelve problemas»
|
|
|
- María Jesús Poblete Miranda
- hace 5 años
- Vistas:
Transcripción
1 S oluciones del apartado «Resuelve problemas» Pág Un café con azúcar es una mezcla homogénea o heterogénea? Es una disolución de sólidos (café y azúcar) en agua. 20 Un material formado por moléculas iguales que pueden descomponerse por procedimientos químicos en dos o más elementos, qué clase de material es? Un compuesto. 21 Un clavo de hierro puro: a) Es un elemento o un compuesto? b) Es una sustancia o una mezcla? Explícalo. a) Un elemento. b) Es una sustancia, pues si se trata de hierro puro todas sus partículas son iguales (átomos de hierro). 22 Un caramelo de azúcar pura: a) Es un compuesto o un elemento? b) Es una sustancia o una mezcla? Explícalo. a) Un compuesto. b) Se trata de una sustancia, pues todas sus partículas son iguales (moléculas de glucosa). 23 Si dos líquidos son inmiscibles, cómo podemos separarlos? Haz un dibujo indicando el proceso. Por decantación. El dibujo deberá ser similar a la siguiente fotografía: 24 Necesitamos un poco de agua limpia para preparar una disolución, pero solo disponemos de agua embarrada procedente de un charco. Qué podemos hacer? Podemos destilarla.
2 Pág Cómo nos las arreglaríamos para obtener oxígeno puro a partir del aire? Es el aire una mezcla heterogénea o una disolución? Primero se licua, a altas presiones, y después se separan sus componentes por destilación. 26 Nos dan un frasco que contiene un líquido incoloro que parece agua. Idea un procedimiento experimental para demostrar si es una sustancia pura o una disolución. El procedimiento podría ser: En primer lugar, oler (con mucho cuidado) para descartar que pueda tratarse de algún líquido incoloro, como alcohol, éter, etc. Si se dispone de un densímetro, obtener la densidad del líquido, y, si es próxima a 1 kg/m 3, deducir que podría ser agua con algo disuelto. Después, calentar muy suavemente; si aparecen burbujas implica que contiene algún gas en disolución. Seguir calentando, y si contiene cualquier otro líquido disuelto se desprenderán vapores. Si hierve a una temperatura próxima a 100 C implica que es agua, y si lo hace a una temperatura superior a 100 C puede ser agua con alguna sustancia sólida disuelta. 27 Hemos mezclado 10 cm 3 de amoniaco (NH 3 ), 3 g de carbonato sódico (Na 2 CO 3 ) y 28 g de cloruro potásico (KCl) con medio litro de agua. Indica cuáles son los solutos y cuál el disolvente. El disolvente es el agua, y el resto son los solutos. 28 Tenemos en el laboratorio un líquido transparente de color amarillo. Se ha sometido a centrifugación y no se ha formado poso alguno. Se ha filtrado y no ha cambiado de color ni dejó rastro sobre el papel. Al evaporarlo a sequedad dejó un polvillo de color amarillo intenso. Se trata de una mezcla o una disolución? Por qué? Una mezcla homogénea, pues hemos conseguido separar sus sustancias por métodos térmicos. 29 El hecho de agitar una disolución aumenta la solubilidad del soluto? Y si calentamos la disolución? Razónalo. La solubilidad no aumenta al agitar la disolución, pero sí al calentarla, pues depende de la temperatura.
3 Pág Qué podría ocurrir si bebemos una cantidad apreciable de agua destilada? Sufriríamos trastornos porque el agua potable debe contener una serie de sales disueltas, para así parecerse a nuestra sangre (en cuanto a concentración de sustancias disueltas). 31 Si metemos dos botellas iguales en el congelador del frigorífico, una con agua y otra con vino, cuál congelará antes? Por qué? El agua, pues el vino es una disolución y congela a menor temperatura que el disolvente puro (descenso crioscópico). 32 A partir de los datos de la gráfica siguiente, calcula: a) La cantidad de nitrato de sodio (NaNO 3 ) que se podrá disolver en 275 cm 3 de agua, a 30 C. b) Las cantidades aproximadas de bromuro potásico (KBr) que podrías añadir a un litro de agua a 70 C, para lograr una disolución diluida, otra concentrada y otra saturada. Concentración (g de soluto en 100 g de H 2 O) NaNO 3 KBr Temperatura (ºC) a) A 30 C, podemos disolver 95 g de nitrato de sodio en 100 g de agua. Por tanto, en 275 g de agua podremos disolver 2,75 veces esta cantidad, es decir, 261,25 g de nitrato de sodio. b) A 70 C, la solubilidad del bromuro de potasio es 90 g por cada 100 g de agua. Si queremos saturar un litro de agua tendremos que añadir, por tanto, 900 g de bromuro. Una disolución diluida contendría cantidades muy pequeñas, menores de 1 g. Todas las disoluciones hechas con cantidades intermedias de bromuro de potasio serían concentradas.
4 Pág Si disolvemos 40 cm 3 de glicerina en medio litro de agua y se forman 540 cm 3 de disolución, cuál será su porcentaje en volumen? Qué volumen de glicerina habrá en 2,75 L de disolución? El porcentaje en volumen de la disolución será: V 40 cm % en volumen = 100 = 3 soluto (cm 3 ) de glicerina 100 = 7,4% V 540 cm 3 disolución (cm 3 ) de disolución Y el volumen de glicerina en 2,75 L de disolución lo obtenemos a partir del tanto por ciento en volumen de la disolución: 100 cm 3 de disolución 7,4 cm 3 de glicerina x L de glicerina = = 7,4 cm 3 2,75 L 100 cm 3 2,75 L de disolución x L de glicerina = 0,2 L de glicerina 34 Calcula la riqueza, en tanto por ciento en masa, de una disolución formada por 20 gramos de nitrato de sodio (NaNO 3 ) y 300 cm 3 de agua. m soluto (g) 20 g de NaNO 3 % en masa = 100 = 100 = 6,25% m disolución (g) 320 g de disolución 35 Se prepara una disolución añadiendo 10 gramos de cloruro de sodio (NaCl) a 20 g de agua. Una vez disuelta, el volumen de la disolución es de 22 cm 3. Calcula la concentración de la disolución expresada en tanto por ciento en masa. m soluto (g) 10 g de NaCl % en masa = 100 = 100 = 33,33% m disolución (g) 30 g de disolución 36 Qué cantidad de azúcar contendrá 1,5 litros de disolución al 20% en masa? Dato: La densidad de la disolución es 1,2 g/cm 3. Calculamos, en primer lugar, la masa de la disolución: m = V d = 1500 cm 3 1,2 g/cm 3 = g Con este dato ya podemos calcular la masa de soluto: 100 g de disolución 20 g de azúcar x g de azúcar = = 20 g g 100 g g de disolución x g de azúcar = 360 g de azúcar
5 Pág Hemos disuelto 5 moles de sulfato potásico (K 2 ) en agua hasta formar 3 litros de disolución. Calcula: a) La concentración de la disolución. b)el volumen de disolución que habrá que tomar para que en él haya 0,2 moles de sal. n soluto (mol) 5 mol de K a) Concentración (mol/l) = = 2 = 1,67 mol/l V disolución (L) 3 L de disolución n soluto (mol) 0,2 mol de K b) V disolución (L) = = 2 = 0,12 L Concentración (mol/l) 1,67 mol/l
Materia: es aquello que ocupa un lugar en el espacio y cuyas propiedades percibimos por los sentidos. Es diversa y discontinua.
 Sistemas materiales Materia: es aquello que ocupa un lugar en el espacio y cuyas propiedades percibimos por los sentidos. Es diversa y discontinua. Mezcla Heterogénea: unión de dos o más sustancias de
Sistemas materiales Materia: es aquello que ocupa un lugar en el espacio y cuyas propiedades percibimos por los sentidos. Es diversa y discontinua. Mezcla Heterogénea: unión de dos o más sustancias de
Tema 4: Sustancias puras y mezclas
 Tema 4: Sustancias puras y mezclas Esquema de trabajo: 1. Sustancias puras: Tipos: elementos y compuestos. 2. Mezclas: Tipos: Homogénea y heterogénea 3. Disoluciones Concepto Componentes Tipos de disoluciones
Tema 4: Sustancias puras y mezclas Esquema de trabajo: 1. Sustancias puras: Tipos: elementos y compuestos. 2. Mezclas: Tipos: Homogénea y heterogénea 3. Disoluciones Concepto Componentes Tipos de disoluciones
MEZCLAS Y DISOLUCIONES - CUESTIONES Y EJERCICIOS
 MEZCLAS Y DISOLUCIONES - CUESTIONES Y EJERCICIOS Concentración de una disolución 1º.- Calcula la masa de nitrato de hierro (II), Fe(NO 3 ) 2, existente en 100 ml de disolución acuosa al 6 % en masa. Dato:
MEZCLAS Y DISOLUCIONES - CUESTIONES Y EJERCICIOS Concentración de una disolución 1º.- Calcula la masa de nitrato de hierro (II), Fe(NO 3 ) 2, existente en 100 ml de disolución acuosa al 6 % en masa. Dato:
MEZCLAS Y DISOLUCIONES. Física y Química 3º de E.S.O. IES Isidra de Guzmán
 MEZCLAS Y DISOLUCIONES Física y Química 3º de E.S.O. IES Isidra de Guzmán Introducción Ya sabes que los sistemas materiales se pueden clasificar según su composición en sustancias puras y mezclas. Las
MEZCLAS Y DISOLUCIONES Física y Química 3º de E.S.O. IES Isidra de Guzmán Introducción Ya sabes que los sistemas materiales se pueden clasificar según su composición en sustancias puras y mezclas. Las
DISOLUCIONES. Líquido (H 2 O)
 DISOLUCIONES Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos a más sustancias. En las disoluciones hay que distinguir el soluto, el disolvente y la
DISOLUCIONES Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos a más sustancias. En las disoluciones hay que distinguir el soluto, el disolvente y la
03 DISOLUCIONES. 2 Observando la curva de solubilidad del clorato potásico, responder:
 03 DISOLUCIONES 1 Sabemos que cierta disolución tiene una concentración de c = 512 g/l. Si su densidad es1,43 g/l, expresa el valor de su concentración en tanto por ciento. 2 Observando la curva de solubilidad
03 DISOLUCIONES 1 Sabemos que cierta disolución tiene una concentración de c = 512 g/l. Si su densidad es1,43 g/l, expresa el valor de su concentración en tanto por ciento. 2 Observando la curva de solubilidad
Tema 7. Las mezclas. Introducción
 Tema 7. Las mezclas Introducción Ya sabes que los sistemas materiales se pueden clasificar según su composición en sustancias puras y mezclas. Las sustancias puras son los elementos y los compuestos que
Tema 7. Las mezclas Introducción Ya sabes que los sistemas materiales se pueden clasificar según su composición en sustancias puras y mezclas. Las sustancias puras son los elementos y los compuestos que
TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS
 TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS 1. LA MATERIA Y SU ASPECTO Los sistemas materiales, formados por una o varias sustancias, pueden clasificarse en: - Sistemas materiales heterogéneos: presentan
TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS 1. LA MATERIA Y SU ASPECTO Los sistemas materiales, formados por una o varias sustancias, pueden clasificarse en: - Sistemas materiales heterogéneos: presentan
Apuntes Disoluciones
 Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos a más sustancias. En las disoluciones hay que distinguir el soluto, el disolvente y la propia disolución
Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos a más sustancias. En las disoluciones hay que distinguir el soluto, el disolvente y la propia disolución
TEMA Nº 7. DIVERSIDAD DE LA MATERIA
 TEMA Nº 7. DIVERSIDAD DE LA MATERIA 1.- La materia se constituye de: a) Sustancias puras. b) Mezclas. Define cada uno de los componentes de la materia. Respuesta: a) Sustancia pura.- Está formada por partículas
TEMA Nº 7. DIVERSIDAD DE LA MATERIA 1.- La materia se constituye de: a) Sustancias puras. b) Mezclas. Define cada uno de los componentes de la materia. Respuesta: a) Sustancia pura.- Está formada por partículas
SOLUCIONES SOLIDA LIQUIDA GASEOSA. mezclas homogéneas de dos sustancias: SEGÚN EL ESTADO FISICO DEL SOLVENTE
 Soluciones SOLUCIONES mezclas homogéneas de dos sustancias: SOLUTO SOLVENTE SEGÚN EL ESTADO FISICO DEL SOLVENTE SOLIDA LIQUIDA GASEOSA Cuando un sólido se disuelve en un líquido las partículas que lo
Soluciones SOLUCIONES mezclas homogéneas de dos sustancias: SOLUTO SOLVENTE SEGÚN EL ESTADO FISICO DEL SOLVENTE SOLIDA LIQUIDA GASEOSA Cuando un sólido se disuelve en un líquido las partículas que lo
1. a) Define Sustancia pura: Es aquella que tiene la misma composición y las mismas propiedades. b) Define Disolución: Es una mezcla homogénea.
 Tema 3. LA MATERIA Y SU ASPECTO MEZCLAS Y SUSTANCIAS PURAS 1. a) Define Sustancia pura: Es aquella que tiene la misma composición y las mismas propiedades. b) Define Disolución: Es una mezcla homogénea.
Tema 3. LA MATERIA Y SU ASPECTO MEZCLAS Y SUSTANCIAS PURAS 1. a) Define Sustancia pura: Es aquella que tiene la misma composición y las mismas propiedades. b) Define Disolución: Es una mezcla homogénea.
PROBLEMAS MEZCLAS Y DISOLUCIONES
 PROBLEMAS MEZCLAS Y DISOLUCIONES 1. Clasifica como homogéneos o heterogéneos los siguientes sistemas materiales: un trozo de cobre, agua salada, hierro oxidado, una ensalada. 2. Al mezclar dos sistemas
PROBLEMAS MEZCLAS Y DISOLUCIONES 1. Clasifica como homogéneos o heterogéneos los siguientes sistemas materiales: un trozo de cobre, agua salada, hierro oxidado, una ensalada. 2. Al mezclar dos sistemas
SUSTANCIAS PURAS (Repaso) MEZCLAS (Repaso)
 Física y Química 4 ESO DISOLUCIONES Pág. 1 SUSTANCIAS PURAS (Repaso) MEZCLAS (Repaso) Pág. 2 DISOLUCIONES Física y Química 4 ESO DISOLUCIONES CONCEPTO DE DISOLUCIÓN. COMPONENTES DE UNA DISOLUCIÓN. Una
Física y Química 4 ESO DISOLUCIONES Pág. 1 SUSTANCIAS PURAS (Repaso) MEZCLAS (Repaso) Pág. 2 DISOLUCIONES Física y Química 4 ESO DISOLUCIONES CONCEPTO DE DISOLUCIÓN. COMPONENTES DE UNA DISOLUCIÓN. Una
FyQ 1. IES de Castuera Bloque 2 Aspectos Cuantitativos de la Química Unidad Didáctica 2
 Física y Química 1º Bachillerato LOMCE FyQ 1 IES de Castuera Bloque 2 Aspectos Cuantitativos de la Química 2015 2016 Unidad Didáctica 2 Rev 01 Las Disoluciones. Métodos Actuales para el Análisis de Sustancias
Física y Química 1º Bachillerato LOMCE FyQ 1 IES de Castuera Bloque 2 Aspectos Cuantitativos de la Química 2015 2016 Unidad Didáctica 2 Rev 01 Las Disoluciones. Métodos Actuales para el Análisis de Sustancias
TEMA 13: LA MATERIA, BASE DEL UNIVERSO
 TEMA 13: LA MATERIA, BASE DEL UNIVERSO Qué es materia? Materia es todo aquello que posee masa y ocupa un volumen. Está formada de partículas muy pequeñas llamadas átomos. La masa y el volumen se consideran
TEMA 13: LA MATERIA, BASE DEL UNIVERSO Qué es materia? Materia es todo aquello que posee masa y ocupa un volumen. Está formada de partículas muy pequeñas llamadas átomos. La masa y el volumen se consideran
TEMA 2: LA MATERIA: CÓMO SE PRESENTA?
 TEMA 2: LA MATERIA: CÓMO SE PRESENTA? 1.- La materia: sustancias puras y mezclas. 1.1.- Recordatorio. 1.2.- Sustancias puras. 1.3.- Mezclas. 1.4.- Cómo distinguir un coloide de una mezcla homogénea. 2.-
TEMA 2: LA MATERIA: CÓMO SE PRESENTA? 1.- La materia: sustancias puras y mezclas. 1.1.- Recordatorio. 1.2.- Sustancias puras. 1.3.- Mezclas. 1.4.- Cómo distinguir un coloide de una mezcla homogénea. 2.-
1. MATERIA Y SU ASPECTO
 1. MATERIA Y SU ASPECTO El aspecto de un sistema material puede variar según el método de observación. Algunos sistemas materiales como la leche, la sangre o la mantequilla a simple vista parecen uniformes,
1. MATERIA Y SU ASPECTO El aspecto de un sistema material puede variar según el método de observación. Algunos sistemas materiales como la leche, la sangre o la mantequilla a simple vista parecen uniformes,
La materia se puede definir como todo aquello que tiene masa y ocupa un volumen.
 Tema 2: LA MATERIA Que es la materia? La materia se puede definir como todo aquello que tiene masa y ocupa un volumen. Clasificación de la materia (criterio: separación) Mezclas Sustancias puras Composición
Tema 2: LA MATERIA Que es la materia? La materia se puede definir como todo aquello que tiene masa y ocupa un volumen. Clasificación de la materia (criterio: separación) Mezclas Sustancias puras Composición
2.-. Realiza los siguientes cambios de unidades, expresando el resultado en notación científica: b. 0,2 l a cm3. m s a km f. 1500
 Curso 3º ESO Asignatura: FÍSICA Y QUÍMICA Alumn@: Curso: La resolución de estas actividades debe ser individual, y nunca copia de otro/a compañero/a. 1. Asocia cada cantidad con su magnitud indicando el
Curso 3º ESO Asignatura: FÍSICA Y QUÍMICA Alumn@: Curso: La resolución de estas actividades debe ser individual, y nunca copia de otro/a compañero/a. 1. Asocia cada cantidad con su magnitud indicando el
Acuerdo 286. Química. Disoluciones. Recopiló: M.C. Macaria Hernández Chávez
 Acuerdo 286 Química Disoluciones Recopiló: M.C. Macaria Hernández Chávez Disolución: Es una mezcla homogénea de dos o más sustancias. La sustancia que se encuentra en mayor proporción se llama disolvente
Acuerdo 286 Química Disoluciones Recopiló: M.C. Macaria Hernández Chávez Disolución: Es una mezcla homogénea de dos o más sustancias. La sustancia que se encuentra en mayor proporción se llama disolvente
Materia: FÍSICA Y QUÍMICA 3º E.S.O Curso
 ACTIVIDADES FÍSICA Y QUÍMICA 3º ESO PROGRAMA DE REFUERZO. PRIMERA PARTE 1.-Calcular el tanto por ciento en peso y en volumen de una disolución que se prepara al disolver 40 ml de ácido nítrico cuya densidad
ACTIVIDADES FÍSICA Y QUÍMICA 3º ESO PROGRAMA DE REFUERZO. PRIMERA PARTE 1.-Calcular el tanto por ciento en peso y en volumen de una disolución que se prepara al disolver 40 ml de ácido nítrico cuya densidad
So S l o u l c u i c o i n o e n s e
 Soluciones SOLUCIONES mezclas homogéneas de dos sustancias: SOLUTO SOLVENTE SEGÚN EL ESTADO FISICO DEL SOLVENTE SOLIDA LIQUIDA GASEOSA Cuando un sólido se disuelve en un líquido las partículas que lo
Soluciones SOLUCIONES mezclas homogéneas de dos sustancias: SOLUTO SOLVENTE SEGÚN EL ESTADO FISICO DEL SOLVENTE SOLIDA LIQUIDA GASEOSA Cuando un sólido se disuelve en un líquido las partículas que lo
SISTEMAS MATERIALES. Departamento de Física y Química 2º ESO
 SISTEMAS MATERIALES Departamento de Física y Química 2º ESO 0. Mapa conceptual MATERIA Sustancias puras Mezclas Heterogéneas Homogéneas Sistemas coloidales Técnicas de separación Disoluciones Soluto Disolvente
SISTEMAS MATERIALES Departamento de Física y Química 2º ESO 0. Mapa conceptual MATERIA Sustancias puras Mezclas Heterogéneas Homogéneas Sistemas coloidales Técnicas de separación Disoluciones Soluto Disolvente
Todo lo que vemos es materia
 Todo lo que vemos es materia CLASIFICACIÓN DE LA MATERIA La materia se presenta en la naturaleza en forma de sustancias puras y mezclas, de modo que podemos establecer la siguiente clasificación: CLASIFICACIÓN
Todo lo que vemos es materia CLASIFICACIÓN DE LA MATERIA La materia se presenta en la naturaleza en forma de sustancias puras y mezclas, de modo que podemos establecer la siguiente clasificación: CLASIFICACIÓN
CLASIFICACIÓN DE LA MATERIA
 1. Clasificación de la materia por su aspecto CLASIFICACIÓN DE LA MATERIA La materia homogénea es la que presenta un aspecto uniforme, en la cual no se pueden distinguir a simple vista sus componentes.
1. Clasificación de la materia por su aspecto CLASIFICACIÓN DE LA MATERIA La materia homogénea es la que presenta un aspecto uniforme, en la cual no se pueden distinguir a simple vista sus componentes.
DISOLUCIONES. Líquido (H 2 O)
 DISOLUCIONES IES La Magdalena. Avilés. Asturias Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos a más sustancias. En las disoluciones hay que distinguir
DISOLUCIONES IES La Magdalena. Avilés. Asturias Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos a más sustancias. En las disoluciones hay que distinguir
Física 4º E.S.O. 2014/15
 Física 4º E.S.O. 2014/15 Problemas de Química Ficha número 13 1.- Ajusta las siguientes reacciones químicas: a) Na 2 CO 3 + HCl NaCl + CO 2 + H 2 O (Sol: Na 2 CO 3 + 2 HCl 2 NaCl + CO 2 + H 2 O) b) PBr
Física 4º E.S.O. 2014/15 Problemas de Química Ficha número 13 1.- Ajusta las siguientes reacciones químicas: a) Na 2 CO 3 + HCl NaCl + CO 2 + H 2 O (Sol: Na 2 CO 3 + 2 HCl 2 NaCl + CO 2 + H 2 O) b) PBr
INTRUCCIONES PARA LA RECUPERACIÓN
 INTRUCCIONES PARA LA RECUPERACIÓN Se entrega una relación de actividades. Dichas actividades deberán ser entregadas antes de la fecha límite de entrega, pudiéndose ser consultado el profesor cuantas veces
INTRUCCIONES PARA LA RECUPERACIÓN Se entrega una relación de actividades. Dichas actividades deberán ser entregadas antes de la fecha límite de entrega, pudiéndose ser consultado el profesor cuantas veces
d (g/cm 3 ) d (kg/l) Masa Volumen a) Un kilogramo de etanol ocupa más volumen que un kilogramo de acetona.
 La materia. Los líquidos Ficha de trabajo 1 Nombre y apellidos:... Curso:... Fecha: La densidad de los líquidos El líquido más abundante es el agua, cuya densidad es de 1 kg/l; debido a ello, estamos habituados
La materia. Los líquidos Ficha de trabajo 1 Nombre y apellidos:... Curso:... Fecha: La densidad de los líquidos El líquido más abundante es el agua, cuya densidad es de 1 kg/l; debido a ello, estamos habituados
Si un cuerpo tiene una masa muy grande, su densidad tiene que ser necesariamente muy elevada? Por qué?
 TITULO (edite antes de imprimir) NOMBRE: CURSO: 1) Qué cantidad de alcohol ingiere una persona si toma dos vasos de cerveza de 355 ml cada uno, si su etiqueta indica que su contenido en alcohol es de 5?
TITULO (edite antes de imprimir) NOMBRE: CURSO: 1) Qué cantidad de alcohol ingiere una persona si toma dos vasos de cerveza de 355 ml cada uno, si su etiqueta indica que su contenido en alcohol es de 5?
En la primera unidad clasificábamos estos sistemas materiales de la siguiente forma: MATERIA
 La materia dispersa. Las mezclas. Disoluciones En temas anteriores ya hemos estudiado algunas características de las mezclas. Por su extraordinaria importancia vamos a dedicar un capítulo a un tipo de
La materia dispersa. Las mezclas. Disoluciones En temas anteriores ya hemos estudiado algunas características de las mezclas. Por su extraordinaria importancia vamos a dedicar un capítulo a un tipo de
Física y Química: guía interactiva para la resolución de ejercicios
 Física y Química: guía interactiva para la resolución de ejercicios CLASIFICACIÓN DE LA MATERIA I.E.S. Élaios Departamento de Física y Química EJERCICIO 1 (a) En un vaso tenemos alcohol que calentamos
Física y Química: guía interactiva para la resolución de ejercicios CLASIFICACIÓN DE LA MATERIA I.E.S. Élaios Departamento de Física y Química EJERCICIO 1 (a) En un vaso tenemos alcohol que calentamos
Materia: FÍSICA Y QUÍMICA Curso
 ACTIVIDADES DE REFUERZO FÍSICA Y QUÍMICA 3º ESO. JUNIO 2015. 1.- Realizar las configuraciones electrónicas de todos los elementos de los tres primeros periodos de la tabla periódica. 2.- Razonar cuales
ACTIVIDADES DE REFUERZO FÍSICA Y QUÍMICA 3º ESO. JUNIO 2015. 1.- Realizar las configuraciones electrónicas de todos los elementos de los tres primeros periodos de la tabla periódica. 2.- Razonar cuales
TRABAJO DE RECUPERACIÓN. FÍSICA Y QUÍMICA ESO3 Segunda evaluación. Curso
 TRABAJO DE RECUPERACIÓN. FÍSICA Y QUÍMICA ESO3 Segunda evaluación. Curso 2017-2018 1. Cuál es la presión a la que está sometido 0,50 mol de un gas encerrado en un recipiente de 2,5 L y a una temperatura
TRABAJO DE RECUPERACIÓN. FÍSICA Y QUÍMICA ESO3 Segunda evaluación. Curso 2017-2018 1. Cuál es la presión a la que está sometido 0,50 mol de un gas encerrado en un recipiente de 2,5 L y a una temperatura
TEMA 2: DIVERSIDAD DE LA MATERIA
 TEMA 2: DIVERSIDAD DE LA MATERIA 1.- La materia: sustancias puras y mezclas. 1.1.- La materia. 1.1.1.- Estados de agregación de la materia. 1.1.2.- Propiedades generales y características de la materia.
TEMA 2: DIVERSIDAD DE LA MATERIA 1.- La materia: sustancias puras y mezclas. 1.1.- La materia. 1.1.1.- Estados de agregación de la materia. 1.1.2.- Propiedades generales y características de la materia.
LA MATERIA. - Masa - Volumen -Energía - Carga eléctrica. Propiedades generales
 TEMA 2 La Materia LA MATERIA Propiedades generales - Masa - Volumen -Energía - Carga eléctrica Propiedades características - Densidad - Punto de fusión - Punto de ebullición -Conductividad eléctrica -
TEMA 2 La Materia LA MATERIA Propiedades generales - Masa - Volumen -Energía - Carga eléctrica Propiedades características - Densidad - Punto de fusión - Punto de ebullición -Conductividad eléctrica -
COLEGIO JORGE ELIÉCER GAITÁN. QUÍMICA II SOLUCIONES 1 Parte: Conceptos, Clases de soluciones, Solubilidad, concentración física de las soluciones.
 COLEGIO JORGE ELIÉCER GAITÁN QUÍMICA II SOLUCIONES 1 Parte: Conceptos, Clases de soluciones,, concentración física de las soluciones. NOMBRE: CURSO LAS SOLUCIONES En la naturaleza es muy raro encontrar
COLEGIO JORGE ELIÉCER GAITÁN QUÍMICA II SOLUCIONES 1 Parte: Conceptos, Clases de soluciones,, concentración física de las soluciones. NOMBRE: CURSO LAS SOLUCIONES En la naturaleza es muy raro encontrar
CONTENIDOS MÍNIMOS Y CRITERIOS DE EVALUACIÓN
 4 La materia: estados de agregación. Objetivos Observar el aspecto y otras características de la materia, en sus diversos estados de agregación: sólido, líquido y gaseoso. Distinguir y aplicar a ejercicios
4 La materia: estados de agregación. Objetivos Observar el aspecto y otras características de la materia, en sus diversos estados de agregación: sólido, líquido y gaseoso. Distinguir y aplicar a ejercicios
Soluciones y unidades de concentración
 MATERIA Soluciones y unidades de concentración MEZCLAS SISTEMAS HETEROGÉNEOS Leche Arena Sal y azúcar SISTEMAS HOMOGÉNEOS Sal en agua Aire Acero COMPUESTOS Agua Etanol Benceno SUSTANCIAS PURAS ELEMENTOS
MATERIA Soluciones y unidades de concentración MEZCLAS SISTEMAS HETEROGÉNEOS Leche Arena Sal y azúcar SISTEMAS HOMOGÉNEOS Sal en agua Aire Acero COMPUESTOS Agua Etanol Benceno SUSTANCIAS PURAS ELEMENTOS
Soluciones y unidades de concentración
 Soluciones y unidades de concentración Dra. Dra. Patricia Patricia Satti, Satti, UNRN UNRN MATERIA MEZCLAS SUSTANCIAS PURAS SISTEMAS HETEROGÉNEOS Leche Arena Sal y azúcar SISTEMAS HOMOGÉNEOS Sal en agua
Soluciones y unidades de concentración Dra. Dra. Patricia Patricia Satti, Satti, UNRN UNRN MATERIA MEZCLAS SUSTANCIAS PURAS SISTEMAS HETEROGÉNEOS Leche Arena Sal y azúcar SISTEMAS HOMOGÉNEOS Sal en agua
Actividades para repasar el examen de septiembre
 Actividades para repasar el examen de septiembre 1. Qué es una magnitud? Qué es medir? Pon un ejemplo que ayude a entender este concepto, utiliza un dibujo explicativo. Pon ejemplos de magnitudes y de
Actividades para repasar el examen de septiembre 1. Qué es una magnitud? Qué es medir? Pon un ejemplo que ayude a entender este concepto, utiliza un dibujo explicativo. Pon ejemplos de magnitudes y de
COLECCIÓN DE PROBLEMAS TEMA 0 QUÍMICA 2º BACHILLERATO. SANTILLANA. Dónde habrá mayor número de átomos, en 1 mol de metanol o en 1 mol
 COLECCIÓN DE PROBLEMAS TEMA 0 QUÍMICA 2º BACHILLERATO. SANTILLANA. Dónde habrá mayor número de átomos, en 1 mol de metanol o en 1 mol de ácido metanoico (ácido fórmico)? Si tenemos en cuenta las fórmulas
COLECCIÓN DE PROBLEMAS TEMA 0 QUÍMICA 2º BACHILLERATO. SANTILLANA. Dónde habrá mayor número de átomos, en 1 mol de metanol o en 1 mol de ácido metanoico (ácido fórmico)? Si tenemos en cuenta las fórmulas
Tema 3 CLASIFICACIÓN DE LA MATERIA
 Clasificación de la materia 1 Tema 3 CLASIFICACIÓN DE LA MATERIA 1. ÁTOMOS Y MOLÉCULAS... 1 2. SUSTANCIAS PURAS Y MEZCLAS.... 2 2.1. SUSTANCIAS PURAS... 2 2.2. MEZCLAS... 2 3. SEPARACIÓN DE LOS COMPONENTES
Clasificación de la materia 1 Tema 3 CLASIFICACIÓN DE LA MATERIA 1. ÁTOMOS Y MOLÉCULAS... 1 2. SUSTANCIAS PURAS Y MEZCLAS.... 2 2.1. SUSTANCIAS PURAS... 2 2.2. MEZCLAS... 2 3. SEPARACIÓN DE LOS COMPONENTES
Disoluciones y cálculos de concentraciones
 Disoluciones y cálculos de concentraciones Disoluciones Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos o más sustancias en proporciones variables.
Disoluciones y cálculos de concentraciones Disoluciones Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos o más sustancias en proporciones variables.
1 Disponemos de un ácido nítrico comercial (HNO3) de densidad 1,15 g/cm 3 y riqueza 25,48% en masa.
 Relación de Problemas Unidades de Concentración 1 Disponemos de un ácido nítrico comercial (HNO3) de densidad 1,15 g/cm 3 y riqueza 25,48% en masa. a) Determina la molaridad del ácido nítrico comercial.
Relación de Problemas Unidades de Concentración 1 Disponemos de un ácido nítrico comercial (HNO3) de densidad 1,15 g/cm 3 y riqueza 25,48% en masa. a) Determina la molaridad del ácido nítrico comercial.
UNIDAD EDUCATIVA COLEGIO SAN ANTONIO DEL TUY OCUMARE DEL TUY, ESTADO MIRANDA
 UNIDAD EDUCATIVA COLEGIO SAN ANTONIO DEL TUY OCUMARE DEL TUY, ESTADO MIRANDA CURSO: 4 TO AÑO PROFESOR: CARLOS M. LANDAETA H. GUÍA N 2: SOLUCIONES. UNIDADES DE CONCENTRACIÓN. LEY DE RAOULT Y PROPIEDADES
UNIDAD EDUCATIVA COLEGIO SAN ANTONIO DEL TUY OCUMARE DEL TUY, ESTADO MIRANDA CURSO: 4 TO AÑO PROFESOR: CARLOS M. LANDAETA H. GUÍA N 2: SOLUCIONES. UNIDADES DE CONCENTRACIÓN. LEY DE RAOULT Y PROPIEDADES
Componentes de una disolución. El disolvente El soluto Concentración de una disolución. concentración solubilidad
 Componentes de una disolución. Todas las disoluciones tienen dos componentes: El disolvente es el componente que se encuentra en mayor proporción. Este componente no cambia de estado. El soluto es el componente
Componentes de una disolución. Todas las disoluciones tienen dos componentes: El disolvente es el componente que se encuentra en mayor proporción. Este componente no cambia de estado. El soluto es el componente
UNIVERSIDAD DE CÓRDOBA FACULTAD DE EDUCACIÓN Y CIENCIAS HUMANAS LICENCIATURA EN CIENCIAS NATURALES Y EDUCACION AMBIENTAL V SEMESTRE
 Química Analítica UNIVERSIDAD DE CÓRDOBA FACULTAD DE EDUCACIÓN Y CIENCIAS HUMANAS LICENCIATURA EN CIENCIAS NATURALES Y EDUCACION AMBIENTAL V SEMESTRE 2015 Una solución es una mezcla homogénea de dos o
Química Analítica UNIVERSIDAD DE CÓRDOBA FACULTAD DE EDUCACIÓN Y CIENCIAS HUMANAS LICENCIATURA EN CIENCIAS NATURALES Y EDUCACION AMBIENTAL V SEMESTRE 2015 Una solución es una mezcla homogénea de dos o
EJERCICIOS TEMA 2. LA MATERIA Y SUS PROPIEDADES.
 EJERCICIOS TEMA 2. LA MATERIA Y SUS PROPIEDADES. 1. La materia puede presentarse en tres estados de agregación. Cuáles son? 2. Cómo son la forma y el volumen de un sólido? Y de un líquido? Y de un gas?
EJERCICIOS TEMA 2. LA MATERIA Y SUS PROPIEDADES. 1. La materia puede presentarse en tres estados de agregación. Cuáles son? 2. Cómo son la forma y el volumen de un sólido? Y de un líquido? Y de un gas?
FICHA 5: DISOLUCIONES %masa y % volumen
 FICHA 5: DISOLUCIONES %masa y % volumen 1. Calcula el % en masa de una disolución que contiene 30 g de soluto en 1 L de agua. Sol.: 2,9% 2. El vinagre es una disolución de ácido acético en agua al 3% en
FICHA 5: DISOLUCIONES %masa y % volumen 1. Calcula el % en masa de una disolución que contiene 30 g de soluto en 1 L de agua. Sol.: 2,9% 2. El vinagre es una disolución de ácido acético en agua al 3% en
QUÍMICA 2º BACHILLERATO
 DISOLUCIONES: CONCENTRACIÓN DE LAS MISMAS 1.-/ Se disuelven 7 g de cloruro de sodio en 43 g de agua. Determine la concentración centesimal de la disolución, así como la fracción molar de cada componente
DISOLUCIONES: CONCENTRACIÓN DE LAS MISMAS 1.-/ Se disuelven 7 g de cloruro de sodio en 43 g de agua. Determine la concentración centesimal de la disolución, así como la fracción molar de cada componente
Una mezcla es un compuesto formado por varias sustancias con distintas propiedades
 COMPOSICIÓN DE LA MATERIA Mezclas homogéneas y heterogéneas Una mezcla es un compuesto formado por varias sustancias con distintas propiedades Algunos sistemas materiales como la leche a simple vista parecen
COMPOSICIÓN DE LA MATERIA Mezclas homogéneas y heterogéneas Una mezcla es un compuesto formado por varias sustancias con distintas propiedades Algunos sistemas materiales como la leche a simple vista parecen
LA DIVERSIDAD DE LA MATERIA
 Tema 3 LA DIVERSIDAD DE LA MATERIA 1 Clasificación de la materia Un sistema material es una porción de materia que se separa para realizar un estudio experimental. Es aquella parte del universo que se
Tema 3 LA DIVERSIDAD DE LA MATERIA 1 Clasificación de la materia Un sistema material es una porción de materia que se separa para realizar un estudio experimental. Es aquella parte del universo que se
QUÍMICA 2º BACHILLERATO
 DISOLUCIONES: CONCENTRACIÓN DE LAS MISMAS 1.-/ Se disuelven 7 g de cloruro de sodio en 43 g de agua. Determine la concentración centesimal de la disolución, así como la fracción molar de cada componente
DISOLUCIONES: CONCENTRACIÓN DE LAS MISMAS 1.-/ Se disuelven 7 g de cloruro de sodio en 43 g de agua. Determine la concentración centesimal de la disolución, así como la fracción molar de cada componente
CAPITULO 6 : Soluciones
 CAPITULO 6 : Soluciones Gran parte de los líquidos que conocemos o que manejamos habitualmente son soluciones o disoluciones. El agua de mar, la saliva, la orina, la lavandina, el vinagre y al agua que
CAPITULO 6 : Soluciones Gran parte de los líquidos que conocemos o que manejamos habitualmente son soluciones o disoluciones. El agua de mar, la saliva, la orina, la lavandina, el vinagre y al agua que
Problemas disoluciones
 Problemas disoluciones Determinar la concentración de una disolución expresada de diferentes formas: g/l, % en masa y en volumen, Molaridad y fracción molar Preparar disoluciones a partir de solutos sólidos
Problemas disoluciones Determinar la concentración de una disolución expresada de diferentes formas: g/l, % en masa y en volumen, Molaridad y fracción molar Preparar disoluciones a partir de solutos sólidos
FÍSICA Y QUÍMICA 3º ESO
 TEMA 5 SISTEMAS MATERIALES FÍSICA Y QUÍMICA 3º ESO C.C. SANTO ANGEL CLASIFICACIÓN DE LA MATERIA La clasificación más general de la materia es la que se basa en sus constituyentes. Se distinguen así: -
TEMA 5 SISTEMAS MATERIALES FÍSICA Y QUÍMICA 3º ESO C.C. SANTO ANGEL CLASIFICACIÓN DE LA MATERIA La clasificación más general de la materia es la que se basa en sus constituyentes. Se distinguen así: -
EJERCIOS DE CONCENTRACIÓN DE SOLUCIONES
 Preuniversitario Liceo de Aplicación Química 4º 2010 Profesora Paola Lizama V. GUÍA 4: DISOLUCIONES EJERCIOS DE CONCENTRACIÓN DE SOLUCIONES 01.- Calcular la cantidad de sosa cáustica (NaOH) y de agua que
Preuniversitario Liceo de Aplicación Química 4º 2010 Profesora Paola Lizama V. GUÍA 4: DISOLUCIONES EJERCIOS DE CONCENTRACIÓN DE SOLUCIONES 01.- Calcular la cantidad de sosa cáustica (NaOH) y de agua que
Clasificación de la materia
 Clasificación de la materia Sustancias Puras Son caracterizados por su composición y propiedades definidas y constantes bajo condiciones determinadas. Sustancias puras: Elementos Son sustancias puras formadas
Clasificación de la materia Sustancias Puras Son caracterizados por su composición y propiedades definidas y constantes bajo condiciones determinadas. Sustancias puras: Elementos Son sustancias puras formadas
1 Completar las definiciones: a) El % en peso expresa el número de contenidos en de. b) Su fórmula es:
 IES Menéndez Tolosa 3º ESO (Física y Química) Completar las definiciones: a) El % en peso expresa el número de contenidos en de. b) Su fórmula es: ( ) %peso = masade + masade 00 Completar las definiciones:
IES Menéndez Tolosa 3º ESO (Física y Química) Completar las definiciones: a) El % en peso expresa el número de contenidos en de. b) Su fórmula es: ( ) %peso = masade + masade 00 Completar las definiciones:
III. D ISOLU L CIONES E
 III. DISOLUCIONES III. DISOLUCIONES Índice 1. Disoluciones 2. Solubilidad 3. Factores que favorecen la disolución de las sustancias 4. Propiedades coligativas de las disoluciones 5. Suspensiones y disoluciones
III. DISOLUCIONES III. DISOLUCIONES Índice 1. Disoluciones 2. Solubilidad 3. Factores que favorecen la disolución de las sustancias 4. Propiedades coligativas de las disoluciones 5. Suspensiones y disoluciones
Departamento Ciencias. Física y Química MATERIA. se clasifica en. SUSTANCIAS PURAS pueden ser. por métodos. físicos originan. Compuestos.
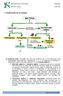 1. Clasificación de la materia MATERIA se clasifica en MEZCLAS pueden ser por métodos físicos originan SUSTANCIAS PURAS pueden ser Heterogéneas Homogéneas Compuestos como las Disoluciones formados por
1. Clasificación de la materia MATERIA se clasifica en MEZCLAS pueden ser por métodos físicos originan SUSTANCIAS PURAS pueden ser Heterogéneas Homogéneas Compuestos como las Disoluciones formados por
CLASIFICACIÓN DE LA MATERIA
 CLASIFICACIÓN DE LA MATERIA Clasificación de la materia. Sistemas materiales Sustancias puras Mezclas Un solo componente Dos o mas componentes Simples Compuestas Homogénas Heterogénas Un solo tipo de átomo.
CLASIFICACIÓN DE LA MATERIA Clasificación de la materia. Sistemas materiales Sustancias puras Mezclas Un solo componente Dos o mas componentes Simples Compuestas Homogénas Heterogénas Un solo tipo de átomo.
CuO (s) + H 2 SO 4(aq) CuSO 4(aq) +H 2 O (aq)
 Relación de problemas Química 4º ESO CDP. NTRA. SRA. DE LORETO 1. El trióxido de azufre se sintetiza a partir de dióxido de azufre y oxígeno molecular. Calcula la masa y el volumen de los reactivos que
Relación de problemas Química 4º ESO CDP. NTRA. SRA. DE LORETO 1. El trióxido de azufre se sintetiza a partir de dióxido de azufre y oxígeno molecular. Calcula la masa y el volumen de los reactivos que
DISOLUCIONES QUÍMICAS
 DISOLUCIONES QUÍMICAS Las disoluciones son mezclas homogéneas de dos o más sustancias, es decir, cuyos componentes no se pueden distinguir a simple vista. Siempre que se esta en presencia de una mezcla
DISOLUCIONES QUÍMICAS Las disoluciones son mezclas homogéneas de dos o más sustancias, es decir, cuyos componentes no se pueden distinguir a simple vista. Siempre que se esta en presencia de una mezcla
Ejercicios. 1. Disolvemos 15 g de ClNa en 60 g de agua. Calcular la concentración en masa de la mezcla.
 TEMA 4: 4 : DISOLUCIONES MATERÍA HOMOGENEA Y HETEROGÉNEA Si la materia que examinamos es uniforme, es decir, sus propiedades y su composición son las mismas en todos los puntos de su masa, decimos que
TEMA 4: 4 : DISOLUCIONES MATERÍA HOMOGENEA Y HETEROGÉNEA Si la materia que examinamos es uniforme, es decir, sus propiedades y su composición son las mismas en todos los puntos de su masa, decimos que
Si un objeto tiene mayor densidad que otro y ambos tienen el mismo tamaño. Cuál es el que tiene menos masa?
 TITULO (edite antes de imprimir) NOMBRE: CURSO: 1) Calcular la densidad de los siguientes materiales: a) 9 litros de nafta que tienen una masa de 6,120 gramos. b) 2 litros de leche que tienen una masa
TITULO (edite antes de imprimir) NOMBRE: CURSO: 1) Calcular la densidad de los siguientes materiales: a) 9 litros de nafta que tienen una masa de 6,120 gramos. b) 2 litros de leche que tienen una masa
CÁTEDRA: QUÍMICA GUÍA DE PROBLEMAS Nº6
 CÁTEDRA: QUÍMICA GUÍA DE PROBLEMAS Nº6 TEMA: PROPIEDADES COLIGATIVAS OBJETIVOS: Aplicar las propiedades coligativas para el cálculo de masas molares de solutos y de las propiedades físicas de las soluciones.
CÁTEDRA: QUÍMICA GUÍA DE PROBLEMAS Nº6 TEMA: PROPIEDADES COLIGATIVAS OBJETIVOS: Aplicar las propiedades coligativas para el cálculo de masas molares de solutos y de las propiedades físicas de las soluciones.
Unidad 13. Mix. Sustancias puras y mezclas
 Unidad 13. Mix. Sustancias puras y mezclas La materia y su clasificación Recuerda que materia es todo aquello que tiene masa y ocupa un volumen. Según su composición la materia se puede clasificar en sustancias
Unidad 13. Mix. Sustancias puras y mezclas La materia y su clasificación Recuerda que materia es todo aquello que tiene masa y ocupa un volumen. Según su composición la materia se puede clasificar en sustancias
REACCIONES QUÍMICAS. Cálculos en Química Velocidad de reacción Oxidación-reducción. Pilas
 Velocidad de reacción Oxidación-reducción. Pilas REACCIONES QUÍMICAS Física y Química 4º ESO: guía interactiva para la resolución de ejercicios I.E.S. Élaios Departamento de Física y Química EJERCICIO
Velocidad de reacción Oxidación-reducción. Pilas REACCIONES QUÍMICAS Física y Química 4º ESO: guía interactiva para la resolución de ejercicios I.E.S. Élaios Departamento de Física y Química EJERCICIO
SUSTANCIA QUÍMICA mercurio oxígeno
 ELEMENTO O SUSTANCIA ELEMENTAL: Sustancia formada por un mismo tipo de átomos, por ejemplo: Hg, H 2, Cu, O 2 SUSTANCIA QUÍMICA mercurio oxígeno COMPUESTO O SUSTANCIA COMPUESTA: Sustancia formada por dos
ELEMENTO O SUSTANCIA ELEMENTAL: Sustancia formada por un mismo tipo de átomos, por ejemplo: Hg, H 2, Cu, O 2 SUSTANCIA QUÍMICA mercurio oxígeno COMPUESTO O SUSTANCIA COMPUESTA: Sustancia formada por dos
2º CUADERNILLO DE FÍSICA Y QUÍMICA
 2º CUADERNILLO DE FÍSICA Y QUÍMICA Alumnos de 4º ESO con la asignatura de Física y Química de 3º ESO suspensa NOMBRE CURSO ENLACES 1. Representa mediante un diagrama de Lewis las siguientes moléculas:
2º CUADERNILLO DE FÍSICA Y QUÍMICA Alumnos de 4º ESO con la asignatura de Física y Química de 3º ESO suspensa NOMBRE CURSO ENLACES 1. Representa mediante un diagrama de Lewis las siguientes moléculas:
Sustituir fotografía. Sustituir texto
 Soluciones Sustituir fotografía Sustituir texto Tipos de soluciones. Hidrólisis. Solubilidad y el efecto de la temperatura. Unidades de concentración: Expresiones físicas de concentración (%m/m, %m/v,
Soluciones Sustituir fotografía Sustituir texto Tipos de soluciones. Hidrólisis. Solubilidad y el efecto de la temperatura. Unidades de concentración: Expresiones físicas de concentración (%m/m, %m/v,
TEMA 3 LAS DISOLUCIONES
 TEMA 3 LAS DISOLUCIONES 1.- DISOLUCIÓN: COMPONENTES Y TIPOS DE DISOLUCIONES 1.1- EL PROCESO DE DISOLUCIÓN - FACTORES QUE AFECTAN AL PROCESO DE DISOLUCIÓN 1.2-LA CONCENTRACIÓN - % EN MASA -% EN VOLUMEN
TEMA 3 LAS DISOLUCIONES 1.- DISOLUCIÓN: COMPONENTES Y TIPOS DE DISOLUCIONES 1.1- EL PROCESO DE DISOLUCIÓN - FACTORES QUE AFECTAN AL PROCESO DE DISOLUCIÓN 1.2-LA CONCENTRACIÓN - % EN MASA -% EN VOLUMEN
SUSTANCIA PURA ELEMENTO COMPUESTO 1
 SUSTANCIA PURA ELEMENTO COMPUESTO 1 MATERIA MEZCLA Sustancia pura Sistema material en el que se han combinado dos o más sustancias Mezcla de agua y azúcar Mezcla homogénea Sistema formado por dos o más
SUSTANCIA PURA ELEMENTO COMPUESTO 1 MATERIA MEZCLA Sustancia pura Sistema material en el que se han combinado dos o más sustancias Mezcla de agua y azúcar Mezcla homogénea Sistema formado por dos o más
6ª UNIDAD REACCIONES QUÍMICAS
 6ª UNIDAD REACCIONES QUÍMICAS 3º E.S.O. Grupo FÍSICA Y QUÍMICA 3º ESO 1 Apellidos: Nombre: 1.- QUÉ SUCEDE DURANTE UNA REACCIÓN QUÍMICA? COMENZAREMOS ESTABLECIENDO CLARAMENTE LA DIFERENCIA ENTRE CAMBIOS
6ª UNIDAD REACCIONES QUÍMICAS 3º E.S.O. Grupo FÍSICA Y QUÍMICA 3º ESO 1 Apellidos: Nombre: 1.- QUÉ SUCEDE DURANTE UNA REACCIÓN QUÍMICA? COMENZAREMOS ESTABLECIENDO CLARAMENTE LA DIFERENCIA ENTRE CAMBIOS
TEMA 7. DISOLUCIONES Y PROPIEDADES COLIGATIVAS
 TEMA 7. DISOLUCIONES Y PROPIEDADES COLIGATIVAS 1. Una solución saturada A) Contiene más soluto que disolvente. B) Contiene más disolvente que soluto. C) Contiene el mismo número de moles de soluto que
TEMA 7. DISOLUCIONES Y PROPIEDADES COLIGATIVAS 1. Una solución saturada A) Contiene más soluto que disolvente. B) Contiene más disolvente que soluto. C) Contiene el mismo número de moles de soluto que
1. Ajusta la siguiente reacción: El cloro diatómico reacciona con el hidrógeno diatómico para formar cloruro de hidrógeno
 TEMA 4. CÁLCULOS QUÍMICOS ACTIVIDADES 1. Ajuste de ecuaciones químicas 1. Ajusta la siguiente reacción: El cloro diatómico reacciona con el hidrógeno diatómico para formar cloruro de hidrógeno 2. Ajusta
TEMA 4. CÁLCULOS QUÍMICOS ACTIVIDADES 1. Ajuste de ecuaciones químicas 1. Ajusta la siguiente reacción: El cloro diatómico reacciona con el hidrógeno diatómico para formar cloruro de hidrógeno 2. Ajusta
La diversidad de la materia
 La diversidad de la materia Física y Química Los sistemas materiales Oxford University Press España, S. A. Física y Química 3º ESO 2 Un sistema material es una porción de materia que se aísla física o
La diversidad de la materia Física y Química Los sistemas materiales Oxford University Press España, S. A. Física y Química 3º ESO 2 Un sistema material es una porción de materia que se aísla física o
TEMA 3. CLASIFICACIÓN DE LA MATERIA.
 TEMA 3. CLASIFICACIÓN DE LA MATERIA. FÍSICA Y QUÍMICA 3º ESO 1. CLASIFICACIÓN DE LA MATERIA SUSTANCIAS PURAS. Son las que tienen siempre las mismas propiedades físicas y químicas. - Elemento. Es una sustancia
TEMA 3. CLASIFICACIÓN DE LA MATERIA. FÍSICA Y QUÍMICA 3º ESO 1. CLASIFICACIÓN DE LA MATERIA SUSTANCIAS PURAS. Son las que tienen siempre las mismas propiedades físicas y químicas. - Elemento. Es una sustancia
FÍSICA Y QUÍMICA TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS
 Física y Química 3º Curso Educación Secundaria Obligatoria Curso académico 2015/2016 1 FÍSICA Y QUÍMICA TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS Física y Química 3º Curso Educación Secundaria Obligatoria
Física y Química 3º Curso Educación Secundaria Obligatoria Curso académico 2015/2016 1 FÍSICA Y QUÍMICA TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS Física y Química 3º Curso Educación Secundaria Obligatoria
Ejercicios de recuperación de
 1 Ejercicios de recuperación de Física y Química de 3 er de ESO 1ª PARTE 1. a) Definir hipótesis científica y señalar sus características más importantes. b) De qué manera procede el método científico
1 Ejercicios de recuperación de Física y Química de 3 er de ESO 1ª PARTE 1. a) Definir hipótesis científica y señalar sus características más importantes. b) De qué manera procede el método científico
TEMA 3: MEZCLAS REFLEXIÓN INICIAL
 TEMA 3: MEZCLAS REFLEXIÓN INICIAL El aire que respiramos es una mezcla de muchos gases: nitrógeno, oxígeno, dióxido de carbono Casi todos los materiales naturales o artificiales de nuestro entorno son
TEMA 3: MEZCLAS REFLEXIÓN INICIAL El aire que respiramos es una mezcla de muchos gases: nitrógeno, oxígeno, dióxido de carbono Casi todos los materiales naturales o artificiales de nuestro entorno son
Soluciones. Instituto Espíritu Santo Química. Diferentes estados de soluto y solventes
 Instituto Espíritu Santo Química Soluciones Las soluciones son sistemas homogéneos fraccionables formados por dos o más sustancias puras. Los componentes de una solución pueden estar en estado sólido,
Instituto Espíritu Santo Química Soluciones Las soluciones son sistemas homogéneos fraccionables formados por dos o más sustancias puras. Los componentes de una solución pueden estar en estado sólido,
CLASIFICACIÓN DE LA MATERIA
 CLASIFICACIÓN DE LA MATERIA Clasificación de la materia SUSTACIACIAS PURAS SIMPLES UN SOLO TIPO DE ÁTOMO Mercurio (l) átomo de Hg Cloro(g) átomo de Cl SUSTANCIA PURA COMPUESTA S C O Zn Un solo tipo de
CLASIFICACIÓN DE LA MATERIA Clasificación de la materia SUSTACIACIAS PURAS SIMPLES UN SOLO TIPO DE ÁTOMO Mercurio (l) átomo de Hg Cloro(g) átomo de Cl SUSTANCIA PURA COMPUESTA S C O Zn Un solo tipo de
TEMA 2: Diversidad de la materia. T_m[ 2: Div_rsi^[^ ^_ l[ m[t_ri[ 1
 TEMA 2: Diversidad de la materia T_m[ 2: Div_rsi^[^ ^_ l[ m[t_ri[ 1 ESQUEMA DE LA UNIDAD 1.- La materia: sustancias puras y mezclas. 1.1.- La materia. 1.1.1.- Estados de agregación de la materia. 1.1.2.-
TEMA 2: Diversidad de la materia T_m[ 2: Div_rsi^[^ ^_ l[ m[t_ri[ 1 ESQUEMA DE LA UNIDAD 1.- La materia: sustancias puras y mezclas. 1.1.- La materia. 1.1.1.- Estados de agregación de la materia. 1.1.2.-
SOLUCIONES EJERCICIOS TEMA 3
 SOLUCIONES EJERCICIOS TEMA 3 1 Completar la definición siguiente: Los sistemas materiales son los que presentan distinta y distintas en las diferentes partes del sistema. Los componentes de un pueden distinguirse
SOLUCIONES EJERCICIOS TEMA 3 1 Completar la definición siguiente: Los sistemas materiales son los que presentan distinta y distintas en las diferentes partes del sistema. Los componentes de un pueden distinguirse
Física y Química 1ºBachillerato Ejemplo Examen. Formulación. (1 puntos) Formula correctamente los siguientes compuestos: Ioduro de Calcio:
 Física y Química 1ºBachillerato Ejemplo Examen Formulación. (1 puntos) Formula correctamente los siguientes compuestos: Óxido Fosfórico: Silano: Carburo Potásico: Ácido perclórico: Fosfato de Sodio: Hidruro
Física y Química 1ºBachillerato Ejemplo Examen Formulación. (1 puntos) Formula correctamente los siguientes compuestos: Óxido Fosfórico: Silano: Carburo Potásico: Ácido perclórico: Fosfato de Sodio: Hidruro
Disoluciones Químicas
 Disoluciones Químicas Las disoluciones son mezclas homogéneas de dos o más sustancias, es decir, cuyos componentes no se pueden distinguir a simple vista. Siempre que se esta en presencia de una mezcla
Disoluciones Químicas Las disoluciones son mezclas homogéneas de dos o más sustancias, es decir, cuyos componentes no se pueden distinguir a simple vista. Siempre que se esta en presencia de una mezcla
Resolución: Para calcular los g/l debemos ver la relación entre gramos de soluto y litros de disolución:
 TEMA 4. CÁLCULOS QUÍMICOS SOLUCIONES 1. Disoluciones 1. Disolvemos 3,8 gramos de hidróxido de sodio en metanol hasta completar 20 ml de disolución. Expresa la composición de la disolución en gramos por
TEMA 4. CÁLCULOS QUÍMICOS SOLUCIONES 1. Disoluciones 1. Disolvemos 3,8 gramos de hidróxido de sodio en metanol hasta completar 20 ml de disolución. Expresa la composición de la disolución en gramos por
Disoluciones. Mezclas: Asociación de dos o más sustancias distintas.
 Mezclas: Asociación de dos o más sustancias distintas. Mezclas heterogéneas: en las que sus componentes no están uniformemente distribuidos y conservan sus propiedades individuales. Se clasifican como
Mezclas: Asociación de dos o más sustancias distintas. Mezclas heterogéneas: en las que sus componentes no están uniformemente distribuidos y conservan sus propiedades individuales. Se clasifican como
Materia. Mezclas Son aquellas que están formados por 2 o más sustancias.
 Qué es la materia? Materia Sustancias Puras Son aquellas que tienen una composición y propiedades DEFINIDAS. Mezclas Son aquellas que están formados por 2 o más sustancias. Elementos No se pueden separar
Qué es la materia? Materia Sustancias Puras Son aquellas que tienen una composición y propiedades DEFINIDAS. Mezclas Son aquellas que están formados por 2 o más sustancias. Elementos No se pueden separar
CURSO 2016 / Tema 3. Sistemas. materiales. Física y química para 2º ESO. Nombre..
 CURSO 2016 / 2017 Tema 3. Sistemas materiales. Física y química para 2º ESO Nombre.. Índice general: 1. Concepto de mezcla. Tipos. 2. Las disoluciones. 3. Tipos de disoluciones. 3.1. Según el estado físico
CURSO 2016 / 2017 Tema 3. Sistemas materiales. Física y química para 2º ESO Nombre.. Índice general: 1. Concepto de mezcla. Tipos. 2. Las disoluciones. 3. Tipos de disoluciones. 3.1. Según el estado físico
EJERCICIOS RESUELTOS DISOLUCIONES
 EJERIIOS RESUELTOS DISOLUIONES 1.- Se disuelven 20 g de NaOH en 560 g de agua. alcula a) la concentración de la en % en masa y b) su molalidad. Ar(Na) 2. Ar(O)16. Ar(H)1. NaOH 20 a) % NaOH.100 % NaOH.100
EJERIIOS RESUELTOS DISOLUIONES 1.- Se disuelven 20 g de NaOH en 560 g de agua. alcula a) la concentración de la en % en masa y b) su molalidad. Ar(Na) 2. Ar(O)16. Ar(H)1. NaOH 20 a) % NaOH.100 % NaOH.100
INSTITUCION EDUCATIVA LA PRESENTACION NOMBRE ALUMNA: CIENCIAS NATURALES Y EDUCACIÓN AMBIENTAL ASIGNATURA: QUÍMICA NOTA
 INDICADORES DE DESEMPEÑO INSTITUCION EDUCATIVA LA PRESENTACION NOMBRE ALUMNA: AREA : CIENCIAS NATURALES Y EDUCACIÓN AMBIENTAL ASIGNATURA: QUÍMICA NOTA DOCENTE: LEADY RODRIGUEZ TIPO DE GUIA: CONCEPTUAL
INDICADORES DE DESEMPEÑO INSTITUCION EDUCATIVA LA PRESENTACION NOMBRE ALUMNA: AREA : CIENCIAS NATURALES Y EDUCACIÓN AMBIENTAL ASIGNATURA: QUÍMICA NOTA DOCENTE: LEADY RODRIGUEZ TIPO DE GUIA: CONCEPTUAL
LOGO. Soluciones. M. C. Rita Paz Samaniego
 LOGO Soluciones M. C. Rita Paz Samaniego Contenido Qué es una solución Terminología de solubilidad Solubilidad de compuestos Unidades de concentración de soluciones Qué es una solución? Una solución es
LOGO Soluciones M. C. Rita Paz Samaniego Contenido Qué es una solución Terminología de solubilidad Solubilidad de compuestos Unidades de concentración de soluciones Qué es una solución? Una solución es
FÍSICA Y QUÍMICA 2º ESO TEMA VI COMPOSICIÓN DE LA MATERIA
 FÍSICA Y QUÍMICA 2º ESO TEMA VI COMPOSICIÓN DE LA MATERIA 1) MEZCLAS HOMOGÉNEAS Y HETEROGÉNEAS Una mezcla es una composición de sustancias con distintas propiedades. Una mezcla es homogénea si está formada
FÍSICA Y QUÍMICA 2º ESO TEMA VI COMPOSICIÓN DE LA MATERIA 1) MEZCLAS HOMOGÉNEAS Y HETEROGÉNEAS Una mezcla es una composición de sustancias con distintas propiedades. Una mezcla es homogénea si está formada
Disoluciones químicas
 Disoluciones químicas Contenidos 1.- Las disoluciones. Clasificación. 2.- Concentración de una disolución 2.1. Porcentaje en masa (% en masa) 2.2. Porcentaje en volumen (% en volumen) 2.3. Concentración
Disoluciones químicas Contenidos 1.- Las disoluciones. Clasificación. 2.- Concentración de una disolución 2.1. Porcentaje en masa (% en masa) 2.2. Porcentaje en volumen (% en volumen) 2.3. Concentración
