GUIA PARA LA PRODUCCIÓN DE Metarhizium anisopliae
|
|
|
- Juan Francisco Javier Quintana Salazar
- hace 7 años
- Vistas:
Transcripción
1 CENTRO DE INVESTIGACIÓN DE LA CAÑA DE AZUCAR DEL ECUADOR CINCAE PUBLICACIÓN TÉCNICA Nо. 5 GUIA PARA LA PRODUCCIÓN DE Metarhizium anisopliae Patricia Gómez Pereira Jorge Mendoza Mora El Triunfo, Guayas, Ecuador Octubre del
2 GUIA PARA LA PRODUCCIÓN DE Metarhizium anisopliae I. INTRODUCCIÓN Patricia Gómez Pereira Jorge Mendoza Mora En algunas ocasiones, el ataque de insectos plagas constituye una de las causas de la baja producción y rendimiento de la caña de azúcar. En Ecuador, existen varias especies de insectos que pueden afectar el cultivo, siendo las más importantes el saltahojas, Perkinsiella saccharicida y el salivazo, Mahanarva andigena (Mendoza, 2001; Mendoza, et. al, 2001). En un esfuerzo por evitar tales problemas, los cultivadores de caña vienen utilizando insecticidas químicos, como única alternativa para controlar estas plagas. Esta práctica, lejos de ser una solución duradera, económica y ecológica, ha traído como consecuencia la ruptura del equilibrio biológico del agro-ecosistema, con manifestaciones evidentes de resurgencia de plagas claves, surgimiento de nuevas plagas y, problemas relacionados con la salud y el medio ambiente (Mendoza. 2001). Esta situación está demandando la búsqueda de nuevas alternativas de control que sustenten el desarrollo de una agricultura sostenible. En varios países, el uso de hongos entomopatógenos es una alternativa que se ha venido abriendo espacio en los programas de manejo de plagas en caña de azúcar. Estos microorganismos poseen la capacidad de regular las poblaciones de algunos insectos plagas (Rodríguez y Sáenz, 2000; Estrada y López, s.f.; Mendonca, 1996). Actualmente, se conocen más de 700 especies de hongos que afectan a insectos de diversos órdenes (Devoto, Gerding y France, 2003); algunos de los cuales, están siendo utilizados exitosamente en programas de control biológico (Monzón. 2001). Por ahora, el grupo más importante de hongos entomopatógenos, con fines prácticos de manejo, esta constituido por Metarhizium anisopliae y Beauveria bassiana (Monzón. s.f.). En el caso de M. anisopliae es un patógeno que ataca naturalmente a más de 300 especies de insectos de diferentes órdenes, entre los cuales se encuentran el saltahojas, Perkinsiella saccharicida, y diversas especies de salivazo que afectan la caña de azúcar (Mendonca, 1996; Alves, 1998; Mendoza, 2003). El trabajo realizado hasta ahora con M. anisopliae en el Centro de Investigación de la Caña de Azúcar del Ecuador (CINCAE), ha permitido establecer una metodología para la producción de este entomopatógeno con miras a su utilización en programas de manejo integrado de plagas en caña de azúcar. Asistente de Investigación y Entomólogo del CINCAE. 2
3 II. PROCESO DE PRODUCCION 1. Recolección de muestras en el campo Para la obtención de cepas del entomopatógeno se hacen recolecciones en el campo de insectos muertos que presenten síntomas o signos del patógeno que se desea aislar (micelio o esporulación). Estos insectos se colocan individualmente en frascos de vidrio, cajitas o fundas plásticas, limpias o esterilizadas, y se trasladan al laboratorio. Aquí se hace una desinfección de los especimenes, sumergiendo en solución de hipoclorito de sodio (NaClO) al 0.5%, durante 2 minutos, y se enjuagan tres veces en agua destilada estéril (ADE). Posteriormente se colocan sobre papel filtro estéril para extraer el exceso de humedad. Una vez desinfectados los especimenes, se colocan en cajas petri acondicionadas como cámara húmeda estériles, con papel filtro, una bolita de algodón humedecido y dos portaobjetos colocados en cruz, sobre los cuales se colocan los especimenes desinfectados (Figura 1). A B B C C Figura 1. Cámara húmeda (A), crecimiento de micelio (B) y esporulación de M. anisopliae (C) sobre adultos de Perkinsiella saccharicida 2. Aislamiento Para los aislamientos se toman los insectos de la cámara húmeda que presenten una esporulación uniforme y estén libres de contaminantes (Figura 2). Este aislamiento se puede efectuar de dos maneras: En el primer caso se prepara una suspensión retirando las conidias del cuerpo del insecto y colocándolas en un frasco con 9 ml de ADE una gota de Tween 20. A partir de esta suspensión se hacen siembras en el medio de cultivo con la ayuda de un asa de platino. En el otro caso se retiran las conidias del insecto con el asa de platino y se siembran directamente utilizando la técnica del rayado sobre el medio de cultivo. El aislamiento se efectúa en cajas petri o tubos de ensayo conteniendo PDA 1 (papa, dextrosa y agar) más extracto de levadura. Para evitar el crecimiento de bacterias se agrega una gota de ácido láctico sobre el medio de cultivo en cada caja petri o tubo de ensayo. Las cajas petri se sellan con parafilm y los tubos de ensayo con algodón y papel aluminio (Figura 3). Posteriormente se colocan en una incubadora a 27 ºC con luz permanente. 1/ 200 g de papa, 20 g de dextrosa, 15 g de agar, 5 g de extracto de levadura y 1000 ml de agua destilada 3
4 A B Figura 2. Adulto de salivazo cubierto con micelio y conidias de Metarhizium anisopliae. Figura 3. Aislamientos de M. anisopliae en caja petri (A) y tubo de ensayo (B) 3. Reactivación Partiendo de una cepa seleccionada, sea nativa o introducida, es necesario mantener la patogenicidad y virulencia de este organismo a través de dos reactivaciones al año. Para esto se utilizan insectos vivos procedentes de la cría del laboratorio o del campo, que no muestren síntomas de afectación por algún patógeno. Para el caso del salivazo se desinfectan con una solución de hipoclorito de sodio (NaClO) al 0.5%, durante 2 minutos, y se enjuagan por tres ocasiones con ADE; luego se colocan sobre papel filtro estéril para eliminar el exceso de humedad y posteriormente se inoculan con el hongo. El método de inoculación consiste en sumergir el insecto en una suspensión de 1x10 8 conidias/ml o pasar una pincelada en el dorso del mismo. Los insectos inoculados son colocados individualmente en cajas petri, proporcionándoles humedad y alimento hasta que se produzca la muerte del mismo. En el caso de Perkinsiela, se paralizan momentáneamente colocándolas en la nevera durante 33 a 45 segundos e inmediatamente se inoculan haciendo una pulverización con un atomizador manual. Posteriormente se colocan sobre papel filtro para eliminar el exceso de humedad y se transfieren a jaulas entomológicas en donde se las mantiene con pedazos de hojas de caña desinfectadas hasta que se produzca la muerte del insecto. Los insectos muertos son acondicionados en cámara húmeda (caja petri) como se indicó anteriormente, para que se produzca el desarrollo y la esporulación del hongo. 4. Producción del inóculo en cajas petri Una vez obtenida la colonia pura del patógeno se prepara una suspensión de conidias y con la ayuda de un esparcidor o rastrillo de vidrio se siembran sobre el medio de cultivo (PDA más extracto de levadura). Las cajas petri se sellan con parafilm y se colocan en una incubadora a 27 C, donde permanecen con luz continua durante 15 días, tiempo en el cual el hongo completa su desarrollo y alcanza a esporular completamente (Figura 4). Una vez esporulado el hongo, y mientras permanecen en la incubadora, se retira el parafilm de las cajas petri para que la colonia vaya perdiendo humedad y se mejore el intercambio gaseoso. Posteriormente, estas cajas pasan a la refrigeradora (4 a 8 C) en donde pueden conservarse hasta seis meses. 4
5 5. Preparación de matrices Para formar las matrices se utilizan Erlenmeyer de 500 ml conteniendo 100 ml de PDA más extracto de levadura y dos gotas de ácido láctico. En estas matrices se siembra el inóculo proveniente de las cajas petri llenas. Para ello se prepara una suspensión con una concentración de alrededor de 1 x 10 8 conidias/ml, de la cual se toman 2 ml para inocular cada matriz. Estas se colocan en la incubadora o en un ambiente a 27 C, con luz permanente o fotoperiodo normal. Al cabo de 15 días el hongo estará completamente esporulado y podrá ser utilizado en la producción masiva del mismo (Figura 5). Figura 4. Producción de inóculo en caja petri. Figura 5. Matrices sólidas para producción de M. anisopliae 6. Preparación del sustrato Para la producción masiva del hongo se utiliza arroz precocido. Para preparar este sustrato se coloca el arroz en una olla con agua en estado de ebullición, por el lapso de 5 a 10 minutos. El arroz precocido debe mostrar una consistencia suave y que quiebre con facilidad al ser partido con la uña. Posteriormente, este arroz es transferido a una zaranda para escurrir el exceso de humedad y enfriarlo. El arroz precocido se puede colocar en botellas de vidrio, fundas de polipropileno o tarrinas autoclavables. En el CINCAE se utiliza fundas de polipropileno de 8" x 12", con capacidad para 400 g de arroz precocido. Las fundas se cierran haciéndoles tres dobleces y sellándolas con grapas. El material así preparado, se esteriliza en autoclave a 121 C con 15 psi, durante 30 minutos. Después de esterilizar las fundas, se deben remover con el objeto de evitar aglomeraciones del arroz y facilitar el crecimiento del hongo. 7. Inoculación del sustrato A partir de cada matriz sólida se prepara 500 ml de una suspensión de conidias del hongo, que puede tener una concentración de 1 x 10 8 conidias/ml. Inicialmente se agrega 100 ml de ADE + Tween 20 al 0.05%, con el cual se hace un primer lavado de las conidias de la matriz, posteriormente se hacen otros lavados sucesivos hasta completar 500 m1 de suspensión del hongo. A esta suspensión se le agrega 62.5 mg de cloranfenicol, para evitar el crecimiento de bacterias. Para la inoculación del sustrato se utilizan 5 ml de esta suspensión por funda (Figura 6). 5
6 Las fundas inoculadas se trasladan al cuarto de crecimiento (Figura 7), donde permanecen expuestas a un fotoperiodo normal y con una temperatura de 26 a 28 C. Al tercer o cuarto día se remueve el contenido de las fundas para lograr un crecimiento uniforme y una buena esporulación. Al cabo de 15 días el sustrato con el hongo esporulado es trasladado al cuarto de secado. A A B Figura 6. Cámara de aislamientos (A) y cámara de flujo laminar (B) utilizadas en los procesos de aislamiento e inoculación de hongos entomopatógenos. Figura 7. Colocación de las fundas inoculadas en el cuarto de crecimiento y esporulación de M. anisopliae 8. Secado del producto El sustrato con el hongo proveniente del cuarto de crecimiento se coloca en el cuarto de secado, a una temperatura no mayor de 28 C, con baja humedad relativa (<70%) y sin entrada de rayos solares. Un cuarto con acondicionador de aire provee las condiciones adecuadas para el secado de este material. El material se esparce sobre papel periódico y sobre un plástico negro, manteniéndose por 12 días, hasta que el contenido de humedad descienda al 12 ó 14% (Figura 8). En estas condiciones el material es enfundado en recipientes de 1 Kg (Figura 9) y estará listo para ser utilizado directamente en las aplicaciones en el campo ó almacenarse en refrigeración (4 a 8 C). En este último caso, el hongo puede permanecer viable hasta por 6 meses. 6
7 Figura 8. Sistema para el secado del sustrato arroz- hongo. Figura 9. Enfundado del producto final III. PRUEBAS MICROBIOLÓGICAS O PRUEBAS DE CALIDAD 1. Concentración de esporas Para la cuantificación de la concentración de esporas se toman cuatro submuestras de un gramo de arroz-hongo, de cada lote de producción. Cada submuestra se coloca en un frasco con 10 ml de ADE más una gota de Tween 20, que constituye la suspensión madre. Luego, de cada suspensión madre se toma 1 ml y se coloca en un segundo frasco que contiene 9 ml de ADE, con lo cual queda preparada la dilución 1 x Posteriormente se repite este procedimiento hasta obtener una dilución de 1 x 10-3 (Figura 10), la que permite contar el número de conidias en la cámara de Neubauer o Hemocitómetro. El conteo de conidias se hace en cinco campos (los cuatro de las esquinas y el central) de la cámara de Neubauer (Figura 11 y 12.). Se suma la cantidad total de los cinco campos y se obtiene el promedio. Este valor se multiplica por que es el factor de la cámara, por el inverso de la dilución, que en este caso será 10 3 y por el volumen de la suspensión madre (10 ml). Este valor será el estimado del número de conidias por gramo de arroz. Figura 10. Procedimiento para preparar las diluciones seriadas a partir de la suspensión madre. 7
8 1 mm mm Figura 11. Retículo de la cámara de Neubauer y cuadrados utilizados para el conteo de conidias Figura 12. Conteo de conidias en uno de los cuadrantes centrales de la cámara de Neubauer. Las conidias que están sobre la línea derecha e inferior no se cuentan 2. Prueba de germinación Esta prueba sirve para establecer la viabilidad del hongo y, en combinación con el estimado del número de esporas por gramo de arroz se puede calcular la cantidad de esporas viables por unidad de peso o volumen. Este estimado se hace con cada una de las cuatro submuestras preparadas para el conteo de conidias. Se prepara una caja petri para cada submuestra, con 15 ml de agar-agua, sin acidificar. Se marcan cinco puntos en la superficie externa inferior de la caja, que corresponden a los puntos en los cuales se depositan las alícuotas que contienen las esporas. De la dilución 1x10-3 de cada submuestra preparada para la prueba anterior, y previamente agitada, se toman cinco alícuotas de 5 ul, para depositar sobre el medio de cultivo, en los puntos que fueron marcados en la caja petri (Figura 13). Las cajas petri inoculadas se incuban en un cuarto a 27 C, durante 20 a 24 horas. Transcurrido este tiempo se agrega una gota de azul de lactofenol a cada alícuota con el propósito de detener la germinación y a la vez teñir las esporas del hongo (Figura 14). Luego, se cortan las alícuotas depositándolas sobre una lamina porta objetos y se coloca un cubreobjeto (Figura 15). La observación se hace con el objetivo de 40 X contando un mínimo de 100 esporas (germinadas y no germinadas), por alícuota (Figura 16). Con los datos obtenidos en las cuatro submuestras se calcula el porcentaje de germinación. 8
9 Figura 13. Depósito de las alícuotas de la suspensión del hongo en la caja petri para la prueba de germinación Figura 14 Tinción con azul de lactofenol de las conidias de M. anisopliae. Figura 15. Preparación de placas para el conteo de conidias germinadas y no germinadas Figura 18. Conidias de M. anisopliae germinadas y no germinadas, 24 horas después de la inoculación en agar- agua, (objetivo de 40 X). 3. Prueba de pureza La prueba de pureza tiene como propósito establecer la proporción del agente biológico e identificar los contaminantes, ayudando a mejorar el proceso de producción del entomopatógeno. El medio Papa Dextrosa Agar (PDA) más cloranfenicol (0,016%) se prepara adicionando 1 ml de la solución de cloranfenicol ( 0.25 gramos de cloranfenicol en 100 ml de ADE) en 150 ml de PDA. Este medio se dispensa en cantidades de 10 a 15 ml por cada caja petri esterilizada. Luego se toman los tubos de la dilución 10-3 de cada submuestra, se agitan en el vortex durante un minuto y se toma 50 ul para inocular en cada caja, dispersando el inóculo con la ayuda de un rastrillo bacteriológico esterilizado. Las cajas inoculadas se incuban a una temperatura de 27 C, con el fin de promover el desarrollo de las unidades formadoras de colonias (UFC). Diariamente se cuenta el número de UFC de cada organismo durante 7 días, en todas las submuestras. Al final de las lecturas, se identifica cada uno de los microorganismos presentes y se anota el número de UFC de Metarhizium anisopliae y el número de UFC de otros microorganismos (hongos, bacterias y levaduras). Para el cálculo de pureza (P) se utiliza la siguiente formula: UFC del hongo deseado % P = x 100 UFC totales 9
10 IV. BIBLIOGRAFÍA ALVES, S Controle microbiano de insetos. 2 da. Ed. Brasil, 1163 p. FEALQ, Piracicaba, ALVES, S y PEREIRA, R. M Producao de fungos entomopatogénicos. In S. B. Alves (ed.), Controle microbiano de insetos. 2 da. Ed. FEALQ, Piracicaba, Brasil, 1163 p DEVOTO, L; GERDING, M y FRANCE Hongos entomopatógenos: Una alternativa para la obtención de biopesticidas. Informativo Agropecuario, BIOLECHE-INIA QUILAMAPU. ttp:// ESTRADA, J y LOPEZ, M.T. (s.f.). Los Plaguicidas en la Agricultura Sostenible Cubana. Instituto de Investigaciones Fundamentales de Agricultura Tropical Alejandro de Humboldt (INIFAT). C. De la Habana. p. 1-2 GUTIERREZ, G Manual de Instrucciones para Determinar la DL 50, como Criterio para Evaluar Resistencia. Managua, Nicaragua, D.D.F/SAVEIMAG. 23.p. MARIN, P y BUSTILLO, A Pruebas microbiológicas y físico-químicas para el control de calidad de hongos entomopatógenos. In. Memorias del Curso Internacional Teórico Práctico sobre Entomopatógenos, Parasitoides y otros Enemigos de la Broca del Café. CENICAFE, Chinchiná, Colombia, marzo 11 al 15 del p MENDONCA, A Pragas da cana de acucar. Maceico, Brasil. Insectos & CIS. 239 p. MENDOZA, J; MARTINEZ, I; ALVAREZ, A.M; AYORA, A y LUZURIAGA, V Manejo del Saltahojas de la Caña de Azúcar, Perkinsiella saccharicida (Homoptera: Delphacidae), en el Ecuador. Memorias. Primer Taller Latinoamericano Sobre Plagas de la Caña de Azúcar. Guayaquil-Ecuador. p MENDOZA, J Bioecología del Salivazo de la Caña de Azúcar, Mahanarva andigena (Homoptera: Cercopidae); en el Ecuador. Memorias. Primer Taller Latinoamericano sobre Plagas de la Caña de Azúcar. Guayaquil, Ecuador. p MENDOZA, J Control Biológico del Salivazo de la Caña de Azúcar, Mahanarva andigena. In Memorias del Primer Seminario Nacional de Control Biológico Universidad de Cuenca, Ecuador. P
11 MONZÓN, A Producción, uso y control de calidad de hongos entomopatógenos en Nicaragua. Manejo Integrado de plagas, CATIE. Costa Rica. Nο.63. pp MONZÓN, A. (s.f.). Producción y uso de hongos Entomopatógenos. FUNICA; CATIE. Nicaragua.63p. RODRÍGUEZ, D Hongos Entomopatógenos Contribución del Programa Nacional de Entomología del ICA. Bogota (Colombia). p RODRÍGUEZ, A y SAEN, C Uso biológico del Metarhizium anisopliae (METCH) SOROK, como estrategia para el control de salivazo (Hom.: Cercopidae), en la caña de azúcar. DIECA-LAICA. Costa Rica. p ROGG, H Guía práctica de producción masiva del entomopatógeno Beauveria bassiana para el control biológico de insectos plaga y vectores en Bolivia. Universidad Autónoma Gabriel René Moreno, Santa Cruz de la Sierra, Bolivia. 36 p. 11
12 ANEXO De acuerdo al proceso establecido para la producción de Metarhizium anisopliae, el laboratorio debe disponer de las siguientes salas o ambientes: sala para matrices, sala para preparación del sustrato, sala para inoculación, sala para crecimiento del hongo y sala para el secado. Los requisitos mínimos en cada una de estas salas son los siguientes: Sala para matrices. En esta sala se mantienen las matrices, para lo cual se puede disponer de una incubadora a 27 ºC y con luz permanente. Si no se dispone de la incubadora, las matrices se pueden mantener al ambiente con temperatura de 26 a 28 ºC. Además, en esta sala se debe disponer de una nevera, un microscopio y la cámara de Neubauer. Sala para preparación de medios de cultivo y el sustrato de arroz. En esta sala se realiza el proceso de preparación de los medios de cultivos y, el precocido y esterilización del arroz. Los equipos necesarios para este proceso son el autoclave, una cocina industrial de dos hornillas, una balanza electrónica y una refrigeradora. Los medios de cultivo, antibióticos y el agua destilada estéril se deben conservar en refrigeración ( 4 a 8ºC). Sala para inoculación. En esta sala se efectúan los aislamientos e inoculación del hongo en los medios de cultivo (cajas petri, matríces) y en el sustrato de arroz. Para este proceso se requiere de una cámara de flujo laminar o una cámara de aislamiento con luz ultravioleta, un mechero a gas o alcohol, un plato agitador calentador y un vortex. Esta sala debe disponer de un acondicionador de aire y se debe mantener en condiciones de asepsia. Sala para crecimiento del hongo. En esta sala se mantienen las fundas inoculadas durante el tiempo que requiere la fase de crecimiento y esporulación del hongo. Las fundas se colocan individualmente en los estantes metálicos evitando su aglomeración. Esta sala se debe mantener entre 26 a 28 C, humedad relativa del 80% y fotoperiodo de 8 horas. Para mejorar las condiciones de humedad de esta sala se recomienda el uso de un humidificador. Sala de secado del hongo. Esta sala debe ser independiente de las otras salas, debe tener buena ventilación, temperatura no mayor a 28 C, humedad relativa menor a 70 % y no permitir la entrada de rayos solares, para esto se puede colocar en las ventanas una película antisolar. Para mejorar las condiciones de secado de esta sala se puede disponer de un acondicionador de aire encendido. Nota: Todas las salas requieren de buenas condiciones de limpieza y desinfección, especialmente las salas para mantenimiento de matrices, inoculación y crecimiento del hongo. Esta desinfección debe hacerse diariamente con una mezcla de amonio cuaternario, a razón de 13 ml por litro de agua; ó, hipoclorito de sodio al 0.25 %. 12
13 CINCAE Centro de Investigación de la Caña de Azúcar del Ecuador Km 49.6, vía Durán Tambo Teléfonos: / 67, Ext
PRÁCTICAS DEL LABORATORIO DE MICROBIOLOGÍA GENERAL Trimestre 14-I
 PRÁCTICAS DEL LABORATORIO DE MICROBIOLOGÍA GENERAL Trimestre 14-I P # 1 P # 2 P # 3 P # 4 P # 5 P # 6 Uso y cuidados en el manejo del Microscopio Esterilización de materiales y medios Técnicas de Tinción
PRÁCTICAS DEL LABORATORIO DE MICROBIOLOGÍA GENERAL Trimestre 14-I P # 1 P # 2 P # 3 P # 4 P # 5 P # 6 Uso y cuidados en el manejo del Microscopio Esterilización de materiales y medios Técnicas de Tinción
TRABAJO PRÁCTICO N 6 FERTILIZANTES BIOLÓGICOS: DESARROLLO Y CONTROL DE CALIDAD DE INOCULANTES
 TRABAJO PRÁCTICO N 6 FERTILIZANTES BIOLÓGICOS: DESARROLLO Y CONTROL DE CALIDAD DE INOCULANTES Objetivos Conocer los parámetros para la selección de cepas. Conocer las metodologías y procedimientos microbiológicos
TRABAJO PRÁCTICO N 6 FERTILIZANTES BIOLÓGICOS: DESARROLLO Y CONTROL DE CALIDAD DE INOCULANTES Objetivos Conocer los parámetros para la selección de cepas. Conocer las metodologías y procedimientos microbiológicos
PRACTICA N 02: PROCESOS FERMENTATIVOS: PRODUCCION DE PROTEÍNA UNICELULAR O BIOMASA
 PRACTICA N 02: PROCESOS FERMENTATIVOS: PRODUCCION DE PROTEÍNA UNICELULAR O BIOMASA Capacidades a lograr: 1. Conoce y aplica técnicas de siembra, cultivo y cuantificación del proceso fermentativo para producción
PRACTICA N 02: PROCESOS FERMENTATIVOS: PRODUCCION DE PROTEÍNA UNICELULAR O BIOMASA Capacidades a lograr: 1. Conoce y aplica técnicas de siembra, cultivo y cuantificación del proceso fermentativo para producción
PRACTICA Núm. 20 DETERMINACION DE CLOSTRIDIOS SULFITO REDUCTORES EN AGUA
 PRACTICA Núm. 20 DETERMINACION DE CLOSTRIDIOS SULFITO REDUCTORES EN AGUA I. OBJETIVO Determinar la presencia de Clostridios sulfito reductores en agua por el método de recuento en tubo. II. INTRODUCCION
PRACTICA Núm. 20 DETERMINACION DE CLOSTRIDIOS SULFITO REDUCTORES EN AGUA I. OBJETIVO Determinar la presencia de Clostridios sulfito reductores en agua por el método de recuento en tubo. II. INTRODUCCION
- Mencionar las Normas de Bioseguridad y precauciones necesarias para trabajar en el laboratorio microbiológico.
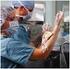 Microbiología General e Inmunología Año 2012 Trabajo Práctico Nº1 Objetivos: Que el alumno sea capaz de: - Mencionar las Normas de Bioseguridad y precauciones necesarias para trabajar en el laboratorio
Microbiología General e Inmunología Año 2012 Trabajo Práctico Nº1 Objetivos: Que el alumno sea capaz de: - Mencionar las Normas de Bioseguridad y precauciones necesarias para trabajar en el laboratorio
ENUMERACIÓN DE ENTEROBACTERIACEAE EN ALIMENTOS SIN RESUSCITACIÓN. TÉCNICA RECUENTO EN PLACA
 PRT-712.03-040 Página 1 de 6 1. OBJETIVO Determinar el número de Enterobactereaceae presentes en un alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos
PRT-712.03-040 Página 1 de 6 1. OBJETIVO Determinar el número de Enterobactereaceae presentes en un alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos
PROCEDIMIENTO DETECCIÓN Y ENUMERACIÓN POR NUMERO MAS PROBABLE (NMP) CON ETAPA DE PRE- ENRIQUECIMIENTO DE ENTEROBACTERIACEAE EN ALIMENTOS
 Página 1 de 5 1. OBJETIVO Estimar el número de Enterobacteriaceae presentes en el alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos de consumo humano
Página 1 de 5 1. OBJETIVO Estimar el número de Enterobacteriaceae presentes en el alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos de consumo humano
NMP PARA LA DETERMINACION DE COLIFORMESY COLIFORMES FECALES EN AGUAS
 PRT-712.03-005 Página 1 de 6 1. OBJETIVO Este método es utilizado para estimar la densidad de bacterias del grupo coliformes y conocer la calidad sanitaria en aguas crudas 2. CAMPO DE APLICACIÓN Y ALCANCE
PRT-712.03-005 Página 1 de 6 1. OBJETIVO Este método es utilizado para estimar la densidad de bacterias del grupo coliformes y conocer la calidad sanitaria en aguas crudas 2. CAMPO DE APLICACIÓN Y ALCANCE
PRODUCCION DE MICELIO. ( Pleourotus Spp.)
 PRODUCCION DE MICELIO ( Pleourotus Spp.) Aislamiento y mantenimiento de cepas Medios de cultivo Para el desarrollo del micelio de los hongos en el laboratorio, se emplean medios de cultivo sólidos que
PRODUCCION DE MICELIO ( Pleourotus Spp.) Aislamiento y mantenimiento de cepas Medios de cultivo Para el desarrollo del micelio de los hongos en el laboratorio, se emplean medios de cultivo sólidos que
PRACTICA Núm. 22 INVESTIGACION DE COLIFORMES TOTALES Y FECALES EN DESECHOS SOLIDOS Y COMPOSTA
 PRACTICA Núm. 22 INVESTIGACION DE COLIFORMES TOTALES Y FECALES EN DESECHOS SOLIDOS Y COMPOSTA I. OBJETIVO Determinar la presencia de coliformes totales y fecales en un desecho sólido por el método del
PRACTICA Núm. 22 INVESTIGACION DE COLIFORMES TOTALES Y FECALES EN DESECHOS SOLIDOS Y COMPOSTA I. OBJETIVO Determinar la presencia de coliformes totales y fecales en un desecho sólido por el método del
BIORREACTRES. Estudios básicos y aplicados sobre procesos de fermentación
 BIORREACTRES Ing. en Alimentos Estudios básicos y aplicados sobre procesos de fermentación Mg. Anahí V. Cuellas Docente investigadora Universidad Nacional de Quilmes TRABAJO PRACTICO Obtención de enzimas
BIORREACTRES Ing. en Alimentos Estudios básicos y aplicados sobre procesos de fermentación Mg. Anahí V. Cuellas Docente investigadora Universidad Nacional de Quilmes TRABAJO PRACTICO Obtención de enzimas
INSTITUTO DOMINICANO DE INVESTIGACIONES AGROPECUARIAS Y FORESTALES
 INSTITUTO DOMINICANO DE INVESTIGACIONES AGROPECUARIAS Y FORESTALES 7mo Congreso de la Sociedad Dominicana de Investigadores Agropecuarios y Forestales (SODIAF) Adaptación in vitro de cuatro cepas nativas
INSTITUTO DOMINICANO DE INVESTIGACIONES AGROPECUARIAS Y FORESTALES 7mo Congreso de la Sociedad Dominicana de Investigadores Agropecuarios y Forestales (SODIAF) Adaptación in vitro de cuatro cepas nativas
Objetivos. S Determinar la presencia de bacterias coliformes en una muestra de agua
 Análisis del agua S Objetivos S Determinar la presencia de bacterias coliformes en una muestra de agua Introducción S Las tres pruebas básicas para determinar la presencia de bacterias coliformes (asociada
Análisis del agua S Objetivos S Determinar la presencia de bacterias coliformes en una muestra de agua Introducción S Las tres pruebas básicas para determinar la presencia de bacterias coliformes (asociada
PRÁCTICA 5. Aislamiento de Microorganismos (1ª Sesión)
 PRÁCTICA 5. Aislamiento de Microorganismos (1ª Sesión) Objetivos Al finalizar esta práctica el alumno será capaz de: Explicar el fundamento de diferentes medios de cultivo y condiciones de incubación para
PRÁCTICA 5. Aislamiento de Microorganismos (1ª Sesión) Objetivos Al finalizar esta práctica el alumno será capaz de: Explicar el fundamento de diferentes medios de cultivo y condiciones de incubación para
Evaluación n de medios de cultivo para inducir la esporulación n del acaropatógeno. Hirsutella nodulosa OBJETIVO ESPECIFICO
 Evaluación n de medios de cultivo para inducir la esporulación n del acaropatógeno Hirsutella nodulosa Elaborado por: Ruth León n González OBJETIVO ESPECIFICO Evaluar distintos medios de cultivo para inducir
Evaluación n de medios de cultivo para inducir la esporulación n del acaropatógeno Hirsutella nodulosa Elaborado por: Ruth León n González OBJETIVO ESPECIFICO Evaluar distintos medios de cultivo para inducir
DETERMINACION DE LA IMPORTANCIA DEL PICUDO RAYADO, Metamasius hemipterus L., EN CAÑA DE AZÚCAR
 DETERMINACION DE LA IMPORTANCIA DEL PICUDO RAYADO, Metamasius hemipterus L., EN CAÑA DE AZÚCAR I. INTRODUCCION Jorge Mendoza Mora 1 Alfonso Ayora Rodríguez 2 Darío Gualle Alvarado 3 El picudo rayado de
DETERMINACION DE LA IMPORTANCIA DEL PICUDO RAYADO, Metamasius hemipterus L., EN CAÑA DE AZÚCAR I. INTRODUCCION Jorge Mendoza Mora 1 Alfonso Ayora Rodríguez 2 Darío Gualle Alvarado 3 El picudo rayado de
PRODUCCIÓN DE SEMILLA COMERCIAL DE HONGOS COMESTIBLES Y MEDICINALES
 Proyecto: Adaptación e implementación de cinco cepas de hongos comestibles en diferentes subproductos agrícolas para mejorar la productividad y competitividad de ASOFUNGICOL en el Huila PRODUCCIÓN DE SEMILLA
Proyecto: Adaptación e implementación de cinco cepas de hongos comestibles en diferentes subproductos agrícolas para mejorar la productividad y competitividad de ASOFUNGICOL en el Huila PRODUCCIÓN DE SEMILLA
Métodos de aislamiento
 Métodos de aislamiento Aislamiento de hongos y bacterias Unidad de Fitopatología Dto. de Protección Vegetal Facultad de Agronomía. Dr. Pedro Mondino Métodos de aislamiento Técnicas de Aislamiento de hongos
Métodos de aislamiento Aislamiento de hongos y bacterias Unidad de Fitopatología Dto. de Protección Vegetal Facultad de Agronomía. Dr. Pedro Mondino Métodos de aislamiento Técnicas de Aislamiento de hongos
Instructivo. Manejo de los Residuos Infecciosos
 Página 1 de 5 1. Objetivo Describir las actividades necesarias (clasificación, almacenamiento, tratamiento y eliminación), para realizar el manejo de los residuos infeciosos. 2. Alcance Se aplica a todas
Página 1 de 5 1. Objetivo Describir las actividades necesarias (clasificación, almacenamiento, tratamiento y eliminación), para realizar el manejo de los residuos infeciosos. 2. Alcance Se aplica a todas
PREPARACIÓN DE MEDIOS DE CULTIVO
 Introducción Clasificación de los medios de cultivo Almacenamiento de los medios de cultivo Trabajo Práctico Nº 6 PREPARACIÓN DE MEDIOS DE CULTIVO Objetivo Fundamento Procedimiento Resultados Bibliografía
Introducción Clasificación de los medios de cultivo Almacenamiento de los medios de cultivo Trabajo Práctico Nº 6 PREPARACIÓN DE MEDIOS DE CULTIVO Objetivo Fundamento Procedimiento Resultados Bibliografía
LABORATORIO DE MICROBIOLOGÍA EXPERIMENTAL Grupo 2 (10:00 13:00 hrs) Semestre Profesores: Guadalupe Tsuzuki Reyes y Rosalba Esquivel-Cote
 Semana 2 Semana 1 LABORATORIO DE EXPERIMENTAL Grupo 2 (10:00 13:00 hrs) Semestre 2013-2 Profesores: Guadalupe Tsuzuki Reyes y Rosalba Esquivel-Cote CALENDARIO DE ACTIVIDADES UNIDAD Lunes 28 ENERO Miércoles
Semana 2 Semana 1 LABORATORIO DE EXPERIMENTAL Grupo 2 (10:00 13:00 hrs) Semestre 2013-2 Profesores: Guadalupe Tsuzuki Reyes y Rosalba Esquivel-Cote CALENDARIO DE ACTIVIDADES UNIDAD Lunes 28 ENERO Miércoles
Control de calidad en los procesos de producción de hongos entomopatógenos y del parasitoide Cotesia flavipes en Costa Rica.
 Control de calidad en los procesos de producción de hongos entomopatógenos y del parasitoide Cotesia flavipes en Costa Rica. Resumen Biol. Laura María Castro Alfaro* Es importante implementar no solo un
Control de calidad en los procesos de producción de hongos entomopatógenos y del parasitoide Cotesia flavipes en Costa Rica. Resumen Biol. Laura María Castro Alfaro* Es importante implementar no solo un
PRACTICA Núm. 18 INVESTIGACION DE COLIFORMES TOTALES Y FECALES EN AGUA RESIDUAL
 I. OBJETIVO PRACTICA Núm. 18 INVESTIGACION DE COLIFORMES TOTALES Y FECALES EN AGUA RESIDUAL Determinar la presencia de coliformes totales y fecales en agua residual por el método del Número Más Probable,
I. OBJETIVO PRACTICA Núm. 18 INVESTIGACION DE COLIFORMES TOTALES Y FECALES EN AGUA RESIDUAL Determinar la presencia de coliformes totales y fecales en agua residual por el método del Número Más Probable,
Dr. Oscar Gutiérrez Coronado Microbiologia Práctica No. 1 Preparación y esterilización de materiales y medios de cultivo
 Dr. Oscar Gutiérrez Coronado Microbiologia Práctica No. 1 Preparación y esterilización de materiales y medios de cultivo Objetivos. Que el alumno conozca los principios generales de las técnicas de esterilización
Dr. Oscar Gutiérrez Coronado Microbiologia Práctica No. 1 Preparación y esterilización de materiales y medios de cultivo Objetivos. Que el alumno conozca los principios generales de las técnicas de esterilización
En la naturaleza los microorganismos se encuentran en poblaciones mixtas de varios tipos. Para todos los estudios llevados a cabo en el laboratorio
 En la naturaleza los microorganismos se encuentran en poblaciones mixtas de varios tipos. Para todos los estudios llevados a cabo en el laboratorio de microbiología se requiere un cultivo axénico, es decir,
En la naturaleza los microorganismos se encuentran en poblaciones mixtas de varios tipos. Para todos los estudios llevados a cabo en el laboratorio de microbiología se requiere un cultivo axénico, es decir,
UNIVERSIDAD PEDAGOGICA Y TECNOLOGICA DE COLOMBIA FITOPATOLOGIA GENERAL GUIA PARA LA OBSERVACION MICROSCOPICA DE HONGOS FITOPATÓGENOS
 UNIVERSIDAD PEDAGOGICA Y TECNOLOGICA DE COLOMBIA FITOPATOLOGIA GENERAL GUIA PARA LA OBSERVACION MICROSCOPICA DE HONGOS FITOPATÓGENOS INTRODUCCIÓN. Para el diagnóstico y estudio de enfermedades, en la mayoría
UNIVERSIDAD PEDAGOGICA Y TECNOLOGICA DE COLOMBIA FITOPATOLOGIA GENERAL GUIA PARA LA OBSERVACION MICROSCOPICA DE HONGOS FITOPATÓGENOS INTRODUCCIÓN. Para el diagnóstico y estudio de enfermedades, en la mayoría
CURSO DE CONTROL BIOLÓGICO DE PATÓGENOS DE PLANTAS
 CURSO DE CONTROL BIOLÓGICO DE PATÓGENOS DE PLANTAS Introducción: Se considera que en la actualidad el Control Biológico de las enfermedades de plantas ha tomado una trascendental importancia. Esto es debido
CURSO DE CONTROL BIOLÓGICO DE PATÓGENOS DE PLANTAS Introducción: Se considera que en la actualidad el Control Biológico de las enfermedades de plantas ha tomado una trascendental importancia. Esto es debido
PRACTICA Núm. 12 AISLAMIENTO DE 2 MICROORGANISMOS Y OBTENCION DE UN CULTIVO AXENICO
 PRACTICA Núm. 12 AISLAMIENTO DE 2 MICROORGANISMOS Y OBTENCION DE UN CULTIVO AXENICO I. OBJETIVO Aislar dos microorganismos por la técnica de siembra de dilución por estría en placa de agar y obtener un
PRACTICA Núm. 12 AISLAMIENTO DE 2 MICROORGANISMOS Y OBTENCION DE UN CULTIVO AXENICO I. OBJETIVO Aislar dos microorganismos por la técnica de siembra de dilución por estría en placa de agar y obtener un
GUÍA DE LABORATORIO Nº 1 MEDIOS DE CULTIVO. OBJETIVO Comprender la utilidad de los medios de cultivo en el trabajo microbiológico.
 GUÍA DE LABORATORIO Nº 1 MEDIOS DE CULTIVO OBJETIVO Comprender la utilidad de los medios de cultivo en el trabajo microbiológico. MATERIALES Placas de agar sangre y agar McConkey. Tubos con agar TSI, agar
GUÍA DE LABORATORIO Nº 1 MEDIOS DE CULTIVO OBJETIVO Comprender la utilidad de los medios de cultivo en el trabajo microbiológico. MATERIALES Placas de agar sangre y agar McConkey. Tubos con agar TSI, agar
Manejo del hongo en el laboratorio
 Guía Práctica 8 Sclerotium rolfsii Manejo del hongo en el laboratorio Contenido Guillermo Castellanos, Experto en Investigación 2 Carlos Jara, Ing. Agr. M.Sc., Asociado en Investigación Gloria Mosquera,
Guía Práctica 8 Sclerotium rolfsii Manejo del hongo en el laboratorio Contenido Guillermo Castellanos, Experto en Investigación 2 Carlos Jara, Ing. Agr. M.Sc., Asociado en Investigación Gloria Mosquera,
Laboratorio Bromatología Balanzas Analíticas
 Laboratorio Bromatología Balanzas Analíticas Instrumentos de medida de peso con valor de precisión de lectura de 0.0001 g a 260 g y 0.001 a 220 g Laboratorio Bromatología Mufla Equipo utilizado para incinerar
Laboratorio Bromatología Balanzas Analíticas Instrumentos de medida de peso con valor de precisión de lectura de 0.0001 g a 260 g y 0.001 a 220 g Laboratorio Bromatología Mufla Equipo utilizado para incinerar
UNIVERSIDAD DE CIENCIAS Y ARTES DE CHIAPAS
 1 FACULTAD DE CIENCIAS DE LA NUTRICIÓN Y ALIMENTOS LICENCIATURA EN NUTRIOLOGÍA MANUAL DE PRÁCTICAS PARA LA EXPERIENCIA ACADÉMICA MICROBIOLOGÍA DE ALIMENTOS ELABORO: M. EN C. GILBER VELA GUTIÉRREZ Y M.
1 FACULTAD DE CIENCIAS DE LA NUTRICIÓN Y ALIMENTOS LICENCIATURA EN NUTRIOLOGÍA MANUAL DE PRÁCTICAS PARA LA EXPERIENCIA ACADÉMICA MICROBIOLOGÍA DE ALIMENTOS ELABORO: M. EN C. GILBER VELA GUTIÉRREZ Y M.
RECOPILADO POR: EL PROGRAMA UNIVERSITARIO DE ALIMENTOS
 NMX-F-187-1978. DETERMINACIÓN DEL NÚMERO MÁS PROBABLE DE GÉRMENES. METHOD OF TEST FOR GERMS MOST PROBABLE NUMBER. NORMAS MEXICANAS. DIRECCIÓN GENERAL DE NORMAS. PREFACIO En la elaboración de esta Norma
NMX-F-187-1978. DETERMINACIÓN DEL NÚMERO MÁS PROBABLE DE GÉRMENES. METHOD OF TEST FOR GERMS MOST PROBABLE NUMBER. NORMAS MEXICANAS. DIRECCIÓN GENERAL DE NORMAS. PREFACIO En la elaboración de esta Norma
PROCEDIMIENTO ENUMERACION DE LEVADURAS Y MOHOS EN ALIMENTOS BAM ONLINE
 PRT-712.02-048 Página 1 de 7 1. OBJETIVO Detectar el número de unidades formadoras de colonias (ufc) de levaduras y de mohos en el alimento 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a
PRT-712.02-048 Página 1 de 7 1. OBJETIVO Detectar el número de unidades formadoras de colonias (ufc) de levaduras y de mohos en el alimento 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a
05/01/ Prof. Luis Bautista Universidad del Táchira UNET
 05/01/2010 1 Prof. Luis Bautista Universidad del Táchira UNET 05/01/2010 2 05/01/2010 3 4 Es el uso racional y adecuado de organismos vivos benéficos para el combate de insectos plaga. Uso de enemigos
05/01/2010 1 Prof. Luis Bautista Universidad del Táchira UNET 05/01/2010 2 05/01/2010 3 4 Es el uso racional y adecuado de organismos vivos benéficos para el combate de insectos plaga. Uso de enemigos
y desinfección. Medios de cultivo. Objetivos Métodos de esterilización Definiciones Calor seco Calor seco MECÁNICOS FISICOS: QUIMICOS
 Métodos de esterilización y desinfección. n. Medios de cultivo. Curso: Diagnósticos en Fitopatología 17 de setiembre de 2015 Ing. Agr. MSc. Vivienne Gepp Objetivos Familiarizarse con los procesos de desinfección
Métodos de esterilización y desinfección. n. Medios de cultivo. Curso: Diagnósticos en Fitopatología 17 de setiembre de 2015 Ing. Agr. MSc. Vivienne Gepp Objetivos Familiarizarse con los procesos de desinfección
6. 5. Trazabilidad del proceso de esterilización
 6. 5. Trazabilidad del proceso de esterilización El proceso de esterilización sólo puede garantizarse mediante la monitorización de controles de rutina físicos, químicos o biológicos; algunos son complejos
6. 5. Trazabilidad del proceso de esterilización El proceso de esterilización sólo puede garantizarse mediante la monitorización de controles de rutina físicos, químicos o biológicos; algunos son complejos
1ª PRÁCTICA DE MICROBIOLOGÍA:
 1ª PRÁCTICA DE MICROBIOLOGÍA: INTRODUCCIÓN A LAS TÉCNICAS DE CULTIVO EN MICROBIOLOGÍA (O COMO HACER VISIBLES ORGANISMOS INVISIBLES) INTRODUCCIÓN El objetivo de esta práctica es aislar y observar algunos
1ª PRÁCTICA DE MICROBIOLOGÍA: INTRODUCCIÓN A LAS TÉCNICAS DE CULTIVO EN MICROBIOLOGÍA (O COMO HACER VISIBLES ORGANISMOS INVISIBLES) INTRODUCCIÓN El objetivo de esta práctica es aislar y observar algunos
PRÁCTICA No. 4 Métodos de cultivo y descripción morfológica de hongos Introducción
 PRÁCTICA No. 4 Métodos de cultivo y descripción morfológica de hongos Objetivos. Que el alumno aprenda las técnicas de cultivo y manipulación de diferentes tipos de hongos. Que el estudiante conozca las
PRÁCTICA No. 4 Métodos de cultivo y descripción morfológica de hongos Objetivos. Que el alumno aprenda las técnicas de cultivo y manipulación de diferentes tipos de hongos. Que el estudiante conozca las
PRÁCTICO N 4. Análisis de fertilidad del suelo
 PRÁCTICO N 4 Análisis de fertilidad del suelo OBJETIVOS Conocer las técnicas actuales de recuento de microorganismos. Conocer la importancia del monitoreo de abundancia, actividad y diversidad de los microorganismos
PRÁCTICO N 4 Análisis de fertilidad del suelo OBJETIVOS Conocer las técnicas actuales de recuento de microorganismos. Conocer la importancia del monitoreo de abundancia, actividad y diversidad de los microorganismos
Oferta tecnológica: Uso del quitosano para incrementar la esporulación de hongos
 Oferta tecnológica: Uso del quitosano para incrementar la esporulación de hongos Oferta tecnológica: Uso del quitosano para incrementar la esporulación de hongos RESUMEN El grupo de investigación ha desarrollado
Oferta tecnológica: Uso del quitosano para incrementar la esporulación de hongos Oferta tecnológica: Uso del quitosano para incrementar la esporulación de hongos RESUMEN El grupo de investigación ha desarrollado
Guía. Producción artesanal de Paecilomyces lilacinus para el control de nematodos
 Guía Producción artesanal de Paecilomyces lilacinus para el control de nematodos Guía Producción artesanal de Paecilomyces lilacinus para el control de nematodos (Borrador) UNA, UCATSE, UCOSEMUN, APROFOSC,
Guía Producción artesanal de Paecilomyces lilacinus para el control de nematodos Guía Producción artesanal de Paecilomyces lilacinus para el control de nematodos (Borrador) UNA, UCATSE, UCOSEMUN, APROFOSC,
Para la elaboración de la bebida láctea fesmentada se siguió el siguiente proceso metodológico. Aislamiento de Bacterias Ácido Lácticas (BAL)
 Desarrollo metodológico de elaboración de los productos Para la elaboración de la bebida láctea fesmentada se siguió el siguiente proceso metodológico 1ª etapa Aislamiento de Bacterias Ácido Lácticas (BAL)
Desarrollo metodológico de elaboración de los productos Para la elaboración de la bebida láctea fesmentada se siguió el siguiente proceso metodológico 1ª etapa Aislamiento de Bacterias Ácido Lácticas (BAL)
HONGOS ENTOMOPATÓGENOS PARA EL CONTROL DE HORMIGAS CORTADORAS
 HONGOS ENTOMOPATÓGENOS PARA EL CONTROL DE HORMIGAS CORTADORAS Laboratorio de Micología Facultad de Ciencias/Facultad de Ingeniería Sandra Lupo Lina Bettucci Susana Tiscornia Belen Corallo Alicia Sanchez
HONGOS ENTOMOPATÓGENOS PARA EL CONTROL DE HORMIGAS CORTADORAS Laboratorio de Micología Facultad de Ciencias/Facultad de Ingeniería Sandra Lupo Lina Bettucci Susana Tiscornia Belen Corallo Alicia Sanchez
3. Para preparar disoluciones de concentración molar específica, qué tipo de material de vidrio se recomienda usar?
 Equipo: Práctica 11: Preparación de disoluciones Preguntas a responder al final de la sesión En la preparación de disoluciones Para cuáles expresiones de concentración es fundamental conocer el volumen
Equipo: Práctica 11: Preparación de disoluciones Preguntas a responder al final de la sesión En la preparación de disoluciones Para cuáles expresiones de concentración es fundamental conocer el volumen
BUENAS PRÁCTICAS DE MUESTREO PARA LA RECOLECCION DE AGUA PARA EL ANALISIS MICROBIOLOGICO
 BUENAS PRÁCTICAS DE MUESTREO PARA LA RECOLECCION DE AGUA PARA EL ANALISIS MICROBIOLOGICO OBJETIVO Asegurar las condiciones de las tareas de toma de muestra de aguas a las que luego se les realizará análisis
BUENAS PRÁCTICAS DE MUESTREO PARA LA RECOLECCION DE AGUA PARA EL ANALISIS MICROBIOLOGICO OBJETIVO Asegurar las condiciones de las tareas de toma de muestra de aguas a las que luego se les realizará análisis
PLANIFICACIÓN DE SESIÓN DE APRENDIZAJE
 PLANIFICACIÓN DE SESIÓN DE APRENDIZAJE GRADO UNIDAD SESIÓN HORAS CUARTO 2 6/9 3 TÍTULO DE LA SESIÓN La energía que impulsa la vida APRENDIZAJES ESPERADOS COMPETENCIAS CAPACIDADES INDICADORES Indaga, mediante
PLANIFICACIÓN DE SESIÓN DE APRENDIZAJE GRADO UNIDAD SESIÓN HORAS CUARTO 2 6/9 3 TÍTULO DE LA SESIÓN La energía que impulsa la vida APRENDIZAJES ESPERADOS COMPETENCIAS CAPACIDADES INDICADORES Indaga, mediante
Titulo: Obtención de un nuevo sustrato para el desarrollo de microorganismos utilizados
 Titulo: Obtención de un nuevo sustrato para el desarrollo de microorganismos utilizados para el control de plagas y enfermedades en la caña de azúcar y otros cultivos. Autores: Flora Reyes González Roberto
Titulo: Obtención de un nuevo sustrato para el desarrollo de microorganismos utilizados para el control de plagas y enfermedades en la caña de azúcar y otros cultivos. Autores: Flora Reyes González Roberto
PRÁCTICO N 3. Técnicas para la observación, aislamiento y conservación de microorganismos
 PRÁCTICO N 3 Técnicas para la observación, aislamiento y conservación de microorganismos Objetivos Conocer el manejo del microscopio óptico, sus partes y utilidad en el laboratorio de microbiología. Conocer
PRÁCTICO N 3 Técnicas para la observación, aislamiento y conservación de microorganismos Objetivos Conocer el manejo del microscopio óptico, sus partes y utilidad en el laboratorio de microbiología. Conocer
Métodos de inoculación
 Métodos de inoculación Curso: Métodos en fitopatología Unidad de Fitopatología Dto. de Protección Vegetal Facultad de Agronomía. Dr. Pedro Mondino Inoculación en plantas La inoculación en plantas la realizamos
Métodos de inoculación Curso: Métodos en fitopatología Unidad de Fitopatología Dto. de Protección Vegetal Facultad de Agronomía. Dr. Pedro Mondino Inoculación en plantas La inoculación en plantas la realizamos
METODOLOGÍA PARA LA CUANTIFICACIÓN DE INDIVIDUOS DEL ÁCARO DE LA CAÑA DE AZÚCAR Abacarus sacchari Channabasavanna
 DIRECCIÓN DE INVESTIGACIÓN Y EXTENSIÓN DE LA CAÑA DE AZÚCAR DEPARTAMENTO DE ENTOMOLOGÍA Y VERTEBRADOS METODOLOGÍA PARA LA CUANTIFICACIÓN DE INDIVIDUOS DEL ÁCARO DE LA CAÑA DE AZÚCAR Abacarus sacchari Channabasavanna
DIRECCIÓN DE INVESTIGACIÓN Y EXTENSIÓN DE LA CAÑA DE AZÚCAR DEPARTAMENTO DE ENTOMOLOGÍA Y VERTEBRADOS METODOLOGÍA PARA LA CUANTIFICACIÓN DE INDIVIDUOS DEL ÁCARO DE LA CAÑA DE AZÚCAR Abacarus sacchari Channabasavanna
Valoración de desinfectantes. Método de diluciónneutralización.
 A. ÁLVAREZ ALCÁNTARA, E. ESPIGARES RODRÍGUEZ y R. GÁLVEZ VARGAS 1 Higiene y Sanidad Ambiental, 1: 1-5 (2001) Valoración de desinfectantes. Método de diluciónneutralización. A. Álvarez Alcántara, E. Espigares
A. ÁLVAREZ ALCÁNTARA, E. ESPIGARES RODRÍGUEZ y R. GÁLVEZ VARGAS 1 Higiene y Sanidad Ambiental, 1: 1-5 (2001) Valoración de desinfectantes. Método de diluciónneutralización. A. Álvarez Alcántara, E. Espigares
CAPÍTULO 2 MATERIALES Y MÉTODOS. En los experimentos de desinfección conducidos en este proyecto se utilizaron
 CAPÍTULO 2 MATERIALES Y MÉTODOS 2.1 Preparación de Microorganismos En los experimentos de desinfección conducidos en este proyecto se utilizaron esporas de B. subtilis. La Tabla 2.1 muestra una relación
CAPÍTULO 2 MATERIALES Y MÉTODOS 2.1 Preparación de Microorganismos En los experimentos de desinfección conducidos en este proyecto se utilizaron esporas de B. subtilis. La Tabla 2.1 muestra una relación
VII. MATERIALES Y MÉTODOS
 VII. MATERIALES Y MÉTODOS 7.1 DIAGRAMA DE TRABAJO Material biológico Saccharomyces cerevisiae UDLAP-07 y CM-05 Resiembra en papa dextrosa agar para verificar pureza y viabilidad Curva de crecimiento en
VII. MATERIALES Y MÉTODOS 7.1 DIAGRAMA DE TRABAJO Material biológico Saccharomyces cerevisiae UDLAP-07 y CM-05 Resiembra en papa dextrosa agar para verificar pureza y viabilidad Curva de crecimiento en
ACTIVIDAD BACTERIOSTÁTICA DEL PROPÓLEO VERDE DEL ESTADO DE MINAS GERAIS (BRASIL) CONTRA ESPORAS DE PAENIBACILLUS LARVAE
 ACTIVIDAD BACTERIOSTÁTICA DEL PROPÓLEO VERDE DEL ESTADO DE MINAS GERAIS (BRASIL) CONTRA ESPORAS DE PAENIBACILLUS LARVAE Esther Margarida Alves Ferreira Bastos 1 ; Moreira, A.C.P. 1 ; Scoaris, D.O. 1 1
ACTIVIDAD BACTERIOSTÁTICA DEL PROPÓLEO VERDE DEL ESTADO DE MINAS GERAIS (BRASIL) CONTRA ESPORAS DE PAENIBACILLUS LARVAE Esther Margarida Alves Ferreira Bastos 1 ; Moreira, A.C.P. 1 ; Scoaris, D.O. 1 1
PROCEDIMIENTO ENUMERACION DE LEVADURAS Y MOHOS EN ALIMENTOS BAM ONLINE
 PRT-712.02-048 Página 1 de 7 1. OBJETIVO Detectar el número de unidades formadoras de colonias (ufc) de levaduras y de mohos en el alimento 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a
PRT-712.02-048 Página 1 de 7 1. OBJETIVO Detectar el número de unidades formadoras de colonias (ufc) de levaduras y de mohos en el alimento 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a
AISLAMIENTO DE MICROORGANISMOS
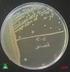 PRÁCTICA5 AISLAMIENTO DE MICROORGANISMOS Introducción En la naturaleza, la mayoría de los microorganismos no se encuentran aislados, sino integrados en poblaciones mixtas. Para llevar a cabo el estudio
PRÁCTICA5 AISLAMIENTO DE MICROORGANISMOS Introducción En la naturaleza, la mayoría de los microorganismos no se encuentran aislados, sino integrados en poblaciones mixtas. Para llevar a cabo el estudio
PROCEDIMIENTO DE TOMA Y PRESERVACION DE MUESTRAS DE AGUA POTABLE
 Nit. 900041159-2 PROCEDIMIENTO DE TOMA Y PRESERVACION DE MUESTRAS DE AGUA POTABLE La metodología utilizada para colectar las muestras, provenientes de un sistema de distribución de agua para consumo humano,
Nit. 900041159-2 PROCEDIMIENTO DE TOMA Y PRESERVACION DE MUESTRAS DE AGUA POTABLE La metodología utilizada para colectar las muestras, provenientes de un sistema de distribución de agua para consumo humano,
El Efecto de los desinfectantes y antisépticos en el crecimiento bacteriano
 PANAMERICAN SCHOOL Algo más que educación: Un reto al futuro, sin fronteras Estudiante: Grado: El Efecto de los desinfectantes y antisépticos en el crecimiento bacteriano Introducción: Hay tres tipos de
PANAMERICAN SCHOOL Algo más que educación: Un reto al futuro, sin fronteras Estudiante: Grado: El Efecto de los desinfectantes y antisépticos en el crecimiento bacteriano Introducción: Hay tres tipos de
Manejo del hongo en el laboratorio
 Guía Práctica 7 Rhizoctonia solani Enfermedad: Pudrición radical por Rizoctonia Manejo del hongo en el laboratorio Guillermo Castellanos, Experto en Investigación 2 Carlos Jara, Ing. Agr. M.Sc., Asociado
Guía Práctica 7 Rhizoctonia solani Enfermedad: Pudrición radical por Rizoctonia Manejo del hongo en el laboratorio Guillermo Castellanos, Experto en Investigación 2 Carlos Jara, Ing. Agr. M.Sc., Asociado
Técnicas de monitoreo para la detección de microorganismos en el medio ambiente
 Técnicas de monitoreo para la detección de microorganismos en el medio ambiente Gloria Alicia Figueroa Aguilar Condiciones Ambientales REQUISITO: El laboratorio debe asegurarse que las condiciones ambientales,
Técnicas de monitoreo para la detección de microorganismos en el medio ambiente Gloria Alicia Figueroa Aguilar Condiciones Ambientales REQUISITO: El laboratorio debe asegurarse que las condiciones ambientales,
REPRODUCCION DE ORQUIDEAS 2016
 REPRODUCCION DE ORQUIDEAS 2016 Cómo se reproducen las orquídeas: Resumen: 1) De semilla. 2) De la vara floral, (Phalaenopsis). 3) De la caña, (Dendrobium). 4) De un meristema Elegir plantas adultas, fuertes
REPRODUCCION DE ORQUIDEAS 2016 Cómo se reproducen las orquídeas: Resumen: 1) De semilla. 2) De la vara floral, (Phalaenopsis). 3) De la caña, (Dendrobium). 4) De un meristema Elegir plantas adultas, fuertes
RECOPILADO POR: EL PROGRAMA UNIVERSITARIO DE ALIMENTOS
 NMX-F-286-1992. ALIMENTOS. PREPARACIÓN Y DILUCIÓN DE MUESTRAS DE ALIMENTOS PARA ANÁLISIS MICROBIOLÓGICOS. FOODS. PREPARATION AND DILUTION OF FOOD SAMPLES FOR MICROBIOLOGICAL ANALYSIS. NORMAS MEXICANAS.
NMX-F-286-1992. ALIMENTOS. PREPARACIÓN Y DILUCIÓN DE MUESTRAS DE ALIMENTOS PARA ANÁLISIS MICROBIOLÓGICOS. FOODS. PREPARATION AND DILUTION OF FOOD SAMPLES FOR MICROBIOLOGICAL ANALYSIS. NORMAS MEXICANAS.
GUÍA REALIZACIÓN DE CULTIVOS MICROBIOLÓGICOS
 ESCUELA DE SALUD GUÍA REALIZACIÓN DE CULTIVOS MICROBIOLÓGICOS DIRIGIDO A ALUMNOS DE: Técnico de laboratorio Clínico y Banco de Sangre Técnico de Enfermería Técnico de Radiodiagnóstico y Radioterapia Informática
ESCUELA DE SALUD GUÍA REALIZACIÓN DE CULTIVOS MICROBIOLÓGICOS DIRIGIDO A ALUMNOS DE: Técnico de laboratorio Clínico y Banco de Sangre Técnico de Enfermería Técnico de Radiodiagnóstico y Radioterapia Informática
MINISTERIO DE AGRICULTURA Y GANADERÍA ESCUELA NACIONAL DE AGRICULTURA ROBERTO QUIÑÓNEZ
 MINISTERIO DE AGRICULTURA Y GANADERÍA ESCUELA NACIONAL DE AGRICULTURA ROBERTO QUIÑÓNEZ MICROPROPAGACIÓN DE CAÑA DE AZÚCAR Saccharum Officinarum ETAPA I 1.2. COLECTA DE YEMAS. - Se seleccionan varas que
MINISTERIO DE AGRICULTURA Y GANADERÍA ESCUELA NACIONAL DE AGRICULTURA ROBERTO QUIÑÓNEZ MICROPROPAGACIÓN DE CAÑA DE AZÚCAR Saccharum Officinarum ETAPA I 1.2. COLECTA DE YEMAS. - Se seleccionan varas que
Título de la gráfica: Crecimiento/ No crecimiento
 Resultados de la semana anterior (TSB) Título de la gráfica: # tubo TSB 1-24 Crecimiento/ No crecimiento Descripción del crecimiento Resultados de la semana anterior (TSA slant) Título de la gráfica: tubo
Resultados de la semana anterior (TSB) Título de la gráfica: # tubo TSB 1-24 Crecimiento/ No crecimiento Descripción del crecimiento Resultados de la semana anterior (TSA slant) Título de la gráfica: tubo
PROCEDIMIENTO DE EVALUACIÓN Y ACREDITACIÓN DE LAS COMPETENCIAS PROFESIONALES CUESTIONARIO DE AUTOEVALUACIÓN PARA LAS TRABAJADORAS Y TRABAJADORES
 MINISTERIO DE EDUCACIÓN SECRETARÍA DE ESTADO DE EDUCACIÓN Y FORMACIÓN PROFESIONAL DIRECCIÓN GENERAL DE FORMACIÓN PROFESIONAL INSTITUTO NACIONAL DE LAS CUALIFICACIONES PROCEDIMIENTO DE EVALUACIÓN Y ACREDITACIÓN
MINISTERIO DE EDUCACIÓN SECRETARÍA DE ESTADO DE EDUCACIÓN Y FORMACIÓN PROFESIONAL DIRECCIÓN GENERAL DE FORMACIÓN PROFESIONAL INSTITUTO NACIONAL DE LAS CUALIFICACIONES PROCEDIMIENTO DE EVALUACIÓN Y ACREDITACIÓN
RepublicofEcuador EDICTOFGOVERNMENT±
 RepublicofEcuador EDICTOFGOVERNMENT± Inordertopromotepubliceducationandpublicsafety,equaljusticeforal, abeterinformedcitizenry,theruleoflaw,worldtradeandworldpeace, thislegaldocumentisherebymadeavailableonanoncommercialbasis,asit
RepublicofEcuador EDICTOFGOVERNMENT± Inordertopromotepubliceducationandpublicsafety,equaljusticeforal, abeterinformedcitizenry,theruleoflaw,worldtradeandworldpeace, thislegaldocumentisherebymadeavailableonanoncommercialbasis,asit
PRODUCCIÓN DE MICROALGAS.
 PRODUCCIÓN DE MICROALGAS. El cultivo de algas posee gran importancia para el adecuado desarrollo y manutención de las otras. Debido a que son sin más, la principal fuente de alimentación de las mismas,
PRODUCCIÓN DE MICROALGAS. El cultivo de algas posee gran importancia para el adecuado desarrollo y manutención de las otras. Debido a que son sin más, la principal fuente de alimentación de las mismas,
Biplaca que se utiliza para evaluar la contaminación microbiológica de las superficies (Paredes, Techos, Equipos, Pisos, etc.) o Líquidos.
 BIPLACA HYCHECK Biplaca que se utiliza para evaluar la contaminación microbiológica de las superficies (Paredes, Techos, Equipos, Pisos, etc.) o Líquidos. Son estadísticamente comparables a una Torunda
BIPLACA HYCHECK Biplaca que se utiliza para evaluar la contaminación microbiológica de las superficies (Paredes, Techos, Equipos, Pisos, etc.) o Líquidos. Son estadísticamente comparables a una Torunda
TRABAJO PRÁCTICO Nº 5 AÑO-SECCIÓN: EQUIPO: FECHA:
 República Bolivariana de Venezuela Ministerio del Poder Popular para la Educación U.E. Colegio Santo Tomás de Villanueva Departamento de Ciencias Cátedra: Ciencias Biológicas Año: 3 A, B y C Prof. Luis
República Bolivariana de Venezuela Ministerio del Poder Popular para la Educación U.E. Colegio Santo Tomás de Villanueva Departamento de Ciencias Cátedra: Ciencias Biológicas Año: 3 A, B y C Prof. Luis
INSTRUMENTOS BÁSICOS DE UN LABORATORIO
 INSTRUMENTOS BÁSICOS DE UN LABORATORIO Trasfondo y Contenido En un laboratorio se utiliza una amplia variedad de instrumentos o herramientas que, en su conjunto, se denominan material de laboratorio. Pueden
INSTRUMENTOS BÁSICOS DE UN LABORATORIO Trasfondo y Contenido En un laboratorio se utiliza una amplia variedad de instrumentos o herramientas que, en su conjunto, se denominan material de laboratorio. Pueden
Insecticida biológico
 Insecticida biológico Beauveria bassiana Características generales El producto contiene como principio activo conidios del hongo entomopatógeno Beauveria bassiana. Este hongo crece de forma natural en
Insecticida biológico Beauveria bassiana Características generales El producto contiene como principio activo conidios del hongo entomopatógeno Beauveria bassiana. Este hongo crece de forma natural en
Antes de comenzar el procesamiento, lavarse las manos y colocarse gorro, y guantes.
 Directrices Banco de Leche Humana Itinerario al Ingresar al BLH: 1) Control de temperatura de freezer (menor a -20 ºC) y estufa (36 +/- 1ºC) y registro el cuaderno correspondiente 2) Limpieza y Desinfección
Directrices Banco de Leche Humana Itinerario al Ingresar al BLH: 1) Control de temperatura de freezer (menor a -20 ºC) y estufa (36 +/- 1ºC) y registro el cuaderno correspondiente 2) Limpieza y Desinfección
COMO ABORDAR Y RESOLVER ASPECTOS PRÁCTICOS DE MICROBIOLOGÍA
 COMO ABORDAR Y RESOLVER ASPECTOS PRÁCTICOS DE MICROBIOLOGÍA 1. DILUCIONES Y CONCENTRACIONES. S LÍQUIDAS Y SÓLIDAS Inés Arana, Maite Orruño e Isabel Barcina Departamento Inmunología, Microbiología y Parasitología
COMO ABORDAR Y RESOLVER ASPECTOS PRÁCTICOS DE MICROBIOLOGÍA 1. DILUCIONES Y CONCENTRACIONES. S LÍQUIDAS Y SÓLIDAS Inés Arana, Maite Orruño e Isabel Barcina Departamento Inmunología, Microbiología y Parasitología
PROCEDIMIENTO TECNICA NMP STAPHYLOCOCCUS AUREUS EN ALIMENTOS. BAM ONLINE 2001
 PRT-712.02-025 Página 1 de 9 1. OBJETIVO Estimar la densidad de bacterias S. aureus en matrices de alimento o agua como indicador sanitario 2. CAMPO DE APLICACIÓN Y ALCANCE El método de NMP es recomendado
PRT-712.02-025 Página 1 de 9 1. OBJETIVO Estimar la densidad de bacterias S. aureus en matrices de alimento o agua como indicador sanitario 2. CAMPO DE APLICACIÓN Y ALCANCE El método de NMP es recomendado
Laboratorio Lavado y Arreglo de material
 1 de 5 TABLA DE CONTENIDO INDICE PÁGINA 1. PROCESO 2 2. RESPONSABLES 2 3. OBJETIVO GENERAL 2 4. ALCANCE 2 5. MARCO LEGAL 2 6. DESCRIPCIÓN DE LA ACTIVIDAD 3 7. INSUMOS, REACTIVOS Y EQUIPOS 4 8.1 Insumos
1 de 5 TABLA DE CONTENIDO INDICE PÁGINA 1. PROCESO 2 2. RESPONSABLES 2 3. OBJETIVO GENERAL 2 4. ALCANCE 2 5. MARCO LEGAL 2 6. DESCRIPCIÓN DE LA ACTIVIDAD 3 7. INSUMOS, REACTIVOS Y EQUIPOS 4 8.1 Insumos
UNIVERSIDAD TECNOLOGICA NACIONAL
 UNIVERSIDAD TECNOLOGICA NACIONAL FACULTAD REGIONAL ROSARIO DEPARTAMENTO DE INGENIERIA QUIMICA CATEDRA DE BIOTECNOLOGIA Trabajo práctico n 3 Siembra y recuento de microorganismos. 2009 Jefe de Cátedra:
UNIVERSIDAD TECNOLOGICA NACIONAL FACULTAD REGIONAL ROSARIO DEPARTAMENTO DE INGENIERIA QUIMICA CATEDRA DE BIOTECNOLOGIA Trabajo práctico n 3 Siembra y recuento de microorganismos. 2009 Jefe de Cátedra:
PRACTICA Núm. 19 DETERMINACION DE ESTREPTOCOCOS FECALES EN AGUA
 PRACTICA Núm. 19 DETERMINACION DE ESTREPTOCOCOS FECALES EN AGUA I. OBJETIVO Investigar la presencia de Estreptococos fecales en una muestra de agua mediante la técnica del Número Más Probable (NMP) usando
PRACTICA Núm. 19 DETERMINACION DE ESTREPTOCOCOS FECALES EN AGUA I. OBJETIVO Investigar la presencia de Estreptococos fecales en una muestra de agua mediante la técnica del Número Más Probable (NMP) usando
PREPARACIONES Y TINCIONES
 PREPARACIONES Y TINCIONES PREPARACIONES En fresco Temporales: Microcultivos de hongos, preparaciones de tejidos Fijas: Gram, Ziehl Nielsen, Sheaffer y fulton, SEM, TEM, naranja de acridina. CONTRASTE DE
PREPARACIONES Y TINCIONES PREPARACIONES En fresco Temporales: Microcultivos de hongos, preparaciones de tejidos Fijas: Gram, Ziehl Nielsen, Sheaffer y fulton, SEM, TEM, naranja de acridina. CONTRASTE DE
ANEXOS MEDIOS DE CULTIVO
 Caracterización de tres cepas de Beauveria brongniartii (Saccardo) Petch y su virulencia en Phthorimaea operculella (Zeller) y Symmetrischema tangolias (Gyen). Vargas Flores, Melisa Elisée Derechos reservados
Caracterización de tres cepas de Beauveria brongniartii (Saccardo) Petch y su virulencia en Phthorimaea operculella (Zeller) y Symmetrischema tangolias (Gyen). Vargas Flores, Melisa Elisée Derechos reservados
PRACTICA N 1 RECONOCIMIENTO DEL EQUIPO DE LABORATORIO
 PRACTICA N 1 RECONOCIMIENTO DEL EQUIPO DE LABORATORIO Objetivo: Conocer detalladamente cada instrumento utilizado en las prácticas de microbiología (forma, uso, material con el que está elaborado etc.).
PRACTICA N 1 RECONOCIMIENTO DEL EQUIPO DE LABORATORIO Objetivo: Conocer detalladamente cada instrumento utilizado en las prácticas de microbiología (forma, uso, material con el que está elaborado etc.).
CAPÍTULO IV 6. MATERIALES Y METODOS. Puré de manzana mínimamente procesado marca Santa Clara.
 6. MATERIALES Y METODOS 6.1. Materia prima Puré de manzana mínimamente procesado marca Santa Clara. Canela ( Cinnamoun cyminum), vainillina ( Sigma Chemical, Co, St. Luis, MO) y sorbato de potasio ( Sigma
6. MATERIALES Y METODOS 6.1. Materia prima Puré de manzana mínimamente procesado marca Santa Clara. Canela ( Cinnamoun cyminum), vainillina ( Sigma Chemical, Co, St. Luis, MO) y sorbato de potasio ( Sigma
MANUAL DE OPERACIONES. DIRECCIÓN DE INVESTIGACIÓN Fecha: JUN 15 SUBDIRECCIÓN DE INVESTIGACIÓN BIOMÉDICA MANUAL DE TINCIONES
 A Hoja: de 0 MANUAL DE TINCIONES Elaboró: Autorizó: Puesto QUÍMICO JEFE DE LABORATORIO Firma Hoja: 2 de 0. Propósito Establecer las técnicas y condiciones para la realización de tinciones utilizadas en
A Hoja: de 0 MANUAL DE TINCIONES Elaboró: Autorizó: Puesto QUÍMICO JEFE DE LABORATORIO Firma Hoja: 2 de 0. Propósito Establecer las técnicas y condiciones para la realización de tinciones utilizadas en
FORRAJE VERDE HIDROPONICO
 FORRAJE VERDE HIDROPONICO Ing. Agrónomo Ortiz Marín Walter Docente en el IESTP Huando Desde hace algunos años, en el instituto superior tecnológico Huando, se está produciendo el forraje verde hidropónico
FORRAJE VERDE HIDROPONICO Ing. Agrónomo Ortiz Marín Walter Docente en el IESTP Huando Desde hace algunos años, en el instituto superior tecnológico Huando, se está produciendo el forraje verde hidropónico
-9 Ampolletas Colilert - Franelas - Bata
 El día jueves 24 de mayo del año en curso se realizaron las pruebas de calidad del agua, utilizando el Método de Quanty Tray. Materiales: Elaborado por: Bitelio Daniel Ordoñez González, Prestado de Servicio
El día jueves 24 de mayo del año en curso se realizaron las pruebas de calidad del agua, utilizando el Método de Quanty Tray. Materiales: Elaborado por: Bitelio Daniel Ordoñez González, Prestado de Servicio
El primer paso del proceso de empaque es el vaciado
 Adrian Colodner INTA ALTO VALLE colodner.adrian@inta.gob.ar Sanitización del agua en el hidroinmersor El primer paso del proceso de empaque es el vaciado de los cajones bin en los que se transporta la
Adrian Colodner INTA ALTO VALLE colodner.adrian@inta.gob.ar Sanitización del agua en el hidroinmersor El primer paso del proceso de empaque es el vaciado de los cajones bin en los que se transporta la
MANUAL DE PRODUCCIÓN Y USO DE HONGOS ENTOMOPATÓGENOS
 MANUAL DE PRODUCCIÓN Y USO DE HONGOS ENTOMOPATÓGENOS Hilda Gómez Ramírez Anny Zapata Granja Enrique Torres Del Aguila Martín Tenorio Cantoral 2014 P á g i n a 2 CONTENIDO Páginas INTRODUCCIÓN 5 HONGOS
MANUAL DE PRODUCCIÓN Y USO DE HONGOS ENTOMOPATÓGENOS Hilda Gómez Ramírez Anny Zapata Granja Enrique Torres Del Aguila Martín Tenorio Cantoral 2014 P á g i n a 2 CONTENIDO Páginas INTRODUCCIÓN 5 HONGOS
ANEXO 1 Medios de cultivo y reconstitución de cepas
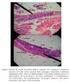 conservamos 31 ANEXO 1 Medios de cultivo y reconstitución de cepas Agar tripticasa de soya (TSA) -Triptona, digestión pancreática de caseína -Peptona de soya, digestión pancreática de harina de soya -Cloruro
conservamos 31 ANEXO 1 Medios de cultivo y reconstitución de cepas Agar tripticasa de soya (TSA) -Triptona, digestión pancreática de caseína -Peptona de soya, digestión pancreática de harina de soya -Cloruro
PRACTICA Núm. 6 TINCION DE FLAGELOS BACTERIANOS POR EL METODO DE LEIFSON
 PRACTICA Núm. 6 TINCION DE FLAGELOS BACTERIANOS POR EL METODO DE LEIFSON I. OBJETIVO Demostrar la presencia de flagelos mediante tinción y observar la movilidad que presentan algunas bacterias diferenciándola
PRACTICA Núm. 6 TINCION DE FLAGELOS BACTERIANOS POR EL METODO DE LEIFSON I. OBJETIVO Demostrar la presencia de flagelos mediante tinción y observar la movilidad que presentan algunas bacterias diferenciándola
Programa donde se inscribe la beca y/o la tesis: Interacciones biológicas: de las
 Titulo: Potencial uso simultáneo de micopatógenos biocontroladores de hormigas cortadoras de hojas. Autores: Natalia G. Armando, Jorge A. Marfetán, Patricia J. Folgarait Correo: ng.armando14@gmail.com
Titulo: Potencial uso simultáneo de micopatógenos biocontroladores de hormigas cortadoras de hojas. Autores: Natalia G. Armando, Jorge A. Marfetán, Patricia J. Folgarait Correo: ng.armando14@gmail.com
Obtención de Agentes de Control Biológico.
 Obtención de Agentes de Control Biológico. Métodos de aislamiento y selección Objetivos: de ACB Transmitir la importancia de los procesos de búsqueda y selección de ACB como base del éxito de un programa
Obtención de Agentes de Control Biológico. Métodos de aislamiento y selección Objetivos: de ACB Transmitir la importancia de los procesos de búsqueda y selección de ACB como base del éxito de un programa
PRÁCTICA # 01 PREPARACIÓN DE DISOLUCIONES
 REPÚBLICA BOLIVARIANA DE VENEZUELA MINISTERIO DEL PODER POPULAR PARA LA DEFENSA AVIACIÓN MILITAR VENEZOLANA U.E.A.M LIBERTADOR ASIGNATURA: QUÍMICA PROF(A): ANGÉLICA RODRÍGUEZ MARBELIS MELENDEZ CURSO: 4to
REPÚBLICA BOLIVARIANA DE VENEZUELA MINISTERIO DEL PODER POPULAR PARA LA DEFENSA AVIACIÓN MILITAR VENEZOLANA U.E.A.M LIBERTADOR ASIGNATURA: QUÍMICA PROF(A): ANGÉLICA RODRÍGUEZ MARBELIS MELENDEZ CURSO: 4to
Laboratorio Nacional de Salud Pública
 1. Tinción de Gram 2. Objeto y campo de aplicación La técnica de tinción de Gram se utiliza para la tinción de bacterias, levaduras y actinomicetos aerobios. Este procedimiento operativo estándar es aplicable
1. Tinción de Gram 2. Objeto y campo de aplicación La técnica de tinción de Gram se utiliza para la tinción de bacterias, levaduras y actinomicetos aerobios. Este procedimiento operativo estándar es aplicable
2. Observación de hongos de interés industrial
 2. Observación de hongos de interés industrial En esta práctica se realizarán observaciones en fresco de varios hongos de interés industrial. 2.1 Preparaciones para el estudio microscópico de los aislados
2. Observación de hongos de interés industrial En esta práctica se realizarán observaciones en fresco de varios hongos de interés industrial. 2.1 Preparaciones para el estudio microscópico de los aislados
BEAUVERIA BASSIANA, HONGO ENTOMOPATÓGENO PARA EL CONTROL BIOLÓGICO DE HORMIGAS CORTADORAS (YSAÚ)
 PROTOCOLOS PARA FORMULACIÓN Y APLICACIÓN DEL BIO-INSUMO: BEAUVERIA BASSIANA, HONGO ENTOMOPATÓGENO PARA EL CONTROL BIOLÓGICO DE HORMIGAS CORTADORAS (YSAÚ) Hernán Chiriboga P. Graciela Gómez B. Karla Garcés
PROTOCOLOS PARA FORMULACIÓN Y APLICACIÓN DEL BIO-INSUMO: BEAUVERIA BASSIANA, HONGO ENTOMOPATÓGENO PARA EL CONTROL BIOLÓGICO DE HORMIGAS CORTADORAS (YSAÚ) Hernán Chiriboga P. Graciela Gómez B. Karla Garcés
SECRETARIA DE COMERCIO FOMENTO INDUSTRIAL NORMA MEXICANA NMX-F PASTEL DE CARNE MEAAT PIE
 SECRETARIA DE COMERCIO Y FOMENTO INDUSTRIAL NORMA MEXICANA NMX-F-203-1971 PASTEL DE CARNE MEAAT PIE DIRECCION GENERAL DE NORMAS PASTEL DE CARNE MEAAT PIE 1 GENERALIDADES Y DEFINICIONES 1.1 Generalidades
SECRETARIA DE COMERCIO Y FOMENTO INDUSTRIAL NORMA MEXICANA NMX-F-203-1971 PASTEL DE CARNE MEAAT PIE DIRECCION GENERAL DE NORMAS PASTEL DE CARNE MEAAT PIE 1 GENERALIDADES Y DEFINICIONES 1.1 Generalidades
TRANSFERENCIAS ASÉPTICAS
 Introducción Objetivo Procedimiento Trabajo Práctico Nº 3 TRANSFERENCIAS ASÉPTICAS Resultados Observaciones Bibliografía INTRODUCCIÓN La inoculación de medios de cultivo y la manipulación de cultivos microbianos
Introducción Objetivo Procedimiento Trabajo Práctico Nº 3 TRANSFERENCIAS ASÉPTICAS Resultados Observaciones Bibliografía INTRODUCCIÓN La inoculación de medios de cultivo y la manipulación de cultivos microbianos
