TP3: Electroforesis en gel de poliacrilamida
|
|
|
- Andrea San Segundo Olivares
- hace 7 años
- Vistas:
Transcripción
1 TP3: Electroforesis en gel de poliacrilamida Objetivos Comparar las fracciones de proteínas obtenidas en el TP Nº2 mediante SDS-PAGE. Calcular la movilidad electroforética de diferentes bandas proteicas. Introducción La técnica de electroforesis en gel es un método para separar, identificar y purificar DNA, RNA o proteínas, entre las matrices más utilizadas se encuentra la de azarosa (para ácidos nucleicos) y la de poliacrilamida (para proteínas y ácidos nucleicos pequeños). La localización de la biomolécula en el gel puede ser determinada mediante la utilización de distintos colorantes que tienen afinidad específica por la biomolécula a resolver. El fenómeno denominado electroforesis sucede cuando una molécula con una carga neta en solución se desplaza por acción de una campo eléctrico; de esta manera la molécula migra hacia uno u otro electrodo según su carga: los aniones (-) irán hacia el ánodo (+) y los cationes (+) hacia el cátodo (-). En estas condiciones las moléculas disueltas migran a una velocidad proporcional a la relación carga:masa. Por lo tanto la velocidad de migración en estas condiciones a través del campo eléctrico dependerá de: carga neta, tamaño y forma de la molécula, fuerza del campo eléctrico, fuerza iónica, viscosidad y temperatura del medio v: velocidad de migración de la molécula v= Ez E: intensidad del campo eléctrico f z: carga neta de la molécula f: coeficiente de fricción (depende tanto de masa como de la forma de la molécula) Las separaciones electroforéticas generalmente se realizan sobre matrices que sirven de tamices moleculares que potencian la separación. Las moléculas más pequeñas que los poros se desplazan fácilmente a través de él, mientras que las de mayor tamaño quedan retenidas y las intermedias se desplazan con distinto grado de dificultad dependiendo de su tamaño. La forma, tamaño, porosidad y tipo de matriz del gel puede variar dependiendo del tamaño y la biomolécula a ser analizada. Independientemente del tipo de matriz elegida, la misma debe ser eléctricamente neutra, tal que no se produzca un flujo de solvente hacia uno u otro electrodo debido a la presencia de grupos cargados inmovilizados en la matriz (electro endósmosis) que disminuye la resolución de la muestra. Los geles de poliacrilamida son utilizados para separar la mayoría de las proteínas o pequeños oligonucleótidos. A los fines de este práctico se explicara únicamente la aplicabilidad de estos geles para la separación de proteínas. En presencia de radicales libres, que son proporcionados por el persulfato de amonio (APS) y estabilizados por el TEMED, se genera una reacción en cadena que es iniciada con monómeros 1
2 de acrilamida que polimeriza en largas cadenas que son entrecruzadas con la bis-acrilamida para formar la matriz del gel. Esta polimerización es inhibida por el oxígeno. Para la electroforesis en gel de poliacrilamida de muestras proteicas se puede utilizar un sistema de buffers continuo o discontinuo. El sistema continuo tiene una única clase de gel, el separador (separating) y usa el mismo buffer que el de corrida. El discontinuo esta formado por dos geles distintos. En la parte de arriba se coloca un gel separador con un tamaño de poro mayor (stacking) que sirve a diferencia del stacking sirve para concentrar las muestras (en una banda) antes de que ingresen al gel separador. Cada uno esta compuesto de un buffer que son distintos entre si y a su vez distinto que el de corrida. El sistema discontinuo otorga una mayor resolución ya que las proteínas ingresan como una banda discreta al gel de separación. La polimerización de los geles se realiza entre dos vidrios verticales, que funcionan como moldes, para dar un gel de 0,5, 0,75, 1 o 1,5 mm de espesor. Inmediatamente después de preparar la mezcla de archilamida/bisacrilamida, buffer, APS y temed, se coloca entre los vidrios el borde superior del gel se cubre con agua y para evitar el contacto con el oxígeno que inhibe la polimerización. SDS-PAGE (sodium dodecyl sulfate-polyacrylamide gel electrophoresis) La mayoría de las electroforesis analíticas de proteínas se llevan a cabo bajo condiciones que aseguren la disociación de las proteínas en sus subunidades individuales y que minimicen la agregación, para ello se utiliza la combinación de un detergente aniónico como el SDS (dodecilsulfato de sodio), un agente reductor (β-mercaptoetanol o DTT) y calor para disociar las proteínas. Los polipéptidos desnaturalizados unidos al SDS obtienen una carga neta (-), las moléculas de detergente se unen a razón de un SDS por cada 2 aminoácidos lo que otorga una carga proporcional a la masa de la proteína. El tratamiento conjunto de SDS (rompe uniones no covalentes) más el agente reductor (rompe puentes disulfuro) eliminan los efectos de las diferentes conformaciones de las proteínas tal que la longitud de la cadena, que refleja la masa, es la única que determina la velocidad de migración en una SDS-PAGE. Las proteínas de menor tamaño se resuelven en la parte inferior del gel, y las de mayor tamaño van quedando retrasadas al atravesar la malla del gel, observándose en la parte superior. En la siguiente tabla se muestra el rango de linealidad teniendo en cuenta el porcentaje de archilamida con que esté preparado el gel: Rango efectivo de separación en geles de SDS-PAGE acrilamida-bisacrilamida* (%) Rango lineal de separación (kda) , * La relación molar entre acrilamida y bisacrilamida es de 1:29 El desplazamiento de las cadenas polipeptídicas es proporcional al logaritmo de la masa, esto nos permite estimar el peso molecular de una proteína comparándola con la distancia de migración de un patrón de proteínas de peso molecular conocido (Markers). 2
3 Entonces, con los valores del marcador de peso molecular, se construye primero una curva de calibración donde se gráfica los log (PM) vs. el R f. El R f es la relación entre la distancia de migración de la banda proteica (d) y la longitud de corrida total del gel (I) o sea la distancia desde el borde superior del gel hasta el frente de corrida. Con estos valores se obtiene la ecuación lineal log(pm)=m x R f +b (m=pendiente; b=ordenada al origen) Luego se calcula el R f de la proteína incógnita y se extrapola en la curva el log (PM), y aplicando el antilogaritmo se obtiene el PM de la proteína incógnita Ejemplo: SDS-PAGE de extracto de proteínas totales de tres bacterias lácticas teñido con coomasie blue en separating gel 12%T 2.67%C. La primera u la última calle es el marcador de peso molecular (Sigma Marker Wide range, Sigma; las bandas son 205,0; 116,0; 97,4; 84,0; 66,0; 55,0; 46,0; 36,0; 29,0; 24,0; 20,1 y 14,2 kda). Las calles 1, 2, 3 fueron sembradas con tres diferentes extracctos de Enterococcus faecium ATCC14434; las calles 4, 5, 6 con tres extractos diferentes de Lactobacillus paracasei subsp. paracasei DSM4905; 7, 8 y 9 se sembraron tres extractos de Lactococcus lactis subsp. lactis DSM20481 PM (kda) Rf 205 0, ,3 97,4 0, ,4 66 0, , , ,7 29 0,9 24 0, ,4 84,0 66,0 55,0 46,0 36,0 29,0 24,0 20,1 Rf vs PM Curva de calibración Pm (KDa) Log(PM) 2,5 2 1,5 1 Log (PM) = -0,2239 Rf + 2,4045 R 2 = 0, ,1 0,2 0,3 0,4 0,5 0,6 0,7 0,8 0,9 1 Rf 0,5 0 0,1 0,2 0,3 0,4 0,5 0,6 0,7 0,8 0,9 1 Bibliografía Alberts B., Bray D., Lewis J., Raff M., Roberts K., Watson J.D. Biología Molecular de la Célula (1996) Omega. Lodish H, Baltimore D., Berk A., Zipursky S.L., Matsudaira P., Damell J. Molecular Cell Biology (1995) Scientific American Books.. Old R.W., Primrose S. B. Principios de manipulación genética (1987) Editorial Acribia S.A.. Maniatis, T., Fritsch, E.F. & Sambrook, J. Molecular cloning, A Laboratory Manual (1982) Cold Spring Harbor Laboratory. Rf 3
4 Procedimiento El práctico se iniciará sembrando geles prearmados 10) Preparar las muestras para sembrar, teniendo en cuenta que el volumen final para sembrar es 20 µl, que el sample buffer está 4X y que deben contener 1 µl de extracto de proteína si la cuantificación fue mayor a 50 mg/ml y 5 µl de extracto si fue menor. H 2 O µl Extracto de proteínas µl Buffer µl Volumen Final 20 µl 11) Colocar los geles en el soporte que porta los electrodos e introducirlo en la cuba. 12) Agregar running buffer en ambos compartimentos; asegurarse que los mismos no estén en contacto. 13) Sembrar 7 µl del marcador de peso molecular (MWM) y el total del volumen de cada una de las muestras. 14) Conectar a la fuente. Correr a 80 voltios hasta que las muestras entren en el separating gel y a 130 voltios hasta que el colorante del frente de corrida llegue al borde inferior del gel (aproximadamente 1,5 horas). 15) Una vez finalizada la corrida, apagar la fuente y desarmar cuidadosamente depositando el gel en un recipiente para efectuar la tinción. 16) Agregar la solución de Coomassie blue y teñir en agitación por 30 minutos. 17) Enjuagar con solución de destinción hasta que, al observar en un transiluminador, se distingan las bandas de proteínas y se vean azules contra un fondo claro. 18) Agregar H 2 0 destilada para frenar la destinción. 19) Escanear los geles y obtener los valores necesarios para calcular los Rf Sample buffer 4X: Para preparar 8 ml: 2 ml Tris-HCl 1,5M ph 6,8; 3.2 ml SDS 10% p/v; 1,6 ml Glicerol; 0,4 ml Bromofenol Blue 1% (p/v); 0,8 ml β-mercaptoetanol 14,3 M Solución de Coomasie Blue: Brillant Blue R-250 0,3% en Metanol:Acético:Agua (3:1:6) Solución de destinción: Metanol:Acético:Agua (3:1:6) Para practicar el armado de los geles (y que el protocolo esté completo!): 1) Armar el equipo según las indicaciones de las instructoras 4
5 PARA PREPARAR Y MANIPULAR LOS GELES DEBEN UTILIZARSE GUANTES YA QUE LA ACRILAMIDA ES NEUROTÓXICA. 2) SEPARATING GEL (7.5%): para un gel preparar 5 ml agregando los volúmenes indicados de cada componente en el orden dado, EXCEPTO EL APS Y EL TEMED que se agregan inmediatamente antes de colocar entre los vidrios: H 2 0 desionizada 2.4 ml Buffer Tris 1,5 M DH ml 10% SDS 50 µl 30% Acrilamida/Bis (29:1) 1.25 ml 10% APS 35 µl TEMED 5 µl 3) STACKING GEL (4%): preparar 5 ml, agregando los volúmenes indicados de cada componente en el orden dado EXCEPTO EL APS Y EL TEMED que se agregan inmediatamente antes de colocar entre los vidrios: H 2 0 desionizada 3 ml Buffer Tris 0,5 M ph ml 10% SDS 50 µl 30% Acrilamida/Bis (29:1) 0.7 ml 10% APS 35 µl TEMED 5 µl 4) Agregar el APS y el TEMED al Separating gel, agitar rápidamente y sembrar 3.7 ml entre los vidrios (puede hacerse sobre un borde, pegado a uno de los separadores) 5) Agregar inmediatamente H 2 0 desionizada con una pipeta Pasteur hasta el borde del vidrio más chico. Cerrar el tubo en el cual se preparó el gel para dejarlo como testigo de la polimerización (es decir, cuando polimerice el tuvo indicará que el gel entre los vidrios también ah polimerizado). Se pueden incubar a 37 C para acelerar la polimerización 6) Después de que haya gelificado, remover el agua y terminar de secar con trozos de papel de filtro. 7) Agregar APS y el TEMED al tubo del stacking gel y sembrarlo, dejando rebalsar apenas por el borde del vidrio. 8) Colocar enseguida el peine (que servirá para formar las calles donde se sembrarán las muestras). Cerrar el tubo en el que se preparó el gel para usarlo como testigo. Dejar polimerizar. 9) Sacar los peines y enjuagar con agua, eliminando los restos de gel, si quedaran. 5
TP3: Electroforesis en gel de poliacrilamida
 Objetivos TP3: Electroforesis en gel de poliacrilamida Comparar los perfiles proteicos obtenidos mediante SDS-PAGE. Calcular la movilidad electroforética de diferentes bandas proteicas. Introducción La
Objetivos TP3: Electroforesis en gel de poliacrilamida Comparar los perfiles proteicos obtenidos mediante SDS-PAGE. Calcular la movilidad electroforética de diferentes bandas proteicas. Introducción La
ELECTROFORESIS EN GEL DE POLIACRILAMIDA CON SDS SDS-PAGE
 1. FUNDAMENTO TEÓRICO ELECTROFORESIS EN GEL DE POLIACRILAMIDA CON SDS SDS-PAGE Departamento de Bioquímica La electroforesis es una técnica de separación de moléculas cargadas por migración en un campo
1. FUNDAMENTO TEÓRICO ELECTROFORESIS EN GEL DE POLIACRILAMIDA CON SDS SDS-PAGE Departamento de Bioquímica La electroforesis es una técnica de separación de moléculas cargadas por migración en un campo
ELECTROFORESIS EN GEL DE POLIACRILAMIDA CON SDS SDS-PAGE
 Departamento de Biología de Sistemas Unidad Docente de Bioquímica y Biología Molecular ELECTROFORESIS EN GEL DE POLIACRILAMIDA CON SDS SDS-PAGE 1. FUNDAMENTO TEÓRICO La electroforesis es una técnica de
Departamento de Biología de Sistemas Unidad Docente de Bioquímica y Biología Molecular ELECTROFORESIS EN GEL DE POLIACRILAMIDA CON SDS SDS-PAGE 1. FUNDAMENTO TEÓRICO La electroforesis es una técnica de
Monitoreo de un proceso de purificación de proteínas. Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa
 Monitoreo de un proceso de purificación de proteínas Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa Qué es la electroforesis? Es la técnica que permite la separación
Monitoreo de un proceso de purificación de proteínas Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa Qué es la electroforesis? Es la técnica que permite la separación
MONITOREO DE UN PROCESO DE PURIFICACIÓN DE PROTEÍNAS. Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa.
 MONITOREO DE UN PROCESO DE PURIFICACIÓN DE PROTEÍNAS Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa. Qué es la electroforesis? Es la técnica que permite la
MONITOREO DE UN PROCESO DE PURIFICACIÓN DE PROTEÍNAS Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa. Qué es la electroforesis? Es la técnica que permite la
Electroforesis de proteínas en geles de poliacrilamida
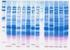 Electroforesis de proteínas en geles de poliacrilamida Electroforesis de proteínas en geles de poliacrilamida: Introducción y técnica básica La electroforesis de proteínas en geles con una matriz de poliacrilamida,
Electroforesis de proteínas en geles de poliacrilamida Electroforesis de proteínas en geles de poliacrilamida: Introducción y técnica básica La electroforesis de proteínas en geles con una matriz de poliacrilamida,
Trabajo Práctico 5: Electroforesis de proteínas Electroforesis de proteínas en Acetato de celulosa
 Trabajo Práctico 5: Electroforesis de proteínas Electroforesis de proteínas en Acetato de celulosa OBJETIVO: -Realizar electroforesis de las proteínas presentes en suero utilizando acetato de celulosa
Trabajo Práctico 5: Electroforesis de proteínas Electroforesis de proteínas en Acetato de celulosa OBJETIVO: -Realizar electroforesis de las proteínas presentes en suero utilizando acetato de celulosa
BIOLOGIA CELULAR Y MOLECULAR. LABORATORIO No 9: ELECTROFORESIS EN GELES DE POLIACRILAMIDA (SDS-PAGE)
 BIOLOGIA CELULAR Y MOLECULAR LABORATORIO No 9: ELECTROFORESIS EN GELES DE POLIACRILAMIDA (SDS-PAGE) 1. INTRODUCCIÓN Uno de los métodos que permite la purificación y separación de proteínas de un organismo
BIOLOGIA CELULAR Y MOLECULAR LABORATORIO No 9: ELECTROFORESIS EN GELES DE POLIACRILAMIDA (SDS-PAGE) 1. INTRODUCCIÓN Uno de los métodos que permite la purificación y separación de proteínas de un organismo
ELECTROFORESIS Q U Í M I C A B I O L Ó G I C A. D E P A R T A M E N T O D E B Q C A. F C N Y C S. U N P S J B
 ELECTROFORESIS Q U Í M I C A B I O L Ó G I C A. D E P A R T A M E N T O D E B Q C A. F C N Y C S. U N P S J B 2 0 1 7 Que es la electroforesis? Qué permite analizar? Que factores influyen? Separar y analizar
ELECTROFORESIS Q U Í M I C A B I O L Ó G I C A. D E P A R T A M E N T O D E B Q C A. F C N Y C S. U N P S J B 2 0 1 7 Que es la electroforesis? Qué permite analizar? Que factores influyen? Separar y analizar
GENERALIDADES Y APLICACIONES DE LA ELECTROFORESIS. Influencia de campo cargado eléctricamente Movimiento al cátodo (-) o al anodo (+)
 GENERALIDADES Y APLICACIONES DE LA ELECTROFORESIS Electroforésis Separación de especies cargadas (anión (-) y catión (+) ) Influencia de campo cargado eléctricamente Movimiento al cátodo (-) o al anodo
GENERALIDADES Y APLICACIONES DE LA ELECTROFORESIS Electroforésis Separación de especies cargadas (anión (-) y catión (+) ) Influencia de campo cargado eléctricamente Movimiento al cátodo (-) o al anodo
ELECTROFORESIS EN GELES DE POLIACRILAMIDA SDS-PAGE. Presencia de Sodio Dodecil Sulfato bajo condiciones reductoras (SDSPAGE)
 ELECTROFORESIS EN GELES DE POLIACRILAMIDA SDSPAGE Presencia de Sodio Dodecil Sulfato bajo condiciones reductoras (SDSPAGE) Método rápido, reproducible y de bajo costo Utilizado para cuantificar, comparar
ELECTROFORESIS EN GELES DE POLIACRILAMIDA SDSPAGE Presencia de Sodio Dodecil Sulfato bajo condiciones reductoras (SDSPAGE) Método rápido, reproducible y de bajo costo Utilizado para cuantificar, comparar
Easy PDF Creator is professional software to create PDF. If you wish to remove this line, buy it now.
 1 Virología y Micología Veterinaria Trabajo Práctico No. 4 ELECTROFORESIS La electroforesis es una técnica utilizada para separar grandes moléculas por tamaño a través de la aplicación de un campo eléctrico
1 Virología y Micología Veterinaria Trabajo Práctico No. 4 ELECTROFORESIS La electroforesis es una técnica utilizada para separar grandes moléculas por tamaño a través de la aplicación de un campo eléctrico
Electroforesis de proteínas
 Electroforesis de proteínas Introducción general La electroforesis es un método de separación basado en la tasa diferencial de migración de especies cargadas al estar en un campo eléctrico de DC La electroforesis
Electroforesis de proteínas Introducción general La electroforesis es un método de separación basado en la tasa diferencial de migración de especies cargadas al estar en un campo eléctrico de DC La electroforesis
Diagnóstico Avanzado en Enfermedades Tropicales
 Diagnóstico Avanzado en Enfermedades Tropicales Máster universitario en Enfermedades Tropicales Código 302731 (3 créditos ECTS) Área de Parasitología Departamento de Biología Animal, Parasitología, Ecología,
Diagnóstico Avanzado en Enfermedades Tropicales Máster universitario en Enfermedades Tropicales Código 302731 (3 créditos ECTS) Área de Parasitología Departamento de Biología Animal, Parasitología, Ecología,
Biología Celular y Molecular. Guía de TP Nro. 5. Actividad proteolítica celular.
 Biología Celular y Molecular. Guía de TP Nro. 5 Actividad proteolítica celular. Introducción La actividad proteolítica secretada por las células es un elemento indispensable para la proliferación y migración
Biología Celular y Molecular. Guía de TP Nro. 5 Actividad proteolítica celular. Introducción La actividad proteolítica secretada por las células es un elemento indispensable para la proliferación y migración
PRÁCTICA 9 ELECTROFORESIS EN GEL DE AGAROSA
 INTRODUCCIÓN PRÁCTICA 9 ELECTROFORESIS EN GEL DE AGAROSA La electroforesis es una técnica que permite separar moléculas cargadas eléctricamente, entre las cuales se encuentran los ácidos nucleicos (DNA
INTRODUCCIÓN PRÁCTICA 9 ELECTROFORESIS EN GEL DE AGAROSA La electroforesis es una técnica que permite separar moléculas cargadas eléctricamente, entre las cuales se encuentran los ácidos nucleicos (DNA
DETERMINACIÓN DEL PESO MOLECULAR DE PROTEÍNAS
 DETERMINACIÓN DEL PESO MOLECULAR DE PROTEÍNAS 6 grupos de estudiantes 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es desarrollar el conocimiento de la estructura de las proteínas y determinar
DETERMINACIÓN DEL PESO MOLECULAR DE PROTEÍNAS 6 grupos de estudiantes 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es desarrollar el conocimiento de la estructura de las proteínas y determinar
ELECTROFORESIS GENERALIDADES Y APLICACIONES CLINICAS
 ELECTROFORESIS GENERALIDADES Y APLICACIONES CLINICAS Marcelo Castillo Navarrrete, T.M. MsCs (C) Facultad de Medicina Carrera Tecnología Médica 18 de Noviembre de 2004 Fundamentos de Electroforesis Alta
ELECTROFORESIS GENERALIDADES Y APLICACIONES CLINICAS Marcelo Castillo Navarrrete, T.M. MsCs (C) Facultad de Medicina Carrera Tecnología Médica 18 de Noviembre de 2004 Fundamentos de Electroforesis Alta
CROMATOGRAFÍA DE AMINOÁCIDOS
 CROMATOGRAFÍA DE AMINOÁCIDOS Electroforesis.- Es un método de laboratorio en el que se utiliza una corriente eléctrica controlada con la finalidad de separar aminoácidos (y otras biomoléculas) según su
CROMATOGRAFÍA DE AMINOÁCIDOS Electroforesis.- Es un método de laboratorio en el que se utiliza una corriente eléctrica controlada con la finalidad de separar aminoácidos (y otras biomoléculas) según su
Electroforesis en gel de poliacrilamida y electrotransferencia
 Electroforesis en gel de poliacrilamida y electrotransferencia INDICE ELECTROFORESIS Fundamento y características Tipos de electroforesis: libre y de zona Electroforesis en papel, acetato de celulosa Electroforesis
Electroforesis en gel de poliacrilamida y electrotransferencia INDICE ELECTROFORESIS Fundamento y características Tipos de electroforesis: libre y de zona Electroforesis en papel, acetato de celulosa Electroforesis
ELECTROFORESIS EN GEL DE POLIACRILAMIDA CON SDS SDS-PAGE
 ELECTROFORESIS EN GEL DE POLIACRILAMIDA CON SDS SDS-PAGE FUNDAMENTO TEÓRICO La electroforesis es una técnica de separación de moléculas cargadas por migración en un campo eléctrico. Las moléculas se separan
ELECTROFORESIS EN GEL DE POLIACRILAMIDA CON SDS SDS-PAGE FUNDAMENTO TEÓRICO La electroforesis es una técnica de separación de moléculas cargadas por migración en un campo eléctrico. Las moléculas se separan
Universidad de Los Andes Facultad de Medicina Instituto Inmunología Clínica Maestría en Inmunología
 TÉCNICAS EN BIOLOGÍA MOLECULAR RESPONSABLE: Dra. Lisbeth Berrueta. CREDITOS: 2 El curso de Técnicas de Biología Molecular está destinado a profesionales del área biomédica con conocimientos básicos relativos
TÉCNICAS EN BIOLOGÍA MOLECULAR RESPONSABLE: Dra. Lisbeth Berrueta. CREDITOS: 2 El curso de Técnicas de Biología Molecular está destinado a profesionales del área biomédica con conocimientos básicos relativos
ELECTROFORESIS AVANZADA
 Ref. ELECAVANZADA (4 prácticas) 1. OBJETIVO DEL EXPERIMENTO ELECTROFORESIS AVANZADA El objetivo de este experimento es introducir a los alumnos en el conocimiento de la teoría electroforética y familiarizarse
Ref. ELECAVANZADA (4 prácticas) 1. OBJETIVO DEL EXPERIMENTO ELECTROFORESIS AVANZADA El objetivo de este experimento es introducir a los alumnos en el conocimiento de la teoría electroforética y familiarizarse
Técnicas de Estudio de las células
 Técnicas de Estudio de las células Microscopia Preparaciones permanentes: Fijación Deshidratación Inclusión Corte Fijación: Acidos, solventes orgánicos como alcohol, aldehídos (Formaldehído, glutaraldehídos)
Técnicas de Estudio de las células Microscopia Preparaciones permanentes: Fijación Deshidratación Inclusión Corte Fijación: Acidos, solventes orgánicos como alcohol, aldehídos (Formaldehído, glutaraldehídos)
Purificación de Proteínas Parte II
 Purificación de Proteínas Parte II Fase I. Obtención del extracto crudo Lisis celular. Válido para células sin pared celular como las células de tejidos animales, pero no es suficiente para células vegetales
Purificación de Proteínas Parte II Fase I. Obtención del extracto crudo Lisis celular. Válido para células sin pared celular como las células de tejidos animales, pero no es suficiente para células vegetales
Módulo 2 Biología Molecular Genética Molecular II Módulo 2. Clonación y Selección de moléculas recombinantes
 Módulo 2 Clonación y Selección de moléculas recombinantes El fragmento de ADN amplificado por PCR en el módulo anterior se introdujo en un vector pgem T Easy (Ver Anexo 2) utilizando una ligasa. En la
Módulo 2 Clonación y Selección de moléculas recombinantes El fragmento de ADN amplificado por PCR en el módulo anterior se introdujo en un vector pgem T Easy (Ver Anexo 2) utilizando una ligasa. En la
DESARROLLO COGNOSCITIVO Y APRENDIZAJE
 Prof. Jhonis Valbuena Cátedra: Análisis Instrumental La Electrofóresis es un método de la Química Analítica que utiliza corriente eléctrica controlada con la finalidad de separar biomolèculas según su
Prof. Jhonis Valbuena Cátedra: Análisis Instrumental La Electrofóresis es un método de la Química Analítica que utiliza corriente eléctrica controlada con la finalidad de separar biomolèculas según su
ELECTROFORESIS EN GELES DE AGAROSA. Agustín Garrido. agugarrido@hotmail.com
 1 ELECTROFORESIS EN GELES DE AGAROSA Agustín Garrido agugarrido@hotmail.com Introducción En este trabajo práctico se utilizó la técnica de electroforesis. Este proceso se basa en la migración de las moléculas
1 ELECTROFORESIS EN GELES DE AGAROSA Agustín Garrido agugarrido@hotmail.com Introducción En este trabajo práctico se utilizó la técnica de electroforesis. Este proceso se basa en la migración de las moléculas
EXTRACCIÓN DE ADN (Doyle & Doyle, 1987)
 EXTRACCIÓN DE ADN (Doyle & Doyle, 1987) MATERIALES Y REACTIVOS (Grado biología molecular a analítico) Cloroformo Alcohol Isoamilico Isopropanol. Etanol al 70%. Bloques de Hielo Microcentrifuga Bloque de
EXTRACCIÓN DE ADN (Doyle & Doyle, 1987) MATERIALES Y REACTIVOS (Grado biología molecular a analítico) Cloroformo Alcohol Isoamilico Isopropanol. Etanol al 70%. Bloques de Hielo Microcentrifuga Bloque de
Al igual que en la centrifugación también hay dos criterios de separación con el mismo concepto:
 Electroforesis En la técnica de separación anterior hemos utilizado la fuerza centrífuga para que asociada a la diferencia de masa o densidad de las partículas a separar nos las diferencie, ahora vamos
Electroforesis En la técnica de separación anterior hemos utilizado la fuerza centrífuga para que asociada a la diferencia de masa o densidad de las partículas a separar nos las diferencie, ahora vamos
4. TIPADO GENÉTICO DE BACTERIAS PATÓGENAS MEDIANTE ELECTROFORESIS EN CAMPOS PULSADOS (PFGE) Materiales - Bacterias crecidas en placas de agar
 4. TIPADO GENÉTICO DE BACTERIAS PATÓGENAS MEDIANTE ELECTROFORESIS EN CAMPOS PULSADOS (PFGE) Materiales - Bacterias crecidas en placas de agar - Agarosa de grado molecular - Agarosa de bajo punto de fusión
4. TIPADO GENÉTICO DE BACTERIAS PATÓGENAS MEDIANTE ELECTROFORESIS EN CAMPOS PULSADOS (PFGE) Materiales - Bacterias crecidas en placas de agar - Agarosa de grado molecular - Agarosa de bajo punto de fusión
MANUAL DE PRÁCTICAS DE LABORATORIO
 MANUAL DE PRÁCTICAS DE LABORATORIO INGENIERIA ENBIOTECNOLOGÍA INGENIERÍA GENÉTICA FICHA TECNICA FICHA TÉCNICA SEMINARIO DE BIOTECNOLOGÍA MÉDICO-FARMACÉUTICA Fecha: Nombre del catedrático: 10-Julio-2012
MANUAL DE PRÁCTICAS DE LABORATORIO INGENIERIA ENBIOTECNOLOGÍA INGENIERÍA GENÉTICA FICHA TECNICA FICHA TÉCNICA SEMINARIO DE BIOTECNOLOGÍA MÉDICO-FARMACÉUTICA Fecha: Nombre del catedrático: 10-Julio-2012
Practica 6 ELECTROFORESIS HORIZONTAL Corrimiento y visualización de ADN
 Practica 6 ELECTROFORESIS HORIZONTAL Corrimiento y visualización de ADN La Biología Molecular es una ciencia cuyo objetivo fundamental es la comprensión de todos aquellos procesos celulares que contribuyen
Practica 6 ELECTROFORESIS HORIZONTAL Corrimiento y visualización de ADN La Biología Molecular es una ciencia cuyo objetivo fundamental es la comprensión de todos aquellos procesos celulares que contribuyen
Universidad de la República Oriental del Uruguay Facultad de Ingeniería Instituto de Ingeniería Eléctrica MANUAL DE USUARIO ELECTROFORESIS
 Universidad de la República Oriental del Uruguay Facultad de Ingeniería Instituto de Ingeniería Eléctrica MANUAL DE USUARIO ELECTROFORESIS DICIEMBRE 2006 Tratamiento de Imágenes por Computadora Proyecto
Universidad de la República Oriental del Uruguay Facultad de Ingeniería Instituto de Ingeniería Eléctrica MANUAL DE USUARIO ELECTROFORESIS DICIEMBRE 2006 Tratamiento de Imágenes por Computadora Proyecto
TP2: Extracción y cuantificación de proteínas
 Objetivo TP2: Extracción y cuantificación de proteínas Comparar métodos de extracción de proteínas a partir de distintos organismos. Cuantificar las proteínas resultantes de cada extracto. Introducción
Objetivo TP2: Extracción y cuantificación de proteínas Comparar métodos de extracción de proteínas a partir de distintos organismos. Cuantificar las proteínas resultantes de cada extracto. Introducción
CROMATOGRAFÍA. A.- INTERCAMBIO IONICO: A.1. ANIONICA A.2. CATIONCA B.- FILTRACIÓN EN GEL
 CROMATOGRAFÍA. A.- INTERCAMBIO IONICO: A.1. ANIONICA A.2. CATIONCA B.- FILTRACIÓN EN GEL C.- AFINIDAD B. CROMATOGRAFÍA DE FILTRACIÓN EN GEL. 1. Principios. No requiere la unión de la proteína, lo cual
CROMATOGRAFÍA. A.- INTERCAMBIO IONICO: A.1. ANIONICA A.2. CATIONCA B.- FILTRACIÓN EN GEL C.- AFINIDAD B. CROMATOGRAFÍA DE FILTRACIÓN EN GEL. 1. Principios. No requiere la unión de la proteína, lo cual
Tema 6 Cuantificación de proteínas
 Tema 6 Cuantificación de proteínas Procedimiento de estudio de proteínas Selección de fuente Fraccionamiento de células Centrifugación Cromatografía Cromatografía en capa fina Cromatografía en columna
Tema 6 Cuantificación de proteínas Procedimiento de estudio de proteínas Selección de fuente Fraccionamiento de células Centrifugación Cromatografía Cromatografía en capa fina Cromatografía en columna
Ensayos de restricción
 Ensayos de restricción Vector con inserto= Vector recombinante 6500pb Objetivos de ensayos de restricción de plásmidos Conocer el principio de separación y detección de ácidos nucleicos en geles de agarosa.
Ensayos de restricción Vector con inserto= Vector recombinante 6500pb Objetivos de ensayos de restricción de plásmidos Conocer el principio de separación y detección de ácidos nucleicos en geles de agarosa.
Técnicas de Caracterización y purificación
 Técnicas de Caracterización y purificación hidrofobicidad carga Propiedades de las proteínas utilizadas para caracterizar y purificar Carga Tamaño Forma Actividad biologica Hidrofobicidad PM Estabilidad
Técnicas de Caracterización y purificación hidrofobicidad carga Propiedades de las proteínas utilizadas para caracterizar y purificar Carga Tamaño Forma Actividad biologica Hidrofobicidad PM Estabilidad
CROMATOGRAFÍA. A.- INTERCAMBIO IONICO: A.1. ANIONICA A.2. CATIONCA B.- FILTRACIÓN EN GEL
 CROMATOGRAFÍA. A.- INTERCAMBIO IONICO: A.1. ANIONICA A.2. CATIONCA B.- FILTRACIÓN EN GEL C.- AFINIDAD A. CROMATOGRAFÍA DE INTERCAMBIO IÓNICO. Usos 1.- Purificar Proteínas 2.- Concentrar Proteínas Ventajas
CROMATOGRAFÍA. A.- INTERCAMBIO IONICO: A.1. ANIONICA A.2. CATIONCA B.- FILTRACIÓN EN GEL C.- AFINIDAD A. CROMATOGRAFÍA DE INTERCAMBIO IÓNICO. Usos 1.- Purificar Proteínas 2.- Concentrar Proteínas Ventajas
PURIFICACIÓN DE PROTEÍNAS
 PURIFICACIÓN DE PROTEÍNAS ESQUEMA DE PURIFICACIÓN DE UNA PROTEÍNA tejido vegetal animal homogeneizar cultivo celular bacterias levaduras células mamíferos PREPARACIÓN EXTRACTO crudo fraccionamiento subcelular
PURIFICACIÓN DE PROTEÍNAS ESQUEMA DE PURIFICACIÓN DE UNA PROTEÍNA tejido vegetal animal homogeneizar cultivo celular bacterias levaduras células mamíferos PREPARACIÓN EXTRACTO crudo fraccionamiento subcelular
Electroforesis de proteínas en geles de poliacrilamida. Electroforesis de proteínas en geles de poliacrilamida: Introducción y técnica básica
 Electroforesis de proteínas en geles de poliacrilamida Electroforesis de proteínas en geles de poliacrilamida: Introducción y técnica básica La electroforesis de proteínas en geles con una matriz de poliacrilamida,
Electroforesis de proteínas en geles de poliacrilamida Electroforesis de proteínas en geles de poliacrilamida: Introducción y técnica básica La electroforesis de proteínas en geles con una matriz de poliacrilamida,
Ensayos southwestern y northwestern
 Búsqueda de proteínas que se unen a DNA (secuencia conocida, promotor) Ensayo southwestern encontrar proteínas ligantes de DNA que reconozcan en éste una determinada secuencia de nucleótidos Ensayo northwestern
Búsqueda de proteínas que se unen a DNA (secuencia conocida, promotor) Ensayo southwestern encontrar proteínas ligantes de DNA que reconozcan en éste una determinada secuencia de nucleótidos Ensayo northwestern
PROPIEDADES FISICOQUÍMICAS DE LOS ÁCIDOS NUCLEICOS. Es un ácido capaz de formar sales con iones cargados
 Extracción de ADN Genética molecular PROPIEDADES FISICOQUÍMICAS DE LOS ÁCIDOS NUCLEICOS Es un ácido capaz de formar sales con iones cargados positivamente (cationes). Es soluble en soluciones concentradas
Extracción de ADN Genética molecular PROPIEDADES FISICOQUÍMICAS DE LOS ÁCIDOS NUCLEICOS Es un ácido capaz de formar sales con iones cargados positivamente (cationes). Es soluble en soluciones concentradas
Separación e identificación de lípidos de membrana
 Separación e identificación de lípidos de membrana Objetivos Separación e identificación de especies de fosfolípidos por cromatografía de capa fina (TLC, Thin Layer Chromatography) TLC monodimensional
Separación e identificación de lípidos de membrana Objetivos Separación e identificación de especies de fosfolípidos por cromatografía de capa fina (TLC, Thin Layer Chromatography) TLC monodimensional
Electroforesis. Dr. Héctor L. Ayala del Río AMGEN Bruce Wallace Program Departamento de Biología UPR-Humacao VER VIDEO CARGADO GEL
 Electroforesis Dr. Héctor L. Ayala del Río AMGEN Bruce Wallace Program Departamento de Biología UPR-Humacao VER VIDEO CARGADO GEL 1 Electroforesis l Método utilizado para separar y purificar macromoléculas:
Electroforesis Dr. Héctor L. Ayala del Río AMGEN Bruce Wallace Program Departamento de Biología UPR-Humacao VER VIDEO CARGADO GEL 1 Electroforesis l Método utilizado para separar y purificar macromoléculas:
Material elaborado por F. Agius, O. Borsani, P.Díaz, S. Gonnet, P. Irisarri, F. Milnitsky y J. Monza. Bioquímica. Facultad de Agronomía.
 AMINOACIDOS Las proteínas de bacterias, hongos, plantas y animales están constituidas a partir de las mismas 20 unidades o monómeros: los á-aminoácidos. Los aminoácidos tienen un grupo amino y un grupo
AMINOACIDOS Las proteínas de bacterias, hongos, plantas y animales están constituidas a partir de las mismas 20 unidades o monómeros: los á-aminoácidos. Los aminoácidos tienen un grupo amino y un grupo
CROMATOGRAFIA DE TAMIZADO MOLECULAR / FILTRACION EN GEL / EXCLUSION MOLECULAR
 CROMATOGRAFIA DE TAMIZADO MOLECULAR / FILTRACION EN GEL / EXCLUSION MOLECULAR 1.-FUNDAMENTOS DE LA CROMATOGRAFIA DE TAMIZADO MOLECULAR. Las biomoléculas presentan una serie de propiedades físicas (tamaño,
CROMATOGRAFIA DE TAMIZADO MOLECULAR / FILTRACION EN GEL / EXCLUSION MOLECULAR 1.-FUNDAMENTOS DE LA CROMATOGRAFIA DE TAMIZADO MOLECULAR. Las biomoléculas presentan una serie de propiedades físicas (tamaño,
Tópicos en Biofísica Molecular 2do Cuatrimestre de 2015 Docentes: Lía Pietrasanta y Alan Bush
 Tópicos en Biofísica Molecular 2do Cuatrimestre de 2015 Docentes: Lía Pietrasanta y Alan Bush Guía 4: Electroforesis Northern, Southern y Western blots. Problema 1 Una proteína en su estado nativo tiene
Tópicos en Biofísica Molecular 2do Cuatrimestre de 2015 Docentes: Lía Pietrasanta y Alan Bush Guía 4: Electroforesis Northern, Southern y Western blots. Problema 1 Una proteína en su estado nativo tiene
ELECTROFORESIS VERTICAL DE PROTEÍNAS
 6 grupos de estudiantes ELECTROFORESIS VERTICAL DE PROTEÍNAS 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es aprender el uso de la ELECTOFORESIS DESNATURALIZANTE EN GEL DE POLIACRILAMIDA-SDS
6 grupos de estudiantes ELECTROFORESIS VERTICAL DE PROTEÍNAS 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es aprender el uso de la ELECTOFORESIS DESNATURALIZANTE EN GEL DE POLIACRILAMIDA-SDS
qprotein (BCA) Kit para cuantificar proteinas totales PB-L Productos Bio-Lógicos
 qprotein () Kit para cuantificar proteinas totales PB-L http://www.pb-l.com.ar qprotein () Cat. no. RA03 CONTENIDO Componentes RA0301 RA0302 Buffer A 250 ml 500 ml Buffer B 5 ml 10 ml Proteína Patrón 5
qprotein () Kit para cuantificar proteinas totales PB-L http://www.pb-l.com.ar qprotein () Cat. no. RA03 CONTENIDO Componentes RA0301 RA0302 Buffer A 250 ml 500 ml Buffer B 5 ml 10 ml Proteína Patrón 5
TRABAJO PRÁCTICO Nº 2 CUANTIFICACIÓN DE PROTEÍNAS POR EL MÉTODO DE BRADFORD.
 AÑO 2010 PRIMER SEMESTRE LABORATORIO ASIGNATURA DE BIOQUÍMICA. PLAN COMÚN AGRONOMÍA E INGENIERÍA FORESTAL FACULTAD CIENCIAS SILVOAGROPECUARIAS TRABAJO PRÁCTICO Nº 2 CUANTIFICACIÓN DE PROTEÍNAS POR EL MÉTODO
AÑO 2010 PRIMER SEMESTRE LABORATORIO ASIGNATURA DE BIOQUÍMICA. PLAN COMÚN AGRONOMÍA E INGENIERÍA FORESTAL FACULTAD CIENCIAS SILVOAGROPECUARIAS TRABAJO PRÁCTICO Nº 2 CUANTIFICACIÓN DE PROTEÍNAS POR EL MÉTODO
Tópicos en Biofísica Molecular
 Tópicos en Biofísica Molecular 2do Cuatrimestre de 2013 Docentes: Lía Pietrasanta y Catalina von Bilderling Práctica de laboratorio nº 1: Soluciones, ph OBJETIVOS Familiarizarse con el material de uso
Tópicos en Biofísica Molecular 2do Cuatrimestre de 2013 Docentes: Lía Pietrasanta y Catalina von Bilderling Práctica de laboratorio nº 1: Soluciones, ph OBJETIVOS Familiarizarse con el material de uso
16. Electroforesis desnaturalizante en geles de poliacrilamida. Análisis de proteínas de hojas de Arabidopsis thaliana
 16. Electroforesis desnaturalizante en geles de poliacrilamida. Análisis de proteínas de hojas de Arabidopsis thaliana Ana María Maldonado Alconada, Jesús V. Jorrín Novo Departamento de Bioquímica y Biología
16. Electroforesis desnaturalizante en geles de poliacrilamida. Análisis de proteínas de hojas de Arabidopsis thaliana Ana María Maldonado Alconada, Jesús V. Jorrín Novo Departamento de Bioquímica y Biología
IBCM 1 GUIA DE PROBLEMAS DE PROTEINAS
 IBCM 1 1-Complete los esquemas II y III. Además señale: extremo NH2 terminal, extremo 5 del mrna, extremo 3 del trna, sitio P, sitio A, codones y anticodones (complételos con las bases correspondientes)
IBCM 1 1-Complete los esquemas II y III. Además señale: extremo NH2 terminal, extremo 5 del mrna, extremo 3 del trna, sitio P, sitio A, codones y anticodones (complételos con las bases correspondientes)
Purificación de la enzima lactato deshidrogenasa de músculo esquelético de pollo
 Purificación de la enzima lactato deshidrogenasa de músculo esquelético de pollo ESQUEMA GENERAL Sesión 1. Extracción y precipitación con sulfato de amonio. Sesión 2. Purificación por cromatografía Sesión
Purificación de la enzima lactato deshidrogenasa de músculo esquelético de pollo ESQUEMA GENERAL Sesión 1. Extracción y precipitación con sulfato de amonio. Sesión 2. Purificación por cromatografía Sesión
Proyecto de Fin de Cursos
 Universidad de la República Oriental del Uruguay Proyecto de Fin de Cursos ELECTROFORESIS EN GEL DE MOLÉCULAS DE ADN Noviembre de 2006 Carolina Etchart C.I. 3.757.708-8 Marcelo Lavagna C.I. 3.508.715-8
Universidad de la República Oriental del Uruguay Proyecto de Fin de Cursos ELECTROFORESIS EN GEL DE MOLÉCULAS DE ADN Noviembre de 2006 Carolina Etchart C.I. 3.757.708-8 Marcelo Lavagna C.I. 3.508.715-8
Trabajo práctico Calor de la reacción de descomposición del agua oxigenada
 Trabajo práctico Calor de la reacción de descomposición del agua oxigenada Objetivo Determinar el calor de reacción para la descomposición del agua oxigenada. Introducción Se prepara una solución de H
Trabajo práctico Calor de la reacción de descomposición del agua oxigenada Objetivo Determinar el calor de reacción para la descomposición del agua oxigenada. Introducción Se prepara una solución de H
ELECTROFORESIS Fundamento.
 ELECTROFORESIS La electroforesis es un método de laboratorio en el que se utiliza una corriente eléctrica controlada con la finalidad de separar biomoleculas según su tamaño y carga eléctrica a través
ELECTROFORESIS La electroforesis es un método de laboratorio en el que se utiliza una corriente eléctrica controlada con la finalidad de separar biomoleculas según su tamaño y carga eléctrica a través
PCR SIMULADA. Ref.PCR Simulada (4 prácticas) 1. OBJETIVO DEL EXPERIMENTO
 Ref.PCR Simulada (4 prácticas) 1. OBJETIVO DEL EXPERIMENTO PCR SIMULADA El objetivo de este experimento es introducir a los estudiantes en los principios y práctica de la Reacción en Cadena de la Polimerasa
Ref.PCR Simulada (4 prácticas) 1. OBJETIVO DEL EXPERIMENTO PCR SIMULADA El objetivo de este experimento es introducir a los estudiantes en los principios y práctica de la Reacción en Cadena de la Polimerasa
Química Biológica TP 1: ESPECTROFOTOMETRIA.
 TP 1: ESPECTROFOTOMETRIA. Introducción Al observar una solución acuosa de un colorante a trasluz, observamos una leve coloración, la cual se debe a la interacción entre las moléculas del colorante y la
TP 1: ESPECTROFOTOMETRIA. Introducción Al observar una solución acuosa de un colorante a trasluz, observamos una leve coloración, la cual se debe a la interacción entre las moléculas del colorante y la
Los principales mecanismos que intervienen en la separación cromatográfica son:
 TP 8 CROMATOGRAFIA EN PAPEL, Introducción Los métodos cromatográficos son un conjunto de técnicas empleadas para separar compuestos químicos de una mezcla. Su nombre significa escribir con color ya que
TP 8 CROMATOGRAFIA EN PAPEL, Introducción Los métodos cromatográficos son un conjunto de técnicas empleadas para separar compuestos químicos de una mezcla. Su nombre significa escribir con color ya que
Proceso que cuenta con varias etapas cuyo objetivo es separar una proteína de interés de una mezcla de proteínas.
 Proceso que cuenta con varias etapas cuyo objetivo es separar una proteína de interés de una mezcla de proteínas. La selección de técnicas de purificación depende de las propiedades de las proteínas. Características
Proceso que cuenta con varias etapas cuyo objetivo es separar una proteína de interés de una mezcla de proteínas. La selección de técnicas de purificación depende de las propiedades de las proteínas. Características
Código: IDK-006 Ver: 1 MTHFR A1298C. Sistema para detección de la alteración A1298C en el gene de la Mutilen Tetrahidrofolato Reductasa
 Sistema para detección de la alteración A1298C en el gene de la Mutilen Tetrahidrofolato Reductasa Reg. MSP 21199 Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336
Sistema para detección de la alteración A1298C en el gene de la Mutilen Tetrahidrofolato Reductasa Reg. MSP 21199 Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336
REVISIÓN DE MÉTODOS ESPECTROSCÓPICOS Y ELABORACIÓN DE CURVA ESTÁNDAR DE PROTEÍNA
 REVISIÓN DE MÉTODOS ESPECTROSCÓPICOS Y ELABORACIÓN DE CURVA ESTÁNDAR DE PROTEÍNA OBJETIVOS Aplicar un método espectrofotométrico para medir la concentración de una proteína. Conocer el manejo de micropipetas
REVISIÓN DE MÉTODOS ESPECTROSCÓPICOS Y ELABORACIÓN DE CURVA ESTÁNDAR DE PROTEÍNA OBJETIVOS Aplicar un método espectrofotométrico para medir la concentración de una proteína. Conocer el manejo de micropipetas
CYP 2C9 A1075C CYP2C9*3
 CYP 2C9 A1075C Sistema para la detección de la mutación A1075C en el gene del citocromo P450 2C9. Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336 71 60. Info@atgen.com.uy
CYP 2C9 A1075C Sistema para la detección de la mutación A1075C en el gene del citocromo P450 2C9. Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336 71 60. Info@atgen.com.uy
UNIVERSIDAD DE PUERTO RICO EN AGUADILLA DEPARTAMENTO DE CIENCIAS NATURALES. Laboratorio de Genética BIOL 3306
 UNIVERSIDAD DE PUERTO RICO EN AGUADILLA DEPARTAMENTO DE CIENCIAS NATURALES Laboratorio de Genética BIOL 3306 Liza V. Jiménez Rodríguez, Ph.D. Agosto, 2014 Pre-prueba I. Pareo 1) Geles de agarosa 2) Loading
UNIVERSIDAD DE PUERTO RICO EN AGUADILLA DEPARTAMENTO DE CIENCIAS NATURALES Laboratorio de Genética BIOL 3306 Liza V. Jiménez Rodríguez, Ph.D. Agosto, 2014 Pre-prueba I. Pareo 1) Geles de agarosa 2) Loading
Código: KIT-005 Ver: 1 MTHFR C677T
 Sistema para detección de la alteración C677T en el gene que codifica para la Metilen-tetrahidrofolato reductasa humana 1 Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598)
Sistema para detección de la alteración C677T en el gene que codifica para la Metilen-tetrahidrofolato reductasa humana 1 Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598)
5. PROBLEMAS SOBRE EQUILIBRIOS ACIDO BASE & AMINOACIDOS
 Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 5. PROBLEMAS SOBRE EQUILIBRIOS ACIDO BASE & AMINOACIDOS Para realizar estos problemas se aconseja consultar una tabla con las
Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 5. PROBLEMAS SOBRE EQUILIBRIOS ACIDO BASE & AMINOACIDOS Para realizar estos problemas se aconseja consultar una tabla con las
Grado en Química. 4º Curso Bioquímica. Guión de Prácticas
 Grado en Química 4º Curso Bioquímica Guión de Prácticas UTILES A TRAER POR EL ALUMNO Bata Gafas de Seguridad Cuaderno de Laboratorio NORMAS DE TRABAJO Antes de empezar Antes de empezar cada práctica, el
Grado en Química 4º Curso Bioquímica Guión de Prácticas UTILES A TRAER POR EL ALUMNO Bata Gafas de Seguridad Cuaderno de Laboratorio NORMAS DE TRABAJO Antes de empezar Antes de empezar cada práctica, el
Ventajas de las columnas Agilent AdvanceBio SEC para análisis biofarmacéuticos
 Ventajas de las columnas Agilent AdvanceBio SEC para análisis biofarmacéuticos Comparación de columnas de diferentes fabricantes para mejorar la calidad de los datos Resumen técnico Introducción La cromatografía
Ventajas de las columnas Agilent AdvanceBio SEC para análisis biofarmacéuticos Comparación de columnas de diferentes fabricantes para mejorar la calidad de los datos Resumen técnico Introducción La cromatografía
Bqca.. Esp. Marcela Alejandra Guastavino Dra. María a Mercedes Tiscornia
 Bqca.. Esp. Marcela Alejandra Guastavino Dra. María a Mercedes Tiscornia Cátedra de Biología Molecular y Genética - 2015 OBJETIVOS Comprender el fundamento teórico de las técnicas t básicas de aislamiento
Bqca.. Esp. Marcela Alejandra Guastavino Dra. María a Mercedes Tiscornia Cátedra de Biología Molecular y Genética - 2015 OBJETIVOS Comprender el fundamento teórico de las técnicas t básicas de aislamiento
ELABORACIÓN N DE MEZCLA PARA PCR. Raquel Asunción Lima Cordón
 ELABORACIÓN N DE MEZCLA PARA PCR Raquel Asunción Lima Cordón PCR Polymerase Chain reaction (reacción en cadena de la polimerasa) Sintetizar muchas veces un fragmento de ADN PCR: simulación de lo que sucede
ELABORACIÓN N DE MEZCLA PARA PCR Raquel Asunción Lima Cordón PCR Polymerase Chain reaction (reacción en cadena de la polimerasa) Sintetizar muchas veces un fragmento de ADN PCR: simulación de lo que sucede
LABORATORIO Nº 3 Determinación de la capacidad amortiguadora de un buffer
 LABORATORIO Nº 3 - Es obligatorio la asistencia al práctico con túnica y lentes de seguridad. - El protocolo de la práctica y el fundamento teórico de la misma deben haber sido leídos por el estudiante
LABORATORIO Nº 3 - Es obligatorio la asistencia al práctico con túnica y lentes de seguridad. - El protocolo de la práctica y el fundamento teórico de la misma deben haber sido leídos por el estudiante
DEPARTAMENTO DE GENÉTICA UNIVERSIDAD DE GRANADA FUNDAMENTOS DE BIOLOGÍA APLICADA I 4º CURSO DE BIOLOGÍA
 DEPARTAMENTO DE GENÉTICA UNIVERSIDAD DE GRANADA FUNDAMENTOS DE BIOLOGÍA APLICADA I 4º CURSO DE BIOLOGÍA MÓDULO DE GENÉTICA TÉCNICAS MOLECULARES DE ANÁLISIS GENÉTICO AISLAMIENTO Y CLONACIÓN DE ADN SATÉLITE
DEPARTAMENTO DE GENÉTICA UNIVERSIDAD DE GRANADA FUNDAMENTOS DE BIOLOGÍA APLICADA I 4º CURSO DE BIOLOGÍA MÓDULO DE GENÉTICA TÉCNICAS MOLECULARES DE ANÁLISIS GENÉTICO AISLAMIENTO Y CLONACIÓN DE ADN SATÉLITE
41. Comprobación de colonias transformantes mediante PCR y electroforesis
 41. Comprobación de colonias transformantes mediante PCR y electroforesis Aurora Galván Cejudo, Manuel Tejada, Antonio Camargo, José Javier Higuera, Vicente Mariscal, Emilio Fernández Reyes Departamento
41. Comprobación de colonias transformantes mediante PCR y electroforesis Aurora Galván Cejudo, Manuel Tejada, Antonio Camargo, José Javier Higuera, Vicente Mariscal, Emilio Fernández Reyes Departamento
METODOLOGÍA DE EXTRACCIÓN Y PURIFICACIÓN DE INHIBIDORES DE PROTEASAS EN Opuntia streptacantha
 METODOLOGÍA DE EXTRACCIÓN Y PURIFICACIÓN DE INHIBIDORES DE PROTEASAS EN Opuntia streptacantha RESUMEN Estudiante: Jannet Alejandra Vargas Sánchez Instituto Tecnológico de Roque jannettitajm@hotmail.com
METODOLOGÍA DE EXTRACCIÓN Y PURIFICACIÓN DE INHIBIDORES DE PROTEASAS EN Opuntia streptacantha RESUMEN Estudiante: Jannet Alejandra Vargas Sánchez Instituto Tecnológico de Roque jannettitajm@hotmail.com
CONFERENCIA 6 TÍTULO: COMPONENTES MOLECULARES: MACROMOLÉCULAS. PROTEÍNAS.
 MORFOFISIOLOGÍA HUMANA I. PRIMER TRIMESTRE. PRIMER AÑO. CONFERENCIA 6 TÍTULO: COMPONENTES MOLECULARES: MACROMOLÉCULAS. PROTEÍNAS. Sabe Ud. que es la sangre? Adultos contienen de 5-6L Adultos contienen
MORFOFISIOLOGÍA HUMANA I. PRIMER TRIMESTRE. PRIMER AÑO. CONFERENCIA 6 TÍTULO: COMPONENTES MOLECULARES: MACROMOLÉCULAS. PROTEÍNAS. Sabe Ud. que es la sangre? Adultos contienen de 5-6L Adultos contienen
Código: IDK-003 Ver: 1. Factor V Leiden
 Sistema para detección de la alteración G1691A en el gene que codifica para el Factor V de la coagulación humana Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336 71
Sistema para detección de la alteración G1691A en el gene que codifica para el Factor V de la coagulación humana Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336 71
TRABAJO PRACTICO Nº 1 COMPOSICION QUIMICA DE LA CELULA
 TRABAJO PRACTICO Nº 1 COMPOSICION QUIMICA DE LA CELULA Alumno:..... Comisión:.. OBJETIVOS: - Identificar los compuestos orgánicos de importancia biológica. - Detectar la presencia de algunos tipos de biomoléculas
TRABAJO PRACTICO Nº 1 COMPOSICION QUIMICA DE LA CELULA Alumno:..... Comisión:.. OBJETIVOS: - Identificar los compuestos orgánicos de importancia biológica. - Detectar la presencia de algunos tipos de biomoléculas
Propiedades fisicoquímicas y funcionales de los alimentos 2015
 TRABAJO PRÁCTICO N 2: EMULSIONES DETERMINACIÓN DE LA ESTABILIDAD DE EMULSIONES POR CONDUCTIMETRÍA, MICROSCOPÍA Y TURBIDIMETRÍA. OBJETIVOS: 1. Determinar la estabilidad de emulsiones por conductimetría,
TRABAJO PRÁCTICO N 2: EMULSIONES DETERMINACIÓN DE LA ESTABILIDAD DE EMULSIONES POR CONDUCTIMETRÍA, MICROSCOPÍA Y TURBIDIMETRÍA. OBJETIVOS: 1. Determinar la estabilidad de emulsiones por conductimetría,
Purificación de proteínas
 Purificación de proteínas Purificación Proceso que cuenta con varias etapas cuyo objetivo es lograr la concentración diferencial de la proteína o molécula de interés Condiciones generales a evaluar Calidad
Purificación de proteínas Purificación Proceso que cuenta con varias etapas cuyo objetivo es lograr la concentración diferencial de la proteína o molécula de interés Condiciones generales a evaluar Calidad
TRABAJO PRACTICO Nº 3. PROTEINAS Y ENZIMAS.
 UNIVERSIDAD NACIONAL DE LA PATAGONIA SAN JUAN BOSCO FACULTAD DE CIENCIAS NATURALES DEPARTAMENTO DE FARMACIA CATEDRA DE FARMACOGNOSIA TRABAJO PRACTICO Nº 3. PROTEINAS Y ENZIMAS. Objetivo - Utilizar reacciones
UNIVERSIDAD NACIONAL DE LA PATAGONIA SAN JUAN BOSCO FACULTAD DE CIENCIAS NATURALES DEPARTAMENTO DE FARMACIA CATEDRA DE FARMACOGNOSIA TRABAJO PRACTICO Nº 3. PROTEINAS Y ENZIMAS. Objetivo - Utilizar reacciones
39. Aislamiento y purificación del DNA de un plásmido recombinante
 39. Aislamiento y purificación del DNA de un plásmido recombinante Aurora Galván Cejudo, Manuel Tejada, Antonio Camargo, José Javier Higuera, Vicente Mariscal, Emilio Fernández Reyes Departamento de Bioquímica
39. Aislamiento y purificación del DNA de un plásmido recombinante Aurora Galván Cejudo, Manuel Tejada, Antonio Camargo, José Javier Higuera, Vicente Mariscal, Emilio Fernández Reyes Departamento de Bioquímica
ESTRUCTURA Y FUNCIÓN DE LAS PROTEÍNAS BIOLOGÍA SESIÓN 4
 ESTRUCTURA Y FUNCIÓN DE LAS PROTEÍNAS BIOLOGÍA SESIÓN 4 Creado bajo licencia Creative Commons AUTORES: Emilia Matallana Redondo Julia Yumbe Baca Biología SESIÓN 4 BIOLOGÍA Estructura Y Función De Las Proteínas
ESTRUCTURA Y FUNCIÓN DE LAS PROTEÍNAS BIOLOGÍA SESIÓN 4 Creado bajo licencia Creative Commons AUTORES: Emilia Matallana Redondo Julia Yumbe Baca Biología SESIÓN 4 BIOLOGÍA Estructura Y Función De Las Proteínas
DETERMINACIÓN DEL MAPA DE UN PLÁSMIDO CON ENZIMAS DE RESTRICCIÓN
 DETERMINACIÓN DEL MAPA DE UN PLÁSMIDO CON ENZIMAS DE RESTRICCIÓN 6 grupos de estudiantes 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es desarrollar un conocimiento del mapaje de ADN determinando
DETERMINACIÓN DEL MAPA DE UN PLÁSMIDO CON ENZIMAS DE RESTRICCIÓN 6 grupos de estudiantes 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es desarrollar un conocimiento del mapaje de ADN determinando
LABORATORIO N 3 SOLUCIONES ACIDO-BASE Y BUFFER
 LABORATORIO N 3 SOLUCIONES ACIDO-BASE Y BUFFER 1.- INTRODUCCIÓN Soluciones Ácido-Base Los solutos disueltos en agua pueden clasificarse como electrolitos y no electrolitos en función de su capacidad de
LABORATORIO N 3 SOLUCIONES ACIDO-BASE Y BUFFER 1.- INTRODUCCIÓN Soluciones Ácido-Base Los solutos disueltos en agua pueden clasificarse como electrolitos y no electrolitos en función de su capacidad de
RESULTADOS Y DISCUSIÓN
 RESULTADOS Y DISCUSIÓN Estimación de la Concentración Proteica del Filtrado de Cultivo de Mycobacterium tuberculosis H37Rv La curva estándar con la que se estimó la concentración proteica del filtrado
RESULTADOS Y DISCUSIÓN Estimación de la Concentración Proteica del Filtrado de Cultivo de Mycobacterium tuberculosis H37Rv La curva estándar con la que se estimó la concentración proteica del filtrado
PRÁCTICAS AMPLIACIÓN DE MICROBIOLOGÍA
 PRÁCTICAS AMPLIACIÓN DE MICROBIOLOGÍA Día 1º.- EXPLICACIÓN GENERAL. TRANSFORMACIONES: E. coli, Streptomyces Día 2º.- INOCULAR MINIPREPS (8:45 de la mañana). OBTENCIÓN DE PLÁSMIDO ( MINIPREPS, Lisis alcalina)
PRÁCTICAS AMPLIACIÓN DE MICROBIOLOGÍA Día 1º.- EXPLICACIÓN GENERAL. TRANSFORMACIONES: E. coli, Streptomyces Día 2º.- INOCULAR MINIPREPS (8:45 de la mañana). OBTENCIÓN DE PLÁSMIDO ( MINIPREPS, Lisis alcalina)
Análisis de la Presencia de Organismos Genéticamente Modificados en Muestras de Alimentos
 Análisis de la Presencia de Organismos Genéticamente Modificados en Muestras de Alimentos Sesión nº 5 Electroforesis en gel de agarosa M. Somma, M. Querci WORLD HEALTH ORGANIZATION REGIONAL OFFICE FOR
Análisis de la Presencia de Organismos Genéticamente Modificados en Muestras de Alimentos Sesión nº 5 Electroforesis en gel de agarosa M. Somma, M. Querci WORLD HEALTH ORGANIZATION REGIONAL OFFICE FOR
ANEXO 1 ELECTROFORESIS DE PROTEINAS EN GELES DE POLIACRILAMIDA
 ANEXO 1 ELECTROFORESIS DE PROTEINAS EN GELES DE POLIACRILAMIDA Las proteínas son las macromoléculas más grandes y de más amplia distribución en la célula. Sus propiedades biológicas, así como muchas de
ANEXO 1 ELECTROFORESIS DE PROTEINAS EN GELES DE POLIACRILAMIDA Las proteínas son las macromoléculas más grandes y de más amplia distribución en la célula. Sus propiedades biológicas, así como muchas de
TEMA 6: PROTEÍNAS. Definición de proteínas y aminoácidos
 TEMA 6: PROTEÍNAS Dra. Mariana L. Ferramola Bioquímica Lic. en Enfermería 2016 Definición de proteínas y aminoácidos Las proteínas son macromoléculas de gran abundancia. Son polímeros formados por monómeros
TEMA 6: PROTEÍNAS Dra. Mariana L. Ferramola Bioquímica Lic. en Enfermería 2016 Definición de proteínas y aminoácidos Las proteínas son macromoléculas de gran abundancia. Son polímeros formados por monómeros
Se van a purificar dos proteínas, una de origen animal, la lisozima de la clara de huevo y otra vegetal la galactosidasa de hojas de espinaca.
 PRÁCTICA 1 PURIFICACIÓN DE ENZIMAS OBJETIVO: Extraer y purificar enzimas mediante cromatografía de intercambio iónico utilizando SP Sepharose y Q Sepharose, para posteriormente cuantificarlas en las diferentes
PRÁCTICA 1 PURIFICACIÓN DE ENZIMAS OBJETIVO: Extraer y purificar enzimas mediante cromatografía de intercambio iónico utilizando SP Sepharose y Q Sepharose, para posteriormente cuantificarlas en las diferentes
SAPONIFICACIÓN: SÍNTESIS DE JABÓN
 SAPONIFICACIÓN: SÍNTESIS DE JABÓN Objetivos: 1. Preparar jabón a partir de aceite vegetal 2. Observar las propiedades del jabón al someterlo a distintas pruebas. Introducción: Las propiedades de las grasas
SAPONIFICACIÓN: SÍNTESIS DE JABÓN Objetivos: 1. Preparar jabón a partir de aceite vegetal 2. Observar las propiedades del jabón al someterlo a distintas pruebas. Introducción: Las propiedades de las grasas
CUANTIFICACIÓN DE LA ACTIVIDAD ENZIMÁTICA Y DE LA ACTIVIDAD ESPECÍFICA DE LAS ENZIMAS
 CUANTIFICACIÓN DE LA ACTIVIDAD ENZIMÁTICA Y DE LA ACTIVIDAD ESPECÍFICA DE LAS ENZIMAS I. INTRODUCCIÓN No siendo posible medir la cantidad de enzima directamente de los líquidos y estructuras biológicas
CUANTIFICACIÓN DE LA ACTIVIDAD ENZIMÁTICA Y DE LA ACTIVIDAD ESPECÍFICA DE LAS ENZIMAS I. INTRODUCCIÓN No siendo posible medir la cantidad de enzima directamente de los líquidos y estructuras biológicas
TP2: Extracción y cuantificación de proteínas
 TP2: Extracción y cuantificación de proteínas Objetivos Obtener un extracto crudo de proteínas a partir de distintos órganos. Realizar un fraccionamiento a partir de una precipitación con Sulfato de Amonio.
TP2: Extracción y cuantificación de proteínas Objetivos Obtener un extracto crudo de proteínas a partir de distintos órganos. Realizar un fraccionamiento a partir de una precipitación con Sulfato de Amonio.
Estado de oxidación (E.O.)
 Reacciones Redox Estado de oxidación (E.O.) Es la carga que tendría un átomo si todos sus enlaces fueran iónicos. En el caso de enlaces covalentes polares habría que suponer que la pareja de electrones
Reacciones Redox Estado de oxidación (E.O.) Es la carga que tendría un átomo si todos sus enlaces fueran iónicos. En el caso de enlaces covalentes polares habría que suponer que la pareja de electrones
PURIFICACION PARCIAL DE LA CASEINA PRESENTE EN
 EXPERIMENTO 9 PURIFICACION PARCIAL DE LA CASEINA PRESENTE EN LA LECHE Y DETERMINACION DE SU PESO MOLECULAR Y DEL PRODUCTO DE LA HIDROLISIS POR LA ENZIMA BROMELINA DE LA PIÑA MEDIANTE ELECTROFORESIS REQUISITOS
EXPERIMENTO 9 PURIFICACION PARCIAL DE LA CASEINA PRESENTE EN LA LECHE Y DETERMINACION DE SU PESO MOLECULAR Y DEL PRODUCTO DE LA HIDROLISIS POR LA ENZIMA BROMELINA DE LA PIÑA MEDIANTE ELECTROFORESIS REQUISITOS
REPARTIDO DE PRÁCTICO DE ACTIVIDAD ENZIMATICA
 REPARTIDO DE PRÁCTICO DE ACTIVIDAD EZIMATICA Las enzimas son macromoléculas biológicas que aceleran la velocidad de una reacción hasta lograr el equilibrio. La enorme mayoría de las enzimas conocidas son
REPARTIDO DE PRÁCTICO DE ACTIVIDAD EZIMATICA Las enzimas son macromoléculas biológicas que aceleran la velocidad de una reacción hasta lograr el equilibrio. La enorme mayoría de las enzimas conocidas son
Ácidos nucléicos. Los ácidos nucleicos fueron descubiertos por Freidrich Miescher en Mirel Nervenis
 Ácidos nucléicos Los ácidos nucleicos fueron descubiertos por Freidrich Miescher en 1869 La información genética o genoma, está contenida en unas moléculas llamadas ácidos nucleicos. Existen dos tipos
Ácidos nucléicos Los ácidos nucleicos fueron descubiertos por Freidrich Miescher en 1869 La información genética o genoma, está contenida en unas moléculas llamadas ácidos nucleicos. Existen dos tipos
