HAVRIX vacuna para la prevención de la hepatitis A
|
|
|
- Sergio Méndez Aguilar
- hace 7 años
- Vistas:
Transcripción
1 Folleto Pediatras Havrix 720:Maquetación 1 29/09/10 17:30 Página 1 HAVRIX vacuna para la prevención de la hepatitis A Havrix 720 Pediátrica, para niños y adolescentes a partir de 1 año de edad hasta los 18 años inclusive10 HAVRIX 720 Pediátrica n Los niños inmunizados con Havrix consiguen altos niveles de anticuerpos protectores después de la 2ª dosis11. n Havrix es la vacuna frente a hepatitis A con datos de persistencia de inmunidad a largo plazo, seguimiento 10 años10. n Havrix pauta vacunal de 2 dosis n % de los niños y adolescentes alcanzan títulos protectores con la primera dosis12. vía intramuscular
2 Folleto Pediatras Havrix 720:Maquetación 1 29/09/10 17:31 Página 2 Pediátrica vacuna para la prevención de la hepatitis A
3 La hepatitis A es una de las enfermedades inmunoprevenibles más frecuentes La hepatitis A se transmite principalmente por vía fecal-oral 1 : n En un 50% de los casos no hay ningún factor de riesgo 1. Hepatitis A: impacto según la edad2 (Adaptado de la tabla 7) n La gravedad de la enfermedad aumenta con la edad 1. n En niños <6 años, la enfermedad suele ser asintomática, produciéndose ictericia sólo en el 10% de los casos 3. n En niños >6 años, la infección normalmente lleva a la enfermedad clínica, acompañada de ictericia en más del 70% de los casos 3. Manifestaciones clínicas: n Periodo de incubación: días (media de 28 días) 3,4. n Signos y síntomas 4. w Ictericia w Fiebre w Astemia w Pérdida de apetito w Náuseas w Molestias abdominales w Coluria n Sintomatología por grupo de edad 5. w < 3 años:16% w 3-4 años: 50% w >5 años: 80% n La infección clínica puede durar hasta 2 4.
4 n La hepatitis A es un problema de salud a nivel mundial. La OMS declara más de 1,4 millones de casos casos sintomáticos anualmente 1. Distribución geográfica de la infección por el virus de la hepatitis A 1. ESPAÑA Endemicidad 1 Incidencia 1 Edad media de los pacientes 1 Pico de edad de infección 1 Patrón de transmisión 1 Intermedia 5-60/ Infancia tardía, Adolescentes, Adultos jóvenes Persona a persona; Brotes epidémicos Pediátrica Vacuna frente a hepatitis A
5 Folleto Pediatras Havrix 720:Maquetación 1 29/09/10 17:31 Página 5 En un estudio realizado en EE.UU. se estimó que por cada caso declarado puede haber 10 infecciones asintomáticas o no declaradas2. Según disminuye la endemicidad, aumenta la gravedad de la enfermedad6. Mejora en las condiciones socioeconómicas Incremento del coste económico Descenso en la endemicidad Pediátrica Vacuna frente a hepatitis A Incremento de la edad de infección Incremento de la gravedad de la enfermedad
6 Folleto Pediatras Havrix 720:Maquetación 1 29/09/10 17:31 Página 6 Recomendaciones de Vacunación para la Hepatitis A Recomendaciones de la Asociación Española de Pediatría (AEP)7 CALENDARIO VACUNAL DE LA ASOCIACIÓN ESPAÑOLA DE PEDIATRIA 2010 COMITÉ ASESOR DE VACUNAS EDAD AÑOS EDAD MESES VACUNAS HB HB HB HB Difteria,Tétanos y Tos ferina2 DTPa DTPa DTPa DTPa Poliomielitis3 VPI VPI VPI VPI Haemophilus Influenzae tipo b4 Hib Hib Hib Hib Meningococo C5 MenC Neumococo6 VNC Hepatitis B MenC VNC Sarampión, Rubeola y Parotiditis DTPa VNC Tdpa VNC SRP SRP VPH - 3 d. RV - 2 ó 3 dosis Var Varicela10 Var Var - 2 d. Gripe Gripe11 HA - 2 dosis Hepatitis A12 Sistemáticas MenC Virus del Papiloma Humano8 Rotavirus Recomendable Grupo de riesgo n Vacuna antihepatitis A (HA).- 2 dosis con un intervalo de 6-12 m a partir de los 12 m de edad. Vacunación de pacientes con indicación por viajes internacionales a países con endemicidad intermedia o alta, o por pertenecer a grupos de riesgo7.
7 Folleto Pediatras Havrix 720:Maquetación 1 29/09/10 17:31 Página 7 Recomendaciones de Vacunación para la Hepatitis A Recomendaciones de la Organización Mundial de la Salud (OMS)3 n En las zonas en las que la transmisión en el conjunto de la población se produce sobre todo de una persona a otra, a menudo con brotes periódicos frecuentes, la lucha contra la hepatitis A se puede llevar a cabo mediante programas de inmunización generalizada. Recomendaciones del Comité Asesor de Vacunas de EE.UU. (ACIP)8 n Se recomienda la vacunación frente a la Hepatitis A a todos los niños >12 con un esquema de dosis separadas al menos 6. Pediátrica Vacuna frente a hepatitis A
8 CALENDARIO DE VACUNACIÓN RECOMENDADO PARA PERSONAS DE 0 A 6 AÑOS DE EDAD PARA LAS PERSONAS QUE ESTÉN ATRASADAS EN EL CALENDARIO DE VACUNACIÓN O COMIENCEN TARDE, CONSULTAR EL CALENDARIO DE ACTUALIZACIÓN 8 VACUNAS EDAD años 4-6 años Hepatitis B 1 Hep B HepB Ver referencia 1 HepB Rotavirus 2 Rota Rota 2 Difteria, Tétanos, Tos ferina 3 Haemophilus influezae tipo b 4 Antineumocócica 5 DTaP Hib PCV DTaP DTaP Ver referencia 3 DTaP DTaP Hib Hib 4 Hib PCV PCV PCV PPSV Antipoliomielítica inactivada Influenza (gripe) 6 Sarampión, Paperas, Rubéola 7 IPV IPV IPV IPV Influenza (anualmente) MMR Ver referencia 7 MMR Varicela 8 Varicela Ver referencia 8 Varicela Hepatitis A 9 HepA (2 dosis) Seria HepA Antimeningocócica 10 MCV Rango de edades recomendadas Ciertos grupos de alto riesgo CALENDARIO DE VACUNACIÓN RECOMENDADO PARA PERSONAS DE 7 A 18 AÑOS DE EDAD PARA LAS PERSONAS QUE ESTÉN ATRASADAS EN EL CALENDARIO DE VACUNACIÓN O COMIENCEN TARDE, CONSULTAR EL CALENDARIO SIGUIENTE Y EL CALENDARIO DE ACTUALIZACIÓN 9 VACUNAS EDAD 7-10 años años años Tétanos, Difteria, Tos ferina 1 Ver referencia 1 Tdap Tdap Virus del papiloma humano 2 Ver referencia 2 HPV (3 dosis) Serie HPV Antimeningocócica 3 MCV MCV MCV Influenza (gripe) 4 Inluenza (anualmente) Antineumocócica 5 PPSV Hepatitis A 6 Serie HepA Hepatitis B 7 Serie HepB Antipoliomielítica inactivada 8 Serie IPV Sarampión, paperas, rubéola 9 Serie MMR Varicela 10 Serie varicela Rango de edades recomendadas Ciertos grupos de alto riesgo Vacunación de actualización
9 Pediátrica HAVRIX vacuna para la prevención de la Hepatitis A 10 n HAVRIX es una vacuna de virus inactivados 10. HAVRIX 720 Pediátrica n HAVRIX 720, para niños y adolescentes a partir de 1 año de edad hasta los 18 años inclusive 10. HAVRIX 720 Pediátrica n Proporciona una rápida seroconversión tras la administración de una dosis 10. Adaptado de ficha técnica Havrix
10 n HAVRIX 720 ha demostrado ser eficaz en el control de brotes 10. n Estudios clínicos demostraron que la vacunación con Havrix condujo a la finalización de los brotes en diferentes comunidades (Alaska, Eslovaquia, Estados Unido, Reino Unido, Israel e Italia). n Una dosis de recuerdo entre 6-12 después de la 1ª dosis debería administrase para asegurar la protección a largo plazo 10. n Los resultados disponibles después de 10 años predicen que al menos el 97% de los sujetos continuarán siendo seropositivos 25 años después de la vacunación. HAVRIX 720 Pediátrica n Pauta vacunal de 2 dosis, por vía intramuscular 10. n Primovacunación: 1 dosis. A partir del año de edad hasta los 18 años inclusive n Dosis de recuerdo: entre los 6 y 12 después de la primovacunación 10. HAVRIX 720 Pediátrica n Havrix 720 tiene un buen perfil de seguridad 10. n Los síntomas solicitados (cefalea, malestar, vómitos, fiebre, náuseas y pérdida de apetito) fueron leves y no duraron más de 24 horas. Pediátrica Vacuna frente a hepatitis A
11 Pediátrica 1. NOMBRE DEL MEDICAMENTO. HAVRIX 1440, suspensión inyectable en jeringa precargada. HAVRIX 720, suspensión inyectable en jeringa precargada. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA. Havrix es una suspensión estéril que contiene el virus de la hepatitis A (VHA) (cepa HM 175) inactivado con formaldehído y adsorbido en hidróxido de aluminio. El virus se propaga en células diploides humanas MRC5. Antes de proceder a la extracción viral, las células se lavan cuidadosamente para eliminar los componentes del medio de cultivo. Después se obtiene una suspensión de virus mediante lisis de las células, seguido de purificación, empleando técnicas de ultrafiltración y cromatografía en gel. Los virus se inactivan con formalina. Havrix, cumple con los requisitos de la Organización Mundial de la Salud para la fabricación de productos biológicos. Havrix contiene una suspensión estéril purificada del virus de la hepatitis A inactivado: el contenido de antígeno viral se determina por una prueba ELISA. La dosis de Havrix 1440 para adultos, se estandariza para asegurar un contenido de no menos de 1440 Unidades ELISA de antígeno viral, en 1 ml de volumen. La dosis de Havrix 720 para niños y adolescentes, se estandariza para asegurar un contenido de no menos de 720 Unidades ELISA de antígeno viral, en 0,5 ml de volumen. Durante el proceso de producción se utiliza sulfato de neomicina. Tras el proceso de purificación solo existen residuos en la vacuna menores de 20 nanogramos/dosis en HAVRIX 1440 y menores de 10 nanogramos/dosis en Havrix 720. Asimismo, el formaldehído no alcanza más de 100 μg/ml. Para consultar la lista completa de excipientes, ver sección FORMA FARMACÉUTICA. suspensión para administración intramuscular en jeringa precargada. 4. DATOS CLÍNICOS Indicaciones terapéuticas. Havrix, esta indicado para la inmunización activa frente a la infección por el virus de la hepatitis A, en personas en riesgo de exposición al VHA. Havrix, no previene la hepatitis causada por otros agentes tales como el virus de la hepatitis B, hepatitis C, hepatitis E u otros patógenos conocidos que pueden infectar el hígado. No se conoce la duración de la inmunidad de la vacuna. Los individuos con anticuerpos específicos frente al VHA no precisan de la vacunación, no obstante, no es necesaria la realización de estudios serológicos previos a la vacunación. La vacunación de personas inmunes no presenta riesgo añadido Posología y forma de administración. Posología. Adultos a partir de 19 años de edad y en adelante. Para la vacunación primaria: administrar una dosis única de Havrix 1440 (1 ml de suspensión). Niños y adolescentes a partir de 1 año de edad hasta los 18 años inclusive. Para la vacunación primaria: administrar una dosis única de Havrix 720 (0,5 ml de suspensión). Para asegurar protección a largo plazo, se recomienda que se administre una dosis de recuerdo de Havrix 1440 (adultos) ó Havrix 720 (niños y adolescentes) en cualquier momento entre los 6 y 12 después de la vacunación primaria. En el caso de individuos que requieran tanto profilaxis postexposición como protección combinada inmediata o a largo plazo, puede administrarse simultáneamente inmunoglobulina utilizando diferentes sitios de inyección. Forma de administración. Havrix se debe administrar por vía intramuscular. En adultos, adolescentes y niños mayores, la vacuna debe inyectarse en la región deltoidea; en los niños muy pequeños, en la cara anterolateral del muslo. En pacientes hemofílicos o con trombocitopenia, la vacuna debe administrarse por vía subcutánea. Havrix debe administrarse con precaución en personas con trombocitopenia o trastornos hemorrágicos ya que se puede producir un sangrado tras de la administración intramuscular de la vacuna en estos sujetos Debería ejercerse una fuerte presión en el lugar de la inyección (sin frotar) durante al menos 2 minutos. Bajo ninguna circunstancia debe administrarse Havrix por vía intravenosa. La vacuna no debe administrarse por vía intramuscular en la región glútea, ni por vía subcutánea/intradérmica, dado que ello puede conducir a una menor respuesta de anticuerpos anti-vha Contraindicaciones. Como ocurre con otras vacunas, se debe posponer la administración de Havrix en personas con una enfermedad febril grave y aguda. Sin embargo, la presencia de una infección leve no es una contraindicación para la vacunación. No se debe administrar Havrix a personas con hipersensibilidad conocida a cualquier componente de la vacuna, ni a quienes hayan presentado signos de hipersensibilidad tras una administración anterior de Havrix Advertencias y precauciones especiales de empleo. Es posible que algunas personas se encuentren en el periodo de incubación de una infección por hepatitis A en el momento de la vacunación. No se sabe si en estos casos Havrix prevendrá frente a la hepatitis A en estos sujetos. Havrix puede ser administrado a personas infectadas por VIH. En pacientes sometidos a hemodiálisis y en personas con un sistema inmunológico deficiente, puede que no se obtengan títulos de anticuerpos anti-vha adecuados tras la dosis única de Havrix. Por tanto, estos pacientes podrán requerir la administración de dosis adicionales de vacuna. Como con todas las vacunas inyectables, se debe disponer de tratamiento médico adecuado para el caso poco común que se presente una reacción anafiláctica tras la administración de la vacuna. Por esta razón, el vacunado debería permanecer bajo supervisión médica durante 30 minutos tras la vacunación. Bajo ninguna circunstancia debe administrarse Havrix por vía intravenosa Interacción con otros medicamentos y otras formas de interacción. Dado que Havrix es una vacuna inactivada, es poco probable que su utilización concomitante con otras vacunas inactivadas, produzca interferencia con las respuestas inmunes. Cuando se considere necesaria la administración concomitante con otras vacunas, estas se tienen que administrar con jeringas diferentes y en lugares de inyección distintos. Se puede administrar inmunoglobulina y Havrix de manera simultánea en dos lugares diferentes. Las tasas de seroconversión no se modifican, pero los títulos de anticuerpos podrían ser menores que tras la vacunación con Havrix sola Embarazo y Lactancia. Embarazo. No se ha evaluado el efecto de Havrix sobre el desarrollo fetal. No hay datos disponibles adecuados para su uso en embarazo o lactancia, ni estudios de reproducción en animales. Sin embargo, como sucede con todas las vacunas víricas inactivadas, los riesgos para el feto se consideran mínimos. Havrix se debe utilizar durante el embarazo solo cuando sea claramente necesario. Lactancia. No están disponibles estudios en humanos durante la lactancia y de reproducción en animales. Aunque el riesgo puede ser considerado mínimo, Havrix solo debe ser usado durante la lactancia si es claramente necesario Efectos sobre la capacidad para conducir y utilizar máquinas. Es poco probable que la vacuna produzca algún efecto sobre la capacidad de conducir vehículos y utilizar maquinaria Reacciones adversas. Havrix presenta buena tolerancia. En estudios clínicos controlados, se monitorizaron en todas las personas los signos y síntomas durante los cuatro días posteriores a la administración de la vacuna. Para ello se utilizaron listas de comprobación de síntomas. También se solicitó a los vacunados que comunicaran cualquier acontecimiento clínico que ocurriera durante el periodo de estudio. La frecuencia de los acontecimientos adversos solicitados fue más baja tras la dosis de recuerdo de Havrix. La mayoría de los acontecimientos comunicados fueron considerados por los sujetos como leves y no duraron más de 24 horas. La frecuencia de los acontecimientos adversos solicitados tras la administración de Havrix, no es diferente de la comunicada tras la administración de otras vacunas de antígenos purificados adsorbidos en aluminio. De los acontecimientos adversos locales solicitados, el comunicado con mayor frecuencia fue dolor en el lugar de la inyección (menos del 0,5% informado como intenso) que remitió espontáneamente. Otros acontecimientos adversos locales solicitados y comunicados fueron ligero enrojecimiento e hinchazón, producidos con una frecuencia aproximada del 4 % de todas las vacunaciones. Los acontecimientos adversos sistémicos comunicados por los vacunados fueron esencialmente leves, la mayoría no duraron más de 24 horas e incluyeron cefalea, malestar, vómitos, fiebre, náuseas y pérdida de apetito. Estos acontecimientos se comunicaron con una frecuencia que variaba entre el 0,8% y el 12,8% de las vacunaciones. Todos ellos remitieron espontáneamente. La naturaleza de los signos y síntomas observados en los niños es similar a la de los adultos, sin embargo, se comunicaron con menor frecuencia. En muy raras ocasiones se han comunicado casos de fatiga, diarrea, mialgia, artralgia y reacciones alérgicas incluyendo reacciones anafilácticas y convulsiones Sobredosis. No procede. 5. PROPIEDADES FARMACOLÓGICAS Propiedades farmacodinámicas. Grupo farmacoterapéutico: Vacunas antihepatitis A, código ATC: J07BC02. Havrix, protege frente a la hepatitis A, mediante la inducción de anticuerpos específicos anti- VHA. En ensayos clínicos, el 99% de los vacunados seroconvirtieron 30 días después de la primera dosis. En un subgrupo de los estudios clínicos en los que fue estudiada la cinética de la respuesta inmunitaria, se demostró seroconversión temprana y rápida tras la administración de una dosis única de Havrix en un 79% de los vacunados en el día 13, un 86.3% en el día 15, un 95.2% en el día 17 y un 100% en el día 19, que es menor que el periodo medio de incubación de la hepatitis A (4 semanas). (Ver información preclínica). La eficacia de Havrix ha sido evaluada en diferentes brotes en comunidades (Alaska, Eslovaquia, Estados Unidos, Reino Unido, Israel e Italia). Los estudios demostraron que la vacunación con Havrix condujo a la finalización de los brotes. Una cobertura vacunal del 80% conduce a la interrupción de los brotes en un periodo de 4 a 8 semanas. Para asegurar la protección a largo plazo, debería administrarse una dosis de recuerdo entre 6 y 12 después de la primera dosis con Havrix 1440 o con Havrix 720. En los ensayos clínicos, prácticamente, todos los vacunados fueron seropositivos un mes después de la dosis de recuerdo. Sin embargo, si la dosis de recuerdo no se ha administrado entre 6 y 12 después de la primera dosis, la administración de esta dosis de recuerdo puede retrasarse hasta 5 años. En un ensayo clínico comparativo, la administración de una dosis de recuerdo hasta 5 años después de la primera dosis indujo títulos de anticuerpos similares a los conseguidos tras la administración de una dosis de recuerdo entre 6 y 12 después de la primera dosis. La persistencia de los títulos de anticuerpos de hepatitis A a largo plazo ha sido evaluada tras 2 dosis de Havrix administradas con una separación entre 6 y 12. Los resultados disponibles después de 10 años predicen que al menos un 97% de los sujetos continuarán siendo seropositivos (>20 mui/ml) 25 años después de la vacunación. Los datos actuales no justifican la necesidad de una dosis de recuerdo en individuos inmunocompetentes después de un ciclo de vacunación de 2 dosis Propiedades farmacocinéticas. No procede.5.3. Datos preclínicos sobre seguridad. Toxicología animal y/o farmacológica. Se han realizado los correspondientes ensayos sobre seguridad. En un experimento en 8 primates no humanos, los animales fueron expuestos a una cepa heteróloga de hepatitis A y vacunados 2 días después de la exposición. Esta vacunación post exposición dio como resultado la protección de todos los animales. 6. DATOS FARMACÉUTICOS Lista de excipientes. Hidróxido de aluminio (0,5 mg de ion aluminio/ml), aminoácidos para inyección, fosfato disódico, fosfato monopotásico, polisorbato 20, cloruro de potasio, cloruro de sodio, residuos de sulfato de neomicina (menos de 20 nanogramos/dosis en Havrix 1440 y menos de 10 nanogramos/dosis en Havrix 720) y agua para preparaciones inyectables. Para información sobre componentes residuales, ver sección Incompatibilidades. Havrix no se debe mezclar con otras vacunas en la misma jeringa Periodo de validez. La fecha de caducidad se indica en la etiqueta de la jeringa y en la caja. El periodo de validez de Havrix es de 3 años, cuando se conserva a la temperatura recomendada entre 2ºC y 8ºC Precauciones especiales de conservación. Conservar en nevera (entre 2ºC y 8ºC). No congelar. Desechar la vacuna si ha sido congelada Naturaleza y contenido del envase. Havrix se presentan en jeringa precargada. Las jeringas son de vidrio neutro tipo I y cumple con los requisitos de la Farmacopea Europea. Durante el almacenamiento, el contenido puede presentar un fino depósito blanquecino y un sobrenadante transparente incoloro Precauciones especiales de eliminación y otras manipulaciones. Antes de la administración, se debe inspeccionar visualmente la vacuna para detectar la presencia de partículas extrañas y/o cambios de color. Antes de utilizar Havrix se deberá agitar bien la jeringa para obtener una suspensión blanquecina ligeramente opaca. Desechar la vacuna, si el contenido aparece con otro aspecto. La eliminación del medicamento no utilizado y de todos los materiales que hayan estado en contacto con él, se realizará de acuerdo con la normativa local. 7. TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN. GlaxoSmithKline, S.A. PTM - Severo Ochoa, Tres Cantos. Madrid. 8. CONDICIONES DE PRESCRIPCION Y DISPENSACION. Con receta medica, cupón diferenciado. Reembolsable por el Sistema Nacional de Salud. Havrix 1440 P.V.P. 26,70, P.V.P. IVA 27,77. Havrix 720 P.V.P. 17,50, P.V.P. IVA 18,20 REFERENCIAS: 1. World Health Organization, Department of communicable disease surveillance and response. Hepatitis A. WHO/CDS/CSR/EDC/ CDC. Centers for Disease Control and Prevention. Hepatitis Surveillance Report No. 61. Atlanta, GA: U.S. Department of Health and Human Services, Centers for Disease Control and Prevention, Vacunas contra la hepatitis A. Información y recomendaciones sobre las vacunas utilizadas en el marco del programa Ampliado de inmunización (PAI). (Accedido Septiembre 2010) 4. CDC. Hepatitis A. Pink Book ; Feigein RD, Cherry MD, Demmler G, Kaplan S. Textbook of pediatric Infectious Diseases. 5ª edición. Volume Capítulo 172, página Andre FE. Universal mass vaccination against hepatitis A. Curr Top Microbiol Immunol 2006; 304: Mares J, Van Esso D, Arístegui J, Ruis J, González J, Merino M. et al. Calendario de vacunaciones de la asociación española de pediatría: recomendaciones An Pediatr (Barc) 2010;72 (6):443.e1-433.e Recommended immunization schedule for persons Aged 0 through 6 years (United states-2010) (Accedido Septiembre 2010) 9. Recommended immunization schedule for persons Aged 7 through 18 years (United states-2010) (Accedido Septiembre 2010) 10. Ficha técnica Havrix. 11. Ashur Y, Adler R, Rowe M, Shouval D. Comparison of immunogenicity of two hepatitis A vaccines- Vaqta and Havrix - in young adults. Vaccine 1999; 17: Fiore FE, Wasley A, Bell BP. Prevention of hepatitis A through active or passive immunization. Recommendations of the advisory committee on immunization practices (ACIP). MMWR Morb Mortal Wkly Rep Recommendations and reports 2006; 55 (RR07): REFERENCIAS CALENDARIO VACUNAL DE LA AEP: (1) Vacuna anti hepatitis B (HB): 3 dosis según dos pautas equivalentes: 0, 2, 6 ó 2, 4, 6. Ambas adecuadas para hijos de madres seronegativas (HBsAg negativo). Pacientes no vacunados según las pautas anteriores recibirán a cualquier edad 3 dosis según pauta 0, 1, 6. Hijos de madre HBsAg positivas recibirán en las primeras 12 horas de vida la 1ª dosis de vacuna + 0,5 ml de inmunoglobulina antihepatitis B, segunda dosis de vacuna al mes y la tercera dosis a los 6. Si la serología materna es desconocida debe administrase la 1ª dosis de vacuna en las primeras 12 horas de vida e investigar la serología inmediatamente, y si resulta positiva administrar la inmunoglobulina antihepatitis B en la primera semana de vida (preferentemente en las primeras 72 horas de vida). La administración de 4 dosis de vacuna anti-vhb es aceptable si se emplea la vacuna combinada hexavalente a los 2, 4 y 6 de edad en niños vacunados de HB al nacimiento. (2) Vacuna frente a difteria, tétanos, tos ferina acelular (DTPa / Tdpa): 6 dosis: Primovacunación con 3 dosis de vacuna DTPa. Dosis de refuerzo a los (cuarta dosis), 4-6 años (quinta dosis) con DTPa y a los años (sexta dosis) con el preparado para adultos de baja carga antigénica de difteria y tos ferina (Tdpa). (3) Vacuna antipoliomielitis inactivada (VPI): 4 dosis: Primovacunación con 3 dosis y dosis de refuerzo a los (cuarta dosis). (4) Vacuna conjugada frente a Haemophilus influenzae tipo b (Hib): 4 dosis: Primovacunación a los 2, 4, 6 y dosis de refuerzo a los (cuarta dosis). (5) Vacuna conjugada frente a meningococo C (MenC): 3 dosis: La primera a los 2, la segunda a los 4 ó 6, la tercera entre los 12 y 18. (6) Vacuna conjugada frente a neumococo (VNC): 4 dosis: Las tres primeras a los 2, 4, 6 con dosis
12 de refuerzo entre los (cuarta dosis). (7) Vacuna frente a sarampión, rubéola y parotiditis (SRP): 2 dosis de vacuna sarampión-rubéola-parotiditis (triple vírica). La primera a los y la segunda a los 3-4 años. (8) Vacuna frente al virus del papiloma humano (VPH): 3 dosis entre los años. Pauta vacunal según preparado comercial. Gardasil pauta 0, 2, 6 y Cervarix pauta 0, 1, 6. (9) Vacuna antirrotavirus (RV): 2 ó 3 dosis de vacuna frente a rotavirus según el preparado comercial. Rotarix 2 dosis a los 2 y 4. Rotateq 3 dosis a los 2, 4, 6 ó a los 2, 3, 4. La pauta debe completarse antes de las semanas de edad.(10) Vacuna frente a varicela (Var): 2 dosis: La primera a los y la segunda a los 3-4 años. En pacientes susceptibles fuera de las anteriores edades, vacunación con 2 dosis con un intervalo entre ellas de al menos 1 mes según edad en el momento de la vacunación. (11) Vacuna antigripal (Gripe): 1 dosis de vacuna antigripal inactivada a partir de los 6 de edad. Vacunación anual de pacientes con factores de riesgo para gripe; 1 dosis en mayores de 9 años; entre 6 y 9 años se administrarán 2 dosis la primera vez con un intervalo de un mes y revacunación anual con 1 dosis en los años siguientes. A la edad de 6 a 35 la dosis es de 0,25ml, mientras que a partir de 36 es de 0,5 ml. (12) Vacuna anti hepatitis A (HA): 2 dosis con un intervalo de 6-12 a partir de los 12 de edad. Vacunación de pacientes con indicación por viajes internacionales a países con endemicidad alta o por pertenecer a grupos de riesgo. REFERENCIAS CALENDARIO PERSONAS 0 A 6 AÑOS EN EE.UU. 1. Hepatitis B vaccine (HepB). (Minimum age: birth) At birth: Administer monovalent HepB to all newborns before hospital discharge. If mother is hepatitis B surface antigen (HBsAg)-positive, administer HepB and 0.5 ml of hepatitis B immune globulin (HBIG) within 12 hours of birth. If mother s HBsAg status is unknown, administer HepB within 12 hours of birth. Determine mother s HBsAg status as soon as possible and, if HBsAg-positive, administer HBIG (no later than age 1 week). After the birth dose: The HepB series should be completed with either monovalent HepB or a combination vaccine containing HepB. The second dose should be administered at age 1 or 2 months. Monovalent HepB vaccine should be used for doses administered before age 6 weeks. The final dose should be administered no earlier than age 24 weeks. Infants born to HBsAg-positive mothers should be tested for HBsAg and antibody to HBsAg 1 to 2 months after completion of at least 3 doses of the HepB series, at age 9 through 18 months (generally at the next well-child visit). Administration of 4 doses of HepB to infants is permissible when a combination vaccine containing HepB is administered after the birth dose. The fourth dose should be administered no earlier than age 24 weeks. 2. Rotavirus vaccine (RV). (Minimum age: 6 weeks) Administer the first dose at age 6 through 14 weeks (maximum age: 14 weeks 6 days). Vaccination should not be initiated for infants aged 15 weeks 0 days or older. The maximum age for the final dose in the series is 8 months 0 days. If Rotarix is administered at ages 2 and 4 months, a dose at 6 months is not indicated. 3. Diphtheria and tetanus toxoids and acellular pertussis vaccine (DTaP). (Minimum age: 6 weeks) The fourth dose may be administered as early as age 12 months, provided at least 6 months have elapsed since the third dose. Administer the final dose in the series at age 4 through 6 years. 4. Haemophilus influenzae type b conjugate vaccine (Hib). (Minimum age: 6 weeks) If PRP-OMP (PedvaxHIB or Comvax [HepB-Hib]) is administered at ages 2 and 4 months, a dose at age 6 months is not indicated. TriHiBit (DTaP/Hib) and Hiberix (PRP-T) should not be used for doses at ages 2, 4, or 6 months for the primary series but can be used as the final dose in children aged 12 months through 4 years. 5. Pneumococcal vaccine. (Minimum age: 6 weeks for pneumococcal conjugate vaccine [PCV]; 2 years for pneumococcal polysaccharide vaccine [PPSV]) PCV is recommended for all children aged younger than 5 years. Administer 1 dose of PCV to all healthy children aged 24 through 59 months who are not completely vaccinated for their age. Administer PPSV 2 or more months after last dose of PCV to children aged 2 years or older with certain underlying medical conditions, including a cochlear implant. See MMWR 1997;46(No. RR-8). 6. Inactivated poliovirus vaccine (IPV). (Minimum age: 6 weeks) The final dose in the series should be administered on or after the fourth birthday and at least 6 months following the previous dose. If 4 doses are administered prior to age 4 years a fifth dose should be administered at age 4 through 6 years. See MMWR 2009;58(30): Influenza vaccine (seasonal). (Minimum age: 6 months for trivalent inactivated influenza vaccine [TIV]; 2 years for live, attenuated influenza vaccine [LAIV]) Administer annually to children aged 6 months through 18 years. For healthy children aged 2 through 6 years (i.e., those who do not have underlying medical conditions that predispose them to influenza complications), either LAIV or TIV may be used, except LAIV should not be given to children aged 2 through 4 years who have had wheezing in the past 12 months. Children receiving TIV should receive 0.25 ml if aged 6 through 35 months or 0.5 ml if aged 3 years or older. Administer 2 doses (separated by at least 4 weeks) to children aged younger than 9 years who are receiving influenza vaccine for the first time or who were vaccinated for the first time during the previous influenza season but only received 1 dose. For recommendations for use of influenza A (H1N1) 2009 monovalent vaccine see MMWR 2009;58(No. RR-10). 8. Measles, mumps, and rubella vaccine (MMR). (Minimum age: 12 months) Administer the second dose routinely at age 4 through 6 years. However, the second dose may be administered before age 4, provided at least 28 days have elapsed since the first dose. 9. Varicella vaccine. (Minimum age: 12 months) Administer the second dose routinely at age 4 through 6 years. However, the second dose may be administered before age 4, provided at least 3 months have elapsed since the first dose. For children aged 12 months through 12 years the minimum interval between doses is 3 months. However, if the second dose was administered at least 28 days after the first dose, it can be accepted as valid. 10. Hepatitis A vaccine (HepA). (Minimum age: 12 months) Administer to all children aged 1 year (i.e., aged 12 through 23 months). Administer 2 doses at least 6 months apart. Children not fully vaccinated by age 2 years can be vaccinated at subsequent visits HepA also is recommended for older children who live in areas where vaccination programs target older children, who are at increased risk for infection, or for whom immunity against hepatitis A is desired. 11. Meningococcal vaccine. (Minimum age: 2 years for meningococcal conjugate vaccine [MCV4] and for meningococcal polysaccharide vaccine [MPSV4]) Administer MCV4 to children aged 2 through 10 years with persistent complement component deficiency, anatomic or functional asplenia, and certain other conditions placing tham at high risk. Administer MCV4 to children previously vaccinated with MCV4 or MPSV4 after 3 years if first dose administered at age 2 through 6 years. See MMWR 2009; 58: REFERENCIAS CALENDARIO PERSONAS 7 A 18 AÑOS EN EE.UU. 1. Tetanus and diphtheria toxoids and acellular pertussis vaccine (Tdap). (Minimum age: 10 years for Boostrix and 11 years for Adacel) Administer at age 11 or 12 years for those who have completed the recommended childhood DTP/DTaP vaccination series and have not received a tetanus and diphtheria toxoid (Td) booster dose. Persons aged 13 through 18 years who have not received Tdap should receive a dose. A 5-year interval from the last Td dose is encouraged when Tdap is used as a booster dose; however, a shorter interval may be used if pertussis immunity is needed. 2. Human papillomavirus vaccine (HPV). (Minimum age: 9 years) Two HPV vaccines are licensed: a quadrivalent vaccine (HPV4) for the prevention of cervical, vaginal and vulvar cancers (in females) and genital warts (in females and males), and a bivalent vaccine (HPV2) for the prevention of cervical cancers in females. HPV vaccines are most effective for both males and females when given before exposure to HPV through sexual contact. HPV4 or HPV2 is recommended for the prevention of cervical precancers and cancers in females. HPV4 is recommended for the prevention of cervical, vaginal and vulvar precancers and cancers and genital warts in females. Administer the first dose to females at age 11 or 12 years. Administer the second dose 1 to 2 months after the first dose and the third dose 6 months after the first dose (at least 24 weeks after the first dose). Administer the series to females at age 13 through 18 years if not previously vaccinated. HPV4 may be administered in a 3-dose series to males aged 9 through 18 years to reduce their likelihood of acquiring genital warts. 3. Meningococcal conjugate vaccine (MCV4). Administer at age 11 or 12 years, or at age 13 through 18 years if not previously vaccinated. Administer to previously unvaccinated college freshmen living in a dormitory. Administer MCV4 to children aged 2 through 10 years with persistent complement component deficiency, anatomic or functional asplenia, or certain other conditions placing them at high risk. Administer to children previously vaccinated with MCV4 or MPSV4 who remain at increased risk after 3 years (if first dose administered at age 2 through 6 years) or after 5 years (if first dose administered at age 7 years or older). Persons whose only risk factor is living in on-campus housing are not recommended to receive an additional dose. See MMWR 2009;58: Influenza vaccine (seasonal). Administer annually to children aged 6 months through 18 years. For healthy nonpregnant persons aged 7 through 18 years (i.e., those who do not have underlying medical conditions that predispose them to influenza complications), either LAIV or TIV may be used. Administer 2 doses (separated by at least 4 weeks) to children aged younger than 9 years who are receiving influenza vaccine for the first time or who were vaccinated for the first time during the previous influenza season but only received 1 dose. For recommendations for use of influenza A (H1N1) 2009 monovalent vaccine. See MMWR 2009;58(No. RR-10) 5. Pneumococcal polysaccharide vaccine (PPSV). Administer to children with certain underlying medical conditions, including a cochlear implant. A single revaccination should be administered after 5 years to children with functional or anatomic asplenia or an immunocompromising condition. See MMWR 1997;46(No. RR-8). 6. Hepatitis A vaccine (HepA). Administer 2 doses at least 6 months apart. HepA is recommended for children aged older than 23 months who live in areas where vaccination programs target older children, who are at increased risk for infection, or for whom immunity against hepatitis A is desired. 7. Hepatitis B vaccine (HepB). Administer the 3-dose series to those not previously vaccinated. A 2-dose series (separated by at least 4 months) of adult formulation Recombivax HB is licensed for children aged 11 through 15 years. 8. Inactivated poliovirus vaccine (IPV). The final dose in the series should be administered on or after the fourth birthday and at least 6 months following the previous dose. If both OPV and IPV were administered as part of a series, a total of 4 doses should be administered, regardless of the child s current age. 9. Measles, mumps, and rubella vaccine (MMR). If not previously vaccinated, administer 2 doses or the second dose for those who have received only 1 dose, with at least 28 days between doses. 10. Varicella vaccine. For persons aged 7 through 18 years without evidence of immunity (see MMWR 2007;56[No. RR-4]), administer 2 doses if not previously vaccinated or the second dose if only 1 dose has been administered. For persons aged 7 through 12 years, the minimum interval between doses is 3 months. However, if the second dose was administered at least 28 days after the first dose, it can be accepted as valid. For persons. ESP/HAV72/0001/10 OCTUBRE 2010 Pediátrica Vacuna frente a hepatitis A
NÚMERO DE DOSIS RECOMENDADO DE CADA VACUNA SEGÚN LA EDAD Asociación Española de Pediatría 2015 Comité Asesor de Vacunas.
 1 de enero de 2015 Esta tabla indica el número de necesarias según la edad, para los niños y los adolescentes con el calendario de vacunación incompleto o que comienzan la vacunación tardíamente. No se
1 de enero de 2015 Esta tabla indica el número de necesarias según la edad, para los niños y los adolescentes con el calendario de vacunación incompleto o que comienzan la vacunación tardíamente. No se
CALENDARIO DE VACUNACIONES DE LA ASOCIACIÓN ESPAÑOLA DE PEDIATRÍA Comité Asesor de Vacunas 2014
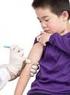 1 Esta tabla indica el número de necesarias, según la edad, para los niños y los adolescentes con el calendario de vacunación incompleto o que comienzan la vacunación tardíamente. No se ha de reiniciar
1 Esta tabla indica el número de necesarias, según la edad, para los niños y los adolescentes con el calendario de vacunación incompleto o que comienzan la vacunación tardíamente. No se ha de reiniciar
4. a dosis. 3 o dosis cuarta ver la nota a pie 5. 4. a. dosis. dosis. la primera. dosis. la primera. dosis. Ver la nota a pie 13
 Figura 1. Calendario de inmunización recomendado para las personas desde que nacen hasta los 18 años de edad 2013. (EN LO QUE RESPECTA A LAS PERSONAS QUE SE ATRASEN O SE TARDEN EN EMPEZAR, VEA EL CALENDARIO
Figura 1. Calendario de inmunización recomendado para las personas desde que nacen hasta los 18 años de edad 2013. (EN LO QUE RESPECTA A LAS PERSONAS QUE SE ATRASEN O SE TARDEN EN EMPEZAR, VEA EL CALENDARIO
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO. VANGUARD R Suspensión inyectable para perros, gatos, bovino, porcino, ovino, caprino, equino y hurones
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO VANGUARD R Suspensión inyectable para perros, gatos, bovino, porcino, ovino, caprino, equino y hurones 2. COMPOSICIÓN
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO VANGUARD R Suspensión inyectable para perros, gatos, bovino, porcino, ovino, caprino, equino y hurones 2. COMPOSICIÓN
No se necesita ninguna otra dosis si la primera dosis fue administrada a los 15 meses de edad o más
 Calendario de actualización de vacunas para personas de 4 a 18 años de edad que comienzan tarde a recibir las vacunas o están 1 mes o más atrasadas Estados Unidos, 2011 La tabla siguiente indica los calendarios
Calendario de actualización de vacunas para personas de 4 a 18 años de edad que comienzan tarde a recibir las vacunas o están 1 mes o más atrasadas Estados Unidos, 2011 La tabla siguiente indica los calendarios
IM cara anterolateral del muslo en los lactantes o el músculo deltoides de la parte superior del brazo en los niños.
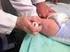 ESQUEMA CON VACUNAS ESPECIALES VACUNACION NO CUBIERTA POR EL PAN OBLIGATORIO DE SALUD Hepatitis B Anti hepatitis B A partir de los 5 º dosis en la fecha elegida. ª un mes después de la primera dosis. ª
ESQUEMA CON VACUNAS ESPECIALES VACUNACION NO CUBIERTA POR EL PAN OBLIGATORIO DE SALUD Hepatitis B Anti hepatitis B A partir de los 5 º dosis en la fecha elegida. ª un mes después de la primera dosis. ª
CALENDARIO DE VACUNACIONES DE LA ASOCIACIÓN ESPAÑOLA DE PEDIATRÍA Comité Asesor de Vacunas 2016
 1 de enero de 2016 Esta tabla indica el número de necesarias, según la edad, para los niños y los adolescentes con el calendario de vacunación incompleto o que comienzan la vacunación tardíamente. No se
1 de enero de 2016 Esta tabla indica el número de necesarias, según la edad, para los niños y los adolescentes con el calendario de vacunación incompleto o que comienzan la vacunación tardíamente. No se
Vacuna contra la poliomielitis. (Comentarios a las fichas técnicas)
 Vacuna contra la poliomielitis (Comentarios a las fichas técnicas) Prof. Ángel Gil de Miguel, Catedrático de Medicina Preventiva y Salud Pública, Universidad Rey Juan Carlos, Comunidad de Madrid Composición
Vacuna contra la poliomielitis (Comentarios a las fichas técnicas) Prof. Ángel Gil de Miguel, Catedrático de Medicina Preventiva y Salud Pública, Universidad Rey Juan Carlos, Comunidad de Madrid Composición
FICHA TÉCNICA. Adsorbido en hidróxido de aluminio hidratado Total: 0,50 mg Al 3+ Una dosis (0,5 ml) de Havrix 720 contiene: 720 Unidades ELISA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Havrix 1440 suspensión inyectable en jeringa precargada Havrix 720 suspensión inyectable en jeringa precargada Vacuna antihepatitis A (inactivada, adsorbida) 2.
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Havrix 1440 suspensión inyectable en jeringa precargada Havrix 720 suspensión inyectable en jeringa precargada Vacuna antihepatitis A (inactivada, adsorbida) 2.
REEMBOLSO DE GASTOS DE FARMACIA 2016
 REEMBOLSO DE GASTOS DE FARMACIA 2016 Garantía prestada desde 1 de enero de 2014 exclusivamente para clientes particulares de los productos Caser Salud Prestigio, Caser Salud Integral y Caser Salud Activa.
REEMBOLSO DE GASTOS DE FARMACIA 2016 Garantía prestada desde 1 de enero de 2014 exclusivamente para clientes particulares de los productos Caser Salud Prestigio, Caser Salud Integral y Caser Salud Activa.
FICHA TÉCNICA. VAXIGRIP 2016 Vacuna anti-influenza inactivada suspensión inyectable
 FICHA TÉCNICA VAXIGRIP 2016 Vacuna anti-influenza inactivada suspensión inyectable 1. NOMBRE DEL MEDICAMENTO VAXIGRIP, suspensión inyectable en jeringa precargada Vacuna antiinfluenza de virus fraccionados,
FICHA TÉCNICA VAXIGRIP 2016 Vacuna anti-influenza inactivada suspensión inyectable 1. NOMBRE DEL MEDICAMENTO VAXIGRIP, suspensión inyectable en jeringa precargada Vacuna antiinfluenza de virus fraccionados,
Guía de Referencia Rápida. Vacunación en la Embarazada GPC. Guía de Práctica Clínica. Catálogo maestro de guías de práctica clínica: IMSS-580-12
 Guía de Referencia Rápida Vacunación en la Embarazada GPC Guía de Práctica Clínica Catálogo maestro de guías de práctica clínica: IMSS-580-12 Guía de Referencia Rápida Z24 Necesidad de inmunización contra
Guía de Referencia Rápida Vacunación en la Embarazada GPC Guía de Práctica Clínica Catálogo maestro de guías de práctica clínica: IMSS-580-12 Guía de Referencia Rápida Z24 Necesidad de inmunización contra
INFORME DE UTILIDAD TERAPÉUTICA VACUNA ANTINEUMOCÓCICA CONJUGADA DE 13 SEROTIPOS, PREVENAR 13
 INFORME DE UTILIDAD TERAPÉUTICA VACUNA ANTINEUMOCÓCICA CONJUGADA DE 13 SEROTIPOS, PREVENAR 13 Este informe está destinado al personal sanitario Fecha de elaboración del informe: 11 de abril de 2013 Versión
INFORME DE UTILIDAD TERAPÉUTICA VACUNA ANTINEUMOCÓCICA CONJUGADA DE 13 SEROTIPOS, PREVENAR 13 Este informe está destinado al personal sanitario Fecha de elaboración del informe: 11 de abril de 2013 Versión
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO BOVILIS BVD Suspensión inyectable para bovino. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por dosis
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO BOVILIS BVD Suspensión inyectable para bovino. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por dosis
SFGH FHC Healthy Children Vaccination Program Frequently Asked Questions
 SFGH FHC Healthy Children Vaccination Program Frequently Asked Questions The Family Health Center (FHC) Healthy Children Vaccination Program at SF General Hospital (SFGH) provides immunization services
SFGH FHC Healthy Children Vaccination Program Frequently Asked Questions The Family Health Center (FHC) Healthy Children Vaccination Program at SF General Hospital (SFGH) provides immunization services
CALENDARIOS DE VACUNACIÓN INFANTIL DE ARAGÓN. Serie cronológica VPO VPO VPO DTP SRP VPO DTP HB* SRP. 0 m 2 m 4 m 6 m 15 m 18 m 6 a 11 a 14 a.
 CALENDARIOS DE VACUNACIÓN INFANTIL DE ARAGÓN 1984 1995 Serie cronológica Versión 21/03/2016 0 m 1 m 3 m 5 m 7 m 15 m 18 m 6 años 11 a 14 a DT T T * * * 1984: se incluye la vacuna de Polio atenuada trivalente
CALENDARIOS DE VACUNACIÓN INFANTIL DE ARAGÓN 1984 1995 Serie cronológica Versión 21/03/2016 0 m 1 m 3 m 5 m 7 m 15 m 18 m 6 años 11 a 14 a DT T T * * * 1984: se incluye la vacuna de Polio atenuada trivalente
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO DIFTAVAX suspensión inyectable en jeringa precargada Vacuna antidiftero-tetánica (adsorbida) para adultos y adolescentes. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO DIFTAVAX suspensión inyectable en jeringa precargada Vacuna antidiftero-tetánica (adsorbida) para adultos y adolescentes. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
Vacuna Nacimiento 2 meses 4 meses 6 meses 9 meses 12 meses 15 meses 18 meses Hepatitis B 1 1ª dosis 2ª dosis 3ª dosis
 1 Calendario de vacunación recomendado para las personas de 0-18 años años de edad, ESTADOS UNIDOS DE NORTEAMERICA, 2015. Este programa incluye recomendaciones vigentes a partir del 1 de enero de 2015.
1 Calendario de vacunación recomendado para las personas de 0-18 años años de edad, ESTADOS UNIDOS DE NORTEAMERICA, 2015. Este programa incluye recomendaciones vigentes a partir del 1 de enero de 2015.
INFORME DE UTILIDAD TERAPÉUTICA VACUNA ANTIMENINGOCÓCICA TETRAVALENTE CONJUGADA, NIMENRIX
 INFORME DE UTILIDAD TERAPÉUTICA VACUNA ANTIMENINGOCÓCICA TETRAVALENTE CONJUGADA, NIMENRIX Este informe está destinado al personal sanitario Fecha de elaboración del informe: 30 de mayo 2013 Versión: 1
INFORME DE UTILIDAD TERAPÉUTICA VACUNA ANTIMENINGOCÓCICA TETRAVALENTE CONJUGADA, NIMENRIX Este informe está destinado al personal sanitario Fecha de elaboración del informe: 30 de mayo 2013 Versión: 1
LABORATORIOS NORMON, S.A. AMBROXOL NORMON 15 mg/5 ml Jarabe EFG
 1. NOMBRE DEL MEDICAMENTO 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada 5 ml de jarabe contienen: AMBROXOL (D.C.I.) hidrocloruro 15 mg Excipientes, ver apartado 6.1. 3. FORMA FARMACEUTICA Jarabe. 4. DATOS
1. NOMBRE DEL MEDICAMENTO 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada 5 ml de jarabe contienen: AMBROXOL (D.C.I.) hidrocloruro 15 mg Excipientes, ver apartado 6.1. 3. FORMA FARMACEUTICA Jarabe. 4. DATOS
Vacunas Tosferina. Quién debe recibir la vacuna?
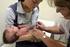 Vacunas Tosferina Dos vacunas nuevas que contienen la vacuna acelular contra la tosferina fueron aprobadas en el 2005 por la FDA para uso en personas mayores. Estas vacunas son abreviadas Tdap. Una es
Vacunas Tosferina Dos vacunas nuevas que contienen la vacuna acelular contra la tosferina fueron aprobadas en el 2005 por la FDA para uso en personas mayores. Estas vacunas son abreviadas Tdap. Una es
CENTROS DE VACUNACIÓN
 Vacunación Infantil INTRODUCCIÓN a vacunación constituye una de las medidas más eficaces de la moderna salud pública para la prevención de importantes enfermedades que afectan a todos los ciudadanos, pero
Vacunación Infantil INTRODUCCIÓN a vacunación constituye una de las medidas más eficaces de la moderna salud pública para la prevención de importantes enfermedades que afectan a todos los ciudadanos, pero
La vacunación frente a la tos ferina: no es sólo para niños
 GSKEDC-SPN-2010-Boostrix-1210_D12:Layout 1 6/14/2010 6:39 PM Page 1 La vacunación frente a la tos ferina: no es sólo para niños La tos ferina es una de las enfermedades infecciosas más contagiosas y actualmente
GSKEDC-SPN-2010-Boostrix-1210_D12:Layout 1 6/14/2010 6:39 PM Page 1 La vacunación frente a la tos ferina: no es sólo para niños La tos ferina es una de las enfermedades infecciosas más contagiosas y actualmente
Inflexal V, suspensión inyectable Vacuna antigripal (antígeno de superficie, inactivado, virosoma). Campaña 2013/2014
 RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Inflexal V, suspensión inyectable Vacuna antigripal (antígeno de superficie, inactivado, virosoma). Campaña 2013/2014 2. COMPOSICIÓN
RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Inflexal V, suspensión inyectable Vacuna antigripal (antígeno de superficie, inactivado, virosoma). Campaña 2013/2014 2. COMPOSICIÓN
PRIMERA REUNION NACIONAL DE HEPATITIS B y C. Marcela Avendaño V. Enfermera Departamento de Vacunas e Inmunizaciones Ministerio de Salud
 PRIMERA REUNION NACIONAL DE HEPATITIS B y C Marcela Avendaño V. Enfermera Departamento de Vacunas e Inmunizaciones Ministerio de Salud Misión: Protección de la población chilena frente a enfermedades inmunoprevenibles
PRIMERA REUNION NACIONAL DE HEPATITIS B y C Marcela Avendaño V. Enfermera Departamento de Vacunas e Inmunizaciones Ministerio de Salud Misión: Protección de la población chilena frente a enfermedades inmunoprevenibles
Aproveche la atención preventiva como herramienta para controlar su salud
 Aproveche la atención preventiva como herramienta para controlar su salud La prevención de enfermedades y la detección de problemas de salud en una etapa inicial, cuando los hay, son importantes para llevar
Aproveche la atención preventiva como herramienta para controlar su salud La prevención de enfermedades y la detección de problemas de salud en una etapa inicial, cuando los hay, son importantes para llevar
ACTUALIZACIÓN VACUNAS. Clínica Médica A Prof. Dra. Gabriela Ormaechea Junio 2015 Dr. Leonardo Oliva Sala 1
 ACTUALIZACIÓN VACUNAS Clínica Médica A Prof. Dra. Gabriela Ormaechea Junio 2015 Dr. Leonardo Oliva Sala 1 Edward Jenner 1749-1823 OBJETIVOS Realizar breve introducción al actual CEV en nuestro país Destacar
ACTUALIZACIÓN VACUNAS Clínica Médica A Prof. Dra. Gabriela Ormaechea Junio 2015 Dr. Leonardo Oliva Sala 1 Edward Jenner 1749-1823 OBJETIVOS Realizar breve introducción al actual CEV en nuestro país Destacar
CALENDARIO DE VACUNACIÓN INFANTIL CASTILLA - LA MANCHA 2016
 INTRODUCCIÓN CALENDARIO DE VACUNACIÓN INFANTIL CASTILLA - LA MANCHA 2016 El calendario de inmunización infantil establece las vacunas recomendadas en esta etapa de la vida y sus pautas de administración.
INTRODUCCIÓN CALENDARIO DE VACUNACIÓN INFANTIL CASTILLA - LA MANCHA 2016 El calendario de inmunización infantil establece las vacunas recomendadas en esta etapa de la vida y sus pautas de administración.
INFORMACIÓN QUE DEBE FIGURAR EN EL EMBALAJE EXTERIOR. Vacuna antigripal pandémica (antígenos de superficie, inactivada, adyuvada)
 A. ETIQUETADO 28 INFORMACIÓN QUE DEBE FIGURAR EN EL EMBALAJE EXTERIOR CAJA DE CARTÓN PARA JERINGA 1. NOMBRE DEL MEDICAMENTO Focetria suspensión inyectable en jeringa precargada Vacuna antigripal pandémica
A. ETIQUETADO 28 INFORMACIÓN QUE DEBE FIGURAR EN EL EMBALAJE EXTERIOR CAJA DE CARTÓN PARA JERINGA 1. NOMBRE DEL MEDICAMENTO Focetria suspensión inyectable en jeringa precargada Vacuna antigripal pandémica
ORDEN FORAL /2015, de, del Consejero de Salud, por la que se modifica el Calendario Oficial de Vacunaciones Infantiles de Navarra.
 ORDEN FORAL /2015, de, del Consejero de Salud, por la que se modifica el Calendario Oficial de Vacunaciones Infantiles de Navarra. Por Orden Foral 9/1996, de 25 de enero, del Consejero de Salud, se creó
ORDEN FORAL /2015, de, del Consejero de Salud, por la que se modifica el Calendario Oficial de Vacunaciones Infantiles de Navarra. Por Orden Foral 9/1996, de 25 de enero, del Consejero de Salud, se creó
Recomendaciones de vacunación para los estudiantes de Ciencias de la Salud que realicen prácticas en Centros Sanitarios del Principado de Asturias
 CIRCULAR: 07/2015 de 30 de octubre de 2015 ORIGEN: Dirección General de ÁMBITO: Programa de Vacunaciones de Asturias ASUNTO: Recomendaciones de vacunación para los estudiantes de Ciencias de la Salud que
CIRCULAR: 07/2015 de 30 de octubre de 2015 ORIGEN: Dirección General de ÁMBITO: Programa de Vacunaciones de Asturias ASUNTO: Recomendaciones de vacunación para los estudiantes de Ciencias de la Salud que
100 UI 80 mg 95% IgG
 1. NOMBRE DEL MEDICAMENTO IGANTIBE 200 UI/ml solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA - Principio activo: 100 UI/0,5 ml 600 UI/3 ml 1000 UI/5 ml Inmunoglobulina humana antihepatitis
1. NOMBRE DEL MEDICAMENTO IGANTIBE 200 UI/ml solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA - Principio activo: 100 UI/0,5 ml 600 UI/3 ml 1000 UI/5 ml Inmunoglobulina humana antihepatitis
Corrección de calendario vacunal abril María Rosa Albañil Pediatra CS Cuzco GPI- AEPap
 Corrección de calendario vacunal abril 2016 María Rosa Albañil Pediatra CS Cuzco GPI- AEPap Niño de 2 años y 3 meses Nacido en Londres, donde ha residido hasta ahora Sano, no patología previa, no recibe
Corrección de calendario vacunal abril 2016 María Rosa Albañil Pediatra CS Cuzco GPI- AEPap Niño de 2 años y 3 meses Nacido en Londres, donde ha residido hasta ahora Sano, no patología previa, no recibe
Vacuna frente a Haemophilus influenzae tipo b
 Vacuna frente a Haemophilus influenzae tipo b Prof. Ángel Gil de Miguel, Catedrático de Medicina Preventiva y Salud Pública, Universidad Rey Juan Carlos, Comunidad de Madrid Previo al empleo sistemático
Vacuna frente a Haemophilus influenzae tipo b Prof. Ángel Gil de Miguel, Catedrático de Medicina Preventiva y Salud Pública, Universidad Rey Juan Carlos, Comunidad de Madrid Previo al empleo sistemático
Más allá de proteger al vacunado. Dra. Juanita Zamorano R. Pediatra-Infectologa Universidad de los Andes Clínica Santa María
 Más allá de proteger al vacunado Dra. Juanita Zamorano R. Pediatra-Infectologa Universidad de los Andes Clínica Santa María Más allá de proteger al vacunado Inmunidad de rebaño Estrategia capullo Inmunización
Más allá de proteger al vacunado Dra. Juanita Zamorano R. Pediatra-Infectologa Universidad de los Andes Clínica Santa María Más allá de proteger al vacunado Inmunidad de rebaño Estrategia capullo Inmunización
Ayude a proteger a su hijo. Guía rápida de las vacunas infantiles.
 Ayude a proteger a su hijo. Guía rápida de las vacunas infantiles. Por qué son importantes las vacunas. Gracias a los programas de vacunación masiva, se han eliminado muchas de las enfermedades que pueden
Ayude a proteger a su hijo. Guía rápida de las vacunas infantiles. Por qué son importantes las vacunas. Gracias a los programas de vacunación masiva, se han eliminado muchas de las enfermedades que pueden
MINISTERIO DE SALUD PANAMA PROGRAMA AMPLIADO DE INMUNIZACION
 MINISTERIO DE SALUD PANAMA PROGRAMA AMPLIADO DE INMUNIZACION La vacunación de la población escolar, adolescentes y adultos jóvenes: análisis de casos en HPV, acp, MMR, Hepatitis B Enf Argelis Espinosa
MINISTERIO DE SALUD PANAMA PROGRAMA AMPLIADO DE INMUNIZACION La vacunación de la población escolar, adolescentes y adultos jóvenes: análisis de casos en HPV, acp, MMR, Hepatitis B Enf Argelis Espinosa
El sistema inmune y las vacunas
 SESIÓN DE INFORMACIÓN SOBRE VACUNAS, Santiago, Chile 7 de mayo 9 mayo, 2014 El sistema inmune y las vacunas Dra. Juanita Zamorano R Pediatra- Infectóloga jzamorano@uandes.cl 1 Jenner: En 1796 inicia la
SESIÓN DE INFORMACIÓN SOBRE VACUNAS, Santiago, Chile 7 de mayo 9 mayo, 2014 El sistema inmune y las vacunas Dra. Juanita Zamorano R Pediatra- Infectóloga jzamorano@uandes.cl 1 Jenner: En 1796 inicia la
I. Principado de Asturias
 núm. 49 de 29-ii-2016 1/5 I. Principado de Asturias Ot r a s Disposiciones Consejería de Sanidad Resolución de 17 de febrero de 2016, de la Consejería de Sanidad, por la que se aprueba el nuevo calendario
núm. 49 de 29-ii-2016 1/5 I. Principado de Asturias Ot r a s Disposiciones Consejería de Sanidad Resolución de 17 de febrero de 2016, de la Consejería de Sanidad, por la que se aprueba el nuevo calendario
sobre VACUNAS 15 respuestas a las 15 preguntas más frecuentes 1. Qué son las vacunas?
 15 respuestas a las 15 preguntas más frecuentes sobre VACUNAS 1.- Qué son las vacunas? 2.- Cómo funcionan las vacunas? 3. Por qué debo vacunar a mi hijo? 4. Qué enfermedades evitan las vacunas? 5. Cuántas
15 respuestas a las 15 preguntas más frecuentes sobre VACUNAS 1.- Qué son las vacunas? 2.- Cómo funcionan las vacunas? 3. Por qué debo vacunar a mi hijo? 4. Qué enfermedades evitan las vacunas? 5. Cuántas
Inmunización. Vacunación de mujeres embarazadas: De rutina: Para viajes y otras indicaciones:
 1 de 10 02/06/2008 16:13 CDC en Español Acerca de los CDC Suscríbase Temas de salud A-Z Empleo Búsqueda Contáctenos CDC in English Temas generales Grupos específicos Otros enlaces e idiomas Eventos y conferencias
1 de 10 02/06/2008 16:13 CDC en Español Acerca de los CDC Suscríbase Temas de salud A-Z Empleo Búsqueda Contáctenos CDC in English Temas generales Grupos específicos Otros enlaces e idiomas Eventos y conferencias
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Fevaxyn Pentofel, suspensión inyectable para gatos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Fevaxyn Pentofel, suspensión inyectable para gatos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
Triple-S Salud / Cubierta Estándar de Vacunación para Niños y Adolescentes
 Triple-S Salud / Cubierta Estándar de Vacunación para Niños y Adolescentes La tabla en esta página define la cubierta estándar de vacunas de Triple-S Salud. Las excepciones a la cubierta estándar, se señalan
Triple-S Salud / Cubierta Estándar de Vacunación para Niños y Adolescentes La tabla en esta página define la cubierta estándar de vacunas de Triple-S Salud. Las excepciones a la cubierta estándar, se señalan
Servicio de Vigilancia Epidemiológica Dirección General de Salud Pública Consejería de Sanidad
 Servicio de Vigilancia Epidemiológica Dirección General de Salud Pública Consejería de Sanidad El Programa de Vacunaciones de Asturias desea agradecer a todos los profesionales implicados, sanitarios y
Servicio de Vigilancia Epidemiológica Dirección General de Salud Pública Consejería de Sanidad El Programa de Vacunaciones de Asturias desea agradecer a todos los profesionales implicados, sanitarios y
RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO
 DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Poulvac Marek CVI Suspensión y disolvente para suspensión inyectable para
DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Poulvac Marek CVI Suspensión y disolvente para suspensión inyectable para
GUÍA DE MANEJO CLÍNICO ADDENDUM. esto se correlacione con falta de protección; no siendo esto indicación para revacunar. Ver gráficas I y II.
 GUÍA DE MANEJO CLÍNICO ESQUEMA DE INMUNIZACIONES PARA NIÑOS, NIÑAS Y ADOLESCENTES EN VENEZUELA. RECOMENDACIONES PARA 2013-2014 SOCIEDAD VENEZOLANA DE PUERICULTURA Y PEDIATRIA Carrizo Ch Juan T(1), Izaguirre
GUÍA DE MANEJO CLÍNICO ESQUEMA DE INMUNIZACIONES PARA NIÑOS, NIÑAS Y ADOLESCENTES EN VENEZUELA. RECOMENDACIONES PARA 2013-2014 SOCIEDAD VENEZOLANA DE PUERICULTURA Y PEDIATRIA Carrizo Ch Juan T(1), Izaguirre
CHARLA DE VACUNACIÓN INFANTIL PARA MADRES Y PADRES
 CHARLA DE VACUNACIÓN INFANTIL PARA MADRES Y PADRES José Tomás Rojas Centro de Salud Zaidín Sur INFECCIONES Enfermedades producidas por microbios (microscópicos), muy frecuente en la infancia, la mayoría
CHARLA DE VACUNACIÓN INFANTIL PARA MADRES Y PADRES José Tomás Rojas Centro de Salud Zaidín Sur INFECCIONES Enfermedades producidas por microbios (microscópicos), muy frecuente en la infancia, la mayoría
K:\Jenner_Public\QSS\VACCINE QUALITY & REGULATION GROUP\Inserts\Spanish\esp_Insert measles rubella Vd2-rev.doc
 MODELO DE PROSPECTO VACUNA COMBINADA CONTRA EL SARAMPIÓN Y LA RUBÉOLA (MR) DESCRIPCIÓN La vacuna MR es un polvo liofilizado que contiene dos antígenos, el del sarampión y el de la rubéola. Debe reconstituirse
MODELO DE PROSPECTO VACUNA COMBINADA CONTRA EL SARAMPIÓN Y LA RUBÉOLA (MR) DESCRIPCIÓN La vacuna MR es un polvo liofilizado que contiene dos antígenos, el del sarampión y el de la rubéola. Debe reconstituirse
COOPEXXONMOBIL Y CRECER CENTRO DE VACUNACIÓN LTDA. Entidad que busca fomentar la promoción y el control de enfermedades infecciosas, brindando
 COOPEXXONMOBIL Y CRECER CENTRO DE VACUNACIÓN LTDA. Entidad que busca fomentar la promoción y el control de enfermedades infecciosas, brindando siempre una atención profesional con alto conocimiento científico.
COOPEXXONMOBIL Y CRECER CENTRO DE VACUNACIÓN LTDA. Entidad que busca fomentar la promoción y el control de enfermedades infecciosas, brindando siempre una atención profesional con alto conocimiento científico.
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Twinrix Adultos, suspensión inyectable Vacuna (HAB) (adsorbida) antihepatitis A (inactivada) y antihepatitis
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Twinrix Adultos, suspensión inyectable Vacuna (HAB) (adsorbida) antihepatitis A (inactivada) y antihepatitis
CALENDARIO VACUNAL INFANTIL. 2013
 CALENDARIO VACUNAL INFANTIL. 2013 2013 Dr. Fernando Malmierca Sánchez Salamanca 2013 CALENDARIO VACUNAL INFANTIL. 2013 PREHISTORIA DE LAS VACUACIONES EL MÉTODO CIENTÍFICO DE JENNER (1796) Inoculó material
CALENDARIO VACUNAL INFANTIL. 2013 2013 Dr. Fernando Malmierca Sánchez Salamanca 2013 CALENDARIO VACUNAL INFANTIL. 2013 PREHISTORIA DE LAS VACUACIONES EL MÉTODO CIENTÍFICO DE JENNER (1796) Inoculó material
If you need this information in English, please call us.
 Juntos en... prevención Guía Preventiva de Salud Kern Family Health Care quiere que usted tenga el mejor cuidado de salud. Esta guía preventiva le ayudará a mantenerse saludable mediante la prevención
Juntos en... prevención Guía Preventiva de Salud Kern Family Health Care quiere que usted tenga el mejor cuidado de salud. Esta guía preventiva le ayudará a mantenerse saludable mediante la prevención
CALENDARIOS DE VACUNACIÓN INFANTIL DE ARAGÓN. Serie cronológica VPO VPO VPO DTP SRP VPO DTP HB* SRP. 0 m 2 m 4 m 6 m 15 m 18 m 6 a 11 a 14 a.
 CALENDARIOS DE VACUNACIÓN INFANTIL DE ARAGÓN Serie cronológica 1984 1995 Versión 2/02/2016 0 m 1 m 3 m 5 m 7 m 15 m 18 m 6 años 11 a 14 a DT T T * * * 1984: se incluye la vacuna de Polio atenuada trivalente
CALENDARIOS DE VACUNACIÓN INFANTIL DE ARAGÓN Serie cronológica 1984 1995 Versión 2/02/2016 0 m 1 m 3 m 5 m 7 m 15 m 18 m 6 años 11 a 14 a DT T T * * * 1984: se incluye la vacuna de Polio atenuada trivalente
HEPATITIS B INTRODUCCIÓN
 HEPATITIS B 9 INTRODUCCIÓN El virus de la hepatitis B es un virus tipo ADN de la clase hepadnaviridae que se reproduce en el hígado y causa trastornos a este nivel. Se trata de una enfermedad infecciosa
HEPATITIS B 9 INTRODUCCIÓN El virus de la hepatitis B es un virus tipo ADN de la clase hepadnaviridae que se reproduce en el hígado y causa trastornos a este nivel. Se trata de una enfermedad infecciosa
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. DIFTAVAX jeringa precargada Vacuna Antidiftero-tetánica adsorbida para adultos y adolescentes.
 agencia española de medicamentos y productos sanitarios FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO DIFTAVAX jeringa precargada Vacuna Antidiftero-tetánica adsorbida para adultos y adolescentes. 2. COMPOSICION
agencia española de medicamentos y productos sanitarios FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO DIFTAVAX jeringa precargada Vacuna Antidiftero-tetánica adsorbida para adultos y adolescentes. 2. COMPOSICION
Las vacunas contra Rotavirus y Neumococo en el nuevo esquema de vacunación. IX ANIVERSARIO CENTRO ESTATAL DE CAPACITACION
 Las vacunas contra Rotavirus y Neumococo en el nuevo esquema de vacunación. IX ANIVERSARIO CENTRO ESTATAL DE CAPACITACION 23 AGOSTO 2007 Un grupo de estudiantes de Geografía, estudiaban las nueva Siete
Las vacunas contra Rotavirus y Neumococo en el nuevo esquema de vacunación. IX ANIVERSARIO CENTRO ESTATAL DE CAPACITACION 23 AGOSTO 2007 Un grupo de estudiantes de Geografía, estudiaban las nueva Siete
Esquema nacional de vacunación 2015
 Esquema nacional de vacunación 2015 Definiciones en el PAI Susceptible Cualquier persona o animal que supuestamente no posee suficiente resistencia contra un agente patógeno determinado, que le proteja
Esquema nacional de vacunación 2015 Definiciones en el PAI Susceptible Cualquier persona o animal que supuestamente no posee suficiente resistencia contra un agente patógeno determinado, que le proteja
Campaña de Vacunación frente a Hepatitis A en inmigrantes de segunda generación de origen marroquí
 Campaña de Vacunación frente a Hepatitis A en inmigrantes de segunda generación de origen marroquí SERVICIO DE PREVENCION Y PROTECCION DE LA SALUD DIRECCION GENERAL DE SALUD PÚBLICA Y DROGODEPENDENCIAS
Campaña de Vacunación frente a Hepatitis A en inmigrantes de segunda generación de origen marroquí SERVICIO DE PREVENCION Y PROTECCION DE LA SALUD DIRECCION GENERAL DE SALUD PÚBLICA Y DROGODEPENDENCIAS
Child-Care Facilities
 2010-2011 Texas Minimum State Vaccine Requirements for Child-Care Facilities AUTHIZATION This chart summarizes the vaccine requirements incorporated in Title 25 Health Services, 97.61-97.72 of the Texas
2010-2011 Texas Minimum State Vaccine Requirements for Child-Care Facilities AUTHIZATION This chart summarizes the vaccine requirements incorporated in Title 25 Health Services, 97.61-97.72 of the Texas
PROGRAMA AMPLIADO DE INMUNIZACIONES. Paraguay
 PROGRAMA AMPLIADO DE INMUNIZACIONES Paraguay Programa Ampliado de Inmunizaciones-PAI Es una acción conjunta de los países de la Región y del mundo para apoyar acciones tendientes a mejorar coberturas de
PROGRAMA AMPLIADO DE INMUNIZACIONES Paraguay Programa Ampliado de Inmunizaciones-PAI Es una acción conjunta de los países de la Región y del mundo para apoyar acciones tendientes a mejorar coberturas de
CALENDARIO DE VACUNACIÓN INFANTIL 2010. Vacuna conjugada frente al neumococo 13 valente
 CALENDARIO DE VACUNACIÓN INFANTIL 2010 Vacuna conjugada frente al neumococo 13 valente ÍNDICE 1. Calendario de vacunación infantil 2010 2. Transito de la vacuna de 7 serotipos a la vacuna de 13 serotipos
CALENDARIO DE VACUNACIÓN INFANTIL 2010 Vacuna conjugada frente al neumococo 13 valente ÍNDICE 1. Calendario de vacunación infantil 2010 2. Transito de la vacuna de 7 serotipos a la vacuna de 13 serotipos
EVALUACIÓN POSJORNADAS. Prueba tipo test, con una respuesta
 EVALUACIÓN POSJORNADAS. Prueba tipo test, con una respuesta verdadera entre las 4 expuestas. 1. Son las vacunas incluidas en los calendarios de vacunaciones autonómicos obligatorias para el niño? a) Son
EVALUACIÓN POSJORNADAS. Prueba tipo test, con una respuesta verdadera entre las 4 expuestas. 1. Son las vacunas incluidas en los calendarios de vacunaciones autonómicos obligatorias para el niño? a) Son
Vacunación Infantil. www.madrid.org
 Vacunación Infantil www.madrid.org INTRODUCCIÓN a vacunación constituye una de las medidas más eficaces de la moderna salud pública para la prevención de importantes enfermedades que afectan a todos los
Vacunación Infantil www.madrid.org INTRODUCCIÓN a vacunación constituye una de las medidas más eficaces de la moderna salud pública para la prevención de importantes enfermedades que afectan a todos los
Requisitos de vacunas
 Requisitos de vacunas 2013-2014 La ley estatal y el reglamento de NEISD requieren que se mantengan archivados los certificados de vacunas actualizados de todos los estudiantes. Los certificados deben estar
Requisitos de vacunas 2013-2014 La ley estatal y el reglamento de NEISD requieren que se mantengan archivados los certificados de vacunas actualizados de todos los estudiantes. Los certificados deben estar
Vacunación en embarazadas
 X Jornadas sobre Vacunas en Atención Primaria Vacunación en embarazadas Purificación n Robles Raya ABS Sant Just Desvern (Barcelona) Grupo de Trabajo Infecciosas camfic INTRODUCCIÓN El embarazo aún a n
X Jornadas sobre Vacunas en Atención Primaria Vacunación en embarazadas Purificación n Robles Raya ABS Sant Just Desvern (Barcelona) Grupo de Trabajo Infecciosas camfic INTRODUCCIÓN El embarazo aún a n
Las vacunas protegen. el futuro de los adolescentes. Las vacunas ayudan a mantener saludables a los adolescentes.
 Las vacunas protegen el futuro de los adolescentes Las vacunas ayudan a mantener saludables a los adolescentes. Las vacunas protegen el futuro de los adolescentes Hepatitis B La hepatitis B puede causar
Las vacunas protegen el futuro de los adolescentes Las vacunas ayudan a mantener saludables a los adolescentes. Las vacunas protegen el futuro de los adolescentes Hepatitis B La hepatitis B puede causar
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO. RISPOVAL IBR-MARKER VIVUM Liofilizado y disolvente para suspensión inyectable para bovino
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO RISPOVAL IBR-MARKER VIVUM Liofilizado y disolvente para suspensión inyectable para bovino 2. COMPOSICIÓN CUALITATIVA
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO RISPOVAL IBR-MARKER VIVUM Liofilizado y disolvente para suspensión inyectable para bovino 2. COMPOSICIÓN CUALITATIVA
PROTOCOLO DE VACUNACIÓN DE PACIENTES ADULTOS CON TRASPLANTE DE ÓRGANO SÓLIDO
 Los pacientes trasplantados presentan un mayor riesgo de padecer enfermedades infecciosas y mayor gravedad. La necesidad de vacunación de estos pacientes se justifica por la disminución de su capacidad
Los pacientes trasplantados presentan un mayor riesgo de padecer enfermedades infecciosas y mayor gravedad. La necesidad de vacunación de estos pacientes se justifica por la disminución de su capacidad
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO VECOXAN 2,5 mg/ml SUSPENSION ORAL TERNEROS Y CORDEROS Diclazurilo 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO VECOXAN 2,5 mg/ml SUSPENSION ORAL TERNEROS Y CORDEROS Diclazurilo 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada
Pruebas de Chequeo del Niño Sano y Récord de Vacunas
 Departamento de Salud de la iudad de Milwaukee Fuentes: Tom arrett, Mayor evan K. aker, ommissioner of Health www.milwaukee.gov/health Hagan JF, Shaw JS, Duncan PM, eds. 2008 irth Futures Guidelines for
Departamento de Salud de la iudad de Milwaukee Fuentes: Tom arrett, Mayor evan K. aker, ommissioner of Health www.milwaukee.gov/health Hagan JF, Shaw JS, Duncan PM, eds. 2008 irth Futures Guidelines for
VACUNAS Y DIÁLISIS. Lo que debe saber. www.kidney.org
 VACUNAS Y DIÁLISIS Lo que debe saber www.kidney.org Acerca de la información incluida en este folleto Sabía que la National Kidney Foundation (NKF) ofrece pautas y comentarios que ayudan a su proveedor
VACUNAS Y DIÁLISIS Lo que debe saber www.kidney.org Acerca de la información incluida en este folleto Sabía que la National Kidney Foundation (NKF) ofrece pautas y comentarios que ayudan a su proveedor
Rhode Island Department of Health Three Capitol Hill Providence, RI 02908-5094
 Rhode Island Department of Health Three Capitol Hill Providence, RI 02908-5094 www.health.ri.gov Date: December 30, 2009 To: Parents and guardians of school-aged children in Rhode Island From: Director
Rhode Island Department of Health Three Capitol Hill Providence, RI 02908-5094 www.health.ri.gov Date: December 30, 2009 To: Parents and guardians of school-aged children in Rhode Island From: Director
RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO. 25 μg
 agencia española de medicamentos y productos sanitarios RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO HibTITER solución inyectable Vacuna conjugada frente a Haemophilus influenzae tipo
agencia española de medicamentos y productos sanitarios RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO HibTITER solución inyectable Vacuna conjugada frente a Haemophilus influenzae tipo
Department of Health and Human Services Food and Drug Administration 5600 Fishers Lane (HFI-40) Rockville, MD 20857. January 2002 (FDA) 02-9019S
 Department of Health and Human Services Food and Drug Administration 5600 Fishers Lane (HFI-40) Rockville, MD 20857 January 2002 (FDA) 02-9019S La Administración de Drogas y Alimentos, (FDA) es una agencia
Department of Health and Human Services Food and Drug Administration 5600 Fishers Lane (HFI-40) Rockville, MD 20857 January 2002 (FDA) 02-9019S La Administración de Drogas y Alimentos, (FDA) es una agencia
Reflexiones de los cambios en el calendario vacunal
 Reflexiones de los cambios en el calendario vacunal Javier González de Dios Servicio de Pediatría. Hospital General Universitario de Alicante. Departamento de Pediatría. Universidad Miguel Hernández. Alicante.
Reflexiones de los cambios en el calendario vacunal Javier González de Dios Servicio de Pediatría. Hospital General Universitario de Alicante. Departamento de Pediatría. Universidad Miguel Hernández. Alicante.
VACUNACIÓN del personal sanitario
 VACUNACIÓN del personal sanitario 21 INTRODUCCIÓN El personal que trabaja en el ámbito sanitario constituye un grupo de riesgo de adquisición y de transmisión de determinadas enfermedades infecciosas,
VACUNACIÓN del personal sanitario 21 INTRODUCCIÓN El personal que trabaja en el ámbito sanitario constituye un grupo de riesgo de adquisición y de transmisión de determinadas enfermedades infecciosas,
Vacunación. Infantil
 Vacunación Infantil E N C A S T I L L A - L A M A N C H A Edición Dirección General de Salud Pública y Consumo Consejería de Sanidad Junta de Comunidades de Castilla-La Mancha Actualizado Febrero 2016
Vacunación Infantil E N C A S T I L L A - L A M A N C H A Edición Dirección General de Salud Pública y Consumo Consejería de Sanidad Junta de Comunidades de Castilla-La Mancha Actualizado Febrero 2016
El día a día en el vacunatorio
 Jornadas Nacionales del Centenario de la Sociedad Argentina de Pediatría Infectología Pediátrica El día a día en el vacunatorio Coordinadora: Dra. Andrea Uboldi Secretario: Dr. Pedro Quintana Vacunas en
Jornadas Nacionales del Centenario de la Sociedad Argentina de Pediatría Infectología Pediátrica El día a día en el vacunatorio Coordinadora: Dra. Andrea Uboldi Secretario: Dr. Pedro Quintana Vacunas en
CALENDARIO DE VACUNACIÓN INFANTIL 2015 Sistemático, acelerado y otras recomendaciones
 CALENDARIO DE VACUNACIÓN INFANTIL 2015 Sistemático, acelerado y otras recomendaciones Enero 2015 INTRODUCCIÓN La Ley General de Salud Pública aprobada en 2011 establece que el Consejo Interterritorial
CALENDARIO DE VACUNACIÓN INFANTIL 2015 Sistemático, acelerado y otras recomendaciones Enero 2015 INTRODUCCIÓN La Ley General de Salud Pública aprobada en 2011 establece que el Consejo Interterritorial
principios y recomendaciones generales
 VACUNAS 1 principios y recomendaciones generales INTRODUCCIÓN Y DEFINICIONES La protección frente a las enfermedades infecciosas se basa en el desarrollo de inmunidad frente a las mismas y aunque los términos
VACUNAS 1 principios y recomendaciones generales INTRODUCCIÓN Y DEFINICIONES La protección frente a las enfermedades infecciosas se basa en el desarrollo de inmunidad frente a las mismas y aunque los términos
Calendario de vacunación recomendado para adultos
 Calendario de vacunación recomendado para adultos Nota: además de estas recomendaciones, deben leerse también las notas a pie de página. Tabla 1. Calendario de vacunación recomendado para adultos, por
Calendario de vacunación recomendado para adultos Nota: además de estas recomendaciones, deben leerse también las notas a pie de página. Tabla 1. Calendario de vacunación recomendado para adultos, por
MENJUGATE KIT 10 microgramos polvo y disolvente para suspensión inyectable.
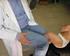 1. NOMBRE DEL MEDICAMENTO MENJUGATE KIT 10 microgramos polvo y disolvente para suspensión inyectable. Vacuna conjugada frente al meningococo del grupo C. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Una dosis
1. NOMBRE DEL MEDICAMENTO MENJUGATE KIT 10 microgramos polvo y disolvente para suspensión inyectable. Vacuna conjugada frente al meningococo del grupo C. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Una dosis
AUTOR. Dr. César Velasco Muñoz. Medicina Preventiva y Salud Pública
 Fiebre Amarilla AUTOR. Dr. César Velasco Muñoz. Medicina Preventiva y Salud Pública La fiebre amarilla es una infección aguda causada por un Arbovirus del género flavivirus, transmitida por la picadura
Fiebre Amarilla AUTOR. Dr. César Velasco Muñoz. Medicina Preventiva y Salud Pública La fiebre amarilla es una infección aguda causada por un Arbovirus del género flavivirus, transmitida por la picadura
Actualización de vacunas en el medio laboral
 Actualización de vacunas en el medio laboral Congreso de la Sociedad Española de Salud Laboral en la Administración Pública Reus, del 12 al 14 de mayo de 2004 Dra Anna Vilella Centro de Vacunación de Adultos.Servicio
Actualización de vacunas en el medio laboral Congreso de la Sociedad Española de Salud Laboral en la Administración Pública Reus, del 12 al 14 de mayo de 2004 Dra Anna Vilella Centro de Vacunación de Adultos.Servicio
Esquema de vacunación recomendado para la población de 0 a 18 años de edad
 Esquema de vacunación recomendado para la población de 0 a 18 años de edad Enero de 2014 Contenidos Página Introducción 2 Tabla 1. Esquema de vacunación recomendado para personas de 0 a 18 años de edad
Esquema de vacunación recomendado para la población de 0 a 18 años de edad Enero de 2014 Contenidos Página Introducción 2 Tabla 1. Esquema de vacunación recomendado para personas de 0 a 18 años de edad
Nuevas estrategias de control de la tos ferina: embarazadas, estrategia del nido, adolescentes, sanitarios.
 Nuevas estrategias de control de la tos ferina: embarazadas, estrategia del nido, adolescentes, sanitarios. Jornadas de Vacunas AEP 2013 Valencia 14-15 febrero 2013 Dr. Javier Arístegui Hospital Universitario
Nuevas estrategias de control de la tos ferina: embarazadas, estrategia del nido, adolescentes, sanitarios. Jornadas de Vacunas AEP 2013 Valencia 14-15 febrero 2013 Dr. Javier Arístegui Hospital Universitario
2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA INGREDIENTES ACTIVOS Cada dosis de 0,5 ml de vacuna reconstituida contiene:
 1. NOMBRE DEL MEDICAMENTO PENTAVAC Vacuna de difteria, tétanos, tosferina acelular y poliomielitis inactivada, adsorbida y Vacuna de Haemophilus influenzae tipo b conjugada. 2. COMPOSICIÓN CUALITATIVA
1. NOMBRE DEL MEDICAMENTO PENTAVAC Vacuna de difteria, tétanos, tosferina acelular y poliomielitis inactivada, adsorbida y Vacuna de Haemophilus influenzae tipo b conjugada. 2. COMPOSICIÓN CUALITATIVA
Vacunas en la etapa preconcepcional, durante
 Vazquez 18-23 5/31/11 00:51 PM Página 18 Revisión Vacunas en la etapa preconcepcional, durante el embarazo y en el postparto Reproducción 2011;26:18-23 Introducción Las vacunas administradas en la etapa
Vazquez 18-23 5/31/11 00:51 PM Página 18 Revisión Vacunas en la etapa preconcepcional, durante el embarazo y en el postparto Reproducción 2011;26:18-23 Introducción Las vacunas administradas en la etapa
FICHA TÉCNICA. no menos de 20 Unidades Internaciones (UI) (5 Lf) 1adsorbidos en hidróxido de aluminio hidratado (Al(OH)3)
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Boostrix suspensión inyectable en jeringa precargada Vacuna antidiftérica, antitetánica y antitos ferina (componente acelular) (adsorbida, contenido antigénico reducido)
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Boostrix suspensión inyectable en jeringa precargada Vacuna antidiftérica, antitetánica y antitos ferina (componente acelular) (adsorbida, contenido antigénico reducido)
Inmunizaciones. Vacunas Infantiles. Objetivo: Disminuir la morbilidad y mortalidad de la enfermedades transmisible. Objetivo:
 Inmunizaciones Vacunas Infantiles Objetivo: Objetivo: Disminuir la morbilidad y mortalidad de la enfermedades transmisible. Definición: n: Administración n de microorganismos o sus toxinas previamente
Inmunizaciones Vacunas Infantiles Objetivo: Objetivo: Disminuir la morbilidad y mortalidad de la enfermedades transmisible. Definición: n: Administración n de microorganismos o sus toxinas previamente
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 ACICLOVIR 5% Crema CREMA ANTIVIRAL Página 1 ACICLOVIR 5% Crema Crema Principio Activo Aciclovir Excipientes necesarios
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 ACICLOVIR 5% Crema CREMA ANTIVIRAL Página 1 ACICLOVIR 5% Crema Crema Principio Activo Aciclovir Excipientes necesarios
POR QUÉ SE VACUNA CUANDO SON TAN PEQUEÑOS Y TANTAS VECES?
 2.5.- LAS VACUNAS La vacunación consiste en la administración de un germen (bacteria o virus), o parte de él, modificados para que no produzcan enfermedad, con objeto de producir defensas contra las enfermedades
2.5.- LAS VACUNAS La vacunación consiste en la administración de un germen (bacteria o virus), o parte de él, modificados para que no produzcan enfermedad, con objeto de producir defensas contra las enfermedades
FICHA TÉCNICA. La vacuna MSD Antirrubéola cumple los requisitos de la OMS para productos biológicos y vacunas Antirrubéola.
 1. NOMBRE DEL MEDICAMENTO VACUNA MSD ANTIRRUBEOLA FICHA TÉCNICA 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Vacuna MSD Antirrubéola (vacuna con virus de la rubéola vivos) es una vacuna de virus vivos para
1. NOMBRE DEL MEDICAMENTO VACUNA MSD ANTIRRUBEOLA FICHA TÉCNICA 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Vacuna MSD Antirrubéola (vacuna con virus de la rubéola vivos) es una vacuna de virus vivos para
Vacuna conjugada frente al neumococo. Javier Díez Domingo, III Jornadas sobre Vacunas en Atención primaria
 Vacuna conjugada frente al neumococo Javier Díez Domingo, III Jornadas sobre Vacunas en Atención primaria Edad Tasa de incidencia por 100.000 niños y año < 2 años < 5 años < 15 años 16,8 10,5 4,6 Díez
Vacuna conjugada frente al neumococo Javier Díez Domingo, III Jornadas sobre Vacunas en Atención primaria Edad Tasa de incidencia por 100.000 niños y año < 2 años < 5 años < 15 años 16,8 10,5 4,6 Díez
CALENDARIOS ACELERADOS PAUTAS CORRECTORAS. Dr. Cristóbal Coronel Rodríguez C.S. AMANTE LAFFON. Sevilla
 CALENDARIOS ACELERADOS PAUTAS CORRECTORAS Dr. Cristóbal Coronel Rodríguez C.S. AMANTE LAFFON. Sevilla AGRADECIMIENTOS Y CONFLICTO DE INTERESES A MIS AMIGOS Y COMPAÑEROS: LOS DRS MARTINEZ-MONTERO Y RIPOLL
CALENDARIOS ACELERADOS PAUTAS CORRECTORAS Dr. Cristóbal Coronel Rodríguez C.S. AMANTE LAFFON. Sevilla AGRADECIMIENTOS Y CONFLICTO DE INTERESES A MIS AMIGOS Y COMPAÑEROS: LOS DRS MARTINEZ-MONTERO Y RIPOLL
Alivio de los sofocos que aparecen durante la menopausia como consecuencia de la deprivación estrogénica.
 1. NOMBRE DEL MEDICAMENTO Normosoy 40 mg cápsulas duras 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada cápsula contiene: 290 mg de extracto etanólico 85% V/V seco de semillas de Glycine max (L.) Merr.
1. NOMBRE DEL MEDICAMENTO Normosoy 40 mg cápsulas duras 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada cápsula contiene: 290 mg de extracto etanólico 85% V/V seco de semillas de Glycine max (L.) Merr.
ESTÁN SUFICIENTEMENTE PROTEGIDOS LOS ADOLESCENTES? EL PAPEL DE LAS VACUNAS
 1 ESTÁN SUFICIENTEMENTE PROTEGIDOS LOS ADOLESCENTES? EL PAPEL DE LAS VACUNAS IX Curso para padres de adolescentes. Alicante 14 de noviembre 2015 Autor: Javier González de Dios Servicio de Pediatría. Hospital
1 ESTÁN SUFICIENTEMENTE PROTEGIDOS LOS ADOLESCENTES? EL PAPEL DE LAS VACUNAS IX Curso para padres de adolescentes. Alicante 14 de noviembre 2015 Autor: Javier González de Dios Servicio de Pediatría. Hospital
Vacuna frente a la difteria, tétanos y tos ferina. (Comentarios a las fichas técnicas)
 Vacuna frente a la difteria, tétanos y tos ferina (Comentarios a las fichas técnicas) Prof. Ángel Gil de Miguel, Catedrático de Medicina Preventiva y Salud Pública, Universidad Rey Juan Carlos, Comunidad
Vacuna frente a la difteria, tétanos y tos ferina (Comentarios a las fichas técnicas) Prof. Ángel Gil de Miguel, Catedrático de Medicina Preventiva y Salud Pública, Universidad Rey Juan Carlos, Comunidad
CALENDARIO DE VACUNACIÓN INFANTIL 2015 Sistemático, acelerado y otras recomendaciones
 CALENDARIO DE VACUNACIÓN INFANTIL 2015 Sistemático, acelerado y otras recomendaciones (Actualización 17/03/2015) Calle San Martín de Porres, 6, planta baja. 28035 Madrid. Teléfono 913700920 0 INTRODUCCIÓN
CALENDARIO DE VACUNACIÓN INFANTIL 2015 Sistemático, acelerado y otras recomendaciones (Actualización 17/03/2015) Calle San Martín de Porres, 6, planta baja. 28035 Madrid. Teléfono 913700920 0 INTRODUCCIÓN
La varicela PETROLEROS ASOCIADOS S.A. RIESGOS DE SALUD PUBLICA
 La varicela PETROLEROS ASOCIADOS S.A. RIESGOS DE SALUD PUBLICA VARICELA Definición: La varicela es una enfermedad infecciosa causada por un virus llamado Varicela zoster (VVZ). Cuando se produce la reactivación
La varicela PETROLEROS ASOCIADOS S.A. RIESGOS DE SALUD PUBLICA VARICELA Definición: La varicela es una enfermedad infecciosa causada por un virus llamado Varicela zoster (VVZ). Cuando se produce la reactivación
