DOCUMENTO LOCAL DEL PRODUCTO
|
|
|
- César Cabrera Ramos
- hace 9 años
- Vistas:
Transcripción
1 1 DOCUMENTO LOCAL DEL PRODUCTO Título de documento del producto: Lincomicina Fecha de reemplazo de CDS: 14 de noviembre de 2013 Fecha de vigencia : 28 de octubre de NOMBRE(S) DEL MEDICAMENTO LINCOCIN 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA LINCOCIN 600 mg/2 ml solución inyectable: Cada ampolla de 2 ml contiene lincomicina base 600 mg. 3. FORMAS FARMACÉUTICAS Solución inyectable. 4. DETALLES CLÍNICOS 4.1 Indicaciones Terapéuticas Infecciones causadas por gérmenes sensibles a la lincomicina. La lincomicina ha demostrado ser eficaz en el tratamiento de las siguientes infecciones causadas por cepas susceptibles de aerobios grampositivos tales como estreptococos, neumococos, y estafilococos, o por bacterias anaerobias susceptibles. Infecciones del tracto respiratorio superior incluyendo amigdalitis, faringitis, otitis media, sinusitis, fiebre escarlatina y como coadyuvante en el tratamiento de la difteria. Podría ser eficaz en el tratamiento de la mastoiditis. Infecciones del tracto respiratorio inferior, entre ellas, bronquitis aguda y crónica y neumonía. Infecciones de la piel y de los tejidos blandos, entre ellas, celulitis, forúnculos, abscesos, impétigo, acné e infecciones de heridas. Condiciones tales como erisipelas, linfoadenitis, paroniquias (panaritium), mastitis y gangrena cutánea
2 2 deberán responder de manera adecuada, si son causadas por microorganismos susceptibles al tratamiento con lincomicina, Infecciones de huesos y articulaciones, como por ejemplo, osteomielitis y artritis séptica. Septicemia y endocarditis. Casos seleccionados de septicemia o endocarditis causados por microorganismos susceptibles han respondido bien a la lincomicina. Sin embargo, en estas infecciones se prefiere con frecuencia el uso de medicamentos bactericidas. Disentería bacilar. Aunque la Shigella es resistente a la lincomicina in vitro (CMI de aproximadamente 200 a 400 mcg/ml), la lincomicina ha sido efectiva en su tratamiento debido a los niveles bien altos de lincomicina obtenidos en el intestino (aproximadamente 3000 a 7000 mcg/gramos de materia fecal). 4.2 Posología y Forma de Administración Posología en Adultos Inyección intramuscular 1) 600 mg IM cada 24 horas. 2) En infecciones más severas: 600 mg IM cada 12 horas (o con una frecuencia mayor) dependiendo de la gravedad de la infección. Infusión intravenosa Las dosis intravenosas se suministran tomando como base 1 gramo de lincomicina diluido en no menos de 100 ml de una solución apropiada y se infunden en el transcurso de un período no inferior a 1 hora. NOTA: Han ocurrido reacciones cardiopulmonares severas luego de la administración del medicamento a una concentración y velocidad superiores a las recomendadas. 1) 600 mg a 1 gramo cada 8 a 12 horas. 2) En infecciones más severas, es posible que estas dosis deban incrementarse. 3) En situaciones con compromiso de la vida del paciente, se han suministrado dosis diarias intravenosas de hasta 8 gramos. Dilución y velocidades de infusión Dosis Volumen del diluyente Tiempo
3 3 600 mg 100 ml 1 h 1 gramo 100 ml 1 h 2 gramos 200 ml 2 h 3 gramos 300 ml 3 h 4 gramos 400 ml 4 h Estas dosis pueden repetirse con la frecuencia que sea requerida y dentro del límite de la dosis diaria máxima recomendada de 8 gramos de lincomicina. Posología en niños (mayores de 1 mes de edad) Inyección intramuscular 1) 10 mg/kg/día en una inyección intramuscular. 2) Infecciones más graves: 10 mg/kg cada 12 horas o con una frecuencia mayor. Infusión intravenosa 10 a 20 mg/kg/día, dependiendo de la severidad de la infección, pueden infundirse en dosis divididas como se describe en la sección Dilución y velocidades de infusión. Posología en pacientes con función renal o hepática deficiente En pacientes con deterioro de la función hepática o deterioro de la función renal, la vida media en suero de la lincomicina sufre un incremento. Deberá considerarse la disminución de la frecuencia de administración de lincomicina en pacientes con deterioro de la función renal o de la función hepática. En caso de que se requiera el tratamiento con lincomicina en individuos con deterioro grave de la función renal, una dosis apropiada es del 25% al 30% de la dosis recomendada para pacientes con función renal normal. Infecciones causadas por estreptococos beta-hemolíticos En este tipo de infecciones, el tratamiento deberá continuarse durante por lo menos 10 días. Incompatibilidades (La siguiente lista puede no ser exhaustiva debido a los múltiples factores que influencian los datos de la compatibilidad entre los medicamentos). La combinación en una solución para infusión de lincomicina con novobiocina, o con kanamicina, o con fenitoína, da lugar en cada caso a una incompatibilidad física con lincomicina.
4 4 4.3 Contraindicaciones El uso de lincomicina está contraindicado en pacientes con previo conocimiento de su sensibilidad a la lincomicina, a la clindamicina, o a cualquier otro componente del producto. Pacientes con estados diarreicos. 4.4 Advertencias y Precauciones Especiales para el Uso Adminístrese con precaución en pacientes con deterioro de la función hepática, agranulocitosis, trombocitopenia y leucopenia La formulación en inyección de la lincomicina contiene alcohol bencílico. El conservante alcohol bencílico se ha asociado con eventos adversos graves, incluido el síndrome de gasping (ahogamiento) y la muerte en pacientes pediátricos. Aunque las dosis terapéuticas normales de este producto comúnmente contienen cantidades de alcohol bencílico que son sustancialmente menores a las informadas en asociación con el síndrome de gasping, se desconoce la cantidad mínima de alcohol bencílico a la cual se produce la toxicidad. El riesgo de toxicidad del alcohol bencílico depende de la cantidad administrada y de la capacidad hepática para detoxificar el químico. Los infantes prematuros y de bajo peso pueden tener mayores probabilidades de verse afectados por la toxicidad. Se ha informado colitis pseudomembranosa con casi la totalidad de los agentes antibacterianos, incluyendo la lincomicina, la cual puede variar en gravedad desde casos leves hasta casos en donde existe compromiso de la vida del paciente. Por lo tanto, es importante considerar su diagnóstico en pacientes que presenten diarrea posterior a la administración de agentes antibacterianos. El tratamiento con agentes antibacterianos altera la flora normal del colon y puede permitir el crecimiento exacerbado de microorganismos del género clostridia. Estudios indican que una toxina producida por Clostridium difficile es la causa principal de la colitis asociada a antibióticos. Una vez que se haya establecido el diagnóstico primario de la colitis pseudomembranosa, deberán iniciarse las medidas terapéuticas correspondientes. Los casos leves de colitis pseudomembranosa usualmente responden a la sola suspensión del medicamento. En casos moderados a graves, deberá considerarse el manejo con fluidos y electrolitos, suplementos de proteínas, y el tratamiento con un antibacteriano clínicamente eficaz contra la colitis por Clostridium difficile. Si bien existe evidencia de que la lincomicina se diluye en el líquido cefalorraquídeo (LCR), los niveles de lincomicina alcanzados en el LCR pueden resultar inadecuados para el tratamiento de la meningitis. Por consiguiente, el
5 5 medicamento no deberá usarse en el tratamiento de la meningitis. En caso de que se requiera un tratamiento prolongado con lincomicina, deberán ejecutarse pruebas tanto de la función hepática como de la función renal. El uso de antibióticos puede dar como resultado el crecimiento exacerbado de microorganismos no susceptibles, particularmente de levaduras. Se ha informado clostridium difficile asociado a diarrea (CDAD) con el uso de casi todos los agentes antibacterianos, incluida la lincomicina, y fue catalogada en gravedad como una diarrea leve hasta una colitis fatal. El tratamiento con agentes antibacterianos altera la flora normal del colon y conlleva al crecimiento exacerbado del C. difficile. C. difficile produce las toxinas A y B, las cuales contribuyen al desarrollo de CDAD. La hipertoxicidad creada por el C. difficile causa un aumento en la morbilidad y la mortalidad, ya que estas infecciones pueden ser refractarias al tratamiento antimicrobiano y pueden requerir colectomía. Se debe tener en cuenta el diagnóstico de CDAD en todos los pacientes que presenten diarrea posterior a uso antibiótico. Es necesario realizar una minuciosa historia clínica desde el informe de inicio de la CDAD hasta dos meses después de la administración de los agentes antibacterianos. La lincomicina no deberá inyectarse por vía IV a manera de bolo. En cambio, deberá infundirse en la forma descrita en la sección Posología y forma de administración. 4.5 Interacciones con Otros Medicamentos y Otras Formas de Interacción Se ha demostrado el antagonismo entre la lincomicina y la eritromicina in vitro. Debido a la posible importancia clínica de este fenómeno, estos dos medicamentos no deberán administrarse concurrentemente. Se ha revelado que la lincomicina posee propiedades bloqueadoras neuromusculares que pueden intensificar la acción de otros bloqueadores neuromusculares. Por lo tanto, la lincomicina deberá usarse con cautela en pacientes que reciban tales agentes. 4.6 Fertilidad, Embarazo y Lactancia El alcohol bencílico puede atravesar la placenta. Consulte la sección
6 6 Advertencias y precauciones especiales para el uso. En estudios realizados en ratas usando dosis orales de lincomicina hasta de 1000 mg/kg (7,5 veces la dosis máxima humana de 8 g/día), no se observaron efectos adversos sobre la sobrevivencia de la prole desde el nacimiento hasta el destete. En un estudio realizado en ratas, no se detectaron efectos teratogénicos luego de su tratamiento con dosis que eran 55 veces superiores a la dosis más alta recomendada de 8 g/día para humanos adultos. En humanos, la lincomicina atraviesa la placenta y alcanza niveles séricos en el cordón umbilical que son aprox. el 25% de los niveles séricos maternos. No ocurreacumulación significativa en el fluido amniótico. No se han efectuadoestudios controlados en mujeres embarazadas; sin embargo, luego de un seguimiento de hasta siete años después del nacimiento, la progenie de 302 pacientes tratadas con lincomicina en diversas etapas del embarazo no reveló incremento en anomalías congénitas, ni retardo en el desarrollo, en comparación con el grupo de control. La lincomicina debe administrarse durante el embarazo únicamente si es necesaria. la lincomicina s excreta en la leche materna humana en concentraciones de 0,5 2,4 mcg/ml. 4.7 Reacciones Adversas Tabla de Reacciones Adversas Sistema de clasificación de órganos Infecciones e infestaciones de la sangre y del sistema linfático del sistema inmunológico cardíacos vasculares Frecuentes ( 1/10) Frecue ntes ( 1/100 a <1/10) Pocos frecuent es ( 1/1000 to <1/100) Infección vaginal Raras ( 1/10,000 a <1/1000) raras (<1/10, 000) Frecuencia no conocida (No puede estimarse a partir de los datos disponibles) Colitis Pseudomembranosa, Colitis por Clostridium difficile Pancitopenia, agranulocitosis, anemia aplásica, neutropenia, leucopenia, púrpura trombocitopénica Reacción anafiláctica, angioedema, enfermedad del suero Arresto cardiorespiratorio a Hypotensión, b tromboflebitis Después de la administración
7 7 Tabla de Reacciones Adversas Sistema de clasificación de órganos gastrointestinales hepatobiliares de la piel y del tejido subcutáneo general y condiciones del lugar de administración Frecuentes ( 1/10) Frecue ntes ( 1/100 a <1/10) Diarrea, Náusea, Vómito Pocos frecuent es ( 1/1000 to <1/100) Rash, Urticaria Raras ( 1/10,000 a <1/1000) Prurito raras (<1/10, 000) Frecuencia no conocida (No puede estimarse a partir de los datos disponibles) parenteral, particularmente después de la administración demasiado rápida. c Esofagitis d, malestar abdominal Ictericia, pruebas de función anormal del hígado Síndrome de Stevens- Johnson, Dermatitis bullosa, Dermatitis exfoliativa, Eritema multiforme Lugar de inyección absceso estéril e, Induración en el lugar de inyección, Dolor en el lugar de inyección, irritación en el lugar de inyección a. En raras ocasiones, se han reportado después de la administración intravenosa demasiado rápida.. b. Después de la administración parenteral, particularmente después de la administración demasiado rápida. c. Evento se ha comunicado con la inyección intravenosa. d. Evento se ha comunicado con las preparaciones orales. e. Reportado con inyección intramuscular. 4.8 Sobredosis Tanto la hemodiálisis como la diálisis peritoneal no eliminan eficazmente la lincomicina de la sangre.
PROSPECTOS. LINCOMICINA NORMON 300 mg solución inyectable LINCOMICINA NORMON 300 mg solución inyectable
 PROSPECTOS LINCOMICINA NORMON 300 mg solución inyectable LINCOMICINA NORMON 300 mg solución inyectable LINCOMICINA NORMON 300 mg solución inyectable (LINCOMICINA) INYECTABLE VIA INTRAMUSCULAR E INTRAVENOSA
PROSPECTOS LINCOMICINA NORMON 300 mg solución inyectable LINCOMICINA NORMON 300 mg solución inyectable LINCOMICINA NORMON 300 mg solución inyectable (LINCOMICINA) INYECTABLE VIA INTRAMUSCULAR E INTRAVENOSA
Eni* Tabletas e Inyectable. Ciprofloxacino
 Tabletas e Inyectable Ciprofloxacino Descripción Es ciprofloxacino, la fluoroquinolona bactericida potente, con amplio espectro antibacteriano que incluye grampositivos y gramnegativos. Tiene alta eficacia
Tabletas e Inyectable Ciprofloxacino Descripción Es ciprofloxacino, la fluoroquinolona bactericida potente, con amplio espectro antibacteriano que incluye grampositivos y gramnegativos. Tiene alta eficacia
LABORATORIOS NORMON, S.A. AMBROXOL NORMON 15 mg/5 ml Jarabe EFG
 1. NOMBRE DEL MEDICAMENTO 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada 5 ml de jarabe contienen: AMBROXOL (D.C.I.) hidrocloruro 15 mg Excipientes, ver apartado 6.1. 3. FORMA FARMACEUTICA Jarabe. 4. DATOS
1. NOMBRE DEL MEDICAMENTO 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada 5 ml de jarabe contienen: AMBROXOL (D.C.I.) hidrocloruro 15 mg Excipientes, ver apartado 6.1. 3. FORMA FARMACEUTICA Jarabe. 4. DATOS
PROSPECTO. CEFTRIAXONA REIG JOFRÉ 1 g IM. Polvo y disolvente para solución inyectable. E.F.G. Ceftriaxona (D.C.I.)
 PROSPECTO Lea todo el prospecto detenidamente antes de empezar a usar el medicamento. - Conserve este prospecto. Puede tener que volver a leerlo. - Si tiene alguna duda, consulte a su médico o farmacéutico.
PROSPECTO Lea todo el prospecto detenidamente antes de empezar a usar el medicamento. - Conserve este prospecto. Puede tener que volver a leerlo. - Si tiene alguna duda, consulte a su médico o farmacéutico.
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Mupirocina ISDIN 20 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene 20 mg de mupirocina. Para consultar
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Mupirocina ISDIN 20 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene 20 mg de mupirocina. Para consultar
DELOS OTIC CIPROFLOXACINA CLORHIDRATO - HIDROCORTISONA. Gotas Óticas. Hidrocortisona 1,00 g. Ciprofloxacina Clorhidrato 0,20 g.
 DELOS OTIC CIPROFLOXACINA CLORHIDRATO - HIDROCORTISONA Gotas Óticas Industria Argentina Venta bajo receta FORMULA Cada 100 ml contienen: Hidrocortisona 1,00 g. Ciprofloxacina Clorhidrato 0,20 g. Excipientes:
DELOS OTIC CIPROFLOXACINA CLORHIDRATO - HIDROCORTISONA Gotas Óticas Industria Argentina Venta bajo receta FORMULA Cada 100 ml contienen: Hidrocortisona 1,00 g. Ciprofloxacina Clorhidrato 0,20 g. Excipientes:
Cefalosporinas Indicaciones y Contraindicaciones
 Cefalosporinas Indicaciones y Contraindicaciones Dra. Ma. Consuelo Rojas Cefalosporinas Sustancias químicas producidas por una especie de hongo cephalosporium acremonium. Son betalactámicos Químicamente
Cefalosporinas Indicaciones y Contraindicaciones Dra. Ma. Consuelo Rojas Cefalosporinas Sustancias químicas producidas por una especie de hongo cephalosporium acremonium. Son betalactámicos Químicamente
DOCUMENTO DE PRODUCTO LOCAL PFIZER VENEZUELA, S.A. Preparado por Pfizer Inc. Fecha efectiva de CDS: 28 DIC Fecha CDS que reemplaza: 25 JUN 2014
 MALEATO DE TRIMEBUTINA 28 DIC 2015 DOCUMENTO DE PRODUCTO LOCAL PFIZER VENEZUELA, S.A. Preparado por Pfizer Inc. Fecha efectiva de CDS: 28 DIC 2015 Fecha CDS que reemplaza: 25 JUN 2014 MALEATO DE TRIMEBUTINA
MALEATO DE TRIMEBUTINA 28 DIC 2015 DOCUMENTO DE PRODUCTO LOCAL PFIZER VENEZUELA, S.A. Preparado por Pfizer Inc. Fecha efectiva de CDS: 28 DIC 2015 Fecha CDS que reemplaza: 25 JUN 2014 MALEATO DE TRIMEBUTINA
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 COTRIMOXAZOL 200/40/5 ml SUSPENSIÓN ANTIINFECCIOSO-ANTIBACTERIANO Página 1 COTRIMOXAZOL 200/40/5 ml Suspensión Principio
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 COTRIMOXAZOL 200/40/5 ml SUSPENSIÓN ANTIINFECCIOSO-ANTIBACTERIANO Página 1 COTRIMOXAZOL 200/40/5 ml Suspensión Principio
Nombre: Lincomicina Condición de venta: con receta médica Clasificación: antibiotico Disponible en: Nombres de marca:
 Nombre: Lincomicina Condición de venta: con receta médica Clasificación: antibiotico Disponible en: Nombres de marca: Lea cuidadosamente este folleto antes de la administración de este medicamento. Contiene
Nombre: Lincomicina Condición de venta: con receta médica Clasificación: antibiotico Disponible en: Nombres de marca: Lea cuidadosamente este folleto antes de la administración de este medicamento. Contiene
ENOXPRIM. Solución inyectable. Solución inyectable estéril, libre de pirógenos, contenida en jeringas pre-llenadas listas para usarse.
 ENOXPRIM Solución inyectable ENOXAPARINA FORMA FARMACÉUTICA Y FORMULACIÓN Cada jeringa contiene: Enoxaparina sódica 20 mg 40 mg Equivalente a 2,000 U.I. 4,000 U.I. Agua inyectable, c.b.p. 0.2 ml 0.4 ml
ENOXPRIM Solución inyectable ENOXAPARINA FORMA FARMACÉUTICA Y FORMULACIÓN Cada jeringa contiene: Enoxaparina sódica 20 mg 40 mg Equivalente a 2,000 U.I. 4,000 U.I. Agua inyectable, c.b.p. 0.2 ml 0.4 ml
INTOXICACIÓN POR SULFONAMIDAS
 INTOXII ICACIÓN POR SULFONAMIIDAS Las sulfas fueron las primeras drogas usadas efectivamente para combatir las infecciones. La morbimortalidad por infecciones disminuyó en forma considerable desde que
INTOXII ICACIÓN POR SULFONAMIIDAS Las sulfas fueron las primeras drogas usadas efectivamente para combatir las infecciones. La morbimortalidad por infecciones disminuyó en forma considerable desde que
Prospecto: información para el usuario. Cedax 400 mg cápsulas duras Ceftibuteno
 Prospecto: información para el usuario Cedax 400 mg cápsulas duras Ceftibuteno Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene información importante para
Prospecto: información para el usuario Cedax 400 mg cápsulas duras Ceftibuteno Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene información importante para
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 ACICLOVIR 5% Crema CREMA ANTIVIRAL Página 1 ACICLOVIR 5% Crema Crema Principio Activo Aciclovir Excipientes necesarios
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 ACICLOVIR 5% Crema CREMA ANTIVIRAL Página 1 ACICLOVIR 5% Crema Crema Principio Activo Aciclovir Excipientes necesarios
ADVIL Ibuprofeno Cápsulas ADVIL. Ibuprofeno
 INFORMACIÓN PARA PRESCRIBIR AMPLIA ADVIL Cápsulas 1. NOMBRE COMERCIAL 2. NOMBRE GENÉRICO ADVIL 3. FORMA FARMACÉUTICA Y FORMULACIÓN Cápsulas Fórmula: cada cápsula contiene: Excipiente c.b.p. 200 mg ó 400
INFORMACIÓN PARA PRESCRIBIR AMPLIA ADVIL Cápsulas 1. NOMBRE COMERCIAL 2. NOMBRE GENÉRICO ADVIL 3. FORMA FARMACÉUTICA Y FORMULACIÓN Cápsulas Fórmula: cada cápsula contiene: Excipiente c.b.p. 200 mg ó 400
CLINDAMICINA BIOL CLINDAMICINA 150 mg/ml. Inyectable
 CLINDAMICINA BIOL CLINDAMICINA 150 mg/ml. Inyectable Industria Argentina Venta bajo receta archivada FÓRMULA: Cada ml contiene: Clindamicina Fosfato(como base) 150 mg. Alcohol Bencílico 9,45 mg. Edetato
CLINDAMICINA BIOL CLINDAMICINA 150 mg/ml. Inyectable Industria Argentina Venta bajo receta archivada FÓRMULA: Cada ml contiene: Clindamicina Fosfato(como base) 150 mg. Alcohol Bencílico 9,45 mg. Edetato
INFORMACIÓN PARA PRESCRIBIR AMPLIA 1. NOMBRE COMERCIAL Y GENÉRICO ADVIL IBUPROFENO. 2. FORMA FARMACÉUTICA Y FORMULACION Tabletas
 INFORMACIÓN PARA PRESCRIBIR AMPLIA 1. NOMBRE COMERCIAL Y GENÉRICO ADVIL IBUPROFENO 2. FORMA FARMACÉUTICA Y FORMULACION Tabletas Fórmula: cada gragea contiene: Ibuprofeno Excipiente c.b.p. 200 mg 1 tableta
INFORMACIÓN PARA PRESCRIBIR AMPLIA 1. NOMBRE COMERCIAL Y GENÉRICO ADVIL IBUPROFENO 2. FORMA FARMACÉUTICA Y FORMULACION Tabletas Fórmula: cada gragea contiene: Ibuprofeno Excipiente c.b.p. 200 mg 1 tableta
- Como disolvente de medicamentos en polvo o liofilizados, previamente a su administración. - Como diluyente de soluciones y/o medicamentos.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Agua para preparaciones inyectables SERRACLINICS. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada 100 ml contienen agua para preparaciones inyectables. ph: 5,0-7,0
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Agua para preparaciones inyectables SERRACLINICS. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada 100 ml contienen agua para preparaciones inyectables. ph: 5,0-7,0
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 AZITROMICINA 500 mg COMPRIMIDOS RECUBIERTOS ANTIBACTERIANO Página 1 AZITROMICINA 500 mg Comprimidos Recubiertos
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 AZITROMICINA 500 mg COMPRIMIDOS RECUBIERTOS ANTIBACTERIANO Página 1 AZITROMICINA 500 mg Comprimidos Recubiertos
PROSPECTO PARA el liberador del lote Ecuphar NV: ACTIMARBO 80 MG COMPRIMIDOS SABOR PARA PERROS
 DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS PROSPECTO PARA el liberador del lote Ecuphar NV: ACTIMARBO 80 MG COMPRIMIDOS SABOR PARA PERROS 1. NOMBRE O RAZÓN SOCIAL Y DOMICILIO O SEDE SOCIAL DEL TITULAR DE
DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS PROSPECTO PARA el liberador del lote Ecuphar NV: ACTIMARBO 80 MG COMPRIMIDOS SABOR PARA PERROS 1. NOMBRE O RAZÓN SOCIAL Y DOMICILIO O SEDE SOCIAL DEL TITULAR DE
THIPENTHAL. TIOPENTAL SÓDICO 1 g INYECTABLE. VENTA BAJO RECETA ARCHIVADA (Lista III) FÓRMULA CUALI Y CUANTITATIVA. Cada frasco ampolla contiene:
 THIPENTHAL TIOPENTALSÓDICO1g INYECTABLE VENTABAJORECETAARCHIVADA(ListaIII) FÓRMULACUALIYCUANTITATIVA Cadafrascoampollacontiene: Tiopentalsódicoestéril 1g ACCIÓNTERAPÉUTICA: Anestésicogeneral,barbitúrico.CódigoATC:N01AF03.
THIPENTHAL TIOPENTALSÓDICO1g INYECTABLE VENTABAJORECETAARCHIVADA(ListaIII) FÓRMULACUALIYCUANTITATIVA Cadafrascoampollacontiene: Tiopentalsódicoestéril 1g ACCIÓNTERAPÉUTICA: Anestésicogeneral,barbitúrico.CódigoATC:N01AF03.
LLD Abreviado de Zoloft. Todo medicamento debe conservarse fuera del alcance de los niños.
 LLD Abreviado de Zoloft Versión: 19.0 Fecha: 20 de febrero de 2015 Aprobación ARCSA: 23 febrero de 2016 Todo medicamento debe conservarse fuera del alcance de los niños. 1. Presentación: Sertralina que
LLD Abreviado de Zoloft Versión: 19.0 Fecha: 20 de febrero de 2015 Aprobación ARCSA: 23 febrero de 2016 Todo medicamento debe conservarse fuera del alcance de los niños. 1. Presentación: Sertralina que
Antihiperkalémico - Antihipermagnesémico. Composición. Cada 10 ml de solución contiene: Gluconato de Calcio 1.0 g. Excipientes:
 Antihiperkalémico - Antihipermagnesémico. Composición Cada 10 ml de solución contiene: Gluconato de Calcio 1.0 g Excipientes: 1 / 21 Sacarato de calcio agua para inyectables c.s. Proporciona: Calcio 0.465
Antihiperkalémico - Antihipermagnesémico. Composición Cada 10 ml de solución contiene: Gluconato de Calcio 1.0 g Excipientes: 1 / 21 Sacarato de calcio agua para inyectables c.s. Proporciona: Calcio 0.465
Polvo para preparar Solución Inyectable. Cefazolina 1000 mg. Línea de Desarrollo: Antiinfecciosos Vía General
 Polvo para preparar Solución Inyectable Cefazolina 1000 mg Línea de Desarrollo: Antiinfecciosos Vía General FÓRMULA: Cefazolina (como Cefazolina sódica) 1000mg ZOLCEF 1000 mg Venta bajo receta profesional
Polvo para preparar Solución Inyectable Cefazolina 1000 mg Línea de Desarrollo: Antiinfecciosos Vía General FÓRMULA: Cefazolina (como Cefazolina sódica) 1000mg ZOLCEF 1000 mg Venta bajo receta profesional
TECNOLOGÍA EN SALUD DE INTERÉS Deferasirox
 TECNOLOGÍA EN SALUD DE INTERÉS Deferasirox 1. RESUMEN Título del reporte: Evaluación de efectividad y seguridad de deferasirox en Hemosiderosis Transfusional Información general de la tecnología: deferasirox
TECNOLOGÍA EN SALUD DE INTERÉS Deferasirox 1. RESUMEN Título del reporte: Evaluación de efectividad y seguridad de deferasirox en Hemosiderosis Transfusional Información general de la tecnología: deferasirox
Prospecto: información para el usuario. Cedax 36 mg/ml polvo para suspensión oral Ceftibuteno
 Prospecto: información para el usuario Cedax 36 mg/ml polvo para suspensión oral Ceftibuteno Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene información importante
Prospecto: información para el usuario Cedax 36 mg/ml polvo para suspensión oral Ceftibuteno Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene información importante
FOLLETO DE INFORMACIÓN AL PACIENTE
 FOLLETO DE INFORMACIÓN AL PACIENTE NIMESULIDA Lea cuidadosamente este folleto antes de la administración de este medicamento. Contiene información importante acerca de su tratamiento. Si tiene cualquier
FOLLETO DE INFORMACIÓN AL PACIENTE NIMESULIDA Lea cuidadosamente este folleto antes de la administración de este medicamento. Contiene información importante acerca de su tratamiento. Si tiene cualquier
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Lactulosa Level 667,5 mg/ml solución oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 mililitro de solución oral contiene
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Lactulosa Level 667,5 mg/ml solución oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 mililitro de solución oral contiene
Reacciones Adversas de los Fármacos
 Reacciones Adversas de los Fármacos -Talidomida se administró a embarazadas, con el fin de disminuir los efectos propios del embarazo(náuseas, vómitos). Primero se probó en animales y cuando se usó en
Reacciones Adversas de los Fármacos -Talidomida se administró a embarazadas, con el fin de disminuir los efectos propios del embarazo(náuseas, vómitos). Primero se probó en animales y cuando se usó en
Convenia 80 mg/ml polvo y disolvente para solución inyectable para perros y gatos.
 . DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Convenia 0 mg/ml polvo y disolvente para solución inyectable para perros y gatos.. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada vial de polvo liofilizado contiene:
. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Convenia 0 mg/ml polvo y disolvente para solución inyectable para perros y gatos.. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada vial de polvo liofilizado contiene:
AZITROMICINA 500 mg Tableta
 AZITROMICINA 500 mg Tableta AZITROMICINA 500 mg - Tabletas COMPOSICION: Azitromicina base (como Azitromicina dihidrato)...500 mg Excipientes c.s.p....1 tableta INDICACIONES Y USOS: AZITROMICINA 500 mg
AZITROMICINA 500 mg Tableta AZITROMICINA 500 mg - Tabletas COMPOSICION: Azitromicina base (como Azitromicina dihidrato)...500 mg Excipientes c.s.p....1 tableta INDICACIONES Y USOS: AZITROMICINA 500 mg
Pacientes de edad avanzada: debe considerarse la conveniencia de ampliar el intervalo de dosificación (Ver Propiedades Famacocinéticas).
 FT290191-B+2 1. NOMBRE DEL MEDICAMENTO DARVON 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Dextropropoxifeno (D.C.I.) napsilato 100 mg. 3. FORMA FARMACÉUTICA Cápsulas para administración por vía oral. 4.
FT290191-B+2 1. NOMBRE DEL MEDICAMENTO DARVON 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Dextropropoxifeno (D.C.I.) napsilato 100 mg. 3. FORMA FARMACÉUTICA Cápsulas para administración por vía oral. 4.
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO RIMADYL SOLUCIÓN INYECTABLE PARA BOVIN0 50 mg/ml 2. COMPOSICIÓN CUALITATIVA
DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO RIMADYL SOLUCIÓN INYECTABLE PARA BOVIN0 50 mg/ml 2. COMPOSICIÓN CUALITATIVA
PAROXETINA COMPRIMIDOS CON RECUBRIMIENTO ENTÉRICO 12,5mg-25mg
 PAROXETINA COMPRIMIDOS CON RECUBRIMIENTO ENTÉRICO 12,5mg-25mg Lea cuidadosamente este folleto antes de la administración de este medicamento, contiene información importante acerca de su tratamiento. Si
PAROXETINA COMPRIMIDOS CON RECUBRIMIENTO ENTÉRICO 12,5mg-25mg Lea cuidadosamente este folleto antes de la administración de este medicamento, contiene información importante acerca de su tratamiento. Si
TETRACICLINAS Y FENICOLES CLASIFICACION Y ESPECTRO
 CLASIFICACION Y ESPECTRO TETRACICLINAS: - DE ACCION CORTA: + CLORTETRACICLINA (AUREOMICINA): * FUE LA PRIMERA (1948). + OXITETRACICLINA. + TETRACICLINA. - DE ACCION LARGA: + MINOCICLINA. + DOXICICLINA.
CLASIFICACION Y ESPECTRO TETRACICLINAS: - DE ACCION CORTA: + CLORTETRACICLINA (AUREOMICINA): * FUE LA PRIMERA (1948). + OXITETRACICLINA. + TETRACICLINA. - DE ACCION LARGA: + MINOCICLINA. + DOXICICLINA.
MACROLIDOS CLASIFICACION Y ESPECTRO
 MACROLIDOS CLASIFICACION Y ESPECTRO CLASIFICACION: MACROCICLO LACTONICO DE 14 ATOMOS: + ERITROMICINA (PROTOTIPO). + CLARITROMICINA. + DIRITROMICINA. + TELITROMICINA (CETOLIDO) MACROCICLO LACTONICO DE 15
MACROLIDOS CLASIFICACION Y ESPECTRO CLASIFICACION: MACROCICLO LACTONICO DE 14 ATOMOS: + ERITROMICINA (PROTOTIPO). + CLARITROMICINA. + DIRITROMICINA. + TELITROMICINA (CETOLIDO) MACROCICLO LACTONICO DE 15
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO. VANGUARD R Suspensión inyectable para perros, gatos, bovino, porcino, ovino, caprino, equino y hurones
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO VANGUARD R Suspensión inyectable para perros, gatos, bovino, porcino, ovino, caprino, equino y hurones 2. COMPOSICIÓN
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO VANGUARD R Suspensión inyectable para perros, gatos, bovino, porcino, ovino, caprino, equino y hurones 2. COMPOSICIÓN
La varicela PETROLEROS ASOCIADOS S.A. RIESGOS DE SALUD PUBLICA
 La varicela PETROLEROS ASOCIADOS S.A. RIESGOS DE SALUD PUBLICA VARICELA Definición: La varicela es una enfermedad infecciosa causada por un virus llamado Varicela zoster (VVZ). Cuando se produce la reactivación
La varicela PETROLEROS ASOCIADOS S.A. RIESGOS DE SALUD PUBLICA VARICELA Definición: La varicela es una enfermedad infecciosa causada por un virus llamado Varicela zoster (VVZ). Cuando se produce la reactivación
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Fevaxyn Pentofel, suspensión inyectable para gatos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Fevaxyn Pentofel, suspensión inyectable para gatos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
Universidad Nacional de Rosario - Facultad de Ciencias Médicas Cátedra de Microbiología, Virología y Parasitología
 Universidad Nacional de Rosario - Facultad de Ciencias Médicas Cocos gram positivos. Streptococcus Área Injuria - 2015 Streptococcus Objetivos: Conocer las principales características biológicas, su capacidad
Universidad Nacional de Rosario - Facultad de Ciencias Médicas Cocos gram positivos. Streptococcus Área Injuria - 2015 Streptococcus Objetivos: Conocer las principales características biológicas, su capacidad
En mujeres con cistitis aguda no complicada se recomienda una dosis de 400 mg diarios, en forma única, durante 3 días. En caso de insuficiencia renal
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO - CEFIXIMA NORMON 200 mg Cápsulas EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA - Cada cápsula de CEFIXIMA NORMON 200 mg contiene: Cefixima (DOE) (en forma de trihidrato)...
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO - CEFIXIMA NORMON 200 mg Cápsulas EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA - Cada cápsula de CEFIXIMA NORMON 200 mg contiene: Cefixima (DOE) (en forma de trihidrato)...
Resumen de las Características del Producto. Excipientes: Para consultar la lista completa de excipientes, ver sección 6.1.
 1. NOMBRE DEL MEDICAMENTO ASPITOPIC 50 mg/g gel Resumen de las Características del Producto 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de gel contiene: Etofenamato (DOE) 50 mg Excipientes: Para
1. NOMBRE DEL MEDICAMENTO ASPITOPIC 50 mg/g gel Resumen de las Características del Producto 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de gel contiene: Etofenamato (DOE) 50 mg Excipientes: Para
Excipientes con efecto conocido: Cada gramo de crema contiene 200 mg de propilenglicol, 75 mg de alcohol estearílico y 20 mg de alcohol cetílico.
 1. NOMBRE DEL MEDICAMENTO Ketoisdin 20 mg/g crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de crema contiene 20 mg de ketoconazol. Excipientes con efecto conocido: Cada gramo de crema contiene
1. NOMBRE DEL MEDICAMENTO Ketoisdin 20 mg/g crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de crema contiene 20 mg de ketoconazol. Excipientes con efecto conocido: Cada gramo de crema contiene
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 COMPLEJO B COMPRIMIDOS RECUBIERTOS VITAMINA Página 1 COMPLEJO B Comprimidos Recubiertos Principio Activo Tiamina
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 COMPLEJO B COMPRIMIDOS RECUBIERTOS VITAMINA Página 1 COMPLEJO B Comprimidos Recubiertos Principio Activo Tiamina
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO DIFTAVAX suspensión inyectable en jeringa precargada Vacuna antidiftero-tetánica (adsorbida) para adultos y adolescentes. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO DIFTAVAX suspensión inyectable en jeringa precargada Vacuna antidiftero-tetánica (adsorbida) para adultos y adolescentes. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
Paracetamol DC 90 equivalente a mg de Paracetamol
 INFORMACION PARA PRESCRIBIR AMPLIA 1. Nombre comercial: TAFIROL 2. Nombre genérico PARACETAMOL 3. Forma farmacéutica y formulación: Cada tableta contiene: Paracetamol DC 90 equivalente a. 1000 mg de Paracetamol
INFORMACION PARA PRESCRIBIR AMPLIA 1. Nombre comercial: TAFIROL 2. Nombre genérico PARACETAMOL 3. Forma farmacéutica y formulación: Cada tableta contiene: Paracetamol DC 90 equivalente a. 1000 mg de Paracetamol
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Marbocyl P 5 mg 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Sustancia activa: Marbofloxacino Excipientes: Excipiente
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Marbocyl P 5 mg 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Sustancia activa: Marbofloxacino Excipientes: Excipiente
FICHA TÉCNICA. 1. NOMBRE DEL MEDICAMENTO AMOXICILINA UR 500 mg cápsulas EFG
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO AMOXICILINA UR 500 mg cápsulas EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA AMOXICILINA UR 500 mg cápsulas EFG Cada cápsula contiene: Amoxicilina (D.C.I.) trihidrato,
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO AMOXICILINA UR 500 mg cápsulas EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA AMOXICILINA UR 500 mg cápsulas EFG Cada cápsula contiene: Amoxicilina (D.C.I.) trihidrato,
FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO Hodernal 800 mg/ml solución oral Parafina líquida 1. NOMBRE DEL MEDICAMENTO Hodernal 800 mg/ml solución oral. 2. COMPOSICIÓN CUANTITATIVA Y CUALITATIVA
FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO Hodernal 800 mg/ml solución oral Parafina líquida 1. NOMBRE DEL MEDICAMENTO Hodernal 800 mg/ml solución oral. 2. COMPOSICIÓN CUANTITATIVA Y CUALITATIVA
La ceftriaxona es una moderna cefalosporina de amplio espectro y acción prolongada, para uso parenteral, que posee las siguientes propiedades:
 CETRIAF Vial Cefalosporina de 3ra. Generación Descripción La ceftriaxona es una moderna cefalosporina de amplio espectro y acción prolongada, para uso parenteral, que posee las siguientes propiedades:
CETRIAF Vial Cefalosporina de 3ra. Generación Descripción La ceftriaxona es una moderna cefalosporina de amplio espectro y acción prolongada, para uso parenteral, que posee las siguientes propiedades:
DOCUMENTO LOCAL DE PRODUCTO
 DOCUMENTO LOCAL DE PRODUCTO Título del documento de producto: Tinidazol Fecha de CDS que reemplaza: 17 de octubre de 2012 Fecha efectiva 11 de julio de 2013 CDS Versión 6.0 1. NOMBRE(S) DEL PRODUCTO MEDICINAL
DOCUMENTO LOCAL DE PRODUCTO Título del documento de producto: Tinidazol Fecha de CDS que reemplaza: 17 de octubre de 2012 Fecha efectiva 11 de julio de 2013 CDS Versión 6.0 1. NOMBRE(S) DEL PRODUCTO MEDICINAL
ORIFUNGAL Crema KETOCONAZOL
 ORIFUNGAL Crema KETOCONAZOL JANSSEN-CILAG Venta bajo receta Para uso externo exclusivamente Industria Brasileña FORMULA: Cada gramo de crema contiene: Ketoconazol 20 mg. Excipientes: Propilenglicol, Alcohol
ORIFUNGAL Crema KETOCONAZOL JANSSEN-CILAG Venta bajo receta Para uso externo exclusivamente Industria Brasileña FORMULA: Cada gramo de crema contiene: Ketoconazol 20 mg. Excipientes: Propilenglicol, Alcohol
METFORMINA CLORHIDRATO COMPRIMIDOS DE 500 mg y 850 mg
 METFORMINA CLORHIDRATO COMPRIMIDOS DE 500 mg y 850 mg Lea cuidadosamente este folleto antes de la administración de este medicamento. Contiene información importante acerca de su tratamiento. Si tiene
METFORMINA CLORHIDRATO COMPRIMIDOS DE 500 mg y 850 mg Lea cuidadosamente este folleto antes de la administración de este medicamento. Contiene información importante acerca de su tratamiento. Si tiene
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 ERITROMICINA 125 mg/5 ml POLVO PARA SUSPENSION ANTIHISTAMINICO Página 1 ERITROMICINA 125 mg/5 ml Polvo Para Suspensión
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 ERITROMICINA 125 mg/5 ml POLVO PARA SUSPENSION ANTIHISTAMINICO Página 1 ERITROMICINA 125 mg/5 ml Polvo Para Suspensión
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. 2. COMPOSICIÓN CUALITATIVA y CUANTITATIVA 3. FORMA FARMACÉUTICA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ketoconazol Abamed 2% crema 2. COMPOSICIÓN CUALITATIVA y CUANTITATIVA Composición por gramo: Ketoconazol (DOE)... 20 mg Para excipientes véase sección 6.1 3. FORMA
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ketoconazol Abamed 2% crema 2. COMPOSICIÓN CUALITATIVA y CUANTITATIVA Composición por gramo: Ketoconazol (DOE)... 20 mg Para excipientes véase sección 6.1 3. FORMA
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO. 2. Composición cualitativa y cuantitativa en principios activos y componentes del excipiente.
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. Denominación del medicamento. GENTAVALL 2. Composición cualitativa y cuantitativa en principios activos y componentes del excipiente. Gentamicina (sulfato
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. Denominación del medicamento. GENTAVALL 2. Composición cualitativa y cuantitativa en principios activos y componentes del excipiente. Gentamicina (sulfato
Es una sustancia antibiótica producida por los hongos Penicillium notatum y P. chrysogenum de la familia Aspergiliaceas.
 En 1940 se logró extraer la penicilina del hongo y recién en 1941 se la empleó con eficacia para tratar una infección por estafilococo y estreptococo. En el mismo año comenzó a producirse la penicilina
En 1940 se logró extraer la penicilina del hongo y recién en 1941 se la empleó con eficacia para tratar una infección por estafilococo y estreptococo. En el mismo año comenzó a producirse la penicilina
RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO SYNULOX POLVO PARA GOTAS ORALES EN SUSPENSIÓN 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada frasco contiene: Sustancias
RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO SYNULOX POLVO PARA GOTAS ORALES EN SUSPENSIÓN 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada frasco contiene: Sustancias
Además, la riboflavina puede administrarse a los infantes que presentan niveles altos de bilirrubina (hiperbilirrubinemia).
 Riboflavina (Vitamina B2) (Por vía oral) Índice de contenidos - DESCRIPCIÓN GENERAL - A TENER EN CUENTA - UTILIZACIÓN - ADVERTENCIAS - EFECTOS SECUNDARIOS - COMENTARIOS DESCRIPCIÓN GENERAL Las vitaminas
Riboflavina (Vitamina B2) (Por vía oral) Índice de contenidos - DESCRIPCIÓN GENERAL - A TENER EN CUENTA - UTILIZACIÓN - ADVERTENCIAS - EFECTOS SECUNDARIOS - COMENTARIOS DESCRIPCIÓN GENERAL Las vitaminas
METRONIDAZOL 500 mg Tabletas
 METRONIDAZOL 500 mg Tabletas METRONIDAZOL 500 mg TABLETAS *COMPOSICION: METRONIDAZOL 500 MG - TABLETAS: Metronidazol...500 mg Excipientes c.s.p...1 tab *INDICACIONES Y USOS: METRONIDAZOL está indicado
METRONIDAZOL 500 mg Tabletas METRONIDAZOL 500 mg TABLETAS *COMPOSICION: METRONIDAZOL 500 MG - TABLETAS: Metronidazol...500 mg Excipientes c.s.p...1 tab *INDICACIONES Y USOS: METRONIDAZOL está indicado
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Ácido Fusídico Isdin 20 mg/g crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo contiene 20 mg de ácido fusídico.
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Ácido Fusídico Isdin 20 mg/g crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo contiene 20 mg de ácido fusídico.
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 BROMHEXINA 4 mg/5 ml JARABE MUCOLÍTICO, EXPECTORANTE Página 1 BROMHEXINA 4 mg/5 ml Jarabe Principio Activo Bromhexina
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 BROMHEXINA 4 mg/5 ml JARABE MUCOLÍTICO, EXPECTORANTE Página 1 BROMHEXINA 4 mg/5 ml Jarabe Principio Activo Bromhexina
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Nombre del producto: Forma farmacéutica: Fortaleza: Presentación: Titular del Registro Sanitario, país: Fabricante, país: Número de Registro Sanitario: MEROPENEM
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Nombre del producto: Forma farmacéutica: Fortaleza: Presentación: Titular del Registro Sanitario, país: Fabricante, país: Número de Registro Sanitario: MEROPENEM
FICHA TÉCNICA. ENTEROSTREP SP 500mg/g polvo para administración en agua de bebida para conejos
 FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO ENTEROSTREP SP 500mg/g polvo para administración en agua de bebida para conejos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada g contiene: Sustancia
FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO ENTEROSTREP SP 500mg/g polvo para administración en agua de bebida para conejos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada g contiene: Sustancia
Trasplante de microbiota fecal (FMT)
 CLOSTRIDIUM DIFFICILE (C. DIFFICILE) Trasplante de microbiota fecal (FMT) El Trasplante de microbiota fecal (FMT) es cuando las heces de un donante saludable se convierten en una mezcla líquida y se transfieren
CLOSTRIDIUM DIFFICILE (C. DIFFICILE) Trasplante de microbiota fecal (FMT) El Trasplante de microbiota fecal (FMT) es cuando las heces de un donante saludable se convierten en una mezcla líquida y se transfieren
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 INDOMETACINA 25 mg COMPRIMIDOS RECUBIERTOS ANTIINFLAMATORIO ANTIRREUMÁTICO Página 1 INDOMETACINA 25 mg Comprimidos
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 INDOMETACINA 25 mg COMPRIMIDOS RECUBIERTOS ANTIINFLAMATORIO ANTIRREUMÁTICO Página 1 INDOMETACINA 25 mg Comprimidos
RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO PARACETAMOL SP, 300 mg/ml Solución para administración en agua de bebida, para cerdos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO PARACETAMOL SP, 300 mg/ml Solución para administración en agua de bebida, para cerdos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
TRIAX 500mg + Una ampolla de Agua Esterilizada Inyectable 10ml. TRIAX 1g + Una ampolla de Agua Esterilizada Inyectable 10ml.
 AZTREONAM TRIAX 500mg + Una ampolla de Agua Esterilizada Inyectable 10ml. TRIAX 1g + Una ampolla de Agua Esterilizada Inyectable 10ml. Descripción El aztreonam es un antibiótico beta-lactámico, derivado
AZTREONAM TRIAX 500mg + Una ampolla de Agua Esterilizada Inyectable 10ml. TRIAX 1g + Una ampolla de Agua Esterilizada Inyectable 10ml. Descripción El aztreonam es un antibiótico beta-lactámico, derivado
Documento Local del Producto
 1 Documento Local del Producto Título del Documento de Producto: Alprazolam Fecha de CDS que reemplaza: 14 de octubre de 2013 Fecha Efectiva: 12 de diciembre de 2013 Versión CDS: 8.0 1. NOMBRE DEL MEDICAMENTO
1 Documento Local del Producto Título del Documento de Producto: Alprazolam Fecha de CDS que reemplaza: 14 de octubre de 2013 Fecha Efectiva: 12 de diciembre de 2013 Versión CDS: 8.0 1. NOMBRE DEL MEDICAMENTO
OFLOXACINO. Tableta. 200 mg. 24 meses
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Nombre del producto: OFLOXACINO Forma farmacéutica: Fortaleza: Presentación: Titular del Registro Sanitario, país: Fabricante, país: Tableta 200 mg Estuche por
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Nombre del producto: OFLOXACINO Forma farmacéutica: Fortaleza: Presentación: Titular del Registro Sanitario, país: Fabricante, país: Tableta 200 mg Estuche por
IM cara anterolateral del muslo en los lactantes o el músculo deltoides de la parte superior del brazo en los niños.
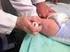 ESQUEMA CON VACUNAS ESPECIALES VACUNACION NO CUBIERTA POR EL PAN OBLIGATORIO DE SALUD Hepatitis B Anti hepatitis B A partir de los 5 º dosis en la fecha elegida. ª un mes después de la primera dosis. ª
ESQUEMA CON VACUNAS ESPECIALES VACUNACION NO CUBIERTA POR EL PAN OBLIGATORIO DE SALUD Hepatitis B Anti hepatitis B A partir de los 5 º dosis en la fecha elegida. ª un mes después de la primera dosis. ª
FOLLETO DE INFORMACIÓN AL PROFESIONAL DEBRIDAT COMPRIMIDOS RECUBIERTOS 100 mg
 FOLLETO DE INFORMACIÓN AL PROFESIONAL DEBRIDAT COMPRIMIDOS RECUBIERTOS 100 mg 1. NOMBRE(S) DEL PRODUCTO MEDICINAL DEBRIDAT COMPRIMIDOS RECUBIERTOS 100 mg 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada
FOLLETO DE INFORMACIÓN AL PROFESIONAL DEBRIDAT COMPRIMIDOS RECUBIERTOS 100 mg 1. NOMBRE(S) DEL PRODUCTO MEDICINAL DEBRIDAT COMPRIMIDOS RECUBIERTOS 100 mg 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Glucosamina KERN PHARMA 1.500 mg polvo para solución oral EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada sobre
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Glucosamina KERN PHARMA 1.500 mg polvo para solución oral EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada sobre
Prevención, Diagnóstico y Tratamiento de la Infección de Vías Urinarias No Complicada en Menores de 18 años en el Primero y Segundo Nivel de Atención
 Guía de Referencia Rápida Prevención, Diagnóstico y Tratamiento de la Infección de Vías Urinarias No Complicada en Menores de 18 años en el Primero y Segundo Nivel de Atención Guía de Referencia Rápida
Guía de Referencia Rápida Prevención, Diagnóstico y Tratamiento de la Infección de Vías Urinarias No Complicada en Menores de 18 años en el Primero y Segundo Nivel de Atención Guía de Referencia Rápida
Ictericia Neonatal. Ictericia e hiperbilirrubinemia son conceptos semejantes. Hiperbilirrubinemia se refiere al alza sérica de la bilirrubina.
 Ictericia Neonatal Ictericia e hiperbilirrubinemia son conceptos semejantes. Ictericia es el signo clínico. Hiperbilirrubinemia se refiere al alza sérica de la bilirrubina. Es la coloración amarillenta
Ictericia Neonatal Ictericia e hiperbilirrubinemia son conceptos semejantes. Ictericia es el signo clínico. Hiperbilirrubinemia se refiere al alza sérica de la bilirrubina. Es la coloración amarillenta
CENAVUL Suspensión inyectable
 Camí Pedra Estela s/n 43205 Reus Telf. 977 75 72 73 Fax. 977 75 13 98 www.cenavisa.com E-mail: [email protected] FICHA TÉCNICA: CENAVUL Suspensión inyectable Reg. nº: 2145 ESP FICHA TÉCNICA (RESUMEN
Camí Pedra Estela s/n 43205 Reus Telf. 977 75 72 73 Fax. 977 75 13 98 www.cenavisa.com E-mail: [email protected] FICHA TÉCNICA: CENAVUL Suspensión inyectable Reg. nº: 2145 ESP FICHA TÉCNICA (RESUMEN
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 CALCIO-500 D COMPRIMIDOS RECUBIERTOS SUPLEMENTO MINERAL Página 1 CALCIO-500 D Comprimidos Recubiertos Principio
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 CALCIO-500 D COMPRIMIDOS RECUBIERTOS SUPLEMENTO MINERAL Página 1 CALCIO-500 D Comprimidos Recubiertos Principio
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO BOVILIS BVD Suspensión inyectable para bovino. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por dosis
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO BOVILIS BVD Suspensión inyectable para bovino. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por dosis
LOPERAMIDA 2 mg Tableta
 LOPERAMIDA 2 mg Tableta LOPERAMIDA 2 mg Tabletas Antidiarreico COMPOSICION: Cada tableta contiene : Loperamida Clorhidrato...2,00 mg Excipientes c.s.p....1 tableta INDICACIONES: La eficacia de algunos
LOPERAMIDA 2 mg Tableta LOPERAMIDA 2 mg Tabletas Antidiarreico COMPOSICION: Cada tableta contiene : Loperamida Clorhidrato...2,00 mg Excipientes c.s.p....1 tableta INDICACIONES: La eficacia de algunos
FICHA TÉCNICA. 3. FORMA FARMACÉUTICA Comprimidos recubiertos. Biconvexos, ovales, de color blanco o blanquecino grisáceo jaspeado.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO FUCIDINE 250 mg comprimidos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 250 mg de fusidato de sodio. Excipiente: 72 mg de lactosa por comprimido.
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO FUCIDINE 250 mg comprimidos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 250 mg de fusidato de sodio. Excipiente: 72 mg de lactosa por comprimido.
MEROPENEM 500mg 1000mg
 MEROPENEM 500mg 1000mg 1. Identificación del Medicamento Nombre Comercial Meropenem para Inyección USP Nombre Genérico Meropenem Concentración 500mg 1000mg Denominación Común Internacional Meropenem N
MEROPENEM 500mg 1000mg 1. Identificación del Medicamento Nombre Comercial Meropenem para Inyección USP Nombre Genérico Meropenem Concentración 500mg 1000mg Denominación Común Internacional Meropenem N
La citarabina, ARA-C o arabinósido de citocina es un antimetabolito específico de la fase S del ciclo celular; impide la síntesis de ADN.
 INFORMACION PARA PRESCRIBIR AMPLIA 1. Nombre Comercial: MEDSARA 2. Nombre Genérico: CITARABINA 3. Forma Farmacéutica y Formulación: SOLUCIÓN INYECTABLE Cada frasco ámpula contiene: Citarabina.. 500 mg
INFORMACION PARA PRESCRIBIR AMPLIA 1. Nombre Comercial: MEDSARA 2. Nombre Genérico: CITARABINA 3. Forma Farmacéutica y Formulación: SOLUCIÓN INYECTABLE Cada frasco ámpula contiene: Citarabina.. 500 mg
RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO. 25 μg
 agencia española de medicamentos y productos sanitarios RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO HibTITER solución inyectable Vacuna conjugada frente a Haemophilus influenzae tipo
agencia española de medicamentos y productos sanitarios RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO HibTITER solución inyectable Vacuna conjugada frente a Haemophilus influenzae tipo
BUENOS AIRES, VISTO el Expediente NO 1-0047-0000-022126-10-5 del Registro de
 ~desai«d SeeuúvÚ4 de 'PeGtíea6. 'Rt9UÚef4.e e 1 'f4tim-tu A.1t.??t.A. 7. DISposrcrON N~ O 5 8 1 BUENOS AIRES, 25 ENE ldii VISTO el Expediente NO 1-0047-0000-022126-10-5 del Registro de la Administración
~desai«d SeeuúvÚ4 de 'PeGtíea6. 'Rt9UÚef4.e e 1 'f4tim-tu A.1t.??t.A. 7. DISposrcrON N~ O 5 8 1 BUENOS AIRES, 25 ENE ldii VISTO el Expediente NO 1-0047-0000-022126-10-5 del Registro de la Administración
FICHA TÉCNICA. La dosis a utilizar dependerá de la evolución de los síntomas y deberá utilizarse siempre la menor dosis efectiva.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ultra-Levura 250 mg cápsulas duras 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada cápsula contiene: Saccharomyces boulardii 250 mg Excipientes con efecto conocido:
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ultra-Levura 250 mg cápsulas duras 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada cápsula contiene: Saccharomyces boulardii 250 mg Excipientes con efecto conocido:
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. MAGNESIUM PYRE 64 mg comprimidos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO MAGNESIUM PYRE 64 mg comprimidos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 64 mg de magnesio (en forma de 550 mg de cloruro de magnesio,
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO MAGNESIUM PYRE 64 mg comprimidos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 64 mg de magnesio (en forma de 550 mg de cloruro de magnesio,
CUADRO 01 MORBILIDAD HOSPITALARIA PEDIATRIA MEDICA INFECCIOSA ENERO 2011
 CUADRO 01 ENERO 2011 1 A91 FIEBRE DEL DENGUE HEMORRAGICO 8 22,86 2 J18 NEUMONIA, ORGANISMO NO ESPECIFICADO 5 14,29 3 A37 TOS FERINA (TOS CONVULSIVA) 2 5,71 4 A87 MENINGITIS VIRAL 2 5,71 5 J21 BRONQUIOLITIS
CUADRO 01 ENERO 2011 1 A91 FIEBRE DEL DENGUE HEMORRAGICO 8 22,86 2 J18 NEUMONIA, ORGANISMO NO ESPECIFICADO 5 14,29 3 A37 TOS FERINA (TOS CONVULSIVA) 2 5,71 4 A87 MENINGITIS VIRAL 2 5,71 5 J21 BRONQUIOLITIS
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. Apirofeno 4% suspensión oral 2. COMPOSICION CUALITATIVA Y CUANTITATIVA
 agencia española de medicamentos y productos sanitarios FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Apirofeno 4% suspensión oral 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada ml de suspensión oral contiene:
agencia española de medicamentos y productos sanitarios FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Apirofeno 4% suspensión oral 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada ml de suspensión oral contiene:
Salvacolina 2 mg comprimidos
 Prospecto: información para el paciente Salvacolina 2 mg comprimidos Loperamida hidrocloruro Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene información importante
Prospecto: información para el paciente Salvacolina 2 mg comprimidos Loperamida hidrocloruro Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene información importante
NOMBRE DEL MEDICAMENTO
 1. NOMBRE DEL MEDICAMENTO DURACEF 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA DURACEF 250 mg/5 ml: Por 60 ml: Cefadroxilo (monohidrato) (DCI) 3 g Benzoato de sodio Celulosa microcristalina Saborizante limón
1. NOMBRE DEL MEDICAMENTO DURACEF 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA DURACEF 250 mg/5 ml: Por 60 ml: Cefadroxilo (monohidrato) (DCI) 3 g Benzoato de sodio Celulosa microcristalina Saborizante limón
La cafeína también se puede usar para otras condiciones según lo determine su médico.
 Cafeína (Por vía oral) Índice de contenidos - DESCRIPCIÓN GENERAL - A TENER EN CUENTA - UTILIZACIÓN - ADVERTENCIAS - EFECTOS SECUNDARIOS - COMENTARIOS DESCRIPCIÓN GENERAL La cafeína corresponde al grupo
Cafeína (Por vía oral) Índice de contenidos - DESCRIPCIÓN GENERAL - A TENER EN CUENTA - UTILIZACIÓN - ADVERTENCIAS - EFECTOS SECUNDARIOS - COMENTARIOS DESCRIPCIÓN GENERAL La cafeína corresponde al grupo
FICHA TÉCNICA. VAXIGRIP 2016 Vacuna anti-influenza inactivada suspensión inyectable
 FICHA TÉCNICA VAXIGRIP 2016 Vacuna anti-influenza inactivada suspensión inyectable 1. NOMBRE DEL MEDICAMENTO VAXIGRIP, suspensión inyectable en jeringa precargada Vacuna antiinfluenza de virus fraccionados,
FICHA TÉCNICA VAXIGRIP 2016 Vacuna anti-influenza inactivada suspensión inyectable 1. NOMBRE DEL MEDICAMENTO VAXIGRIP, suspensión inyectable en jeringa precargada Vacuna antiinfluenza de virus fraccionados,
PROSPECTO: INFORMACIÓN PARA EL USUARIO. Zitromax 500 mg comprimidos recubiertos con película Azitromicina
 PROSPECTO: INFORMACIÓN PARA EL USUARIO Zitromax 500 mg comprimidos recubiertos con película Azitromicina Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento - Conserve este prospecto
PROSPECTO: INFORMACIÓN PARA EL USUARIO Zitromax 500 mg comprimidos recubiertos con película Azitromicina Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento - Conserve este prospecto
THIAFELINE 2,5 mg COMPRIMIDOS RECUBIERTOS CON PELÍCULA PARA GATOS
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO THIAFELINE 2,5 mg COMPRIMIDOS RECUBIERTOS CON PELÍCULA PARA GATOS 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO THIAFELINE 2,5 mg COMPRIMIDOS RECUBIERTOS CON PELÍCULA PARA GATOS 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada
PROSPECTO SUPRASEC LOPERAMIDA
 PROSPECTO SUPRASEC LOPERAMIDA Venta bajo receta Industria Brasileña FÓRMULA CUALITATIVA Y CUANTITATIVA Loperamida clorhidrato (ClH) 2 mg por comprimido. Lista de Excipientes: Lactosa monohidratada, almidón
PROSPECTO SUPRASEC LOPERAMIDA Venta bajo receta Industria Brasileña FÓRMULA CUALITATIVA Y CUANTITATIVA Loperamida clorhidrato (ClH) 2 mg por comprimido. Lista de Excipientes: Lactosa monohidratada, almidón
Para la lista completa de excipientes, véase la sección Indicaciones de uso, especificando las especies de destino
 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Metacam 2 mg/ml solución inyectable para gatos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un ml contiene: Sustancia activa: Meloxicam Excipientes: Etanol 2 mg
1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Metacam 2 mg/ml solución inyectable para gatos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un ml contiene: Sustancia activa: Meloxicam Excipientes: Etanol 2 mg
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 Nombre del producto: DCI Forma farmacéutica: Fortaleza: RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Cetimer 5 mg (Levocetirizina) Comprimido recubierto 5 mg Presentación: Estuche por 10 blísteres de PVC/AL
Nombre del producto: DCI Forma farmacéutica: Fortaleza: RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Cetimer 5 mg (Levocetirizina) Comprimido recubierto 5 mg Presentación: Estuche por 10 blísteres de PVC/AL
Desórdenes renales. Profa. Noemí Díaz Ruberté, MSN
 Desórdenes renales Profa. Noemí Díaz Ruberté, MSN 1 Glomerulonefritis posestreptococcica aguda Reacción inmunológica (antígeno-anticuerpo) a una infección del organismo que suele ser provocada por una
Desórdenes renales Profa. Noemí Díaz Ruberté, MSN 1 Glomerulonefritis posestreptococcica aguda Reacción inmunológica (antígeno-anticuerpo) a una infección del organismo que suele ser provocada por una
SERPIENTES Definición:
 SERPIENTES Definición: Las serpientes u ofidios son reptiles caracterizados por la ausencia de extremidades y un cuerpo muy alargado. En España hay solo dos familias de serpientes venenosas: las víboras
SERPIENTES Definición: Las serpientes u ofidios son reptiles caracterizados por la ausencia de extremidades y un cuerpo muy alargado. En España hay solo dos familias de serpientes venenosas: las víboras
