|
|
|
- Yolanda Lara Páez
- hace 7 años
- Vistas:
Transcripción
1 DAGUERROTIPOS - Fotografía artística En 1839, cuando Daguerre inventó la forma de hacer retratos por medio de una lente y con productos químicos, el mundo quedó tan atónito como quedamos nosotros, no hace muchos años, cuando se dieron a conocer los principios de la radio. Los bisabuelos de la generación actual posaban durante las tres horas necesarias para la exposición daguerrotipo, notable contraste con las exposiciones de una fracción de segundo, posibles ahora con las cámaras más económicas. Este artículo explica la forma de sacar daguerrotipos. AUN existen algunos pocos daguerrotipos originales, altamente estimados por sus poseedores. Ahora se pueden sacar fotografías por este mismo sistema, facilitado, sin embargo, por las ventajas ofrecidas por descubrimientos posteriores, trabajando con una cámara de mano, y con una exposición de pocos segundos. En esta forma se conserva toda la belleza del sistema original: una delicada fotografía en plata y oro, sobre una chapa de cobre pulido, digna de adornar cualquier habitación, o de ser exhibida ante amigos que nunca hayan visto un ejemplo de la técnica con que se hacían las fotografías cien años atrás.
2 Se comienza por cortar una chapa completamente exenta de marcas, de cobre grueso, dándole las dimensiones necesarias para que entre en el soporte de la película de una cámara de mano; si la cámara es de rollo, la chapa de cobre puede descansar contra los rodillos de la película. Se limpia la placa con una solución de ácido nítrico y luego se frota con polvo de piedra pómez húmedo, y finalmente se pule con blanco de España y agua. Mientras se seca, y durante cada una de las operaciones subsiguientes, la placa se sujeta por los bordes. La superficie pulida se platea y vuelve a pulirse; una solución fría producirá una capa de plata suficientemente pesada, y para ponerla no se necesita más que una frotación con una muñeca de algodón. En 28 gr. (una onza) de agua destilada se disuelven los siguientes productos, en el orden indicado: 1,5 gramos (25 granos) de nitrato de plata; 2,7 gramos (45 granos) de tiosulfato de sodio (hiposulfito); 1,8 gramos (30 granos) de cloruro de amonio, y so agregan 1,2 gramos (20 granos) de blanco de España. La superficie de plata debe pulirse con un paño suave, para asegurarse los mejores resultados. La operación que sigue se practica en una habitación obscura. Mientras se realiza el proceso de "iodización" se usa luz amarilla, pero cuando se trabaja con bromo, y después, la luz será roja. Se empapa una hoja de papel secante con una solución de yodo común (el usado en cirugía) y cuando esté seco, se lo deposita en el fondo de una caja de madera (una de cigarros podría servir). La superficie de la placa pulida y bañada en plata se coloca contra el papel secante, separándolas en los bordes con varillitas de diámetro aproximado al de un fósforo grueso, como se ve en la fig. 4. Los vapores del yodo atacarán lentamente la plata, y cuando se vea que ésta ha tomado un color entre dorado y anaranjado, se la puede considerar en condiciones de
3 seguir con las demás operaciones del procedimiento. De la mayor o la menor exposición a los vapores de yodo depende la sensibilidad final de la placa a la luz. Enseguida se expone la placa, den tro de la caja de cigarros, a los vapores del bromo. Estos se conducen a la caja por medio de un tubo de goma que parte de un generador constituido, sencillamente, por un tubo de ensayo, de vidrio, en el que se han colocado 1,5 gramos (25 granos) de bromuro de potasio; 1,8 gramos (30 granos) de dióxido de manganeso y la cantidad necesaria de ácido sulfúrico para que ambos productos químicos se saturen bien. El calor de un fósforo bastará para producir una reacción mediante la cual se generarán gases de bromo. Cuando la placa tome un color rosa estará ya completamente sensibilizada, y deberá ser cuidadosamente manipulada bajo luz roja. Se coloca la placa sensible en la cámara, con la superficie plateada dirigida hacia la lente de la misma, y se está listo para hacer la exposición, la cámara tiene que estar en un lugar completamente firme, sea un trípode o una mesa; la luz tiene que ser brillante; el diafragma o la abertura de la cámara se gradúa a f:8 y el tiempo de exposición prolongarse de cinco a diez segundos. Si la exposición fracasara, se limpia la placa y se repite el procedimiento. En la cámara obscura se tiene preparada una caja de cigarros sobre una placa eléctrica; como se ve en la fig. 6, en el fondo de la caja se ha hecho un orificio sobre el que se coloca un vidrio o un platito de loza, en el que se vuelcan unas cuantas gotas de mercurio. La placa se suspende por sus bordes, con la cara sensibilizada mirando hacia abajo, sobre los dos bloques que se ven en la fig. 6. Se cierra la caja y se enciende el calentador eléctrico de plancha, dando el calor necesario para calentar el mercurio.
4 Mediante alguna' inspección se comprobará que la fotografía va haciéndose visible lentamente. Cuando se haya completado el proceso de revelación so pone la placa en una cubeta conteniendo una solución sencilla de hiposulfito, para fijarla. La fotografía fijada no queda en blanco y negro, sino en plata y cobre, colores que pueden mejorarse entonándolos, con lo que adquiere esa rica tonalidad dorada y plateada, que hace tan atractivos a los daguerrotipos, aún en nuestros días. La placa se coloca en una solución en la que se la tiene durante unos cinco o diez minutos, consistente en: tiosulfato do sodio, 56 gramos (2 onzas); agua destilada, 28 gramos (una onza). A esto se agregan 0,3 gramos (5 granos) de cloruro de oro disueltos en 28 gramos (una onza) de agua destilada.
5 Después de enjuagar se deja que el delicado cuadrito se seque sin tocar su superficie, y luego se pasa por ella una mano de algún barniz transparente y de poco cuerpo, sin cuya protección la plata se obscurecería, provocando la desaparición de la figura. Para el mayor lucimiento de esta foto conviene un buen marco de estilo antiguo, como el ilustrado.
6 El cloruro de oro es muy costoso, pero el aficionado lo puede preparar por sí mismo disolviendo un pedacito de alguna antigua alhaja de oro en agua regia (una parte de ácido nítrico mezclada con tres partes de ácido clorhídrico puro), que se diluye doblando su volumen con agua destilada. Se agregan luego pequeñas cantidades de solución de sulfato de hierro hasta que el líquido pierda su aspecto turbio. Al pasarlo por un papel de filtro, el oro quedará depositado sobre el papel. Se lava con agua, se vuelve a disolver en la misma mezcla de ácido nítrico ácido clorhídrico anteriormente mencionado y se deja evaporar en una cubeta de vidrio o de loza, calentada; solamente quedará el cloruro de sodio.
PRACTICA No.9 REACCIONES QUIMICAS I
 PRACTICA No.9 REACCIONES QUIMICAS I INTRODUCCION: Las transformaciones de la materia se conocen como REACCIONES QUIMICAS. En ellas se opera un cambio en la estructura íntima de las sustancias reaccionantes
PRACTICA No.9 REACCIONES QUIMICAS I INTRODUCCION: Las transformaciones de la materia se conocen como REACCIONES QUIMICAS. En ellas se opera un cambio en la estructura íntima de las sustancias reaccionantes
EJERCITACIÓN SOLUCIONES I
 Ejercicios sobre soluciones %/, %/v, g/l Reducciones entre %/, %/v, g/l EJERCITACIÓN SOLUCIONES I MOMENCLATURA s : Masa de solución sv : Masa de solvente. s : Masa de soluto δ : Densidad de la solución
Ejercicios sobre soluciones %/, %/v, g/l Reducciones entre %/, %/v, g/l EJERCITACIÓN SOLUCIONES I MOMENCLATURA s : Masa de solución sv : Masa de solvente. s : Masa de soluto δ : Densidad de la solución
Nombre: País Código. 1.- Calcula el contenido de cada metal en la escobilla expresado en % en masa.
 Problema. La recuperación de oro, plata y platino en un taller de platería. 1 PUNTOS En la mesa de trabajo de los plateros se acumula un residuo que, entre los profesionales, se denomina escobilla. Está
Problema. La recuperación de oro, plata y platino en un taller de platería. 1 PUNTOS En la mesa de trabajo de los plateros se acumula un residuo que, entre los profesionales, se denomina escobilla. Está
Materia: FÍSICA Y QUÍMICA Curso
 ACTIVIDADES DE REFUERZO FÍSICA Y QUÍMICA 3º ESO. JUNIO 2015. 1.- Realizar las configuraciones electrónicas de todos los elementos de los tres primeros periodos de la tabla periódica. 2.- Razonar cuales
ACTIVIDADES DE REFUERZO FÍSICA Y QUÍMICA 3º ESO. JUNIO 2015. 1.- Realizar las configuraciones electrónicas de todos los elementos de los tres primeros periodos de la tabla periódica. 2.- Razonar cuales
CANTIDAD DE PARTICULAS LIVIANAS EN LOS AGREGADOS PETREOS I.N.V. E
 CANTIDAD DE PARTICULAS LIVIANAS EN LOS AGREGADOS PETREOS I.N.V. E 221 07 1. OBJETO 1.1 Esta norma tiene por objeto establecer el método para determinar el porcentaje de partículas livianas en los agregados
CANTIDAD DE PARTICULAS LIVIANAS EN LOS AGREGADOS PETREOS I.N.V. E 221 07 1. OBJETO 1.1 Esta norma tiene por objeto establecer el método para determinar el porcentaje de partículas livianas en los agregados
DETERMINACIÓN DEL PORCENTAJE DE PLOMO MTC E
 DETERMINACIÓN DEL PORCENTAJE DE PLOMO MTC E 1219 2000 Este Modo Operativo está basado en la Norma ASTM D 49, el mismo que se han adaptado al nivel de implementación y a las condiciones propias de nuestra
DETERMINACIÓN DEL PORCENTAJE DE PLOMO MTC E 1219 2000 Este Modo Operativo está basado en la Norma ASTM D 49, el mismo que se han adaptado al nivel de implementación y a las condiciones propias de nuestra
Qué especie actúa generalmente como comburente? Es esta especie el único comburente? Objetivo: Demostrar el papel del oxígeno como comburente.
 RESUMEN: Aquí podrás encontrar algunas actividades experimentales que te podrán resultar útiles para la unidad de proceso de combustión, del programa de 2 EMT opciones: Electromecánica, Electro-electró
RESUMEN: Aquí podrás encontrar algunas actividades experimentales que te podrán resultar útiles para la unidad de proceso de combustión, del programa de 2 EMT opciones: Electromecánica, Electro-electró
ESTEQUIOMETRÍA. cobre(ii) y se descompone, cuántas moles de dióxido de nitrógeno se formarán? A moles B moles C moles D. 0.
 ESTEQUIOMETRÍA 1 Al calentarse fuertemente, el nitrato de cobre(ii) se descompone en óxido de cobre(ii), dióxido de nitrógeno y oxígeno elemental (O 2 ). Si calentamos 0.10 moles de nitrato de cobre(ii)
ESTEQUIOMETRÍA 1 Al calentarse fuertemente, el nitrato de cobre(ii) se descompone en óxido de cobre(ii), dióxido de nitrógeno y oxígeno elemental (O 2 ). Si calentamos 0.10 moles de nitrato de cobre(ii)
Clasificador por Objeto del Gasto Clasificador por Objeto del Gasto
 20199020000001 20199 020 000001 Clasificador por Objeto del 20199020000011 20199 020 000011 Clasificador por Objeto del 20199020000060 20199 020 000060 Clasificador por Objeto del 20199020000300 20199
20199020000001 20199 020 000001 Clasificador por Objeto del 20199020000011 20199 020 000011 Clasificador por Objeto del 20199020000060 20199 020 000060 Clasificador por Objeto del 20199020000300 20199
Solubilidad. Material de apoyo, Segundo Medio monica.ibanez@lbvm. onica.ibanez@lbvm.clcl 15:21
 Solubilidad Material de apoyo, Segundo Medio monica.ibanez@lbvm. onica.ibanez@lbvm.clcl Obj. de hoy: Señalar que es Solubilidad y los factores que la afectan. Qué es algo SOLUBLE? La Solubilidad corresponde
Solubilidad Material de apoyo, Segundo Medio monica.ibanez@lbvm. onica.ibanez@lbvm.clcl Obj. de hoy: Señalar que es Solubilidad y los factores que la afectan. Qué es algo SOLUBLE? La Solubilidad corresponde
EQUILIBRIO QUÍMICO 2
 EQUILIBRIO QUÍMICO 2 Los desplazamientos de equilibrio con la transferencia de energía. Termómetros químicos. Muchos de los intercambios de ligandos en la formación de complejos ocurren con absorción o
EQUILIBRIO QUÍMICO 2 Los desplazamientos de equilibrio con la transferencia de energía. Termómetros químicos. Muchos de los intercambios de ligandos en la formación de complejos ocurren con absorción o
El sulfato de cobre, en la proporción del 15 % aproximadamente, produce el verde azul pálido.
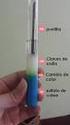 1 Estos materiales se obtienen mezclando, con las materias vitrificables sometidas a fusión en los crisoles, algunos óxidos metálicos, aislados o mezclados, pero siempre en pequeñísimas proporciones. Bastará
1 Estos materiales se obtienen mezclando, con las materias vitrificables sometidas a fusión en los crisoles, algunos óxidos metálicos, aislados o mezclados, pero siempre en pequeñísimas proporciones. Bastará
Formula y nombra los siguientes compuestos. Fórmula Nomenclatura sistemática Nomenclatura StocK Nomenclatura tradicional Ba O
 Co I3 Formula y nombra los siguientes compuestos Fórmula Nomenclatura sistemática Nomenclatura StocK Nomenclatura tradicional Ba O Cu2O Al2 O3 Na H Ca H2 Al H3 Au H Co H3 Fe H2 H F H Cl H2 S H2 Se Al2
Co I3 Formula y nombra los siguientes compuestos Fórmula Nomenclatura sistemática Nomenclatura StocK Nomenclatura tradicional Ba O Cu2O Al2 O3 Na H Ca H2 Al H3 Au H Co H3 Fe H2 H F H Cl H2 S H2 Se Al2
1) Agrupar las siguientes propiedades según sean extensivas o intensivas:
 Sistemas Materiales Guía de Ejercitación 1) Agrupar las siguientes propiedades según sean extensivas o intensivas: a) Volumen b) Densidad c) Olor d) Pto. de fusión e) Presión f) Sabor g) Pto. de ebullición
Sistemas Materiales Guía de Ejercitación 1) Agrupar las siguientes propiedades según sean extensivas o intensivas: a) Volumen b) Densidad c) Olor d) Pto. de fusión e) Presión f) Sabor g) Pto. de ebullición
Disoluciones. AUTHOR: VICENTE GUZMÁN BROTÓNS
 Disoluciones AUTHOR: VICENTE GUZMÁN BROTÓNS http://bencenoanhidro.blogspot.com Disoluciones AUTHOR: VICENTE GUZMÁN BROTÓNS http://bencenoanhidro.blogspot.com Problemas de disoluciones 1. Calcula la concentración
Disoluciones AUTHOR: VICENTE GUZMÁN BROTÓNS http://bencenoanhidro.blogspot.com Disoluciones AUTHOR: VICENTE GUZMÁN BROTÓNS http://bencenoanhidro.blogspot.com Problemas de disoluciones 1. Calcula la concentración
Práctica 3. Solubilidad
 PREGUNTS RESPONDER L FINL DE L PRÁTI Práctica 3. Solubilidad Revisaron: M. en. Martha Magdalena Flores Leonar Dr. Víctor Manuel Ugalde Saldívar QF. Fabiola González Olguín La concentración es una propiedad
PREGUNTS RESPONDER L FINL DE L PRÁTI Práctica 3. Solubilidad Revisaron: M. en. Martha Magdalena Flores Leonar Dr. Víctor Manuel Ugalde Saldívar QF. Fabiola González Olguín La concentración es una propiedad
Acuerdo 286. Química. Disoluciones. Recopiló: M.C. Macaria Hernández Chávez
 Acuerdo 286 Química Disoluciones Recopiló: M.C. Macaria Hernández Chávez Disolución: Es una mezcla homogénea de dos o más sustancias. La sustancia que se encuentra en mayor proporción se llama disolvente
Acuerdo 286 Química Disoluciones Recopiló: M.C. Macaria Hernández Chávez Disolución: Es una mezcla homogénea de dos o más sustancias. La sustancia que se encuentra en mayor proporción se llama disolvente
DETERMINACIÓN DE LA DEMANDA QUÍMICA DE OXÍGENO, DQO, TOTAL EN UNA MUESTRA DE AGUA RESIDUAL DOMÉSTICA
 EXPERIMENTO 4 DETERMINACIÓN DE LA DEMANDA QUÍMICA DE OXÍGENO, DQO, TOTAL EN UNA MUESTRA DE AGUA RESIDUAL DOMÉSTICA Objetivo general Determinación de Demanda Química de Oxígeno total (DQO) en una muestra
EXPERIMENTO 4 DETERMINACIÓN DE LA DEMANDA QUÍMICA DE OXÍGENO, DQO, TOTAL EN UNA MUESTRA DE AGUA RESIDUAL DOMÉSTICA Objetivo general Determinación de Demanda Química de Oxígeno total (DQO) en una muestra
Teoria de insolación de PCB
 Página 1 de 5 Teoria de insolación de PCB 1.- Introducción: En primer lugar explicaré la constitución de los materiales que utilizaremos para la creación de circuitos impresos - Placa Fotosensible: Por
Página 1 de 5 Teoria de insolación de PCB 1.- Introducción: En primer lugar explicaré la constitución de los materiales que utilizaremos para la creación de circuitos impresos - Placa Fotosensible: Por
REACCIONES DE TRANSFERENCIA DE ELECTRONES 2ºBACH
 1. Ajusta las siguientes reacciones redox, utilizando el método del ion electrón: a) HNO 3 + Cu Cu(NO 3 ) 2 + NO 2 + H 2 O b) K 2 Cr 2 O 7 +HI + HClO 4 Cr(ClO 4 ) 3 +I 2 +KClO 4 + H 2 O c) H 2 SO 4 + HI
1. Ajusta las siguientes reacciones redox, utilizando el método del ion electrón: a) HNO 3 + Cu Cu(NO 3 ) 2 + NO 2 + H 2 O b) K 2 Cr 2 O 7 +HI + HClO 4 Cr(ClO 4 ) 3 +I 2 +KClO 4 + H 2 O c) H 2 SO 4 + HI
Masas atómicas (g/mol): O = 16; S = 32; Zn = 65,4. Sol: a) 847 L; b) 710,9 g; c) 1,01 atm.
 1) Dada la siguiente reacción química: 2 AgNO3 + Cl2 N2O5 + 2 AgCl + ½ O2. a) Calcule los moles de N2O5 que se obtienen a partir de 20 g de AgNO3. b) Calcule el volumen de O2 obtenido, medido a 20 ºC y
1) Dada la siguiente reacción química: 2 AgNO3 + Cl2 N2O5 + 2 AgCl + ½ O2. a) Calcule los moles de N2O5 que se obtienen a partir de 20 g de AgNO3. b) Calcule el volumen de O2 obtenido, medido a 20 ºC y
E.8 Q. Guía de Química FUNCIONES QUÍMICAS. PROSERQUISA DE C.V. - Todos los Derechos Reservados
 FUNCIONES QUÍMICAS Guía de Química EXPERIMENTO N 8 IDENTIFICACIÓN DE FUNCIONES QUIMICAS OBJETVOS: Que el estudiante logre identificar experimentalmente las funciones químicas: Óxido, Ácido, Base y Sal.
FUNCIONES QUÍMICAS Guía de Química EXPERIMENTO N 8 IDENTIFICACIÓN DE FUNCIONES QUIMICAS OBJETVOS: Que el estudiante logre identificar experimentalmente las funciones químicas: Óxido, Ácido, Base y Sal.
1 Disponemos de un ácido nítrico comercial (HNO3) de densidad 1,15 g/cm 3 y riqueza 25,48% en masa.
 Relación de Problemas Unidades de Concentración 1 Disponemos de un ácido nítrico comercial (HNO3) de densidad 1,15 g/cm 3 y riqueza 25,48% en masa. a) Determina la molaridad del ácido nítrico comercial.
Relación de Problemas Unidades de Concentración 1 Disponemos de un ácido nítrico comercial (HNO3) de densidad 1,15 g/cm 3 y riqueza 25,48% en masa. a) Determina la molaridad del ácido nítrico comercial.
PALACORRE. TEMA 2: Los cambios de aspecto de la materia I.E.S. LA CORREDORIA OVIEDO 1º ESO GRUPO: ALUMNO: DPTO. CIENCIAS NATURALES
 PALACORRE I.E.S. LA CORREDORIA OVIEDO DPTO. CIENCIAS NATURALES TEMA 2: Los cambios de aspecto de la materia 1º ESO ALUMNO: GRUPO: TEMA 2: LOS CAMBIOS DE ASPECTO DE LA MATERIA Nombre y apellidos: Fecha:
PALACORRE I.E.S. LA CORREDORIA OVIEDO DPTO. CIENCIAS NATURALES TEMA 2: Los cambios de aspecto de la materia 1º ESO ALUMNO: GRUPO: TEMA 2: LOS CAMBIOS DE ASPECTO DE LA MATERIA Nombre y apellidos: Fecha:
Espátulas, navecillas y embudos CÁPSULAS EN ACERO INOX. Y NÍQUEL. CRISOLES EN ACERO INOX., NÍQUEL Y ZIRCONIO.
 Espátulas, navecillas y embudos CÁPSULAS EN ACERO INOX. Y NÍQUEL. CRISOLES EN ACERO INOX., NÍQUEL Y ZIRCONIO. MICROESPÁTULA DOBLE PLANA 1027680 80 mm. 4 mm. 1276120 1. 4 mm. 1276150 150 mm. 4 mm. 1276210
Espátulas, navecillas y embudos CÁPSULAS EN ACERO INOX. Y NÍQUEL. CRISOLES EN ACERO INOX., NÍQUEL Y ZIRCONIO. MICROESPÁTULA DOBLE PLANA 1027680 80 mm. 4 mm. 1276120 1. 4 mm. 1276150 150 mm. 4 mm. 1276210
Flowchart Variolink N LC
 Flowchart Variolink N LC DIENTE - Carilla - Composite - Variolink N LC - Tetric N-Bond 1 El temporal es retirado Retirada del provisional. Si fuese necesario retirar cualquier resto de cemento provisional
Flowchart Variolink N LC DIENTE - Carilla - Composite - Variolink N LC - Tetric N-Bond 1 El temporal es retirado Retirada del provisional. Si fuese necesario retirar cualquier resto de cemento provisional
PLANCHA A VAPOR BA-390
 PLANCHA A VAPOR BA-390 Manual de Instrucciones 1 Estimado Cliente Electron Felicitaciones por escoger un producto Electron. Al hacer esta elección de calidad, usted se ha asegurado un uso libre de problemas
PLANCHA A VAPOR BA-390 Manual de Instrucciones 1 Estimado Cliente Electron Felicitaciones por escoger un producto Electron. Al hacer esta elección de calidad, usted se ha asegurado un uso libre de problemas
ELECTROQUÍMICA. 1- Concepto de potencial normal. Electrodo de referencia
 ELECTROQUÍMICA 1 Concepto de potencial normal. Electrodo de referencia 2 Se forma una pila con un electrodo de níquel y otro de plata. Indica el electrodo que eléctricamente es el polo positivo, el que
ELECTROQUÍMICA 1 Concepto de potencial normal. Electrodo de referencia 2 Se forma una pila con un electrodo de níquel y otro de plata. Indica el electrodo que eléctricamente es el polo positivo, el que
LEASE ESTE INSTRUCTIVO ANTES DE USAR EL PRODUCTO TOATADOR ELECTRICO PARA CUATRO REBANADAS
 LEASE ESTE INSTRUCTIVO ANTES DE USAR EL PRODUCTO TOATADOR ELECTRICO PARA CUATRO REBANADAS Modelo T401 INSTRUCCIONES DE SEGURIDAD Cuando se usan aparatos electrónicos, deben tomarse algunas precauciones,
LEASE ESTE INSTRUCTIVO ANTES DE USAR EL PRODUCTO TOATADOR ELECTRICO PARA CUATRO REBANADAS Modelo T401 INSTRUCCIONES DE SEGURIDAD Cuando se usan aparatos electrónicos, deben tomarse algunas precauciones,
Práctica 3. Solubilidad
 Práctica 3. Solubilidad PREGUNTS RESPONDER L FINL DE L PRÁTI La concentración es una propiedad intensiva o extensiva? Por qué? Por qué al aumentar la temperatura aumenta la solubilidad de una disolución
Práctica 3. Solubilidad PREGUNTS RESPONDER L FINL DE L PRÁTI La concentración es una propiedad intensiva o extensiva? Por qué? Por qué al aumentar la temperatura aumenta la solubilidad de una disolución
5007 Reacción de anhidrido ftálico con resorcina para obtener fluoresceina
 57 Reacción de anhidrido ftálico con resorcina para obtener fluoresceina CH H H + 2 + 2 H 2 H C 8 H 4 3 C 6 H 6 2 C 2 H 12 5 (148.1) (11.1) (332.3) Clasificación Tipos de reacción y clases de productos
57 Reacción de anhidrido ftálico con resorcina para obtener fluoresceina CH H H + 2 + 2 H 2 H C 8 H 4 3 C 6 H 6 2 C 2 H 12 5 (148.1) (11.1) (332.3) Clasificación Tipos de reacción y clases de productos
LABORATORIO 6. TITULO : Propiedades de los Gases
 37 LABORATORIO 6. TITULO : Propiedades de los Gases OBJETIVOS: Demostrar la ley de difusión de los gases (ley de Graham) Comparar la velocidad de difusión de los gases con la de los líquidos. MATERIALES
37 LABORATORIO 6. TITULO : Propiedades de los Gases OBJETIVOS: Demostrar la ley de difusión de los gases (ley de Graham) Comparar la velocidad de difusión de los gases con la de los líquidos. MATERIALES
TRABAJO PRÁCTICO N 0 3 TERMOQUÍMICA
 TRABAJO PRÁCTICO N 0 3 TERMOQUÍMICA OBJETIVOS Determinación de la variación de entalpía asociada a procesos químicos. Aplicación de conceptos termodinámicos: temperatura, calor, entalpía. Verificación
TRABAJO PRÁCTICO N 0 3 TERMOQUÍMICA OBJETIVOS Determinación de la variación de entalpía asociada a procesos químicos. Aplicación de conceptos termodinámicos: temperatura, calor, entalpía. Verificación
Joya de Autor. Pieza Original: Broche
 Consigna: A partir de una joya dada, rediseñar en base a su propia visión como diseñador, modificando si o sí la utilidad, y desarrollar a partir de la modificación y reinterpretacion de la morfología
Consigna: A partir de una joya dada, rediseñar en base a su propia visión como diseñador, modificando si o sí la utilidad, y desarrollar a partir de la modificación y reinterpretacion de la morfología
REACCIONES REDOX. Tubos de ensayo, permanganato de potasio, peróxido de hidrógeno, ácido sulfúrico.
 REACCIONES REDOX PRÁCTICA 1 Cápsula de porcelana, mechero, limaduras de cobre Se coloca en una capsula de porcelana limaduras de cobre y se calienta. Al cabo de cierto tiempo se observa que las limaduras
REACCIONES REDOX PRÁCTICA 1 Cápsula de porcelana, mechero, limaduras de cobre Se coloca en una capsula de porcelana limaduras de cobre y se calienta. Al cabo de cierto tiempo se observa que las limaduras
PROCEDIMIENTO ESPECÍFICO. Código G-140-01 Edición 0
 Índice 1. TABLA RESUMEN... 2 2. OBJETO... 2 3. ALCANCE... 2 4. RESPONSABILIDADES... 3 5. ENTRADAS... 3 6. SALIDAS... 3 7. PROCESOS RELACIONADOS... 3 8. DIAGRAMA DE FLUJO... 4 9. DESARROLLO... 5 9.1. REVELADO...
Índice 1. TABLA RESUMEN... 2 2. OBJETO... 2 3. ALCANCE... 2 4. RESPONSABILIDADES... 3 5. ENTRADAS... 3 6. SALIDAS... 3 7. PROCESOS RELACIONADOS... 3 8. DIAGRAMA DE FLUJO... 4 9. DESARROLLO... 5 9.1. REVELADO...
RepublicofEcuador EDICTOFGOVERNMENT±
 RepublicofEcuador EDICTOFGOVERNMENT± Inordertopromotepubliceducationandpublicsafety,equaljusticeforal, abeterinformedcitizenry,theruleoflaw,worldtradeandworldpeace, thislegaldocumentisherebymadeavailableonanoncommercialbasis,asit
RepublicofEcuador EDICTOFGOVERNMENT± Inordertopromotepubliceducationandpublicsafety,equaljusticeforal, abeterinformedcitizenry,theruleoflaw,worldtradeandworldpeace, thislegaldocumentisherebymadeavailableonanoncommercialbasis,asit
NORMA MEXICANA NMX-F-492-SCFI-2009 ALIMENTOS ACEITES Y GRASAS VEGETALES DETERMINACIÓN DE CONTENIDO DE JABÓN- MÉTODO DE PRUEBA
 NORMA MEXICANA NMX-F-492-SCFI-2009 ALIMENTOS ACEITES Y GRASAS VEGETALES DETERMINACIÓN DE CONTENIDO DE JABÓN- MÉTODO DE PRUEBA FOODS VEGETABLE FATS AND OILS DETERMINATION OF SOAP CONTENT- TEST METHOD P
NORMA MEXICANA NMX-F-492-SCFI-2009 ALIMENTOS ACEITES Y GRASAS VEGETALES DETERMINACIÓN DE CONTENIDO DE JABÓN- MÉTODO DE PRUEBA FOODS VEGETABLE FATS AND OILS DETERMINATION OF SOAP CONTENT- TEST METHOD P
Trabajo Práctico N 3. Reconocimiento de sustancias ácidas, básicas y neutras. mediante el empleo de indicadores químicos.
 Trabajo Práctico N 3 Reconocimiento de sustancias ácidas, básicas y neutras mediante el empleo de indicadores químicos. Objetivos: Diferenciar mediante el empleo de indicadores u el cambio de color de
Trabajo Práctico N 3 Reconocimiento de sustancias ácidas, básicas y neutras mediante el empleo de indicadores químicos. Objetivos: Diferenciar mediante el empleo de indicadores u el cambio de color de
EJERCIOS DE CONCENTRACIÓN DE SOLUCIONES
 Preuniversitario Liceo de Aplicación Química 4º 2010 Profesora Paola Lizama V. GUÍA 4: DISOLUCIONES EJERCIOS DE CONCENTRACIÓN DE SOLUCIONES 01.- Calcular la cantidad de sosa cáustica (NaOH) y de agua que
Preuniversitario Liceo de Aplicación Química 4º 2010 Profesora Paola Lizama V. GUÍA 4: DISOLUCIONES EJERCIOS DE CONCENTRACIÓN DE SOLUCIONES 01.- Calcular la cantidad de sosa cáustica (NaOH) y de agua que
LECTURA DIFERENCIA ENTRE METALES Y NO METALES POR SU COMPORTAMIENTO FRENTE AL OXÍGENO.
 LECTURA DIFERENCIA ENTRE METALES Y NO METALES POR SU COMPORTAMIENTO FRENTE AL OXÍGENO. Prácticamente todos los elementos conocidos, metales y no metales, reaccionan o son oxidados por el oxígeno formando
LECTURA DIFERENCIA ENTRE METALES Y NO METALES POR SU COMPORTAMIENTO FRENTE AL OXÍGENO. Prácticamente todos los elementos conocidos, metales y no metales, reaccionan o son oxidados por el oxígeno formando
GUIA DEL ESTUDIANTE-CLASE 4
 GUIA DEL ESTUDIANTE-CLASE 4 1.-Recuerda que los elementos químicos están formados por un solo tipo de átomos,. Qué elementos químicos conoces y qué características tienen? 2.- Realiza una lista de elementos
GUIA DEL ESTUDIANTE-CLASE 4 1.-Recuerda que los elementos químicos están formados por un solo tipo de átomos,. Qué elementos químicos conoces y qué características tienen? 2.- Realiza una lista de elementos
Tenga en cuenta el espacio pequeño. Me pareció que el espacio aéreo más, un CDS más débiles se produjo. Tanto como el 50% menos!
 Cómo preparo CDS a través del "Shot Glass" Método Cómo preparar un litro o cuarto de galón de solución de 25 ppm de dióxido de cloro - 26 de septiembre 212 Descargo de responsabilidad: Este procedimiento
Cómo preparo CDS a través del "Shot Glass" Método Cómo preparar un litro o cuarto de galón de solución de 25 ppm de dióxido de cloro - 26 de septiembre 212 Descargo de responsabilidad: Este procedimiento
MANUAL DE INSTRUCCIONES
 Contraste de fases MANUAL DE INSTRUCCIONES Modelo B-380 B-500 B-800 B-1000 Versión: 2 Publicado: 18, 08, 2014 Introducción al contraste de fases Las preparaciones sin teñir y por lo tanto transparentes
Contraste de fases MANUAL DE INSTRUCCIONES Modelo B-380 B-500 B-800 B-1000 Versión: 2 Publicado: 18, 08, 2014 Introducción al contraste de fases Las preparaciones sin teñir y por lo tanto transparentes
NOMENCLATURA QUIMICA
 Universidad Católica del Norte Departamento de Química Practica Nº 2 NOMENCLATURA QUIMICA Nomenclatura química Objetivos 1. Familiarizar a los estudiantes con las funciones químicas como son: óxidos, hidróxidos,
Universidad Católica del Norte Departamento de Química Practica Nº 2 NOMENCLATURA QUIMICA Nomenclatura química Objetivos 1. Familiarizar a los estudiantes con las funciones químicas como son: óxidos, hidróxidos,
GUIA DE RESISTENCIAS QUIMICAS PARA TUBERIA DE POLIPROPILENO COPOLIMERO RANDOM (TUBOPLUS)
 GUIA DE RESISTENCIAS QUIMICAS PARA TUBERIA DE POLIPROPILENO COPOLIMERO RANDOM (TUBOPLUS) R = Alta resistencia RM = Resistencia media NR = No resiste Reactivo químico Concentración Temperatura 20º Temperatura
GUIA DE RESISTENCIAS QUIMICAS PARA TUBERIA DE POLIPROPILENO COPOLIMERO RANDOM (TUBOPLUS) R = Alta resistencia RM = Resistencia media NR = No resiste Reactivo químico Concentración Temperatura 20º Temperatura
http://www.rubenprofe.com.ar
 SOLUCIONES Objetivos: Mínimo: Definir las concentraciones Molar, normal, % m/m, % m/v y % v/v. Describir la forma de preparar soluciones de concentraciones definidas. Realizar cálculos con concentraciones
SOLUCIONES Objetivos: Mínimo: Definir las concentraciones Molar, normal, % m/m, % m/v y % v/v. Describir la forma de preparar soluciones de concentraciones definidas. Realizar cálculos con concentraciones
RepublicofEcuador EDICTOFGOVERNMENT±
 RepublicofEcuador EDICTOFGOVERNMENT± Inordertopromotepubliceducationandpublicsafety,equaljusticeforal, abeterinformedcitizenry,theruleoflaw,worldtradeandworldpeace, thislegaldocumentisherebymadeavailableonanoncommercialbasis,asit
RepublicofEcuador EDICTOFGOVERNMENT± Inordertopromotepubliceducationandpublicsafety,equaljusticeforal, abeterinformedcitizenry,theruleoflaw,worldtradeandworldpeace, thislegaldocumentisherebymadeavailableonanoncommercialbasis,asit
Problemas de Estequiometría (ampliación) Pág. Nº 1
 Problemas de Estequiometría (ampliación) Pág. Nº 1 MOLES, MOLÉCULAS Y ÁTOMOS: 1.- Calcular la masa de agua que contienen 0,23 moles de agua. Sol: 4,14 g 2.- Calcular la masa de una molécula de agua. Sol:
Problemas de Estequiometría (ampliación) Pág. Nº 1 MOLES, MOLÉCULAS Y ÁTOMOS: 1.- Calcular la masa de agua que contienen 0,23 moles de agua. Sol: 4,14 g 2.- Calcular la masa de una molécula de agua. Sol:
Reemplazo Nvidia Escudo Tablet K1 Puerto micro USB
 Reemplazo Nvidia Escudo Tablet K1 Puerto micro USB Esta es una guía para la retirada y sustitución del puerto micro USB. Escrito por: Ryan Butler INTRODUCCIÓN El puerto USB Micro es para cargar la tableta.
Reemplazo Nvidia Escudo Tablet K1 Puerto micro USB Esta es una guía para la retirada y sustitución del puerto micro USB. Escrito por: Ryan Butler INTRODUCCIÓN El puerto USB Micro es para cargar la tableta.
Contenido 1. Qué es la fotografía?... 46 2. Historia de la fotografía... 46 3. La cámara fotográfica... 48 La cámara oscura... 48 4.
 Contenido 1. Qué es la fotografía?... 46 2. Historia de la fotografía... 46 3. La cámara fotográfica... 48 La cámara oscura... 48 4. Componentes de la cámara fotográfica... 49 A. Diafragma... 50 B. Obturador...
Contenido 1. Qué es la fotografía?... 46 2. Historia de la fotografía... 46 3. La cámara fotográfica... 48 La cámara oscura... 48 4. Componentes de la cámara fotográfica... 49 A. Diafragma... 50 B. Obturador...
1)OBJETIVOS DE LA PRACTICA
 1)OBJETIVOS DE LA PRACTICA Comprobar que una mezcla es simplemente la unión física de sustancias y que por lo tanto, dichas sustancias se pueden separar mediante procedimientos físicos. Separar los componentes
1)OBJETIVOS DE LA PRACTICA Comprobar que una mezcla es simplemente la unión física de sustancias y que por lo tanto, dichas sustancias se pueden separar mediante procedimientos físicos. Separar los componentes
REACCIONES REDOX CON DICROMATO POTÁSICO
 REACCIONES REDOX CON DICROMATO POTÁSICO Se han comenzado los trabajos de Química a la gota con las reacciones redox del permanganato potásico, un oxidante característico y visualmente muy interesante por
REACCIONES REDOX CON DICROMATO POTÁSICO Se han comenzado los trabajos de Química a la gota con las reacciones redox del permanganato potásico, un oxidante característico y visualmente muy interesante por
Introducción a la Química. Sistemas Materiales y Conceptos Fundamentales. Seminario de Problemas N 1
 Sistemas Materiales Introducción a la Química Seminario de Problemas N 1 1. Dibuja un esquema con los tres estados de la materia (sólido, líquido y gas) indicando el nombre de los cambios de estado. 2.
Sistemas Materiales Introducción a la Química Seminario de Problemas N 1 1. Dibuja un esquema con los tres estados de la materia (sólido, líquido y gas) indicando el nombre de los cambios de estado. 2.
COLEGIO DE BACHILLERES DEL ESTADO DE TLAXCALA DIRECCIÓN ACADÉMICA DEPARTAMENTO DE BIBLIOTECAS Y LABORATORIOS
 DIRECCIÓN ACADÉMICA DEPARTAMENTO DE BIBLIOTECAS Y LABORATORIOS ACTIVIDAD EXPERIMENTAL NÚM. 2 TABLA PERIÓDICA PROPIEDAD DE LOS NO METALES EN COMPARACIÓN CON LOS METALES (BLOQUE IV) INTRODUCCIÓN Una de las
DIRECCIÓN ACADÉMICA DEPARTAMENTO DE BIBLIOTECAS Y LABORATORIOS ACTIVIDAD EXPERIMENTAL NÚM. 2 TABLA PERIÓDICA PROPIEDAD DE LOS NO METALES EN COMPARACIÓN CON LOS METALES (BLOQUE IV) INTRODUCCIÓN Una de las
FIMET BS Proceso para ennegrecimiento de hierro y acero
 Proceso para ennegrecimiento de hierro y acero INTRODUCCION FIMET BS es un producto en polvo que disuelto en agua está especialmente desarrollado para ennegrecer el hierro y acero por simple inmersión,
Proceso para ennegrecimiento de hierro y acero INTRODUCCION FIMET BS es un producto en polvo que disuelto en agua está especialmente desarrollado para ennegrecer el hierro y acero por simple inmersión,
Química. Equilibrio ácido-base Nombre:
 Química DEPARTAMENTO DE FÍSICA E QUÍMICA Equilibrio ácido-base 25-02-08 Nombre: Cuestiones y problemas 1. a) Qué concentración tiene una disolución de amoníaco de ph =10,35? [1½ PUNTO] b) Qué es una disolución
Química DEPARTAMENTO DE FÍSICA E QUÍMICA Equilibrio ácido-base 25-02-08 Nombre: Cuestiones y problemas 1. a) Qué concentración tiene una disolución de amoníaco de ph =10,35? [1½ PUNTO] b) Qué es una disolución
Indice. PN/L/E/004/00 Página 1 de 7 Rev.: 0 Fecha de Edición: FARMACIA FUNCIONAMIENTO Y MANTENIMIENTO DEL BAÑO TERMOSTÁTICO (BAÑO MARÍA)
 FARMACIA EQUIPOS FUNCIONAMIENTO Y MANTENIMIENTO DEL BAÑO TERMOSTÁTICO (BAÑO MARÍA) Página 1 de 7 Rev.: 0 Fecha de Edición: Procedimientos relacionados: FUNCIONAMIENTO Y MANTENIMIENTO DEL BAÑO TERMOSTÁTICO
FARMACIA EQUIPOS FUNCIONAMIENTO Y MANTENIMIENTO DEL BAÑO TERMOSTÁTICO (BAÑO MARÍA) Página 1 de 7 Rev.: 0 Fecha de Edición: Procedimientos relacionados: FUNCIONAMIENTO Y MANTENIMIENTO DEL BAÑO TERMOSTÁTICO
REACTIVOS Y SOLUCIONES
 REACTIVOS Y SOLUCIONES 1. Especificaciones de reactivos Se realizará la consulta al GE sobre la calidad de los reactivos a utilizar (ACS, HPLC, etc.) hay que definir. Almidón- El almidón separado de los
REACTIVOS Y SOLUCIONES 1. Especificaciones de reactivos Se realizará la consulta al GE sobre la calidad de los reactivos a utilizar (ACS, HPLC, etc.) hay que definir. Almidón- El almidón separado de los
RepublicofEcuador EDICTOFGOVERNMENT±
 RepublicofEcuador EDICTOFGOVERNMENT± Inordertopromotepubliceducationandpublicsafety,equaljusticeforal, abeterinformedcitizenry,theruleoflaw,worldtradeandworldpeace, thislegaldocumentisherebymadeavailableonanoncommercialbasis,asit
RepublicofEcuador EDICTOFGOVERNMENT± Inordertopromotepubliceducationandpublicsafety,equaljusticeforal, abeterinformedcitizenry,theruleoflaw,worldtradeandworldpeace, thislegaldocumentisherebymadeavailableonanoncommercialbasis,asit
Análisis Cualitativo de Muestras Sólidas
 Facultad de Ciencias - Escuela de Química LABORATORIO DE QUIMICA ANALITICA Análisis Cualitativo de Muestras Sólidas Basado en el original publicado en: Semimicro Qualitative Analysis. Franck Welcher and
Facultad de Ciencias - Escuela de Química LABORATORIO DE QUIMICA ANALITICA Análisis Cualitativo de Muestras Sólidas Basado en el original publicado en: Semimicro Qualitative Analysis. Franck Welcher and
TEMA 3 GENERADORES DE CORRIENTE CONTINUA
 TEMA 3 GENERADORES DE CORRIENTE CONTINUA En todo circuito eléctrico es necesaria una fuente de energía que sea capaz de poner en movimiento a los electrones, a la cual llamamos generador. Si existen dos
TEMA 3 GENERADORES DE CORRIENTE CONTINUA En todo circuito eléctrico es necesaria una fuente de energía que sea capaz de poner en movimiento a los electrones, a la cual llamamos generador. Si existen dos
Historia de la Fotografía
 Historia de la Fotografía Qué es la fotografía? Etimológicamente, la palabra proviene del griego: FOTO GRAFÍA!"# $%&!'# PHOS GRAFIS Luz Dibujar Qué es la fotografía? La aparición de la fotografía y su
Historia de la Fotografía Qué es la fotografía? Etimológicamente, la palabra proviene del griego: FOTO GRAFÍA!"# $%&!'# PHOS GRAFIS Luz Dibujar Qué es la fotografía? La aparición de la fotografía y su
IES Real Instituto Jovellanos 1º BACHILLERATO. SERIE 17
 1.- Ajustar las siguientes reacciones: a) Propano + oxígeno === dióxido de carbono + agua b) Carbonato de sodio + ácido clorhídrico === cloruro de sodio + agua c) Tribromuro de fósforo + agua === ácido
1.- Ajustar las siguientes reacciones: a) Propano + oxígeno === dióxido de carbono + agua b) Carbonato de sodio + ácido clorhídrico === cloruro de sodio + agua c) Tribromuro de fósforo + agua === ácido
EJERCICIOS RESUELTOS DISOLUCIONES
 EJERCICIOS RESUELTOS DISOLUCIONES 1- Se disuelven 20 g de NaOH en 560 g de agua Calcula a) la concentración de la en % en masa b) su molalidad Ar(Na) 2 Ar(O)16 Ar(H)1 NaOH 20 a) % NaOH % NaOH % NaOH,45
EJERCICIOS RESUELTOS DISOLUCIONES 1- Se disuelven 20 g de NaOH en 560 g de agua Calcula a) la concentración de la en % en masa b) su molalidad Ar(Na) 2 Ar(O)16 Ar(H)1 NaOH 20 a) % NaOH % NaOH % NaOH,45
TEMA 2 CONCEPTOS BÁSICOS Cálculos estequiométricos
 TEMA 2 CONCEPTOS BÁSICOS Cálculos estequiométricos ÍNDICE 1. Ecuaciones (reacciones) químicas 2. Cálculos estequiométricos. Reactivo limitante y reacciones consecutivas 3. Pureza de un reactivo 4. Rendimiento
TEMA 2 CONCEPTOS BÁSICOS Cálculos estequiométricos ÍNDICE 1. Ecuaciones (reacciones) químicas 2. Cálculos estequiométricos. Reactivo limitante y reacciones consecutivas 3. Pureza de un reactivo 4. Rendimiento
DISOLUCIONES. Líquido (H 2 O)
 DISOLUCIONES Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos a más sustancias. En las disoluciones hay que distinguir el soluto, el disolvente y la
DISOLUCIONES Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos a más sustancias. En las disoluciones hay que distinguir el soluto, el disolvente y la
de todos los dados el correcto será el: a) A b) B c) C d) D
 Redox 3 41*. Uno de los experimentos que puedes hacer perfectamente en el laboratorio y que te permitiría recordar el proceso de la pila Daniell, sería sumergir una lámina o chapa de cinc en un vaso de
Redox 3 41*. Uno de los experimentos que puedes hacer perfectamente en el laboratorio y que te permitiría recordar el proceso de la pila Daniell, sería sumergir una lámina o chapa de cinc en un vaso de
RepublicofEcuador EDICTOFGOVERNMENT±
 RepublicofEcuador EDICTOFGOVERNMENT± Inordertopromotepubliceducationandpublicsafety,equaljusticeforal, abeterinformedcitizenry,theruleoflaw,worldtradeandworldpeace, thislegaldocumentisherebymadeavailableonanoncommercialbasis,asit
RepublicofEcuador EDICTOFGOVERNMENT± Inordertopromotepubliceducationandpublicsafety,equaljusticeforal, abeterinformedcitizenry,theruleoflaw,worldtradeandworldpeace, thislegaldocumentisherebymadeavailableonanoncommercialbasis,asit
ESPECIFICACIÓN DE LOS ÍTEMES DE PRUEBA
 Técnicas de Panadería Alimentación Química ESPECIFICACIÓN DE LOS ÍTEMES DE PRUEBA Aprendizaje Esperado Establecer relaciones cuantitativas en diversas reacciones químicas 1. Juan, debe diseñar un programa
Técnicas de Panadería Alimentación Química ESPECIFICACIÓN DE LOS ÍTEMES DE PRUEBA Aprendizaje Esperado Establecer relaciones cuantitativas en diversas reacciones químicas 1. Juan, debe diseñar un programa
Control de distancia de aparcamiento, trasero
 Installation instructions, accessories Nº instrucciones 31339804 Versión Nº pieza 1.2 31359219, 31339973, 31339803 Control de distancia de aparcamiento, trasero Volvo Car Corporation Control de distancia
Installation instructions, accessories Nº instrucciones 31339804 Versión Nº pieza 1.2 31359219, 31339973, 31339803 Control de distancia de aparcamiento, trasero Volvo Car Corporation Control de distancia
SUSTANCIA QUÍMICA mercurio oxígeno
 ELEMENTO O SUSTANCIA ELEMENTAL: Sustancia formada por un mismo tipo de átomos, por ejemplo: Hg, H 2, Cu, O 2 SUSTANCIA QUÍMICA mercurio oxígeno COMPUESTO O SUSTANCIA COMPUESTA: Sustancia formada por dos
ELEMENTO O SUSTANCIA ELEMENTAL: Sustancia formada por un mismo tipo de átomos, por ejemplo: Hg, H 2, Cu, O 2 SUSTANCIA QUÍMICA mercurio oxígeno COMPUESTO O SUSTANCIA COMPUESTA: Sustancia formada por dos
UNIDAD 10.- LAS UNIONES ENTRE ÁTOMOS. Cuestiones de evaluación inicial. 2.- Cuántos protones y cuantos neutrones tiene el Carbono?
 UNIDAD 10.- LAS UNIONES ENTRE ÁTOMOS Cuestiones de evaluación inicial 1.- Cuántos elementos químicos conoces? 2.- Cuántos protones y cuantos neutrones tiene el Carbono? 3.- Qué es el sistema periódico?
UNIDAD 10.- LAS UNIONES ENTRE ÁTOMOS Cuestiones de evaluación inicial 1.- Cuántos elementos químicos conoces? 2.- Cuántos protones y cuantos neutrones tiene el Carbono? 3.- Qué es el sistema periódico?
SEPARACIÓN DE LOS COMPONENTES DE UNA MEZCLA
 PRÁCTICA Nº 3 SEPARACIÓN DE LOS COMPONENTES DE UNA MEZCLA OBJETIVOS: Establecer los fundamentos teóricos de los proceso de separación. Separar los componentes de diversas muestras problema. I. FUNDAMENTOS
PRÁCTICA Nº 3 SEPARACIÓN DE LOS COMPONENTES DE UNA MEZCLA OBJETIVOS: Establecer los fundamentos teóricos de los proceso de separación. Separar los componentes de diversas muestras problema. I. FUNDAMENTOS
El propósito principal de la deshidratación de alimentos es prolongar la durabilidad
 1.1 INTRODUCCIÓN El propósito principal de la deshidratación de alimentos es prolongar la durabilidad del producto final. El objetivo primordial del proceso de deshidratación es reducir el contenido de
1.1 INTRODUCCIÓN El propósito principal de la deshidratación de alimentos es prolongar la durabilidad del producto final. El objetivo primordial del proceso de deshidratación es reducir el contenido de
ASPECTOS CUANTITATIVOS EN QUÍMICA
 5 ASPECTOS CUANTITATIVOS EN QUÍMICA SOLUCIONES A LAS ACTIVIDADES DE FINAL DE UNIDAD Cantidades en Química. La masa atómica de la plata que encontramos en las tablas es de 07,87 u. Determina la abundancia
5 ASPECTOS CUANTITATIVOS EN QUÍMICA SOLUCIONES A LAS ACTIVIDADES DE FINAL DE UNIDAD Cantidades en Química. La masa atómica de la plata que encontramos en las tablas es de 07,87 u. Determina la abundancia
RECOPILADO POR: EL PROGRAMA UNIVERSITARIO DE ALIMENTOS
 NMX-F-312-1978. DETERMINACIÓN DE REDUCTORES DIRECTOS Y TOTALES EN ALIMENTOS. METHOD OF TEST FOR TOTAL AND DIRECT REDUCING SUBSTANCES IN FOOD. NORMAS MEXICANAS. DIRECCIÓN GENERAL DE NORMAS. PREFACIO En
NMX-F-312-1978. DETERMINACIÓN DE REDUCTORES DIRECTOS Y TOTALES EN ALIMENTOS. METHOD OF TEST FOR TOTAL AND DIRECT REDUCING SUBSTANCES IN FOOD. NORMAS MEXICANAS. DIRECCIÓN GENERAL DE NORMAS. PREFACIO En
Desperdicios peligrosos
 Desperdicios peligrosos 1 1 2 California-Arizona Consortium, Programa de Salud Laboral, Universidad de California, Berkeley Contenido 1. Sustancias peligrosas 2. Desperdicios peligrosos inflamable corrosivo
Desperdicios peligrosos 1 1 2 California-Arizona Consortium, Programa de Salud Laboral, Universidad de California, Berkeley Contenido 1. Sustancias peligrosas 2. Desperdicios peligrosos inflamable corrosivo
ENTRENAMIENTO EN PELICULA POLAROID Películas Integrales
 ENTRENAMIENTO EN PELICULA POLAROID Películas Integrales ENTRENAMIENTO EN PELICULA POLAROID Evaluación del seminario 1. Favor indicar si el objetivo del seminario estaba claramente estipulado. 2. Piensa
ENTRENAMIENTO EN PELICULA POLAROID Películas Integrales ENTRENAMIENTO EN PELICULA POLAROID Evaluación del seminario 1. Favor indicar si el objetivo del seminario estaba claramente estipulado. 2. Piensa
UN PISO DE MADERA CÓMO PULIR Y VITRIFICAR?
 ALTO nivel dificultad REMODELACIÓN Y CONSTRUCCIÓN PI-TU08 CÓMO PULIR Y VITRIFICAR? UN PISO DE MADERA Reparar y vitrificar los pisos de madera es una labor que podemos hacer nosotros mismos. Aunque parezca
ALTO nivel dificultad REMODELACIÓN Y CONSTRUCCIÓN PI-TU08 CÓMO PULIR Y VITRIFICAR? UN PISO DE MADERA Reparar y vitrificar los pisos de madera es una labor que podemos hacer nosotros mismos. Aunque parezca
PRACTICA No.10 ESTEQUIOMETRIA EN LAS REACCIONES QUIMICAS REACTIVO LIMITANTE Y RENDIMIENTO PORCENTUAL
 PRACTICA No.10 ESTEQUIOMETRIA EN LAS REACCIONES QUIMICAS REACTIVO LIMITANTE Y RENDIMIENTO PORCENTUAL INTRODUCCION: Los cambios químicos implican interacciones partícula con partícula(s) y no gramo a gramo,
PRACTICA No.10 ESTEQUIOMETRIA EN LAS REACCIONES QUIMICAS REACTIVO LIMITANTE Y RENDIMIENTO PORCENTUAL INTRODUCCION: Los cambios químicos implican interacciones partícula con partícula(s) y no gramo a gramo,
3º de E.S.O. Física y Química Ejercicios de Repaso para septiembre
 I.E.S. EL ESCORIAL 3º de E.S.O. Física y Química Ejercicios de Repaso para septiembre Apellidos: Nombre: Curso: Fecha: 1. Expresa en notación científica las siguientes cantidades: Magnitud Medida Notación
I.E.S. EL ESCORIAL 3º de E.S.O. Física y Química Ejercicios de Repaso para septiembre Apellidos: Nombre: Curso: Fecha: 1. Expresa en notación científica las siguientes cantidades: Magnitud Medida Notación
Las tuberías deben identificarse inequívocamente por placas que describan la materia de paso
 UNE 1063 OBJETO Y CAMPO DE APLICACIÓN Esta norma sirve para la caracterización de las materias que circulan por tuberías no puestas a tierra. Esta caracterización se realiza por medio de colores en los
UNE 1063 OBJETO Y CAMPO DE APLICACIÓN Esta norma sirve para la caracterización de las materias que circulan por tuberías no puestas a tierra. Esta caracterización se realiza por medio de colores en los
Problemas disoluciones
 Problemas disoluciones Determinar la concentración de una disolución expresada de diferentes formas: g/l, % en masa y en volumen, Molaridad y fracción molar Preparar disoluciones a partir de solutos sólidos
Problemas disoluciones Determinar la concentración de una disolución expresada de diferentes formas: g/l, % en masa y en volumen, Molaridad y fracción molar Preparar disoluciones a partir de solutos sólidos
Problemas en la medición de ph y su resolución.
 Problemas en la medición de ph y su resolución. Un sistema de medición de ph consta de varias partes : Medidor, Electrodos, Cables y Tampones de calibración. Cuando se presenta un problema al hacer una
Problemas en la medición de ph y su resolución. Un sistema de medición de ph consta de varias partes : Medidor, Electrodos, Cables y Tampones de calibración. Cuando se presenta un problema al hacer una
PRÁCTICA N 3 SOLUBILIDAD (CURVA DE SOLUBILIDAD Y CRISTALIZACIÓN FRACCIONADA)
 PRÁCTICA N 3 SOLUBILIDAD (CURVA DE SOLUBILIDAD Y CRISTALIZACIÓN FRACCIONADA) I. OBJETIVO GENERAL Establecer de forma experimental, la dependencia de la solubilidad con la temperatura. Utilizar la variación
PRÁCTICA N 3 SOLUBILIDAD (CURVA DE SOLUBILIDAD Y CRISTALIZACIÓN FRACCIONADA) I. OBJETIVO GENERAL Establecer de forma experimental, la dependencia de la solubilidad con la temperatura. Utilizar la variación
PROBLEMAS DE DISOLUCIONES 1º Bachillerato.-
 1 - Cuántos gramos de ácido nítrico son necesarios para preparar 1,5 litros de disolución acuosa de dicho ácido 0,6 M?. (Solución: 56,7 g) 2 - Una disolución 0,25 m de cloruro de sodio contiene 58,5 g
1 - Cuántos gramos de ácido nítrico son necesarios para preparar 1,5 litros de disolución acuosa de dicho ácido 0,6 M?. (Solución: 56,7 g) 2 - Una disolución 0,25 m de cloruro de sodio contiene 58,5 g
Practica 2ª : Destilación continua computerizada
 Practica 2ª : Destilación continua computerizada DESTILACIÓN DE SISTEMAS BINARIOS CON COMPORTAMIENTO AZEOTRÓPICO Unidad de Des
Practica 2ª : Destilación continua computerizada DESTILACIÓN DE SISTEMAS BINARIOS CON COMPORTAMIENTO AZEOTRÓPICO Unidad de Des
de aire. Determinar la composicion de la mezcla resultante. Cuál es el porcentaje en exceso de aire, suponiendo conversion completa?
 C A P Í T U L O 2 Dada la importancia que tienen los procesos de combustión en la generación de contaminantes, en este capítulo se han incluido algunos ejercicios relacionados con la combustión estequiométrica.
C A P Í T U L O 2 Dada la importancia que tienen los procesos de combustión en la generación de contaminantes, en este capítulo se han incluido algunos ejercicios relacionados con la combustión estequiométrica.
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2010 QUÍMICA TEMA 1: LA TRANSFORMACIÓN QUÍMICA
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 010 QUÍMICA TEMA 1: LA TRANSFORMACIÓN QUÍMICA Junio, Ejercicio, Opción B Reserva 1, Ejercicio 5, Opción A Reserva 1, Ejercicio 5, Opción B Reserva, Ejercicio
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 010 QUÍMICA TEMA 1: LA TRANSFORMACIÓN QUÍMICA Junio, Ejercicio, Opción B Reserva 1, Ejercicio 5, Opción A Reserva 1, Ejercicio 5, Opción B Reserva, Ejercicio
Métodos para la cuantificación de nitrógeno y proteína
 Practica 5 Métodos para la cuantificación de nitrógeno y proteína Antecedentes Para la determinación de proteínas en muestras de alimentos se cuenta con una gran variedad de métodos, basados en diferentes
Practica 5 Métodos para la cuantificación de nitrógeno y proteína Antecedentes Para la determinación de proteínas en muestras de alimentos se cuenta con una gran variedad de métodos, basados en diferentes
3ºESO-A PROFESORA LUCÍA ROMERO
 PLAN DE REFUERZO ÁREA PENDIENTE DE CIENCIAS NATURALES 3ºESO-A PROFESORA LUCÍA ROMERO BIOLOGÍA Y GEOLOGÍA: Resumen de cada tema del libro y las siguientes actividades: PRIMER TRIMESTRE: - Tema 1: La salud
PLAN DE REFUERZO ÁREA PENDIENTE DE CIENCIAS NATURALES 3ºESO-A PROFESORA LUCÍA ROMERO BIOLOGÍA Y GEOLOGÍA: Resumen de cada tema del libro y las siguientes actividades: PRIMER TRIMESTRE: - Tema 1: La salud
Determinación de la constante de los gases ideales
 Prácticas de Química. Determinación de la constante de los gases ideales I. Introducción teórica y objetivos........................................ 2 II. Material................................................................
Prácticas de Química. Determinación de la constante de los gases ideales I. Introducción teórica y objetivos........................................ 2 II. Material................................................................
EJEMPLOS DE PREGUNTA. Prueba de QUÍMICA. febrero 2010
 EJEMPLS DE PREGUNTA 2010 Prueba de QUÍMICA febrero 2010 PREGUNTAS DE SELECCIÓN MÚLTIPLE CN ÚNICA RESPUESTA. (TIP I) Las preguntas de este tipo constan de un enunciado y de cuatro opciones de respuesta,
EJEMPLS DE PREGUNTA 2010 Prueba de QUÍMICA febrero 2010 PREGUNTAS DE SELECCIÓN MÚLTIPLE CN ÚNICA RESPUESTA. (TIP I) Las preguntas de este tipo constan de un enunciado y de cuatro opciones de respuesta,
EJERCICIOS RESUELTOS DISOLUCIONES
 EJERIIOS RESUELTOS DISOLUIONES 1.- Se disuelven 20 g de NaOH en 560 g de agua. alcula a) la concentración de la en % en masa y b) su molalidad. Ar(Na) 2. Ar(O)16. Ar(H)1. NaOH 20 a) % NaOH.100 % NaOH.100
EJERIIOS RESUELTOS DISOLUIONES 1.- Se disuelven 20 g de NaOH en 560 g de agua. alcula a) la concentración de la en % en masa y b) su molalidad. Ar(Na) 2. Ar(O)16. Ar(H)1. NaOH 20 a) % NaOH.100 % NaOH.100
Sustancias puras, procesos de cambios de fase, diagramas de fase. Estado 3 Estado 4 Estado 5. P =1 atm T= 100 o C. Estado 3 Estado 4.
 TERMODINÁMICA Departamento de Física Carreras: Ing. Industrial y Mecánica Trabajo Práctico N 2: PROPIEDADES DE LAS SUSTANCIAS PURAS La preocupación por el hombre y su destino debe ser el interés primordial
TERMODINÁMICA Departamento de Física Carreras: Ing. Industrial y Mecánica Trabajo Práctico N 2: PROPIEDADES DE LAS SUSTANCIAS PURAS La preocupación por el hombre y su destino debe ser el interés primordial
Universidad Tecnológica de Panamá Centro de Investigaciones Hidráulicas e Hidrotécnicas Laboratorio de Sistemas Ambientales
 Página: 1 de 6 1. Introducción: Para la prueba de cloro y cloraminas en aguas potable, servidas (aguas negras), aguas salinas o de mar. El método de DPD-colorimetrico, N, N,-dietil-parafenildiamina, permite
Página: 1 de 6 1. Introducción: Para la prueba de cloro y cloraminas en aguas potable, servidas (aguas negras), aguas salinas o de mar. El método de DPD-colorimetrico, N, N,-dietil-parafenildiamina, permite
Manual de Laboratorio de Química Analítica
 PRÁCTICA 4: DETERMINACIÓN DE LA CONCENTRACIÓN DE ÁCIDO ACÉTICO EN UNA MUESTRA DE VINAGRE BLANCO INTRODUCCIÓN El vinagre blanco es una solución de ácido acético obtenida por fermentación. El análisis se
PRÁCTICA 4: DETERMINACIÓN DE LA CONCENTRACIÓN DE ÁCIDO ACÉTICO EN UNA MUESTRA DE VINAGRE BLANCO INTRODUCCIÓN El vinagre blanco es una solución de ácido acético obtenida por fermentación. El análisis se
CONCURSO NACIONAL DE OFERTA DE PRECIOS DNCAE No. 12-2006 LISTADO DE ESPECIFICACIONES DE LOS PRODUCTOS A OFERTAR ANEXO II
 de los productos a cotizar detallados en 54 renglones, fianzas y cantidades estimadas. 1 233 01 290 UNIFORMES (JUEGOS DE PANTS) TALLA S COMPUESTOS ASÍ: PLAYERA, PANTALONETA, CHUMPA Y PANTALÓN; TODOS CON
de los productos a cotizar detallados en 54 renglones, fianzas y cantidades estimadas. 1 233 01 290 UNIFORMES (JUEGOS DE PANTS) TALLA S COMPUESTOS ASÍ: PLAYERA, PANTALONETA, CHUMPA Y PANTALÓN; TODOS CON
