Acidificar a ph 1-2 con H 2SO 4 o HCl 1mes - para excluir el aire) Refrigerar 14 días
|
|
|
- Ángel Chávez Pinto
- hace 6 años
- Vistas:
Transcripción
1 Anexo II TÉCNICAS DE CONSERVACIÓN DE MUESTRAS Análisis químicos y físico-químicos de muestras acuosas. máx. Técnica de V lavado con Aceites y Grasas - disolvente Acidez, Alcalinidad y Bicarbonatos - para excluir el aire) 14 días Amoniaco, libre e ionizado o HCl 1mes - y 21 días Filtrar in situ antes de conservar P mes Filtrar in situ antes de conservar Aniones: Br, F, Cl, horas Filtrar in situ antes de conservar NO 2, NO 3, SO 4 y PO 4 - P mes Filtrar in situ antes de conservar 100 (llenar por Boro - P completo, excluir el aire) - 1 mes Puede ser estable 6 meses Bromato mes - Bromo residual horas determiar "in situ" Bromuro y compuestos de Bromo mes - Calcio y Dureza total HNO 3 1 mes - Carbono Orgánico 100 Acidificar con ph 1-2 y Adecuado acidificar a ph 1-2 con H3PO4. Si hay COV no es adecuado Total (COT) - P mes acidificar. Analizar en las primeras 8 h. Cianuro fácilmente liberado - P 500 Añadir NaOH hasta ph>12 y ó 24 h si hay sulfuro Mantener en oscuridad Cianuro por difusión a ph 6 - P 500 Añadir NaOH hasta ph>12 y 24 horas - Cianuro total - P 500 Añadir NaOH hasta ph>12 y 14 días Mantener en oscuridad Cloramina min. determinar "in situ" Clorato Página 1 de 7
2 Técnica de Clorito min. determinar "in situ" Cloro residual min.. Medida in situ horas Filtrar y extraer con etano P 1000 en caliente, congelar 1 mes Clorofila - P 1000 Tras filtrar, congelar a -80ºC 1 mes Transportar en vidrio color topacio Cloruro mes - Cloruro de cianógeno - P horas - Color días. En aguas subterráneas, ricas en Fe(II), medir in situ en 5 min. Compuestos organoestánnicos - V 500 Extraer "in situ" Compuestos purgables por purga y trampa - V, con tapón revestido de PTFE días. En muestras cloradas, añadir 80 mg muestra. Conductividad - B 100 (llenar por completo para excluir el aire) 24 h Preferible medir in situ. Cromo (VI) - P con lavado ácido ó V con lavado ácido h La oxido-reducción durante almacenamiento puede cambiar la concentración h DBO - P 1000 (llenar por completo para excluir el aire) 1 mes 100 DQO - P mes Puede ser estable 6 meses Dióxido de carbono - para excluir el aire) 24 h Preferible medir in situ. Dióxido de cloro min. determiar "in situ" Disolventes clorados - V, viales de espacio de cabeza con tapones de PTFE 250 (llenar por competo para excluir aire) HCl 24 horas En muestras cloradas, añadir 20 mg Na2S2O3 5H2O por cada 250 ml. El HCl interfiere en la purga y trampa. Página 2 de 7
3 Fenoles - VB, ámbar, lavado con disolvente, con tapón revestido de PTFE No pre-aclarar con muestra el recipiente; los analitos se adhieren a las paredes. No llenar completamente. Técnica de Acidificar a ph<4 con H3PO4 o H2SO4 3 semanas. Para clorofenoles el periodo de extracción son 2 días. Fluoruro - P, no PTFE mes - Fósforo y V o VB o P Ortofosfatos Disuelto P mes Conviene filtrar in situ en la toma. Fósforo y, refrigerar y oscuridad Ortofosfatos Total V o VB o P mes Puede ser estable 6 meses Halógenos orgánicos 1000 (llenar por completo para excluir el aire) HNO 3, refrigerar 6ºC y oscuridad 5 días adsorbibles (AOX) - P mes - Herbicidas ácidos - V, tapón o septum revestido de PTFE 1000 (no aclarar el recipiente ni llenarlo por completo) HCl y 2 semanas Hidracina - V 500 Acidificar con HCl hasta 1 mol/l 24 horas Hidrocarburos, Petróleo y derivados - V (no pre-aclarar con muestra el recipiente ni llenarlo completamente) o HCl 1mes Extraer in situ si es posible Hidrocarburos aromáticos monocíclicos - Hidrocarburos aromáticos policíclicos (PAHs) - Hierro (II) - V ámbar, viales con septum revestido con PTFE Índice de fenol - V 1000 para excluir el aire) V ámbar, lavado con disolvente, tapón revestido de PTFE 500 P con lavado ácido ó HCl y VB con lavado ácido 100 sin O 2 atmosférico - Adicionar CuSO4 para inhibir oxidación bioquímica y acidificar a ph<4 con H3PO4 21 días - Extraer in situ si es posible. En muestras cloradas, añadir 80 mg Página 3 de 7
4 Técnica de 8 mol/l 2 días Índice de y oscuridad 2 días permanganto - P 500 a 1 mes Iodo - V horas Ioduro - V mes - Analizar lo antes posible Litio - P 100 HNO 3 1 mes - Magnesio - P con lavado ácido ó VB con lavado ácido 100 HNO 3 1 mes - Total HNO 3 Mercurio Disuelto VB con lavado ácido 500 Filtrar "in situ" y acidificar a ph 1-2 con HNO3 28 días - Total HNO 3 Metales (excepto Hg, Disuelto Filtrar "in situ" y acidificar a ph 1-2 con HNO3 Li, Fe (II) y Cr 6+) Suspendido B 500 Filtrar "in situ" 1 mes Puede ser estable 6 meses 24 h Nitrato - P mes Nitrito h B Nitrógeno Kjeldahl - P mes. Puede ser estable 6 meses. Nitrógeno total Total P mes - Olor - V h Preferible medir in situ Oxígeno (llenar por completo para excluir el aire) - 4 días Fijar el oxígeno "in situ".. Pesticidas V lavado con disolvente 14 días carbamatos - P mes Página 4 de 7
5 Pesticidas organoclorados, organofosforados y organonitrogenados - ph - Técnica de V, lavado con disolvente, con tapón revestido de PTFE días 100 (llenar por completo. Extraer en las 24 horas al muestreo. para excluir el aire) 6 horas Preferible medir in situ Policloro bifenilos (PCBs) - V ámbar, lavado con disolvente, sellado con tapón revestido de PTFE (no pre-aclarar con muestra el recipiente ni llenarlo completamente) Preferible extraer "in situ". En muestras cloradas, añadir 80 mg Na 2S 2O 3 5H 2O por cada ml muestra al recipiente Potasio - P 100 HNO 3 1 mes - Disuelto 200 Filtrar "in situ". Silicatos Total P mes - Disuelto h - Total h - Sólidos Suspendido días - Sodio HNO 3 1 mes - Sulfato mes - Sulfito - Sulfuro (fácilmente liberable) - P Surfactantes aniónicos - Surfactantes catiónicos - para excluir el aire) - 2 días para excluir el aire) 1 semana V, aclarado con metanol 500. V, aclarado con metanol días Fijar "in situ" adicionando 1 ml de solución EDTA al 2,5% (masa) por cada 100 ml muestra Fijar "in situ" adicionando 2 ml de acetato zinc 10% (masa). En muestras cloradas, añadir 80 mg Na2S2O3 5H2O por cada 100 ml Evitar lavar el material de vidrio con detergente. Se puede combinar con no iónicos Evitar lavar el material de vidrio con detergente Evitar lavar el material de vidrio con detergente. Cuidado con los vapores de formaldehído En muestras cloradas, añadir 8 mg Na 2S 2O 3 5H 2O por cada 100 ml muestra Surfactantes no iónicos - V 500 (llenar por completo) Añadir formaldehído al 37% (volumen) V, viales con septum 100 (llenar por completo Trihalometanos - revestido de PTFE para excluir el aire) 2 días Turbidez h Preferible determinación de campo Página 5 de 7
6 Análisis químicos y físico-químicos de muestras sólidas. Parámetro Tipo de recipiente Peso típico (g) Técnica de ; acidificar a ph Aceites y Grasas V con H2SO4 o HCl 28 días - Boro P Carbamatos V, vial lleno sellado con cierre de teflón 250 Cationes P Cianuro P 5 28 días - Compuestos aromáticos V, vial lleno sellado con septum de volátiles teflón días Compuestos orgánicos semivolátiles V, vial lleno sellado con cierre de teflón 250 Compuestos orgánicos volátiles V, vial lleno sellado con cierre de teflón días COT días - 30 días hasta la extracción - Cromo hexavalente P con lavado ácido ó V con lavado ácido 100 desde la extracción hasta el análisis - Fenoles V, vial lleno sellado con cierre de teflón 250 Herbicidas clorados V, vial lleno sellado con cierre de teflón 250 Hidrocarburos extractables V, vial ámbar 125 ml Hidrocarburos del petróleo V días V, vial lleno sellado con septum de Hidrocarburos volátiles teflón días Mercurio VB con lavado ácido días - Metales (excepto Hg y Cr 6+) B Nitratos B 200 Análisis inmediato - PAH V, vial lleno sellado con cierre de teflón 250 Página 6 de 7
7 Parámetro Tipo de recipiente Peso típico (g) Técnica de Plaguicidas y PCBs V, vial lleno sellado con cierre de teflón 250 ph 20 - Análisis inmediato - Sulfuro P 100 Fijar las muestras "in situ" por adición de 2 ml de solución de acetato de zinc al 10%; refrigerar. - Análisis microbiológico. Matriz Tipo de recipiente Técnica de Aguas V o P estéril, con espacio de aire. : (3±2)ºC -Productos estables: temperatura ambiente (15ºC y 30ºC); -Productos congelados: Alimentos V o P estéril, menos de -15ºC; -Otros productos inestables a temperatura ambiente: entre 3 ± 2ºC. Menos de 24 h Preferiblemente en un plazo de 24 h a 36 h Si se va a superar el plazo de 36 horas las muestras se congelarían a una temperatura inferior a -15ºC. P = Plásticos [por ejemplo: polietileno, PTFE (politetrafluoroetileno), PVC (cloruro de polivinilo), PET (polietileno teraftalato)] V = Vidrio VB = Vidrio borosilicatado Página 7 de 7
Instructivo para la toma de muestra de suelos/lodos para análisis microbiológicos, físicoquímicos
 Instructivo para la toma de muestra de suelos/lodos para análisis microbiológicos, físicoquímicos y contaminantes 1. ENVASES: Precauciones generales: Se recomienda utilizar para la toma de muestras, los
Instructivo para la toma de muestra de suelos/lodos para análisis microbiológicos, físicoquímicos y contaminantes 1. ENVASES: Precauciones generales: Se recomienda utilizar para la toma de muestras, los
LISTADO DE ANÁLISIS Y MÉTODOS AGUA RESIDUAL (DOMESTICA E INDUSTRIAL)
 LISTADO DE ANÁLISIS Y MÉTODOS AGUA RESIDUAL (DOMESTICA E INDUSTRIAL) CARACTERIZACIONES DE AGUA RESIDUALES Comprenden los análisis de laboratorio que permiten conocer los contenidos de contaminantes orgánicos
LISTADO DE ANÁLISIS Y MÉTODOS AGUA RESIDUAL (DOMESTICA E INDUSTRIAL) CARACTERIZACIONES DE AGUA RESIDUALES Comprenden los análisis de laboratorio que permiten conocer los contenidos de contaminantes orgánicos
INDICE 1 - AGUAS DE CONSUMO 2 - AGUAS RESIDUALES 3 - AGUAS CONTINENTALES Y RESIDUALES 4 - CONTROL DE LEGIONELLA 5 - AGUAS DE BAÑO, RIEGO Y OTROS TIPOS
 INDICE 1 - AGUAS DE CONSUMO 2 - AGUAS RESIDUALES 3 - AGUAS CONTINENTALES Y RESIDUALES 4 - CONTROL DE LEGIONELLA 5 - AGUAS DE BAÑO, RIEGO Y OTROS TIPOS 6 - SUELOS 7- MATERIAL VEGETAL 8- LODOS 3 8 9 11 12
INDICE 1 - AGUAS DE CONSUMO 2 - AGUAS RESIDUALES 3 - AGUAS CONTINENTALES Y RESIDUALES 4 - CONTROL DE LEGIONELLA 5 - AGUAS DE BAÑO, RIEGO Y OTROS TIPOS 6 - SUELOS 7- MATERIAL VEGETAL 8- LODOS 3 8 9 11 12
1. PRODUCTOS ALIMENTICIOS PRIMARIOS DE ORIGEN VEGETAL
 Página 1 de 5 1. PRODUCTOS ALIMENTICIOS PRIMARIOS DE ORIGEN VEGETAL Frutas y hortalizas frescas incluidas las patatas y las remolachas azucareras y exceptuadas las hierbas aromáticas Clasificación del
Página 1 de 5 1. PRODUCTOS ALIMENTICIOS PRIMARIOS DE ORIGEN VEGETAL Frutas y hortalizas frescas incluidas las patatas y las remolachas azucareras y exceptuadas las hierbas aromáticas Clasificación del
GOBIERNO NACIONAL DE LA REPÚBLICA DEL ECUADOR SECRETARÍA DEL AGUA
 SECRETARÍA DEL AGUA PLAN DE MONITOREO DE CALIDAD DEL AGUA DE LOS SISTEMAS DE AGUA DE ABASTECIMIENTO PÚBLICO DE PORTOVIEJO, MANTA, CHONE, PEDERNALES, JAMA, BAHIA DE CARÁQUEZ, SAN VICENTE, CANOA, CALCETA,
SECRETARÍA DEL AGUA PLAN DE MONITOREO DE CALIDAD DEL AGUA DE LOS SISTEMAS DE AGUA DE ABASTECIMIENTO PÚBLICO DE PORTOVIEJO, MANTA, CHONE, PEDERNALES, JAMA, BAHIA DE CARÁQUEZ, SAN VICENTE, CANOA, CALCETA,
ANÁLISIS FISICOQUÍMICO Y MICROBIOLÓGICO DEL AGUA
 ANÁLISIS FISICOQUÍMICO Y MICROBIOLÓGICO DEL AGUA Dr. Andrés León. Departamento de Análisis y Control. Facultad de Farmacia y Bioanálisis. Universidad de los Andes. Mérida. Venezuela. Dr. Félix Andueza.
ANÁLISIS FISICOQUÍMICO Y MICROBIOLÓGICO DEL AGUA Dr. Andrés León. Departamento de Análisis y Control. Facultad de Farmacia y Bioanálisis. Universidad de los Andes. Mérida. Venezuela. Dr. Félix Andueza.
DATOS DE IDENTIFICACIÓN DEL LABORATORIO
 Hoja 1 de 8 DATOS DE IDENTIFICACIÓN DEL LABORATORIO LABORATORIOS VERIFICADORES MEDIOAMBIENTALES CAVENDISH S.L. POL. IND. JUNCARIL, C/ Baza, Parcela 6-I CTRA. Castellón-Alcora Km 19,5 18220 Albolote (Granada)
Hoja 1 de 8 DATOS DE IDENTIFICACIÓN DEL LABORATORIO LABORATORIOS VERIFICADORES MEDIOAMBIENTALES CAVENDISH S.L. POL. IND. JUNCARIL, C/ Baza, Parcela 6-I CTRA. Castellón-Alcora Km 19,5 18220 Albolote (Granada)
OFERTA DE SERVICIOS DEL LABORATORIO DE ANÁLISIS DE AGUAS
 OFERTA DE SERVICIOS DEL LABORATORIO DE ANÁLISIS DE AGUAS Código: D-4.4-01 Revisó: Subsidirector Jurídico y Administrativo Fecha: 12 de Octubre de 2010 Resolución: 300-03-10-23-1426-2010 Corporación para
OFERTA DE SERVICIOS DEL LABORATORIO DE ANÁLISIS DE AGUAS Código: D-4.4-01 Revisó: Subsidirector Jurídico y Administrativo Fecha: 12 de Octubre de 2010 Resolución: 300-03-10-23-1426-2010 Corporación para
CATÁLOGO DE SERVICIOS ANALÍTICOS ACREDITADOS EN EL LABORATORIO DE GALASA
 CATÁLOGO DE SERVICIOS ANALÍTICOS ACREDITADOS EN EL LABORATORIO DE GALASA CATÁLOGO DE SERVICIOS ANALÍTICOS Hoja 1 de 7 TEMPERATURA Y AGUA DETERMINACIÓN DE LA TEMPERATURA in situ. PNT-004 ph DETERMINACIÓN
CATÁLOGO DE SERVICIOS ANALÍTICOS ACREDITADOS EN EL LABORATORIO DE GALASA CATÁLOGO DE SERVICIOS ANALÍTICOS Hoja 1 de 7 TEMPERATURA Y AGUA DETERMINACIÓN DE LA TEMPERATURA in situ. PNT-004 ph DETERMINACIÓN
REGLAMENTO TÉCNICO DGNTI-COPANIT / MUESTREOS Y ANALISIS 4.1. GENERALIDADES.
 REGLAMENTO TÉCNICO DGNTI-COPANIT 35-2000 /39-2000 MUESTREOS Y ANALISIS 4.1. GENERALIDADES. La toma de muestras debe ser efectuada por personal idóneo del laboratorio l autorizado o acreditado, y realizada
REGLAMENTO TÉCNICO DGNTI-COPANIT 35-2000 /39-2000 MUESTREOS Y ANALISIS 4.1. GENERALIDADES. La toma de muestras debe ser efectuada por personal idóneo del laboratorio l autorizado o acreditado, y realizada
Ejercicios Nomenclatura Inorgánica
 Ejercicios Nomenclatura Inorgánica 1. De nombre a los siguientes compuestos: 1. Cl 2 O 7 2. FeO 3. N 2 O 4. SO 3 5. Cr 2 O 3 6. P 2 O 5 2. Indique la fórmula de los siguientes compuestos: 1. Trióxido de
Ejercicios Nomenclatura Inorgánica 1. De nombre a los siguientes compuestos: 1. Cl 2 O 7 2. FeO 3. N 2 O 4. SO 3 5. Cr 2 O 3 6. P 2 O 5 2. Indique la fórmula de los siguientes compuestos: 1. Trióxido de
DR 1900 V Uso Lab/Portátil. Colorímetros Portatiles. DR900 Pocket Colorímetro II
 ESPECTROFOTÓMETROS Y COLORIMETROS EQUIPOS PARA ANALISIS DE CALIDAD DE AGUA EN LABORATORIO Los espectrofotómetros y Colorímetros de HACH Company, son instrumentos diseñados para ofrecer la confiabilidad
ESPECTROFOTÓMETROS Y COLORIMETROS EQUIPOS PARA ANALISIS DE CALIDAD DE AGUA EN LABORATORIO Los espectrofotómetros y Colorímetros de HACH Company, son instrumentos diseñados para ofrecer la confiabilidad
Pozo Coodenadas Fecha de recolección Parametros de calidad de agua X Y Coliformes 100 ML 1 CN 232 356419 286438 17/07/1989 Totales Fecales 2400 2400
 X Y Coliformes 100 ML 1 CN 232 356419 286438 17/07/1989 Totales Fecales 2400 2400 Color verdadero Turbiedad Sólidos en suspención 0,17 ph 7,25 ph Saturación 7,3 Indice de saturación 0,05 Indice de estabilidad
X Y Coliformes 100 ML 1 CN 232 356419 286438 17/07/1989 Totales Fecales 2400 2400 Color verdadero Turbiedad Sólidos en suspención 0,17 ph 7,25 ph Saturación 7,3 Indice de saturación 0,05 Indice de estabilidad
FOTO 15. Mal estado de las componentes disueltos en el agua superficial y
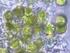 Los cuerpos de agua (ríos, lagos, lagunas, acuiferos, etc) que se constituyen como suministros naturales de agua no son puros en el sentido de que carecen de productos químicos disueltos como sucede con
Los cuerpos de agua (ríos, lagos, lagunas, acuiferos, etc) que se constituyen como suministros naturales de agua no son puros en el sentido de que carecen de productos químicos disueltos como sucede con
Félix Ripollés Pascual IPROMA Grupo de Trabajo de Inspección de Vertidos y Laboratorio. Comisión V de AEAS
 Félix Ripollés Pascual IPROMA fripolles@iproma.com Grupo de Trabajo de Inspección de Vertidos y Laboratorio. Comisión V de AEAS Evolución complejidad analítica 10-2 10-3 10-6 10-9 10-12 10-15 Sales disueltas
Félix Ripollés Pascual IPROMA fripolles@iproma.com Grupo de Trabajo de Inspección de Vertidos y Laboratorio. Comisión V de AEAS Evolución complejidad analítica 10-2 10-3 10-6 10-9 10-12 10-15 Sales disueltas
Uso eficiente del agua en la Minería
 Uso eficiente del agua en la Minería Taller Alemania : Soluciones para la Gestión del Agua en la Minería e Industria Richard L.A. Marohn Agenda 1. Introducción 2. Procesos Metalúrgicos 3. Uso del Agua
Uso eficiente del agua en la Minería Taller Alemania : Soluciones para la Gestión del Agua en la Minería e Industria Richard L.A. Marohn Agenda 1. Introducción 2. Procesos Metalúrgicos 3. Uso del Agua
Instructivo para la toma de muestra de Agua para Análisis Microbiológicos, Físico-químicos y Contaminantes
 1. ENVASES: Manual de Procedimientos LOG 001 Anexo 7 rev1 Instructivo para la toma de muestra de Agua para Análisis Microbiológicos, Físico-químicos y Contaminantes Precauciones generales: Todos los recipientes
1. ENVASES: Manual de Procedimientos LOG 001 Anexo 7 rev1 Instructivo para la toma de muestra de Agua para Análisis Microbiológicos, Físico-químicos y Contaminantes Precauciones generales: Todos los recipientes
INFORME DE ENSAYO Nº 101
 Página 1 de 11 INFORME DE ENSAYO Nº 101 1 ANTECEDENTES DEL CLIENTE Nombre : Manuel Durán Dirección : Av. Suecia Nº 3304, Ñuñoa. Santiago. Teléfono : 2741872 Proyecto : AES GENER Alto Maipo Número de solicitud
Página 1 de 11 INFORME DE ENSAYO Nº 101 1 ANTECEDENTES DEL CLIENTE Nombre : Manuel Durán Dirección : Av. Suecia Nº 3304, Ñuñoa. Santiago. Teléfono : 2741872 Proyecto : AES GENER Alto Maipo Número de solicitud
ANEXO I: Normativa para el análisis de muestras de suelo
 Anexo I: Normativa para el análisis de muestras de suelo ANEXO I: Normativa para el análisis de muestras de suelo IHOBE, S.A. 141 GUÍA METODOGÓGICA DE ANÁLISIS QUÍMICO 142 IHOBE, S.A. Anexo I: Normativa
Anexo I: Normativa para el análisis de muestras de suelo ANEXO I: Normativa para el análisis de muestras de suelo IHOBE, S.A. 141 GUÍA METODOGÓGICA DE ANÁLISIS QUÍMICO 142 IHOBE, S.A. Anexo I: Normativa
VÍDEOS EJERCICIOS OXIDACIÓN-REDUCCIÓN RESUELTOS: ENUNCIADOS
 VÍDEOS EJERCICIOS OXIDACIÓN-REDUCCIÓN RESUELTOS: ENUNCIADOS Ejercicio 1 Determinación del número de oxidación según las normas Determina el número de oxidación de los átomos de los siguientes compuestos:
VÍDEOS EJERCICIOS OXIDACIÓN-REDUCCIÓN RESUELTOS: ENUNCIADOS Ejercicio 1 Determinación del número de oxidación según las normas Determina el número de oxidación de los átomos de los siguientes compuestos:
Seminario de Química 2º Bachillerato LOGSE Unidad 0: Repaso Química 1º Bachillerato
 A) Composición Centesimal y Fórmulas químicas 1.- Determina la composición centesimal del Ca3(PO4)2. Datos: Masas atómicas (g/mol): Ca=40; P=31; O=16 S: Ca= 38,7%; P=20%; O=41,3% 2.- Determina la composición
A) Composición Centesimal y Fórmulas químicas 1.- Determina la composición centesimal del Ca3(PO4)2. Datos: Masas atómicas (g/mol): Ca=40; P=31; O=16 S: Ca= 38,7%; P=20%; O=41,3% 2.- Determina la composición
LE 751 Modificación 1
 ALCANCE DE LA ACREDITACION DE LA DIVISION QUIMICA Y ALIMENTOS DEL CENTRO DE ESTUDIOS, MEDICION Y CERTIFICACION DE CALIDAD, CESMEC S.A., SEDE IQUIQUE, COMO LABORATORIO DE ENSAYO AREA : FISICO-QUIMICA Y
ALCANCE DE LA ACREDITACION DE LA DIVISION QUIMICA Y ALIMENTOS DEL CENTRO DE ESTUDIOS, MEDICION Y CERTIFICACION DE CALIDAD, CESMEC S.A., SEDE IQUIQUE, COMO LABORATORIO DE ENSAYO AREA : FISICO-QUIMICA Y
3ºESO-A PROFESORA LUCÍA ROMERO
 PLAN DE REFUERZO ÁREA PENDIENTE DE CIENCIAS NATURALES 3ºESO-A PROFESORA LUCÍA ROMERO BIOLOGÍA Y GEOLOGÍA: Resumen de cada tema del libro y las siguientes actividades: PRIMER TRIMESTRE: - Tema 1: La salud
PLAN DE REFUERZO ÁREA PENDIENTE DE CIENCIAS NATURALES 3ºESO-A PROFESORA LUCÍA ROMERO BIOLOGÍA Y GEOLOGÍA: Resumen de cada tema del libro y las siguientes actividades: PRIMER TRIMESTRE: - Tema 1: La salud
FÍSICA Y QUÍMICA cuaderno de ejercicios
 FÍSICA Y QUÍMICA cuaderno de ejercicios FORMULACIÓN y nomenclatura 1.** Determinen si las siguientes afirmaciones se refieren a metales o a no metales. 1.1. Presentan un brillo característico. 1.2. Los
FÍSICA Y QUÍMICA cuaderno de ejercicios FORMULACIÓN y nomenclatura 1.** Determinen si las siguientes afirmaciones se refieren a metales o a no metales. 1.1. Presentan un brillo característico. 1.2. Los
Materiales recopilados por la Ponencia Provincial de Química para Selectividad TEMA 1: QUÍMICA DESCRIPTIVA EJERCICIOS DE SELECTIVIDAD 96/97
 TEMA 1: QUÍMICA DESCRIPTIVA EJERCICIOS DE SELECTIVIDAD 96/97 1. De un recipiente que contiene 32 g de metano, se extraen 9 10 23 moléculas. a) Los moles de metano que quedan. b) Las moléculas de metano
TEMA 1: QUÍMICA DESCRIPTIVA EJERCICIOS DE SELECTIVIDAD 96/97 1. De un recipiente que contiene 32 g de metano, se extraen 9 10 23 moléculas. a) Los moles de metano que quedan. b) Las moléculas de metano
Números de Oxidación
 Iones Una buena proporción de toda la actividad química implica la transferencia de electrones entre elementos. Cuando un átomo gana o pierde un electrón se convierte en un ión. Un ión es un átomo o conjunto
Iones Una buena proporción de toda la actividad química implica la transferencia de electrones entre elementos. Cuando un átomo gana o pierde un electrón se convierte en un ión. Un ión es un átomo o conjunto
Nombre del no metal- uro de metal. Nombres de los aniones monoatómicos derivados de no metales
 NOMENCLATURA DE COMPUESTOS QUÍMICOS Compuestos binarios de un metal con un no metal Un compuesto binario está formado por átomos de dos elementos diferentes. Cuando uno es un metal y el otro un no metal,
NOMENCLATURA DE COMPUESTOS QUÍMICOS Compuestos binarios de un metal con un no metal Un compuesto binario está formado por átomos de dos elementos diferentes. Cuando uno es un metal y el otro un no metal,
REACCIONES DE TRANSFERENCIA DE ELECTRONES, AJUSTE Y ESTEQUIOMETRÍA. 1-Nombra tres sustancias que sean oxidantes enérgicos Por qué?
 REACCIONES DE TRANSFERENCIA DE ELECTRONES, AJUSTE Y ESTEQUIOMETRÍA 1-Nombra tres sustancias que sean oxidantes enérgicos Por qué? 2- Nombra tres cuerpos que sean fuertes reductores por qué? 3- Qué se entiende
REACCIONES DE TRANSFERENCIA DE ELECTRONES, AJUSTE Y ESTEQUIOMETRÍA 1-Nombra tres sustancias que sean oxidantes enérgicos Por qué? 2- Nombra tres cuerpos que sean fuertes reductores por qué? 3- Qué se entiende
Materia: FÍSICA Y QUÍMICA Curso
 ACTIVIDADES DE REFUERZO FÍSICA Y QUÍMICA 3º ESO. JUNIO 2015. 1.- Realizar las configuraciones electrónicas de todos los elementos de los tres primeros periodos de la tabla periódica. 2.- Razonar cuales
ACTIVIDADES DE REFUERZO FÍSICA Y QUÍMICA 3º ESO. JUNIO 2015. 1.- Realizar las configuraciones electrónicas de todos los elementos de los tres primeros periodos de la tabla periódica. 2.- Razonar cuales
El laboratorio de la Agencia
 El laboratorio de la Agencia Métodos generales Métodos para el establecimiento del Canon del agua Enero 2010 Introducción La inspección y el control de la calidad generan una gran demanda de ensayos analíticos.
El laboratorio de la Agencia Métodos generales Métodos para el establecimiento del Canon del agua Enero 2010 Introducción La inspección y el control de la calidad generan una gran demanda de ensayos analíticos.
TEMA I: REACCIONES Y ESTEQUIOMETRIA
 TEMA I: REACCIONES Y ESTEQUIOMETRIA 1. De un recipiente que contiene 32 g de metano, se extraen 9 10 23 moléculas. a) Los moles de metano que quedan. b) Las moléculas de metano que quedan. c) Los gramos
TEMA I: REACCIONES Y ESTEQUIOMETRIA 1. De un recipiente que contiene 32 g de metano, se extraen 9 10 23 moléculas. a) Los moles de metano que quedan. b) Las moléculas de metano que quedan. c) Los gramos
Química de Aguas Aquacheck Formulario de Solicitud del Programa Aquacheck
 Química de Aguas Aquacheck 2016-2017 Formulario de Solicitud del Programa Aquacheck Puede consultar el calendario de las rondas para el año 2016-2017. Por favor complete las secciones del formulario de
Química de Aguas Aquacheck 2016-2017 Formulario de Solicitud del Programa Aquacheck Puede consultar el calendario de las rondas para el año 2016-2017. Por favor complete las secciones del formulario de
INFORME DE MONITOREO DE CALIDAD DE EFLUENTES Y CUERPO RECEPTOR CENTRAL ILO 1 ENERSUR S.A
 INFORME DE MONITOREO DE CALIDAD DE EFLUENTES Y CUERPO RECEPTOR CENTRAL ILO 1 ENERSUR S.A PREPARADO POR: CORPORACION DE LABORATORIOS AMBIENTALES DEL PERU S.A.C. SETIEMBRE 2012 1 I. INDICE I. INDICE... 2
INFORME DE MONITOREO DE CALIDAD DE EFLUENTES Y CUERPO RECEPTOR CENTRAL ILO 1 ENERSUR S.A PREPARADO POR: CORPORACION DE LABORATORIOS AMBIENTALES DEL PERU S.A.C. SETIEMBRE 2012 1 I. INDICE I. INDICE... 2
TRANSFERENCIA DE ELECTRONES AJUSTE DE REACCIONES REDOX
 TRANSFERENCIA DE ELECTRONES AJUSTE DE REACCIONES REDOX E1A.S2012 El dióxido de manganeso reacciona en medio hidróxido potásico con clorato de potasio para dar permanganato de potasio, cloruro de potasio
TRANSFERENCIA DE ELECTRONES AJUSTE DE REACCIONES REDOX E1A.S2012 El dióxido de manganeso reacciona en medio hidróxido potásico con clorato de potasio para dar permanganato de potasio, cloruro de potasio
DIRECCIÓN DE DIAGNÓSTICO VEGETAL LABORATORIO DE CONTROL DE SUELOS, FOLIARES Y AGUAS (SUELOS)
 DIRECCIÓN DE DIAGNÓSTICO VEGETAL LABORATORIO DE CONTROL DE SUELOS, FOLIARES Y AGUAS (SUELOS) TIPO DE ANÁLISIS TÉCNICA Paquete 1 Paquete 2 ph Materia orgánica Nitrógeno (N) Fósforo (P) Potasio (K) ph Materia
DIRECCIÓN DE DIAGNÓSTICO VEGETAL LABORATORIO DE CONTROL DE SUELOS, FOLIARES Y AGUAS (SUELOS) TIPO DE ANÁLISIS TÉCNICA Paquete 1 Paquete 2 ph Materia orgánica Nitrógeno (N) Fósforo (P) Potasio (K) ph Materia
CROMATOGRAFÍA IÓNICA Aplicaciones
 CROMATOGRAFÍA IÓNICA Aplicaciones chloride NO 3-12 11 10 9 8 7 6 5 4 3 2 1 Conductivity [µs/cm] nitrite phophate fluoride bromide nitrate sulphate 0 0 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 time [min]
CROMATOGRAFÍA IÓNICA Aplicaciones chloride NO 3-12 11 10 9 8 7 6 5 4 3 2 1 Conductivity [µs/cm] nitrite phophate fluoride bromide nitrate sulphate 0 0 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 time [min]
REACCIONES DE TRANSFERENCIA DE ELECTRONES 2ºBACH
 1. Ajusta las siguientes reacciones redox, utilizando el método del ion electrón: a) HNO 3 + Cu Cu(NO 3 ) 2 + NO 2 + H 2 O b) K 2 Cr 2 O 7 +HI + HClO 4 Cr(ClO 4 ) 3 +I 2 +KClO 4 + H 2 O c) H 2 SO 4 + HI
1. Ajusta las siguientes reacciones redox, utilizando el método del ion electrón: a) HNO 3 + Cu Cu(NO 3 ) 2 + NO 2 + H 2 O b) K 2 Cr 2 O 7 +HI + HClO 4 Cr(ClO 4 ) 3 +I 2 +KClO 4 + H 2 O c) H 2 SO 4 + HI
5) En 20 g de Ni 2 (CO 3 ) 3 : a) Cuántos moles hay de dicha sal? b) Cuántos átomos hay de oxígeno? c) Cuántos moles hay de iones carbonato?
 QUÍMICA 2º BACH. SELECTIVIDAD: MOL-N A 1) Para un mol de agua, justifique la veracidad o falsedad de las siguientes afirmaciones: a) En condiciones normales de presión y temperatura, ocupa un volumen de
QUÍMICA 2º BACH. SELECTIVIDAD: MOL-N A 1) Para un mol de agua, justifique la veracidad o falsedad de las siguientes afirmaciones: a) En condiciones normales de presión y temperatura, ocupa un volumen de
Registro de Laboratorios de Análisis Ambientales
 Registro de Laboratorios de Análisis Ambientales Laboratorio Ambiental Diciembre, 2009 Laboratorio Ambiental - 2007Laboratorio Ambiental 1 - Objetivos: Establecer requisitos y criterios que los laboratorios
Registro de Laboratorios de Análisis Ambientales Laboratorio Ambiental Diciembre, 2009 Laboratorio Ambiental - 2007Laboratorio Ambiental 1 - Objetivos: Establecer requisitos y criterios que los laboratorios
5) Cuando un metal y un no metal reaccionan el tiende a perder electrones y el tiende a ganar electrones.
 Enlaces y compuestos iónicos. Opción Múltiple. Revisión PSI Química Nombre Electrones de valencia Aniones y Cationes 1) Los Metales tienden a electrones y no metales tienden a electrones. A) ganar, ganar
Enlaces y compuestos iónicos. Opción Múltiple. Revisión PSI Química Nombre Electrones de valencia Aniones y Cationes 1) Los Metales tienden a electrones y no metales tienden a electrones. A) ganar, ganar
Compuestos Químicos. Capítulo 3 Sec. 3.1-3.6 Rosamil Rey, PhD CHEM 2115
 Compuestos Químicos Capítulo 3 Sec. 3.1-3.6 Rosamil Rey, PhD CHEM 2115 Tipos de enlaces Enlaces covalentes comparten electrones entre átomos y forman compuestos moleculares. Estos compuestos son representados
Compuestos Químicos Capítulo 3 Sec. 3.1-3.6 Rosamil Rey, PhD CHEM 2115 Tipos de enlaces Enlaces covalentes comparten electrones entre átomos y forman compuestos moleculares. Estos compuestos son representados
Resumen del Informe del Comité Científico de la CARU
 Resumen del Informe del Comité Científico de la CARU El 26 de octubre de 2016, el Comité Científico hizo entrega a la CARU de un informe con los resultados de análisis de laboratorio y mediciones de campo
Resumen del Informe del Comité Científico de la CARU El 26 de octubre de 2016, el Comité Científico hizo entrega a la CARU de un informe con los resultados de análisis de laboratorio y mediciones de campo
QUÍMICA 2º BACHILLERATO
 REACCIONES DE TRANSFERENCIA DE ELECTRONES: Y ESTEQUIOMETRÍA 1.-/ Iguale por el método del ion-electrón la ecuación: Cu + HNO 3 Cu(NO 3 ) 2 + NO + H 2 O, correspondiente a la reacción del cobre con el ácido
REACCIONES DE TRANSFERENCIA DE ELECTRONES: Y ESTEQUIOMETRÍA 1.-/ Iguale por el método del ion-electrón la ecuación: Cu + HNO 3 Cu(NO 3 ) 2 + NO + H 2 O, correspondiente a la reacción del cobre con el ácido
Análisis Cualitativo de Muestras Sólidas
 Facultad de Ciencias - Escuela de Química LABORATORIO DE QUIMICA ANALITICA Análisis Cualitativo de Muestras Sólidas Basado en el original publicado en: Semimicro Qualitative Analysis. Franck Welcher and
Facultad de Ciencias - Escuela de Química LABORATORIO DE QUIMICA ANALITICA Análisis Cualitativo de Muestras Sólidas Basado en el original publicado en: Semimicro Qualitative Analysis. Franck Welcher and
TEMA 0: QUÍMICA DESCRIPTIVA EJERCICIOS DE SELECTIVIDAD 96/97
 TEMA 0: QUÍMICA DESCRIPTIVA EJERCICIOS DE SELECTIVIDAD 96/97 1. De un recipiente que contiene 32 g de metano, se extraen 9 10 23 moléculas. Calcule: a) Los moles de metano que quedan. b) Las moléculas
TEMA 0: QUÍMICA DESCRIPTIVA EJERCICIOS DE SELECTIVIDAD 96/97 1. De un recipiente que contiene 32 g de metano, se extraen 9 10 23 moléculas. Calcule: a) Los moles de metano que quedan. b) Las moléculas
CLASE Nº 2 ESTEQUIOMETRÍA
 UNIVERSIDAD NACIONAL EXPERIMENTAL POLITECNICA ANTONIO JOSÉ DE SUCRE VICERRECTORADO BARQUISIMETO DEPARTAMENTO DE INGENIERÍA QUÍMICA QUÍMICA GENERAL CLASE Nº 2 ESTEQUIOMETRÍA 1 Estequiometría Leyes que rigen
UNIVERSIDAD NACIONAL EXPERIMENTAL POLITECNICA ANTONIO JOSÉ DE SUCRE VICERRECTORADO BARQUISIMETO DEPARTAMENTO DE INGENIERÍA QUÍMICA QUÍMICA GENERAL CLASE Nº 2 ESTEQUIOMETRÍA 1 Estequiometría Leyes que rigen
IES Atenea (S.S. de los Reyes) Departamento de Física y Química. PAU Química. Septiembre Fase específica OPCIÓN A
 1 PAU Química. Septiembre 2010. Fase específica OPCIÓN A Cuestión 1A. Considere las sustancias: cloruro de potasio, agua, cloro y sodio. a) Indique el tipo de enlace que presenta cada una de ellas. b)
1 PAU Química. Septiembre 2010. Fase específica OPCIÓN A Cuestión 1A. Considere las sustancias: cloruro de potasio, agua, cloro y sodio. a) Indique el tipo de enlace que presenta cada una de ellas. b)
Acuerdo 286. Química. Disoluciones. Recopiló: M.C. Macaria Hernández Chávez
 Acuerdo 286 Química Disoluciones Recopiló: M.C. Macaria Hernández Chávez Disolución: Es una mezcla homogénea de dos o más sustancias. La sustancia que se encuentra en mayor proporción se llama disolvente
Acuerdo 286 Química Disoluciones Recopiló: M.C. Macaria Hernández Chávez Disolución: Es una mezcla homogénea de dos o más sustancias. La sustancia que se encuentra en mayor proporción se llama disolvente
INFORME PARCIAL DE ENSAYO Nº /02
 INFORME PARCIAL DE ENSAYO Nº 1023652/02 mbre del solicitante: BOTNIA S.A Dirección: CEBOLLATI 1474 (PLANTA BAJA) ENTREGAR FACT. ZABALA 1377 Número de muestra (LATU): 355753 ANÁLISIS MICROBIOLÓGICOS Extracción
INFORME PARCIAL DE ENSAYO Nº 1023652/02 mbre del solicitante: BOTNIA S.A Dirección: CEBOLLATI 1474 (PLANTA BAJA) ENTREGAR FACT. ZABALA 1377 Número de muestra (LATU): 355753 ANÁLISIS MICROBIOLÓGICOS Extracción
EVALUACIÓN DE LA CALIDAD DEL AGUA EN LA ZONA COSTERA DE IXTAPA-ZIHUATANEJO
 UNIVERSIDAD AUTÓNOMA DE QUERÉTARO Centro de Estudios Académicos sobre Contaminación Ambiental FACULTAD DE QUÍMICA Laboratorio de Ciencias Ambientales EVALUACIÓN DE LA CALIDAD DEL AGUA EN LA ZONA COSTERA
UNIVERSIDAD AUTÓNOMA DE QUERÉTARO Centro de Estudios Académicos sobre Contaminación Ambiental FACULTAD DE QUÍMICA Laboratorio de Ciencias Ambientales EVALUACIÓN DE LA CALIDAD DEL AGUA EN LA ZONA COSTERA
Masas atómicas (g/mol): O = 16; S = 32; Zn = 65,4. Sol: a) 847 L; b) 710,9 g; c) 1,01 atm.
 1) Dada la siguiente reacción química: 2 AgNO3 + Cl2 N2O5 + 2 AgCl + ½ O2. a) Calcule los moles de N2O5 que se obtienen a partir de 20 g de AgNO3. b) Calcule el volumen de O2 obtenido, medido a 20 ºC y
1) Dada la siguiente reacción química: 2 AgNO3 + Cl2 N2O5 + 2 AgCl + ½ O2. a) Calcule los moles de N2O5 que se obtienen a partir de 20 g de AgNO3. b) Calcule el volumen de O2 obtenido, medido a 20 ºC y
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2002 QUÍMICA TEMA 7: REACCIONES REDOX
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 00 QUÍMICA TEMA 7: REACCIONES REDOX Junio, Ejercicio, Opción B Reserva 1, Ejercicio 6, Opción B Reserva, Ejercicio 5, Opción A Reserva, Ejercicio 5, Opción A
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 00 QUÍMICA TEMA 7: REACCIONES REDOX Junio, Ejercicio, Opción B Reserva 1, Ejercicio 6, Opción B Reserva, Ejercicio 5, Opción A Reserva, Ejercicio 5, Opción A
EJERCICIOS DE DISOLUCIONES Y ESTEQUIOMETRÍA
 EJERCICIOS DE DISOLUCIONES Y ESTEQUIOMETRÍA REACCIONES: 1. La descomposición térmica del carbonato de calcio produce óxido de calcio y dióxido de carbono gas. Qué volumen de dióxido de carbono, medido
EJERCICIOS DE DISOLUCIONES Y ESTEQUIOMETRÍA REACCIONES: 1. La descomposición térmica del carbonato de calcio produce óxido de calcio y dióxido de carbono gas. Qué volumen de dióxido de carbono, medido
CURSO DE AGUAS SUBTERRANEAS TEMA 13: LA CALIDAD DEL AGUA SUBTERRÁNEA
 CURSO DE AGUAS SUBTERRANEAS 2010 TEMA 13: LA CALIDAD DEL AGUA SUBTERRÁNEA Mario Valencia Cuesta Geólogo AGUAS SUBTERRÁNEAS LTDA. aguassubterraneas@gmail.com INTRODUCCION A LAS AGUAS SUBTERRANEAS 2010 TEMA
CURSO DE AGUAS SUBTERRANEAS 2010 TEMA 13: LA CALIDAD DEL AGUA SUBTERRÁNEA Mario Valencia Cuesta Geólogo AGUAS SUBTERRÁNEAS LTDA. aguassubterraneas@gmail.com INTRODUCCION A LAS AGUAS SUBTERRANEAS 2010 TEMA
Compuesto N. Stock N. tradicional N. sistemática. óxido de hierro (III) óxido férrico trióxido de dihierro
 Ejemplos de óxidos básicos FeO Fe 2 O 3 Cu 2 O CuO CaO PbO 2 óxido de hierro (II) óxido ferroso monóxido de hierro óxido de hierro (III) óxido férrico trióxido de dihierro óxido de cobre (I) óxido cuproso
Ejemplos de óxidos básicos FeO Fe 2 O 3 Cu 2 O CuO CaO PbO 2 óxido de hierro (II) óxido ferroso monóxido de hierro óxido de hierro (III) óxido férrico trióxido de dihierro óxido de cobre (I) óxido cuproso
Calcio(2+) Hierro(3+)
 CATIONES MONOATÓMICOS MONOATÓMICOS La carga se indica con un superíndice a la derecha del símbolo del elemento seguido del signo + Ca + Fe 3+ La carga se indica con un superíndice a la derecha seguido
CATIONES MONOATÓMICOS MONOATÓMICOS La carga se indica con un superíndice a la derecha del símbolo del elemento seguido del signo + Ca + Fe 3+ La carga se indica con un superíndice a la derecha seguido
PROBLEMAS DE ESTEQUIOMETRÍA DE 1º DE BACHILLERATO
 PROBLEMAS DE ESTEQUIOMETRÍA DE 1º DE BACHILLERATO COLECCIÓN PRIMERA. 1. La descomposición térmica del carbonato de calcio produce óxido de calcio y dióxido de carbono gas. Qué volumen de dióxido de carbono,
PROBLEMAS DE ESTEQUIOMETRÍA DE 1º DE BACHILLERATO COLECCIÓN PRIMERA. 1. La descomposición térmica del carbonato de calcio produce óxido de calcio y dióxido de carbono gas. Qué volumen de dióxido de carbono,
Por qué analizar agua para consumo?
 Por qué analizar agua para consumo? El agua es un alimento esencial en la vida de las personas. Según la Organización Mundial de la Salud (OMS), el agua para consumo inocua o agua potable se define como
Por qué analizar agua para consumo? El agua es un alimento esencial en la vida de las personas. Según la Organización Mundial de la Salud (OMS), el agua para consumo inocua o agua potable se define como
Universidad de Cantabria. Contaminación del agua
 Universidad de Cantabria Contaminación del agua Necesidades y calidad del agua» Biológica» Doméstica» Industrial» Agrícola» Recreativa Cantidad mínima diaria: 50 litros / persona Cantidad mínima recomendada:
Universidad de Cantabria Contaminación del agua Necesidades y calidad del agua» Biológica» Doméstica» Industrial» Agrícola» Recreativa Cantidad mínima diaria: 50 litros / persona Cantidad mínima recomendada:
Colegio Superior de Señoritas Tema: Formación de Compuestos Químicos Septiembre 2010 Prof.: NVM 8vo Nivel Departamento de Ciencias
 COMPUESTOS QUÍMICOS Y SU CLASIFICACIÓN El número de oxidación: representa la cantidad de electrones que puede ganar o perder un elemento. El hidrógeno tiene número de oxidación +1 y puede perder un electrón;
COMPUESTOS QUÍMICOS Y SU CLASIFICACIÓN El número de oxidación: representa la cantidad de electrones que puede ganar o perder un elemento. El hidrógeno tiene número de oxidación +1 y puede perder un electrón;
8 - COLOMBIA PBX: (1) 2486777 FAX: (1) 3125008 CELULAR:
 Tarifas Servicio de diagnóstico ambiental convenio Asociación Colombiana de Porcicultores-FNP (Asoporcicultores- FNP) y Corporación Autónoma Regional de las Cuencas de los Ríos Negro y Nare- Cornare Con
Tarifas Servicio de diagnóstico ambiental convenio Asociación Colombiana de Porcicultores-FNP (Asoporcicultores- FNP) y Corporación Autónoma Regional de las Cuencas de los Ríos Negro y Nare- Cornare Con
Seminarios de Química 1
 Seminarios de Química 1 Transformaciones Químicas Primera parte: Estequiometría Conceptos importantes Ley de servación de la masa en reacciones químicas. Representación de las reacciones químicas mediante
Seminarios de Química 1 Transformaciones Químicas Primera parte: Estequiometría Conceptos importantes Ley de servación de la masa en reacciones químicas. Representación de las reacciones químicas mediante
QUÍMICA - 2º DE BACHILLERATO EJERCICIOS DE SELECTIVIDAD UNIDAD 6: ÁCIDO - BASE CUESTIONES 1
 CUESTIONES 1 HOJA 6-1 2003 modelo: Conocidos los ácidos HA (K a =3,6.10-6 ), HB (K a =2,5.10-3 ) y HC (K a =1,2.10-12 ) a) Cuál es el ácido más débil. b) Cuál es el que posee la base conjugada más débil.
CUESTIONES 1 HOJA 6-1 2003 modelo: Conocidos los ácidos HA (K a =3,6.10-6 ), HB (K a =2,5.10-3 ) y HC (K a =1,2.10-12 ) a) Cuál es el ácido más débil. b) Cuál es el que posee la base conjugada más débil.
CIIA CENTRO DE INVESTIGACIÓN Y DESARROLLO DE INGENIERÍA AMBIENTAL. Misión. Campos de Acción. Disponibilidades
 CIIA CENTRO DE INVESTIGACIÓN Y DESARROLLO DE INGENIERÍA AMBIENTAL Misión Investigar, desarrollar, producir y comercializar servicios relativos a la preservación y control de los recursos naturales y a
CIIA CENTRO DE INVESTIGACIÓN Y DESARROLLO DE INGENIERÍA AMBIENTAL Misión Investigar, desarrollar, producir y comercializar servicios relativos a la preservación y control de los recursos naturales y a
Tema 7: Medidas de contaminación atmosférica I
 Tema 7: Medidas de contaminación atmosférica I 7.1 Muestreo y análisis 7.2 Muestreo y análisis de partículas 7.3 Análisis de metales en partículas 7.4 Análisis de materia orgánica en partículas 7.1 Muestreo
Tema 7: Medidas de contaminación atmosférica I 7.1 Muestreo y análisis 7.2 Muestreo y análisis de partículas 7.3 Análisis de metales en partículas 7.4 Análisis de materia orgánica en partículas 7.1 Muestreo
FORMULACIÓN QUÍMICA INORGÁNICA
 FORMULACIÓN QUÍMICA INORGÁNICA 1. VALENCIAS DE LOS ELEMENTOS QUÍMICOS MÁS CONOCIDOS Se entiende que las valencias con signo negativo se dan frente a elementos electropositivos y las valencias con signo
FORMULACIÓN QUÍMICA INORGÁNICA 1. VALENCIAS DE LOS ELEMENTOS QUÍMICOS MÁS CONOCIDOS Se entiende que las valencias con signo negativo se dan frente a elementos electropositivos y las valencias con signo
PROCESOS ENERGÉTICOS
 PROCESOS ENERGÉTICOS Tubería de salida del vapor vapor Nivel del agua Tubos de humo TUBO DE FUEGO Lodos Purga Tubería de entrada de agua de alimentación CIRCULACIÓN DE AGUA EN UNA CALDERA DE TUBOS DE
PROCESOS ENERGÉTICOS Tubería de salida del vapor vapor Nivel del agua Tubos de humo TUBO DE FUEGO Lodos Purga Tubería de entrada de agua de alimentación CIRCULACIÓN DE AGUA EN UNA CALDERA DE TUBOS DE
repercusiones respuestas sobre los organismos NORMAS DE CALIDAD FIJAR LÍMITES Análisis de aguas
 Normas de calidad de las aguas Legislación Sistemas de muestreo y conservación de la muestra Determinación de parámetros globales de calidad Determinación de nutrientes principales en aguas naturales Criterios
Normas de calidad de las aguas Legislación Sistemas de muestreo y conservación de la muestra Determinación de parámetros globales de calidad Determinación de nutrientes principales en aguas naturales Criterios
Universidad de San Carlos de Guatemala Facultad de Agronomia Computo I CALIDAD DE AGUA SUPERFICIAL EN LATINOAMERICA
 Universidad de San Carlos de Guatemala Facultad de Agronomia Computo I CALIDAD DE AGUA SUPERFICIAL EN LATINOAMERICA Cinthia Claudette Hurtado Moreno Carnet: 199811467 Guatemala, 30 de abril de 2013 TABLA
Universidad de San Carlos de Guatemala Facultad de Agronomia Computo I CALIDAD DE AGUA SUPERFICIAL EN LATINOAMERICA Cinthia Claudette Hurtado Moreno Carnet: 199811467 Guatemala, 30 de abril de 2013 TABLA
EJERCICIOS DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA 4º ESO
 EJERCICIOS DE FORMULACIÓN Y DE QUÍMICA INORGÁNICA 4º ESO 1 COMPUESTOS BINARIOS 1.1 CON OXÍGENO 1.1.1 Y UN METAL (ÓXIDOS) 1 BaO Monóxido de bario Óxido de bario 2 Na 2 O Monóxido de disodio Óxido de sodio
EJERCICIOS DE FORMULACIÓN Y DE QUÍMICA INORGÁNICA 4º ESO 1 COMPUESTOS BINARIOS 1.1 CON OXÍGENO 1.1.1 Y UN METAL (ÓXIDOS) 1 BaO Monóxido de bario Óxido de bario 2 Na 2 O Monóxido de disodio Óxido de sodio
Formulación de Química Inorgánica
 Formulación de Química Inorgánica F. G. Calvo-Flores 1. VALENCIA. Es la capacidad que tiene un átomo de un elemento para combinarse con los átomos de otros elementos y formar compuestos. La valencia es
Formulación de Química Inorgánica F. G. Calvo-Flores 1. VALENCIA. Es la capacidad que tiene un átomo de un elemento para combinarse con los átomos de otros elementos y formar compuestos. La valencia es
DISOLUCIÓN Y PRECIPITACIÓN DE SALES CAPITULO V. 5.1. Solubilidad 5.2. Disolución de compuestos poco solubles. 5.3. Precipitación Fraccionada
 CAPITULO V DISOLUCIÓN Y PRECIPITACIÓN DE SALES 5.1. Solubilidad 5.2. Disolución de compuestos poco solubles. 5.3. Precipitación Fraccionada El fenómeno de precipitación, así como el de disolución de precipitados
CAPITULO V DISOLUCIÓN Y PRECIPITACIÓN DE SALES 5.1. Solubilidad 5.2. Disolución de compuestos poco solubles. 5.3. Precipitación Fraccionada El fenómeno de precipitación, así como el de disolución de precipitados
ESTEQUIOMETRÍA. cobre(ii) y se descompone, cuántas moles de dióxido de nitrógeno se formarán? A moles B moles C moles D. 0.
 ESTEQUIOMETRÍA 1 Al calentarse fuertemente, el nitrato de cobre(ii) se descompone en óxido de cobre(ii), dióxido de nitrógeno y oxígeno elemental (O 2 ). Si calentamos 0.10 moles de nitrato de cobre(ii)
ESTEQUIOMETRÍA 1 Al calentarse fuertemente, el nitrato de cobre(ii) se descompone en óxido de cobre(ii), dióxido de nitrógeno y oxígeno elemental (O 2 ). Si calentamos 0.10 moles de nitrato de cobre(ii)
Anexo G-4. Estándares de Calidad Ambiental para Agua (ECA)
 Anexo G-4 Estándares de Calidad Ambiental para Agua (ECA) ESTÁNDARES DE CALIDAD AMBIENTAL DE AGUA MINISTERIO DEL AMBIENTE PARÁMETRO ESTÁNDARES NACIONALES DE CALIDAD AMBIENTAL PARA AGUA D.S. Nº 002-2008-MINAM
Anexo G-4 Estándares de Calidad Ambiental para Agua (ECA) ESTÁNDARES DE CALIDAD AMBIENTAL DE AGUA MINISTERIO DEL AMBIENTE PARÁMETRO ESTÁNDARES NACIONALES DE CALIDAD AMBIENTAL PARA AGUA D.S. Nº 002-2008-MINAM
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2008 QUÍMICA TEMA 1: LA TRANSFORMACIÓN QUÍMICA
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2008 QUÍMICA TEMA 1: LA TRANSFORMACIÓN QUÍMICA Junio, Ejercicio 2, Opción B Junio, Ejercicio 5, Opción B Reserva 1, Ejercicio 5, Opción A Reserva 1, Ejercicio
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2008 QUÍMICA TEMA 1: LA TRANSFORMACIÓN QUÍMICA Junio, Ejercicio 2, Opción B Junio, Ejercicio 5, Opción B Reserva 1, Ejercicio 5, Opción A Reserva 1, Ejercicio
5. Cuánto pesan 1,025 moles de amoníaco más 6, átomos de plata? Expresa el resultado en gramos. Dato: 1 u = 1, g Sol: 125,295 g
 EJERCICIOS DE REPASO 2º BACH CANTIDADES EN QUÍMICA 1. La masa atómica de la plata que encontramos en las tablas es de 107,87 u. Determina la abundancia relativa de los dos isótopos que tiene, sabiendo
EJERCICIOS DE REPASO 2º BACH CANTIDADES EN QUÍMICA 1. La masa atómica de la plata que encontramos en las tablas es de 107,87 u. Determina la abundancia relativa de los dos isótopos que tiene, sabiendo
Ambos servicios se realizarán de acuerdo a normas internacionales consensuadas por la C.T.N. que figuran en sus respectivos Anexos.
 CONVOCATORIA PARA PRESENTAR MANIFESTACIONES DE INTERÉS PARA LA PRESTACIÓN DE SERVICIOS DE TOMA Y ANÁLISIS DE MUESTRAS DE AGUAS DE LA CUENCA DEL RÍO PILCOMAYO Resumen: Servicios de toma de muestras y análisis
CONVOCATORIA PARA PRESENTAR MANIFESTACIONES DE INTERÉS PARA LA PRESTACIÓN DE SERVICIOS DE TOMA Y ANÁLISIS DE MUESTRAS DE AGUAS DE LA CUENCA DEL RÍO PILCOMAYO Resumen: Servicios de toma de muestras y análisis
TRANSFORMACIONES QUÍMICAS. ESTEQUIOMETRÍA.
 Tema 3 Estequiometría 1 TEMA 3. TRANSFORMACIONES QUÍMICAS. ESTEQUIOMETRÍA. 2. LAS REACCIONES QUÍMICAS. 1.- Señala justificándolas, las respuestas correctas: Se produce un cambio químico: a) Cuando las
Tema 3 Estequiometría 1 TEMA 3. TRANSFORMACIONES QUÍMICAS. ESTEQUIOMETRÍA. 2. LAS REACCIONES QUÍMICAS. 1.- Señala justificándolas, las respuestas correctas: Se produce un cambio químico: a) Cuando las
LABORATORIO BROMATOLOGICO. Análisis fisicoquímico de agua
 2003 - CISMA S.A. [Centro de Investigación de Salud y Medio Ambiente] LABORATORIO BROMATOLOGICO Análisis fisicoquímico de agua Propiedades organolépticas: color, olor, turbiedad Amoníaco Nitritos Dureza
2003 - CISMA S.A. [Centro de Investigación de Salud y Medio Ambiente] LABORATORIO BROMATOLOGICO Análisis fisicoquímico de agua Propiedades organolépticas: color, olor, turbiedad Amoníaco Nitritos Dureza
PRACTICA N 12 ANÁLISIS FISICO Y QUÍMICO DEL AGUA UTILIZADA EN LAS INDUSTRIAS DE ALIMENTOS
 PRACTICA N 12 ANÁLISIS FISICO Y QUÍMICO DEL AGUA UTILIZADA EN LAS INDUSTRIAS DE ALIMENTOS I. INTRODUCCIÓN: Es universalmente reconocido el principio del que el agua de consumo debe estar libre de microorganismos
PRACTICA N 12 ANÁLISIS FISICO Y QUÍMICO DEL AGUA UTILIZADA EN LAS INDUSTRIAS DE ALIMENTOS I. INTRODUCCIÓN: Es universalmente reconocido el principio del que el agua de consumo debe estar libre de microorganismos
ANÁLISIS DE AGUAS INTRODUCCIÓN A LOS ANÁLISIS DE AGUAS. MEDICIONES DE : DUREZA CLORURO ACIDEZ-pH OXÍGENO DISUELTO CONDUCTIVIDAD
 ANÁLISIS DE AGUAS INTRODUCCIÓN A LOS ANÁLISIS DE AGUAS. MEDICIONES DE : DUREZA CLORURO ACIDEZ-pH OXÍGENO DISUELTO CONDUCTIVIDAD Instalación de tratamiento de agua y caldera. ANÁLISIS DE AGUAS El agua químicamente
ANÁLISIS DE AGUAS INTRODUCCIÓN A LOS ANÁLISIS DE AGUAS. MEDICIONES DE : DUREZA CLORURO ACIDEZ-pH OXÍGENO DISUELTO CONDUCTIVIDAD Instalación de tratamiento de agua y caldera. ANÁLISIS DE AGUAS El agua químicamente
1 EJERCICIOS (Nomenclatura de Compuestos inorgánicos)
 1 EJERCICIOS (Nomenclatura de Compuestos inorgánicos) HCl Bromato de bario H 2 Te Hidróxido de manganeso (II) Yoduro de cobre (II) Ayala MnO 2 NO Hidruro de bario Óxido de férrico FeCl 3 Zn(OH) 2 Sulfato
1 EJERCICIOS (Nomenclatura de Compuestos inorgánicos) HCl Bromato de bario H 2 Te Hidróxido de manganeso (II) Yoduro de cobre (II) Ayala MnO 2 NO Hidruro de bario Óxido de férrico FeCl 3 Zn(OH) 2 Sulfato
0,225. 0, ,15 0,92
 1.- El ácido clorhídrico reacciona con el mármol (carbonato de calcio) formando cloruro de calcio, dióxido de carbono gas y agua. a) Escribe y ajusta la reacción química. (0,5 p) b) Halla el volumen de
1.- El ácido clorhídrico reacciona con el mármol (carbonato de calcio) formando cloruro de calcio, dióxido de carbono gas y agua. a) Escribe y ajusta la reacción química. (0,5 p) b) Halla el volumen de
CAPITULO II REVISIÓN DE LITERATURA
 CAPITULO I 1. INTRODUCCIÓN... 1 1.1 EL PROBLEMA... 2 1.2 JUSTIFICACIÓN... 3 1.3 OBJETIVOS... 4 1.3.1 GENERAL... 4 1.3.2 ESPECÍFICOS... 4 1.4. PREGUNTA DIRECTRIZ... 4 CAPITULO II REVISIÓN DE LITERATURA
CAPITULO I 1. INTRODUCCIÓN... 1 1.1 EL PROBLEMA... 2 1.2 JUSTIFICACIÓN... 3 1.3 OBJETIVOS... 4 1.3.1 GENERAL... 4 1.3.2 ESPECÍFICOS... 4 1.4. PREGUNTA DIRECTRIZ... 4 CAPITULO II REVISIÓN DE LITERATURA
Muestreo 1, 1A 15, 15 A. Emisiones Atmosféricas
 Muestreo Emisiones Atmosféricas AAIR Environmental posee un laboratorio de fuentes fijas acreditado ante la SEREMI de Salud, y además, posee convenios por análisis con laboratorios locales que se encuentran
Muestreo Emisiones Atmosféricas AAIR Environmental posee un laboratorio de fuentes fijas acreditado ante la SEREMI de Salud, y además, posee convenios por análisis con laboratorios locales que se encuentran
ALCANCE DE ACREDITACIÓN
 SERVICIO DE ACREDITACIÓN ECUATORIANO - SAE ALCANCE DE ACREDITACIÓN Av. Rodrigo Pachano s/n y Montalvo, Ed. Plaza Ficoa, Of. 202, Teléfono: 03-2420106 E-mail: gerencia@lacquanalisis.com Ambato - Ecuador
SERVICIO DE ACREDITACIÓN ECUATORIANO - SAE ALCANCE DE ACREDITACIÓN Av. Rodrigo Pachano s/n y Montalvo, Ed. Plaza Ficoa, Of. 202, Teléfono: 03-2420106 E-mail: gerencia@lacquanalisis.com Ambato - Ecuador
IES Atenea (S.S. de los Reyes) Departamento de Física y Química. PAU Química. Junio 2008 PRIMERA PARTE
 1 PAU Química. Junio 2008 PRIMERA PARTE Cuestión 1. Dados los elementos Na, C, Si y Ne: a) Escriba sus configuraciones electrónicas. Cuántos electrones desapareados presenta cada uno en su estado fundamental?
1 PAU Química. Junio 2008 PRIMERA PARTE Cuestión 1. Dados los elementos Na, C, Si y Ne: a) Escriba sus configuraciones electrónicas. Cuántos electrones desapareados presenta cada uno en su estado fundamental?
INCOMPATIBILIDAD I N C O M P A T I B L E S P R O D U C T O S BASES METALES SULFUROS CIANUROS ACIDOS OTROS ACIDOS ACIDOS FUERTES
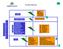 INCOMPATIBILIDAD ACIDOS BASES METALES SULFUROS CIANUROS ACIDOS FUERTES OTROS ACIDOS P R O D U C T O S I N C O M P A T I B L E S OXIDANTES CLORATOS CROMATOS DICROMATOS HALOGENOS NITRATOS PERCLORATOS PEROXIDOS
INCOMPATIBILIDAD ACIDOS BASES METALES SULFUROS CIANUROS ACIDOS FUERTES OTROS ACIDOS P R O D U C T O S I N C O M P A T I B L E S OXIDANTES CLORATOS CROMATOS DICROMATOS HALOGENOS NITRATOS PERCLORATOS PEROXIDOS
REACCIONES DE TRANSFERENCIA DE ELECTRONES SEPTIEMBRE 2015
 REACCIONES DE TRANSFERENCIA DE ELECTRONES SEPTIEMBRE 2015 1- El permanganato de potasio actúa como oxidante en medio ácido, dando como producto Mn 2+. Por el contrario, como oxidante en medio básico el
REACCIONES DE TRANSFERENCIA DE ELECTRONES SEPTIEMBRE 2015 1- El permanganato de potasio actúa como oxidante en medio ácido, dando como producto Mn 2+. Por el contrario, como oxidante en medio básico el
COMPOSICIÓN CUALITATIVA DE LAS AGUAS RESIDUALES
 COMPOSICIÓN CUALITATIVA DE LAS AGUAS RESIDUALES Es muy difícil de definir. Se pueden clasificar los parámetros que sirven para su caracterización en tres grupos: 1.- Parámetros físicos Sólidos en suspensión:
COMPOSICIÓN CUALITATIVA DE LAS AGUAS RESIDUALES Es muy difícil de definir. Se pueden clasificar los parámetros que sirven para su caracterización en tres grupos: 1.- Parámetros físicos Sólidos en suspensión:
DISOLUCIONES Y ESTEQUIOMETRÍA
 DISOLUCIONES Y ESTEQUIOMETRÍA DISOLUCIONES 1.-/ Se disuelven 7 gramos de NaCl en 50 gramos de agua. Cuál es la concentración centesimal de la disolución? Sol: 12,28 % de NaCl 2.-/ En 20 ml de una disolución
DISOLUCIONES Y ESTEQUIOMETRÍA DISOLUCIONES 1.-/ Se disuelven 7 gramos de NaCl en 50 gramos de agua. Cuál es la concentración centesimal de la disolución? Sol: 12,28 % de NaCl 2.-/ En 20 ml de una disolución
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2014 QUÍMICA TEMA 7: REACCIONES REDOX
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 014 QUÍMICA TEMA 7: REACCIONES REDOX Junio, Ejercicio 6, Opción B Reserva 1, Ejercicio, Opción B Reserva, Ejercicio 5, Opción A Reserva, Ejercicio, Opción A Reserva,
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 014 QUÍMICA TEMA 7: REACCIONES REDOX Junio, Ejercicio 6, Opción B Reserva 1, Ejercicio, Opción B Reserva, Ejercicio 5, Opción A Reserva, Ejercicio, Opción A Reserva,
3. Calcula la cantidad estequiométrica de hidrógeno molecular, en moles, necesaria para reaccionar con 5 moles de oxígeno en la síntesis del agua.
 CÁLCULOS ESTEQUIOMÉTRICOS BÁSICOS 1. Ajusta las siguientes reacciones químicas: C 3 H 6 (g) + O 2 (g) CO 2 (g) + H 2 O (g) N 2 (g) + H 2 (g) NH 3 (g) KClO 3 (aq) KCl (aq) + O 2 (g) H 2 O 2 (l) O 2 (g)
CÁLCULOS ESTEQUIOMÉTRICOS BÁSICOS 1. Ajusta las siguientes reacciones químicas: C 3 H 6 (g) + O 2 (g) CO 2 (g) + H 2 O (g) N 2 (g) + H 2 (g) NH 3 (g) KClO 3 (aq) KCl (aq) + O 2 (g) H 2 O 2 (l) O 2 (g)
DIVERSIDAD Y ESTRUCTURA DE LA MATERIA. 2º ESO Ciencias de la naturaleza
 DIVERSIDAD Y ESTRUCTURA DE LA MATERIA 2º ESO Ciencias de la naturaleza Todo lo que vemos es materia CLASIFICACIÓN DE LA MATERIA La materia se presenta en la naturaleza en forma de sustancias puras y mezclas,
DIVERSIDAD Y ESTRUCTURA DE LA MATERIA 2º ESO Ciencias de la naturaleza Todo lo que vemos es materia CLASIFICACIÓN DE LA MATERIA La materia se presenta en la naturaleza en forma de sustancias puras y mezclas,
ENSAYOS COSMÉTICOS, DENTÍFRICOS, PRODUCTOS DE HIGIENE Y PRODUCTOS DE LIMPIEZA
 ENSAYOS COSMÉTICOS, DENTÍFRICOS, PRODUCTOS DE HIGIENE Y PRODUCTOS DE LIMPIEZA INDICE POR ORDEN ALFABÉTICO Acetato de Zinc Valoración Complexométrica LB-I-417 Ácido Cítrico Valoración Volumétrica LB-I-434
ENSAYOS COSMÉTICOS, DENTÍFRICOS, PRODUCTOS DE HIGIENE Y PRODUCTOS DE LIMPIEZA INDICE POR ORDEN ALFABÉTICO Acetato de Zinc Valoración Complexométrica LB-I-417 Ácido Cítrico Valoración Volumétrica LB-I-434
INSTITUTO POLITECNICO NACIONAL
 INSTITUTO POLITECNICO NACIONAL CECYT NO. 1 GONZALO VÁZQUEZ VELA GUÍA DE QUÍMICA I PERIÓDO ESCOLAR 2015-2016 ACADEMIA DE QUÍMICA TURNO VESPERTINO 1 Materia y Energía 1.- Calcula la energía, en Joules y
INSTITUTO POLITECNICO NACIONAL CECYT NO. 1 GONZALO VÁZQUEZ VELA GUÍA DE QUÍMICA I PERIÓDO ESCOLAR 2015-2016 ACADEMIA DE QUÍMICA TURNO VESPERTINO 1 Materia y Energía 1.- Calcula la energía, en Joules y
El hidróxido de magnesio es una sustancia ligeramente soluble en agua. El ph de una disolución saturada de dicho hidróxido es de 10,38.
 Calcula la solubilidad en g/l del fosfato de plomo (II) sabiendo que su producto de solubilidad es 1,5.10-32. Datos: Pb = 207,2; P = 31; O = 16. Sol: 1,37.10-11 g/l. Sabiendo que la solubilidad en g/l
Calcula la solubilidad en g/l del fosfato de plomo (II) sabiendo que su producto de solubilidad es 1,5.10-32. Datos: Pb = 207,2; P = 31; O = 16. Sol: 1,37.10-11 g/l. Sabiendo que la solubilidad en g/l
CONFERENCIA No. 1 Página 1 de 4. DE: Septiembre 7 del 2015 A : Septiembre 25 del 2015
 CONFERENCIA No. 1 Página 1 de 4 ÁREA: TEMA: PROFESOR: TIEMPO DE REALIZACIÓN: CIENCIAS NATURALES Y EDUCACIÓN GRADO: DÉCIMO AMBIENTAL - QUÍMICA Nomenclatura y reacciones de obtención de óxido, ácidos, bases
CONFERENCIA No. 1 Página 1 de 4 ÁREA: TEMA: PROFESOR: TIEMPO DE REALIZACIÓN: CIENCIAS NATURALES Y EDUCACIÓN GRADO: DÉCIMO AMBIENTAL - QUÍMICA Nomenclatura y reacciones de obtención de óxido, ácidos, bases
PRUEBA ACCESO A CICLOS FORMATIVOS DE GRADO SUPERIOR OPCIÓN C QUÍMICA
 PRUEBA ACCESO A CICLOS FORMATIVOS DE GRADO SUPERIOR OPCIÓN C QUÍMICA DATOS DEL ASPIRANTE Apellidos: CALIFICACIÓN PRUEBA Nombre: D.N.I. o Pasaporte: Fecha de nacimiento: / / Instrucciones: Lee atentamente
PRUEBA ACCESO A CICLOS FORMATIVOS DE GRADO SUPERIOR OPCIÓN C QUÍMICA DATOS DEL ASPIRANTE Apellidos: CALIFICACIÓN PRUEBA Nombre: D.N.I. o Pasaporte: Fecha de nacimiento: / / Instrucciones: Lee atentamente
FORMULACIÓN QUÍMICA INORGÁNICA. Combinaciones ternarias (combinaciones de tres elementos) Hidróxidos = Metal - (OH) El grupo (OH): - 1
 FORMULACIÓN QUÍMICA INORGÁNICA I.E.S. Juan.A. Suanzes Combinaciones ternarias (combinaciones de tres elementos) Hidróxidos = Metal - (OH) Ca(OH) 2 ; NaOH ; Al(OH) 3 X (OH) m AgOH ; Zn(OH) 2 ; Cr(OH) 3
FORMULACIÓN QUÍMICA INORGÁNICA I.E.S. Juan.A. Suanzes Combinaciones ternarias (combinaciones de tres elementos) Hidróxidos = Metal - (OH) Ca(OH) 2 ; NaOH ; Al(OH) 3 X (OH) m AgOH ; Zn(OH) 2 ; Cr(OH) 3
