PRINCIPIOS DE ANESTESIA CUANTITATIVA
|
|
|
- Elena Lucero Montero
- hace 6 años
- Vistas:
Transcripción
1 Rev. Col. Anest. 12: 123, 1984 PRINCIPIOS DE ANESTESIA CUANTITATIVA Dr. Carlos Julio Parra Higuera* Esta nueva técnica para administrar anestésicos inhalatorios, con flujos bajos y sistema cerrado, ha sido posible desarrollarse, por los avances recientes en Tecnología Biomédica y Electrónica, que facilitan la administración de los anestésicos en dosis precisas. Los conocimientos de la absorción, distribución y eliminación de los agentes anestésicos volátiles, han revolucionado nuestros conceptos de anestesia inhalatoria y han hecho posible su administración por dicha técnica, La profundidad de la anestesia general, producida por agentes inhalatorios, está dada básicamente por la presión parcial (tensión) del anestésico en el cerebro. La velocidad de la inducción el mantenimiento anestésico y la recuperación, dependen de la rapidez de los cambios de presión en este tejido. La presión parcial del anestésico en el tejido cerebral varía obedeciendo a diversos factores * Médico Anestesiólogo del Instituto Nacional de Cancerología, Bogotá Colombia. Docente Adjunto, Sección de Anestesiología Hospital San Juan de Dios. Bogotá Colombia. y tiende a ser igual a la presión del gas en la sangre arterial. Por lo tanto, debemos analizar estos factores en los diferentes compartimentos que atraviesa el gas anestésico y determinan la presión parcial arterial y cerebral. E circuito respiratorio, los alvéolos, la sangre y los tejidos del organismo, son los cuatro compartimentos donde actúan los diferentes factores que modifican la absorción, distribución y captación de los agentes anestésicos. El estudio y análisis de estos factores constituyen los fundamentos científicos de la Anestesia Cuantitativa. Concentración Alveolar Mínima (Mac). Se define en términos de porcentaje de una atmósfera, por consiguiente, es la presión parcial alveolar del agente anestésico, siendo igual a cualquier altura, puesto que estando en equilibrio la presión parcial del anestésico, debe ser igual en todos los tejidos del cuerpo, más no la concentración, En el cerebro, sitio de acción del anestésico, la presión parcial debe ser igual a la presión 123
2 Parra C.J. parcial alveolar. Es por esto que la concentración alveolar mínima, ha sido considerada, en los últimos años como el mayor índice de potencia anestésica. De Jong y Eger, recientemente introdujeron el concepto del AD95, el cual se define como: la concentración alveolar mínima que anestesia el 95 /o de los pacientes y se representa razonable-. mente como 1.3 veces el MAC, Por lo anterior, cualquier concentración alveolar anestésica (CA) puede considerarse como el factor 1.3 por el MAC. Ahora bien, la concentración alveolar depende básicamente del MAC y éste se encuentra afectado por ciertos factores a saber: A) Cambios de temperatura en el cuerpo. B) Stress Excesivo. C) Liberación de catecolaminas por el sistema nervioso central (Hipertensión o hipotensión). D) Edad. E) Drogas generales en la anestesia general. Por otra parte existen factores que no modifican el MAC a saber: A) El grado de estímulo y la duración de éste. B) Sexo. C) Cambios ácido - básicos. D) Cambio en la PaC02 de 10-90mmHg. E) Cambios en la oxigenación (PaO mmhg). F) Isovolemia anémica. Se puede decir que el MAC se usa fundamentalmente porque hasta el momento es la medida más precisa para dosificar la potencia de un agente anestésico. Varios escritos, de evidencias experimentales, sugieren que las curvas de la dosis anestésica y la respuesta del sistema nervioso central, son claramente paralelas. Coeficiente de Solubilidad de los Anestésicos Esta medida se expresa por el coeficiente de reparto sangre/gas, que es la relación de la concentración del anestésico en la sangre y la concentración del mismo en la fase gaseosa cuando las dos fases están en equilibrio. Cuanto más soluble es un anestésico en la sangre, mayor cantidad de él debe absorberse para que se eleve su presión parcial en la sangre en forma apreciable; por lo tanto, la presión de los anestésicos solubles en la sangre aumente lentamente. El reservorio o depósito potencial para gases comparativamente insolubles es pequeño y puede ocuparse con rapidez. Como consecuencia, la presión parcial en la sangre puede aumentar más rápidamente. como la velocidad de difusión a través de la membrana alveolar es proporcional a la diferencia entre la presión del gas en los alveolos y la presión en la sangre venosa, el volumen del gas transferido a la sangre arterial en cada minuto, desciende con el tiempo. Por lo tanto, la presión del anestésico en la sangre arterial, aumenta lentamente en la parte final de la curva de absorción. Solubilidad de los Lípidos - Teoría de la Concentración crítica molar. Dentro de las teorías sobre el mecanismo de acción de los anestésicos, la teoría de los lípidos formulada por MEYER y OVERTON, independientemente, plantea la existencia de una estrecha correlación entre la afinidad de un anestésico por un lípido y su acción deprimente. Como las células nerviosas y sus membranas contienen lípidos, se cree que el anestésico llega al tejido nervioso merced a su solubilidad en los lípidos. Aunque existe un paralelismo entre la potencia anestésica de diversos anestésicos por inhalación y sus coeficientes de reparto aceite/gas, hoy se sabe que los anestésicos (por inhalación) interactúan con las proteínas. Este enfoque examina el sitio de la localización o acumulación de los agentes anestésicos, pero no su mecanismo de acción. La capacidad de los lípidos del cerebro (10% del total de la masa cerebral) para almacenar cada anestésico a 1.3 MAC, se puede calcular del coeficiente de partición tejido cerebral/gas, substrayendo de la cantidad del anestésico presente, el vapor anes- 124
3 Anestesia cuantitativa tésico disuelto en el agua del tejido cerebral. La concentración crítica molar de cada agente anestésico, disuelta en los lipidos del cerebro a 1.3 MAC, es aproximadamente de 21 milimoles por litro. "La concentración crítica molar" se define como la concentración molar del agente anestésico en los fosfolípidos del cerebro asociada a la anestesia. El fin primordial del anestesiólogo, es obtener y mantener esta única concentración molar en los fosfolípidos del tejido cerebral, durante la anestesia. Por otra parte, sabemos que la concentración arterial (CA) y el gasto cardíaco determinan el grado de saturación de los tejidos con moléculas anestésicas, de tal forma que el producto Ca por el gasto cardíaco (Q), es la cantidad de anestésico entregado minuto a minuto a los tejidos. Observamos que la inducción resultará más rápida cuanto más sea la concentración alveolar. La solubilidad es un factor en este producto y la concentración alveolar del agente anestésico, administrado correctamente es otro factor importante del producto ideal. Constante de Tiempo. Cuando llega a los tejidos un flujo y concentración constante de gas anestésico, la captación de este se puede representar como una función de tiempo, como el tiempo en minutos que se necesita para producir un cambio del 63.2% en la concentración a- nestésica de un tejido. Para alcanzar el 95 /o de equilibrio en la saturación, se necesitan tres constantes de tiempo. La constante de tiempo nos demuestra la velocidad con la cual un órgano acumula el anestésico y la forma de calcular la dosis anestésica necesaria para conseguir y mantener una concentración crítica molar en el cerebro. Distribución de los Anestésicos. En 1962 Mapleson demostró cómo manteniendo una presión de vapor inspiratoria constante de halothano, la captación de éste disminuía significativamente con el tiempo. A partir de esta fecha se fueron desarrollando modelos de captación y distribución deanestésicos en sistema cerrado. Hampton y Flickínger fueron tal vez los primeros en usar un modelo de captación anestésica administrando vapor de Halothane, en cantidades conocidas. Sin embargo, a medida que iban apareciendo nuevos modelos de captación y distribución, el cálculo de la dosis anestésica parecía más difícil. Su conocimiento es esencial en el circuito cerrado, donde el oxígeno y los gases anestésicos deben administrarse en una relación igual a la captación que hace el organismo, para mantener en el sistema un volumen y composición constante. La cantidad del anestésico captado por el organismo, está relacionada con la concentración alveolar (CA) la que a su vez mantiene una concentración arterial y a su turno sustenta la concentración anestésica en los tejidos. Por consiguiente la concentración alveolar (CA) es el factor determinante en la captación anestésica. El Dr. Harry Lowe en 1972 presentó un modelo para circuito cerrado empleando una concentración alveolar de vapor anestésico constante a 1.3 MAC con oxígeno o con 65% de N2O. Básicamente el modelo de captación y distribución lo componen diez compartimentos en que se han distribuido los órganos analizados con sus respectivos porcentajes de gasto cardíaco, pesos promedio y flujo de sangre por minuto. Manteniendo una concentración constante cada órgano del sistema capta un agente anestésico en una relación exponencial diferente para cada órgano, determinada por el coeficiente de solubilidad tejido/sangre, el volumen de cada órgano (igual al peso) y la proporción del gasto cardíaco (flujo de sangre por minuto). El coeficiente de partición tejido/sangre se usa para calcular la cantidad total de vapor anestésico que cada órgano puede acumular. El valor de esta cantidad se calcula multiplicando la CA (ml/dl) por el coeficiente T/S y el volumen de cada órgano expresado en DL. De una manera práctica podemos decir que, entre más alta sea la solubilidad en el te- 125
4 Parra C.J. jido de un órgano, mayor es su capacidad para acumular vapor anestésico y más largo es el período requerido para saturarse, cuando la concentración arterial por minuto es constante. Los órganos gradualmente acumulan el vapor anestésico y los mejor perfundidos se saturan en los primeros 30 minutos. Después dé aproximadamente 180 minutos han alcanzado su capacidad total a excepción del tejido graso. La suma del contenido anestésico en todos los órganos en un momento dado, representa la dosis total necesaria para mantener la concentración crítica molar en el tejido cerebral. Resumiendo podemos decir, que, la forma como cada agente anestésico logra copar la capacidad de los órganos del cuerpo depende de: la concentración arterial, del gasto cardíaco, del volumen de cada órgano y de su solubilidad. Captación de los agentes anestésicos. Lo expuesto anteriormente ha sido analizado en una forma estática, lo cual constituye la base para determinar el ritmo de captación y acumulación del vapor anestésico por el organismo en función del tiempo. Fundamentalmente está demostrado que: A) El ritmo de captación de cada anestésico es. inversamente proporcional a la raíz cuadrada del tiempo. B) Las demandas de vapor anestésico (dosis acumulativas) son directamente proporcionales a la raíz cuadrada del tiempo. Por lo tanto la cantidad de vapor anestésico que capta el organismo, disminuye a medida que transcurre el tiempo. "El tiempo "real" en este caso será el cuadrado del tiempo: minutos etc. y los intervalos son la progresión aritmética de los números impares: etc. A la cantidad de vapor anestésico absorbida, Lowe la denominó "dosis unidad" y ha demostrado, que la captación total del organismo (Q an), en un tiempo dado, es igual a la concentración en sangre por minuto, dividida por la raiz cuadrada del tiempo. Qan = 1.3 x MAC xs/gx QxT - 1 / 2 Sabiendo que la "dosis unidad" es la cantidad de vapor anestésico que se absorbe en cada intervalo de tiempo, el cálculo de esta es igual a: Dosis Unidad = 2Ca x Q x 1. La concentración arterial se mantiene constante con las siguientes entregas de "dosis unidad" al circuito. Cada agente anestésico es absorbido en un modelo idéntico, pero a diferentes valores absolutos, los cuales son proporcionales a su respectiva concentración arterial. Técnicas para la aplicación clínica de la Anestesia Cuantitativa El principal impedimento para.el uso de los agentes anestésicos volátiles en el circuito cerrado, es el desconocimiento de la cantidad de vapor anestésico que introducimos al sistema. Mientras que utilizando el método convencional la concentración anestésica se expresa en porcentajes, utilizando la dosis cuantitativa, calculamos la cantidad precisa de vapor anestésico minuto a minuto en términos de ml. de vapor que pasan del circuito a los diversos tejidos. Reemplazando los valores respectivos para cada agente anestésico y determinado paciente, calculamos la respectiva dosis. En nuestra práctica, el valor de la dosis de impregnación es igual a la dosis unidad, usando cualquier agente anestésico. Esta antigua técnica de administrar volúmenes conocidos de líquido anestésico al flujo de gas del circuito, ha sido renovada y descrita por Weingarten y Lowe. Usando la inyección de líquido anestésico al circuito, se administra una cantidad exacta de agente anestésico, independientemente de la presión de vapor o de la temperatura del medio ambiente. Para introducir el líquido anestésico al circuito respiratorio, hemos ideado un adaptador metálico colocado en el lado expiratorio. Contienen en su interior un tubo pequeño del calibre de una aguja No. 14 con el fin de dirigir el líquido anestésico hacia la manguera expiratoria. Está armado con una 126
5 Anestesia cuantitativa llave metálica de tres vías, en la cual acondicionamos dos jeringas, preferiblemente de plástico sin émbolo de caucho; una de 3 ml que facilita la medición de la dosis unidad y otra de 20 ml. que se utiliza como reservorio del líquido anestésico, con un volumen suficiente para un período de tiempo largo, dependiendo del agente anestésico que se u- tilice. Con el fin de obviar los cálculos de la dosis unidad para cada paciente, hemos elaborado un esquema práctico, para los tres anestésicos halogenados más usados en nuestro medio. Este, es el resultado de un análisis estadístico del peso del paciente, la dosis unidad obtenida por la fórmula de H. Lowe y la respuesta clínica observada. Ventajas de la Anestesia Cuantitativa. Además de ser una técnica segura para el paciente, proporcionándole al anestesiólogo nuevos parámetros para el control clínico de la anestesia, debemos tener en cuenta las siguientes ventajas: A) La humidificación y el mantenimiento de una adecuada temperatura de los gases inspirados permiten una disminución de la incidencia de la morbilidad pulmonar post - operatoria. B) Disminuye la contaminación anestésica en salas de cirugía. Es evidente por estudios serios que la inhalación crónica de gases anestésicos produce en el personal que labora en salas de cirugía, efectos tóxicos (carcinogenéticos - teratogénicos, daño celular, etc). C) La economía que ofrece el uso del circuito cerrado debe ser considerada como una solución para disminuir el costo de los a- nestésicos en nuestro medio. BIBLIOGRAFÍA Merkel G. Eger II: A Comparative study of halothane and halopropane anesthesia. Including meths for determinig equipotency. Anesthesiology 24: , Saidman LJ, Eger EL 11: Effect of nitrous oxide and of narcotic premedication and the alveolar concentration of halothane required for anesthesia Anesthesiology 25: , De Jong RH and Eger, EL II: MAC expanded: AD 50 and AD 95 valves of common inhalation anestetics n man. Anesthesiology 42: ,1975. Gregory Ga, Eger EL II, Munson ES: The relationship beween age andhalothane, requirement in man. Anesthesiology 30: , Quasha, AL et al: Determination and aplications of MAC Anesthesiology 53: , Mapleson, WW: The rate of halothane vapour in man. Br. J. Anaesth 34: 11-18, Hamton LJ. and Flickinger: Closed circuit anesthesia utilizing Known ncrements of halothane. Anesthesiology 22: , Mapleson WW: The concentration of anesthetics in closed circuit, sith special reference to halothane I: Theoretical study: Br. J. Anaesth 32: , Hampton LJ. and Flickinger H: Closed circuit anesthesia utilizing known increments of halothane. Anesthesiology 22: , Lowe JH, and Ernst EA: The quantitative Williams and Wilkins, Baltimore. pp 11-23, Smith, NT Zwart, A, and Beneken, JW: Interaction between the circulatory effects and the uptake and distribution of halothane. Use of a múltiple model: Anesthesiology 37: 47-58,
6 rra C.J. Lowe JH and Ernst, EA: The quantitative William and Wilkins. Baltimore, pp 55-63, Lowe HJ: The anesthetic continuun. In low flow and closed System Anesthesia. Eds. JA. Aldrete, HJ. Lowe and RW. Virtue. Gruñe Straton. New YOrk, pp 11-37, Lowe HJ, and Ernst, EA: The quantitative Williams and Wilkins. Baltimore, pp: 67-74, Weingarten M: Low flow and closed circuit anesthesia. In Low Flor and Closed System anesthesia. Eds. JA. Aldrete. HJ Low and RW virtue. Gruñe & Straton, New York, pp: 68, Weingarten M, Lowe HJ: A new circuit injection techníc for syringe measured administration of Methoxuflurane: A new dimensión n anesthesia. Anesth. Analg 52: , Lowe HJ. Mackrel TN. et al: Quantitative closed circuit anesthesia, Anesthesiol, Rev 1:11, Aldrete JA. De los flujos altos a los flujos bajos: a donde hemos llegado. Rev. col Anest 9: 235, Lowe HJ. and Ernst EA. The quantitative Williams and Wilkins, Baltimore pp 16, Peña J.E. Madiedo N: Flujos bajos y sistema cerrado en anestesia. Rev. Col. Anest. 8: , Parra CJ: Enfluorano: Dosis cuantitativas en sistema cerrado Rev Col. Anest 8: 36-45, Parra CJ: Esquema práctico para la anestesia cuantitativa Rev. Col. Anest. 10: N.1, Alvarez, T. Noreña, A. Ospina S: Informe preliminar sobre la morbilidad y mortalidad de los Anestesiólogos en Antioquia y sobre los riesgos ocupaciones a los cuales se, exponen estos profesionales. Rev. Col. Anest 4: , Herrera J. Mantilla M: Efectos teratogénicos de los Halogenados en ratones. Rev. Col. Anest 4: , Aldrete JA. Cubillos P. and Sherril D; Humidity and Temperature changes during Low Flow and closed Sistem Anesthesia. Acta anaesth scand 25: , Los médicos son como los obispos: aquellos dan recetas y estos siempre echan las bendiciones, aunque las personas a quienes las dan no las quieran o se burlen de ellos. Simón Bolívar
FISIOLOGIA RESPIRATORIA DR. JOSÉ CARLOS MORALES NÁJERA
 FISIOLOGIA RESPIRATORIA DR. JOSÉ CARLOS MORALES NÁJERA PRINCIPIOS BASICOS: FÍSICA DE LOS GASES La ventilación y la perfusión pulmonares y la transferencia de los gases obedecen estrictamente a fuerzas
FISIOLOGIA RESPIRATORIA DR. JOSÉ CARLOS MORALES NÁJERA PRINCIPIOS BASICOS: FÍSICA DE LOS GASES La ventilación y la perfusión pulmonares y la transferencia de los gases obedecen estrictamente a fuerzas
Anestesiología. Objetivo del Tema IAGS 27/02/2006. Programa de Anestesiología. Farmacología aplicada de los anestésicos inhalatorios
 Anestesiología Tema 5 Farmacología aplicada de los anestésicos inhalatorios ANESTESIOLOGÍA VETERINARIA A - Anestesia General 1. Introducción a la anestesia: concepto y nomenclatura. 2. Evaluación preanestésica
Anestesiología Tema 5 Farmacología aplicada de los anestésicos inhalatorios ANESTESIOLOGÍA VETERINARIA A - Anestesia General 1. Introducción a la anestesia: concepto y nomenclatura. 2. Evaluación preanestésica
INHALATORIA. Profesor Pablo E. Otero Anestesiología y Algiología Facultad de Ciencias Veterinarias Universidad de Buenos Aires
 ANESTESIA INHALATORIA Profesor Pablo E. Otero Anestesiología y Algiología Facultad de Ciencias Veterinarias Universidad de Buenos Aires Buenos Aires, Argentina Objetivos 1. Administrar la dosis correcta
ANESTESIA INHALATORIA Profesor Pablo E. Otero Anestesiología y Algiología Facultad de Ciencias Veterinarias Universidad de Buenos Aires Buenos Aires, Argentina Objetivos 1. Administrar la dosis correcta
Ventilación Pulmonar. -durante al ejercicio- Elaborado por Lic. Manuel Salazar Leitón
 Ventilación Pulmonar -durante al ejercicio- Elaborado por Lic. Manuel Salazar Leitón Funciones básicas de la ventilación pulmonar Intercambio gaseoso con el ambiente. Regular el acidez en sangre. Comunicación
Ventilación Pulmonar -durante al ejercicio- Elaborado por Lic. Manuel Salazar Leitón Funciones básicas de la ventilación pulmonar Intercambio gaseoso con el ambiente. Regular el acidez en sangre. Comunicación
GASES IDEALES. Contiene una mezcla de gases CP + O 2. Volumen = 1 litro Temperatura = 23 C = ,15 = 298,15K =585 = 0,7697 =250 = 0,3289
 GASES IDEALES PROBLEMA 10 Mezclas de los gases ciclopropano (C 3H 8) y oxígeno se utilizan mucho como anestésicos. a) Cuántos moles de cada gas están presentes en un recipiente de 1 litro a 23 C, si la
GASES IDEALES PROBLEMA 10 Mezclas de los gases ciclopropano (C 3H 8) y oxígeno se utilizan mucho como anestésicos. a) Cuántos moles de cada gas están presentes en un recipiente de 1 litro a 23 C, si la
Unidad 5 Equilibrio. 1. Razone el efecto que provocará en la síntesis de amoniaco:
 Unidad 5 Equilibrio OPCIÓN A. Razone el efecto que provocará en la síntesis de amoniaco: N (g) + 3H (g) NH 3 (g) H º 9,4 kj a) Un aumento de la presión en el reactor. Un aumento de la presión origina que
Unidad 5 Equilibrio OPCIÓN A. Razone el efecto que provocará en la síntesis de amoniaco: N (g) + 3H (g) NH 3 (g) H º 9,4 kj a) Un aumento de la presión en el reactor. Un aumento de la presión origina que
DISOLUCIONES. Las disoluciones son mezclas homogéneas de dos o más sustancias (componentes) en proporciones variables.
 DISOLUCIONES Las disoluciones son mezclas homogéneas de dos o más sustancias (componentes) en proporciones variables. Soluto es la sustancia que se encuentra en menor proporción. Disolvente es la sustancia
DISOLUCIONES Las disoluciones son mezclas homogéneas de dos o más sustancias (componentes) en proporciones variables. Soluto es la sustancia que se encuentra en menor proporción. Disolvente es la sustancia
A continuación se detallan cada una de las propiedades coligativas:
 PREGUNTA (Técnico Profesional) Se prepara una solución con 2 mol de agua y 0,5 mol de un electrolito no volátil. Al respecto, cuál es la presión de vapor a 25 ºC de esta solución, si la presión del agua
PREGUNTA (Técnico Profesional) Se prepara una solución con 2 mol de agua y 0,5 mol de un electrolito no volátil. Al respecto, cuál es la presión de vapor a 25 ºC de esta solución, si la presión del agua
LEYES DE LOS GASES. El volumen es directamente proporcional a la cantidad de gas:
 LEYES DE LOS GASES LEY DE AVOGADRO: Esta ley, descubierta por Avogadro a principios del siglo XIX, establece la relación entre la cantidad de gas y su volumen cuando se mantienen constantes la temperatura
LEYES DE LOS GASES LEY DE AVOGADRO: Esta ley, descubierta por Avogadro a principios del siglo XIX, establece la relación entre la cantidad de gas y su volumen cuando se mantienen constantes la temperatura
Proteínas plasmáticas. Proteínas plasmáticas. Sales de litio 0% Ampicilina 18% Morfina 35% Aspirina 50% Fenitoína 90% Diazepam 98% Warfarina 99%
 Distribución Distribución y fijación de fármacos Paso del fármaco desde la sangre a los diversos tejidos La capacidad de los fármacos para distribuirse en el organismo va a depender de: a) Características
Distribución Distribución y fijación de fármacos Paso del fármaco desde la sangre a los diversos tejidos La capacidad de los fármacos para distribuirse en el organismo va a depender de: a) Características
2. Sobre los valores de las diferentes presiones parciales de los gases, marca con una cruz (X) la respuesta correcta según corresponda.
 Semana 7 Consolidación 7. 1. Acerca de la mecánica de la ventilación pulmonar, escribe en el espacio en blanco (V) si son verdaderos o (F) si son falsos los siguientes planteamientos: a) _F_ Los intercostales
Semana 7 Consolidación 7. 1. Acerca de la mecánica de la ventilación pulmonar, escribe en el espacio en blanco (V) si son verdaderos o (F) si son falsos los siguientes planteamientos: a) _F_ Los intercostales
ABSORCIÓN, DISTRIBUCIÓN Y ELIMINACIÓN DE LOS TÓXICOS EN EL ORGANISMO
 Toxicología alimentaria Diplomatura de Nutrición humana y dietética Curso 2010-2011 ABSORCIÓN, DISTRIBUCIÓN Y ELIMINACIÓN DE LOS TÓXICOS EN EL ORGANISMO Dr. Jesús Miguel Hernández-Guijo Dpto. Farmacología
Toxicología alimentaria Diplomatura de Nutrición humana y dietética Curso 2010-2011 ABSORCIÓN, DISTRIBUCIÓN Y ELIMINACIÓN DE LOS TÓXICOS EN EL ORGANISMO Dr. Jesús Miguel Hernández-Guijo Dpto. Farmacología
Fisiologia respiratorio
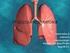 Fisiologia respiratorio MVR/LC El proceso respiratorio Ventilación pulmonar: inspiración y espiración. Intercambio gaseoso entre el aire y la sangre. Transporte de los gases por la sangre. Intercambio
Fisiologia respiratorio MVR/LC El proceso respiratorio Ventilación pulmonar: inspiración y espiración. Intercambio gaseoso entre el aire y la sangre. Transporte de los gases por la sangre. Intercambio
Sistema respiratorio. Fisiología Licenciatura en Enfermería. Dra. Maria Eugenia Victoria Bianchi Año 2012
 Sistema respiratorio Enfermería. Dra. Maria Eugenia Victoria Bianchi Año 2012 Volúmenes y capacidades Volumen corriente:(vt) es el volumen de aire inspirado y expirado en una respiración normal Volumen
Sistema respiratorio Enfermería. Dra. Maria Eugenia Victoria Bianchi Año 2012 Volúmenes y capacidades Volumen corriente:(vt) es el volumen de aire inspirado y expirado en una respiración normal Volumen
Dr. Miguel Ángel González Sosa
 Dr. Miguel Ángel González Sosa Presentación realizada en el curso de Clinopatología del Aparato Respiratorio dentro de la Licenciatura de Médico Cirujano del Área Académica de Medicina en el semestre Julio
Dr. Miguel Ángel González Sosa Presentación realizada en el curso de Clinopatología del Aparato Respiratorio dentro de la Licenciatura de Médico Cirujano del Área Académica de Medicina en el semestre Julio
O Un elemento químico es una sustancia que no puede dividirse en otras sustancias por medios químicos comunes. Actualmente los químicos reconocen 92
 BIOELEMENTOS BIOELEMENTOS O La vida se compone de materia, que es todo lo que ocupa espacio y tiene masa. La materia, en forma tan diversas como una roca, madera, metal y aire, se compone de elementos
BIOELEMENTOS BIOELEMENTOS O La vida se compone de materia, que es todo lo que ocupa espacio y tiene masa. La materia, en forma tan diversas como una roca, madera, metal y aire, se compone de elementos
Capítulo 10. Efectos de superficie. Sistema respiratorio
 Capítulo 10 Efectos de superficie. Sistema respiratorio 1 Tensión superficial El coeficiente de tensión superficial γ es la fuerza por unidad de longitud que hay que realizar para aumentar una superficie:
Capítulo 10 Efectos de superficie. Sistema respiratorio 1 Tensión superficial El coeficiente de tensión superficial γ es la fuerza por unidad de longitud que hay que realizar para aumentar una superficie:
Náuseas y vómitos en el postoperatorio. Dr. Jorge Aguilera S.
 Náuseas y vómitos en el postoperatorio Dr. Jorge Aguilera S. Incidencia N.V.P.O Cx. Ambulatoria -Adeno-amigdalectomía 60% -Ginecológica 54-92% Cx. Hospitalizado -Ginecológica >60% -Estrabismo >55% -Abdominal
Náuseas y vómitos en el postoperatorio Dr. Jorge Aguilera S. Incidencia N.V.P.O Cx. Ambulatoria -Adeno-amigdalectomía 60% -Ginecológica 54-92% Cx. Hospitalizado -Ginecológica >60% -Estrabismo >55% -Abdominal
TEMA 2: LEYES Y CONCEPTOS BÁSICOS EN QUÍMICA
 1. SUSTANCIAS PURAS Y MEZCLAS 2. LEYES PONDERALES DE LAS COMBINACIONES QUÍMICAS 2.1. LEY DE CONSERVACIÓN DE LA MATERIA Enunciada en 1783 por Lavoisier: La materia ni se crea ni se destruye, únicamente
1. SUSTANCIAS PURAS Y MEZCLAS 2. LEYES PONDERALES DE LAS COMBINACIONES QUÍMICAS 2.1. LEY DE CONSERVACIÓN DE LA MATERIA Enunciada en 1783 por Lavoisier: La materia ni se crea ni se destruye, únicamente
Equilibrio Químico. CI4102 Ingeniería Ambiental Profesor Marcelo Olivares A.
 Equilibrio Químico CI4102 Ingeniería Ambiental Profesor Marcelo Olivares A. Introducción Las reacciones químicas que se ha considerado hasta este punto se denominan irreversibles debido a que ellas proceden
Equilibrio Químico CI4102 Ingeniería Ambiental Profesor Marcelo Olivares A. Introducción Las reacciones químicas que se ha considerado hasta este punto se denominan irreversibles debido a que ellas proceden
TAREA 1. Nombre Núm. de lista Grupo Turno Núm. de Expediente Fecha
 TAREA 1 Nombre Núm. de lista Grupo Turno Núm. de Expediente Fecha INSTRUCCIONES: Investiga como es el puente de Hidrógeno en las estructuras del H 2 O, NH 3 y HF. Dibuja los modelos resaltando con color
TAREA 1 Nombre Núm. de lista Grupo Turno Núm. de Expediente Fecha INSTRUCCIONES: Investiga como es el puente de Hidrógeno en las estructuras del H 2 O, NH 3 y HF. Dibuja los modelos resaltando con color
E.E.T. Nº9. Físico-Química de 2do año. Guía Nº3. Profesor: Alumno: Curso:
 E.E.T. Nº9 Físico-Química de 2do año Guía Nº3 Profesor: Alumno: Curso: Soluciones Una solución es un sistema homogéneo formado por dos o más componentes. En una solución formada por dos componentes se
E.E.T. Nº9 Físico-Química de 2do año Guía Nº3 Profesor: Alumno: Curso: Soluciones Una solución es un sistema homogéneo formado por dos o más componentes. En una solución formada por dos componentes se
DEPARTAMENTO DE INGENIERIA QUÍMICA CÁTEDRA DE FISICOQUÍMICA TRABAJO PRÁCTICO DE LABORATORIO Nº 4
 Universidad Tecnológica Nacional Facultad Regional La Plata DEPARTAMENTO DE INGENIERIA QUÍMICA CÁTEDRA DE FISICOQUÍMICA TRABAJO PRÁCTICO DE LABORATORIO Nº 4 Descenso crioscópico Objeto de la experiencia:
Universidad Tecnológica Nacional Facultad Regional La Plata DEPARTAMENTO DE INGENIERIA QUÍMICA CÁTEDRA DE FISICOQUÍMICA TRABAJO PRÁCTICO DE LABORATORIO Nº 4 Descenso crioscópico Objeto de la experiencia:
Disoluciones. Química General II 2011
 Disoluciones Química General II 2011 Disolución Es una mezcla homogénea de dos o mas sustancias. Componentes: Soluto: Sustancia (s) presente (s) en menor cantidad en una disolución, son las sustancias
Disoluciones Química General II 2011 Disolución Es una mezcla homogénea de dos o mas sustancias. Componentes: Soluto: Sustancia (s) presente (s) en menor cantidad en una disolución, son las sustancias
BASES FARMACOCINÉTICAS PARA EL DISEÑO O DE UNA PAUTA TERAPÉUTICA. Dr. Pedro Guerra López
 BASES FARMACOCINÉTICAS PARA EL DISEÑO O DE UNA PAUTA TERAPÉUTICA Dr. Pedro Guerra López Pautas terapeuticas Objetivos de esta lección. - Conocer el interés clínico de la farmacocinética en general en cuanto
BASES FARMACOCINÉTICAS PARA EL DISEÑO O DE UNA PAUTA TERAPÉUTICA Dr. Pedro Guerra López Pautas terapeuticas Objetivos de esta lección. - Conocer el interés clínico de la farmacocinética en general en cuanto
Programa de Acceso Inclusivo, Equidad y Permanencia PAIEP U. de Santiago. Química
 Gases RECUERDEN QUE: En los ejercicios de gases SIEMPRE deben trabajar con la temperatura en K ( C + 273). Además, por conveniencia, en esta unidad cuando hablemos de masa molar en gases, usaremos la sigla
Gases RECUERDEN QUE: En los ejercicios de gases SIEMPRE deben trabajar con la temperatura en K ( C + 273). Además, por conveniencia, en esta unidad cuando hablemos de masa molar en gases, usaremos la sigla
Bases del Deporte Educativo. Sesión 9 Función de carbohidratos, proteínas y grasas en el cuerpo.
 Bases del Deporte Educativo Sesión 9 Función de carbohidratos, proteínas y grasas en el cuerpo. Contextualización En esta sesión aprenderás el beneficio del consumo de proteínas, carbohidratos y grasas
Bases del Deporte Educativo Sesión 9 Función de carbohidratos, proteínas y grasas en el cuerpo. Contextualización En esta sesión aprenderás el beneficio del consumo de proteínas, carbohidratos y grasas
GUÍA DE EJERCICIOS GASES
 GUÍA DE EJERCICIOS GASES Área Química Resultados de aprendizaje Aplicar conceptos básicos de gases en la resolución de ejercicios. Desarrollar pensamiento lógico y sistemático en la resolución de problemas.
GUÍA DE EJERCICIOS GASES Área Química Resultados de aprendizaje Aplicar conceptos básicos de gases en la resolución de ejercicios. Desarrollar pensamiento lógico y sistemático en la resolución de problemas.
La producción de acero en Monterrey N.L. (México) en millones de toneladas, durante el año de 1992 a partir del mes de enero se muestra en la tabla:
 El objetivo al estudiar el concepto razón de cambio, es analizar tanto cuantitativa como cualitativamente las razones de cambio instantáneo y promedio de un fenómeno, lo cual nos permite dar solución a
El objetivo al estudiar el concepto razón de cambio, es analizar tanto cuantitativa como cualitativamente las razones de cambio instantáneo y promedio de un fenómeno, lo cual nos permite dar solución a
ESTIMACION DE LA PRESION DE CONVERGENCIA, CONSTANTE DE EQUILIBRIO Y FASES DEL GAS NATURAL
 República Bolivariana de Venezuela Ministerio del Poder Popular para la Educación Superior Universidad Nacional Experimental Rafael María Baralt Programa: Ingeniería y Tecnología Proyecto: Ingeniería en
República Bolivariana de Venezuela Ministerio del Poder Popular para la Educación Superior Universidad Nacional Experimental Rafael María Baralt Programa: Ingeniería y Tecnología Proyecto: Ingeniería en
URGRAV 2004 LESIÓN PULMONAR INDUCIDA POR EL VENTILADOR. (VILI)
 URGRAV 2004 LESIÓN PULMONAR INDUCIDA POR EL VENTILADOR. (VILI) Dr. Elías Béquer García Hospital Arnaldo Milián Castro. Villa Clara LESIÓN PULMONAR INDUCIDA POR EL VENTILADOR. (VILI) Definición: Lesión
URGRAV 2004 LESIÓN PULMONAR INDUCIDA POR EL VENTILADOR. (VILI) Dr. Elías Béquer García Hospital Arnaldo Milián Castro. Villa Clara LESIÓN PULMONAR INDUCIDA POR EL VENTILADOR. (VILI) Definición: Lesión
Biología General V TRANSPORTE A TRAVÉS DE LA MEMBRANA CELULAR
 Biología General V TRANSPORTE A TRAVÉS DE LA MEMBRANA CELULAR 81 Libardo Ariel Blandón Londoño Biología General TEMA V TRANSPORTE A TRAVÉS DE LA MEMBRANA CELULAR Como habíamos dicho antes, toda célula
Biología General V TRANSPORTE A TRAVÉS DE LA MEMBRANA CELULAR 81 Libardo Ariel Blandón Londoño Biología General TEMA V TRANSPORTE A TRAVÉS DE LA MEMBRANA CELULAR Como habíamos dicho antes, toda célula
Profesora: Teresa Esparza Araña ASPECTOS CUANTITATIVOS DE LA QUÍMICA. UNIDAD 2: Los gases ideales
 Departamento de Física y Química Profesora: Teresa Esparza Araña CEAD P. Félix Pérez Parrilla ASPECTOS CUANTITATIVOS DE LA QUÍMICA UNIDAD 2: Los gases ideales ÍNDICE 1. LOS GASES SEGÚN LA TEORÍA CINÉTICA
Departamento de Física y Química Profesora: Teresa Esparza Araña CEAD P. Félix Pérez Parrilla ASPECTOS CUANTITATIVOS DE LA QUÍMICA UNIDAD 2: Los gases ideales ÍNDICE 1. LOS GASES SEGÚN LA TEORÍA CINÉTICA
BATERIAS CONCEPTOS BASICOS. Conceptos básicos sobre las propiedades de las baterías, indicaciones técnicas, ratio de descarga, potencia y durabilidad.
 BATERIAS CONCEPTOS BASICOS Conceptos básicos sobre las propiedades de las baterías, indicaciones técnicas, ratio de descarga, potencia y durabilidad. 08/02/2012 Página 2 de 8 Contenido 1. INTRODUCCION...
BATERIAS CONCEPTOS BASICOS Conceptos básicos sobre las propiedades de las baterías, indicaciones técnicas, ratio de descarga, potencia y durabilidad. 08/02/2012 Página 2 de 8 Contenido 1. INTRODUCCION...
Problemas resueltos de disoluciones y sus diferentes medidas de concentración.
 UNIVERSIDAD CENTRAL DE VENEZUELA FACULTAD DE CIENCIAS ESCUELA DE QUÍMICA Problemas resueltos de disoluciones y sus diferentes medidas de concentración. 1. Qué es una disolución? Una disolución consiste
UNIVERSIDAD CENTRAL DE VENEZUELA FACULTAD DE CIENCIAS ESCUELA DE QUÍMICA Problemas resueltos de disoluciones y sus diferentes medidas de concentración. 1. Qué es una disolución? Una disolución consiste
UNIDAD 2. CINÉTICA QUÍMICA
 UNIDAD 2. CINÉTICA QUÍMICA Introducción. Velocidad de reacción Cómo se producen las reacciones químicas Ecuación de la velocidad de reacción Factores que afectan a la velocidad de reacción Mecanismo de
UNIDAD 2. CINÉTICA QUÍMICA Introducción. Velocidad de reacción Cómo se producen las reacciones químicas Ecuación de la velocidad de reacción Factores que afectan a la velocidad de reacción Mecanismo de
CAPITULO 5 PROCESO DE SECADO. Se entiende por secado de alimentos la extracción deliberada del agua que contienen,
 CAPITULO 5 PROCESO DE SECADO 5.1 SECADO DE ALIMENTOS Se entiende por secado de alimentos la extracción deliberada del agua que contienen, operación que se lleva a cabo en la mayoría de los casos evaporando
CAPITULO 5 PROCESO DE SECADO 5.1 SECADO DE ALIMENTOS Se entiende por secado de alimentos la extracción deliberada del agua que contienen, operación que se lleva a cabo en la mayoría de los casos evaporando
Profesora: Teresa Esparza Araña LA CANTIDAD DE SUSTANCIA EN QUÍMICA. UNIDAD 6: Los gases ideales
 Departamento de Física y Química Profesora: Teresa Esparza Araña CEAD P. Félix Pérez Parrilla LA CANTIDAD DE SUSTANCIA EN QUÍMICA UNIDAD 6: Los gases ideales 1. LOS GASES SEGÚN LA TEORÍA CINÉTICA DE LA
Departamento de Física y Química Profesora: Teresa Esparza Araña CEAD P. Félix Pérez Parrilla LA CANTIDAD DE SUSTANCIA EN QUÍMICA UNIDAD 6: Los gases ideales 1. LOS GASES SEGÚN LA TEORÍA CINÉTICA DE LA
Bioquímica Tema 2: Soluciones. Unidades Año: 2013
 TEMA 2: SOLUCIONES Al estudio de las soluciones se le asigna gran importancia, teniendo en cuenta que la mayoría de las reacciones químicas ocurren entre soluciones, particularmente en medios acuosos.
TEMA 2: SOLUCIONES Al estudio de las soluciones se le asigna gran importancia, teniendo en cuenta que la mayoría de las reacciones químicas ocurren entre soluciones, particularmente en medios acuosos.
Durante muchos años la anestesia por inhalación se practicó sin los equipos
 FUNCIONAMIENTO Y ELECCIÓN DE LOS CIRCUITOS RESPIRATORIOS DE ANESTESIA M.V María José Caruso Docente Área Anestesiología. Facultad de Ciencias Veterinarias UBA Anestesióloga Hospital Escuela FCV UBA Anestesióloga
FUNCIONAMIENTO Y ELECCIÓN DE LOS CIRCUITOS RESPIRATORIOS DE ANESTESIA M.V María José Caruso Docente Área Anestesiología. Facultad de Ciencias Veterinarias UBA Anestesióloga Hospital Escuela FCV UBA Anestesióloga
ESTADOS DE LA MATERIA
 ESTADOS DE LA MATERIA M en C Alicia Cea Bonilla 1 Existen tres estados de la materia: sólido, líquido y gaseoso, dependiendo de la distancia entre sus partículas, de las fuerzas de atracción entre éstas
ESTADOS DE LA MATERIA M en C Alicia Cea Bonilla 1 Existen tres estados de la materia: sólido, líquido y gaseoso, dependiendo de la distancia entre sus partículas, de las fuerzas de atracción entre éstas
ENOXPRIM. Solución inyectable. Solución inyectable estéril, libre de pirógenos, contenida en jeringas pre-llenadas listas para usarse.
 ENOXPRIM Solución inyectable ENOXAPARINA FORMA FARMACÉUTICA Y FORMULACIÓN Cada jeringa contiene: Enoxaparina sódica 20 mg 40 mg Equivalente a 2,000 U.I. 4,000 U.I. Agua inyectable, c.b.p. 0.2 ml 0.4 ml
ENOXPRIM Solución inyectable ENOXAPARINA FORMA FARMACÉUTICA Y FORMULACIÓN Cada jeringa contiene: Enoxaparina sódica 20 mg 40 mg Equivalente a 2,000 U.I. 4,000 U.I. Agua inyectable, c.b.p. 0.2 ml 0.4 ml
Ley de Boyle. Resumen
 Ley de Boyle Dr. Guillermo Becerra Córdova Universidad Autónoma Chapingo Dpto. de Preparatoria Agrícola Área de Física Profesor-Investigador 5959521500 ext. 5239 E-mail: gllrmbecerra@yahoo.com Km. 38.5
Ley de Boyle Dr. Guillermo Becerra Córdova Universidad Autónoma Chapingo Dpto. de Preparatoria Agrícola Área de Física Profesor-Investigador 5959521500 ext. 5239 E-mail: gllrmbecerra@yahoo.com Km. 38.5
INTRODUCCIÓN. Otras investigaciones mostraron que el incremento de la glicemia basal en ayunas en hipertiroideos fue más alta que en normales (4,5,6).
 INTRODUCCIÓN La alteración en el metabolismo de la glucosa ha sido descrita en pacientes con hipertiroidismo; muchas investigaciones se han realizado al respecto, siendo sus resultados controversiales.
INTRODUCCIÓN La alteración en el metabolismo de la glucosa ha sido descrita en pacientes con hipertiroidismo; muchas investigaciones se han realizado al respecto, siendo sus resultados controversiales.
Determinación de la Masa Molar del Magnesio
 Determinación de la Masa Molar del Magnesio Introducción teórica Como en muchas reacciones químicas, los reactivos o sus productos o ambos son gases, es más común medir éstos en función del volumen usando
Determinación de la Masa Molar del Magnesio Introducción teórica Como en muchas reacciones químicas, los reactivos o sus productos o ambos son gases, es más común medir éstos en función del volumen usando
1. MATERIA Y SU ASPECTO
 1. MATERIA Y SU ASPECTO El aspecto de un sistema material puede variar según el método de observación. Algunos sistemas materiales como la leche, la sangre o la mantequilla a simple vista parecen uniformes,
1. MATERIA Y SU ASPECTO El aspecto de un sistema material puede variar según el método de observación. Algunos sistemas materiales como la leche, la sangre o la mantequilla a simple vista parecen uniformes,
Instituto Carlos Tejedor Educación Secundaria Fisicaquímica Segundo año A Profesor Carlos Castañón. Trabajo Práctico: Leyes de los gases
 Instituto Carlos Tejedor Educación Secundaria Fisicaquímica Segundo año A Profesor Carlos Castañón Trabajo Práctico: Leyes de los gases 1) La ley de Boyle establece que, a temperatura constante, la presión
Instituto Carlos Tejedor Educación Secundaria Fisicaquímica Segundo año A Profesor Carlos Castañón Trabajo Práctico: Leyes de los gases 1) La ley de Boyle establece que, a temperatura constante, la presión
BLOQUE 1: ASPECTOS CUANTATIVOS DE LA QUÍMICA
 BLOQUE 1: ASPECTOS CUANTATIVOS DE LA QUÍMICA Unidad 2: Los gases ideales Teresa Esparza araña 1 Índice 1. Los estados de agregación de la materia a. Los estados de la materia b. Explicación según la teoría
BLOQUE 1: ASPECTOS CUANTATIVOS DE LA QUÍMICA Unidad 2: Los gases ideales Teresa Esparza araña 1 Índice 1. Los estados de agregación de la materia a. Los estados de la materia b. Explicación según la teoría
GASES. Contenidos. Leyes de los gases y su aplicación en la resolución de problemas numéricos.
 GASES Contenidos Postulados de la teoría cinética de los gases y su relación con las características (expansión, comprensión y difusión) y las propiedades ( presión, volumen y temperatura) que los definen.
GASES Contenidos Postulados de la teoría cinética de los gases y su relación con las características (expansión, comprensión y difusión) y las propiedades ( presión, volumen y temperatura) que los definen.
Teoría Disoluciones Fórmula empírica y molecular Física y Química. 1º bachiller DISOLUCIONES
 Teoría Disoluciones Fórmula empírica y molecular Física y Química. 1º bachiller 18-1-2015 CONCEPTO DE DISOLUCIÓN DISOLUCIONES Una disolución es una mezcla homogénea de sustancias en igual o distintos estados
Teoría Disoluciones Fórmula empírica y molecular Física y Química. 1º bachiller 18-1-2015 CONCEPTO DE DISOLUCIÓN DISOLUCIONES Una disolución es una mezcla homogénea de sustancias en igual o distintos estados
INTERPRETACION DE LOS GASES ARTERIALES
 INTERPRETACION DE LOS GASES ARTERIALES ph PaO2 PaCO2 HCO3 BE Hb SaO2 Bloque 6 Modulo 2 Dr Erick Valencia Anestesiologo Intensivista. Que son los Gases Arteriales? Una muestra de sangre anticoagulada que
INTERPRETACION DE LOS GASES ARTERIALES ph PaO2 PaCO2 HCO3 BE Hb SaO2 Bloque 6 Modulo 2 Dr Erick Valencia Anestesiologo Intensivista. Que son los Gases Arteriales? Una muestra de sangre anticoagulada que
Guía de Problemas de Equilibrio de Fases Métodos de estimación de coeficientes de actividad Termodinámica de Ingeniería Química
 Guía de Problemas de Equilibrio de Fases Métodos de estimación de coeficientes de actividad Termodinámica de Ingeniería Química Profesor: Julio Romero F. Ayudante: Francisca Luna F. Problema 1 Calcule
Guía de Problemas de Equilibrio de Fases Métodos de estimación de coeficientes de actividad Termodinámica de Ingeniería Química Profesor: Julio Romero F. Ayudante: Francisca Luna F. Problema 1 Calcule
Laboratorio de Física para Ingeniería
 Laboratorio de para Ingeniería 1. Al medir la longitud de un cilindro se obtuvieron las siguientes medidas: x [cm] 8,45 8,10 8,40 8,55 8,45 8,30 Al expresar la medida en la forma x = x + x resulta: (a)
Laboratorio de para Ingeniería 1. Al medir la longitud de un cilindro se obtuvieron las siguientes medidas: x [cm] 8,45 8,10 8,40 8,55 8,45 8,30 Al expresar la medida en la forma x = x + x resulta: (a)
Aparato circulatorio: Transporta el oxígeno y los nutrientes a todas las células, y recoge el CO 2 y los desechos. ~ 1 ~
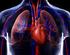 PUNTO 1º - APARATOS IMPLICADOS EN LA NUTRICIÓN Los aparatos implicados en la nutrición son : Aparato digestivo: Digiere los alimentos y los transforma en nutrientes. Aparato respiratorio: Se ocupa del
PUNTO 1º - APARATOS IMPLICADOS EN LA NUTRICIÓN Los aparatos implicados en la nutrición son : Aparato digestivo: Digiere los alimentos y los transforma en nutrientes. Aparato respiratorio: Se ocupa del
Organización Funcional y el Medio Interno
 Organización Funcional y el Medio Interno Aproximadamente el 50 % del cuerpo humano es líquido y la mayor parte es intracelular, la tercera parte es extracelular, la misma que se encuentra en movimiento
Organización Funcional y el Medio Interno Aproximadamente el 50 % del cuerpo humano es líquido y la mayor parte es intracelular, la tercera parte es extracelular, la misma que se encuentra en movimiento
TEMA 1: SISTEMAS MODELADOS POR ECUACIONES DIFERENCIALES EN INGENIERÍA QUÍMICA. CLASIFICACIÓN. GENERALIDADES.
 TEMA 1: SISTEMAS MODELADOS POR ECUACIONES DIFERENCIALES EN INGENIERÍA QUÍMICA. CLASIFICACIÓN. GENERALIDADES. 1. INTRODUCCIÓN. PLANTEAMIENTO DE PROBLEMAS EN INGENIERÍA QUÍMICA 2. PROBLEMAS EXPRESADOS MEDIANTE
TEMA 1: SISTEMAS MODELADOS POR ECUACIONES DIFERENCIALES EN INGENIERÍA QUÍMICA. CLASIFICACIÓN. GENERALIDADES. 1. INTRODUCCIÓN. PLANTEAMIENTO DE PROBLEMAS EN INGENIERÍA QUÍMICA 2. PROBLEMAS EXPRESADOS MEDIANTE
NUTRICION PARENTERAL DEL RECIEN NACIDO. Dra. Reina Valdés Armenteros Hospital América Arias
 NUTRICION PARENTERAL DEL RECIEN Dra. Reina Valdés Armenteros Hospital América Arias PRINCIPIOS EN LA NUTRICIÓN DEL RECIÉN No debe suprimirse el aporte de nutrientes al nacimiento. Proteínas y energía son
NUTRICION PARENTERAL DEL RECIEN Dra. Reina Valdés Armenteros Hospital América Arias PRINCIPIOS EN LA NUTRICIÓN DEL RECIÉN No debe suprimirse el aporte de nutrientes al nacimiento. Proteínas y energía son
LA NUTRICIÓN EN LAS PLANTAS
 LA NUTRICIÓN EN LAS PLANTAS LOS SERES VIVOS COMO SISTEMAS LA NUTRICIÓN COMO INTERCAMBIO DE MATERIA Y ENERGÍA LOS ORGANISMOS SEGÚN LA FORMA DE OBTENER LA ENERGÍA PROCESOS EN LA NUTRICIÓN EN LAS PLANTAS
LA NUTRICIÓN EN LAS PLANTAS LOS SERES VIVOS COMO SISTEMAS LA NUTRICIÓN COMO INTERCAMBIO DE MATERIA Y ENERGÍA LOS ORGANISMOS SEGÚN LA FORMA DE OBTENER LA ENERGÍA PROCESOS EN LA NUTRICIÓN EN LAS PLANTAS
PROTOCOLO DE OXIGENOTERAPIA EN LA INSUFICIENCIA RESPIRATORIA AGUDA
 PROTOCOLO DE OXIGENOTERAPIA EN LA INSUFICIENCIA RESPIRATORIA Página 1 de 8 ÍNDICE 1) Objeto. 2 2) Profesionales implicados. 2 3) Población diana. 2 4) Desarrollo. 2 5) Indicadores de evaluación. 8 6) Control
PROTOCOLO DE OXIGENOTERAPIA EN LA INSUFICIENCIA RESPIRATORIA Página 1 de 8 ÍNDICE 1) Objeto. 2 2) Profesionales implicados. 2 3) Población diana. 2 4) Desarrollo. 2 5) Indicadores de evaluación. 8 6) Control
Práctica No 12. Determinación experimental de la Presión de vapor de un líquido puro
 Práctica No 12 Determinación experimental de la Presión de vapor de un líquido puro 1. Objetivo general: Evaluar la entalpía de vaporización mediante el modelo de Clausius y Clapeyron. 2. Marco teórico:
Práctica No 12 Determinación experimental de la Presión de vapor de un líquido puro 1. Objetivo general: Evaluar la entalpía de vaporización mediante el modelo de Clausius y Clapeyron. 2. Marco teórico:
QUIMICA UNIVERSIDAD DE BURGOS QUÍMICA GUÍA DOCENTE Denominación de la asignatura: QUIMICA. Titulación
 GUÍA DOCENTE 2012-2013 QUIMICA 1. Denominación de la asignatura: QUIMICA Titulación Ingeniería Electrónica Industrial y Automática Código 6400 2. Materia o módulo a la que pertenece la asignatura: Química
GUÍA DOCENTE 2012-2013 QUIMICA 1. Denominación de la asignatura: QUIMICA Titulación Ingeniería Electrónica Industrial y Automática Código 6400 2. Materia o módulo a la que pertenece la asignatura: Química
Nutrición Vegetal. Absorción de sales minerales
 Nutrición Vegetal Absorción de sales minerales Absorción - Es el proceso mediante el cual un ión o molécula ingresa a una célula o un cuerpo a través de una membrana. No intervienen fuerzas intermoleculares.
Nutrición Vegetal Absorción de sales minerales Absorción - Es el proceso mediante el cual un ión o molécula ingresa a una célula o un cuerpo a través de una membrana. No intervienen fuerzas intermoleculares.
OXIGENOTERAPIA II JORNADAS INTERNACIONALES DE INVESTIGACIÓN EN EDUCACIÓN Y SALUD:
 OXIGENOTERAPIA II JORNADAS INTERNACIONALES DE INVESTIGACIÓN EN EDUCACIÓN Y SALUD: "Experiencias en educación y salud transcultural" AUTORES: Fernández Sánchez, Pedro. Diplomado en enfermería. Hospital
OXIGENOTERAPIA II JORNADAS INTERNACIONALES DE INVESTIGACIÓN EN EDUCACIÓN Y SALUD: "Experiencias en educación y salud transcultural" AUTORES: Fernández Sánchez, Pedro. Diplomado en enfermería. Hospital
EQUILIBRIO QUÍMICO. 1. Equilibrio químico. 2. La constante de equilibrio. 3. EL principio de LeChatelier. Química 2º bachillerato Equilibrio químico 1
 EQUILIBRIO QUÍMICO 1. Equilibrio químico. 2. La constante de equilibrio. 3. EL principio de LeChatelier. Química 2º bachillerato Equilibrio químico 1 0. CONOCIMIENTOS Los conocimientos previos que son
EQUILIBRIO QUÍMICO 1. Equilibrio químico. 2. La constante de equilibrio. 3. EL principio de LeChatelier. Química 2º bachillerato Equilibrio químico 1 0. CONOCIMIENTOS Los conocimientos previos que son
UNIDAD 1 La materia y sus cambios
 UNIDAD 1 La materia y sus cambios Tema 1.3 Propiedades características de las sustancias: físicas, organolépticas, químicas; intensivas y extensivas. NMLV 1 Propiedades de las sustancias Organolépticas
UNIDAD 1 La materia y sus cambios Tema 1.3 Propiedades características de las sustancias: físicas, organolépticas, químicas; intensivas y extensivas. NMLV 1 Propiedades de las sustancias Organolépticas
1. Qué es la hipertensión arterial?
 1. Qué es la hipertensión arterial? Es una elevación mantenida de la presión arterial (mal llamada tensión arterial ) cuyas cifras están permanentemente igual o por encima de 140 mmhg de presión sistólica
1. Qué es la hipertensión arterial? Es una elevación mantenida de la presión arterial (mal llamada tensión arterial ) cuyas cifras están permanentemente igual o por encima de 140 mmhg de presión sistólica
CLASIFICACIÓN DE LA MATERIA
 1. Clasificación de la materia por su aspecto CLASIFICACIÓN DE LA MATERIA La materia homogénea es la que presenta un aspecto uniforme, en la cual no se pueden distinguir a simple vista sus componentes.
1. Clasificación de la materia por su aspecto CLASIFICACIÓN DE LA MATERIA La materia homogénea es la que presenta un aspecto uniforme, en la cual no se pueden distinguir a simple vista sus componentes.
ANTICONCEPCIÓN EN MUJERES CON PATOLOGÍA VASCULAR CEREBRAL
 ANTICONCEPCIÓN EN MUJERES CON PATOLOGÍA VASCULAR CEREBRAL Dr. Eduardo López-Arregui Clínica Euskalduna. Bilbao. cambiando actitudes 9º Congreso S.E.C. Sevilla. PATOLOGÍA VASCULAR CEREBRAL * HIPOXIA......ISQUEMIA......INFARTO
ANTICONCEPCIÓN EN MUJERES CON PATOLOGÍA VASCULAR CEREBRAL Dr. Eduardo López-Arregui Clínica Euskalduna. Bilbao. cambiando actitudes 9º Congreso S.E.C. Sevilla. PATOLOGÍA VASCULAR CEREBRAL * HIPOXIA......ISQUEMIA......INFARTO
Fisiopatología del aparato respiratorio II _ Pruebas complementarias
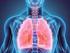 Fisiopatología del aparato respiratorio II _ Pruebas complementarias Gasometría arterial (GSA) Gasometría arterial: Punción de una arteria periférica Determina el equilibrio ácido-base: - ph - Las concentraciones
Fisiopatología del aparato respiratorio II _ Pruebas complementarias Gasometría arterial (GSA) Gasometría arterial: Punción de una arteria periférica Determina el equilibrio ácido-base: - ph - Las concentraciones
-aproximadamente 60% del organismo humano. -componente mas abundante en la mayoría de los alimentos
 EL AGUA -aproximadamente 60% del organismo humano -componente mas abundante en la mayoría de los alimentos -responsable del carácter apetecible de muchos alimentos y también de la aptitud al deterioro
EL AGUA -aproximadamente 60% del organismo humano -componente mas abundante en la mayoría de los alimentos -responsable del carácter apetecible de muchos alimentos y también de la aptitud al deterioro
LOS GASES Y LAS DISOLUCIONES. Departamento de Física y Química 3º ESO
 LOS GASES Y LAS DISOLUCIONES Departamento de Física y Química 3º ESO 0. Mapa conceptual SÓLIDO ESTADOS DE LA MATERIA LÍQUIDO Presión atmosférica GAS Solubilidad Disolución saturada Disoluciones Soluto
LOS GASES Y LAS DISOLUCIONES Departamento de Física y Química 3º ESO 0. Mapa conceptual SÓLIDO ESTADOS DE LA MATERIA LÍQUIDO Presión atmosférica GAS Solubilidad Disolución saturada Disoluciones Soluto
GASES - PREGUNTAS DE TEST (2016) En la última página se ofrecen las soluciones
 GASES - PREGUNTAS DE TEST (2016) En la última página se ofrecen las soluciones Grupo A - CONCEPTOS GENERALES: CONCEPTO DE GAS Y VAPOR Grupo B - LEYES GENERALES DE LOS GASES IDEALES: Grupo C- LEY DE GRAHAM
GASES - PREGUNTAS DE TEST (2016) En la última página se ofrecen las soluciones Grupo A - CONCEPTOS GENERALES: CONCEPTO DE GAS Y VAPOR Grupo B - LEYES GENERALES DE LOS GASES IDEALES: Grupo C- LEY DE GRAHAM
Sistema de administración
 Sistema de administración El sistema de alto flujo: El flujo total de gas que suministra el equipo es suficiente para proporcionar la totalidad del gas inspirado Utilizan el mecanismo Venturi para tomar
Sistema de administración El sistema de alto flujo: El flujo total de gas que suministra el equipo es suficiente para proporcionar la totalidad del gas inspirado Utilizan el mecanismo Venturi para tomar
Estadística Inferencial. Estadística Descriptiva
 INTRODUCCIÓN Estadística: Ciencia que trata sobre la teoría y aplicación de métodos para coleccionar, representar, resumir y analizar datos, así como realizar inferencias a partir de ellos. Recogida y
INTRODUCCIÓN Estadística: Ciencia que trata sobre la teoría y aplicación de métodos para coleccionar, representar, resumir y analizar datos, así como realizar inferencias a partir de ellos. Recogida y
FÍSICA APLICADA Y FISICOQUÍMICA I. Tema 2. El Primer Principio de la Termodinámica
 María del Pilar García Santos GRADO EN FARMACIA FÍSICA APLICADA Y FISICOQUÍMICA I Tema 2 El Primer Principio de la Termodinámica Esquema Tema 2. Primer Principio de la Termodinámica 2.1 Primer Principio
María del Pilar García Santos GRADO EN FARMACIA FÍSICA APLICADA Y FISICOQUÍMICA I Tema 2 El Primer Principio de la Termodinámica Esquema Tema 2. Primer Principio de la Termodinámica 2.1 Primer Principio
ABSORCION, DISTRIBUCION, METABOLISMO Y ELIMINACION DE MEDICAMENTOS. Farm. B. L. Zylbersztajn
 ABSORCION, DISTRIBUCION, METABOLISMO Y ELIMINACION DE MEDICAMENTOS Farm. B. L. Zylbersztajn Farmacocinética Estudia el movimiento del fármaco en el individuo. Farmacocinética LADME Liberación El fármaco
ABSORCION, DISTRIBUCION, METABOLISMO Y ELIMINACION DE MEDICAMENTOS Farm. B. L. Zylbersztajn Farmacocinética Estudia el movimiento del fármaco en el individuo. Farmacocinética LADME Liberación El fármaco
CENTRO REGIONAL UNIVERSITARIO BARILOCHE TALLER DE MATEMATICA INGRESO 2016 LIC. ENFERMERÍA PRACTICO UNIDAD 3
 PRACTICO UNIDAD 3 Nota: Los ejercicios propuestos en los prácticos deben servirle para afianzar y practicar temas. Si nota que algunos ejercicios ya los sabe hacer bien, continúe con otros que le impliquen
PRACTICO UNIDAD 3 Nota: Los ejercicios propuestos en los prácticos deben servirle para afianzar y practicar temas. Si nota que algunos ejercicios ya los sabe hacer bien, continúe con otros que le impliquen
UNIVERSIDAD DE ANTIOQUIA FACULTAD DE QUÍMICA FARMACÉUTICA LABORATORIO DE QUÍMICA GENERAL Profesor: Jaime O. Pérez
 UNIVERSIDAD DE ANTIOQUIA FACULTAD DE QUÍMICA FARMACÉUTICA LABORATORIO DE QUÍMICA GENERAL Profesor: Jaime O. Pérez Práctica: Determinación de Densidades. Fecha: 24 de noviembre de 2009 DEYMER GÓMEZ CORREA:
UNIVERSIDAD DE ANTIOQUIA FACULTAD DE QUÍMICA FARMACÉUTICA LABORATORIO DE QUÍMICA GENERAL Profesor: Jaime O. Pérez Práctica: Determinación de Densidades. Fecha: 24 de noviembre de 2009 DEYMER GÓMEZ CORREA:
EQUILIBRIO ÁCIDO-BASE
 EQUILIBRIO ÁCIDO-BASE - Departamento de Fisiopatología - Facultad de Medicina Br. Inés Lujambio CONCEPTOS BÁSICOS. Ácido: toda sustancias capaz de ceder protones de hidrógeno (H + ). HCl H + + Cl - Base:
EQUILIBRIO ÁCIDO-BASE - Departamento de Fisiopatología - Facultad de Medicina Br. Inés Lujambio CONCEPTOS BÁSICOS. Ácido: toda sustancias capaz de ceder protones de hidrógeno (H + ). HCl H + + Cl - Base:
Capítulo 6. Valoración respiratoria
 498 Capítulo 6. Valoración respiratoria 6.19. La respiración. Intercambio gaseoso y modificaciones durante el esfuerzo 6.19 La respiración. Intercambio gaseoso y modificaciones durante el esfuerzo 499
498 Capítulo 6. Valoración respiratoria 6.19. La respiración. Intercambio gaseoso y modificaciones durante el esfuerzo 6.19 La respiración. Intercambio gaseoso y modificaciones durante el esfuerzo 499
Titulaciones en Química Analítica. Capítulo 13 CHEM 3320 Rosamil Rey Santos, Ph.D.
 Titulaciones en Química Analítica Capítulo 13 CHEM 3320 Rosamil Rey Santos, Ph.D. Introducción En el análisis volumétrico, la concentración se determina midiendo su capacidad de reaccionar con un reactivo
Titulaciones en Química Analítica Capítulo 13 CHEM 3320 Rosamil Rey Santos, Ph.D. Introducción En el análisis volumétrico, la concentración se determina midiendo su capacidad de reaccionar con un reactivo
Anestesiología. Anestesia inhalatoria
 Anestesiología Anestesia inhalatoria Objetivo del Tema Conocer y comprender el efecto de los principales fármacos f anestésicos sicos inhalatorios y los equipos necesarios para su administración Premedicación
Anestesiología Anestesia inhalatoria Objetivo del Tema Conocer y comprender el efecto de los principales fármacos f anestésicos sicos inhalatorios y los equipos necesarios para su administración Premedicación
Guía de estudio y prueba de conocimientos sobre: CAPITULO 4: Fluidos Hidrostáticos
 Guía de estudio y prueba de conocimientos sobre: CAPITULO 4: Fluidos Hidrostáticos Sección 901. Nombre: Cuenta: Nombre: Cuenta: Instrucciones: Contesta lo que se te pide clara y ordenadamente, si necesitas
Guía de estudio y prueba de conocimientos sobre: CAPITULO 4: Fluidos Hidrostáticos Sección 901. Nombre: Cuenta: Nombre: Cuenta: Instrucciones: Contesta lo que se te pide clara y ordenadamente, si necesitas
b) Aplicar la regla de las fases a cada una de las regiones, líneas y puntos significativos y determina el número de grados de libertad existentes.
 1.- El platino y el oro son totalmente solubles en estado sólido y en estado líquido. El punto de fusión del platino son 1774 C y el del oro 1063 C. Una aleación formada por un 40% de oro comienza a solidificar
1.- El platino y el oro son totalmente solubles en estado sólido y en estado líquido. El punto de fusión del platino son 1774 C y el del oro 1063 C. Una aleación formada por un 40% de oro comienza a solidificar
Terapia Inhalatoria en la EPOC. D.U.E. Jose Luis Valera Enfermero del Gabinete de Función Respiratoria Hospital Son Espases
 Terapia Inhalatoria en la EPOC D.U.E. Jose Luis Valera Enfermero del Gabinete de Función Respiratoria Hospital Son Espases Definición de EPOC La Enfermedad Pulmonar Obstructiva Crónica (EPOC) se define
Terapia Inhalatoria en la EPOC D.U.E. Jose Luis Valera Enfermero del Gabinete de Función Respiratoria Hospital Son Espases Definición de EPOC La Enfermedad Pulmonar Obstructiva Crónica (EPOC) se define
Aparatos que intervienen en la nutrición
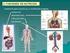 Aparatos que intervienen en la nutrición El ser humano necesita ingerir alimentos y agua diariamente, para el mantenimiento de sus constantes vitales. De los alimentos se utilizan distintos nutrientes,
Aparatos que intervienen en la nutrición El ser humano necesita ingerir alimentos y agua diariamente, para el mantenimiento de sus constantes vitales. De los alimentos se utilizan distintos nutrientes,
Proporciona el oxígeno que el cuerpo necesita y elimina el dióxido de carbono o gas carbónico que se produce en todas las células.
 Proporciona el oxígeno que el cuerpo necesita y elimina el dióxido de carbono o gas carbónico que se produce en todas las células. La respiración es un proceso involuntario y automático, en que se extrae
Proporciona el oxígeno que el cuerpo necesita y elimina el dióxido de carbono o gas carbónico que se produce en todas las células. La respiración es un proceso involuntario y automático, en que se extrae
MÓDULO III. MEDIDAS DE TENDENCIA CENTRAL, DISPERSIÓN Y ASIMETRÍA
 1 UNIVERSIDAD NACIONAL EXPERIMENTAL DE LOS LLANOS OCCIDENTALES EZEQUIEL ZAMORA VICE-RECTORADO DE PLANIFICACIÓN Y DESARROLLO SOCIAL PROGRAMA CIENCIAS SOCIALES Y JURIDICAS SUBPROGRAMA ADMINISTRACIÓN SUBPROYECTO:
1 UNIVERSIDAD NACIONAL EXPERIMENTAL DE LOS LLANOS OCCIDENTALES EZEQUIEL ZAMORA VICE-RECTORADO DE PLANIFICACIÓN Y DESARROLLO SOCIAL PROGRAMA CIENCIAS SOCIALES Y JURIDICAS SUBPROGRAMA ADMINISTRACIÓN SUBPROYECTO:
Respuesta: a) La fracción molar de NaCl es 0,072 b) La concentración másica volumétrica de NaCl es 0,231 g/cc
 Ejercicio 1: La densidad a 4 ºC de una solución acuosa de NaCl al 20% en peso es 1,155 g/cc a) Calcule la fracción molar de NaCl b) Calcule la concentración másica volumétrica de NaCl La masa molecular
Ejercicio 1: La densidad a 4 ºC de una solución acuosa de NaCl al 20% en peso es 1,155 g/cc a) Calcule la fracción molar de NaCl b) Calcule la concentración másica volumétrica de NaCl La masa molecular
Apuntes Disoluciones
 Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos a más sustancias. En las disoluciones hay que distinguir el soluto, el disolvente y la propia disolución
Una disolución es una mezcla homogénea (los componentes no se pueden distinguir a simple vista) de dos a más sustancias. En las disoluciones hay que distinguir el soluto, el disolvente y la propia disolución
Importancia del ph y la Conductividad Eléctrica (CE) en los sustratos para plantas
 2 Importancia del ph y la Conductividad Eléctrica (CE) en los sustratos para plantas Importancia del ph y la Conductividad Eléctrica (CE) en los sustratos para plantas ph El ph es una medida de la acidez
2 Importancia del ph y la Conductividad Eléctrica (CE) en los sustratos para plantas Importancia del ph y la Conductividad Eléctrica (CE) en los sustratos para plantas ph El ph es una medida de la acidez
CAPITULO V TERMODINAMICA - 115 -
 CAPIULO V ERMODINAMICA - 5 - 5. EL GAS IDEAL Es el conjunto de un gran número de partículas diminutas o puntuales, de simetría esférica, del mismo tamaño y de igual volumen, todas del mismo material. Por
CAPIULO V ERMODINAMICA - 5 - 5. EL GAS IDEAL Es el conjunto de un gran número de partículas diminutas o puntuales, de simetría esférica, del mismo tamaño y de igual volumen, todas del mismo material. Por
Pregunta 1. Pregunta 2. Pregunta 3. Pregunta 4. Pregunta 5. Pregunta 6. Pregunta 7. Comenzado el lunes, 25 de marzo de 2013, 17:24
 Comenzado el lunes, 25 de marzo de 2013, 17:24 Estado Finalizado Finalizado en sábado, 30 de marzo de 2013, 17:10 Tiempo empleado 4 días 23 horas Puntos 50,00/50,00 Calificación 10,00 de un máximo de 10,00
Comenzado el lunes, 25 de marzo de 2013, 17:24 Estado Finalizado Finalizado en sábado, 30 de marzo de 2013, 17:10 Tiempo empleado 4 días 23 horas Puntos 50,00/50,00 Calificación 10,00 de un máximo de 10,00
Hidrodinámica. Conceptos
 Conceptos Hidrostática tica Caudal Es la cantidad de líquido que pasa en un cierto tiempo. Concretamente, el caudal sería el volumen de líquido que circula dividido el tiempo: Sus unidades son volumen
Conceptos Hidrostática tica Caudal Es la cantidad de líquido que pasa en un cierto tiempo. Concretamente, el caudal sería el volumen de líquido que circula dividido el tiempo: Sus unidades son volumen
GUIA DE EJERCICIOS (Equilibrio Químico y Cinética Química Empírica)
 Universidad de Santiago de Chile Departamento de Ingeniería Química GUIA DE EJERCICIOS (Equilibrio Químico y Cinética Química Empírica) Autor: Prof. Julio Romero 1. Describa aplicando el principio de Le
Universidad de Santiago de Chile Departamento de Ingeniería Química GUIA DE EJERCICIOS (Equilibrio Químico y Cinética Química Empírica) Autor: Prof. Julio Romero 1. Describa aplicando el principio de Le
C: GASES Y PRESIÓN DE VAPOR DEL AGUA
 hecho el vacío. Calcula a) Cantidad de gas que se tiene ; b) la presión en los dos recipientes después de abrir la llave de paso y fluir el gas de A a B, si no varía la temperatura. C) Qué cantidad de
hecho el vacío. Calcula a) Cantidad de gas que se tiene ; b) la presión en los dos recipientes después de abrir la llave de paso y fluir el gas de A a B, si no varía la temperatura. C) Qué cantidad de
El sistema respiratorio
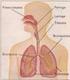 El sistema respiratorio Así como es indispensable incorporar materia del medio, también es importante liberar la energía química que se encuentra almacenada en las distintas moléculas orgánicas incorporadas.
El sistema respiratorio Así como es indispensable incorporar materia del medio, también es importante liberar la energía química que se encuentra almacenada en las distintas moléculas orgánicas incorporadas.
Efecto de diferentes intervalos entre partos y producción por lactancia sobre la productividad esperada por hectárea.
 Efecto de diferentes intervalos entre partos y producción por lactancia sobre la productividad esperada por hectárea. Ing. Agr. Roberto Rubio Introducción En las situaciones productivas de los tambos el
Efecto de diferentes intervalos entre partos y producción por lactancia sobre la productividad esperada por hectárea. Ing. Agr. Roberto Rubio Introducción En las situaciones productivas de los tambos el
So S l o u l c u i c o i n o e n s e
 Soluciones SOLUCIONES mezclas homogéneas de dos sustancias: SOLUTO SOLVENTE SEGÚN EL ESTADO FISICO DEL SOLVENTE SOLIDA LIQUIDA GASEOSA Cuando un sólido se disuelve en un líquido las partículas que lo
Soluciones SOLUCIONES mezclas homogéneas de dos sustancias: SOLUTO SOLVENTE SEGÚN EL ESTADO FISICO DEL SOLVENTE SOLIDA LIQUIDA GASEOSA Cuando un sólido se disuelve en un líquido las partículas que lo
