Ayuda para el diagnóstico de la infección tuberculosa PROSPECTO. Para diagnóstico in vitro. Este prospecto se refiere al uso de:
|
|
|
- Juan Bustamante Aguilar
- hace 6 años
- Vistas:
Transcripción
1 Ayuda para el diagnóstico de la infección tuberculosa PROSPECTO Para diagnóstico in vitro Este prospecto se refiere al uso de: T-SPOT.TB 8 (Formato de placa con tira de 8 pocillos multiuso. Número de catálogo: TB.300) PI-TB-IVD-ES-V2
2 Índice Página Uso previsto 2 Introducción 2 Principios del procedimiento 2 Limitaciones 3 Advertencias y precauciones de seguridad 4 Materiales suministrados 4 Conservación 4 Estabilidad 5 Equipo y materiales requeridos pero no suministrados 5 Preparación de los reactivos 5 Procedimiento 6 Recogida y preparación de las muestras 6 Recuento celular y dilución 8 Preparación e incubación de la placa 8 Revelado y recuento de las manchas 9 Control de calidad 10 Interpretación de los resultados y criterios de análisis 11 Características de productividad del análisis 11 Bibliografía 12 Glosario de símbolos 12 1 PI-TB-IVD-ES-V2
3 Uso previsto El análisis T-SPOT.TB es una prueba diagnóstica in vitro para la detección de células T efectoras que responden a la estimulación por antígenos de Mycobacterium tuberculosis que está diseñada para facilitar el diagnóstico de la infección tuberculosa (TB). El análisis T-SPOT.TB es una versión simplificada del método de análisis inmunoenzimático (ELISPOT) de recuento individual de células T efectoras activadas específicas de la TB. Introducción La Organización Mundial de la Salud estima que un tercio de la población mundial está infectada por M. tuberculosis. Cada persona portadora de infección tuberculosa latente (ITBL) tiene una probabilidad de aproximadamente el 10% de evolucionar hacia la enfermedad activa. Esta tasa de evolución es más alta en determinados grupos, como los infectados recientemente o los que tienen el sistema inmunitario debilitado. La respuesta inmunitaria a la infección por M. tuberculosis es predominantemente una respuesta inmunitaria mediada por células (IMC). Como parte de esta respuesta, las células T están sensibilizadas a los antígenos de M. tuberculosis. Las células T efectoras activadas, tanto CD4 como CD8, separadas específicamente de la sangre, pueden contarse por su capacidad para ser estimuladas in vitro por dichos antígenos 1,2. El uso de antígenos seleccionados para el complejo M. tuberculosis (M. tuberculosis, M. bovis, M. africanum, M. microti, M. canetti) mejora la especificidad del análisis para estos microorganismos al reducir la reactividad cruzada con la vacuna BCG y con casi todas las micobacterias ambientales 3,4. Se utilizan dos paneles separados de antígenos, que simulan las proteínas ESAT-6 y CFP10 bien definidas, para optimizar la sensibilidad de la prueba. El análisis T-SPOT.TB es una variante simplificada de la técnica ELISPOT. El ensayo ELISPOT tiene una sensibilidad excepcional porque la diana citocina es capturada directamente en torno a la célula que la secreta, antes de que se diluya en el sobrenadante, capturada por células contiguas o degradada. Esto hace que el método ELISPOT sea mucho más sensible que el tradicional ELISA 5. El análisis T-SPOT.TB se ha diseñado para la detección de células T efectoras que responden a la estimulación por antígenos específicos de M. tuberculosis 3,4,6-9. El análisis recuenta células T activadas específicas de TB. Es adecuado para usarse en todos los pacientes con riesgo de ITBL o sospecha de infección tuberculosa 10,11, con independencia de su edad, sexo, origen étnico, tratamiento o estado inmunitario. Principios del procedimiento Se separan los mononucleares de sangre periférica (MNSP) de una muestra de sangre total y se lavan para eliminar cualquier fuente de fondo que pueda provocar interferencias. A continuación se cuentan los MNSP para garantizar que en el ensayo se usa un número normalizado de células. Esto asegura que incluso quienes presentan títulos bajos de células T debido al debilitamiento del sistema inmunitario (pacientes inmunodeprimidos e inmunosuprimidos) aporten un número suficiente de células a pocillos de microtitulación. Las etapas de lavado y recuento y la técnica ELISPOT están en el origen del superior rendimiento de detección de la enfermedad tuberculosa y de la infección tuberculosa latente. Para cada muestra se requieren cuatro pocillos (véase la Figura 1): 1. Un Control Nulo para identificar la activación celular inespecífica. 2. Antígenos específicos de la TB, Panel A (ESAT-6). 3. Antígenos específicos de la TB, Panel B (CFP10). 4. Un Control Positivo con una fitohemaglutinina (PHA, un conocido activador policlonal 12 ) para confirmar la funcionalidad de los MNSP. 2 PI-TB-IVD-ES-V2
4 Recogida sangre venosa periférica Centrifugado Plasma MNSP Eritrocitos Separación de MNSP, lavado y recuento Incubación durante una noche Pocillos recubiertos previamente Adición de MNSP y antígenos a 4 pocillos Lavado, revelado y secado de la placa Recuento de manchas coloreadas en cada pocillo Figura 1: Principales etapas del análisis T-SPOT.TB. Recuérdese que cada placa tiene 96 pocillos. Los MNSP se incuban con los antígenos para permitir la estimulación de cualquier célula T sensibilizada presente. La citocina secretada es capturada por anticuerpos específicos de la membrana, que forma la base del pocillo, y se eliminan las células y otros materiales no deseados mediante lavado. Se añade un segundo anticuerpo, conjugado con fosfatasa alcalina y dirigido contra un epítopo diferente de la molécula de citocina, que se une a la citocina capturada en la superficie de la membrana. Todo conjugado no ligado se elimina mediante lavado. Se añade un sustrato soluble a cada pocillo; el sustrato es escindido por la enzima ligada para formar una mancha de precipitado insoluble en el punto de reacción. Cada mancha representa la huella de una célula T individual secretora de citocinas y la evaluación del número de manchas obtenidas determina la abundancia de células T efectoras sensibles a M. tuberculosis en sangre periférica. Limitaciones Para uso diagnóstico in vitro. Para uso profesional. El kit T-SPOT.TB 96 está diseñado para un único uso, mientras que el kit T-SPOT.TB 8 es para multiuso. No mezclar componentes de diferentes lotes de kit. Léanse cuidadosamente las instrucciones del análisis antes de usarlo. Obsérvese una técnica aséptica para evitar la contaminación de los reactivos, los pocillos de análisis, las suspensiones de células y los medios de cultivo celular. Las variaciones respecto de lo establecido en cuanto a técnicas de pipeteado y lavado, tiempos de incubación y/o temperaturas pueden influir sobre los resultados reales obtenidos, por lo que deberán evitarse. La sangre se obtendrá y procesará para su análisis en un plazo de 8 horas. Esta limitación de tiempo se puede resolver utilizando el reactivo T-Cell Xtend (comercializado por Oxford Immunotec). Cuando se usa el reactivo T-Cell Xtend con el análisis T-SPOT.TB, el tiempo de conservación de la muestra aumenta hasta 32 horas. Conservar las muestras de sangre y transportarlas al laboratorio a temperatura ambiente (18-25 C). Si se utiliza el reactivo T-Cell Xtend, las muestras pueden transportarse y conservarse a C. No refrigerar ni congelar las muestras de sangre total. El análisis T-SPOT.TB se utilizará e interpretará exclusivamente como parte del cuadro clínico global. Un resultado negativo no descarta la posibilidad de exposición o infección por M. tuberculosis. 3 PI-TB-IVD-ES-V2
5 Los antígenos ESAT-6 y CFP10 están ausentes de las cepas de BCG y de la mayoría de micobacterias ambientales, con la excepción de M. kansasii, M. szulgai, M. marinum 3,4 y M. gordonae. Advertencias y precauciones de seguridad El material de origen humano se manipulará con precaución. Todas las muestras de sangre se considerarán potencialmente infecciosas. Para la manipulación, uso, conservación y eliminación de las muestras de sangre y de los componentes del análisis se aplicarán los procedimientos definidos en las recomendaciones o regulaciones nacionales sobre seguridad y riesgos biológicos. Las sustancias químicas se manipularán con precaución. Todas las sustancias químicas se considerarán potencialmente peligrosas. Materiales suministrados El kit T-SPOT.TB 8 contiene: 1. 1 placa de microtitulación: 96 pocillos, suministrada como tiras de 12 x 8 pocillos en un soporte, recubiertos con un anticuerpo monoclonal murino contra la citocina interferón (IFN viales (de 0,8 ml cada uno) de Panel A: contiene antígenos ESAT-6, albúmina sérica bovina y antibióticos viales (de 0,8 ml cada uno) de Panel B: contiene antígenos CFP10, albúmina sérica bovina y antibióticos viales (de 0,8 ml cada uno) de Control Positivo: contiene fitohemaglutinina (PHA) que se usará como control de la funcionalidad celular, albúmina sérica bovina y antibióticos vial (50 µl) de reactivo conjugado concentrado (200 veces): anticuerpo monoclonal murino contra la citocina IFN conjugada con fosfatasa alcalina frasco (25 ml) de solución sustrato: solución BCIP/NBT plus preparada para usar. 7. Instrucciones de uso, que se encuentran en el CD junto con la Ficha técnica de seguridad, la Guía de adiestramiento, la calculadora de dilución celular T-SPOT, la calculadora de dilución del conjugado, la calculadora de velocidad de centrifugación y el programa T-SPOT.AutoReporter. Conservación Consérvense todos los componentes del equipo a 2-8 C. Evítese la exposición prolongada a la luz de la solución sustrato. Estabilidad No mezcle los componentes entre diferentes lotes de kit. Conserve el kit sin abrir a 2-8 C. Los componentes del kit son estables hasta la fecha de caducidad que figura en la caja del kit, cuando se conservan y manipulan en las condiciones recomendadas. El kit no se debe utilizar después de la fecha de caducidad que figura en la etiqueta. Una vez abierto, conserve el kit a 2-8 C y utilice todos los materiales antes de 8 semanas. Equipo y materiales necesarios, pero no suministrados 1. Soporte de placa con tiras de 8 pocillos (comercializado por Oxford Immunotec) para uso con un kit T-SPOT.TB Cabina microbiológica clase II (recomendado). 3. Tubos de recogida de sangre: como Vacutainer CPT (comercializados por Oxford Immunotec) o tubos heparinizados. 4. Materiales de separación FICOLL-PAQUE* PLUS o alternativos para MNSP. 4 PI-TB-IVD-ES-V2
6 5. Con muestras obtenidas con más de 8 horas de antelación puede utilizarse el reactivo T-Cell Xtend (comercializado por Oxford Immunotec). 6. Pueden utilizarse tubos Leucosep para simplificar la separación de MNSP por el método de FICOLL*. 7. Centrífuga para la preparación de MNSP (que alcance como mínimo 1800 G y pueda mantener las muestras a temperatura ambiente (18-25 C)). 8. Equipo y reactivos para el recuento de MNSP; manual con azul de tripano y un hemocitómetro en un microscopio o automático con un analizador hematológico adecuado. 9. Una incubadora con humidificador que alcance una temperatura de 37 ± 1 C con suministro de CO 2 del 5%. 10. Una lavadora de placas de microtitulación o equipo para el lavado manual de las placas. 11. Pipetas y puntas estériles de pipetas. 12. Solución de D-PBS estéril: como GIBCO 1 x D-PBS (Invitrogen; número de catálogo ). 13. Agua destilada o desionizada. 14. Un medio de lectura de placas, como un microscopio, un microscopio digital, una lupa o un reproductor de imágenes de placas. 15. Medio de cultivo celular estéril como GIBCO AIM V (Invitrogen; número de catálogo ): se recomienda encarecidamente el uso de este medio exento de suero para la etapa de incubación. Puede utilizarse RPMI 1640 (Invitrogen; número de catálogo ) en las etapas iniciales de preparación de la muestra. Se recomienda que los medios de cultivo celular se conserven en alícuotas apropiadas y se deseche el material sobrante tras el uso. El medio de cultivo celular debe precalentarse a 37 C antes de usarlo con el análisis T-SPOT.TB. Preparación de los reactivos 1. Placa de microtitulación. La placa de microtitulación de T-SPOT.TB 8 se suministra preparada para usar. Extraer del envase el número necesario de tiras de 8 pocillos y dejar que alcance la temperatura ambiente. Volver a introducir las tiras restantes en el envoltorio exterior de aluminio e incluir la bolsa de desecante. 2. Los viales de antígenos ESAT-6 de M. tuberculosis (Panel A) se suministran preparados para usar. 3. Los viales de antígenos CFP10 de M. tuberculosis (Panel B) se suministran listos para usar. 4. Los viales de Control Positivo se suministran listos para usar. 5. Preparar una dilución 1:200 de la solución de trabajo de reactivo conjugado. Calcular el volumen necesario de solución de trabajo de reactivo conjugado (véase la calculadora de dilución del conjugado T-SPOT en el CD que acompaña a cada kit de análisis) y prepararla inmediatamente antes de su uso. 6. La solución de sustrato se suministra preparada para usar. Extraer del embalaje y dejar que alcance la temperatura ambiente. Procedimiento El análisis se practicará de acuerdo con los principios de Buenas Prácticas de Laboratorio y siguiendo estrictamente estas instrucciones de uso. Oxford Immunotec Ltd ha preparado una Guía de adiestramiento que describe la recogida y preparación de muestras, la selección de medios de cultivo celular y métodos de recuento de manchas. Este material se encuentra en el CD que acompaña a cada kit de análisis y pueden solicitarse llamando al +44 (0) u obtenerse de Recogida y preparación de muestras Cada usuario validará sus procedimientos de recogida de MNSP, recuento de MNSP y elección de medios adecuados para apoyar la funcionalidad de las células T durante la etapa de incubación primaria del análisis. En el caso de un paciente inmunocompetente, normalmente pueden 5 PI-TB-IVD-ES-V2
7 obtenerse MNSP suficientes para el análisis a partir de muestras de sangre venosa de acuerdo con las siguientes directrices: Adultos y niños de edad igual o superior a 10 años: un tubo CPT de 8 ml o dos tubos CPT de 4 ml o un tubo de heparina de 6 ml Niños de 2 a 9 años: un tubo CPT o de heparina de 4 ml Niños hasta de 2 años: un tubo pediátrico de 2 ml Las muestras de sangre se conservarán a temperatura ambiente y se analizarán en el curso de las 8 horas siguientes a su extracción, o en el curso de las 32 horas siguientes si la muestra se trata con el reactivo T-Cell Xtend, y se conservarán a C. El medio de cultivo celular debe precalentarse a 37 C antes de usarlo con el análisis T-SPOT.TB. Procedimiento 1. Recoger la muestra de sangre de acuerdo con las instrucciones suministradas con el dispositivo de recogida. Conservar la sangre recogida a temperatura ambiente (18-25 C) o a C si se usa el reactivo T-Cell Xtend. No refrigerar ni congelar. Notas 1. Las muestras de sangre pueden recogerse en tubos de varios tipos. En nuestros laboratorios, hemos utilizado con resultados satisfactorios tubos Vacutainer CPT con citrato, CPT con heparina y tubos estándar con heparina. Con el reactivo T-Cell Xtend sólo pueden utilizarse tubos con heparina. No se recomiendan los tubos con EDTA. 6 PI-TB-IVD-ES-V2
8 2. Si se usan tubos de recogida CPT, síganse las instrucciones del fabricante para la separación de MNSP. Si se emplean métodos alternativos de recogida, separar los MNSP mediante centrifugación con FICOLL-PAQUE PLUS siguiendo los procedimientos publicados. 2. Centrifugar los tubos CPT de 8 ml a 1600 G durante 28 min o los tubos CPT de 4 ml a 1800 G durante 30 min a 18 C si se dispone de una centrifugadora refrigerada. Esperar a que la centrifugadora llegue a 18 C si antes se había utilizado a temperaturas más bajas. Si se utiliza una centrifugadora sin refrigeración, hay que asegurarse de que la temperatura no sobrepasa los 25 C. Otra opción es diluir la sangre con un volumen equivalente de medio RPMI Depositar cuidadosamente en capas la sangre diluida (2-3 volúmenes) sobre FICOLL-PAQUE PLUS (1 volumen) y centrifugar a 1000 G durante 22 min a una temperatura de 18 a 25 C. La calculadora de velocidades de centrifugación del CD que acompaña al kit de análisis ayuda a convertir las velocidades de centrifugación entre G y rpm. Si las muestras tienen entre 8 y 32 horas, deben mezclarse con el reactivo T-Cell Xtend antes de depositarlas en capas en FICOLL- PAQUE PLUS. El procedimiento se describe completamente en el prospecto suministrado con el reactivo T-Cell Xtend. 3. Recoger la banda blanca nebulosa de MNSP con una pipeta y transferir a un tubo de centrifugado cónico de 15 ml. Enrasar a 10 ml con medio de cultivo celular. 4. Centrifugar a 600 G durante 7 min. Verter el sobrenadante y resuspender el gránulo en 1 ml de medio. 5. Enrasar a 10 ml con medio fresco y centrifugar a 350 G durante 7min. 6. Retirar el sobrenadante y volver a suspender el gránulo en 0,7 ml de medio de cultivo AIM V. Si se utilizan tubos Leucosep o el reactivo T-Cell Xtend (comercializado por Oxford Immunotec), síganse los protocolos que acompañan a los reactivos mencionados. 3. Puede utilizarse una variedad de medios para el lavado de las células durante este proceso. En nuestros laboratorios, se han utilizado AIM V y RPMI 1640 con buenos resultados y se recomienda su uso. 4. Véase 3, más arriba. 5. Véase 3, más arriba. 6. En esta etapa, se utilizará el medio de cultivo para la incubación durante la noche para resuspender el gránulo. En nuestros laboratorios se ha utilizado el medio sin suero AIM V con buenos resultados y se recomienda encarecidamente. Se han utilizado con éxito células T obtenidas de otros líquidos corporales, como lavado broncoalveolar (LBA), derrame pleural (DP) o fluido cerebroespinal (FCS), con el análisis T-SPOT.TB para identificar la infección y la enfermedad TB (Jafari et al (2006) Am. J. Respir. Crit. Care Med , Jafari et al (20) Eur. Resp. J , Strassburg et al (2008) Eur. Resp. J , Jafari et al (2009) Am. J. Respir. Crit. Care Med. 180(7) , Dheda et al (2009) Thorax 64(10) y Patel et al (2010) Am. J. Respir. Crit. Care Med. 182(4) ). Si se utilizan muestras distintas de la sangre, los usuarios deben validar los procedimientos para la recogida de células mononucleares suficientes. Los métodos para el procesamiento de las muestras de LBA se describen en las publicaciones mencionadas anteriormente. 7 PI-TB-IVD-ES-V2
9 Nota 1: No se han estudiado con detenimiento el valor de corte para un resultado positivo y controles válidos del análisis, empleando muestras distintas de la sangre, y podrían diferir de los correspondientes al análisis de sangre. Los usuarios deben definir sus criterios de interpretación del análisis. Los médicos deben aplicar su juicio clínico al examinar los resultados. Nota 2: No se ha estudiado con detenimiento la duración de la obtención de la muestra para comenzar el análisis. Recuento celular y dilución El análisis T-SPOT.TB requiere 2,5 x 10 5 MNSP viables por pocillo. Se precisa un total de cuatro pocillos para cada muestra. A cada pocillo debe añadirse un número correcto de células; en caso contrario, la interpretación del resultado será incorrecta. Procedimiento Notas 1. Efectuar un recuento de células viables. 1. Las células pueden contarse con diversos métodos, como el recuento manual con azul de tripano y un hemocitómetro o el recuento automatizado con un instrumento adecuado. 2. En resumen, para el recuento manual con un hemocitómetro Neubauer, añadir 10 µl de la suspensión celular final a 40 µl de solución de azul de tripano al 0,4% (p/v). Colocar una alícuota adecuada en el hemocitómetro y contar las células en la cuadrícula. Para otros 2. Se asegurará que la suspensión de células está completamente mezclada inmediatamente antes de retirar de alícuotas para la dilución o para el recuento. Las células pueden posarse en el fondo del tubo, lo que provocaría una interpretación incorrecta del número real de tipos de hemocitómetros y dispositivos células. automatizados, síganse las instrucciones de los fabricantes. 3. Calcular la concentración de células viables en la suspensión celular madre. 4. Preparar 500 µl de la suspensión celular final en una concentración de 2,5 x 10 5 células / 100 µl. 3. Garantizar que los cálculos del sistema de recuento celular son correctos, pues el uso de un número insuficiente o excesivo de células puede motivar una interpretación incorrecta de los resultados. La calculadora de dilución celular T-SPOT del CD que acompaña a cada kit de análisis facilita este cálculo. 4. Garantizar que las células se mezclan completamente antes de retirar una alícuota para la dilución. Preparación e incubación de la placa El análisis T-SPOT.TB requiere el uso de cuatro pocillos por muestra. Se efectuará un Control Nulo y un Control Positivo de funcionalidad celular con cada muestra individual. Se recomienda que las muestras se dispongan verticalmente en la placa como se ilustra a continuación. Control Nulo Panel A Panel B Control Positivo 8 PI-TB-IVD-ES-V2
10 Procedimiento 1. Extraer del envase las tiras de 8 pocillos recubiertas de antemano, sujetarlas a un soporte de placas y dejar que alcancen la temperatura ambiente. 2. Cada muestra requiere el uso de 4 pocillos individuales. (i) Añadir 50 µl de medio de cultivo AIM V a cada pocillo de Control Nulo. (ii) Añadir 50 µl de solución del Panel A a los pocillos a los que sea necesario. (iii) Añadir 50 µl de solución del Panel B a los pocillos a los que sea necesario. (iv) Añadir 50 µl de solución de Control Positivo a cada pocillo de control de funcionalidad celular. 3. Añadir a cada uno de los 4 pocillos que se usarán para la muestra de un paciente 100 µl de la suspensión celular final del paciente (que contiene células viables). 4. Incubar la placa en una incubadora con humidificador a 37 C con CO 2 al 5% durante horas. Notes 1. Extraer únicamente el número necesario de tiras y volver a meter en resto en el envase. Sujetar las tiras que se vayan a usar a un soporte de placas vacío que tenga cubierta y tapa. Los soportes, las cubiertas y las tapas se deben conservar y reutilizar. 2. Impedir que la punta de la pipeta toque la membrana. Las muescas en la membrana causadas por la punta de la pipeta pueden causar artefactos en los pocillos. Puede ser necesario golpear suavemente la placa para garantizar que las soluciones cubren la membrana en la base de cada pocillo. No agitar de forma vigorosa para minimizar la contaminación cruzada de los antígenos entre los pocillos. 3. Pipetear cuidadosamente la suspensión celular hacia arriba y abajo para garantizar una mezcla completa antes de retirar cada alícuota de 100 µl. Se recomienda utilizar una punta nueva para cada adición de células de cada paciente, para evitar la contaminación cruzada de los antígenos entre los 4 pocillos. 4. No alterar la placa una vez que esté en la incubadora. No apilar las placas, pues ello determinaría la distribución irregular de la temperatura y la ventilación. El incumplimiento del tiempo y las condiciones recomendados de incubación podría originar una interpretación incorrecta del resultado. Asegurarse de que la incubadora contiene agua suficiente para mantener la humedad durante el tiempo de incubación. Revelado y recuento de las manchas Durante las etapas de lavado y revelado no se tocarán las membranas con las puntas de las pipetas ni con las puntas de la lavadora automática de pocillos. Las muescas en la membrana causadas por las puntas de las pipetas o las lavadoras de pocillos pueden provocar artefactos en los pocillos que podrían interferir con el recuento de las manchas. Procedimiento 1. Retirar la palca de la incubadora y desechar el medio de cultivo celular. 2. Añadir 200 µl de solución D-PBS a cada pocillo. 3. Desechar la solución D-PBS. Repetir el lavado del pocillo 3 veces más con solución D- PBS nueva para cada lavado. 4. Diluir el reactivo conjugado concentrado 200 veces en D-PBS para crear la solución a concentración de trabajo. Notas 1. En este momento, extraer la solución sustrato del equipo y dejar que alcance la temperatura ambiente. 3. Desechar todo el D-PBS de la etapa de lavado final invirtiendo la placa sobre papel absorbente antes de continuar. 4. No utilizar D-PBS que contenga Tween u otros detergentes, pues esto provocar recuentos de fondo elevados. Hay que asegurarse de que sólo se prepara un pequeño exceso (para 9 PI-TB-IVD-ES-V2
11 compensar las pérdidas) de solución a concentración de trabajo. Así, para T-SPOT.TB 96, en el que cada uno de los 96 pocillos necesita 50 μl, se preparan 5 ml de solución a concentración de trabajo añadiendo 25 μl de reactivo conjugado concentrado a μl de D-PBS. 5. Añadir 50 µl de solución de reactivo conjugado a concentración de trabajo a cada pocillo e incubar a 2-8 C durante 1 hora. 6. Desechar el conjugado y efectuar cuatro lavados con D-PBS como se describe en las etapas 2 y 3, más arriba. 7. Añadir 50 µl de solución de sustrato a cada pocillo e incubar a temperatura ambiente durante 7 min. 8. Lavar la placa minuciosamente con agua destilada o agua desionizada para detener la reacción de detección. 9. Dejarla secar en un área bien ventilada o en un horno a una temperatura máxima de 37 C. 10. Contar y registrar el número de manchas azul oscuro, bien diferenciadas, en la membrana de cada pocillo. Aplicar la interpretación de los resultados y los criterios de análisis (véase más adelante) para determinar si la muestra de un paciente es Positiva o Negativa a los antígenos de la tuberculosis. Para T-SPOT.TB 8 y para cada tira de 8 pocillos (cada pocillo necesita 50 µl), se preparan 500 µl de solución a concentración de trabajo añadiendo 25 μl de reactivo conjugado concentrado a 497,5 µl de D-PBS. Puede utilizarse para esta operación la calculadora de dilución del conjugado del CD que acompaña a cada kit de análisis. 5. El incumplimiento del tiempo recomendado de incubación puede causar una interpretación incorrecta del resultado. 7. El incumplimiento del tiempo recomendado de incubación puede causar una interpretación incorrecta del resultado. 9. Las manchas se hacen más visibles a medida que se seca la placa. Dejar secar 4 horas a 37 C o durante una noche a temperatura ambiente. 10. Las manchas pueden visualizarse con varios métodos: manualmente con una lupa, un microscopio adecuado, un microscopio digital o con un reproductor de imágenes de placas ELISPOT específico. En la página web de Oxford Immunotec puede obtenerse una guía de formación de recuento de manchas (el programa T-SPOT.Tutor). Control de calidad Un resultado típico tendría pocas manchas o ninguna en el Control Nulo y más de 20 manchas en el Control Positivo. Un recuento de manchas del Control Nulo superior a 10 deberá considerarse Indeterminado. Consulte las posibles causas en la Guía de adiestramiento de T-SPOT.TB (puede descargarlo de Hay que obtener otra muestra del paciente y analizarla. Típicamente, el recuento de manchas del Control Positivo de funcionalidad celular debería ser 20 o presentar saturación (demasiadas manchas que impiden el recuento). Una pequeña proporción de pacientes pueden tener células T que muestren sólo una respuesta limitada a la PHA 13,14. Cuando el recuento del Control Positivo sea < 20 manchas debe considerarse como Indeterminado, salvo que el Panel A o el Panel B sean Positivos tal como se describe en Interpretación de los resultados y Criterios de Análisis (véase a continuación), circunstancias en las que el resultado se considerará válido. Debido a las posibles variaciones biológicas y sistemáticas, cuando el valor más alto de (panel A menos control nulo) y (panel B menos control nulo) sea 5, 6 o 7 manchas, el resultado puede 10 PI-TB-IVD-ES-V2
12 considerarse límite (equívoco). Los resultados límite (equívocos), aunque válidos, son menos fiables que aquéllos en los que el recuento de manchas está más alejado del punto de corte. Por tanto, se recomienda repetir el análisis del paciente con una muestra nueva. Si el resultado sigue siendo límite (equívoco), hay que emplear otras pruebas diagnósticas o recurrir a información epidemiológica para determinar el estado de infección tuberculosa del paciente. Aunque los antígenos ESAT-6 y CFP10 están ausentes de las cepas de BCG de M. bovis y de la mayoría de micobacterias ambientales, es posible que un resultado T-SPOT.TB Positivo se deba a una infección por M. kansasii, M. szulgai, M. marinum o M. gordonae. Si se sospechan tales infecciones, hay que usar análisis alternativos. Interpretación de los resultados y Criterios de Análisis Véase el apartado de Control de calidad antes de aplicar los criterios siguientes. Los resultados de T-SPOT.TB se interpretan restando el recuento de manchas del pocillo de control nulo del recuento de cada uno de los paneles, aplicando el algoritmo siguiente: El resultado es "Positivo" si (panel A menos control nulo) y/o (panel B menos control nulo) 6 manchas. El resultado es "Negativo" si tanto (panel A menos control nulo) como (panel B menos control nulo) 5 manchas. Esto incluye los valores inferiores a cero. Un resultado Positivo indica que la muestra contiene células T efectoras reactivas a M. tuberculosis. Un resultado Negativo indica que la muestra probablemente no contiene células T efectoras reactivas a M. tuberculosis. Características de rendimiento del análisis La especificidad se evaluó mediante el análisis de 93 muestras de donantes a los que se adjudicó un riesgo bajo de infección por M. tuberculosis a partir de la historia clínica y la información personal. Se calculó que la especificidad del análisis T-SPOT.TB era del 100% (93/93) (límites de confianza del 95%, 95,8% - 100%). La sensibilidad se evaluó mediante el análisis de 87 muestras de cultivos de casos confirmados de infección por M. tuberculosis infección, con inclusión de grupos inmunodeprimidos. Se calculó que la sensibilidad del análisis T-SPOT.TB era del 98,8% (86/87) (límites de confianza del 95%, 90,8% - 99,9%). La reproducibilidad se evaluó, como marcador indirecto de la variación intraanalítica, mediante análisis de muestras de sangre duplicadas efectuados en la misma placa. Se analizaron por duplicado 145 muestras de sangre de 140 donantes individuales (dos pocillos del Panel A y dos pocillos del Panel B) mediante el análisis T-SPOT.TB. Se observó concordancia clínica en 142/145 (97,9%) análisis duplicados. Dos análisis duplicados produjeron resultados discordantes limítrofes y sólo 1/145 muestras produjeron resultados discrepantes. 11 PI-TB-IVD-ES-V2
13 Bibliografía 1. Janeway y Travers (1996) Immunobiology 2 nd Ed. 2. Staines y cols. (1999) Introducing Immunology 2 nd Ed. 3. Chapman y cols. (2002) AIDS, 16 (17): Ewer y cols. (2003) Lancet, 361: Véase 6. Pathan y cols. (2001) J. Immunol., 167: Lalvani y cols. (2001) Lancet, 357: Lalvani y cols. (2001) Am. J. Resp. Crit. Care Med., 163: Lalvani y cols. (2001) J. Infect. Dis., 183: Meier y cols. (2005) Eur. J. Clin. Microbiol. Infect. Dis., 24: Zellweger y cols. (2005) Int. J. Tuberculosis y Lung Dis., 9(11): Directrices aprobadas del NCCLS. Performance of single Cell Immune Response Assays, I/LA26-A 13. Koller y cols. (2003) Clin. Exp. Immunol., 132(2): Apollonj y cols. (1975) Immunol. Commum., 4(5): Glosario de símbolos» Uso preferente /Fecha de caducidad (Año-Mes-Día) 3 Número de lote 4 Número de catálogo Atención, véanse las instrucciones de uso Ó Fabricante i Suficiente para n pruebas 1 Dispositivo de diagnóstico in vitro j Limitación de temperatura/consérvese entre ² Véanse las instrucciones de uso T-SPOT, T-Cell Xtend y el logotipo de Oxford Immunotec son marcas registradas de Oxford Immunotec Limited. AIM V y GIBCO son marcas registradas de Invitrogen. CPT y Vacutainer son marcas registradas de Becton Dickinson. * FICOLL y FICOLL-PAQUE son marcas registradas de las empresas GE. Tween es una marca registrada de Uniqema Americas LLC. El análisis T-SPOT.TB está protegida por las siguientes patentes y patentes en trámite: US , US12/510,594, EP941478, JP , AU728357, CA , US , US , EP , JP , ZA , US , US ; US13/489,621; US , US , US11/801,112, EP , JP , AU727602, CA , CN , CZ300953, HU , NO , TR2009/01109, ZA , ZW10496; US , EP , AU682879, CA , NZ267984, US , US , EP , JP , AU , CA El uso del reactivo T-Cell Xtend está protegido por las siguientes patentes y patentes en trámite: EP ; US13/253,598, CN , AU , JP , IN2165/DELNP/2009, CA El análisis T-SPOT.TB incorpora tecnología patentada bajo licencia de Statens Serum Institut, Copenhagen, Dinamarca e Isis Innovation Limited, Oxford, RU. Oxford Immunotec Limited, Reservados todos los derechos. Fabricante Oxford Immunotec Ltd 94C Innovation Drive, Milton Park, Abingdon Oxfordshire, OX14 4RZ, RU 12 PI-TB-IVD-ES-V2
Tubos Leucosep LTK.615 PROSPECTO. Para uso diagnóstico in vitro PI-LT.615-ES-V3
 Tubos Leucosep LTK.615 PROSPECTO Para uso diagnóstico in vitro PI-LT.615-ES-V3 Información e instrucciones Uso previsto El uso previsto de los tubos Leucosep es la recogida y la separación de células mononucleares
Tubos Leucosep LTK.615 PROSPECTO Para uso diagnóstico in vitro PI-LT.615-ES-V3 Información e instrucciones Uso previsto El uso previsto de los tubos Leucosep es la recogida y la separación de células mononucleares
PROSPECTO. Para uso diagnóstico in vitro. Para uso en la preparación y aislamiento de linfocitos purificados directamente de sangre entera.
 Para uso en la preparación y aislamiento de linfocitos purificados directamente de sangre entera. PROSPECTO Para uso diagnóstico in vitro PI-TT.610-ES-V5 Información e instrucciones Uso previsto El reactivo
Para uso en la preparación y aislamiento de linfocitos purificados directamente de sangre entera. PROSPECTO Para uso diagnóstico in vitro PI-TT.610-ES-V5 Información e instrucciones Uso previsto El reactivo
WITNESS RELAXIN (plasma, serum) RLX RLX u d 9 n n ersio V X RLX L R -W IO B S
 WITNESS RELAXIN (plasma, serum) SBIO-W Version n 9 du 28.07.2010 WITNESS RELAXIN WITNESS RELAXIN GENERALIDADES El kit WITNESS RELAXIN permite diagnosticar la gestación en la perra y en la gata, y permite
WITNESS RELAXIN (plasma, serum) SBIO-W Version n 9 du 28.07.2010 WITNESS RELAXIN WITNESS RELAXIN GENERALIDADES El kit WITNESS RELAXIN permite diagnosticar la gestación en la perra y en la gata, y permite
DANAGENE BLOOD DNA KIT
 Ref. 0601 100 ml Ref. 0602 200 ml DANAGENE BLOOD DNA KIT 1.INTRODUCCION DANAGENE BLOOD DNA Kit provee un método para la extracción de ADN genómico de alta calidad a partir de sangre total o médula ósea.
Ref. 0601 100 ml Ref. 0602 200 ml DANAGENE BLOOD DNA KIT 1.INTRODUCCION DANAGENE BLOOD DNA Kit provee un método para la extracción de ADN genómico de alta calidad a partir de sangre total o médula ósea.
TECHNOLOGY. CROSSMATCH TEST canino. primer test inmunocromatografico para reaccion cruzada con antiglobulina canina especifica.
 CROSSMATCH TEST canino primer test inmunocromatografico para reaccion cruzada con antiglobulina canina especifica 20 minutos TECHNOLOGY - ahorra tiempo - facil manipulacion - resultados fiables - facil
CROSSMATCH TEST canino primer test inmunocromatografico para reaccion cruzada con antiglobulina canina especifica 20 minutos TECHNOLOGY - ahorra tiempo - facil manipulacion - resultados fiables - facil
TEMA 14. Métodos inmunológicos para la identificación microbiana
 TEMA 14 Métodos inmunológicos para la identificación microbiana Tema 14. Métodos inmunológicos para la identificación microbiana 1. Introducción 2. Detección de antígenos 2.1. Obtención de anticuerpos
TEMA 14 Métodos inmunológicos para la identificación microbiana Tema 14. Métodos inmunológicos para la identificación microbiana 1. Introducción 2. Detección de antígenos 2.1. Obtención de anticuerpos
QUE ES? Es la búsqueda de anticuerpos preformados contra los linfocitos de un posible donante en el suero de un paciente.
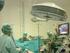 CROSS MATCH QUE ES? Es la búsqueda de anticuerpos preformados contra los linfocitos de un posible donante en el suero de un paciente. Pueden estar específicamente dirigidos contra los antígenos HLA o contra
CROSS MATCH QUE ES? Es la búsqueda de anticuerpos preformados contra los linfocitos de un posible donante en el suero de un paciente. Pueden estar específicamente dirigidos contra los antígenos HLA o contra
Métodos para Inmunidad Viral
 Métodos para Inmunidad Viral Radioinmunoensayo (RIA) Técnica muy sensible basada en la competencia de unión al anticuerpo específico entre el antígeno a cuantificar y cantidades conocidas del antígeno
Métodos para Inmunidad Viral Radioinmunoensayo (RIA) Técnica muy sensible basada en la competencia de unión al anticuerpo específico entre el antígeno a cuantificar y cantidades conocidas del antígeno
HBsAg CONFIRMATORY TEST Para la confirmación de muestras positivas con el UMELISA HBsAg PLUS
 HBsAg CONFIRMATORY TEST Para la confirmación de muestras positivas con el UMELISA HBsAg PLUS INTERES CLÍNICO Con el descubrimiento del antígeno de superficie del virus de la Hepatitis B (1) se crearon
HBsAg CONFIRMATORY TEST Para la confirmación de muestras positivas con el UMELISA HBsAg PLUS INTERES CLÍNICO Con el descubrimiento del antígeno de superficie del virus de la Hepatitis B (1) se crearon
ScanGel ScanBrom ml
 ScanGel ScanBrom 86445 12 ml BROMELINA PARA PRUEBAS CRUZADAS IVD Todos los productos fabricados y comercializados por la sociedad Bio-Rad se hallan bajo un sistema de garantía de calidad desde la recepción
ScanGel ScanBrom 86445 12 ml BROMELINA PARA PRUEBAS CRUZADAS IVD Todos los productos fabricados y comercializados por la sociedad Bio-Rad se hallan bajo un sistema de garantía de calidad desde la recepción
50 kits de recolección de muestras con torunda multitest Aptima (N.º de catálogo PRD-03546) Cada kit contiene:
 Uso previsto El kit de recolección de muestras con torunda se utiliza con los ensayos Aptima. El kit de recolección de muestras con torunda multitest Aptima se utiliza para que médico y paciente puedan
Uso previsto El kit de recolección de muestras con torunda se utiliza con los ensayos Aptima. El kit de recolección de muestras con torunda multitest Aptima se utiliza para que médico y paciente puedan
50 kits de recolección de muestras con torunda multitest Aptima (N.º de catálogo PRD-03546) Cada kit contiene:
 Uso previsto El kit de recolección de muestras con torunda se utiliza con los ensayos Aptima. El kit de recolección de muestras con torunda multitest Aptima se utiliza para que médico y paciente puedan
Uso previsto El kit de recolección de muestras con torunda se utiliza con los ensayos Aptima. El kit de recolección de muestras con torunda multitest Aptima se utiliza para que médico y paciente puedan
Instrucciones de uso MBT Galaxy HCCA Matrix GPR
 Instrucciones de uso MBT Galaxy HCCA Matrix GPR Sustancia matriz purificada para uso en espectrometría de masas de desorción/ionización láser asistida por matriz y tiempo de vuelo (MALDI-TOF-MS). Los productos
Instrucciones de uso MBT Galaxy HCCA Matrix GPR Sustancia matriz purificada para uso en espectrometría de masas de desorción/ionización láser asistida por matriz y tiempo de vuelo (MALDI-TOF-MS). Los productos
1. OBJETIVO Detectar enterotoxina A de C. perfringens por método de aglutinación pasiva en látex en cepas aisladas de alimentos
 PRT-712.04-080 Página 1 de 9 1. OBJETIVO Detectar enterotoxina A de C. perfringens por método de aglutinación pasiva en látex en cepas aisladas de alimentos 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este
PRT-712.04-080 Página 1 de 9 1. OBJETIVO Detectar enterotoxina A de C. perfringens por método de aglutinación pasiva en látex en cepas aisladas de alimentos 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este
Hoja de protocolo del instrumento QIAsymphony SP
 Hoja de protocolo del instrumento QIAsymphony SP Protocolo VirusBlood200_V5_DSP Información general Para uso en diagnóstico in vitro. Este protocolo está indicado para la purificación de ADN viral a partir
Hoja de protocolo del instrumento QIAsymphony SP Protocolo VirusBlood200_V5_DSP Información general Para uso en diagnóstico in vitro. Este protocolo está indicado para la purificación de ADN viral a partir
COMO ABORDAR Y RESOLVER ASPECTOS PRÁCTICOS DE MICROBIOLOGÍA
 COMO ABORDAR Y RESOLVER ASPECTOS PRÁCTICOS DE MICROBIOLOGÍA 1. DILUCIONES Y CONCENTRACIONES. S LÍQUIDAS Y SÓLIDAS Inés Arana, Maite Orruño e Isabel Barcina Departamento Inmunología, Microbiología y Parasitología
COMO ABORDAR Y RESOLVER ASPECTOS PRÁCTICOS DE MICROBIOLOGÍA 1. DILUCIONES Y CONCENTRACIONES. S LÍQUIDAS Y SÓLIDAS Inés Arana, Maite Orruño e Isabel Barcina Departamento Inmunología, Microbiología y Parasitología
RESOLUCIÓN OIV/OENO 427/2010
 RESOLUCIÓN OIV/OENO 427/2010 CRITERIOS PARA LOS MÉTODOS DE CUANTIFICACIÓN DE LOS RESIDUOS, POTENCIALMENTE ALERGÉNICOS, DE PROTEÍNAS USADAS EN LA CLARIFICACIÓN DE LOS VINOS La ASAMBLEA GENERAL, De conformidad
RESOLUCIÓN OIV/OENO 427/2010 CRITERIOS PARA LOS MÉTODOS DE CUANTIFICACIÓN DE LOS RESIDUOS, POTENCIALMENTE ALERGÉNICOS, DE PROTEÍNAS USADAS EN LA CLARIFICACIÓN DE LOS VINOS La ASAMBLEA GENERAL, De conformidad
PPD y Quantiferon: diagnóstico de TB latente? Dr. Enrique Valdivia Núñez Médico neumólogo HNCH- UPCH
 PPD y Quantiferon: diagnóstico de TB latente? Dr. Enrique Valdivia Núñez Médico neumólogo HNCH- UPCH Aunque las tasas TBC están decayendo. Se encontró que aquellos que tienen infección latente basado en
PPD y Quantiferon: diagnóstico de TB latente? Dr. Enrique Valdivia Núñez Médico neumólogo HNCH- UPCH Aunque las tasas TBC están decayendo. Se encontró que aquellos que tienen infección latente basado en
CURSO INTERNACIONAL INMUNIDAD INNATA EN SALUD Y ENFERMEDADES INFECCIOSAS
 CURSO INTERNACIONAL INMUNIDAD INNATA EN SALUD Y ENFERMEDADES INFECCIOSAS 29 de agosto - 9 de septiembre de 2016 Comité Organizador: Eva María Salinas Miralles (Universidad Autónoma de Aguascalientes) y
CURSO INTERNACIONAL INMUNIDAD INNATA EN SALUD Y ENFERMEDADES INFECCIOSAS 29 de agosto - 9 de septiembre de 2016 Comité Organizador: Eva María Salinas Miralles (Universidad Autónoma de Aguascalientes) y
RESULTADOS Y DISCUSIÓN
 RESULTADOS Y DISCUSIÓN Estimación de la Concentración Proteica del Filtrado de Cultivo de Mycobacterium tuberculosis H37Rv La curva estándar con la que se estimó la concentración proteica del filtrado
RESULTADOS Y DISCUSIÓN Estimación de la Concentración Proteica del Filtrado de Cultivo de Mycobacterium tuberculosis H37Rv La curva estándar con la que se estimó la concentración proteica del filtrado
Diagnóstico de la Infección Tuberculosa Latente. Cuál es la Importancia Clínica y Epidemiológica de Diagnosticar la Infección Tuberculosa?
 Diagnóstico de la Infección Tuberculosa Latente Cuál es la Importancia Clínica y Epidemiológica de Diagnosticar la Infección Tuberculosa? Prueba Tuberculínica o PPD PPD (Derivado Proteico Purificado):
Diagnóstico de la Infección Tuberculosa Latente Cuál es la Importancia Clínica y Epidemiológica de Diagnosticar la Infección Tuberculosa? Prueba Tuberculínica o PPD PPD (Derivado Proteico Purificado):
SSI IMMUVIEW LEGIONELLA BLOOD TEST ANÁLISIS DE SANGRE IMMUVIEW LEGIONELLA
 SSI IMMUVIEW LEGIONELLA BLOOD TEST ANÁLISIS DE SANGRE IMMUVIEW LEGIONELLA Aplicación El análisis de sangre ImmuView Legionella de Statens Serum Institute se ha creado para el diagnóstico de una infección
SSI IMMUVIEW LEGIONELLA BLOOD TEST ANÁLISIS DE SANGRE IMMUVIEW LEGIONELLA Aplicación El análisis de sangre ImmuView Legionella de Statens Serum Institute se ha creado para el diagnóstico de una infección
ScanGel ReverScan A1, B x 5 ml ReverScan A1, A2, B, O x 5 ml
 ScanGel ReverScan A1, B 86790 2 x 5 ml ReverScan A1, A2, B, O 86795 4 x 5 ml GLÓBULOS ROJOS TEST DE ORIGEN HUMANO PARA LA PRUEBA SÉRICA DEL TIPAJE ABO IVD Todos los productos fabricados y comercializados
ScanGel ReverScan A1, B 86790 2 x 5 ml ReverScan A1, A2, B, O 86795 4 x 5 ml GLÓBULOS ROJOS TEST DE ORIGEN HUMANO PARA LA PRUEBA SÉRICA DEL TIPAJE ABO IVD Todos los productos fabricados y comercializados
Hoja de protocolo del instrumento QIAsymphony SP
 Hoja de protocolo del instrumento QIAsymphony SP Protocolo DNA_Blood_200_V7_DSP Información general Para uso en diagnóstico in vitro. Este protocolo está indicado para la purificación de ADN mitocondrial
Hoja de protocolo del instrumento QIAsymphony SP Protocolo DNA_Blood_200_V7_DSP Información general Para uso en diagnóstico in vitro. Este protocolo está indicado para la purificación de ADN mitocondrial
INSTRUCCIONES DE REFERENCIA RÁPIDA Uso exclusivo con el Analizador Sofia.
 Analizador y FIA INSTRUCCIONES DE REFERENCIA RÁPIDA Uso exclusivo con el Analizador Sofia. Procedimiento de prueba Lea el Prospecto y el Manual del usuario detenidamente antes de usar las Instrucciones
Analizador y FIA INSTRUCCIONES DE REFERENCIA RÁPIDA Uso exclusivo con el Analizador Sofia. Procedimiento de prueba Lea el Prospecto y el Manual del usuario detenidamente antes de usar las Instrucciones
GELES FORMULADOS CON REACTIVOS MONOCLONALES DE ORIGEN MURINO O HUMANO O GEL NEUTRO
 ScanGel ABO Complete/RH/K Duo 86719 2 x 24 tarjetas 86709 2 x 144 tarjetas ScanGel ABO Complete/RH1 Duo y ScanGel Monoclonal RH/K Phenotypes Duo tarjetas GELES FORMULADOS CON REACTIVOS MONOCLONALES DE
ScanGel ABO Complete/RH/K Duo 86719 2 x 24 tarjetas 86709 2 x 144 tarjetas ScanGel ABO Complete/RH1 Duo y ScanGel Monoclonal RH/K Phenotypes Duo tarjetas GELES FORMULADOS CON REACTIVOS MONOCLONALES DE
PRÁCTICA III. AISLAMIENTO DE MITOCONDRIAS: ACTIVIDAD MALATO DESHIDROGENASA
 PRÁCTICA III. AISLAMIENTO DE MITOCONDRIAS: ACTIVIDAD MALATO DESHIDROGENASA 1. Fundamento Teórico La mayoría de los procesos bioquímicos que producen energía química se realizan en orgánulos intracelulares
PRÁCTICA III. AISLAMIENTO DE MITOCONDRIAS: ACTIVIDAD MALATO DESHIDROGENASA 1. Fundamento Teórico La mayoría de los procesos bioquímicos que producen energía química se realizan en orgánulos intracelulares
Toma de Muestras Microbiológicas
 Toma de Muestras Microbiológicas MICROBIOLOGÍA CLÍNICA DIAGNÓSTICO DE ENFERMEDADES INFECCIOSAS MUESTRA AISLAMIENTO IDENTIFICACIÓN SENSIBILIDAD A ANTIMICROBIANOS Detección de anticuerpos, antígenos y ácidos
Toma de Muestras Microbiológicas MICROBIOLOGÍA CLÍNICA DIAGNÓSTICO DE ENFERMEDADES INFECCIOSAS MUESTRA AISLAMIENTO IDENTIFICACIÓN SENSIBILIDAD A ANTIMICROBIANOS Detección de anticuerpos, antígenos y ácidos
INSTRUCTIVO DETERMINACIÓN DE GRUPOS A,B,O Y RH-D
 1. OBJETIVO: Desarrollar la clasificación de Grupo y Rh a los usuarios del Hospital Regional de Arica Dr. Juan Noé Crevani, de acuerdo con los antígenos y anticuerpos presentes en la sangre, esto con el
1. OBJETIVO: Desarrollar la clasificación de Grupo y Rh a los usuarios del Hospital Regional de Arica Dr. Juan Noé Crevani, de acuerdo con los antígenos y anticuerpos presentes en la sangre, esto con el
NO VACÍO SERIES DE GRAVEDAD MÉTODO GV-65 PARA EL ANALISIS DE PENCICLIDINA (PCP) EN ORINA POR GC/MS.
 NO VACÍO SERIES DE GRAVEDAD MÉTODO GV-65 PARA EL ANALISIS DE PENCICLIDINA (PCP) EN ORINA POR GC/MS. Aunque este método ha dado buenos resultados en nuestro laboratorio. Este tiene que ser validado por
NO VACÍO SERIES DE GRAVEDAD MÉTODO GV-65 PARA EL ANALISIS DE PENCICLIDINA (PCP) EN ORINA POR GC/MS. Aunque este método ha dado buenos resultados en nuestro laboratorio. Este tiene que ser validado por
UNIVERSIDAD NACIONAL DEL NORDESTE Facultad de Ciencias Exactas y Naturales y Agrimensura Departamento de Biología - Área Zoología EMBRIOLOGÍA ANIMAL
 UNIVERSIDAD NACIONAL DEL NORDESTE Facultad de Ciencias Exactas y Naturales y Agrimensura Departamento de Biología - Área Zoología EMBRIOLOGÍA ANIMAL PROTOCOLO PARA OBTENCIÓN DE EMBRIONES DE POLLO EN LABORATORIO
UNIVERSIDAD NACIONAL DEL NORDESTE Facultad de Ciencias Exactas y Naturales y Agrimensura Departamento de Biología - Área Zoología EMBRIOLOGÍA ANIMAL PROTOCOLO PARA OBTENCIÓN DE EMBRIONES DE POLLO EN LABORATORIO
El Laboratorio en el diagnóstico de las tuberculosis y Micobacterias atípicas: Herramientas diagnósticas disponibles en Chile
 El Laboratorio en el diagnóstico de las tuberculosis y Micobacterias atípicas: Herramientas diagnósticas disponibles en Chile Dra. Patricia González A. Médico Microbiólogo Laboratorio Clínica Alemana Facultad
El Laboratorio en el diagnóstico de las tuberculosis y Micobacterias atípicas: Herramientas diagnósticas disponibles en Chile Dra. Patricia González A. Médico Microbiólogo Laboratorio Clínica Alemana Facultad
Olanzapina en polvo y disolvente para suspensión inyectable de liberación prolongada
 ZYPADHERA Olanzapina en polvo y disolvente para suspensión inyectable de liberación prolongada Instrucciones para la reconstitución y administración dirigido a Profesionales Sanitarios Información sobre
ZYPADHERA Olanzapina en polvo y disolvente para suspensión inyectable de liberación prolongada Instrucciones para la reconstitución y administración dirigido a Profesionales Sanitarios Información sobre
Biología Celular e Histología. Prácticas de Biología Celular. Cultivos celulares y Procesamiento de tejidos.
 Biología Celular e Histología Prácticas de Biología Celular Cultivos celulares y Procesamiento de tejidos. Suspensiones celulares. Inmunodetección directa. Identificación celular tras cultivo. Manejo del
Biología Celular e Histología Prácticas de Biología Celular Cultivos celulares y Procesamiento de tejidos. Suspensiones celulares. Inmunodetección directa. Identificación celular tras cultivo. Manejo del
INSTRUCCIONES PARA AISLAMIENTO DE LEUCOCITOS A PARTIR DE SANGRE TOTAL
 INSTRUCCIONES PARA AISLAMIENTO DE LEUCOCITOS A PARTIR DE SANGRE TOTAL EL PRIMER PASO, ES LEER PRIMERO Y LUEGO SEGUIR TODAS LAS INSTRUCCIONES!!!!! ALFREDO URIBE ARDILA M.SC. REACTIVOS SOLUCION DEXTRAN-HEPARINA
INSTRUCCIONES PARA AISLAMIENTO DE LEUCOCITOS A PARTIR DE SANGRE TOTAL EL PRIMER PASO, ES LEER PRIMERO Y LUEGO SEGUIR TODAS LAS INSTRUCCIONES!!!!! ALFREDO URIBE ARDILA M.SC. REACTIVOS SOLUCION DEXTRAN-HEPARINA
BIOSEGURIDAD EN EL LABORATORIO DE MYCOBACTERIAS. Dr. Martin Yagui Moscoso
 BIOSEGURIDAD EN EL LABORATORIO DE MYCOBACTERIAS Dr. Martin Yagui Moscoso Contenido Brotes de TB en el laboratorio Riesgos de transmisión TB Barreras de contención Buenas Prácticas de Laboratorio Cabinas
BIOSEGURIDAD EN EL LABORATORIO DE MYCOBACTERIAS Dr. Martin Yagui Moscoso Contenido Brotes de TB en el laboratorio Riesgos de transmisión TB Barreras de contención Buenas Prácticas de Laboratorio Cabinas
Introducción Principio del test
 El equipo ImmunoComb II VIH 1 & 2 TriSpot Ag-Ab es una prueba Inmuno Ensayo Enzimático para la determinación cualitativa y diferencial de anticuerpos contra el virus de inmunodeficiencia humano tipo 1
El equipo ImmunoComb II VIH 1 & 2 TriSpot Ag-Ab es una prueba Inmuno Ensayo Enzimático para la determinación cualitativa y diferencial de anticuerpos contra el virus de inmunodeficiencia humano tipo 1
ANEXOS. Anexo 1. Solución Reguladora de Acetato 0.1 M, ph 4.0 y metanol al 2% (v/v).
 ANEXOS Anexo 1 Solución Reguladora de Acetato 0.1 M, ph 4.0 y metanol al 2% (v/v). 1. Tomar 6.011mL de ácido acético y aforar a 1L de agua HPLC. 2. Pesar 13.609 g de acetato de sodio y aforar a 1L de agua
ANEXOS Anexo 1 Solución Reguladora de Acetato 0.1 M, ph 4.0 y metanol al 2% (v/v). 1. Tomar 6.011mL de ácido acético y aforar a 1L de agua HPLC. 2. Pesar 13.609 g de acetato de sodio y aforar a 1L de agua
EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS
 EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS Los hongos poseen un genoma complejo consistente en: ADN nuclear (n ADN) ADN mitocondrial (mt ADN) en algunos casos ADN plasmídico EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS
EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS Los hongos poseen un genoma complejo consistente en: ADN nuclear (n ADN) ADN mitocondrial (mt ADN) en algunos casos ADN plasmídico EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS
SSI DERMATOPHYTE PCR KIT PRUEBA PCR DERMATOFITO
 SSI DERMATOPHYTE PCR KIT PRUEBA PCR DERMATOFITO 2 Prueba de PCR para la detección de dermatofitos y Trichophyton rubrum Para uso diagnóstico in vitro Aplicación La prueba de PCR para dermatofitos en uñas
SSI DERMATOPHYTE PCR KIT PRUEBA PCR DERMATOFITO 2 Prueba de PCR para la detección de dermatofitos y Trichophyton rubrum Para uso diagnóstico in vitro Aplicación La prueba de PCR para dermatofitos en uñas
Fortel PROSTATE (PSA)
 Fortel PROSTATE (PSA) Test para Screening Simple, realizable y confidencial [Seleccione la fecha] Un test visual fácil, para detectar niveles anormales del Antígeno Prostático Específico (PSA), sobre rango
Fortel PROSTATE (PSA) Test para Screening Simple, realizable y confidencial [Seleccione la fecha] Un test visual fácil, para detectar niveles anormales del Antígeno Prostático Específico (PSA), sobre rango
MANUAL DE NORMAS Y PROCEDIMIENTOS PROCEDIMIENTO: OPERATIVOS DE ORINAS
 SERVICIO DE LABORATORIO 1 DE 5 1. OBJETIVO El objetivo del presente documento es describir el procedimiento para determinar las características físicas, química y microscópicas de muestras de orinas. 2.
SERVICIO DE LABORATORIO 1 DE 5 1. OBJETIVO El objetivo del presente documento es describir el procedimiento para determinar las características físicas, química y microscópicas de muestras de orinas. 2.
Examen de laboratorio: Chagas. Obtención de sangre Cantidad Características Conservación Procesa miento En capilares Heparinizados.
 Examen de laboratorio: Chagas Examen de laboratorio Microconcentra ción en Micrométodo en tubo centración Strout ELISA IFI HAI Tipo de muestra venosa o Venosa Suero o plasma sanguíneo Obtención de sangre
Examen de laboratorio: Chagas Examen de laboratorio Microconcentra ción en Micrométodo en tubo centración Strout ELISA IFI HAI Tipo de muestra venosa o Venosa Suero o plasma sanguíneo Obtención de sangre
qprotein (BCA) Kit para cuantificar proteinas totales PB-L Productos Bio-Lógicos
 qprotein () Kit para cuantificar proteinas totales PB-L http://www.pb-l.com.ar qprotein () Cat. no. RA03 CONTENIDO Componentes RA0301 RA0302 Buffer A 250 ml 500 ml Buffer B 5 ml 10 ml Proteína Patrón 5
qprotein () Kit para cuantificar proteinas totales PB-L http://www.pb-l.com.ar qprotein () Cat. no. RA03 CONTENIDO Componentes RA0301 RA0302 Buffer A 250 ml 500 ml Buffer B 5 ml 10 ml Proteína Patrón 5
PROCEDIMIENTO DETECCIÓN Y ENUMERACIÓN POR NUMERO MAS PROBABLE (NMP) CON ETAPA DE PRE- ENRIQUECIMIENTO DE ENTEROBACTERIACEAE EN ALIMENTOS
 Página 1 de 5 1. OBJETIVO Estimar el número de Enterobacteriaceae presentes en el alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos de consumo humano
Página 1 de 5 1. OBJETIVO Estimar el número de Enterobacteriaceae presentes en el alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos de consumo humano
One Step Dengue IgG/IgM Antibody Test
 One Step Dengue IgG/IgM Antibody Test Instrucciones de uso Formato: Cassette Espécimen: Suero/Plasma y Sangre Entera Numero de Catalogo: A03-08- 322 * Por favor, lea atentamente las instrucciones antes
One Step Dengue IgG/IgM Antibody Test Instrucciones de uso Formato: Cassette Espécimen: Suero/Plasma y Sangre Entera Numero de Catalogo: A03-08- 322 * Por favor, lea atentamente las instrucciones antes
EVALUACIÓN CIENTÍFICA DE LOS ADITIVOS ALIMENTARIOS
 EVALUACIÓN CIENTÍFICA DE LOS ADITIVOS ALIMENTARIOS La Evaluación científica de los aditivos alimentarios es el paso posterior a la solicitud por parte de la Comisión, dentro del procedimiento para la autorización
EVALUACIÓN CIENTÍFICA DE LOS ADITIVOS ALIMENTARIOS La Evaluación científica de los aditivos alimentarios es el paso posterior a la solicitud por parte de la Comisión, dentro del procedimiento para la autorización
3. MATERIALES Y MÉTODOS
 3. MATERIALES Y MÉTODOS En este trabajo se realizó un estudio experimental en muestras de sangre periférica de individuos del sexo masculino aparentemente sanos de Hermosillo, Sonora, México. Se empleo
3. MATERIALES Y MÉTODOS En este trabajo se realizó un estudio experimental en muestras de sangre periférica de individuos del sexo masculino aparentemente sanos de Hermosillo, Sonora, México. Se empleo
INSTRUCCIONES PARA LA PROFICIENCIA DE JUNIO
 15 de agosto de 2016 Laboratorios Participantes Programa de Proficiencia Laboratorios de Salud Pública De Puerto Rico Programa de Proficiencia Laboratorios de Salud Pública De Puerto Rico Programa de Proficiencia
15 de agosto de 2016 Laboratorios Participantes Programa de Proficiencia Laboratorios de Salud Pública De Puerto Rico Programa de Proficiencia Laboratorios de Salud Pública De Puerto Rico Programa de Proficiencia
BIORREACTRES. Estudios básicos y aplicados sobre procesos de fermentación
 BIORREACTRES Ing. en Alimentos Estudios básicos y aplicados sobre procesos de fermentación Mg. Anahí V. Cuellas Docente investigadora Universidad Nacional de Quilmes TRABAJO PRACTICO Obtención de enzimas
BIORREACTRES Ing. en Alimentos Estudios básicos y aplicados sobre procesos de fermentación Mg. Anahí V. Cuellas Docente investigadora Universidad Nacional de Quilmes TRABAJO PRACTICO Obtención de enzimas
CONTROL DE CAMBIOS Y MEJORAS
 Página: 1 de 5 CONTROL DE CAMBIOS Y MEJORAS NIVEL DE REVISIÓN SECCIÓN Y/O PÁGINA DESCRIPCIÓN DE LA MODIFICACIÓN Y MEJORA FECHA DE MODIFICACIÓN 01 Políticas Descripción de las actividades Se cambio el horario
Página: 1 de 5 CONTROL DE CAMBIOS Y MEJORAS NIVEL DE REVISIÓN SECCIÓN Y/O PÁGINA DESCRIPCIÓN DE LA MODIFICACIÓN Y MEJORA FECHA DE MODIFICACIÓN 01 Políticas Descripción de las actividades Se cambio el horario
Estudios microbiológicos.procedimientos. 1. Urocultivos
 Estudios microbiológicos.procedimientos 1. Urocultivos Se realizará el cultivo de orina a todas las muestras llegadas al laboratorio, que cumplan con los requisitos para la toma, conservación y transporte
Estudios microbiológicos.procedimientos 1. Urocultivos Se realizará el cultivo de orina a todas las muestras llegadas al laboratorio, que cumplan con los requisitos para la toma, conservación y transporte
Inmunohematología. Dra. Ana Cecilia Haro
 Inmunohematología 2016 Dra. Ana Cecilia Haro Sensibilización Aglutinación Ag + Ac Ag-Ac Enzimas LISS SAGH PEG Polibrene Albúmina Potencial zeta Tipo de Ac Densidad antigénica Tiempo de incubación Fuerza
Inmunohematología 2016 Dra. Ana Cecilia Haro Sensibilización Aglutinación Ag + Ac Ag-Ac Enzimas LISS SAGH PEG Polibrene Albúmina Potencial zeta Tipo de Ac Densidad antigénica Tiempo de incubación Fuerza
BD ProbeTec ET Instrucciones de equipos periféricos para micobacterias
 BD ProbeTec ET Instrucciones de equipos periféricos para micobacterias 2003/07 Becton, Dickinson and Company Número de documento: L 006357(B) 7 Loveton Circle Sparks, Maryland 21152 EE.UU. Tel: 800.638.8663
BD ProbeTec ET Instrucciones de equipos periféricos para micobacterias 2003/07 Becton, Dickinson and Company Número de documento: L 006357(B) 7 Loveton Circle Sparks, Maryland 21152 EE.UU. Tel: 800.638.8663
Conceptos básicos para la toma, muestra, transporte, conservación y almacenamiento de muestras.
 Conceptos básicos para la toma, muestra, transporte, conservación y almacenamiento de muestras. A continuación se muestran los conceptos básicos para una buena toma de muestras cualquier información relevante,
Conceptos básicos para la toma, muestra, transporte, conservación y almacenamiento de muestras. A continuación se muestran los conceptos básicos para una buena toma de muestras cualquier información relevante,
Experto en Análisis de Muestras en el Laboratorio de Microbiología
 Experto en Análisis de Muestras en el Laboratorio de Microbiología Sanidad, Dietética y Nutrición Ficha Técnica Categoría Laboratorios, Microbiología y Farmacia Contenido del Pack - 1 Manual Teórico -
Experto en Análisis de Muestras en el Laboratorio de Microbiología Sanidad, Dietética y Nutrición Ficha Técnica Categoría Laboratorios, Microbiología y Farmacia Contenido del Pack - 1 Manual Teórico -
SOLICITUD DE COTIZACIÓN REACTIVOS PARA LABORATORIO CLINICO Proceso de Compra Menor
 CAJA DE SALUD DE LA BANCA PRIVADA www.csbp.com.bo REGIONAL Cochabamba SOLICITUD DE COTIZACIÓN REACTIVOS PARA LABORATORIO CLINICO Proceso de Compra Menor N RL-06/13 N RL-06/13 Cochabamba 5 de Agosto de
CAJA DE SALUD DE LA BANCA PRIVADA www.csbp.com.bo REGIONAL Cochabamba SOLICITUD DE COTIZACIÓN REACTIVOS PARA LABORATORIO CLINICO Proceso de Compra Menor N RL-06/13 N RL-06/13 Cochabamba 5 de Agosto de
PRACTICA Núm. 22 INVESTIGACION DE COLIFORMES TOTALES Y FECALES EN DESECHOS SOLIDOS Y COMPOSTA
 PRACTICA Núm. 22 INVESTIGACION DE COLIFORMES TOTALES Y FECALES EN DESECHOS SOLIDOS Y COMPOSTA I. OBJETIVO Determinar la presencia de coliformes totales y fecales en un desecho sólido por el método del
PRACTICA Núm. 22 INVESTIGACION DE COLIFORMES TOTALES Y FECALES EN DESECHOS SOLIDOS Y COMPOSTA I. OBJETIVO Determinar la presencia de coliformes totales y fecales en un desecho sólido por el método del
Material tomado del Manual d Estades en Pràctiques Tutelades, Facultat de Farmàcia, UB.
 Material tomado del Manual d Estades en Pràctiques Tutelades, Facultat de Farmàcia, UB. Que hay que saber para implementar el servicio de cribado del VIH en la farmacia M.Angeles Via, Marian March Profesoras
Material tomado del Manual d Estades en Pràctiques Tutelades, Facultat de Farmàcia, UB. Que hay que saber para implementar el servicio de cribado del VIH en la farmacia M.Angeles Via, Marian March Profesoras
INSTRUCCIÓN TÉCNICA DISTRIBUCIÓN: Jefe de la Unidad de Calidad SUMARIO DE MODIFICACIONES
 Determinación del antígeno D Débil Du Página 1 de 5 DISTRIBUCIÓN: DEPARTAMENTO Dirección Hematología Enfermería RESPONSABLE Jefe de la Unidad de Calidad Jefe de la Unidad de Hematología Coordinadora de
Determinación del antígeno D Débil Du Página 1 de 5 DISTRIBUCIÓN: DEPARTAMENTO Dirección Hematología Enfermería RESPONSABLE Jefe de la Unidad de Calidad Jefe de la Unidad de Hematología Coordinadora de
PV-1 Agitador vórtex personal
 PV-1 Agitador vórtex personal Manual de funcionamiento Certificado para la versión V.1AW Contenidos 1. Precauciones de seguridad 2. Información general 3. Cómo empezar 4. Funcionamiento 5. Especificaciones
PV-1 Agitador vórtex personal Manual de funcionamiento Certificado para la versión V.1AW Contenidos 1. Precauciones de seguridad 2. Información general 3. Cómo empezar 4. Funcionamiento 5. Especificaciones
Esmalte Directo Sobre Hierro y Óxido Forja
 Esmalte Directo Sobre Hierro y Óxido Forja DEFINICIÓN PRODUCTO Óxido brinda una protección óptima de hasta 8 años a las barandillas y rejas de metal. Su fórmula especial actúa a la vez como fondo eficaz
Esmalte Directo Sobre Hierro y Óxido Forja DEFINICIÓN PRODUCTO Óxido brinda una protección óptima de hasta 8 años a las barandillas y rejas de metal. Su fórmula especial actúa a la vez como fondo eficaz
Ficha técnica del producto. Agente Floculante Aquabase Plus P P Agente Floculante Base agua
 Ficha técnica del producto MASTER INTERNACIONAL Agente Floculante Aquabase Plus P872-1000 Producto Descripción P872-1000 Agente Floculante Base agua Descripción del producto P872-1000 se ha desarrollado
Ficha técnica del producto MASTER INTERNACIONAL Agente Floculante Aquabase Plus P872-1000 Producto Descripción P872-1000 Agente Floculante Base agua Descripción del producto P872-1000 se ha desarrollado
RESULTADOS Y DISCUSIÓN
 RESULTADOS Y DISCUSIÓN Extracción de ADN en sangre periférica La técnica de extracción por GeneClean empleada en este trabajo dio un buen rendimiento, ya que la cantidad de ADN y el nivel de purificación
RESULTADOS Y DISCUSIÓN Extracción de ADN en sangre periférica La técnica de extracción por GeneClean empleada en este trabajo dio un buen rendimiento, ya que la cantidad de ADN y el nivel de purificación
TÍTULO: Determinación de hidrocarburos en muestras de suelo mediante espectrofotometría
 Página 1 de 7 1.- INTRODUCCIÓN El presente método es aplicable para el análisis de residuos de aceites minerales en suelo, en concentraciones superiores a 20 mg/kg. El análisis mediante espectrofotometría,
Página 1 de 7 1.- INTRODUCCIÓN El presente método es aplicable para el análisis de residuos de aceites minerales en suelo, en concentraciones superiores a 20 mg/kg. El análisis mediante espectrofotometría,
NycoCard CRP Single Test
 NycoCard CRP Single Test ES DESCRIPCION DEL PRODUCTO Aplicaciones NycoCard CRP Single Test es un test de diagnóstico in vitro para medir de una forma rápida la proteína C reactiva (CRP) en la sangre humana.
NycoCard CRP Single Test ES DESCRIPCION DEL PRODUCTO Aplicaciones NycoCard CRP Single Test es un test de diagnóstico in vitro para medir de una forma rápida la proteína C reactiva (CRP) en la sangre humana.
Indicadores Químicos y Biológicos para la esterilización térmica de cargas líquidas
 Indicadores Químicos y Biológicos para la esterilización térmica de cargas líquidas Terragene ofrece un método simple y eficaz para controlar con precisión el proceso de esterilización en la industria
Indicadores Químicos y Biológicos para la esterilización térmica de cargas líquidas Terragene ofrece un método simple y eficaz para controlar con precisión el proceso de esterilización en la industria
PRÁCTICA 1: MÉTODOS DE RUPTURA CELULAR
 PRÁCTICA 1: MÉTODOS DE RUPTURA CELULAR FUNDAMENTO TEÓRICO Para estudiar la estructura y/o las funciones metabólicas de los distintos compartimentos celulares hay que aislarlos del resto de los orgánulos.
PRÁCTICA 1: MÉTODOS DE RUPTURA CELULAR FUNDAMENTO TEÓRICO Para estudiar la estructura y/o las funciones metabólicas de los distintos compartimentos celulares hay que aislarlos del resto de los orgánulos.
DIRECTRICES QUALANOD HOJA DE ACTUALIZACIÓN Nº 16 Edición Página 1 de 5 INSPECCIONES RUTINARIAS A LICENCIATARIOS
 Página 1 de 5 INSPECCIONES RUTINARIAS A LICENCIATARIOS Propuesta: Comité Técnico Decisión de QUALANOD: Reunión noviembre 2012 Fecha de aplicación: 1 de julio de 2013 Parte de las Directrices a la que afecta:
Página 1 de 5 INSPECCIONES RUTINARIAS A LICENCIATARIOS Propuesta: Comité Técnico Decisión de QUALANOD: Reunión noviembre 2012 Fecha de aplicación: 1 de julio de 2013 Parte de las Directrices a la que afecta:
ACCUTREND GCT Manual formación. Ref:
 ACCUTREND GCT Manual formación Ref: 04898249001 Accutrend GCT Determinación inmediata de los principales factores de riesgo cardiovascular Gracias a la tecnología de la química seca es posible realizar
ACCUTREND GCT Manual formación Ref: 04898249001 Accutrend GCT Determinación inmediata de los principales factores de riesgo cardiovascular Gracias a la tecnología de la química seca es posible realizar
Ficha Técnica. Categoría. Contenido del Pack. Sinopsis. Laboratorios, Microbiología y Farmacia. - 2 Manual Teórico - 1 Cuaderno de Ejercicios
 Ficha Técnica Categoría Laboratorios, Microbiología y Farmacia Contenido del Pack - 2 Manual Teórico - 1 Cuaderno de Ejercicios Sinopsis La importancia del auxiliar de laboratorio radica en la importancia
Ficha Técnica Categoría Laboratorios, Microbiología y Farmacia Contenido del Pack - 2 Manual Teórico - 1 Cuaderno de Ejercicios Sinopsis La importancia del auxiliar de laboratorio radica en la importancia
TITULO DEL PROCEDIMIENTO RECUENTO DE LEUCOCITOS EN SANGRE TOTAL
 PAGINA: 1 de n RECUENTO DE LEUCOCITOS EN SANGRE TOTAL OBJETO Establecer el procedimiento para realizar el recuento de leucocitos o glóbulos blancos en el laboratorio CALIDAD. CAMPO DE APLICACIÓN Este procedimiento
PAGINA: 1 de n RECUENTO DE LEUCOCITOS EN SANGRE TOTAL OBJETO Establecer el procedimiento para realizar el recuento de leucocitos o glóbulos blancos en el laboratorio CALIDAD. CAMPO DE APLICACIÓN Este procedimiento
DECISIÓN DE LA COMISIÓN
 L 336/36 Diario Oficial de la Unión Europea 18.12.2009 DECISIÓN DE LA COMISIÓN de 15 de diciembre de 2009 por la que se modifica el anexo D de la Directiva 64/432/CEE del Consejo en lo relativo a las pruebas
L 336/36 Diario Oficial de la Unión Europea 18.12.2009 DECISIÓN DE LA COMISIÓN de 15 de diciembre de 2009 por la que se modifica el anexo D de la Directiva 64/432/CEE del Consejo en lo relativo a las pruebas
PRACTICA #5 BIOLOGIA CELULAR VETERINARIA SOLUCIONES HIPERTONICAS E HIPOTONICAS
 PRACTICA #5 BIOLOGIA CELULAR VETERINARIA SOLUCIONES HIPERTONICAS E HIPOTONICAS OBJETIVO: Observar el efecto de las soluciones con diferente concentración de soluto en células sanguíneas. FUNDAMENTO: Todas
PRACTICA #5 BIOLOGIA CELULAR VETERINARIA SOLUCIONES HIPERTONICAS E HIPOTONICAS OBJETIVO: Observar el efecto de las soluciones con diferente concentración de soluto en células sanguíneas. FUNDAMENTO: Todas
Número total de casos declarados en el último año. Población total del país de ese año
 5. Indicadores del Plan A. Tasa de notificación de casos Es un indicador del European Center for Disease Prevention and Control (ECDC), informa sobre la carga de enfermedad, el número de casos declarados
5. Indicadores del Plan A. Tasa de notificación de casos Es un indicador del European Center for Disease Prevention and Control (ECDC), informa sobre la carga de enfermedad, el número de casos declarados
Técnico en Hematología y Hemoterapia. Sanidad, Dietética y Nutrición
 Técnico en Hematología y Hemoterapia Sanidad, Dietética y Nutrición Ficha Técnica Categoría Sanidad, Dietética y Nutrición Referencia 166762-1501 Precio 50.36 Euros Sinopsis La sangre es la especialidad
Técnico en Hematología y Hemoterapia Sanidad, Dietética y Nutrición Ficha Técnica Categoría Sanidad, Dietética y Nutrición Referencia 166762-1501 Precio 50.36 Euros Sinopsis La sangre es la especialidad
FUNDAMENTO MATERIAL Y EQUIPOS. Entre otros materiales es necesario disponer de:
 González,E.yAlloza,A.M. Ensayos para determinar las propiedades mecánicas y físicas de los áridos: métodos para la determinación de la resistencia a la fragmentación. Determinación de la resistencia a
González,E.yAlloza,A.M. Ensayos para determinar las propiedades mecánicas y físicas de los áridos: métodos para la determinación de la resistencia a la fragmentación. Determinación de la resistencia a
ph DE LOS SUELOS I.N.V. E
 ph DE LOS SUELOS I.N.V. E 131 07 1. OBJETO 1.1 Este método de prueba cubre la determinación del ph de los suelos para usos diferentes de la prueba de corrosión. Tales determinaciones se usan en campos
ph DE LOS SUELOS I.N.V. E 131 07 1. OBJETO 1.1 Este método de prueba cubre la determinación del ph de los suelos para usos diferentes de la prueba de corrosión. Tales determinaciones se usan en campos
CYP 2C9 A1075C CYP2C9*3
 CYP 2C9 A1075C Sistema para la detección de la mutación A1075C en el gene del citocromo P450 2C9. Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336 71 60. Info@atgen.com.uy
CYP 2C9 A1075C Sistema para la detección de la mutación A1075C en el gene del citocromo P450 2C9. Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336 71 60. Info@atgen.com.uy
Fotosíntesis. 6CO 2 + 6H 2 O C 6 H 12 O 6 ( Glucosa) + O 2. Enzimas. Clorofila
 Fotosíntesis Proceso de biosíntesis ( vía anabólica). Químicamente: reducción. Transformación: energía lumínica a química. Ubicación: eucariotas : cloroplastos. procariotas: cromatóforos. Fuente de energía:
Fotosíntesis Proceso de biosíntesis ( vía anabólica). Químicamente: reducción. Transformación: energía lumínica a química. Ubicación: eucariotas : cloroplastos. procariotas: cromatóforos. Fuente de energía:
PREPARACIÓN DE MEDIOS DE CULTIVO
 Introducción Clasificación de los medios de cultivo Almacenamiento de los medios de cultivo Trabajo Práctico Nº 6 PREPARACIÓN DE MEDIOS DE CULTIVO Objetivo Fundamento Procedimiento Resultados Bibliografía
Introducción Clasificación de los medios de cultivo Almacenamiento de los medios de cultivo Trabajo Práctico Nº 6 PREPARACIÓN DE MEDIOS DE CULTIVO Objetivo Fundamento Procedimiento Resultados Bibliografía
Familia de Productos BD Microtainer
 Familia de Productos BD Microtainer Cuando cada gota cuenta Presentamos el NUEVO BD Microtainer MAP Tubo para microrecolección para proceso automatizado En el cuidado de sus pacientes más frágiles, mantenga
Familia de Productos BD Microtainer Cuando cada gota cuenta Presentamos el NUEVO BD Microtainer MAP Tubo para microrecolección para proceso automatizado En el cuidado de sus pacientes más frágiles, mantenga
Reglamento de Laboratorio de Químico
 REGLAMENTO DE laboratorio químico 111 Reglamento de Laboratorio de Químico REGLAMENTO DEL LABORATORIO QUÍMICO El laboratorio de Química está diseñado para que se entienda y profundice en algunos conceptos,
REGLAMENTO DE laboratorio químico 111 Reglamento de Laboratorio de Químico REGLAMENTO DEL LABORATORIO QUÍMICO El laboratorio de Química está diseñado para que se entienda y profundice en algunos conceptos,
> NT-32 rev. 2 ENAC Tipo III: Métodos basados en métodos de referencia Tipo IV: Otros métodos.
 > NT-32 rev. 2 ENAC Tipo III: Métodos basados en métodos de referencia. Métodos descritos en procedimientos internos del laboratorio, que están basados claramente en métodos de referencia y que no suponen
> NT-32 rev. 2 ENAC Tipo III: Métodos basados en métodos de referencia. Métodos descritos en procedimientos internos del laboratorio, que están basados claramente en métodos de referencia y que no suponen
TEMA 8: HEMATOLOGÍA. Hematíes: < Anemia, > Policitemia Leucocitos:<Leucopenia,>Leucocitosis Plaquetas: <Trombocitopenia, > Trombocitosis
 b) Métodos automáticos: basados en variaciones en la conductividad o resistencia, basados en la difracción Células: TEMA 8: HEMATOLOGÍA Hematíes: < Anemia, > Policitemia Leucocitos:Leucocitosis
b) Métodos automáticos: basados en variaciones en la conductividad o resistencia, basados en la difracción Células: TEMA 8: HEMATOLOGÍA Hematíes: < Anemia, > Policitemia Leucocitos:Leucocitosis
OBTENCIÓN, PREPARACIÓN Y ENVÍO DE BIOPSIAS DE BAZO
 1 de 7 MANUAL DE PROCEDIMIENTOS OBTENCIÓN, PREPARACIÓN Y ENVÍO DE BIOPSIAS DE BAZO CONTROLADA Nº DESTINATARIO FECHA ENTREGA ENTREGADO POR Nombre Firma NO CONTROLADA ENTRADA EN REVISIÓN REALIZADO FECHA
1 de 7 MANUAL DE PROCEDIMIENTOS OBTENCIÓN, PREPARACIÓN Y ENVÍO DE BIOPSIAS DE BAZO CONTROLADA Nº DESTINATARIO FECHA ENTREGA ENTREGADO POR Nombre Firma NO CONTROLADA ENTRADA EN REVISIÓN REALIZADO FECHA
J. Muestras Proficiencia para Contaje de Espermatozoides.
 22 de febrero de 2016 Laboratorios Participantes Programa de Proficiencia Laboratorios de Salud Pública De Puerto Rico Programa de Proficiencia Laboratorios de Salud Pública De Puerto Rico Programa de
22 de febrero de 2016 Laboratorios Participantes Programa de Proficiencia Laboratorios de Salud Pública De Puerto Rico Programa de Proficiencia Laboratorios de Salud Pública De Puerto Rico Programa de
PRÁCTICA NÚMERO 2 DETERMINACIÓN DE DENSIDAD: MÉTODO DEL PICNÓMETRO
 PRÁCTICA NÚMERO 2 DETERMINACIÓN DE DENSIDAD: MÉTODO DEL PICNÓMETRO I. Objetivo Haciendo uso del picnómetro: 1. Determinar la densidad absoluta del agua. 2. Determinar la variación de la densidad con la
PRÁCTICA NÚMERO 2 DETERMINACIÓN DE DENSIDAD: MÉTODO DEL PICNÓMETRO I. Objetivo Haciendo uso del picnómetro: 1. Determinar la densidad absoluta del agua. 2. Determinar la variación de la densidad con la
Jueves 13 de septiembre de 2012 DIARIO OFICIAL (Segunda Sección) 91
 Jueves 13 de septiembre de 2012 DIARIO OFICIAL (Segunda Sección) 91 NOTA Aclaratoria a la Primera Actualización de la Edición 2011 del Cuadro Básico y Catálogo de Auxiliares de Diagnóstico, publicada el
Jueves 13 de septiembre de 2012 DIARIO OFICIAL (Segunda Sección) 91 NOTA Aclaratoria a la Primera Actualización de la Edición 2011 del Cuadro Básico y Catálogo de Auxiliares de Diagnóstico, publicada el
PROCEDIMIENTO DE EVALUACIÓN Y ACREDITACIÓN DE LAS COMPETENCIAS PROFESIONALES CUESTIONARIO DE AUTOEVALUACIÓN PARA LAS TRABAJADORAS Y TRABAJADORES
 MINISTERIO DE EDUCACIÓN SECRETARÍA DE ESTADO DE EDUCACIÓN Y FORMACIÓN PROFESIONAL DIRECCIÓN GENERAL DE FORMACIÓN PROFESIONAL INSTITUTO NACIONAL DE LAS CUALIFICACIONES PROCEDIMIENTO DE EVALUACIÓN Y ACREDITACIÓN
MINISTERIO DE EDUCACIÓN SECRETARÍA DE ESTADO DE EDUCACIÓN Y FORMACIÓN PROFESIONAL DIRECCIÓN GENERAL DE FORMACIÓN PROFESIONAL INSTITUTO NACIONAL DE LAS CUALIFICACIONES PROCEDIMIENTO DE EVALUACIÓN Y ACREDITACIÓN
Determinación de Alcalinidad en aguas naturales y residuales
 QUÍMICA ANALITICA APLICADA INORGÁNICA QMC 613 Determinación de Alcalinidad en aguas naturales y residuales Procedimiento Operativo Estándar Lic. Luis Fernando Cáceres Choque 29/09/2013 Método Titulométrico
QUÍMICA ANALITICA APLICADA INORGÁNICA QMC 613 Determinación de Alcalinidad en aguas naturales y residuales Procedimiento Operativo Estándar Lic. Luis Fernando Cáceres Choque 29/09/2013 Método Titulométrico
ANALISIS CITOMETRICO DEL CONTENIDO EN DNA EN SANGRE Y MEDULA OSEA
 ANALISIS CITOMETRICO DEL CONTENIDO EN DNA EN SANGRE Y MEDULA OSEA Sistema DNA-Prep (Beckman-Coulter) DNA-Prep LPR: Reactivo de lisis de los eritrocitos y permeabilización de membranas celulares DNA-Prep
ANALISIS CITOMETRICO DEL CONTENIDO EN DNA EN SANGRE Y MEDULA OSEA Sistema DNA-Prep (Beckman-Coulter) DNA-Prep LPR: Reactivo de lisis de los eritrocitos y permeabilización de membranas celulares DNA-Prep
OBTENCIÓN, PREPARACIÓN Y ENVÍO DE MUESTRAS DE SANGRE
 1 de 5 MANUAL DE PROCEDIMIENTOS OBTENCIÓN, PREPARACIÓN Y ENVÍO DE MUESTRAS DE SANGRE CONTROLADA Nº DESTINATARIO FECHA ENTREGA ENTREGADO POR Nombre Firma NO CONTROLADA REVISIÓN REALIZADO FECHA APROBADO
1 de 5 MANUAL DE PROCEDIMIENTOS OBTENCIÓN, PREPARACIÓN Y ENVÍO DE MUESTRAS DE SANGRE CONTROLADA Nº DESTINATARIO FECHA ENTREGA ENTREGADO POR Nombre Firma NO CONTROLADA REVISIÓN REALIZADO FECHA APROBADO
REPÚBLICA DE CUBA MINISTERIO DE SALUD PÚBLICA CENTRO PARA EL CONTROL ESTATAL DE LA CALIDAD DE LOS MEDICAMENTOS. REGULACIÓN No.
 REPÚBLICA DE CUBA MINISTERIO DE SALUD PÚBLICA CENTRO PARA EL CONTROL ESTATAL DE LA CALIDAD DE LOS MEDICAMENTOS REGULACIÓN No. 6-2003 REQUISITOS DE LOS CONCENTRADOS LEUCOCITARIOS HUMANOS COMO MATERIA PRIMA
REPÚBLICA DE CUBA MINISTERIO DE SALUD PÚBLICA CENTRO PARA EL CONTROL ESTATAL DE LA CALIDAD DE LOS MEDICAMENTOS REGULACIÓN No. 6-2003 REQUISITOS DE LOS CONCENTRADOS LEUCOCITARIOS HUMANOS COMO MATERIA PRIMA
TECNICA DE INMUNOHISTOQUIMICA *IHQ*
 Hospital General ISSS TECNICA DE INMUNOHISTOQUIMICA *IHQ* Tec. Delmy de Chávez Sep/2010 Estufa EQUIPO BASICO Baño de María EQUIPO BASICO Microscopio EQUIPO BASICO Medidor de ph. EQUIPO BASICO Refrigeradora
Hospital General ISSS TECNICA DE INMUNOHISTOQUIMICA *IHQ* Tec. Delmy de Chávez Sep/2010 Estufa EQUIPO BASICO Baño de María EQUIPO BASICO Microscopio EQUIPO BASICO Medidor de ph. EQUIPO BASICO Refrigeradora
- Mencionar las Normas de Bioseguridad y precauciones necesarias para trabajar en el laboratorio microbiológico.
 Microbiología General e Inmunología Año 2012 Trabajo Práctico Nº1 Objetivos: Que el alumno sea capaz de: - Mencionar las Normas de Bioseguridad y precauciones necesarias para trabajar en el laboratorio
Microbiología General e Inmunología Año 2012 Trabajo Práctico Nº1 Objetivos: Que el alumno sea capaz de: - Mencionar las Normas de Bioseguridad y precauciones necesarias para trabajar en el laboratorio
REPÚBLICA DE PANAMÁ MINISTERIO DE SALUD. DECRETO EJECUTIVO No (De 27 de agosto de 2007 ) EL PRESIDENTE DE LA REPÚBLICA,
 1 REPÚBLICA DE PANAMÁ MINISTERIO DE SALUD DECRETO EJECUTIVO No. 340 (De 27 de agosto de 2007 ) "Por el cual se modifica el Capítulo V del Título II del Decreto Ejecutivo 178 de 12 de julio de 2001, Que
1 REPÚBLICA DE PANAMÁ MINISTERIO DE SALUD DECRETO EJECUTIVO No. 340 (De 27 de agosto de 2007 ) "Por el cual se modifica el Capítulo V del Título II del Decreto Ejecutivo 178 de 12 de julio de 2001, Que
REPUBLICA DE CUBA MINISTERIO DE SALUD PUBLICA CENTRO PARA EL CONTROL ESTATAL DE LA CALIDAD DE LOS MEDICAMENTOS. REGULACION No.
 REPUBLICA DE CUBA MINISTERIO DE SALUD PUBLICA CENTRO PARA EL CONTROL ESTATAL DE LA CALIDAD DE LOS MEDICAMENTOS REGULACION No. 35 2003 REQUISITOS DEL PLASMA HUMANO COMO MATERIA PRIMA FARMACEUTICA CECMED,
REPUBLICA DE CUBA MINISTERIO DE SALUD PUBLICA CENTRO PARA EL CONTROL ESTATAL DE LA CALIDAD DE LOS MEDICAMENTOS REGULACION No. 35 2003 REQUISITOS DEL PLASMA HUMANO COMO MATERIA PRIMA FARMACEUTICA CECMED,
Nadia Isabel Hornquist Hurtarte Química Bióloga Clínica de Enfermedades Infecciosas Hospital Roosevelt
 Nadia Isabel Hornquist Hurtarte Química Bióloga Clínica de Enfermedades Infecciosas Hospital Roosevelt Fase aguda: Entre el 40% a 90% sintomáticos (similar mononucleosis) Fase crónica: asintomaticos El
Nadia Isabel Hornquist Hurtarte Química Bióloga Clínica de Enfermedades Infecciosas Hospital Roosevelt Fase aguda: Entre el 40% a 90% sintomáticos (similar mononucleosis) Fase crónica: asintomaticos El
- Obtención y duplicación de células OMKs. - Infección y obtención de sobrenadante. - Proveedores.
 INMUNOLOGÍA http://www.ucm.es/info/inmuno/regueiro.htm FACULTAD DE MEDICINA UNIVERSIDAD COMPLUTENSE TEL: 91 3941642 28040 MADRID FAX: 91 3941641 rmorenop@med.ucm.es Teresa Español Unidad de Inmunología
INMUNOLOGÍA http://www.ucm.es/info/inmuno/regueiro.htm FACULTAD DE MEDICINA UNIVERSIDAD COMPLUTENSE TEL: 91 3941642 28040 MADRID FAX: 91 3941641 rmorenop@med.ucm.es Teresa Español Unidad de Inmunología
