PROCEDIMIENTO BÁSICOS
|
|
|
- Diego Jiménez Montes
- hace 8 años
- Vistas:
Transcripción
1 PROCEDIMIENTO BÁSICOS TABLA 3: PROCEDIMIENTOS BÁSICOS EN MICOLOGÍA EL LABORATORIO en las MICOSIS CUTÁNEAS Toma de muestras Examen directo (ED) Cultivo Identificación TOMA DE MUESTRA Reviste una importancia primordial. El diagnóstico va a depender en buena medida de la calidad de la muestra que va a procesarse. No debemos olvidar, pues, algunos condicionantes básicos a la hora de la recogida de muestras en las dermatomicosis. a) Asegurarse de que no haya habido tratamiento antifúngico previo, sobre todo sistémico. En tal caso, demorar la toma de muestras hasta pasadas al menos dos semanas. b) Recoger una cantidad suficiente de material patológico. c) Utilizar el instrumental adecuado al tipo de muestra de que se trate. El instrumental para la toma de muestras comprende pequeños utensilios adecuados para practicar el raspado de las lesiones y obtener las escamas y fragmentos de pelo que van a estudiarse. A tal fin, pueden emplearse hojas de bisturí, curettes, plumillas metálicas o incluso los bordes de los portaobjetos. Nosotros adoptamos hace tiempo el uso de los vacinostilos, que ofrecen múltiples ventajas: son estériles, desechables, fáciles de obtener, de coste muy bajo, y su forma permite emplearlos tanto para raspar en superficie mediante su extremo plano, como para obtener material del lecho ungueal en las onicomicosis por medio de su extremo punzante. En las micosis ungueales, sin embargo, preferimos tomar la muestra con la pequeña cucharilla del cuchillo de Le Cron, un instrumento de uso habitual en odontología y fácil de encontrar en las tiendas o proveedores de instrumental médico (Fig. 1). 13
2 EL LABORATORIO en las MICOSIS CUTÁNEAS Comenzamos por limpiar bien la zona sospechosa con alcohol o lavado jabonoso, eliminando restos de pomadas, suciedad y restos epidérmicos. Nos aseguramos de que no ha existido tratamiento antifúngico en los últimos días, en caso afirmativo lo suspendemos y retrasamos la toma una o dos semanas. Diferenciamos una serie de detalles para la toma micológica según la realicemos, en una pitiriasis versicolor, una tiña, una candidosis o en micosis ungueales (Tabla 4). 1. PITIRIASIS VERSICOLOR TABLA 4: TOMA DE MUESTRAS 2. TIÑAS Tiñas del pelo Tiñas de la piel lampiña 3. CANDIDOSIS Candidosis cutáneas Candidosis mucosas 4. MICOSIS UNGUEALES PITIRIASIS VERSICOLOR Lo más sencillo, es el raspado de las escamas furfuráceas y finas de las lesiones con el borde de un portaobjeto, depositando el producto del raspado en otro portaobjeto que colocamos en posición horizontal bajo la lesión. Existen otros procedimientos entre los que destacamos la utilización de la cinta adhesiva ( cello, cinta adhesiva), con la que presionamos fuertemente sobre la lesión y a continuación pegamos en un portaobjeto. La maniobra también puede llevarse a cabo con un portaobjeto en el que hemos depositado previamente unas gotas de cola de contacto de cianocrilato. Esperando unos segundos, la aplicamos sobre una plaquita de la enfermedad, al endurecerse la cola y retirar el portaobjeto arrancamos la superficie escamosa, lista para teñir (Figs. 2, 3). 15
3 Atlas de MICOLOGÍA CUTÁNEA Fig. 2. Pitiriasis toma con fixo 16 Fig. 3. Pitiriasis toma con portaobjeto
4 EL LABORATORIO en las MICOSIS CUTÁNEAS TIÑAS Sin olvidar las premisas indicadas al principio, describiremos la toma según sea la tiña de piel lampiña o glabra (sin cabellos), de zonas pilosas o bien de uñas. Toma de muestra de piel lampiña (Tinea corporis, tinea faciei, tinea cruris, tinea manuum y tinea pedis). Raspamos en la periferia de la lesión, ya que la zona central de la misma, redondeada casi siempre, está escasamente parasitada. Lo realizamos con un bisturí, vacinoestilo, escalpelo o con el borde de un portaobjeto. Recogemos en otro portaobjeto las escamas, las guardamos entre dos portaobjetos e identificamos con sumo cuidado la toma. Si la lesión presenta vesículas (tinea pedis, tiñas inflamatorias) rompemos las mismas (Figs. 4-6). Fig. 4. Tiña toma con portaobjeto 17
5 Atlas de MICOLOGÍA CUTÁNEA Fig. 5. Tiña toma con portaobjeto 18 Fig. 6. Tiña toma vacionestilo
6 EL LABORATORIO en las MICOSIS CUTÁNEAS Toma de muestra de zonas pilosas (Tinea capitis, tinea barbae). Lo más sencillo es raspar enérgicamente el borde de la lesión con lo que obtenemos no sólo escamas sino también pelos parasitados. Es útil el uso de pinzas de depilación para obtener pelos parasitados, que no ofrecen resistencia a la tracción, y que nos permiten el examen directo del parasitismo piloso en el cultivo. En las tiñas inflamatorias de estas localizaciones o bien, obtenemos los pelos como hemos indicado, o simplemente tomamos el material purulento con un hisopo bacteriológico estéril. En ocasiones, se lleva a cabo con cepillos de plástico estériles o bien, con un fragmento cuadrado de moqueta estéril, con los que frotamos la zona sospechosa, y a continuación se inoculan directamente las placas de Petri con el medio. No hay que olvidar que los cabellos o pelos de la barba sanos (ofrecen resistencia a la tracción) obtenidos con pinzas no están parasitados y por tanto, no son útiles para el estudio. La luz de Wood puede ser útil en algunas tiñas causadas por Microsporum, al permitir encontrar más fácilmente los pelos parasitados por su fluorescencia verdosa (Figs. 7.1,7.2, 8). Fig Tiña toma zona pilosa 19
7 Atlas de MICOLOGÍA CUTÁNEA Fig Tiña toma zona pilosa 20 Fig. 8. Tiña barba, toma pelo
8 EL LABORATORIO en las MICOSIS CUTÁNEAS El material así obtenido en las diversas formas se puede depositar directamente en el portaobjetos para el examen directo, en una placa de Petri estéril o en un sobre estéril. Llamamos de nuevo la atención en el cuidado de la identificación correcta de la muestra. Para terminar, recordar que en las lesiones inflamatorias, las costras, secreciones y pelos, especialmente los centrales, no suelen contener hongos, por ello es necesario eliminarlos previamente. Y siempre es positivo realizar la toma en los bordes de la lesión. CANDIDOSIS Diferenciamos según la localización mucosa, cutánea o ungueal. En las mucosas (boca, genitales, ano) la recogida se puede realizar con hisopo bacteriológico de algodón estéril, o con esponjas de poliester humedecidas previamente en medios de cultivo líquido. En orofaringe, asimismo, podemos realizar enjuagues con suero fisiológico, que se siembra sobre una placa de Petri con medio sólido y permite hacer recuento del número de colonias. En las lesiones de piel la recogida la realizamos con el método descrito en las tiñas, pero señalando que es más aconsejable el fondo del pliegue para la toma. Si la lesión es húmeda utilizamos un hisopo estéril (Figs. 9,10). Fig. 9. Candidosis, toma bucal 21
9 Atlas de MICOLOGÍA CUTÁNEA 22 Fig. 10. Candidosis, toma en pliegues En la toma de las candidosis es preciso, no olvidar las condiciones previas pero, especialmente, tener en cuenta las condiciones de traslado al laboratorio, para evitar la desecación del material, ya que las candidas no sobreviven más de 24 horas en una toma seca. Por ello, es aconsejable utilizar hisopos con dispositivo de humedad, y siempre intentar que la muestra llegue inmediatamente al laboratorio. MICOSIS UNGUEALES Los resultados del estudio micológico van a depender en gran medida de la técnica utilizada para la obtención de muestras. En las uñas hay que extremar el cuidado, dado el alto porcentaje de falsos negativos. La técnica consiste en recortar con tijeras (alicates de podólogo para uñas de pies), procurando llegar hasta la frontera entre la invasión fúngica y la zona de uña sana, lugar donde los hongos son viables y por tanto cultivables. A continuación raspar con el extremo romo (cucharilla) del cuchillo de Le Cron. También se puede realizar con escarpelos, curetas o con el mismo ángulo del portaobjeto. Asimismo, puede utilizarse una fresa rotatoria (pequeño taladro) o incluso una biopsia punch ungueal. El material así obtenido se deposita entre dos portaobjetos, en una placa de Petri estéril o en un sobre estéril. Repartimos el material obtenido, para examen directo y para los diversos cultivos. Es aconsejable realizar, antes de la toma, un lavado enérgico y asegurarnos que no ha existido tratamiento antifúngico previo. Con estos cuidados hemos mejorado muy positivamente los porcentajes de falsos negativos (Figs. 11,12).
10 EL LABORATORIO en las MICOSIS CUTÁNEAS Fig. 11. Toma ungueal. Primero recortar Fig. 12. Toma ungueal. Segundo raspar 23
11 EL LABORATORIO en las MICOSIS CUTÁNEAS EXAMEN DIRECTO (KOH) Se denomina Examen Directo (ED) a la técnica diagnóstica cuya finalidad estriba en detectar u observar el agente infeccioso directamente en la muestra patológica, con ayuda de unos reactivos o colorantes simples. A diferencia de la histopatología, la muestra destinada al examen directo no necesita fijación ni preparación previa, y la observación puede llevarse a cabo de forma inmediata. No participamos en la afirmación de facilidad o sencillez con que se refieren la mayoría de los autores al ED, porque necesita un aprendizaje detallado; pero si compartimos la idea de que es una técnica muy práctica para identificar con rapidez la presencia de dermatofitos, levaduras y mohos. La técnica es bien simple. Sobre el material que habíamos destinado a ello en un portaobjetos se deposita una gota del reactivo elegido, habitualmente una solución de potasa, y se cubre con un cubreobjetos. Es indispensable calentar ligeramente la preparación a la llama de un mechero, y presionar suave y repetidamente con el mango del asa sobre el cubre, hasta que la muestra aparezca completamente disociada, es decir, hasta que el material queratinoso se haya disuelto bajo la acción de la potasa. Acto seguido, se procede a la observación al microscopio, utilizando primero los aumentos bajos (10X) y acto seguido, los altos (20X y 40X). El objetivo de inmersión no suele ser necesario. El Examen Directo es una técnica sumamente rentable. La dificultad radica fundamentalmente en la aparición de una serie de artefactos, que luego citaremos, que se asemejan en gran medida las verdaderas hifas del micelio. La solución a esta dificultad radica en hacer una adecuada preparación, la utilización del disgregante-colorante más idóneo y la práctica diaria de la observación microscópica, o sea de la experiencia personal. Describimos la técnica detalladamente (Figs ,14). 25
12 Atlas de MICOLOGÍA CUTÁNEA 1. Preparación: Depositamos una porción del material obtenido (escamas, pelos, uñas) en un portaobjetos, añadimos unas gotas del disgregante-colorante, se mezcla, se fragmenta mecánicamente (con la ayuda de un punzón), se coloca un cubreobjetos y se flamea suavemente evitando la ebullición. Si la muestra se obtuvo mediante torunda o escobillón puede practicarse el examen directo frotando un poco del mismo en un portaobjeto. A continuación aplicamos: Disgregante-colorante: Sustancias que facilitan la observación de filamentos, produciendo una separación de las escamas y fragmentos de uñas. La más usada es el hidróxido de potasio (KOH) en agua destilada al 20-40%. La capacidad disgregante de la potasa, para cabellos y uñas, aumenta si le añadimos dimetilsulfósido. Si le agregamos glicerina, aumenta la duración de la preparación hasta 48 horas, ya que evita la formación de cristales de potasa. La observación se facilita añadiendo un colorante a la potasa. El más usado era la tinta azul negra Parker Superchrome. En la actualidad, se está utilizando la solución de Swartz- Lamkins, que da resultados similares a la antigua fórmula. Existen numerosos colorantes como el clorazol, lactofenol, técnicas de fluorescencia, pero no se utilizan de rutina en el laboratorio. 2. Observación: Se realiza mediante microscopio óptico, mejor con condensador de contraste de fase, ya que los elementos fúngicos son refringentes. Comenzamos con un pequeño aumento (x 10), para tener una visión panorámica de las escamas y buscar mejor la posible presencia de filamentos. Para confirmarlo, pasamos a un mayor aumento (x 40). 3. Interpretación: Comentaremos los dermatofitos, las levaduras, los mohos y terminaremos describiendo algunos artefactos. Los dermatofitos aparecen de forma diferente según estudiemos las escamas o el pelo. En el ED de las escamas se presentan como filamentos hialinos, de bordes nítidos y regulares, de paredes paralelas, septados (este hecho es muy importante) y con la presencia de ramificaciones, que toman color azul. No tienen relación con los bordes celulares, a los que atraviesan sin orden determinado. A menudo, estas hifas se muestran fragmentadas en artroconidias cuboidales. Este patrón diagnostíca genéricamente a los dermatofitos, pero no podemos precisar la especie (Figs. 15.1,15.2,16.1,16.2). 28
13 EL LABORATORIO en las MICOSIS CUTÁNEAS Fig ED KOH x 100 Fig ED KOH x
14 Atlas de MICOLOGÍA CUTÁNEA Fig ED KOH 30 Fig Examen directo. KOH tinta Parker. X1000
15 EL LABORATORIO en las MICOSIS CUTÁNEAS Si estudiamos el pelo tenemos que precisar que la "utilización" de la queratina de los pelos por los dermatofitos curiosamente varía según sea "in vivo" o "in vitro". "In vivo" presenta dos patrones fundamentales, bien sea el parasitismo interior al pelo (endotrix) o exterior al mismo (ectotrix). Este proceder sí nos permite identificar la especie. El patrón endotrix tiene a su vez dos tipos: Uno, artrosporado, que es el genuino endotrix, que presenta todo el interior del pelo repleto de cadenas de conidios, artrosporados, de 3-4 nm de diámetro (T. tonsurans, T. violaceum). Otro tipo de endotrix es el fávico, dentro del pelo encontramos filamentos dispuestos a lo largo del mismo, ondulados unos, ramificados otros. Son típicas las burbujas de aire (T. schoenleinii) (Fig. 17). Fig. 17. Examen directo de Tinea capitos. Parasitismo endotrix. KOH-tinta. X400 El patrón ectotrix presenta así mismo tres modelos: Uno, tipo en mosaico, en el que las esporas son pequeñas (2-3 nm diámetro), redondas, formando una densa y compacta vaina alrededor del pelo, que no se dispersa con la potasa. En el interior del pelo hay filamentos (M. canis, M. audouinii). Otro, tipo microide, presenta también pequeñas esporas (2-4 nm de diámetro), pero dispuestas de forma irregular en el exterior del pelo, ya que son fácilmente dispersables con la KOH, filamentos en el interior (T. mentagrophytes, T. rubrum, M. gypseum). Y un tercero, tipo megasporado, con esporas de mayor tamaño (4-6 nm), en el exterior del pelo, dispuestas en grumos o racimos y otras sueltas. Filamentos intrapilares (T. verrucosum) (Fig. 18). 31
16 Atlas de MICOLOGÍA CUTÁNEA Fig. 18. Examen directo de Tinea capitis. Parasitismo ectotrix en mosaico. KOH-tinta.X400 TABLA 5: EL PARASITISMO PILOSO DE LOS DERMATOFITOS ENDOTRIX ECTOTRIX Artrosporado Fávica En mosaico Microide Megasporado T. violaceum T. tonsurans T. schoenleinii M. canis M. audouinii T. mentagrophytes M. gypseum T. verrucosum 32 "In vitro" algunos dermatofitos atacan el pelo de una determinada forma, lo que constituye una prueba de diagnóstico diferencial, como es la producción de órganos perforantes, que se utiliza para diferenciar el T. mentagrophytes del T. rubrum, el primero produce órganos perforantes y el segundo no (Fig. 19).
17 Atlas de MICOLOGÍA CUTÁNEA Las levaduras suelen presentarse bajo el aspecto de blastoconidias en gemación y pseudomicelio. Su observación puede plantear mayores dificultades que la de los dermatofitos. En el caso de la pitiriasis versicolor, la imagen es patognomónica, estando constituida por una mezcla de blastosporos singulares provistos de un nítido collarete de gemación y pseudomicelio corto y grueso. Todos estos elementos se tiñen con gran rapidez mediante la tinta Parker azul permanente o el colorante de Swartz-Lamkins (Fig. 20). Fig. 20. Examen directo de queilitis candidiasica. Blastoconidias y pseudomicelio. KOH-tinta X
18 Atlas de MICOLOGÍA CUTÁNEA Las gotas de grasa pueden tomarse por células de levadura, aunque su esfericidad, su distinta tonalidad y su variado tamaño ayudan a distinguirlas. La imagen conocida como hongo en mosaico ( mosaic fungi ) puede resultar muy engañosa, ya que estas estructuras, constituidas por cristales de colesterol y de otras substancias, se parecen mucho a las artroconidias de los dermatofitos, de las que pueden diferenciarse por su disposición a lo largo del borde de las células epidérmicas y por su forma irregular. Finalmente, de modo ocasional, pueden observarse en los exámenes directos macroconidias, que en ningún caso corresponden a dermatofitos, siendo la mayoría de las veces, testimonio de la presencia de un moho contaminante u oportunista. Para terminar, haremos unos breves comentarios: el examen directo es interesante, rápido, aproximativo, pero repetimos, no permite distinguir las diversas especies de dermatofitos. Es fácil cuando es positivo, es difícil cuando es negativo. El examen directo no excluye el cultivo, que es imprescindible para el diagnóstico de las diferentes especies de dermatofitos. SIEMBRA/CULTIVO El Examen Directo puede permitirnos detectar la presencia del agente causal en la muestra patológica, pero nada o casi nada nos dice de la identidad de ese agente, salvo muy limitadas excepciones (Malassezia globosa en la pitiriasis versicolor y Scopulariopsis brevicaulis en ciertas onicomicosis). El diagnóstico definitivo de una micosis requiere un segundo paso: el aislamiento e identificación del hongo responsable de la misma, mediante cultivo. El cultivo se lleva a cabo depositando una cantidad de la muestra patológica en la superficie de uno o varios medios de cultivo, dispuestos en recipientes que pueden ser de dos tipos: tubos y placas. Nosotros preferimos las placas de Petri, de 9-10 cm de diámetro, porque permiten una mejor disposición del inóculo y facilitan la observación y el estudio de las colonias. Tienen la desventaja de ofrecer más riesgo a la contaminación, pero este problema puede limitarse con la adición de ciertos antibióticos y practicando las siembras cuidadosamente (trabajando siempre junto a la llama del mechero) (Figs , 23.1, 23.2, 24.1, 24.2). 36
19 Atlas de MICOLOGÍA CUTÁNEA 40 Las placas o tubos, una vez inoculados, se incuban a temperatura ambiente o, mejor, en estufa a 25ºC. Esta es la temperatura ideal para el desarrollo de la mayoría de los agentes causantes de dermatomicosis, aunque algunos de ellos, como T. verrucosum o las levaduras del género Candida crecen con mayor rapidez a 37ºC. El cultivo de las levaduras lipofílicas del género Malassezia, que requieren temperaturas de 30ºC a 32ºC, no se lleva a cabo de forma rutinaria, por no ser indispensables para el diagnóstico de la pitiriasis versicolor, pero constituye un prometedor campo de investigación en otras dermatosis y es posible que se generalice en el futuro. Cuando la incubación se realiza en estufa, a temperaturas por encima de los 30ºC, o cuando se prolonga más allá de las dos semanas, es aconsejable disponer las placas en bolsas de plástico cerradas, para evitar la desecación del medio. IDENTIFICACIÓN Los cultivos deben examinarse periódicamente a lo largo del tiempo de incubación, y no deben desecharse como negativos hasta transcurridas tres semanas a partir de su siembra. Debe vigilarse la aparición de cualquier tipo de colonia, levaduriforme o filamentosa, teniendo en cuenta que los hongos contaminantes que pudieran estar presentes en el material patológico, o introducirse en el medio al practicar las siembras o durante la incubación, crecen con más rapidez que los patógenos, pudiendo fácilmente cubrirlos o ahogarlos en pocos días, impidiéndonos su aislamiento (Fig. 25). Las colonias sospechosas, una vez detectadas, deben replicarse en medios frescos si se observa contaminación. Una vez se estima alcanzada la madurez de la colonia, se procede a anotar sus características macromorfológicas, esto es su color, textura (granulosa, pulverulenta, anteada, vellosa, algodonosa o glabra), superficie (plana, elevada, plegada, crateriforme) y color del reverso. Con la práctica, el aspecto macroscópico de las colonias a menudo basta para orientar la identificación de la especie, al menos en los hongos filamentosos, de modo similar a lo que ocurre con las plantas. Esta observación debe completarse siempre con el estudio de los caracteres micromorfológicos, lo que llevaremos a cabo tomando una muestra de la superficie de la colonia por medio de un papel adhesivo transparente. Éste, se coloca acto seguido sobre un portaobjeto en el que previamente habremos depositado una gota de la solución colorante, habitualmente azul de lactofenol. La observación se realiza al microscopio, generalmente, con aumentos bajos (de x 100 a x 400) y debe centrarse en la morfología de las estructuras reproductoras, en especial, los distintos tipos de conidias. En aquellos casos en que la micromorfología no permita alcanzar una identificación definitiva de la especie aislada, se recurre a ciertas técnicas auxiliares (tests fisiológicos o bioquímicos) que se detallan en los capítulos correspondientes. Esto reza sobre todo para las levaduras, cuya morfología es mucho más pobre que la de los hongos filamentosos.
20 Atlas de MICOLOGÍA CUTÁNEA Examen macroscópico En primer lugar observaremos si la colonia tiene aspecto levaduriforme (como gota de queso fundido) (Fig. 25 A) o filamentoso (vulgarmente moho). En el segundo supuesto anotar si el crecimiento es muy rápido (mohos) (Fig. 25 C) o lento (dermatofitos) (Fig. 25 B). En general, para los dermatofitos, es solo orientativo, pero con experiencia podremos sospechar las especies mas frecuentes en nuestro medio: E. floccosum, M. canis, M. gypseum, T. mentagrophytes, T. rubrum, T. violaceum, T. verrucosum... Realizamos la observación con el siguiente orden: 1. Color: Tanto del anverso (micelio aéreo): blanco, crema, amarillo, anaranjado, rojo, violeta...; como del reverso (micelio vegetativo): amarillento casi siempre, puede ser rojo, marrón, violeta o sin color. 2. Superficie: Pulverulenta, vellosa, aterciopelada, algodonosa Relieve: Plano, crateriforme, elevado cupuliforme, radiado Borde: Neto, con vellosidades Velocidad de crecimiento: Similar para casi todos (+/- 10 mm/semana), lento (1 mm/semana): T. verrucosum, T. violaceum. 42
21 EL LABORATORIO en las MICOSIS CUTÁNEAS Debemos tener en cuenta que los caracteres morfológicos de los dermatofitos varían según las condiciones del cultivo, tipo de medios, temperatura y en especial para el color, la luz que reciba la colonia. Por esto, la experiencia personal para las cepas del propio laboratorio es tan valiosa. Algunos medios naturales (harina de maíz, patata, etc.) estimulan la producción de pigmentos y otros medios artificiales como el DTM, específico para los dermatofitos, colorean el medio. Examen microscópico Se lleva a cabo de una manera sencilla obteniendo un fragmento del cultivo, con espátula o con un trozo de cinta adhesiva, de la zona central de la colonia y montándolo entre porta y cubre, con unas gotas de azul de lactofenol, permite observar al microscopio óptico (x 100, x 400) los caracteres microscópicos del micelio fúngico. 1. Micelio tabicado, hifas septadas, ramificadas, formando una maraña. Observamos la periferia de la misma para encontrar conidias (macro y microconidias) o bien algunas estructuras morfológicamante interesantes para el diagnóstico micológico. 2. Conidias: Microconidias, son unicelulares, pequeñas, redondas, ovales o piriformes. Presentan dos tipos de disposición: a lo largo de la hifa (tipo acladium) en forma de racimos (cruz de Lorena). Unas veces son sesiles, otras nacen sobre cortos esterigmas. Las macroconidias, son multicelulares, grandes, con tabiques transversales. Existen diversos tipos: fusiformes, en raquetas y en lápiz o maza. A su vez pueden tener las paredes gruesas o finas, ser lisas o rugosas, aisladas o en racimos. 3. Estructuras morfológicas especiales: Casi todas variantes de tamaño y forma de las hifas septadas: Espirales: hifa fina enrollada en espiral. Hifa en raqueta: ensanchamiento oval de una porción media o terminal de una hifa. Cuerpos nodulares: filamentos engrosados formando nudos sobre si mismo. Candelabro fávico: división terminal de una hifa en dos o tres puntas engrosadas. Hifa peptinada: pequeñas prolongaciones en un solo lado de la hifa, que adopta así forma de peine. Hifa retrógrada: hifa que nace en sentido contrario, en ángulo agudo, al resto de las ramificaciones. 43
22 ESTRATEGIA DE LABORATORIO EL LABORATORIO en las MICOSIS CUTÁNEAS Recordemos que la estrategia consiste en dividir el desarrollo del aprendizaje en tres niveles. El primer nivel va destinado a todos los dermatólogos, aunque no tengan conocimientos de laboratorio ni de micología. El segundo nivel, está dirigido a aquellos dermatólogos que poseen algunos medios, conocimientos y el interés científico de investigar los hongos. El tercer nivel, va destinado a aquellos investigadores que trabajan con los hongos como protagonistas. TABLA 6: ESTRATEGIA EN PITIRIASIS VERSICOLOR PRIMER NIVEL Examen con luz de Wood SEGUNDO NIVEL Examen directo con cinta adhesiva TERCER NIVEL Identificación especies Malassezia ESTRATEGIA DE LABORATORIO DE LA PITIRIASIS VERSICOLOR PRIMER NIVEL Objetivo: Confirmar el diagnóstico clínico de pitiriasis versicolor. Método: Aplicación de luz de Wood. Observamos una fluorescencia amarilla, verde amarillenta. Aconsejamos oscuridad absoluta en la habitación de exploración, cerciorándose de que no existe tratamiento previo de la lesión con cremas o ungüentos porque imposibilitan la fluorescencia. Podemos observar lesiones no perceptibles a simple vista. Lo único que necesitamos es una lámpara de Wood, de fácil adquisición en la actualidad. Este proceder, aunque no sea propiamente de laboratorio, lo incluimos por su simplicidad y para complementar el signo clínico de la uñada de Besnier. Es útil tanto para confirmar el diagnóstico como para valorar la eficacia del tratamiento (Figs. 26.1, 26.2). 45
23 Atlas de MICOLOGÍA CUTÁNEA Fig Pitiriasis 1º nivel luz de Wood 46 Fig Pitiriasis 1º nivel luz de Wood 2
24 EL LABORATORIO en las MICOSIS CUTÁNEAS SEGUNDO NIVEL Objetivo: Demostrar la presencia de Malassezia en unas lesiones clínicas sospechosas de pitiriasis versicolor. Método: Examen directo de las escamas cutáneas obtenidas con cinta adhesiva. Presionamos con un fragmento de cinta adhesiva sobre una lesión típica, lo separamos de la piel y lo pegamos sobre un portaobjeto. Depositamos una gota de KOH al 20-30% (con tinta azul Parker o bien la solución de Swartz-Lamkins) en un cubreobjeto y observamos al microscopio. Encontraremos racimos de células levaduriformes, redondeadas, de 4-8 micras, con gemaciones y junto a estos racimos, podemos hallar filamentos cortos, tabicados e incluso ramificados. Esta imagen es patognomónica. Sólo necesitamos cinta adhesiva, un portaobjeto y cubreobjetos, una gota de potasa y un sencillo microscopio (Figs. 27,28). Fig. 27. Pitiriasis 2º nivel ED X400 Fig. 28. Pitiriasis 2º nivel ED X
25 Atlas de MICOLOGÍA CUTÁNEA ESTRATEGIA DE LABORATORIO DE LAS TIÑAS O DERMATOFICIAS TABLA 7: ESTRATEGIA EN LAS TIÑAS PRIMER NIVEL Cultivo en medio DTM/DTA SEGUNDO NIVEL Identificación genérica de dermatofitos TERCER NIVEL Identificación de las especies de dermatofitos frecuentes PRIMER NIVEL Objetivo: Demostrar si en una lesión dermatológica sospechosa, existen o no dermatofitos, con una finalidad epidemiológica y fundamentalmente, terapéutica. Método: Siembra en medio DTM/DTA. Ya se ha comentado la toma de muestras para las tiñas, repasemos ahora la siembra: el material que hemos obtenido, (escamas, pelos, fragmentos de uñas) lo depositamos, con la ayuda de un asa de platino estéril, en la superficie del medio (tanto en tubo, como en placas de Petri) en varios puntos. La siembra en este primer nivel la realizamos en medio DTM o DTA y, a la semana, el medio (que es de color amarillo miel) cambia el color a rojizo, sólo y exclusivamente si el hongo que crece es un dermatofito. Sin embargo, el medio no cambia de color si el hongo que crece no es un dermatofito. No necesitamos microscopio, sólo como indicamos en la siembra: un mechero de alcohol, un asa de platino y un tubo/placa con el medio DTM o DTA (Fig. 31). 50
26 EL LABORATORIO en las MICOSIS CUTÁNEAS Fig. 31.Tiñas 1º nivel cultivo en DTM SEGUNDO NIVEL Objetivo: Identificación genérica y rápida de dermatofitos. Método: La realizamos mediante el examen directo y el parasitismo piloso. Incluimos en este nivel el Examen Directo, y no lo hicimos en el primer nivel porque necesita microscopio y, además, porque, después de muchos años realizándolo, seguimos pensando que representa cierta dificultad y precisa cierto aprendizaje y "oficio" de laboratorio. Con el examen directo incluimos el estudio del parasitismo piloso. Ambos representan algo muy interesante y rápido en el diagnóstico de los dermatofitos como origen fúngico de una dermatosis. Examen directo (ED) Recordamos y resumimos que los dermatofitos aparecen de forma diferente según estudiemos las escamas o el pelo. En el ED de las escamas se presentan como filamentos hialinos, de bordes nítidos y regulares, de paredes paralelas, tabicados (este hecho es muy importante) y con la presencia de ramificaciones, que toman color azul. No tienen relación con los bordes celulares, a los que atraviesan sin orden determinado. Este patrón diagnostíca genéricamente a los dermatofitos, pero no podemos precisar la especie (Fig. 15.1, 15.2, 16.1). 51
27 EL LABORATORIO en las MICOSIS CUTÁNEAS Fig. 32. E. floccosum colonia Fig. 33. E. floccosum micro 55
28 Atlas de MICOLOGÍA CUTÁNEA Punta fina: M. canis (Figs. 34, 35). Presentan macroconidias grandes, de gruesas paredes, fusiformes, espinulosas, con sus extremos puntiagudos, en ocasiones el distal en forma curva. Normalmente, son muy numerosas. Tienen escasas microconidias, a veces abundantes. Las colonias son de color amarillo anaranjado, más acentuado en la periferia, de aspecto plumoso. Es un hongo zoofílico. Fig. 34. M. canis colonia 56 Fig. 35. M. canis micro
29 EL LABORATORIO en las MICOSIS CUTÁNEAS Punta redondeada: M. gypseum (Figs. 36, 37). Presenta conidias grandes, gruesas paredes, espinuladas, muy parecidas hasta aquí a las del M. canis, pero las puntas son redondeadas, menos agudas; asimismo, son menos numerosas. Puede haber microconidias en racimos. La colonia es muy típica, granulosa, de color canela, que la diferencia a simple vista de la de M. canis. M. gypseum es un dermatofito geofílico. Fig. 36. M. gypseum colonia Fig. 37. M. gypseum micro 57
30 EL LABORATORIO en las MICOSIS CUTÁNEAS Fig. 39. T. mentagrophytes micro La presencia de hifas espirales es casi exclusiva de esta especie. Si lo unimos a los caracteres de la colonia: blanco ocre, pulverulento para la variedad mentagrophytes (zoofílico) y blanco algodonoso para la variedad interdigitale (antropofílico), y a la presencia de numerosas microconidias, redondeadas dispuestas en racimos, no tendremos dudas en el diagnóstico. En caso de duda sembramos en medio Agar-Urea, en el que T. mentagrophytes cambia el color del medio (vira a rosa intenso/rojizo), mientras que T. rubrum no. Otra prueba diferencial sería la formación de órganos perforantes, que es positivo para T. mentagrophytes y negativa para T. rubrum. Si no existen hifas espirales: Siembra en medio potato dextrosa agar (PDA): - Positivo (Colonia roja): T. rubrum (Figs. 40, 41). 59
31 Atlas de MICOLOGÍA CUTÁNEA Fig. 40. T. rubrum. Colonia: izquierda en MGS, derecha en PDA 60 Fig. 41. T. rubrum micro
32 EL LABORATORIO en las MICOSIS CUTÁNEAS Las colonias de T. rubrum presentan en este medio una coloración rojiza, vinosa, especialmente en el reverso. Sus típicas microconidias en lágrimas, están dispersas o dispuestas a ambos lados de las hifas (según el tipo "acladium"). Hay escasas macroconidias en forma de lápiz, finas, lisas y multiseptadas, muy semejantes a las que produce T. mentagrophytes. Repasamos los caracteres diferenciales de T. rubrum, que en cierto modo ya han aparecido: No hay formas espirales. Ureasa negativo. Formación de órganos perforantes negativa y especialmente positiva en medio potato dextrosa agar (PDA), con colonias de intenso y notorio color rojo-vino, especialmente en el anverso. Es un dermatofito antropofílico, con preferencia por la invasión de las uñas. - Negativo (colonia blanca): T. tonsurans (Figs. 42, 43). Fig. 42. T. tonsurans colonia Fig. 43. T. tonsurans. Microconidias. X400 61
33 Atlas de MICOLOGÍA CUTÁNEA Visto así, el diagnóstico det. tonsurans es por exclusión y con dificultades. Nos ayuda en su diagnóstico el hecho de conocer que la toma micológica procede de una tiña de la cabeza, de tipo puntos negros. No presenta hifas espirales. Las colonias son blancas en medio PDA y forman microconidias redondeadas, que nacen con una base aplanada, muchas veces en forma de clavo. También, es típica la presencia de clamidosporos terminales e intercalares. Es un hongo antropofílico y en la actualidad en España, apenas se aísla. De todas formas, dadas estas dificultades, es necesario en ocasiones recurrir al crecimiento en medios agar-trichophyton, especialmente los números 1, 2, 3 y 4, donde crece abundantemente en los nº 3 y 4, pero no en los dos primeros (no tienen tiamina), mientras que T. mentagrophytes y T. rubrum crecen bien en los cuatro medios. SI NO EXISTEN NI MACRO NI MICROCONIDIAS Tres especies pertenecientes al género Trichophyton, todas de crecimiento lento, no producen conidias normalmente, sólo observamos hifas y algunos elementos que describimos a continuación. Colonia violácea: T. violaceum (Figs. 44, 45). Presenta colonias de crecimiento muy lento, pequeñas, de consistencia cérea, con un color violeta oscuro (vino tinto), aterciopeladas, en el reverso se ve muy bien su coloración. El crecimiento mejora en medios con tiamina (Agar trichophyton nº 3 y 4). No produce conidias. Sólo se observa una maraña de hifas de color violeta, con algunos engrosamientos intercalados, a veces en cadenas. Es un dermatofito antropofílico. Hifas toruloides: T. verrucosum (Figs. 46, 47). Lo que primero llama la atención es el lento crecimiento de la colonia (30 días), crecimiento que mejora si se incuba a 37ºC y en medios con tiamina (Agar trichophyton 3 y 4). También ciertos caracteres microscópico de la colonia: como ser crateriforme, de color ocre-amarillento a grisáceo, superficie lisa y plegada, y suele penetrar en el agar. Microscópicamente sólo aparecen hifas, no conidias. En las hifas se intercalan cadenas de clamidosporos, de diferentes tamaños, dando lugar a las típicas hifas toruloides. Es un hongo zoofílico. 62
34 EL LABORATORIO en las MICOSIS CUTÁNEAS Fig. 44. T. violaceum colonia Fig. 45. T. violaceum micro 63
35 Atlas de MICOLOGÍA CUTÁNEA Fig. 46. T. verrucosum colonia 64 Fig. 47. T. verrucosum micro
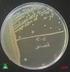
36 EL LABORATORIO en las MICOSIS CUTÁNEAS ESTRATEGIA EN EL LABORATORIO DE LAS CANDIDOSIS TABLA 10: ESTRATEGIA EN LAS CANDIDOSIS PRIMER NIVEL Diagnóstico del género Candida SEGUNDO NIVEL Diagnósitico de la especie C. albicans TERCER NIVEL Diagnóstico de todas las especies de género Candida PRIMER NIVEL Objetivo: Diagnóstico del género Candida. Demostrar si en una afectación cutánea, mucosa o ungueal, si existen o no levaduras pertenecientes al género Candida, con finalidad terapéutica. Método: Siembra en medio glucosado de Sabouraud (MGS). Recordamos las precauciones que deben tenerse en cuenta al realizar la toma micológica. Se efectúa con hisopo (torunda) bacteriológico estéril en lesiones mucosas y lesiones cutáneas húmedas, y en piel y uñas, como indicamos en el capítulo de toma micológica. Hay que prestar atención a la escasa supervivencia de las candidas en la muestra por lo que es aconsejable la siembra inmediata. La siembra la realizamos en medio glucosado de Sabouraud (MGS) con cloramfenicol, mediante el hisopo que utilizamos en la toma o con un asa de platino. Incubamos a temperatura ambiente y a las 48 horas obtenemos unas colonias blancas o blanco-marfil, cremosas, brillantes, como gotas de queso fundido. Son colonias tan típicas, que son diagnósticas por si mismas. Lo único que necesitamos es un hisopo estéril, un mechero de alcohol y un tubo o placa con medio glucosado de Sabouraud. En horas podemos hacer el diagnóstico con una simple visualización del tubo o placa (Fig. 48). SEGUNDO NIVEL Objetivo: Identificación de la especie C. albicans, imputada como causa de la mayoría de las candidosis. Método: Partimos de la colonia que nos ha crecido en el primer nivel, sobre medio de Sabouraud y realizamos una resiembra en un medio específico. 65
37 Atlas de MICOLOGÍA CUTÁNEA Fig. 48 Candida, primer nivel, colonia blanca en MGS Para simplificar esta identificación se han propuesto numerosos medios, que tienen en común una rápida identificación de C. albicans, basándose en el aspecto macroscópico y color que adquieren sus colonias. Usamos el medio ChromAgar Candida, en el que la colonia de C. albicans se tiñe de color verdoso, facilitando el diagnóstico rápido y fácil. Sólo necesitamos un asa de platino, un mechero de alcohol y una placa de medio CROMAgar candida (Fig. 49). 66 Fig. 49 Candida, segundo nivel, colonia verde a la izquierda (C. albicans) en medio ChromAgar
38 PATRONES DE DIAGNÓSTICO DE LOS HONGOS MÁS FRECUENTES: DERMATOFITOS (FIGS ) EL LABORATORIO en las MICOSIS CUTÁNEAS Fig. 54. E. floccosum. SGA. 2 semanas Fig. 55. E. floccosum. Macroconidias. ALFX
39 Atlas de MICOLOGÍA CUTÁNEA Fig. 56. M. canis. SGA. Colonias de 2 semanas 72 Fig. 57. M. canis. Macroconidias (detalle). ALF X1000
40 EL LABORATORIO en las MICOSIS CUTÁNEAS Fig. 58. M. gypseum. SGA. Colonias de 10 días Fig. 59. M. gypseum. Macroconidias. ALF X
41 Atlas de MICOLOGÍA CUTÁNEA Fig. 60. T. mentagrophytes var. mentagrophytes. SGA. Colonias de 3 semanas 74 Fig. 61. T. mentagrophytes var. interdigitale. SGA. Colonias de 3 semanas
42 EL LABORATORIO en las MICOSIS CUTÁNEAS Fig. 62. T. mentagrophytes var. mentagrophytes. Macro y microconidias. ALF X400 Fig. 63 T. mentagrophytes var. mentagrophytes. Microconidias y espirales. ALF X400 75
43 Atlas de MICOLOGÍA CUTÁNEA Fig. 64. T. rubrum. SGA. Colonias de 3 semanas 76 Fig. 65. T. rubrum. PDA. Colonias de 3 semanas
44 EL LABORATORIO en las MICOSIS CUTÁNEAS Fig. 66. T. rubrum. Microconidias. ALF X400 Fig. 67. T. rubrum var raubistchekii. Macro y microconidias. ALF X
45 Atlas de MICOLOGÍA CUTÁNEA Fig. 68. T. tonsurans var sulphureum. SGA. 3 semanas 78 Fig. 69.T. tonsurans. Microconidias. ALF X40
46 EL LABORATORIO en las MICOSIS CUTÁNEAS Fig. 70 T. violaceum. SGA. 3 semanas Fig. 71. T. violaceum. ALF X
47 Atlas de MICOLOGÍA CUTÁNEA Fig. 72. T. verrucosum. SGA. 3 semanas 80 Fig. 73. T. verrucosum. Hifas toruloides. ALF X1000
48 EL LABORATORIO en las MICOSIS CUTÁNEAS LEVADURAS (FIGS ) Fig. 74. Candida albicans. SGA Fig. 75. Candida albicans. Clamidosporos. CMA X200 81
49 Atlas de MICOLOGÍA CUTÁNEA Fig. 76. Candida parapsilosis. SGA 82 Fig. 77. Candida parapsilosis. CMA X100
50 EL LABORATORIO en las MICOSIS CUTÁNEAS Fig. 78. Malassezia globosa. mdixon Fig. 79. Malassezia globosa en cultivo. ALF X
51 Atlas de MICOLOGÍA CUTÁNEA MOHOS (FIGS ) Fig. 80. Scopulariopsis brevicaulis. SGA 84 Fig. 81. S. brevicaulis. ALF X1000
52 EL LABORATORIO en las MICOSIS CUTÁNEAS Fig. 82. Alternaria alternata. SGA Fig. 83. Alternaria alternata. Dyctiosporos. ALF X
53 EL LABORATORIO en las MICOSIS CUTÁNEAS Fig. 86. A. flavus. SGA Fig. 87. A. flavus-oryzae. ALF X
54 Atlas de MICOLOGÍA CUTÁNEA Fig. 88 A. terreus. SGA 88 Fig. 89. A. terreus. ALF X1000
55 EL LABORATORIO en las MICOSIS CUTÁNEAS Fig. 90. Fusarium sp. SGA Fig. 91. Fusarium sp. Macro y microconidias. ALF X
MÓDULO III DERMATOFITOSIS
 MAESTRÍA EN MICOLOGÍA MÉDICA Universidad Nacional del Nordeste COHORTE 2012-2013 MÓDULO III DERMATOFITOSIS MAESTRÍA EN MICOLOGÍA MÉDICA Universidad Nacional del Nordeste COHORTE 2012-2013 GÉNERO EPIDERMOPHYTON
MAESTRÍA EN MICOLOGÍA MÉDICA Universidad Nacional del Nordeste COHORTE 2012-2013 MÓDULO III DERMATOFITOSIS MAESTRÍA EN MICOLOGÍA MÉDICA Universidad Nacional del Nordeste COHORTE 2012-2013 GÉNERO EPIDERMOPHYTON
GUIA DE TRABAJOS PRÁCTICOS MICOLOGÍA
 GUIA DE TRABAJOS PRÁCTICOS MICOLOGÍA Departamento de Microbiología Facultad de Medicina UBA 2009 Guía de Trabajos Prácticos 2009 1 Observación de escamas con micelios y levaduras. Digestión con KOH 40%.
GUIA DE TRABAJOS PRÁCTICOS MICOLOGÍA Departamento de Microbiología Facultad de Medicina UBA 2009 Guía de Trabajos Prácticos 2009 1 Observación de escamas con micelios y levaduras. Digestión con KOH 40%.
Micosis Superficiales I Dermatofitosis
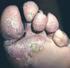 Micosis Superficiales I Dermatofitosis Micosis Superficiales Son aquellas micosis que invaden la capa superficial de piel, mucosas y fáneras (pelo y uñas). Sin atravesar la membrana basal del epitelio.
Micosis Superficiales I Dermatofitosis Micosis Superficiales Son aquellas micosis que invaden la capa superficial de piel, mucosas y fáneras (pelo y uñas). Sin atravesar la membrana basal del epitelio.
GUÍA DE TRABAJOS PRÁCTICOS MICROBIOLOGÍA FARMACIA
 1 GUÍA DE TRABAJOS PRÁCTICOS MICROBIOLOGÍA FARMACIA ÁREA MICOLOGÍA AÑO 2014 2 TRABAJO PRÁCTICO N 1 Tema: - Macromorfología de las colonias fúngicas - Micromorfología del desarrollo fúngico vegetativo -
1 GUÍA DE TRABAJOS PRÁCTICOS MICROBIOLOGÍA FARMACIA ÁREA MICOLOGÍA AÑO 2014 2 TRABAJO PRÁCTICO N 1 Tema: - Macromorfología de las colonias fúngicas - Micromorfología del desarrollo fúngico vegetativo -
Tema IV Micología Médica
 Tema IV Micología Médica Generalidades de Micología Colectivo de autores Microbiología y Parasitología Objetivos 1. Argumentar la importancia de los hongos. 2. Explicar las diferencias elementales entre
Tema IV Micología Médica Generalidades de Micología Colectivo de autores Microbiología y Parasitología Objetivos 1. Argumentar la importancia de los hongos. 2. Explicar las diferencias elementales entre
TEMA 10. DIAGNÓSTICO DE LABORATORIO DE LAS ENFERMEDADES INFECCIOSAS BUCODENTALES
 TEMA 10. DIAGNÓSTICO DE LABORATORIO DE LAS ENFERMEDADES INFECCIOSAS BUCODENTALES 1. Objetivo del diagnóstico microbiológico 2. Toma de muestra 3. Diagnóstico directo - bacterias - hongos - protozoos -
TEMA 10. DIAGNÓSTICO DE LABORATORIO DE LAS ENFERMEDADES INFECCIOSAS BUCODENTALES 1. Objetivo del diagnóstico microbiológico 2. Toma de muestra 3. Diagnóstico directo - bacterias - hongos - protozoos -
TINEA CORPORIS EN PACIENTE INMIGRANTE INFECTADA POR EL VIH. CASO 503
 TINEA CORPORIS EN PACIENTE INMIGRANTE INFECTADA POR EL VIH. CASO 503 Mujer de 29 años nigeriana, de raza negra, que regresa a España, donde ha residido los últimos 5 años, después de una estancia de 4
TINEA CORPORIS EN PACIENTE INMIGRANTE INFECTADA POR EL VIH. CASO 503 Mujer de 29 años nigeriana, de raza negra, que regresa a España, donde ha residido los últimos 5 años, después de una estancia de 4
Tema 42 Hongos productores de micosis superficiales, subcutáneas y sistémicas
 Tema 42 Hongos productores de micosis superficiales, subcutáneas y sistémicas Miguel Ángel Bratos Pérez Micosis superficiales: etiología, cuadros clínicos, diagnóstico Micosis cutáneas: etiología, cuadros
Tema 42 Hongos productores de micosis superficiales, subcutáneas y sistémicas Miguel Ángel Bratos Pérez Micosis superficiales: etiología, cuadros clínicos, diagnóstico Micosis cutáneas: etiología, cuadros
TINEA BARBAE PROFUNDA POR TRICHOPHYTON MENTAGROPHYTES. CASO 359
 TINEA BARBAE PROFUNDA POR TRICHOPHYTON MENTAGROPHYTES. CASO 359 Hombre de 38 años de edad con insuficiencia renal crónica como consecuencia de nefritis intersticial por uropatía obstructiva congénita,
TINEA BARBAE PROFUNDA POR TRICHOPHYTON MENTAGROPHYTES. CASO 359 Hombre de 38 años de edad con insuficiencia renal crónica como consecuencia de nefritis intersticial por uropatía obstructiva congénita,
Easy PDF Creator is professional software to create PDF. If you wish to remove this line, buy it now.
 1 Unidad Curricular: Virología y Micología Veterinaria TRABAJO PRÁCTICO No. 6 MICOLOGÍA OBJETIVO 1. Estudiar las características morfológicas de los hongos y su crecimiento en los medios de cultivo. GENERALIDADES
1 Unidad Curricular: Virología y Micología Veterinaria TRABAJO PRÁCTICO No. 6 MICOLOGÍA OBJETIVO 1. Estudiar las características morfológicas de los hongos y su crecimiento en los medios de cultivo. GENERALIDADES
Microscopio y observación de células
 I.E.S. Rayuela - Departamento de Biología y Geología Práctica nº1 de Anatomía Aplicada Microscopio y observación de células Las células suelen ser de tamaño muy pequeño de modo que permanecen invisibles
I.E.S. Rayuela - Departamento de Biología y Geología Práctica nº1 de Anatomía Aplicada Microscopio y observación de células Las células suelen ser de tamaño muy pequeño de modo que permanecen invisibles
ONICOMICOSIS AA/CAI. Estamos en la tierra de nadie Charly García
 ONICOMICOSIS Estamos en la tierra de nadie Charly García Dra. Alicia Arechavala Jefa de la Unidad Micología Hospital Muñiz Prof. Dra. Cristina Iovannitti Centro de Micología Facultad Medicina UBA Hoja
ONICOMICOSIS Estamos en la tierra de nadie Charly García Dra. Alicia Arechavala Jefa de la Unidad Micología Hospital Muñiz Prof. Dra. Cristina Iovannitti Centro de Micología Facultad Medicina UBA Hoja
Generalidades de Micosis superficiales. Jorge Luis Finquelievich Centro de Micología Departamento de Microbiología. Facultad de Medicina.
 Generalidades de Micosis superficiales Jorge Luis Finquelievich Centro de Micología Departamento de Microbiología. Facultad de Medicina. UBA MICOSIS SUPERFICIALES Son las infecciones fúngicas de la piel,
Generalidades de Micosis superficiales Jorge Luis Finquelievich Centro de Micología Departamento de Microbiología. Facultad de Medicina. UBA MICOSIS SUPERFICIALES Son las infecciones fúngicas de la piel,
GUÍA DE LABORATORIO Nº 1 MEDIOS DE CULTIVO. OBJETIVO Comprender la utilidad de los medios de cultivo en el trabajo microbiológico.
 GUÍA DE LABORATORIO Nº 1 MEDIOS DE CULTIVO OBJETIVO Comprender la utilidad de los medios de cultivo en el trabajo microbiológico. MATERIALES Placas de agar sangre y agar McConkey. Tubos con agar TSI, agar
GUÍA DE LABORATORIO Nº 1 MEDIOS DE CULTIVO OBJETIVO Comprender la utilidad de los medios de cultivo en el trabajo microbiológico. MATERIALES Placas de agar sangre y agar McConkey. Tubos con agar TSI, agar
PRACTICA Núm. 12 AISLAMIENTO DE 2 MICROORGANISMOS Y OBTENCION DE UN CULTIVO AXENICO
 PRACTICA Núm. 12 AISLAMIENTO DE 2 MICROORGANISMOS Y OBTENCION DE UN CULTIVO AXENICO I. OBJETIVO Aislar dos microorganismos por la técnica de siembra de dilución por estría en placa de agar y obtener un
PRACTICA Núm. 12 AISLAMIENTO DE 2 MICROORGANISMOS Y OBTENCION DE UN CULTIVO AXENICO I. OBJETIVO Aislar dos microorganismos por la técnica de siembra de dilución por estría en placa de agar y obtener un
MANUAL DE OPERACIONES. DIRECCIÓN DE INVESTIGACIÓN Fecha: JUN 15 SUBDIRECCIÓN DE INVESTIGACIÓN BIOMÉDICA MANUAL DE TINCIONES
 A Hoja: de 0 MANUAL DE TINCIONES Elaboró: Autorizó: Puesto QUÍMICO JEFE DE LABORATORIO Firma Hoja: 2 de 0. Propósito Establecer las técnicas y condiciones para la realización de tinciones utilizadas en
A Hoja: de 0 MANUAL DE TINCIONES Elaboró: Autorizó: Puesto QUÍMICO JEFE DE LABORATORIO Firma Hoja: 2 de 0. Propósito Establecer las técnicas y condiciones para la realización de tinciones utilizadas en
2. Observación de hongos de interés industrial
 2. Observación de hongos de interés industrial En esta práctica se realizarán observaciones en fresco de varios hongos de interés industrial. 2.1 Preparaciones para el estudio microscópico de los aislados
2. Observación de hongos de interés industrial En esta práctica se realizarán observaciones en fresco de varios hongos de interés industrial. 2.1 Preparaciones para el estudio microscópico de los aislados
Trichophyton tonsurans
 Trichophyton tonsurans Araceli Monzón y Juan Luis Rodríguez Tudela. Unidad de Micología. Centro Nacional de Microbiología, Instituto de Salud Carlos III. Majadahonda, Madrid El género Trichophyton, al
Trichophyton tonsurans Araceli Monzón y Juan Luis Rodríguez Tudela. Unidad de Micología. Centro Nacional de Microbiología, Instituto de Salud Carlos III. Majadahonda, Madrid El género Trichophyton, al
PRÁCTICA 2. PREPARACIONES MICROSCOPICAS 1. CÉLULA EUCARIOTA VEGETAL: EPIDERMIS DE CEBOLLA.
 AMPLIACIÓN BIOLOGÍA 4º ESO Taller Biología 4º E.S.O. BLOQUE 2. MICROSCOPÍA Y CITOLOGÍA PRÁCTICA 2. PREPARACIONES MICROSCOPICAS 1. CÉLULA EUCARIOTA VEGETAL: EPIDERMIS DE CEBOLLA. OBJETIVOS o Adquirir práctica
AMPLIACIÓN BIOLOGÍA 4º ESO Taller Biología 4º E.S.O. BLOQUE 2. MICROSCOPÍA Y CITOLOGÍA PRÁCTICA 2. PREPARACIONES MICROSCOPICAS 1. CÉLULA EUCARIOTA VEGETAL: EPIDERMIS DE CEBOLLA. OBJETIVOS o Adquirir práctica
PRÁCTICA No. 4 Métodos de cultivo y descripción morfológica de hongos Introducción
 PRÁCTICA No. 4 Métodos de cultivo y descripción morfológica de hongos Objetivos. Que el alumno aprenda las técnicas de cultivo y manipulación de diferentes tipos de hongos. Que el estudiante conozca las
PRÁCTICA No. 4 Métodos de cultivo y descripción morfológica de hongos Objetivos. Que el alumno aprenda las técnicas de cultivo y manipulación de diferentes tipos de hongos. Que el estudiante conozca las
GENERALIDADES DE HONGOS. Micología 1
 GENERALIDADES DE HONGOS Micología 1 CARACTERÍSTICAS DE LOS HONGOS DE IMPORTANCIA MÉDICA Reino Fungi Organismos eucariotas Se nutren por absorción-heterótrofos Aerobios Desarrollo a 28ºC; 37ºC Pared celular
GENERALIDADES DE HONGOS Micología 1 CARACTERÍSTICAS DE LOS HONGOS DE IMPORTANCIA MÉDICA Reino Fungi Organismos eucariotas Se nutren por absorción-heterótrofos Aerobios Desarrollo a 28ºC; 37ºC Pared celular
22.- Introducción a la Micología
 22.- Introducción a la Micología Introducción a la Micología Los hongos son organismos eucarióticos, no fotosintéticos (quimioorganotropos). Son abundantes en la naturaleza, en los suelos, cuerpos de agua,
22.- Introducción a la Micología Introducción a la Micología Los hongos son organismos eucarióticos, no fotosintéticos (quimioorganotropos). Son abundantes en la naturaleza, en los suelos, cuerpos de agua,
PRACTICA Núm. 6 TINCION DE FLAGELOS BACTERIANOS POR EL METODO DE LEIFSON
 PRACTICA Núm. 6 TINCION DE FLAGELOS BACTERIANOS POR EL METODO DE LEIFSON I. OBJETIVO Demostrar la presencia de flagelos mediante tinción y observar la movilidad que presentan algunas bacterias diferenciándola
PRACTICA Núm. 6 TINCION DE FLAGELOS BACTERIANOS POR EL METODO DE LEIFSON I. OBJETIVO Demostrar la presencia de flagelos mediante tinción y observar la movilidad que presentan algunas bacterias diferenciándola
Carrera de Microbiología Clínica Módulo Micología Clínica Año Guía de trabajos prácticos
 Carrera de Microbiología Clínica Año 2013 Guía de trabajos prácticos Carrera de Microbiología Clínica DIRECTORES Dra. Liliana Guelfand Dr. Rolando Soloaga GUÍA DE TRABAJOS PRÁCTICOS 2013 DOCENTES Claudia
Carrera de Microbiología Clínica Año 2013 Guía de trabajos prácticos Carrera de Microbiología Clínica DIRECTORES Dra. Liliana Guelfand Dr. Rolando Soloaga GUÍA DE TRABAJOS PRÁCTICOS 2013 DOCENTES Claudia
PROPOSICIÓN DE UN CICLO EN EL QUE SE ESTABLECEN RELACIONES ENTRE LAS DISTINTAS FORMAS DE PULLULAR1A PULLULANS
 Anal. Inst. Bot. Cavanilles 31 (2): 149-153 (1974) PROPOSICIÓN DE UN CICLO EN EL QUE SE ESTABLECEN RELACIONES ENTRE LAS DISTINTAS FORMAS DE PULLULAR1A PULLULANS por S. RAMOS e I. GARCÍA ACHA Pullularia
Anal. Inst. Bot. Cavanilles 31 (2): 149-153 (1974) PROPOSICIÓN DE UN CICLO EN EL QUE SE ESTABLECEN RELACIONES ENTRE LAS DISTINTAS FORMAS DE PULLULAR1A PULLULANS por S. RAMOS e I. GARCÍA ACHA Pullularia
Micosis superficiales y oportunistas
 Universidad Nacional de Rosario - Facultad de Ciencias Médicas Micosis superficiales y oportunistas Área Injuria - 2015 HONGOS RECORDEMOS Eucariotas Inmóviles Pared celular con quitina Membrana citoplasmática
Universidad Nacional de Rosario - Facultad de Ciencias Médicas Micosis superficiales y oportunistas Área Injuria - 2015 HONGOS RECORDEMOS Eucariotas Inmóviles Pared celular con quitina Membrana citoplasmática
LEVADURAS DE INTERÉS MÉDICO PRUEBAS DE IDENTIFICACIÓN
 LEVADURAS DE INTERÉS MÉDICO PRUEBAS DE IDENTIFICACIÓN Levaduras de Importancia Médica Levaduras del género Candida Levaduras del género Cryptococcus Levaduras del género Malassezia Levaduras del género
LEVADURAS DE INTERÉS MÉDICO PRUEBAS DE IDENTIFICACIÓN Levaduras de Importancia Médica Levaduras del género Candida Levaduras del género Cryptococcus Levaduras del género Malassezia Levaduras del género
1ª PRÁCTICA DE MICROBIOLOGÍA:
 1ª PRÁCTICA DE MICROBIOLOGÍA: INTRODUCCIÓN A LAS TÉCNICAS DE CULTIVO EN MICROBIOLOGÍA (O COMO HACER VISIBLES ORGANISMOS INVISIBLES) INTRODUCCIÓN El objetivo de esta práctica es aislar y observar algunos
1ª PRÁCTICA DE MICROBIOLOGÍA: INTRODUCCIÓN A LAS TÉCNICAS DE CULTIVO EN MICROBIOLOGÍA (O COMO HACER VISIBLES ORGANISMOS INVISIBLES) INTRODUCCIÓN El objetivo de esta práctica es aislar y observar algunos
ESTUDIO MICROSCÓPICO DE LAS BACTERIAS DEL YOGUR
 ESTUDIO MICROSCÓPICO DE LAS BACTERIAS DEL YOGUR 1- Prepara un portaobjetos bien limpio con una gota de agua. 2 - Coge una porción pequeña de yogur con un palillo o una aguja enmangada y hacer una extensión
ESTUDIO MICROSCÓPICO DE LAS BACTERIAS DEL YOGUR 1- Prepara un portaobjetos bien limpio con una gota de agua. 2 - Coge una porción pequeña de yogur con un palillo o una aguja enmangada y hacer una extensión
Identificación de hongos dermatofitos 12-1
 Identificación de hongos dermatofitos 12-1 F. Javier Cabañes Saenz 12.1. Introducción Los dermatofitos son un grupo de hongos relacionados entre sí que presentan la capacidad de invadir los tejidos queratinizados
Identificación de hongos dermatofitos 12-1 F. Javier Cabañes Saenz 12.1. Introducción Los dermatofitos son un grupo de hongos relacionados entre sí que presentan la capacidad de invadir los tejidos queratinizados
FICHAS DE PRÁCTICAS DE BIOLOGÍA 4º ESO BIOLOGÍA
 FICHAS DE PRÁCTICAS DE BIOLOGÍA 4º ESO BIOLOGÍA UNIDAD DIDÁCTICA : CÉLULAS Y TEJIDOS 01.- Células animales y vegetales Duración Estimada: 1h 40 min Capacidad Terminal Observación de células animales y
FICHAS DE PRÁCTICAS DE BIOLOGÍA 4º ESO BIOLOGÍA UNIDAD DIDÁCTICA : CÉLULAS Y TEJIDOS 01.- Células animales y vegetales Duración Estimada: 1h 40 min Capacidad Terminal Observación de células animales y
ONICOMICOSIS POR UNA ESPECIE DE CHAETOMIUM. CASO 566
 ONICOMICOSIS POR UNA ESPECIE DE CHAETOMIUM. CASO 566 Mujer de 41 años de edad, con diabetes no dependiente de insulina, que acude al Servicio de Dermatología por presentar, en el dedo pulgar de la mano
ONICOMICOSIS POR UNA ESPECIE DE CHAETOMIUM. CASO 566 Mujer de 41 años de edad, con diabetes no dependiente de insulina, que acude al Servicio de Dermatología por presentar, en el dedo pulgar de la mano
UNIVERSIDAD DE MAYORES PRÁCTICAS DE MICROBIOLOGÍA DEPARTAMENTO DE BIOMEDICINA Y BIOTECNOLOGÍA MICROBIOLOGÍA I
 UNIVERSIDAD DE MAYORES PRÁCTICAS DE MICROBIOLOGÍA DEPARTAMENTO DE BIOMEDICINA Y BIOTECNOLOGÍA MICROBIOLOGÍA I DRAS. MARÍA LUISA ORTIZ Y ANA PEDREGOSA 1 PRÁCTICAS DE MICROBIOLOGÍA DEPARTAMENTO DE BIOMEDICINA
UNIVERSIDAD DE MAYORES PRÁCTICAS DE MICROBIOLOGÍA DEPARTAMENTO DE BIOMEDICINA Y BIOTECNOLOGÍA MICROBIOLOGÍA I DRAS. MARÍA LUISA ORTIZ Y ANA PEDREGOSA 1 PRÁCTICAS DE MICROBIOLOGÍA DEPARTAMENTO DE BIOMEDICINA
MICOSIS SUPERFICIALES : DIAGNÓSTICO Y TRATAMIENTO
 MICOSIS SUPERFICIALES : DIAGNÓSTICO Y TRATAMIENTO C. Figueras Unidad de Patología Infecciosa e Inmunodeficiencias de Pediatría HUVH. Barcelona REVISADO EN JUNIO 2008 MICOSIS SUPERFICIALES : DIAGNÓSTICO
MICOSIS SUPERFICIALES : DIAGNÓSTICO Y TRATAMIENTO C. Figueras Unidad de Patología Infecciosa e Inmunodeficiencias de Pediatría HUVH. Barcelona REVISADO EN JUNIO 2008 MICOSIS SUPERFICIALES : DIAGNÓSTICO
CONTRIBUCIÓN FOTOGRÁFICA AL ESTUDIO DE MICROHONGOS FILAMENTOSOS DEL PÁRAMO DE GUASCA
 1 CONTRIBUCIÓN FOTOGRÁFICA AL ESTUDIO DE MICROHONGOS FILAMENTOSOS DEL PÁRAMO DE GUASCA Investigador principal: Rubén Darío Torrenegra G. Otros Investigadores: Ludis Samira Rueda Blanco. Grupo de Investigación:
1 CONTRIBUCIÓN FOTOGRÁFICA AL ESTUDIO DE MICROHONGOS FILAMENTOSOS DEL PÁRAMO DE GUASCA Investigador principal: Rubén Darío Torrenegra G. Otros Investigadores: Ludis Samira Rueda Blanco. Grupo de Investigación:
PREPARACIONES Y TINCIONES
 PREPARACIONES Y TINCIONES PREPARACIONES En fresco Temporales: Microcultivos de hongos, preparaciones de tejidos Fijas: Gram, Ziehl Nielsen, Sheaffer y fulton, SEM, TEM, naranja de acridina. CONTRASTE DE
PREPARACIONES Y TINCIONES PREPARACIONES En fresco Temporales: Microcultivos de hongos, preparaciones de tejidos Fijas: Gram, Ziehl Nielsen, Sheaffer y fulton, SEM, TEM, naranja de acridina. CONTRASTE DE
Dermatofitosis. Tiña de la Uña Fernando Gómez Daza, Postgrado de Dermatología, Universidad de Carabobo, Sep. 2008
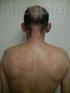 Dermatofitosis. Tiña de la Uña Fernando Gómez Daza, Postgrado de Dermatología, Universidad de Carabobo, Sep. 2008 Esta dermatomicosis se define como toda infección dermatofítica en las uñas de las manos
Dermatofitosis. Tiña de la Uña Fernando Gómez Daza, Postgrado de Dermatología, Universidad de Carabobo, Sep. 2008 Esta dermatomicosis se define como toda infección dermatofítica en las uñas de las manos
en dermatología Guía de recogida de muestras 1 Raspados superficiales y profundos 4 Cultivo microbiológico v24
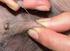 v24 Guía de recogida de muestras en dermatología Citología, tricograma, raspados, cultivos, etc. Seguro que has oído hablar de todas estas técnicas. Pero, sabes cómo tomar la muestra para llevarlas a cabo
v24 Guía de recogida de muestras en dermatología Citología, tricograma, raspados, cultivos, etc. Seguro que has oído hablar de todas estas técnicas. Pero, sabes cómo tomar la muestra para llevarlas a cabo
Tabla 5. Otras afecciones dermatológicas susceptibles de ser confundidas con DA
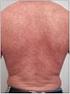 El picor, su condición de enfermedad crónica recurrente con evolución a brotes, así como la morfología y distribución de las lesiones, facilitan notablemente el diagnóstico. Existen, sin embargo, cuadros
El picor, su condición de enfermedad crónica recurrente con evolución a brotes, así como la morfología y distribución de las lesiones, facilitan notablemente el diagnóstico. Existen, sin embargo, cuadros
INTRODUCCIÓN AL ESTUDIO DE HONGOS
 UNIVERSIDAD AUTÓNOMA DE NUEVO LEÓN FACULTAD DE CIENCIAS QUÍMICAS INTRODUCCIÓN AL ESTUDIO DE HONGOS M.C. Francisco Javier Gómez Vega Mayo del 2005 H O N G O S No existe un acuerdo general sobre los límites
UNIVERSIDAD AUTÓNOMA DE NUEVO LEÓN FACULTAD DE CIENCIAS QUÍMICAS INTRODUCCIÓN AL ESTUDIO DE HONGOS M.C. Francisco Javier Gómez Vega Mayo del 2005 H O N G O S No existe un acuerdo general sobre los límites
UNIVERSIDAD PEDAGOGICA Y TECNOLOGICA DE COLOMBIA FITOPATOLOGIA GENERAL GUIA PARA LA OBSERVACION MICROSCOPICA DE HONGOS FITOPATÓGENOS
 UNIVERSIDAD PEDAGOGICA Y TECNOLOGICA DE COLOMBIA FITOPATOLOGIA GENERAL GUIA PARA LA OBSERVACION MICROSCOPICA DE HONGOS FITOPATÓGENOS INTRODUCCIÓN. Para el diagnóstico y estudio de enfermedades, en la mayoría
UNIVERSIDAD PEDAGOGICA Y TECNOLOGICA DE COLOMBIA FITOPATOLOGIA GENERAL GUIA PARA LA OBSERVACION MICROSCOPICA DE HONGOS FITOPATÓGENOS INTRODUCCIÓN. Para el diagnóstico y estudio de enfermedades, en la mayoría
QUERATITIS POR FUSARIUM OXYSPORUM. CASO 652
 QUERATITIS POR FUSARIUM OXYSPORUM. CASO 652 Mujer de 60 años que presenta como antecedentes una intervención de cataratas en ambos ojos en enero de 2014, desarrollando días después una úlcera corneal herpética
QUERATITIS POR FUSARIUM OXYSPORUM. CASO 652 Mujer de 60 años que presenta como antecedentes una intervención de cataratas en ambos ojos en enero de 2014, desarrollando días después una úlcera corneal herpética
Estructuras celulares de protozoarios y hongos
 Estructuras celulares de protozoarios y hongos Luis David Rosario Jimenez, Instituto Tecnológico Superior de los Ríos, departamento de ingeniería bioquímica, CP 86930, carretera Balancán- Villahermosa
Estructuras celulares de protozoarios y hongos Luis David Rosario Jimenez, Instituto Tecnológico Superior de los Ríos, departamento de ingeniería bioquímica, CP 86930, carretera Balancán- Villahermosa
- Mencionar las Normas de Bioseguridad y precauciones necesarias para trabajar en el laboratorio microbiológico.
 Microbiología General e Inmunología Año 2012 Trabajo Práctico Nº1 Objetivos: Que el alumno sea capaz de: - Mencionar las Normas de Bioseguridad y precauciones necesarias para trabajar en el laboratorio
Microbiología General e Inmunología Año 2012 Trabajo Práctico Nº1 Objetivos: Que el alumno sea capaz de: - Mencionar las Normas de Bioseguridad y precauciones necesarias para trabajar en el laboratorio
MICOSIS CUTÁNEAS. Los hongos, como seres vivos necesitan para su crecimiento:
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA CENTRO UNIVERSITARIO METROPOLITANO FACULTAD DE CIENCIAS MÉDICAS MICROBIOLOGÍA TERCER AÑO MICOSIS CUTÁNEAS Los hongos son seres eucariotas. La mayoría de los hongos
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA CENTRO UNIVERSITARIO METROPOLITANO FACULTAD DE CIENCIAS MÉDICAS MICROBIOLOGÍA TERCER AÑO MICOSIS CUTÁNEAS Los hongos son seres eucariotas. La mayoría de los hongos
DERMATOFITOSIS DEFINICION:
 DERMATOFITOSIS DEFINICION: Los dermatofitos son un grupo de hongos estrechamente relacionados que tienen la capacidad de invadir tejidos queratinizados ( piel, pelos y uñas ) produciendo infección en el
DERMATOFITOSIS DEFINICION: Los dermatofitos son un grupo de hongos estrechamente relacionados que tienen la capacidad de invadir tejidos queratinizados ( piel, pelos y uñas ) produciendo infección en el
Dermatofitosis en la infancia. Silvia Moreno
 Dermatofitosis en la infancia Silvia Moreno Área comprometida Tipo de Hongo Estado inmunológico del huésped Tiña Capitis Cualquier dermatofito Epidermofitum flocosum Tricofitum concentricum Tricofitum
Dermatofitosis en la infancia Silvia Moreno Área comprometida Tipo de Hongo Estado inmunológico del huésped Tiña Capitis Cualquier dermatofito Epidermofitum flocosum Tricofitum concentricum Tricofitum
RECONOCIMIENTO DE LOS PRINCIPIOS INMEDIATOS QUE HAY EN UN ALIMENTO
 RECONOCIMIENTO DE LOS PRINCIPIOS INMEDIATOS QUE HAY EN UN ALIMENTO Fundamento Los alimentos se diferencian entre sí por las sustancias o principios inmediatos que contienen y por la cantidad de cada uno
RECONOCIMIENTO DE LOS PRINCIPIOS INMEDIATOS QUE HAY EN UN ALIMENTO Fundamento Los alimentos se diferencian entre sí por las sustancias o principios inmediatos que contienen y por la cantidad de cada uno
Hongos. Hongos ornamentales. Psilocybes Amanita muscaria Cortinarius violaceus
 Hongos Hongos ornamentales Psilocybes Amanita muscaria Cortinarius violaceus Hongos alimenticios Ustilago maydis (zeae) Amanita cesarea Boletus edulis Agaricus campestris Rossula brevipes (stuntzii) Candida
Hongos Hongos ornamentales Psilocybes Amanita muscaria Cortinarius violaceus Hongos alimenticios Ustilago maydis (zeae) Amanita cesarea Boletus edulis Agaricus campestris Rossula brevipes (stuntzii) Candida
AcuaNatura ÍNDICE TÉCNICAS DE TINCIÓN
 TÉCNICAS DE TINCIÓN ÍNDICE 1. Introducción 3 2. Tipos de tinciones 4 2.1. Tinción de Gram 4 2.2. Tinción ácido alcohol resistencia 5 2.3. Tinción de esporas 5 2.4. Tinción negativa 6 3. Precauciones 7
TÉCNICAS DE TINCIÓN ÍNDICE 1. Introducción 3 2. Tipos de tinciones 4 2.1. Tinción de Gram 4 2.2. Tinción ácido alcohol resistencia 5 2.3. Tinción de esporas 5 2.4. Tinción negativa 6 3. Precauciones 7
Instructivo. Manejo de los Residuos Infecciosos
 Página 1 de 5 1. Objetivo Describir las actividades necesarias (clasificación, almacenamiento, tratamiento y eliminación), para realizar el manejo de los residuos infeciosos. 2. Alcance Se aplica a todas
Página 1 de 5 1. Objetivo Describir las actividades necesarias (clasificación, almacenamiento, tratamiento y eliminación), para realizar el manejo de los residuos infeciosos. 2. Alcance Se aplica a todas
Teórico: Micosis superficiales
 Teórico: Micosis superficiales Jorge Luis Finquelievich Médico Profesor Adjunto Departamento de Microbiología, Parasitología e Inmunología Facultad de medicina. UBA Las micosis superficiales son infecciones
Teórico: Micosis superficiales Jorge Luis Finquelievich Médico Profesor Adjunto Departamento de Microbiología, Parasitología e Inmunología Facultad de medicina. UBA Las micosis superficiales son infecciones
HONGOS CONTAMINANTES COMUNES. Ruby N. Gutiérrez 5.1
 HONGOS CONTAMINANTES COMUNES. Ruby N. Gutiérrez 5.1 - Medios de Sabouraud y Mycosel - El agar Mycosel contiene cicloheximida y cloranfenicol (antibióticos) que inhiben el crecimiento de casi todas las
HONGOS CONTAMINANTES COMUNES. Ruby N. Gutiérrez 5.1 - Medios de Sabouraud y Mycosel - El agar Mycosel contiene cicloheximida y cloranfenicol (antibióticos) que inhiben el crecimiento de casi todas las
CUADRO CARACTERÍSTICO DEL GENERO BOLETUS
 CUADRO CARACTERÍSTICO DEL GENERO BOLETUS Autor Alfonso Rey Pazos lunes, 12 de noviembre de 2007 Agrupación Micológica A Zarrota CUADRO DE CARACTERÍSTICAS MACROSCÓPICAS Y MORFOLÓGICAS PARA LA IDENTIFICACIÓN
CUADRO CARACTERÍSTICO DEL GENERO BOLETUS Autor Alfonso Rey Pazos lunes, 12 de noviembre de 2007 Agrupación Micológica A Zarrota CUADRO DE CARACTERÍSTICAS MACROSCÓPICAS Y MORFOLÓGICAS PARA LA IDENTIFICACIÓN
Materiales. Cultivos puros de bacterias: Streptomyces griseus Streptomyces erythraeus
 Unidad 3. Estudio de cultivos bacterianos puros y Unidad 4. Estudio microscópico y cultivo de hongos, algas y protozoarios Práctica 6. Técnicas de siembra y cultivo de actinomicetos y hongos Objetivos
Unidad 3. Estudio de cultivos bacterianos puros y Unidad 4. Estudio microscópico y cultivo de hongos, algas y protozoarios Práctica 6. Técnicas de siembra y cultivo de actinomicetos y hongos Objetivos
AISLAMIENTO DE MICROORGANISMOS
 PRÁCTICA5 AISLAMIENTO DE MICROORGANISMOS Introducción En la naturaleza, la mayoría de los microorganismos no se encuentran aislados, sino integrados en poblaciones mixtas. Para llevar a cabo el estudio
PRÁCTICA5 AISLAMIENTO DE MICROORGANISMOS Introducción En la naturaleza, la mayoría de los microorganismos no se encuentran aislados, sino integrados en poblaciones mixtas. Para llevar a cabo el estudio
PRÁCTICA 5 FASES DE LA MITOSIS. ESTIMACIÓN DE LOS ÍNDICES MITÓTICO Y DE FASE
 PRÁCTICA 5 FASES DE LA MITOSIS. ESTIMACIÓN DE LOS ÍNDICES MITÓTICO Y DE FASE INTRODUCCIÓN La mitosis es la división nuclear asociada a las células somáticas (las células de un organismo eucariótico que
PRÁCTICA 5 FASES DE LA MITOSIS. ESTIMACIÓN DE LOS ÍNDICES MITÓTICO Y DE FASE INTRODUCCIÓN La mitosis es la división nuclear asociada a las células somáticas (las células de un organismo eucariótico que
Tema 4.- Técnicas de siembra y aislamiento
 Tema 4.- Técnicas de siembra y aislamiento La siembra consiste en tomar con el asa de platino, previamente flameado, o con hisopo estéril una pequeña cantidad de muestra a estudiar y repartirla por toda
Tema 4.- Técnicas de siembra y aislamiento La siembra consiste en tomar con el asa de platino, previamente flameado, o con hisopo estéril una pequeña cantidad de muestra a estudiar y repartirla por toda
MANUAL DE NORMAS Y PROCEDIMIENTOS PROCEDIMIENTO: OPERATIVOS DE ORINAS
 SERVICIO DE LABORATORIO 1 DE 5 1. OBJETIVO El objetivo del presente documento es describir el procedimiento para determinar las características físicas, química y microscópicas de muestras de orinas. 2.
SERVICIO DE LABORATORIO 1 DE 5 1. OBJETIVO El objetivo del presente documento es describir el procedimiento para determinar las características físicas, química y microscópicas de muestras de orinas. 2.
GPC. Guía de Referencia Rápida. Diagnóstico y Tratamiento de Tiña y Onicomicosis en el Primer Nivel de Atención
 Guía de Referencia Rápida Diagnóstico y Tratamiento de Tiña y Onicomicosis en el Primer Nivel de Atención GPC Guía de Práctica Clínica Catalogo Maestro de Guías de Práctica Clínica IMSS-086-08 Guía de
Guía de Referencia Rápida Diagnóstico y Tratamiento de Tiña y Onicomicosis en el Primer Nivel de Atención GPC Guía de Práctica Clínica Catalogo Maestro de Guías de Práctica Clínica IMSS-086-08 Guía de
La micología médica ha cobrado importancia
 Dermatología Rev Mex 2007;51(4):161-65 Comentario Micología médica y su relación con la cultura Jorge Mayorga* RESUMEN El propósito de este trabajo es mostrar algunas semejanzas entre los hallazgos micológicos
Dermatología Rev Mex 2007;51(4):161-65 Comentario Micología médica y su relación con la cultura Jorge Mayorga* RESUMEN El propósito de este trabajo es mostrar algunas semejanzas entre los hallazgos micológicos
IDENTIFICACIÓN DE LOS HONGOS CONTAMINANTES MÁS FRECUENTES EN EL CULTIVO DE SETAS COMESTIBLES Y MEDICINALES PROTOCOLO
 Proyecto: Adaptación e implementación de cinco cepas de hongos comestibles en diferentes subproductos agrícolas para mejorar la productividad y competitividad de ASOFUNGICOL en el Huila IDENTIFICACIÓN
Proyecto: Adaptación e implementación de cinco cepas de hongos comestibles en diferentes subproductos agrícolas para mejorar la productividad y competitividad de ASOFUNGICOL en el Huila IDENTIFICACIÓN
MICOLOGÍA Datos de identificación: Introducción: Objetivo general:
 MICOLOGÍA Datos de identificación: Universidad de Sonora. División de Ciencias Biológicas y de la Salud. Licenciaturas Usuarias: Químico Biólogo Clínico. Nombre de la Materia o asignatura: Micología. Eje
MICOLOGÍA Datos de identificación: Universidad de Sonora. División de Ciencias Biológicas y de la Salud. Licenciaturas Usuarias: Químico Biólogo Clínico. Nombre de la Materia o asignatura: Micología. Eje
Micología médica básica, 5ª. Ed. Alexandro Bonifaz Bonifaz Capítulo 2. Propiedades generales de los hongos
 Micología médica básica, 5ª. Ed. Alexandro Bonifaz Micología médica básica, 5ª. Ed. Parte I. Inducción y generalidades 1. Introducción a la micología 2. Propiedades generales de los hongos 3. Propiedades
Micología médica básica, 5ª. Ed. Alexandro Bonifaz Micología médica básica, 5ª. Ed. Parte I. Inducción y generalidades 1. Introducción a la micología 2. Propiedades generales de los hongos 3. Propiedades
PONTIFICIA UNIVERSIDAD JAVERIANA FACULTAD DE CIENCIAS CARRERA DE BACTERIOLOGÍA
 PONTIFICIA UNIVERSIDAD JAVERIANA FACULTAD DE CIENCIAS CARRERA DE BACTERIOLOGÍA ESTANDARIZACIÓN E IMPLEMENTACIÓN DE LAS TÉCNICAS EN EL DIAGNÓSTICO CLÍNICO DE MICOSIS CUTÁNEAS EN EL LABORATORIO DE MICOLOGÍA
PONTIFICIA UNIVERSIDAD JAVERIANA FACULTAD DE CIENCIAS CARRERA DE BACTERIOLOGÍA ESTANDARIZACIÓN E IMPLEMENTACIÓN DE LAS TÉCNICAS EN EL DIAGNÓSTICO CLÍNICO DE MICOSIS CUTÁNEAS EN EL LABORATORIO DE MICOLOGÍA
UNIVERSIDAD TÉCNICA DE AMBATO FACULTAD DE CIENCIAS DE LA SALUD CARRERA DE LABORATORIO CLÍNICO
 UNIVERSIDAD TÉCNICA DE AMBATO FACULTAD DE CIENCIAS DE LA SALUD CARRERA DE LABORATORIO CLÍNICO INFORME DE INVESTIGACIÓN SOBRE: IDENTIFICACIÓN DE DERMATOFITOS Y SU RELACIÓN CON TIÑA CAPITIS. Requisito previo
UNIVERSIDAD TÉCNICA DE AMBATO FACULTAD DE CIENCIAS DE LA SALUD CARRERA DE LABORATORIO CLÍNICO INFORME DE INVESTIGACIÓN SOBRE: IDENTIFICACIÓN DE DERMATOFITOS Y SU RELACIÓN CON TIÑA CAPITIS. Requisito previo
PRÁCTICAS DE MICROBIOLOGÍA CLÍNICA (CURSO )
 PRÁCTICAS DE MICROBIOLOGÍA CLÍNICA (CURSO 2012 2013) PRÁCTICAS A REALIZAR ANÁLISIS CUANTITATIVO DE ORINA ANÁLISIS CUALITATIVO DE ORINA M-1 M-2 M-3 M-4 Lectura de la placa de Agar CLED Identificación presuntiva
PRÁCTICAS DE MICROBIOLOGÍA CLÍNICA (CURSO 2012 2013) PRÁCTICAS A REALIZAR ANÁLISIS CUANTITATIVO DE ORINA ANÁLISIS CUALITATIVO DE ORINA M-1 M-2 M-3 M-4 Lectura de la placa de Agar CLED Identificación presuntiva
Petrifilm. Levaduras y Mohos. Guía de Interpretación
 3 Petrifilm Levaduras y Mohos Guía de Interpretación Hacer un recuento con placas Petrifilm Levaduras y Mohos es fácil. Contienen un indicador colorante para levaduras y mohos para proporcionar contraste
3 Petrifilm Levaduras y Mohos Guía de Interpretación Hacer un recuento con placas Petrifilm Levaduras y Mohos es fácil. Contienen un indicador colorante para levaduras y mohos para proporcionar contraste
GUÍA REALIZACIÓN DE CULTIVOS MICROBIOLÓGICOS
 ESCUELA DE SALUD GUÍA REALIZACIÓN DE CULTIVOS MICROBIOLÓGICOS DIRIGIDO A ALUMNOS DE: Técnico de laboratorio Clínico y Banco de Sangre Técnico de Enfermería Técnico de Radiodiagnóstico y Radioterapia Informática
ESCUELA DE SALUD GUÍA REALIZACIÓN DE CULTIVOS MICROBIOLÓGICOS DIRIGIDO A ALUMNOS DE: Técnico de laboratorio Clínico y Banco de Sangre Técnico de Enfermería Técnico de Radiodiagnóstico y Radioterapia Informática
Casos Clinicos. Dra Beatriz Pi Postgrado Enfermedades Infecciosas Facultad de Medicina Enero 2012
 Casos Clinicos Dra Beatriz Pi Postgrado Enfermedades Infecciosas Facultad de Medicina Enero 2012 Sexo Femenino. 29 años. VIH diagnosticado en 2008, Recibiendo TARV desde julio 2011 ABC/3TC/EFV. CV 25000
Casos Clinicos Dra Beatriz Pi Postgrado Enfermedades Infecciosas Facultad de Medicina Enero 2012 Sexo Femenino. 29 años. VIH diagnosticado en 2008, Recibiendo TARV desde julio 2011 ABC/3TC/EFV. CV 25000
COMPROBACIÓN DE LA PRESENCIA DE ALMIDÓN EN EMBUTIDOS
 NOMBRE: GRUPO: PRÁCTICA: FECHA: COMPROBACIÓN DE LA PRESENCIA DE ALMIDÓN EN EMBUTIDOS El almidón es un polisacárido que se encuentra en el citoplasma de las células vegetales Es muy abundante en los tubérculos,
NOMBRE: GRUPO: PRÁCTICA: FECHA: COMPROBACIÓN DE LA PRESENCIA DE ALMIDÓN EN EMBUTIDOS El almidón es un polisacárido que se encuentra en el citoplasma de las células vegetales Es muy abundante en los tubérculos,
Microbiología. Trabajo Práctico 3. Cultivo e identificación de bacterias. GRACIELA NATALIA PUCCI
 Microbiología Trabajo Práctico 3. Cultivo e identificación de bacterias. GRACIELA NATALIA PUCCI Objetivos: Reconocer los distintos medios de cultivo utilizados para la recuperación de bacterias, y comprender
Microbiología Trabajo Práctico 3. Cultivo e identificación de bacterias. GRACIELA NATALIA PUCCI Objetivos: Reconocer los distintos medios de cultivo utilizados para la recuperación de bacterias, y comprender
Mem. Inst. Investig. Cienc. Salud, Vol. 1(1) 2001/ Dermatofitos y hongos levaduriformes productores de micosis superficiales
 Mem. Inst. Investig. Cienc. Salud, Vol. 1(1) 2001/02 63 ARTICULO ORIGINAL Dermatofitos y hongos levaduriformes productores de micosis superficiales Mycosis produced by dermatophytes and yeasts *Sanabria
Mem. Inst. Investig. Cienc. Salud, Vol. 1(1) 2001/02 63 ARTICULO ORIGINAL Dermatofitos y hongos levaduriformes productores de micosis superficiales Mycosis produced by dermatophytes and yeasts *Sanabria
TRICHOSPORONOSIS. Dra. Marisa Biasoli Centro de Referencia de Micología
 TRICHOSPORONOSIS Dra. Marisa Biasoli Centro de Referencia de Micología Definición: n: es una infección n oportunista causada por hongos levaduriformes del género Trichosporon, que producen lesiones superficiales
TRICHOSPORONOSIS Dra. Marisa Biasoli Centro de Referencia de Micología Definición: n: es una infección n oportunista causada por hongos levaduriformes del género Trichosporon, que producen lesiones superficiales
Profesora: Ana María Gallardo Suárez. Observación de hongos MOHO DEL PAN Y DE LA FRUTA. PRACTICA Nº 3 CURSO: 3 ESO. Recursos ana.fjb.
 Observación de hongos MOHO DEL PAN Y DE LA FRUTA. PRACTICA Nº 3 CURSO: 3 ESO Recursos ana.fjb.es Objetivos de la Práctica Estudio de hongos descomponedores de alimentos: * Observación macroscópica del
Observación de hongos MOHO DEL PAN Y DE LA FRUTA. PRACTICA Nº 3 CURSO: 3 ESO Recursos ana.fjb.es Objetivos de la Práctica Estudio de hongos descomponedores de alimentos: * Observación macroscópica del
GUÍA OBSERVACIÓN DE MICROORGANISMOS Y USO DE TINCIONES
 ESCUELA DE SALUD GUÍA OBSERVACIÓN DE MICROORGANISMOS Y USO DE TINCIONES DIRIGIDO A ALUMNOS DE: Técnico de laboratorio Clínico y Banco de Sangre Técnico de Enfermería Técnico de Radiodiagnóstico y Radioterapia
ESCUELA DE SALUD GUÍA OBSERVACIÓN DE MICROORGANISMOS Y USO DE TINCIONES DIRIGIDO A ALUMNOS DE: Técnico de laboratorio Clínico y Banco de Sangre Técnico de Enfermería Técnico de Radiodiagnóstico y Radioterapia
Guía teórico - Práctica
 UNIVERSIDAD NACIONAL DE ENTRE RÍOS FACULTAD DE CIENCIAS AGROPECUARIAS Guía teórico - Práctica BOTÁNICA MORFOLÓGICA 2017 UNIVERSIDAD NACIONAL DE ENTRE RÍOS FACULTAD DE CIENCIAS AGROPECUARIAS Prof. María
UNIVERSIDAD NACIONAL DE ENTRE RÍOS FACULTAD DE CIENCIAS AGROPECUARIAS Guía teórico - Práctica BOTÁNICA MORFOLÓGICA 2017 UNIVERSIDAD NACIONAL DE ENTRE RÍOS FACULTAD DE CIENCIAS AGROPECUARIAS Prof. María
Atlas Digital del Departamento de Biología Celular y Tisular de la Facultad de Medicina
 UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO Atlas Digital del Departamento de Biología Celular y Tisular de la Facultad de Medicina El primer paso de toda técnica histológica es la obtención de la muestra.
UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO Atlas Digital del Departamento de Biología Celular y Tisular de la Facultad de Medicina El primer paso de toda técnica histológica es la obtención de la muestra.
ANALISIS RETROSPECTIVO DE PACIENTES,
 453 DERMATOMICOSIS ANALISIS RETROSPECTIVO DE 2.336 PACIENTES, 1976-1980 L. SANTA MARIA, H. VELEZ, G. GUZMAN Se presentan 2.336 casos de dermatomicosis observados en el periodo 1976-1980 en el Laboratorio
453 DERMATOMICOSIS ANALISIS RETROSPECTIVO DE 2.336 PACIENTES, 1976-1980 L. SANTA MARIA, H. VELEZ, G. GUZMAN Se presentan 2.336 casos de dermatomicosis observados en el periodo 1976-1980 en el Laboratorio
Micología Diagnóstica (2177)
 Micología Diagnóstica (2177) 1.-Introducción Los alumnos que llegan a cursar Micología Diágnostica (2177) han cursado Micología (2115), por lo tanto tienen conocimientos sobre los contenidos vertidos en
Micología Diagnóstica (2177) 1.-Introducción Los alumnos que llegan a cursar Micología Diágnostica (2177) han cursado Micología (2115), por lo tanto tienen conocimientos sobre los contenidos vertidos en
MICOLOGÍA MÉDICA CARACTERÍSTICAS GENERALES DE LOS HONGOS:
 MICOLOGÍA MÉDICA INTRODUCCIÓN Los hongos agrupan una gran variedad de organismos suficientemente caracterizados para constituir un grupo particular de seres vivos, distinto del reino animal y vegetal,
MICOLOGÍA MÉDICA INTRODUCCIÓN Los hongos agrupan una gran variedad de organismos suficientemente caracterizados para constituir un grupo particular de seres vivos, distinto del reino animal y vegetal,
TEMA 9 MÉTODOS ÓPTICOS PARA EL DIAGNÓSTICO DE LABORATORIO DE ENFERMEDADES INFECCIOSAS
 TEMA 9 MÉTODOS ÓPTICOS PARA EL DIAGNÓSTICO DE LABORATORIO DE ENFERMEDADES INFECCIOSAS INDICE DE CONTENIDOS Introducción Tipos de microscopía óptica Microscopía de campo claro Microscopía de campo oscuro
TEMA 9 MÉTODOS ÓPTICOS PARA EL DIAGNÓSTICO DE LABORATORIO DE ENFERMEDADES INFECCIOSAS INDICE DE CONTENIDOS Introducción Tipos de microscopía óptica Microscopía de campo claro Microscopía de campo oscuro
La micología médica ha sufrido un cambio radical
 FORMACIÓN Procesos micológicos y sus cuidados 8 María José Iriarte Ayestarán, Enfermera de Dermatología. Colaboradoras: Dra. Rosa Taberner, Dra. Antònia Vila y Dra Cristina Nadal. Unidad de Dermatología,
FORMACIÓN Procesos micológicos y sus cuidados 8 María José Iriarte Ayestarán, Enfermera de Dermatología. Colaboradoras: Dra. Rosa Taberner, Dra. Antònia Vila y Dra Cristina Nadal. Unidad de Dermatología,
Identificación de fibras por microscopía
 Identificación de fibras por microscopía 1 Objetivos... 3 2 Introducción teórica... 3 3 Materiales, equipos y útiles de trabajo... 6 4 Procedimiento experimental... 7 5 Normas específicas de trabajo y
Identificación de fibras por microscopía 1 Objetivos... 3 2 Introducción teórica... 3 3 Materiales, equipos y útiles de trabajo... 6 4 Procedimiento experimental... 7 5 Normas específicas de trabajo y
MICROSPORUM CANIS - PRODUCCION DE "ORGANOS PERFORADORES" DE PELOS EN CULTIVO SEGUN LA TECNICA DE AJELLO Y GEORG* Corrado Capretti**
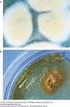 MICROSPORUM CANIS - PRODUCCION DE "ORGANOS PERFORADORES" DE PELOS EN CULTIVO SEGUN LA TECNICA DE AJELLO Y GEORG* Corrado Capretti** INTR0DUCCION Vanbreuseghem describió en 19492 una técnica para el cultivo
MICROSPORUM CANIS - PRODUCCION DE "ORGANOS PERFORADORES" DE PELOS EN CULTIVO SEGUN LA TECNICA DE AJELLO Y GEORG* Corrado Capretti** INTR0DUCCION Vanbreuseghem describió en 19492 una técnica para el cultivo
UNIVERSIDAD DE TALCA FACULTAD DE CIENCIAS DE LA SALUD ESCUELA DE TECNOLOGÍA MÉDICA
 UNIVERSIDAD DE TALCA FACULTAD DE CIENCIAS DE LA SALUD ESCUELA DE TECNOLOGÍA MÉDICA PREVALENCIA DE MICOSIS SUPERFICIALES Y CUTÁNEAS EN PERSONAL MILITAR DEL REGIMIENTO DE TALCA MEMORIA PARA OPTAR AL GRADO
UNIVERSIDAD DE TALCA FACULTAD DE CIENCIAS DE LA SALUD ESCUELA DE TECNOLOGÍA MÉDICA PREVALENCIA DE MICOSIS SUPERFICIALES Y CUTÁNEAS EN PERSONAL MILITAR DEL REGIMIENTO DE TALCA MEMORIA PARA OPTAR AL GRADO
Diagnóstico microbiológico de las micosis cutáneas superficiales
 Diagnóstico microbiológico de las micosis cutáneas superficiales Josep M. Torres-Rodríguez Unidad de Investigación en Micología Experimental y Clínica. IMIM/IMAS. Universidad Autónoma de Barcelona. Barcelona.
Diagnóstico microbiológico de las micosis cutáneas superficiales Josep M. Torres-Rodríguez Unidad de Investigación en Micología Experimental y Clínica. IMIM/IMAS. Universidad Autónoma de Barcelona. Barcelona.
EXPLICACIÓN DE TRABAJOS PRÁCTICOS COLORACIONES
 EXPLICACIÓN DE TRABAJOS PRÁCTICOS COLORACIONES Microbiología General Carrera: Tecnicatura Universitaria en Esterilización Analista Biológico 2015 DIFERENCIA ENTRE CÉLULA PROCARIOTA Y CÉLULA EUCARIOTA Morfología
EXPLICACIÓN DE TRABAJOS PRÁCTICOS COLORACIONES Microbiología General Carrera: Tecnicatura Universitaria en Esterilización Analista Biológico 2015 DIFERENCIA ENTRE CÉLULA PROCARIOTA Y CÉLULA EUCARIOTA Morfología
 NILOPIROX terbinafina comp. 250 mg terbinafina crema 1% Dr. Luis Mauricio Saavedra Aguirre ASESOR MEDICO LABORATORIOS FARMACÉUTICOS LAFAR Septiembre -2010 PIEL Órgano más extenso del organismo. Recubre
NILOPIROX terbinafina comp. 250 mg terbinafina crema 1% Dr. Luis Mauricio Saavedra Aguirre ASESOR MEDICO LABORATORIOS FARMACÉUTICOS LAFAR Septiembre -2010 PIEL Órgano más extenso del organismo. Recubre
UNIVERSIDAD DECUENCA FACULTAD DECIENCIAS QUÍMICAS CARRERA DE BIOQUÍMICA Y FARMACIA
 UNIVERSIDAD DECUENCA FACULTAD DECIENCIAS QUÍMICAS CARRERA DE BIOQUÍMICA Y FARMACIA Determinación de la prevalencia de dermatofitosis en los niños de la Escuela de Educación General Básica Padre Juan Bautista
UNIVERSIDAD DECUENCA FACULTAD DECIENCIAS QUÍMICAS CARRERA DE BIOQUÍMICA Y FARMACIA Determinación de la prevalencia de dermatofitosis en los niños de la Escuela de Educación General Básica Padre Juan Bautista
