Instrucciones de Uso
|
|
|
- Francisco Javier del Río Paz
- hace 6 años
- Vistas:
Transcripción
1 Instrucciones de Uso Vástago no Cementado en Titanio Clave de los símbolos adoptados en el etiquetado del producto Número en el catálogo Producto Estéril - Esterilizado por Raciación Gamma Fecha de Fabricación XXXX Código de lote Producto certificado en conformidad con la Directiva 93/42/CEE). Cuando aplicable Válido hasta Consultar las instrucciones de uso Producto de uso único No utilizar si el envase está dañado No reesterilizar Mantener al abrigo del sol Frágil, manipular con cuidado Mantener seco Límite de Temperatura (40 C) Características e especificaciones técnicas del producto Nombre Técnico: Material Implantable Nombre Comercial: Vástago no Cementado en Titanio Modelos Comerciales: Prótesis Femoral MD4 Porous Coated; Prótesis Femoral MD4 Plasma Spray; Prótesis Femoral EZ-Fit PS Ti; Prótesis Femoral PHENM PS Ti; Materias Primas: Prótesis (sustrato) Revestimiento: Titanio (Porous Coated o Plasma Spray); Producto Estéril Método de esterilización: Radiación Gamma (dosis 25 kgy) Caducidad: 05 años (después de la fecha de esterilización) Descripción La familia de Vástago No Cementado en Titanio consiste en dispositivos implantables, invasivos quirúrgicamente, de uso a largo plazo, utilizado en procedimientos de reemplazo articular de la cadera. Compuesta por los modelos comerciales Prótesis Femoral MD4 (con revestimiento de titanio Porous Coated o por aspersión de Plasma Spray), Prótesis Femoral EZ-Fit PS Ti y Prótesis Femoral PHENM PS Ti, cada una con su propia indicación, destinan-se al reemplazo de la articulación natural en procedimientos parcial o total de artroplastia de la cadera. Fabricadas a partir de la aleación de titanio (Ti-6A-4V), las prótesis femorales se componen del cono (sistema cónico tipo Morse 12/14), lo que permite la modularidad de la cabeza femoral y del cuerpo longitudinal con revestimiento de titanio. La forma de fijación al canal intramedular del fémur es no cementada por medio de la impactación (press-fit), en el cual la migración distal del componente crea fuerzas de compresión radiales que estabilizan el implante y disminuyen los esfuerzos de tensión para la interfaz implante-hueso, garantizando mayor longevidad a la reconstrucción protésica.
2 La familia del Vástago no Cementado en Titanio es destinado a pacientes esqueléticamente maduros para la reconstrucción de la porción femoral en artroplastias parciales o totales de la cadera en pacientes que presentan daños a esta articulación debido a la enfermedad articular degenerativa no inflamatoria (osteoartrosis), necrosis avascular de la cabeza femoral, protrusión acetabular, osteoartrosis secundario a los traumatismos, el epifisiolisis femoral proximal, y secuelas de fracturas de la pelvis, anquilosis o artrodesis quirúrgico de la cadera. La Prótesis Femoral MD4 tiene dos opciones de revestimiento rugoso, microesferas de titanio denominado Porous Coated o polvo de titanio asperjado por Plasma Spray, que promueve la adherencia de la prótesis al hueso. Es indicada para los procedimientos primarios, el vástago tiene ¾ de la superficie longitudinal revestido, y la de revisión, vástago con toda la extensión longitudinal revestido. Disponibles comercialmente en varias longitudes y diámetros, la prótesis tienen angulación de 135º en relación con su eje protésico longitudinal. Primaria Revisión Primaria Revisión Prótesis Femoral MD4 Porous Coated Prótesis Femoral MD4 Plasma Spray La Prótesis Femoral EZ-Fit PS Ti tiene una superficie exterior revestida de titanio por aspersión de plasma spray, es indicada para procedimientos primarios con fijación proximal. Tiene una forma cónica que le proporciona una mayor estabilidad axial y una mejor transmisión de los esfuerzos mecánicos al hueso. La prótesis es acanalada para una mayor estabilidad rotacional y tiene aletas por todo el cuerpo longitudinal que estimula el crecimiento óseo en estas áreas, potenciando la fijación de la prótesis en el canal intramedular. El cuello del vástago se presenta con angulaciones de 130º, 135º y 140º grados en relación con el eje protésico longitudinal y cinco variaciones de off-set 33, 37, 40, 43 y 47 mm, que asociada a las posibilidades de variación de las cabezas femorales proporcionan al cirujano una amplia gama de posibilidades para el montaje del implante según sea necesario para el paciente. Disponible para la comercialización con diámetros que varían de 14 a 20 mm, tiene longitud de 100 mm. Prótesis Femoral EZ-Fit PS Ti La Prótesis Femoral PHENM PS Ti tiene una superficie exterior revestida de titanio por aspersión de plasma spray, se presenta en las versiones para procedimientos primarios y de revisión. La versión para procedimientos primarios tiene una forma cónica que le proporciona una mayor estabilidad axial y una mejor transmisión de los esfuerzos mecánicos al hueso. Tiene 3/4 del cuerpo longitudinal con revestimiento de titanio que estimula el crecimiento óseo y potencia la fijación de la prótesis en el canal intramedular.
3 El cuello del vástago se presenta con angulación de 135º en relación con el eje protésico longitudinal y off-set variable de 35.0 a 42.5 mm. Está disponible para la comercialización con diámetros de 10 a 18 mm y longitudes que varían de 137 a 185 mm. La versión para procedimientos de revisión tiene la porción proximal del cuerpo longitudinal revestida de titanio. En la porción distal, la prótesis es acanelada para una mayor estabilidad rotacional y tiene aletas que estimulan el crecimiento óseo y potencia la fijación en el canal intramedular. El cuello del vástago se presenta con angulación de 135º y 130º en relación con el eje protésico longitudinal y off-sets de 37.5 y 42.5 mm, respectivamente. Está disponible para la comercialización con diámetros de 12,5 a 20,0 mm y longitudes que varían de 180 a 260 mm. Primaria Revisión Prótesis Femoral PHENM PS Ti Composición Los materiales seleccionados para la fabricación reúnen las propiedades físico-químicas y mecánicas requeridas para alcanzar el desempeño que se pretende para el producto. La selección consideró factores como la fabricación, la manipulación, la esterilización, el almacenamiento, así como posibles reacciones del material con los tejidos humanos y los fluidos corporales. La familia del Vástago No Cementado en Titanio es fabricada a partir de la (Ti- 6Al-4V). El material de fabricación es compatible con los tejidos biológicos, células y los tejidos corporales, con los cuales entran en contacto en el estado implantable, comprobado por el histórico de utilización en aplicaciones similares disponibles en la literatura científica y clínica mundial. Esta comprobación también se aplica a los posibles productos de desgaste y degradación de los materiales en niveles aceptables al largo de su utilización. El material utilizado para la fabricación del producto y sus respectivas combinaciones para las superficies de articulación y de contacto, están relacionadas respectivamente en los anexos A, B y C de la norma ABNT NBR IS Implantes para cirurgia não-ativos Implantes para substituição de articulações Requisitos Particulares, que establece la relación de normas para materiales considerados aceptables a través del uso comprobado por la literatura científica y clínica, para la fabricación de implantes. La aleación de titanio (Ti-6Al-4V) utilizada para la fabricación del producto cumple los requisitos especificados por la norma ASTM F-136 Standard Specification for Wrought Titanium-6Aluminum- 4Vanadium ELI (Extra Low Interstitial) Alloy for Surgical Implant Applications. El revestimiento de titanio aplicado sobre los modelos comerciales Prótesis Femoral MD4 (porous coated y plasma spray), Prótesis Femoral EZ-Fit PS Ti, Prótesis Femoral PHENM PS Ti, cumple los requisitos especificados por la norma ASTM F-1580 Standard Specification for Titanium and Titanium-6 Aluminum-4 Vanadium Alloy Powders for Coatings of Surgical Implants. La elección de estos materiales para la fabricación de los modelos comerciales que componen la familia del Vástago No Cementado en Titanio se basó en criterios de similitud (resultados ampliamente descriptos en la literatura) y por sus características de biocompatibilidad y propiedades físico-química y mecánica comprobadas por las normas de especificación de estos materiales. Indicación y Finalidad Los modelos de negocios que componen la familia de Vástago No Cementado en Titanio están indicados para uso en pacientes esqueléticamente maduros, como parte de la reconstrucción de la porción femoral en artroplastias parciales o totales de la cadera en pacientes que presentan daños en
4 esta articulación, derivados de la enfermedad articular degenerativa no inflamatoria (osteoartritis), necrosis vascular de la cabeza femoral, la protrusión acetabular, la osteoartritis secundaria a un traumatismo, epifisiolisis femoral proximal y las secuelas de fractura de la pelvis, la anquilosis o artrodesis quirúrgica de la cadera. El producto tiene por finalidad la fijación proximal no cementada por impactación (press-fit) en procedimientos de artroplastia parcial o total de la cadera, tanto para los casos primarios como para los casos de revisión. Los productos aquí descriptos fueron desarrollados para la utilización en las circunstancias arriba mencionadas, de modo que cualquier otro uso es considerado contraindicado o sin base científica que lo respalde. Contraindicaciones A continuación, son listadas las contraindicaciones relativas para la utilización del dispositivo, quedando a cargo del cirujano responsable, tras un estudio minucioso del caso, la indicación de los procedimientos: Pacientes con infecciones activas generales o específicas que puedan llevar a complicaciones; Pacientes con estado general comprometido y/o inmunodeprimidos imposibilitados de someterse a un procedimiento quirúrgico; Pacientes con sensibilidad a cuerpos extraños, siendo que en estos casos deberán realizarse pruebas; Pacientes con osteoporosis y/u otras afecciones óseas que puedan comprometer el resultado de la artroplastia; Pacientes portadores de enfermedades óseas rápidamente destructivas u osteonecrosis postirradiación; Pacientes portadores de enfermedades neurológicas progresivas; Pacientes portadores de enfermedades circulatorias locales y con insuficiencias arteriales o venosas; Pacientes que hacen uso de sustancias entorpecedoras, alcohólicas o tabaco; Pacientes con ausencia de soporte óseo que permita una fijación adecuada del implante; Pacientes con ausencia o paresia de la musculatura que controla la cadera. Forma de Presentación Los modelos de negocio que componen la familia del Vástago No Cementado en Titanio son dispuestos unitariamente en un sistema de envase o empaque primario tipo blister sellada con papel de grado quirúrgico (tipo Tyvec ) o en sistema de envase quirúrgico tipo Tyvec, que funcionan como barrera de esterilización. El producto se suministra para comercialización en la condición estéril, siendo que el método adoptado es la esterilización por radiación gamma (dosis 25 kgy), procedimiento realizado por una empresa tercerizada debidamente cualificada. Después de esterilizados, los componentes envasados en sus envases o empaque primario debidamente rotulado, son dispuestos en un envase o empaque de cartón (envase secundario), el cual sigue acompañado de cinco vías de la etiqueta de rastreo y un folleto con las instrucciones de uso para la correcta utilización y manejo del producto. Sobre el envase o empaque primario y sobre el cartón lleva pegado un rótulo, que contiene las informaciones necesarias para la identificación del producto.
5 Formas de Presentación La familia de Vástago no Cementado en Titanio se presenta en los siguientes modelos comerciales y cada uno de estos modelos está disponibles para consumo en las siguientes dimensiones: Lista de los modelos comerciales que componen la familia del Vástago no Cementado en Titanio Imagen Ilustrativa Código Descripción Dimensiones Material de Fabricación Cantidad envasada XXXXX Prótesis Femoral MD4 c/ Porous Coated Cono 10/11 Primaria Diámetro: 09, 10, 11, 12, 13, 14, 15, 16, 17 mm; Longitud: 117, 122, 127, 132, 137, 142, 147, 152, 157 mm; Cono: 10/11 mm; Ángulo cervical diafisario: 135º; Diámetro: 07, 08, 09, 10, 11, 12, 13, 14, 15, 16, 17 mm; Longitud: 107, 112, 117, 122, 127, 132, 137, 142, 147, 152, 157, 160, 180, 200 mm; Cono: 12/14 mm; Ángulo cervical diafisario: 135º; (Ti-6Al-4V)/ microesferas titanio (Porous Coated) XXXXX Prótesis Femoral MD4 c/ Porous Coated Cono 12/14 Primaria (Ti-6Al-4V)/ microesferas titanio (Porous Coated) XXXXX Prótesis Femoral MD4 c/ Porous Coated Cono 10/11 Revisión Diámetro: 09, 10, 11, 12, 13, 14, 15, 16, 17 mm; Longitud: 117, 170, 180, 190, 200, 210, 220, 230, 240 mm Cono: 10/11 mm; Ángulo cervical diafisario: 135º; (Ti-6Al-4V)/ microesferas titanio (Porous Coated) XXXXX Prótesis Femoral MD4 c/ Porous Coated Cono 12/14 Revisión Diámetro: 09, 10, 11, 12, 13, 14, 15, 16, 17 mm; Longitud: 170, 180, 190, 200, 210, 220, 240, 260, 300 mm; Cono: 12/14 mm; Ángulo cervical diafisario: 135º; (Ti-6Al-4V)/ microesferas titanio (Porous Coated) XXXXX Prótesis Femoral MD4 Ti c/ Plasma Spray Cono 12/14 Primaria Diámetro: 07, 08, 09, 10, 11, 12, 13, 14, 15, 16, 17 mm; Longitud: 107, 112, 117, 122, 127, 132, 137, 142, 147, 152, 157, 160, 180, 200 mm; Cono: 12/14 mm; Ángulo cervical diafisario: 135º; (Ti-6Al-4V) titanio por aspersión de Plasma Spray XXXXX Prótesis Femoral MD4 Ti c/ Plasma Spray Cono 12/14 Revisión Diámetro: 09, 10, 11, 12, 13, 14, 15, 16, 17 mm; Longitud: 170, 180, 190, 200, 210, 220, 230, 240, 260 mm; Cono: 12/14 mm; Ángulo cervical diafisario: 135º; (Ti-6Al-4V) titanio por aspersión de Plasma Spray
6 XXXXX XXXXX XXXXX XXXXX XXXXX Prótesis Femoral EZ-Fit PS Ti Diámetro: 14, 15, 16, 17, 18, 19 y 20 mm; Longitud: 100 mm; Cono: 12/14 mm; ff-set: 33, 37, 40, 43, 47 mm; Ángulo cervical diafisario: 140º, 135º, 130º; (Ti-6Al-4V) titanio por aspersión de Plasma Spray XXXXX Prótesis Femoral PHENM PS Ti Primaria XXXXX XXXXX Prótesis Femoral PHENM PS Ti Revisión ff-set 37,5mm Prótesis Femoral PHENM PS Ti Revisión ff-set 42,5mm Diámetro: 10, 11, 12, 13, 14, 15, 16, 17, 18 mm; Longitud: 137, 143, 149, 155, 161, 167, 173, 179, 185 mm; Cono: 12/14 mm; ff-set: 35,0 à 42,5 mm Ángulo cervical diafisario: 135º; Diámetro: 12.5, 14, 15.5, 17, 18.5, 20 mm; Longitud: 180, 220, 260 mm; Cono: 12/14 mm; ff-set: 37.5 mm; Ángulo cervical diafisario: 135º; Diámetro: 15.5, 17, 18.5, 20 mm; Longitud: 180, 220, 260 mm; Cono: 12/14 mm; ff-set: 42.5 mm; Ángulo cervical diafisario: 130º; (Ti-6Al-4V) titanio por aspersión de Plasma Spray (Ti-6Al-4V) titanio por aspersión de Plasma Spray (Ti-6Al-4V) titanio por aspersión de Plasma Spray
7 Componentes Ancilares A continuación, son listados los componentes ancilares compatibles con los modelos comerciales que componen la familia del Vástago No Cementado en Titanio: Cotilos Bipolares; Cotilos Cementados; Cotilos no Cementados; Insertos para Cotilos; Cabezas Femorales Intercambiables (metálica y cerámica); El Cotilo Bipolar es fabricado a partir de la aleación de acero inoxidable (18Cr-14Ni-2.5Mo) que cumple los requisitos especificados por la norma ASTM F-138 Standard Specification for Wrought 18 Chromium-14 Nickel-2.5 Molybdenum Stainless Steel Bar and Wire for Surgical Implants, y a partir del polímero polietileno ultra alto peso molecular (UHMWPE) que cumple los requisitos especificados por la norma ASTM F-648 Standard Specification for Ultra-High-Molecular-Weight Polyethylene Powder and Fabricated Form for Surgical Implants, a través del proceso de forja seguido de mecanizado (cúpula) y mecanizado (inserto y traba) Los Cotilos Cementados, modelos Máxima y SPAC NG son fabricados por mecanizado, a partir del polímero polietileno ultra alto peso molecular (UHMWPE) que cumple los requisitos especificados por la norma ASTM F-648 Standard Specification for Ultra-High-Molecular-Weight Polyethylene Powder and Fabricated Form for Surgical Implants, a través del proceso de mecanizado. El anillo y los espaciadores en la porción externa del producto son fabricados a partir de la aleación de acero inoxidable (18Cr-14Ni-2,5Mo) y el polímero Polimetilmetacrilato (PMMA), que cumplen los requisitos especificados por las normas ASTM F-138 Standard Specification for Wrought 18 Chromium-14 Nickel-2.5 Molybdenum Stainless Steel Bar and Wire for Surgical Implants (UNS S31673) y NBR IS 5833 Implantes para Cirugía cementos de resina acrílica, respectivamente. El Cotilo No Cementado, modelos MD5 es fabricado a partir de la aleación fundida de cobalto cromo Molibdeno (Co-28Cr-6Mo) que cumple los requisitos especificados por la norma ASTM F-75 Specification for Cobalt-28 Chromium-6 Molybdenum Alloy Castings and Casting Alloy for Surgical Implants (UNS R30075). El revestimiento de microesferas (porous coated) de cobalto cromo molibdeno (Co-28Cr-06Mo) que recubre el cotilo MD5 cumple los requisitos especificados por la norma ASTM F-1377 Standard Specification for Cobalt- 28Chromium-6Molybdenum Powder for Coating of rthopedic Implants (UNS R30075). Los implantes cuando producidos a partir de este material se obtienen a través del proceso fabril de micofrusión seguido de mecanizado. Los Cotilos no Cementados, modelos MD4 y MD son fabricados a partir de la aleación de titanio (Ti-6Al- 4V) que cumple los requisitos especificados por la norma ASTM F136 Standard Specification for Wrought Titanium-6Aluminum -4Vanadium ELI (Extra Low Interstitial) Alloy for Surgical Implant Applications. El revestimiento de titanio (por aspersión por plasma spray) que recubre los cotilos cumple los requisitos especificados por la norma ASTM F-1580 Standard Specification for Titanium and Titanium-6 Aluminum-4 Vanadium Alloy Powders for Coatings of Surgical Implants. Los implantes cuando producidos a partir de este material se obtienen a través del proceso fabril de forja seguido de mecanizado. El Inserto para Cotilo 09 Puntos es fabricado a partir del polímero polietileno ultra alto peso molecular (UHMWPE) que cumple los requisitos especificados por la norma ASTM F-648 Standard Specification for Ultra-High-Molecular-Weight Polyethylene Powder and Fabricated Form for Surgical Implants, a través del proceso de mecanizado. Los componentes cerámicos Inserto para Cotilo Cerámica Delta y las Cabezas Femorales Intercambiables Cerámicas (Forte y Delta), son fabricados a partir de la cerámica alúmina de alta pureza (Al 2 3 ), que cumple los requisitos especificados por la norma IS 6474 Implants for surgery Ceramic materials based on high purity alumina, a través del proceso de sinterización, suministrada por empresa tercerizada (CeramTec) debidamente cualificada. Las Cabezas Femorales Intercambiables metálicas son fabricadas a partir de la aleación de acero inoxidable (18Cr-14Ni-2.5Mo) y de la aleación de acero Inoxidable con alto tenor de nitrógeno (21Cr-10Ni-3Mn- 2.5Mo), que cumple los requisitos especificados por las normas ASTM F138 Standard Specification for Wrought 18 Chromium-14 Nickel-2.5 Molybdenum Stainless Steel Bar and Wire for Surgical Implants y ASTM F-1586 Standard Specification for Wrought Nitrogen Strengthened 21Cromiun 10Nickel 3Manganese 2.5Molybdenum Stainless Steel Alloy Bar for Surgical Implants, respectivamente, a través del proceso de mecanizado. La correcta selección de los modelos, medidas y combinaciones de los modelos comerciales que componen la familia del Vástago No Cementado en Titanio, así como los ancilares a implantar, es de responsabilidad del cirujano que también es responsable por la técnica adoptada, debiendo estar familiarizado con el material, el método de aplicación y el procedimiento quirúrgico a realizar.
8 El éxito del procedimiento está vinculado a la correcta selección, combinación, posicionamiento y la fijación de los dispositivos, que es de responsabilidad del médico que evalúa al paciente y decide cuáles son los implantes a utilizar. También, está vinculado al riguroso cumplimiento de los cuidados postoperatorios recomendados por el médico responsable.
9 A continuación sigue la indicación de los componentes ancilares y su correcta combinación con los modelos comerciales que componen la familia del Vástago No Cementado en Titanio, para las siguientes posibilidades de montaje: Sistema para Artroplastia Parcial de Cadera No Cementada Componente Ancilar: Cotilo Bipolar Aleación de Acero Inoxidable (18Cr-14Ni-2.5Mo) Modelos Comerciales: Vástago No Cementado en Titanio Prótesis Femoral MD4 Porous Coated Prótesis Femoral MD4 Plasma Spray Cabezas Femorales Intercambiables Cabeza Femoral Intercambiable Aleación de Acero Inoxidable (18Cr-14Ni-2.5Mo) Cabeza Femoral Intercambiable HN Aleación de Acero Inoxidable (21Cr-10Ni-3Mn-2.5Mo) Componente Ancilar: Cotilo Bipolar Aleación de Acero Inoxidable (18Cr-14Ni-2.5Mo) Modelos Comerciales Vástago No Cementado en Titanio Prótesis Femoral EZ-Fit PS Ti Prótesis Femoral PHENM PS Ti Cabezas Femorales Intercambiables Cabeza Femoral Intercambiable Aleación de Acero Inoxidable (18Cr-14Ni-2.5Mo) Cabeza Femoral Intercambiable HN Aleación de Acero Inoxidable (21Cr-10Ni-3Mn-2.5Mo) Cabeza Femoral Intercambiable Cerámica Forte Cerámica Alumina (Al 2 3) Cabeza Femoral Intercambiable Cerámica Delta Cerámica Alumina (Al 2 3)
10 Sistema para Artroplastia Total de Cadera No Cementada Cotilos No Cementados Cotilo MD4 Plasma Spray + Inserto para Cotilo 09 Puntos Cotilo MD5 Porous Coated Aleación de Cobalto Cromo Molibdeno (Co-28Cr-6Mo) + Inserto para Cotilo 09 Pontos Modelos Comerciales: Vástago No Cementado en Titanio Prótesis Femoral MD4 Porous Coated Prótesis Femoral MD4 Plasma Spray Prótesis Femoral EZ-Fit PS Ti Prótesis Femoral PHENM PS Ti Liga de Titanio (Ti-6Al-4V) Cabezas Femorales Intercambiables metálicas Cabeza Femoral Intercambiable Aleación de Acero Inoxidable (18Cr-14Ni-2.5Mo) Cabeza Femoral Intercambiable HN Aleación de Acero Inoxidable (21Cr-10Ni-3Mn-2.5Mo) Cotilos No Cementados Cotilo MD4 Plasma Spray + Inserto para Cotilo 9 Puntos Cotilo MD5 Porous Coated Aleación de Cobalto Cromo Molibdeno (Co-28Cr-6Mo) + Inserto para Cotilo 09 Puntos Modelos Comerciales: Vástago No Cementado en Titanio Prótesis Femoral EZ-Fit PS Ti Prótesis Femoral PHENM PS Ti Cabezas Femorales Intercambiables cerámicas Cabeza Femoral Intercambiable Cerámica Forte Cerámica Alumina (Al 2 3) Cabeza Femoral Intercambiable cerámica Delta Cerámica Alumina (Al 2 3) Cotilos No Cementados Calota MD Acetabular Ti + Inserto para Cotilo Cerámica Delta Cerámica Alumina (Al 2 3) Modelos Comerciales: Vástago No Cementado en Titanio Prótesis Femoral EZ-Fit PS Ti Prótesis Femoral PHENM PS Ti Cabezas Femorales Intercambiables Cabeza Femoral Intercambiable cerámica Forte Cerámica Alumina (Al 2 3) Cabeza Femoral Intercambiable cerámica Delta Cerámica Alumina (Al 2 3)
11 Sistema para Artroplastia Total de Cadera Híbrida Cotilos Cementados Cotilo Máxima (Con o sin espaciador) Aleación de Acero Inoxidable (18Cr-14Ni-2.5Mo) Polimetilmetacrilato (PMMA) Cotilo SPAC NG (Con o sin espaciador) Aleación de Acero Inoxidable (18Cr-14Ni-2.5Mo) Modelos Comerciales: Vástago No Cementado en Titanio Prótesis Femoral MD4 Porous Coated Prótesis Femoral MD4 Plasma Spray Cabezas Femorales Intercambiables Cabeza Femoral Intercambiable Aleación de Acero Inoxidable (18Cr-14Ni-2.5Mo) Cabeza Femoral Intercambiable HN Aleación de Acero Inoxidable (21Cr-10Ni-3Mn-2.5Mo) Cotilos Cementados Cotilo Máxima (Con o sin espaciador) Aleación de Acero Inoxidable (18Cr-14Ni-2.5Mo) Polimetilmetacrilato (PMMA) Cotilo SPAC NG (Con o sin espaciador) Aleación de Acero Inoxidable (18Cr-14Ni-2.5Mo) Modelos Comerciales Vástago No Cementado en Titanio Prótesis Femoral EZ-Fit PS Ti Prótesis Femoral PHENM PS Ti Cabezas Femorales Intercambiables Cabeza Femoral Intercambiable Aleación de Acero Inoxidable (18Cr-14Ni-2.5Mo) Cabeza Femoral Intercambiable HN Aleación de Acero Inoxidable (21Cr-10Ni-3Mn-2.5Mo) Cabeza Femoral Intercambiable Cerámica Forte Cerámica Alumina (Al 2 3) Cabeza Femoral Intercambiable Cerámica Delta Cerámica Alumina (Al 2 3)
12 Imagen Ilustrativa Lista de los componentes ancilares compatibles con los modelos comerciales que componen la familia del Vástago no Cementado en Titanio Cotilo Bipolar Código Descripción Dimensiones Material de Fabricación Cantidad Envasada 04...XXXXX Cotilo Bipolar con Traba Ø 22 mm 32, 34, 36, 38, 40, 42, 44, 46, 48, 50, 52, 54 mm; Ø 26 mm 40, 42, 44, 46, 48, 50, 52, 54, 56 mm; Ø 28 mm 42, 44, 46, 48, 50, 52, 54, 56, 58, 60; Ø 32 mm 42, 44, 46, 48, 50, 52, 54, 56, 58, 60; Polietileno (UHMWPE) Aleación de Acero Inoxidable (18Cr-14Ni-2,5Mo) Cotilos Cementados Imagen Ilustrativa Código Descripción Dimensiones Material de Fabricación Cantidad Envasada XXXXX Cotilo Máxima STD Ø 26 mm 44, 46, 48, 50, 52, 54, 56, 58, 60 mm; Ø 28 mm 44, 46, 48, 50, 52, 54, 56, 58, 60 mm; Polietileno (UHMWPE) Aleación de Acero Inoxidable (18Cr-14Ni-2,5Mo) XXXXX Cotilo Máxima STD c/ Espaciador Ø 26 mm 44, 46, 48, 50, 52, 54, 56, 58, 60 mm. Ø 28 mm 44, 46, 48, 50, 52, 54, 56, 58, 60 mm; Polietileno (UHMWPE) Aleación de Acero Inoxidable (18Cr-14Ni-2,5Mo) Polimetilmetacrilato (PMMA) XXXXX Cotilo Cementado SPAC NG Ø 22 mm 38, 40, 42, 44, 46, 48, 50, 52, 54, 56, 58, 60, 62, 64, 66, 68, 70 mm; Ø 26 mm 42, 44, 46, 48, 50, 52, 54, 56, 58, 60, 62, 64, 66, 68, 70 mm; Ø 28 mm 44, 46, 48, 50, 52, 54, 56, 58, 60, 62, 64, 66, 68, 70 mm; Ø 32 mm 48, 50, 52, 54, 56, 58, 60, 62, 64, 66, 68, 70 mm; Polietileno (UHMWPE) Aleación de Acero Inoxidable (18Cr-14Ni-2,5Mo)
13 XXXXX Cotilo Cementado SPAC NG c/ PMMA Ø 22 mm 40, 42, 44, 46, 48, 50, 52, 54, 56, 58, 60, 62, 64, 66, 68, 70 mm; Ø 26 mm 44, 46, 48, 50, 52, 54, 56, 58, 60, 62, 64, 66, 68, 70 mm; Ø 28 mm 46, 48, 50, 52, 54, 56, 58, 60, 62, 64, 66, 68, 70 mm; Ø 32 mm 50, 52, 54, 56, 58, 60, 62, 64, 66, 68, 70 mm; Polietileno (UHMWPE) Aleación de Acero Inoxidable (18Cr-14Ni-2,5Mo) Polimetilmetacrilato (PMMA) Cotilos No Cementados Imagen Ilustrativa Código Descripción Dimensiones Material de Fabricación Cantidad Envasada XXXXX Cotilo MD4 Plasma Spray Diámetros: 44, 46, 48, 50, 52, 54, 56, 58, 60, 62, 66, 68, 70 mm; (Ti-6Al-4V)/ titanio por aspersión de Plasma Spray XXXXX Cotilo MD5 Porous Coated Diámetros: 44, 46, 48, 50, 52, 54, 56, 58, 60, 62, 66, 68, 70 mm; Aleación de Cobalto (Co-28-6Mo)/ microesferas cobalto (Porous Coated) XXXXX Copa MD Acetabular Ti (con agujeros) XXXXX Copa MD Acetabular Ti (sin agujeros) Diámetros: 46x35 mm; Ø 48x35 mm; 50x37 mm; 52x37 mm; 54x39 mm; 56x41 mm; 58x44 mm; 60x44 mm; 62x48 mm; 64x48 mm; 66x52 mm; 68x52 mm; 70x52 mm; (Ti-6Al-4V)/ titanio por aspersión de Plasma Spray
14 Insertos para Cotilos Imagen Ilustrativa Código Descripción Dimensiones Material de Fabricación Cantidad Envasada XXXXX Inserto p/ Cotilo 09 Puntos Ø 22 mm 44, 46, 48 mm; Ø 26 mm 48, 50, 52, 54, 56, 58, 60, 62 mm; Ø 28 mm 50, 52, 54, 56, 58, 60, 62, 64, 66, 68, 70 mm; Ø 32 mm 54, 56, 58, 60, 62, 64, 66, 68, 70 mm; Polietileno (UHMWPE) XXXXX Inserto p/ Cotilo Cerámica Delta Ø 28 mm A, B; Ø 32 mm C, D, E, F; Ø 36 mm E, F, G; Ø 40 mm F, G; Cerámica Delta Alumina (Al 2 3) Cabezas Intercambiables Femorales Imagen Ilustrativa Código Descripción Dimensiones Material de Fabricación Cantidad Envasada XXXXX Cabeza Femoral Intercambiable Ø 22 mm: -2, Std, +3 mm; Ø 26 mm: -4, -2, Std, +3, +6, + 9 mm; Ø 28 mm: -4, -3.5, -2, Std, +3, +3.5, +6, +9 mm; Ø 32 mm: -4, -2, Std, +3, +4, +6, +7, +9 mm; Aleación de Acero Inoxidable (18Cr-14Ni-2.5Mo) XXXXX Cabeza Femoral Intercambiable HN Ø 22 mm: -2, Std, +3 mm; Ø 26 mm: -4, -2, Std, +3, +6, + 9 mm; Ø 28 mm: -4, -3.5, -2, Std, +3, +3.5, +6, +9 mm; Ø 32 mm: -4, -2, Std, +3, +4, +6, +7, +9 mm; Aleación de Acero Inoxidable c/ Alto Tenor de Nitrógeno (21Cr-10Ni-3Mn- 2.5Mo) XXXXX Cabeza Femoral Intercambiable Cerámica Forte Ø 28 mm: -3,5, Std, +3,5 mm; Ø 32 mm: -4,0, Std, +4,0, +7,0 mm Ø 36 mm: -4,0, Std, +4,0, +8,0 mm Ø 40 mm: -4,0, Std, +4,0, +8,0 mm Cerámica Forte Alumina (Al 2 3) XXXXX Cabeza Femoral Intercambiable Cerámica Delta Ø 28 mm: -3,5, Std, +3,5 mm; Ø 32 mm: -4,0, Std, +4,0, +7,0 mm; Ø 36 mm: -4,0, Std, +4,0, +8,0 mm; Ø 40 mm: -4,0, Std, +4,0, +8,0 mm; Cerámica Delta Alumina (Al 2 3) Los componentes ancilares listados arriba no son objeto de ese proceso de registro, por lo tanto, deben adquirirse por separado y siempre desde el mismo fabricante o de indicado por aquél.
15 Material de Apoyo Los materiales de apoyo son los instrumentales designados únicamente para la implantación del Vástago no Cementado en Titanio y sus respectivos ancilares supracitados. Estos instrumentales son fabricados en acero inoxidable que cumple los requisitos especificados por la norma ASTM F-899 Standard Specification for Stainless Steel for Surgical Instruments, que les proporcionan alta resistencia y durabilidad. Los instrumentales listados a continuación no son objeto de este proceso de registro, debiendo, por lo tanto, adquirirse por separado y siempre del mismo fabricante del implante o de fabricante indicado por aquél. Vea abajo una lista de los instrumentales suministrados por el fabricante o por fabricante indicado por él para la implantación del Vástago No Cementado en Titanio y sus respectivos ancilares: Instrumental Bipolar Instrumental Acetabular Unique (Raspas Nacionales) Instrumental Acetabular Unique (Raspas Importadas) Instrumental Acetabular Unique Next Instrumental MD4 Femoral Instrumental EZ-Fit/ Razor Fit Fijación Proximal Instrumental PHENM Primaria No Cementada Los instrumentales se suministran descontaminados, pero no esterilizados. La esterilización inadecuada del instrumental quirúrgico puede causar infecciones. Los instrumentos quirúrgicos están sujetos a desgaste durante su utilización normal y pueden romperse. Los instrumentales deben utilizarse solamente para los fines a que se destinan, y deben inspeccionarse regularmente para la verificación de posibles desgastes y daños. Para más información acerca del instrumental, consulte al representante. Precauciones y Advertencias Para la utilización del producto, el equipo responsable debe considerar las siguientes advertencias y precauciones: El producto debe ser utilizado tras un análisis detallado del procedimiento quirúrgico a realizar y de la lectura de estas instrucciones de uso; El producto solamente debe ser utilizado por equipos quirúrgicos especializados, con conocimiento y capacitación específica sobre las técnicas de artroplastias, siendo de responsabilidad del cirujano la elección y el dominio de la técnica a aplicar; La selección y elección inadecuada de los implantes a utilizar, así como errores en la indicación, manipulación y técnica de aplicación, pueden provocar tensiones y tracciones excesivas sobre el implante, pudiendo acarrear la falla por fatiga, fractura e inclusive su desprendimiento; Los resultados clínicos y la durabilidad de los implantes dependen extremadamente de una técnica quirúrgica precisa; La implantación bajo lecho óseo inadecuado puede causar aflojamiento prematuro y pérdida progresiva del stock óseo. En esos casos, deben adoptarse métodos suplementarios de injerto óseo en conjunto con mallas y refuerzos; El producto no debe ser utilizado en conjunto con cemento óseo; La utilización en pacientes con predisposición a desobedecer las orientaciones médicas y restricciones postoperatorias, como niños, adultos de edad avanzada, individuos con alteraciones neurológicas o dependientes químicos, representa un riesgo mayor de falla del implante; Los riesgos de falla del implante serán mayores en pacientes que ejerzan actividades de esfuerzo o que practiquen actividades deportivas durante el período postoperatorio, contrariando las restricciones médicas; Las complicaciones postoperatorias representan un riesgo mayor en caso de utilización del producto en pacientes con expectativas funcionales más allá de las que pueden alcanzarse por el reemplazo articular, pacientes con obesidad mórbida y pacientes con osamenta pequeña;
16 El producto y sus respectivos ancilares no deben ser utilizados en caso de que no se obtenga un soporte óseo adecuado que garantice la estabilidad del implante; El paciente debe hacer acompañamiento médico periódico para chequear las condiciones del implante, del hueso y de los tejidos adyacentes; A criterio médico, puede hacerse uso de antibioticoterapia profiláctica pre- y perioperatoria, así como antibioticoterapia en caso de predisposición local y/o sistémica o aparición de infecciones; El implante no debe ser utilizado con componentes de otros fabricantes o finalidad. La combinación de implantes de fabricantes o finalidades distintas puede tener como resultado la incongruencia entre los componentes; Debe observarse rigurosamente la identificación del producto y no se permiten combinaciones con componentes de otros fabricantes o finalidad; Los cuidados con este material son de responsabilidad de personal habilitado, el cual debe seguir las normativas y/o demás reglamentaciones locales aplicables; Las caídas o aplastamiento sobre superficies duras pueden causar daños al producto. De esta forma, es necesario que el usuario realice una inspección, verificando la integridad del producto en el momento de la apertura del envase y, si observa alguna anormalidad, no lo utilice; La apertura del envase para la utilización quirúrgica debe ser realizada por personal habilitado para ese procedimiento; No utilice el producto con el plazo de validez expirado o con el envase violado; Manipule con cuidado; Producto de uso único No reutilizar; Los implantes NUNCA deben ser reutilizados. Aunque puedan parecer en perfectas condiciones, las tensiones previas a que fueron sometidos pueden originar imperfecciones que reducirían el tiempo de vida útil del producto en un reimplante; PRHIBID REPRCESAR; Producto estéril No reesterilizar; Fecha de fabricación, plazo de validez y nº de lote: lea el rótulo. Efectos Adversos Todo procedimiento quirúrgico presenta riesgos y la posibilidad de complicaciones, siendo algunos riesgos comunes: las infecciones, sangrado, reacciones alérgicas medicamentosas y riesgos anestésicos, entre otros. Además, pueden asociarse a la implantación del producto las siguientes complicaciones y efectos adversos: Aflojamiento, dislocación, deformación, fractura del implante u osteólisis; Dolores postoperatorios, incomodidad o sensaciones anormales debido al producto; Reacciones a cuerpo extraño; Reacciones inflamatorias, asociadas o no al aflojamiento y/o desprendimiento del implante; Necrosis ósea o de los tejidos blandos adyacentes; Rotura del implante que pueda tornar su remoción difícil o impracticable. Instrucciones de Uso Para la correcta utilización del producto, deben adoptarse las siguientes instrucciones: Los cuidados con este material son de responsabilidad del personal habilitado, el cual debe seguir las normativas y/o demás reglamentaciones locales aplicables; El producto debe ser manipulado con los debidos cuidados en locales adecuados (centro de materiales y salas de operaciones o quirófanos); El producto solamente debe ser utilizado por equipos quirúrgicos especializados, con conocimiento y capacitación específica sobre las técnicas de artroplastia, siendo de responsabilidad del cirujano la elección y el dominio de la técnica a realizar; A criterio médico, deben adoptarse métodos de injerto óseo (asociados o no a la utilización de mallas y refuerzos) para el restablecimiento del stock óseo, en casos en que no se obtenga una cavidad medular con lecho óseo viable; Es necesario el lavado y secado del cono del vástago antes de la implantación dos demás componentes ancilares, a fin de garantizar que no hay residuo del hueso o de tejido en la junción entre los componentes;
17 El periodo de vida útil establecido para el producto es de 10 (diez) años, desde que los dispositivos sean implantados por medio de una técnica quirúrgica adecuada y se observen las informaciones de los tópicos Indicación y Finalidad, Contraindicaciones, Advertencias y Precauciones e Instrucciones de Uso ; A criterio médico, podrá ser necesaria la realización de la cirugía de revisión una vez pasado el periodo de vida útil, en caso de que se observe el desgaste y/o desprendimiento de componentes; La correcta combinación del producto y sus respectivos componentes ancilares está indicada en el tópico Componentes Ancilares, no debiendo utilizarse, dada la posibilidad de incompatibilidad dimensional y funcional, con otros componentes que no sean los indicados por el fabricante. Para la aplicación del producto y sus respectivos componentes ancilares es necesario el uso de un instrumental específico, indicado en el tópico Material de Apoyo, no siendo permitida, debido a la posibilidad de incompatibilidad dimensional y/o funcional, la utilización de otros instrumentos que no sean los indicados por el fabricante. rientaciones al Paciente y/o al Representante Legal El equipo responsable debe orientar al paciente y/o a su representante legal sobre: Los cuidados adecuados y las restricciones del periodo postoperatorio. La capacidad y la voluntad del paciente de seguir esas orientaciones constituyen uno de los aspectos más importantes en un procedimiento quirúrgico; El hecho de que los riesgos son mayores en caso de utilización en pacientes con predisposición a desobedecer las orientaciones médicas, cuidados y restricciones postoperatorias, como niños, adultos de edad avanzada, individuos con alteraciones neurológicas o dependientes químicos; El hecho de que el producto no suple totalmente el hueso normal ni posee su mismo desempeño y que, por lo tanto, puede romperse, deformarse o desprenderse como consecuencia de esfuerzos o actividades excesivas, de carga precoz y otras situaciones; Todas las restricciones postoperatorias, sobre todo, las relacionadas con las actividades deportivas y ocupacionales; El hecho de que las complicaciones postoperatorias representan un riesgo mayor en caso de utilización del producto en pacientes con expectativas funcionales más allá de las que pueden alcanzarse por la sustitución articular, pacientes con obesidad mórbida y pacientes con osamenta pequeña; La necesidad de utilización, exclusivamente a criterio médico, de soportes externos, ayuda para desplazarse y aparatos ortopédicos, proyectados para limitar movimientos y/o carga; La necesidad de acompañamiento médico periódico para chequear las condiciones del implante, del hueso y de los tejidos adyacentes; El hecho de que la no realización de la cirugía de revisión, en caso de desprendimiento de los componentes, puede tener como resultado la pérdida progresiva del stock óseo; El hecho de que los implantes pueden interferir en los resultados de exámenes por imágenes. De esta forma, portadores de implantes deben informar tal condición en caso de realizarse exámenes de ese tipo; Las complicaciones relativas a los procedimientos de artroplastia de la cadera, así como las informaciones listadas en este tópico rientaciones al Paciente y/o al Representante Legal y en el tópico Efectos Adversos. Esterilización Los modelos comerciales que componen la familia de Vástago No Cementado en Titanio son suministrados en condición de producto estéril. El método adoptado es la esterilización por Radiación Gamma (dosis 25 kgy). La fabricación del producto se realiza con gran cuidado, de modo que se alcance el desempeño pretendido para el producto. De esta forma, el equipo quirúrgico y los demás involucrados deben manipular los dispositivos adecuadamente para minimizar los riesgos de infección. Producto estéril no reesterilizar. No utilice el producto si el envase está violado.
18 Riesgo de Contaminación Por tratarse de un producto implantable, en los casos en que sea necesaria la explantación del producto, existen riesgos de contaminación biológica y transmisión de enfermedades virales. Para minimizar esos riesgos, los componentes explantados deben ser tratados como material potencialmente contaminante, debiéndose adoptar las normativas y/o demás reglamentaciones locales aplicables. Descarte del Producto Los componentes explantados o considerados inadecuados para uso deben ser descartados. Se recomienda que, antes del descarte, el producto sea destruido. Para tanto, las piezas pueden ser cortadas, torcidas o limadas. Los implantes deben ser descartados en locales apropiados, a fin de evitar la contaminación del medioambiente y demás individuos. Se recomienda la adopción de las reglamentaciones legales locales para el descarte de productos potencialmente contaminantes. Producto de uso único no reutilizar Rastreo Para garantizar el rastreo del producto implantado, y cumplir los requisitos de vigilancia sanitaria, el cirujano o su equipo deben registrar en el legajo o historia clínica del paciente las informaciones acerca del producto. Además, esas informaciones deben ser comunicadas al distribuidor del producto y al paciente, de modo que se complete el ciclo de rastreo del producto implantado. Las informaciones necesarias para el rastreo son aquellas relativas al producto utilizado, cirugía y paciente, como sigue abajo: Nombre del paciente que recibió el implante; Nombre del cirujano; Nombre del hospital; Nombre del fabricante; Nombre del abastecedor; Fecha de la cirugía; Código del producto; Número de lote; Cantidades utilizadas; Registro del producto en la ANVISA. El cirujano responsable y su equipo deben hacer uso de las etiquetas de rastreo suministradas en cinco (05) vías en el envase del producto, pegándolas en el legajo o historia clínica del paciente para mantenimiento del rastreo del producto implantado. Además, debe entregarse una de las etiquetas al paciente para que él tenga informaciones acerca del producto implantado en su procedimiento quirúrgico. En las etiquetas, constan los datos del producto, como su código, descripción, lote, registro ANVISA del mismo, entre otras informaciones. Las informaciones de rastreo son necesarias para la notificación por parte del servicio de salud y/o del paciente a la Agencia de Vigilancia Sanitaria ANVISA y al fabricante, en caso de que ocurran eventos adversos graves, para la conducción de las investigaciones correspondientes. Almacenamiento y Transporte Para el almacenamiento, se recomienda local seco y ventilado, sin exposición a la luz, a la humedad o a sustancias contaminantes. Por tratarse de un producto estéril, la humedad y la temperatura del local de almacenamiento deben ser monitoreadas, y esta última mantenida por debajo de los 40ºC. Los implantes no pueden almacenarse directamente sobre el suelo. Por eso, se recomienda la utilización de estantes con una altura mínima de 20 cm.
19 El producto debe mantenerse en sus envases originales hasta el momento de uso, siendo que la apertura del envase para la utilización quirúrgica y manipulación del producto deberá ser realizada por personal habilitado para ese procedimiento. El producto debe ser transportado adecuadamente, evitándose caídas y roces que puedan dañar la estructura y superficie de la pieza. Para información acerca de la fecha de fabricación, plazo de validez y n. de lote: lea el rótulo. tras Informaciones Fabricado y distribuido por: MDT Indústria Comércio Importação e Exportação de Implantes SA Dirección: Av. Brasil, nº Distrito Industrial Rio Claro/SP Brasil CEP: Tel./Fax: (55-19) CNPJ: /00-92 Responsable Técnico: Miguel Lopes Monte Júnior CREA: Registro ANVISA nº.: Revisión: 02 Emisión: 31/03/24 ALERTA INSTRUCCIÓN DE US Estas INSTRUCCINES DE US están disponibles en formato no impreso, disponibles en el la dirección electrónica del fabricante Las INSTRUCCINES DE US están indexadas en el sitio web a través del NUMER REGISTR/ ANVISA y el respectivo NMBRE CMERCIAL del producto, informados en el rótulo del producto adquirido. Todas las INSTRUCCINES DE US disponibles en el sitio web tienen la identificación de la revisión y fecha de emisión del documento. Siendo que el usuario debe estar atento para la correcta versión (revisión y fecha de emisión) del documento en relación a la FECHA DE FABRICACIÓN informada en el rótulo del producto adquirido. Caso sea de interés del usuario, las INSTRUCCINES DE US podrán ser suplidas en formato impreso, sin costo adicional. Siendo que la solicitación de las mismas deberá ser realizada junto al CAP (Canal de Atendimiento al Público) del fabricante, informado en secuencia: Canal de Atendimiento al Público CAP: Teléfono: FAX: Avenida Brasil, 2983 Distrito Industrial CEP: Rio Claro São Paulo Brasil Horario de atendimiento: 8hs a las 17hs, de lunes hasta viernes, excepto días festivos.
Instrucciones de Uso
 Instrucciones de Uso Sistema para Artroplastia de Rodilla Rotaflex Número en el catálogo Clave de los símbolos utilizados en los envases o empaques Producto Estéril Esterilizado por Radiación Gamma XXXX
Instrucciones de Uso Sistema para Artroplastia de Rodilla Rotaflex Número en el catálogo Clave de los símbolos utilizados en los envases o empaques Producto Estéril Esterilizado por Radiación Gamma XXXX
Instrucción de uso. Sistema para Artroplastia de Cadera Híbrido. Clave de los símbolos adoptados en el envase del producto
 Instrucción de uso Sistema para Artroplastia de Cadera Híbrido Clave de los símbolos adoptados en el envase del producto Número en el catálogo Producto Estéril Esterilizado por Radiación Gamma Fecha de
Instrucción de uso Sistema para Artroplastia de Cadera Híbrido Clave de los símbolos adoptados en el envase del producto Número en el catálogo Producto Estéril Esterilizado por Radiación Gamma Fecha de
Instrucciones de Uso
 Instrucciones de Uso Tornillo para Fijación de Ligamento Clave de los símbolos adoptados en la rotulación del producto Número en el catálogo Código de lote Fecha de Fabricación Consultar las instrucciones
Instrucciones de Uso Tornillo para Fijación de Ligamento Clave de los símbolos adoptados en la rotulación del producto Número en el catálogo Código de lote Fecha de Fabricación Consultar las instrucciones
Instrucciones de Uso
 Instrucciones de Uso Universal Bloqueado Claves de los símbolos utilizados en los envases Número en el catálogo Código de lote Fecha de Fabricación Consultar Instrucciones de uso Producto de uso único
Instrucciones de Uso Universal Bloqueado Claves de los símbolos utilizados en los envases Número en el catálogo Código de lote Fecha de Fabricación Consultar Instrucciones de uso Producto de uso único
Instrucciones de Uso
 Instrucciones de Uso Fijador Externo Huesos Cortos I Clave de los Símbolos adoptados en los Envases o Empaques Número en el catálogo Producto Estéril Esterilizado por Radiación Gamma Fecha de Fabricación
Instrucciones de Uso Fijador Externo Huesos Cortos I Clave de los Símbolos adoptados en los Envases o Empaques Número en el catálogo Producto Estéril Esterilizado por Radiación Gamma Fecha de Fabricación
Instrucción de Uso. Clavo de Schanz. Leyendas de la simbología adoptada en el rotulado del producto
 Instrucción de Uso Clavo de Schanz Leyendas de la simbología adoptada en el rotulado del producto Número en el catálogo Producto Estéril Esterilizado por Radiación Gama Fecha de Fabricación Consultar instrucciones
Instrucción de Uso Clavo de Schanz Leyendas de la simbología adoptada en el rotulado del producto Número en el catálogo Producto Estéril Esterilizado por Radiación Gama Fecha de Fabricación Consultar instrucciones
Instrucciones de Uso
 Instrucciones de Uso Tornillo de Interferencia PEEK ÓPTIMA Número de referencia Esterilizado por radiación Clave de los símbolos utilizados en los envases o empaques Código de lote Producto certificado
Instrucciones de Uso Tornillo de Interferencia PEEK ÓPTIMA Número de referencia Esterilizado por radiación Clave de los símbolos utilizados en los envases o empaques Código de lote Producto certificado
Instrucciones de Uso
 Instrucciones de Uso Cofias de Impresión Poliméricas Clave de los símbolos utilizados en los envases o empaques Número en el catálogo Código de lote Fecha de Fabricación Válido hasta Consultar las instrucciones
Instrucciones de Uso Cofias de Impresión Poliméricas Clave de los símbolos utilizados en los envases o empaques Número en el catálogo Código de lote Fecha de Fabricación Válido hasta Consultar las instrucciones
Instrucciones de Uso
 Instrucciones de Uso Sistema Anterior para Columna Cervical C-Lock Clave de los símbolos utilizados en los envases o empaques Código del Producto Código o Número de Lote Fecha de Fabricación Consultar
Instrucciones de Uso Sistema Anterior para Columna Cervical C-Lock Clave de los símbolos utilizados en los envases o empaques Código del Producto Código o Número de Lote Fecha de Fabricación Consultar
Instrucciones de Uso
 Instrucciones de Uso Cilindro CrCo Clave de los símbolos utilizados en los envases o empaques Número en el catálogo Fecha de Fabricación Código de lote Consultar las instrucciones de uso Frágil, manipular
Instrucciones de Uso Cilindro CrCo Clave de los símbolos utilizados en los envases o empaques Número en el catálogo Fecha de Fabricación Código de lote Consultar las instrucciones de uso Frágil, manipular
Instrucciones de Uso. Tornillo Canulado Translaminar Transfacetário MI 360º
 Instrucciones de Uso Tornillo Canulado Translaminar Transfacetário MI 360º Clave de los símbolos utilizados en los envases o empaques Número de referencia Mantener seco No Estéril Fecha de Fabricación
Instrucciones de Uso Tornillo Canulado Translaminar Transfacetário MI 360º Clave de los símbolos utilizados en los envases o empaques Número de referencia Mantener seco No Estéril Fecha de Fabricación
Instrucciones de Uso
 Instrucciones de Uso Cofias de Impresión Clave de los símbolos utilizados en los envases o empaques Número en el catálogo; Código de lote; Fecha de Fabricación; Válido hasta; Consultar las instrucciones
Instrucciones de Uso Cofias de Impresión Clave de los símbolos utilizados en los envases o empaques Número en el catálogo; Código de lote; Fecha de Fabricación; Válido hasta; Consultar las instrucciones
Instrucciones de Uso
 Instrucciones de Uso Tornillo Pedicular Clave de los símbolos utilizados en los envases o empaques Código del Producto Mantener seco Fecha de Fabricación Código o Número de Lote Producto de uso único No
Instrucciones de Uso Tornillo Pedicular Clave de los símbolos utilizados en los envases o empaques Código del Producto Mantener seco Fecha de Fabricación Código o Número de Lote Producto de uso único No
Instrucciones de Uso
 Instrucciones de Uso Sistema para Columna Posterior SAFE Código del Producto Clave de los símbolos utilizados en los envases o empaques Código o Número de Lote Fecha de Fabricación Producto de Uso Único
Instrucciones de Uso Sistema para Columna Posterior SAFE Código del Producto Clave de los símbolos utilizados en los envases o empaques Código o Número de Lote Fecha de Fabricación Producto de Uso Único
Instrucciones de Uso
 Instrucciones de Uso Sistema para Columna Posterior Pedicol Advanced BP Clave de los símbolos utilizados en los envases o empaques Código do Producto Fecha de Fabricación Producto de Uso Único No Estéril
Instrucciones de Uso Sistema para Columna Posterior Pedicol Advanced BP Clave de los símbolos utilizados en los envases o empaques Código do Producto Fecha de Fabricación Producto de Uso Único No Estéril
Instrucciones de Uso. Tornillo de Compresión
 Instrucciones de Uso Tornillo de Compresión Clave de los símbolos utilizados en los envases o empaques Número de catálogo Fecha de Fabricación Frágil, manipular con cuidado Mantener seco No usar si el
Instrucciones de Uso Tornillo de Compresión Clave de los símbolos utilizados en los envases o empaques Número de catálogo Fecha de Fabricación Frágil, manipular con cuidado Mantener seco No usar si el
Instrucciones de Uso
 Instrucciones de Uso Cage Intersomático No Expansivo Peek Óptima STERILE R Número en el catálogo Clave de los símbolos utilizados en los envases o empaques Producto Estéril Esterilizado por Radiación Gamma
Instrucciones de Uso Cage Intersomático No Expansivo Peek Óptima STERILE R Número en el catálogo Clave de los símbolos utilizados en los envases o empaques Producto Estéril Esterilizado por Radiación Gamma
Barra para Tornillo Pedicular
 Instrucciones de Uso Barra para Tornillo Pedicular Clave de los símbolos utilizados en los envases o empaques Código del Producto Evitar la exposición directa a la luz solar Número de Lote Mantener Protegido
Instrucciones de Uso Barra para Tornillo Pedicular Clave de los símbolos utilizados en los envases o empaques Código del Producto Evitar la exposición directa a la luz solar Número de Lote Mantener Protegido
Instrucciones de Uso
 Instrucciones de Uso Hilo para Fijación Ósea Leyendas de los Símbolos Utilizados en los Envases Código del Producto Mantener fuera de la luz solar directa Número de Lote Mantener Protegido de Humedad Material
Instrucciones de Uso Hilo para Fijación Ósea Leyendas de los Símbolos Utilizados en los Envases Código del Producto Mantener fuera de la luz solar directa Número de Lote Mantener Protegido de Humedad Material
Instrucciones del uso
 Instrucciones del uso Caja Intersomática No Expansiva PEEK OPTIMA Legendas dos símbolos utilizados nas embalagens Número em el catálogo Producto Estéril - Esterilizado por Radiación Gamma Fecha de Fabricación
Instrucciones del uso Caja Intersomática No Expansiva PEEK OPTIMA Legendas dos símbolos utilizados nas embalagens Número em el catálogo Producto Estéril - Esterilizado por Radiación Gamma Fecha de Fabricación
INSTRUCCIONES DE USO TORNILLOS PARA MINI Y MICRO FRAGMENTOS
 Página 1 de 17 Fabricado por: Tóride Indústria e Comércio Ltda. EPP. Avenida Caetano Schincariol 97 Parque das Empresas Mogi Mirim-SP Teléfono: + 55 (19) 3862-4037 Fax: + 55 (19) 3862-5858 e-mail: toride@torideimplantes.com.br
Página 1 de 17 Fabricado por: Tóride Indústria e Comércio Ltda. EPP. Avenida Caetano Schincariol 97 Parque das Empresas Mogi Mirim-SP Teléfono: + 55 (19) 3862-4037 Fax: + 55 (19) 3862-5858 e-mail: toride@torideimplantes.com.br
QUE ES LA ARTROPLASTÍA TOTAL DE CADERA
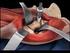 QUE ES LA ARTROPLASTÍA TOTAL DE CADERA Sinónimos: reemplazo total de cadera, sustitución protésica de cadera, prótesis total de cadera, implante total de rodilla La articulación de la cadera también denominada
QUE ES LA ARTROPLASTÍA TOTAL DE CADERA Sinónimos: reemplazo total de cadera, sustitución protésica de cadera, prótesis total de cadera, implante total de rodilla La articulación de la cadera también denominada
1-El cemento óseo puede provocar reacciones adversas importantes como infarto de miocardio, taquicardias, embolia cerebral o respiratoria.
 D-Reacciones 1-El cemento óseo puede provocar reacciones adversas importantes como infarto de miocardio, taquicardias, embolia cerebral o respiratoria. 2-Las reacciones más comunes son: descenso temporal
D-Reacciones 1-El cemento óseo puede provocar reacciones adversas importantes como infarto de miocardio, taquicardias, embolia cerebral o respiratoria. 2-Las reacciones más comunes son: descenso temporal
Instrucciones de Uso
 Instrucciones de Uso Tornillo Deslizante Clave de los símbolos utilizados en los envases o empaques Código del Producto Mantener fuera de la luz solar directa Material SS Código o Número de Lote Consultar
Instrucciones de Uso Tornillo Deslizante Clave de los símbolos utilizados en los envases o empaques Código del Producto Mantener fuera de la luz solar directa Material SS Código o Número de Lote Consultar
Implante monobloque tipo Thompson Aleación metálica cromo-cobalto o titanio Medidas entre 38 y 58 mm. con incrementos de 1 mm.
 PLIEGO DE PRESCRIPCIONES TÉCNICAS QUE HA DE REGIR EN LA CONTRATACIÓN DEL SUMINISTRO DE PROTESIS DE CADERA, MEDIANTE PROCEDIMIENTO ABIERTO Nº 001/2011/3004, CON PLURALIDAD DE CRITERIOS DE VALORACION. 1.
PLIEGO DE PRESCRIPCIONES TÉCNICAS QUE HA DE REGIR EN LA CONTRATACIÓN DEL SUMINISTRO DE PROTESIS DE CADERA, MEDIANTE PROCEDIMIENTO ABIERTO Nº 001/2011/3004, CON PLURALIDAD DE CRITERIOS DE VALORACION. 1.
El suministro se efectuará en el horario y lugar establecido por cada Centro dependiente del SERMAS.
 Ref: 07/865631.9/12 PLIEGO DE PRESCRIPCIONES TÉCNICAS DEL ACUERDO MARCO PARA EL SUMINISTRO DE DIVERSOS PRODUCTOS SANITARIOS (PRÓTESIS DE CADERA Y PRÓTESIS DE RODILLA), CON DESTINO A LOS HOSPITALES DEPENDIENTES
Ref: 07/865631.9/12 PLIEGO DE PRESCRIPCIONES TÉCNICAS DEL ACUERDO MARCO PARA EL SUMINISTRO DE DIVERSOS PRODUCTOS SANITARIOS (PRÓTESIS DE CADERA Y PRÓTESIS DE RODILLA), CON DESTINO A LOS HOSPITALES DEPENDIENTES
Procesos y Controles. Control de Certificados de Calidad de Materia Prima / Análisis Químico. 2. Generación de Órdenes y Documentos de Fabricación
 BP Procesos y Controles 1. Materia Prima: * Proveedores ISO 9000 *A inoxº / quirúrgico / aleaciones especiales *Aleaciones de titanio uso biomédico *Polietileno de ultra alto peso molecular Control de
BP Procesos y Controles 1. Materia Prima: * Proveedores ISO 9000 *A inoxº / quirúrgico / aleaciones especiales *Aleaciones de titanio uso biomédico *Polietileno de ultra alto peso molecular Control de
EXPEDIENTE 242/2015 LOTE Núm.2
 EXPEDIENTE 242/15 LOTE NÚM. 2 : PRÓTESIS DE CADERA: SUBLOTE Nº1 PTC PRIMARIA DE CADERA HIDROXIAPATITA N/CEMENTADA GAE142 GAE143 Vástago femoral titanio /hidroxiapatita en todas sus medidas GAJ032 Cótilo
EXPEDIENTE 242/15 LOTE NÚM. 2 : PRÓTESIS DE CADERA: SUBLOTE Nº1 PTC PRIMARIA DE CADERA HIDROXIAPATITA N/CEMENTADA GAE142 GAE143 Vástago femoral titanio /hidroxiapatita en todas sus medidas GAJ032 Cótilo
ESPECIFICACIONES TÉCNICAS PRÓTESIS. Vº Bº Subdirector de Gestión y SS.GG. Manuel Cuerva García del Castillo
 ESPECIFICACIONES TÉCNICAS PRÓTESIS Vº Bº Subdirector de Gestión y SS.GG. Manuel Cuerva García del Castillo 0 VASTAGO LOTE 1 PROTESIS CADERA CIRUGIA Aleación Titanio PRIMARIA NO CEMENTADA No cementado Morfología
ESPECIFICACIONES TÉCNICAS PRÓTESIS Vº Bº Subdirector de Gestión y SS.GG. Manuel Cuerva García del Castillo 0 VASTAGO LOTE 1 PROTESIS CADERA CIRUGIA Aleación Titanio PRIMARIA NO CEMENTADA No cementado Morfología
Español. Furlong es una prótesis con collar, de vástago recto, fabricada con aleación de titanio Ti-6Al-4V y totalmente recubierta de cerámica de
 Información importante Sistema de RTC H-A.C. Furlong Por favor, lea estas instrucciones antes de utilizar el dispositivo en un emplazamiento clínico. El cirujano debería estar familiarizado con la técnica
Información importante Sistema de RTC H-A.C. Furlong Por favor, lea estas instrucciones antes de utilizar el dispositivo en un emplazamiento clínico. El cirujano debería estar familiarizado con la técnica
CARACTERÍSTICAS TÉCNICAS
 CARACTERÍSTICAS TÉCNICAS LOTE 1: PRÓTESIS TOTAL DE RODILLA Cirugía primaria, cementada y sin cementar Nº ORDEN CODIGO 1 263300 Bandeja tibial Monoblock (bandeja con vástago incorporado) en aleación Cr-Co
CARACTERÍSTICAS TÉCNICAS LOTE 1: PRÓTESIS TOTAL DE RODILLA Cirugía primaria, cementada y sin cementar Nº ORDEN CODIGO 1 263300 Bandeja tibial Monoblock (bandeja con vástago incorporado) en aleación Cr-Co
Aesculap Excia 12/14. Sistema de endoprótesis de cadera. Aesculap Orthopaedics
 Aesculap Excia 12/14 Sistema de endoprótesis de cadera Aesculap Orthopaedics Excia Excelencia en Artroplastia Reims Namur París Nancy Grenoble Aviñón Orthez El sistema de cadera Excia se basa en muchos
Aesculap Excia 12/14 Sistema de endoprótesis de cadera Aesculap Orthopaedics Excia Excelencia en Artroplastia Reims Namur París Nancy Grenoble Aviñón Orthez El sistema de cadera Excia se basa en muchos
Cabezas femorales de cerámica e insertos de cotilos acetabulares. Español
 Información importante Por favor, lea estas instrucciones antes de utilizar el dispositivo en un emplazamiento clínico. El cirujano debería estar familiarizado con la técnica operatoria. Precaución La
Información importante Por favor, lea estas instrucciones antes de utilizar el dispositivo en un emplazamiento clínico. El cirujano debería estar familiarizado con la técnica operatoria. Precaución La
Ortopedia y Traumatología Soluciones innovadoras para Cadera
 Ortopedia y Traumatología Soluciones innovadoras para Cadera Zimmer ZMR (Argentina) Revisión Modular de Cadera El primer objetivo de una revisión de cadera es establecer una fijación, de esta manera se
Ortopedia y Traumatología Soluciones innovadoras para Cadera Zimmer ZMR (Argentina) Revisión Modular de Cadera El primer objetivo de una revisión de cadera es establecer una fijación, de esta manera se
Instrucciones de Uso TORNILLOS DE TITANIO
 Instrucciones de Uso TORNILLOS DE TITANIO Las técnicas para el uso de los Tornillos de Titanio Signo Vinces son altamente especializadas y envuelven procedimientos específicos, que deben ser realizados
Instrucciones de Uso TORNILLOS DE TITANIO Las técnicas para el uso de los Tornillos de Titanio Signo Vinces son altamente especializadas y envuelven procedimientos específicos, que deben ser realizados
Instrucciones de Uso INSTRUMENTAL DE PERFORACIÓN ÓSEA
 Instrucciones de Uso INSTRUMENTAL DE PERFORACIÓN ÓSEA Las técnicas utilizadas para la realización de cirugías con estos Instrumentales de Perforaciones óseas son altamente especializadas y envuelven procedimientos
Instrucciones de Uso INSTRUMENTAL DE PERFORACIÓN ÓSEA Las técnicas utilizadas para la realización de cirugías con estos Instrumentales de Perforaciones óseas son altamente especializadas y envuelven procedimientos
UNIDAD , , , ,00 autobloqueante.
 PLIEGO DE PRESCRIPCIONES TÉCNICAS LOTE DESCRIPCION DE TIPO IGIC TOTAL 2009-2010 (IGIC no incluido) (IGIC incluido) CANTIDAD TOTAL TOTAL (IGIC no incluido) (IGIC incluido) LOTE 1 Prótesis parcial de cadera
PLIEGO DE PRESCRIPCIONES TÉCNICAS LOTE DESCRIPCION DE TIPO IGIC TOTAL 2009-2010 (IGIC no incluido) (IGIC incluido) CANTIDAD TOTAL TOTAL (IGIC no incluido) (IGIC incluido) LOTE 1 Prótesis parcial de cadera
PLIEGO DE BASES TECNICAS / SUMINISTRO DE PROTESIS DE CADERA ARTROPLASTIA PRIMARIA NO CEMENTADA
 PLIEGO DE BASES TECNICAS / SUMINISTRO DE PROTESIS DE CADERA ARTROPLASTIA PRIMARIA NO CEMENTADA LOTE DENOMINACION UND PRECIO UND IMPRTE TOTAL 1 PROTESIS CON REVESTIMIENTO DE HIDROXIAPATITA TOTAL LOTE 217.813,60
PLIEGO DE BASES TECNICAS / SUMINISTRO DE PROTESIS DE CADERA ARTROPLASTIA PRIMARIA NO CEMENTADA LOTE DENOMINACION UND PRECIO UND IMPRTE TOTAL 1 PROTESIS CON REVESTIMIENTO DE HIDROXIAPATITA TOTAL LOTE 217.813,60
Prótesis para Cadera Meta Bio
 Prótesis para Cadera Meta Bio Los primeros registros de reemplazo de articulaciones datan del siglo 19 (1). En el siglo pasado, durante la década de 30, el Dr. Phillip Wiles, médico del Middlesex Hospital,
Prótesis para Cadera Meta Bio Los primeros registros de reemplazo de articulaciones datan del siglo 19 (1). En el siglo pasado, durante la década de 30, el Dr. Phillip Wiles, médico del Middlesex Hospital,
Instrucciones de Uso COMPONENTES PROTÉSICOS BASE METÁLICA
 Instrucciones de Uso COMPONENTES PROTÉSICOS BASE METÁLICA Las técnicas utilizadas para realizar la prótesis sobre implantes son altamente especializadas y envuelven procedimientos específicos, que deben
Instrucciones de Uso COMPONENTES PROTÉSICOS BASE METÁLICA Las técnicas utilizadas para realizar la prótesis sobre implantes son altamente especializadas y envuelven procedimientos específicos, que deben
A N E X O HOSPITAL SAN ELOY -BARAKALDO OBJETO DEL EXPEDIENTE: Adquisición de prótesis de rodilla Nº EXPEDIENTE: G/110/20/1/1 /O651/0000/102013
 A N E X O IV HOSPITAL SAN ELOY -BARAKALDO OBJETO DEL EXPEDIENTE: Adquisición de prótesis de rodilla Nº EXPEDIENTE: G/110/20/1/1 /O651/0000/102013 LOTE/SUBL OTE DESCRIPCIÓN CANTIDAD (UNIDADES) PRECIO UNITARIO
A N E X O IV HOSPITAL SAN ELOY -BARAKALDO OBJETO DEL EXPEDIENTE: Adquisición de prótesis de rodilla Nº EXPEDIENTE: G/110/20/1/1 /O651/0000/102013 LOTE/SUBL OTE DESCRIPCIÓN CANTIDAD (UNIDADES) PRECIO UNITARIO
Instrucciones de Uso COMPONENTES DE TITANIO
 Instrucciones de Uso COMPONENTES DE TITANIO Las técnicas empleadas para la ejecución de la prótesis sobre implantes son altamente especializadas y envuelven procedimientos específicos, que un profesional
Instrucciones de Uso COMPONENTES DE TITANIO Las técnicas empleadas para la ejecución de la prótesis sobre implantes son altamente especializadas y envuelven procedimientos específicos, que un profesional
Acetabulares. H-A.C. Furlong JRI. Español
 Información importante Léase antes de su uso en un emplazamiento clínico. El cirujano debería estar familiarizado con la técnica operatoria. Precaución Leyes federales (EEUU) impiden la venta de este dispositivo
Información importante Léase antes de su uso en un emplazamiento clínico. El cirujano debería estar familiarizado con la técnica operatoria. Precaución Leyes federales (EEUU) impiden la venta de este dispositivo
MANIPULACIÓN DE INSTRUMENTOS PERSONALIZADOS DESECHABLES PROPHECY DE MICROPORT
 ES MANIPULACIÓN DE INSTRUMENTOS PERSONALIZADOS DESECHABLES PROPHECY DE MICROPORT 150807-0 Este paquete incluye los idiomas siguientes: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es)
ES MANIPULACIÓN DE INSTRUMENTOS PERSONALIZADOS DESECHABLES PROPHECY DE MICROPORT 150807-0 Este paquete incluye los idiomas siguientes: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es)
C1250 INSTRUCCIONES DE USO. Formato electrónico
 Formato electrónico INSTRUCCIONES DE USO Los manuales están sujetos a modificaciones; la versión más actualizada de cada manual está siempre disponible en línea. Impreso en: 25 de noviembre de 2015 M PB
Formato electrónico INSTRUCCIONES DE USO Los manuales están sujetos a modificaciones; la versión más actualizada de cada manual está siempre disponible en línea. Impreso en: 25 de noviembre de 2015 M PB
EXACTECH CADERA. Técnica quirúrgica. Vástago recto cementado: Acero inoxidable Cromo cobalto Cotilo de polietileno Cabeza bipolar Cabeza monopolar
 EXACTECH CADERA Técnica quirúrgica Vástago recto cementado: Acero inoxidable Cromo cobalto Cotilo de polietileno Cabeza bipolar Cabeza monopolar ÍNDICE PLANIFICACIÓN PREOPERATORIA... 4 PLANIFICACIÓN PREOPERATORIA
EXACTECH CADERA Técnica quirúrgica Vástago recto cementado: Acero inoxidable Cromo cobalto Cotilo de polietileno Cabeza bipolar Cabeza monopolar ÍNDICE PLANIFICACIÓN PREOPERATORIA... 4 PLANIFICACIÓN PREOPERATORIA
Nuevas tecnologías en cirugía de reemplazo articular de cadera y rodilla
 Nuevas tecnologías en cirugía de reemplazo articular de cadera y rodilla En la actualidad y gracias al continuo desarrollo de implantes, instrumental y técnicas quirúrgicas en el campo de la cirugía de
Nuevas tecnologías en cirugía de reemplazo articular de cadera y rodilla En la actualidad y gracias al continuo desarrollo de implantes, instrumental y técnicas quirúrgicas en el campo de la cirugía de
Soluciones de placas Sistema de placas de bloqueo periarticulares de Zimmer
 Resumen de las características del producto Soluciones de placas Sistema de placas de bloqueo periarticulares de Zimmer Óptima adaptación Trayectoria de los Tornillos Perfil decreciente (de grueso a delgado)
Resumen de las características del producto Soluciones de placas Sistema de placas de bloqueo periarticulares de Zimmer Óptima adaptación Trayectoria de los Tornillos Perfil decreciente (de grueso a delgado)
La Respuesta Biológica a los Implantes Ortopédicos. Profesor: Dr.Federico Angel Rodriguez Dr. Aldo Vilchez Villalobos
 La Respuesta Biológica a los Implantes Ortopédicos Profesor: Dr.Federico Angel Rodriguez Dr. Aldo Vilchez Villalobos Biocompatibilidad Es la capacidad de los materiales para no afectar de manera adversa
La Respuesta Biológica a los Implantes Ortopédicos Profesor: Dr.Federico Angel Rodriguez Dr. Aldo Vilchez Villalobos Biocompatibilidad Es la capacidad de los materiales para no afectar de manera adversa
Sistema de Grandes Fragmentos
 Distribuidor Autorizado Sistema de Grandes Fragmentos Indicaciones Fijación interna de fracturas de húmero, fémur y tibia. Cirugía de revisión de pseudoartrosis, no unión y mal-unión Osteotomías, Artrodesis
Distribuidor Autorizado Sistema de Grandes Fragmentos Indicaciones Fijación interna de fracturas de húmero, fémur y tibia. Cirugía de revisión de pseudoartrosis, no unión y mal-unión Osteotomías, Artrodesis
INSTRUCCIONES DE USO TORNILLOS DE OSTEOSÍNTESIS AUTORROSCANTES
 INSTRUCCIONES DE USO TORNILLOS DE OSTEOSÍNTESIS AUTORROSCANTES Rogamos lean con especial atención las indicaciones descritas a continuación para garantizar la utilización del producto con plena seguridad
INSTRUCCIONES DE USO TORNILLOS DE OSTEOSÍNTESIS AUTORROSCANTES Rogamos lean con especial atención las indicaciones descritas a continuación para garantizar la utilización del producto con plena seguridad
Presupuesto máximo estimado 1 año IVA excluido: ,74
 PLIEGO DE PRESCRIPCIONES TÉCNICAS PARA EL SUMINISTRO DE PRÓTESIS TRAUMATOLÓGICAS DE HOMBRO Y RODILLA PARA LA OSI BILBAO BASURTO C.P. Ref.: G/111/20/1/0750/O621/0000/042014 Presupuesto máximo estimado 1
PLIEGO DE PRESCRIPCIONES TÉCNICAS PARA EL SUMINISTRO DE PRÓTESIS TRAUMATOLÓGICAS DE HOMBRO Y RODILLA PARA LA OSI BILBAO BASURTO C.P. Ref.: G/111/20/1/0750/O621/0000/042014 Presupuesto máximo estimado 1
INTRODUCCIÓN Y OBJETIVOS
 Capítulo 1 INTRODUCCIÓN Y OBJETIVOS 1.1. Motivación El reemplazo total de cadera, conocido también como artroplastia de cadera, es una de las intervenciones más comunes en cirugía ortopédica, y uno de
Capítulo 1 INTRODUCCIÓN Y OBJETIVOS 1.1. Motivación El reemplazo total de cadera, conocido también como artroplastia de cadera, es una de las intervenciones más comunes en cirugía ortopédica, y uno de
INSTRUCCIONES DE UTILIZACIÓN DRENAJES TIMPÁNICOS
 INSTRUCCIONES DE UTILIZACIÓN DRENAJES TIMPÁNICOS Rogamos lean con especial atención las indicaciones descritas a continuación para garantizar la utilización del producto con plena seguridad y adecuadamente.
INSTRUCCIONES DE UTILIZACIÓN DRENAJES TIMPÁNICOS Rogamos lean con especial atención las indicaciones descritas a continuación para garantizar la utilización del producto con plena seguridad y adecuadamente.
El presente pliego técnico recoge los lotes que conforman el Procedimiento de Prótesis de Rodilla y Cadera.
 PLIEGO DE CONDICIONES TÉCNICAS QUE HAN DE REGIR LA CONTRATACIÓN DEL SUMINISTRO DE PRÓTESIS TRAUMATOLÓGICAS PROCEDIMIENTO ABIERTO PARA EL COMPLEJO HOSPITALARIO UNIVERSITARIO DE CANARIAS (HUC CA - ) El presente
PLIEGO DE CONDICIONES TÉCNICAS QUE HAN DE REGIR LA CONTRATACIÓN DEL SUMINISTRO DE PRÓTESIS TRAUMATOLÓGICAS PROCEDIMIENTO ABIERTO PARA EL COMPLEJO HOSPITALARIO UNIVERSITARIO DE CANARIAS (HUC CA - ) El presente
Sustituto de injerto óseo PRO-DENSE Este paquete incluye los idiomas siguientes:
 ES Sustituto de injerto óseo PRO-DENSE 150831-0 Este paquete incluye los idiomas siguientes: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese
ES Sustituto de injerto óseo PRO-DENSE 150831-0 Este paquete incluye los idiomas siguientes: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 - Chinese
CAGE CERVICAL. Técnica Quirúrgica. Cage intersomáticoo para fusión cervical. Fabricación de implantes de columna e implantes dentales en Argentina
 CAGE CERVICAL Cage intersomáticoo para fusión cervical Técnica Quirúrgica Fabricación de implantes de columna e implantes dentales en Argentina Control radiológico con el intensificador de imágenes Advertencia:
CAGE CERVICAL Cage intersomáticoo para fusión cervical Técnica Quirúrgica Fabricación de implantes de columna e implantes dentales en Argentina Control radiológico con el intensificador de imágenes Advertencia:
Sistema de prótesis de cadera TriboFit. Español
 Información importante: Lea antes de utilizar en un entorno clínico. El cirujano debería estar familiarizado con la técnica quirúrgica y con toda la información de este prospecto. Descripción: El Sistema
Información importante: Lea antes de utilizar en un entorno clínico. El cirujano debería estar familiarizado con la técnica quirúrgica y con toda la información de este prospecto. Descripción: El Sistema
XVI REUNION INTERNACIONAL SOCIEDAD MEXICANA DE CIRUGIA DE CADERA BIOTECNOLOGIA EN CIRUGIA DE CADERA
 XVI REUNION INTERNACIONAL SOCIEDAD MEXICANA DE CIRUGIA DE CADERA BIOTECNOLOGIA EN CIRUGIA DE CADERA PROFESORES INTERNACIONALES España España Ing. Ricardo Heros Alemania PROFESORES NACIONALES Dr. Edwin
XVI REUNION INTERNACIONAL SOCIEDAD MEXICANA DE CIRUGIA DE CADERA BIOTECNOLOGIA EN CIRUGIA DE CADERA PROFESORES INTERNACIONALES España España Ing. Ricardo Heros Alemania PROFESORES NACIONALES Dr. Edwin
Sistema de prótesis de cadera TriboFit. Español
 Información importante: Lea antes de utilizar en un entorno clínico. El cirujano debería estar familiarizado con la técnica quirúrgica y con toda la información de este prospecto. Descripción: El Sistema
Información importante: Lea antes de utilizar en un entorno clínico. El cirujano debería estar familiarizado con la técnica quirúrgica y con toda la información de este prospecto. Descripción: El Sistema
SISTEMA ESTABILIZACIÓN DINÁMICA DYNESYS
 SISTEMA ESTABILIZACIÓN DINÁMICA DYNESYS Fabricante Zimmer GMBH Unidad de producción Sulzer-Allee 8 CH-8404 Wintherthur, Suiza Recomendación de uso Estabilización dinámica posterior Composición -Tornillos
SISTEMA ESTABILIZACIÓN DINÁMICA DYNESYS Fabricante Zimmer GMBH Unidad de producción Sulzer-Allee 8 CH-8404 Wintherthur, Suiza Recomendación de uso Estabilización dinámica posterior Composición -Tornillos
PLIEGO DE ESPECIFICACIONES TECNICAS
 PLIEGO DE ESPECIFICACIONES TECNICAS LOTE Nº ORDEN CÓDIGO ARTÍCULO ESPECIFICACIONES TÉCNICAS 1 PROTESIS DE HOMBRO PARA TRAUMATOLOGIA SISTEMA MODULAR DE ARTROPLASTIA DE HOMBRO PARA SU IMPLANTACION EN FRACTURAS
PLIEGO DE ESPECIFICACIONES TECNICAS LOTE Nº ORDEN CÓDIGO ARTÍCULO ESPECIFICACIONES TÉCNICAS 1 PROTESIS DE HOMBRO PARA TRAUMATOLOGIA SISTEMA MODULAR DE ARTROPLASTIA DE HOMBRO PARA SU IMPLANTACION EN FRACTURAS
EXACTECH RODILLA. Técnica quirúrgica. Espaciador tibial proximal (PTS) Anexo a las técnicas quirúrgicas Optetrak CR/PS y revisión de Tibia
 EXACTECH RODILLA Técnica quirúrgica Espaciador tibial proximal () Anexo a las técnicas quirúrgicas Optetrak CR/PS y revisión de Tibia ÍNDICE INTRODUCCIÓN...3 ESPECIFICACIONES DE DISEÑO...3 COMPATIBILIDAD
EXACTECH RODILLA Técnica quirúrgica Espaciador tibial proximal () Anexo a las técnicas quirúrgicas Optetrak CR/PS y revisión de Tibia ÍNDICE INTRODUCCIÓN...3 ESPECIFICACIONES DE DISEÑO...3 COMPATIBILIDAD
PLIEGO DE BASES TÉCNICAS G/110/80/1/0943/O141/0000/062014
 DEBAGOIENEKO ERAKUNDE SANITARIO INTEGRATUA ORGANIZACION SANITARIA INTEGRADA ALTO DEBA PLIEGO DE BASES TÉCNICAS G/110/80/1/0943/O141/0000/062014 1.- OBJETO: Mediante esta contratación se pretende cubrir
DEBAGOIENEKO ERAKUNDE SANITARIO INTEGRATUA ORGANIZACION SANITARIA INTEGRADA ALTO DEBA PLIEGO DE BASES TÉCNICAS G/110/80/1/0943/O141/0000/062014 1.- OBJETO: Mediante esta contratación se pretende cubrir
EXACTECH HOMBRO. Técnica quirúrgica. Prótesis de hombro inverso Implantes aumentados. Surgeon focused. Patient driven. TM
 EXACTECH HOMBRO Técnica quirúrgica Prótesis de hombro inverso Implantes aumentados Surgeon focused. Patient driven. TM ÍNDICE INTRODUCCIÓN... 2 ESPECIFICACIONES DEL SISTEMA... 3 PLACA GLENOIDEA CON AUMENTO
EXACTECH HOMBRO Técnica quirúrgica Prótesis de hombro inverso Implantes aumentados Surgeon focused. Patient driven. TM ÍNDICE INTRODUCCIÓN... 2 ESPECIFICACIONES DEL SISTEMA... 3 PLACA GLENOIDEA CON AUMENTO
EXPEDIENTE Nº G/111/20/1/0977/O301/0000/ OBJETO: PRÓTESIS DE CADERA PLIEGO DE BASES TECNICAS
 EXPEDIENTE Nº G/111/20/1/0977/O301/0000/072012 OBJETO: PRÓTESIS DE CADERA PLIEGO DE BASES TECNICAS LOTE 1.1.- PROTESIS DE CADERA CEMENTADA TIPO OHST - Vástago de titanio super pulido para cementar (12
EXPEDIENTE Nº G/111/20/1/0977/O301/0000/072012 OBJETO: PRÓTESIS DE CADERA PLIEGO DE BASES TECNICAS LOTE 1.1.- PROTESIS DE CADERA CEMENTADA TIPO OHST - Vástago de titanio super pulido para cementar (12
Instrucciones de uso. Sistema de Placas y Tornillos para Buco Maxilo-Facial. Leyenda de los símbolos en los envases o empaques
 Instrucciones de uso Sistema de Placas y Tornillos para Buco Maxilo-Facial Leyenda de los símbolos en los envases o empaques Número de referencia Mantener alejado de la luz solar Material Código do lote
Instrucciones de uso Sistema de Placas y Tornillos para Buco Maxilo-Facial Leyenda de los símbolos en los envases o empaques Número de referencia Mantener alejado de la luz solar Material Código do lote
El implante que se entregará, tendrá la misma referencia y volumen del que se está remplazando.
 Política del Programa de Reposición Premium de BellaGel Que esperar del Programa de Reposición Premium de BellaGel: En caso de ruptura de un implante mamario BellaGel, causada por un defecto de fabricación,
Política del Programa de Reposición Premium de BellaGel Que esperar del Programa de Reposición Premium de BellaGel: En caso de ruptura de un implante mamario BellaGel, causada por un defecto de fabricación,
MATERIAL DE OSTEOSÍNTESIS Y ENDOPRÓTESIS PRECIOS DE REFERENCIA PARA EL SUMINISTRO DEL SERVICIO
 MATERIAL DE OSTEOSÍNTESIS Y ENDOPRÓTESIS PRECIOS DE REFERENCIA PARA EL SUMINISTRO DEL SERVICIO 2013-2014 CONCEPTO Agujas para hueso, tipo Kirschner, no roscado con punta de trocar. Diámetro de 1.0 mm a
MATERIAL DE OSTEOSÍNTESIS Y ENDOPRÓTESIS PRECIOS DE REFERENCIA PARA EL SUMINISTRO DEL SERVICIO 2013-2014 CONCEPTO Agujas para hueso, tipo Kirschner, no roscado con punta de trocar. Diámetro de 1.0 mm a
HUMELOCK INVERTIDA PRESS FIT O CEMENTABLE BLOQUEABLE
 HUMELOCK INVERTIDA PRESS FIT O CEMENTABLE BLOQUEABLE 1 TABLA DE CONTENIDOS 1. PARTE HUMERAL Sin pruebas Polietileno humeral Parte epifisaria Diseño adaptado para farcturas Bloqueable o cementable Jaula
HUMELOCK INVERTIDA PRESS FIT O CEMENTABLE BLOQUEABLE 1 TABLA DE CONTENIDOS 1. PARTE HUMERAL Sin pruebas Polietileno humeral Parte epifisaria Diseño adaptado para farcturas Bloqueable o cementable Jaula
Grapas. Figura 1 Modelo de grapas Astrolabe.
 Grapas 1. Fabricante ASTROLABE Fabrico de implantes Médicos R. José Gomes Ferreira, 2 Armazém 1 2660-517 São Julião do Tojal Portugal 2. Presentación e indicaciones Clínicas Las grapas (staples) se presentan
Grapas 1. Fabricante ASTROLABE Fabrico de implantes Médicos R. José Gomes Ferreira, 2 Armazém 1 2660-517 São Julião do Tojal Portugal 2. Presentación e indicaciones Clínicas Las grapas (staples) se presentan
Instrucciones de Uso IMPLANTE DENTARIO SIGNO VINCES
 Instrucciones de Uso IMPLANTE DENTARIO SIGNO VINCES Este dispositivo médico de implante requiere procedimientos específicos y altamente especializados. Solamente deberá ser realizado por cirujanos dentistas
Instrucciones de Uso IMPLANTE DENTARIO SIGNO VINCES Este dispositivo médico de implante requiere procedimientos específicos y altamente especializados. Solamente deberá ser realizado por cirujanos dentistas
MANIPULACIÓN DE INSTRUMENTOS PERSONALIZADOS DESECHABLES PROPHECY DE MICROPORT Este paquete incluye los idiomas siguientes:
 ES MANIPULACIÓN DE INSTRUMENTOS PERSONALIZADOS DESECHABLES PROPHECY DE MICROPORT 150807-1 Español (esfr) Este paquete incluye los idiomas siguientes: Para otros idiomas, visite nuestro sitio web en www.ortho.microport.com
ES MANIPULACIÓN DE INSTRUMENTOS PERSONALIZADOS DESECHABLES PROPHECY DE MICROPORT 150807-1 Español (esfr) Este paquete incluye los idiomas siguientes: Para otros idiomas, visite nuestro sitio web en www.ortho.microport.com
ANEXO 2 DESCRIPCIÓN DE LOS BIENES, CANTIDAD, PRECIO Y CARACTERISTICAS
 ANEXO 2 DESCRIPCIÓN DE LOS BIENES, CANTIDAD, PRECIO Y CARACTERISTICAS Delegac. Clave presupuestal 18 Morelos 180112072151 HGRMF 1 Unidad médica Localidad Zona Sist. Plan de Ayala 4 12 18 Morelos 181103022151
ANEXO 2 DESCRIPCIÓN DE LOS BIENES, CANTIDAD, PRECIO Y CARACTERISTICAS Delegac. Clave presupuestal 18 Morelos 180112072151 HGRMF 1 Unidad médica Localidad Zona Sist. Plan de Ayala 4 12 18 Morelos 181103022151
Bruno Meola Gioia Telefono: (574) Celulares: (57) (57) Medellin - Colombia
 Bruno Meola Gioia Telefono: (574) 2664207 Celulares: (57) 311 7999997 (57) 311 6356743 Medellin - Colombia meolagbruno@hotmail.com Versatilidad y múltiples opciones de montajes. Rótulas universales para
Bruno Meola Gioia Telefono: (574) 2664207 Celulares: (57) 311 7999997 (57) 311 6356743 Medellin - Colombia meolagbruno@hotmail.com Versatilidad y múltiples opciones de montajes. Rótulas universales para
RECEPCIÓN TECNICA Y VERIFICACIÓN DE DISPOSITIVOS MEDICOS
 RECEPCIÓN TECNICA Y VERIFICACIÓN DE DISPOSITIVOS MEDICOS POR: DIANA P. LONDOÑO RIVERA QUIMICA FARMACEUTICA UNIVERSIDAD DE ANTIOQUIA Su Apoyo Farmacéutico Integral Es responsabilidad de todos los funcionarios
RECEPCIÓN TECNICA Y VERIFICACIÓN DE DISPOSITIVOS MEDICOS POR: DIANA P. LONDOÑO RIVERA QUIMICA FARMACEUTICA UNIVERSIDAD DE ANTIOQUIA Su Apoyo Farmacéutico Integral Es responsabilidad de todos los funcionarios
PLIEGO DE PRESCRIPCIONES TÉCNICAS Nº EXPEDIENTE: PA 60/2011 ADQUISICION DE PROTESIS DE RODILLA EN EL H.U. SEVERO OCHOA
 PLIEGO DE PRESCRIPCIONES TÉCNICAS Nº EXPEDIENTE: PA 60/2011 ADQUISICION DE PROTESIS DE RODILLA EN EL H.U. SEVERO PLIEGO DE PRESCRIPCIONES TÉCNICAS QUE HA DE REGIR LA CONTRATACIÓN DE ADQUISICION DE PROTESIS
PLIEGO DE PRESCRIPCIONES TÉCNICAS Nº EXPEDIENTE: PA 60/2011 ADQUISICION DE PROTESIS DE RODILLA EN EL H.U. SEVERO PLIEGO DE PRESCRIPCIONES TÉCNICAS QUE HA DE REGIR LA CONTRATACIÓN DE ADQUISICION DE PROTESIS
ET445 Amarre preformado para cable cubierto de 15 kv y 34.5 kv
 ET445 Amarre preformado para cable cubierto de 15 kv y 34.5 kv ESPECIFICACIÓN TÉCNICA Elaborado por: Dpto Planificacion e Ingenieria de MT Revisado por: Dpto Planificacion e Ingenieria de MT Revisión #:
ET445 Amarre preformado para cable cubierto de 15 kv y 34.5 kv ESPECIFICACIÓN TÉCNICA Elaborado por: Dpto Planificacion e Ingenieria de MT Revisado por: Dpto Planificacion e Ingenieria de MT Revisión #:
Hospital Ramón y Cajal
 CARACTERÍSTICAS TÉCNICAS DE CLAVOS OSTEOSÍNTESIS (TRAUMATOLOGÍA) 1 CLAVO CADERA TIPO GAMMA Sistema de enclavado intramedular con bloqueo para fracturas proximales (intertrocantéreas, pertrocantéreas y
CARACTERÍSTICAS TÉCNICAS DE CLAVOS OSTEOSÍNTESIS (TRAUMATOLOGÍA) 1 CLAVO CADERA TIPO GAMMA Sistema de enclavado intramedular con bloqueo para fracturas proximales (intertrocantéreas, pertrocantéreas y
FICHA TECNICA PLEXUR P
 COM-24 V.1 FICHA TECNICA PLEXUR P GENERALIDADES INVIMA 2007 DM-0000733 DERIVADO DE DONANTES VOLUNTARIOS CADAVERICOS CADA UNIDAD ESTÁ INDICADA PARA UN ÚNICO PACIENTE Y UN ÚNICO USO DESCRIPCION DEL PRODUCTO
COM-24 V.1 FICHA TECNICA PLEXUR P GENERALIDADES INVIMA 2007 DM-0000733 DERIVADO DE DONANTES VOLUNTARIOS CADAVERICOS CADA UNIDAD ESTÁ INDICADA PARA UN ÚNICO PACIENTE Y UN ÚNICO USO DESCRIPCION DEL PRODUCTO
norma española UNE-EN ISO EXTRACTO DEL DOCUMENTO UNE-EN ISO Dispositivos de seguridad para la protección contra la presión excesiva
 norma española UNE-EN ISO 4126-2 Septiembre 2003 TÍTULO Dispositivos de seguridad para la protección contra la presión excesiva Parte 2: Dispositivos de seguridad con disco de ruptura (ISO 4126-2:2003)
norma española UNE-EN ISO 4126-2 Septiembre 2003 TÍTULO Dispositivos de seguridad para la protección contra la presión excesiva Parte 2: Dispositivos de seguridad con disco de ruptura (ISO 4126-2:2003)
Sistema de extracción de cotilo acetabular Explant. Técnica Quirúrgica
 Sistema de extracción de cotilo acetabular Explant Técnica Quirúrgica Técnica quirúrgica del Sistema de extracción de cotilo acetabular Explant 1 Minimiza la pérdida ósea acetabular La disección ósea
Sistema de extracción de cotilo acetabular Explant Técnica Quirúrgica Técnica quirúrgica del Sistema de extracción de cotilo acetabular Explant 1 Minimiza la pérdida ósea acetabular La disección ósea
Proposición técnica PRÓTESIS DE HOMBRO Y CODO P1107 P1109 P1110 P2107 P2108 P3107 P Julio 2015 Página. Concurso Nº
 31. Julio 2015 1 Concurso Nº 16SM0035P PRÓTESIS DE HOMBRO Y CODO Cód. Lote Descripción P1107 P1109 P1110 P2107 P2108 P3107 P5110 PRÓTESIS DE HOMBRO PRÓTESIS HOMBRO INVERTIDA SIN VÁSTAGO PROTESIS FRACTURAS
31. Julio 2015 1 Concurso Nº 16SM0035P PRÓTESIS DE HOMBRO Y CODO Cód. Lote Descripción P1107 P1109 P1110 P2107 P2108 P3107 P5110 PRÓTESIS DE HOMBRO PRÓTESIS HOMBRO INVERTIDA SIN VÁSTAGO PROTESIS FRACTURAS
Sistema de placas para fijación de calcáneo ORTHOLOC Este paquete incluye los idiomas siguientes:
 ES Español (es) Sistema de placas para fijación de calcáneo ORTHOLOC 147998-0 Este paquete incluye los idiomas siguientes: Para otros idiomas, visite nuestra página Web, en la dirección www.wmt.com. A
ES Español (es) Sistema de placas para fijación de calcáneo ORTHOLOC 147998-0 Este paquete incluye los idiomas siguientes: Para otros idiomas, visite nuestra página Web, en la dirección www.wmt.com. A
RELLENO DE HUECO ÓSEO OSTEOSET XR Los siguientes idiomas se incluyen en este paquete:
 ES RELLENO DE HUECO ÓSEO OSTEOSET XR 150841-0 Los siguientes idiomas se incluyen en este paquete: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 -
ES RELLENO DE HUECO ÓSEO OSTEOSET XR 150841-0 Los siguientes idiomas se incluyen en este paquete: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) 中文 -
SISTEMA DE VIGILANCIA DE PRODUCTOS SANITARIOS RESPONSABLE DE VIGILANCIA DE PRODUCTOS SANITARIOS. Jornada Tecnología Sanitaria Barcelona 9 octubre 2015
 Jornada Tecnología Sanitaria Barcelona 9 octubre 2015 SISTEMA DE VIGILANCIA DE PRODUCTOS SANITARIOS RESPONSABLE DE VIGILANCIA DE PRODUCTOS SANITARIOS Mª Carmen Abad Luna Jefe del Departamento de Productos
Jornada Tecnología Sanitaria Barcelona 9 octubre 2015 SISTEMA DE VIGILANCIA DE PRODUCTOS SANITARIOS RESPONSABLE DE VIGILANCIA DE PRODUCTOS SANITARIOS Mª Carmen Abad Luna Jefe del Departamento de Productos
Información para el paciente Sobre la prótesis de disco intervertebral Prodisc -C para la columna cervical.
 Información para el paciente Sobre la prótesis de disco intervertebral Prodisc -C para la columna cervical. Tareas y funciones de la columna vertebral Estabilidad La columna vertebral sirve principalmente
Información para el paciente Sobre la prótesis de disco intervertebral Prodisc -C para la columna cervical. Tareas y funciones de la columna vertebral Estabilidad La columna vertebral sirve principalmente
Cementless Hip System
 Cementless Hip System www.arzzt.com Técnicas ARZZT Cementless Hip System DESCRIPCIÓN DEL PRODUCTO Copa Acetabular Metálica No Cementada Copa de polipropileno no cementada Vástago femoral no cementado Instrumental
Cementless Hip System www.arzzt.com Técnicas ARZZT Cementless Hip System DESCRIPCIÓN DEL PRODUCTO Copa Acetabular Metálica No Cementada Copa de polipropileno no cementada Vástago femoral no cementado Instrumental
SISTEMA TOTAL DE HOMBRO Los siguientes idiomas se incluyen en este paquete:
 ES SISTEMA TOTAL DE HOMBRO 126399-5 Los siguientes idiomas se incluyen en este paquete: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) - Chinese (sch)
ES SISTEMA TOTAL DE HOMBRO 126399-5 Los siguientes idiomas se incluyen en este paquete: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português (pt) - Chinese (sch)
Instrucciones de Uso COMPONENTE PATELAR. Leyenda de los Símbolos Utilizados em los envases
 Instrucciones de Uso COMPONENTE PATELAR Material UHMWPE Leyenda de los Símbolos Utilizados em los envases Código del Producto Numero de Lote Lea las Instrucciones de uso Polietileno Peso Molecular Ultra
Instrucciones de Uso COMPONENTE PATELAR Material UHMWPE Leyenda de los Símbolos Utilizados em los envases Código del Producto Numero de Lote Lea las Instrucciones de uso Polietileno Peso Molecular Ultra
1.4 AGUJAS DE KISRSCHNER
 1.4 AGUJAS DE KIRSCHNER AGUJAS DE KISRSCHNER Antes de utilizar el producto La funcionalidad de los implantes y los instrumentos para operar deberán ser comprobados cuidadosamente antes de cada uso. No
1.4 AGUJAS DE KIRSCHNER AGUJAS DE KISRSCHNER Antes de utilizar el producto La funcionalidad de los implantes y los instrumentos para operar deberán ser comprobados cuidadosamente antes de cada uso. No
SISTEMA TOTAL DE TOBILLO INBONE CON DIÁFISIS CALCÁNEA Los siguientes idiomas se incluyen en este paquete:
 ES SISTEMA TOTAL DE TOBILLO INBONE CON DIÁFISIS CALCÁNEA 142742-2 Los siguientes idiomas se incluyen en este paquete: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it)
ES SISTEMA TOTAL DE TOBILLO INBONE CON DIÁFISIS CALCÁNEA 142742-2 Los siguientes idiomas se incluyen en este paquete: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it)
Los siguientes idiomas se incluyen en este paquete:
 ES SISTEMA DE ANCLAJE DE SUTURA G-FORCE PEEK-OPTIMA 144880-0 Los siguientes idiomas se incluyen en este paquete: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português
ES SISTEMA DE ANCLAJE DE SUTURA G-FORCE PEEK-OPTIMA 144880-0 Los siguientes idiomas se incluyen en este paquete: English (en) Deutsch (de) Nederlands (nl) Français (fr) Español (es) Italiano (it) Português
SISTEMA DE PLACAS DE HUESOS PEQUEÑOS ORTHOLOC 3Di Los siguientes idiomas se incluyen en este paquete:
 ES SISTEMA DE PLACAS DE HUESOS PEQUEÑOS ORTHOLOC 3Di 153464-00 Los siguientes idiomas se incluyen en este paquete: Para otros idiomas, visite nuestro sitio web www.wright.com y haga clic en la opción Prescribing
ES SISTEMA DE PLACAS DE HUESOS PEQUEÑOS ORTHOLOC 3Di 153464-00 Los siguientes idiomas se incluyen en este paquete: Para otros idiomas, visite nuestro sitio web www.wright.com y haga clic en la opción Prescribing
Soluciones de placas Sistema de placas de bloqueo poliaxial NCB
 Resumen de las características del producto Soluciones de placas Sistema de placas de bloqueo poliaxial Diseño innovador de la placa Poliaxialidad Tipos de tornillos Instrumental MIS Libertad de elección
Resumen de las características del producto Soluciones de placas Sistema de placas de bloqueo poliaxial Diseño innovador de la placa Poliaxialidad Tipos de tornillos Instrumental MIS Libertad de elección
Instrucción de Uso. Instrumentos Quirúrgicos para Implantes Ortopédicos
 Instrucción de Uso Instrumentos Quirúrgicos para Implantes Ortopédicos Legenda de los símbolos utilizados en embalajes Número en el catálogo Código de lote Fecha de Fabricación Consultar las instrucciones
Instrucción de Uso Instrumentos Quirúrgicos para Implantes Ortopédicos Legenda de los símbolos utilizados en embalajes Número en el catálogo Código de lote Fecha de Fabricación Consultar las instrucciones
PLIEGO DE PRESCRIPCIONES TÉCNICAS PARA LA ADQUISICION DE MATERIAL PARA PRÓTESIS DE TRAUMATOLOGÍA DEL HOSPITAL UNIVERSITARIO DE CEUTA.
 PLIEGO DE PRESCRIPCIONES TÉCNICAS PARA LA ADQUISICION DE MATERIAL PARA PRÓTESIS DE TRAUMATOLOGÍA DEL HOSPITAL UNIVERSITARIO DE CEUTA. Las condiciones establecidas en el presente pliego de prescripciones
PLIEGO DE PRESCRIPCIONES TÉCNICAS PARA LA ADQUISICION DE MATERIAL PARA PRÓTESIS DE TRAUMATOLOGÍA DEL HOSPITAL UNIVERSITARIO DE CEUTA. Las condiciones establecidas en el presente pliego de prescripciones
2. DENOMINACIÓN DEL MATERIAL, CARACTERÍSTICAS E IMPORTES DE LICITACIÓN Denominación e importe de los lotes
 PLIEGO DE PRESCRIPCIONES TÉCNICAS PARA EL SUMINISTRO DE PROTESIS DE TRAUMATOLOGIA CON DESTINO A LA AGENCIA PÚBLICA EMPRESARIAL SANITARIA HOSPITAL DE PONIENTE DE CONTENIDO 1. OBJETO DEL CONTRATO. 2. DENOMINACIÓN
PLIEGO DE PRESCRIPCIONES TÉCNICAS PARA EL SUMINISTRO DE PROTESIS DE TRAUMATOLOGIA CON DESTINO A LA AGENCIA PÚBLICA EMPRESARIAL SANITARIA HOSPITAL DE PONIENTE DE CONTENIDO 1. OBJETO DEL CONTRATO. 2. DENOMINACIÓN
Hospital Ramón y Cajal
 CARACTERÍSTICAS TÉCNICAS DE CLAVOS OSTEOSÍNTESIS (TRAUMATOLOGÍA) 1 CLAVO CADERA TIPO GAMMA Sistema de enclavado intramedular con bloqueo para fracturas proximales (intertrocantéreas, pertrocantéreas y
CARACTERÍSTICAS TÉCNICAS DE CLAVOS OSTEOSÍNTESIS (TRAUMATOLOGÍA) 1 CLAVO CADERA TIPO GAMMA Sistema de enclavado intramedular con bloqueo para fracturas proximales (intertrocantéreas, pertrocantéreas y
