MINISTERIO DE SALUD PÚBLICA DEPARTAMENTO DE FARMACOEPIDEMIOLOGIA UNIDAD COORDINADORA NACIONAL DE FARMACOVIGILANCIA INFORME ANUAL
|
|
|
- Vicenta Quintana Piñeiro
- hace 5 años
- Vistas:
Transcripción
1 MINISTERIO DE SALUD PÚBLICA DEPARTAMENTO DE FARMACOEPIDEMIOLOGIA UNIDAD COORDINADORA NACIONAL DE FARMACOVIGILANCIA INFORME ANUAL 2010 Durante el año 2010 se recibieron notificaciones de reacciones adversas medicamentosas (RAM), notificándose RAM a razón de 1.8 RAM por notificación, de ellas 7737 fueron importantes para un 57.7% (según criterios para determinar RAM importantes de la UCNFv, en las Normas y procedimientos de trabajo del Sistema cubano de Farmacovigilancia. La tasa de notificación anual fue de 1194 notificaciones por millón de habitantes. La tasa de notificación continúa siendo mayor de 600 reportes por millón de habitantes, lo cual es un indicador importante para los centros nacionales. Este aumento notable de la tasa de reporte en el presente año se debe a que se han incorporado al sistema resultados de estudios de vigilancia activa de productos, como el oseltamivir y las vacunas preventivas. Además se han incluido los resultados de más de seis tesis de terminación de Maestría en Farmacoepidemiología, siendo en su totalidad estudios prospectivos. La tabla 1 muestra las notificaciones procesadas en sistema de farmacovigilancia nacional en el período Tabla 1: Total de notificaciones y tasa de notificación anual. Años Año No reportes Tasa reporte anual x x x x x x En la tabla 2 se observa el comportamiento de las notificaciones en el año según grupos de edades. Tabla 2: Distribución de notificaciones por grupos de edades. Año 2010 Grupo de edad Notificaciones % Pediatría Adultos Geriatría
2 Las provincias que tuvieron mayor tasa de notificación en este año fueron: Villa Clara (35,6 x habitantes/año), Granma (31,0 x habitantes/año), Holguín (23,9 x habitantes/año), Sancti Spiritus (19,7 x habitantes/año), Las Tunas (14,7 x habitantes/año), Camaguey (13,2 x habitantes/año) y Matanzas (10,2 x habitantes/año). Los municipios que más reportaron durante este año fueron: Holguín (1331), Bayazo (996), Manzanillo (846), Camaguey (786) y Santa Clara (682). La distribución por sexo sigue igual comportamiento que años anteriores, siendo el sexo femenino el más relacionado con sospechas de efectos adversos (8780 notificaciones, 65.4%), mientras que el sexo masculino estuvo menos afectado (4638 notificaciones, 34.6%). Se mantiene el patrón de notificación de los cinco años anteriores, siendo los más notificados los adultos, y el sexo femenino. El nivel de atención que más reportes realiza es APS (10622, 79.2%), la AS reportó en un 20.2% (2715 reportes en el año y el tercer nivel de atención alcanzó un 0.6% (81 casos). El indicador de porcentaje de reporte en la atención secundaria de salud, se alcanza este año por primera vez, en el que se ha superado el 20% de notificaciones, en este importante nivel de atención de salud. Se mantuvo como método de trabajo en el periodo la combinación de métodos pasivos y activos de farmacovigilancia. En cuanto a los especialistas que notifican los médicos (7195, 53.6%) siguen siendo los que más reportan, aunque se nota el aumento del reporte por otros profesionales, le siguen en orden de importancia los licenciados en enfermería (2687, 20.0%), los licenciados en farmacia (2432, 18.1%), los técnicos en farmacia (419, 3.1%) y los técnicos en enfermería (410, 3.0%). Además hubo participación de otros especialistas y técnicos (222, 1.6%), de los estomatólogos (29, 0.2%) y de los estudiantes y la industria, con 12 reportes para un 0.1% respectivamente. La relación de Causalidad se comportó de igual manera que en el transcurso del año siendo el 73.9% reacciones probables. Tabla 3. Distribución de las reacciones adversas según causalidad Causalidad No % Definitivas Probables Posibles Condicionales No Relacionadas En la Tabla 4 se muestran la distribución de las notificaciones según severidad durante los años 2005 al Tabla 4. Distribución de notificaciones de RAM según severidad Severidad
3 No % No % No % No % No % Leves Moderadas Graves Mortales La tabla 5 muestra la severidad en el año Tabla 5. Distribución de reacciones adversas según severidad. Año Severidad 2010 No % Leves Moderadas Graves Mortales Razón de leves / graves y moderadas: 54.8 / 45.2 favorable a la detección de los primeros, lo cual puede explicarse porque en el presente año se realizaron dos seguimientos activos a vacunas y medicamentos utilizados para el tratamiento de la gripe A H1N1, notificándose las sospechas de reacciones adversas desde la atención primaria de salud y en estos casos se recogieron la totalidad de los eventos adversos, independientemente de su severidad. En la Tabla 6 se muestran los fármacos a los cuales se notificó el mayor número de reacciones adversas y la gravedad de las mismas. Tabla 6. Distribución de los fármacos más notificados durante el año 2010 según severidad Fármacos No Reportes % Leves % Moderadas % Graves % Mortales % Vacuna Pandemrix Vacuna Pentavalente Captopril Oseltamivir Amoxicilina
4 Ibuprofeno Ciprofloxacina Penicilina Rapilenta Espasmoforte Nodegrip Los sistemas de órganos más afectados durante el año fueron Piel y anejos (2877, 21.4%), General (2855, 21.3%), Gastrointestinal (2764, 20.6%), Sistema nervioso central (2014, 15.0%), Cardiovascular (869, 6.5%) y Respiratorio (805, 6.0%). Las reacciones adversas más frecuentes fueron fiebre, vómitos, erupción cutánea, cefalea, mareos, eritema, tos, taquicardia, náuseas, prurito, urticaria y malestar epigástrico. En su mayoría leves y conocidas. La tabla 7 muestra el comportamiento por grupos farmacológicos, el cual ha variado en el año, debido a los seguimientos activos realizados a las vacunas preventivas del sistema nacional de salud y a la vacuna de la gripe A H1N1. Los antivirales se incluyen en esta ocasión, por razones antes expuestas. El resto de los grupos concuerda con años anteriores. Tabla 7. Distribución de notificaciones según grupo farmacológico GRUPO FARMACOLOGICO No % Vacunas Antimicrobianos Analgésicos no opioides Antihipertensivos Antivirales Se reportaron un total de 309 notificaciones de Medicina Natural y tradicional para un 2.3% en el año, aumentando discretamente la cifra en relación al año anterior. La Tabla 8 muestra los medicamentos que más se reportaron por producir reacciones adversas graves. Tabla 8: Fármacos que más produjeron RAM graves Fármaco Notificaciones RAM Vacuna Pandemrix 12 Anafilaxia, bronconeumonía, convulsión febril, convulsiones,
5 disnea, edema de la glotis, hipertensión arterial, lipotimia y somnolencia Heberprot-P 11 Edema de pulmón, inconsciencia, infarto de miocardio, infección inducida, lipotimia y precordialgia Penicilina Rapilenta 7 Disnea, lipotimia, parada respiratoria, shock anafiláctico Carboplatino 7 Deshidratación, diarrea, neutropenia, anemia aplásica y sequedad bucal Penicilina Cristalina 5 Edema de glotis, convulsiones, disnea, lipotimia y shock anafiláctico Ceftriaxona 4 Edema de glotis, anafilaxia, inconsciencia y taquicardia Dipirona 4 Disnea, inconciencia Bupivacaína 3 Taquicardia ventricular Taxol 3 Edema de glotis, contracción uterina Vacuna Pentavalente 3 Apnea, cianosis y convulsión febril Cefazolina 3 Shock anafiláctico Cefuroxima 2 Edema de la glotis, glositis Metrotexato 3 Hemorragia digestiva, mucositis, síndrome de Steven Johnson Cisdiscloro diamino platino 2 Insuficiencia renal aguda, neutropenia Fenitoina 2 Necrolisis toxica epidérmica, inconciencia Lidocaína con Epinefrina 2 Edema de glotis, hipotension Tramadol 2 Edema de pulmón Los fármacos alkaseltzer, alopurinol, bicalutamida, cefotaxima, cimetidina, ciprofloxacina, cotrimoxazol, dextrosa, diatrizoato compuesto, dinitrato de isosorbida, enalapril, espasmoforte, estreptoquinasa, etoposido, factor de transferencia, fenitoina, gelatina liquida, glóbulos, ibuprofeno, ifosfamida, insulina NPH, iopramide, penicilina benzatinica, procaína, rifampicina, tinidazol, plasma, urografina, valproato de sodio y vancomicina también presentaron reacciones graves para completar 106 notificaciones de RAM graves las cuales fueron reportadas en las primeras 24 horas de su conocimiento. En al tabla 9 se muestran las sospechas de reacciones adversas medicamentosas con desenlace mortal en el año Tabla 9: Sospechas de Reacciones Mortales Año 2010 FARMACO (No de casos) Heberprot-P (11) REACCIÓN OTROS FARMACOS IMPUTABILIDAD Infarto de miocardio (5) Digoxina, glibenclamida, insulina lenta, dinitrato de isosorbide, ciprofloxacina, enalapril, espironolactona, furosemida, omeprazol Condicional
6 Carboplatino (2) Cisdiscloro diaminoplatino (2) Penicilina Benzatínica (2) Insulina lenta, glibenclamida, Condicional Tromboembolismo (2) clortalidona Posible Edema de pulmón (1) Insulina lenta, amiodarona, heparina Condicional Fibrilación ventricular (1) Insulina lenta, pentoxifilina, aspirina Condicional Hemorragia intracraneal (1) Insulina lenta, glibenclamida, atenolol Condicional Paro cardíaco (1) Insulina lenta, pentoxifilina, atenolol Condicional Insuficiencia renal aguda Ifosfamida, etoposido, mesna Posible Pancitopenia Etoposido Posible Broncoaspiración Etoposido, bleomicina, ondansetron Posible Neurotoxicidad Shock anafiláctico 5 Fluoracilo Posible Enalapril, digoxina, nitropental Polivit, dinitrato de isosorbide Posible Cefazolina (1) Disnea - Posible Cefotaxima (1) Paro cardiorrespiratorio Diclofenaco, vincristina, prednisona Posible Estreptoquinasa recombinante (1) Hemorragia - Posible Metrotexato (1) Muerte súbita Citarabina Posible Penicilina sódica (1) Shock anafiláctico - Probable Penicilina rapilenta (1) Shock anafiláctico Ibuprofeno Probable Procaína (1) Agitación psicomotora - Posible Rituximab (1) Neumonía Flutarabina, ciclofosfamida, cotrimoxazol Posible Vacuna Pandemrix (1) Muerte Captopril, salbutamol, teofilina Condicional En total el presente año cerró con 26 sospechas de reacciones adversas mortales, disminuyendo el número con respecto al año anterior, pero manteniéndose los antimicrobianos entre los medicamentos más notificados como productores de RAM mortales. Los casos de Heberprot-P obedecen a una serie de casos de cuatro años, después de finalizada la investigación pertinente, por lo que no constituyó motivo de señal en el presente año ni para el producto, los pacientes tenían múltiples causas alternativas y se consideraron como de alto riesgo cardiovascular, por lo que las reacciones adversas fueron vistas como condicionales y no descritas, pero sujetas a un proceso de revisión por parte del grupo de investigadores del estudio fase IV y del laboratorio productor. Entre las asociaciones Fármaco RAM muy importantes y con baja frecuencia de aparición se reportaron en total unas 4386 (32.7%) en el año. De ellas el 8.3% (1110) fueron reacciones no descritas en la literatura revisada. (Formulario nacional de Medicamentos). Tabla 10. Tabla 10. Distribución de reportes según frecuencia de aparición. Año 2010
7 Frecuencia RAM No % Frecuentes Ocasionales Raras No descritas Los fármacos que más produjeron estos efectos se muestran en la tabla 11. Tabla 11. Fármacos que más se relacionaron con efectos adversos de baja frecuencia de aparición FARMACO No de Casos (%)* REACCION ADVERSA Vacuna Pandemrix 521 (23.4) Vómitos, taquicardia, disnea, somnolencia, lipotimia, hipertensión, cianosis, broncoespasmo, ataxia, hipoglicemia, sincope, anafilaxia, parestesia, opresión precordial, trombocitopenia, neuritis. Dipirona 278 (83.7) Lipotimia, vómitos, eritema, cianosis, hipersensibilidad, inconciencia, sincope. Nodegrip 233 (92.1) Erupción cutánea, vómitos, epigastralgia, disnea, edema angioneurótico, dolor articular, dolor precordial, mialgia, palpitaciones, otalgia Captopril 206 (31.6) Inconciencia, parestesia, cianosis, hipoglicemia, disnea, laringitis, angioedema. Ibuprofeno 179 (50.4) Parestesia, lipotimia, hematoma, síndrome cushingoide, urticaria, disnea, vértigo, edema angioneurótico, coluria, eritema multiforme, broncoespasmo. Espasmoforte 149 (54.0) Lipotimia, vértigo, visión borrosa, disnea, somnolencia, temblor, hipotensión, cianosis, hipersensibilidad, taquiarritmia, desmayo, rubefacción. Ciprofloxacina 114 (32.9) Vértigos, lipotimia, trastorno del habla, taquicardia, urticaria, disnea, depresión, alergia, angioedema. Metronidazol 57 (25.6) Erupción cutánea, dolor anginoso, petequias, urticaria Oseltamivir 57 (10.1) Edema angioneurótico, somnolencia, urticaria, epixtasis, taquicardia, diarrea, hipertensión, poliuria. * Del total de reportes del fármaco. La tabla 12 presenta las notificaciones graves más relevantes en pediatría. Tabla 12: Notificaciones graves relevantes en pediatría Edad Sexo Medicamento RAM Severidad Causalidad 4 f AMOXICILINA HEMORRAGIA GINGIVAL moderada probable 11 m DIFENHIDRAMINA AGITACION moderada probable 15 f IBUPROFEN BRONCOESPASMO moderada probable 1 m CO-TRIMOXAZOL HIPOTERMIA moderada condicional
8 15 f DICLOFENACO EDEMA CONJUNTIVAL moderada probable 6 m LEVAMISOL PALPITACIONES moderada probable 11 f AMINOFILINA HIPOTENSION moderada probable 7 m PIPERAZINA TEMBLORES moderada probable 1 f AZITROMICINA RETENCION URINARIA moderada definitiva 6 m NODEGRIP HABONES moderada condicional 7 f NODEGRIP VOMITOS moderada condicional 11 f CIPROFLOXACINA DISNEA moderada posible 5 m OSELTAMIVIR IRRITABILIDAD moderada probable 2 m OSELTAMIVIR EPISTAXIS moderada probable 0,6 m OSELTAMIVIR URTICARIA moderada probable 2 f FENITOINA ATAXIA grave probable 12 f NODEGRIP DISNEA moderada condicional 3 f VANCOMICINA ANAFILAXIA grave probable 14 m ALCAZELTZER EDEMA DE GLOTIS grave probable 0,8 m PENICILINA RAPILENTA SHOCK ANAFILACTICO grave probable 14 m VACUNA ANTIALERGICA DS4 ANGIOEDEMA moderada probable 1 f INDINAVIR DIARREA moderada probable 0,5 m FACTOR DE TRANSFERENCIA CIANOSIS grave posible 0,4 m VACUNA PENTAVALENTE CIANOSIS grave posible 4 m VACUNA A H1N1 PANDEMRIX CONVULSIONES grave condicional 13 m LIDOCAINA 2%-EPINEFRINA HEMORRAGIA ORAL moderada probable 2 m VACUNA A H1N1 PANDEMRIX TROMBOCITOPENIA moderada probable 1 m CEFALEXINA PETEQUIAS moderada probable 2 m OSELTAMIVIR EPISTAXIS moderada probable 3 f CARBOPLATINO ANEMIA APLASICA grave posible 1 f ACIDO NALIDIXICO BRONCOESPASMO moderada probable 0,6 m AMOXICILINA ERITEMA MULTIFORME moderada probable 10 f METILFENIDATO TICS moderada condicional 5 m HIERRO DEXTRANA DISNEA moderada probable 0,1 f DIFENHIDRAMINA RETENCION URINARIA moderada probable En el año se siguieron 15 expedientes conjuntos con la industria, en los que se retuvieron productos por quejas de calidad y reacciones adversas. La tabla 13 muestra un resumen de las mismas. Tabla 13. Expedientes de calidad y seguridad
9 No Estado Producto Lote / Vence 1 Liberado ASA 125 mg / Retirado Ibuprofeno IBU / Vigilar Salbutamol spray 4 Liberado Solución Diálisis Peritoneal 5 Revisar Urografina indicacion y 76% dosis 6 Retenido Lidocaína carpules 7 Cumplir con el procedimiento de uso C064, C074, C085 / , / B / , / Bupivacaína B 10001A / Liberado Solución Diálisis Peritoneal / Seguimiento Cloruro Sodio / Liberar( lote Amiodarona A6002, A6003) A Vigilar Penicilina Rapilenta / Vigilar Vancomicina 0005 / Investigacion Insulina NPH YS61402, YS Retenido ASA 125 mg 0056 / Investigacion Salbutamol spray Fabricante Reporte Calidad SRAM Hebei Jiheng Group Pharmaceutical, China Gaurov Pharma Pvt. Ltd, India Pequeños cristales en las tabletas Tabletas moteadas de negro y olor Cefalea y mareos Síndrome de Stevens - Johnson desagradable Aldo Unión, España Sabor etílico Sensación de disnea, náuseas y broncoespasmo. Lesiones en piel con sangramiento. Adalberto Pesant IMPORTADO New Stetic, S.A Empresa Laboratorios LIORAD Adalberto Pesant Lab. Oriente Empresa Laboratorios AICA Shijiazhuang Pharma, China Julio Trigo Novo Nordik Lab. Oriente Frascos con suspensiones de partículas y tapas flojas. No cambio organoléptico Cambio de coloración No logra el efecto terapéutico No cambio organoléptico No cambio organoléptico Cambio de coloración No cambio organoléptico Cambio de coloración al reconstituir. Producto precipitado Frasco con tabletas de diferentes tamaños 0194 / ELF Reinaldo Gutiérrez Sabor amargo inusual. Líquidos turbios, dolor de peritoneo y nauseas Urticaria y vómito. Sangramiento en 16 casos. Taquicardia Dolor abdominal, líquidos turbios. Mareos Flebitis Rash cutáneo, habones, falta de aire Prurito y enrojecimiento Visión borrosa, midriasis, perdida del equilibrio, mareo y sudoración. Vómitos Punzadas a nivel de garganta y pecho. En cuanto a otras actividades desarrolladas por la UCNFv en el año 2010 se presenta un resumen de las mismas en la tabla 14. Tabla 14. Seguimiento y Retroalimentación. Año PARAMETROS 2009
10 No de contactos con la Industria y otros centros 15 No de Conferencias 8 No Búsquedas en la base de datos e Internet 57 No de investigaciones en ejecución 14 No de investigaciones terminadas 9 Participación en Eventos 6 Cursos impartidos y recibidos 5 No de publicaciones 8 Cumplimiento de proyecciones: De un total de 6 objetivos trazados como proyecciones para el 2010, se cumplieron 4 totales (66.7%), 1 cumplido de forma parcial (16.7%) y 1 no cumplido (16.6%). Los mismos fueron: 1. Detección de un número importante de sospechas de reacciones adversas medicamentosas moderadas, graves y mortales. Porcentaje de más de un 50% de notificaciones detectadas clasificadas en cuanto a severidad como moderada, grave y mortal. CUMPLIDO PARCIALMENTE (debido a que no se alcanzó el 50% pero si un 45.2%, el desplazamiento de este indicador responde al aumento de los reportes de atención primaria de salud por los protocolos de vigilancia activa de oseltamivir y vacunas realizados) 2. Detección de efectos adversos de baja frecuencia de aparición no descritos en la literatura y/o de mecanismo de producción desconocido. Registro en el año de no menos de 10 asociaciones fármaco-ram que puedan representar posibles señales en el país. CUMPLIDO 3. Incremento de los reportes en la atención secundaria de salud Alcanzar en el año hasta un 20% de reportes de atención secundaria. CUMPLIDO 4. Mantener envíos de la Vigibase Cuba al Centro Internacional de Uppsala. Mantener envío de la base de datos con periodicidad semestral. NO CUMPLIDO (debido a problemas con el formato y la homogenización de la base de datos nacional y el programa necesario para el envío) 5. Mantener la actividad de formación en Farmacovigilancia para conservar los índices alcanzados.. Hacer en el año al menos 3 cursos, 1 capacitación a personal de la red y 4 publicaciones. CUMPLIDO
11 6. Mantener la actividad de investigación en Farmacovigilancia.. Tener en el año al menos 5 tutorías de tesis y la evaluación satisfactoria de al menos 2 proyectos de investigación. CUMPLIDO Limitaciones principales durante el año 2010: 1. Problemas con las revisiones de las notificaciones y manejo de la base de datos que entorpece la calidad de las mismas. 2. Deficiencias en las discusiones de los grupos de expertos provinciales y envío de la información de graves y mortales en tiempo. 3. Deficiencias con las computadoras a nivel nacional y provincial, así como con la conectividad y el correo electrónico. Las Proyecciones para el 2011 de la sección de Farmacovigilancia se mantendrán con iguales criterios de medición que el año pasado, para alcanzar los índices propuestos por el sistema, se agrega solo una proyección con la tasa de reporte que debe ser mantenida en el país: Proyecciones Detección de un número importante de sospechas de reacciones adversas medicamentosas que mantenga la tasa de reporte reconocida a nivel internacional para un buen sistema de farmacovigilancia. Mantener la tasa de reporte de sospechas de reacciones adversas medicamentosas por encima de 300 notificaciones por millón de habitantes. 2. Detección de un número importante de sospechas de reacciones adversas medicamentosas moderadas, graves y mortales. Porcentaje de más de un 50% de notificaciones detectadas clasificadas en cuanto a severidad como moderada, grave y mortal que deben ser informadas en las 24 horas siguientes a su ocurrencia y conocimiento. 3. Detección de efectos adversos de baja frecuencia de aparición no descritos en la literatura y/o de mecanismo de producción desconocido. Registro en el año de no menos de 10 asociaciones fármaco-ram que puedan representar posibles señales en el país. 4. Incremento de los reportes en la atención secundaria de salud Alcanzar en el año hasta un 20% de reportes de atención secundaria. 5. Mantener envíos de la Vigibase Cuba al Centro Internacional de Uppsala. Mantener envío de la base de datos con periodicidad semestral.
12 6. Mantener la actividad de formación en Farmacovigilancia para conservar los índices alcanzados.. Hacer en el año al menos 3 cursos, 1 capacitación a personal de la red y 4 publicaciones. 7. Mantener la actividad de investigación en Farmacovigilancia.. Tener en el año al menos 5 tutorías de tesis y la evaluación satisfactoria de al menos 2 proyectos de investigación. UNIDAD COORDINADORA NACIONAL DE FARMACOVIGILANCIA 14 de Enero 2011
Acumulado año 2004 Acumulado año 2005 Acumulado año Fuente: Unidad Nacional Coordinadora Farmacovigilancia.
 CENTRO PARA EL DESARROLLO DE LA FARMACOEPIDEMIOLOGIA UNIDAD COORDINADORA NACIONAL DE FARMACOVIGILANCIA INFORME ANUAL 2006 Durante el año 2006 se recibieron 8261 notificaciones de reacciones adversas medicamentosas
CENTRO PARA EL DESARROLLO DE LA FARMACOEPIDEMIOLOGIA UNIDAD COORDINADORA NACIONAL DE FARMACOVIGILANCIA INFORME ANUAL 2006 Durante el año 2006 se recibieron 8261 notificaciones de reacciones adversas medicamentosas
Acumulado año 2004 Acumulado año Fuente: Unidad Nacional Coordinadora Farmacovigilancia.
 CENTRO PARA EL DESARROLLO DE LA FARMACOEPIDEMIOLOGIA UNIDAD COORDINADORA NACIONAL DE FARMACOVIGILANCIA INFORME ANUAL 2005 Durante el año 2005 se recibieron 7025 notificaciones de reacciones adversas medicamentosas
CENTRO PARA EL DESARROLLO DE LA FARMACOEPIDEMIOLOGIA UNIDAD COORDINADORA NACIONAL DE FARMACOVIGILANCIA INFORME ANUAL 2005 Durante el año 2005 se recibieron 7025 notificaciones de reacciones adversas medicamentosas
Fuente: Unidad Nacional Coordinadora Farmacovigilancia.
 CENTRO PARA EL DESARROLLO DE LA FARMACOEPIDEMIOLOGIA UNIDAD COORDINADORA NACIONAL DE FARMACOVIGILANCIA INFORME ANUAL 2009 Durante el año 2008 se recibieron 8053 notificaciones de reacciones adversas medicamentosas
CENTRO PARA EL DESARROLLO DE LA FARMACOEPIDEMIOLOGIA UNIDAD COORDINADORA NACIONAL DE FARMACOVIGILANCIA INFORME ANUAL 2009 Durante el año 2008 se recibieron 8053 notificaciones de reacciones adversas medicamentosas
Acumulado año 2003 Acumulado año Fuente: Unidad Nacional Coordinadora Farmacovigilancia.
 CENTRO PARA EL DESARROLLO DE LA FARMACOEPIDEMIOLOGIA UNIDAD COORDINADORA NACIONAL DE FARMACOVIGILANCIA INFORME ANUAL 2004 Durante el año 2004 se recibieron 7063 notificaciones de reacciones adversas medicamentosas
CENTRO PARA EL DESARROLLO DE LA FARMACOEPIDEMIOLOGIA UNIDAD COORDINADORA NACIONAL DE FARMACOVIGILANCIA INFORME ANUAL 2004 Durante el año 2004 se recibieron 7063 notificaciones de reacciones adversas medicamentosas
Acumulado año Fuente: Unidad Nacional Coordinadora Farmacovigilancia.
 CENTRO PARA EL DESARROLLO DE LA FARMACOEPIDEMIOLOGIA UNIDAD COORDINADORA NACIONAL DE FARMACOVIGILANCIA INFORME ANUAL 2003 Durante el año 2003 se recibieron 12601 notificaciones de reacciones adversas medicamentosas
CENTRO PARA EL DESARROLLO DE LA FARMACOEPIDEMIOLOGIA UNIDAD COORDINADORA NACIONAL DE FARMACOVIGILANCIA INFORME ANUAL 2003 Durante el año 2003 se recibieron 12601 notificaciones de reacciones adversas medicamentosas
# Notificaciones Año (0.9%) 362 (5.2%)
 CENTRO PARA EL DESARROLLO DE LA FARMACOEPIDEMIOLOGIA UNIDAD COORDINADORA NACIONAL DE FARMACOVIGILANCIA INFORME ANUAL DE SOSPECHAS DE RAM A LA MEDICINA NATURAL Y TRADICIONAL AÑO 2007 Durante el año 2007
CENTRO PARA EL DESARROLLO DE LA FARMACOEPIDEMIOLOGIA UNIDAD COORDINADORA NACIONAL DE FARMACOVIGILANCIA INFORME ANUAL DE SOSPECHAS DE RAM A LA MEDICINA NATURAL Y TRADICIONAL AÑO 2007 Durante el año 2007
REACCIONES ADVERSAS A LOS ANTIMICROBIANOS AÑO 2004
 REACCIONES ADVERSAS A LOS ANTIMICROBIANOS AÑO 2004 Dra Giset Jiménez López UNIDAD COORDINADORA NACIONAL DE FARMACOVIGILANCIA CDF Taller de Antimicrobianos. Enero 2005 % PRINCIPALES RESULTADOS Los antimicrobianos
REACCIONES ADVERSAS A LOS ANTIMICROBIANOS AÑO 2004 Dra Giset Jiménez López UNIDAD COORDINADORA NACIONAL DE FARMACOVIGILANCIA CDF Taller de Antimicrobianos. Enero 2005 % PRINCIPALES RESULTADOS Los antimicrobianos
CENTRO PARA EL DESARROLLO DE LA FARMACOEPIDEMIOLOGIA UNIDAD COORDINADORA NACIONAL DE FARMACOVIGILANCIA
 CENTRO PARA EL DESARROLLO DE LA FARMACOEPIDEMIOLOGIA UNIDAD COORDINADORA NACIONAL DE FARMACOVIGILANCIA INFORME ANUAL DE SOSPECHAS DE RAM A LA MEDICINA NATURAL Y TRADICIONAL AÑO 2008 Durante el año 2008
CENTRO PARA EL DESARROLLO DE LA FARMACOEPIDEMIOLOGIA UNIDAD COORDINADORA NACIONAL DE FARMACOVIGILANCIA INFORME ANUAL DE SOSPECHAS DE RAM A LA MEDICINA NATURAL Y TRADICIONAL AÑO 2008 Durante el año 2008
CENTRO PARA EL DESARROLLO DE LA FARMACOEPIDEMIOLOGIA UNIDAD COORDINADORA NACIONAL DE FARMACOVIGILANCIA
 CENTRO PARA EL DESARROLLO DE LA FARMACOEPIDEMIOLOGIA UNIDAD COORDINADORA NACIONAL DE FARMACOVIGILANCIA INFORME DE SOSPECHAS DE RAM A LA MEDICINA NATURAL Y TRADICIONAL 2do TRIMESTRE AÑO 2008 Durante el
CENTRO PARA EL DESARROLLO DE LA FARMACOEPIDEMIOLOGIA UNIDAD COORDINADORA NACIONAL DE FARMACOVIGILANCIA INFORME DE SOSPECHAS DE RAM A LA MEDICINA NATURAL Y TRADICIONAL 2do TRIMESTRE AÑO 2008 Durante el
CENTRO PARA EL DESARROLLO DE LA FARMACOEPIDEMIOLOGIA UNIDAD COORDINADORA NACIONAL DE FARMACOVIGILANCIA
 CENTRO PARA EL DESARROLLO DE LA FARMACOEPIDEMIOLOGIA UNIDAD COORDINADORA NACIONAL DE FARMACOVIGILANCIA Informe de sospechas de RAM a la Medicina Natural y Tradicional 1er. semestre año 009 Durante el primer
CENTRO PARA EL DESARROLLO DE LA FARMACOEPIDEMIOLOGIA UNIDAD COORDINADORA NACIONAL DE FARMACOVIGILANCIA Informe de sospechas de RAM a la Medicina Natural y Tradicional 1er. semestre año 009 Durante el primer
Principales resultados del sistema cubano de Farmacovigilancia en el año 2004
 Rev Cubana Farm 2005;39(3) Centro para el Desarrollo de la Farmacoepidemiología Principales resultados del sistema cubano de Farmacovigilancia en el año 2004 Francisco Debesa García, 1 Giset Jiménez, 2
Rev Cubana Farm 2005;39(3) Centro para el Desarrollo de la Farmacoepidemiología Principales resultados del sistema cubano de Farmacovigilancia en el año 2004 Francisco Debesa García, 1 Giset Jiménez, 2
Durante el año se recibieron en nuestro Centro notificaciones de Reacciones Adversas Medicamentosas (RAM) que contenian sospechas de RAM.
 UNIDAD COORDINADORA NACIONAL DE FARMACOVIGILANCIA INFORME ANUAL, 2000. Durante el año se recibieron en nuestro Centro 28450 notificaciones de Reacciones Adversas Medicamentosas (RAM) que contenian 39777
UNIDAD COORDINADORA NACIONAL DE FARMACOVIGILANCIA INFORME ANUAL, 2000. Durante el año se recibieron en nuestro Centro 28450 notificaciones de Reacciones Adversas Medicamentosas (RAM) que contenian 39777
Reporte Anual Farmacovigilancia 2017
 Reporte Anual Farmacovigilancia 2017 Vigilancia activa La vigilancia activa de la seguridad de los medicamentos en el 2017 incluyó 33 puntos focales, conformados por 19 sitios institucionales, donde se
Reporte Anual Farmacovigilancia 2017 Vigilancia activa La vigilancia activa de la seguridad de los medicamentos en el 2017 incluyó 33 puntos focales, conformados por 19 sitios institucionales, donde se
Unidad Coordinadora Nacional de Farmacovigilancia.
 Unidad Coordinadora Nacional de Farmacovigilancia. Comunicación a profesionales sanitarios sobre Identificación de señales en reacciones adversas de baja frecuencia. Alerta No 13 del Sistema Cubano de
Unidad Coordinadora Nacional de Farmacovigilancia. Comunicación a profesionales sanitarios sobre Identificación de señales en reacciones adversas de baja frecuencia. Alerta No 13 del Sistema Cubano de
CARACTERIZACIÓN DE LAS REACCIONES ADVERSAS MEDICAMENTOSAS DE BAJA FRECUENCIA DE APARICIÓN
 INVESTIGACIÓN CARACTERIZACIÓN DE LAS REACCIONES ADVERSAS MEDICAMENTOSAS DE BAJA FRECUENCIA DE APARICIÓN Characterization of low frequency of onset s adverse drug reactions Leidy Santos Muñoz 1* Giset Jiménez
INVESTIGACIÓN CARACTERIZACIÓN DE LAS REACCIONES ADVERSAS MEDICAMENTOSAS DE BAJA FRECUENCIA DE APARICIÓN Characterization of low frequency of onset s adverse drug reactions Leidy Santos Muñoz 1* Giset Jiménez
mhtml:file://d:\web version Junio-07\CDF\fv\Notas\Diatrizoato.mht
 Page 1 of 5 Unidad Coordinadora Nacional de Farmacovigilancia. Comunicación a profesionales sanitarios sobre Diatrizoato de Meglumine. Alerta 19 de Abril 2004 La inyección de Meglumina Diatrizoada Compuesta,
Page 1 of 5 Unidad Coordinadora Nacional de Farmacovigilancia. Comunicación a profesionales sanitarios sobre Diatrizoato de Meglumine. Alerta 19 de Abril 2004 La inyección de Meglumina Diatrizoada Compuesta,
DIRECCIÓN DE REGULACIÓN DE PRODUCTOS DE INTERÉS SANITARIO CENTRO NACIONAL DE FARMACOVIGILANCIA
 DIRECCIÓN DE REGULACIÓN DE PRODUCTOS DE INTERÉS SANITARIO CENTRO NACIONAL DE FARMACOVIGILANCIA INFORME I SEMESTRE DEL 2016 SOSPECHAS DE REACCIÓN ADVERSA A MEDICAMENTO Durante el primer semestre del 2016
DIRECCIÓN DE REGULACIÓN DE PRODUCTOS DE INTERÉS SANITARIO CENTRO NACIONAL DE FARMACOVIGILANCIA INFORME I SEMESTRE DEL 2016 SOSPECHAS DE REACCIÓN ADVERSA A MEDICAMENTO Durante el primer semestre del 2016
Análisis de las sospechas de reacciones adversas producidas por analgésicos no opioides. Cuba-2007
 Boletín Fármacos Advierten...Investigaciones Volumen 12, número 2, abril de 2009 Análisis de las sospechas de reacciones adversas producidas por analgésicos no opioides. Cuba-2007 1 Ashley Lázaro Chao
Boletín Fármacos Advierten...Investigaciones Volumen 12, número 2, abril de 2009 Análisis de las sospechas de reacciones adversas producidas por analgésicos no opioides. Cuba-2007 1 Ashley Lázaro Chao
DIRECCIÓN DE REGULACIÓN DE PRODUCTOS DE INTERÉS SANITARIO CENTRO NACIONAL DE FARMACOVIGILANCIA
 DIRECCIÓN DE REGULACIÓN DE PRODUCTOS DE INTERÉS SANITARIO CENTRO NACIONAL DE FARMACOVIGILANCIA INFORME II SEMESTRE DEL 2016 SOSPECHAS DE REACCIÓN ADVERSA A MEDICAMENTO Durante el segundo semestre del 2016
DIRECCIÓN DE REGULACIÓN DE PRODUCTOS DE INTERÉS SANITARIO CENTRO NACIONAL DE FARMACOVIGILANCIA INFORME II SEMESTRE DEL 2016 SOSPECHAS DE REACCIÓN ADVERSA A MEDICAMENTO Durante el segundo semestre del 2016
DIRECCIÓN DE REGULACIÓN DE PRODUCTOS DE INTERÉS SANITARIO CENTRO NACIONAL DE FARMACOVIGILANCIA
 DIRECCIÓN DE REGULACIÓN DE PRODUCTOS DE INTERÉS SANITARIO CENTRO NACIONAL DE FARMACOVIGILANCIA INFORME I CUATRIMESTRE DEL 2017 SOSPECHAS DE REACCIÓN ADVERSA A MEDICAMENTO Durante el primer cuatrimestre
DIRECCIÓN DE REGULACIÓN DE PRODUCTOS DE INTERÉS SANITARIO CENTRO NACIONAL DE FARMACOVIGILANCIA INFORME I CUATRIMESTRE DEL 2017 SOSPECHAS DE REACCIÓN ADVERSA A MEDICAMENTO Durante el primer cuatrimestre
Investigaciones Rápidas
 N 26 Septiembre 2007 Investigaciones Rápidas Centro para el Desarrollo de la Farmacoepidemiología Sección de investigaciones Reacciones adversas a medicamentos referidas por la población adulta de Ciudad
N 26 Septiembre 2007 Investigaciones Rápidas Centro para el Desarrollo de la Farmacoepidemiología Sección de investigaciones Reacciones adversas a medicamentos referidas por la población adulta de Ciudad
DIRECCIÓN DE REGULACIÓN DE LA SALUD CENTRO NACIONAL DE FARMACOVIGILANCIA
 DIRECCIÓN DE REGULACIÓN DE LA SALUD CENTRO NACIONAL DE FARMACOVIGILANCIA INFORME I SEMESTRE DEL 2014 SOSPECHAS DE REACCIÓN ADVERSA A MEDICAMENTO Durante el primer semestre de 2014 (enero de 2014 hasta
DIRECCIÓN DE REGULACIÓN DE LA SALUD CENTRO NACIONAL DE FARMACOVIGILANCIA INFORME I SEMESTRE DEL 2014 SOSPECHAS DE REACCIÓN ADVERSA A MEDICAMENTO Durante el primer semestre de 2014 (enero de 2014 hasta
DIRECCIÓN DE REGULACIÓN DE PRODUCTOS DE INTERÉS SANITARIO CENTRO NACIONAL DE FARMACOVIGILANCIA
 DIRECCIÓN DE REGULACIÓN DE PRODUCTOS DE INTERÉS SANITARIO CENTRO NACIONAL DE FARMACOVIGILANCIA INFORME I SEMESTRE DEL 2015 SOSPECHAS DE REACCIÓN ADVERSA A MEDICAMENTO Durante el primer semestre del 2015
DIRECCIÓN DE REGULACIÓN DE PRODUCTOS DE INTERÉS SANITARIO CENTRO NACIONAL DE FARMACOVIGILANCIA INFORME I SEMESTRE DEL 2015 SOSPECHAS DE REACCIÓN ADVERSA A MEDICAMENTO Durante el primer semestre del 2015
DIRECCIÓN DE REGULACIÓN DE LA SALUD CENTRO NACIONAL DE FARMACOVIGILANCIA
 DIRECCIÓN DE REGULACIÓN DE LA SALUD CENTRO NACIONAL DE FARMACOVIGILANCIA INFORME II SEMESTRE DEL 2014 SOSPECHAS DE REACCIÓN ADVERSA A MEDICAMENTO Durante el segundo semestre de 2014 (julio de 2014 hasta
DIRECCIÓN DE REGULACIÓN DE LA SALUD CENTRO NACIONAL DE FARMACOVIGILANCIA INFORME II SEMESTRE DEL 2014 SOSPECHAS DE REACCIÓN ADVERSA A MEDICAMENTO Durante el segundo semestre de 2014 (julio de 2014 hasta
MUJER MADUREZ Y ENVEJECIMIENTO USO Y ABUSO DE MEDICAMENTOS. Dra. Verónica Acevedo Pastora. Médico Toxicóloga. Nicaragua.
 MUJER MADUREZ Y ENVEJECIMIENTO USO Y ABUSO DE MEDICAMENTOS Dra. Verónica Acevedo Pastora. Médico Toxicóloga. Nicaragua. USO DE MEDICAMENTOS AINES Acetaminofén IECA Enalapril Captopril Analgésicos HTA BLOQUEADORES
MUJER MADUREZ Y ENVEJECIMIENTO USO Y ABUSO DE MEDICAMENTOS Dra. Verónica Acevedo Pastora. Médico Toxicóloga. Nicaragua. USO DE MEDICAMENTOS AINES Acetaminofén IECA Enalapril Captopril Analgésicos HTA BLOQUEADORES
Dirección Provincial de Salud Cienfuegos COMPORTAMIENTO DE LAS NOTIFICACIONES DE SOSPECHAS DE
 Dirección Provincial de Salud Cienfuegos COMPORTAMIENTO DE LAS NOTIFICACIONES DE SOSPECHAS DE REACCIONES ADVERSAS A MEDICAMENTOS EN CIENFUEGOS. 2005-2010 Bárbara Rodríguez Denis I, Mirayda Baute Rodríguez
Dirección Provincial de Salud Cienfuegos COMPORTAMIENTO DE LAS NOTIFICACIONES DE SOSPECHAS DE REACCIONES ADVERSAS A MEDICAMENTOS EN CIENFUEGOS. 2005-2010 Bárbara Rodríguez Denis I, Mirayda Baute Rodríguez
VITAE, REVISTA DE LA FACULTAD DE QUÍMICA FARMACÉUTICA Volumen 8, Números 1 y 2, 2001 Universidad de Antioquia
 VITAE, REVISTA DE LA FACULTAD DE QUÍMICA FARMACÉUTICA Volumen 8, Números 1 y 2, 2001 Universidad de Antioquia Análisis de la situación Garantizar que todas las medicaciones estén indicadas, son efectivas,
VITAE, REVISTA DE LA FACULTAD DE QUÍMICA FARMACÉUTICA Volumen 8, Números 1 y 2, 2001 Universidad de Antioquia Análisis de la situación Garantizar que todas las medicaciones estén indicadas, son efectivas,
PNO: 003 Página 1 de 6 Aprobado por: Dr Julián Pérez Peña Edición: 01 Cargo: Director Fecha:
 Página 1 de 6 Este documento establece la metodología a seguir para el análisis de las sospechas de Reacción Adversa a Medicamentos (RAM) no descritas en el Formulario Nacional de Medicamentos. 1. OBJETIVOS.
Página 1 de 6 Este documento establece la metodología a seguir para el análisis de las sospechas de Reacción Adversa a Medicamentos (RAM) no descritas en el Formulario Nacional de Medicamentos. 1. OBJETIVOS.
Reacciones Adversas de los Fármacos
 Reacciones Adversas de los Fármacos -Talidomida se administró a embarazadas, con el fin de disminuir los efectos propios del embarazo(náuseas, vómitos). Primero se probó en animales y cuando se usó en
Reacciones Adversas de los Fármacos -Talidomida se administró a embarazadas, con el fin de disminuir los efectos propios del embarazo(náuseas, vómitos). Primero se probó en animales y cuando se usó en
Unidad Coordinadora Nacional de Farmacovigilancia 1
 Informe anual, 00 UNIDAD COORDINADORA NACIONAL DE FARMACOVIGILANCIA INFORME ANUAL, 00. Durante el año se recibieron en nuestra Unidad 806 notificaciones de Reacciones Adversas Medicamentosas (RAM) que
Informe anual, 00 UNIDAD COORDINADORA NACIONAL DE FARMACOVIGILANCIA INFORME ANUAL, 00. Durante el año se recibieron en nuestra Unidad 806 notificaciones de Reacciones Adversas Medicamentosas (RAM) que
Unidad Coordinadora Provincial de Farmacovigilancia. Pinar del Río Comunicación a profesionales sanitarios sobre Quinolonas, Uso y Reacciones
 Unidad Coordinadora Provincial de Farmacovigilancia. Pinar del Río Comunicación a profesionales sanitarios sobre Quinolonas, Uso y Reacciones Adversas. Alerta No 12 del Sistema Cubano de Farmacovigilancia.
Unidad Coordinadora Provincial de Farmacovigilancia. Pinar del Río Comunicación a profesionales sanitarios sobre Quinolonas, Uso y Reacciones Adversas. Alerta No 12 del Sistema Cubano de Farmacovigilancia.
Eventos adversos en la inmunoterapia alergeno específica. ( el lado oscuro )
 Eventos adversos en la inmunoterapia alergeno específica ( el lado oscuro ) Seguridad de la IT La IT puede dar lugar a eventos adversos esperados (de naturaleza alérgica) e inesperados El problema más
Eventos adversos en la inmunoterapia alergeno específica ( el lado oscuro ) Seguridad de la IT La IT puede dar lugar a eventos adversos esperados (de naturaleza alérgica) e inesperados El problema más
MINISTERIO DE SALUD PUBLICA CENTRO PARA EL DESARROLLO DE LA FARMACOEPIDEMIOLOGIA UNIDAD COORDINADORA NACIONAL DE FARMACOVIGILANCIA
 Acciones a desarrollar en el sistema cubano de PNO: 001 Página 1 de 7 1. OBJETIVO. El presente procedimiento establece la metodología a seguir en caso de notificación de sospecha de reacción adversa de
Acciones a desarrollar en el sistema cubano de PNO: 001 Página 1 de 7 1. OBJETIVO. El presente procedimiento establece la metodología a seguir en caso de notificación de sospecha de reacción adversa de
SISTEMA CUBANO DE FARMACOVIGILANCIA. Dra Giset Jiménez López Unidad Coordinadora nacional de Farmacovigilancia
 SISTEMA CUBANO DE FARMACOVIGILANCIA Dra Giset Jiménez López Unidad Coordinadora nacional de Farmacovigilancia Taller Alerta temprana ante brotes y epidemias UATS ENSAP 8 de Mayo 2007 UN MEDICAMENTO PUEDE
SISTEMA CUBANO DE FARMACOVIGILANCIA Dra Giset Jiménez López Unidad Coordinadora nacional de Farmacovigilancia Taller Alerta temprana ante brotes y epidemias UATS ENSAP 8 de Mayo 2007 UN MEDICAMENTO PUEDE
Vitae ISSN: Universidad de Antioquia Colombia
 Vitae ISSN: 0121-4004 vitae@udea.edu.co Universidad de Antioquia Colombia Castro Arango, Sol Beatriz VIGILANCIA INTENSIVA DE REACCIONES ADVERSAS ASOCIADAS AL USO DE WARFARINA EN PACIENTES HOSPITALIZADOS
Vitae ISSN: 0121-4004 vitae@udea.edu.co Universidad de Antioquia Colombia Castro Arango, Sol Beatriz VIGILANCIA INTENSIVA DE REACCIONES ADVERSAS ASOCIADAS AL USO DE WARFARINA EN PACIENTES HOSPITALIZADOS
GUÍA PARA LA ATENCIÓN DEL PACIENTE CON ANAFILAXIA
 GUÍA PARA LA ATENCIÓN DEL PACIENTE CON ANAFILAXIA Sanchis Peris, C. SERVICIO DE URGENCIAS HOSPITAL DE SAGUNTO 2014 1. INTRODUCCIÓN La anafilaxia se define como una reacción alérgica grave de inicio rápido
GUÍA PARA LA ATENCIÓN DEL PACIENTE CON ANAFILAXIA Sanchis Peris, C. SERVICIO DE URGENCIAS HOSPITAL DE SAGUNTO 2014 1. INTRODUCCIÓN La anafilaxia se define como una reacción alérgica grave de inicio rápido
PROTOCOLO DE VIGILANCIA EPIDEMIOLÓGICA DE GRIPE (A/H1N1) EN HUMANOS (Versión 8 de 13 de Julio de 2009).
 PROTOCOLO DE VIGILANCIA EPIDEMIOLÓGICA DE GRIPE (A/H1N1) EN HUMANOS (Versión 8 de 13 de Julio de 2009). PRESCRIPCIÓN DE OSELTAMIVIR: El médico que atienda al paciente realizará la prescripción en receta
PROTOCOLO DE VIGILANCIA EPIDEMIOLÓGICA DE GRIPE (A/H1N1) EN HUMANOS (Versión 8 de 13 de Julio de 2009). PRESCRIPCIÓN DE OSELTAMIVIR: El médico que atienda al paciente realizará la prescripción en receta
FICHA TECNICA. Adultos en prediálisis o en diálisis: 1 dosis (40 µg) de 1 ml en cada inyección.
 1. NOMBRE DEL MEDICAMENTO RECOMBIVAX HB 40 mg Vacuna recombinante antihepatitis B. FICHA TECNICA 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Una dosis de RECOMBIVAX HB 40microgramos/ ml, suspensión inyectable
1. NOMBRE DEL MEDICAMENTO RECOMBIVAX HB 40 mg Vacuna recombinante antihepatitis B. FICHA TECNICA 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Una dosis de RECOMBIVAX HB 40microgramos/ ml, suspensión inyectable
Revista Cubana de Hematología, Inmunología y Hemoterapia. 2017; 36 (Suplemento).
 Seguridad clínica del anticuerpo monoclonal CIMABIOR en pacientes con linfoma no hodgkiniano: revisión integrada de datos 1 García-Vega Y 1, Hernández-Casaña P 1, Saumell-Nápoles Y 1, Fernández-Águila
Seguridad clínica del anticuerpo monoclonal CIMABIOR en pacientes con linfoma no hodgkiniano: revisión integrada de datos 1 García-Vega Y 1, Hernández-Casaña P 1, Saumell-Nápoles Y 1, Fernández-Águila
Autor.Prof.Adj.Lic.Esp.Silvana Larrude Montevideo 2011
 Autor.Prof.Adj.Lic.Esp.Silvana Larrude Montevideo 2011 NORMAS BÁSICAS DE ADMINISTRACIÓN DE MEDICAMENTOS OBJETIVO: Evitar errores en la administración de la medicación para: Proteger a los usuarios Proteger
Autor.Prof.Adj.Lic.Esp.Silvana Larrude Montevideo 2011 NORMAS BÁSICAS DE ADMINISTRACIÓN DE MEDICAMENTOS OBJETIVO: Evitar errores en la administración de la medicación para: Proteger a los usuarios Proteger
SISTEMA NACIONAL DE REGISTRO SANITARIO DE PRODUCTOS FARMACEUTICOS CERTIFICADO DE CONDICIONES DE COMERCIALIZACION
 SISTEMA NACIONAL DE REGISTRO SANITARIO DE PRODUCTOS FARMACEUTICOS CERTIFICADO DE CONDICIONES DE COMERCIALIZACION El Instituto Nacional de Higiene Rafael Rangel de conformidad con lo previsto en los artículos
SISTEMA NACIONAL DE REGISTRO SANITARIO DE PRODUCTOS FARMACEUTICOS CERTIFICADO DE CONDICIONES DE COMERCIALIZACION El Instituto Nacional de Higiene Rafael Rangel de conformidad con lo previsto en los artículos
Uso de Paracetamol en Chile: Reacciones adversas y su regulación.
 Instituto de Salud Pública Ministerio de Salud Uso de Paracetamol en Chile: Reacciones adversas y su regulación. Autor: QF. María Francisca Aldunate González. Revisor: QF. Carmen Gloria Lobos Saldías.
Instituto de Salud Pública Ministerio de Salud Uso de Paracetamol en Chile: Reacciones adversas y su regulación. Autor: QF. María Francisca Aldunate González. Revisor: QF. Carmen Gloria Lobos Saldías.
Caracterización de las reacciones adversas medicamentosas en ancianos. Cuba,
 ARTÍCULOS ORIGINALES Caracterización de las reacciones adversas medicamentosas en ancianos. Cuba, 2003-2005 Characterization of the adverse reactions to drugs in the elderly. Cuba, 2003-2005 Dra. Raisa
ARTÍCULOS ORIGINALES Caracterización de las reacciones adversas medicamentosas en ancianos. Cuba, 2003-2005 Characterization of the adverse reactions to drugs in the elderly. Cuba, 2003-2005 Dra. Raisa
1 Ministerio de la Protección Social República de Colombia CIRCULAR N 048.
 1 CIRCULAR N 048. PARA: GOBERNADORES, ALCALDES, SECRETARIOS TERRITORIALES DE SALUD, ADMINISTRADORES Y PRESTADORES DE SERVICIOS DE SALUD. DE: ASUNTO: MINISTERIO DE LA PROTECCIÓN SOCIAL ACTUALIZACIÓN DE
1 CIRCULAR N 048. PARA: GOBERNADORES, ALCALDES, SECRETARIOS TERRITORIALES DE SALUD, ADMINISTRADORES Y PRESTADORES DE SERVICIOS DE SALUD. DE: ASUNTO: MINISTERIO DE LA PROTECCIÓN SOCIAL ACTUALIZACIÓN DE
INFORME SEMESTRAL SOBRE EL ESTADO DE LOS PROYECTOS RAMALES
 INFORME SEMESTRAL SOBRE EL ESTADO DE LOS PROYECTOS RAMALES 1- Nombre del Proyecto: Desarrollo del Programa de Farmacovigilancia activa dirigido a pacientes, para la regulación de la seguridad de los medicamentos.
INFORME SEMESTRAL SOBRE EL ESTADO DE LOS PROYECTOS RAMALES 1- Nombre del Proyecto: Desarrollo del Programa de Farmacovigilancia activa dirigido a pacientes, para la regulación de la seguridad de los medicamentos.
FICHA DE INFORMACIÓN AL PACIENTE: MAPROTILINA
 FICHA DE INFORMACIÓN AL PACIENTE: MAPROTILINA 1.- QUÉ ES Y PARA QUE SE UTILIZA 1.1 Acción: Antidepresivo, con actividad anticolinérgica. 1.2 Cómo actúa este fármaco: Bloquea la recaptación de neurotransmisores
FICHA DE INFORMACIÓN AL PACIENTE: MAPROTILINA 1.- QUÉ ES Y PARA QUE SE UTILIZA 1.1 Acción: Antidepresivo, con actividad anticolinérgica. 1.2 Cómo actúa este fármaco: Bloquea la recaptación de neurotransmisores
Reacción Adversa a Medicamentos. Dr. José Antonio Buenfil López C.R.A.I.C. H.U. U.A.N.L.
 Reacción Adversa a Medicamentos Dr. José Antonio Buenfil López C.R.A.I.C. H.U. U.A.N.L. Reacción Adversa a Medicamentos Cualquier medicamento o agente biológico puede potencialmente provocar una reacción
Reacción Adversa a Medicamentos Dr. José Antonio Buenfil López C.R.A.I.C. H.U. U.A.N.L. Reacción Adversa a Medicamentos Cualquier medicamento o agente biológico puede potencialmente provocar una reacción
Estudio de consumo de atenolol 50mg, enalapril 20mg e irbesartán 150mg en el Hospital México durante los años 2011, 2012 y 2013
 Estudio de consumo de atenolol 50mg, enalapril 20mg e irbesartán 150mg en el Hospital México durante los años 2011, 2012 y 2013 Carolina Chavarría Víquez Carolina González Pérez Carolina Vargas Montero
Estudio de consumo de atenolol 50mg, enalapril 20mg e irbesartán 150mg en el Hospital México durante los años 2011, 2012 y 2013 Carolina Chavarría Víquez Carolina González Pérez Carolina Vargas Montero
Prospecto: información para el paciente. Carnicor 200 mg/ml solución inyectable L-carnitina
 Prospecto: información para el paciente Carnicor 200 mg/ml solución inyectable L-carnitina Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante
Prospecto: información para el paciente Carnicor 200 mg/ml solución inyectable L-carnitina Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante
SISTEMA NACIONAL DE REGISTRO SANITARIO DE PRODUCTOS FARMACEUTICOS CERTIFICADO DE CONDICIONES DE COMERCIALIZACION
 SISTEMA NACIONAL DE REGISTRO SANITARIO DE PRODUCTOS FARMACEUTICOS CERTIFICADO DE CONDICIONES DE COMERCIALIZACION El Instituto Nacional de Higiene Rafael Rangel de conformidad con lo previsto en los artículos
SISTEMA NACIONAL DE REGISTRO SANITARIO DE PRODUCTOS FARMACEUTICOS CERTIFICADO DE CONDICIONES DE COMERCIALIZACION El Instituto Nacional de Higiene Rafael Rangel de conformidad con lo previsto en los artículos
ACTUALIZACIÓN EN MEDICINA INTERNA
 ACTUALIZACIÓN EN MEDICINA INTERNA 160 Curso 01 INTRO- DUCCIÓN La medicina interna constituye uno de los pilares de la práctica clínica, siendo una de las especialidades más amplias en su quehacer clínico;
ACTUALIZACIÓN EN MEDICINA INTERNA 160 Curso 01 INTRO- DUCCIÓN La medicina interna constituye uno de los pilares de la práctica clínica, siendo una de las especialidades más amplias en su quehacer clínico;
UNIDAD COORDINADORA NACIONAL DE FARMACOVIGILANCIA INFORME ANUAL, 2001.
 Informe anual, 00 UNIDAD COORDINADORA NACIONAL DE FARMACOVIGILANCIA INFORME ANUAL, 00. Durante el año se recibieron en nuestro Centro 695 notificaciones de Reacciones Adversas Medicamentosas (RAM) que
Informe anual, 00 UNIDAD COORDINADORA NACIONAL DE FARMACOVIGILANCIA INFORME ANUAL, 00. Durante el año se recibieron en nuestro Centro 695 notificaciones de Reacciones Adversas Medicamentosas (RAM) que
PROSPECTO : INFORMACIÓN PARA EL USUARIO. Cetirizina Alter 10 mg comprimidos recubiertos con película EFG
 PROSPECTO : INFORMACIÓN PARA EL USUARIO Cetirizina Alter 10 mg comprimidos recubiertos con película EFG Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento. - Conserve este prospecto,
PROSPECTO : INFORMACIÓN PARA EL USUARIO Cetirizina Alter 10 mg comprimidos recubiertos con película EFG Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento. - Conserve este prospecto,
IDENTIFICACIÓN Y CARACTERIZACIÓN DE REACCIONES ADVERSAS EN PACIENTE CRITICO
 IDENTIFICACIÓN Y CARACTERIZACIÓN DE REACCIONES ADVERSAS EN PACIENTE CRITICO QF. Marcial Cariqueo Arriagada Farmacéutico Clínico Departamento de Paciente Critico Departamento de Farmacia Clínica Alemana
IDENTIFICACIÓN Y CARACTERIZACIÓN DE REACCIONES ADVERSAS EN PACIENTE CRITICO QF. Marcial Cariqueo Arriagada Farmacéutico Clínico Departamento de Paciente Critico Departamento de Farmacia Clínica Alemana
3. PROPIEDADES FARMACOLOGICAS Grupo farmacoterapéutico: Simpaticomiméticos usados como descongestivos. Código ATC: S01GA
 1. NOMBRE DEL PRINCIPIO ACTIVO (DCI) NAFAZOLINA CLORHIDRATO 2. VIA DE ADMINISTRACION TOPICO NASAL 3. PROPIEDADES FARMACOLOGICAS Grupo farmacoterapéutico: Simpaticomiméticos usados como descongestivos.
1. NOMBRE DEL PRINCIPIO ACTIVO (DCI) NAFAZOLINA CLORHIDRATO 2. VIA DE ADMINISTRACION TOPICO NASAL 3. PROPIEDADES FARMACOLOGICAS Grupo farmacoterapéutico: Simpaticomiméticos usados como descongestivos.
Prospecto: Información para el usuario. Cetirizina Sandoz 10 mg/ml gotas orales en solución EFG
 Prospecto: Información para el usuario Cetirizina Sandoz 10 mg/ml gotas orales en solución EFG Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene información
Prospecto: Información para el usuario Cetirizina Sandoz 10 mg/ml gotas orales en solución EFG Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene información
Domperidona: pequeño aumento del riesgo de arritmias ventriculares graves o muerte cardiaca súbita.
 Pág. 1 de 5 Domperidona: pequeño aumento del riesgo de arritmias ventriculares graves o muerte cardiaca súbita. El objetivo de esta alerta internacional es difundir información sobre la seguridad y eficacia
Pág. 1 de 5 Domperidona: pequeño aumento del riesgo de arritmias ventriculares graves o muerte cardiaca súbita. El objetivo de esta alerta internacional es difundir información sobre la seguridad y eficacia
Cefuroxima Sandoz 750 mg polvo para solución / suspensión inyectable
 Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento. - Conserve este prospecto. Puede tener que volver a leerlo. - Si tiene alguna duda, consulte a su médico o farmacéutico. - Este
Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento. - Conserve este prospecto. Puede tener que volver a leerlo. - Si tiene alguna duda, consulte a su médico o farmacéutico. - Este
Guía Farmacológica de Consulta para Estudiantes de Enfermería
 ii Guía Farmacológica de Consulta para Estudiantes de Enfermería Ms. Patricia Bolaños Grau. Licenciada en Enfermería Universidad Nacional de Trujillo Maestra en Enfermería, mención en Salud de la Mujer
ii Guía Farmacológica de Consulta para Estudiantes de Enfermería Ms. Patricia Bolaños Grau. Licenciada en Enfermería Universidad Nacional de Trujillo Maestra en Enfermería, mención en Salud de la Mujer
Unidad Coordinadora Nacional de Farmacovigilancia. Comunicación a profesionales sanitarios sobre AGONISTAS DOPAMINÉRGICOS ERGÓTICOS Alerta No 7
 1 Diciembre 2008 Unidad Coordinadora Nacional de Farmacovigilancia. Comunicación a profesionales sanitarios sobre AGONISTAS DOPAMINÉRGICOS ERGÓTICOS Alerta No 7 Una alternativa a la levodopa es el uso
1 Diciembre 2008 Unidad Coordinadora Nacional de Farmacovigilancia. Comunicación a profesionales sanitarios sobre AGONISTAS DOPAMINÉRGICOS ERGÓTICOS Alerta No 7 Una alternativa a la levodopa es el uso
LISTA BÁSICA DE MEDICAMENTOS PARA EL TURNO FARMACÉUTICO
 LISTA BÁSICA DE MEDICAMENTOS PARA EL TURNO FARMACÉUTICO INTRODUCCIÓN La publicación de la presente Lista Básica de Medicamentos para el Turno Farmacéutico surge del interés del Ministerio de Salud y Deportes
LISTA BÁSICA DE MEDICAMENTOS PARA EL TURNO FARMACÉUTICO INTRODUCCIÓN La publicación de la presente Lista Básica de Medicamentos para el Turno Farmacéutico surge del interés del Ministerio de Salud y Deportes
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. RECOMBIVAX HB 5 mg Vacuna recombinante antihepatitis B. 2. COMPOSICION CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO RECOMBIVAX HB 5 mg Vacuna recombinante antihepatitis B. 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Una dosis de RECOMBIVAX HB 5 microgramos/ 0,5 ml, suspensión inyectable
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO RECOMBIVAX HB 5 mg Vacuna recombinante antihepatitis B. 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Una dosis de RECOMBIVAX HB 5 microgramos/ 0,5 ml, suspensión inyectable
Mujeres - De R00 a R99
 R00. Anormalidades del latido cardíaco R01. Soplos y otros sonidos cardíacos R02. Gangrena, no clasificada en otra R03. Lectura de presión sanguínea anormal, sin diagnóstico R04. Hemorragias de las vías
R00. Anormalidades del latido cardíaco R01. Soplos y otros sonidos cardíacos R02. Gangrena, no clasificada en otra R03. Lectura de presión sanguínea anormal, sin diagnóstico R04. Hemorragias de las vías
FICHA DE INFORMACIÓN AL PACIENTE: MIANSERINA
 FICHA DE INFORMACIÓN AL PACIENTE: MIANSERINA 1.- QUÉ ES Y PARA QUE SE UTILIZA 1.1 Acción: Antidepresivo, con intensa actividad sedante, ligera antihistamínica H-1 y escasa anticolinérgica. 1.2 Cómo actúa
FICHA DE INFORMACIÓN AL PACIENTE: MIANSERINA 1.- QUÉ ES Y PARA QUE SE UTILIZA 1.1 Acción: Antidepresivo, con intensa actividad sedante, ligera antihistamínica H-1 y escasa anticolinérgica. 1.2 Cómo actúa
PIROXICAM ACCIONES: Analgésica Antiinflamatoria Antipirética Antitrombótica
 ÁCIDOS ENÓLICOS PIROXICAM ACCIONES: Analgésica Antiinflamatoria Antipirética Antitrombótica MECANISMO DE ACCIÓN de prostaglandinas. INHIBICIÓN DE LA COX Inhibe la migración de PMN y monocitos a lugar de
ÁCIDOS ENÓLICOS PIROXICAM ACCIONES: Analgésica Antiinflamatoria Antipirética Antitrombótica MECANISMO DE ACCIÓN de prostaglandinas. INHIBICIÓN DE LA COX Inhibe la migración de PMN y monocitos a lugar de
Caracterización de las reacciones adversas medicamentosas en ancianos. Matanzas
 UNIDAD PROVINCIAL COORDINADORA DE FARMACOVIGILANCIA. MATANZAS Caracterización de las reacciones adversas medicamentosas en ancianos. Characterization of the adverse drug reactions in elder people. AUTORAS
UNIDAD PROVINCIAL COORDINADORA DE FARMACOVIGILANCIA. MATANZAS Caracterización de las reacciones adversas medicamentosas en ancianos. Characterization of the adverse drug reactions in elder people. AUTORAS
NODOLFEN 400 mg comprimidos Ibuprofeno. El principio activo es Ibuprofeno. Cada comprimido contiene 400 mg.
 Lea todo el prospecto detenidamente porque contiene información importante para usted. Este medicamento puede obtenerse sin receta, para el tratamiento de afecciones menores sin la intervención de un médico.
Lea todo el prospecto detenidamente porque contiene información importante para usted. Este medicamento puede obtenerse sin receta, para el tratamiento de afecciones menores sin la intervención de un médico.
ARSENAL FARMACOLÓGICO POSTA DE SALUD RURAL
 1. MEDICAMENTOS USADOS EN ANESTESIA LOCAL 1. LIDOCAÍNA CLORHIDRATO 2% AM 5 ML. 2. ANTIINFLAMATORIOS Y ANTIRREUMÁTICOS NO ESTEROIDALES 2.1. Aines DICLOFENACO SÓDICO CM 50 MG DICLOFENACO SÓDICO SUP 12,5
1. MEDICAMENTOS USADOS EN ANESTESIA LOCAL 1. LIDOCAÍNA CLORHIDRATO 2% AM 5 ML. 2. ANTIINFLAMATORIOS Y ANTIRREUMÁTICOS NO ESTEROIDALES 2.1. Aines DICLOFENACO SÓDICO CM 50 MG DICLOFENACO SÓDICO SUP 12,5
INTOXICACIÓN POR SULFONAMIDAS
 INTOXII ICACIÓN POR SULFONAMIIDAS Las sulfas fueron las primeras drogas usadas efectivamente para combatir las infecciones. La morbimortalidad por infecciones disminuyó en forma considerable desde que
INTOXII ICACIÓN POR SULFONAMIIDAS Las sulfas fueron las primeras drogas usadas efectivamente para combatir las infecciones. La morbimortalidad por infecciones disminuyó en forma considerable desde que
Guía de manejo y administración del Rituximab.
 Hospital Clínico Universitario Valladolid Rocío López Garcia Teresa Gordaliza Rodríguez Ana Mª González Gutiérrez Cristina Fernández Cuadrado Mª Teresa Nieto Poza Mercedes Verano Moral Cristina Barragán
Hospital Clínico Universitario Valladolid Rocío López Garcia Teresa Gordaliza Rodríguez Ana Mª González Gutiérrez Cristina Fernández Cuadrado Mª Teresa Nieto Poza Mercedes Verano Moral Cristina Barragán
Incidentes y casi incidentes. Dra. Mercedes Elena Mijares Rodríguez
 Incidentes y casi incidentes Dra. Mercedes Elena Mijares Rodríguez SOCIEDAD VENEZOLANA DE HEMATOLOGÍA EDUCACIÓN MÉDICA CONTÍNUA DECLARACIÓN DE POTENCIALES CONFLICTOS DE INTERESES Conferencia:Incidentes
Incidentes y casi incidentes Dra. Mercedes Elena Mijares Rodríguez SOCIEDAD VENEZOLANA DE HEMATOLOGÍA EDUCACIÓN MÉDICA CONTÍNUA DECLARACIÓN DE POTENCIALES CONFLICTOS DE INTERESES Conferencia:Incidentes
ANTIBIOTICOS ELABORADO POR: MARTHA NOHELIA ESPINOSA NORMA DE COMPETENCIA ADMINISTRAR MEDICAMENTOS SEGÚN DELEGACION.
 ANTIBIOTICOS ELABORADO POR: MARTHA NOHELIA ESPINOSA NORMA DE COMPETENCIA ADMINISTRAR MEDICAMENTOS SEGÚN DELEGACION. INTRODUCCIÓN Los medicamentos que veremos a continuación están clasificados por grupos
ANTIBIOTICOS ELABORADO POR: MARTHA NOHELIA ESPINOSA NORMA DE COMPETENCIA ADMINISTRAR MEDICAMENTOS SEGÚN DELEGACION. INTRODUCCIÓN Los medicamentos que veremos a continuación están clasificados por grupos
Prospecto: información para el usuario. cetirizina cinfa 10 mg comprimidos recubiertos con película EFG
 Prospecto: información para el usuario cetirizina cinfa 10 mg comprimidos recubiertos con película EFG Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene información
Prospecto: información para el usuario cetirizina cinfa 10 mg comprimidos recubiertos con película EFG Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene información
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. RECOMBIVAX HB 10 mg jeringa precargada Vacuna recombinante antihepatitis B.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO RECOMBIVAX HB 10 mg jeringa precargada Vacuna recombinante antihepatitis B. 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Una dosis de RECOMBIVAX HB 10 microgramos /
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO RECOMBIVAX HB 10 mg jeringa precargada Vacuna recombinante antihepatitis B. 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Una dosis de RECOMBIVAX HB 10 microgramos /
3. TERMINOS Y DEFINICIONES:
 Página 1 de 6 1. OBJETIVOS. Este documento establece la metodología a seguir para la discusión, en los grupos de expertos de farmacovigilancia a todos los niveles de las sospechas de Reacción Adversa a
Página 1 de 6 1. OBJETIVOS. Este documento establece la metodología a seguir para la discusión, en los grupos de expertos de farmacovigilancia a todos los niveles de las sospechas de Reacción Adversa a
Enfermedad producida por el Mycobacterium Tuberculosis, que tiene al hombre casi como único reservorio y que afecta a los pulmones y otros órganos
 Antituberculosos TUBERCULOSIS Enfermedad producida por el Mycobacterium Tuberculosis, que tiene al hombre casi como único reservorio y que afecta a los pulmones y otros órganos ANTITUBERCULOSOS TUBERCULOSIS
Antituberculosos TUBERCULOSIS Enfermedad producida por el Mycobacterium Tuberculosis, que tiene al hombre casi como único reservorio y que afecta a los pulmones y otros órganos ANTITUBERCULOSOS TUBERCULOSIS
INFORME SEMESTRAL SOBRE EL ESTADO DE LOS PROYECTOS RAMALES
 INFORME SEMESTRAL SOBRE EL ESTADO DE LOS PROYECTOS RAMALES 1- Nombre del Proyecto: Desarrollo del Programa de Farmacovigilancia activa dirigido a pacientes, para la regulación de la seguridad de los medicamentos.
INFORME SEMESTRAL SOBRE EL ESTADO DE LOS PROYECTOS RAMALES 1- Nombre del Proyecto: Desarrollo del Programa de Farmacovigilancia activa dirigido a pacientes, para la regulación de la seguridad de los medicamentos.
FOLLETO DE INFORMACIÓN AL PACIENTE DOLGENAL SOLUCIÓN INYECTABLE 30mg/1mL
 FOLLETO DE INFORMACIÓN AL PACIENTE DOLGENAL SOLUCIÓN INYECTABLE 30mg/1mL DOLGENAL Ketorolaco Trometamol 30 mg/1 ml Solución inyectable Vía de Administración: I.M. - I.V. Venta bajo receta médica en establecimientos
FOLLETO DE INFORMACIÓN AL PACIENTE DOLGENAL SOLUCIÓN INYECTABLE 30mg/1mL DOLGENAL Ketorolaco Trometamol 30 mg/1 ml Solución inyectable Vía de Administración: I.M. - I.V. Venta bajo receta médica en establecimientos
ARSENAL FARMACOLOGICO SAPU/SAR APS 2018 SERVICIO DE SALUD CONCEPCIÓN.
 ARSENAL FARMACOLOGICO SAPU/SAR APS 2018 SERVICIO DE SALUD CONCEPCIÓN. GRUPOS FARMACO FORMA FARMACEUTICA DOSIS OBSERVACIONES Grupo 1 01.00. MEDICAMENTOS USADOS EN ANESTESIA Y GASES MEDICINALES 01.02. Anestésicos
ARSENAL FARMACOLOGICO SAPU/SAR APS 2018 SERVICIO DE SALUD CONCEPCIÓN. GRUPOS FARMACO FORMA FARMACEUTICA DOSIS OBSERVACIONES Grupo 1 01.00. MEDICAMENTOS USADOS EN ANESTESIA Y GASES MEDICINALES 01.02. Anestésicos
INSTRUCTIVO PARA EL LLENADO DEL FORMULARIO DE RAM
 1 INSTRUCTIVO PARA EL LLENADO DEL FORMULARIO DE RAM El presente formulario fue diseñado para la notificación bajo formato digitalizado de los eventos sospechosos de Reacciones Adversas a Medicamentos (RAM),
1 INSTRUCTIVO PARA EL LLENADO DEL FORMULARIO DE RAM El presente formulario fue diseñado para la notificación bajo formato digitalizado de los eventos sospechosos de Reacciones Adversas a Medicamentos (RAM),
UNIDAD DE FISIOTERAPIA EN REHABILITACIÓN CARDÍACA. Maribel Montávez Begoña Criado
 UNIDAD DE FISIOTERAPIA EN REHABILITACIÓN CARDÍACA Maribel Montávez Begoña Criado Ejercicio físico en paciente coronario ENTRENAR SEGÚN INTENSIDAD Se consideran 5 zonas de entrenamiento. 1. Zona de actividad
UNIDAD DE FISIOTERAPIA EN REHABILITACIÓN CARDÍACA Maribel Montávez Begoña Criado Ejercicio físico en paciente coronario ENTRENAR SEGÚN INTENSIDAD Se consideran 5 zonas de entrenamiento. 1. Zona de actividad
Prospecto: Información para el usuario DOLOSTOP 650 mg comprimidos Paracetamol
 Prospecto: Información para el usuario DOLOSTOP 650 mg comprimidos Paracetamol Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene información importante para
Prospecto: Información para el usuario DOLOSTOP 650 mg comprimidos Paracetamol Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene información importante para
Reacción mediada por Ig E, ocurre al exponerse a un antígeno en un paciente previamente sensibilizado.
 Reacción mediada por Ig E, ocurre al exponerse a un antígeno en un paciente previamente sensibilizado. La severidad de la reacción puede variar desde leve hasta choque y muerte Emergencia que pone en peligro
Reacción mediada por Ig E, ocurre al exponerse a un antígeno en un paciente previamente sensibilizado. La severidad de la reacción puede variar desde leve hasta choque y muerte Emergencia que pone en peligro
Coulergin 10 mg comprimidos recubiertos con película Cetirizina dihidrocloruro
 PROSPECTO: INFORMACIÓN PARA EL USUARIO Coulergin 10 mg comprimidos recubiertos con película Cetirizina dihidrocloruro Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento Este medicamento
PROSPECTO: INFORMACIÓN PARA EL USUARIO Coulergin 10 mg comprimidos recubiertos con película Cetirizina dihidrocloruro Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento Este medicamento
Medicamentos notificados como productores de reacciones adversas graves en Cuba en un período de diez años
 INVESTIGACIÓN Medicamentos notificados como productores de reacciones adversas graves en Cuba en un período de diez años Notified drugs causing severe adverse reactions in Cuba in a ten-year period MSc.
INVESTIGACIÓN Medicamentos notificados como productores de reacciones adversas graves en Cuba en un período de diez años Notified drugs causing severe adverse reactions in Cuba in a ten-year period MSc.
Oxicodona. . Agonista puro opioide de los receptores mu, Kappa y delta, con efecto analgésico, ansiolítico y sedante.
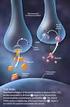 Oxicodona 1. Grupo Farmacoterapéutico:. Agonista puro opioide de los receptores mu, Kappa y delta, con efecto analgésico, ansiolítico y sedante. 2.- Formas farmacéuticas registradas:. Comprimidos de 10mg
Oxicodona 1. Grupo Farmacoterapéutico:. Agonista puro opioide de los receptores mu, Kappa y delta, con efecto analgésico, ansiolítico y sedante. 2.- Formas farmacéuticas registradas:. Comprimidos de 10mg
La Drospirenona como principio activo en Anticonceptivos orales y riesgo de Eventos Tromboembólicos.
 Pág. 1 de 5 La Drospirenona como principio activo en Anticonceptivos orales y riesgo de Eventos Tromboembólicos. El objetivo es difundir información sobre la seguridad y eficacia de los medicamentos basados
Pág. 1 de 5 La Drospirenona como principio activo en Anticonceptivos orales y riesgo de Eventos Tromboembólicos. El objetivo es difundir información sobre la seguridad y eficacia de los medicamentos basados
Fármacos Antihipertensivos y RAM frecuentes. Parte II
 Instituto de Salud Pública Ministerio de Salud Fármacos Antihipertensivos y RAM frecuentes. Parte II Q.F. Carmen Gloria Lobos Saldías Bloqueadores β-adrenérgicos Los Betabloqueantes son sustancias que
Instituto de Salud Pública Ministerio de Salud Fármacos Antihipertensivos y RAM frecuentes. Parte II Q.F. Carmen Gloria Lobos Saldías Bloqueadores β-adrenérgicos Los Betabloqueantes son sustancias que
Índice de contenidos DESCRIPCIÓN GENERAL. Ambroxol
 Ambroxol Índice de contenidos - DESCRIPCIÓN GENERAL - A TENER EN CUENTA - UTILIZACIÓN - ADVERTENCIAS - EFECTOS SECUNDARIOS - COMENTARIOS DESCRIPCIÓN GENERAL El Ambroxol es un medicamento con propiedades
Ambroxol Índice de contenidos - DESCRIPCIÓN GENERAL - A TENER EN CUENTA - UTILIZACIÓN - ADVERTENCIAS - EFECTOS SECUNDARIOS - COMENTARIOS DESCRIPCIÓN GENERAL El Ambroxol es un medicamento con propiedades
ANEXO III ENMIENDA DE LA FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Y PROSPECTO
 ANEXO III ENMIENDA DE LA FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Y PROSPECTO 1 ENMIENDA A INCLUIR EN LAS SECCIONES RELEVANTES DE LA FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL
ANEXO III ENMIENDA DE LA FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Y PROSPECTO 1 ENMIENDA A INCLUIR EN LAS SECCIONES RELEVANTES DE LA FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL
RELIF 1g comprimidos Nabumetona. Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento.
 RELIF 1g comprimidos Nabumetona Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento. - Conserve este prospecto, ya que puede tener que volver a leerlo. - Si tiene alguna duda, consulte
RELIF 1g comprimidos Nabumetona Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento. - Conserve este prospecto, ya que puede tener que volver a leerlo. - Si tiene alguna duda, consulte
Principales resultados del sistema cubano de Farmacovigilancia en el año 2002
 1 de 7 16/03/2010 11:14 CENTRO PARA EL DESARROLLO DE LA FARMACOEPIDEMIOLOGIA CDF Principales resultados del sistema cubano de Farmacovigilancia en el año 2002 AUTORES: Lic. Francisco Debesa García *, Dra.
1 de 7 16/03/2010 11:14 CENTRO PARA EL DESARROLLO DE LA FARMACOEPIDEMIOLOGIA CDF Principales resultados del sistema cubano de Farmacovigilancia en el año 2002 AUTORES: Lic. Francisco Debesa García *, Dra.
VIGILANCIA FARMACOLOGICA EN CUBA. SITUACION ACTUAL
 1 de 6 16/03/2010 11:23 VIGILANCIA FARMACOLOGICA EN CUBA. SITUACION ACTUAL Francisco Debesa García 1, Giset Jiménez 2, Julián Pérez Peña 3 1 Sección de Información Científica-terapéutica y Farmacovigilancia,
1 de 6 16/03/2010 11:23 VIGILANCIA FARMACOLOGICA EN CUBA. SITUACION ACTUAL Francisco Debesa García 1, Giset Jiménez 2, Julián Pérez Peña 3 1 Sección de Información Científica-terapéutica y Farmacovigilancia,
