cadena lateral Un -aminoácido una sección corta de una proteína glicina aminoácidos individuales
|
|
|
- Sebastián Cáceres Romero
- hace 8 años
- Vistas:
Transcripción
1
2 carbono grupo -amino cadena lateral Un -aminoácido enlaces peptídicos una sección corta de una proteína alanina serina glicina aminoácidos individuales cisteína valina
3 AMINÁCIDS Los aminoácidos son cadenas carbonadas con la función ácido (-CH) en un carbono terminal y la función amino (-NH 2 ), en el carbono anterior (carbono )
4 PRPIEDADES DE LS AMINÁCIDS: ESTEREQUÍMICA
5 PRPIEDADES DE LS AMINÁCIDS: ESTEREQUÍMICA Todos los aminoácidos (menos uno) presentan, al menos, el carbono asimétrico, con lo que existirán 2 n isómeros ópticos. Por similitud con el D-gliceraldehído, se denominan D-aminoácidos si tienen el grupo NH 2 a la derecha. En la naturaleza sólo aparecen L- aminoácidos salvo algunas bacterias y ciertos antibióticos.
6 PRPIEDADES DE LS AMINÁCIDS: ÁCID-BASE Los aminoácidos presentan distintos estados de ionización dependiendo del ph:
7 PRPIEDADES DE LS AMINÁCIDS: ÁCID-BASE Cuando el ph es ácido, en el medio abundan los protones y todos los grupos funcionales están saturados de H + : la carga del aminoácido (sin tener en cuenta el radical) es (+)
8 PRPIEDADES DE LS AMINÁCIDS: ÁCID-BASE A medida que el ph se va neutralizando, la [H+] va disminuyendo y el/los grupos ácidos van perdiendo primero los protones, conservándolos el grupo amino (básico). El aminoácido adquiere el estado de ion dipolar, con dos extremos con cargas opuestas.
9 PRPIEDADES DE LS AMINÁCIDS: ÁCID-BASE Cuando la [H+] se hace mínima, el medio adquiere carácter básico. En este punto, el grupo amino pierde un H y el aminoácido adquiere carga (-)
10 PRPIEDADES DE LS AMINÁCIDS: ÁCID-BASE Los aminoácidos tienen una serie de propiedades físicoquímicas derivadas de su carácter de molécula cargada: Solubilidad alta en disolventes polares. Puntos de fusión elevados (>200ºC), ya que las atracciones iónicas fuertes hacen que tiendan a cristalizar.
11 PRPIEDADES DE LS AMINÁCIDS: ÁCID-BASE El punto isoeléctrico de se calcula un aminoácido como la es el ph en el cual el semisuma de los pk 1 aminoácido no tiene carga y pk 2 que neta originan (es un estado una especie de ion iónica dipolar si con el carga resultado neta es 0 (el que no hay carga neta) y pka y pkb, en no migra en un campo eléctrico aminoácidos cuyo radical no tiene carga)
12 Algunos aminoácidos tienen hidrógenos ionizables en sus cadenas laterales histidina
13 El punto isoeléctrico (pi) de un aminoácido es el ph en el cual el aminoácido no tiene carga alanina
14 El pi de un aminoácido que tenga una cadena lateral ionizable es el promedio de los valores de pk a de los grupos ionizantes que sean similares lisina Ácido glutámico
15 Todos los objetos tienen imágenes especulares. Al igual que muchas moléculas, los aminoácidos existen como formas que guardan una relación de imagen especular (estéreoisómeros) que no son superponibles. Solo los isómeros L de los aminoácidos son lo que se encuentran en la naturaleza (La imagen de Venus, (1898), Sir Edward Burne-Jones/Mueseu Calouste Gulbenkian Lisbon/The Birdgeman Art Library)
16 (S)-ALANINA L-ALANINA L-(-)-GLICERALDEHÍD UN L-AMINÁCID CNFIGURACIÓN (S) CNFIGURACIÓN (R)
17 Aminoácidos comunes
18 CLASIFICACIÓN DE LS AMINÁCIDS N PLARES (NP). HIDRÓFBS PLARES SIN CARGA (PSC) PLARES CN CARGA NEGATIVA (P+) (DICARBXÍLICS) PLARES CN CARGA PSITIVA (P-) (DIAMINADS) Aminoácidos esenciales
19 LA CADENA LATERAL ES H UN GRUP ALQUIL (N PLAR) Nombre Símbolo Abreviación Estructura Grupo funcional En la cadena lateral pi glicina ninguno alanina grupo alquilo valina* grupo alquilo leucina* grupo alquilo isoleucina* grupo alquilo fenilalanina* grupo aromático prolina estructura rígida cíclica *aminoácido esencial
20 AMINÁCIDS CN UN GRUP H Nombre Símbolo Abreviación Estructura Grupo funcional pi en la cadena lateral serina treonina* grupo hidroxilo grupo hidroxilo tirosina grupo H fenólico *aminoácido esencial
21 AMINÁCIDS CN UN ÁTM DE S Nombre Símbolo Abreviación Estructura Grupo funcional pi en la cadena lateral cisteína tiol metionina* sulfuro *aminoácido esencial
22 AMINÁCIDS CN UN ÁTM DE N N BÁSIC Nombre Símbolo Abreviación Estructura Grupo funcional pi en la cadena lateral asparagina amida glutamina amida triptofano* indol *aminoácido esencial
23 AMINÁCIDS CN UN GRUP CARBXIL Nombre Símbolo Abreviación Estructura Grupo funcional pi en la cadena lateral ácido aspártico ácido carboxílico ácido glutámico ácido carboxílico *aminoácido esencial
24 AMINÁCIDS CN UN ÁTM DE N BÁSIC Nombre Símbolo Abreviación Estructura Grupo funcional pi en la cadena lateral lisina* grupo amino arginina* grupo guanidino histidina* anillo de imidazol *aminoácido esencial
25 PRPIEDADES DE LS AMINÁCIDS: ÁCID-BASE
26 Estructura sin carga Ion dipolar (ó zwitterion) (componente minoritario) (componente principal) Para un aminoácido con solo un grupo amino y un grupo carboxilo, el pi se puede calcular por el valor medio de los valores de pka de esta molécula
27 Aniónico, arriba de ph 9.6 Punto isoeléctrico pi = 6 Ion dipolar, cerca del punto isoeléctrico Catiónico, abajo de ph 2.3 Equivalentes de H: - adicionados
28 Cálculo del pi en aminoácidos dicarboxílicos: ejemplo Aspártico
29 Asp + Asp + - Asp - Asp 2-
30 Qué carga tiene el aminoácido por debajo y por encima del pi? ph + -
31 Cálculo del pi en aminoácidos dibásicos: ejemplo Lisina Lys 2+ Lys + Lys +/- Lys -
32 Qué carga tiene el aminoácido por debajo y por encima del pi? 9.74 ph + -
33 Una mezcla de aminoácidos se puede separar por medio de la electroforesis con base en sus valores de pi cátodo ánodo arginina alanina aspartato La ninhidrina se usa para detectar a los aminoácidos individuales
34 ELECTRFRESIS FUENTE DE PDER inicio Cátodo Ánodo Húmedo con una solución buffer ph 6 FUENTE DE PDER Muestra conteniendo Ala, Lys, Asp fin Cátodo Ánodo Asp - se mueve hacia la carga positiva Ala no se mueve Lis + se mueve hacia la carga negativa
35 Banda para electroforesis Moléculas cargadas positivamente (+) La muestra a analizar se coloca aquí Moléculas cargadas negativamente (-) Buffer Buffer Cátodo (-) Ánodo (+) milivolts miliamperes
36 PRPIEDADES DE LS AMINÁCIDS: ABSRCIÓN DE LUZ ULTRAVILETA Los aminoácidos presentan una absorbancia de radiación máxima a 280 nm. La absorción es proporcional a la concentración.
37 AMINÁCIDS PRTEICS N FRECUENTES En En el la colágeno elastina En proteínas musculares
38 AMINÁCIDS N PRTEICS No forman parte de proteínas, sino que aparecen solubles, como intermediarios metabólicos o formando parte de las paredes bacterianas. Son, b, o g-aminoácidos, y formas D o L (D-Ala, D-Ser)
39 AMINÁCIDS N PRTEICS Es Son un intermediarios precursor neurotransmisor del en ácido el central metabolismo ciclo pantoténico de inhibidor, la urea, de (vitamina el en los más la aminoácidos síntesis abundante B5) que de interviene Argininina del cerebro, como componente estando presente del coenzima entre el 25-40% A y de otras de las moléculas sinapsis cerebrales. importantes. Juega un papel muy importante en el funcionamiento del metabolismo celular y del sistema nervioso e inmunitario
40 DERIVADS DE AMINÁCIDS De De la la Glicina Histidina: Serina: Arginina Histamina: Esfingosina: Son Creatinina: factores Vasodilatador; de da almacenamiento lugar a los neurotransmisor de fosfatos cerebral vinculado esfingolípidos crecimiento energéticos. a las de emociones muchos microorganismos Ácido glicocólico y y taurocólico: SALES estabilizan BILIARES las (Emulsión de las grasas) estructuras de ribosomas, virus y ADN en muchos organismos
41 DERIVADS DE AMINÁCIDS De la Tirosina: LevoDPA Dopamina: Noradrenalina Adrenalina (levógira): Es (norepinefrina): (epinefrina): el un principal neurotransmisor medicamento cerebral Es una neurotransmisor hormona relacionado en de la con del la tratamiento enfermedad sistema corteza suprarrenal nervioso del Parkinson, simpático, una (en relacionado preparatoria enfermedad que se con ante destruyen las en la que las se neuronas respuestas situaciones produce dopaminérgicas) a una de situaciones estrés e degeneración y inductora la alerta, esquizofrenia. aceleración las de mismas la La del sustancia presencia ritmo respuestas cardíaco, de negra que dopamina la cerebral, es que esencial broncodilatación noradenalina. produce para dopamina, que y los subida y que movimientos de la se tensión encarga se arterial. del realicen control de y forma del control efectiva y coordinación y armónica, del ahí movimiento, los síntomas del tono del muscular Parkinson. y de la postura. Se En usa la esquizofrenia, en lugar de la una dopamina, de las posibles al ser causas un es precursor un exceso de aquella, actividad que puede dopaminérgica atravesar en la el barrera hematoencefálica. cerebro.
42 DERIVADS DE AMINÁCIDS De la Tirosina: piáceos: Anfetamina morfina y heroína Alucinógenos o drogas psicodélicas derivadas de la Es La mescalina una morfina droga es sintética un alcaloide que actúa (sustancia como estimulante nitrogenada del alcalina sistema La derivada nervioso mescalina y de como aminoácidos) es un anoréxico alcaloide aislada y natural que se de extraído sintetizó la adormidera del buscando cactus (Papaver peyote un somniferum) sustituto del en antiasmático 1805 y usada natural como efedrina! analgésico y anestésico y como droga inhibidora del sistema nervioso central, con un gran carácter adictivo. La heroína es el derivado sintético obtenido por primera vez por Bayer, en 1898, mediante la acetilación de la morfina, para ser usado como antitusígeno no adictivo!
43 DERIVADS DE AMINÁCIDS Del Triptófano: Vasoconstrictor Molécula Hormonas encargada implicadas y neurotransmisor de en la el pigmentación crecimiento vinculado y de ritmo a la la percepción Hormona de sensorial crecimiento vegetal regulación metabólico de los ciclos circadianos (día-noche)
44 Síntesis de Aminoácidos
45 SÍNTESIS DE STRECKER Strecker, A. Ann. Chem. Pharm. 1850, 75, 27. Strecker, A. Ann. Chem. Pharm. 1854, 91, 349.
46 Adolph Strecker ( ).
47 PAS 1. FRMACIÓN DE LA IMINA ALDEHÍD IMINA IMINA PAS 2. ADICIÓN DEL IN CIANUR IMINA -AMINNITRIL
48 Mecanismo de la síntesis de Strecker La reacción es promovida por el medio ácido, y el HCN debe proporcionarse o bien generarse in situ a partir de sales de cianuro. En el último caso, se debe consumir un equivalente de ácido en la reacción
49 El primer paso, es muy probable que sea la condensación del amoniaco con el aldehído para formar una imina El cianuro se adiciona como nucleófilo al carbono de la imina, generando el α-aminonitrilo
50 El α-aminonitrilo puede ser hidrolizado al correspondiente α-aminoácido:
51 LA SÍNTESIS DE STRECKER DE LA ALANINA ACETALDEHÍD -AMINPRPINITRIL (D,L)-ALANINA (60 %)
52 H H H H
53 Solvent-Free Synthesis of Racemic α-aminonitriles A. Baeza, C. Nájera, J. M. Sansano, Synthesis, 2007, ) 3) 2) 4) 5)
54 MECANISM DE REACCIÓN (REACCIÓN MULTICMPNENTE) Y DE LA HIDRÓLISIS DEL NITRIL Entrada: Apellidos 1 A a C 2 D a F 3 G a L 4 M a R 5 S a Z
55 ne-pot Three-Component Synthesis of α-iminonitriles by IBX/TBAB-Mediated xidative Strecker Reaction P. Fontaine, A. Chiaroni, G. Masson, J. Zhu, rg. Lett., 2008, 10, ) 3) 4) 2) 5)
56 PERYDAN DE DESS-MARTIN
57 MECANISM DE LA XIDACIÓN DE DESS-MARTIN
58 Buscar catalizadores quirales para llevar a cabo la hidrogenación catalítica en fase homogenea Reacción: diasterofazdiferenciadora Entrada: Apellidos 1 A a C 2 D a F 3 G a L 4 M a R 5 S a Z
59 LA SÍNTESIS DE GABRIEL-ÉSTER MALÓNIC Grupo éster temporal calor ÉSTER N-FTALIMID MALÓNIC ALQUILAD HIDRLIZAD -AMINÁCID
60 BTENCIÓN DE LA (-)-L-METIL DPA
61 A partir del ácido pirúvico DS IMINAS EN EQUILIBRI
62 -CETÁCID AMINÁCID PIRUVAT AMINTRANSFERASA ALANINA
63 AMINTRANSFERASA ASPARTAT -CETÁCID GLUTAMINA ATP ASPARAGINA SINTETASA AMP + PPi AMINÁCID GLUTAMAT XALACETAT ASPARAGINA
64 -CETÁCID AMINÁCID -CETÁCID -CETGLUTARAT AMIN- TRANSFERASA GLUTAMAT AMINÁCID AMIN- TRANSFERASA GLUTAMINA SINTETASA GLUTAMINA INTERMEDIARI FSFAT DE g-glutamil
65 3-FSFGLICERAT 3-FSFGLICERAT 3-FSFGLICERAT DESHIDRGENASA 3-FSFGLICERAT DESHIDRGENASA AMINTRANSFERASA AMINTRANSFERASA 3-FSFHIDRXIPIRUVAT 3-FSFHIDRXIPIRUVAT GLUTAMAT GLUTAMAT -CET- GLUTARAT -CET- GLUTARAT SERINA FSFSERINA FSFATASA FSFSERINA FSFATASA 3-FSFSERINA SERINA 3-FSFSERINA
66 RESLUCIÓN DE MEZCLAS RACÉMICAS L-aminoácido acilasa L es desacilado D-aminoácido aminoácido racémico acilado D no reacciona La mezcla se separa con facilidad
67 REACCIÓN DE IDENTIFICACIÓN CN LA NINHIDRINA piridina AMINÁCID NINHIDRINA PÚRPURA DE RUHEMANN
68 H 2 N H C R C H + 2 H H C + CH + R N H PÚRPURA DE RUHEMANN H H H 2 N H C R C H H HC N H R C H + H H H + H H N CH R + C
69 H N CH R + H H H H H H N C H H R H H H H H N H H R + H N H H H H H N H H H H N H H H H N H
70 H H N H + H H N H N H PÚRPURA DE RUHEMANN + H H
71 Amida plana Enlace peptídico
 Aminoácidos I Br. Cecilia López Área Bioquímica Departamento de Biología Molecular y Celular Marzo 2012 Aminoácidos Proteínas Neurotransmisores (GABA, dopamina) Mediadores de la inflamación (Histamina)
Aminoácidos I Br. Cecilia López Área Bioquímica Departamento de Biología Molecular y Celular Marzo 2012 Aminoácidos Proteínas Neurotransmisores (GABA, dopamina) Mediadores de la inflamación (Histamina)
Unidad 5 (Parte 5) Aminoácidos, Péptidos y Proteínas.
 Unidad 5 (Parte 5) Aminoácidos, Péptidos y Proteínas. Las proteínas se encuentran en todos los organismos vivos, son de muchos tipos diferentes y desempeñan muchas funciones biológicas distintas. La queratina
Unidad 5 (Parte 5) Aminoácidos, Péptidos y Proteínas. Las proteínas se encuentran en todos los organismos vivos, son de muchos tipos diferentes y desempeñan muchas funciones biológicas distintas. La queratina
Unidad 5 (Parte 6) Aminoácidos, Péptidos y Proteínas.
 Unidad 5 (Parte 6) Aminoácidos, Péptidos y Proteínas. Las proteínas se encuentran en todos los organismos vivos, son de muchos tipos diferentes y desempeñan muchas funciones biológicas distintas. La queratina
Unidad 5 (Parte 6) Aminoácidos, Péptidos y Proteínas. Las proteínas se encuentran en todos los organismos vivos, son de muchos tipos diferentes y desempeñan muchas funciones biológicas distintas. La queratina
Los polímeros naturales están presentes en sustancias como la celulosa, el caucho natural y la seda, pero su mayor relevancia está al interior de
 Polímeros Naturales Los polímeros naturales están presentes en sustancias como la celulosa, el caucho natural y la seda, pero su mayor relevancia está al interior de nuestro propio cuerpo y se denomina
Polímeros Naturales Los polímeros naturales están presentes en sustancias como la celulosa, el caucho natural y la seda, pero su mayor relevancia está al interior de nuestro propio cuerpo y se denomina
ESTRUCTURA Y PROPIEDADES DE AMINOÁCIDOS Y PÉPTIDOS AMINOÁCIDOS
 ESTRUCTURA Y PROPIEDADES DE AMINOÁCIDOS Y PÉPTIDOS Fabián Rodríguez Julio 2011 AMINOÁCIDOS Un aminoácido es una molécula orgánica que en su estructura contiene un grupo amino (NH 2 ) y un grupo carboxilo
ESTRUCTURA Y PROPIEDADES DE AMINOÁCIDOS Y PÉPTIDOS Fabián Rodríguez Julio 2011 AMINOÁCIDOS Un aminoácido es una molécula orgánica que en su estructura contiene un grupo amino (NH 2 ) y un grupo carboxilo
METABOLISMO DEL NITRÓGENO
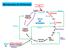 METABLISM DEL NITRÓGEN Descomposición por microorganismos Compuesto rgánicos Nitrogenados ANIMALES Desechos orgánicos Amonificación CICL DEL NITRÓGEN N 3 Nitrificación Nitrosomonas Nitrosación N 2 Nitratación
METABLISM DEL NITRÓGEN Descomposición por microorganismos Compuesto rgánicos Nitrogenados ANIMALES Desechos orgánicos Amonificación CICL DEL NITRÓGEN N 3 Nitrificación Nitrosomonas Nitrosación N 2 Nitratación
Aminoácidos, péptidos y proteinas
 Aminoácidos, péptidos y proteinas Generalidades sobre los aminoácidos Compuestos que contienen un grupo -NH 2 y un grupo -CO 2 H esos grupos en realidad están presentes como -NH 3+ and -CO 2 respectivamente.
Aminoácidos, péptidos y proteinas Generalidades sobre los aminoácidos Compuestos que contienen un grupo -NH 2 y un grupo -CO 2 H esos grupos en realidad están presentes como -NH 3+ and -CO 2 respectivamente.
Aminoácidos Pi Primera Parte
 Proteínas Aminoácidos Pi Primera Parte 1 Introducción a proteínas Las proteínas están constituidas básicamente por unidades elementales (monómeros) denominadas aminoácidos. Hay 20 aminoácidos diferentes,
Proteínas Aminoácidos Pi Primera Parte 1 Introducción a proteínas Las proteínas están constituidas básicamente por unidades elementales (monómeros) denominadas aminoácidos. Hay 20 aminoácidos diferentes,
3. AMINOACIDOS. PROPIEDADES ACIDO-BASE
 Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 3. AMINOACIDOS. PROPIEDADES ACIDO-BASE ESQUEMA - Aminoácidos. Definición, funciones y clasificación - Tipos de aminoácidos: aminoácidos
Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 3. AMINOACIDOS. PROPIEDADES ACIDO-BASE ESQUEMA - Aminoácidos. Definición, funciones y clasificación - Tipos de aminoácidos: aminoácidos
XII SIMPOSIUM INTERNACIONAL DE LA UVA DE MESA - SIUVA
 Rol de los Aminoácidos en el Cultivo de Vid XII SIMPOSIUM INTERNACIONAL DE LA UVA DE MESA - SIUVA 2011 La Molina, 06 y 07 de Julio, 2011 Ing. M.Sc. Federico Ramírez D. Gerente Técnico Aminoácidos Las plantas
Rol de los Aminoácidos en el Cultivo de Vid XII SIMPOSIUM INTERNACIONAL DE LA UVA DE MESA - SIUVA 2011 La Molina, 06 y 07 de Julio, 2011 Ing. M.Sc. Federico Ramírez D. Gerente Técnico Aminoácidos Las plantas
SEMANA 29 AMINOACIDOS Y PÉPTIDOS Elaborado por: Lic. Fernando Andrade
 +UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS UNIDAD DIDÁCTICA DE QUÍMICA, PRIMER AÑO GUIA DE ESTUDIO 2016 SEMANA 29 AMINOACIDOS Y PÉPTIDOS Elaborado por: Lic. Fernando Andrade Lea
+UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS UNIDAD DIDÁCTICA DE QUÍMICA, PRIMER AÑO GUIA DE ESTUDIO 2016 SEMANA 29 AMINOACIDOS Y PÉPTIDOS Elaborado por: Lic. Fernando Andrade Lea
AMINOÁCIDOS Y PÉPTIDOS
 TEMA 4 AMINOÁCIDOS Y PÉPTIDOS 1. Estructura y clasificación de los aminoácidos. 2. Propiedades ácido-base de los aminoácidos y péptidos 3. El enlace peptídico 4. Péptidos: hidrólisis y secuenciación 1.
TEMA 4 AMINOÁCIDOS Y PÉPTIDOS 1. Estructura y clasificación de los aminoácidos. 2. Propiedades ácido-base de los aminoácidos y péptidos 3. El enlace peptídico 4. Péptidos: hidrólisis y secuenciación 1.
CLASIFICACION POR LA CADENA LATERAL POR SU REQUERIMIENTO POR SU POLARIDAD. Esenciales No esenciales CADENA LATERAL CON GRUPO
 29 2018 AMINOACIDOS Y PEPTIDOS Licda. Lilian Judith Guzmán Melgar AMINOACIDOS Compuestos que contienen un grupo carboxílico y un grupo amino. Los más importantes en el mundo biológico son los α-aminoácidos,
29 2018 AMINOACIDOS Y PEPTIDOS Licda. Lilian Judith Guzmán Melgar AMINOACIDOS Compuestos que contienen un grupo carboxílico y un grupo amino. Los más importantes en el mundo biológico son los α-aminoácidos,
CLASIFICACION POR LA CADENA LATERAL POR SU REQUERIMIENTO POR SU POLARIDAD. Esenciales No esenciales CADENA LATERAL CON GRUPO
 AMINOACIDOS Y PEPTIDOS Licda. Lilian Judith Guzmán Melgar 2016 29 AMINOACIDOS Compuestos que contienen un grupo carboxílico y un grupo amino. Los más importantes en el mundo biológico son los α-aminoácidos,
AMINOACIDOS Y PEPTIDOS Licda. Lilian Judith Guzmán Melgar 2016 29 AMINOACIDOS Compuestos que contienen un grupo carboxílico y un grupo amino. Los más importantes en el mundo biológico son los α-aminoácidos,
ESTRUCTURA GENERAL DE LOS AMINOACIDOS A ph FISIOLOGICO
 ESTRUCTURA GENERAL DE LOS AMINOACIDOS A ph FISIOLOGICO Todos los aminoácidos tienen, como mínimo, dos grupos titulables o ionizables, cada uno con un pka característico y, por tanto, con dos zonas tampón
ESTRUCTURA GENERAL DE LOS AMINOACIDOS A ph FISIOLOGICO Todos los aminoácidos tienen, como mínimo, dos grupos titulables o ionizables, cada uno con un pka característico y, por tanto, con dos zonas tampón
BIOQUÍMICA GENERAL. MSc. Dania Martín
 BIOQUÍMICA GENERAL MSc. Dania Martín UNIDAD # 3: PROTEÍNAS Clase #7 OBJETIVOS Conceptuales Procedimentales Actitudinales CONTENIDOS Analizar el objeto de Diferenciar el objeto de Ser consciente de la 1.
BIOQUÍMICA GENERAL MSc. Dania Martín UNIDAD # 3: PROTEÍNAS Clase #7 OBJETIVOS Conceptuales Procedimentales Actitudinales CONTENIDOS Analizar el objeto de Diferenciar el objeto de Ser consciente de la 1.
AMINOÁCIDOS y proteínas
 AMINOÁCIDOS y proteínas La Luciferina es una proteína Marijose Artolozaga Sustacha, MSc Las proteínas son las macromoléculas biológicas más abundantes y variadas. Diferentes estructuras y funciones Las
AMINOÁCIDOS y proteínas La Luciferina es una proteína Marijose Artolozaga Sustacha, MSc Las proteínas son las macromoléculas biológicas más abundantes y variadas. Diferentes estructuras y funciones Las
AMINOÁCIDOS 3B EXPLIQUE EL COMPORTAMIENTO DEL ACIDO ASPARTICO A UNA SOLUCION CON PH DE 8
 AMINOÁCIDOS 1A EXPLIQUE LOS AMINOACIDOS GLUCOCETOGENICOS Los aminoácidos glucocetogénicos son aquellos que producen acetil-coenzima A que posteriormente ayudara en la formación de lípidos, y los intermediarios
AMINOÁCIDOS 1A EXPLIQUE LOS AMINOACIDOS GLUCOCETOGENICOS Los aminoácidos glucocetogénicos son aquellos que producen acetil-coenzima A que posteriormente ayudara en la formación de lípidos, y los intermediarios
Las proteínas están constituidas por la unión de sustancias químicas denominadas aminoácidos. Son estos la unidad estructural de las proteínas.
 AMINÁCIDS Las proteínas están constituidas por la unión de sustancias químicas denominadas aminoácidos. Son estos la unidad estructural de las proteínas. Un aminoácido, posee dos grupos funcionales característicos
AMINÁCIDS Las proteínas están constituidas por la unión de sustancias químicas denominadas aminoácidos. Son estos la unidad estructural de las proteínas. Un aminoácido, posee dos grupos funcionales característicos
QUÍMICA DE ALIMENTOS I Tarea 10: Las Proteínas en los alimentos. Agua (o humedad, si se conoce)*
 QUÍMICA DE ALIMENTOS I Tarea 10: Las Proteínas en los alimentos. Entregar el 21 de Mayo. Selecciona un alimento, de preferencia de los que consumes con regularidad, que contenga proteínas. 1. De acuerdo
QUÍMICA DE ALIMENTOS I Tarea 10: Las Proteínas en los alimentos. Entregar el 21 de Mayo. Selecciona un alimento, de preferencia de los que consumes con regularidad, que contenga proteínas. 1. De acuerdo
UNIDAD 5. AMINOÁCIDOS Y PROTEÍNAS
 UNIDAD 5. AMINOÁCIDOS Y PROTEÍNAS Dr en C. MPA MVZ Carlos Gutiérrez Olvera AMINOÁCIDOS: Como su nombre lo implica, los aminoácidos son moléculas orgánicas que contienen un grupo amino (NH2) en uno de los
UNIDAD 5. AMINOÁCIDOS Y PROTEÍNAS Dr en C. MPA MVZ Carlos Gutiérrez Olvera AMINOÁCIDOS: Como su nombre lo implica, los aminoácidos son moléculas orgánicas que contienen un grupo amino (NH2) en uno de los
Estructura y propiedades de las proteínas
 Estructura y propiedades de las proteínas Matilde Julián Seguí Introducción Las proteínas son las macromoléculas biológicas más importantes. Hay gran variedad de proteínas y cumplen gran variedad de funciones
Estructura y propiedades de las proteínas Matilde Julián Seguí Introducción Las proteínas son las macromoléculas biológicas más importantes. Hay gran variedad de proteínas y cumplen gran variedad de funciones
PROTEINAS AMINOACIDOS
 PROTEINAS AMINOACIDOS 1 2 PROTEINAS Las proteínas son las moléculas constituyentes de los seres vivos que, además de ocupar el 50% del peso seco de los tejidos, tienen la máxima importancia por las funciones
PROTEINAS AMINOACIDOS 1 2 PROTEINAS Las proteínas son las moléculas constituyentes de los seres vivos que, además de ocupar el 50% del peso seco de los tejidos, tienen la máxima importancia por las funciones
PROTEINAS AMINOÁCIDOS
 PROTEINAS Las proteínas son biomóleculas formadas básicamente por carbono, hidrógeno, oxígeno y nitrógeno. Pueden además contener azufre y en algunos tipos de proteínas, fósforo, hierro, magnesio y cobre
PROTEINAS Las proteínas son biomóleculas formadas básicamente por carbono, hidrógeno, oxígeno y nitrógeno. Pueden además contener azufre y en algunos tipos de proteínas, fósforo, hierro, magnesio y cobre
AMINOÁCIDOS, PÉPTIDOS Y PROTEINAS. M.Sc. GABY MÓNICA FELIPE BRAVO
 AMINÁCIDS, PÉPTIDS Y PRTEINAS M.Sc. GABY MÓNICA FELIPE BRAV AMINÁCIDS C H 2 N C H R TDS LS AMINÁCIDS QUE FRMAN PARTE DE LAS PRTEÍNAS SN L-AMINÁCIDS CLASIFICACIÓN DE LS AMINÁCIDS ALIFÁTICS N PLARES ARMÁTICS
AMINÁCIDS, PÉPTIDS Y PRTEINAS M.Sc. GABY MÓNICA FELIPE BRAV AMINÁCIDS C H 2 N C H R TDS LS AMINÁCIDS QUE FRMAN PARTE DE LAS PRTEÍNAS SN L-AMINÁCIDS CLASIFICACIÓN DE LS AMINÁCIDS ALIFÁTICS N PLARES ARMÁTICS
PROTEINAS AMINOÁCIDOS FUNCIONES DE LOS AMINOÁCIDOS
 PROTEINAS Las proteínas son biomóleculas formadas básicamente por carbono, hidrógeno, oxígeno y nitrógeno. Pueden además contener azufre y en algunos tipos de proteínas, fósforo, hierro, magnesio y cobre
PROTEINAS Las proteínas son biomóleculas formadas básicamente por carbono, hidrógeno, oxígeno y nitrógeno. Pueden además contener azufre y en algunos tipos de proteínas, fósforo, hierro, magnesio y cobre
Biomoléculas. Se clasifican básicamente en 4 grandes grupos: Hidratos de carbono Proteínas Lípidos Ácidos nucleicos
 Biomoléculas Se clasifican básicamente en 4 grandes grupos: Hidratos de carbono Proteínas Lípidos Ácidos nucleicos Aminoácidos, péptidos y proteínas Las proteínas cumplen importantes funciones biológicas:
Biomoléculas Se clasifican básicamente en 4 grandes grupos: Hidratos de carbono Proteínas Lípidos Ácidos nucleicos Aminoácidos, péptidos y proteínas Las proteínas cumplen importantes funciones biológicas:
Ciclo de Krebbs, de los ácidos tricarboxílicos o del ácido cítrico
 Catabolismo Es un metabolismo descendente : confluye en un punto común, que va de macromoléculas (complejas) a compuestos sencillos. Se diferencian en tres etapas: Las grandes macromoléculas ingieren se
Catabolismo Es un metabolismo descendente : confluye en un punto común, que va de macromoléculas (complejas) a compuestos sencillos. Se diferencian en tres etapas: Las grandes macromoléculas ingieren se
Proteínas. Tabla 1: Funciones de las proteínas
 Colegio Lectura Hispano Complementaria Americano Depto. de Ciencias - Biología Nivel: 4to medio Unidad I Proteínas 1 En las células, son las proteínas las macromoléculas más abundantes y las que constituyen
Colegio Lectura Hispano Complementaria Americano Depto. de Ciencias - Biología Nivel: 4to medio Unidad I Proteínas 1 En las células, son las proteínas las macromoléculas más abundantes y las que constituyen
Funciones básicas de los aminoácidos
 Funciones básicas de los aminoácidos Ácido Glutámico: sirve principalmente como "combustible" del cerebro y ayuda a absorber el exceso de amoniaco (afecta a las funciones cerebrales) Alanina: es uno de
Funciones básicas de los aminoácidos Ácido Glutámico: sirve principalmente como "combustible" del cerebro y ayuda a absorber el exceso de amoniaco (afecta a las funciones cerebrales) Alanina: es uno de
BIOSINTESIS DE AMINOÁCIDOS INTEGRANTES: ZACHARY FERNANDA CUELLAR CARDOZO PAOLA ANDREA CASTAÑO PAYA
 BIOSINTESIS DE AMINOÁCIDOS INTEGRANTES: ZACHARY FERNANDA CUELLAR CARDOZO PAOLA ANDREA CASTAÑO PAYA Aminoácidos Es una molécula orgánica con un grupo amino (-NH 2 ) y un grupo carboxilo (- COOH). Los aminoácidos
BIOSINTESIS DE AMINOÁCIDOS INTEGRANTES: ZACHARY FERNANDA CUELLAR CARDOZO PAOLA ANDREA CASTAÑO PAYA Aminoácidos Es una molécula orgánica con un grupo amino (-NH 2 ) y un grupo carboxilo (- COOH). Los aminoácidos
Metabolismo de AMINOÁCIDOS
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,013 Metabolismo de AMINOÁCIDOS Dr. Mynor A. Leiva Enríquez La digestión
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,013 Metabolismo de AMINOÁCIDOS Dr. Mynor A. Leiva Enríquez La digestión
Por. Harvey Arjona D., I.A., Ph.D.
 Los Aminoácidos en la Agricultura Moderna Por Harvey Arjona D., I.A., Ph.D. CONTENIDO 1. Generalidades 2. Clasificación de a.a. 3. Metabolismo de los a.a. 4. Absorción de a.a. exógenos 5. Obtención industrial
Los Aminoácidos en la Agricultura Moderna Por Harvey Arjona D., I.A., Ph.D. CONTENIDO 1. Generalidades 2. Clasificación de a.a. 3. Metabolismo de los a.a. 4. Absorción de a.a. exógenos 5. Obtención industrial
PRACTICA 4 ELECTROFORESIS EN PAPEL DE AMINOACIDOS
 PRACTICA 4 ELECTROFORESIS EN PAPEL DE AMINOACIDOS 1.- OBJETIVO: El objetivo fundamental de la practica es la comprobación de la migración electroforética de los aminoácidos sometidos a un campo eléctrico
PRACTICA 4 ELECTROFORESIS EN PAPEL DE AMINOACIDOS 1.- OBJETIVO: El objetivo fundamental de la practica es la comprobación de la migración electroforética de los aminoácidos sometidos a un campo eléctrico
2.2- FENOLES. Como ya hemos indicado, se obtienen al sustituir uno o más átomos de hidrógeno del benceno por radicales OH.
 2.2- FENOLES Como ya hemos indicado, se obtienen al sustituir uno o más átomos de hidrógeno del benceno por radicales OH. Si se sustituye un solo átomo de hidrógeno, se obtienen los fenoles; si se sustituyen
2.2- FENOLES Como ya hemos indicado, se obtienen al sustituir uno o más átomos de hidrógeno del benceno por radicales OH. Si se sustituye un solo átomo de hidrógeno, se obtienen los fenoles; si se sustituyen
TEMA 2.- PROTEÍNAS. AMINOÁCIDOS
 TEMA 2.- PROTEÍNAS. AMINOÁCIDOS Diversidad estructural y funcional de las proteínas. Aminoácidos: características estructurales y clasificación. Aminoácidos estándares y derivados. Aminoácidos esenciales
TEMA 2.- PROTEÍNAS. AMINOÁCIDOS Diversidad estructural y funcional de las proteínas. Aminoácidos: características estructurales y clasificación. Aminoácidos estándares y derivados. Aminoácidos esenciales
Estereoisomerismo en los alfaaminoácidos.
 Estructura general de un aminoácido. Esta estructura es común a todos los alfaaminoácidos, con una única excepción. (La excepción es la prolina, un aminoácido cíclico). El grupo R o cadenal lateral (en
Estructura general de un aminoácido. Esta estructura es común a todos los alfaaminoácidos, con una única excepción. (La excepción es la prolina, un aminoácido cíclico). El grupo R o cadenal lateral (en
TUBERMINE GP PROTEÍNA DE PATATA
 TUBERMINE GP PROTEÍNA DE PATATA Especificaciones Técnicas: GP Proteína extraída del jugo de la patata industrial por un proceso de separación y purificación física. Media de los resultados de los análisis
TUBERMINE GP PROTEÍNA DE PATATA Especificaciones Técnicas: GP Proteína extraída del jugo de la patata industrial por un proceso de separación y purificación física. Media de los resultados de los análisis
Lehninger Principles of Biochemistry Fourth Edition
 David L. Nelson and Michael M. Cox Lehninger Principles of Biochemistry Fourth Edition Capítulo 3: Amino Acidos, Péptidos, y Proteínas Copyright 2004 by W. H. Freeman & Company Estereoquímica de Aminoácidos
David L. Nelson and Michael M. Cox Lehninger Principles of Biochemistry Fourth Edition Capítulo 3: Amino Acidos, Péptidos, y Proteínas Copyright 2004 by W. H. Freeman & Company Estereoquímica de Aminoácidos
AMINOACIDOS Y PEPTIDOS. SEMANA 29 Licda. Lilian Judith Guzmán Melgar
 AMINOACIDOS Y PEPTIDOS SEMANA 29 Licda. Lilian Judith Guzmán Melgar AMINOACIDOS Compuestos que contienen un grupo carboxílico y un grupo amino. Los mas importantes en el mundo biológico son los α-aminoácidos,
AMINOACIDOS Y PEPTIDOS SEMANA 29 Licda. Lilian Judith Guzmán Melgar AMINOACIDOS Compuestos que contienen un grupo carboxílico y un grupo amino. Los mas importantes en el mundo biológico son los α-aminoácidos,
Proteínas: Leche y caseína
 Proteínas: Leche y caseína El papel de la leche en la naturaleza es para alimentar y proporcionar una protección inmunológica para los mamíferos jóvenes. La leche ha sido una fuente de alimento para los
Proteínas: Leche y caseína El papel de la leche en la naturaleza es para alimentar y proporcionar una protección inmunológica para los mamíferos jóvenes. La leche ha sido una fuente de alimento para los
En el APOENZIMA se distinguen tres tipos de aminoácidos:
 1. Concepto de biocatalizador. Son sustancias que consiguen que las reacciones se realicen a gran velocidad a bajas temperaturas, ya que disminuyen la energía de activación de los reactivos. Pueden ser:
1. Concepto de biocatalizador. Son sustancias que consiguen que las reacciones se realicen a gran velocidad a bajas temperaturas, ya que disminuyen la energía de activación de los reactivos. Pueden ser:
Metabolismo de AMINOÁCIDOS
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,011 Metabolismo de AMINOÁCIDOS Dr. Mynor A. Leiva Enríquez Fuente:
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,011 Metabolismo de AMINOÁCIDOS Dr. Mynor A. Leiva Enríquez Fuente:
AMINOÁCIDOS, PEPTIDOS Y PROTEÍNAS. Profesor Carlos Urzúa Stricker
 AMINÁIDS, PEPTIDS Y PRTEÍNAS Profesor arlos Urzúa Stricker H 3 N AMIN AIDS: BLQUES DE NSTRUIÓN DE LAS PRTEÍNAS Químicamente los aminoácidos son ácidos carboxílicos que poseen un grupo amino. H R H 3 N
AMINÁIDS, PEPTIDS Y PRTEÍNAS Profesor arlos Urzúa Stricker H 3 N AMIN AIDS: BLQUES DE NSTRUIÓN DE LAS PRTEÍNAS Químicamente los aminoácidos son ácidos carboxílicos que poseen un grupo amino. H R H 3 N
5. PROBLEMAS SOBRE EQUILIBRIOS ACIDO BASE & AMINOACIDOS
 Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 5. PROBLEMAS SOBRE EQUILIBRIOS ACIDO BASE & AMINOACIDOS Para realizar estos problemas se aconseja consultar una tabla con las
Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 5. PROBLEMAS SOBRE EQUILIBRIOS ACIDO BASE & AMINOACIDOS Para realizar estos problemas se aconseja consultar una tabla con las
AMINOACIDOS Y PEPTIDOS. SEMANA 29 Licda. Lilian Judith Guzmán Melgar
 AMINOACIDOS Y PEPTIDOS SEMANA 29 Licda. Lilian Judith Guzmán Melgar AMINOACIDOS Compuestos que contienen un grupo carboxílico y un grupo amino. Los mas importantes en el mundo biológico son los α-aminoácidos,
AMINOACIDOS Y PEPTIDOS SEMANA 29 Licda. Lilian Judith Guzmán Melgar AMINOACIDOS Compuestos que contienen un grupo carboxílico y un grupo amino. Los mas importantes en el mundo biológico son los α-aminoácidos,
Clasificación de los AA en familias, según su biosíntesis
 Tema 15: : Aspectos generales de la biosíntesis de aminoácidos. Fijación n del nitrógeno a cadenas carbonadas. Algunos ejemplos de interés s biológico. T 15 síntesis AA Los AA se clasifican en esenciales
Tema 15: : Aspectos generales de la biosíntesis de aminoácidos. Fijación n del nitrógeno a cadenas carbonadas. Algunos ejemplos de interés s biológico. T 15 síntesis AA Los AA se clasifican en esenciales
PROTEÍNAS. 1 Nestlé Confidencial Uso Interno únicamente Material de Capacitación Prohibida su copia o reproducción
 PROTEÍNAS 1 Nestlé Confidencial Uso Interno únicamente Qué, Como y Pará que? Objetivo. Repasar las bases y generalidades los aminoácidos y proteínas, así como sus funciones y principios fundamentales para
PROTEÍNAS 1 Nestlé Confidencial Uso Interno únicamente Qué, Como y Pará que? Objetivo. Repasar las bases y generalidades los aminoácidos y proteínas, así como sus funciones y principios fundamentales para
Proteínas. Características generales
 Proteínas Características generales Son las macromoléculas más abundantes en las células. Constituyen hasta el 50% del peso. Forman moléculas específicas en cada especie, incluso entre individuos. Además,
Proteínas Características generales Son las macromoléculas más abundantes en las células. Constituyen hasta el 50% del peso. Forman moléculas específicas en cada especie, incluso entre individuos. Además,
TEMA 5. LAS PROTEÍNAS.
 TEMA 5. LAS PROTEÍNAS. 1.- CARACTERÍSTICAS GENERALES. Son macromoléculas formadas por C, H, O y N. (en algunas ocasiones S). Son importantes porque son las biomoléculas más abundantes en peso seco (50%)
TEMA 5. LAS PROTEÍNAS. 1.- CARACTERÍSTICAS GENERALES. Son macromoléculas formadas por C, H, O y N. (en algunas ocasiones S). Son importantes porque son las biomoléculas más abundantes en peso seco (50%)
CLASIFICACIÓN SEGÚN SU POLARIDAD NO POLARES POLARES NEUTROS ACIDOS BASICOS
 AMINOACIDOS Y PEPTIDOS Licda. Lilian Judith Guzmán Melgar 2015 29 AMINOACIDOS Compuestos que contienen un grupo carboxílico y un grupo amino. Los más importantes en el mundo biológico son los α-aminoácidos,
AMINOACIDOS Y PEPTIDOS Licda. Lilian Judith Guzmán Melgar 2015 29 AMINOACIDOS Compuestos que contienen un grupo carboxílico y un grupo amino. Los más importantes en el mundo biológico son los α-aminoácidos,
METABOLISMO CELULAR. Es el conjunto de reacciones químicas a través de las cuales el organismo intercambia materia y energía con el medio
 METABOLISMO CELULAR Es el conjunto de reacciones químicas a través de las cuales el organismo intercambia materia y energía con el medio Reacciones Celulares Básicas. Los sistemas vivos convierten la energía
METABOLISMO CELULAR Es el conjunto de reacciones químicas a través de las cuales el organismo intercambia materia y energía con el medio Reacciones Celulares Básicas. Los sistemas vivos convierten la energía
PROTEINAS CITOESQUELETO AMINOACIDOS
 PROTEINAS CITOESQUELETO AMINOACIDOS 1 Constituyen, en nuestro estudio de la célula, el 3er. concepto químico funcional. Esta asociado en sus aspectos estructurales: - al citoesqueleto celular - a las fosfolipo-proteínas
PROTEINAS CITOESQUELETO AMINOACIDOS 1 Constituyen, en nuestro estudio de la célula, el 3er. concepto químico funcional. Esta asociado en sus aspectos estructurales: - al citoesqueleto celular - a las fosfolipo-proteínas
I) Biomoléculas 2) El agua I-2 EL AGUA
 I-2 EL AGUA IMPRTANCIA DEL AGUA PARA LS SERES VIVS El agua es el líquido más abundante de la corteza y uno de los pocos líquidos naturales. No es de extrañar entonces que el agua sea una sustancia esencial
I-2 EL AGUA IMPRTANCIA DEL AGUA PARA LS SERES VIVS El agua es el líquido más abundante de la corteza y uno de los pocos líquidos naturales. No es de extrañar entonces que el agua sea una sustancia esencial
Estructura y función de proteínas
 Estructura y función de proteínas Luciferina y uciferasa. Producción de luz. Hemoglobina. Transporte de oxígeno. Queratina: Principal componente estructural de pelo, escamas, cuernos, lana, uñas y plumas.
Estructura y función de proteínas Luciferina y uciferasa. Producción de luz. Hemoglobina. Transporte de oxígeno. Queratina: Principal componente estructural de pelo, escamas, cuernos, lana, uñas y plumas.
Metodologías básicas del procesamiento de Proteinas
 Metodologías básicas del procesamiento de Proteinas Alejandra Kun Departamento de Proteínas y Ácidos Nucleicos-IIBCE Unidad Asociada Sección Bioquímica Facultad de Ciencias 13 de octubre 2014 Curso Introducción
Metodologías básicas del procesamiento de Proteinas Alejandra Kun Departamento de Proteínas y Ácidos Nucleicos-IIBCE Unidad Asociada Sección Bioquímica Facultad de Ciencias 13 de octubre 2014 Curso Introducción
La electrólisis CONTENIDOS. Electrolitos. Iones. Carga eléctrica negativa. www.codelcoeduca.cl
 La electrólisis Las moléculas de ciertos compuestos químicos, cuando se encuentran en disolución acuosa, presentan la capacidad de separarse en sus estructuras moleculares más simples y/o en sus átomos
La electrólisis Las moléculas de ciertos compuestos químicos, cuando se encuentran en disolución acuosa, presentan la capacidad de separarse en sus estructuras moleculares más simples y/o en sus átomos
a) Aminoácidos b) Estructura primaria
 Estructura y función de proteínas a) Aminoácidos b) Estructura primaria Luciferina y luciferasa. Producción de luz. Hemoglobina. Transporte de oxígeno. Queratina: Principal componente estructural de pelo,
Estructura y función de proteínas a) Aminoácidos b) Estructura primaria Luciferina y luciferasa. Producción de luz. Hemoglobina. Transporte de oxígeno. Queratina: Principal componente estructural de pelo,
Problema 1.- Escriba la estructura de la (L)-leucina: a) A ph bajo. b) En el ph isoeléctrico. c) A ph alto. Solución: Zwitterión CH 3 H 3 C H O H 3 N
 Problema 1.- Escriba la estructura de la (L)-leucina: a) A ph bajo. b) En el ph isoeléctrico. c) A ph alto. CH 3 CH 3 CH 3 H 3 C H 3 N H H 3 C H 3 N H 3 C H 2 N ph bajo ph = 6 ph alto Zwitterión Problema
Problema 1.- Escriba la estructura de la (L)-leucina: a) A ph bajo. b) En el ph isoeléctrico. c) A ph alto. CH 3 CH 3 CH 3 H 3 C H 3 N H H 3 C H 3 N H 3 C H 2 N ph bajo ph = 6 ph alto Zwitterión Problema
MÉTODOS CROMATOGRÁFICOS: 1. Exclusión molecular 2. Intercambio iónico 3. Afinidad SSN
 MÉTODOS CROMATOGRÁFICOS: 1. Exclusión molecular 2. Intercambio iónico 3. Afinidad SSN Propiedades de una proteína que son útiles para su purificación por cromatografía Peso molecular Carga iónica Hidrofobicidad
MÉTODOS CROMATOGRÁFICOS: 1. Exclusión molecular 2. Intercambio iónico 3. Afinidad SSN Propiedades de una proteína que son útiles para su purificación por cromatografía Peso molecular Carga iónica Hidrofobicidad
GUIA DE ESTUDIO Nº 9: Aminoácidos, Proteínas y Enzimas
 GUIA DE ESTUDIO Nº 9: Aminoácidos, Proteínas y Enzimas I.- Conceptos básicos: Aminoácidos: Estructura y propiedades ácido base de los aminoácidos. Clasificación según su polaridad. Capacidad buffer. El
GUIA DE ESTUDIO Nº 9: Aminoácidos, Proteínas y Enzimas I.- Conceptos básicos: Aminoácidos: Estructura y propiedades ácido base de los aminoácidos. Clasificación según su polaridad. Capacidad buffer. El
Síntesis de aminoácidos
 Síntesis de aminoácidos 2. Aminoácidos esenciales y no esenciales Los 20 aminoácidos son biológicamente imprescindibles o esenciales! Se llaman aá esenciales los que deben ser suministrados en la dieta
Síntesis de aminoácidos 2. Aminoácidos esenciales y no esenciales Los 20 aminoácidos son biológicamente imprescindibles o esenciales! Se llaman aá esenciales los que deben ser suministrados en la dieta
El agua como disolvente
 hidrofobicas El agua como disolvente El elevado momento dipolar del agua y su facilidad para formar puentes de hidrógeno hacen que el agua sea un excelente disolvente. Una molécula o ión es soluble en
hidrofobicas El agua como disolvente El elevado momento dipolar del agua y su facilidad para formar puentes de hidrógeno hacen que el agua sea un excelente disolvente. Una molécula o ión es soluble en
CONDENSACIONES. Nucleofilo O. O Reactante que sufre adición OH - C H. Reactante que sufre sustitución H 2 O C O -
 NDENSAINES En química orgánica, se conoce como reacciones de condensación a aquellas que se llevan a cabo entre dos compuestos, los cuales tienen el grupo funcional carbonilo dentro de su estructura (
NDENSAINES En química orgánica, se conoce como reacciones de condensación a aquellas que se llevan a cabo entre dos compuestos, los cuales tienen el grupo funcional carbonilo dentro de su estructura (
TEMA 5 BIOMOLÉCULAS ORGÁNICAS (III) PROTEÍNAS. A.- Concepto de prótidos y clasificación B.-Los aminoácidos
 TEMA 5 BIOMOLÉCULAS ORGÁNICAS (III) PROTEÍNAS A.- Concepto de prótidos y clasificación B.-Los aminoácidos Estructura química y funciones Propiedades químicas. El enlace peptídico C.- Estructura tridimensional
TEMA 5 BIOMOLÉCULAS ORGÁNICAS (III) PROTEÍNAS A.- Concepto de prótidos y clasificación B.-Los aminoácidos Estructura química y funciones Propiedades químicas. El enlace peptídico C.- Estructura tridimensional
FACULTAD DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA. CURSO DE BIOQUÍMICA (CLAVE 1508) Licenciaturas de QFB y QA
 FACULTAD DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA CURSO DE BIOQUÍMICA (CLAVE 1508) Licenciaturas de QFB y QA Prof. Laura Carmona Salazar Grupos: 09 Semestre: 16-I Este material es exclusivamente para uso
FACULTAD DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA CURSO DE BIOQUÍMICA (CLAVE 1508) Licenciaturas de QFB y QA Prof. Laura Carmona Salazar Grupos: 09 Semestre: 16-I Este material es exclusivamente para uso
Conceptos básicos de biología molecular, I
 Dr. Eduardo A. RODRÍGUEZ TELLO CINVESTAV-Tamaulipas 21 de mayo del 2013 Dr. Eduardo RODRÍGUEZ T. (CINVESTAV) Conceptos básicos de biología molecular 21 de mayo del 2013 1 / 28 1 Introducción Tarea Dr.
Dr. Eduardo A. RODRÍGUEZ TELLO CINVESTAV-Tamaulipas 21 de mayo del 2013 Dr. Eduardo RODRÍGUEZ T. (CINVESTAV) Conceptos básicos de biología molecular 21 de mayo del 2013 1 / 28 1 Introducción Tarea Dr.
Proteínas y su Papel Biológico
 Proteínas Proteínas y su Papel Biológico Las proteínas son macromoléculas de gran diversidad de formas y versatilidad de funciones. Pueden servir como componentes estructurales de células y tejidos (pelo,
Proteínas Proteínas y su Papel Biológico Las proteínas son macromoléculas de gran diversidad de formas y versatilidad de funciones. Pueden servir como componentes estructurales de células y tejidos (pelo,
Todo lo que los padres deben saber para que su hijo se alimente bien y crezca sano
 http://www.librosaguilar.com/es/ Empieza a leer... Primeros capítulos ANA Mª REQUEJO ROSA Mª ORTEGA Todo lo que los padres deben saber para que su hijo se alimente bien y crezca sano NUTRIENTES Clasificación,
http://www.librosaguilar.com/es/ Empieza a leer... Primeros capítulos ANA Mª REQUEJO ROSA Mª ORTEGA Todo lo que los padres deben saber para que su hijo se alimente bien y crezca sano NUTRIENTES Clasificación,
H + =10-7 y ph=7. H + <10-7 y ph>7.
 REACCIÓN DEL SUELO Las letras ph son una abreviación de "pondus hydrogenii", traducido como potencial de hidrógeno, y fueron propuestas por Sorensen en 1909, que las introdujo para referirse a concentraciones
REACCIÓN DEL SUELO Las letras ph son una abreviación de "pondus hydrogenii", traducido como potencial de hidrógeno, y fueron propuestas por Sorensen en 1909, que las introdujo para referirse a concentraciones
FACULTAD DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA. CURSO DE BIOQUÍMICA (CLAVE 1508) Licenciaturas de QFB y QA
 FACULTAD DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA CURSO DE BIOQUÍMICA (CLAVE 1508) Licenciaturas de QFB y QA Prof. Laura Carmona Salazar Grupos: 03 Semestre: 13-I Este material es exclusivamente para uso
FACULTAD DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA CURSO DE BIOQUÍMICA (CLAVE 1508) Licenciaturas de QFB y QA Prof. Laura Carmona Salazar Grupos: 03 Semestre: 13-I Este material es exclusivamente para uso
Area Química Biológica Curso: Bioquímica. Tema 6: PROTEINAS. Dra. Silvia M. Varas
 Area Química Biológica Curso: Bioquímica Tema 6: PROTEINAS Dra. Silvia M. Varas Las proteínas están formadas por unidades básicas que corresponden a los aminoácidos, los cuales se unen entre sí para formar
Area Química Biológica Curso: Bioquímica Tema 6: PROTEINAS Dra. Silvia M. Varas Las proteínas están formadas por unidades básicas que corresponden a los aminoácidos, los cuales se unen entre sí para formar
AMINOÁCIDOS AGRARES 7
 AMINOÁCIDOS AGRARES 7 1 INTRODUCCIÓN: Los aminoácidos son de una vital importancia en el metabolismo de los seres vivos, desde su condición de ser las unidades estructurales de las proteínas; intervienen
AMINOÁCIDOS AGRARES 7 1 INTRODUCCIÓN: Los aminoácidos son de una vital importancia en el metabolismo de los seres vivos, desde su condición de ser las unidades estructurales de las proteínas; intervienen
A M I N O Á C I D O S
 A M I N O Á C I D O S Qué son? Son componentes básicos, estructurales o funcionales de los pép-dos y las proteínas. Presentan: un grupo carboxilo COOH (ácido) y un grupo amino NH2 (básico) Todos los aminoácidos
A M I N O Á C I D O S Qué son? Son componentes básicos, estructurales o funcionales de los pép-dos y las proteínas. Presentan: un grupo carboxilo COOH (ácido) y un grupo amino NH2 (básico) Todos los aminoácidos
FUNDAMENTOS BIOLÓGICOS DEL APRENDIZAJE Y LA MEMORIA
 Departamento de Biología a Ambiental y Salud PúblicaP FUNDAMENTOS BIOLÓGICOS DEL APRENDIZAJE Y LA MEMORIA La base celular y físico-química del impulso y transmisión de la señal nerviosa. La neurona. Potencial
Departamento de Biología a Ambiental y Salud PúblicaP FUNDAMENTOS BIOLÓGICOS DEL APRENDIZAJE Y LA MEMORIA La base celular y físico-química del impulso y transmisión de la señal nerviosa. La neurona. Potencial
FACULTAD DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA. CURSO DE BIOQUÍMICA (CLAVE 1508) Licenciaturas de QFB y QA
 FACULTAD DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA CURSO DE BIOQUÍMICA (CLAVE 1508) Licenciaturas de QFB y QA Prof. Laura Carmona Salazar Grupos: 09 Semestre: 14-I Este material es exclusivamente para uso
FACULTAD DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA CURSO DE BIOQUÍMICA (CLAVE 1508) Licenciaturas de QFB y QA Prof. Laura Carmona Salazar Grupos: 09 Semestre: 14-I Este material es exclusivamente para uso
Guía nutricional acerca de las propiedades del chorizo
 Guía nutricional acerca de las propiedades del chorizo Fuente: Los Alimentos, Recopilaciones & El Portal del Chacinado Entre los alimentos que tenemos disponibles en nuestra tienda o supermercado habitual,
Guía nutricional acerca de las propiedades del chorizo Fuente: Los Alimentos, Recopilaciones & El Portal del Chacinado Entre los alimentos que tenemos disponibles en nuestra tienda o supermercado habitual,
Bioquímica Estructural y Metabólica. Tema 2. Aminoácidos
 TEMA 2. Aminoácidos. Estructura y propiedades de los aminoácidos. Estereoisomería. Clasificación de los aminoácidos según sus cadenas laterales. Aminoácidos esenciales y no esenciales. Modificaciones post-
TEMA 2. Aminoácidos. Estructura y propiedades de los aminoácidos. Estereoisomería. Clasificación de los aminoácidos según sus cadenas laterales. Aminoácidos esenciales y no esenciales. Modificaciones post-
ácidos orgánicos con un grupo amino en posición alfa
 AMINOÁIDOS ASPETOS GENERALES Desde el punto de vista químico, los aminoácidos (AA) son ácidos orgánicos con un grupo amino en posición alfa. Según esta definición, los cuatro sustituyentes del carbono
AMINOÁIDOS ASPETOS GENERALES Desde el punto de vista químico, los aminoácidos (AA) son ácidos orgánicos con un grupo amino en posición alfa. Según esta definición, los cuatro sustituyentes del carbono
QUÍMICA DE LAS BIOMOLÉCULAS
 QUÍMICA DE LAS BIMLÉCULAS AMINÁCIDS Y PRTEÍNAS Tema 11: Aminoácidos Tema 12: Proteínas A - Z Unidad 5: Aminoácidos y Proteínas Veterinaria AMINÁCIDS H 2 N CH C R H CLASIFICACIÓN: 1- AMINÁCIDS MNAMIN-MNCARBXÍLICS
QUÍMICA DE LAS BIMLÉCULAS AMINÁCIDS Y PRTEÍNAS Tema 11: Aminoácidos Tema 12: Proteínas A - Z Unidad 5: Aminoácidos y Proteínas Veterinaria AMINÁCIDS H 2 N CH C R H CLASIFICACIÓN: 1- AMINÁCIDS MNAMIN-MNCARBXÍLICS
Biomoléculas PROTEÍNAS
 Biomoléculas PROTEÍNAS Las proteínas son biomoléculas orgánicas, formadas por unidades menores llamadas aminoácidos. Son polímeros sintetizados a partir de la unión de varios monómeros a través de un enlace
Biomoléculas PROTEÍNAS Las proteínas son biomoléculas orgánicas, formadas por unidades menores llamadas aminoácidos. Son polímeros sintetizados a partir de la unión de varios monómeros a través de un enlace
METABOLISMO DE AMINOACIDOS
 METABOLISMO DE AMINOACIDOS BIOSÍNTESIS DE AMINOÁCIDOS El ion amonio se incorpora a los aminoácidos a través de glutamato y de glutamina El glutamato y la glutamina desempeñan un papel crucial en la la
METABOLISMO DE AMINOACIDOS BIOSÍNTESIS DE AMINOÁCIDOS El ion amonio se incorpora a los aminoácidos a través de glutamato y de glutamina El glutamato y la glutamina desempeñan un papel crucial en la la
METABOLISMO DE AMINOACIDOS. Kinesiología 2011
 METABOLISMO DE AMINOACIDOS Kinesiología 2011 BALANCE NITROGENADO BN=Nitrógeno total ingerido Nitrógeno total excretado BN=0 existe equilibrio nitrogenado BN es negativo, cuando hay condiciones de síntesis
METABOLISMO DE AMINOACIDOS Kinesiología 2011 BALANCE NITROGENADO BN=Nitrógeno total ingerido Nitrógeno total excretado BN=0 existe equilibrio nitrogenado BN es negativo, cuando hay condiciones de síntesis
Tema 1. Introducción
 Tema 1. Introducción - Bioquímica: concepto, y objetivos - Importancia de la Bioquímica en la Lic. De Farmacia - Composición química del cuerpo humano: Bioelementos Bioelementos primarios o principales
Tema 1. Introducción - Bioquímica: concepto, y objetivos - Importancia de la Bioquímica en la Lic. De Farmacia - Composición química del cuerpo humano: Bioelementos Bioelementos primarios o principales
CAPITULO 4: METABOLÍSMO DE AMINOÁCIDOS
 Introducción CAPITUL 4: METABLÍSM DE AMINÁCIDS Los aminoácidos además de ser unidades monoméricas de las proteínas, son metabolitos energéticos y precursores de muchos compuestos biológicamente activos
Introducción CAPITUL 4: METABLÍSM DE AMINÁCIDS Los aminoácidos además de ser unidades monoméricas de las proteínas, son metabolitos energéticos y precursores de muchos compuestos biológicamente activos
PROTEÍNAS. Largas cadenas de aminoácidos que se pliegan con una estructura definida Son responsables de la mayoría de las funciones bioquímicas:
 PROTEÍNAS Largas cadenas de aminoácidos que se pliegan con una estructura definida Son responsables de la mayoría de las funciones bioquímicas: Tipos de Proteínas ESTRUCTURA DE LAS PROTEÍNAS Estructura
PROTEÍNAS Largas cadenas de aminoácidos que se pliegan con una estructura definida Son responsables de la mayoría de las funciones bioquímicas: Tipos de Proteínas ESTRUCTURA DE LAS PROTEÍNAS Estructura
Profesor Cristian Omar Alvarez De La Cruz
 Aminoácidos by Cristian Omar Alvarez is licensed under a Creative Commons Reconocimiento-NoComercial-CompartirIgual 3.0 Unported License. Profesor Cristian Omar Alvarez De La Cruz Son las unidades monoméricas
Aminoácidos by Cristian Omar Alvarez is licensed under a Creative Commons Reconocimiento-NoComercial-CompartirIgual 3.0 Unported License. Profesor Cristian Omar Alvarez De La Cruz Son las unidades monoméricas
Mecanismo de reacción de la citrato sintasa
 Reacción 1. Citrato sintasa: Condensación del acetilo y el oxalacetato. Es una reacción muy exergónica (-32,2 Kj/mol). Mecanismo de reacción de la citrato sintasa La reacción es semejante a una condensación
Reacción 1. Citrato sintasa: Condensación del acetilo y el oxalacetato. Es una reacción muy exergónica (-32,2 Kj/mol). Mecanismo de reacción de la citrato sintasa La reacción es semejante a una condensación
Dietética y Nutrición
 Dietética y Nutrición Macronutrientes Tema 3 Macronutrientes 1-. Características y metabolismo de carbohidra- tos, grasas y proteínas.- 2-. Nutrientes esenciales y no esenciales.- 3-. Calidad de las proteínas.-
Dietética y Nutrición Macronutrientes Tema 3 Macronutrientes 1-. Características y metabolismo de carbohidra- tos, grasas y proteínas.- 2-. Nutrientes esenciales y no esenciales.- 3-. Calidad de las proteínas.-
Singularidad del carbono
 Singularidad del carbono Su configuración electrónica y su tamaño determinan que sea el único elemento químico que puede: Formar enlaces covalentes sencillos, dobles o triples con otros átomos de carbono.
Singularidad del carbono Su configuración electrónica y su tamaño determinan que sea el único elemento químico que puede: Formar enlaces covalentes sencillos, dobles o triples con otros átomos de carbono.
ESCUELA SUPERIOR POLITECNICA DEL LITORAL OFICINA DE ADMISIONES CURSO DE NIVELACION DE CARRERA SEGUNDO PARCIAL DE QUIMICA Marzo de 2014
 ESCUELA SUPERIOR POLITECNICA DEL LITORAL OFICINA DE ADMISIONES CURSO DE NIVELACION DE CARRERA SEGUNDO PARCIAL DE QUIMICA Marzo de 2014 NOMBRE: PARALELO: FECHA: El presente examen ha sido elaborado para
ESCUELA SUPERIOR POLITECNICA DEL LITORAL OFICINA DE ADMISIONES CURSO DE NIVELACION DE CARRERA SEGUNDO PARCIAL DE QUIMICA Marzo de 2014 NOMBRE: PARALELO: FECHA: El presente examen ha sido elaborado para
Clase 11: Reacciones de condensación, formación del Ión Enolato y reacciones que de esto derivan
 Clase 11: Reacciones de condensación, formación del Ión Enolato y reacciones que de esto derivan Mario Manuel Rodas Morán Departamento de Química Orgánica Facultad de Ciencias Químicas y Farmacia Universidad
Clase 11: Reacciones de condensación, formación del Ión Enolato y reacciones que de esto derivan Mario Manuel Rodas Morán Departamento de Química Orgánica Facultad de Ciencias Químicas y Farmacia Universidad
LAS PROTEÍNAS, LOS GLÚCIDOS Y LAS GRASAS
 LAS PROTEÍNAS, LOS GLÚCIDOS Y LAS GRASAS Las proteínas son elementos de construcción. Hombre de 65 kilos 65 gramos de proteínas Las necesidades diarias de proteínas se estiman en 1 g por kilo de peso.
LAS PROTEÍNAS, LOS GLÚCIDOS Y LAS GRASAS Las proteínas son elementos de construcción. Hombre de 65 kilos 65 gramos de proteínas Las necesidades diarias de proteínas se estiman en 1 g por kilo de peso.
Identificación de proteínas, lípidos y carbohidratos. En productos lácteos. Ramírez Gutiérrez Donají Mariana Torres Martínez Jocelyn Astrid
 Identificación de proteínas, lípidos y carbohidratos. En productos lácteos. Ramírez Gutiérrez Donají Mariana Torres Martínez Jocelyn Astrid Objetivos Comprobar de forma sencilla la existencia de proteínas,
Identificación de proteínas, lípidos y carbohidratos. En productos lácteos. Ramírez Gutiérrez Donají Mariana Torres Martínez Jocelyn Astrid Objetivos Comprobar de forma sencilla la existencia de proteínas,
TECNOLOGIA RESUMEN DEL TEMA 3 (NOCIONES DE ELECTRICIDAD Y MAGNETISMO)
 TECNOLOGIA RESUMEN DEL TEMA 3 (NOCIONES DE ELECTRICIDAD Y MAGNETISMO) Existen 2 clases de electrización, la positiva (que se representa con + ), y la negativa (que se representa con - ). Hay una partícula
TECNOLOGIA RESUMEN DEL TEMA 3 (NOCIONES DE ELECTRICIDAD Y MAGNETISMO) Existen 2 clases de electrización, la positiva (que se representa con + ), y la negativa (que se representa con - ). Hay una partícula
Síntesis de proteínas. Dra. Carmen Aída Martínez
 Síntesis de proteínas Dra. Carmen Aída Martínez Proteínas Cadena de aminoácidos Enzimas Estructurales Señalización Transporte Almacenamiento Traducción Síntesis de proteínas mediada por un molde de ARNm.
Síntesis de proteínas Dra. Carmen Aída Martínez Proteínas Cadena de aminoácidos Enzimas Estructurales Señalización Transporte Almacenamiento Traducción Síntesis de proteínas mediada por un molde de ARNm.
METABOLISMO DE AMINOÁCIDOS: ESQUELETOS DE CARBONO NITRÓGENO
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO METABOLISMO DE AMINOÁCIDOS: ESQUELETOS DE CARBONO NITRÓGENO Dr. Mynor A. Leiva Enríquez
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO METABOLISMO DE AMINOÁCIDOS: ESQUELETOS DE CARBONO NITRÓGENO Dr. Mynor A. Leiva Enríquez
La Absorción del Agua
 La Absorción del Agua Importancia del Agua en las Plantas Es el cons5tuyente principal del protoplasma celular, en ocasiones representa hasta el 95% del peso total de la planta. Es el solvente en el que
La Absorción del Agua Importancia del Agua en las Plantas Es el cons5tuyente principal del protoplasma celular, en ocasiones representa hasta el 95% del peso total de la planta. Es el solvente en el que
SÍNTESIS DE AMINOÁCIDOS Y ORIGEN. INTRODUCCIÓN
 SÍNTESIS DE AMINOÁCIDOS Y ORIGEN. INTRODUCCIÓN La mayoría son ingeridos como proteínas en la dieta. Estas proteínas sufren un proceso de digestión para dar lugar a los aminoácidos que las forman. Además,
SÍNTESIS DE AMINOÁCIDOS Y ORIGEN. INTRODUCCIÓN La mayoría son ingeridos como proteínas en la dieta. Estas proteínas sufren un proceso de digestión para dar lugar a los aminoácidos que las forman. Además,
