SÍNDROMES MIELODISPLÁSICOS
|
|
|
- Laura Maestre San Martín
- hace 9 años
- Vistas:
Transcripción
1 SÍNDROMES MIELODISPLÁSICOS Indice Tabla de resumen Estudios genéticos al diagnóstico Anomalías del 5q- Situaciones específicas o El SMD que no dispone de citogenética o Genética de SMD sin SMD o SMD secundario Seguimiento y evaluación de la respuesta Bibliografía Anexos: clasificaciones e índices pronósticos 1. Resumen del diagnóstico genético Diagnóstico Muestra Citogenética Convencional FISH* Biología molecular CRDU (AR, NR,TR) MO Siempre NO NO ARSA MO Siempre NO NO CRDM MO Siempre NO NO AREB-1 MO Siempre NO NO AREB-2 MO Siempre NO NO SMD 5q- MO Siempre SI* NO *FISH si no tenemos citogenética adecuada o si sospecha de Síndrome 5q- pero el cariotipo es normal; Otros estudios genéticos (mutaciones, reordenamientos específicos) no están indicados de rutina. No hay criterios claramente definidos para realizar estudios genéticos durante el seguimiento. Muestra: MO en heparina.
2 2. Estudios genéticos al diagnóstico a. Citogenética Indicación: la Genética es un pilar básico, por cuanto que: Puede permitirnos distinguir un síndrome mielodisplásico (SMD) de bajo grado de enfermedades causantes de displasia transitoria (fármacos, tóxicos, infección por VIH). Es un parámetro fundamental en los modelos pronósticos de uso actual (IPSS, WPSS). La citogenética es la prueba genética estándar y está indicada en todos los pacientes al diagnóstico y en algunos casos durante el seguimiento 1,2. Deben analizarse al menos 20 metafases, sobre todo si son normales. Si la muestra no es adecuada o no se obtienen metafases debe completarse el estudio con FISH. Muestra: Médula ósea en tubo con heparina sódica (tapón verde). Sangre periférica (también en heparina) solo si aspirado seco (por fibrosis), o médula hipocelular o cualquier otro impedimento para obtener una muestra medular. La SP no es una buena muestra excepto si hay alto componente blástico. Significado clínico Aproximadamente el 50% de los SMD se asocian a una anomalía genética identificable por citogenética convencional. La frecuencia de anomalías es mayor en la AREB, AREB-T y SMD-t (80-90%) y más baja en la ARSA y LMMC (20-30%). La mayoría son translocaciones no balanceadas y pérdidas de material genético por deleciones, siendo la más frecuente la deleción intersticial del brazo largo del cromosoma 5. Las grandes aneuploidías son infrecuentes (<5%), por ello el estudio de ploidía de DNA por citometría no es útil en el SMD. Hay un SMD definido por la deleción de la región cromosómica 5q y <5% de blastos, denominado síndrome 5q-, Las anomalías del cromosoma 5 se tratan en un apartado propio, ya que existe un fármaco, la lenalidomida, especialmente útil en este grupo. La citogenética es un factor de riesgo para transformación a leucemia y para supervivencia. El IPSS 3 y el WPSS 4 definen el riesgo de la citogenética de la siguiente manera: Bueno: normal, aislado -Y, del(5q) única, y del(20q) única. Malo: complejo definido como 3 ó más anomalías y/o cualquier anomalía en el cr. 7 Intermedio: cualquier otra anomalía distinta a la de mal o buen pronóstico. El significado pronóstico es relativamente bien conocido para las anomalías más frecuentes (al menos 3% de cada una) que son las incluidas en el IPSS, pero no hay un acuerdo sobre el significado pronóstico para la mayoría de las anomalías menos frecuentes. En los anexos se muestra el significado pronóstico individual de cada anomalía citogenética según datos del Grupo Alemán de SMD, la serie mayor publicada hasta la fecha 5. Las anomalías cromosómicas con frecuencia son complejas. Las anomalías que afectan a dos cromosomas no suelen tener un pronóstico muy diferente que las que afectan a uno solo,
3 en cambio a partir de 2 anomalías el pronóstico se hace más adverso cuanto más complejo sea el cariotipo. La citogenética modifica el pronóstico en todos los tipos OMS del SMD, aunque el efecto sobre la AR y ARSA es muy pequeño. Algunos tratamientos como la azacitidina, decitabina y lenalidomida pueden modificar el significado pronóstico de algunas anomalías citogenéticas, pero se precisa mayor seguimiento y nuevos estudios. Aun está por definirse la importancia de la carga de la anomalía citogenética 6, es decir el porcentaje de metafases anormales. Los datos actuales sugieren que las anomalías -7/7q- se asocian a mal pronóstico independientemente de la proporción de metafases. En cambio el pronóstico de las anomalías del 5q y 8 podría verse modulada por la proporción de metafases anormales. El SMD asociado a quimioterapia presenta anomalías características que se comentan en un apartado específico. La presencia de una t(8;21), inv(16) ó una t(15;17) es diagnóstica de una LMA con independencia del número de blastos 1. No hay consenso definido sobre si ocurre lo mismo con otras anomalías: t(9;11)(p22;q23); t(6;9)(p23;q34); inv(3)(q21q26.2); t(1,22)(p13;q13). b. FISH y PCR Indicación: No indicada de rutina. El FISH es útil cuando la citogenética convencional no es posible por falta de crecimiento o malas metafases. Por lo tanto su realización habitualmente la indicará el Laboratorio de Citogenética. Se utilizan sondas para las regiones cromosómias más frecuentemente afectadas: 5q33, 7q35, 20q21 y centromérica 8. El estudio por FISH para 5q33 merece una consideración especial y se trata a continuación. Muestra. Para FISH: no es necesario enviar muestra específica si ya fue enviada para cariotipo. Las técnicas basadas en PCR debe solicitarse en muestra de EDTA en SP o MO. Estos estudios, generalmente mutaciones, pueden estar indicadas en casos atípicos con componente mieloproliferativo. La solicitud de estudios genéticos distintos de la citogenética convencional (+- FISH) debe estar justificado por la sospecha diagnóstica.. Indicaciones específicas y significado clínico La utilidad principal del FISH será detectar anomalías del(5q) dada la eficacia de la lenalidomida en el SMD con del(5q), especialmente cuando es una anomalía aislada 7. El FISH con panel para las alteraciones citogenéticas más frecuentes puede detectar anomalías en el 10-20% de SMD con cariotipo normal, pero solo en 2,5% detectará una del5q si el estudio citogenético fue de buena calidad 7. Por ello con un cariotipo normal el FISH para 5q es poco eficiente pero pensando en un tratamiento con lenalidomida podría estar justificada en el SMD de riesgo bajo o intermedio. En cambio el FISH con sondas para la región 5q31-33 puede ser positivo en una alta proporción de SMD de bajo riesgo con muestra
4 no adecuada para citogenética convencional. Las indicaciones de FISH, por tanto, habría que restringirlas a 7 : o Ausencia de estudio genético valorable o En todos pacientes susceptibles de ser tratado con lenalidomida con independencia de los hallazgos citogenéticos. Especialmente indicado si la sospecha es un síndrome 5q-. Dada la respuesta a la lenalidomida en el SMD de bajo riesgo con anomalía en 5q, podría indicarse en cualquier otro SMD de bajo riesgo con independencia del resultado del análisis citogenético. En estos casos debe notificarse expresamente al Laboratorio de Genética. o Diagnóstico diferencial entre SMD y causas de mielodisplasia transitoria cuando no hay un estudio genético valorable o si la citogenética es normal. Especialmente cuando se precisa de una resolución pronta del diagnóstico diferencial. Entidades sensibles a imatinib. Este capítulo no analiza las neoplasias mielodisplásicas/mieloproliferativas (SMD/NMP) ni las formas inclasificables o presentaciones atípicas de las NMP. Sin embargo es obligado señalar la importancia de los estudios genéticos (cariotipo, FISH o PCR) para excluir cuadros sensibles a imatinib 1. Ante un aparente SMD con monocitosis debe buscarse el reordenamiento p190 BCR-ABL. Cuando estudiamos un posible SMD con monocitosis y eosinofilia es esencial excluir una translocación generalmente críptica, la ETV6-PDGFRB también sensible a imatinib. En estos casos debe consultarse con el Laboratorio de Genética o realizar una solicitud debidamente justificada. Mutación JAK2V617F 8 (estudio por PCR, muestra SP en EDTA). Indicado en pacientes ARSA y trombocitosis ya que estos cuadros probablemente son una TE. La mutación JAK2 también puede encontrarse ocasionalmente en formas sin trombocitosis sobre todo cuando hay fibrosis medular. Mutaciones de LAM con citogenética normal. La mutación FLT3-TKD 10 implica muy mal pronóstico, sin embargo afecta a menos del 10% de los SMD de alto grado y 0% en los de bajo grado, además no está claro si aporte valor pronóstico independiente del IPSS. En general, se puede afirmar que el estudio de estas mutaciones no van a aportar nuevos datos, por lo que no se deben incluir de rutina. En los anexos al final del capítulo se describen otras anomalías genéticas frecuentes en los SMD. La más frecuente es la mutación en TET2 (20-25%), tal vez asociada a buen pronóstico 8,9, pero se necesitan estudios confirmatorios antes de aconsejar su incorporación en el diagnóstico clínico. 3. Anomalías de 5q Dado el enorme cambio que ha supuesto la lenalidomida 11 en la evolución de los pacientes con anomalías de este cromosoma, es necesario precisar con más detalle todo lo referente a este grupo de pacientes. La del(5q) se encuentra en el 30% de los SMD: 14% como anomalía aislada; 5% asociado a otra anomalía; 11% dentro de un cariotipo complejo 12. No todas las del(5q) son iguales. Las deleciones intersticiales más frecuentes son: del(5)(q13q31), del(5)(q13q33) y del(5)(q22q33), que engloban la denominada región común delecionada o CDR (5q31q33). Se cree que las deleciones más centroméricas se asocian a formas de peor pronóstico en SMD mientras que la deleción en el síndrome 5q- es más telomérica en 5q32. Sin embargo, en la mayoría de los
5 pacientes la deleción es en una gran región 5q31 y 5q32 donde se encuentra la proteína ribosómica S14 (RPS14). La anomalía se puede demostrar en elementos en diferenciación de las series eritroide, megacariocítica y mieloide, pero apenas en linfocitos. Por este motivo, el estudio en SP es de escasa utilidad. El síndrome 5q- NO ES cualquier SMD con alteraciones del cromosoma 5 o Síndrome 5q OMS-2008 Van den Berghe (1973) SMD con del5(q) aislada -Alteración genética única -Predominio en mujeres (no exclusivo) -Anemia severa con macrocitosis marcada -Leucopenia y trombopenia, leves o ausentes -Plaquetas normales o trombocitosis -Transformación rara a LAM ( 10%) -Larga supervivencia -Elevados requerimientos transfusionales -Alteración genética única -Anemia severa con/sin otras citopenias, con/sin trombocitosis -<5% blastos en MO y <1% en SP. -Ausencia de bastones de Auer -Distrombopoyesis marcada: megacariocitos hipo o monolobulados -Frecuente pero no constante: hipoplasia eritroide; severidad de la anemia; macrocitosis Los datos favorables publicados en cuanto a supervivencia son exclusivos del síndrome. 5q-: supervivencia media: meses. Supervivencia a los 3, 5, y 10 años: 82%, 73% y 64% respectivamente. o La del5q31-33 como alteración única 14 debe matizarse siempre con los criterios de la OMS. Entre todos los pacientes posibles con del5q: El 50% de los casos ni siquiera entran en la categoría de SMD de la clasificación OMS Son un grupo muy heterogéneo que engloba síndromes mieloproliferativos, sobre todo mielofibrosis, SMD/NMP tipo LMMC y SMD con mayor porcentaje de blastos. El otro 50% sí se incluye en la categoría SMD de la OMS En cualquier caso, pensemos que si no fuera por esta genética: Aproximadamente el 10% no reúne criterios morfológicos suficientes de SMD, y serían clasificados como SMD-U. Menos del 5% se asocian con un porcentaje >15% de sideroblastos en anillo, y por lo tanto serían considerados como ARS. El 60% serían CRDM, en general diseritropoyesis y distrombopoyesis. Sólo un 20% tienen los rasgos típicos del síndrome: trombocitosis, megacariocitos monolobulados y recuento de plaquetas normal o elevado. Con estos datos es fácil entender que en el global de los SMD con 5q- aislada sin otra limitación, los resultados en cuanto a supervivencia son claramente peores que en el síndrome 5q-: supervivencia media 18 meses, supervivencia a los 3, 5, y 10 años del 37%, 26% y 21% respectivamente. o Asociación de 5q- con otras anomalías genéticas. Según los datos de GCECHG 2, la presencia de 1 sola anomalía genética adicional no supone gran cambio en cuanto a supervivencia (56 m. vs 73m.). En cambio es pronóstico empeora significativamente cuando se asocian más de dos anomalías (Supervivencia 8 meses). Por ello hay una propuesta todavía no consensuada de asimilar las anomaliás 5q aisladas con las anomalía 5q más otra adicional.
6 o Monosomía La alteración aislada es muy rara (es habitual formando parte de cariotipos complejos), si bien le son aplicables los mismos conceptos que para 5q- El síndrome 5q- NO ES el único SMD que puede cursar con trombocitosis o El nº elevado de plaquetas y distrombopoyesis significativa pueden verse en SMD con alteraciones en 3q26 EVI1: suele asociarse con fibrosis y pésimo pronóstico SMP / SMD (provisional) tipo RARS-t: 60% presentan mutación Jak2 V617F. o La ausencia de trombocitosis no es criterio excluyente de síndrome 5q-: sólo un tercio de los casos de síndrome 5q- la presentan. 4. Situaciones especiales a. SMD en los que no se dispone de genética Se trataría de aquellos casos en los que en muestras repetidas no se obtienen metafases evaluables. Suelen asociarse, aunque no de forma exclusiva, con SMD con mielofibrosis o hipoplásicos. Considerar 3 enfoques posibles con vistas a poder adscribir el paciente a un grupo pronóstico: Estudio por FISH de las anomalías ya descritas en el material de médula ósea del que se pueda disponer. El IPSS original asigna un peso relativamente escaso a la genética frente a la blastosis: si el porcentaje de blastos es >10%, ya puntúa 1 5, lo que al menos coloca al paciente con IPSS Int-2, y permite obviar el resultado de la genética. Si 10% blastos puede emplearse de base un modelo pronóstico alternativo que no incluya genética, i.e. el Modelo Español 16 (ver anexo). Equiparar este grupo de genética no-obtenible (NO son todos los SMD en los que no se dispone de genética por diversos motivos) al grupo de riesgo intermedio de la genética del IPSS, según los datos de GCECGH 17 b. Genética de SMD sin SMD En la OMS 2008 se incluyó por vez primera como una de las 3 categorías de los SMD-U (inclasificables): pacientes con citopenia(-s) persistentes(-s), <1% blastos en SP, <5% blastos en MO, rasgos displásicos insuficientes (<10% elementos) y genética sugestiva de SMD. Por esto entendemos: o Balanceadas: t(11;16)(q23;p13.3); t(3,21)(q26;q22.1); t(1;3)(p36,3;q21.2); t(2,11)(p21;q23); inv(3)(q21q26.2); t(6;9)(p23;q34). o No balanceadas: -7 ó del(7q); -5 ó del(5q); i(17q) ó t(17p); -13 ó del(13q); del(11q); del(12p) ó t(12p); del(9q); idic(x)(q13); complejo? o NO SON: +8, del(20q), -Y A efectos prácticos, son SMD, aunque durante el seguimiento debe tenderse a que se les pueda adscribir a alguna de las otras categorías.
7 c. SMD secundarios Según la OMS , deben llamarse SMD / LAM therapy-related (relacionados con terapia). Al igual que en la OMS 2001, se distinguen 2 entidades: o Relacionados con alquilantes o radioterapia. Anomalías tipo -5/-5q y/o -7/-7q y/o cariotipo complejo. Periodo de latencia en general de > 5 años. Suele haber una fase de SMD-t previa al desarrollo de LAM-t. o Relacionados con inhibidores de topoisomerasa tipo II. Suele asociarse con translocaciones balanceadas (afectando 11q23 MLL) o inversiones. Aparecen con intervalo de latencia mucho menor. El IPSS en conjunto pierde valor pronóstico, no así su genética, si bien con 2 matizaciones 18 : o Se restringe a 2 subgrupos: alto riesgo vs. intermedio + bajo (7 meses vs 11 5 meses de supervivencia media). o Mayor importancia de la complejidad: 11 7 meses si < 3 alteraciones vs. 5 5 meses si 3. Los datos de SMD-t son superponibles a las LAM secundarias (de hecho en la clasificación OMS-2008 no se distinguen de los SMD-t). A tener en cuenta que, aunque excepcionales, puede haber casos con t(15;17), inv(16) ó t(8;21), cuyo pronóstico es asimilable al de las LAM de novo Seguimiento y evaluación de la respuesta La frecuencia de estudios citogenéticos en el paciente con SMD debe individualizarse. Está indicado repetir el estudio cuando se sospecha una pérdida de respuesta o progresión. En ausencia de progresión algunos autores han sugerido hacerlos cada 6-12 meses, pero esta práctica actualmente solo está justificada en las siguientes situaciones 12 : o Paciente en espera de un trasplante alogénico para la detección precoz de una progresión. o En el pos trasplante alogénico para la detección precoz de pérdida de respuesta con el objetivo de programar una ILD o quimioterapia pos trasplante. o Paciente en tratamiento con agentes capaces de inducir una respuesta citogenética, como la lenalidomida en el síndrome 5q-. Con lenalidomida la respuesta citogenética acompaña a la respuesta hematológica y se asocia a mejor pronóstico. Se desconoce el significado pronóstico de la respuesta citogenética en el SMD con otras terapias. En la evaluación de la respuesta puede estar justificado el uso de FISH ó PCR (ej la mutación JAK2V617F) para una anomalía ya conocida por la mayor sensibilidad sobre al citogenética convencional. Sin embargo el uso de FISH no debe sustituir sino complementar al cariotipo pues las pérdidas de la respuesta se asocian a nuevas anomalías citogenéticas. Criterios de respuesta citogenética en el SMD 20 o Respuesta citogenética mayor: desaparición de la anomalía o Respuesta citogenética menor: reducción del 50% o más de la anomalía
8 6. Bibliografía seleccionada 1. WHO Classification of Tumours of Hematopoietic and Lymphoid Tissues. Swerdlow SH et al. IARC. WHO Publishing Office, Geneve Solé F et al. Identification of novel cytogenetic markers with prognostic significance in a series of 968 patients with primary myelodysplastic syndromes. Haematologica 2005; 90: Greenberg P, et al. International scoring system for evaluating prognosis in myelodysplastic syndromes. Blood.1997; 89(6): Malcovati L et al. Time-Dependent Prognostic Scoring System for Predicting Survival and Leukemic Evolution in Myelodysplastic Syndromes. J Clin Oncol 25: Haase D et al. New insights into the prognostic impact of the karyotype in MDS and correlation with subtypes: evidence from a core dataset of 2124 patients. Blood. 2007;110: Mallo M et al (GCECGH, GASMSG, IWG on MDS Cytogenetics). Prognostic Impact of the proportion of aberrant metaphases in patients with a primary MDS. Leuk Res 2009;33 (S1):S Mallo M et al. Fluorescence in situ hybridization improves the detection of 5q31 deletion in myelodysplastic syndromes without cytogenetic evidence of 5q. Haematologica 2008;93:7 8. Hellstrom-Lindberg E. Significance of JAK2 and TET2 mutations in myelodysplastic syndromes. Blood Rev 2010; 24; Kosmider O et al. TET2 mutation is an independent favorable prognostic factor in myelodysplastic syndromes (MDSs). Blood. 2009;114: Shih L-Y et al. Internal Tandem Duplication of fms-like Tyrosine Kinase 3 Is Associated with Poor Outcome in Patients with Myelodysplastic Syndrome. Cancer 2004;101: List A et al. Lenalidomide in the Myelodysplastic Syndrome with Chromosome 5q Deletion. N Engl J Med 2006;355: Haferlach C. Myelodysplastic syndromes with del(5q): indications and strategies for cytogenetic testing. Cancer Genetics and Cytogenetics 187 (2008) 101e Van der Berghe H et al. Distinct hematological disorder with deletion of long arm no. 5 chromosome. Nature. 1974; 251: Cermak J et al. A limited benefit of isolated 5q deletions on prognosis results of a long term retrospective analysis. Leuk Res 2009;33 (S1):S Galvan AB et al. Does monosomy 5 really exist in myelodysplastic syndromes and acute myeloid leukemia? Leuk Res Mar 31. [Epub] 16. Sanz GF, et al. Two regression models and a scoring system for predicting survival and planning treatment in myelodysplastic syndromes: a multivariate analysis of prognostic factors in 370 patients. Blood. 1989; 74(1): Cervera J. et al. Prognostic impact on survival of an unsuccessful conventional cytogenetic study in patients with myelodysplastic syndromes. Leuk Res 2009:33 (S1) 18. Singh Z et al. Therapy-Related Myelodysplastic Syndrome. Morphologic Subclassification May Not Be clinically Relevant. Am J Clin Pathol 2007;127: Schoch C et al. Karyotype is an independent prognostic parameter in therapy-related acute myeloid leukemia (t-aml): an analysis of 93 patients with t-aml in comparison to 1091 patients with de novo AML. Leukemia. 2004;18: Cheson BD et al. Clinical application and proposal for modification of the InternationalWorking Group (IWG) response criteria in myelodysplasia. Blood. 2006;108:
9 7. ANEXOS Clasificación OMS 2008 del SMD del adulto 1 CITOPENIAS REFRACTARIAS CON AFECTACIÓN DE UNA SOLA LÍNEA (CRDU) -Tres tipos: Anemia (AR); -Neutropenia (NR); y -Trombopenia refractaria (TR) - Displasia de una línea:<= 10% de las células de una línea con displasia. - <5% balastos y <5% de sideroblastos en anillo. Si existe pancitopenia->-smd inclasificable(smd-u). ANEMIA REFRACTARIA CON SIDEROBLASTOS EN ANILLO (ARSA) - Sideroblastos en anillo >=15% - Displasia solo en serie eritroide - <5% de blastos CITOPENIA REFRACTARIA CON DISPLASIA MULTILÍNEA (CRDM) - Citopenias, no blastos (<1% SP, <5% MO), no b.auer; monocitos <1000/mm3 - La displasia afecta al menos a dos líneas mieloides - Puede haber sideroblastos en anillo en cantidad variable Si 2-4% de blastos en SP y <5% en MO->-AREB1 ANEMIA REFRACTARIA CON EXCESO DE BLASTOS-1 (AREB-1) - Citopenias, displasia uni o multilínea, monocitos < 1000/mm3 - SP < 5% de blastos, MO: 5-9% blastos, no bastones de Auer ANEMIA REFRACTARIA CON EXCESO DE BLASTOS-2 (AREB-2) - Citopenias, displasia uni o multilínea, monocitos <1000/mm3 - SP: 5-19% de blastos o MO: 10-19% de blastos, con o sin bastones de Auer. - SP blastos <5% o MO <10% con bastones de Auer SÍNDROME DISPLÁSICO INCLASIFICABLE (SMD-U) - CRDU con pancitopenia - CRDM con 1% blastos en SP - Genética sugestiva de SMD pero rasgos displásicos insuficientes SMD ASOCIADO A 5q- COMO ÚNICA ANOMALÍA (del5q-) - Anemia. Plaquetas normales o altas - Megacariocitos número normal o alto, grandes, hipolobulados - Blastos <1% SP, <5% MO, no bastones de Auer. - Del 5q como anomalía aislada No se contempla como entidades propias en la OMS SMD hipoplásico (5-15%): Más frecuente en mujeres; Puede darse en todos los subtipos de SMD, incluidos los pediátricos; más frecuente en los SMD-t; Pancitopenia marcada; Biopsia ósea: celularidad < al 30% en pacientes < de 60años, y <20% en pacientes > de 60 años; Aumento de mastocitos; Displasia multilínea marcada; Obliga a la búsqueda de clones HPN. Frecuente fibrosis reticulínica; Citogenética inespecífica: -7, +6, +8, -5; Frecuente evolución a LAM; Diagnóstico diferencial con aplasia medular y leucemia aguda hipocelular SMD con fibrosis (10-15%): Más frecuente en AREB; Pancitopenia intensa; Ausencia de dacriocitos y de síndrome leucoeritroblástico; No esplenomegalia; Aspirado medular seco; Biopsia ósea: hipercelular, fibrosis reticulínica difusa y proliferación megacariocítica con displasia trilineal; A menudo son diagnosticados erróneamente como mielofibrosis o como SMD de bajo riesgo. Mal pronóstico
10 Anomalías citogenéticas más frecuentes en SMD No balanceadas: Las más frecuentes son:+8, -7 o del(7q), -5 o del(5q), cada una un 10%. En SMDt la anomalía del 7 y/o del 5 casi todos los casos Menos frecuentes (10% en total): del(20q), -Y, i(17q) o t(17p), -13 o del (13q), del(11q), del(12p) o t(12p), del(9q) Traslocaciones: Son infrecuentres, < del 1% cada una: t(1;3), t(2;11), inv(3)(q21q26), t(6;9). En el SMDt las más frecuentes son t(11;16) (3%) y t(3;21)(q26;q21) (2%) No existe una alteración exclusiva de los SMD diagnóstico integrado Alteraciones Genéticas/Moleculares JAK2V617F: 3% de los casos (síndrome 5q- ; ARSA-t) NRAS: frecuencia baja en la mayoría de los estudios (<5%) pero alta en algunos. TET2: 20% de los casos (40-50% en LMMC) Otras: mutaciones p53, FMS, sobreexpresión WT1 Mutaciones tipo LMA: FLT3-TKD, MLL-PTD, FLT3-LM, KITD816: en general poco frecuentes (<5%) suele asociarse con AREB-T y LMAs IPSS 3 PUNTOS 0 0,5 1 1,5 2 Blastos MO % < Citogenética Buena Intermedia Mala Citopenias 0/1 2/3 Citogenética buena: normal, del 5q,del 20q, -Y. Intermedia: otras no incluidas en bueno ni malo Malo: anomalías muy complejas (>=3), anomalías del 7 Citopenias: Hb< 10 g/dl, plaquetas < /mm3, neutrófilos < 1500/mm3 Riesgo Bajo (0 puntos): frecuencia 31%, supervivencia 5,7 años; R. Intermedio 1 (0,5-1): frecuencia 31%, supervivencia 3,5 años; R Intermedio 2 (1,5-2): frecuencia 22%, supervivencia 1,2 años; R Alto (2,5-3): frecuencia 8%, supervivencia 4 meses WPSS 4 PUNTOS Categoría OMS AR,ARSA, 5q- CRDM.CRDM- AREB-1 AREB-2 SA Cariotipo Bueno Intermedio Malo - Requerimiento No Si - transfusional Riesgo muy bajo (0 puntos): super 8,5 años; R bajo (1 p): super 6 años; R intermedio (2 p): 3,3 años; R alto (3-4 p): super 1,7 años; R muy alto (5-6 p): super 1 año Cariotipo igual que el IPSS Al menos una transfusión de hematíes cada 8 semanas en un periodo de 4 meses Indice pronóstico español 16 PUNTOS Blastos MO < 5% Edad en años <60 >=60 Plaquetas10 9 /L > <=50 Bajo riesgo: 0-1; Intermedio 2-3. Alto 4-5
11 Frecuencia de citogenética de mal pronóstico (según definición del IPSS) y los subtipos de SMD (FAB and WHO) 5 FAB % Cg adversa WHO % Cg adversa RA RARS RAEB RAEB-t AML 13% 16% 32% 32% 36% RA RARS RCMD RSCMD RAEB-I RAEB-II 16% 0% 20% 29% 31% 23% Frecuencia y mediana de supervivencia según citogenética 5 Anomalía Frecuencia % Super. med meses Cg buen pronóstico del(9q), NC 0.4 NR del(15q), NC 0.4 NR t(15q), NC 0.4 NR del(12p), NC , NC Y, del(5q), aislada , del(5q), NC del(20q), aislada del(20q), NC X, NC No (cariotipo normal) del(5q), , Y, NC Y, aislada /+1q, NC t(1q), NC t(7q), NC t(11q), NC , NC Cg pronóstico intermedio del(11q), NC , NC , aislado t(11q23), NC Rea 3q, NC , NC del(7q), aislada and NC anomalía del(11q), aislada , , NC , sole , NC Cg mal pronóstico Compleja (>3 anomalías) t(5q), NC Compleja 4-5 anomalías Compleja > NC: cariotipo no complejo; NR, no alcanzado
12 Manual de diagnóstico genético y seguimiento de las neoplasias hematológicas. Editado por el Grupo para el Estudio de las Hemopatías Malignas de Galicia (GEHMA) de la Asociación Gallega de Hematología y Hemoterapia (AGHH) Capítulo: Síndrome mielodisplásico Autores: Adriana Simiele Narvarte (Hospital POVISA, Vigo) y Carlos Ulibarrena Redondo (Servicio de Hematología, Complejo Hospitalario de Ourense) Revisión por Teresa González y Celsa Quinteiro. Fundación Pública de Medicina Xenómica (FPMX) de Galicia. Actualizado a 7/09/10.
Los sindromes mielodisplásicos son un grupo de enfermedades clonales de las células madres hematopoyéticas (Stem Cell); caracterizadas por:
 Los sindromes mielodisplásicos son un grupo de enfermedades clonales de las células madres hematopoyéticas (Stem Cell); caracterizadas por: Citopenias únicas o múltiples. Displasia en una o más de las
Los sindromes mielodisplásicos son un grupo de enfermedades clonales de las células madres hematopoyéticas (Stem Cell); caracterizadas por: Citopenias únicas o múltiples. Displasia en una o más de las
Guía de Práctica Clínica GPC. Diagnóstico y Tratamiento del Síndrome Mielodisplásico
 Guía de Práctica Clínica GPC Diagnóstico y Tratamiento del Síndrome Mielodisplásico Guía de Referencia Rápida Catalogo Maestro de Guías de Práctica Clínica: IMSS-407-10 Guía de Referencia Rápida D46 Síndromes
Guía de Práctica Clínica GPC Diagnóstico y Tratamiento del Síndrome Mielodisplásico Guía de Referencia Rápida Catalogo Maestro de Guías de Práctica Clínica: IMSS-407-10 Guía de Referencia Rápida D46 Síndromes
PAPEL DE LA CITOMETRÍA DE FLUJO EN EL DIAGNÓSTICO DE SMD Y MM
 PAPEL DE LA CITOMETRÍA DE FLUJO EN EL DIAGNÓSTICO DE SMD Y MM CITOMETRÍA DE FLUJO PARA HEMATÓLOGOS Mayo 2014 Patricia Rodríguez Domínguez Coordinadora de las Unidades de Citometría Banco Municipal de Sangre
PAPEL DE LA CITOMETRÍA DE FLUJO EN EL DIAGNÓSTICO DE SMD Y MM CITOMETRÍA DE FLUJO PARA HEMATÓLOGOS Mayo 2014 Patricia Rodríguez Domínguez Coordinadora de las Unidades de Citometría Banco Municipal de Sangre
Manual para la codificación de Neoplasias Hematológicas Neoplasias Mieloides
 Manual para la codificación de Neoplasias Hematológicas Neoplasias Mieloides 17-18 de Febrero de 2015 HEMATOPOYESIS Línea MIELOIDE Línea LINFOIDE Nuevo concepto en 1994 (REAL clasificacion) Nueva clasificación
Manual para la codificación de Neoplasias Hematológicas Neoplasias Mieloides 17-18 de Febrero de 2015 HEMATOPOYESIS Línea MIELOIDE Línea LINFOIDE Nuevo concepto en 1994 (REAL clasificacion) Nueva clasificación
Clasificación de los síndromes mielodisplásicos
 Clasificación de los síndromes mielodisplásicos Edit N. Pintos y María del Rosario Cabrejo Servicio de Hematología del Sanatorio Julio Méndez. CABA. Tel/fax 011-49027347 e-mail: [email protected]
Clasificación de los síndromes mielodisplásicos Edit N. Pintos y María del Rosario Cabrejo Servicio de Hematología del Sanatorio Julio Méndez. CABA. Tel/fax 011-49027347 e-mail: [email protected]
CURSO DE MÉDULA ÓSEA La médula ósea para patólogos generales:
 CURSO DE MÉDULA ÓSEA La médula ósea para patólogos generales: SINDROMES MIELODISPLÁSICOS (SMD), SÍNDROMES MIELODISPLÁSICOS/NEOPLASIAS MIELOPROLIFERATIVAS CRÓNICAS (SMD/NMPC) y LEUCEMIAS AGUDAS (LA) Mar
CURSO DE MÉDULA ÓSEA La médula ósea para patólogos generales: SINDROMES MIELODISPLÁSICOS (SMD), SÍNDROMES MIELODISPLÁSICOS/NEOPLASIAS MIELOPROLIFERATIVAS CRÓNICAS (SMD/NMPC) y LEUCEMIAS AGUDAS (LA) Mar
Síndromes Mielodisplásicos (SMD) Dr. Enrique Payn Borrego
 Síndromes Mielodisplásicos (SMD) Dr. Enrique Payn Borrego 1 Historia 1900: Anemia grave rápidamente progresiva con cambios simultáneos en la sangre periférica, sugestivos de leucemia (von Leube, Klin Wochenschr)
Síndromes Mielodisplásicos (SMD) Dr. Enrique Payn Borrego 1 Historia 1900: Anemia grave rápidamente progresiva con cambios simultáneos en la sangre periférica, sugestivos de leucemia (von Leube, Klin Wochenschr)
EOSINOFILIA QUÉ HACER CUANDO HAY EOSINOFILIA >1500?
 EOSINOFILIA QUÉ HACER CUANDO HAY EOSINOFILIA >1500? 1 INDICE PROTOCOLO DE ESTUDIO Introducción a las neoplasias PDGFRA, PDGFRB Y FGFR1 Sospecha: NEOPLASIA MIELOIDE Y LINFOIDE CON EOSINOFILIA Y PDGFRA+
EOSINOFILIA QUÉ HACER CUANDO HAY EOSINOFILIA >1500? 1 INDICE PROTOCOLO DE ESTUDIO Introducción a las neoplasias PDGFRA, PDGFRB Y FGFR1 Sospecha: NEOPLASIA MIELOIDE Y LINFOIDE CON EOSINOFILIA Y PDGFRA+
Sindromes Mielodisplásticos
 Sindromes Mielodisplásticos Dr. Mauricio Ocqueteau T PROGRAMA DE CANCER PONTIFICIA UNIVERSIDAD CATOLICA DE CHILE Hematopoiesis Normal 1 Oncogénesis: oncogenes y genes supresores Proto-oncogenes oncogenes
Sindromes Mielodisplásticos Dr. Mauricio Ocqueteau T PROGRAMA DE CANCER PONTIFICIA UNIVERSIDAD CATOLICA DE CHILE Hematopoiesis Normal 1 Oncogénesis: oncogenes y genes supresores Proto-oncogenes oncogenes
Sindromes Mielodisplásticos
 Sindromes Mielodisplásticos Dr. Mauricio Ocqueteau T PROGRAMA DE CANCER PONTIFICIA UNIVERSIDAD CATOLICA DE CHILE Hematopoiesis Normal Oncogénesis: oncogenes y genes supresores Proto-oncogenes oncogenes
Sindromes Mielodisplásticos Dr. Mauricio Ocqueteau T PROGRAMA DE CANCER PONTIFICIA UNIVERSIDAD CATOLICA DE CHILE Hematopoiesis Normal Oncogénesis: oncogenes y genes supresores Proto-oncogenes oncogenes
LEUCEMIA. Profa. N. Díaz, MSN
 LEUCEMIA Profa. N. Díaz, MSN 1 Definición Neoplasias más frecuentes en niños. Proliferaciones clonales malignas de células precursoras linfoides o mieloides, en distintos grados de diferenciación. Pueden
LEUCEMIA Profa. N. Díaz, MSN 1 Definición Neoplasias más frecuentes en niños. Proliferaciones clonales malignas de células precursoras linfoides o mieloides, en distintos grados de diferenciación. Pueden
: Azacitidina 100mg polvo para inyección. Indicaciones clínicas formalmente aprobadas y fecha de aprobación:
 EVALUACIÓN DE MEDICAMENTOS PARA LA ELABORACIÓN DE LA LISTA COMPLEMENTARIA DE MEDICAMENTOS PARA EL TRATAMIENTO DE ENFERMEDADES NEOPLASICAS AL PETITORIO NACIONAL UNICO DE MEDICAMENTOS ESENCIALES I. DATOS
EVALUACIÓN DE MEDICAMENTOS PARA LA ELABORACIÓN DE LA LISTA COMPLEMENTARIA DE MEDICAMENTOS PARA EL TRATAMIENTO DE ENFERMEDADES NEOPLASICAS AL PETITORIO NACIONAL UNICO DE MEDICAMENTOS ESENCIALES I. DATOS
LEUCEMIA MIELOIDE AGUDA. Luis Humberto Cruz Contreras Residente Anatomía Patológica Hospital General «Dr. Miguel Silva»
 LEUCEMIA MIELOIDE AGUDA Luis Humberto Cruz Contreras Residente Anatomía Patológica Hospital General «Dr. Miguel Silva» Definición Mínimo de Blastos en MO o Sangre periférica: FAB: 30% (20-30% MDS) WHO:
LEUCEMIA MIELOIDE AGUDA Luis Humberto Cruz Contreras Residente Anatomía Patológica Hospital General «Dr. Miguel Silva» Definición Mínimo de Blastos en MO o Sangre periférica: FAB: 30% (20-30% MDS) WHO:
- Citogenética y FISH en Leucemias Agudas.
 Contribución y avances del laboratorio en el diagnóstico y seguimiento de Leucemias agudas - Citogenética y FISH en Leucemias Agudas. Dr. Pablo López. Desarrollo de la Exposición Generalidades de Citogenética
Contribución y avances del laboratorio en el diagnóstico y seguimiento de Leucemias agudas - Citogenética y FISH en Leucemias Agudas. Dr. Pablo López. Desarrollo de la Exposición Generalidades de Citogenética
Síndromes mielodisplásicos. Aspectos diagnósticos con especial referencia a la nueva clasificación OMS/WHO
 I Síndromes mielodisplásicos. Aspectos diagnósticos con especial referencia a la nueva clasificación OMS/WHO Cuadernos de Hematología Dr. Eduardo Ríos Herranz 1 Dr. José F. Falantes González 1 Servicio
I Síndromes mielodisplásicos. Aspectos diagnósticos con especial referencia a la nueva clasificación OMS/WHO Cuadernos de Hematología Dr. Eduardo Ríos Herranz 1 Dr. José F. Falantes González 1 Servicio
ENFERMEDADES MALIGNAS DE LA SANGRE
 Enfermedades malignas de la sangre Page 1 sur 6 Atlas of Genetics and Cytogenetics in Oncology and Haematology ENFERMEDADES MALIGNAS DE LA SANGRE * Introducción Síndromes mieloproliferativos Leucemia mieloide
Enfermedades malignas de la sangre Page 1 sur 6 Atlas of Genetics and Cytogenetics in Oncology and Haematology ENFERMEDADES MALIGNAS DE LA SANGRE * Introducción Síndromes mieloproliferativos Leucemia mieloide
CITOMETRIA DE FLUJO Y LMA C.H.U.S.
 CITOMETRIA DE FLUJO Y LMA José Ángel Díaz D Arias C.H.U.S. INTRODUCCIÓN Qu Qué es la citometría a de flujo (CMF)? Es una tecnología a para caracterización n y el análisis de células c que mide y analiza
CITOMETRIA DE FLUJO Y LMA José Ángel Díaz D Arias C.H.U.S. INTRODUCCIÓN Qu Qué es la citometría a de flujo (CMF)? Es una tecnología a para caracterización n y el análisis de células c que mide y analiza
NMP PH NEGATIVAS: POLICITEMIA VERA, TROMBOCITEMIA ESENCIAL Y MIELOFIBROSIS
 NMP PH NEGATIVAS: POLICITEMIA VERA, TROMBOCITEMIA ESENCIAL Y MIELOFIBROSIS 1. Tablas de resumen de la pruebas genéticas. SOSPECHA DE POLICITEMIA VERA (PV) Diagnóstico Panel PV Muestra Observaciones / significado
NMP PH NEGATIVAS: POLICITEMIA VERA, TROMBOCITEMIA ESENCIAL Y MIELOFIBROSIS 1. Tablas de resumen de la pruebas genéticas. SOSPECHA DE POLICITEMIA VERA (PV) Diagnóstico Panel PV Muestra Observaciones / significado
Grupo Andaluz de Síndromes Mielodisplásicos GUÍA ANDALUZA DE SÍNDROMES MIELODISPLÁSICOS
 Grupo Andaluz de Síndromes Mielodisplásicos GUÍA ANDALUZA DE SÍNDROMES MIELODISPLÁSICOS Grupo Andaluz de Síndromes Mielodisplásicos GUÍA ANDALUZA DE SÍNDROMES MIELODISPLÁSICOS Cualquier forma de reproducción,
Grupo Andaluz de Síndromes Mielodisplásicos GUÍA ANDALUZA DE SÍNDROMES MIELODISPLÁSICOS Grupo Andaluz de Síndromes Mielodisplásicos GUÍA ANDALUZA DE SÍNDROMES MIELODISPLÁSICOS Cualquier forma de reproducción,
Técnicas de citogenética molecular y sus aplicaciones
 Técnicas de citogenética molecular y sus aplicaciones Dra. Blanca Espinet, Dr. Marta Salido, Dr. Francesc Solé. Laboratori de Citogenètica i Biologia Molecular Servei de Patologia Hospital de Mar de Barcelona
Técnicas de citogenética molecular y sus aplicaciones Dra. Blanca Espinet, Dr. Marta Salido, Dr. Francesc Solé. Laboratori de Citogenètica i Biologia Molecular Servei de Patologia Hospital de Mar de Barcelona
LEUCEMIA MIELOIDE CRÓNICA
 LEUCEMIA MIELOIDE CRÓNICA 1. Tablas de resumen de las pruebas genéticas Panel Muestra Observaciones Cariotipo MO Siempre. En SP si aspirado de MO seco FISH MO Muy aconsejable. Obligado si cariotipo no
LEUCEMIA MIELOIDE CRÓNICA 1. Tablas de resumen de las pruebas genéticas Panel Muestra Observaciones Cariotipo MO Siempre. En SP si aspirado de MO seco FISH MO Muy aconsejable. Obligado si cariotipo no
NMP PH NEGATIVAS: POLICITEMIA VERA, TROMBOCITEMIA ESENCIAL Y MIELOFIBROSIS
 NMP PH NEGATIVAS: POLICITEMIA VERA, TROMBOCITEMIA ESENCIAL Y MIELOFIBROSIS 1. Tablas de resumen de la pruebas genéticas. SOSPECHA DE POLICITEMIA VERA (PV) Panel PV Muestra Observaciones / significado Diagnóstico
NMP PH NEGATIVAS: POLICITEMIA VERA, TROMBOCITEMIA ESENCIAL Y MIELOFIBROSIS 1. Tablas de resumen de la pruebas genéticas. SOSPECHA DE POLICITEMIA VERA (PV) Panel PV Muestra Observaciones / significado Diagnóstico
MANEJO PRÁCTICO DE AZACITIDINA Dr. Carlos Ulibarrena Redondo Complexo Hospitalario de Ourense Mayo-2010 Versión 1.4
 A.- INDICACIONES APROBADAS POR LA E.M.E.A. (1) Adultos NO candidatos a TMO con alguna de las siguientes patologías: - Síndrome mielodisplásico según la clasificación de la OMS (2) con IPSS (3) Int-2 ó
A.- INDICACIONES APROBADAS POR LA E.M.E.A. (1) Adultos NO candidatos a TMO con alguna de las siguientes patologías: - Síndrome mielodisplásico según la clasificación de la OMS (2) con IPSS (3) Int-2 ó
Genética Casos clínicos
 Perpetuum Mobile Genética Casos clínicos LAM: casos clínicos El cariotipo es un factor pronóstico independiente en LAM El 40% de las LAM presentan cariotipo normal (intermedio) En Galicia, al menos, 216
Perpetuum Mobile Genética Casos clínicos LAM: casos clínicos El cariotipo es un factor pronóstico independiente en LAM El 40% de las LAM presentan cariotipo normal (intermedio) En Galicia, al menos, 216
VI JORNADA DE FORMACIÓN INTERHOSPITALARIA DEL LABORATORIO CLÍNICO
 VI JORNADA DE FORMACIÓN INTERHOSPITALARIA DEL LABORATORIO CLÍNICO 7. ANTICUERPOS ANTIPÉPTIDO CÍCLICO CITRULINADO EN ARTRITIS REUMATOIDE DAVID PRIETO RUIZ RIII. ANÁLISIS CLÍNICOS ARTRITIS REUMATOIDE GENERALIDADES
VI JORNADA DE FORMACIÓN INTERHOSPITALARIA DEL LABORATORIO CLÍNICO 7. ANTICUERPOS ANTIPÉPTIDO CÍCLICO CITRULINADO EN ARTRITIS REUMATOIDE DAVID PRIETO RUIZ RIII. ANÁLISIS CLÍNICOS ARTRITIS REUMATOIDE GENERALIDADES
SERVICIO DE MEDICINA INTERNA HOSPITAL DE LEÓN
 Hemoglobina: 9,2 Leucocitos: 5.600 Hemoglobina: 9,2 Leucocitos: 5.600 Blastos 1%, Promielo 1%, Mielo 2%, Hemoglobina: 9,2 Leucocitos: 5.600 Blastos 1%, Promielo 1%, Mielo 2%, Metamielo 6%, Cayado 7%, Segmentados
Hemoglobina: 9,2 Leucocitos: 5.600 Hemoglobina: 9,2 Leucocitos: 5.600 Blastos 1%, Promielo 1%, Mielo 2%, Hemoglobina: 9,2 Leucocitos: 5.600 Blastos 1%, Promielo 1%, Mielo 2%, Metamielo 6%, Cayado 7%, Segmentados
Mielodisplasia en Pacientes Pediátricos. Evaluación de Clasificaciones Actuales
 Rev Chil Pediatr 2009; 80 (4): 339-346 ARTÍCULO ORIGINAL RESEARCH REPORT Mielodisplasia en Pacientes Pediátricos. Evaluación de Clasificaciones Actuales VERÓNICA OYARCE L. 1, NATALIE RODRÍGUEZ Z. 2,3,
Rev Chil Pediatr 2009; 80 (4): 339-346 ARTÍCULO ORIGINAL RESEARCH REPORT Mielodisplasia en Pacientes Pediátricos. Evaluación de Clasificaciones Actuales VERÓNICA OYARCE L. 1, NATALIE RODRÍGUEZ Z. 2,3,
PROTOCOLO SINDROMES MIELODISPLÁSICOS
 PROTOCOLO SINDROMES MIELODISPLÁSICOS INTRODUCCIÓN Los síndromes mielodisplásicos (SMD) constituyen un grupo de trastornos clonales de la célula madre hematopoyética, caracterizados por hematopoyesis infectiva
PROTOCOLO SINDROMES MIELODISPLÁSICOS INTRODUCCIÓN Los síndromes mielodisplásicos (SMD) constituyen un grupo de trastornos clonales de la célula madre hematopoyética, caracterizados por hematopoyesis infectiva
Cas clínic citològic
 Cas clínic citològic Rosario López Servei d'hematologia. Hospital Universitari Sant Joan de Déu Althaia. Xarxa Assistencial de Manresa XXXVII Diada de la Societat Catalana d'hematologia i Hemoteràpia:
Cas clínic citològic Rosario López Servei d'hematologia. Hospital Universitari Sant Joan de Déu Althaia. Xarxa Assistencial de Manresa XXXVII Diada de la Societat Catalana d'hematologia i Hemoteràpia:
Congreso Nacional del Laboratorio Clínico 2015
 CITOLOGÍA DE SANGRE PERIFÉRICA Y AUTOMATIZACIÓN EN EL DIAGNÓSTICO DE LAS ENFERMEDADES HEMATOLÓGICAS MALIGNAS 8 de Octubre del 2015 Anna Merino, Cristian Morales-Indiano y Santiago Alférez 1.Cómo la citología
CITOLOGÍA DE SANGRE PERIFÉRICA Y AUTOMATIZACIÓN EN EL DIAGNÓSTICO DE LAS ENFERMEDADES HEMATOLÓGICAS MALIGNAS 8 de Octubre del 2015 Anna Merino, Cristian Morales-Indiano y Santiago Alférez 1.Cómo la citología
Datos de filiación Protocolo intergrupos Pethema-Geltamo BURKIMAB-13
 Datos de filiación DATOS DEL PACIENTE Nº registro: Edad: Fecha de nacimiento: Sexo: Varón Mujer DATOS DEL CENTRO Hospital: Dirección: Teléfono: Fax: Médico responsable: E-mail: Diagnóstico: LAL3 Linfoma
Datos de filiación DATOS DEL PACIENTE Nº registro: Edad: Fecha de nacimiento: Sexo: Varón Mujer DATOS DEL CENTRO Hospital: Dirección: Teléfono: Fax: Médico responsable: E-mail: Diagnóstico: LAL3 Linfoma
LEUCEMIAS AGUDAS. LIC. MACZY GONZÁLEZ RINCÓN MgSc CÁTEDRA DE HEMATOLOGÍA ESCUELA DE BIOANÁLISIS UNIVERSIDAD DEL ZULIA
 LEUCEMIAS AGUDAS LIC. MACZY GONZÁLEZ RINCÓN MgSc CÁTEDRA DE HEMATOLOGÍA ESCUELA DE BIOANÁLISIS UNIVERSIDAD DEL ZULIA LEUCEMIAS AGUDAS CONCEPTO: GRUPO DE ENFERMEDADES CLONALES Y MALIGNAS DEL TEJIDO HEMATOPOYETICO,
LEUCEMIAS AGUDAS LIC. MACZY GONZÁLEZ RINCÓN MgSc CÁTEDRA DE HEMATOLOGÍA ESCUELA DE BIOANÁLISIS UNIVERSIDAD DEL ZULIA LEUCEMIAS AGUDAS CONCEPTO: GRUPO DE ENFERMEDADES CLONALES Y MALIGNAS DEL TEJIDO HEMATOPOYETICO,
SÍNDROMES MIELODISPLASTICOS Diagnóstico, estudio y tratamiento
 Manual de Prácticas Médicas- Hospital Hermanos Ameijeiras SÍNDROMES MIELODISPLASTICOS Diagnóstico, estudio y tratamiento Autor Servicio Dr. José Carnot Uria Hematología Otros servicios Anatomía Patológica,
Manual de Prácticas Médicas- Hospital Hermanos Ameijeiras SÍNDROMES MIELODISPLASTICOS Diagnóstico, estudio y tratamiento Autor Servicio Dr. José Carnot Uria Hematología Otros servicios Anatomía Patológica,
ASTURIAS, CANTABRIA, EUSKADI, ANDALUCÍA
 CANARIAS ASTURIAS, CANTABRIA, EUSKADI, ANDALUCÍA GRUPO CATEGORÍA Nº IMG 1. ANEMIAS (EXCEPTO ANEMIA APLÁSICA) 1.1. ANEMIAS CARENCIALES 1.1.1. ANEMIA FERROPÉNICA 1.1.2. ANEMIA MEGALOBLÁSTICA 1.2. ANEMIAS
CANARIAS ASTURIAS, CANTABRIA, EUSKADI, ANDALUCÍA GRUPO CATEGORÍA Nº IMG 1. ANEMIAS (EXCEPTO ANEMIA APLÁSICA) 1.1. ANEMIAS CARENCIALES 1.1.1. ANEMIA FERROPÉNICA 1.1.2. ANEMIA MEGALOBLÁSTICA 1.2. ANEMIAS
PATOLOGÍA MOLECULAR Y CITOLOGÍA. APLICACIONES DEL FISH EN LA CITOLOGIA NO GINECOLOGICA
 PATOLOGÍA MOLECULAR Y CITOLOGÍA. APLICACIONES DEL FISH EN LA CITOLOGIA NO GINECOLOGICA María Dolores Lozano Departamento de Anatomía Patológica. Clínica Universitaria. Universidad de Navarra. Pamplona.
PATOLOGÍA MOLECULAR Y CITOLOGÍA. APLICACIONES DEL FISH EN LA CITOLOGIA NO GINECOLOGICA María Dolores Lozano Departamento de Anatomía Patológica. Clínica Universitaria. Universidad de Navarra. Pamplona.
PONTIFICIA UNIVERSIDAD CATÓLICA DEL ECUADOR ESCUELA DE BIOANÁLISIS 1. DATOS INFORMATIVOS:
 PONTIFICIA UNIVERSIDAD CATÓLICA DEL ECUADOR ESCUELA DE BIOANÁLISIS 1. DATOS INFORMATIVOS: MATERIA: GENÉTICA CODIGO: 20080 CARRERA: BIOANLISIS CLÍNICO / HISTOCITOLOGÍA NIVEL: SÉPTIMO No. CRÉDITOS: 3 PROFESOR:
PONTIFICIA UNIVERSIDAD CATÓLICA DEL ECUADOR ESCUELA DE BIOANÁLISIS 1. DATOS INFORMATIVOS: MATERIA: GENÉTICA CODIGO: 20080 CARRERA: BIOANLISIS CLÍNICO / HISTOCITOLOGÍA NIVEL: SÉPTIMO No. CRÉDITOS: 3 PROFESOR:
Pregunta y Conoce tu Respuesta
 En LMC Pregunta y Conoce tu Hematológica Citogenética Molecular Conoce la leucemia mieloide crónica Qué es la leucemia mieloide crónica? La leucemia mieloide crónica (LMC) es una enfermedad en la que las
En LMC Pregunta y Conoce tu Hematológica Citogenética Molecular Conoce la leucemia mieloide crónica Qué es la leucemia mieloide crónica? La leucemia mieloide crónica (LMC) es una enfermedad en la que las
LA MULTIMORBILIDAD Y LA EDAD EN HEMATOLOGÍA ONCOLÓGICA LEUCÉMIA MIELOBLÁSTICA AGUDA Y SÍNDROME MIELODISPLÁSICO
 LA MULTIMORBILIDAD Y LA EDAD EN HEMATOLOGÍA ONCOLÓGICA LEUCÉMIA MIELOBLÁSTICA AGUDA Y SÍNDROME MIELODISPLÁSICO Montse Arnan Sangerman Hospital Duran i Reynals MArç 2016 CAMBIOS DEMOGRÁFICOS EL FIN DE LA
LA MULTIMORBILIDAD Y LA EDAD EN HEMATOLOGÍA ONCOLÓGICA LEUCÉMIA MIELOBLÁSTICA AGUDA Y SÍNDROME MIELODISPLÁSICO Montse Arnan Sangerman Hospital Duran i Reynals MArç 2016 CAMBIOS DEMOGRÁFICOS EL FIN DE LA
MÓDULO BÁSICO 2015-2016
 TRASPLANTE DE PROGENITORES HEMATOPOYÉTICOS MÓDULO BÁSICO 2015-2016 Módulo 9 Tema 21: Papel del trasplante de progenitores hematopoyéticos en leucemias agudas. Guillermo Martín Sánchez Especialista en Hematología
TRASPLANTE DE PROGENITORES HEMATOPOYÉTICOS MÓDULO BÁSICO 2015-2016 Módulo 9 Tema 21: Papel del trasplante de progenitores hematopoyéticos en leucemias agudas. Guillermo Martín Sánchez Especialista en Hematología
GPC. Guía de Referencia Rápida. Diagnóstico y Tratamiento de Púrpura Trombocitopénica Inmunológica. Guía de Práctica Clínica
 Guía de Referencia Rápida Diagnóstico y Tratamiento de Púrpura Trombocitopénica Inmunológica GPC Guía de Práctica Clínica Catálogo maestro de guías de práctica clínica: IMSS-143-08 Guía de Referencia Rápida
Guía de Referencia Rápida Diagnóstico y Tratamiento de Púrpura Trombocitopénica Inmunológica GPC Guía de Práctica Clínica Catálogo maestro de guías de práctica clínica: IMSS-143-08 Guía de Referencia Rápida
PROTOCOLO SINDROMES MIELODISPLÁSICOS
 PROTOCOLO SINDROMES MIELODISPLÁSICOS INTRODUCCIÓN Los síndromes mielodisplásicos (SMD) constituyen un grupo de trastornos clonales de la célula madre hematopoyética, caracterizados por hematopoyesis infectiva
PROTOCOLO SINDROMES MIELODISPLÁSICOS INTRODUCCIÓN Los síndromes mielodisplásicos (SMD) constituyen un grupo de trastornos clonales de la célula madre hematopoyética, caracterizados por hematopoyesis infectiva
SÍNDROME DE ALPORT 20
 20 SÍNDROME DE ALPORT 10 Introducción: El síndrome de Alport (SA) es una enfermedad hereditaria con una prevalencia aproximada de 1 caso por cada 50.000 nacidos vivos, aunque probablemente esté infradiagnosticado
20 SÍNDROME DE ALPORT 10 Introducción: El síndrome de Alport (SA) es una enfermedad hereditaria con una prevalencia aproximada de 1 caso por cada 50.000 nacidos vivos, aunque probablemente esté infradiagnosticado
UNIVERSIDAD DE SALAMANCA DEPARTAMENTO DE MEDICINA HEMATOLOGÍA
 UNIVERSIDAD DE SALAMANCA DEPARTAMENTO DE MEDICINA HEMATOLOGÍA TESIS DOCTORAL DATOS CLÍNICO-BIOLÓGICOS QUE PERMITEN SUBCLASIFICAR A LOS PACIENTES CON SÍNDROME MIELODISPLÁSICO EN NUEVOS GRUPOS DE RIESGO
UNIVERSIDAD DE SALAMANCA DEPARTAMENTO DE MEDICINA HEMATOLOGÍA TESIS DOCTORAL DATOS CLÍNICO-BIOLÓGICOS QUE PERMITEN SUBCLASIFICAR A LOS PACIENTES CON SÍNDROME MIELODISPLÁSICO EN NUEVOS GRUPOS DE RIESGO
CLUB DE PATOLOGÍA DE LA MAMA
 CLUB DE PATOLOGÍA DE LA MAMA Aprendiendo de nuestros errores Laura López Vilaró CASO CLÍNICO Mujer 66 años sin antecedentes patológicos destacables Nódulo retro-areolar de mama derecha en mamografía del
CLUB DE PATOLOGÍA DE LA MAMA Aprendiendo de nuestros errores Laura López Vilaró CASO CLÍNICO Mujer 66 años sin antecedentes patológicos destacables Nódulo retro-areolar de mama derecha en mamografía del
FICHAS GUÍAS ESPAÑOLAS PARA EL DIAGNÓSTICO Y TRATAMIENTO DE LOS SMD Y LA LMMC
 GUÍAS ESPAÑOLAS PARA EL DIAGNÓSTICO Y TRATAMIENTO DE LOS SMD Y LA LMMC FICHAS DIAGNÓSTICO DE LOS SMD EVALUACIÓN BASAL 3 ESTRATIFICACIÓN PRONÓSTICA 4 SOPORTE 5 BAJO RIESGO 6 ALTO RIESGO 7 LMMC AGRADECIMIENTOS
GUÍAS ESPAÑOLAS PARA EL DIAGNÓSTICO Y TRATAMIENTO DE LOS SMD Y LA LMMC FICHAS DIAGNÓSTICO DE LOS SMD EVALUACIÓN BASAL 3 ESTRATIFICACIÓN PRONÓSTICA 4 SOPORTE 5 BAJO RIESGO 6 ALTO RIESGO 7 LMMC AGRADECIMIENTOS
Transfusión y pronóstico en los síndromes mielodisplásicos. Dr. Arturo Pereira Hemoterapia y Hemostasia
 Transfusión y pronóstico en los síndromes mielodisplásicos Dr. Arturo Pereira Hemoterapia y Hemostasia Introducción SINDROMES MIELODISPLASICOS Hemopoyesis displásica. Anemia y otras citopenias. Marcada
Transfusión y pronóstico en los síndromes mielodisplásicos Dr. Arturo Pereira Hemoterapia y Hemostasia Introducción SINDROMES MIELODISPLASICOS Hemopoyesis displásica. Anemia y otras citopenias. Marcada
Guía para el manejo de los pacientes con síndrome mielodisplásico en los Servicios de Salud de Petróleos Mexicanos
 ARTÍCULOS ESPECIALES MÉDICO/QUIRÚRGICOS Guía para el manejo de los pacientes con síndrome mielodisplásico en los Servicios de Salud de Petróleos Mexicanos Mijangos Huesca FJ a Galindo Delgado P b Bahena
ARTÍCULOS ESPECIALES MÉDICO/QUIRÚRGICOS Guía para el manejo de los pacientes con síndrome mielodisplásico en los Servicios de Salud de Petróleos Mexicanos Mijangos Huesca FJ a Galindo Delgado P b Bahena
Neoplasias Mieloproliferativas
 CURSO DE MORFOLOGÍA HEMATOLÓGICA Neoplasias Mieloproliferativas Caracas, 10 de julio de 2015 Osiris da Costa I Banco Municipal de Sangre SOCIEDAD VENEZOLANA DE HEMATOLOGÍA EDUCACIÓN MÉDICA CONTÍNUA DECLARACIÓN
CURSO DE MORFOLOGÍA HEMATOLÓGICA Neoplasias Mieloproliferativas Caracas, 10 de julio de 2015 Osiris da Costa I Banco Municipal de Sangre SOCIEDAD VENEZOLANA DE HEMATOLOGÍA EDUCACIÓN MÉDICA CONTÍNUA DECLARACIÓN
Síndromes mielodisplásicos
 SOCIEDAD ARGENTINA DE HEMATOLOGÍA Síndromes mielodisplásicos COORDINADORA Dra. Prates, M. Virginia AUTORES Dra. Basquiera, Ana L. Dra. Belli, Carolina Dra. Canónico, Virginia Dra. Fazio, Patricia Dra.
SOCIEDAD ARGENTINA DE HEMATOLOGÍA Síndromes mielodisplásicos COORDINADORA Dra. Prates, M. Virginia AUTORES Dra. Basquiera, Ana L. Dra. Belli, Carolina Dra. Canónico, Virginia Dra. Fazio, Patricia Dra.
CÁNCER DE PULMÓN. Grado de conocimiento y concienciación (pacientes y Opinión Pública)
 CÁNCER DE PULMÓN Grado de conocimiento y concienciación (pacientes y Opinión Pública) Una encuesta de la Coalición Global sobre Cáncer de Pulmón (GLCC) realizada a 1.250 ciudadanos sanos y a 150 enfermos
CÁNCER DE PULMÓN Grado de conocimiento y concienciación (pacientes y Opinión Pública) Una encuesta de la Coalición Global sobre Cáncer de Pulmón (GLCC) realizada a 1.250 ciudadanos sanos y a 150 enfermos
Panel multi-gen para análisis de genes relacionados con Leucemia Mieloide Aguda (LMA) mediante Next Generation Sequencing
 Panel multi-gen para análisis de genes relacionados con Leucemia Mieloide Aguda (LMA) mediante Next Generation Sequencing Dra. Ana Martínez-Hortigüela Jornada de Innovación en el Sector Sanitario IDIS
Panel multi-gen para análisis de genes relacionados con Leucemia Mieloide Aguda (LMA) mediante Next Generation Sequencing Dra. Ana Martínez-Hortigüela Jornada de Innovación en el Sector Sanitario IDIS
Hipotiroidismo Subclínico. Dr. Fernando Andrés Jiménez Endocrinología Hospital San Juan de Dios. blogdehormonas.wordpress.com
 Hipotiroidismo Subclínico Dr. Fernando Andrés Jiménez Endocrinología Hospital San Juan de Dios blogdehormonas.wordpress.com TIROIDITIS DE HASHIMOTO Fase de hipotiroidismo subclínico: TSH elevado (menor
Hipotiroidismo Subclínico Dr. Fernando Andrés Jiménez Endocrinología Hospital San Juan de Dios blogdehormonas.wordpress.com TIROIDITIS DE HASHIMOTO Fase de hipotiroidismo subclínico: TSH elevado (menor
Caracterización molecular y pronóstica de las LMA con cariotipo normal. Barcelona, 23 de octubre del 2009
 Caracterización molecular y pronóstica de las LMA con cariotipo normal Barcelona, 23 de octubre del 2009 LMA cariotipo normal LMA-CN: 45% de las LMA de adulto. Supervivencia a 5 años: 24-42%. Lowenberg,
Caracterización molecular y pronóstica de las LMA con cariotipo normal Barcelona, 23 de octubre del 2009 LMA cariotipo normal LMA-CN: 45% de las LMA de adulto. Supervivencia a 5 años: 24-42%. Lowenberg,
Síndromes mielodisplásicos y síndromes de superposición mielodisplasia/neoplasia mieloproliferativa
 Síndromes mielodisplásicos y síndromes de superposición mielodisplasia/neoplasia mieloproliferativa Coordinadores: Flores, María Gabriela [email protected] Belli, Carolina [email protected]
Síndromes mielodisplásicos y síndromes de superposición mielodisplasia/neoplasia mieloproliferativa Coordinadores: Flores, María Gabriela [email protected] Belli, Carolina [email protected]
Controversias diagnósticas en policitemia vera, trombocitemia
 Controversias diagnósticas en policitemia vera, trombocitemia esencial y mielofibrosis Francisco Cervantes Servicio de Hematología, Hospital Clínic, Universidad de Barcelona Introducción Las neoplasias
Controversias diagnósticas en policitemia vera, trombocitemia esencial y mielofibrosis Francisco Cervantes Servicio de Hematología, Hospital Clínic, Universidad de Barcelona Introducción Las neoplasias
Estudio de los Síndromes Mielodisplásicos en la población gallega: Análisis descriptivo y pronóstico.
 FACULTADE DE MEDICINA E ODONTOLOXÍA Departamento de Medicina Estudio de los Síndromes Mielodisplásicos en la población gallega: Análisis descriptivo y pronóstico. Nicolás Antonio Díaz Varela Curso 2013-2014
FACULTADE DE MEDICINA E ODONTOLOXÍA Departamento de Medicina Estudio de los Síndromes Mielodisplásicos en la población gallega: Análisis descriptivo y pronóstico. Nicolás Antonio Díaz Varela Curso 2013-2014
Recaídas posterior a Trasplante de Médula Ósea. V jornadas de Trasplante de Médula ósea Dr. Jorge Herrera Maracaibo 2016 Marcos Hernández J CHET UC
 Recaídas posterior a Trasplante de Médula Ósea V jornadas de Trasplante de Médula ósea Dr. Jorge Herrera Maracaibo 2016 Marcos Hernández J CHET UC RECAÍDAS POSTERIOR A TRASPLANTE Indicaciones de consulta
Recaídas posterior a Trasplante de Médula Ósea V jornadas de Trasplante de Médula ósea Dr. Jorge Herrera Maracaibo 2016 Marcos Hernández J CHET UC RECAÍDAS POSTERIOR A TRASPLANTE Indicaciones de consulta
HISTORIA NATURAL Y MANIFESTACIONES. de la INFECCION POR VIH
 HISTORIA NATURAL Y MANIFESTACIONES CLÍNICAS de la INFECCION POR VIH Dra C. REDONDO UNIDAD VIH. SERVICIO de MEDICINA INTERNA. HOSPITAL UNIVERSITARIO VIRGEN DE LA ARRIXACA.MURCIA. ESPAÑA Células diana de
HISTORIA NATURAL Y MANIFESTACIONES CLÍNICAS de la INFECCION POR VIH Dra C. REDONDO UNIDAD VIH. SERVICIO de MEDICINA INTERNA. HOSPITAL UNIVERSITARIO VIRGEN DE LA ARRIXACA.MURCIA. ESPAÑA Células diana de
Síndromes mielodisplásicos en pediatría. Realidad en nuestro país de una enfermedad infrecuente y grave
 Síndromes mielodisplásicos en pediatría. Realidad en nuestro país de una enfermedad infrecuente y grave Myelodysplastic Syndromes in Pediatric patients. Reality of a rare and severe disease Escobar NF,
Síndromes mielodisplásicos en pediatría. Realidad en nuestro país de una enfermedad infrecuente y grave Myelodysplastic Syndromes in Pediatric patients. Reality of a rare and severe disease Escobar NF,
Aproximación al tema por medio de algunos pacientes vividos estos últimos dos años y que se presentaron con un cuadro clínico muy similar
 Aproximación al tema por medio de algunos pacientes vividos estos últimos dos años y que se presentaron con un cuadro clínico muy similar EDAD (AÑOS) 49 40 32 44 45 32 22 24 ENFERMEDAD ACTUAL Disnea Disnea
Aproximación al tema por medio de algunos pacientes vividos estos últimos dos años y que se presentaron con un cuadro clínico muy similar EDAD (AÑOS) 49 40 32 44 45 32 22 24 ENFERMEDAD ACTUAL Disnea Disnea
Dra. Ada Hernández. Conferencias dictadas por el Dr. Pierre Fenaux y el Dr. Plastzbecker.
 Dra. Ada Hernández. Conferencias dictadas por el Dr. Pierre Fenaux y el Dr. Plastzbecker. SOCIEDAD VENEZOLANA DE HEMATOLOGÍA EDUCACIÓN MÉDICA CONTÍNUA DECLARACIÓN DE POTENCIALES CONFLICTOS DE INTERESES
Dra. Ada Hernández. Conferencias dictadas por el Dr. Pierre Fenaux y el Dr. Plastzbecker. SOCIEDAD VENEZOLANA DE HEMATOLOGÍA EDUCACIÓN MÉDICA CONTÍNUA DECLARACIÓN DE POTENCIALES CONFLICTOS DE INTERESES
Citogenética: breve descripción de las principales técnicas utilizadas para realizar un estudio cromosómico
 Diagnóstico Bioquímico Citogenética: breve descripción de las principales técnicas utilizadas para realizar un estudio cromosómico Introducción Dra. Pilar Corral diversas técnicas de bandeo cromosómico
Diagnóstico Bioquímico Citogenética: breve descripción de las principales técnicas utilizadas para realizar un estudio cromosómico Introducción Dra. Pilar Corral diversas técnicas de bandeo cromosómico
Hemograma. El Hemograma es una parte del análisis de sangre que nos proporciona el recuento de glóbulos rojos, blancos y plaquetas.
 10.Prevención de la salud Hemograma El Hemograma es una parte del análisis de sangre que nos proporciona el recuento de glóbulos rojos, blancos y plaquetas. 11 Para poder realizar un hemograma la sangre
10.Prevención de la salud Hemograma El Hemograma es una parte del análisis de sangre que nos proporciona el recuento de glóbulos rojos, blancos y plaquetas. 11 Para poder realizar un hemograma la sangre
2 o. Curso De Formación Continuada en Hematología
 2 o Curso De Formación Continuada en Hematología 11 de Febrero 13 de Marzo 8 de Abril 15 de Mayo 16 de Octubre 13 de Noviembre 2014 Director Dr. Francesc Bosch Jefe de Servicio de Hematología. Hospital
2 o Curso De Formación Continuada en Hematología 11 de Febrero 13 de Marzo 8 de Abril 15 de Mayo 16 de Octubre 13 de Noviembre 2014 Director Dr. Francesc Bosch Jefe de Servicio de Hematología. Hospital
Leucemias agudas Sindomes Mielodisplásticos Leucemia Mieloide Crónica. Juan Dupont CEMIC AMA 2018
 Leucemias agudas Sindomes Mielodisplásticos Leucemia Mieloide Crónica Juan Dupont CEMIC AMA 2018 LA s. Definición y epidemiologìa: Proliferación clonal de células hemato/linfopoyèticas inmaduras y anormales
Leucemias agudas Sindomes Mielodisplásticos Leucemia Mieloide Crónica Juan Dupont CEMIC AMA 2018 LA s. Definición y epidemiologìa: Proliferación clonal de células hemato/linfopoyèticas inmaduras y anormales
Estudios Citogenéticos y Mecanismos Moleculares en los Síndromes Mielodisplásicos
 Estudios Citogenéticos y Mecanismos Moleculares en los Síndromes Mielodisplásicos Carolina B. Belli 1, Silvia Benasayag 2, María I. Gallino 2, Walter A. Correa 2, Irene B. Larripa 1 Departamento de Genética,
Estudios Citogenéticos y Mecanismos Moleculares en los Síndromes Mielodisplásicos Carolina B. Belli 1, Silvia Benasayag 2, María I. Gallino 2, Walter A. Correa 2, Irene B. Larripa 1 Departamento de Genética,
Pulmón y Síndrome de Sjögren primario: afección bronquial o intersticial? S. Medicina Interna H. U. Puerta del Mar (Cádiz)
 Pulmón y Síndrome de Sjögren primario: afección bronquial o intersticial? María a José Soto CárdenasC S. Medicina Interna H. U. Puerta del Mar (Cádiz) Síndrome de Sjögren Afectación glandular Xerostomía
Pulmón y Síndrome de Sjögren primario: afección bronquial o intersticial? María a José Soto CárdenasC S. Medicina Interna H. U. Puerta del Mar (Cádiz) Síndrome de Sjögren Afectación glandular Xerostomía
GUÍAS ESPAÑOLAS PARA EL DIAGNÓSTICO Y TRATAMIENTO DE LOS SMD Y LA LMMC
 GUÍAS ESPAÑOLAS PARA EL DIAGNÓSTICO Y TRATAMIENTO DE LOS SMD Y LA LMMC VERSIÓN REDUCIDA Grupo Español de Síndromes Mielodisplásicos (GESMD) 1ª EDICIÓN SEPTIEMBRE 2013 Sociedad Española de Hematología y
GUÍAS ESPAÑOLAS PARA EL DIAGNÓSTICO Y TRATAMIENTO DE LOS SMD Y LA LMMC VERSIÓN REDUCIDA Grupo Español de Síndromes Mielodisplásicos (GESMD) 1ª EDICIÓN SEPTIEMBRE 2013 Sociedad Española de Hematología y
CONCEPTOS PRACTICOS EN EL MANEJO DE LOS SINDROMES MIELODISPLASICOS Y LAS NEOPLASIAS MIELOPROLIFERATIVAS
 CONCEPTOS PRACTICOS EN EL MANEJO DE LOS SINDROMES MIELODISPLASICOS Y LAS NEOPLASIAS MIELOPROLIFERATIVAS POR QUE ESTE TEMA Porque existe una subutilización del diagnostico histopatológico en éste área Porque
CONCEPTOS PRACTICOS EN EL MANEJO DE LOS SINDROMES MIELODISPLASICOS Y LAS NEOPLASIAS MIELOPROLIFERATIVAS POR QUE ESTE TEMA Porque existe una subutilización del diagnostico histopatológico en éste área Porque
Instructivo para la derivación de material
 LABORATORIO ESPECIALIZADO DE HEMATOLOGÍA, ONCOLOGÍA Y GENÉTICA Instructivo para la derivación de material 1. Estudios de Anemia: Extendidos de sangre periférica con gota directa de la aguja (sin anticoagulante)
LABORATORIO ESPECIALIZADO DE HEMATOLOGÍA, ONCOLOGÍA Y GENÉTICA Instructivo para la derivación de material 1. Estudios de Anemia: Extendidos de sangre periférica con gota directa de la aguja (sin anticoagulante)
Importancia de la genética en pediatría
 Neonatología Tema 2 Genética. Clasificación de las anomalías cromosómicas. Estudio de los principales cuadros. Diagnóstico prenatal: indicaciones y metodología Importancia de la genética en pediatría Ambiental
Neonatología Tema 2 Genética. Clasificación de las anomalías cromosómicas. Estudio de los principales cuadros. Diagnóstico prenatal: indicaciones y metodología Importancia de la genética en pediatría Ambiental
Serie Roja. Hemograma. Hemograma 13/09/2011. Anemias Hb < 12 gr% en la mujer y 14 gr% en el hombre.
 Hemograma Serie Roja Dra. Patricia Fardella Bello Hematólogo Sección Quimioterapia Fundación Arturo López Pérez 12 septiembre 2011 Serie Blanca 3 series: Pancitopenia Serie Megacariocitica Hemograma Serie
Hemograma Serie Roja Dra. Patricia Fardella Bello Hematólogo Sección Quimioterapia Fundación Arturo López Pérez 12 septiembre 2011 Serie Blanca 3 series: Pancitopenia Serie Megacariocitica Hemograma Serie
TECNICAS PARA EL ESTUDIO GENÉTICO DE LA OSTEOGENESIS IMPERFECTA Dra. Pilar Madero Barrajón. Centro de Análisis Genéticos. Zaragoza
 TECNICAS PARA EL ESTUDIO GENÉTICO DE LA OSTEOGENESIS IMPERFECTA Dra. Pilar Madero Barrajón. Centro de Análisis Genéticos. Zaragoza Definición: La Osteogénesis imperfecta literalmente significa hueso que
TECNICAS PARA EL ESTUDIO GENÉTICO DE LA OSTEOGENESIS IMPERFECTA Dra. Pilar Madero Barrajón. Centro de Análisis Genéticos. Zaragoza Definición: La Osteogénesis imperfecta literalmente significa hueso que
APLICACIONES DE LA CITOMETRIA DE FLUJO EN ONCOHEMATOLOGIA
 APLICACIONES DE LA CITOMETRIA DE FLUJO EN ONCOHEMATOLOGIA Bioquimica Esp.en Hematologia Susana Rubiolo Citometriade Flujo Estudia suspensiones celulares u otras particulas biologicas Analiza en forma rápida
APLICACIONES DE LA CITOMETRIA DE FLUJO EN ONCOHEMATOLOGIA Bioquimica Esp.en Hematologia Susana Rubiolo Citometriade Flujo Estudia suspensiones celulares u otras particulas biologicas Analiza en forma rápida
CRITERIOS PARA LA EVALUACIÓN E INFORMACIÓN DE LAS BIOPSIAS DE MÉDULA ÓSEA EN LA MIELOFIBROSIS PRIMARIA:
 CRITERIOS PARA LA EVALUACIÓN E INFORMACIÓN DE LAS BIOPSIAS DE MÉDULA ÓSEA EN LA MIELOFIBROSIS PRIMARIA: INFORME DIAGNÓSTICO ESTANDARIZADO Aprobado para publicación el 3 de junio de 2014 Consenso de expertos
CRITERIOS PARA LA EVALUACIÓN E INFORMACIÓN DE LAS BIOPSIAS DE MÉDULA ÓSEA EN LA MIELOFIBROSIS PRIMARIA: INFORME DIAGNÓSTICO ESTANDARIZADO Aprobado para publicación el 3 de junio de 2014 Consenso de expertos
Frecuencia de leucemias agudas en un hospital de referencia
 PRÁCTICA CLÍNICO-QUIRÚRGICA Wendy Marlene González-Salas, Irma Olarte-Carrillo, Mario Gutiérrez-Romero, Efreen Horacio Montaño-Figueroa, Carlos Martínez-Murillo, Christian Omar Ramos-Peñafiel Frecuencia
PRÁCTICA CLÍNICO-QUIRÚRGICA Wendy Marlene González-Salas, Irma Olarte-Carrillo, Mario Gutiérrez-Romero, Efreen Horacio Montaño-Figueroa, Carlos Martínez-Murillo, Christian Omar Ramos-Peñafiel Frecuencia
Estrategias para Pacientes y Cuidadores VIVIR con SMD
 Spanish Edition (Latin America) Estrategias para Pacientes y Cuidadores VIVIR con SMD por Sandra Kurtin Una iniciativa de promoción global de pacientes, tanto impresa como en internet, que provee un programa
Spanish Edition (Latin America) Estrategias para Pacientes y Cuidadores VIVIR con SMD por Sandra Kurtin Una iniciativa de promoción global de pacientes, tanto impresa como en internet, que provee un programa
Evolución del envejecimiento de los pacientes VIH en la epidemia española. José R. Blanco Hospital San Pedro CIBIR Logroño
 Evolución del envejecimiento de los pacientes VIH en la epidemia española José R. Blanco Hospital San Pedro CIBIR Logroño Conflictos de interés Abbive BMS Janssen Gilead MSD ViiV Fuentes consultadas Organismos
Evolución del envejecimiento de los pacientes VIH en la epidemia española José R. Blanco Hospital San Pedro CIBIR Logroño Conflictos de interés Abbive BMS Janssen Gilead MSD ViiV Fuentes consultadas Organismos
DOCUMENTO DE INDICACIONES DE BÚSQUEDA DE DONANTES NO EMPARENTADOS. COMITÉ DE EXPERTOS DE TPH
 DOCUMENTO DE INDICACIONES DE BÚSQUEDA DE DONANTES NO EMPARENTADOS. COMITÉ DE EXPERTOS DE TPH SUBCOMISIÓN DE TRASPLANTE DE PROGENITORES HEMOPOYÉTICOS 4 de febrero de 2014 COMISIÓN DE TRASPLANTES 18 de marzo
DOCUMENTO DE INDICACIONES DE BÚSQUEDA DE DONANTES NO EMPARENTADOS. COMITÉ DE EXPERTOS DE TPH SUBCOMISIÓN DE TRASPLANTE DE PROGENITORES HEMOPOYÉTICOS 4 de febrero de 2014 COMISIÓN DE TRASPLANTES 18 de marzo
Linfoma de Células Precursoras. Dr. Juan F García
 Linfoma de Células Precursoras Dr. Juan F García Linfoma/Leucemia de Células Precursoras Linfoma linfoblástico B / Leucemia linfoblástica (aguda) de precursores B Linfoma linfoblástico T / Leucemia linfoblástica
Linfoma de Células Precursoras Dr. Juan F García Linfoma/Leucemia de Células Precursoras Linfoma linfoblástico B / Leucemia linfoblástica (aguda) de precursores B Linfoma linfoblástico T / Leucemia linfoblástica
Fiebre mediterránea familiar (FMF)
 www.printo.it/pediatric-rheumatology/es_es/intro Fiebre mediterránea familiar (FMF) Versión de 2016 2. DIAGNÓSTICO Y TRATAMIENTO 2.1 Cómo se diagnostica? Por lo general, se sigue la siguiente aproximación:
www.printo.it/pediatric-rheumatology/es_es/intro Fiebre mediterránea familiar (FMF) Versión de 2016 2. DIAGNÓSTICO Y TRATAMIENTO 2.1 Cómo se diagnostica? Por lo general, se sigue la siguiente aproximación:
Reporte de caso transformación de síndrome mielodisplasico a leucemia aguda de linaje mixto con translocación (9;22).(q34;q11.
 CASOS CLÍNICOS PARTICULARES Reporte de caso transformación de síndrome mielodisplasico a leucemia aguda de linaje mixto con translocación Barrios-Hernández IL* Hernández-Sánchez MC**, Saucedo-Montes EE**
CASOS CLÍNICOS PARTICULARES Reporte de caso transformación de síndrome mielodisplasico a leucemia aguda de linaje mixto con translocación Barrios-Hernández IL* Hernández-Sánchez MC**, Saucedo-Montes EE**
Francisco de Asís Aparisi Aparisi. Hospital Virgen de los Lirios, Alcoy
 Estudio fase II de cisplatino (CDDP) y vinorelbina oral (VRLO) concomitante con radioterapia (RT) como tratamiento del cáncer de pulmón no microcítico localmente avanzado(cpnm-la): Resultados del objetivo
Estudio fase II de cisplatino (CDDP) y vinorelbina oral (VRLO) concomitante con radioterapia (RT) como tratamiento del cáncer de pulmón no microcítico localmente avanzado(cpnm-la): Resultados del objetivo
Diagnóstico Integrado de Leucemias Agudas
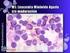 Diagnóstico Integrado de Leucemias Agudas Aspirado de médula osea Frotis (Wright-Giemsa) Sección de coágulo (hematoxilina-eosina) Análisis cromosómico convencional Citometría de flujo FISH Estudio de mutaciones
Diagnóstico Integrado de Leucemias Agudas Aspirado de médula osea Frotis (Wright-Giemsa) Sección de coágulo (hematoxilina-eosina) Análisis cromosómico convencional Citometría de flujo FISH Estudio de mutaciones
Paciente de Alto Riesgo
 Paciente de Alto Riesgo Caso Clinico Dr. Tomas Garcia Cerecedo Hospital Universitario Arnau de Vilanova de Lleida. 2015 1 /19 Paciente mujer de 64 años Antecedentes: Bocio Multinodular En 2008 LLC A0 (61
Paciente de Alto Riesgo Caso Clinico Dr. Tomas Garcia Cerecedo Hospital Universitario Arnau de Vilanova de Lleida. 2015 1 /19 Paciente mujer de 64 años Antecedentes: Bocio Multinodular En 2008 LLC A0 (61
Guías españolas de diagnóstico y tratamiento de los síndromes mielodisplásicos y la leucemia mielomonocítica crónica
 ISSN 1138-0381 Órgano oficial de la Sociedad Española de Hematología y Hemoterapia y la Sociedad Española de Trombosis y Hemostasia. Edición en español www.sehh.org www.seth.es Publicada por Grupo Acción
ISSN 1138-0381 Órgano oficial de la Sociedad Española de Hematología y Hemoterapia y la Sociedad Española de Trombosis y Hemostasia. Edición en español www.sehh.org www.seth.es Publicada por Grupo Acción
LEUCEMIAS. LIC. MACZY GONZÁLEZ RINCÓN MgSc CÁTEDRA DE HEMATOLOGÍA ESCUELA DE BIOANÁLISIS UNIVERSIDAD DEL ZULIA
 LEUCEMIAS LIC. MACZY GONZÁLEZ RINCÓN MgSc CÁTEDRA DE HEMATOLOGÍA ESCUELA DE BIOANÁLISIS UNIVERSIDAD DEL ZULIA LEUCEMIAS: DEFINICIÓN ENFERMEDADES DE ORIGEN CLONAL DONDE SE AFECTA EL STEM CELL LINFOIDE O
LEUCEMIAS LIC. MACZY GONZÁLEZ RINCÓN MgSc CÁTEDRA DE HEMATOLOGÍA ESCUELA DE BIOANÁLISIS UNIVERSIDAD DEL ZULIA LEUCEMIAS: DEFINICIÓN ENFERMEDADES DE ORIGEN CLONAL DONDE SE AFECTA EL STEM CELL LINFOIDE O
3ºCongreso Bioquímico de Córdoba 2015
 3ºCongreso Bioquímico de Córdoba 2015 Dra. Graciela Lucero. Unidad de Investigaciones Oncohematológicas - Oncolab. Buenos Aires. INFECCIONES BACTERIANAS ALERGIA ENFERMEDADES INFLAMATORIAS CAUSAS NECROSIS
3ºCongreso Bioquímico de Córdoba 2015 Dra. Graciela Lucero. Unidad de Investigaciones Oncohematológicas - Oncolab. Buenos Aires. INFECCIONES BACTERIANAS ALERGIA ENFERMEDADES INFLAMATORIAS CAUSAS NECROSIS
