Control del Equilibrio ácido-base
|
|
|
- Alberto Navarrete Cabrera
- hace 9 años
- Vistas:
Transcripción
1 Control del Equilibrio ácido-base
2 Escala de ph ph Concentración de H + en Eq/L
3 ÁLCALI: sustancia capaz de aceptar un H + ÁCIDO: sustancia capaz de donar un H+ Fuente: Bioquímica de Mathews, 3ª. Edición.
4 Equilibrio ácido-base 1. El tampon de bicarbonato 2. El intercambio alveolo-capilar de los gases 3. Componente respiratorio del equilibrio 4. Componente metabólico del equilibrio 5. La ACIDOSIS 6. La ALCALOSIS 7. Afecciones clínicas relacionadas al desequilibrio ácido-base
5 Tampones en el cuerpo humano Tampón Ácido Base conjugada Acción Hemoglobina HHb Hb - Eritrocitos Proteínas Hprot Prot - Intracelular Fosfato H2PO4 - HPO4 -- Intracelular Bicarbonato CO2 H2CO3 HCO3 - Extracelular Fuente: Bioquímica Médica 2ª. Edición. Baynes & Dominiczak
6 Fuente: Bioquímica Médica 2ª. Edición. Baynes & Dominiczak Balance Ácido-base. Los órganos y tejidos implicados en el mantenimiento del equilibrio ácido-base son los pulmones, los eritrocitos y los riñones. Los pulmones controlan el intercambio de dióxido de carbono y de oxígeno entre la sangre y la atmósfera exterior. Los eritrocitos transportan gases entre los pulmones y los tejidos y Los riñones controlan la concentración de bicarbonato en el plasma y excretan el ión hidrógeno en la orina.
7 Sistema de Amortiguación: BICARBONATO 1. El coeficiente de solubilidad del CO2 en el plasma es 0.23 en kpa (o 0.03 si se mide la pco2 en mmhg) kpa = 7.5 mmhg y 1 mmhg = kpa 3. A una pco2 normal de 5.3 kpa (40 mmhg), la concentración del CO2 disuelto (dco2) es: 4. dco2 (mmol/l) = 5.3 kpa x 0.23 = 1.2 mmol/l
8 Sistema de Amortiguación: BICARBONATO La Ecuación de Henderson-Hasselbalch [bicarbonato] (base) ph = pk + log pco2 x 0.23 (ácido) [ 24 mmol/l ] (base) ph = log (ácido)
9 Sistema de Amortiguación: BICARBONATO La Ecuación de Henderson-Hasselbalch [bicarbonato] (metabólico) ph = pk + log pco2 x 0.23 (pulmonar) [ 24 mmol/l ] ( 20 ) ph = log ( 1 )
10 Sistema de Amortiguación: BICARBONATO 1. La proporción en las cifras de 20/1 siempre será 1.3. La suma de la constante siempre será el ph normal: Toda desproporción del 20/1 provocará la pérdida del equilibrio (y el ph será diferente de 7.4). 3. Los problemas metabólicos modificarán la cifra del numerador (el bicarbonato de 24). 4. Los problemas respiratorios modificarán la cifra del denominador (el CO2 de 1.2).
11 Componentes del sistema amortiguador de Bicarbonato La concentración de bicarbonato (metabólico) varía de acuerdo a la producción de ácidos no volátiles producidos en los tejidos. La pco2 depende de la frecuencia respiratoria. Fuente: Bioquímica Médica 2ª. Edición. Baynes & Dominiczak
12 Sistema de Amortiguación: En el plasma la reacción BICARBONATO CO2 + H2O a H2CO3 b H + + HCO3 - Ocurre muy lentamente. Los eritrocitos y las células de los túbulos renales aceleran la reacción a por la acción de la enzima anhidrasa carbónica Por medio de esta acción los riñones controlan la concentración de bicarbonato en plasma.
13 Amortiguadores intracelulares: Proteínas, Fosfatos y recambio de Potasio Fuente: Bioquímica Médica 2ª. Edición. Baynes & Dominiczak
14 Amortiguadores intracelulares: Proteínas, Fosfatos y recambio de Potasio Fuente: Bioquímica Médica 2ª. Edición. Baynes & Dominiczak
15 Fuente: Bioquímica Médica 2ª. Edición. Baynes & Dominiczak Balance Ácido-base. 2 1 Cl - 3 Cl - HCO3-1. La anhidrasa carbónica del eritrocito fija CO2 como bicarbonato. 2. El ión hidrógeno resultante, es amortiguado por la hemoglobina. 3. El bicarbonato se intercambia con el ión CLORURO del plasma % del CO2 producido en los tejidos se convierte en bicarbonato % va como carbamino en la Hb % viaja disuelto en el plasma.
16 Balance Ácido-base. 1 Lactato Piruvato Fuente: Bioquímica Médica 2ª. Edición. Baynes & Dominiczak 2 1. Se generan cantidades sustanciales de ácidos inorgánicos como consecuencia de disolverse el CO2 producido del metabolismo oxidativo energético y combinarse con agua, y del metabolismo de aminoácidos sulfurados y fosforados. 2. El ácido láctico es resultado de la glucólisis anaeróbica resultante de la hipoxia (se bloquea la función mitocondrial) y 3. Los cuerpos cetónicos se asocian a exceso de beta-oxidación de ác. Grasos, por descompensación diabética.
17 1 3 Fuente: Bioquímica Médica 2ª. Edición. Baynes & Dominiczak 2 4 Balance Ácido-base. 1. Los pulmones controlan el intercambio gaseoso con el aire atmosférico. 2. El CO2 generado es transportado en el plasma como HCO La Hb amortigua ión hidrógeno 4. Los riñones reabsorben bicarbonato filtrado en los túbulos proximales y generan nuevo bicarbonato en los túbulos distales, donde hay una secreción neta de ión hidrógeno.
18 Trastornos Ácido-base Un aumento primario en la pco2 o una disminución en [HCO3 - ]p lleva a ACIDOSIS. La disminución de la pco2 o el aumento en [HCO3 - ]p lleva a ALCALOSIS. Si el cambio primario afecta a la pco2 es respiratorio Si el cambio primario afecta a la [HCO3 - ]p es metabólico Fuente: Bioquímica Médica 2ª. Edición. Baynes & Dominiczak
19 Intervalo de referencia de los resultados de los gases en sangre Arterial Venosa [H + ] mmol/l mmol/l ph pco kpa kpa po kpa kpa Bicarbonato mmol/l Fuente: Bioquímica Médica 2ª. Edición. Baynes & Dominiczak
20 Función del Pulmón 1. El epitelio bronquial elimina partículas. 2. El centro respiratorio (en el bulbo raquídeo) tiene quimiorreceptores sensibles a pco2 y al ph: > pco2 o < ph > ventilación. 3. En los cuerpos carotídeos del cayado aórtico hay sensores que ante la hipoxia (po2 < 8 kpa o 60mmHg) asumen el control ventilatorio. 4. En condiciones patológica es primero hipoxia que hipercapnia (que indica gravedad).
21 Los gradientes de la presión parcial determinan la difusión de los gases a través de la barrera alveolo-sangre Aire seco Alvéolos Arterias sistémicas Tejido po kpa 13.7 kpa 12 kpa 5.3 kpa pco2 <0.13 kpa 5.3 kpa 5.3 kpa 6 kpa Vapor de agua 6.3 kpa Fuente: Bioquímica Médica 2ª. Edición. Baynes & Dominiczak
22 Función del Pulmón Se compromete la función pulmonar por: 1. Deformidades restrictivas 2. Trauma y colapso pulmonar (< surfactante) 3. Obstrucción de la vía aérea 4. Asma (broncoespasmo) 5. Parálisis respiratoria 6. Edema pulmonar o fibrosis intersticial 7. Shock, ICC, Cáncer.
23 Oxígeno, CO2 y control de la respiración 1 3 Fuente: Bioquímica Médica 2ª. Edición. Baynes & Dominiczak 2 1. La ventilación y la perfusión pulmonares son los principales factores que controlan el intercambio gaseoso. 2. La pco2 afecta a la frecuencia ventilatoria por medio de los quimioreceptores centrales en el tronco encefálico. 3. Tambien la afecta el descenso de la po2 detectada por los receptores periféricos sensibles a la po2 situados en los cuerpos carotídeos del cayado aórtico.
24 Eliminación de CO2 de los tejidos El bicarbonato producido en los eritrocitos se mueve al plasma a cambio de Cl % del CO2 se convierte en bicarbonato 3. 20% se une a hemoglobina y 4. 10% se disuelve en el plasma. Fuente: Bioquímica Médica 2ª. Edición. Baynes & Dominiczak
25 Excreción de CO2 en el aire expirado En los pulmones la mayor po2 facilita la disociación del CO2 de la Hb (efecto Haldane). La Hb libera H + y lleva a producir CO2 + H2O. Fuente: Bioquímica Médica 2ª. Edición. Baynes & Dominiczak
26 Efectos de la perfusión pulmonar po2 alveolar pco2 alveolar po2 arterial pco2 arterial Comentario Mala ventilación, perfusión adecuada Adecuada ventilación, mala perfusión. Disminuida Aumentada Disminuida Normal Aumentada Disminuida Disminuida Aumentada Derivación fisiológica. Espacio muerto fisiológico Fuente: Bioquímica Médica 2ª. Edición. Baynes & Dominiczak
27 Función del Riñón El Sistema Renal Regula la excreción de H + 1. Por reabsorción tubular de HCO3 - filtrado en el glomérulo 2. por regeneración de bicarbonato gastado en la neutralización del ácido fijo, mediante la eliminación de H Para eliminar el exceso de H + por la orina, se combina con tampones intratubulares: 4. acidez titulable o como amonio
28 Reabsorción de bicarbonato en el riñón Fuente: Bioquímica Médica 2ª. Edición. Baynes & Dominiczak Tiene lugar en el túbulo proximal. En este momento no hay una excreción neta de ión hidrógeno. La anhidrasa carbónica está presente en la cara luminal de las células tubulares.
29 Fuente: Bioquímica Médica 2ª. Edición. Baynes & Dominiczak Excreción del ión HIDRÓGENO 1. Ocurre en los túbulos distales del riñón. 2. El H + + amoníaco producen AMONIO que es excretado. 3. El H + también es amortiguado por el fosfato. 4. La excreción diaria de H + es de 50 mmol.
30 Pérdida del Equilibrio Ácido-Base 1. El pulmón y el riñón trabajan de modo concertado para reducir al mínimo los cambios en el ph plasmático y pueden compensarse cuando se producen problemas. 2. Si se modifica la [HCO3-]p (componente metabólico), cambia la cifra del numerador de la proporción 20/1. 3. Si se modifica la pco2 (componente respiratorio), cambia la cifra del denominador de la proporción 20/1. 4. Si el cociente aumenta será alcalosis y 5. Si baja, será acidosis
31 Pérdida del Equilibrio Ácido-Base Acidosis Respiratoria Existe una hipoventilacion alveolar primaria pco2 >40 mmhg ph < 7.35 Alcalosis Respiratoria Existe una hiperventilacion alveolar primaria pco2 <40 mmhg ph > 7.45
32 Pérdida del Equilibrio Ácido-Base Acidosis: Descompensada: cuando la cifra de ph es baja. Compensada: cuando la cifra de ph es normal, pero la cifra del CO2 total es aún anormal Alcalosis: Descompensada: cuando la cifra del ph es alta. Compensada: cuando la cifra de ph es normal, pero la cifra del CO2 total es aún anormal
33 Pérdida del Equilibrio Ácido-Base 1. Acidosis Metabólica: Cuando la alteración reduce la cifra de bicarbonato (el numerador). 2. Acidosis Respiratoria: Cuando la alteración eleva la cifra del CO2 disuelto (el denominador). 1. Alcalosis Metabólica: Cuando la alteración eleva la cifra de bicarbonato. 2. Alcalosis Respiratoria: Cuando la alteración disminuye la cifra del CO2 disuelto.
34 Acidosis metabólica y respiratoria mixta Trastorno ph pco2 Bicarbonato Acidosis metabólica Disminución Disminución (compensación respiratoria) Disminución (cambio primario) Acidosis respiratoria Disminución Aumento (cambio primario) Aumento (compensación metabólica) Acidosis respiratoria y metabólica mixta Gran disminución Aumento (acidosis respiratoria) Disminución (acidosis metabólica) Fuente: Bioquímica Médica 2ª. Edición. Baynes & Dominiczak
35
36 Alcalosis metabólica y respiratoria mixta (infrecuente) Trastorno ph pco2 Bicarbonato Alcalosis metabólica Alcalosis respiratoria Alcalosis respiratoria y metabólica mixta Aumento Aumento Gran aumento Fuente: Bioquímica Médica 2ª. Edición. Baynes & Dominiczak Aumento (compensación respiratoria) Disminución (cambio primario) Disminución (alcalosis respiratoria) Aumento (cambio primario) Disminución (compensación metabólica) Aumento (acidosis metabólica)
37 Compensación respiratoria y metabólica de los trastornos ácido-base Trastorno ácido-base Cambio primario Cambio compensador Escala temporal del cambio compensador Acidosis metabólica [HCO3 - ]p en la pco2 (hiperventilación) Minutos / horas Alcalosis metabólica [HCO3 - ]p en la pco2 (hipoventilación) Minutos / horas Acidosis respiratoria en la pco2 en la reabsorción renal de HCO3 - [HCO3 - ]p Días. Alcalosis respiratoria en la pco2 en la reabsorción renal de HCO3 - [HCO3 - ]p Días Fuente: Bioquímica Médica 2ª. Edición. Baynes & Dominiczak
38 Fuente: Bioquímica Médica 2ª. Edición. Baynes & Dominiczak Causas clínicas de los trastornos ácido-base Acidosis metabólica Acidosis respiratoria Alcalosis metabólica Alcalosis respiratoria D. M. (cetoacidosis) E. P. O. C. Vómitos [H + ] Hiperventilación Acidosis láctica Insuf. Renal (ácidos inorgánicos) Diarrea intensa HCO3 - Drenaje quirúrgico del intestino. Pérdida renal de HCO3 - Acidosis tubular renal Asma intensa Aspiración nasogástrica Enfermedades pulmonares Parada cardíaca Hipopotasemia Anemia Depresión del centro respiratorio (opiáceos) Debilidad de los músculos respiratorios. Deformidades torácicas. Obstrucción vías respiratorias Administración I.V. De Bicarbonato Intoxicación por ASA
39 La brecha aniónica (anion gap) 12 2 meq/l Na HCO3 24 Cl 104
40 Brecha Aniónica o Anion-gap = (Na + ) - {(Cl - ) + (HCO3 - )} El valor normal es de 12 (10 a 14) Causas de ACIDOSIS con Brecha Aniónica AUMENTADA Insuficiencia Renal Acidosis Láctica Cetoacidosis (diabética, de ayuno prolongado o alcohólica) Salicilatos Metanol o Formaldehído Etilenglicol Ingestión excesiva de Paraldehído Tolueno Bebidas alcohólicas Citrato en transfusiones masivas Fuente: Bioquímica Médica 2ª. Edición. Baynes & Dominiczak
41 Brecha Aniónica o Anion-gap ACIDOSIS CON BRECHA ANIÓNICA NORMAL Administración de ácidos Pérdidas de Bicarbonato Alteración de la excresión renal de ácido Fuente: Bioquímica Médica 2ª. Edición. Baynes & Dominiczak Alimentación Parenteral Administración de HCL Gastrointestinal Renal Con hipopotasemia Con hiperpotasemia Por HCL / Colestiramina En alcalosis metab. Severa Diarrea Drenaje biliar/pancreático Ureterosigmoidoscopía Acidosis Tubular R. proximal Cetoacidosis (en el Tx) Post hipocapnia crónica Acidosis Tubular R. distal Hipoaldosteronismo Perfusión renal disminuida
42 Fuente: Bioquímica Médica 2ª. Edición. Baynes & Dominiczak Balance Ácido-base. 1. Los pulmones controlan el intercambio gaseoso con el aire atmosférico. 2. El CO2 generado es transportado en el plasma como HCO La Hb amortigua ión hidrógeno 4. Los riñones reabsorben bicarbonato filtrado en los túbulos proximales y generan nuevo bicarbonato en los túbulos distales, donde hay una secreción neta de ión hidrógeno.
43 Gracias
44
45
EQUILIBRIO ÁCIDO-BASE MANTENIMIENTO DE LA HOMEOSTASIS
 EQUILIBRIO ÁCIDO-BASE MANTENIMIENTO DE LA HOMEOSTASIS EQUILÍBRIO ÁCIDO-BASE La regulación de ph a nivel celular, es necesaria para la supervivencia. Los ácidos y bases entran continuamente en la sangre
EQUILIBRIO ÁCIDO-BASE MANTENIMIENTO DE LA HOMEOSTASIS EQUILÍBRIO ÁCIDO-BASE La regulación de ph a nivel celular, es necesaria para la supervivencia. Los ácidos y bases entran continuamente en la sangre
ESTADO ACIDO BASE ACIDOSIS METABOLICA. ETIOLOGÍA DE LA ACIDOSIS METABÓLICA Inhabilidad Para Secretar La Carga Acida De La Dieta +
 ESTADO ACIDO BASE Los siguientes pasos son usados para evaluar los desordenes acidobase: 1.Determinar la anormalidad de base acidosis metabólica y/o alcalosis metabólica. 2.Determinar los factores contribuyentes
ESTADO ACIDO BASE Los siguientes pasos son usados para evaluar los desordenes acidobase: 1.Determinar la anormalidad de base acidosis metabólica y/o alcalosis metabólica. 2.Determinar los factores contribuyentes
6. MANTENIMIENTO DEL ph EN EL MEDIO EXTRACELULAR
 Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 6. MANTENIMIENTO DEL ph EN EL MEDIO EXTRACELULAR ESQUEMA - Composición iónica de los medios corporales - Capacidad tampón - Mantenimiento
Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 6. MANTENIMIENTO DEL ph EN EL MEDIO EXTRACELULAR ESQUEMA - Composición iónica de los medios corporales - Capacidad tampón - Mantenimiento
Cátedra de Fisiología Humana CAPÍTULO I CAPITULO III. Equilibrio Acido Base PH. Carrera de Enfermería. Universidad Nacional del Nordeste
 CAPÍTULO I Cátedra de Fisiología Humana CAPITULO III Equilibrio Acido Base PH Carrera de Enfermería. Universidad Nacional del Nordeste 37 CAPITULO 3: Cada soluto del organismo, el sodio, el potasio, el
CAPÍTULO I Cátedra de Fisiología Humana CAPITULO III Equilibrio Acido Base PH Carrera de Enfermería. Universidad Nacional del Nordeste 37 CAPITULO 3: Cada soluto del organismo, el sodio, el potasio, el
SOLUCIONES BUFFERS. pk = valor de ph en el cual las concentraciones del ácido y la sal son iguales
 SOLUCIONES BUFFERS Constituidas por un ácido débil y su base conjugada (sal) permite la adición de ácido o base sin variar considerablemente el ph. La capacidad búffer es máximo una unidad por encima y
SOLUCIONES BUFFERS Constituidas por un ácido débil y su base conjugada (sal) permite la adición de ácido o base sin variar considerablemente el ph. La capacidad búffer es máximo una unidad por encima y
Carvajal Ramos M, Sánchez Sánchez M, Cornide Santos I, Panadero Carlavilla FJ
 ALTERACIONES DEL EQUILIBRIO ÁCIDO-BASE Carvajal Ramos M, Sánchez Sánchez M, Cornide Santos I, Panadero Carlavilla FJ El ph refleja la concentración de cationes de hidrógeno presentes en una determinada
ALTERACIONES DEL EQUILIBRIO ÁCIDO-BASE Carvajal Ramos M, Sánchez Sánchez M, Cornide Santos I, Panadero Carlavilla FJ El ph refleja la concentración de cationes de hidrógeno presentes en una determinada
Organización Funcional y el Medio Interno
 Organización Funcional y el Medio Interno Aproximadamente el 50 % del cuerpo humano es líquido y la mayor parte es intracelular, la tercera parte es extracelular, la misma que se encuentra en movimiento
Organización Funcional y el Medio Interno Aproximadamente el 50 % del cuerpo humano es líquido y la mayor parte es intracelular, la tercera parte es extracelular, la misma que se encuentra en movimiento
FISIOPATOLOGIA. Concentración normal H+: 40 nmoles/l. -PH : 6.8-7.35 < -( H+) : 16-160 nmoles/l -PCO2: 36-44 mmhg -BE: -3 a 3
 FISIOPATOLOGIA Concentración normal H+: 40 nmoles/l -PH : 6.8-7.35 < -( H+) : 16-160 nmoles/l -PCO2: 36-44 mmhg -BE: -3 a 3 FISIOPATOLOGIA ACIDO-BASE ACIDO: sustancia capaz de ceder protones BASE: sustancia
FISIOPATOLOGIA Concentración normal H+: 40 nmoles/l -PH : 6.8-7.35 < -( H+) : 16-160 nmoles/l -PCO2: 36-44 mmhg -BE: -3 a 3 FISIOPATOLOGIA ACIDO-BASE ACIDO: sustancia capaz de ceder protones BASE: sustancia
7. ESTUDIO DEL EQUILIBRIO ACIDO BASE DE UN PACIENTE
 Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 7. ESTUDIO DEL EQUILIBRIO ACIDO BASE DE UN PACIENTE ESQUEMA - Estudio del equilibrio ácido-base de un paciente - Trastornos del
Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 7. ESTUDIO DEL EQUILIBRIO ACIDO BASE DE UN PACIENTE ESQUEMA - Estudio del equilibrio ácido-base de un paciente - Trastornos del
Ventilación Pulmonar. -durante al ejercicio- Elaborado por Lic. Manuel Salazar Leitón
 Ventilación Pulmonar -durante al ejercicio- Elaborado por Lic. Manuel Salazar Leitón Funciones básicas de la ventilación pulmonar Intercambio gaseoso con el ambiente. Regular el acidez en sangre. Comunicación
Ventilación Pulmonar -durante al ejercicio- Elaborado por Lic. Manuel Salazar Leitón Funciones básicas de la ventilación pulmonar Intercambio gaseoso con el ambiente. Regular el acidez en sangre. Comunicación
ENFERMERÍA CLÍNICA I Felicitas Merino de la Hoz TEMA 1.2.2 DESEQUILIBRIOS ACIDOBÁSICOS
 TEMA 1.2.2 DESEQUILIBRIOS ACIDOBÁSICOS ÍNDICE 1. Introducción. 2. Análisis e interpretación de los gases arteriales. 3. Alteraciones del equilibrio ácido- base. 3.1. Acidosis respiratoria. 3.2. Alcalosis
TEMA 1.2.2 DESEQUILIBRIOS ACIDOBÁSICOS ÍNDICE 1. Introducción. 2. Análisis e interpretación de los gases arteriales. 3. Alteraciones del equilibrio ácido- base. 3.1. Acidosis respiratoria. 3.2. Alcalosis
DESORDEN ACIDO BASICO
 DESORDEN ACIDO BASICO Cuando se habla de regulacion del equilibrio acido base, se habla en realidad de la Regulacion de la concentracion de iones hidrogenos en los liquidos corporales 1 Como la concentracion
DESORDEN ACIDO BASICO Cuando se habla de regulacion del equilibrio acido base, se habla en realidad de la Regulacion de la concentracion de iones hidrogenos en los liquidos corporales 1 Como la concentracion
capnografia volumetrica NICO Claudia Eyzaguirre G. Enfermera clínica.
 capnografia volumetrica NICO Claudia Eyzaguirre G. Enfermera clínica. El CO2 es un producto final del O2 utilizado por las células después del metabolismo celular. Una vez que el CO2 alcanza los pulmones
capnografia volumetrica NICO Claudia Eyzaguirre G. Enfermera clínica. El CO2 es un producto final del O2 utilizado por las células después del metabolismo celular. Una vez que el CO2 alcanza los pulmones
Trastornos del equilibrio ácido-base
 NOTA DELS COMISSIONARIS: hi ha aclaracions i correccions importants al document Fe d errades, és important que us el mireu de cara a l examen!! Trastornos del equilibrio ácidobase INTRODUCCIÓN CONCEPTOS
NOTA DELS COMISSIONARIS: hi ha aclaracions i correccions importants al document Fe d errades, és important que us el mireu de cara a l examen!! Trastornos del equilibrio ácidobase INTRODUCCIÓN CONCEPTOS
TALLER DE ANALISIS DE GASES ARTERIALES
 TALLER DE ANALISIS DE GASES ARTERIALES Dr. Menfil A Orellana-Barrios Medicina Interna Cursos Precongreso Congreso de Residentes 2012 HGSJDD www.drmenfilorellana.wordpress.com Para qué se utilizan los Gases
TALLER DE ANALISIS DE GASES ARTERIALES Dr. Menfil A Orellana-Barrios Medicina Interna Cursos Precongreso Congreso de Residentes 2012 HGSJDD www.drmenfilorellana.wordpress.com Para qué se utilizan los Gases
Programa 3º Curso. Curso (Prof. M García-Caballero)
 Programa 3º Curso Departamento de Cirugía Curso 2008-09 Equilibrio i hidroelectrolítico lí i y ácido-base (Prof. M García-Caballero) http://www.cirugiadelaobesidad.net/ CAMBIOS DE FLUIDOS Y ELECTROLITOS
Programa 3º Curso Departamento de Cirugía Curso 2008-09 Equilibrio i hidroelectrolítico lí i y ácido-base (Prof. M García-Caballero) http://www.cirugiadelaobesidad.net/ CAMBIOS DE FLUIDOS Y ELECTROLITOS
1. Líquidos corporales. 2. Anatomía y función renal. 3. Hormonas ADH y aldosterona
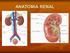 1. Líquidos corporales 2. Anatomía y función renal 3. Hormonas ADH y aldosterona Propiedades de la Homeostasis 1. Importancia tanto del sistema nervioso como del endocrino. 2. Controles antagónicos. 3.
1. Líquidos corporales 2. Anatomía y función renal 3. Hormonas ADH y aldosterona Propiedades de la Homeostasis 1. Importancia tanto del sistema nervioso como del endocrino. 2. Controles antagónicos. 3.
8. CASOS PRACTICOS DE ALTERACIONES DEL EQUILIBRIO ACIDO BASE
 Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 8. CASOS PRACTICOS DE ALTERACIONES DEL EQUILIBRIO ACIDO BASE A continuación se presentan una serie de casos prácticos resueltos,
Departamento de Bioquímica y Biología Molecular ph y equilibrios acido-base 8. CASOS PRACTICOS DE ALTERACIONES DEL EQUILIBRIO ACIDO BASE A continuación se presentan una serie de casos prácticos resueltos,
Dra. María Eugenia Victoria Bianchi Dr. Gustavo Borda Dra Marcela Young. Estudiantes por Concurso según Resolución 1311/95-C-D.
 Dra. María Eugenia Victoria Bianchi Dr. Gustavo Borda Dra Marcela Young. Estudiantes por Concurso según Resolución 1311/95-C-D. Vallejos Javier Serial Marcos Sebastián Rausch Ricardo Simón Laura Solé Juan
Dra. María Eugenia Victoria Bianchi Dr. Gustavo Borda Dra Marcela Young. Estudiantes por Concurso según Resolución 1311/95-C-D. Vallejos Javier Serial Marcos Sebastián Rausch Ricardo Simón Laura Solé Juan
Tema 1. Introducción
 Tema 1. Introducción - Bioquímica: concepto, y objetivos - Importancia de la Bioquímica en la Lic. De Farmacia - Composición química del cuerpo humano: Bioelementos Bioelementos primarios o principales
Tema 1. Introducción - Bioquímica: concepto, y objetivos - Importancia de la Bioquímica en la Lic. De Farmacia - Composición química del cuerpo humano: Bioelementos Bioelementos primarios o principales
Tema 2. El agua, el ph y los equilibrios iónicos
 Tema 2. El agua, el ph y los equilibrios iónicos -Interacciones débiles en sistemas acuosos: puentes de hidrógeno, fuerzas de van der Waals e interacciones iónicas. -Enlaces hidrofóbicos. -Estructura y
Tema 2. El agua, el ph y los equilibrios iónicos -Interacciones débiles en sistemas acuosos: puentes de hidrógeno, fuerzas de van der Waals e interacciones iónicas. -Enlaces hidrofóbicos. -Estructura y
Trastornos respiratorios. Acidosis y alcalosis
 Trastornos respiratorios Acidosis y alcalosis Acidosis Respiratoria Trastorno que se caracteriza por aumento primario de la paco2 con elevación de la concentración de H+ en sangre, disminución del ph y
Trastornos respiratorios Acidosis y alcalosis Acidosis Respiratoria Trastorno que se caracteriza por aumento primario de la paco2 con elevación de la concentración de H+ en sangre, disminución del ph y
Proceso de liberación de energía, requiere aporte continuo de oxigeno(o2) y eliminación de bióxido de carbono(co2) principal función del aparato
 Proceso de liberación de energía, requiere aporte continuo de oxigeno(o2) y eliminación de bióxido de carbono(co2) principal función del aparato respiratorio. En condiciones normales la respiración es
Proceso de liberación de energía, requiere aporte continuo de oxigeno(o2) y eliminación de bióxido de carbono(co2) principal función del aparato respiratorio. En condiciones normales la respiración es
TEST APARATO RESPIRATORIO BIR 2015-2016
 1.- Cuál de los siguientes es el estímulo directo para las neuronas del área quimiosensible de la zona bulbar reguladora de la respiración?: 1. po 2. 2. pco 2. 3. CO 3 H 2. 4. CO 3 H -. 5. Concentración
1.- Cuál de los siguientes es el estímulo directo para las neuronas del área quimiosensible de la zona bulbar reguladora de la respiración?: 1. po 2. 2. pco 2. 3. CO 3 H 2. 4. CO 3 H -. 5. Concentración
Neumologí a Iº SECCIÓN : CIENCIAS BÁSICAS (RESUMEN) ANATOMÍA DEL APARATO RESPIRATORIO. www. PLUS -medica.com
 Neumologí a Iº SECCIÓN : CIENCIAS BÁSICAS (RESUMEN) ANATOMÍA DEL APARATO RESPIRATORIO VIAS AÉREAS 4 Las células de Kultchitsky Se encuentran en el epitelio de la mucosa de tráquea y bronquios. Es una célula
Neumologí a Iº SECCIÓN : CIENCIAS BÁSICAS (RESUMEN) ANATOMÍA DEL APARATO RESPIRATORIO VIAS AÉREAS 4 Las células de Kultchitsky Se encuentran en el epitelio de la mucosa de tráquea y bronquios. Es una célula
FISIOLOGIA RESPIRATORIA
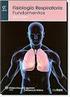 FISIOLOGIA RESPIRATORIA LA RESPIRACION TIENE COMO FUNCION PROPORCIONAR O 2 A LAS CELULAS Y EXTRAER EL EXCESO DE CO 2 PRODUCIDO POR ELLAS Componentes de las vías aéreas TRÁQUEA BRONQUIOS BRONQUÍOLOS ZONA
FISIOLOGIA RESPIRATORIA LA RESPIRACION TIENE COMO FUNCION PROPORCIONAR O 2 A LAS CELULAS Y EXTRAER EL EXCESO DE CO 2 PRODUCIDO POR ELLAS Componentes de las vías aéreas TRÁQUEA BRONQUIOS BRONQUÍOLOS ZONA
DIFUSIÓN - TRANSPORTE DE GASES EN SANGRE. Material de uso interno
 DIFUSIÓN - TRANSPORTE DE GASES EN SANGRE Material de uso interno 2010 Hoy hablaremos de: * Leyes de los gases: aspectos aplicados * Hematosis ó intercambio alvéolo-capilar * Transporte de gases en sangre
DIFUSIÓN - TRANSPORTE DE GASES EN SANGRE Material de uso interno 2010 Hoy hablaremos de: * Leyes de los gases: aspectos aplicados * Hematosis ó intercambio alvéolo-capilar * Transporte de gases en sangre
INSUFICIENCIA RESPIRATORIA AGUDA GIOVANNY CAMPOMANES ESPINOZA MEDICO INTERNISTA
 INSUFICIENCIA RESPIRATORIA AGUDA GIOVANNY CAMPOMANES ESPINOZA MEDICO INTERNISTA Zona de Conducción TRAQUEA BRONQUIOS BRONQUIOLOS BRONQUIOLOS TERMINALES Z O 1 2 3 4 5 16 Zona de Transición Y Respiratoria
INSUFICIENCIA RESPIRATORIA AGUDA GIOVANNY CAMPOMANES ESPINOZA MEDICO INTERNISTA Zona de Conducción TRAQUEA BRONQUIOS BRONQUIOLOS BRONQUIOLOS TERMINALES Z O 1 2 3 4 5 16 Zona de Transición Y Respiratoria
MEDIO INTERNO ACIDOSIS METABÓLICA DRA. STELLA MARIS DIEGUEZ HTAL. GRAL DE AGUDOS DR. T. ÁLVAREZ
 MEDIO INTERNO ACIDOSIS METABÓLICA DRA. STELLA MARIS DIEGUEZ HTAL. GRAL DE AGUDOS DR. T. ÁLVAREZ 1-Historia clínica G D Varón de 1 año y 5 meses MOTIVO DE CONSULTA retraso del crecimiento ANTECEDENTES RNTPAEG
MEDIO INTERNO ACIDOSIS METABÓLICA DRA. STELLA MARIS DIEGUEZ HTAL. GRAL DE AGUDOS DR. T. ÁLVAREZ 1-Historia clínica G D Varón de 1 año y 5 meses MOTIVO DE CONSULTA retraso del crecimiento ANTECEDENTES RNTPAEG
Transporte de oxígeno y de dióxido de carbono (CO 2 ) en la sangre. La hemoglobina aumenta la capacidad de la sangre para transportar oxígeno.
 Transporte de oxígeno y de dióxido de carbono (CO 2 ) en la sangre La sangre transporta los gases respiratorios por todo el organismo. El O2 se transporta desde los pulmones hasta todos los tejidos del
Transporte de oxígeno y de dióxido de carbono (CO 2 ) en la sangre La sangre transporta los gases respiratorios por todo el organismo. El O2 se transporta desde los pulmones hasta todos los tejidos del
SEMINARIO: ESTUDIO DEL PH FETAL INTRAPARTO
 Fecha: 1 de Diciembre de 2010 Nombre: Dra. Ana Fuentes Rozalén R2 Tipo de Sesión: Seminario SEMINARIO: ESTUDIO DEL PH FETAL INTRAPARTO El objetivo de este seminario es que entendamos la fisiopatología
Fecha: 1 de Diciembre de 2010 Nombre: Dra. Ana Fuentes Rozalén R2 Tipo de Sesión: Seminario SEMINARIO: ESTUDIO DEL PH FETAL INTRAPARTO El objetivo de este seminario es que entendamos la fisiopatología
Curso Superior de Medicina Intensiva y Cuidados Críticos Necochea, 2007-2009
 Trastornos del equilibrio ácido-base Introducción Las primeras definiciones contemporáneas de ácido y base pueden atribuirse a Arrhenius, quien en 1887 definió ácido como un donante de ion hidrógeno y
Trastornos del equilibrio ácido-base Introducción Las primeras definiciones contemporáneas de ácido y base pueden atribuirse a Arrhenius, quien en 1887 definió ácido como un donante de ion hidrógeno y
Práctica clínica. Interpretación de los resultados de los gases en sangre
 Práctica clínica Para interpretar los gases en sangre es necesaria la evaluación sistemática de la oxigenación, el ph, el bicarbonato estándar (shco3 ) y el exceso de bases, la presión parcial de anhídrido
Práctica clínica Para interpretar los gases en sangre es necesaria la evaluación sistemática de la oxigenación, el ph, el bicarbonato estándar (shco3 ) y el exceso de bases, la presión parcial de anhídrido
ABSORCIÓN, DISTRIBUCIÓN Y ELIMINACIÓN DE LOS TÓXICOS EN EL ORGANISMO
 Toxicología alimentaria Diplomatura de Nutrición humana y dietética Curso 2010-2011 ABSORCIÓN, DISTRIBUCIÓN Y ELIMINACIÓN DE LOS TÓXICOS EN EL ORGANISMO Dr. Jesús Miguel Hernández-Guijo Dpto. Farmacología
Toxicología alimentaria Diplomatura de Nutrición humana y dietética Curso 2010-2011 ABSORCIÓN, DISTRIBUCIÓN Y ELIMINACIÓN DE LOS TÓXICOS EN EL ORGANISMO Dr. Jesús Miguel Hernández-Guijo Dpto. Farmacología
Alteraciones de los Fluidos Corporales, Electrolitos
 Alteraciones de los Fluidos Corporales, Electrolitos Introducción Abner J. Gutiérrez Chávez, MVZ, MC. Facultad de Medicina Veterinaria y Zootecnia, UNAM. Dpto. Producción Animal: Rumiantes Existen diversas
Alteraciones de los Fluidos Corporales, Electrolitos Introducción Abner J. Gutiérrez Chávez, MVZ, MC. Facultad de Medicina Veterinaria y Zootecnia, UNAM. Dpto. Producción Animal: Rumiantes Existen diversas
El equilibrio ácido-base del organismo es posible merced a la interrelación de tres sistemas:
 ALTERACIONES DEL EQUILIBRIO ACIDO BÁSICO Dr.- Benito Saínz Menéndez (1) 1. INTRODUCCIÓN. Los procesos metabólicos intracelulares producen ácidos, es decir, sustancias capaces de liberar iones H+, por oxidación
ALTERACIONES DEL EQUILIBRIO ACIDO BÁSICO Dr.- Benito Saínz Menéndez (1) 1. INTRODUCCIÓN. Los procesos metabólicos intracelulares producen ácidos, es decir, sustancias capaces de liberar iones H+, por oxidación
Sistema respiratorio CLASE 1
 Sistema respiratorio CLASE 1 En la respiración celular se libera dióxido de carbono y, para obtener energía, las células oxidan compuestos que contienen carbono, en reacciones químicas que requieren oxígeno.
Sistema respiratorio CLASE 1 En la respiración celular se libera dióxido de carbono y, para obtener energía, las células oxidan compuestos que contienen carbono, en reacciones químicas que requieren oxígeno.
Aspectos destacados del sistema cardiocirculatorio y respiratorio, ligados al entrenamiento deportivo. Dr. Juan Carlos Mazza (Argentina)
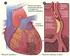 Aspectos destacados del sistema cardiocirculatorio y respiratorio, ligados al entrenamiento deportivo Dr. Juan Carlos Mazza (Argentina) SISTEMA CARDIOVASCULAR Cualquier sistema de circulación requiere
Aspectos destacados del sistema cardiocirculatorio y respiratorio, ligados al entrenamiento deportivo Dr. Juan Carlos Mazza (Argentina) SISTEMA CARDIOVASCULAR Cualquier sistema de circulación requiere
2.- Sistema renal: Instauración tardía (24-48 horas) y de acción más duradera. Los riñones regulan el bicarbonato plasmático mediante tres procesos:
 Santos Nores, Juan*; Borrajo Prol, María Paz*; Camba Caride, María Jesús* *Servicio de Nefrología INTRODUCCIÓN Y CONCEPTOS: El metabolismo normal produce constantemente radicales ácidos. Sin embargo, el
Santos Nores, Juan*; Borrajo Prol, María Paz*; Camba Caride, María Jesús* *Servicio de Nefrología INTRODUCCIÓN Y CONCEPTOS: El metabolismo normal produce constantemente radicales ácidos. Sin embargo, el
Pauta de corrección guía IV medio Homeostasis
 Pauta de corrección guía IV medio Homeostasis Actividad 1.- Registra la temperatura ambiental en un día cada una hora. Así mismo registra la temperatura corporal que tu cuerpo tiene en cada hora. Grafica
Pauta de corrección guía IV medio Homeostasis Actividad 1.- Registra la temperatura ambiental en un día cada una hora. Así mismo registra la temperatura corporal que tu cuerpo tiene en cada hora. Grafica
INTOXICACION CON ASPIRINA
 INTOXICACION CON ASPIRINA La intoxicación con aspirina es un hecho sumamente común en la práctica médica. La misma responde entre otras cosas, a que es un medicamento que puede adquirirse sin receta en
INTOXICACION CON ASPIRINA La intoxicación con aspirina es un hecho sumamente común en la práctica médica. La misma responde entre otras cosas, a que es un medicamento que puede adquirirse sin receta en
TRASTORNOS DEL EQUILIBRIO ÁCIDO-BASE
 TRASTORNOS DEL EQUILIBRIO ÁCIDO-BASE AUTORES: MARIA JOSE RUIZ MARQUEZ CARMEN ORTIZ GARCIA JUAN JOSE SANCHEZ LUQUE ANA PEÑA AGÜERA LABORATORIO DEL HOSPITAL CLÍNICO UNIVERSITARIO VIRGEN DE LA VICTORIA DE
TRASTORNOS DEL EQUILIBRIO ÁCIDO-BASE AUTORES: MARIA JOSE RUIZ MARQUEZ CARMEN ORTIZ GARCIA JUAN JOSE SANCHEZ LUQUE ANA PEÑA AGÜERA LABORATORIO DEL HOSPITAL CLÍNICO UNIVERSITARIO VIRGEN DE LA VICTORIA DE
Aparatos que intervienen en la nutrición
 Aparatos que intervienen en la nutrición El ser humano necesita ingerir alimentos y agua diariamente, para el mantenimiento de sus constantes vitales. De los alimentos se utilizan distintos nutrientes,
Aparatos que intervienen en la nutrición El ser humano necesita ingerir alimentos y agua diariamente, para el mantenimiento de sus constantes vitales. De los alimentos se utilizan distintos nutrientes,
LA RESPIRACIÓN EN ANIMALES
 LA RESPIRACIÓN EN ANIMALES Adaptado de Julio Sánchez, Curtis-Barnes Mª Luisa Fanjul, Marcia Hiriart IMÁGENES LIBRES DE INTERNET CONCEPTOS PREVIOS RESPIRACIÓN CELULAR Reacción química del oxígeno en el
LA RESPIRACIÓN EN ANIMALES Adaptado de Julio Sánchez, Curtis-Barnes Mª Luisa Fanjul, Marcia Hiriart IMÁGENES LIBRES DE INTERNET CONCEPTOS PREVIOS RESPIRACIÓN CELULAR Reacción química del oxígeno en el
Bioelementos y biomoléculas 1-Moleculas inorganicas Sales minerales. Verónica Pantoja. Lic. MSP.
 Bioelementos y biomoléculas 1-Moleculas inorganicas Sales minerales Professor: Kinesiologia Verónica Pantoja. Lic. MSP. 1.Precipitadas Formando estructuras sólidas, insolubles, con función esquelética.
Bioelementos y biomoléculas 1-Moleculas inorganicas Sales minerales Professor: Kinesiologia Verónica Pantoja. Lic. MSP. 1.Precipitadas Formando estructuras sólidas, insolubles, con función esquelética.
Alteraciones ácido-base Simples y Mixtos: Una Aproximación Práctica Robert C Narins, M.D. y Michael Emmett, M.D. Modificado por Mauricio Durán, M.D.
 1 Alteraciones ácido-base Simples y Mixtos: Una Aproximación Práctica Robert C Narins, M.D. y Michael Emmett, M.D. Modificado por Mauricio Durán, M.D. Revisiones recientes del metabolismo ácido-base se
1 Alteraciones ácido-base Simples y Mixtos: Una Aproximación Práctica Robert C Narins, M.D. y Michael Emmett, M.D. Modificado por Mauricio Durán, M.D. Revisiones recientes del metabolismo ácido-base se
Lección 24. Fármacos Diuréticos UNIDAD VII: PROBLEMAS CARDIOVASCULARES Y SANGUÍNEOS. Ricardo Brage e Isabel Trapero - Farmacología Lección 24
 Ricardo Brage e Isabel Trapero - Lección 24 UNIDAD VII: PROBLEMAS CARDIOVASCULARES Y SANGUÍNEOS Lección 24 Fármacos Diuréticos Guión Ricardo Brage e Isabel Trapero - Lección 24 1. BASES CONCEPTUALES. 2.
Ricardo Brage e Isabel Trapero - Lección 24 UNIDAD VII: PROBLEMAS CARDIOVASCULARES Y SANGUÍNEOS Lección 24 Fármacos Diuréticos Guión Ricardo Brage e Isabel Trapero - Lección 24 1. BASES CONCEPTUALES. 2.
TEMA 11 I. ABSORCIÓN DE AGUA Y ELECTROLITOS
 1 TEMA 11 I. ABSORCIÓN DE AGUA Y ELECTROLITOS 1. Introducción 2. Conceptos 2.1 ósmosis, molaridad y osmolaridad de soluciones, 2.2 presión osmótica, presión hidrostática. 2.3 soluciones isotónicas, hipotónicas,
1 TEMA 11 I. ABSORCIÓN DE AGUA Y ELECTROLITOS 1. Introducción 2. Conceptos 2.1 ósmosis, molaridad y osmolaridad de soluciones, 2.2 presión osmótica, presión hidrostática. 2.3 soluciones isotónicas, hipotónicas,
Verónica Mate García Isabel Moreno Moraleda Gracia Guajardo-Fajardo Adriana Serrano Olave
 Verónica Mate García Isabel Moreno Moraleda Gracia Guajardo-Fajardo Adriana Serrano Olave Introducción Efectos del tabaco fumado Afectaciones por polución aérea Intoxicación por CO Intoxicación por oxígeno
Verónica Mate García Isabel Moreno Moraleda Gracia Guajardo-Fajardo Adriana Serrano Olave Introducción Efectos del tabaco fumado Afectaciones por polución aérea Intoxicación por CO Intoxicación por oxígeno
MEDICINA II. DR. EFRAIN ESTRADA CHOQUE, M.D. Lima, Perú GOMEZ LOPEZ JHAQUELINE PIEDRA RIOS CARLOS VARGA MORENO GUILLERMO. www.reeme.arizona.
 MEDICINA II DR. EFRAIN ESTRADA CHOQUE, M.D. Lima, Perú GOMEZ LOPEZ JHAQUELINE PIEDRA RIOS CARLOS VARGA MORENO GUILLERMO El anàlisis de gases arteriales es un procedimiento que tiene por finalidad: Evaluar
MEDICINA II DR. EFRAIN ESTRADA CHOQUE, M.D. Lima, Perú GOMEZ LOPEZ JHAQUELINE PIEDRA RIOS CARLOS VARGA MORENO GUILLERMO El anàlisis de gases arteriales es un procedimiento que tiene por finalidad: Evaluar
INDICE - Parte 3 7.6 VIAJE DEL DIOXIDO DE CARBONO DE LAS CELULAS AL AIRE - PROBLEMAS Y PREGUNTAS - VALORES USADOS EN ESTE CAPITULO
 Capítulo 7 PARTE 3/3 7.6 VIAJE DEL DIOXIDO DE CARBONO DE LAS CELULAS AL AIRE Después de haber seguido el O2 desde los pulmones a las células, le toca el turno al CO2 en su viaje en sentido inverso. Es
Capítulo 7 PARTE 3/3 7.6 VIAJE DEL DIOXIDO DE CARBONO DE LAS CELULAS AL AIRE Después de haber seguido el O2 desde los pulmones a las células, le toca el turno al CO2 en su viaje en sentido inverso. Es
TÍTULO: VENTILACIÓN Y TEMPERATURA INSTITUTO SUPERIOR PEDAGOGICO ENRIQUE JOSE VARONA, LA HABANA
 TÍTULO: VENTILACIÓN Y TEMPERATURA AUTOR: PROFESOR TITULAR INSTITUTO SUPERIOR PEDAGOGICO ENRIQUE JOSE VARONA, LA HABANA Ambiente Térmico Cambios Fisiológicos y Psicomotores (Cambios ambientales extremos)
TÍTULO: VENTILACIÓN Y TEMPERATURA AUTOR: PROFESOR TITULAR INSTITUTO SUPERIOR PEDAGOGICO ENRIQUE JOSE VARONA, LA HABANA Ambiente Térmico Cambios Fisiológicos y Psicomotores (Cambios ambientales extremos)
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. Bicarbonato Sódico 1M Grifols Solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Bicarbonato Sódico 1M Grifols Solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ampolla de 10 ml de solución contiene: Hidrogenocarbonato de sodio
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Bicarbonato Sódico 1M Grifols Solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ampolla de 10 ml de solución contiene: Hidrogenocarbonato de sodio
Ácido: Especie que tiene tendencia a ceder un H + Base: Especie que tiene tendencia a aceptar un H +
 Reacciones ácido-base 1 Brønsted-Lowry (1923) Ácido: Especie que tiene tendencia a ceder un H + Base: Especie que tiene tendencia a aceptar un H + CH 3 COOH (aq) + H 2 O (l) H 3 O + (aq) + CH 3 COO (aq)
Reacciones ácido-base 1 Brønsted-Lowry (1923) Ácido: Especie que tiene tendencia a ceder un H + Base: Especie que tiene tendencia a aceptar un H + CH 3 COOH (aq) + H 2 O (l) H 3 O + (aq) + CH 3 COO (aq)
TEMA 7: REACCIONES DE TRANSFERENCIA DE PROTONES
 TEMA 7: REACCIONES DE TRANSFERENCIA DE PROTONES 1. Concepto de ácido y de base De las distintas teorías que existen de ácidos y bases, sólo vamos a exponer dos de las más utilizadas, la teoría de Arrhenius
TEMA 7: REACCIONES DE TRANSFERENCIA DE PROTONES 1. Concepto de ácido y de base De las distintas teorías que existen de ácidos y bases, sólo vamos a exponer dos de las más utilizadas, la teoría de Arrhenius
REGULACIÓN DEL ph. Teoría Acido-Base - Anfolitos. Por lo común lo vemos representado como ph = - log [H + ]
![REGULACIÓN DEL ph. Teoría Acido-Base - Anfolitos. Por lo común lo vemos representado como ph = - log [H + ] REGULACIÓN DEL ph. Teoría Acido-Base - Anfolitos. Por lo común lo vemos representado como ph = - log [H + ]](/thumbs/40/20899659.jpg) REGULACIÓN DEL ph Teoría Acido-Base - Anfolitos Que es el ph??? Por lo común lo vemos representado como ph = - log [H ] Estrictamente, ph = - log a H En soluciones diluídas expresarlo en concentración
REGULACIÓN DEL ph Teoría Acido-Base - Anfolitos Que es el ph??? Por lo común lo vemos representado como ph = - log [H ] Estrictamente, ph = - log a H En soluciones diluídas expresarlo en concentración
Alteraciones del Equilibrio Ácido Base
 Alteraciones del Equilibrio Ácido Base Pedro Jiménez Santana Fuente: Dr. Aberman Equilibrio ácido base ph arterial VALOR NORMAL : 7.37 7.43 ACIDEMIA: < 7.37 ALCALEMIA: > 7.43 Equilibrio ácido base PaCO2
Alteraciones del Equilibrio Ácido Base Pedro Jiménez Santana Fuente: Dr. Aberman Equilibrio ácido base ph arterial VALOR NORMAL : 7.37 7.43 ACIDEMIA: < 7.37 ALCALEMIA: > 7.43 Equilibrio ácido base PaCO2
Pruebas de función pulmonar. Diana Carolina Góngora
 Pruebas de función pulmonar Diana Carolina Góngora Definición Grupo de exámenes para medir la eficiencia de los pulmones para tomar y liberar aire, para movilizar gases, como el oxígeno, desde la atmósfera
Pruebas de función pulmonar Diana Carolina Góngora Definición Grupo de exámenes para medir la eficiencia de los pulmones para tomar y liberar aire, para movilizar gases, como el oxígeno, desde la atmósfera
INSUFICIENCIA RENAL AGUDA
 INSUFICIENCIA RENAL AGUDA La insuficiencia renal aguda es un síndrome clínico que se produce por una reducción brusca de la filtración glomerular con retención progresiva de productos nitrogenados en sangre
INSUFICIENCIA RENAL AGUDA La insuficiencia renal aguda es un síndrome clínico que se produce por una reducción brusca de la filtración glomerular con retención progresiva de productos nitrogenados en sangre
Terapia Líquida en Pediatría
 PROGRAMA DE EDUCACIÓN MEDICA CONTINUADA TERCER CURSO DE 1974-1975 LÍQUIDOS Y ELECTROLITOS EN LA PRACTICA MEDICA Terapia Líquida en Pediatría Dr. Francisco Cleaves T. La administración de líquidos parenterales
PROGRAMA DE EDUCACIÓN MEDICA CONTINUADA TERCER CURSO DE 1974-1975 LÍQUIDOS Y ELECTROLITOS EN LA PRACTICA MEDICA Terapia Líquida en Pediatría Dr. Francisco Cleaves T. La administración de líquidos parenterales
Química. Equilibrio ácido-base Nombre:
 Química DEPARTAMENTO DE FÍSICA E QUÍMICA Equilibrio ácido-base 25-02-08 Nombre: Cuestiones y problemas 1. a) Qué concentración tiene una disolución de amoníaco de ph =10,35? [1½ PUNTO] b) Qué es una disolución
Química DEPARTAMENTO DE FÍSICA E QUÍMICA Equilibrio ácido-base 25-02-08 Nombre: Cuestiones y problemas 1. a) Qué concentración tiene una disolución de amoníaco de ph =10,35? [1½ PUNTO] b) Qué es una disolución
Fotosíntesis y Respiración Celular
 Fotosíntesis y Respiración Celular INTRODUCCIÓN La energía lumínica es capturada por las plantas verdes y otros organismos fotosintéticos, que la transforman en energía química fijada en moléculas como
Fotosíntesis y Respiración Celular INTRODUCCIÓN La energía lumínica es capturada por las plantas verdes y otros organismos fotosintéticos, que la transforman en energía química fijada en moléculas como
MEDIO INTERNO HOMEOSTASIS. Estructura del medio interno. Se denomina asi al medio extracelular, el medio que rodea a las celulas
 MEDIO INTERNO Se denomina asi al medio extracelular, el medio que rodea a las celulas HOMEOSTASIS Estructura del medio interno El agua representa el 40-60% del peso corporal del organismo. 1 Distribución
MEDIO INTERNO Se denomina asi al medio extracelular, el medio que rodea a las celulas HOMEOSTASIS Estructura del medio interno El agua representa el 40-60% del peso corporal del organismo. 1 Distribución
Ácidos, Bases, ph y Soluciones Reguladoras María De La Luz Velázquez Monroy & Miguel Ángel Ordorica Vargas
 Introducción Ácidos, Bases, ph y Soluciones Reguladoras María De La Luz Velázquez Monroy & Miguel Ángel Ordorica Vargas Las propiedades ácido básicas de los compuestos orgánicos son importantes para su
Introducción Ácidos, Bases, ph y Soluciones Reguladoras María De La Luz Velázquez Monroy & Miguel Ángel Ordorica Vargas Las propiedades ácido básicas de los compuestos orgánicos son importantes para su
RIÑÓN Y LÍQUIDOS CORPORALES. 29. Regulación del equilibrio ácido-base
 RIÑÓN Y LÍQUIDOS CORPORALES 29. Regulación del equilibrio ácido-base INTRODUCCIÓN La concentración de iones H + libres en sangre se mantiene normalmente entre 40 y 45 nmol/litro, lo cual da un valor de
RIÑÓN Y LÍQUIDOS CORPORALES 29. Regulación del equilibrio ácido-base INTRODUCCIÓN La concentración de iones H + libres en sangre se mantiene normalmente entre 40 y 45 nmol/litro, lo cual da un valor de
Anatomía y Fisiología. de Vía aérea inferior. Dra. Ana M. Koatz
 Anatomía y Fisiología de Vía aérea inferior Dra. Ana M. Koatz Gersdorff, Hans von (d. 1529). Título: Feldtbůch der Wundartzney : newlich getruckt und gebessert. Anatomía a Respiratoria ESTRUCTURAS BÁSICASB
Anatomía y Fisiología de Vía aérea inferior Dra. Ana M. Koatz Gersdorff, Hans von (d. 1529). Título: Feldtbůch der Wundartzney : newlich getruckt und gebessert. Anatomía a Respiratoria ESTRUCTURAS BÁSICASB
SALES MINERALES , CO 3. Aniones: Cl -, PO 4. , NO 3, Cationes: Na +, Ca 2+, Mg 2+, Fe 2+, Fe 3+, K +
 SALES MINERALES Aniones: Cl -, PO 4 3-, CO 3 2-, NO 3, Cationes: Na +, Ca 2+, Mg 2+, Fe 2+, Fe 3+, K + SALES PRECIPITADAS Vieira SALES PRECIPITADAS: CaCO 3 Exoesqueleto de Ca Sales de Ca: caparazones
SALES MINERALES Aniones: Cl -, PO 4 3-, CO 3 2-, NO 3, Cationes: Na +, Ca 2+, Mg 2+, Fe 2+, Fe 3+, K + SALES PRECIPITADAS Vieira SALES PRECIPITADAS: CaCO 3 Exoesqueleto de Ca Sales de Ca: caparazones
PROSPECTO: INFORMACIÓN PARA EL USUARIO. Bicarbonato Sódico 1M Grifols Solución inyectable Hidrogenocarbonato de sodio
 PROSPECTO: INFORMACIÓN PARA EL USUARIO Bicarbonato Sódico 1M Grifols Solución inyectable Hidrogenocarbonato de sodio Lea todo el prospecto detenidamente antes de empezar a usar el medicamento. - Conserve
PROSPECTO: INFORMACIÓN PARA EL USUARIO Bicarbonato Sódico 1M Grifols Solución inyectable Hidrogenocarbonato de sodio Lea todo el prospecto detenidamente antes de empezar a usar el medicamento. - Conserve
Prospecto: información para el usuario. Bicarbonato Sódico 1/6 M Braun solución para perfusión Hidrogenocarbonato de sodio
 Prospecto: información para el usuario Bicarbonato Sódico 1/6 M Braun solución para perfusión Hidrogenocarbonato de sodio Lea todo el prospecto detenidamente antes de empezar a usar el medicamento - Conserve
Prospecto: información para el usuario Bicarbonato Sódico 1/6 M Braun solución para perfusión Hidrogenocarbonato de sodio Lea todo el prospecto detenidamente antes de empezar a usar el medicamento - Conserve
ALTERACIONES DEL EQUILIBRIO ACIDO BÁSICO
 Rev Cubana Cir 2006; 45(1) ALTERACIONES DEL EQUILIBRIO ACIDO BÁSICO INTRODUCCIÓN Los procesos metabólicos intracelulares producen ácidos, es decir, sustancias capaces de liberar iones H+, por oxidación
Rev Cubana Cir 2006; 45(1) ALTERACIONES DEL EQUILIBRIO ACIDO BÁSICO INTRODUCCIÓN Los procesos metabólicos intracelulares producen ácidos, es decir, sustancias capaces de liberar iones H+, por oxidación
Fisiología del evento ISQUEMIA / ANOXIA. Rodolfo A. Cabrales Vega MD Docente Programa de Medicina Universidad Tecnológica de Pereira
 Fisiología del evento ISQUEMIA / ANOXIA Rodolfo A. Cabrales Vega MD Docente Programa de Medicina Universidad Tecnológica de Pereira Porque cualquier miembro suelto, ya esté recubierto por piel o por carne,
Fisiología del evento ISQUEMIA / ANOXIA Rodolfo A. Cabrales Vega MD Docente Programa de Medicina Universidad Tecnológica de Pereira Porque cualquier miembro suelto, ya esté recubierto por piel o por carne,
COMPLICACIONES AGUDAS DE LA DIABETES MELLITUS
 COMPLICACIONES AGUDAS DE LA DIABETES MELLITUS Jornadas Inter-Hospitalarias Hospital Universitario La Paz Octubre 2005 EVA CASADO AMANDA OSPINA R4 DE BIOQUIMICA CLINICA COMPLICACIONES AGUDAS CETOACIDOSIS
COMPLICACIONES AGUDAS DE LA DIABETES MELLITUS Jornadas Inter-Hospitalarias Hospital Universitario La Paz Octubre 2005 EVA CASADO AMANDA OSPINA R4 DE BIOQUIMICA CLINICA COMPLICACIONES AGUDAS CETOACIDOSIS
Ventilación Mecánica en el RN Cardiópata con Hiperflujo Pulmonar
 Ventilación Mecánica en el RN Cardiópata con Hiperflujo Pulmonar Dra. Ximena Alegría Palazón Profesor Adjunto Universidad de Valparaíso Unidad de Neonatología Hospital Carlos Van Buren VM Cardiopatías
Ventilación Mecánica en el RN Cardiópata con Hiperflujo Pulmonar Dra. Ximena Alegría Palazón Profesor Adjunto Universidad de Valparaíso Unidad de Neonatología Hospital Carlos Van Buren VM Cardiopatías
EXAMEN DE PROBLEMAS INSTRUCCIONES 3 horas código de alumno
 EXAMEN DE PROBLEMAS INSTRUCCIONES 1. Se presentan cuatro problemas para resolver en un tiempo máximo de 3 horas.. Escribir el código de alumno en cada una de las hojas de los problemas. No deben existir
EXAMEN DE PROBLEMAS INSTRUCCIONES 1. Se presentan cuatro problemas para resolver en un tiempo máximo de 3 horas.. Escribir el código de alumno en cada una de las hojas de los problemas. No deben existir
Intoxicación por Metanol
 Intoxicación por Metanol Tatiana García Rodríguez San Miguel Lluis Marruecos Sant Indalecio Morán Chorro Medicina Intensiva Hospital de Santa Creu i Sant Pau 02 Generalidades Farmacología Clínica Diagnóstico
Intoxicación por Metanol Tatiana García Rodríguez San Miguel Lluis Marruecos Sant Indalecio Morán Chorro Medicina Intensiva Hospital de Santa Creu i Sant Pau 02 Generalidades Farmacología Clínica Diagnóstico
Análisis sistemático del equilibrio ácido-base en formato automatizado. Principios básicos y propuesta
 Trabajo de investigación Huerta Torrijos et al. Análisis sistemático del equilibrio ácido-base en formato automatizado Revista de la Asociación Mexicana de 69 pp 69-79 Vol. XV, Núm. 3 / May.-Jun. 2001
Trabajo de investigación Huerta Torrijos et al. Análisis sistemático del equilibrio ácido-base en formato automatizado Revista de la Asociación Mexicana de 69 pp 69-79 Vol. XV, Núm. 3 / May.-Jun. 2001
Clase 8. Funciones principales y estructura de los riñones
 Clase 8 Funciones principales y estructura de los riñones Funciones principales de los riñones La principal misión de los riñones es la excreción diferencial de diversas sustancias, de forma que la composición
Clase 8 Funciones principales y estructura de los riñones Funciones principales de los riñones La principal misión de los riñones es la excreción diferencial de diversas sustancias, de forma que la composición
Fisiología y envejecimiento Aparato urinario. Tema 11
 Tema 11 Funciones generales. Anatomía Nefrona Filtración glomerular Reabsorción tubular Secreción tubular Micción Envejecimiento Funciones generales * Mantenimiento de la homeostasis hídrica y electrolítica.
Tema 11 Funciones generales. Anatomía Nefrona Filtración glomerular Reabsorción tubular Secreción tubular Micción Envejecimiento Funciones generales * Mantenimiento de la homeostasis hídrica y electrolítica.
EQUILIBRIO ACIDO BASE
 EQUILIBRIO ACIDO BASE DR. EFRAIN ESTRADA CHOQUE, M.D. Lima, Perú EQUILIBRIO ACIDO BASE Es el mantenimiento de un nivel normal de la concentración n de iones hidrogeno (H+) en los fluidos del organismo.
EQUILIBRIO ACIDO BASE DR. EFRAIN ESTRADA CHOQUE, M.D. Lima, Perú EQUILIBRIO ACIDO BASE Es el mantenimiento de un nivel normal de la concentración n de iones hidrogeno (H+) en los fluidos del organismo.
Formación de la orina
 tema 2 Formación de la orina 1. Formación de la orina La función principal del riñón es la de retener y reabsorber las sustancias esenciales, excretando a su vez aquellos productos de desecho producidos
tema 2 Formación de la orina 1. Formación de la orina La función principal del riñón es la de retener y reabsorber las sustancias esenciales, excretando a su vez aquellos productos de desecho producidos
Fisiología del evento Isquemia / Anoxia. Rodolfo A. Cabrales Vega MD Profesor Asociado Programa de Medicina
 Fisiología del evento Isquemia / Anoxia Rodolfo A. Cabrales Vega MD Profesor Asociado Programa de Medicina Porque cualquier miembro suelto, ya esté recubierto por piel o por carne, está hueco. Y, cuando
Fisiología del evento Isquemia / Anoxia Rodolfo A. Cabrales Vega MD Profesor Asociado Programa de Medicina Porque cualquier miembro suelto, ya esté recubierto por piel o por carne, está hueco. Y, cuando
Sistema renal. Odontología 2008
 Sistema renal Odontología 2008 Sistema renal Los riñones Si están bien perfundidos Mediante los mecanismos básicos: Filtración Reabsorción Secreción Regulan el medio interno Eliminan sustancias de deshecho
Sistema renal Odontología 2008 Sistema renal Los riñones Si están bien perfundidos Mediante los mecanismos básicos: Filtración Reabsorción Secreción Regulan el medio interno Eliminan sustancias de deshecho
EL APARATO URINARIO. 1. Patología. 2. Procedimientos relacionados TERESA ULLOA NEIRA ET 310
 EL APARATO URINARIO 1. Patología 2. Procedimientos relacionados TERESA ULLOA NEIRA ET 310 Hormonas implicadas en la formación de orina: H. ANTIDIURÉTICA (ADH): Regula la absorción y eliminación del agua
EL APARATO URINARIO 1. Patología 2. Procedimientos relacionados TERESA ULLOA NEIRA ET 310 Hormonas implicadas en la formación de orina: H. ANTIDIURÉTICA (ADH): Regula la absorción y eliminación del agua
OXIGENOTERAPIA II JORNADAS INTERNACIONALES DE INVESTIGACIÓN EN EDUCACIÓN Y SALUD:
 OXIGENOTERAPIA II JORNADAS INTERNACIONALES DE INVESTIGACIÓN EN EDUCACIÓN Y SALUD: "Experiencias en educación y salud transcultural" AUTORES: Fernández Sánchez, Pedro. Diplomado en enfermería. Hospital
OXIGENOTERAPIA II JORNADAS INTERNACIONALES DE INVESTIGACIÓN EN EDUCACIÓN Y SALUD: "Experiencias en educación y salud transcultural" AUTORES: Fernández Sánchez, Pedro. Diplomado en enfermería. Hospital
PUNTO 1º - LA FUNCIÓN DE NUTRICIÓN
 PUNTO 1º - LA FUNCIÓN DE NUTRICIÓN Definición Nutrición: Conjunto de procesos mediante los cuales los seres vivos toman materia y energía del exterior y la transforman en materia propia y en energía. Definición
PUNTO 1º - LA FUNCIÓN DE NUTRICIÓN Definición Nutrición: Conjunto de procesos mediante los cuales los seres vivos toman materia y energía del exterior y la transforman en materia propia y en energía. Definición
REPÚBLICA BOLIVARIANA DE VENEZUELA MINISTERIO DE EDUCACIÓN SUPERIOR
 REPÚBLICA BOLIVARIANA DE VENEZUELA MINISTERIO DE EDUCACIÓN SUPERIOR PROGRAMA NACIONAL DE FORMACIÓN DE MEDICINA INTEGRAL COMUNITARIA PLAN CALENDARIO. DISCIPLINA: MORFOFISIOLOGÍA Asignatura: Morfofisiología
REPÚBLICA BOLIVARIANA DE VENEZUELA MINISTERIO DE EDUCACIÓN SUPERIOR PROGRAMA NACIONAL DE FORMACIÓN DE MEDICINA INTEGRAL COMUNITARIA PLAN CALENDARIO. DISCIPLINA: MORFOFISIOLOGÍA Asignatura: Morfofisiología
EJERCICIOS. UNIDAD 2. La nutrición humana.
 EJERCICIOS. UNIDAD 2. La nutrición humana. 1. El intercambio de materia y energía que todo ser vivo realiza con su medio, corresponde a la función de: a) Nutrición b) Relación c) Reproducción d) Adaptación
EJERCICIOS. UNIDAD 2. La nutrición humana. 1. El intercambio de materia y energía que todo ser vivo realiza con su medio, corresponde a la función de: a) Nutrición b) Relación c) Reproducción d) Adaptación
Metabolismo de AMINOÁCIDOS
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,011 Metabolismo de AMINOÁCIDOS Dr. Mynor A. Leiva Enríquez Fuente:
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,011 Metabolismo de AMINOÁCIDOS Dr. Mynor A. Leiva Enríquez Fuente:
Dr. Miguel Ángel González Sosa
 Dr. Miguel Ángel González Sosa Presentación realizada en el curso de Clinopatología del Aparato Respiratorio dentro de la Licenciatura de Médico Cirujano del Área Académica de Medicina en el semestre Julio
Dr. Miguel Ángel González Sosa Presentación realizada en el curso de Clinopatología del Aparato Respiratorio dentro de la Licenciatura de Médico Cirujano del Área Académica de Medicina en el semestre Julio
Proporciona el oxígeno que el cuerpo necesita y elimina el dióxido de carbono o gas carbónico que se produce en todas las células.
 Proporciona el oxígeno que el cuerpo necesita y elimina el dióxido de carbono o gas carbónico que se produce en todas las células. La respiración es un proceso involuntario y automático, en que se extrae
Proporciona el oxígeno que el cuerpo necesita y elimina el dióxido de carbono o gas carbónico que se produce en todas las células. La respiración es un proceso involuntario y automático, en que se extrae
Un adulto sano, suele ser capaz de mantener los equilibrios hidroelectrolíticos y ácido-base.
 BALANCE HIDRICO BALANCE HIDRICO Para conservar la salud y mantener las funcíones corporales, es necesario un EQUILIBRIO líquido, electrolítico y ácido báse. El requerimiento es: aporte y eliminación armónico
BALANCE HIDRICO BALANCE HIDRICO Para conservar la salud y mantener las funcíones corporales, es necesario un EQUILIBRIO líquido, electrolítico y ácido báse. El requerimiento es: aporte y eliminación armónico
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2010 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 010 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE Junio, Ejercicio 6, Opción A Junio, Ejercicio 4, Opción B Reserva 1, Ejercicio 4, Opción A Reserva, Ejercicio 5, Opción
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 010 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE Junio, Ejercicio 6, Opción A Junio, Ejercicio 4, Opción B Reserva 1, Ejercicio 4, Opción A Reserva, Ejercicio 5, Opción
ALCALOSIS RESPIRATORIA
 ALCALOSIS RESPIRATORIA El presente artículo es una actualización al mes de julio del 2006 del Capítulo del Dr. Carlos Lovesio, del Libro Medicina Intensiva, Dr. Carlos Lovesio, Editorial El Ateneo, Buenos
ALCALOSIS RESPIRATORIA El presente artículo es una actualización al mes de julio del 2006 del Capítulo del Dr. Carlos Lovesio, del Libro Medicina Intensiva, Dr. Carlos Lovesio, Editorial El Ateneo, Buenos
Gases Respiración Externa
 Gases Respiración Externa Respiración Interna o Celular Externa 1 Respiración Interna o Celular - Común a casi todos los seres vivos - Implica el intercambio de ciertos gases entre el medio y las células.
Gases Respiración Externa Respiración Interna o Celular Externa 1 Respiración Interna o Celular - Común a casi todos los seres vivos - Implica el intercambio de ciertos gases entre el medio y las células.
Bioingeniería - UNER. Cátedra de Fisiopatología. Fisiopatología respiratoria (diapositivas proyectadas en clases)
 Bioingeniería - UNER Cátedra de Fisiopatología Fisiopatología respiratoria (diapositivas proyectadas en clases) Prof. Dr. Armando Pacher Dr. Roberto Lombardo 2006 Fisiopatología de aparatos y sistemas
Bioingeniería - UNER Cátedra de Fisiopatología Fisiopatología respiratoria (diapositivas proyectadas en clases) Prof. Dr. Armando Pacher Dr. Roberto Lombardo 2006 Fisiopatología de aparatos y sistemas
Volemia y Glóbulos Rojos
 UNIVERSIDAD CENTROCCIDENTAL LISANDRO ALVARADO DECANATO DE CIENCIAS DE LA SALUD DEPARTAMENTO DE FISIOLOGIA ENFERMERIA Volemia y Glóbulos Rojos Lic. Ana López-Fonseca [email protected] CONTENIDO.-Sangre
UNIVERSIDAD CENTROCCIDENTAL LISANDRO ALVARADO DECANATO DE CIENCIAS DE LA SALUD DEPARTAMENTO DE FISIOLOGIA ENFERMERIA Volemia y Glóbulos Rojos Lic. Ana López-Fonseca [email protected] CONTENIDO.-Sangre
Concepto de ph. ph = - log [H + ]
![Concepto de ph. ph = - log [H + ] Concepto de ph. ph = - log [H + ]](/thumbs/39/19109627.jpg) Fuerza de Ácidos y Bases Concepto de ph Ácidos Los ácidos se diferencian de acuerdo a su capacidad para ceder protones al medio, o químicamente dicho, por su capacidad de disociación, esa también es la
Fuerza de Ácidos y Bases Concepto de ph Ácidos Los ácidos se diferencian de acuerdo a su capacidad para ceder protones al medio, o químicamente dicho, por su capacidad de disociación, esa también es la
