Estructuras Cristalinas
|
|
|
- María Cristina Pérez Vega
- hace 6 años
- Vistas:
Transcripción
1 Estructuras Cristalinas Bibliografía: Solid State Chemistry: An introduction, L. Smart and E. Moore Solid State Chemistry and its applications, A.R. West
2 Enlace en Cerámicos Iónico Mezcla Pauling: % Carácter Iónico= Covalente e ( X A X B ) 4 Porcentaje de carácter iónico y covalente del enlace para algunos materiales cerámicos determina la ESTRUCTURA CRISTALINA 2 Material Cerámico MgO Mg O 2, Al 2 O 3 Al O 2, SiO 2 Si O 1, Si 3 N 4 Si N 1, SiC Átomos enlazados Si-C X A -X B 0,7 % Carácter iónico 11 % Carácter covalente 89 2
3 Empaquetamiento de iones en estructuras iónicas Estructura iónica: empaquetamiento de aniones con cationes en intersticios Los iones tienden a empaquetarse densamente para E total Tamaño C + A - (en general r catión < r anión ) Electroneutralidad Índice de coordinación (Al I.C. estabilidad) h.o h.t En estructuras COMPACTAS es cierto que FCC h.o Nº huecos tetraédricos=2n Nº huecos Octaédricos=n n = Nº átomos de la celda unidad h.t 3
4 La relación de radios cuando los A - y C + están en contacto Relación de radios crítica Empaquetamiento de iones en estructuras iónicas Número de Coordinación r C /r A Geometría de coordinación ESTABLES <0,155 0,155-0,225 0,225-0,414 0,414-0,732 0,732-1 A cada lado Vértices de un triángulo Vértices de un tetraedro Vértices de un octaedro Vértices de un cubo INESTABLE vibra en su jaula de A - 4
5 Empaquetamiento de iones en estructuras iónicas Índice de Coordinación para los sólidos iónicos CsCl y NaCl? Cs + =0,170 nm Na + =0,102 nm Cl - =0,181 nm r r Cs Cl + = 0,94 > 0,732 I. C = 8 Coord.Cúbica r r Na Cl + = 0,56 > 0,414 I. C = 6 Coord. Octaédrica I.C. r C /r A Geometría 6 8 0,414-0,732 0,732-1 Vértices de un octaedro Vértices de un cubo 5
6 Empaquetamiento de iones en estructuras iónicas 6
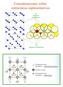
7 a) Estructura cristalina tipo NaCl Cl - : empaquetamiento fcc Na: todos h.o., I.C.: 6 Celdilla unidad: 4 Na + y 4 Cl - Cerámicas que adoptan este tipo estructural: haluros alcalinos (excp. Cs y Tl), MgO, CaO, FeO, NiO b) Estructura cristalina tipo CsCl Cerámico prop. Aislante eléctrico Cl - : empaquetamiento cúbico primitivo Cs + : centro de cubo I.C (Cs).: 8 Cerámicas que adoptan este tipo estructural: CsBr, TlCl, TlBr, aleaciones CuZn, AlNi. 7
8 c) Estructura cristalina tipo blenda, ZnS S 2- : empaquetamiento fcc Zn 2+ : ½ h.t. I.C.: 4 4 Zn 2+ y 4 S 2- por celda unidad r r Zn S 2+ 2 = I. C. = 4 Según Pauling enlace Zn-S ~87% covalente Cerámicas que adoptan este tipo estructural: CdS, HgS Células solares: Fotoconductores cerámicos Si todos los atm. fueran iguales: Estructura diamante 8
9 d) Estructura cristalina tipo FLUORITA CaF 2 Ca 2+ : empaquetamiento fcc F - : todos h.t. (8) I.C.(Ca 2+ ): 8 ; I.C.(F - ): 4 Ca 2+ F - R(Ca 2+ )<R(F - ) Empaquetamiento cúbico primitivo de F - Ca 2+ : centro cubo Cerámicas que adoptan este tipo estructural: UO 2, ThO 2, CeO 2,, 9
10 e) Estructura cristalina tipo PEROVSKITA, ABO 3 (BaTiO 3 ) A y B cationes con diferente tamaño (r A >>>r B ) O 2- y Ca 2+ : empaquetamiento fcc Ti 4+ : 1/4 h.0. I.C.(Ti 2+ ): 6 ; I.C.(Ca 2+ ): 12 Cerámicas que adoptan este tipo estructural: BaTiO 3, CaTiO 3, SrTiO 3, PbZrO 3,, KNbO 3, LiNbO 3, Materiales ferroeléctricos, Superconductores: YBa 2 Cu 3 O 7 TIPO A 10
11 f) Estructura cristalina tipo ESPINELA, AB 2 O 4 A 2+ B 2 3+ O 4 Empaquetamiento casi fcc: O 2- Celda Unidad: 56 iones (8 A, 16 B y 32 O) y 96 posiciones reticulares: 64: h. Tetraédricas (1/8) : 8 h.t. 32: h. Octaédricas (1/2) : 16 h.o. Sol. Sólidas (A 1-x B x ) t (B 2-x A x ) o O 4 ESPINELA NORMAL ESPINELA INVERSA A 2+ : 8 h.t. B 3+ : 16 ho A 2+ : 8 h.o. B 3+ : 8 h.o. B 3+ : 8 h.t. Los cerámicos magnéticos comerciales están basados en la estructura espinela: MgFe 2 O 4, NiFe 2 O 4, MnFe 2 O 4, y otros óxidos ferrimagnéticos. 11
12 g) Estructura cristalina tipo CORINDÓN Al 2 O 3 O 2- : empaquetamiento hcp 6 iones/celdilla Al 3+ : 2/3 h.o. (ELECTRONEUTRALIDAD) I.C. (Al 3+ ): 6 ; I.C.(O 2- ): 6 Cerámicas que adoptan este tipo estructural: Cr 2 O 3, α-fe 2 O 3, 12
13 h) Estructura cristalina tipo Rutilo: TiO2 Adopta un desordenado h.c.p de O 2- con ½ h.t. ocupados (Ti 4+ ) c Celda unidad: TETRAGONAL a i.c. (Ti): 6 (octaedro distorsionado) i.c. (O): 3 (triángulo casi equilátero) Capas planares ideales de O 2 Llenas Ti 4+ a o y vacíos a 1/2 Vacías a 0 y llenos a 1/2 hcp de O 2- a:b: A c: A 13
14 h) Estructura cristalina tipo Rutilo: TiO2 Átomos de O octaedros Difusión de iones peq. Li +, H + a través de túneles (ELECTRODOS en dispositivos electroquímicos) Blanqueantes (Pinturas, plásticos, ): No tóxicos Cada O es compartido tres octaedros PbO: muy tóxico Octaedros ( 90º) compartiendo vértices y lados 14
15 Cerámicas Covalentes Predominio de Enl. Covalente, pero también enl. iónico DIAMANTE Tipo Blenda ( de Zn) Muy duro: abrasivo BN Estructura hexagonal ( grafito) Muy dúctil: lubricante 22% iónico Pf: 3000ºC SiC 12% ionico Ej: SiO 2 : 51% enl. iónico MgO, NaCl: 70% enl. iónico Tipo Blenda ( de Zn) Muy duro: abrasivo, refractario Cer. Estructural resist. desgaste Pf: 2700ºC 15
16 Cerámicas Covalentes Si 3 N 4 Si hibridación sp 3 i.c.: 4 Tetraedros de SiN 4 N hibridación sp 2 i.c.: 3 N unido a 3 Si 30% enl. ionico Pf: 1900ºC Estrc. ABIERTA 2 politipos (hexagonales): Diferente secuencia de apilamiento en dirección c N Si α-si 3 N 4 abcd Si 12 N 16 β-si 3 N 4 abab Si 6 N 8 SIALONES: Familia de S.S: Si-Al-O-N 16
17 Estructuras Cristalinas de los silicatos Si y O son los elementos más abundantes en la corteza terrestre Base de cerámicas tradicionales Bajo precio Materiales útiles Gran disponibilidad Propiedades especiales Construcción cemento vidrio) (ladrillos, Mat. aislantes eléctricos y térmicos ( T fusión) 17
18 Estructuras Cristalinas de los silicatos Clasificación de los silicatos en función de la ordenación de los tetraedros [SiO 4 ] 4-. Unidad básica estructural SiO 4 4- a)aislados Si en coordinación tetraédrica tetraedros unidos por vértices Tipo de enlace (Pauling): 50%iónico-50% covalente r C /r A = 0.29 estruct. estable con coord. tetraédr. Multitud de posibles estructuras: a) Estructuras de silicatos aislados b) Estructuras de anillo y cadena c) Estructuras laminares d) Estructuras tridimensionales Anillo Cadena Laminar 3D 18
19 Estructuras Cristalinas de los silicatos Unidad básica estructural SiO 4 4- Si en coordinación tetraédrica tetraedros unidos por vértices Tipo de enlace (Pauling): 50%iónico-50% covalente rc /r A = 0.29 estruct. estable con coord. tetraédr. Multitud de posibles estructuras: a) Estructuras de silicatos aislados b) Estructuras de anillo y cadena c) Estructuras laminares d)estructuras tridimensionales 19
20 Estructuras Cristalinas de los silicatos Aislados Anillo Cadena Laminar 20
21 Estructuras Cristalinas de los silicatos b) Estrucutra de anillo y cadenas 2 de los 4 átomos de O - del tetraedro SiO 4 4- están unidos a otro tetraedro para formar cadenas de silicato c) Estructura Láminar Fórmula: (SiO 3 ) n 2n- 3 de los 4 átomos de O - del tetraedro SiO 4 4- están unidos a otro tetraedro para formar capas de silicato un O - sin enlazar en cada tetraedro Fórmula: Si 2 O 5 2- carga (-) Se une a láminas (+) Formación de la CAOLINITA Caolinita Al 2 (OH) 4 2+ Talco: Mg 3 (OH)
22 Estructuras Cristalinas de los silicatos d) Silicatos Tridimensionales Unidad: tetraedros SiO 4-4 Se comparten todos los vértices del tetraedro Polimorfismos Sílice Componente importante en muchas cerámicas tradicionales y muchos tipos de vidrio 870ºC cuarzo tridimita 1470ºC cristobalita 1710ºC fundido Cristobalita: Si0 4 : 22
Tema 14.- Definición, Clasificación y Conformado
 BLOQUE V.- MATERIALES CERÁMICOS Tema 14.- Definición, y Conformado William D. Callister, Jr Introducción a la Ciencia e Ingeniería de los Materiales. Tomo **. Ed. Reverté James F. Shackerlford Introducción
BLOQUE V.- MATERIALES CERÁMICOS Tema 14.- Definición, y Conformado William D. Callister, Jr Introducción a la Ciencia e Ingeniería de los Materiales. Tomo **. Ed. Reverté James F. Shackerlford Introducción
Estructura de sólidos
 Estructura de sólidos Química Inorgánica - 2006 Tipos de estructuras cristalinas cristal enlace características molecular covalente-baja energía cristales blandos, bajo p.f. red covalente covalente cristales
Estructura de sólidos Química Inorgánica - 2006 Tipos de estructuras cristalinas cristal enlace características molecular covalente-baja energía cristales blandos, bajo p.f. red covalente covalente cristales
TEMA 8: SÓLIDOS INORGÁNICOS. 2.- Redes bidimensionales y tridimensionales
 TEMA 8: SÓLIDOS INORGÁNICOS 1.- Tipos de sólidos 2.- Redes bidimensionales y tridimensionales 3.- Celda unidad y sus parámetros: - nº de átomos / celda - nº de coordinación (NC) - fracción de volumen ocupado
TEMA 8: SÓLIDOS INORGÁNICOS 1.- Tipos de sólidos 2.- Redes bidimensionales y tridimensionales 3.- Celda unidad y sus parámetros: - nº de átomos / celda - nº de coordinación (NC) - fracción de volumen ocupado
Los sólidos iónicos. Estructuras características de los sólidos iónicos
 Los sólidos iónicos Los compuestos iónicos suelen presentar una serie de características físicas que los distinguen de los covalentes. Así, los sólidos iónicos como el cloruro sódico y el nitrato de potasio
Los sólidos iónicos Los compuestos iónicos suelen presentar una serie de características físicas que los distinguen de los covalentes. Así, los sólidos iónicos como el cloruro sódico y el nitrato de potasio
Tipos de estructuras. Introducción a la Ciencia de Materiales. M. Bizarro F. M. Sánchez
 Tipos de estructuras Empaquetamiento compacto Son estructuras formadas por átomos de igual tamaño que se unen mediante enlace metálico (esferas duras) A B A : A B C : FCC vs HCP El factor de empaquetamiento
Tipos de estructuras Empaquetamiento compacto Son estructuras formadas por átomos de igual tamaño que se unen mediante enlace metálico (esferas duras) A B A : A B C : FCC vs HCP El factor de empaquetamiento
ESTRUCTURAS CARACTERÍSTICAS
 ESTRUCTURAS CARACTERÍSTICAS En este capítulo se describen algunas estructuras muy simples que permitirán analizar la disposición de los átomos de diversos compuestos característicos en los que el enlace
ESTRUCTURAS CARACTERÍSTICAS En este capítulo se describen algunas estructuras muy simples que permitirán analizar la disposición de los átomos de diversos compuestos característicos en los que el enlace
Ing. Fredy Velázquez Soto
 Ing. Fredy Velázquez Soto TIPOS DE SÓLIDOS Sólidos cristalinos Los átomos, iones o moléculas se empaquetan en un arreglo ordenado Sólidos covalentes ( diamante, cristales de cuarzo), sólidos metálicos,
Ing. Fredy Velázquez Soto TIPOS DE SÓLIDOS Sólidos cristalinos Los átomos, iones o moléculas se empaquetan en un arreglo ordenado Sólidos covalentes ( diamante, cristales de cuarzo), sólidos metálicos,
Bloque II: Silicatos BLOQUE III: CERAMICAS TRADICIONALES SILICATOS. Bibliografía Química Inorgánica, Enrique Gutierrez Rios
 BLOQUE III: CERAMICAS TRADICIONALES SILICATOS Bibliografía Química Inorgánica, Enrique Gutierrez Rios 1 Características generales Estructuras tridimensionales: XRD Эn sólo Estado Sólido Aplicación industriales
BLOQUE III: CERAMICAS TRADICIONALES SILICATOS Bibliografía Química Inorgánica, Enrique Gutierrez Rios 1 Características generales Estructuras tridimensionales: XRD Эn sólo Estado Sólido Aplicación industriales
Tema 4. Cristaloquímica. Descripción estructural y
 Tema 4. Cristaloquímica. Descripción estructural y estructuras tipos Qué objetivos tiene la Cristaloquímica? Las fases cristalinas son componentes esenciales de los materiales, y especificamente de los
Tema 4. Cristaloquímica. Descripción estructural y estructuras tipos Qué objetivos tiene la Cristaloquímica? Las fases cristalinas son componentes esenciales de los materiales, y especificamente de los
Igual número de cationes y aniones. Ejemplos: cloruro de sodio (NaCl), cloruro de cesio (CsCl), blenda (ZnS), etc.
 6. MATERIALES CERÁMICOS 6.1 Estructura de los cerámicos Enlace atómico: parcial o totalmente iónico Iones metálicos: cationes (ceden sus electrones, +), aniones (aceptan electrones, - ). Estructuras cristalinas,
6. MATERIALES CERÁMICOS 6.1 Estructura de los cerámicos Enlace atómico: parcial o totalmente iónico Iones metálicos: cationes (ceden sus electrones, +), aniones (aceptan electrones, - ). Estructuras cristalinas,
Consideraciones sobre estructuras representativas
 Consideraciones sobre estructuras representativas CONSIDERACIONES SOBRE ESTRUCTURAS REPRESENTATIVAS: En el empacamiento compacto hcp y ccp el número de coordinación es 12 Los elementos metálicos son los
Consideraciones sobre estructuras representativas CONSIDERACIONES SOBRE ESTRUCTURAS REPRESENTATIVAS: En el empacamiento compacto hcp y ccp el número de coordinación es 12 Los elementos metálicos son los
Sólidos Arreglos y celdas unitarias. Ramón L. Hernández Castillo Enero 2012
 Sólidos Arreglos y celdas unitarias Ramón L. Hernández Castillo Enero 2012 Importancia de estudiar los sólidos cristalinos La mayoría de los compuestos inorgánicos son sólidos Casi todos los elementos
Sólidos Arreglos y celdas unitarias Ramón L. Hernández Castillo Enero 2012 Importancia de estudiar los sólidos cristalinos La mayoría de los compuestos inorgánicos son sólidos Casi todos los elementos
Tema 2.- Estructura de la Materia
 BLOQUE II.- ESTRUCTURA Estructura de la Materia * James F. Shackerlford Introducción a la Ciencia de Materiales para Ingenieros. Cuarta edición. Ed. Prentice Hall (1998) * Pat L. Mangonon Ciencia de Materiales:
BLOQUE II.- ESTRUCTURA Estructura de la Materia * James F. Shackerlford Introducción a la Ciencia de Materiales para Ingenieros. Cuarta edición. Ed. Prentice Hall (1998) * Pat L. Mangonon Ciencia de Materiales:
Sólidos Covalentes. Tema 4: Estado Sólido. QUIMICA GENERAL Química Inorgánica Sólidos Covalentes
 Sólidos Covalentes Esta obra está licenciada bajo una Licencia Creative Commons Reconocimiento-NoComercial-SinObraDerivada 3.0 España Attribution-NonCommercial-NoDerivs 3.0 Unported CC BY-NC-ND 3.0 http://creativecommons.org/licenses/by-nc-nd/3.0/es/
Sólidos Covalentes Esta obra está licenciada bajo una Licencia Creative Commons Reconocimiento-NoComercial-SinObraDerivada 3.0 España Attribution-NonCommercial-NoDerivs 3.0 Unported CC BY-NC-ND 3.0 http://creativecommons.org/licenses/by-nc-nd/3.0/es/
Sólidos Iónicos El enlace Iónico (1)
 1 Sólidos Iónicos El enlace Iónico (1) 2 * Huheey, J. E., Keiter, R. L., Keiter, E. A., Inorganic Chemistry: Principles of Structure and Reactivity, 4ª Ed., Harper Collins, 1993. Capítulo 4. * Douglas,
1 Sólidos Iónicos El enlace Iónico (1) 2 * Huheey, J. E., Keiter, R. L., Keiter, E. A., Inorganic Chemistry: Principles of Structure and Reactivity, 4ª Ed., Harper Collins, 1993. Capítulo 4. * Douglas,
Conductores Iónicos. BLOQUE IV: CERAMICAS DE ALTAS PRESTACIONES Cerámicas Funcionales
 BLOQUE IV: CERAMICAS DE ALTAS PRESTACIONES Cerámicas Funcionales Conductores Iónicos Bibliografía: Solid State Chemistry: An introduction, L. Smart and E. Moore. 1992 (Cap. 3) Solid State Chemistry and
BLOQUE IV: CERAMICAS DE ALTAS PRESTACIONES Cerámicas Funcionales Conductores Iónicos Bibliografía: Solid State Chemistry: An introduction, L. Smart and E. Moore. 1992 (Cap. 3) Solid State Chemistry and
TECTOSILICATOS INTRODUCCIÓN GRUPO DE LA SILICE ESTRUCTURAS POLIMORFISMO. Magdalena Rodas
 TECTOSILICATOS INTRODUCCIÓN GRUPO DE LA SILICE ESTRUCTURAS POLIMORFISMO Magdalena Rodas TECTOSILICATOS Grupo de la sílice (SiO 2 ) Grupo de los feldespatos (Si 3 Al O 8 ) -1 Grupo de los feldespatóides
TECTOSILICATOS INTRODUCCIÓN GRUPO DE LA SILICE ESTRUCTURAS POLIMORFISMO Magdalena Rodas TECTOSILICATOS Grupo de la sílice (SiO 2 ) Grupo de los feldespatos (Si 3 Al O 8 ) -1 Grupo de los feldespatóides
Cl Electrones de valencia: Cl: 7 3 = 21 P: 5 Total 26 Tres enlaces sencillos: - 6 Electrones restantes: 20
 ESTRUCTURAS DE LEWIS PARA EL ENLACE COVALENTE.- Lewis sugirió que los átomos comparten electrones para alcanzar la configuración de gas noble y tener así una estructura más estable. Salvo en el caso de
ESTRUCTURAS DE LEWIS PARA EL ENLACE COVALENTE.- Lewis sugirió que los átomos comparten electrones para alcanzar la configuración de gas noble y tener así una estructura más estable. Salvo en el caso de
Capítulo 2 La estructura de los sólidos cristalinos
 Capítulo 2 La estructura de los sólidos cristalinos TEMA 2: La estructura de los sólidos cristalinos 1. Los enlaces interatómicos 2. La estructura cristalina 3. Estructuras de empaquetamiento compacto
Capítulo 2 La estructura de los sólidos cristalinos TEMA 2: La estructura de los sólidos cristalinos 1. Los enlaces interatómicos 2. La estructura cristalina 3. Estructuras de empaquetamiento compacto
- Enlace Iónico - Enlace Covalente - Van der Waals - Polimorfismo y Transformaciones - Estructura Vítrea
 TEMA 3. ESTRUCTURA ATÓMICA Y PROPIEDADES FÍSICAS DE LOS MATERIALES CERÁMICOS ENLACE Y ESTRUCTURA - Enlace Iónico - Enlace Covalente - Van der Waals - Polimorfismo y Transformaciones - Estructura Vítrea
TEMA 3. ESTRUCTURA ATÓMICA Y PROPIEDADES FÍSICAS DE LOS MATERIALES CERÁMICOS ENLACE Y ESTRUCTURA - Enlace Iónico - Enlace Covalente - Van der Waals - Polimorfismo y Transformaciones - Estructura Vítrea
Estructura Cristalina de Sólidos
 Estructura Cristalina de Sólidos Relación entre estructura periódica y propiedades Bibliografía: 1. Solid State Physics. Ashcroft and Mermin. 2. Solid State Chemistry. West. 3. Química del Estado Sólido.
Estructura Cristalina de Sólidos Relación entre estructura periódica y propiedades Bibliografía: 1. Solid State Physics. Ashcroft and Mermin. 2. Solid State Chemistry. West. 3. Química del Estado Sólido.
3.- Calcular y compar ar las densidades at ómicas lineales de las dir ecciones : [1,0,0], [1,1,0] y [1,1,1] en la red FCC y en la red BCC.
![3.- Calcular y compar ar las densidades at ómicas lineales de las dir ecciones : [1,0,0], [1,1,0] y [1,1,1] en la red FCC y en la red BCC. 3.- Calcular y compar ar las densidades at ómicas lineales de las dir ecciones : [1,0,0], [1,1,0] y [1,1,1] en la red FCC y en la red BCC.](/thumbs/58/41894864.jpg) GEOMETRÍA CRISTALINA: 1.- Determinar los índices de Miller de una cara del cubo. 2.- Repr esent ar en el espacio del sist ema cúbico, los planos cuyos índices de Miller son (1,0,3), (1,1,1) y (1,0,1) y
GEOMETRÍA CRISTALINA: 1.- Determinar los índices de Miller de una cara del cubo. 2.- Repr esent ar en el espacio del sist ema cúbico, los planos cuyos índices de Miller son (1,0,3), (1,1,1) y (1,0,1) y
Síntesis y Caracterización Estructural de los Materiales Ángel Carmelo Prieto Colorado
 Síntesis y Caracterización Estructural de los Materiales Ángel Carmelo Prieto Colorado Física de la Materia Condensada, Cristalografía y Mineralogía. Facultad de Ciencias. Universidad de Valladolid. Estructura
Síntesis y Caracterización Estructural de los Materiales Ángel Carmelo Prieto Colorado Física de la Materia Condensada, Cristalografía y Mineralogía. Facultad de Ciencias. Universidad de Valladolid. Estructura
Empaquetamiento compacto
 Empaquetamiento compacto Energía y empaquetamiento No denso, empaquetamiento aleatorio Energy Distancia del enlace energía de enlace Denso, empaquetamiento ordenado Energy distancia del enlace r Energía
Empaquetamiento compacto Energía y empaquetamiento No denso, empaquetamiento aleatorio Energy Distancia del enlace energía de enlace Denso, empaquetamiento ordenado Energy distancia del enlace r Energía
Naturaleza del enlace químico Enlace iónico Enlace covalente Enlaces intermoleculares Enlace metálico
 Naturaleza del enlace químico Enlace iónico Enlace covalente Enlaces intermoleculares Enlace metálico Naturaleza del enlace químico Los átomos tienden a adquirir la máxima estabilidad y esto se consigue
Naturaleza del enlace químico Enlace iónico Enlace covalente Enlaces intermoleculares Enlace metálico Naturaleza del enlace químico Los átomos tienden a adquirir la máxima estabilidad y esto se consigue
MATERIALES CERÁMICOS
 MATERIALES CERÁMICOS Son materiales inorgánicos no metálicos, constituidos por elementos metálicos y no metálicos enlazados principalmente mediante enlaces iónicos y/o covalentes. PROPIEDADES 1.En general,
MATERIALES CERÁMICOS Son materiales inorgánicos no metálicos, constituidos por elementos metálicos y no metálicos enlazados principalmente mediante enlaces iónicos y/o covalentes. PROPIEDADES 1.En general,
Materiales-G704/G742. Jesús Setién Marquínez Jose Antonio Casado del Prado Soraya Diego Cavia Carlos Thomas García
 Materiales-G704/G742 Lección 3. Estructura cristalina y amorfa Jesús Setién Marquínez Jose Antonio Casado del Prado Soraya Diego Cavia Carlos Thomas García Departamento de Ciencia e Ingeniería del Terreno
Materiales-G704/G742 Lección 3. Estructura cristalina y amorfa Jesús Setién Marquínez Jose Antonio Casado del Prado Soraya Diego Cavia Carlos Thomas García Departamento de Ciencia e Ingeniería del Terreno
TEMA 8 ESTRUCTURA CRISTALINA
 Tema 8. Estructura cristalina 1 TEMA 8 ESTRUCTURA CRISTALINA Los sólidos pueden clasificarse: 1.- Por su ordenación: 1a. Sólidos amorfos: tienen una estructura desordenada. Sus átomos o moléculas se colocan
Tema 8. Estructura cristalina 1 TEMA 8 ESTRUCTURA CRISTALINA Los sólidos pueden clasificarse: 1.- Por su ordenación: 1a. Sólidos amorfos: tienen una estructura desordenada. Sus átomos o moléculas se colocan
ESTRUCTURA DE SÓLIDOS
 Estructura de sólidos 1 ESTRUCTURA DE SÓLIDOS La mayoría de los compuestos inorgánicos se presentan como sólidos en un arreglo ordenado de átomos, iones o moléculas. Los sólidos pueden ser: cristalinos:
Estructura de sólidos 1 ESTRUCTURA DE SÓLIDOS La mayoría de los compuestos inorgánicos se presentan como sólidos en un arreglo ordenado de átomos, iones o moléculas. Los sólidos pueden ser: cristalinos:
01 Minerales y estructuras
 01 Minerales y estructuras Año 2017 15/08/2017 1 Contenido Minerales metales Mena, ganga, ley mineral Tipo de minerales Estructura de los materiales Tipo de enlaces: iónico, covalente, metálico, van der
01 Minerales y estructuras Año 2017 15/08/2017 1 Contenido Minerales metales Mena, ganga, ley mineral Tipo de minerales Estructura de los materiales Tipo de enlaces: iónico, covalente, metálico, van der
Tema 3. DEFECTOS EN LA ESTRUCTURA CRISTALINA. SOLIDIFICACIÓN DE ME-
 ÍNDICE Prólogo... 15 Tema 1. INTRODUCCIÓN A LA CIENCIA E INGENIERÍA DE MATERIALES... 17 1.1. Introducción... 19 1.2. Los materiales en la sociedad actual... 19 1.3. Propiedades de los materiales... 23
ÍNDICE Prólogo... 15 Tema 1. INTRODUCCIÓN A LA CIENCIA E INGENIERÍA DE MATERIALES... 17 1.1. Introducción... 19 1.2. Los materiales en la sociedad actual... 19 1.3. Propiedades de los materiales... 23
Esquema del tema. Tema 4: Enlace iónico. Un poco de empirismo
 Esquema del tema Modelo iónico Características de los compuestos iónicos Corrigiendo el modelo iónico: Polarización y Módulo 12555- Química Inorgánica Título: Ingeniería Química Responsable: Juan José
Esquema del tema Modelo iónico Características de los compuestos iónicos Corrigiendo el modelo iónico: Polarización y Módulo 12555- Química Inorgánica Título: Ingeniería Química Responsable: Juan José
Estructura Interna de los Materiales
 TEMA III Estructura Interna de los Materiales LECCIÓN 3 Estructura Cristalina y Amorfa 1 3.1 ESTADOS DE LA MATERIA Ciencia y Tecnología de los Materiales La materia puede presentarse en tres estados: gaseoso,
TEMA III Estructura Interna de los Materiales LECCIÓN 3 Estructura Cristalina y Amorfa 1 3.1 ESTADOS DE LA MATERIA Ciencia y Tecnología de los Materiales La materia puede presentarse en tres estados: gaseoso,
TEMA 1: ESTRUCTURA INTERNA DE LOS MATERIALES
 PERIODO Departamento de Tecnología. IES Nuestra Señora de la Almudena Mª Jesús Saiz TEMA 1: ESTRUCTURA INTERNA DE LOS MATERIALES El átomo: Toda la materia está compuesta por átomos y éstos por partículas
PERIODO Departamento de Tecnología. IES Nuestra Señora de la Almudena Mª Jesús Saiz TEMA 1: ESTRUCTURA INTERNA DE LOS MATERIALES El átomo: Toda la materia está compuesta por átomos y éstos por partículas
SÓLIDOS I. Tipos de sólidos. Sólidos cristalinos: los átomos, iones o moléculas se empaquetan en forma ordenada.
 SÓLIDOS I Tipos de sólidos Sólidos cristalinos: los átomos, iones o moléculas se empaquetan en forma ordenada. Sólidos amorfos: no presentan estructuras ordenadas. 1 Sólidos cristalinos Hay posiciones
SÓLIDOS I Tipos de sólidos Sólidos cristalinos: los átomos, iones o moléculas se empaquetan en forma ordenada. Sólidos amorfos: no presentan estructuras ordenadas. 1 Sólidos cristalinos Hay posiciones
Química Inorgánica-63.13- Dra.Silvia E. Jacobo. Sólidos. Estructuras Cristalinas
 Sólidos Estructuras Cristalinas Ordenamientos atómicos En gases no hay orden En líquidos hay orden de corto alcance En sólidos hay orden de largo alcance El ordenamiento está determinado por el tipo de
Sólidos Estructuras Cristalinas Ordenamientos atómicos En gases no hay orden En líquidos hay orden de corto alcance En sólidos hay orden de largo alcance El ordenamiento está determinado por el tipo de
Enlace iónico. elemento poco. elemento muy + electronegativo. compuesto iónico (sal) electronegativo
 Enlace iónico Enlace iónico Necesitamos un nuevo modelo para explicar ciertas peculiaridades (Li2O). Este nuevo modelo es el enlace iónico Se forma por transferencia de electrones (no hay reparto equitativo,
Enlace iónico Enlace iónico Necesitamos un nuevo modelo para explicar ciertas peculiaridades (Li2O). Este nuevo modelo es el enlace iónico Se forma por transferencia de electrones (no hay reparto equitativo,
Enlaces y Propiedades de Sólidos con esos Enlaces
 Enlaces y Propiedades de Sólidos con esos Enlaces PROPIEDADES DE CRISTALES METÁLICOS En estos cristales el enlace predominante es el metálico. 1 Conductividad eléctrica y térmica en materiales metálicos
Enlaces y Propiedades de Sólidos con esos Enlaces PROPIEDADES DE CRISTALES METÁLICOS En estos cristales el enlace predominante es el metálico. 1 Conductividad eléctrica y térmica en materiales metálicos
ENLACE IÓNICO. Dra. Silvia Elena Castillo Blum
 ENLACE IÓNICO Dra. Silvia Elena Castillo Blum Enlace Químico ENLACE IÓNICO ENLACE COVALENTE ENLACE METÁLICO 2 Definición IUPAC Hay un enlace químico entre dos átomos o grupos de átomos cuando las fuerzas
ENLACE IÓNICO Dra. Silvia Elena Castillo Blum Enlace Químico ENLACE IÓNICO ENLACE COVALENTE ENLACE METÁLICO 2 Definición IUPAC Hay un enlace químico entre dos átomos o grupos de átomos cuando las fuerzas
Tema 9. SOLIDOS COVALENTES
 Tema 9. SOLIDOS COVALENTES Introducción Estructuras de no-metales Boro Carbono Fósforo Arsénico, Antimonio y Bismuto Selenio y Telurio Estructuras de óxidos Estructuras basadas en tetraedros Estructuras
Tema 9. SOLIDOS COVALENTES Introducción Estructuras de no-metales Boro Carbono Fósforo Arsénico, Antimonio y Bismuto Selenio y Telurio Estructuras de óxidos Estructuras basadas en tetraedros Estructuras
QUIMICA DE MATERIALES 1.2. NATURALEZA DE LA UNION QUIMICA
 QUIMICA DE MATERIALES 1.2. NATURALEZA DE LA UNION QUIMICA ENLACE COVALENTE Los electrones están compartidos por los átomos IONICO Uno o más electrones son transferidos entre los átomos, formando iones
QUIMICA DE MATERIALES 1.2. NATURALEZA DE LA UNION QUIMICA ENLACE COVALENTE Los electrones están compartidos por los átomos IONICO Uno o más electrones son transferidos entre los átomos, formando iones
M A T E R I A L E S ENLACES QUIMICOS
 M A T E R I A L E S ENLACES QUIMICOS I FUERZAS DE ATRACCIÓN Intramoleculares: entre átomos de una molécula Determinan tipo de sustancia y propiedades químicas. Intermoleculares: entre moléculas Determinan
M A T E R I A L E S ENLACES QUIMICOS I FUERZAS DE ATRACCIÓN Intramoleculares: entre átomos de una molécula Determinan tipo de sustancia y propiedades químicas. Intermoleculares: entre moléculas Determinan
Tema 3.- Defectos-Imperfecciones
 BLOQUE II.- ESTRUCTURA Tema 3.- Defectos-Imperfecciones * James F. Shackerlford Introducción a la Ciencia de Materiales para Ingenieros. Cuarta edición. Ed. Prentice Hall (1998) 1 Objetivos Comprender
BLOQUE II.- ESTRUCTURA Tema 3.- Defectos-Imperfecciones * James F. Shackerlford Introducción a la Ciencia de Materiales para Ingenieros. Cuarta edición. Ed. Prentice Hall (1998) 1 Objetivos Comprender
Tema 8. Sólidos iónicos
 Tema 8. Sólidos iónicos Definiciones Estructuras iónicas Derivadas de CCP Derivadas de HCP Derivadas de empaquetamientos no compactos Racionalización de las estructuras iónicas Principios de Laves Reglas
Tema 8. Sólidos iónicos Definiciones Estructuras iónicas Derivadas de CCP Derivadas de HCP Derivadas de empaquetamientos no compactos Racionalización de las estructuras iónicas Principios de Laves Reglas
CONDICIONES DE VITRIFICACION
 CONDICIONES DE VITRIFICACION No todos les materiales presentan estructura vítrea y el efecto de transición vítrea! Aun enfriando rapidamente! - un vidrio requiere de una cantidad razonable de SiO2 y/o
CONDICIONES DE VITRIFICACION No todos les materiales presentan estructura vítrea y el efecto de transición vítrea! Aun enfriando rapidamente! - un vidrio requiere de una cantidad razonable de SiO2 y/o
CAP. 1:ESTRUCTURAS CRISTALINAS
 CAP. 1:ESTRUCTURAS CRISTALINAS Sólidos cristalinos: amorfos: Disposiciones periódicas en el espacio Disposición al azar Situaciones intermedias: (no periódicas pero ordenadas) Estructuras moduladas Casicristales
CAP. 1:ESTRUCTURAS CRISTALINAS Sólidos cristalinos: amorfos: Disposiciones periódicas en el espacio Disposición al azar Situaciones intermedias: (no periódicas pero ordenadas) Estructuras moduladas Casicristales
4. Estructura atómica, enlaces y Ordenamiento atómico de los metales
 4. Estructura atómica, enlaces y Ordenamiento atómico de los metales Atomo Unidad estructural básica de todos los materiales. En nuestro modelo, los átomos están constituidos por tres partículas subatómicas
4. Estructura atómica, enlaces y Ordenamiento atómico de los metales Atomo Unidad estructural básica de todos los materiales. En nuestro modelo, los átomos están constituidos por tres partículas subatómicas
Tema 2: Fuerzas intermoleculares
 Tema 2: Fuerzas intermoleculares Fuerzas intermoleculares: ion dipolo, dipolo dipolo, dispersión de London y puentes de hidrógeno. Gases ideales y reales. Propiedades de los ĺıquidos. Presión de vapor.
Tema 2: Fuerzas intermoleculares Fuerzas intermoleculares: ion dipolo, dipolo dipolo, dispersión de London y puentes de hidrógeno. Gases ideales y reales. Propiedades de los ĺıquidos. Presión de vapor.
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2010 QUÍMICA TEMA 3: ENLACES QUÍMICOS
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 010 QUÍMICA TEMA : ENLACES QUÍMICOS Junio, Ejercicio, Opción A Reserva 1, Ejercicio, Opción A Reserva, Ejercicio, Opción B Reserva, Ejercicio, Opción B Septiembre,
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 010 QUÍMICA TEMA : ENLACES QUÍMICOS Junio, Ejercicio, Opción A Reserva 1, Ejercicio, Opción A Reserva, Ejercicio, Opción B Reserva, Ejercicio, Opción B Septiembre,
Para qué se unen los átomos? Es la fuerza que mantiene unidos dos átomos cualesquiera.
 Es la fuerza que mantiene unidos dos átomos cualesquiera. Enlace iónico : Es la fuerza que mantiene unidos átomos de electronegatividades muy diferentes. Enlace cova1ente: Es la fuerza que mantiene unidos
Es la fuerza que mantiene unidos dos átomos cualesquiera. Enlace iónico : Es la fuerza que mantiene unidos átomos de electronegatividades muy diferentes. Enlace cova1ente: Es la fuerza que mantiene unidos
ENLACE QUÍMICO. NaCl. Grafito: láminas de átomos de carbono
 NaCl Grafito: láminas de átomos de carbono Se denomina enlace químico al conjunto de fuerzas que mantienen unidos los átomos cuando forman moléculas o cristales, así como las fuerzas que mantienen unidas
NaCl Grafito: láminas de átomos de carbono Se denomina enlace químico al conjunto de fuerzas que mantienen unidos los átomos cuando forman moléculas o cristales, así como las fuerzas que mantienen unidas
Enlaces y Propiedades de Cristales con esos Enlaces
 Enlaces y Propiedades de Cristales con esos Enlaces Enlaces Enlaces Primarios, participan directamente los electrones de valencia. El rol de estos electrones (ser cedidos, compartidos o captados) depende
Enlaces y Propiedades de Cristales con esos Enlaces Enlaces Enlaces Primarios, participan directamente los electrones de valencia. El rol de estos electrones (ser cedidos, compartidos o captados) depende
Tipos de Enlaces Atómicos y Moleculares
 Tipos de Enlaces Atómicos y Moleculares Enlaces atómicos primarios Iónicos Covalentes Metálicos Enlaces atómicos secundarios y moleculares Dipolos permanentes Dipolos fluctuantes Enlaces Iónicos Grandes
Tipos de Enlaces Atómicos y Moleculares Enlaces atómicos primarios Iónicos Covalentes Metálicos Enlaces atómicos secundarios y moleculares Dipolos permanentes Dipolos fluctuantes Enlaces Iónicos Grandes
Ejercicios tabla periódica. Enlace 4º ESO
 1. a) Indica la configuración electrónica de los átomos de los elementos A, B y C cuyos números atómicos son respectivamente: 12, 17 y 19. b) Escribe la configuración electrónica del ion más estable de
1. a) Indica la configuración electrónica de los átomos de los elementos A, B y C cuyos números atómicos son respectivamente: 12, 17 y 19. b) Escribe la configuración electrónica del ion más estable de
UNIVERSIDAD AUTÓNOMA DE SAN LUIS POTOSÍ FACULTAD DE CIENCIAS
 UNIVERSIDAD AUTÓNOMA DE SAN LUIS POTOSÍ FACULTAD DE CIENCIAS Av. Dr. Salvador Nava Mtz. S/N Zona Universitaria Teléfono 8-26-23-17, Fax 8-26-23-21 web www.fciencias.uaslp.mx, email escolar@fc.uaslp.mx
UNIVERSIDAD AUTÓNOMA DE SAN LUIS POTOSÍ FACULTAD DE CIENCIAS Av. Dr. Salvador Nava Mtz. S/N Zona Universitaria Teléfono 8-26-23-17, Fax 8-26-23-21 web www.fciencias.uaslp.mx, email escolar@fc.uaslp.mx
1- Enlaces entre átomos Por qué se unen los átomos? 2- Distintos tipos de enlaces 2.1- Enlace iónico Compuestos iónicos y sus propiedades 2.
 1- Enlaces entre átomos Por qué se unen los átomos? 2- Distintos tipos de enlaces 2.1- Enlace iónico 2.1.1- Compuestos iónicos y sus propiedades 2.2- Enlace covalente 2.2.1-Estructura de Lewis 2.2.2- Compuestos
1- Enlaces entre átomos Por qué se unen los átomos? 2- Distintos tipos de enlaces 2.1- Enlace iónico 2.1.1- Compuestos iónicos y sus propiedades 2.2- Enlace covalente 2.2.1-Estructura de Lewis 2.2.2- Compuestos
MATERIALES METÁLICOS GRUPO 2: Mª Carmen Marco Esteban Soledad Morán Morán Elena Moreno Atahonero
 MATERIALES METÁLICOS GRUPO 2: Mª Carmen Marco Esteban Soledad Morán Morán Elena Moreno Atahonero ÍNDICE 1.TIPO DE SUSTANCIA 7.APLICACIONES 2.CLASIFICACIÓN 6.PROPIEDADES FÍSICAS 3.ESTRUCTURAS CRISTALINAS
MATERIALES METÁLICOS GRUPO 2: Mª Carmen Marco Esteban Soledad Morán Morán Elena Moreno Atahonero ÍNDICE 1.TIPO DE SUSTANCIA 7.APLICACIONES 2.CLASIFICACIÓN 6.PROPIEDADES FÍSICAS 3.ESTRUCTURAS CRISTALINAS
El enlace químico 3 ESO SEK-CATALUNYA
 El enlace químico 3 ESO SEK-CATALUNYA Contenidos Enlace químico Enlace metálico Propiedades de los metales Enlace iónico Propiedades de los compuestos iónicos Enlace covalente Propiedades de los compuestos
El enlace químico 3 ESO SEK-CATALUNYA Contenidos Enlace químico Enlace metálico Propiedades de los metales Enlace iónico Propiedades de los compuestos iónicos Enlace covalente Propiedades de los compuestos
TEMA 4 (Parte I) EL ENLACE QUÍMICO. IÓNICO
 TEMA 4 (Parte I) EL ENLACE QUÍMICO. IÓNICO Mª PILAR RUIZ OJEDA BORJA MUÑOZ LEOZ Contenidos: 1. Introducción 2. Representaciones de Lewis. Regla del Octeto 3. El enlace Iónico 3.1. Redes iónicas 3.2. Energía
TEMA 4 (Parte I) EL ENLACE QUÍMICO. IÓNICO Mª PILAR RUIZ OJEDA BORJA MUÑOZ LEOZ Contenidos: 1. Introducción 2. Representaciones de Lewis. Regla del Octeto 3. El enlace Iónico 3.1. Redes iónicas 3.2. Energía
Objetivo. Introducción. Palabras clave. Desarrollo. Química Unidad 8 Enlace químico. 1. Interacciones entre átomos
 Química Unidad 8 Enlace químico Objetivo Comprender los conceptos básicos de los modelos de enlace iónico, covalente y metálico. Introducción Los electrones cumplen un papel fundamental en la formación
Química Unidad 8 Enlace químico Objetivo Comprender los conceptos básicos de los modelos de enlace iónico, covalente y metálico. Introducción Los electrones cumplen un papel fundamental en la formación
Introducción a los elementos metálicos y metalurgía
 Tema 7. Introducción a los elementos metálicos y Metalurgia. El enlace en los metales. Conductores y semiconductores. Los metales en la naturaleza. Preparación de la mena. Producción de los metales. La
Tema 7. Introducción a los elementos metálicos y Metalurgia. El enlace en los metales. Conductores y semiconductores. Los metales en la naturaleza. Preparación de la mena. Producción de los metales. La
Tema 2: Fuerzas intermoleculares
 Tema 2: Fuerzas intermoleculares Fuerzas intermoleculares: definición y tratamiento general. Interacciones iónicas. Energía reticular. Moléculas polares. Puentes de Hidrógeno. Moléculas apolares. Gases
Tema 2: Fuerzas intermoleculares Fuerzas intermoleculares: definición y tratamiento general. Interacciones iónicas. Energía reticular. Moléculas polares. Puentes de Hidrógeno. Moléculas apolares. Gases
INO-1 PX Magdalena Rodas INOSILICATOS
 INO-1 PX Magdalena Rodas INOSILICATOS INOSILICATOS -Introducción: Rasgos estructurales básicos * Cadenas secillas: Piroxenos y piroxenoides. * Cadenas dobles: Anfíboles Silicatos con estructuras en cadenas
INO-1 PX Magdalena Rodas INOSILICATOS INOSILICATOS -Introducción: Rasgos estructurales básicos * Cadenas secillas: Piroxenos y piroxenoides. * Cadenas dobles: Anfíboles Silicatos con estructuras en cadenas
Enlace químico. José Mariano Lucena Cruz 19 de mayo de 2010
 José Mariano Lucena Cruz chenalc@gmail.com 19 de mayo de 2010 El enlace químico La unión entre átomos, moléculas o iones constituye el llamado enlace químico. Su fundamento siempre es de tipo eléctrico.
José Mariano Lucena Cruz chenalc@gmail.com 19 de mayo de 2010 El enlace químico La unión entre átomos, moléculas o iones constituye el llamado enlace químico. Su fundamento siempre es de tipo eléctrico.
1.2. Celdas Unitarias Parámetros Reticulares
 Capítulo 2 Organización Atómica 1.2. Celdas Unitarias Parámetros Reticulares 1.2.1. Celdas Unitarias La estructura atómica influye en la forma en que los átomos se unen entre sí; esto además nos ayuda
Capítulo 2 Organización Atómica 1.2. Celdas Unitarias Parámetros Reticulares 1.2.1. Celdas Unitarias La estructura atómica influye en la forma en que los átomos se unen entre sí; esto además nos ayuda
NESOSILICATOS-1 OLIVINO
 NESOSILICATOS-1 OLIVINO M. Rodas Tomado de :www/usuarios.lycos.es GRUPO DEL OLIVINO NESOSILICATOS GRUPO DE LOS GRANATES GRUPO DE LOS NESOSILICATOS ALUMINICOS: Andalucita, Sillimanita, Distena o cianita
NESOSILICATOS-1 OLIVINO M. Rodas Tomado de :www/usuarios.lycos.es GRUPO DEL OLIVINO NESOSILICATOS GRUPO DE LOS GRANATES GRUPO DE LOS NESOSILICATOS ALUMINICOS: Andalucita, Sillimanita, Distena o cianita
UNIDAD 3: EL ENLACE QUÍMICO
 UNIDAD 3: EL ENLACE QUÍMICO 1.- REGLA DEL OCTETO Casi todas las sustancias que encontramos en la naturaleza están formadas por átomos unidos. Las fuerzas que mantienen unidos los átomos en las distintas
UNIDAD 3: EL ENLACE QUÍMICO 1.- REGLA DEL OCTETO Casi todas las sustancias que encontramos en la naturaleza están formadas por átomos unidos. Las fuerzas que mantienen unidos los átomos en las distintas
QUÍMICA - 2º BACHILLERATO ENLACE QUÍMICO RESUMEN CONCEPTO DE ENLACE QUÍMICO
 Javier Robledano Arillo Química 2º Bachillerato Enlace Químico - 1 QUÍMICA - 2º BACHILLERATO ENLACE QUÍMICO RESUMEN CONCEPTO DE ENLACE QUÍMICO 1. Enlace químico: conjunto de fuerzas que mantienen unidos
Javier Robledano Arillo Química 2º Bachillerato Enlace Químico - 1 QUÍMICA - 2º BACHILLERATO ENLACE QUÍMICO RESUMEN CONCEPTO DE ENLACE QUÍMICO 1. Enlace químico: conjunto de fuerzas que mantienen unidos
CÚBICA SIMPLE HEXAGONAL ROMBOÉDRICA
 Formas de las celdas CÚBICA SIMPLE HEXAGONAL ROMBOÉDRICA TRICLÍNICA 1 1 2 3 4 C 2 3 4 5 6 5 6 7 B 8 3 1 5 2 8 A 8 6 4 Capa a Capa b Capa a Los cationes (más pequeños) ocupan los huecos formados por el
Formas de las celdas CÚBICA SIMPLE HEXAGONAL ROMBOÉDRICA TRICLÍNICA 1 1 2 3 4 C 2 3 4 5 6 5 6 7 B 8 3 1 5 2 8 A 8 6 4 Capa a Capa b Capa a Los cationes (más pequeños) ocupan los huecos formados por el
Sistemática de minerales. 2. Silicatos
 Sistemática de minerales 2. Silicatos Silicatos Enlace Si-O Geometría: tetraedros Estabilidad máxima Posibilidad polimerización Grupos de Silicatos Nesosilicatos [SiO4] -4 Grupos de Silicatos Sorosilicatos
Sistemática de minerales 2. Silicatos Silicatos Enlace Si-O Geometría: tetraedros Estabilidad máxima Posibilidad polimerización Grupos de Silicatos Nesosilicatos [SiO4] -4 Grupos de Silicatos Sorosilicatos
Tema 3. (Parte 1) Enlace químico y propiedades de las sustancias
 Tema 3. (Parte 1) Enlace químico y propiedades de las sustancias ÍNDICE 3.1. Enlace y estabilidad energética 3.2. Enlace iónico Energía de red Ciclo de Born-Haber Propiedades de las sustancias iónicas
Tema 3. (Parte 1) Enlace químico y propiedades de las sustancias ÍNDICE 3.1. Enlace y estabilidad energética 3.2. Enlace iónico Energía de red Ciclo de Born-Haber Propiedades de las sustancias iónicas
20.-/ a) Cu: Metálico ; BCl 3 : Covalente ; H 2 O: Covalente ; CsF: Iónico b) BCl 3 : Triangular plana y APOLAR ; H 2 O: Angular y POLAR.
 SOLUCIONES EL Y PROPIEDADES HOJA Nº 7 1.-/ a) Lineal b) Tetraédrica c) Angular d) Angular e) Piramidal trigonal 2.-/ a) Tetraédrica b) Tetraédrica c) Lineal d) Triangular e) Tetraédrica 3.-/ a) 769,2 kj/mol
SOLUCIONES EL Y PROPIEDADES HOJA Nº 7 1.-/ a) Lineal b) Tetraédrica c) Angular d) Angular e) Piramidal trigonal 2.-/ a) Tetraédrica b) Tetraédrica c) Lineal d) Triangular e) Tetraédrica 3.-/ a) 769,2 kj/mol
UNIDAD 3. MODIFICACIÓN DE LAS PROPIEDADES DE LOS METALES
 UNIDAD 3. MODIFICACIÓN DE LAS PROPIEDADES DE LOS METALES 1. GENERALIDADES... Pág. 49 2. ESTRUCTURA INTERNA DE LOS METALES... Pág. 49 2.1. Estructuras cristalinas... Pág. 49 2.2. Estructura cristalina cúbica
UNIDAD 3. MODIFICACIÓN DE LAS PROPIEDADES DE LOS METALES 1. GENERALIDADES... Pág. 49 2. ESTRUCTURA INTERNA DE LOS METALES... Pág. 49 2.1. Estructuras cristalinas... Pág. 49 2.2. Estructura cristalina cúbica
PROPIEDADES QUÍMICAS DEL SUELO
 PROPIEDADES QUÍMICAS DEL SUELO DEFINICIONES Ión: Átomos o moléculas que pierden o ganan electrones por lo cual adquieren una determinada carga; si ganan adquieren carga negativa: aniones (Cl -, NO 3- );
PROPIEDADES QUÍMICAS DEL SUELO DEFINICIONES Ión: Átomos o moléculas que pierden o ganan electrones por lo cual adquieren una determinada carga; si ganan adquieren carga negativa: aniones (Cl -, NO 3- );
Enlaces y Propiedades de Compuestos con esos Enlaces
 Enlaces y Propiedades de Compuestos con esos Enlaces Parte 1. Enlaces Primarios Parte 2. Secundarios Parte 3 Propiedades de Cristales Parte 1. Electronegatividad y Enlaces Primarios 1 Compuestos de algunos
Enlaces y Propiedades de Compuestos con esos Enlaces Parte 1. Enlaces Primarios Parte 2. Secundarios Parte 3 Propiedades de Cristales Parte 1. Electronegatividad y Enlaces Primarios 1 Compuestos de algunos
ENLACE QUÍMICO UNIDADES ESTRUCTURALES DE LAS SUSTANCIAS IONES ÁTOMOS MOLÉCULAS ENLACE IÓNICO ENLACE METÁLICO ENLACE COVALENTE ENLACE COVALENTE
 ENLACE QUÍMICO Y TIPOS ENLACE QUÍMICO Enlace químico es la fuerza responsable de la unión entre las unidades estructurales ( iones, átomos o moléculas) que forman la materia. UNIDADES ESTRUCTURALES DE
ENLACE QUÍMICO Y TIPOS ENLACE QUÍMICO Enlace químico es la fuerza responsable de la unión entre las unidades estructurales ( iones, átomos o moléculas) que forman la materia. UNIDADES ESTRUCTURALES DE
Estructura general de los silicatos
 Estructura general de los silicatos Apellidos, nombre Departamento Centro Ibáñez Asensio, Sara (sibanez@prv.upv.es) Moreno Ramón, Héctor (hecmora@prv.upv.es) Gisbert Blanquer, Juan Manuel (jgisbert@prv.upv.es)
Estructura general de los silicatos Apellidos, nombre Departamento Centro Ibáñez Asensio, Sara (sibanez@prv.upv.es) Moreno Ramón, Héctor (hecmora@prv.upv.es) Gisbert Blanquer, Juan Manuel (jgisbert@prv.upv.es)
3. La estructura de sólidos cristalinos 3.1 Conceptos fundamentales 3.2 Celda unitaria 3.3 Redes de Bravias 3.4 Estructuras cristalinas 3.
 Contenido 3. La estructura de sólidos cristalinos 3.1 Conceptos fundamentales 3.2 Celda unitaria 3.3 Redes de Bravias 3.4 Estructuras cristalinas 3.5 Volumen y densidad 3.6 Direcciones y planos cristalográficos
Contenido 3. La estructura de sólidos cristalinos 3.1 Conceptos fundamentales 3.2 Celda unitaria 3.3 Redes de Bravias 3.4 Estructuras cristalinas 3.5 Volumen y densidad 3.6 Direcciones y planos cristalográficos
Física del Estado Sólido REDES CRISTALINAS. Dr. Andrés Ozols. Facultad de Ingeniería Universidad de Buenos Aires. Dr. A. Ozols 1
 Física del Estado Sólido REDES CRISTALINAS Dr. Andrés Ozols Facultad de Ingeniería Universidad de Buenos Aires 2009 Dr. A. Ozols 1 ÁTOMOS EN SÓLIDOS Dr. A. Ozols 2 ORDEN CRISTALINO y FORMA René Just Hauy
Física del Estado Sólido REDES CRISTALINAS Dr. Andrés Ozols Facultad de Ingeniería Universidad de Buenos Aires 2009 Dr. A. Ozols 1 ÁTOMOS EN SÓLIDOS Dr. A. Ozols 2 ORDEN CRISTALINO y FORMA René Just Hauy
Diagrama de correlación de enlaces moleculares Antienlace : rojo 1s similar a 2s
 Redes Cristalinas Ciencia de Materiales Ing. en Mecatrónica Otoño 2009 Lilia Meza Montes-IFUAP Diagrama de correlación de enlaces moleculares Antienlace : rojo 1s similar a 2s Sólidos cristalinos y amorfos
Redes Cristalinas Ciencia de Materiales Ing. en Mecatrónica Otoño 2009 Lilia Meza Montes-IFUAP Diagrama de correlación de enlaces moleculares Antienlace : rojo 1s similar a 2s Sólidos cristalinos y amorfos
ENLACE IÓNICO O ELECTROVALENTE
 ENLACE IÓNICO O ELECTROVALENTE Servicios Educativos Integrales Caracterizado por: o Cesión de electrones por parte de un metal a un no metal o Formación de iones de carga contraria, metal (+) y no metal
ENLACE IÓNICO O ELECTROVALENTE Servicios Educativos Integrales Caracterizado por: o Cesión de electrones por parte de un metal a un no metal o Formación de iones de carga contraria, metal (+) y no metal
Materiales cerámicos. Introducción a la Ciencia de Materiales. M. Bizarro
 Materiales cerámicos Introducción a la Ciencia de Materiales M. Bizarro Materiales cerámicos Son compuestos inorgánicos formados por elementos metálicos y no metálicos cuyos enlaces interatómicos pueden
Materiales cerámicos Introducción a la Ciencia de Materiales M. Bizarro Materiales cerámicos Son compuestos inorgánicos formados por elementos metálicos y no metálicos cuyos enlaces interatómicos pueden
4º E.S.O. FÍSICA Y QUÍMICA 3. ENLACE QUÍMICO. Dpto. de Física y Química. R. Artacho
 4º E.S.O. FÍSICA Y QUÍMICA 3. ENLACE QUÍMICO R. Artacho Dpto. de Física y Química Índice CONTENIDOS 1. Enlace químico en las sustancias 2. Tipos de enlace entre átomos 3. Enlace iónico 4. Enlace covalente
4º E.S.O. FÍSICA Y QUÍMICA 3. ENLACE QUÍMICO R. Artacho Dpto. de Física y Química Índice CONTENIDOS 1. Enlace químico en las sustancias 2. Tipos de enlace entre átomos 3. Enlace iónico 4. Enlace covalente
Enlace químico Educación Secundaria Obligatoria Física y Química
 EL ENLACE QUÍMICO Hay tres maneras en que se unen los átomos: enlace iónico, enlace covalente y enlace metálico. Los enlaces entre átomos se producen porque éstos quieren cumplir la regla del octeto. La
EL ENLACE QUÍMICO Hay tres maneras en que se unen los átomos: enlace iónico, enlace covalente y enlace metálico. Los enlaces entre átomos se producen porque éstos quieren cumplir la regla del octeto. La
Tema 10. FUERZAS INTERMOLECULARES
 Tema 10. FUERZAS INTERMOLECULARES Introducción Polaridad de las moléculas Interacciones de dipolos Interacciones de dipolos inducidos Enlace de hidrógeno Efectos de las fuerzas químicas Tipos de estructuras
Tema 10. FUERZAS INTERMOLECULARES Introducción Polaridad de las moléculas Interacciones de dipolos Interacciones de dipolos inducidos Enlace de hidrógeno Efectos de las fuerzas químicas Tipos de estructuras
! Introducción a los sólidos iónicos! Qué elementos los forman?! Qué tipos de fuerzas mantienen la cohesión del cristal?
 Tema 8. Sólidos iónicos Estructura del NaCl Contenidos! Introducción a los sólidos iónicos! Qué elementos los forman?! Qué tipos de fuerzas mantienen la cohesión del cristal?! Propiedades de los sólidos
Tema 8. Sólidos iónicos Estructura del NaCl Contenidos! Introducción a los sólidos iónicos! Qué elementos los forman?! Qué tipos de fuerzas mantienen la cohesión del cristal?! Propiedades de los sólidos
ENLACE QUÍMICO. Elemento F O Cl N C S H Electronegatividad 4,0 3,5 3,0 3,0 2,5 2,5 2,1
 ENLACE QUÍMICO 1 - a) Diseñe un ciclo de Born-Haber para el MgCl 2. b) Defina el menos cuatro de los siguientes conceptos: - Energía de ionización. - Energía de disociación. - Afinidad electrónica. - Energía
ENLACE QUÍMICO 1 - a) Diseñe un ciclo de Born-Haber para el MgCl 2. b) Defina el menos cuatro de los siguientes conceptos: - Energía de ionización. - Energía de disociación. - Afinidad electrónica. - Energía
SOLUCIONARIO Guía Técnico Profesional
 SOLUCIONARIO Guía Técnico Profesional El enlace químico SGUICTC004TC33-A16V1 Ítem Alternativa Habilidad 1 B Comprensión 2 E Comprensión 3 A Comprensión 4 A Comprensión 5 C Comprensión 6 D Aplicación 7
SOLUCIONARIO Guía Técnico Profesional El enlace químico SGUICTC004TC33-A16V1 Ítem Alternativa Habilidad 1 B Comprensión 2 E Comprensión 3 A Comprensión 4 A Comprensión 5 C Comprensión 6 D Aplicación 7
Son las fuerzas que mantienen unidos a los átomos entre sí para formar moléculas o cristales que son más estables que los átomos por separados..
 ENLACE QUÍMICO Son las fuerzas que mantienen unidos a los átomos entre sí para formar moléculas o cristales que son más estables que los átomos por separados.. Son de tipo eléctrico. Al formarse un enlace
ENLACE QUÍMICO Son las fuerzas que mantienen unidos a los átomos entre sí para formar moléculas o cristales que son más estables que los átomos por separados.. Son de tipo eléctrico. Al formarse un enlace
Tema 17.- Cerámicas Funcionales
 BLOQUE V.- MATERIALES CERÁMICOS Bibliografía: Solid State Chemistry and its applications: Anthony R. West (ed Wiley, (1990) Solid State Chemistry: An introduction, L. Smart and E. Moore. 1992 (Cap. 8)
BLOQUE V.- MATERIALES CERÁMICOS Bibliografía: Solid State Chemistry and its applications: Anthony R. West (ed Wiley, (1990) Solid State Chemistry: An introduction, L. Smart and E. Moore. 1992 (Cap. 8)
TEMA 2. ENLACES QUIMICOS
 TEMA 2. ENLACES QUIMICOS En la naturaleza los átomos que constituyen la materia se encuentran unidos formando moléculas o agrupaciones más complejas. A pesar de ello existen una serie de elementos que
TEMA 2. ENLACES QUIMICOS En la naturaleza los átomos que constituyen la materia se encuentran unidos formando moléculas o agrupaciones más complejas. A pesar de ello existen una serie de elementos que
TEMA 5. Elementos y compuestos 1 CLASIFICACIÓN DE LOS ELEMENTOS
 TEMA 5 Elementos y compuestos 1 CLASIFICACIÓN DE LOS ELEMENTOS La primera clasificación de los elementos fue la que distinguió entre metales y no metales y se basaba en el aspecto que presentaban los elementos
TEMA 5 Elementos y compuestos 1 CLASIFICACIÓN DE LOS ELEMENTOS La primera clasificación de los elementos fue la que distinguió entre metales y no metales y se basaba en el aspecto que presentaban los elementos
24/02/2012 Ealboró Eefrén Giraldo 1
 24/02/2012 Ealboró Eefrén Giraldo 1 OBJETIVO Estudiar la relación intima entre la estructura y propiedades de los materiales. 24/02/2012 Ealboró Eefrén Giraldo 2 24/02/2012 Ealboró Eefrén Giraldo 3 ESTRUCTURA.
24/02/2012 Ealboró Eefrén Giraldo 1 OBJETIVO Estudiar la relación intima entre la estructura y propiedades de los materiales. 24/02/2012 Ealboró Eefrén Giraldo 2 24/02/2012 Ealboró Eefrén Giraldo 3 ESTRUCTURA.
EL ENLACE QUÍMICO. Son las fuerzas que mantienen unidos a los átomos entre sí para formar moléculas o iones.
 EL ENLACE QUÍMICO CONTENIDOS. 1.- El enlace químico. 1.1. Enlace iónico. Reacciones de ionización. 1.2. Enlace covalente. Modelo de Lewis. 2.- Justificación de la fórmula de los principales compuestos
EL ENLACE QUÍMICO CONTENIDOS. 1.- El enlace químico. 1.1. Enlace iónico. Reacciones de ionización. 1.2. Enlace covalente. Modelo de Lewis. 2.- Justificación de la fórmula de los principales compuestos
ENLACE ATÓMICO. Física del Estado Sólido. Facultad de Ingeniería Universidad de Buenos Aires Dr. Andrés Ozols. Enlace Atómico. Dr. A.
 Física del Estado Sólido ENLACE ATÓMICO Dr. Andrés Ozols Facultad de Ingeniería Universidad de Buenos Aires 2009 Dr. A. Ozols 1 Dr. A. Ozols 1 ESPECTROS DE HIDROGENO espectros de emisión espectro de absorción
Física del Estado Sólido ENLACE ATÓMICO Dr. Andrés Ozols Facultad de Ingeniería Universidad de Buenos Aires 2009 Dr. A. Ozols 1 Dr. A. Ozols 1 ESPECTROS DE HIDROGENO espectros de emisión espectro de absorción
07/02/2015 EL ENLACE QUÍMICO. Tema 5
 EL ENLACE QUÍMICO Tema 5 Por qué se unen los átomos? Los átomos, moléculas e iones y se unen entre sí porque al hacerlo se llega a una situación de mínima energía, lo que equivale a decir de máxima estabilidad
EL ENLACE QUÍMICO Tema 5 Por qué se unen los átomos? Los átomos, moléculas e iones y se unen entre sí porque al hacerlo se llega a una situación de mínima energía, lo que equivale a decir de máxima estabilidad
Explicación de las propiedades y los estados de agregación en los compuestos químicos en función de los tipos de enlace. vs.
 Explicación de las propiedades y los estados de agregación en los compuestos químicos en función de los tipos de enlace. vs. Usar las propiedades y los estados de agregación en los compuestos químicos
Explicación de las propiedades y los estados de agregación en los compuestos químicos en función de los tipos de enlace. vs. Usar las propiedades y los estados de agregación en los compuestos químicos
EJERCICIO DE EXAMEN DE QUÍMICA INORGÁNICA
 EJERCICIO DE EXAMEN DE QUÍMICA INORGÁNICA Las 6 preguntas siguientes se refieren a la tabla periódica que se presenta. Los símbolos han sido asignados arbitrariamente. D H B A E M G J L R X Y N P Q Z T
EJERCICIO DE EXAMEN DE QUÍMICA INORGÁNICA Las 6 preguntas siguientes se refieren a la tabla periódica que se presenta. Los símbolos han sido asignados arbitrariamente. D H B A E M G J L R X Y N P Q Z T
