Manual Toma de Muestras Exámenes Genéticos por PCR Herpesvirus Bioingentech Ltd. Teléfono (56)-(41)
|
|
|
- Salvador Ortiz Acuña
- hace 6 años
- Vistas:
Transcripción
1 Manual Toma de Muestras Exámenes Genéticos por PCR Herpesvirus Bioingentech Ltd. Teléfono (56)-(41)
2 Muestras Herpesvirus 1. Introducción Los herpesvirus son miembros de la familia Herpesviridae, capaces de causar enfermedades en múltiples animales, incluido el hombre. Se encuentran ampliamente diseminados en el mundo, pudiendo establecer latencia en las células de los individuos infectados. Al estar latentes no se detectan partículas virales, pero su ADN se encuentra en el núcleo celular. La reactivación de los virus latentes se ha relacionado con ciertas patologías. En ciertas condiciones puede reactivarse, replicándose y formando nuevos virus, a menudo con resultado de muerte celular. 2. Herpesvirus humano 1 y herpesvirus humano 2 a) Sangre obtenida a través de punción periférica Realizar lavado de manos quirúrgico. Mantener técnica aséptica durante todo el procedimiento. Utilizar campo estéril para evitar tener contacto con áreas circundantes que ofrezca el riesgo de contaminación. Colocar mascarilla al paciente. Realizar antisepsia de la zona a puncionar; no palpe la vena sin guantes estériles una vez preparada la piel. Utilizar otros guantes estériles para cada punción. POR ÉSTE MÉTODO NO PUEDEN SER PROCESADAS MUESTRAS CON HEPARINA. En pacientes heparinizados, la toma de muestra debe realizarse en el momento más alejado de la administración del medicamento. La toma deberá hacerse en un lugar perfectamente iluminado y con el paciente cómodamente sentado. Localizar una vena adecuada en la cara anterior del codo y colocar el torniquete en la parte media del brazo. Desinfectar el área con un algodón humedecido con alcohol al 70% e introducir la aguja con el bisel hacia arriba. Si la sangre no fluye espontáneamente y se está utilizando una jeringa, jalar el émbolo y aspirar con suavidad; si se está empleando equipo al vacío presionar el tubo de ensaye hacia arriba. Al empezar a fluir la sangre retirar el torniquete. Una vez que se haya obtenido entre 5-8 ml de sangre, retirar la aguja y colocar una tórula con alcohol sobre el sitio de punción ejerciendo presión para detener la hemorragia. 2
3 a) Sangre obtenida a través de punción periférica En recién nacidos y lactantes, donde no es fácil obtener tanta cantidad de muestra, debe enviarse como mínimo 1 ml de sangre completa. Si la toma se hizo con jeringa, retirar la aguja y verter la sangre a un tubo estéril, dejándola resbalar lentamente por la pared para evitar hemólisis. Tapar el tubo cuidadosamente. Si la muestra necesaria es sangre total utilizar un tubo de hematología con EDTA (venoject ó vacutainer TAPA MORADA). Bata y campos estériles. Gorro y mascarilla con protección ocular. Guantes estériles. Equipo de asepsia (antiséptico, gasas y guantes estériles). Tubo de hematología con EDTA. Jeringas estériles. La muestra debe ser analizada dentro de las 24 hrs. siguientes, en caso contrario puede mantenerse refrigerada a 4ºC hasta una semana. Se recomienda no congelar. b) Líquido pleural, pericárdico, peritoneal,, culdocentesis, amniótico La recolección de muestras de este origen está reservada estrictamente al médico especialista. No se recomienda usar tórulas, la muestra debe ser obtenida por aspirado o drenaje quirúrgico. Los líquidos susceptibles de formar coágulo deben ser colectados en tubos con anticoagulante EDTA (ácido etilendiaminotetracético). En el líquido amniótico los virus que causan infección en el útero son CMV, Parvovirus B-19 y VIH, menos frecuentemente observados virus herpes simplex (HSV) y virus Zoster (VZV). Realice preparación de la piel con técnica aséptica. Puncionar con jeringa y aguja estéril, y recoger entre 1 y 5 ml de líquido. Recolectar en frasco seco. 3
4 b) Líquido pleural, pericárdico, peritoneal, culdocentesis, amniótico Equipo de preparación de piel y anestesia local. Jeringa y aguja estéril. Tubo estéril seco. La muestra puede ser almacenada a temperatura ambiente durante 48 horas y refrigerada hasta por 2 semanas. En el caso del líquido amniótico puede almacenarse a temperatura ambiente por 8 horas y refrigerado a 4ºC hasta por 1 semana. c) Líquido cefalorraquídeo (LCR) Enviar con resumen de historia clínica. Procedimiento realizado por personal médico. Preparación aséptica de la piel: el paciente debe estar recostado sobre un costado con el torso doblado hacia delante. Bajo anestesia local se introduce una aguja larga en el conducto espinal; no necesita ser aspirado, fluye por presión en individuos sanos. Obtener mínimo 3 ml de LCR en tubo estéril tapa rosca. Equipo de asepsia: mascarilla, guantes y campo estériles. Equipo de punción lumbar. La muestra puede ser almacenada a temperatura ambiente durante 8 horas. Puede mantenerse refrigerada a 4ºC hasta por 1 semana. 3
5 d) Secreción de área nasofaríngea La persona que obtiene la muestra debe usar barreras de protección (mascarilla, protección ocular). No hacer gárgaras ni limpieza con ninguna solución bucofaríngea. Tomar la muestra preferiblemente en ayunas. Colocar al paciente bajo una buena fuente de luz. Introducir la tórula flexible hasta la nasofaringe posterior evitando trauma. Rotar la tórula por 10 a 15 segundos para permitir la impregnación del hisopo y retirar lentamente. Barreras de protección (mascarilla y protección ocular). Guantes no estériles. Tórulas estériles flexibles. Tubo estéril. La muestra puede ser almacenada a temperatura ambiente durante 48 horas. Puede mantenerse refrigerada a 4ºC hasta por dos semanas. e) Aspirado nasofaringe La persona que obtiene la muestra debe usar barreras de protección (mascarilla, protección ocular). No hacer gárgaras ni limpieza con ninguna solución bucofaríngea. Tomar la muestra preferiblemente en ayunas. 4
6 e) Aspirado nasofaringe Es colectado mediante el paso de una sonda nelaton de un calibre apropiado dentro de la nasofaringe. Aspirar luego el material con una jeringa estéril u otro mecanismo de succión y colocarlo en tubo estéril seco. En caso de no poder recolectar la muestra en la jeringa, envíe el extremo distal de la sonda con el material aspirado en el tubo estéril seco. Barreras de protección (mascarilla y protección ocular). Guantes no estériles. Tubo estéril seco o medio de transporte para virus. Sonda nelaton. Jeringa estéril. La muestra puede ser almacenada a temperatura ambiente durante 48 horas. Puede mantenerse refrigerada a 4ºC hasta por dos semanas. f) Secreción de la faringe No contaminar la tórula con secreción de cavidad oral o dientes. El hisopado de garganta está contraindicado en pacientes con diagnóstico de epiglotitis. No hacer gárgaras ni limpieza con ninguna solución bucofaríngea. Colocar al paciente bajo una buena fuente de luz. Con un bajalenguas, presionar la lengua hacia abajo para visualizar los pilares de la faringe y del área tonsilar para localizar el área de inflamación y exudado. Rotar la tórula estéril sobre el área. 5
7 f) Secreción de la faringe Guantes. Tórulas estériles. temperatura ambiente durante 48 horas. Puede mantenerse refrigerada a 4ºC hasta por dos semanas. g) Esputo por expectoración espontánea El esputo no es la muestra ideal para el diagnóstico de neumonía; se recomienda preferiblemente el lavado broncoalveolar. Recolectar la muestra en la mañana, en ayunas preferiblemente. Instruir al paciente para realizar cepillado de dientes y lavado de la lengua sólo con agua para remover el exceso de flora oral y retirar prótesis dental en pacientes de edad. Para pacientes pediátricos incapaces de producir un esputo, la terapeuta respiratoria debe obtener la muestra a través de succión. En pacientes ambulatorios sintomáticos respiratorios con sospecha de tuberculosis, la primera muestra se toma el día de la consulta médica y las otras dos al día siguiente, cumpliendo las recomendaciones descritas para paciente hospitalizado. Instruir al paciente para que tosa con fuerza y profundamente, con el fin de obtener una muestra que provenga del tracto respiratorio inferior, libre de saliva contenida en la cavidad oral, la cual debe expectorar directamente en un recipiente estéril de boca ancha de tapa rosca. Frasco estéril de boca ancha, de 5 cm de diámetro, de tapa rosca, con capacidad de 30 a 50 ml, de material fácil de rotular. La muestra puede ser almacenada a temperatura ambiente durante 48 horas. Puede mantenerse refrigerada a 4ºC hasta por dos semanas. 6
8 h) Esputo inducido Instruir al paciente para realizar cepillado de dientes y lavado de lengua solo con agua. Realizar nebulización con solución salina normal. Para pacientes pediátricos incapaces de producir un esputo, la terapeuta respiratoria debe obtener la muestra a través de succión. Instruir al paciente para que tosa con fuerza y profundamente, con el fin de obtener una muestra que provenga del tracto respiratorio inferior, libre de saliva contenida en la cavidad oral, la cual debe expectorar directamente en un recipiente estéril de boca ancha de tapa rosca. Frasco estéril de boca ancha de tapa rosca de 5 cm de diámetro, con una capacidad de 30 a 50 ml y material fácil de rotular. Nebulizador. Solución salina normal. La muestra puede ser almacenada a temperatura ambiente durante 48 horas. Puede mantenerse refrigerada a 4ºC hasta por dos semanas. i) Secreción traqueal Realice el procedimiento con técnica aséptica. De acuerdo con las características de las secreciones, irrigar con solución salina normal previo a realizar el procedimiento. 7
9 i) Secreción traqueal Introducir la sonda sin hacer succión a través del tubo endotraqueal o cánula de traquestomía, hasta ubicarla en el espacio traqueal. Ocluya el orificio distal de la sonda y comience a succionar, retire la sonda lentamente mientras la va limpiando externamente con una gasa estéril. Tenga precaución de suspender la succión, retirando la oclusión de la sonda para que se conserve la muestra obtenida en el trayecto de la misma. Coloque la muestra obtenida en frasco estéril cortando el segmento distal de la sonda, si no es posible el depósito de la muestra sola, para lo cual retira la presión en el orificio de la sonda lo que permitirá la expulsión de la muestra en el recipiente. Guantes estériles. Mascarilla con protección ocular. Sonda de nelaton. Hoja de bisturí. Solución salina normal. Gasas estériles. Frasco de boca ancha estéril o trampa recolectora. La muestra puede ser almacenada a temperatura ambiente durante 48 horas. Puede mantenerse refrigerada a 4ºC hasta por dos semanas. j) Lavado o cepillado broncoalveolar El paciente debe estar en ayunas para realizar el procedimiento, ya que se requiere de sedación. 8
10 j) Lavado o cepillado broncoalveolar A través de técnica de fibrobroncoscopia. Conecte una trampa de Lukens al fibrobroncoscopio. Irrigar con 10 ml de solución salina a través del canal abierto. Succione para obtener la muestra en dos frascos estériles de boca ancha. Equipos de fibrobroncoscopia. Sistema de succión. Recipiente de boca ancha estéril de tapa rosca. La muestra puede ser almacenada a temperatura ambiente durante 48 horas. Puede mantenerse refrigerada a 4ºC hasta por dos semanas. k) Muestras obtenidas por abordaje percutáneo Son todos procedimientos médicos. Dentro de las técnicas invasivas son las que permiten la obtención de muestras más representativas del parénquima pulmonar, no obstante, sólo deben emplearse cuando fracasen otros métodos menos invasivos o cuando la situación del enfermo haga imprescindible conocer el diagnóstico etiológico. Técnica a realizar por personal entrenado. Pueden emplearse las siguientes: 9
11 k) Muestras obtenidas por abordaje percutáneo i. Punción pulmonar aspirativa transtorácica: Obtención del exudado de las lesiones pulmonares a través de una punción transtorácica con aguja ultrafina con control radioscópico o ecográfico. Debe aplicarse ante infiltraciones densas (no intersticiales) y sobre todo si son periféricas. Contraindicado en pacientes con bullas, trastornos de coagulación y sospecha de hidatidosis. Posibles complicaciones, como neumotórax y hemoptisis. Es una muestra ideal para estudio en infección anaerobia grave en niños, especialmente en edades tempranas. ii. Punción biópsica pulmonar: Biopsia transtorácica con trocar. Sólo en casos excepcionales y en caso de lesiones muy periféricas debido al alto riesgo de neumotórax. iii. Biopsia pulmonar por toracotomía: Permite la selección visual del área neumónica a cielo abierto. : La muestra puede ser almacenada a temperatura ambiente durante 48 horas. Puede mantenerse refrigerada a 4ºC hasta por dos semanas. L) Orina de micción espontánea Realizar higiene de genitales: en mujeres, es necesario lavar el vestíbulo vaginal y la entrada de la uretra con agua jabonosa, enjuagar con abundante agua. Secar y separar los labios e iniciar la micción. En el hombre se debe hacer retracción del prepucio y lavar el meato urinario con agua jabonosa, enjuagar con abundante agua y secar. Con el prepucio retraído iniciar la recolección de la orina. En pacientes ambulatorios es ideal recoger la muestra de la primera micción del día. 10
12 L) Orina de micción espontánea Instruir al paciente para que inicie la micción, desechar la primera parte de la orina. Introducir el frasco colector, recoger la parte media de la orina sin detener el flujo urinario (5-10 ml) Terminar de eliminar en el sanitario o pato. Tapar el frasco sin contaminar la muestra. Frasco recolector estéril de boca ancha de tapa rosca. Equipo de higiene: jabón, gasas. La muestra puede ser almacenada a temperatura ambiente durante 24 horas. Posteriormente debe mantenerse refrigerada a 4ºC hasta por una semana. m) Secreción conjuntival m) Secreción conjuntival No usar gotas oftálmicas 18 a 24 horas antes de la muestra. Ausencia de cualquier cosmético. No tomar antibióticos 24 a 48 horas antes. No usar anestésicos que posean actividad antimicrobiana. Deberá utilizarse una tórula para cada ojo. Tome una muestra por cada ojo con tórula previamente humedecidas con suero fisiológico. Obtener la secreción con tórula estéril frotando la conjuntiva tarsal inferior y el fórnix de afuera hacia adentro. Rotar la tórula suavemente para que toda la superficie del algodón se empape de la secreción purulenta. 11
13 m) Secreción conjuntival Guantes estériles Tórula estéril, jeringa y aguja estériles. La muestra puede ser almacenada a temperatura ambiente durante 48 horas. Posteriormente debe mantenerse refrigerada a 4ºC hasta por dos semanas. 3. Herpesvirus humano tipo 3 a) Sangre obtenida a través de punción periférica Realizar lavado de manos quirúrgico. Mantener técnica aséptica durante todo el procedimiento. Utilizar campo estéril para evitar tener contacto con áreas circundantes que ofrezca el riesgo de contaminación. Colocar mascarilla al paciente. Realizar antisepsia de la zona a puncionar; no palpe la vena sin guantes estériles una vez preparada la piel. Utilizar otros guantes estériles para cada punción. POR ÉSTE MÉTODO NO PUEDEN SER PROCESADAS MUESTRAS CON HEPARINA. En pacientes heparinizados, la toma de muestra debe realizarse en el momento más alejado de la administración del medicamento. 12
14 a) Sangre obtenida a través de punción periférica La toma deberá hacerse en un lugar perfectamente iluminado y con el paciente cómodamente sentado. Localizar una vena adecuada en la cara anterior del codo y colocar el torniquete en la parte media del brazo. Desinfectar el área con un algodón humedecido con alcohol al 70% e introducir la aguja con el bisel hacia arriba. Si la sangre no fluye espontáneamente y se está utilizando una jeringa, jalar el émbolo y aspirar con suavidad; si se está empleando equipo al vacío presionar el tubo de ensaye hacia arriba. Al empezar a fluir la sangre retirar el torniquete. Una vez que se haya obtenido entre 5-8 ml de sangre, retirar la aguja y colocar una tórula con alcohol sobre el sitio de punción ejerciendo presión para detener la hemorragia. En recién nacidos y lactantes, donde no es fácil obtener tanta cantidad de muestra, debe enviarse como mínimo 1 ml de sangre completa. Si la toma se hizo con jeringa, retirar la aguja y verter la sangre a un tubo estéril, dejándola resbalar lentamente por la pared para evitar hemólisis. Tapar el tubo cuidadosamente. Si la muestra necesaria es sangre total utilizar un tubo de hematología con EDTA (venoject ó vacutainer TAPA MORADA). Bata y campos estériles. Gorro y mascarilla con protección ocular. Guantes estériles. Equipo de asepsia (antiséptico, gasas y guantes estériles). Tubo de hematología con EDTA. Jeringas estériles. La muestra debe ser analizada dentro de las 24 hrs. siguientes, en caso contrario puede mantenerse refrigerada a 4ºC hasta una semana. Se recomienda no congelar. 13
15 b) Líquido cefalorraquídeo (LCR) Enviar con resumen de historia clínica. Procedimiento realizado por personal médico. Preparación aséptica de la piel: el paciente debe estar recostado sobre un costado con el torso doblado hacia delante. Bajo anestesia local se introduce una aguja larga en el conducto espinal; no necesita ser aspirado, fluye por presión en individuos sanos. Obtener mínimo 3 ml de LCR en tubo estéril tapa rosca. Equipo de asepsia: mascarilla, guantes y campo estériles. Equipo de punción lumbar. La muestra puede ser almacenada a temperatura ambiente durante 8 horas. Posteriormente debe mantenerse refrigerada a 4ºC hasta por una semana. 4. Herpesvirus humano tipo 4 a) Líquido cefalorraquídeo (LCR) Enviar con resumen de historia clínica. Procedimiento realizado por personal médico. 14
16 a) Líquido cefalorraquídeo (LCR) Preparación aséptica de la piel: el paciente debe estar recostado sobre un costado con el torso doblado hacia delante. Bajo anestesia local se introduce una aguja larga en el conducto espinal; no necesita ser aspirado, fluye por presión en individuos sanos. Obtener mínimo 3 ml de LCR en tubo estéril tapa rosca. Equipo de asepsia: mascarilla, guantes y campo estériles. Equipo de punción lumbar. La muestra puede ser almacenada a temperatura ambiente durante 8 horas. Posteriormente debe mantenerse refrigerada a 4ºC hasta por una semana. 5. Herpesvirus humano tipo 5 a) Sangre obtenida a través de punción periférica Realizar lavado de manos quirúrgico. Mantener técnica aséptica durante todo el procedimiento. Utilizar campo estéril para evitar tener contacto con áreas circundantes que ofrezca el riesgo de contaminación. Colocar mascarilla al paciente. Realizar antisepsia de la zona a puncionar; no palpe la vena sin guantes estériles una vez preparada la piel. Utilizar otros guantes estériles para cada punción. POR ÉSTE MÉTODO NO PUEDEN SER PROCESADAS MUESTRAS CON HEPARINA. En pacientes heparinizados, la toma de muestra debe realizarse en el momento más alejado de la administración del medicamento. 15
17 a) Sangre obtenida a través de punción periférica La toma deberá hacerse en un lugar perfectamente iluminado y con el paciente cómodamente sentado. Localizar una vena adecuada en la cara anterior del codo y colocar el torniquete en la parte media del brazo. Desinfectar el área con un algodón humedecido con alcohol al 70% e introducir la aguja con el bisel hacia arriba. Si la sangre no fluye espontáneamente y se está utilizando una jeringa, jalar el émbolo y aspirar con suavidad; si se está empleando equipo al vacío presionar el tubo de ensaye hacia arriba. Al empezar a fluir la sangre retirar el torniquete. Una vez que se haya obtenido entre 5-8 ml de sangre, retirar la aguja y colocar una tórula con alcohol sobre el sitio de punción ejerciendo presión para detener la hemorragia. En recién nacidos y lactantes, donde no es fácil obtener tanta cantidad de muestra, debe enviarse como mínimo 1 ml de sangre completa. Si la toma se hizo con jeringa, retirar la aguja y verter la sangre a un tubo estéril, dejándola resbalar lentamente por la pared para evitar hemólisis. Tapar el tubo cuidadosamente. Si la muestra necesaria es sangre total utilizar un tubo de hematología con EDTA (venoject ó vacutainer TAPA MORADA). Bata y campos estériles. Gorro y mascarilla con protección ocular. Guantes estériles. Equipo de asepsia (antiséptico, gasas y guantes estériles). Tubo de hematología con EDTA. Jeringas estériles. La muestra debe ser analizada dentro de las 24 hrs. siguientes, en caso contrario puede mantenerse refrigerada a 4ºC hasta una semana. Se recomienda no congelar. 16
18 b) Biopsia de tejido de cualquier sitio anatómico Realizar preparación antiséptica del área de donde se va a tomar la biopsia. Conservar la esterilidad de la muestra hasta su recepción en el laboratorio clínico o de patología. Se recomienda tomar biopsia de tejido para lesiones relacionadas con úlceras de presión, úlceras varicosas, quemaduras y pie diabético, realizar limpieza previa con solución salina estéril. Si la biopsia de tejido no es posible de realizar, aspire material inflamatorio de la base de la lesión. Este procedimiento debe ser realizado por el médico. Seccionar la muestra en fresco para enviar al laboratorio clínico. Equipo para preparación de piel. Frasco estéril para la muestra microbiológica. La muestra debe ser analizada dentro de las 24 hrs. siguientes, en caso contrario puede mantenerse refrigerada a 4ºC hasta una semana. Se recomienda no congelar. 17
19 6. Herpesvirus humano tipo 6 a) Sangre obtenida a través de punción periférica Realizar lavado de manos quirúrgico. Mantener técnica aséptica durante todo el procedimiento. Utilizar campo estéril para evitar tener contacto con áreas circundantes que ofrezca el riesgo de contaminación. Colocar mascarilla al paciente. Realizar antisepsia de la zona a puncionar; no palpe la vena sin guantes estériles una vez preparada la piel. Utilizar otros guantes estériles para cada punción. POR ÉSTE MÉTODO NO PUEDEN SER PROCESADAS MUESTRAS CON HEPARINA. En pacientes heparinizados, la toma de muestra debe realizarse en el momento más alejado de la administración del medicamento. La toma deberá hacerse en un lugar perfectamente iluminado y con el paciente cómodamente sentado. Localizar una vena adecuada en la cara anterior del codo y colocar el torniquete en la parte media del brazo. Desinfectar el área con un algodón humedecido con alcohol al 70% e introducir la aguja con el bisel hacia arriba. Si la sangre no fluye espontáneamente y se está utilizando una jeringa, jalar el émbolo y aspirar con suavidad; si se está empleando equipo al vacío presionar el tubo de ensaye hacia arriba. Al empezar a fluir la sangre retirar el torniquete. Una vez que se haya obtenido entre 5-8 ml de sangre, retirar la aguja y colocar una tórula con alcohol sobre el sitio de punción ejerciendo presión para detener la hemorragia. En recién nacidos y lactantes, donde no es fácil obtener tanta cantidad de muestra, debe enviarse como mínimo 1 ml de sangre completa. Si la toma se hizo con jeringa, retirar la aguja y verter la sangre a un tubo estéril, dejándola resbalar lentamente por la pared para evitar hemólisis. Tapar el tubo cuidadosamente. Si la muestra necesaria es sangre total utilizar un tubo de hematología con EDTA (venoject ó vacutainer TAPA MORADA). 18
20 a) Sangre obtenida a través de punción periférica Equipo de asepsia (antiséptico, gasas y guantes estériles). Tubo de hematología con EDTA. Jeringas estériles. b) Líquido cefalorraquídeo (LCR) Enviar con resumen de historia clínica. Procedimiento realizado por personal médico. Preparación aséptica de la piel: el paciente debe estar recostado sobre un costado con el torso doblado hacia delante. Bajo anestesia local se introduce una aguja larga en el conducto espinal; no necesita ser aspirado, fluye por presión en individuos sanos. Obtener mínimo 3 ml de LCR en tubo estéril tapa rosca. Equipo de asepsia: mascarilla, guantes y campo estériles. Equipo de punción lumbar. Equipo de asepsia (antiséptico, gasas y guantes estériles). Tubo de hematología con EDTA. Jeringas estériles. La muestra debe ser analizada dentro de las 24 hrs. siguientes, en caso contrario puede mantenerse refrigerada a 4ºC hasta una semana. Se recomienda no congelar. La muestra puede ser almacenada a temperatura ambiente durante 8 horas. Posteriormente debe mantenerse refrigerada a 4ºC hasta por una semana. 19
21 c) Lavado o cepillado broncoalveolar El paciente debe estar en ayunas para realizar el procedimiento, ya que se requiere de sedación. A través de técnica de fibrobroncoscopia. Conecte una trampa de Lukens al fibrobroncoscopio. Irrigar con 10 ml de solución salina a través del canal abierto. Succione para obtener la muestra en dos frascos estériles de boca ancha. Equipos de fibrobroncoscopia. Sistema de succión. Recipiente de boca ancha estéril de tapa rosca. La muestra puede ser almacenada a temperatura ambiente durante 48 horas. Posteriormente debe mantenerse refrigerada a 4ºC hasta por dos semanas. d) Líquido pleural La recolección de muestras de este origen está reservada estrictamente al médico especialista. No se recomienda usar tórulas, la muestra debe ser obtenida por aspirado o drenaje quirúrgico. Los líquidos susceptibles de formar coágulo deben ser colectados en tubos con anticoagulante EDTA (ácido etilendiaminotetracético). En el líquido amniótico los virus que causan infección en el útero son CMV, Parvovirus B-19 y VIH, menos frecuentemente observados virus herpes simplex (HSV) y virus Zoster (VZV). 20
22 d) Líquido pleural Realice preparación de la piel con técnica aséptica. Puncionar con jeringa y aguja estéril, y recoger entre 1 y 5 ml de líquido. Recolectar en frasco seco. Equipo de preparación de piel y anestesia local. Jeringa y aguja estéril. Tubo estéril seco. La muestra puede ser almacenada a temperatura ambiente durante 4 horas. Posteriormente debe mantenerse refrigerada a 4ºC hasta por una semana. 7. Herpesvirus humano tipo 7 a) Sangre obtenida a través de punción periférica Realizar lavado de manos quirúrgico. Mantener técnica aséptica durante todo el procedimiento. Utilizar campo estéril para evitar tener contacto con áreas circundantes que ofrezca el riesgo de contaminación. Colocar mascarilla al paciente. Realizar antisepsia de la zona a puncionar; no palpe la vena sin guantes estériles una vez preparada la piel. Utilizar otros guantes estériles para cada punción. POR ÉSTE MÉTODO NO PUEDEN SER PROCESADAS MUESTRAS CON HEPARINA. En pacientes heparinizados, la toma de muestra debe realizarse en el momento más alejado de la administración del medicamento. 21
23 a) Sangre obtenida a través de punción periférica La toma deberá hacerse en un lugar perfectamente iluminado y con el paciente cómodamente sentado. Localizar una vena adecuada en la cara anterior del codo y colocar el torniquete en la parte media del brazo. Desinfectar el área con un algodón humedecido con alcohol al 70% e introducir la aguja con el bisel hacia arriba. Si la sangre no fluye espontáneamente y se está utilizando una jeringa, jalar el émbolo y aspirar con suavidad; si se está empleando equipo al vacío presionar el tubo de ensaye hacia arriba. Al empezar a fluir la sangre retirar el torniquete. Una vez que se haya obtenido entre 5-8 ml de sangre, retirar la aguja y colocar una tórula con alcohol sobre el sitio de punción ejerciendo presión para detener la hemorragia. En recién nacidos y lactantes, donde no es fácil obtener tanta cantidad de muestra, debe enviarse como mínimo 1 ml de sangre completa. Si la toma se hizo con jeringa, retirar la aguja y verter la sangre a un tubo estéril, dejándola resbalar lentamente por la pared para evitar hemólisis. Tapar el tubo cuidadosamente. Si la muestra necesaria es sangre total utilizar un tubo de hematología con EDTA (venoject ó vacutainer TAPA MORADA). Bata y campos estériles. Gorro y mascarilla con protección ocular. Guantes estériles. Equipo de asepsia (antiséptico, gasas y guantes estériles). Tubo de hematología con EDTA. Jeringas estériles. La muestra debe ser analizada dentro de las 24 hrs. siguientes, en caso contrario puede mantenerse refrigerada a 4ºC hasta una semana. Se recomienda no congelar. 22
24 b) Líquido cefalorraquídeo (LCR) Enviar con resumen de historia clínica. Procedimiento realizado por personal médico. Preparación aséptica de la piel: el paciente debe estar recostado sobre un costado con el torso doblado hacia delante. Bajo anestesia local se introduce una aguja larga en el conducto espinal; no necesita ser aspirado, fluye por presión en individuos sanos. Obtener mínimo 3 ml de LCR en tubo estéril tapa rosca. Equipo de asepsia: mascarilla, guantes y campo estériles. Equipo de punción lumbar. La muestra puede ser almacenada a temperatura ambiente durante 8 horas. Posteriormente debe mantenerse refrigerada a 4ºC hasta por una semana. c) Lavado o cepillado broncoalveolar El paciente debe estar en ayunas para realizar el procedimiento, ya que se requiere de sedación. A través de técnica de fibrobroncoscopia. Conecte una trampa de Lukens al fibrobroncoscopio. Irrigar con 10 ml de solución salina a través del canal abierto. Succione para obtener la muestra en dos frascos estériles de boca ancha. 23
25 c) Lavado o cepillado broncoalveolar Equipos de fibrobroncoscopia. Sistema de succión. Recipiente de boca ancha estéril de tapa rosca. Se recomienda en los primeros 15 minutos de la recolección, no exceder de dos horas y a temperatura ambiente. d) Líquido pleural La recolección de muestras de este origen está reservada estrictamente al médico especialista. No se recomienda usar tórulas, la muestra debe ser obtenida por aspirado o drenaje quirúrgico. Los líquidos susceptibles de formar coágulo deben ser colectados en tubos con anticoagulante EDTA (ácido etilendiaminotetracético). En el líquido amniótico los virus que causan infección en el útero son CMV, Parvovirus B-19 y VIH, menos frecuentemente observados virus herpes simplex (HSV) y virus Zoster (VZV). Realice preparación de la piel con técnica aséptica. Puncionar con jeringa y aguja estéril, y recoger entre 1 y 5 ml de líquido. Recolectar en frasco seco. Equipo de preparación de piel y anestesia local. Jeringa y aguja estéril. Tubo estéril seco. 24
26 d) Líquido pleural La muestra puede ser almacenada a temperatura ambiente durante 48 horas. Posteriormente debe mantenerse refrigerada a 4ºC hasta por dos semanas. 8. Herpesvirus humano tipo 8 a) Sangre obtenida a través de punción periférica Realizar lavado de manos quirúrgico. Mantener técnica aséptica durante todo el procedimiento. Utilizar campo estéril para evitar tener contacto con áreas circundantes que ofrezca el riesgo de contaminación. Colocar mascarilla al paciente. Realizar antisepsia de la zona a puncionar; no palpe la vena sin guantes estériles una vez preparada la piel. Utilizar otros guantes estériles para cada punción. POR ÉSTE MÉTODO NO PUEDEN SER PROCESADAS MUESTRAS CON HEPARINA. En pacientes heparinizados, la toma de muestra debe realizarse en el momento más alejado de la administración del medicamento. La toma deberá hacerse en un lugar perfectamente iluminado y con el paciente cómodamente sentado. Localizar una vena adecuada en la cara anterior del codo y colocar el torniquete en la parte media del brazo. Desinfectar el área con un algodón humedecido con alcohol al 70% e introducir la aguja con el bisel hacia arriba. Si la sangre no fluye espontáneamente y se está utilizando una jeringa, jalar el émbolo y aspirar con suavidad; si se está empleando equipo al vacío presionar el tubo de ensaye hacia arriba. Al empezar a fluir la sangre retirar el torniquete. 25
27 a) Sangre obtenida a través de punción periférica Una vez que se haya obtenido entre 5-8 ml de sangre, retirar la aguja y colocar una tórula con alcohol sobre el sitio de punción ejerciendo presión para detener la hemorragia. En recién nacidos y lactantes, donde no es fácil obtener tanta cantidad de muestra, debe enviarse como mínimo 1 ml de sangre completa. Si la toma se hizo con jeringa, retirar la aguja y verter la sangre a un tubo estéril, dejándola resbalar lentamente por la pared para evitar hemólisis. Tapar el tubo cuidadosamente. Si la muestra necesaria es sangre total utilizar un tubo de hematología con EDTA (venoject ó vacutainer TAPA MORADA). Bata y campos estériles. Gorro y mascarilla con protección ocular. Guantes estériles. Equipo de asepsia (antiséptico, gasas y guantes estériles). Tubo de hematología con EDTA. Jeringas estériles. La muestra debe ser analizada dentro de las 24 hrs. siguientes, en caso contrario puede mantenerse refrigerada a 4ºC hasta una semana. Se recomienda no congelar. b) Líquido cefalorraquídeo (LCR) Enviar con resumen de historia clínica. Procedimiento realizado por personal médico. 26
28 b) Líquido cefalorraquídeo (LCR) Preparación aséptica de la piel: el paciente debe estar recostado sobre un costado con el torso doblado hacia delante. Bajo anestesia local se introduce una aguja larga en el conducto espinal; no necesita ser aspirado, fluye por presión en individuos sanos. Obtener mínimo 3 ml de LCR en tubo estéril tapa rosca. Equipo de asepsia: mascarilla, guantes y campo estériles. Equipo de punción lumbar. La muestra puede ser almacenada a temperatura ambiente durante 8 horas. Posteriormente debe mantenerse refrigerada a 4ºC hasta por una semana. c) Lavado o cepillado broncoalveolar El paciente debe estar en ayunas para realizar el procedimiento, ya que se requiere de sedación. A través de técnica de fibrobroncoscopia. Conecte una trampa de Lukens al fibrobroncoscopio. Irrigar con 10 ml de solución salina a través del canal abierto. Succione para obtener la muestra en dos frascos estériles de boca ancha. Equipos de fibrobroncoscopia. Recipiente de boca ancha estéril de tapa rosca. Sistema de succión. 27
29 c) Lavado o cepillado broncoalveolar La muestra puede ser almacenada a temperatura ambiente durante 48 horas. Posteriormente debe mantenerse refrigerada a 4ºC hasta por dos semanas. d) Líquido pleural La recolección de muestras de este origen está reservada estrictamente al médico especialista. No se recomienda usar torulas, la muestra debe ser obtenida por aspirado o drenaje quirúrgico. Los líquidos susceptibles de formar coágulo deben ser colectados en tubos con anticoagulante EDTA (ácido etilendiaminotetracético). En el líquido amniótico los virus que causan infección en el útero son CMV, Parvovirus B-19 y VIH, menos frecuentemente observados virus herpes simplex (HSV) y virus Zoster (VZV). Realice preparación de la piel con técnica aséptica. Puncionar con jeringa y aguja estéril, y recoger entre 1 y 5 ml de líquido. Recolectar en frasco seco. Equipo de preparación de piel y anestesia local. Jeringa y aguja estéril. Tubo estéril seco. La muestra puede ser almacenada a temperatura ambiente durante 48 horas. Posteriormente debe mantenerse refrigerada a 4ºC hasta por dos semanas. 28
30 9. Bibliografía Carlberg, D. Cleanroom microbiology for the non microbiologist. Interpharm Press. INC. Buffalo Grove, Illinois Collins CH, Lyne PM, Grange JM. Microbiological methods. 7ma edition. Oxford Forman MS, Valsamakis A, Specimen collection, transport, and processing: Virology. En Murray PR, Baron EJ, Jorgensen JH, Pfaller MA, Yolken RH, editors. Manual of clinical microbiology. 8th ed. Washington: ASM Press; Guerrero Gómez C; Sánchez Carrillo C. Procedimientos en microbiología clínica. Recogida, transporte y procesamientos general de las muestras en el laboratorio de microbiología, Miller JM, Holmes HT. General principles in specimen collection, transport and storage. En Murray PR, Baron EJ, Jorgensen JH, Pfaller MA, Yolken RH, editors. Manual of clinical microbiology. 8th ed. Washington: ASM Press; Organización Mundial de la Salud. Guía para transporte seguro de sustancias infecciosas y especímenes. Ginebra (Suiza): WHO/EM- C/97.3; Procedimientos en microbiología clínica. Emilia Cercenado y Rafael Cantón SEIMC. España. Thomson BR (JR.), and Miller M. Specimen collection, transport, and processing: Bacteriology. En Murray PR, Baron EJ, Jorgensen JH, Pfaller MA, Yolken RH, editors. Manual of clinical microbiology. 8th ed. Washington: ASM Press;
Manual Toma de Muestras Human PCR Kit
 Manual Toma de Muestras Human PCR Kit Contenido 1. Introducción... 2 2. Herpesvirus humano 1 y herpesvirus humano 2... 2 a) Sangre obtenida a través de punción periférica... 2 b) Líquido pleural, pericárdico,
Manual Toma de Muestras Human PCR Kit Contenido 1. Introducción... 2 2. Herpesvirus humano 1 y herpesvirus humano 2... 2 a) Sangre obtenida a través de punción periférica... 2 b) Líquido pleural, pericárdico,
Manual Toma de Muestras Human PCR Kit
 Manual Toma de Muestras Human PCR Kit Tabla de contenido 1. Introducción... 1 2. Infecciones del tracto respiratorio superior... 1 a. Secreción de la zona nasal... 1 b. Secreción de área nasofaríngea...
Manual Toma de Muestras Human PCR Kit Tabla de contenido 1. Introducción... 1 2. Infecciones del tracto respiratorio superior... 1 a. Secreción de la zona nasal... 1 b. Secreción de área nasofaríngea...
Manual Toma de Muestras Human PCR Kit
 Manual Toma de Muestras Human PCR Kit 1. Materia fecal... 9 Contenido MUESTRAS GENITOURINARIAS... 2 1. Genitales femeninos... 2 A. Secreciones cervicales... 2 B. Secreciones vaginales... 3 C. Secreciones
Manual Toma de Muestras Human PCR Kit 1. Materia fecal... 9 Contenido MUESTRAS GENITOURINARIAS... 2 1. Genitales femeninos... 2 A. Secreciones cervicales... 2 B. Secreciones vaginales... 3 C. Secreciones
Toma de Muestras Microbiológicas
 Toma de Muestras Microbiológicas MICROBIOLOGÍA CLÍNICA DIAGNÓSTICO DE ENFERMEDADES INFECCIOSAS MUESTRA AISLAMIENTO IDENTIFICACIÓN SENSIBILIDAD A ANTIMICROBIANOS Detección de anticuerpos, antígenos y ácidos
Toma de Muestras Microbiológicas MICROBIOLOGÍA CLÍNICA DIAGNÓSTICO DE ENFERMEDADES INFECCIOSAS MUESTRA AISLAMIENTO IDENTIFICACIÓN SENSIBILIDAD A ANTIMICROBIANOS Detección de anticuerpos, antígenos y ácidos
TOMA DE MUESTRAS MICROBIOLOGICAS. Dra. Dona Benadof Microbiología Hospital Roberto del Río Comité Vigilancia Infecciones Intrahospitalarias
 TOMA DE MUESTRAS MICROBIOLOGICAS Dra. Dona Benadof Microbiología Hospital Roberto del Río Comité Vigilancia Infecciones Intrahospitalarias INTRODUCCIÓN La confiabilidad de los resultados del estudio microbiológico
TOMA DE MUESTRAS MICROBIOLOGICAS Dra. Dona Benadof Microbiología Hospital Roberto del Río Comité Vigilancia Infecciones Intrahospitalarias INTRODUCCIÓN La confiabilidad de los resultados del estudio microbiológico
Trabajo Práctico Nº4: OBTENCIÓN Y PROCESAMIENTO DE MUESTRAS CLÍNICAS DESTINADAS AL ANÁLISIS MICROBIOLÓGICO. (Lic en Enfermería y Lic en Obstetricia)
 Trabajo Práctico Nº4: OBTENCIÓN Y PROCESAMIENTO DE MUESTRAS CLÍNICAS DESTINADAS AL ANÁLISIS MICROBIOLÓGICO. (Lic en Enfermería y Lic en Obstetricia) INTRODUCCIÓN La actividad que desarrolla el laboratorio
Trabajo Práctico Nº4: OBTENCIÓN Y PROCESAMIENTO DE MUESTRAS CLÍNICAS DESTINADAS AL ANÁLISIS MICROBIOLÓGICO. (Lic en Enfermería y Lic en Obstetricia) INTRODUCCIÓN La actividad que desarrolla el laboratorio
GenPE: estudio Internacional de Genética en Preeclampsia
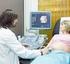 GenPE: estudio Internacional de Genética en Preeclampsia INSTRUCTIVO Toma de muestra proyecto GenPE PAQUETE PARA CAPTACIÓN DE PACIENTE Y TOMA DE MUESTRA. Cuando llegue a su institución la caja del proyecto
GenPE: estudio Internacional de Genética en Preeclampsia INSTRUCTIVO Toma de muestra proyecto GenPE PAQUETE PARA CAPTACIÓN DE PACIENTE Y TOMA DE MUESTRA. Cuando llegue a su institución la caja del proyecto
Extracción de Sangre Venosa Periférica
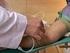 Extracción de Sangre Venosa Periférica Introducción La extracción venosa de sangre es un proceso muy acequiado en el análisis biológico dado que es posible detectar diversas enfermedades o condiciones
Extracción de Sangre Venosa Periférica Introducción La extracción venosa de sangre es un proceso muy acequiado en el análisis biológico dado que es posible detectar diversas enfermedades o condiciones
CATETERISMO VESICAL ELABORADO: CATETERISMO VESICAL
 PAGINA: 1 de 6 REVISADO: COORDINADOR DE CALIDAD ELABORADO: ENFERMERO JEFE COORDINADOR URGENCIAS CATETERISMO VESICAL 1. DEFINICION: Es la introducción de una sonda o catéter a la vejiga por el orificio
PAGINA: 1 de 6 REVISADO: COORDINADOR DE CALIDAD ELABORADO: ENFERMERO JEFE COORDINADOR URGENCIAS CATETERISMO VESICAL 1. DEFINICION: Es la introducción de una sonda o catéter a la vejiga por el orificio
TRATAMIENTO Y RECOGIDA DE MUESTRAS EN EL LABORATORIO
 TRATAMIENTO Y RECOGIDA DE MUESTRAS EN EL LABORATORIO GEMA GÓMEZ LAJARA TEL TEL SERVICIO SERVICIO DE DE LABORATORIO LABORATORIO HOSPITAL SANTA BARBARA. PUERTOLLANO. HOSPITAL SANTA BARBARA. PUERTOLLANO.
TRATAMIENTO Y RECOGIDA DE MUESTRAS EN EL LABORATORIO GEMA GÓMEZ LAJARA TEL TEL SERVICIO SERVICIO DE DE LABORATORIO LABORATORIO HOSPITAL SANTA BARBARA. PUERTOLLANO. HOSPITAL SANTA BARBARA. PUERTOLLANO.
PROCEDIMIENTO DE TOMA DE MUESTRAS PARA UROCULTIVO PROLAB S.A.S LABORATORIO CLÍNICO PARA INSTITUCIONES HOSPITALARIAS
 PROCEDIMIENTO DE TOMA DE MUESTRAS PARA UROCULTIVO PROLAB S.A.S LABORATORIO CLÍNICO PARA INSTITUCIONES HOSPITALARIAS Es importante anotar los datos personales y de la historia clínica del paciente, pues
PROCEDIMIENTO DE TOMA DE MUESTRAS PARA UROCULTIVO PROLAB S.A.S LABORATORIO CLÍNICO PARA INSTITUCIONES HOSPITALARIAS Es importante anotar los datos personales y de la historia clínica del paciente, pues
Normas para la Toma de Muestras. Mediante una torunda estéril se procederá de la siguiente forma:
 Anexo 1: Normas para la Toma de Muestras a) Toma de Frotis Faríngeo: - Se realizará un escobillado (frotado) con hisopo preferiblemente de materia sintético (Ej: tipo Dacron), de la faringe, pilares y
Anexo 1: Normas para la Toma de Muestras a) Toma de Frotis Faríngeo: - Se realizará un escobillado (frotado) con hisopo preferiblemente de materia sintético (Ej: tipo Dacron), de la faringe, pilares y
GUÍA PARA RECOGIDA Y TRANSPORTE DE MUESTRAS
 GUÍA PARA RECOGIDA Y TRANSPORTE DE MUESTRAS SECCIÓN DE MICROBIOLOGÍA H. G. U. A REVISIÓN 2012 Supervisora de Microbiología Mª Ángeles Lillo Hernández NORMAS GENERALES PARA RECOGIDA DE MUESTRAS RECOGER
GUÍA PARA RECOGIDA Y TRANSPORTE DE MUESTRAS SECCIÓN DE MICROBIOLOGÍA H. G. U. A REVISIÓN 2012 Supervisora de Microbiología Mª Ángeles Lillo Hernández NORMAS GENERALES PARA RECOGIDA DE MUESTRAS RECOGER
NOMBRE TOMA DE HEMOCULTIVOS Página 1 de 12 ESTADO DOCUMENTAL EL PORTADOR DE ESTA INFORMACION NO ESTA AUTORIZADO A SACAR COPIAS
 NOMBRE TOMA DE HEMOCULTIVOS Página 1 de 12 ESTADO 1. VALIDACION JERARQUIA NOMBRE CARGO FECHA FIRMA ELABORO PATRICIA SABOGAL ENFERMERA VALIDO ALBERTO VALDERRAMA ENFEMERO VIGILANCIA E APROBO DIANA SOTO COORDINACION
NOMBRE TOMA DE HEMOCULTIVOS Página 1 de 12 ESTADO 1. VALIDACION JERARQUIA NOMBRE CARGO FECHA FIRMA ELABORO PATRICIA SABOGAL ENFERMERA VALIDO ALBERTO VALDERRAMA ENFEMERO VIGILANCIA E APROBO DIANA SOTO COORDINACION
La muestra idónea es la primera orina de la mañana, ya que permite la multiplicación de bacterias durante la noche.
 INSTRUCCCIONES PARA LA TOMA DE MUESTRA DE ORINAS Y HECES ORINA 1. ORINA PARCIAL Y UROCULTIVO La muestra idónea es la primera orina de la mañana, ya que permite la multiplicación de bacterias durante la
INSTRUCCCIONES PARA LA TOMA DE MUESTRA DE ORINAS Y HECES ORINA 1. ORINA PARCIAL Y UROCULTIVO La muestra idónea es la primera orina de la mañana, ya que permite la multiplicación de bacterias durante la
PREVENCION DE INFECCIONES ASOCIADAS A CATETER URINARIO PERMANENTE HOSPITAL DR. ERNESTO TORRES GALDAMES IQUIQUE
 PREVENCION DE INFECCIONES ASOCIADAS A CATETER URINARIO HOSPITAL DR. ERNESTO TORRES GALDAMES IQUIQUE 2013 Página: 2 de 12 INDICE INTRODUCCION 3 PROPOSITO 4 OBJETIVO GENERAL 4 ALCANCE 4 RESPONSABLES 4 DESARROLLO
PREVENCION DE INFECCIONES ASOCIADAS A CATETER URINARIO HOSPITAL DR. ERNESTO TORRES GALDAMES IQUIQUE 2013 Página: 2 de 12 INDICE INTRODUCCION 3 PROPOSITO 4 OBJETIVO GENERAL 4 ALCANCE 4 RESPONSABLES 4 DESARROLLO
Toma de muestra, conservación y transporte para estudios microbiológicos Departamento de Microbiología
 , conservación y transporte para estudios microbiológicos Departamento de Microbiología Indice I- INTRODUCCION I 01 II- ORINA A- Urocultivo Instructivo para laboratorio derivante: II 01 Pacientes que controlan
, conservación y transporte para estudios microbiológicos Departamento de Microbiología Indice I- INTRODUCCION I 01 II- ORINA A- Urocultivo Instructivo para laboratorio derivante: II 01 Pacientes que controlan
INSTRUCTIVO PARA TOMA DE MUESTRAS BACTERIOLÓGICAS
 INSTRUCTIVO PARA TOMA DE MUESTRAS BACTERIOLÓGICAS Toda la información diagnóstica que el laboratorio de microbiología puede proporcionar, depende de la calidad de la muestra recibida. Por ello, una toma
INSTRUCTIVO PARA TOMA DE MUESTRAS BACTERIOLÓGICAS Toda la información diagnóstica que el laboratorio de microbiología puede proporcionar, depende de la calidad de la muestra recibida. Por ello, una toma
TOMA DE MUESTRAS MICROBIOLOGICAS. Dra. Dona Benadof Microbiología Hospital Roberto del Río
 TOMA DE MUESTRAS MICROBIOLOGICAS Dra. Dona Benadof Microbiología Hospital Roberto del Río Temario Definiciones Requisitos Procedimientos de toma de muestras Ejemplos INTRODUCCIÓN La confiabilidad de los
TOMA DE MUESTRAS MICROBIOLOGICAS Dra. Dona Benadof Microbiología Hospital Roberto del Río Temario Definiciones Requisitos Procedimientos de toma de muestras Ejemplos INTRODUCCIÓN La confiabilidad de los
HIGIENE EN EL MEDIO HOSPITALARIO
 HIGIENE EN EL MEDIO HOSPITALARIO Código Nombre Categoría SN_0079 HIGIENE EN EL MEDIO HOSPITALARIO SANIDAD Duración 30 HORAS Modalidad ONLINE Audio SI Vídeo SI Objetivos OFRECER AL PERSONAL DEL CENTRO SANITARIO
HIGIENE EN EL MEDIO HOSPITALARIO Código Nombre Categoría SN_0079 HIGIENE EN EL MEDIO HOSPITALARIO SANIDAD Duración 30 HORAS Modalidad ONLINE Audio SI Vídeo SI Objetivos OFRECER AL PERSONAL DEL CENTRO SANITARIO
TOMA DE MUESTRAS MICROBIOLÓGICAS
 TOMA DE MUESTRAS MICROBIOLÓGICAS Fecha de actualización: Abril de 2008 En vigencia desde: Junio de 2008 DIRIGIDO A: Médicos Enfermeras Matronas Tecnólogos Médicos Técnicos Paramédicos OBJETIVOS: Identificar
TOMA DE MUESTRAS MICROBIOLÓGICAS Fecha de actualización: Abril de 2008 En vigencia desde: Junio de 2008 DIRIGIDO A: Médicos Enfermeras Matronas Tecnólogos Médicos Técnicos Paramédicos OBJETIVOS: Identificar
Dirección de Redes en Salud Pública
 Dirección de Redes en Salud Pública Recolección de muestras para el estudio de Microcefalias y otras mal formaciones del SNC posiblemente asociadas a infección por virus Zika 22 de Febrero de 2016 Confirmación
Dirección de Redes en Salud Pública Recolección de muestras para el estudio de Microcefalias y otras mal formaciones del SNC posiblemente asociadas a infección por virus Zika 22 de Febrero de 2016 Confirmación
G estión de. muestras biológicas
 G estión de muestras biológicas Consulte nuestra página web: www.sintesis.com En ella encontrará el catálogo completo y comentado G estión de muestras biológicas Antonio Cisterna Marín Antonio Cisterna
G estión de muestras biológicas Consulte nuestra página web: www.sintesis.com En ella encontrará el catálogo completo y comentado G estión de muestras biológicas Antonio Cisterna Marín Antonio Cisterna
LIMPIEZA Y DESINFECCION
 PAGINA: 1 de 7 1. DEFINICION: Es el procedimiento, mediante el cual son eliminados los diferentes desechos generados en los procesos de recolección y procesamiento de muestras; y además se describe el
PAGINA: 1 de 7 1. DEFINICION: Es el procedimiento, mediante el cual son eliminados los diferentes desechos generados en los procesos de recolección y procesamiento de muestras; y además se describe el
Prevención, Diagnóstico y Tratamiento de la Infección de Vías Urinarias No Complicada en Menores de 18 años en el Primero y Segundo Nivel de Atención
 Guía de Referencia Rápida Prevención, Diagnóstico y Tratamiento de la Infección de Vías Urinarias No Complicada en Menores de 18 años en el Primero y Segundo Nivel de Atención Guía de Referencia Rápida
Guía de Referencia Rápida Prevención, Diagnóstico y Tratamiento de la Infección de Vías Urinarias No Complicada en Menores de 18 años en el Primero y Segundo Nivel de Atención Guía de Referencia Rápida
CONTROL DE CALIDAD PREANALITICO
 CONTROL DE CALIDAD PREANALITICO TOMA DE MUESTRA LAS FASES DE CONTROL DE CALIDAD SON; PREANALITICO ANALITICO POST ANALITICO CONTROL PREANALITICO *SON TODAS LAS ESPECIFICACIONES QUE SE DEBEN CONSIDERAR,
CONTROL DE CALIDAD PREANALITICO TOMA DE MUESTRA LAS FASES DE CONTROL DE CALIDAD SON; PREANALITICO ANALITICO POST ANALITICO CONTROL PREANALITICO *SON TODAS LAS ESPECIFICACIONES QUE SE DEBEN CONSIDERAR,
INDICACIONES PARA LA HIGIENE DE MANOS
 Medicina Preventiva y Salud Pública H.C.U.V. Actualizado 2010 INDICACIONES PARA LA HIGIENE DE MANOS Debe realizarse higiene de las manos por parte del personal sanitario en las siguientes situaciones A.
Medicina Preventiva y Salud Pública H.C.U.V. Actualizado 2010 INDICACIONES PARA LA HIGIENE DE MANOS Debe realizarse higiene de las manos por parte del personal sanitario en las siguientes situaciones A.
CONDICIONES GENERALES PARA TOMA DE MUESTRAS LABORATORIO CLINICO
 EXAMEN CONDICIONES HEMATOLOGIA PRUEBAS DE COAGULACION (PT, PTT, FIBRINOGENO, DIMERO D) No tomar el anticoagulante hasta después de la toma de Informar que anticoagulante está usando. HEMOGRAMA No es necesario
EXAMEN CONDICIONES HEMATOLOGIA PRUEBAS DE COAGULACION (PT, PTT, FIBRINOGENO, DIMERO D) No tomar el anticoagulante hasta después de la toma de Informar que anticoagulante está usando. HEMOGRAMA No es necesario
Obtener una muestra biológica en condiciones óptimas para su proceso analítico de acuerdo al examén solicitado.
 Código: I-CIRB-AADC-02 Revisión: 03 Página: 1 de 7 1.- OBJETIVO Obtener una muestra biológica en condiciones óptimas para su proceso analítico de acuerdo al examén solicitado. 2.- ALCANCE Aplica para la
Código: I-CIRB-AADC-02 Revisión: 03 Página: 1 de 7 1.- OBJETIVO Obtener una muestra biológica en condiciones óptimas para su proceso analítico de acuerdo al examén solicitado. 2.- ALCANCE Aplica para la
Norma/Política Precauciones, estándares y uso adecuado de desinfectantes
 01.00 de / Modificación: 01/00 Fecha de Vigencia: 27/12/13 Responsable de Gestión de la norma/política: Dra. Inés Staneloni/ Int. 8165 Mail: maria.staneloni@hospitalitaliano.org.ar Estándar: PCI.9 Referencias:
01.00 de / Modificación: 01/00 Fecha de Vigencia: 27/12/13 Responsable de Gestión de la norma/política: Dra. Inés Staneloni/ Int. 8165 Mail: maria.staneloni@hospitalitaliano.org.ar Estándar: PCI.9 Referencias:
SONDAS Y CATÉTERES FIJACIÓN DE SONDAS Y CATÉTERES EN NEONATOLOGÍA
 SONDAS Y CATÉTERES FIJACIÓN DE SONDAS Y CATÉTERES EN NEONATOLOGÍA SONDAS Y CATÉTERES CONSIDERACIONES ESPECÍFICAS Permitir la visualización de las sondas Evitar que se obstruya la salida de las sondas y
SONDAS Y CATÉTERES FIJACIÓN DE SONDAS Y CATÉTERES EN NEONATOLOGÍA SONDAS Y CATÉTERES CONSIDERACIONES ESPECÍFICAS Permitir la visualización de las sondas Evitar que se obstruya la salida de las sondas y
UNIDAD DIDÁCTICA III: INFECCIONES ASOCIADAS A LA ATENCIÓN SANITARIA
 UNIDAD DIDÁCTICA III: INFECCIONES ASOCIADAS A LA ATENCIÓN SANITARIA Apartados de información del Unidad Didáctica III De qué estamos hablando cuando decimos infecciones asociadas a la atención sanitaria?
UNIDAD DIDÁCTICA III: INFECCIONES ASOCIADAS A LA ATENCIÓN SANITARIA Apartados de información del Unidad Didáctica III De qué estamos hablando cuando decimos infecciones asociadas a la atención sanitaria?
Secretaría Distrital de Salud de Bogotá, D. C. Dirección de Salud Pública. Manual para la toma de muestras para análisis microbiológico
 Secretaría Distrital de Salud de Bogotá, D. C. Dirección de Salud Pública Manual para la toma de muestras para análisis microbiológico Samuel Moreno Rojas Alcalde Mayor de Bogotá, D. C. Héctor Zambrano
Secretaría Distrital de Salud de Bogotá, D. C. Dirección de Salud Pública Manual para la toma de muestras para análisis microbiológico Samuel Moreno Rojas Alcalde Mayor de Bogotá, D. C. Héctor Zambrano
MANUAL DE TOMA Y TRANSPORTE DE MUESTRAS MICROBIOLÓGICAS
 Hoja: 1 de 90 MANUAL DE TOMA Y DE MUESTRAS MICROBIOLÓGICAS Elaboró: Autorizó: Puesto QUIMICO JEFE DE LABORATORIO Firma Hoja: 2 de 91 Propósito Definir y describir las condiciones óptimas que deben cumplir
Hoja: 1 de 90 MANUAL DE TOMA Y DE MUESTRAS MICROBIOLÓGICAS Elaboró: Autorizó: Puesto QUIMICO JEFE DE LABORATORIO Firma Hoja: 2 de 91 Propósito Definir y describir las condiciones óptimas que deben cumplir
APÉNDICE B. INSTRUCTIVO DE RECOLECCIÓN Y ENVÍO DE MUESTRAS PARA LOS LABORATO- RIOS DE APOYO A VIGILANCIA EPIDEMIOLÓGICA.
 APÉNDICE B. INSTRUCTIVO DE RECOLECCIÓN Y ENVÍO DE MUESTRAS PARA LOS LABORATO- RIOS DE APOYO A VIGILANCIA EPIDEMIOLÓGICA. La selección, la recolección y el transporte apropiados de especimenes al laboratorio
APÉNDICE B. INSTRUCTIVO DE RECOLECCIÓN Y ENVÍO DE MUESTRAS PARA LOS LABORATO- RIOS DE APOYO A VIGILANCIA EPIDEMIOLÓGICA. La selección, la recolección y el transporte apropiados de especimenes al laboratorio
PROCEDIMIENTO HIGIENE BUCAL
 Pág. 1 de 6 REALIZADO por REVISADO por APROBADO por Nombre: Rocío González Nombre: Silvia de León Nombre: Miriam Gorrasi Asistencial Directora Dpto. Educación Nombre: Silvia Esquibel Nombre: Ana Díaz Nombre:
Pág. 1 de 6 REALIZADO por REVISADO por APROBADO por Nombre: Rocío González Nombre: Silvia de León Nombre: Miriam Gorrasi Asistencial Directora Dpto. Educación Nombre: Silvia Esquibel Nombre: Ana Díaz Nombre:
Universidad de Buenos Aires, Facultad de Medicina. Departamento de Microbiología, Parasitología e Inmunología. Cátedra 1 Microbiología II
 Universidad de Buenos Aires, Facultad de Medicina Departamento de Microbiología, Parasitología e Inmunología Cátedra 1 Microbiología II Teórico 1 Diagnóstico Bacteriológico Cristina Cerquetti ccerquetti@yahoo.com.ar
Universidad de Buenos Aires, Facultad de Medicina Departamento de Microbiología, Parasitología e Inmunología Cátedra 1 Microbiología II Teórico 1 Diagnóstico Bacteriológico Cristina Cerquetti ccerquetti@yahoo.com.ar
Catálogo de Agujas y Accesorios de HOLOGIC para procedimientos de Biopsia de mama por Vacío (BAV) ÍNDICE:
 ÍNDICE: FAMILIA ATEC: PAG Procedimiento por Resonancia: 02-12 - AGUJAS - MARCADORES - ACCESORIOS VARIOS 1 FAMILIA ATEC : Procedimiento por Estereotaxia: - AGUJAS - MARCADORES - GUIAS -ACCESORIOS VARIOS
ÍNDICE: FAMILIA ATEC: PAG Procedimiento por Resonancia: 02-12 - AGUJAS - MARCADORES - ACCESORIOS VARIOS 1 FAMILIA ATEC : Procedimiento por Estereotaxia: - AGUJAS - MARCADORES - GUIAS -ACCESORIOS VARIOS
Patología Clínica Forense Bioquímica Citología Hematologia Inmunologia Microbiologia Patología Molecular Microscopia Electrónica
 TOMA DE MUESTRAS EN PATOLOGIA CLINICA FORENSE Alfredo Goytendia Cortez Medico Patologo Clínico Miembro de la Asociación de Patología Forense Miembro de la American Biological Safety Association 18 de Agosto
TOMA DE MUESTRAS EN PATOLOGIA CLINICA FORENSE Alfredo Goytendia Cortez Medico Patologo Clínico Miembro de la Asociación de Patología Forense Miembro de la American Biological Safety Association 18 de Agosto
EL LAVADO GASTRICO EN EL NEONATO
 PROCEDIMIENTOS DE ENFERMERIA EL LAVADO GASTRICO EN EL NEONATO DEFINICION Es un procedimiento que consiste en la introducción de una sonda hueca, multiperforada en su extremo distal, que se llevará hasta
PROCEDIMIENTOS DE ENFERMERIA EL LAVADO GASTRICO EN EL NEONATO DEFINICION Es un procedimiento que consiste en la introducción de una sonda hueca, multiperforada en su extremo distal, que se llevará hasta
PANENDOSCOPIA ORAL. -Siempre que se detecte o se sospeche la presencia de un sangrado en la parte alta del tubo digestivo.
 PANENDOSCOPIA ORAL 1. Qué es una panendoscopia oral? Es un procedimiento que permite explorar el esófago, el estómago y el duodeno y obtener multitud de información con un mínimo de molestias para el paciente.
PANENDOSCOPIA ORAL 1. Qué es una panendoscopia oral? Es un procedimiento que permite explorar el esófago, el estómago y el duodeno y obtener multitud de información con un mínimo de molestias para el paciente.
PROCEDIMIENTO ADMINISTRACIÓN DE MEDICACIÓN INTRAMUSCULAR
 Pág. 1 de 6 REALIZADO por REVISADO por APROBADO por Nombre: Silvia de León Nombre: Beatriz Bagnasco Nombre: Miriam Gorrasi Cargo: Lic.Enf. Esp. Directora Dpto. Educación Nombre: Ana Díaz Nombre: Nancy
Pág. 1 de 6 REALIZADO por REVISADO por APROBADO por Nombre: Silvia de León Nombre: Beatriz Bagnasco Nombre: Miriam Gorrasi Cargo: Lic.Enf. Esp. Directora Dpto. Educación Nombre: Ana Díaz Nombre: Nancy
La excelencia no es una acción, es un hábito Aristóteles
 RECOMENDACIONES PARA LA TOMA DE MUESTRAS EN BACTERIOLOGÍA CLÍNICA. La excelencia no es una acción, es un hábito Aristóteles ÍNDICE 1. HERIDAS SUPERFICIALES Y ABSCESOS ABIERTOS. 2. ABSCESOS CERRADOS. 3.
RECOMENDACIONES PARA LA TOMA DE MUESTRAS EN BACTERIOLOGÍA CLÍNICA. La excelencia no es una acción, es un hábito Aristóteles ÍNDICE 1. HERIDAS SUPERFICIALES Y ABSCESOS ABIERTOS. 2. ABSCESOS CERRADOS. 3.
Obtención de la muestra
 DIAGNÓSTICO MICROBIOLÓGICO DE LA INFECCIÓN RESPIRATORÍA. Obtención de la muestra Montserrat Brugués ETIOPATOGENIA DE LA NEUMONIA NO ASOCIADA A VENTILACIÓN MECANICA MICROASPIRACIÓN Colonización orofarigea
DIAGNÓSTICO MICROBIOLÓGICO DE LA INFECCIÓN RESPIRATORÍA. Obtención de la muestra Montserrat Brugués ETIOPATOGENIA DE LA NEUMONIA NO ASOCIADA A VENTILACIÓN MECANICA MICROASPIRACIÓN Colonización orofarigea
3.- Higiene de manos y Antisepsia cutánea
 Higiene de manos La medida más sencilla y eficaz para reducir la infección asociada a la asistencia sanitaria Transmisión cruzada de microorganismos a través de las manos: Las manos de los profesionales
Higiene de manos La medida más sencilla y eficaz para reducir la infección asociada a la asistencia sanitaria Transmisión cruzada de microorganismos a través de las manos: Las manos de los profesionales
ADECUACIÓN DE MEDICAMENTOS Y TÉCNICA ASÉPTICA
 ADECUACIÓN DE MEDICAMENTOS Y TÉCNICA ASÉPTICA III Encuentro de Egresados Instituto de Educación Pablo Tobón Uribe Sección de Farmacia Clínica Departamento de Servicios Farmacéuticos QF Sergio Andrés Aguirre
ADECUACIÓN DE MEDICAMENTOS Y TÉCNICA ASÉPTICA III Encuentro de Egresados Instituto de Educación Pablo Tobón Uribe Sección de Farmacia Clínica Departamento de Servicios Farmacéuticos QF Sergio Andrés Aguirre
LISTA DE DISPOSITIVOS MÉDICOS ESENCIALE PARA EVENTOS SÍSMICOS
 MINISTERIO DE SALUD PÚBLICA SUBSECRETARIA NACIONAL DE GOBERNANZA DE LA SALUD PÚBLICA DIRECCIÓN NACIONAL DE MEDICAMENTOS Y DISPOSITIVOS MÉDICOS LISTA DE DISPOSITIVOS MÉDICOS ESENCIALE PARA EVENTOS SÍSMICOS
MINISTERIO DE SALUD PÚBLICA SUBSECRETARIA NACIONAL DE GOBERNANZA DE LA SALUD PÚBLICA DIRECCIÓN NACIONAL DE MEDICAMENTOS Y DISPOSITIVOS MÉDICOS LISTA DE DISPOSITIVOS MÉDICOS ESENCIALE PARA EVENTOS SÍSMICOS
114. Señala a continuación, sistemas de eliminación de líquidos: a) Pulmones. b) Vómitos. c) Intestino. d) Todos son sistemas de eliminación.
 1 111. En condiciones normales el cuerpo elimina un volumen de líquido que oscila entre: a) 2400 y 2500 ml. b) 2300 y 2500 ml. c) 2300 y 2600 ml. d) 2400 y 2700 ml. 112. Qué es el balance?: a) Es el resultado
1 111. En condiciones normales el cuerpo elimina un volumen de líquido que oscila entre: a) 2400 y 2500 ml. b) 2300 y 2500 ml. c) 2300 y 2600 ml. d) 2400 y 2700 ml. 112. Qué es el balance?: a) Es el resultado
El Laboratorio en la Vigilancia de Influenza
 El Laboratorio en la Vigilancia de Influenza QBP MANUEL ARROYO ROJAS Laboratorio de Virus Respiratorios del TIPOS DE MUESTRAS Exudado Faríngeo Exudado Nasofaríngeo Aspirado Bronqueoalveolar Suero (pareados)
El Laboratorio en la Vigilancia de Influenza QBP MANUEL ARROYO ROJAS Laboratorio de Virus Respiratorios del TIPOS DE MUESTRAS Exudado Faríngeo Exudado Nasofaríngeo Aspirado Bronqueoalveolar Suero (pareados)
GASTROSTOMIA EN PACIENTES CON E.L.A.
 GASTROSTOMIA EN PACIENTES CON E.L.A. Rosario Jiménez Bautista Enfermera/gestora de casos Unidad de ELA y Patología Neuromuscular Servicio de Neurología qué es una gastrostomía? La gastrostomía consiste
GASTROSTOMIA EN PACIENTES CON E.L.A. Rosario Jiménez Bautista Enfermera/gestora de casos Unidad de ELA y Patología Neuromuscular Servicio de Neurología qué es una gastrostomía? La gastrostomía consiste
Mª Luisa Maroto - DUE Farmacia
 Mª Luisa Maroto - DUE Farmacia CITOSTÁTICOS Sustancias de distinta naturaleza química utilizadas en el tratamiento farmacológico de enfermedades neoplásicas CITOTÓXICOS Medicamentos que pueden ocasionar
Mª Luisa Maroto - DUE Farmacia CITOSTÁTICOS Sustancias de distinta naturaleza química utilizadas en el tratamiento farmacológico de enfermedades neoplásicas CITOTÓXICOS Medicamentos que pueden ocasionar
INTRODUCCION INDICACIONES CONTRAINDICACIONES EQUIPO NECESARIO. Anestesia local.
 Toracocentesis INTRODUCCION El volumen y la complicación de las grandes operaciones toracoabdominales hacen cada vez más frecuente la existencia de derrames pleurales, que interfieren con el buen curso
Toracocentesis INTRODUCCION El volumen y la complicación de las grandes operaciones toracoabdominales hacen cada vez más frecuente la existencia de derrames pleurales, que interfieren con el buen curso
MINISTERIO DE SALUD PÚBLICA Y BIENESTAR SOCIAL INSTITUTO DE MEDICINA TROPICAL
 MANUAL DE RECOLECCIÓN, TRANSPORTE Y CONSERVACIÓN DE MUESTRAS PARA EXÁMENES BACTERIOLÓGICOS MAYO 2.009 2 DOCUMENTO ELABORADO POR: Dr. Juan D. Irala Ledezma REVISADO POR: Dra. Edelira Ayala de Paredes APROBADO
MANUAL DE RECOLECCIÓN, TRANSPORTE Y CONSERVACIÓN DE MUESTRAS PARA EXÁMENES BACTERIOLÓGICOS MAYO 2.009 2 DOCUMENTO ELABORADO POR: Dr. Juan D. Irala Ledezma REVISADO POR: Dra. Edelira Ayala de Paredes APROBADO
*PRECIOS MÁS I.V.A. **CAMBIOS DE PRECIOS SIN PREVIO AVISO
 DESCRIPCIÓN MARCA PRESENTACIÓN PRECIO C/I.V.A. AGUJAS AGUJA HIPODERMICA 20 X 25 BD CAJA CON 100 $ 79.18 $ 91.85 AGUJA HIPODERMICA 20 X 32 BD CAJA CON 100 $ 79.18 $ 91.85 AGUJA HIPODERMICA 21 X 32 BD CAJA
DESCRIPCIÓN MARCA PRESENTACIÓN PRECIO C/I.V.A. AGUJAS AGUJA HIPODERMICA 20 X 25 BD CAJA CON 100 $ 79.18 $ 91.85 AGUJA HIPODERMICA 20 X 32 BD CAJA CON 100 $ 79.18 $ 91.85 AGUJA HIPODERMICA 21 X 32 BD CAJA
Recogida de Muestras en Pediatría
 Recogida de Muestras en Pediatría Sr. Juan Jareño Talero Supervisor de Urgencias Pediátricas del Hospital Son Dureta Palma de Mallorca Muestras de sangre venosa Hemocultivo Sist. BACTEC Bioquímica Hematología
Recogida de Muestras en Pediatría Sr. Juan Jareño Talero Supervisor de Urgencias Pediátricas del Hospital Son Dureta Palma de Mallorca Muestras de sangre venosa Hemocultivo Sist. BACTEC Bioquímica Hematología
Sistema de administración
 Sistema de administración El sistema de alto flujo: El flujo total de gas que suministra el equipo es suficiente para proporcionar la totalidad del gas inspirado Utilizan el mecanismo Venturi para tomar
Sistema de administración El sistema de alto flujo: El flujo total de gas que suministra el equipo es suficiente para proporcionar la totalidad del gas inspirado Utilizan el mecanismo Venturi para tomar
Toma de Muestras Orofaríngeas para la Vigilancia de la Influenza Aviar de Alta Patogenecidad (IAAP) 2010
 Toma de Muestras Orofaríngeas para la Vigilancia de la Influenza Aviar de Alta Patogenecidad (IAAP) 2010 Paso 1: Reunir los materiales necesarios Equipo de protección personal apropiado - además de vestir
Toma de Muestras Orofaríngeas para la Vigilancia de la Influenza Aviar de Alta Patogenecidad (IAAP) 2010 Paso 1: Reunir los materiales necesarios Equipo de protección personal apropiado - además de vestir
ESTUDIO PARASITOLOGICO DE HECES.
 ESTUDIO PARASITOLOGICO DE HECES. DE MUESTRAS. A:PREPARACIÓN 3 DÍAS ANTES DE LA RECOGIDA DE LAS HECES DEBE SUPRIMIRSE: 1. MEDICAMENTOS QUE CONTENGAN CARBÓN VEGETAL, SALES DE BISMUTO, DE MAGNESIO, CAOLÍN,
ESTUDIO PARASITOLOGICO DE HECES. DE MUESTRAS. A:PREPARACIÓN 3 DÍAS ANTES DE LA RECOGIDA DE LAS HECES DEBE SUPRIMIRSE: 1. MEDICAMENTOS QUE CONTENGAN CARBÓN VEGETAL, SALES DE BISMUTO, DE MAGNESIO, CAOLÍN,
RECOMENDACIONES PARA PADRES CON NIÑOS CON TRAQUEOTOMÍA
 RECOMENDACIONES PARA PADRES CON NIÑOS CON TRAQUEOTOMÍA Hospital de Niños R. Gutiérrez Centro Respiratorio Gallo 1330, Ciudad Autónoma de Buenos Aires. TEL. 4963-3224 www.centrorespiratorio.org Qué es una
RECOMENDACIONES PARA PADRES CON NIÑOS CON TRAQUEOTOMÍA Hospital de Niños R. Gutiérrez Centro Respiratorio Gallo 1330, Ciudad Autónoma de Buenos Aires. TEL. 4963-3224 www.centrorespiratorio.org Qué es una
TOMA DE MUESTRA Y PREPARACIÓN PARA ESTUDIOS DIAGNÓSTICOS
 TOMA DE MUESTRA Y PREPARACIÓN PARA ESTUDIOS DIAGNÓSTICOS OBJETIVOS: Conocer diferentes técnicas de toma de muestra Desarrollo de conocimientos ya adquiridos Extracción de la muestra de sangre: Material
TOMA DE MUESTRA Y PREPARACIÓN PARA ESTUDIOS DIAGNÓSTICOS OBJETIVOS: Conocer diferentes técnicas de toma de muestra Desarrollo de conocimientos ya adquiridos Extracción de la muestra de sangre: Material
RED LABORATORIAL DE ENFERMEDADES FEBRILES EXANTEMÁTICAS. Dirección de Medicina Preventiva Dirección de Epidemiología
 RED LABORATORIAL DE ENFERMEDADES FEBRILES EXANTEMÁTICAS Dirección de Medicina Preventiva Dirección de Epidemiología Qué se debe hacer ante un caso sospechoso? Paciente con fiebre y exantema que se sospecha
RED LABORATORIAL DE ENFERMEDADES FEBRILES EXANTEMÁTICAS Dirección de Medicina Preventiva Dirección de Epidemiología Qué se debe hacer ante un caso sospechoso? Paciente con fiebre y exantema que se sospecha
MANEJO DE SOLUCIONES DESINFECTANTES
 PAGINA: 1 de 8 REVISADO: ELABORADO: COORDINADOR DE CALIDAD 1. DEFINICION ENFERMERO JEFE COORDINADOR CIRUGIA Las soluciones desinfectantes son sustancias que actúan sobre los microorganismos inactivándolos
PAGINA: 1 de 8 REVISADO: ELABORADO: COORDINADOR DE CALIDAD 1. DEFINICION ENFERMERO JEFE COORDINADOR CIRUGIA Las soluciones desinfectantes son sustancias que actúan sobre los microorganismos inactivándolos
Catálogo de Agujas y Accesorios de HOLOGIC para procedimientos de Biopsia de mama por Vacío (BAV) ÍNDICE:
 ÍNDICE: FAMILIA ATEC: PAG Procedimiento por Ecografía: 02-15 - AGUJAS - MARCADORES - ACCESORIOS VARIOS 1 FAMILIA ATEC : Procedimiento por Estereotaxia: - AGUJAS - MARCADORES - GUIAS -ACCESORIOS VARIOS
ÍNDICE: FAMILIA ATEC: PAG Procedimiento por Ecografía: 02-15 - AGUJAS - MARCADORES - ACCESORIOS VARIOS 1 FAMILIA ATEC : Procedimiento por Estereotaxia: - AGUJAS - MARCADORES - GUIAS -ACCESORIOS VARIOS
PROCEDIMIENTO ADMINISTRACIÓN DE MEDICACIÓN POR VÍA SUBCUTÁNEA
 Pág. 1 de 6 REALIZADO por REVISADO por APROBADO por Nombre: Ana Díaz Nombre: Beatriz Bagnasco Nombre: Miriam Gorrasi Cargo:Lic.Enf.Esp. Directora Dpto. Educación Nombre: Silvia de León Nombre: Nancy Fernández
Pág. 1 de 6 REALIZADO por REVISADO por APROBADO por Nombre: Ana Díaz Nombre: Beatriz Bagnasco Nombre: Miriam Gorrasi Cargo:Lic.Enf.Esp. Directora Dpto. Educación Nombre: Silvia de León Nombre: Nancy Fernández
TEMA 8. Selección, recolección y transporte de muestras para examen microbiológico
 TEMA 8 Selección, recolección y transporte de muestras para examen microbiológico Tema 8. Selección, recolección y transporte de muestras para examen microbiológico. 1. Consideraciones generales para la
TEMA 8 Selección, recolección y transporte de muestras para examen microbiológico Tema 8. Selección, recolección y transporte de muestras para examen microbiológico. 1. Consideraciones generales para la
PMD: CARLOS ANDRES SAMBONI PMD: CARLOS ANDRES SAMBONI
 PMD: CARLOS ANDRES SAMBONI PMD: CARLOS ANDRES SAMBONI PRINCIPIO UNIVERSAL DE BIOSEGURIDAD TODOS LOS PACIENTES Y SUS FLUIDOS CORPORALES INDEPENDIENTEMENTE DEL DIAGNOSTICO O MOTIVO DE INGRESO, DEBERAN SER
PMD: CARLOS ANDRES SAMBONI PMD: CARLOS ANDRES SAMBONI PRINCIPIO UNIVERSAL DE BIOSEGURIDAD TODOS LOS PACIENTES Y SUS FLUIDOS CORPORALES INDEPENDIENTEMENTE DEL DIAGNOSTICO O MOTIVO DE INGRESO, DEBERAN SER
Fase preanalítica. Porcentaje de participacion de cada una de las fases en el flujo de trabajo
 Fase preanalítica Porcentaje de participacion de cada una de las fases en el flujo de trabajo Variaciones preanalíticas Cualquier factor fisiológico, técnico o de procedimiento que puede afectar la concentración
Fase preanalítica Porcentaje de participacion de cada una de las fases en el flujo de trabajo Variaciones preanalíticas Cualquier factor fisiológico, técnico o de procedimiento que puede afectar la concentración
ENOXPRIM. Solución inyectable. Solución inyectable estéril, libre de pirógenos, contenida en jeringas pre-llenadas listas para usarse.
 ENOXPRIM Solución inyectable ENOXAPARINA FORMA FARMACÉUTICA Y FORMULACIÓN Cada jeringa contiene: Enoxaparina sódica 20 mg 40 mg Equivalente a 2,000 U.I. 4,000 U.I. Agua inyectable, c.b.p. 0.2 ml 0.4 ml
ENOXPRIM Solución inyectable ENOXAPARINA FORMA FARMACÉUTICA Y FORMULACIÓN Cada jeringa contiene: Enoxaparina sódica 20 mg 40 mg Equivalente a 2,000 U.I. 4,000 U.I. Agua inyectable, c.b.p. 0.2 ml 0.4 ml
CUIDADOS DE HERIDAS QUIRÚRGICAS
 DIRECCION DE CUIDADOS DE HERIDAS QUIRÚRGICAS AUTORES Ultima actualización Alba Mª Álvarez González Enero 2011 REVISORES Comisión Cuidados Enfermería Mayo 2012 AUTORIZADO Dirección de Enfermería Mayo 2012
DIRECCION DE CUIDADOS DE HERIDAS QUIRÚRGICAS AUTORES Ultima actualización Alba Mª Álvarez González Enero 2011 REVISORES Comisión Cuidados Enfermería Mayo 2012 AUTORIZADO Dirección de Enfermería Mayo 2012
HOSPITAL GENERAL REGIONAL IZTAPALAPA CLÍNICA DE CATÉTERES
 HOSPITAL GENERAL REGIONAL IZTAPALAPA CLÍNICA DE CATÉTERES El Gobierno del Distrito Federal a través de la Secretaria de Salud DF pone en marcha simultáneamente el 21 de Septiembre del 2011, las Clínicas
HOSPITAL GENERAL REGIONAL IZTAPALAPA CLÍNICA DE CATÉTERES El Gobierno del Distrito Federal a través de la Secretaria de Salud DF pone en marcha simultáneamente el 21 de Septiembre del 2011, las Clínicas
AISLAMIENTO UNIVERSAL
 AISLAMIENTO UNIVERSAL OBJETIVO: Llevar a cabo las medidas de protección que deben observarse de forma sistemática y generalizada en el ámbito hospitalario. 1 EQUIPAMIENTO NECESARIO: Jabón antiséptico y
AISLAMIENTO UNIVERSAL OBJETIVO: Llevar a cabo las medidas de protección que deben observarse de forma sistemática y generalizada en el ámbito hospitalario. 1 EQUIPAMIENTO NECESARIO: Jabón antiséptico y
EQUIPO NECESARIO I NTRODUCCION INDICACIONES CONTRAINDICACIONES
 09 I NTRODUCCION Las muestras para estudio de gases, de pruebas funcionales respiratorias y otras pruebas de seguimiento de la monitorización de un enfermo con problemas respiratorios, requieren ser tomadas
09 I NTRODUCCION Las muestras para estudio de gases, de pruebas funcionales respiratorias y otras pruebas de seguimiento de la monitorización de un enfermo con problemas respiratorios, requieren ser tomadas
Manual Envío de Muestras Human PCR Kit
 Manual Human PCR Kit a) Sangre total. Medio de Tubo con EDTA como anticoagulante. (tapa morada) Máximo 24 horas a partir de la recolección (temperatura ambiente).. No se debe utilizar heparina como anticoagulante
Manual Human PCR Kit a) Sangre total. Medio de Tubo con EDTA como anticoagulante. (tapa morada) Máximo 24 horas a partir de la recolección (temperatura ambiente).. No se debe utilizar heparina como anticoagulante
UNIVERSIDAD JUÁREZ DEL ESTADO DE DURANGO FACULTAD DE MEDICINA Y NUTRICIÓN Unidad Médica de Simulación Clínica "Dr. José Jorge Talamas Márquez"
 LICENCIATURA EN NUTRICIÓN Practica #10 TOMA DE MUESTRA DE GLUCOSA CAPILAR OBJETIVOS: Al concluir la práctica el alumno será capaz de: 1. Definir y conocer la técnica de toma de muestra de glucosa capilar
LICENCIATURA EN NUTRICIÓN Practica #10 TOMA DE MUESTRA DE GLUCOSA CAPILAR OBJETIVOS: Al concluir la práctica el alumno será capaz de: 1. Definir y conocer la técnica de toma de muestra de glucosa capilar
UNIVERSIDAD NACIONAL DEL NORDESTE Facultad de Ciencias Exactas y Naturales y Agrimensura Departamento de Biología - Área Zoología EMBRIOLOGÍA ANIMAL
 UNIVERSIDAD NACIONAL DEL NORDESTE Facultad de Ciencias Exactas y Naturales y Agrimensura Departamento de Biología - Área Zoología EMBRIOLOGÍA ANIMAL PROTOCOLO PARA OBTENCIÓN DE EMBRIONES DE POLLO EN LABORATORIO
UNIVERSIDAD NACIONAL DEL NORDESTE Facultad de Ciencias Exactas y Naturales y Agrimensura Departamento de Biología - Área Zoología EMBRIOLOGÍA ANIMAL PROTOCOLO PARA OBTENCIÓN DE EMBRIONES DE POLLO EN LABORATORIO
LISTA DE INSUMOS ADHESIVOS AGUJAS
 Camino Real de Betamia, frente a la Farmacia Metro, Ciudad de Panamá, Republica de Panamá e- mail: rapidmedicalsupply@gmail.com / ventas@rapidmedicalsupply.net / Tel: 399-7718 R.U.C. 8-741- 1841 D.V. 05
Camino Real de Betamia, frente a la Farmacia Metro, Ciudad de Panamá, Republica de Panamá e- mail: rapidmedicalsupply@gmail.com / ventas@rapidmedicalsupply.net / Tel: 399-7718 R.U.C. 8-741- 1841 D.V. 05
GUIA Nº2: POSTURA DE GUANTES DE PROCEDIMIENTO Y ESTERILES
 FACULTAD DE ENFERMERÍA ASIGNATURA: CUIDADOS DE ENFERMERÍA EN EL CICLO VITAL I (ENFE-6013) CREADO EQUIPO DOCENTE PAE 1 (2010) ACTUALIZADO EQUIPO DOCENTE CICLO VITAL I (2012-1) TALLER Nº 1 GUIA Nº2: POSTURA
FACULTAD DE ENFERMERÍA ASIGNATURA: CUIDADOS DE ENFERMERÍA EN EL CICLO VITAL I (ENFE-6013) CREADO EQUIPO DOCENTE PAE 1 (2010) ACTUALIZADO EQUIPO DOCENTE CICLO VITAL I (2012-1) TALLER Nº 1 GUIA Nº2: POSTURA
Unidad de Endoscopias Servicio de Digestivo RECOMENDACIONES DE ENFERMERÍA DESPUÉS DE LA GASTROSTOMÍA PERCUTÁNEA
 Unidad de Endoscopias Servicio de Digestivo RECOMENDACIONES DE ENFERMERÍA DESPUÉS DE LA GASTROSTOMÍA PERCUTÁNEA La colocación de una sonda por gastrostomía endoscópica percutánea (PEG) está indicada para
Unidad de Endoscopias Servicio de Digestivo RECOMENDACIONES DE ENFERMERÍA DESPUÉS DE LA GASTROSTOMÍA PERCUTÁNEA La colocación de una sonda por gastrostomía endoscópica percutánea (PEG) está indicada para
2. Precauciones de Rutina para el Control de Infecciones de Enfermedades Respiratorias
 2. PRECAUCIONES DE RUTINA PARA EL CONTROL DE INFECCIONES DE ENFERMEDADES RESPIRATORIAS 2. Precauciones de Rutina para el Control de Infecciones de Enfermedades Respiratorias Precauciones estándar Las precauciones
2. PRECAUCIONES DE RUTINA PARA EL CONTROL DE INFECCIONES DE ENFERMEDADES RESPIRATORIAS 2. Precauciones de Rutina para el Control de Infecciones de Enfermedades Respiratorias Precauciones estándar Las precauciones
Cuánto tiempo tendrá que estar aislado el paciente debido a la presencia de piojos?
 Cuánto tiempo tendrá que estar aislado el paciente debido a la presencia de piojos? a. Desde el momento de observarse 10 días ya que su ciclo de reproducción termina. Incorrecta b. Se mantendrá aislado
Cuánto tiempo tendrá que estar aislado el paciente debido a la presencia de piojos? a. Desde el momento de observarse 10 días ya que su ciclo de reproducción termina. Incorrecta b. Se mantendrá aislado
50 kits de recolección de muestras con torunda multitest Aptima (N.º de catálogo PRD-03546) Cada kit contiene:
 Uso previsto El kit de recolección de muestras con torunda se utiliza con los ensayos Aptima. El kit de recolección de muestras con torunda multitest Aptima se utiliza para que médico y paciente puedan
Uso previsto El kit de recolección de muestras con torunda se utiliza con los ensayos Aptima. El kit de recolección de muestras con torunda multitest Aptima se utiliza para que médico y paciente puedan
AUXILIAR ENFERMERÍA. Test 1- Tema 1 NORMATIVA GENERAL. Tema 2 NORMATIVA GENERAL El Estatuto de Autonomía de la Comunidad Valenciana
 AUXILIAR ENFERMERÍA SESIÓN CONTENIDO DE LA SESIÓN 1 Tema 1 NORMATIVA GENERAL La Constitución Española de 1978: estructura y contenido. Derechos y deberes fundamentales Test 1- Tema 1 NORMATIVA GENERAL
AUXILIAR ENFERMERÍA SESIÓN CONTENIDO DE LA SESIÓN 1 Tema 1 NORMATIVA GENERAL La Constitución Española de 1978: estructura y contenido. Derechos y deberes fundamentales Test 1- Tema 1 NORMATIVA GENERAL
MANUAL DE PROCEDIMIENTOS PUNCION ARTERIAL EN PACIENTES AULA DE SIMULACION USAL
 MANUAL DE PROCEDIMIENTOS PUNCION ARTERIAL EN PACIENTES AULA DE SIMULACION USAL aulasimulacion@usal.edu.ar JUSTIFICACIÓN Los instructores del Laboratorio de Simulación de la USAL hemos elaborado el presente
MANUAL DE PROCEDIMIENTOS PUNCION ARTERIAL EN PACIENTES AULA DE SIMULACION USAL aulasimulacion@usal.edu.ar JUSTIFICACIÓN Los instructores del Laboratorio de Simulación de la USAL hemos elaborado el presente
MANUAL DE PROCEDIMIENTOS PUNCION PLEURAL O TORACOCENTESIS EN PACIENTES AULA DE SIMULACION USAL
 MANUAL DE PROCEDIMIENTOS PUNCION PLEURAL O TORACOCENTESIS EN PACIENTES AULA DE SIMULACION USAL aulasimulacion@usal.edu.ar JUSTIFICACIÓN Los instructores del Laboratorio de Simulación de la USAL hemos elaborado
MANUAL DE PROCEDIMIENTOS PUNCION PLEURAL O TORACOCENTESIS EN PACIENTES AULA DE SIMULACION USAL aulasimulacion@usal.edu.ar JUSTIFICACIÓN Los instructores del Laboratorio de Simulación de la USAL hemos elaborado
Protocolo de toma de muestra arterial MANUAL DE CALIDAD LABORATORIO CLÍNICO. PRO 08 D Ed 01 Protocolo extracción arterial
 MANUAL DE CALIDAD LABORATORIO CLÍNICO Protocolo de toma de muestra arterial Código Fecha emisión/última revisión Revisado Aprobado PRO 08 D Ed 01 18/11/09 Spsor. Rafael Infantes Viano Dr. Vidal Pérez Valero.
MANUAL DE CALIDAD LABORATORIO CLÍNICO Protocolo de toma de muestra arterial Código Fecha emisión/última revisión Revisado Aprobado PRO 08 D Ed 01 18/11/09 Spsor. Rafael Infantes Viano Dr. Vidal Pérez Valero.
Centro Universitario de Salud Alfonso López Administración de Medicamentos
 Código: PM-IS-8.218-PT-9 Versión:1 Fecha de actualización:04-09-2015 1 de 14 1. PROCESO/SUBPROCESO RELACIONADO: Gestión de la Interacción Social/Gestión de Servicios a la Comunidad. 2. RESPONSABLE(S):
Código: PM-IS-8.218-PT-9 Versión:1 Fecha de actualización:04-09-2015 1 de 14 1. PROCESO/SUBPROCESO RELACIONADO: Gestión de la Interacción Social/Gestión de Servicios a la Comunidad. 2. RESPONSABLE(S):
INSTITUTO DE EDUCACIÓN SUPERIOR TECNOLÓGICO PRIVADO SANTA ROSA DE LIMA ENFERMERÍA Y VÍAS DE ADMINISTRACIÓN DE LAS VACUNAS
 INSTITUTO DE EDUCACIÓN SUPERIOR TECNOLÓGICO PRIVADO SANTA ROSA DE LIMA ENFERMERÍA Y VÍAS DE ADMINISTRACIÓN DE LAS VACUNAS LIC. JUDITH ISABEL POLO NICHO 1. PUNTOS CLAVE: Las vacunas deben administrarse
INSTITUTO DE EDUCACIÓN SUPERIOR TECNOLÓGICO PRIVADO SANTA ROSA DE LIMA ENFERMERÍA Y VÍAS DE ADMINISTRACIÓN DE LAS VACUNAS LIC. JUDITH ISABEL POLO NICHO 1. PUNTOS CLAVE: Las vacunas deben administrarse
PROCEDIMIENTO PARA LA EXTRACCIÓN DE HEMOCULTIVOS EN EL SERVICIO DE URGENCIAS
 Página 1 de 5 PROCEDIMIENTO PARA LA EXTRACCIÓN DE HEMOCULTIVOS EN EL SERVICIO DE URGENCIAS Página 2 de 5 TOMA DE MUESTRA PARA HEMOCULTIVOS DESCRIPCIÓN Es la obtención de muestra de sangre para cultivo
Página 1 de 5 PROCEDIMIENTO PARA LA EXTRACCIÓN DE HEMOCULTIVOS EN EL SERVICIO DE URGENCIAS Página 2 de 5 TOMA DE MUESTRA PARA HEMOCULTIVOS DESCRIPCIÓN Es la obtención de muestra de sangre para cultivo
Catálogo de Productos. Soluciones. Innovadoras. Para la Sala de Operaciones
 Catálogo de Productos Soluciones Innovadoras Para la Sala de Operaciones Ministerio de Salud Sabia usted que. En Chile se notifican alrededor de 70.000 IIH anuales y se estima que cada IIH prolonga en
Catálogo de Productos Soluciones Innovadoras Para la Sala de Operaciones Ministerio de Salud Sabia usted que. En Chile se notifican alrededor de 70.000 IIH anuales y se estima que cada IIH prolonga en
Manual Toma de Muestras Microbiología.
 Microbiología. Elaborado por: Revisado por: Aprobado por: TM. M. Elena Díaz F. Dr. Sonia Correa Dr. Adriana Pinto T. TM. Maximiliano Ramírez A. BQ. Rodrigo González. TM. Antonio Sanaguas I. Fecha: 01/08/2011
Microbiología. Elaborado por: Revisado por: Aprobado por: TM. M. Elena Díaz F. Dr. Sonia Correa Dr. Adriana Pinto T. TM. Maximiliano Ramírez A. BQ. Rodrigo González. TM. Antonio Sanaguas I. Fecha: 01/08/2011
Toma de Muestras Microbiológicas aseguramiento de calidad
 Toma de Muestras Microbiológicas aseguramiento de calidad T.M. Carlos Ivovic O Profesor de Microbiología Clínica Facultad de Ciencias Médicas Universidad Pedro de Valdivia Objetivos de la toma de muestras
Toma de Muestras Microbiológicas aseguramiento de calidad T.M. Carlos Ivovic O Profesor de Microbiología Clínica Facultad de Ciencias Médicas Universidad Pedro de Valdivia Objetivos de la toma de muestras
REPARACION LAPAROSCÓPICA HERNIA VENTRAL
 REPARACION LAPAROSCÓPICA HERNIA VENTRAL En la actualidad cada vez se realizan con mayor frecuencia las reparaciones de las hernias ventrales (eventraciones) por vía laparoscópica, sobre todo aquellas que
REPARACION LAPAROSCÓPICA HERNIA VENTRAL En la actualidad cada vez se realizan con mayor frecuencia las reparaciones de las hernias ventrales (eventraciones) por vía laparoscópica, sobre todo aquellas que
SISTEMA DE GESTIÓN AMBIENTAL
 1. PROPÓSITO Contar con un instrumento que especifique los lineamientos y tareas que se deben aplicar en la Universidad para el desarrollo de los trabajos de separación y manejo correcto de Residuos Peligrosos
1. PROPÓSITO Contar con un instrumento que especifique los lineamientos y tareas que se deben aplicar en la Universidad para el desarrollo de los trabajos de separación y manejo correcto de Residuos Peligrosos
LISTADO DE PRECIOS TECHO PARA SEGUNDA OFERTA ECONOMICA INVITACION A COTIZAR
 1 AGUJA DESECHABLE 18 G X1 1/2 0220006 $ 67,28 2 AGUJA DESECHABLE 21 G X 1 1/2 02200001 $ 82,36 3 AGUJA DESECHABLE 23 G X 1 0220005 $ 69,60 4 ALCOHOL ANTISEPTICO X 700 ML 0210008 $ 2.370,00 5 ALCOHOL GLICERINADO
1 AGUJA DESECHABLE 18 G X1 1/2 0220006 $ 67,28 2 AGUJA DESECHABLE 21 G X 1 1/2 02200001 $ 82,36 3 AGUJA DESECHABLE 23 G X 1 0220005 $ 69,60 4 ALCOHOL ANTISEPTICO X 700 ML 0210008 $ 2.370,00 5 ALCOHOL GLICERINADO
INFECCION QUIRURGICA Factores modificables. Medidas intraoperatorias y postoperatorias.
 INFECCION QUIRURGICA Factores modificables. Medidas intraoperatorias y postoperatorias. Montserrat Marcos Sáiz. Enfermera de Quirófano. Hospital de Terrassa Preparación n del paciente antes de la intervención.
INFECCION QUIRURGICA Factores modificables. Medidas intraoperatorias y postoperatorias. Montserrat Marcos Sáiz. Enfermera de Quirófano. Hospital de Terrassa Preparación n del paciente antes de la intervención.
Cuidados preventivos al niño o en diálisis
 5º Congreso Argentino de Nefrología a Pediátrica 3º Jornadas de Enfermería a y de Técnicos T de Nefrología a Pediátrica 21 al 23 de Junio de 2012 Buenos Aires, Argentina Conferencia Cuidados preventivos
5º Congreso Argentino de Nefrología a Pediátrica 3º Jornadas de Enfermería a y de Técnicos T de Nefrología a Pediátrica 21 al 23 de Junio de 2012 Buenos Aires, Argentina Conferencia Cuidados preventivos
CATETER VENOSO CENTRAL
 CATETER VENOSO CENTRAL Definición.- se define como la inserción de un catéter biocompatible en el espacio intravascular, central o periférico, con el fin de administrar soluciones, medicamentos, nutrición
CATETER VENOSO CENTRAL Definición.- se define como la inserción de un catéter biocompatible en el espacio intravascular, central o periférico, con el fin de administrar soluciones, medicamentos, nutrición
TOMA DE MUESTRAS DE HECES PARA COPROCULTIVO. Se debe efectuar la toma antes de comenzar tratamiento antibiótico.
 NORMAS GENERALES PARA LA RECOLECCIÓN DE MUESTRAS CLÍNICAS Las muestras deben ser tomadas: 1.- Antes de la administración de antibióticos, siempre que sea posible. 2.- Del lugar de la infección, evitando
NORMAS GENERALES PARA LA RECOLECCIÓN DE MUESTRAS CLÍNICAS Las muestras deben ser tomadas: 1.- Antes de la administración de antibióticos, siempre que sea posible. 2.- Del lugar de la infección, evitando
DIAGNÓSTICO MOLECULAR CMV Y EBV
 DIAGNÓSTICO MOLECULAR CMV Y EBV DIAGNÓSTICO MOLECULAR REACCIÓN EN CADENA DE LA POLIMERASA (PCR) ALTA SENSIBILIDAD Y ESPECIFICIDAD DIAGNÓSTICO MOLECULAR REACCIÓN EN CADENA DE LA POLIMERASA (PCR) PCR PUNTO
DIAGNÓSTICO MOLECULAR CMV Y EBV DIAGNÓSTICO MOLECULAR REACCIÓN EN CADENA DE LA POLIMERASA (PCR) ALTA SENSIBILIDAD Y ESPECIFICIDAD DIAGNÓSTICO MOLECULAR REACCIÓN EN CADENA DE LA POLIMERASA (PCR) PCR PUNTO
Conservar según el tipo de muestra hasta proceder a su envío al laboratorio.
 Lunes a viernes 9:30 20 h/ Sábado 9:00 13:30 h Tlf: laboratoriosgasset@grupodavsalud.es www.grupodavsalud.es Envío de muestras La hoja de petición del laboratorio debe de cumplimentarse indicando las pruebas
Lunes a viernes 9:30 20 h/ Sábado 9:00 13:30 h Tlf: laboratoriosgasset@grupodavsalud.es www.grupodavsalud.es Envío de muestras La hoja de petición del laboratorio debe de cumplimentarse indicando las pruebas
