PRÁCTICAS DE GENÉTICA Y BIOTECNOLOGÍA AMBIENTAL
|
|
|
- Celia Silva Segura
- hace 6 años
- Vistas:
Transcripción
1 PRÁCTICAS DE GENÉTICA Y BIOTECNOLOGÍA AMBIENTAL Cuaderno del alumno Universidad Rey Juan Carlos. Escuela Superior de Ciencias Experimentales y Tecnología.
2 Prácticas de Genética y BTA Prácticas de Genética y Biotecnología Ambiental. 3 er Curso de CC. Ambientales. NORMAS GENERALES 1. El uso de la bata es obligatorio. 2. Está absolutamente prohibido fumar o comer en el laboratorio. 3. Está absolutamente prohibido pipetear con la boca. 4. Leer cuidadosamente el guión que corresponda antes del comienzo de cada práctica. 5. Las prácticas serán evaluadas mediante examen al final de las mismas. 6. Mantener limpio el puesto de trabajo durante el desarrollo de las prácticas, y una vez acabadas limpiarlo completamente
3 PROGRAMA A DESARROLLAR Sesión I. -Introducción a las técnicas bioquímicas y microbiológicas utilizadas en estas prácticas. -Transformación de bacterias de E. coli con DNA plasmídico y siembra en un medio sólido selectivo (Protocolo 1). Sesión II. -Comprobación de la aparición de colonias de bacterias resistentes en la placa de antibiótico (eficacia de la transformación). Siembra de una colonia en medio líquido selectivo. -Mutagénesis producida por irradiación ultravioleta. El sistema de reparación del ADN (Protocolo 2). Sesión III. -Seguimiento del efecto de la irradiación con UV de las placas de colonia de bacterias mutantes carentes del sistema de reparación de ADN, y de bacterias de una cepa salvaje. -Purificación del ADN plasmídico contenido en las bacterias transformadas (Protocolo 3). Sesión IV. -Incubación del plásmido obtenido con enzimas de restricción (Protocolo 4). -Separación del plásmido en forma de ADN circular, o cortado con enzimas de restricción, mediante electroforesis en gel de agarosa (Protocolo 5). -Discusión general sobre los resultados obtenidos a lo largo de las prácticas. 2
4 SESION I. TRANSFORMACION DE BACTERIAS CON DNA PLASMIDICO Y SELECCION DE CLONES QUE HAN INCORPORADO EL PLASMIDO RECOMBINANTE. Introducción. El proceso por el cual un vector plasmídico es introducido y mantenido de forma estable en una bacteria se denomina transformación. En la bacteria Escherichia coli este proceso no ocurre de forma natural y ha de inducirse en el laboratorio. Para facilitar este proceso, se tratan las bacterias con calcio incubando en frío (a unos 4º C) lo cual estimula la apertura de poros que facilitan la entrada de DNA exógeno. A estas bacterias susceptibles de incorporar DNA exógeno las denominamos bacterias competentes. El vector plasmídico que usaremos en el ensayo de transformación será el plámido pbluescript (denominado de forma abreviada pbl). La introducción de DNA exógeno en las bacterias competentes es un proceso muy ineficaz, y por ello es necesario utilizar un método que nos permita identificar al reducido número de bacterias que han incorporado y mantenido de forma estable el plásmido con el que las hemos transformado. Con este objetivo a los plásmidos se les ha dotado de un sistema de selección, que en el caso de pbl consiste en un gen de resistencia a ampicilina. Este gen confiere a las bacterias transformadas con el plásmido un fenotipo fácilmente diferenciable: sólo las bacterias que han incorporado 3
5 el plásmido serán capaces de crecer en presencia del antibiótico ampicilina cuando son sembradas en una placa petri conteniendo medio de cultivo con el mencionado antibiótico. Figura 1. Esquema del vector plasmídico p Bluescript II sk (-) donde aparecen indicados su origen de replicación (puc ori), el gen que confiere a la bacteria resistencia a la ampicilina (ampicillin), el origen de replicación del bacteriófago filamentoso f1 (f1 (-) ori) el promotor del gen lac (P lac), el gen lacz que codigica para la b-galactosidasa (lacz) Y el sitio de clonaje múltiple (MCS), que aparece descrito con mayor detalle debajo del esquema del vector. 4
6 PROCEDIMIENTO EXPERIMENTAL. A) MEDIOS Y SOLUCIONES Medio de cultivo LB: Extracto de levadura, 5 g; Bactotriptona, 10 g; ClNa, 10 g; H2O hasta 1 l; NaOH, ajustar a ph 6,1 Buffer de transformación y almacenamiento (TSB): medio de cultivo LB a ph 6.1, conteniendo un 10% de polietilen glicol (PEG), 5% de dimetilsulfóxido (DMSO) y 20 mm de Mg++ (10 mm de MgCl mm de MgSO 4 ). Buffer TSB-glucosa: Buffer TSB conteniendo glucosa 20 mm Tris-EDTA (TE): Tris (base) 10 mm; EDTA-Na2, 1 mm; ClH, ajustar a ph 8,0. Tampón de muestras: glicerol 80 ml, 27 %; azul de bromofenol 0,25 g, 0,08 %; H2O hasta 300 ml. Tampón de electroforesis Tris-Borato-EDTA o (TBE): Tris base 10,8 g; ácido bórico 5,5 g; EDTA 0,5 M ph 8.0, 4 ml; H2O hasta 1 litro. B) PRECAUCIONES GENERALES Manipulación de material y soluciones estériles: Las asas de siembra, las puntas de micropipeta, las placas de agar, las soluciones de IPTG y X- Gal, y el medio de cultivo LB deben mantenerse estériles. Mantener abiertos los tubos y placas solo el tiempo mínimo imprescindible. No tocar con los dedos ni con ningún otro material presuntamente contaminado (mesa, etc.) las puntas de micropipeta. Manipulación de bacterias competentes: El tubo que contiene las bacterias competentes debe mantenerse en hielo en todo momento, excepto para el choque térmico a 42 C y la incubación a 37 C. Las bacterias competentes tienen una resistencia mecánica menor que las normales: no agitar con fuerza. Manipulación de compuestos químicos: El Bromuro de Etidio es una sustancia mutagénica, por lo que es absolutamente imprescindible el utilizar guantes cuando se hagan los geles de agarosa. No tocar nunca los geles directamente con las manos sin proteger. 5
7 PROTOCOLO 1. Transformación de bacterias competentes con DNA de plásmidos. 1. Marcar una identificacion del grupo de trabajo en el tubo de bacterias competentes. 2. Pipetear 2 µl (25 ng) de la solución de DNA plasmídico con micropipeta de 20 µl en el tubo de las bacterias competentes. Mezclar lentamente y con cuidado (las bacterias competentes son muy frágiles). Poner el tubo en hielo durante 15 minutos. 3. Marcar la placa de LB/agar + ampicilina con identificación del grupo, el día de la semana y la fecha. 4. Transcurridos los 15 minutos de incubación en hielo, poner el tubo de bacterias competentes en un baño de agua a 42 C durante 2 minutos. 5. Introducir inmediatamente el tubo con bacterias competentes en el recipiente que contiene el hielo. 6. Pipetear 900 µl de buffer TSB-glucosa -precalentado a 37 C- con una micropipeta de 1 ml y añadir los 900 µl al tubo de bacterias transformadas. Cerrar el tubo y mezclar invirtiéndolo con cuidado. Incubar el tubo en un baño de agua a 37 C durante 30 minutos. 7. Sumergir el asa de siembra en etanol y secar al aire. Mezclar por inversión el cultivo contenido en el tubo de bacterias competentes (las bacterias E. coli no son móviles y tienden a sedimentar en cultivos no mantenidos en agitación). 8. Pipetear 100 µl del cultivo sobre la superficie de agar de la placa de LB/agar + ampicilina. Con el asa de siembra, extender los 100 µl sobre toda la superficie de agar. 9. Poner la placa boca abajo en la estufa incubadora a 37 C. Las placas se dejarán incubando a 37 C durante toda la noche. Al día siguiente se comprueba si en la placa han crecido colonias. Si la siembra de las bacterias sobre la superficie de la placa se realizó el día anterior de manera homogénea, las colonias crecidas mostrarán una distribución uniforme sobre toda la superficie de la placa. 6
8 Sesión I: Observaciones y comentarios. 7
9 SESION II ACCION MUTAGENICA DE LA RADIACION ULTRAVIOLETA. La acción mutagénica de la radiación utltravioleta se debe a que este agente físico induce la formación de dímeros de timina en la secuencia del ADN. Los organismos disponen de mecanismos de reparación del ADN, que eliminan tales dímeros e impiden que este fenómeno produzca graves alteraciones en la estructura y función del ADN. Sin embargo es éste actualmente un tema de gran interés ambiental, por cuanto es sabido que la capa de ozono que rodea la Tierra ha disminuido, provocando un aumento en la magnitud de la radiación UV que alcanza la superficie terrestre; paralelamente, se ha observado un aumento en la incidencia de cánceres de piel y de ojo. -BACTERIAS SENSIBLES A LA RADIACIÓN ULTRAVIOLETA. En esta práctica se trata de analizar la sensibilidad de diferentes cepas de la bacteria Escherichia coli a la luz UV. Disponemos de dos cepas de tipo silvestre (E. coli OV2 y E. coli MC1061) que posee los mecanismos normales de reparación de DNA de esta bacteria y que es, por ello, resistentes a la acción de la luz ultravioleta. Además, disponemos de cepas derivada de las anteriores (E. coli OV2 reca Tn10 y E. coli MC1061 reca Tn10) en la que una mutación producida por inserción de un transposón Tn10 ha inutilizado el gen reca. Dado que este gen está involucrado en uno de los mecanismos principales de reparación de lesiones del ADN producidas por UV, las bacterias mutantes tienen una sensibilidad a UV extremadamente alta, que les impide sobrevivir tras exponerlas a dosis moderadas de radiación UV. 8
10 PROTOCOLO Cada grupo de trabajo recibirá cuatro placas de Petri, sobre cuya superficie se sembrarán -en dos áreas perfectamente delimitadas- un inóculo de bacterias OV2 y MC1061, y de bacterias OV2 reca Tn 10 y MC1061 reca Tn10, que se han mantenido en oscuridad. 2. Las bacterias sembradas en las placas de cultivo se iluminan con luz UV en un transiluminador aplicando diferentes dosis de radiación (0,001-0,005 Julios/ cm). 3. Se depositan todas las placas del paso anterior en el incubador a 37º C, y se mantienen hasta el dia siguiente, en que se analizarán los resultados Sesión II: Condiciones experimentales empleadas por el grupo de trabajo. 9
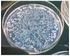
11 Sesión II: Aspecto de las colonias obtenidas en las placas petri irradiadas con luz U.V J/Cm J/Cm 2 OV2 y OV2 reca Tn 10, J/Cm J/Cm 2 MC1061 y MC1061 reca Tn10 10
12 SESION III PURIFICACION DE DNA PLASMIDICO. Se inoculará en medio líquido una colonia (bacterias descendientes de una única célula inicial) en medio líquido de crecimiento. El DNA plasmídico se replica utilizando la maquinaria de la bacteria y el origen de replicación del plásmido (ORI). El número de copias de plásmido por bacteria puede llegar a ser muy elevado. A partir de estos cultivos líquidos de bacterias provenientes de una única bacteria portadora del plásmido recombinante, se obtiene el DNA plasmídico utilizando el protocolo 3, que nos permitirá separarlo del DNA bacteriano. PROTOCOLO 3. Minipreparación de DNA plasmídico. 1. Marcar un tubo de minicentrífuga para identificar el grupo de trabajo. 2. Pipetear 1,5 ml del cultivo en un tubo de minicentrífuga (tres veces 500 µl). 3. Centrifugar durante 1 min. en una minicentrífuga. 4. Extraer el sobrenadante con una pipeta "Pasteur", procurando dejar las bacterias lo más secas posibles. 5. Poner el tubo en hielo. 6. Pipetear 250 µl de disolución de resuspensión (contiene tampón/rnasa) que se encuentra en el frasco de tapón blanco. Resuspender las bacterias agitándolas hasta que la suspensión sea totalmente homogénea. 7. Pipetear 250 µl de disolución de lisis (en el frasco de tapón rojo) sobre la suspensión de bacterias, mezclando con suavidad por inversión del 11
13 tubo 3-6 veces. Incubar a temperatura ambiente durante 5 min. Transcurrido ese tiempo, la solución se vuelve viscosa y clara. 8. Añadir 350 µl de solución tampón de fijación (o binding buffer contenido en el frasco de tapón verde), previamente enfriado en hielo. Mezclar suavemente por inversión del tubo unas 3-6 veces. Incubr los tubos durante 5 min. en hielo. Aparecen flóculos en la solución, con tendencia a precipitar en el fondo del tubo 9. Centrifugar 10 min en la minicentrífuga a aprox rpm. 10. Introducir un filtro High Pure en un tubo colector. Depositar el sobrenadante obtenido tras la centrifugación del paso anterior en la cámara superior del filtro High Pure. Centrifugar de nuevo a rpm durante seg. 11. Separar el filtro del tubo colector y descartar el líquido recogido en éste. Colocar de nuevo el filtro sobre el tubo colector y añadir 700 µl de líquido de lavado (frasco de tapón azul) y centrifugar a rpm durante seg. 12. Separar el filtro del tubo colector y descartar el líquido recogido en éste. Colocar de nuevo el filtro sobre el tubo colector y centrifugar a rpm durante seg. Para eliminar posibles restos de la solución de lavado. 13. Descartar el líquido recogido y el propio tubo colector, que es sustituído por un tubo Eppendorf limpio de 1,5 ml. Añadir 100 µl de tampón de elución (frasco de tapón no coloreado) y centrifugar a rpm durante seg. 14. El tubo de 1,5 ml contiene ahora el plásmido eluído. 12
14 Sesión III: Observaciones y comentarios. 13
15 SESION IV ANALISIS DE RESTRICCION. Se digerirá el plásmido purificado con la endonucleasa de restricción Eco RI, según el Protocolo 4. Los fragmentos obtenidos se separarán por electroforesis en gel de agarosa (Protocolo 5). Se discutirán los resultados obtenidos por cada grupo y se identificarán las diferentes movilidades que muestran los plásmidos intactos, o los que han sido cortados por el enzima de restricción. PROTOCOLO 4. Incubación de DNA con Eco RI. 1. En un tubo Eppendorf de 1,5 ml se pipetean sucesivamente los siguientes componentes de la reacción: DNA de plásmido eluído 10 µl Buffer de restricción 3 µl Endonucleasa Eco RI (Roche) 5 unidades Agua desionizada 27 µl 2. Se incuba a 37º C durante un mínimo de 2 horas. Mientras se incuba la reacción, se procede a preparar un gel de agarosa al 1% (en peso/volumen) en el que cargaremos las reacciones al finalizar la incubación para resolver mediante electroforesis los fragmentos de ADN obtenidos. 14
16 Electroforesis del ADN del plámido en geles de agarosa. Polímero de agarosa Estados sólido-líquido Aparatos utilizados (Cubeta, fuente, transiluminador) 15
17 Protocolo Se toman 20 µl de cada una de las muestras de DNA que se vayan a analizar y se depositan en tubos separados. A cada tubo se le añade ahora 2 µl de solución de muestra para electroforesis y se mezcla bien. 2. Cada muestra se deposita en un pocillo independiente del gel de agarosa, sumergido en el tampón de electroforesis. Además, se incluye una muestra del DNA marcador (mezcla de fragmentos de DNA de peso molecular conocido) para poder calibrar el tamaño de los DNA detectados. 3. Se aplica una corriente de voltaje constante de 100 voltios y se mantiene hasta que el colorante llegue al final del recorrido del gel. 4. Como el gel de electroforesis contiene bromuro de etidio, que es un agente intercalante de DNA, las moléculas de DNA pueden visualizarse mediante irradiación del gel con luz ultravioleta, utilizando un transiluminador adecuado. Sesión IV: Observaciones y comentarios. 16
Práctico: Genética bacteriana 2007.
 Práctico: Genética bacteriana 2007. Actividad integrada Departamento de Genética Departamento de Bacteriología y Virología. OBJETIVOS Objetivos generales El estudiante al terminar la actividad práctica
Práctico: Genética bacteriana 2007. Actividad integrada Departamento de Genética Departamento de Bacteriología y Virología. OBJETIVOS Objetivos generales El estudiante al terminar la actividad práctica
Anexo Conservar a 4 o C.
 Anexo 1 Purificación de ADN viral 1. Partir de un sobrenadante de un cultivo celular infectado y clarificado. 2. Concentrar las formas brotantes de los baculovirus por centrifugación (centrifugrar 1,5
Anexo 1 Purificación de ADN viral 1. Partir de un sobrenadante de un cultivo celular infectado y clarificado. 2. Concentrar las formas brotantes de los baculovirus por centrifugación (centrifugrar 1,5
Construcción de la biblioteca en cósmidos de Azospirillum brasilense CBG 497.
 Construcción de la biblioteca en cósmidos de Azospirillum brasilense CBG 497. Extracción de DNA genómico El DNA de A. brasilense CBG 497 se extrajo siguiendo el método descrito por la casa comercial distribuidora
Construcción de la biblioteca en cósmidos de Azospirillum brasilense CBG 497. Extracción de DNA genómico El DNA de A. brasilense CBG 497 se extrajo siguiendo el método descrito por la casa comercial distribuidora
EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS
 EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS Los hongos poseen un genoma complejo consistente en: ADN nuclear (n ADN) ADN mitocondrial (mt ADN) en algunos casos ADN plasmídico EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS
EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS Los hongos poseen un genoma complejo consistente en: ADN nuclear (n ADN) ADN mitocondrial (mt ADN) en algunos casos ADN plasmídico EXTRACCIÓN DE ADN DE HONGOS FILAMENTOSOS
38. Purificación de ADN plasmídico y electroforesis del mismo en gel de agarosa
 38. Purificación de ADN plasmídico y electroforesis del mismo en gel de agarosa José Luis Caballero Repullo, Enriqueta Moyano, Juan Muñoz Blanco Departamento de Bioquímica y Biología Molecular, Campus
38. Purificación de ADN plasmídico y electroforesis del mismo en gel de agarosa José Luis Caballero Repullo, Enriqueta Moyano, Juan Muñoz Blanco Departamento de Bioquímica y Biología Molecular, Campus
ANEXOS. Anexo 1 Transformación mediante electroporación
 Anexo 1 Transformación mediante electroporación ANEXOS En este método de transformación de E. coli se requieren células electrocompetentes. La preparación de estas células consta de los siguientes pasos:
Anexo 1 Transformación mediante electroporación ANEXOS En este método de transformación de E. coli se requieren células electrocompetentes. La preparación de estas células consta de los siguientes pasos:
Taller Ciencia para Jóvenes CIMAT 2012 Bachillerato julio 8 14 Cinvestav Campus Guanajuato
 Introducción Taller Ciencia para Jóvenes CIMAT 2012 Bachillerato julio 8 14 Cinvestav Campus Guanajuato Visita al CINVESTAV - Irapuato. 19 julio, 2012. Las bacterias son los organismos más abundantes que
Introducción Taller Ciencia para Jóvenes CIMAT 2012 Bachillerato julio 8 14 Cinvestav Campus Guanajuato Visita al CINVESTAV - Irapuato. 19 julio, 2012. Las bacterias son los organismos más abundantes que
CURSO DE EXTENSIÓN TEÓRICO PRÁCTICO HERRAMIENTAS EFICIENTES PARA LA IDENTIFICACIÓN DE LEVADURAS DE INTERÉS AGROINDUSTRIAL
 LIBRO DE MEMORIAS 2 CURSO DE EXTENSIÓN TEÓRICO PRÁCTICO HERRAMIENTAS EFICIENTES PARA LA IDENTIFICACIÓN DE LEVADURAS DE INTERÉS AGROINDUSTRIAL Santiago de Cali, 23 al 28 de agosto de 2010 3 Libro de memorias
LIBRO DE MEMORIAS 2 CURSO DE EXTENSIÓN TEÓRICO PRÁCTICO HERRAMIENTAS EFICIENTES PARA LA IDENTIFICACIÓN DE LEVADURAS DE INTERÉS AGROINDUSTRIAL Santiago de Cali, 23 al 28 de agosto de 2010 3 Libro de memorias
39. Aislamiento y purificación del DNA de un plásmido recombinante
 39. Aislamiento y purificación del DNA de un plásmido recombinante Aurora Galván Cejudo, Manuel Tejada, Antonio Camargo, José Javier Higuera, Vicente Mariscal, Emilio Fernández Reyes Departamento de Bioquímica
39. Aislamiento y purificación del DNA de un plásmido recombinante Aurora Galván Cejudo, Manuel Tejada, Antonio Camargo, José Javier Higuera, Vicente Mariscal, Emilio Fernández Reyes Departamento de Bioquímica
Módulo 1 Biología Molecular Genética Molecular II 2009. Módulo 1. Amplificación de un fragmento de ADN genómico por PCR
 Módulo 1 Amplificación de un fragmento de ADN genómico por PCR En este primer módulo se amplificará por PCR, mediante el uso de oligonucleótidos específicos, un fragmento de ADN genómico de Aspergillus
Módulo 1 Amplificación de un fragmento de ADN genómico por PCR En este primer módulo se amplificará por PCR, mediante el uso de oligonucleótidos específicos, un fragmento de ADN genómico de Aspergillus
17.- Electroforesis de ácidos nucleicos en geles de agarosa. Aislamiento y caracterización electroforética de DNA plasmídico
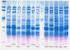 17.- Electroforesis de ácidos nucleicos en geles de agarosa. Aislamiento y caracterización electroforética de DNA plasmídico Carmen Alicia Padilla Peña, Jesús Diez Dapena, Emilia Martínez Galisteo, José
17.- Electroforesis de ácidos nucleicos en geles de agarosa. Aislamiento y caracterización electroforética de DNA plasmídico Carmen Alicia Padilla Peña, Jesús Diez Dapena, Emilia Martínez Galisteo, José
REACCIÓN EN CADENA DE LA POLIMERASA (PCR)
 REACCIÓN EN CADENA DE LA POLIMERASA (PCR) Microbiología General Microbiología M de los Alimentos Licenciatura en Bioquímica i Ingeniería en alimentos c Microbiología r 2015 Licenciatura en Biotecnología
REACCIÓN EN CADENA DE LA POLIMERASA (PCR) Microbiología General Microbiología M de los Alimentos Licenciatura en Bioquímica i Ingeniería en alimentos c Microbiología r 2015 Licenciatura en Biotecnología
REACCIÓN EN CADENA DE LA POLIMERASA (PCR) Microbiología de los Alimentos Ingeniería en alimentos
 REACCIÓN EN CADENA DE LA POLIMERASA (PCR) Microbiología de los Alimentos Ingeniería en alimentos 2015 Desarrollada por Kary Mullis en 1986 Técnica in vitro que permite amplificar enzimáticamente una región
REACCIÓN EN CADENA DE LA POLIMERASA (PCR) Microbiología de los Alimentos Ingeniería en alimentos 2015 Desarrollada por Kary Mullis en 1986 Técnica in vitro que permite amplificar enzimáticamente una región
CUADERNO DE PRÁCTICAS GENETICA MOLECULAR HUMANA. Grado en Medicina
 DEPARTAMENTO DE BIOQUÍMICA Y BIOLOGÍA MOLECULAR III FACULTAD DE MEDICINA UNIVERSIDAD COMPLUTENSE DE MADRID CUADERNO DE PRÁCTICAS GENETICA MOLECULAR HUMANA Grado en Medicina CURSO ACADÉMICO 2014/2015 INDICE
DEPARTAMENTO DE BIOQUÍMICA Y BIOLOGÍA MOLECULAR III FACULTAD DE MEDICINA UNIVERSIDAD COMPLUTENSE DE MADRID CUADERNO DE PRÁCTICAS GENETICA MOLECULAR HUMANA Grado en Medicina CURSO ACADÉMICO 2014/2015 INDICE
PROPIEDADES FISICOQUÍMICAS DE LOS ÁCIDOS NUCLEICOS. Es un ácido capaz de formar sales con iones cargados
 Extracción de ADN Genética molecular PROPIEDADES FISICOQUÍMICAS DE LOS ÁCIDOS NUCLEICOS Es un ácido capaz de formar sales con iones cargados positivamente (cationes). Es soluble en soluciones concentradas
Extracción de ADN Genética molecular PROPIEDADES FISICOQUÍMICAS DE LOS ÁCIDOS NUCLEICOS Es un ácido capaz de formar sales con iones cargados positivamente (cationes). Es soluble en soluciones concentradas
DANAGENE BLOOD DNA KIT
 Ref. 0601 100 ml Ref. 0602 200 ml DANAGENE BLOOD DNA KIT 1.INTRODUCCION DANAGENE BLOOD DNA Kit provee un método para la extracción de ADN genómico de alta calidad a partir de sangre total o médula ósea.
Ref. 0601 100 ml Ref. 0602 200 ml DANAGENE BLOOD DNA KIT 1.INTRODUCCION DANAGENE BLOOD DNA Kit provee un método para la extracción de ADN genómico de alta calidad a partir de sangre total o médula ósea.
PLANIFICACIÓN DE ASIGNATURA
 PLANIFICACIÓN DE ASIGNATURA I IDENTIFICACION GENERAL DE LA ASIGNATURA CARRERA BIOQUIMICA DEPARTAMENTO BIOLOGIA ASIGNATURA BIOLOGIA MOLECULAR II CÓDIGO 1681 PRERREQUISITOS Biología Molecular I CREDITOS
PLANIFICACIÓN DE ASIGNATURA I IDENTIFICACION GENERAL DE LA ASIGNATURA CARRERA BIOQUIMICA DEPARTAMENTO BIOLOGIA ASIGNATURA BIOLOGIA MOLECULAR II CÓDIGO 1681 PRERREQUISITOS Biología Molecular I CREDITOS
PROCEDIMIENTO DETECCIÓN Y ENUMERACIÓN POR NUMERO MAS PROBABLE (NMP) CON ETAPA DE PRE- ENRIQUECIMIENTO DE ENTEROBACTERIACEAE EN ALIMENTOS
 Página 1 de 5 1. OBJETIVO Estimar el número de Enterobacteriaceae presentes en el alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos de consumo humano
Página 1 de 5 1. OBJETIVO Estimar el número de Enterobacteriaceae presentes en el alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos de consumo humano
LA NUEVA BIOTECNOLOGÍA
 LA NUEVA BIOTECNOLOGÍA Ingeniería genética: técnicas que permiten manipular la información genética de un ser vivo. TECNOLOGÍA TRADICIONAL DEL ADN RECOMBINANTE CLONACIÓN DE GENES: Obtención de muchas copias
LA NUEVA BIOTECNOLOGÍA Ingeniería genética: técnicas que permiten manipular la información genética de un ser vivo. TECNOLOGÍA TRADICIONAL DEL ADN RECOMBINANTE CLONACIÓN DE GENES: Obtención de muchas copias
REACCIÓN EN CADENA DE LA POLIMERASA (PCR)
 REACCIÓN EN CADENA DE LA POLIMERASA (PCR) Lic. en Bioquímica Lic. en Biotecnología Microbiología de los Alimentos 2016 Desarrollada por Kary Mullis en 1986 Técnica in vitro que permite amplificar enzimáticamente
REACCIÓN EN CADENA DE LA POLIMERASA (PCR) Lic. en Bioquímica Lic. en Biotecnología Microbiología de los Alimentos 2016 Desarrollada por Kary Mullis en 1986 Técnica in vitro que permite amplificar enzimáticamente
5. DETECCION DE GENES DE VIRULENCIA MEDIANTE HIBRIDACIÓN CON SONDAS DE ADN
 5. DETECCION DE GENES DE VIRULENCIA MEDIANTE HIBRIDACIÓN CON SONDAS DE ADN Materiales - Eppendorf de 1,5 ml estériles - Eppendorf de pared fina para PCR - Puntas de pipeta estériles desechables - Guantes
5. DETECCION DE GENES DE VIRULENCIA MEDIANTE HIBRIDACIÓN CON SONDAS DE ADN Materiales - Eppendorf de 1,5 ml estériles - Eppendorf de pared fina para PCR - Puntas de pipeta estériles desechables - Guantes
ELECTROFORESIS AVANZADA
 Ref. ELECAVANZADA (4 prácticas) 1. OBJETIVO DEL EXPERIMENTO ELECTROFORESIS AVANZADA El objetivo de este experimento es introducir a los alumnos en el conocimiento de la teoría electroforética y familiarizarse
Ref. ELECAVANZADA (4 prácticas) 1. OBJETIVO DEL EXPERIMENTO ELECTROFORESIS AVANZADA El objetivo de este experimento es introducir a los alumnos en el conocimiento de la teoría electroforética y familiarizarse
DETERMINACIÓN DEL MAPA DE UN PLÁSMIDO CON ENZIMAS DE RESTRICCIÓN
 DETERMINACIÓN DEL MAPA DE UN PLÁSMIDO CON ENZIMAS DE RESTRICCIÓN 6 grupos de estudiantes 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es desarrollar un conocimiento del mapaje de ADN determinando
DETERMINACIÓN DEL MAPA DE UN PLÁSMIDO CON ENZIMAS DE RESTRICCIÓN 6 grupos de estudiantes 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es desarrollar un conocimiento del mapaje de ADN determinando
41. Comprobación de colonias transformantes mediante PCR y electroforesis
 41. Comprobación de colonias transformantes mediante PCR y electroforesis Aurora Galván Cejudo, Manuel Tejada, Antonio Camargo, José Javier Higuera, Vicente Mariscal, Emilio Fernández Reyes Departamento
41. Comprobación de colonias transformantes mediante PCR y electroforesis Aurora Galván Cejudo, Manuel Tejada, Antonio Camargo, José Javier Higuera, Vicente Mariscal, Emilio Fernández Reyes Departamento
BIOLOGIA CELULAR Y MOLECULAR. LABORATORIO No 5: ENZIMAS DE RESTRICCION
 BIOLOGIA CELULAR Y MOLECULAR LABORATORIO No 5: ENZIMAS DE RESTRICCION 1. INTRODUCION Las enzimas de restricción, también conocidas como endonucleasas, son enzimas que cortan los enlaces fosfodiéster del
BIOLOGIA CELULAR Y MOLECULAR LABORATORIO No 5: ENZIMAS DE RESTRICCION 1. INTRODUCION Las enzimas de restricción, también conocidas como endonucleasas, son enzimas que cortan los enlaces fosfodiéster del
IV Curso Avanzado WHO GSS 2006 Buenos Aires 15 al 24 de mayo de 2006
 IV Curso Avanzado WHO GSS 2006 Buenos Aires 15 al 24 de mayo de 2006 REACCION EN CADENA DE LA POLIMERASA (PCR) EN EL DIAGNOSTICO DE Campylobacter jejuni/coli Viernes 19 de mayo María Rosa Viñas Servicio
IV Curso Avanzado WHO GSS 2006 Buenos Aires 15 al 24 de mayo de 2006 REACCION EN CADENA DE LA POLIMERASA (PCR) EN EL DIAGNOSTICO DE Campylobacter jejuni/coli Viernes 19 de mayo María Rosa Viñas Servicio
TECHNOLOGY. CROSSMATCH TEST canino. primer test inmunocromatografico para reaccion cruzada con antiglobulina canina especifica.
 CROSSMATCH TEST canino primer test inmunocromatografico para reaccion cruzada con antiglobulina canina especifica 20 minutos TECHNOLOGY - ahorra tiempo - facil manipulacion - resultados fiables - facil
CROSSMATCH TEST canino primer test inmunocromatografico para reaccion cruzada con antiglobulina canina especifica 20 minutos TECHNOLOGY - ahorra tiempo - facil manipulacion - resultados fiables - facil
TRANSFORMACIÓN BACTERIANA CON pgal (colonias azules)
 TRANSFORMACIÓN BACTERIANA CON pgal (colonias azules) 10 grupos de estudiantes 1. OBJETIVO DEL EXPERIMENTO En este experimento los estudiantes explorarán el proceso biológico de la transformación bacteriana
TRANSFORMACIÓN BACTERIANA CON pgal (colonias azules) 10 grupos de estudiantes 1. OBJETIVO DEL EXPERIMENTO En este experimento los estudiantes explorarán el proceso biológico de la transformación bacteriana
TRANSFORMACIÓN BACTERIANA CON PROTEÍNAS FLUORESCENTES VERDES
 TRANSFORMACIÓN BACTERIANA CON PROTEÍNAS FLUORESCENTES VERDES 10 grupos de estudiantes 1. OBJETIVO DEL EXPERIMENTO En este experimento los estudiantes explorarán el proceso biológico de la transformación
TRANSFORMACIÓN BACTERIANA CON PROTEÍNAS FLUORESCENTES VERDES 10 grupos de estudiantes 1. OBJETIVO DEL EXPERIMENTO En este experimento los estudiantes explorarán el proceso biológico de la transformación
AISLAMIENTO DE ÁCIDO DESOXIRRIBONUCLEICO (DNA) GENÓMICO Y PLASMÍDICO
 AISLAMIENTO DE ÁCIDO DESOXIRRIBONUCLEICO (DNA) GENÓMICO Y PLASMÍDICO E l estudio del genoma de los seres vivos a sido uno d los principales objetivos de la Biología. Desde los trabajos de Mendel (1866),
AISLAMIENTO DE ÁCIDO DESOXIRRIBONUCLEICO (DNA) GENÓMICO Y PLASMÍDICO E l estudio del genoma de los seres vivos a sido uno d los principales objetivos de la Biología. Desde los trabajos de Mendel (1866),
5. MATERIALES Y MÉTODOS
 5. MATERIALES Y MÉTODOS 5.1 Equipos Los siguientes termocicladores se emplearon para la amplificación por PCR: - Perkin Elmer, GeneAmp PCR System 2400. - Perkin Elmer, GeneAmp PCR System 9600. - Applied
5. MATERIALES Y MÉTODOS 5.1 Equipos Los siguientes termocicladores se emplearon para la amplificación por PCR: - Perkin Elmer, GeneAmp PCR System 2400. - Perkin Elmer, GeneAmp PCR System 9600. - Applied
UNIVERSIDAD NACIONAL DEL NORDESTE Facultad de Ciencias Exactas y Naturales y Agrimensura Departamento de Biología - Área Zoología EMBRIOLOGÍA ANIMAL
 UNIVERSIDAD NACIONAL DEL NORDESTE Facultad de Ciencias Exactas y Naturales y Agrimensura Departamento de Biología - Área Zoología EMBRIOLOGÍA ANIMAL PROTOCOLO PARA OBTENCIÓN DE EMBRIONES DE POLLO EN LABORATORIO
UNIVERSIDAD NACIONAL DEL NORDESTE Facultad de Ciencias Exactas y Naturales y Agrimensura Departamento de Biología - Área Zoología EMBRIOLOGÍA ANIMAL PROTOCOLO PARA OBTENCIÓN DE EMBRIONES DE POLLO EN LABORATORIO
PRÁCTICA 1: MÉTODOS DE RUPTURA CELULAR
 PRÁCTICA 1: MÉTODOS DE RUPTURA CELULAR FUNDAMENTO TEÓRICO Para estudiar la estructura y/o las funciones metabólicas de los distintos compartimentos celulares hay que aislarlos del resto de los orgánulos.
PRÁCTICA 1: MÉTODOS DE RUPTURA CELULAR FUNDAMENTO TEÓRICO Para estudiar la estructura y/o las funciones metabólicas de los distintos compartimentos celulares hay que aislarlos del resto de los orgánulos.
DIGESTIÓN DEL FAGO LAMBDA CON ENZIMAS DE RESTRICCIÓN
 DIGESTIÓN DEL FAGO LAMBDA CON ENZIMAS DE RESTRICCIÓN Ref.ER2 (4 PRÁCTICAS) 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir los principios de la digestión del ADN con enzimas de
DIGESTIÓN DEL FAGO LAMBDA CON ENZIMAS DE RESTRICCIÓN Ref.ER2 (4 PRÁCTICAS) 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir los principios de la digestión del ADN con enzimas de
BIORREACTRES. Estudios básicos y aplicados sobre procesos de fermentación
 BIORREACTRES Ing. en Alimentos Estudios básicos y aplicados sobre procesos de fermentación Mg. Anahí V. Cuellas Docente investigadora Universidad Nacional de Quilmes TRABAJO PRACTICO Obtención de enzimas
BIORREACTRES Ing. en Alimentos Estudios básicos y aplicados sobre procesos de fermentación Mg. Anahí V. Cuellas Docente investigadora Universidad Nacional de Quilmes TRABAJO PRACTICO Obtención de enzimas
Laboratorio. Objetivos I N T R O D U C C I Ó N. Al finalizar este laboratorio el estudiante podrá:
 Laboratorio 12 Biología molecular Objetivos Al finalizar este laboratorio el estudiante podrá: 1. Conocer los principios básicos de la técnica de electroforesis y su aplicación al análisis del ADN. 2.
Laboratorio 12 Biología molecular Objetivos Al finalizar este laboratorio el estudiante podrá: 1. Conocer los principios básicos de la técnica de electroforesis y su aplicación al análisis del ADN. 2.
INTERPRETACIÓN DE GELES DE DNA DIGERIDOS CON ENZIMAS DE RESTRICCIÓN
 INTERPRETACIÓN DE GELES DE DNA DIGERIDOS CON ENZIMAS DE RESTRICCIÓN El empleo de las enzimas de restricción y los plásmidos es habitual en el laboratorio de Biología Molecular. Con este ejercicio se pretende
INTERPRETACIÓN DE GELES DE DNA DIGERIDOS CON ENZIMAS DE RESTRICCIÓN El empleo de las enzimas de restricción y los plásmidos es habitual en el laboratorio de Biología Molecular. Con este ejercicio se pretende
PRÁCTICAS AMPLIACIÓN DE MICROBIOLOGÍA
 PRÁCTICAS AMPLIACIÓN DE MICROBIOLOGÍA Día 1º.- EXPLICACIÓN GENERAL. TRANSFORMACIONES: E. coli, Streptomyces Día 2º.- INOCULAR MINIPREPS (8:45 de la mañana). OBTENCIÓN DE PLÁSMIDO ( MINIPREPS, Lisis alcalina)
PRÁCTICAS AMPLIACIÓN DE MICROBIOLOGÍA Día 1º.- EXPLICACIÓN GENERAL. TRANSFORMACIONES: E. coli, Streptomyces Día 2º.- INOCULAR MINIPREPS (8:45 de la mañana). OBTENCIÓN DE PLÁSMIDO ( MINIPREPS, Lisis alcalina)
QUE ES? Es la búsqueda de anticuerpos preformados contra los linfocitos de un posible donante en el suero de un paciente.
 CROSS MATCH QUE ES? Es la búsqueda de anticuerpos preformados contra los linfocitos de un posible donante en el suero de un paciente. Pueden estar específicamente dirigidos contra los antígenos HLA o contra
CROSS MATCH QUE ES? Es la búsqueda de anticuerpos preformados contra los linfocitos de un posible donante en el suero de un paciente. Pueden estar específicamente dirigidos contra los antígenos HLA o contra
Grado en Química. 4º Curso Bioquímica. Guión de Prácticas
 Grado en Química 4º Curso Bioquímica Guión de Prácticas UTILES A TRAER POR EL ALUMNO Bata Gafas de Seguridad Cuaderno de Laboratorio NORMAS DE TRABAJO Antes de empezar Antes de empezar cada práctica, el
Grado en Química 4º Curso Bioquímica Guión de Prácticas UTILES A TRAER POR EL ALUMNO Bata Gafas de Seguridad Cuaderno de Laboratorio NORMAS DE TRABAJO Antes de empezar Antes de empezar cada práctica, el
TRABAJO PRÁCTICO Nº 5: ÁCIDOS NUCLEICOS. DOCENTES: Dr. Andrés Ciochinni, Dra. Gabriela Niemirowicz. DESCRIPCIÓN DE LOS MÉTODOS A UTILIZAR
 TRABAJO PRÁCTICO Nº 5: ÁCIDOS NUCLEICOS DOCENTES: Dr. Andrés Ciochinni, Dra. Gabriela Niemirowicz. DESCRIPCIÓN DE LOS MÉTODOS A UTILIZAR Purificación de ácido desoxiribonucleico (ADN). El ADN es un polímero
TRABAJO PRÁCTICO Nº 5: ÁCIDOS NUCLEICOS DOCENTES: Dr. Andrés Ciochinni, Dra. Gabriela Niemirowicz. DESCRIPCIÓN DE LOS MÉTODOS A UTILIZAR Purificación de ácido desoxiribonucleico (ADN). El ADN es un polímero
FISIOLOGÍA BACTERIANA 2015 TÉCNICAS BÁSICAS DE MICROBIOLOGIA - TÉCNICAS ASÉPTICAS - SIEMBRA Y AISLAMIENTO
 FISIOLOGÍA BACTERIANA 2015 1 TRABAJO PRÁCTICO TÉCNICAS BÁSICAS DE MICROBIOLOGIA - TÉCNICAS ASÉPTICAS - SIEMBRA Y AISLAMIENTO OBJETIVOS: Conocer la importancia de la esterilización y familiarizarse con
FISIOLOGÍA BACTERIANA 2015 1 TRABAJO PRÁCTICO TÉCNICAS BÁSICAS DE MICROBIOLOGIA - TÉCNICAS ASÉPTICAS - SIEMBRA Y AISLAMIENTO OBJETIVOS: Conocer la importancia de la esterilización y familiarizarse con
PCR gen 16S ARNr bacteriano
 PCR gen 16S ARNr bacteriano Ref. PCR16S 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir a los estudiantes en los principios y la práctica de la Reacción en Cadena de la Polimerasa
PCR gen 16S ARNr bacteriano Ref. PCR16S 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir a los estudiantes en los principios y la práctica de la Reacción en Cadena de la Polimerasa
PRÁCTICA III. AISLAMIENTO DE MITOCONDRIAS: ACTIVIDAD MALATO DESHIDROGENASA
 PRÁCTICA III. AISLAMIENTO DE MITOCONDRIAS: ACTIVIDAD MALATO DESHIDROGENASA 1. Fundamento Teórico La mayoría de los procesos bioquímicos que producen energía química se realizan en orgánulos intracelulares
PRÁCTICA III. AISLAMIENTO DE MITOCONDRIAS: ACTIVIDAD MALATO DESHIDROGENASA 1. Fundamento Teórico La mayoría de los procesos bioquímicos que producen energía química se realizan en orgánulos intracelulares
Clonación molecular. Clonar significa hacer copias idénticas
 INGENIERÍA GENÉTICA Clonación molecular Clonar significa hacer copias idénticas Este término originalmente fue aplicado al procedimiento de aislar una célula y permitirle reproducirse creando una población
INGENIERÍA GENÉTICA Clonación molecular Clonar significa hacer copias idénticas Este término originalmente fue aplicado al procedimiento de aislar una célula y permitirle reproducirse creando una población
Técnicas de Estudio de las células
 Técnicas de Estudio de las células Microscopia Preparaciones permanentes: Fijación Deshidratación Inclusión Corte Fijación: Acidos, solventes orgánicos como alcohol, aldehídos (Formaldehído, glutaraldehídos)
Técnicas de Estudio de las células Microscopia Preparaciones permanentes: Fijación Deshidratación Inclusión Corte Fijación: Acidos, solventes orgánicos como alcohol, aldehídos (Formaldehído, glutaraldehídos)
PRÁCTICA DE GENÉTICA
 PRÁCTICA DE GENÉTICA Diagnóstico molecular de una enfermedad genética, seguimiento en una genealogía y consejo genético. Profesores responsables: Paloma Martínez Rodríguez y José L. Bella Sombría NORMAS
PRÁCTICA DE GENÉTICA Diagnóstico molecular de una enfermedad genética, seguimiento en una genealogía y consejo genético. Profesores responsables: Paloma Martínez Rodríguez y José L. Bella Sombría NORMAS
37. Purificación de ácidos nucleicos
 37. Purificación de ácidos nucleicos Mª José Prieto Álamo, Juan López Barea, Carmen Pueyo de la Cuesta Departamento de Bioquímica y Biología Molecular, Campus Universitario de Rabanales, Edificio Severo
37. Purificación de ácidos nucleicos Mª José Prieto Álamo, Juan López Barea, Carmen Pueyo de la Cuesta Departamento de Bioquímica y Biología Molecular, Campus Universitario de Rabanales, Edificio Severo
Tema 11. Herramientas de la genética molecular
 Tema 11. Herramientas de la genética molecular Genética CC. Mar 2004-05 Objetivos Técnicas de clonación Construcción de genotecas e identificación de secuencias Mapas de restricción Amplificación (PCR)
Tema 11. Herramientas de la genética molecular Genética CC. Mar 2004-05 Objetivos Técnicas de clonación Construcción de genotecas e identificación de secuencias Mapas de restricción Amplificación (PCR)
UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA
 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA ESCUELA DE CIENCIAS AGRICOLA, PECUARIAS Y DEL MEDIO AMBIENTE ECAPMA PROTOCOLO DE PRÁCTICAS PARA LA ESCUELA Nombre del Curso: Biotecnología II Código: 203019 Fecha:
UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA ESCUELA DE CIENCIAS AGRICOLA, PECUARIAS Y DEL MEDIO AMBIENTE ECAPMA PROTOCOLO DE PRÁCTICAS PARA LA ESCUELA Nombre del Curso: Biotecnología II Código: 203019 Fecha:
ELECTROFORESIS AVANZADA
 Ref.ELECAVANZADA (4 prácticas) 1.OBJETIVO DEL EXPERIMENTO ELECTROFORESIS AVANZADA El objetivo de este experimento es introducir a los alumnos en el conocimiento de la teoría electroforética y familiarizarse
Ref.ELECAVANZADA (4 prácticas) 1.OBJETIVO DEL EXPERIMENTO ELECTROFORESIS AVANZADA El objetivo de este experimento es introducir a los alumnos en el conocimiento de la teoría electroforética y familiarizarse
Por qué en un resultado positivo siempre cambia a amarillo intenso pero solo algunos emiten fluorescencia?
 Biología 3725 L COLILERT Por qué en un resultado positivo siempre cambia a amarillo intenso pero solo algunos emiten fluorescencia? ENTEROLERT Cuál es el propósito de utilizar enterolert, que nos dice
Biología 3725 L COLILERT Por qué en un resultado positivo siempre cambia a amarillo intenso pero solo algunos emiten fluorescencia? ENTEROLERT Cuál es el propósito de utilizar enterolert, que nos dice
C A P Í T U L O 3 M A T E R I A L E S Y M É T O D O. Se ejecutaron varias pruebas para la inactivación de Escherichia Coli ATCC 25922 en agua
 C A P Í T U L O 3 M A T E R I A L E S Y M É T O D O Se ejecutaron varias pruebas para la inactivación de Escherichia Coli ATCC 25922 en agua destilada utilizando Dióxido de Titanio dopado con Nitrógeno,
C A P Í T U L O 3 M A T E R I A L E S Y M É T O D O Se ejecutaron varias pruebas para la inactivación de Escherichia Coli ATCC 25922 en agua destilada utilizando Dióxido de Titanio dopado con Nitrógeno,
GUÍA REALIZACIÓN DE CULTIVOS MICROBIOLÓGICOS
 ESCUELA DE SALUD GUÍA REALIZACIÓN DE CULTIVOS MICROBIOLÓGICOS DIRIGIDO A ALUMNOS DE: Técnico de laboratorio Clínico y Banco de Sangre Técnico de Enfermería Técnico de Radiodiagnóstico y Radioterapia Informática
ESCUELA DE SALUD GUÍA REALIZACIÓN DE CULTIVOS MICROBIOLÓGICOS DIRIGIDO A ALUMNOS DE: Técnico de laboratorio Clínico y Banco de Sangre Técnico de Enfermería Técnico de Radiodiagnóstico y Radioterapia Informática
DANAGENE RNA PURIFICATION KIT
 DANAGENE RNA PURIFICATION KIT REF.0801.1 100 EXTRACCIONES REF.0801.2 500 EXTRACCIONES 1.INTRODUCCION Este kit permite la permite la obtención de ARN total a partir de cultivos celulares, tejidos animales,
DANAGENE RNA PURIFICATION KIT REF.0801.1 100 EXTRACCIONES REF.0801.2 500 EXTRACCIONES 1.INTRODUCCION Este kit permite la permite la obtención de ARN total a partir de cultivos celulares, tejidos animales,
ESTUDIO MICROSCÓPICO DE LAS BACTERIAS DEL YOGUR
 ESTUDIO MICROSCÓPICO DE LAS BACTERIAS DEL YOGUR 1- Prepara un portaobjetos bien limpio con una gota de agua. 2 - Coge una porción pequeña de yogur con un palillo o una aguja enmangada y hacer una extensión
ESTUDIO MICROSCÓPICO DE LAS BACTERIAS DEL YOGUR 1- Prepara un portaobjetos bien limpio con una gota de agua. 2 - Coge una porción pequeña de yogur con un palillo o una aguja enmangada y hacer una extensión
Instrucciones de uso. BAG Cycler Check. Kit de para la validación de la uniformidad de la temperatura en los termocicladores
 Instrucciones de uso BAG Cycler Check Kit de para la validación de la uniformidad de la temperatura en los termocicladores listo para usar, prealicuotado REF 7104 (10 tests) REF 71044 (4 tests) Contenidos
Instrucciones de uso BAG Cycler Check Kit de para la validación de la uniformidad de la temperatura en los termocicladores listo para usar, prealicuotado REF 7104 (10 tests) REF 71044 (4 tests) Contenidos
MANUAL DE PRÁCTICAS DE LABORATORIO
 MANUAL DE PRÁCTICAS DE LABORATORIO INGENIERIA ENBIOTECNOLOGÍA INGENIERÍA GENÉTICA FICHA TECNICA FICHA TÉCNICA SEMINARIO DE BIOTECNOLOGÍA MÉDICO-FARMACÉUTICA Fecha: Nombre del catedrático: 10-Julio-2012
MANUAL DE PRÁCTICAS DE LABORATORIO INGENIERIA ENBIOTECNOLOGÍA INGENIERÍA GENÉTICA FICHA TECNICA FICHA TÉCNICA SEMINARIO DE BIOTECNOLOGÍA MÉDICO-FARMACÉUTICA Fecha: Nombre del catedrático: 10-Julio-2012
Aplicación a escala de laboratorio
 Aplicación a escala de laboratorio Índice de contenidos Velcorin Aplicación a escala de laboratorio págs. 3 5 Introducción pág. 3 Medidas de precaución pág. 3 Método de trabajo (sensorial) pág. 4 Método
Aplicación a escala de laboratorio Índice de contenidos Velcorin Aplicación a escala de laboratorio págs. 3 5 Introducción pág. 3 Medidas de precaución pág. 3 Método de trabajo (sensorial) pág. 4 Método
AISLAMIENTO DE MICROORGANISMOS
 PRÁCTICA5 AISLAMIENTO DE MICROORGANISMOS Introducción En la naturaleza, la mayoría de los microorganismos no se encuentran aislados, sino integrados en poblaciones mixtas. Para llevar a cabo el estudio
PRÁCTICA5 AISLAMIENTO DE MICROORGANISMOS Introducción En la naturaleza, la mayoría de los microorganismos no se encuentran aislados, sino integrados en poblaciones mixtas. Para llevar a cabo el estudio
Digestión de DNA usando Enzimas de Restricción
 Digestión de DNA usando Enzimas de Restricción Objetivos El cortar el DNA con enzimas de restricción es muchas veces el primer paso de los investigadores para estudiar un gen. En este laboratorio se hará
Digestión de DNA usando Enzimas de Restricción Objetivos El cortar el DNA con enzimas de restricción es muchas veces el primer paso de los investigadores para estudiar un gen. En este laboratorio se hará
Técnicas de monitoreo para la detección de microorganismos en el medio ambiente
 Técnicas de monitoreo para la detección de microorganismos en el medio ambiente Gloria Alicia Figueroa Aguilar Condiciones Ambientales REQUISITO: El laboratorio debe asegurarse que las condiciones ambientales,
Técnicas de monitoreo para la detección de microorganismos en el medio ambiente Gloria Alicia Figueroa Aguilar Condiciones Ambientales REQUISITO: El laboratorio debe asegurarse que las condiciones ambientales,
TEMA 14. Métodos inmunológicos para la identificación microbiana
 TEMA 14 Métodos inmunológicos para la identificación microbiana Tema 14. Métodos inmunológicos para la identificación microbiana 1. Introducción 2. Detección de antígenos 2.1. Obtención de anticuerpos
TEMA 14 Métodos inmunológicos para la identificación microbiana Tema 14. Métodos inmunológicos para la identificación microbiana 1. Introducción 2. Detección de antígenos 2.1. Obtención de anticuerpos
Resumen Bioluminiscencia
 Curso de biología molecular CIMAT 2007 Resumen Este curso-taller tiene como propósito mostrar de manera teórica y práctica algunos principios básicos de biología molecular e ingeniería genética. Conocerás
Curso de biología molecular CIMAT 2007 Resumen Este curso-taller tiene como propósito mostrar de manera teórica y práctica algunos principios básicos de biología molecular e ingeniería genética. Conocerás
velocidades de movimiento mediante la aplicación de un campo eléctrico a través de una matriz porosa
 INTRODUCCIÓN En general, la electroforesis es una técnica que separa las moléculas en base a sus diferentes velocidades de movimiento mediante la aplicación de un campo eléctrico a través de una matriz
INTRODUCCIÓN En general, la electroforesis es una técnica que separa las moléculas en base a sus diferentes velocidades de movimiento mediante la aplicación de un campo eléctrico a través de una matriz
CLONAJE DE GENES EN PLÁSMIDOS BACTERIANOS: Construcción del DNA recombinante
 Construcción DNA recombinante 1 Práctica 1 CLONAJE DE GENES EN PLÁSMIDOS BACTERIANOS: Construcción del DNA recombinante Introducción Los plásmidos bacterianos son moléculas de DNA extracromosómico capaces
Construcción DNA recombinante 1 Práctica 1 CLONAJE DE GENES EN PLÁSMIDOS BACTERIANOS: Construcción del DNA recombinante Introducción Los plásmidos bacterianos son moléculas de DNA extracromosómico capaces
LABORATORIO 6. TITULO : Propiedades de los Gases
 37 LABORATORIO 6. TITULO : Propiedades de los Gases OBJETIVOS: Demostrar la ley de difusión de los gases (ley de Graham) Comparar la velocidad de difusión de los gases con la de los líquidos. MATERIALES
37 LABORATORIO 6. TITULO : Propiedades de los Gases OBJETIVOS: Demostrar la ley de difusión de los gases (ley de Graham) Comparar la velocidad de difusión de los gases con la de los líquidos. MATERIALES
Guía Práctica 9. Producción de micelio en medio líquido para extracción de ADN. Micelio de hongos. Contenido
 Guía Práctica 9 Micelio de hongos Producción de micelio en medio líquido para extracción de ADN Guillermo Castellanos, Experto en Investigación 2 Carlos Jara, Ing. Agr. M.Sc., Asociado en Investigación
Guía Práctica 9 Micelio de hongos Producción de micelio en medio líquido para extracción de ADN Guillermo Castellanos, Experto en Investigación 2 Carlos Jara, Ing. Agr. M.Sc., Asociado en Investigación
ECOLOGÍA MICROBIANA Y COMPORTAMIENTO BACTERIANO COMUNITARIO
 5 TRABAJO PRÁCTICO ECOLOGÍA MICROBIANA Y COMPORTAMIENTO BACTERIANO COMUNITARIO OBJETIVOS: 1 Observar y comprender la diversidad bacteriana que coexiste en un mismo nicho en un dado ecosistema y las interrelaciones
5 TRABAJO PRÁCTICO ECOLOGÍA MICROBIANA Y COMPORTAMIENTO BACTERIANO COMUNITARIO OBJETIVOS: 1 Observar y comprender la diversidad bacteriana que coexiste en un mismo nicho en un dado ecosistema y las interrelaciones
Curso de biología molecular CIMAT 2008
 Curso de biología molecular CIMAT 2008 Resumen Este curso-taller tiene como propósito mostrar de manera teórica y práctica algunos principios básicos de biología molecular e ingeniería genética. Conocerás
Curso de biología molecular CIMAT 2008 Resumen Este curso-taller tiene como propósito mostrar de manera teórica y práctica algunos principios básicos de biología molecular e ingeniería genética. Conocerás
12.359,04 IMPORTE MAXIMO LOTE 1: ,92 IMPORTE MAXIMO LOTE 2: IMPORTE MAXIMO LOTE 3: ,54 REACTIVOS PARA AISLAMIENTO DE ACIDOS NUCLEICOS
 HOSPITAL RAMON Y CAJAL RAZON SOCIAL: SUMINISTROS - PETICION DE OFERTAS C.I.F.: SERVICIO DE GENETICA MEDICA DOMICILIO: LOCALIDAD: TRAMITA: HOSPITAL RAMON Y CAJAL TELEFONO/FAX: Nº DE COMPRA: CONCURSO ABIERTO
HOSPITAL RAMON Y CAJAL RAZON SOCIAL: SUMINISTROS - PETICION DE OFERTAS C.I.F.: SERVICIO DE GENETICA MEDICA DOMICILIO: LOCALIDAD: TRAMITA: HOSPITAL RAMON Y CAJAL TELEFONO/FAX: Nº DE COMPRA: CONCURSO ABIERTO
Objetivos. S Determinar la presencia de bacterias coliformes en una muestra de agua
 Análisis del agua S Objetivos S Determinar la presencia de bacterias coliformes en una muestra de agua Introducción S Las tres pruebas básicas para determinar la presencia de bacterias coliformes (asociada
Análisis del agua S Objetivos S Determinar la presencia de bacterias coliformes en una muestra de agua Introducción S Las tres pruebas básicas para determinar la presencia de bacterias coliformes (asociada
TRABAJO PRÁCTICO Nº 5: ÁCIDOS NUCLEICOS DESCRIPCIÓN DE LOS MÉTODOS A UTILIZAR
 TRABAJO PRÁCTICO Nº 5: ÁCIDOS NUCLEICOS DOCENTES: Andrés Ciocchini, Gabriela Niemirowicz. DESCRIPCIÓN DE LOS MÉTODOS A UTILIZAR Purificación de ácido desoxiribonucleico (ADN) por partición diferencial
TRABAJO PRÁCTICO Nº 5: ÁCIDOS NUCLEICOS DOCENTES: Andrés Ciocchini, Gabriela Niemirowicz. DESCRIPCIÓN DE LOS MÉTODOS A UTILIZAR Purificación de ácido desoxiribonucleico (ADN) por partición diferencial
AUTOR: JORGE CONTRERAS PINEDA 1. Titulo:
 Página 1 de 1 1. Titulo: Electroforesis de DNA 2. Objetivo Conocer los principios básicos de la electroforesis horizontal en geles de agarosa y aplicarlo para la separación de DNA humano, plasmídico, recombinante
Página 1 de 1 1. Titulo: Electroforesis de DNA 2. Objetivo Conocer los principios básicos de la electroforesis horizontal en geles de agarosa y aplicarlo para la separación de DNA humano, plasmídico, recombinante
ELABORACIÓN N DE MEZCLA PARA PCR. Raquel Asunción Lima Cordón
 ELABORACIÓN N DE MEZCLA PARA PCR Raquel Asunción Lima Cordón PCR Polymerase Chain reaction (reacción en cadena de la polimerasa) Sintetizar muchas veces un fragmento de ADN PCR: simulación de lo que sucede
ELABORACIÓN N DE MEZCLA PARA PCR Raquel Asunción Lima Cordón PCR Polymerase Chain reaction (reacción en cadena de la polimerasa) Sintetizar muchas veces un fragmento de ADN PCR: simulación de lo que sucede
TRANSFERENCIAS ASÉPTICAS
 Introducción Objetivo Procedimiento Trabajo Práctico Nº 3 TRANSFERENCIAS ASÉPTICAS Resultados Observaciones Bibliografía INTRODUCCIÓN La inoculación de medios de cultivo y la manipulación de cultivos microbianos
Introducción Objetivo Procedimiento Trabajo Práctico Nº 3 TRANSFERENCIAS ASÉPTICAS Resultados Observaciones Bibliografía INTRODUCCIÓN La inoculación de medios de cultivo y la manipulación de cultivos microbianos
RECONOCIMIENTO DE LOS PRINCIPIOS INMEDIATOS QUE HAY EN UN ALIMENTO
 RECONOCIMIENTO DE LOS PRINCIPIOS INMEDIATOS QUE HAY EN UN ALIMENTO Fundamento Los alimentos se diferencian entre sí por las sustancias o principios inmediatos que contienen y por la cantidad de cada uno
RECONOCIMIENTO DE LOS PRINCIPIOS INMEDIATOS QUE HAY EN UN ALIMENTO Fundamento Los alimentos se diferencian entre sí por las sustancias o principios inmediatos que contienen y por la cantidad de cada uno
3. MATERIALES Y MÉTODOS
 3. MATERIALES Y MÉTODOS El proceso general llevado a cabo en la presente tesis se ilustra en el siguiente esquema: Exudado uretral/ cervical y/o biopsias Extracción del ADN PCR Digestión Algoritmo computacional:
3. MATERIALES Y MÉTODOS El proceso general llevado a cabo en la presente tesis se ilustra en el siguiente esquema: Exudado uretral/ cervical y/o biopsias Extracción del ADN PCR Digestión Algoritmo computacional:
ELECTROFORESIS EN GELES DE AGAROSA. Agustín Garrido. agugarrido@hotmail.com
 1 ELECTROFORESIS EN GELES DE AGAROSA Agustín Garrido agugarrido@hotmail.com Introducción En este trabajo práctico se utilizó la técnica de electroforesis. Este proceso se basa en la migración de las moléculas
1 ELECTROFORESIS EN GELES DE AGAROSA Agustín Garrido agugarrido@hotmail.com Introducción En este trabajo práctico se utilizó la técnica de electroforesis. Este proceso se basa en la migración de las moléculas
Curso de biología molecular CIMAT 2010
 Curso de biología molecular CIMAT 2010 INTRODUCCIÓN Este curso-taller tiene como propósito mostrar de manera teórica y práctica algunos principios básicos de biología molecular e ingeniería genética. Conocerás
Curso de biología molecular CIMAT 2010 INTRODUCCIÓN Este curso-taller tiene como propósito mostrar de manera teórica y práctica algunos principios básicos de biología molecular e ingeniería genética. Conocerás
Resultados Práctica Transformación
 Resultados Práctica Transformación Eficiencia de Transformación Para cálculo de eficiencia Número de colonias transformadas Cantidad de plásmido agregado a bacterias que están en placa a. Cantidad
Resultados Práctica Transformación Eficiencia de Transformación Para cálculo de eficiencia Número de colonias transformadas Cantidad de plásmido agregado a bacterias que están en placa a. Cantidad
PRÁCTICA Nº 3 PROPIEDADES COLIGATIVAS: DETERMINACIÓN DE LA MASA MOLECULAR DE UN SOLUTO PROBLEMA POR CRIOSCOPIA
 PRÁCTICA Nº 3 PROPIEDADES COLIGATIVAS: DETERINACIÓN DE LA ASA OLECULAR DE UN SOLUTO PROBLEA POR CRIOSCOPIA OBJETIVOS: El objetivo de la práctica es el estudio del efecto que produce la adición de un soluto
PRÁCTICA Nº 3 PROPIEDADES COLIGATIVAS: DETERINACIÓN DE LA ASA OLECULAR DE UN SOLUTO PROBLEA POR CRIOSCOPIA OBJETIVOS: El objetivo de la práctica es el estudio del efecto que produce la adición de un soluto
Transformación de E. coli con pgal (colonia azul)
 Página 1 of 8 Universidad Interamericana de Puerto Rico Recinto de Fajardo Departamento de Ciencias y Tecnología Transformación de E. coli con pgal (colonia azul) Trasfondo La transformación bacterial
Página 1 of 8 Universidad Interamericana de Puerto Rico Recinto de Fajardo Departamento de Ciencias y Tecnología Transformación de E. coli con pgal (colonia azul) Trasfondo La transformación bacterial
PRÁCTICAS DE MICROBIOLOGÍA CLÍNICA (CURSO )
 PRÁCTICAS DE MICROBIOLOGÍA CLÍNICA (CURSO 2012 2013) PRÁCTICAS A REALIZAR ANÁLISIS CUALITATIVO DE ORINA PRUEBA DE BAUER KIRBY (ANTIBIOGRAMA) PRUEBA DE EPSILON (DETERMINACIÓN DE LA CMI) ANÁLISIS CUALITATIVO
PRÁCTICAS DE MICROBIOLOGÍA CLÍNICA (CURSO 2012 2013) PRÁCTICAS A REALIZAR ANÁLISIS CUALITATIVO DE ORINA PRUEBA DE BAUER KIRBY (ANTIBIOGRAMA) PRUEBA DE EPSILON (DETERMINACIÓN DE LA CMI) ANÁLISIS CUALITATIVO
EXTRACCION SIMPLE Y MULTIPLE Y DEL PRINCIPIO ACTIVO DEL CLORASEPTIC
 PRACTICA X EXTRACCION SIMPLE Y MULTIPLE Y DEL PRINCIPIO ACTIVO DEL CLORASEPTIC I. OBJETIVOS II MATERIAL a) Conocer la técnica de extracción como método de separación y purificación de las sustancias integrantes
PRACTICA X EXTRACCION SIMPLE Y MULTIPLE Y DEL PRINCIPIO ACTIVO DEL CLORASEPTIC I. OBJETIVOS II MATERIAL a) Conocer la técnica de extracción como método de separación y purificación de las sustancias integrantes
DESARROLLO COGNOSCITIVO Y APRENDIZAJE
 Prof. Jhonis Valbuena Cátedra: Análisis Instrumental La Electrofóresis es un método de la Química Analítica que utiliza corriente eléctrica controlada con la finalidad de separar biomolèculas según su
Prof. Jhonis Valbuena Cátedra: Análisis Instrumental La Electrofóresis es un método de la Química Analítica que utiliza corriente eléctrica controlada con la finalidad de separar biomolèculas según su
H TRITIO MARCAJE DE PROTEÍNAS EN CÉLULAS
 Disolución stock 1mCi Forma química: Solución acuosa de [6 3 H]-Timidina Vida Media: 12, 4 años 50 µci Marcaje ADN de las células Solubilización de las células Contador β 3 H TRITIO MARCAJE DE PROTEÍNAS
Disolución stock 1mCi Forma química: Solución acuosa de [6 3 H]-Timidina Vida Media: 12, 4 años 50 µci Marcaje ADN de las células Solubilización de las células Contador β 3 H TRITIO MARCAJE DE PROTEÍNAS
Petrifilm Recuento de Enterobacteriaceae
 3 Petrifilm Recuento de Enterobacteriaceae Guía de Interpretación 1 2 3 1 2 Recuento de Enterobacteriaceae = 13 Es fácil contar las colonias de Enterobacteriaceae en placas Petrifilm Recuento de Enterobacteriaceae.
3 Petrifilm Recuento de Enterobacteriaceae Guía de Interpretación 1 2 3 1 2 Recuento de Enterobacteriaceae = 13 Es fácil contar las colonias de Enterobacteriaceae en placas Petrifilm Recuento de Enterobacteriaceae.
8. PRUEBAS DE SUSCEPTIBILIDAD PARA Mycobacterium tuberculosis. Estudios científicos han determinado que al menos el 1 % de los bacilos tuberculosos
 8. PRUEBAS DE SUSCEPTIBILIDAD PARA Mycobacterium tuberculosis. Estudios científicos han determinado que al menos el 1 % de los bacilos tuberculosos de un paciente determinado son resistentes in Vitro a
8. PRUEBAS DE SUSCEPTIBILIDAD PARA Mycobacterium tuberculosis. Estudios científicos han determinado que al menos el 1 % de los bacilos tuberculosos de un paciente determinado son resistentes in Vitro a
2. NIVEL MEDIO 1. NIVEL BASICO BIOLOGIA MOLECULAR 2.1 DNA SALIVA
 BIOLOGIA MOLECULAR Hemos elaborado un programa en 3 niveles, en función del tipo de estudiante y las posibilidades del centro educativo: 1. NIVEL BASICO 2. NIVEL MEDIO DANAEXTRACTOR KIT Práctica que constituye
BIOLOGIA MOLECULAR Hemos elaborado un programa en 3 niveles, en función del tipo de estudiante y las posibilidades del centro educativo: 1. NIVEL BASICO 2. NIVEL MEDIO DANAEXTRACTOR KIT Práctica que constituye
ACTIVIDAD PRACTICA No. 8 BIOLOGIA CELULAR EXTRACCIÓN DE ADN
 Universidad Centroccidental Lisandro Alvarado Decanato de Ciencias de la Salud ACTIVIDAD PRACTICA No. 8 BIOLOGIA CELULAR EXTRACCIÓN DE ADN Octubre 2009 INTRODUCCION La molécula de ADN (que es la que se
Universidad Centroccidental Lisandro Alvarado Decanato de Ciencias de la Salud ACTIVIDAD PRACTICA No. 8 BIOLOGIA CELULAR EXTRACCIÓN DE ADN Octubre 2009 INTRODUCCION La molécula de ADN (que es la que se
CROMATOGRAFIA DE TAMIZADO MOLECULAR / FILTRACION EN GEL / EXCLUSION MOLECULAR
 CROMATOGRAFIA DE TAMIZADO MOLECULAR / FILTRACION EN GEL / EXCLUSION MOLECULAR 1.-FUNDAMENTOS DE LA CROMATOGRAFIA DE TAMIZADO MOLECULAR. Las biomoléculas presentan una serie de propiedades físicas (tamaño,
CROMATOGRAFIA DE TAMIZADO MOLECULAR / FILTRACION EN GEL / EXCLUSION MOLECULAR 1.-FUNDAMENTOS DE LA CROMATOGRAFIA DE TAMIZADO MOLECULAR. Las biomoléculas presentan una serie de propiedades físicas (tamaño,
EXTRACCIÓN Y DETERMINACIÓN DE ÁCIDOS NUCLEICOS DE LA LEVADURA
 EXTRACCIÓN Y DETERMINACIÓN DE ÁCIDS NUCLEICS DE LA LEVADURA bjetivos: Al finalizar el trabajo práctico los cursantes estarán en capacidad de: - Extraer ARN a partir de células de levadura. - Realizar la
EXTRACCIÓN Y DETERMINACIÓN DE ÁCIDS NUCLEICS DE LA LEVADURA bjetivos: Al finalizar el trabajo práctico los cursantes estarán en capacidad de: - Extraer ARN a partir de células de levadura. - Realizar la
SOUTHERN BLOT. A Fragmentos estándar de ADN. E ADN padre 2 cortado con enzimas de restricción. C ADN Hijo cortado con enzimas de restricción
 SOUTHERN BLOT 5 grupos de estudiantes 1. OBJETIVO DEL EXPERIMENTO El objetivo de esta práctica es introducir a los estudiantes en el conocimiento de una de las técnicas de hibridación utilizadas en laboratorio,
SOUTHERN BLOT 5 grupos de estudiantes 1. OBJETIVO DEL EXPERIMENTO El objetivo de esta práctica es introducir a los estudiantes en el conocimiento de una de las técnicas de hibridación utilizadas en laboratorio,
Preparación de agua de dilución :
 La determinación de la Demanda Bioquímica de Oxígeno es una prueba en la que se determina los requerimientos relativos de oxígeno en aguas contaminadas tal como aguas residuales domésticas e industriales,,
La determinación de la Demanda Bioquímica de Oxígeno es una prueba en la que se determina los requerimientos relativos de oxígeno en aguas contaminadas tal como aguas residuales domésticas e industriales,,
Sistema Integrado de Gestión RECONOCIMIENTO Y PROPIEDADES DE LAS PROTEINAS PROGRAMAS DE DEPORTE Y FISIOTERAPIA GUIA PRÁCTICA N 6
 Sistema Integrado de Gestión RECONOCIMIENTO Y PROGRAMAS DE DEPORTE Y Versión 3 Proceso: Investigación - IV Octubre de 2013 Página 2 de 10 1. OBJETIVOS Reconocer algunas propiedades de las proteínas Determinar
Sistema Integrado de Gestión RECONOCIMIENTO Y PROGRAMAS DE DEPORTE Y Versión 3 Proceso: Investigación - IV Octubre de 2013 Página 2 de 10 1. OBJETIVOS Reconocer algunas propiedades de las proteínas Determinar
PRACTICA 2 TINCION DE GRAM
 PRACTICA 2 TINCION DE GRAM OBJETIVOS DE APRENDIZAJE: Cuando haya completado este experimento, usted debe comprender: 1. La base teórica y química de los procedimientos de tinción diferencial. 2. La base
PRACTICA 2 TINCION DE GRAM OBJETIVOS DE APRENDIZAJE: Cuando haya completado este experimento, usted debe comprender: 1. La base teórica y química de los procedimientos de tinción diferencial. 2. La base
Manual de Uso (Ref /2)
 Fabricado por: BIOTOOLS B&M Labs, S.A. Valle de Tobalina - 52 - Nave 39 28021 Madrid España Tel. (34) 91 710 00 74 Fax (34) 93 843 78 84 e-mail: info@biotools.eu www.biotools.eu Diseñado para la purificación
Fabricado por: BIOTOOLS B&M Labs, S.A. Valle de Tobalina - 52 - Nave 39 28021 Madrid España Tel. (34) 91 710 00 74 Fax (34) 93 843 78 84 e-mail: info@biotools.eu www.biotools.eu Diseñado para la purificación
TÍTULO: Determinación colorimétrica de fenoles en agua por el método de la 4- aminoantipirina
 Página 1 de 6 1.- INTRODUCCIÓN Desde el punto de vista analítico el término fenol engloba este producto y sus homólogos inmediatamente superiores. El fenol se emplea como patrón y el resultado obtenido
Página 1 de 6 1.- INTRODUCCIÓN Desde el punto de vista analítico el término fenol engloba este producto y sus homólogos inmediatamente superiores. El fenol se emplea como patrón y el resultado obtenido
2. ESTRATEGIA PARA EFECTUAR LA CLONACION Y EXPRESION DEL GEN
 1. CONTROL FINAL Nombre Internacional y nombre de la vacuna Nombre del propietario Nombre y dirección del fabricante Número de Lote Fecha de fabricación Fecha de caducidad Temperatura de almacenamiento
1. CONTROL FINAL Nombre Internacional y nombre de la vacuna Nombre del propietario Nombre y dirección del fabricante Número de Lote Fecha de fabricación Fecha de caducidad Temperatura de almacenamiento
