LABORATORIO IV: ELECTROFORESIS DE PROTEÍNAS
|
|
|
- José Luis Coronel Botella
- hace 5 años
- Vistas:
Transcripción
1 LABORATORIO IV: ELECTROFORESIS DE PROTEÍNAS La gran mayoría de los polímeros biológicos presentan carga eléctrica. Las proteínas pueden ser consideradas como polianfolitos débiles. Las cargas derivan de los aminoácidos con grupos laterales ionizables. Éstos son: los residuos básicos de asparagina, lisina e histidina y los residuos ácidos del ácido glutámico y aspártico. Las cadenas laterales de tirosina también contribuyen a la carga total de la proteína. Debido a que estos grupos presentan diferentes grados de ionización la carga neta de las proteínas es muy dependiente del ph del medio. Las modificaciones posttraduccionales como fosforilación y glicosilación también le aportan carga a las proteínas. Al someter moléculas cargadas a un campo eléctrico, producido por el pasaje de corriente eléctrica a través de la solución, éstas se desplazan. Dicho fenómeno se conoce como electroforesis. La velocidad de migración depende de la carga, tamaño y forma de las partículas (Cuadro 1). Esto permite separar componentes de una mezcla compleja, siempre y cuando, presenten velocidades de migración suficientemente diferentes. Cuadro1. Migración electroforética. Para poder entender la teoría de electroforesis se analizará el desplazamiento de una partícula cargada aislada en un campo eléctrico. En el momento que se aplica el campo eléctrico, E (volts/cm), la acción de la fuerza eléctrica (F e ) hará que la partícula se acelere. Esta fuerza depende de la fuerza del campo y de la carga (q) de la partícula: F e =qe Tan pronto como la partícula empieza a moverse por la acción de la fuerza eléctrica, se manifiesta una fuerza que se opone al movimiento, F v, generada por la fricción del medio. F v = -fv f= coeficiente de fricción; v= velocidad de la partícula. Si se asume que la partícula es esférica se puede aplicar la Ley de Stokes y entonces el coeficiente de fricción se define como: f = 6πηr siendo r el radio de la partícula y η la viscosidad del medio. Entonces: F v = 6πηrv Debido a que la fuerza de fricción o fuerza viscosa es proporcional a la velocidad de migración de la partícula ésta se acelerará hasta que la fuerza viscosa se iguale con la fuerza eléctrica. A partir de ese momento la fuerza neta sobre la partícula será nula y se alcanzará un estado estacionario en el que la partícula moverá a velocidad constante. 6πηrv = qe Rearreglando esta ecuación se puede definir la movilidad electroforética (μ) como: v/e = q / 6πηr = μ Dado que la viscosidad está dada por el medio, la movilidad electroforética depende de la relación q/r que presente cada partícula. Partículas con diferente relación q/r podrán moverse con diferente velocidad durante la corrida electroforética y, si esta diferencia es suficiente, se separarán. En la realidad, la separación de macromoléculas ocurre en soluciones acuosas que contienen, además de la macromolécula de interés, los iones constituyentes de los buffers y sales. En este caso no se estudia la macromolécula sola sino en presencia de otras especies cargadas que influenciarán el campo local además de interaccionar con la macromolécula generando una capa de contraiones y dificultando su análisis. En consecuencia, la definición de movilidad electroforética, deducida en el cuadro 1 para el caso ideal de una partícula cargada en una solución diluida de un solvente no conductor, es sólo una aproximación al comportamiento de una macromolécula en condiciones reales. A pesar de los esfuerzos realizados para introducir correcciones a esta ecuación sólo se han logrado aproximaciones. 1
2 Las técnicas electroforéticas son utilizadas para separaciones efectivas y resolución de mezclas de proteínas para su posterior análisis y caracterización así como para controles de pureza. La electroforesis fue descrita como método bioquímico de separación por Tiselius a mediados de Estos primeros experimentos se realizaron en solución libre (sin la presencia de soporte) pero la inestabilidad del aparato y la difusión de la muestra, además del efecto de calentamiento producido por el campo eléctrico comprometían la resolución de la separación. La introducción del medio soporte como los geles de almidón y derivados de papel superó en parte esos problemas. El propósito del medio soporte era contener el electrolito o buffer de corrida y generar algún impedimento al movimiento libre de los componentes de la muestra tal que se minimizara la difusión al azar. Electroforesis en soporte Se han usado muchos medios soportes que se pueden clasificar en dos tipos: los soportes que se utilizan principalmente para minimizar la convección como: papel, acetato de celulosa y los materiales con que se hace cromatografía en capa fina. La separación se basa en la densidad de carga (relación carga/masa) de las proteínas al ph de trabajo de la misma forma que ocurre en la electroforesis libre. los soportes que además de evitar la convección y minimizar la difusión tienen una estructura porosa (geles de almidón, agarosa y poliacrilamida), tal que si el tamaño de las moléculas a separar es del mismo orden que el tamaño del poro, causan un efecto de tamiz molecular. Las moléculas con menor tamaño pasarán por los poros del gel más fácilmente que aquellas con tamaño mayor. La separación de las moléculas dependerá, entonces, de la densidad de carga y del tamaño. De esta forma dos proteínas con igual densidad de carga pero distinto tamaño probablemente no podrán ser separadas mediante electroforesis en papel, mientras que, si la diferencia de tamaño es suficiente, podrían ser separadas por electroforesis en geles de poliacrilamida. Electroforesis en gel Geles de almidón Los geles de almidón son una red tridimensional formada por almidón parcialmente hidrolizado. No se pude controlar demasiado el tamaño de poro. Actualmente son poco usados. Geles de agarosa La agarosa es un polímero de poligalactosa. El tamaño de poro es muy grande y se utiliza para separar moléculas de tamaño mayor a 200 KDa. Variando la concentración de agarosa se puede controlar el tamaño de poro. Se aplica principalmente para la separación de ácidos nucleicos o proteínas muy grandes. Geles de poliacrilamida Los geles de poliacrilamida son ampliamente utilizados para la separación de proteínas y fragmentos pequeños de ácidos nucleicos. El gel se obtiene mediante la polimerización de monómeros de acrilamida generando cadenas largas y el entrecruzamiento de éstas por compuestos bifuncionales como la N,N -metilen bisacrilamida que reaccionan con los grupos funcionales libres en los extremos de las cadenas (figura 1). La reacción de polimerización de acrilamida es iniciada con persulfato de amonio y calor 2
3 o riboflavina fotoactivada. La N,N,N,N -tetrametiletilendiamina (TEMED) actúa como catalizador de la reacción de polimerización. Figura 1. Reacción de copolimerización de monómeros de acrilamida y bisacrilamida para formar un gel poroso. En el sistema persulfato de amonio-temed, este último cataliza la formación de radicales libres de persulfato y éste a su vez inicia la polimerización. El aumento de la concentración de TEMED y persulfato de amonio aumenta la velocidad de polimerización. El oxígeno inhibe la polimerización y por lo tanto la solución del gel generalmente se desairea antes de usar. Los geles de poliacrilamida se describen por la nomenclatura T y C. T = (A+B) 100% y C = B 100% V (A+B) Donde A y B son las cantidades de acrilamida y bisacrilamida, respectivamente, expresadas en gramos. V originalmente fue definido como el volumen de buffer agregado pero por razones prácticas generalmente se considera como el volumen de solución gelificante. Los geles de poliacrilamida pueden ser moldeados en tubos en los que se aplica una única muestra o en placas con varios pocillos en los que se pueden aplicar diferentes muestras. Para fines analíticos las placas son mejores ya que pueden analizarse varias muestras en paralelo bajo las mismas condiciones (figura 2). La solución de macromoléculas se aplica como una capa fina en lo alto del tubo o en los pocillos de la placa. Generalmente, en los sistemas verticales, se incluye glicerol o sacarosa en el buffer de muestra para aumentar la densidad y facilitar la aplicación de la muestra. La cantidad de muestra que se siembra depende en principio de la sensibilidad del método de detección que se usará y de la capacidad de separación del gel. Cuando se hace pasar corriente, la capa de macromoléculas migra. Si existen componentes de diferente movilidad se separarán durante la electroforesis. A la solución de macromoléculas se le adiciona un colorante de bajo PM y alta movilidad (marcador del frente de corrida) que indica el progreso de la corrida. Figura 2. Equipo de electroforesis vertical en placas. Para aumentar la resolución de la electroforesis en geles de poliacrilamida (o sea mejorar la separación de las proteínas), se utiliza frecuentemente un sistema de buffers discontinuo, en el cual el gel está separado en una primera parte concentradora y una segunda parte separadora. El gel concentrador contiene iones cloruro que migran más rápido a través del gel que la muestra de proteínas, mientras que el buffer de corrida contiene iones glicina, que migran más lentamente. Las moléculas de proteínas son atrapadas en una banda delgada entre estos iones; por lo tanto, entrarán todas juntas al gel separador. Cuando las proteínas entran al gel separador, que 3
4 tiene un tamaño de poro menor, un mayor ph y una alta concentración salina respecto al concentrador, la glicina se ioniza y el gradiente de ph se disipa y las proteínas son separadas según su tamaño (figura 3). A Al inicio de la corrida los aniones son ion cloruro (verde) en los geles concentrador y separador y glicina (naranja) en las compartimentos de electrodos. Las proteínas se encuentran en los pocillos (azul). B Al establecerse la banda en el gel concentrador, las proteínas se concentran en una capa delgada entre los iones líderes cloruro y las moléculas de glicina los iones atrasados. C Cuando los componentes alcanzan el gel separador su migración será de acuerdo a sus movilidades individuales como en cualquier sistema homogéneo. Figura 3. Esquema de una electroforesis en geles de poliacrilamida con un sistema de buffers discontinuo. Tipos de electroforesis Electroforesis no desnaturalizante o nativa Una proteína en su estructura nativa tendrá una determinada relación q/r y migrará en un campo eléctrico a una velocidad proporcional a esa relación. Si el medio en que se realiza la electroforesis es un gel con tamaño de poro adecuado además de la relación q/r deberá tenerse en cuenta el efecto tamiz aportado por el gel. Las proteínas poseen una carga neta a valores de ph diferentes de su punto isoeléctrico (PI), en el cual la carga neta de la molécula es nula. La forma de la proteína dependerá de cómo se pliegue la cadena polipeptídica (estructuras secundaria y terciaria) y de su peso molecular. Dos proteínas con igual peso molecular pueden tener diferente forma. Una proteína globular (con forma semejante a una esfera) y una proteína fibrosa (con forma de bastón) con el mismo peso molecular, debido a que tienen formas diferentes, tendrán radios diferentes. Bajo condiciones experimentales seleccionadas (ph, fuerza iónica, características del soporte, voltaje, temperatura, tiempo de corrida) se podrán separar moléculas con diferente relación q/r. Este tipo de electroforesis, al no desnaturalizar la muestra, permite realizar ensayos biológicos posteriores a la separación. La separación electroforética puede realizarse a cualquier ph entre 3 y 11. En caso de emplearse poliacrilamida como soporte, se utiliza la abreviatura PAGE (del inglés polyacrylamide gel electrophoresis). En el cuadro 2 se describen algunos parámetros del sistema que pueden ser variados para optimizar la separación. 4
5 Cuadro 2. Parámetros a variar para optimizar la separación electroforética. 1. Dependientes del campo eléctrico a. Voltaje El gradiente de potencial es V/d si la separación de los electrodos es d (cm) y la diferencia de potencial entre ellos es V (volts). La fuerza sobre un ión que tiene una carga q es por tanto Vq/d y por tanto la velocidad de migración es proporcional a Vq/d. Un aumento en el gradiente de potencial aumenta proporcionalmente la velocidad de migración. b. Corriente Cuando se aplica una diferencia de potencial entre los electrodos, se genera una corriente (medida en Coulomb/segundo o Ampere). La magnitud de esta corriente está determinada por la resistencia del medio y es proporcional al voltaje. La corriente es conducida en la solución entre los electrodos, principalmente por los iones del buffer y en una pequeña proporción por los iones de la muestra. El aumento del voltaje aumentará la carga total/ segundo que converge al electrodo. La distancia migrada por los iones será proporcional a la corriente aplicada y al tiempo. 2. Dependientes de la muestra Carga La velocidad de migración aumenta al aumentar la carga neta. La magnitud de la carga es en general dependiente del ph y por tanto dependiente del sistema de buffers utilizado. 3. Dependientes del soporte Tamiz molecular Este efecto se presenta en geles de almidón, agarosa y poliacrilamida. El movimiento de las moléculas es frenado al tener que pasar a través de los poros. Dependiendo del radio de las proteínas a separar se debe seleccionar el tipo de gel y tamaño de poro adecuado para que exista un efecto tamiz del soporte. Electroforesis desnaturalizante Las proteínas pueden ser desnaturalizadas por una variedad de agentes tales como urea e hidrocloruro de guanidina así como detergentes iónicos fuertemente positivos o negativos. Dentro de éstos, el detergente aniónico dodecil sulfato, normalmente como su sal sódica (SDS del inglés, Sodium Dodecyl Sulfate; fig. 4), ha sido extremadamente útil combinado con separaciones electroforéticas en geles de poliacrilamida (SDS-PAGE). El SDS en la concentración adecuada se une a la mayoría de las proteínas en una relación peso / peso constante (1,4 g de SDS/ g de proteína). Figura 4. Estructura química del SDS. Habrá un número definido de cargas negativas del SDS por residuo de aminoácido y por lo tanto la carga aportada por este detergente será proporcional al PM de la proteína y todos los complejos SDS-proteína tendrán la misma densidad de carga. Además, el SDS al unirse a las proteínas mediante interacciones hidrofóbicas, las desnaturaliza (elimina sus estructuras secundaria, terciaria y cuaternaria). Preparación de la muestra El buffer de muestra se compone de SDS, glicerol, Tris, EDTA, un agente reductor como el ditiotreitol (DTT) y/o 2-mercaptoetanol y azul de bromofenol que sirve como tinta marcadora. El EDTA es un agente preservante que actúa como agente quelante de iones divalentes, lo que reduce la actividad de enzimas proteolíticas que requieren iones Ca 2+ y Mg 2+ como cofactores. El Tris actúa como buffer que es muy importante en los sistemas de electroforesis discontinua que requieren un ph específico. El glicerol hace a la muestra más densa y permite que ésta permanezca en el fondo del pocillo y no se disperse. La tinta permite al investigador seguir y controlar el proceso de electroforesis. El agregado de agentes reductores como 2-mercaptoetanol o ditiotreitol (DTT) y un tratamiento térmico a ebullición durante unos minutos permite lograr la 5
6 completa desnaturalización de las proteínas. Estos agentes reducen los puentes disulfuro intra y/o intercatenarios de las proteínas. Se ha comprobado que todos los complejos SDS-proteína adoptan una conformación extendida o de bastón, eliminándose la influencia de la forma en la movilidad electroforética. Debido a que todos los complejos SDS-proteína tendrán la misma densidad de carga y conformación, en una electroforesis en solución libre (sin la presencia de soporte poroso) migrarán con la misma velocidad y por lo tanto no se separarán. Cuando la electroforesis se realiza en geles de poliacrilamida, con la porosidad adecuada para generar el efecto de tamiz molecular, la separación ocurre exclusivamente en función del peso molecular. Los complejos con mayor tamaño molecular presentarán más resistencia a pasar por los poros del gel y migrarán con menor velocidad que los de menor tamaño. Para cada tipo particular y concentración de gel, existe una relación aproximadamente lineal entre el log del PM de los complejos SDS-proteína y su Rf. El Rf se define como la relación entre la distancia migrada por la proteína y la migrada por el marcador de frente de corrida. Para determinar el PM aparente de las proteínas contenidas en una muestra se corre en el mismo gel un estándar de PM constituido por proteínas con relativa pureza y PM conocido (figura 5). Luego de terminada la electroforesis, teñido y desteñido del gel se determinan los Rf para cada una de las proteínas del estándar y de las proteínas de interés. Al graficar el log PM de las proteínas estándar en función de su Rf generalmente se obtiene una relación lineal. Los PM aparentes de las proteínas de la muestra pueden determinarse combinando su valor de Rf con el punto adecuado en la curva de calibración. Para calcular el Rf debe tenerse en cuenta la variación en las dimensiones del gel antes y después del proceso de teñido. Este tipo de electroforesis es particularmente aplicable cuando se quiere analizar proteínas relativamente insolubles en los buffers comunes ya que en presencia de SDS éstas se solubilizan. Es una técnica relativamente rápida, económica y simple para determinar el PM de proteínas. Figura 5. Determinación del PM de una proteína desconocida mediante SDS-PAGE. (a) En el carril 1 se corrió un estándar de PM y en el carril 2 la proteína desconocida. (b) Se grafica el log PM de las proteínas del estándar en función de sus Rf. Mediante el valor de Rf de la proteína desconocida se obtiene su PM. Algunas proteínas no tienen un comportamiento normal en SDS-PAGE. Las glicoproteínas no unen la cantidad SDS promedio y las estimaciones del PM aparente deben hacerse con mucho cuidado. Los pesos moleculares pueden ser sobrestimados hasta en un 30%. En el caso de las proteínas extremadamente cargadas positivas como las histonas, una cantidad significativa de las cargas pertenecientes al SDS unido está balanceada por las cargas propias de la proteína, lo que hace difícil la estimación de su PM aparente. Las proteínas muy ácidas como la pepsina, papaina y glucosa oxidasa unen cantidades mucho menores de SDS. 6
7 Debe tenerse en cuenta que este método de separación, al desnaturalizar las proteínas, hace que pierdan su actividad biológica. Existen algunas proteínas con estabilidad poco común que mantienen su actividad en presencia de SDS y en otros casos ciertas proteínas pueden recuperar su actividad al cambiar este detergente fuerte por otro más débil. Cuadro 3. Masa molecular y peso molecular La masa molecular (M) se expresa en Daltons (Da). Un Da se define como 1/12 la masa del 12 C. El peso molecular no es lo mismo que la masa molecular. También se conoce como masa molecular relativa (Mr). El peso molecular se define como la proporción de la masa de una macromolécula al 1/12 de la masa del átomo 12 C. Es una cantidad adimensionada. Es incorrecto expresar un peso molecular o Mr en Da, pero de todas maneras se encuentra en la literatura el peso molecular expresado en kilodaltons. Isoelectroenfoque (IEF) Es una técnica electroforética en la cual son fraccionados compuestos anfóteros de acuerdo a su PI a lo largo de un gradiente de ph continuo. Las proteínas (polianfolitos) migrarán hacia el ánodo o cátodo de acuerdo a su carga neta hasta alcanzar la región del gradiente de ph que coincida con su PI. A ph igual a su PI tendrán carga neta cero, no podrán migrar y se concentrarán o enfocarán en zonas estrechas. El gradiente de ph en el gel puede lograrse mediante un sistema buffer con anfolitos transportadores o mediante un sistema de gradiente de ph inmovilizado. El IEF es una técnica de equilibro y el resultado no depende (dentro de límites razonables) del modo de aplicación de la muestra, la carga total de proteína o el tiempo de corrida. Permite determinar un parámetro fisicoquímico intrínseco de las proteínas: su PI. Se alcanzan excelentes resoluciones de proteínas cuyos PI difieren sólo en 0,02 unidades de ph; las bandas de proteína son muy nítidas debido al efecto de enfocado. Luego de una corrida de IEF el gradiente de ph en el gel puede ser medido tanto utilizando un electrodo con membrana para superficies como cortando el gel en pequeños intervalos, eluyendo las muestras de cada trozo y midiendo su ph. Otra alternativa es usar una mezcla de proteínas estándar de PI conocidos para calibrar el gradiente de ph alcanzado durante el IEF. Electroforesis bidimensional Los métodos analizados anteriormente separan mezclas complejas de proteínas y bajo condiciones óptimas pueden resolver hasta 100 zonas diferentes. En los años recientes, se ha vuelto necesario analizar muestras de mayor complejidad como aquellas procedentes de células enteras o tejidos. Este nivel de complejidad no puede analizarse por ninguno de los procedimientos electroforéticos en una dimensión. Además, en cualquiera de estos procedimientos la separación se basa en una única propiedad fisicoquímica (tamaño, carga). En consecuencia, por ejemplo, si se realizó una SDS-PAGE, las bandas obtenidas luego de la separación contendrán todas las proteínas de la muestra con igual PM, que no necesariamente serán una misma proteína. La electroforesis bidimensional resulta de la combinación de dos técnicas electroforéticas en una dimensión en un procedimiento en dos dimensiones. La combinación más usada es realizar un IEF en la primera dimensión y a continuación un SDS-PAGE en la segunda dimensión (figura 6), resultando en una separación basada en dos propiedades fisicoquímicas independientes (carga y tamaño). Esta metodología se ha adaptado a un amplio rango de muestras. Electroforesis capilar Es una técnica surgida recientemente, más rápida y sensible que la electroforesis en gel. La separación electroforética ocurre en capilares de μm de diámetro y 20-60cm de largo. Debido a que la resistencia es grande dada la pequeña sección de los capilares, es posible aplicar 7
8 gradientes de voltaje bastante altos sin que la corriente se incremente demasiado. Esto hace que la separación sea rápida. Debido a que la capilaridad inhibe la mezcla por convección no es necesario utilizar soporte, aunque a veces se incorpora un soporte poroso para generar el efecto tamiz molecular. La detección se realiza por absorbancia UV o fluorescencia a medida que los componentes pasan por un punto determinado en el capilar. La sensibilidad es de fentomoles (10-15 ) con detección UV y zeptomoles (10 21 ) con detección fluorescente. Figura 6. Esquema de un experimento de electroforesis bidimensional en la que se combina IEF en la primera dimensión y SDS-PAGE en la segunda. Métodos de detección de proteínas en el gel Luego de realizada la separación electroforética es necesario visualizar y, en algunos casos, cuantificar las bandas proteicas en el gel. A continuación se describen brevemente algunas de las técnicas más utilizadas. Tinción con colorantes orgánicos El gel es embebido en una solución de colorante que se une a las proteínas. Para la visualización de las bandas proteicas es necesario desteñir el gel con el solvente utilizado para disolver el colorante. Azul de Coomasie (Coomasie Brillant Blue, CBB): Es el método más común de tinción de proteínas. El CBB es un colorante orgánico que en medio ácido se une a las proteínas mediante interacciones electrostáticas con los grupos amino. Luego de teñido y desteñido el gel las 8
9 proteínas se visualizan como bandas azules. La tinción con CBB es simple pero presenta baja sensibilidad; se pueden detectar hasta 0,2 0,5 μg de proteína por banda. Amido Black: Es un colorante orgánico que permite teñir proteínas con una sensibilidad 3 veces menor que la tinción con CBB. Tinción con sales de plata Los procedimientos de tinción con plata se basan en la reducción de la plata y se pueden agrupar en dos categorías. Los métodos alcalinos se basan en el uso de plata amoniacal o como solución diamina. Los iones de plata complejados con las proteínas son reducidos por formaldehído en medio ácido. En el segundo grupo de métodos, se usa una solución débilmente ácida de nitrato de plata para embeber el gel. El revelado se logra por la reducción selectiva de los iones plata a plata metálica por formaldehído en medio alcalino. La tinción con plata es monocromática, produciendo bandas de color marrón oscuro. La sensibilidad es su gran ventaja siendo veces mayor que con CBB y pudiéndose detectar hasta 0,1 ng de proteína por banda. Entre las desventajas se encuentra el alto costo, el hecho de ser un método laborioso, lento y poco reproducible y que no todas las proteínas se tiñen. Marcado con colorantes fluorescentes Se han desarrollado métodos en los que las proteínas son marcadas con colorantes fluorescentes antes de la corrida electroforética y las bandas proteicas son detectadas mediante escaneo. El colorante más usado es la fluorescamina. Las mayores ventajas de este reactivo son su alta sensibilidad (se pueden detectar aproximadamente 5 ng de proteína unida a fluorescamina) y la facilidad de poder monitorear el avance de la separación electroforética exponiendo el gel a luz UV. Otros marcadores fluorescentes usados son MDPF (2-metoxi-2, 4-difenil-3(2H)-furanona), que en geles de poliacrilamida mantienen la fluorescencia por algunos meses y el o-ftaldialdehido (OPA) que presenta una sensibilidad 10 veces mayor que la fluorescamina. Las bandas proteicas también pueden ser detectadas mediante unión a colorantes fluorescentes luego de realizada la electroforesis. Las moléculas usadas son ANS (1-anilina-8-sulfonato de naftaleno) y OPA. Marcado con moléculas radioactivas Se han desarrollado procedimientos por los que se realiza el marcado de las muestras con isótopos radiactivos tanto antes de la separación electroforética como luego de la misma mediante marcado in situ de las bandas proteicas separadas en la matriz. En comparación con los métodos de teñido con colorantes, el uso de marcado radiactivo ofrece algunas ventajas como mayor sensibilidad y en condiciones que pueden ser no desnaturalizantes de forma que los componentes separados pueden ser extraídos manteniendo su actividad biológica. El revelado generalmente se realiza poniendo en contacto el gel con una película de rayos-x durante un tiempo apropiado (autorradiografía). Revelado específico de enzimas Esta técnica consiste en ensayar la actividad enzimática directamente en el gel o recortar y eluir las bandas proteicas separadas y entonces ensayar la actividad enzimática en solución. En el primer caso, luego de la separación electroforética el gel se pone en contacto con una solución apropiada del sustrato (coloreado o fluorescente) o un soporte impregnado con el mismo. Transcurrido el tiempo de reacción adecuado se detecta el producto de la reacción enzimática. Mediante este tipo de revelado es posible identificar las bandas que presentan actividad enzimática del total de bandas proteicas obtenidas en la separación. Western blotting Este procedimiento consiste en transferir las proteínas separadas electroforéticamente desde el gel a una matriz, generalmente nitrocelulosa o membranas de difluoruro de polivinilideno (PVDF). 9
10 Estas matrices son más manejables y permiten el revelado mediante cualquier método general para proteínas. Es posible, además, localizar proteínas de interés mediante anticuerpos específicos para ellas. Debido a que la unión antígeno-anticuerpo es específica se logra de esta forma identificar la proteína buscada. Aplicaciones de la electroforesis de proteínas La electroforesis de proteínas en todas sus variables, tiene numerosas aplicaciones que incluyen: - determinación del peso molecular aparente de las proteínas - identificación de proteínas - control de pureza de una muestra - identificación de puentes disulfuro - cuantificación de proteínas - determinación de pi - estudio de isoformas - estudio de multisubunidades La electroforesis es frecuentemente usada en el diagnóstico clínico. En el suero humano se encuentran las proteínas albúmina, alfa-, beta- y gama- globulinas. La variación en la cantidad relativa de estas proteínas se asocia a algunas patologías. Mediante electroforesis en acetato de celulosa, estas proteínas pueden separarse y cuantificarse para diagnosticar ciertas enfermedades. Además, es empleada como herramienta en estudios evolutivos, taxonómicos, genéticos y de biología de la conservación. La electroforesis de proteínas ha permitido ampliar el conocimiento existente sobre las relaciones de parentesco entre las especies, así como conocer la diversidad y variabilidad genética de las poblaciones y la manera en que se relacionan filogenéticamente. Esto se ha realizado estudiando las aloenzimas (formas alternativas de una enzima codificada por diferentes alelos del mismo locus), las cuales presentan movilidad diferencial en una electroforesis. Algunos ejemplos: - Los patrones de proteínas presentes en la pared celular de levaduras obtenidos por SDS-PAGE han sido utilizados para la identificación de especies. - Las gliadinas son un grupo heterogéneo de proteínas que se encuentran en plantas de trigo. La electroforesis en gel ha sido utilizada para examinar la composición de estas proteínas en diferentes genotipos de trigo, ya que están relacionadas a la taxonomía y evolución de esta especie, así como a su calidad para la elaboración de pan. Bibliografía Andrews, A. Electrophoresis. Theory, Techniques an Biochemical and Clinical Applications (2a edición). Editado por Clarendon Press, Oxford, Dunn, MJ. Gel Electrophoresis: proteins. BIOS Scientific Publishers Limited, 1993, Oxford. Hames,BD & Rickwood D, editores. Gel Electrophoresis of Proteins. A Practical Approach (2a edición). IRL Press, Oxford & New York, Jakoby. Enzyme Purification and Related Techniques En: Methods in Enzymology, vol 104, Part C. Academic Pess, Inc, Laas, Torgny. Electrophoresis in gel En: Protein Purification, Hight-Resolution Methods, and Applications, pp (Segunda edición). Editado por Jan-Christer Janson & Lars Rydén. Wiley-VCH Inc., New York,
11 Análisis de proteínas por electroforesis en geles de poliacrilamida con SDS ( SDS_PAGE) Objetivos: En esta práctica se evaluará el proceso de purificación de lisozima mediante el análisis por SDS- PAGE de las fracciones obtenidas en la práctica anterior. En particular analizaremos -la composición proteica de cada una de las fracciones de la cromatografía de intercambio iónico -el grado de pureza de la fracción F2 obtenida -el peso molecular aparente de la proteína purificada. Reactivos: - Solución Acrilamida: Acrilamida 30%, N,N metilrnbisacrilamida 0.8%. - Buffer I (4X): Tris. HCl 1.5 M, SDS 0.4 %, ph Buffer II (4X): Tris HCl 0.5 M, SDS 0.4 %, ph TEMED: N,N,N,N, tetrametilendiamina. - Buffer de corrida (10X): Tris 50 mm, glicina 384 mm, SDS 10% - Buffer de muestra (4X): 1.52g Tris base, 2g SDS, 2mL 2-mercaptoetanol, 20mL glicerol, 1mg Azul de bromofenol, Ajustar ph 6.8, H 2 O csp 50mL. - Solución colorante de Coomasie: 2g Coomasie Brillant Blue R-250, 300mL etanol, 70mL ácido acético glacial y agua csp 1,0 L. Preparación del gel: 1- Se arman las placas molde del gel de forma vertical. 2- Para un gel separador al 12% de 10 cm X 8 cm X 1 mm, mezclar: 3 ml Solución acrilamida 1,875 ml Buffer I 2,6mL agua 0.5 ml glicerol 25 μl APS 7 μl TEMED 3- Se transfiere esta solución, con ayuda de una pipeta al molde, se dejan 2 cm aprox. del molde sin llenar. Se deja polimerizar (15-30min). 4- Una vez polimerizado el gel separador, se prepara el gel concentrador. Se mezclan: 0.35 ml Solución acrilamida 0.65 ml Buffer II 1,5 ml agua 10 μl APS 5 μl TEMED 5- Se coloca el peine en los 2 cm del molde sin gel y se transfiere la nueva solución a molde del gel. Se deja polimerizar (15-30min). Preparación de la muestra: 1- Mezclar un volumen de Buffer de muestra con 3 volúmenes de muestra 2- Calentar en baño de agua a ebullición durante 5 minutos Corrida electroforética: 1- Una vez polimerizado, colocar el gel en la cuba de electroforesis. 2- Quitar los peines. 3- Agregar el buffer de corrida hasta cubrir totalmente los pocillos y en la cuba inferior 4- Cargar 10 μl de muestra por pocillo. Anotar el orden en que se cargaron las muestras. 11
12 5- Encender la fuente de poder y realizar la corrida a 120V (70 min aprox) 6- Finalizada la corrida, desconectar el equipo, quitar el buffer en la cuba superior y sacar las placas de las cubas. 7- Desmoldar los geles de las placas cuidadosamente, marcar la esquina derecha de cada gel cortando una punta con la espátula 8- Sumergir el gel en la solución colorante durante 5-10 minutos. 9- Retirar la solución colorante (no descartarla), y agregar al recipiente con el gel agua caliente agitando hasta que se satura con colorante. Cambiar el agua y repetir hasta que se observen bandas proteicas azules en un fondo transparente. Preguntas 1. Indique en qué se basa la separación en las siguientes técnicas electroforéticas: a. Electroforesis nativa b. SDS-PAGE c. IEF 2. Se obtienen los siguientes resultados de un SDS-PAGE de una muestra que contiene una proteína aislada: a) La muestra previamente tratada con 2-mercaptoetanol muestra un patrón con dos bandas que migraron 10,0 y 10,6 cm respectivamente. b) Una serie de proteínas estándar migraron según se muestra: PM distancia (cm) seralbumina bovina ovalbumina anhidrasa carbonica inh. de tripsina alfa-lactalbumina c) El azul de bromofenol migró una distancia de 12 cm. Teniendo en cuenta estos resultados qué podría decir sobre la estructura cuaternaria de la proteína de la muestra?. 12
Monitoreo de un proceso de purificación de proteínas. Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa
 Monitoreo de un proceso de purificación de proteínas Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa Qué es la electroforesis? Es la técnica que permite la separación
Monitoreo de un proceso de purificación de proteínas Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa Qué es la electroforesis? Es la técnica que permite la separación
MONITOREO DE UN PROCESO DE PURIFICACIÓN DE PROTEÍNAS. Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa
 MONITOREO DE UN PROCESO DE PURIFICACIÓN DE PROTEÍNAS Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa Qué es la electroforesis? Es la técnica que permite la separación
MONITOREO DE UN PROCESO DE PURIFICACIÓN DE PROTEÍNAS Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa Qué es la electroforesis? Es la técnica que permite la separación
MONITOREO DE UN PROCESO DE PURIFICACIÓN DE PROTEÍNAS. Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa.
 MONITOREO DE UN PROCESO DE PURIFICACIÓN DE PROTEÍNAS Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa. Qué es la electroforesis? Es la técnica que permite la
MONITOREO DE UN PROCESO DE PURIFICACIÓN DE PROTEÍNAS Corrimiento electroforético de las muestras de la purificación de la lactato deshidrogenasa. Qué es la electroforesis? Es la técnica que permite la
ELECTROFORESIS EN GEL DE POLIACRILAMIDA CON SDS SDS-PAGE
 1. FUNDAMENTO TEÓRICO ELECTROFORESIS EN GEL DE POLIACRILAMIDA CON SDS SDS-PAGE Departamento de Bioquímica La electroforesis es una técnica de separación de moléculas cargadas por migración en un campo
1. FUNDAMENTO TEÓRICO ELECTROFORESIS EN GEL DE POLIACRILAMIDA CON SDS SDS-PAGE Departamento de Bioquímica La electroforesis es una técnica de separación de moléculas cargadas por migración en un campo
GENERALIDADES Y APLICACIONES DE LA ELECTROFORESIS. Influencia de campo cargado eléctricamente Movimiento al cátodo (-) o al anodo (+)
 GENERALIDADES Y APLICACIONES DE LA ELECTROFORESIS Electroforésis Separación de especies cargadas (anión (-) y catión (+) ) Influencia de campo cargado eléctricamente Movimiento al cátodo (-) o al anodo
GENERALIDADES Y APLICACIONES DE LA ELECTROFORESIS Electroforésis Separación de especies cargadas (anión (-) y catión (+) ) Influencia de campo cargado eléctricamente Movimiento al cátodo (-) o al anodo
ELECTROFORESIS Q U Í M I C A B I O L Ó G I C A. D E P A R T A M E N T O D E B Q C A. F C N Y C S. U N P S J B
 ELECTROFORESIS Q U Í M I C A B I O L Ó G I C A. D E P A R T A M E N T O D E B Q C A. F C N Y C S. U N P S J B 2 0 1 7 Que es la electroforesis? Qué permite analizar? Que factores influyen? Separar y analizar
ELECTROFORESIS Q U Í M I C A B I O L Ó G I C A. D E P A R T A M E N T O D E B Q C A. F C N Y C S. U N P S J B 2 0 1 7 Que es la electroforesis? Qué permite analizar? Que factores influyen? Separar y analizar
Electroforesis de proteínas
 Electroforesis de proteínas Introducción general La electroforesis es un método de separación basado en la tasa diferencial de migración de especies cargadas al estar en un campo eléctrico de DC La electroforesis
Electroforesis de proteínas Introducción general La electroforesis es un método de separación basado en la tasa diferencial de migración de especies cargadas al estar en un campo eléctrico de DC La electroforesis
ELECTROFORESIS EN GEL DE POLIACRILAMIDA CON SDS SDS-PAGE
 Departamento de Biología de Sistemas Unidad Docente de Bioquímica y Biología Molecular ELECTROFORESIS EN GEL DE POLIACRILAMIDA CON SDS SDS-PAGE 1. FUNDAMENTO TEÓRICO La electroforesis es una técnica de
Departamento de Biología de Sistemas Unidad Docente de Bioquímica y Biología Molecular ELECTROFORESIS EN GEL DE POLIACRILAMIDA CON SDS SDS-PAGE 1. FUNDAMENTO TEÓRICO La electroforesis es una técnica de
Electroforesis de proteínas en geles de poliacrilamida
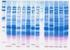 Electroforesis de proteínas en geles de poliacrilamida Electroforesis de proteínas en geles de poliacrilamida: Introducción y técnica básica La electroforesis de proteínas en geles con una matriz de poliacrilamida,
Electroforesis de proteínas en geles de poliacrilamida Electroforesis de proteínas en geles de poliacrilamida: Introducción y técnica básica La electroforesis de proteínas en geles con una matriz de poliacrilamida,
Introducción. Electroforesis zonal Campo aplicado a un soporte estabilizante Muestra dispuesta sobre una zona reducida del soporte
 Introducción Técnica analítica separativa: Transporte de moléculas cargadas bajo la acción de un campo eléctrico Movilidad electroforética depende de: La carga de la molécula Depende del medio ph Fuerza
Introducción Técnica analítica separativa: Transporte de moléculas cargadas bajo la acción de un campo eléctrico Movilidad electroforética depende de: La carga de la molécula Depende del medio ph Fuerza
Trabajo Práctico 5: Electroforesis de proteínas Electroforesis de proteínas en Acetato de celulosa
 Trabajo Práctico 5: Electroforesis de proteínas Electroforesis de proteínas en Acetato de celulosa OBJETIVO: -Realizar electroforesis de las proteínas presentes en suero utilizando acetato de celulosa
Trabajo Práctico 5: Electroforesis de proteínas Electroforesis de proteínas en Acetato de celulosa OBJETIVO: -Realizar electroforesis de las proteínas presentes en suero utilizando acetato de celulosa
Tema 6 Cuantificación de proteínas
 Tema 6 Cuantificación de proteínas Procedimiento de estudio de proteínas Selección de fuente Fraccionamiento de células Centrifugación Cromatografía Cromatografía en capa fina Cromatografía en columna
Tema 6 Cuantificación de proteínas Procedimiento de estudio de proteínas Selección de fuente Fraccionamiento de células Centrifugación Cromatografía Cromatografía en capa fina Cromatografía en columna
ELECTROFORESIS GENERALIDADES Y APLICACIONES CLINICAS
 ELECTROFORESIS GENERALIDADES Y APLICACIONES CLINICAS Marcelo Castillo Navarrrete, T.M. MsCs (C) Facultad de Medicina Carrera Tecnología Médica 18 de Noviembre de 2004 Fundamentos de Electroforesis Alta
ELECTROFORESIS GENERALIDADES Y APLICACIONES CLINICAS Marcelo Castillo Navarrrete, T.M. MsCs (C) Facultad de Medicina Carrera Tecnología Médica 18 de Noviembre de 2004 Fundamentos de Electroforesis Alta
ELECTROFORESIS. Objetivo de la clase. *fundamentos *procedimientos *algunas aplicaciones. Conocer los métodos electroforéticos
 ELECTROFORESIS Objetivo de la clase Conocer los métodos electroforéticos *fundamentos *procedimientos *algunas aplicaciones Definición de electroforesis Proceso de separación que se basa en la diferente
ELECTROFORESIS Objetivo de la clase Conocer los métodos electroforéticos *fundamentos *procedimientos *algunas aplicaciones Definición de electroforesis Proceso de separación que se basa en la diferente
DESARROLLO COGNOSCITIVO Y APRENDIZAJE
 Prof. Jhonis Valbuena Cátedra: Análisis Instrumental La Electrofóresis es un método de la Química Analítica que utiliza corriente eléctrica controlada con la finalidad de separar biomolèculas según su
Prof. Jhonis Valbuena Cátedra: Análisis Instrumental La Electrofóresis es un método de la Química Analítica que utiliza corriente eléctrica controlada con la finalidad de separar biomolèculas según su
Purificación de la enzima lactato deshidrogenasa de músculo esquelético de pollo
 Purificación de la enzima lactato deshidrogenasa de músculo esquelético de pollo ESQUEMA GENERAL Sesión 1. Extracción y precipitación con sulfato de amonio. Sesión 2. Purificación por cromatografía Sesión
Purificación de la enzima lactato deshidrogenasa de músculo esquelético de pollo ESQUEMA GENERAL Sesión 1. Extracción y precipitación con sulfato de amonio. Sesión 2. Purificación por cromatografía Sesión
ANEXOS A: Procedimientos experimentales
 ANEXOS 1 ANEXOS A: Procedimientos experimentales SDS-TRIS-GLICINA-PAGE Procedimiento A.1. Descripción del método de preparación de geles de poliacrilamida. Se trata de un sistema vertical de electroforesis,
ANEXOS 1 ANEXOS A: Procedimientos experimentales SDS-TRIS-GLICINA-PAGE Procedimiento A.1. Descripción del método de preparación de geles de poliacrilamida. Se trata de un sistema vertical de electroforesis,
BIOLOGIA CELULAR Y MOLECULAR. LABORATORIO No 9: ELECTROFORESIS EN GELES DE POLIACRILAMIDA (SDS-PAGE)
 BIOLOGIA CELULAR Y MOLECULAR LABORATORIO No 9: ELECTROFORESIS EN GELES DE POLIACRILAMIDA (SDS-PAGE) 1. INTRODUCCIÓN Uno de los métodos que permite la purificación y separación de proteínas de un organismo
BIOLOGIA CELULAR Y MOLECULAR LABORATORIO No 9: ELECTROFORESIS EN GELES DE POLIACRILAMIDA (SDS-PAGE) 1. INTRODUCCIÓN Uno de los métodos que permite la purificación y separación de proteínas de un organismo
PRÁCTICA 9 ELECTROFORESIS EN GEL DE AGAROSA
 INTRODUCCIÓN PRÁCTICA 9 ELECTROFORESIS EN GEL DE AGAROSA La electroforesis es una técnica que permite separar moléculas cargadas eléctricamente, entre las cuales se encuentran los ácidos nucleicos (DNA
INTRODUCCIÓN PRÁCTICA 9 ELECTROFORESIS EN GEL DE AGAROSA La electroforesis es una técnica que permite separar moléculas cargadas eléctricamente, entre las cuales se encuentran los ácidos nucleicos (DNA
Diagnóstico Avanzado en Enfermedades Tropicales
 Diagnóstico Avanzado en Enfermedades Tropicales Máster universitario en Enfermedades Tropicales Código 302731 (3 créditos ECTS) Área de Parasitología Departamento de Biología Animal, Parasitología, Ecología,
Diagnóstico Avanzado en Enfermedades Tropicales Máster universitario en Enfermedades Tropicales Código 302731 (3 créditos ECTS) Área de Parasitología Departamento de Biología Animal, Parasitología, Ecología,
CROMATOGRAFÍA. A.- INTERCAMBIO IONICO: A.1. ANIONICA A.2. CATIONCA B.- FILTRACIÓN EN GEL
 CROMATOGRAFÍA. A.- INTERCAMBIO IONICO: A.1. ANIONICA A.2. CATIONCA B.- FILTRACIÓN EN GEL C.- AFINIDAD B. CROMATOGRAFÍA DE FILTRACIÓN EN GEL. 1. Principios. No requiere la unión de la proteína, lo cual
CROMATOGRAFÍA. A.- INTERCAMBIO IONICO: A.1. ANIONICA A.2. CATIONCA B.- FILTRACIÓN EN GEL C.- AFINIDAD B. CROMATOGRAFÍA DE FILTRACIÓN EN GEL. 1. Principios. No requiere la unión de la proteína, lo cual
Easy PDF Creator is professional software to create PDF. If you wish to remove this line, buy it now.
 1 Virología y Micología Veterinaria Trabajo Práctico No. 4 ELECTROFORESIS La electroforesis es una técnica utilizada para separar grandes moléculas por tamaño a través de la aplicación de un campo eléctrico
1 Virología y Micología Veterinaria Trabajo Práctico No. 4 ELECTROFORESIS La electroforesis es una técnica utilizada para separar grandes moléculas por tamaño a través de la aplicación de un campo eléctrico
TP3: Electroforesis en gel de poliacrilamida
 Objetivos TP3: Electroforesis en gel de poliacrilamida Comparar los perfiles proteicos obtenidos mediante SDS-PAGE. Calcular la movilidad electroforética de diferentes bandas proteicas. Introducción La
Objetivos TP3: Electroforesis en gel de poliacrilamida Comparar los perfiles proteicos obtenidos mediante SDS-PAGE. Calcular la movilidad electroforética de diferentes bandas proteicas. Introducción La
Proceso que cuenta con varias etapas cuyo objetivo es separar una proteína de interés de una mezcla de proteínas.
 Proceso que cuenta con varias etapas cuyo objetivo es separar una proteína de interés de una mezcla de proteínas. La selección de técnicas de purificación depende de las propiedades de las proteínas. Características
Proceso que cuenta con varias etapas cuyo objetivo es separar una proteína de interés de una mezcla de proteínas. La selección de técnicas de purificación depende de las propiedades de las proteínas. Características
PROPIEDADES FISICOQUÍMICAS DE LOS ÁCIDOS NUCLEICOS. Es un ácido capaz de formar sales con iones cargados
 Extracción de ADN Genética molecular PROPIEDADES FISICOQUÍMICAS DE LOS ÁCIDOS NUCLEICOS Es un ácido capaz de formar sales con iones cargados positivamente (cationes). Es soluble en soluciones concentradas
Extracción de ADN Genética molecular PROPIEDADES FISICOQUÍMICAS DE LOS ÁCIDOS NUCLEICOS Es un ácido capaz de formar sales con iones cargados positivamente (cationes). Es soluble en soluciones concentradas
Técnicas de Estudio de las células
 Técnicas de Estudio de las células Microscopia Preparaciones permanentes: Fijación Deshidratación Inclusión Corte Fijación: Acidos, solventes orgánicos como alcohol, aldehídos (Formaldehído, glutaraldehídos)
Técnicas de Estudio de las células Microscopia Preparaciones permanentes: Fijación Deshidratación Inclusión Corte Fijación: Acidos, solventes orgánicos como alcohol, aldehídos (Formaldehído, glutaraldehídos)
Técnicas de Caracterización y purificación
 Técnicas de Caracterización y purificación hidrofobicidad carga Propiedades de las proteínas utilizadas para caracterizar y purificar Carga Tamaño Forma Actividad biologica Hidrofobicidad PM Estabilidad
Técnicas de Caracterización y purificación hidrofobicidad carga Propiedades de las proteínas utilizadas para caracterizar y purificar Carga Tamaño Forma Actividad biologica Hidrofobicidad PM Estabilidad
 TRABAJO PRACTICO Nº 3. PROTEINAS Y ENZIMAS. www.fcn.unp.edu.ar/sitio/farmacognosia/ Objetivo - Utilizar reacciones generales y técnicas de extracción y separación adecuadas para el análisis de proteínas
TRABAJO PRACTICO Nº 3. PROTEINAS Y ENZIMAS. www.fcn.unp.edu.ar/sitio/farmacognosia/ Objetivo - Utilizar reacciones generales y técnicas de extracción y separación adecuadas para el análisis de proteínas
PRACTICA LABORATORIO Nº 1 PROPIEDADES DE LAS PROTEINAS.
 UNIVERSIDAD CENTRAL DE VENEZUELA FACULTAD DE AGRONOMIA DEPARTAMENTO DE QUIMICA Y TECNOLOGIA CATEDRA DE BIOQUÍMICA PRACTICA LABORATORIO Nº 1 PROPIEDADES DE LAS PROTEINAS. INTRODUCCIÓN Las proteínas son
UNIVERSIDAD CENTRAL DE VENEZUELA FACULTAD DE AGRONOMIA DEPARTAMENTO DE QUIMICA Y TECNOLOGIA CATEDRA DE BIOQUÍMICA PRACTICA LABORATORIO Nº 1 PROPIEDADES DE LAS PROTEINAS. INTRODUCCIÓN Las proteínas son
ELECTROFORESIS Fundamento.
 ELECTROFORESIS La electroforesis es un método de laboratorio en el que se utiliza una corriente eléctrica controlada con la finalidad de separar biomoleculas según su tamaño y carga eléctrica a través
ELECTROFORESIS La electroforesis es un método de laboratorio en el que se utiliza una corriente eléctrica controlada con la finalidad de separar biomoleculas según su tamaño y carga eléctrica a través
FUNDAMENTOS. ELECTROFORESIS/ Versión 3.0/ MÓDULO 3/ CÁTEDRA DE FÍSICA/ FFYB/ UBA/
 FUNDAMENTOS. ELECTROFORESIS/ Versión 3.0/ MÓDULO 3/ CÁTEDRA DE FÍSICA/ FFYB/ UBA/ La electroforesis es una técnica separativa que se basa en el fenómeno de migración diferencial que experimentan partículas
FUNDAMENTOS. ELECTROFORESIS/ Versión 3.0/ MÓDULO 3/ CÁTEDRA DE FÍSICA/ FFYB/ UBA/ La electroforesis es una técnica separativa que se basa en el fenómeno de migración diferencial que experimentan partículas
Práctica: Electroforesis de DNA y transferencia a membranas de celulosa o nylon.
 Biología Celular y Molecular para Medicina Jorge Contreras Pineda Práctica: Electroforesis de DNA y transferencia a membranas de celulosa o nylon. GENERALIDADES La electroforesis es una técnica de laboratorio
Biología Celular y Molecular para Medicina Jorge Contreras Pineda Práctica: Electroforesis de DNA y transferencia a membranas de celulosa o nylon. GENERALIDADES La electroforesis es una técnica de laboratorio
Universidad de la República Oriental del Uruguay Facultad de Ingeniería Instituto de Ingeniería Eléctrica MANUAL DE USUARIO ELECTROFORESIS
 Universidad de la República Oriental del Uruguay Facultad de Ingeniería Instituto de Ingeniería Eléctrica MANUAL DE USUARIO ELECTROFORESIS DICIEMBRE 2006 Tratamiento de Imágenes por Computadora Proyecto
Universidad de la República Oriental del Uruguay Facultad de Ingeniería Instituto de Ingeniería Eléctrica MANUAL DE USUARIO ELECTROFORESIS DICIEMBRE 2006 Tratamiento de Imágenes por Computadora Proyecto
TEMA 6: PROTEÍNAS. Definición de proteínas y aminoácidos
 TEMA 6: PROTEÍNAS Dra. Mariana L. Ferramola Bioquímica Lic. en Enfermería 2016 Definición de proteínas y aminoácidos Las proteínas son macromoléculas de gran abundancia. Son polímeros formados por monómeros
TEMA 6: PROTEÍNAS Dra. Mariana L. Ferramola Bioquímica Lic. en Enfermería 2016 Definición de proteínas y aminoácidos Las proteínas son macromoléculas de gran abundancia. Son polímeros formados por monómeros
CROMATOGRAFÍA DE AMINOÁCIDOS
 CROMATOGRAFÍA DE AMINOÁCIDOS Electroforesis.- Es un método de laboratorio en el que se utiliza una corriente eléctrica controlada con la finalidad de separar aminoácidos (y otras biomoléculas) según su
CROMATOGRAFÍA DE AMINOÁCIDOS Electroforesis.- Es un método de laboratorio en el que se utiliza una corriente eléctrica controlada con la finalidad de separar aminoácidos (y otras biomoléculas) según su
PARTE II REVISIÓN DE MÉTODOS ESPECTROSCÓPICOS Y ELABORACIÓN DE CURVA ESTÁNDTAR DE PROTEÍNA
 PARTE II REVISIÓN DE MÉTODOS ESPECTROSCÓPICOS Y ELABORACIÓN DE CURVA ESTÁNDTAR DE PROTEÍNA OBJETIVOS Aplicar un método espectrofotométrico para medir la concentración de una proteína. Conocer el manejo
PARTE II REVISIÓN DE MÉTODOS ESPECTROSCÓPICOS Y ELABORACIÓN DE CURVA ESTÁNDTAR DE PROTEÍNA OBJETIVOS Aplicar un método espectrofotométrico para medir la concentración de una proteína. Conocer el manejo
Transferencia de material genético II. 1) Aislamiento de plásmidos Lisis alcalina
 Transferencia de material genético II 1) Aislamiento de plásmidos Lisis alcalina ESQUEMA GENERAL SESIÓN I: TRANSFORMAR cepas de E. coli con un plásmido. Verificar que hay células transformantes de acuerdo
Transferencia de material genético II 1) Aislamiento de plásmidos Lisis alcalina ESQUEMA GENERAL SESIÓN I: TRANSFORMAR cepas de E. coli con un plásmido. Verificar que hay células transformantes de acuerdo
REVISIÓN DE MÉTODOS ESPECTROSCÓPICOS Y ELABORACIÓN DE CURVA ESTÁNDAR DE PROTEÍNA
 REVISIÓN DE MÉTODOS ESPECTROSCÓPICOS Y ELABORACIÓN DE CURVA ESTÁNDAR DE PROTEÍNA OBJETIVOS Aplicar un método espectrofotométrico para medir la concentración de una proteína. Conocer el manejo de micropipetas
REVISIÓN DE MÉTODOS ESPECTROSCÓPICOS Y ELABORACIÓN DE CURVA ESTÁNDAR DE PROTEÍNA OBJETIVOS Aplicar un método espectrofotométrico para medir la concentración de una proteína. Conocer el manejo de micropipetas
ELECTROFORESIS EN GELES DE POLIACRILAMIDA SDS-PAGE. Presencia de Sodio Dodecil Sulfato bajo condiciones reductoras (SDSPAGE)
 ELECTROFORESIS EN GELES DE POLIACRILAMIDA SDSPAGE Presencia de Sodio Dodecil Sulfato bajo condiciones reductoras (SDSPAGE) Método rápido, reproducible y de bajo costo Utilizado para cuantificar, comparar
ELECTROFORESIS EN GELES DE POLIACRILAMIDA SDSPAGE Presencia de Sodio Dodecil Sulfato bajo condiciones reductoras (SDSPAGE) Método rápido, reproducible y de bajo costo Utilizado para cuantificar, comparar
PURIFICACIÓN DE PROTEÍNAS
 PURIFICACIÓN DE PROTEÍNAS ESQUEMA DE PURIFICACIÓN DE UNA PROTEÍNA tejido vegetal animal homogeneizar cultivo celular bacterias levaduras células mamíferos PREPARACIÓN EXTRACTO crudo fraccionamiento subcelular
PURIFICACIÓN DE PROTEÍNAS ESQUEMA DE PURIFICACIÓN DE UNA PROTEÍNA tejido vegetal animal homogeneizar cultivo celular bacterias levaduras células mamíferos PREPARACIÓN EXTRACTO crudo fraccionamiento subcelular
Purificación de proteínas
 Purificación de proteínas Purificación Proceso que cuenta con varias etapas cuyo objetivo es lograr la concentración diferencial de la proteína o molécula de interés Condiciones generales a evaluar Calidad
Purificación de proteínas Purificación Proceso que cuenta con varias etapas cuyo objetivo es lograr la concentración diferencial de la proteína o molécula de interés Condiciones generales a evaluar Calidad
Los principales mecanismos que intervienen en la separación cromatográfica son:
 TP 8 CROMATOGRAFIA EN PAPEL, Introducción Los métodos cromatográficos son un conjunto de técnicas empleadas para separar compuestos químicos de una mezcla. Su nombre significa escribir con color ya que
TP 8 CROMATOGRAFIA EN PAPEL, Introducción Los métodos cromatográficos son un conjunto de técnicas empleadas para separar compuestos químicos de una mezcla. Su nombre significa escribir con color ya que
BIOLOGIA MOLECULAR. Dra. Ma. Laura Tondo
 TÉCNICAS BASADAS EN HIBRIDACIÓN MOLECULAR BIOLOGIA MOLECULAR 2016 Dra. Ma. Laura Tondo DESNATURALIZACION Y RENATURALIZACION DEL DNA Cómo se mantienen unidas las dos hebras del DNA? - Puentes de hidrógeno
TÉCNICAS BASADAS EN HIBRIDACIÓN MOLECULAR BIOLOGIA MOLECULAR 2016 Dra. Ma. Laura Tondo DESNATURALIZACION Y RENATURALIZACION DEL DNA Cómo se mantienen unidas las dos hebras del DNA? - Puentes de hidrógeno
Purificación de Proteínas Parte II
 Purificación de Proteínas Parte II Fase I. Obtención del extracto crudo Lisis celular. Válido para células sin pared celular como las células de tejidos animales, pero no es suficiente para células vegetales
Purificación de Proteínas Parte II Fase I. Obtención del extracto crudo Lisis celular. Válido para células sin pared celular como las células de tejidos animales, pero no es suficiente para células vegetales
TÉCNICAS DE ANÁLISIS GENÉTICO: Extracción de ADN.
 Trabajo Práctico 2.2 TÉCNICAS DE ANÁLISIS GENÉTICO: Extracción de ADN. Desde el reconocimiento del ADN como "la molécula de la vida", se conoce que en ella se encuentran cifradas las instrucciones que
Trabajo Práctico 2.2 TÉCNICAS DE ANÁLISIS GENÉTICO: Extracción de ADN. Desde el reconocimiento del ADN como "la molécula de la vida", se conoce que en ella se encuentran cifradas las instrucciones que
TP3: Electroforesis en gel de poliacrilamida
 TP3: Electroforesis en gel de poliacrilamida Objetivos Comparar las fracciones de proteínas obtenidas en el TP Nº2 mediante SDS-PAGE. Calcular la movilidad electroforética de diferentes bandas proteicas.
TP3: Electroforesis en gel de poliacrilamida Objetivos Comparar las fracciones de proteínas obtenidas en el TP Nº2 mediante SDS-PAGE. Calcular la movilidad electroforética de diferentes bandas proteicas.
PRACTICA CROMATOGRAFIA EN GEL Y CUANTIFICACIÓN DE PROTEÍNAS J.A. REIG. 1 de 20 2 de 10 1 moneda de 1 10 monedas monedas monedas de 0.
 PRACTICA CROMATOGRAFIA EN GEL Y CUANTIFICACIÓN DE PROTEÍNAS J.A. REIG Para saber lo que tengo debo separar las partes y cuantificar 1 de 20 2 de 10 1 moneda de 1 10 monedas 0.20 4 monedas 0.10 3 monedas
PRACTICA CROMATOGRAFIA EN GEL Y CUANTIFICACIÓN DE PROTEÍNAS J.A. REIG Para saber lo que tengo debo separar las partes y cuantificar 1 de 20 2 de 10 1 moneda de 1 10 monedas 0.20 4 monedas 0.10 3 monedas
PROTEINAS. Clasificación. Propiedades químicas.
 PROTEINAS Clasificación. Propiedades químicas. Son biopolímeros lineales formados por α L aminoácidos unidos por uniones peptídicas, formando heteropoliamidas de PM elevado, codificados genéticamente y
PROTEINAS Clasificación. Propiedades químicas. Son biopolímeros lineales formados por α L aminoácidos unidos por uniones peptídicas, formando heteropoliamidas de PM elevado, codificados genéticamente y
DETERMINACIÓN DEL PESO MOLECULAR DE PROTEÍNAS
 DETERMINACIÓN DEL PESO MOLECULAR DE PROTEÍNAS 6 grupos de estudiantes 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es desarrollar el conocimiento de la estructura de las proteínas y determinar
DETERMINACIÓN DEL PESO MOLECULAR DE PROTEÍNAS 6 grupos de estudiantes 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es desarrollar el conocimiento de la estructura de las proteínas y determinar
Al igual que en la centrifugación también hay dos criterios de separación con el mismo concepto:
 Electroforesis En la técnica de separación anterior hemos utilizado la fuerza centrífuga para que asociada a la diferencia de masa o densidad de las partículas a separar nos las diferencie, ahora vamos
Electroforesis En la técnica de separación anterior hemos utilizado la fuerza centrífuga para que asociada a la diferencia de masa o densidad de las partículas a separar nos las diferencie, ahora vamos
PRACTICO Nº 2 ENZIMOLOGÍA I
 PRACTICO Nº 2 ENZIMOLOGÍA I I. - INTRODUCCIÓN La mayoría de las reacciones químicas que ocurren en los sistemas vivos, si siguieran sus propios mecanismos, ocurrirían demasiado lentas. Se requiere de catalizadores
PRACTICO Nº 2 ENZIMOLOGÍA I I. - INTRODUCCIÓN La mayoría de las reacciones químicas que ocurren en los sistemas vivos, si siguieran sus propios mecanismos, ocurrirían demasiado lentas. Se requiere de catalizadores
CROMATOGRAFÍA. A.- INTERCAMBIO IONICO: A.1. ANIONICA A.2. CATIONCA B.- FILTRACIÓN EN GEL
 CROMATOGRAFÍA. A.- INTERCAMBIO IONICO: A.1. ANIONICA A.2. CATIONCA B.- FILTRACIÓN EN GEL C.- AFINIDAD A. CROMATOGRAFÍA DE INTERCAMBIO IÓNICO. Usos 1.- Purificar Proteínas 2.- Concentrar Proteínas Ventajas
CROMATOGRAFÍA. A.- INTERCAMBIO IONICO: A.1. ANIONICA A.2. CATIONCA B.- FILTRACIÓN EN GEL C.- AFINIDAD A. CROMATOGRAFÍA DE INTERCAMBIO IÓNICO. Usos 1.- Purificar Proteínas 2.- Concentrar Proteínas Ventajas
La solubilidad es la medida de la capacidad de disolverse una cierta sustancia en un determinado medio, a una temperatura y presión determinadas.
 La solubilidad es la medida de la capacidad de disolverse una cierta sustancia en un determinado medio, a una temperatura y presión determinadas. Las proteínas en disolución muestran grandes cambios en
La solubilidad es la medida de la capacidad de disolverse una cierta sustancia en un determinado medio, a una temperatura y presión determinadas. Las proteínas en disolución muestran grandes cambios en
MÉTODOS DE ESTUDIO DE PROTEÍNAS
 MÉTODOS DE ESTUDIO DE PROTEÍNAS ANÁLISIS DE EXPRESIÓN DE PROTEÍNAS Al estudiar la expresión de un gen puede analizarse el ARN (Northern blot, PCR a tiempo real, etc), y también la expresión de la proteína,
MÉTODOS DE ESTUDIO DE PROTEÍNAS ANÁLISIS DE EXPRESIÓN DE PROTEÍNAS Al estudiar la expresión de un gen puede analizarse el ARN (Northern blot, PCR a tiempo real, etc), y también la expresión de la proteína,
CONFERENCIA 6 TÍTULO: COMPONENTES MOLECULARES: MACROMOLÉCULAS. PROTEÍNAS.
 MORFOFISIOLOGÍA HUMANA I. PRIMER TRIMESTRE. PRIMER AÑO. CONFERENCIA 6 TÍTULO: COMPONENTES MOLECULARES: MACROMOLÉCULAS. PROTEÍNAS. Sabe Ud. que es la sangre? Adultos contienen de 5-6L Adultos contienen
MORFOFISIOLOGÍA HUMANA I. PRIMER TRIMESTRE. PRIMER AÑO. CONFERENCIA 6 TÍTULO: COMPONENTES MOLECULARES: MACROMOLÉCULAS. PROTEÍNAS. Sabe Ud. que es la sangre? Adultos contienen de 5-6L Adultos contienen
ANTECEDENTES. Durante las últimas décadas, la electroforesis en geles de. poliacrilamida ha sido la técnica de elección para el análisis d e la
 5 ANTECEDENTES Durante las últimas décadas, la electroforesis en geles de poliacrilamida ha sido la técnica de elección para el análisis d e la composición proteica de un determinado tipo de célula y el
5 ANTECEDENTES Durante las últimas décadas, la electroforesis en geles de poliacrilamida ha sido la técnica de elección para el análisis d e la composición proteica de un determinado tipo de célula y el
BIOSENSORES ELECTROQUÍMICOS
 BIOSENSORES ELECTROQUÍMICOS Biosensor enzimático de glucosa Josep Martínez Gomar, Sergio González Álvarez Clasificación de biosensores Biosensor: dispositivo analítico compacto que se compone de un elemento
BIOSENSORES ELECTROQUÍMICOS Biosensor enzimático de glucosa Josep Martínez Gomar, Sergio González Álvarez Clasificación de biosensores Biosensor: dispositivo analítico compacto que se compone de un elemento
CUANTIFICACIÓN DE LA ACTIVIDAD ENZIMÁTICA Y DE LA ACTIVIDAD ESPECÍFICA DE LAS ENZIMAS
 CUANTIFICACIÓN DE LA ACTIVIDAD ENZIMÁTICA Y DE LA ACTIVIDAD ESPECÍFICA DE LAS ENZIMAS I. INTRODUCCIÓN No siendo posible medir la cantidad de enzima directamente de los líquidos y estructuras biológicas
CUANTIFICACIÓN DE LA ACTIVIDAD ENZIMÁTICA Y DE LA ACTIVIDAD ESPECÍFICA DE LAS ENZIMAS I. INTRODUCCIÓN No siendo posible medir la cantidad de enzima directamente de los líquidos y estructuras biológicas
AMINOACIDOS. Aminoácidos: Moléculas orgánicas sencillas, que representan la unidad estructural de las proteínas. 12/04/2012
 AMINOACIDOS Aminoácidos: Moléculas orgánicas sencillas, que representan la unidad estructural de las proteínas. 1 FORMULA GENERAL H átomo carbono α grupo amino NH 2 C COOH grupo carboxilo R cadena lateral
AMINOACIDOS Aminoácidos: Moléculas orgánicas sencillas, que representan la unidad estructural de las proteínas. 1 FORMULA GENERAL H átomo carbono α grupo amino NH 2 C COOH grupo carboxilo R cadena lateral
LAS PROTEINAS: ESTRUCTURA Y PLEGAMIENTO
 LAS PROTEINAS: ESTRUCTURA Y PLEGAMIENTO ESTRUCTURA Y FUNCION DE LAS PROTEINAS. Las proteínas son polímeros de aminoácidos unidos por uniones amida, llamadas uniones peptídicas. La cadena polipéptídica
LAS PROTEINAS: ESTRUCTURA Y PLEGAMIENTO ESTRUCTURA Y FUNCION DE LAS PROTEINAS. Las proteínas son polímeros de aminoácidos unidos por uniones amida, llamadas uniones peptídicas. La cadena polipéptídica
Electroforesis en gel de poliacrilamida y electrotransferencia
 Electroforesis en gel de poliacrilamida y electrotransferencia INDICE ELECTROFORESIS Fundamento y características Tipos de electroforesis: libre y de zona Electroforesis en papel, acetato de celulosa Electroforesis
Electroforesis en gel de poliacrilamida y electrotransferencia INDICE ELECTROFORESIS Fundamento y características Tipos de electroforesis: libre y de zona Electroforesis en papel, acetato de celulosa Electroforesis
Ensayos de restricción
 Ensayos de restricción Vector con inserto= Vector recombinante 6500pb Objetivos de ensayos de restricción de plásmidos Conocer el principio de separación y detección de ácidos nucleicos en geles de agarosa.
Ensayos de restricción Vector con inserto= Vector recombinante 6500pb Objetivos de ensayos de restricción de plásmidos Conocer el principio de separación y detección de ácidos nucleicos en geles de agarosa.
Las proteínas. Dra. Nardy Diez García Investigadora
 Las proteínas Dra. Nardy Diez García Investigadora Son la clave de la vida Glicina o glicocola R=H Grupo Carboxilo Grupo Amino Es importante comprender estas propiedades porque son la clave de la estructura
Las proteínas Dra. Nardy Diez García Investigadora Son la clave de la vida Glicina o glicocola R=H Grupo Carboxilo Grupo Amino Es importante comprender estas propiedades porque son la clave de la estructura
IBCM 1 GUIA DE PROBLEMAS DE PROTEINAS
 IBCM 1 1-Complete los esquemas II y III. Además señale: extremo NH2 terminal, extremo 5 del mrna, extremo 3 del trna, sitio P, sitio A, codones y anticodones (complételos con las bases correspondientes)
IBCM 1 1-Complete los esquemas II y III. Además señale: extremo NH2 terminal, extremo 5 del mrna, extremo 3 del trna, sitio P, sitio A, codones y anticodones (complételos con las bases correspondientes)
Guía de TP Nro. 5 Actividad Proteolítica Celular
 Biología Celular y Molecular Guía de TP Nro. 5 Actividad Proteolítica Celular Introducción La actividad proteolítica secretada por las células es un elemento indispensable para la proliferación y migración
Biología Celular y Molecular Guía de TP Nro. 5 Actividad Proteolítica Celular Introducción La actividad proteolítica secretada por las células es un elemento indispensable para la proliferación y migración
PURIFICACIÓN DE ENZIMAS
 PURIFICACIÓN DE ENZIMAS MÉTODOS GENERALES DE EXTRACCIÓN Y PURIFICACIÓN CAMILO BECERRA (TUQ) MARÍA FERNANDA FERRERO (TUQ) INTRODUCCIÓN EN LA NATURALEZA EXISTEN CANTIDADES INIMAGINABLES DE COMPUESTOS, PERO
PURIFICACIÓN DE ENZIMAS MÉTODOS GENERALES DE EXTRACCIÓN Y PURIFICACIÓN CAMILO BECERRA (TUQ) MARÍA FERNANDA FERRERO (TUQ) INTRODUCCIÓN EN LA NATURALEZA EXISTEN CANTIDADES INIMAGINABLES DE COMPUESTOS, PERO
Electroforesis Bidimensional de proteínas. Lucía Monteoliva Díaz
 Electroforesis Bidimensional de proteínas Lucía Monteoliva Díaz Separación de proteínas ELECTROFORESIS: 1D, 2D ALTERNATIVAS A LA 2D: CROMATOGRAFÍAMULTIDIMENSIONAL Y ELECTROFORESIS CAPILAR Análisis proteico
Electroforesis Bidimensional de proteínas Lucía Monteoliva Díaz Separación de proteínas ELECTROFORESIS: 1D, 2D ALTERNATIVAS A LA 2D: CROMATOGRAFÍAMULTIDIMENSIONAL Y ELECTROFORESIS CAPILAR Análisis proteico
Electroforesis capilar
 Electroforesis capilar LUIS ENRIQUE MENDOZA POSTGRADO EN INGENIERÍA A BIOMÉDICA UNIVERSIDAD DE LOS ANDES MÉRIDA VENEZUELA NOVIEMBRE 2006 Electroforesis capilar AGENDA RESUMEN TIPOS DE ELECTROFORESIS EQUIPO
Electroforesis capilar LUIS ENRIQUE MENDOZA POSTGRADO EN INGENIERÍA A BIOMÉDICA UNIVERSIDAD DE LOS ANDES MÉRIDA VENEZUELA NOVIEMBRE 2006 Electroforesis capilar AGENDA RESUMEN TIPOS DE ELECTROFORESIS EQUIPO
2. ESTRUCTURA Y PROPIEDADES DE PROTEÍNAS. Purificación de LDH de músculo de Gallus gallus
 2. ESTRUCTURA Y PROPIEDADES DE PROTEÍNAS Purificación de LDH de músculo de Gallus gallus TRIS 2-amino-2-hidroximetilpropano-1,3-diol pk a = 8.07 Buffer efectivo en un rango de ph= 7.07 y 9.07 PMSF Fluoruro
2. ESTRUCTURA Y PROPIEDADES DE PROTEÍNAS Purificación de LDH de músculo de Gallus gallus TRIS 2-amino-2-hidroximetilpropano-1,3-diol pk a = 8.07 Buffer efectivo en un rango de ph= 7.07 y 9.07 PMSF Fluoruro
Separación de biomoléculas
 Separación de biomoléculas Cromatografía. Aspectos generales, técnicas involucradas. FPLC, HPLC. Electroforesis. Conceptos generales y aplicaciones. Geles de poliacrilamida y agarosa. Isoelectroenfoque.
Separación de biomoléculas Cromatografía. Aspectos generales, técnicas involucradas. FPLC, HPLC. Electroforesis. Conceptos generales y aplicaciones. Geles de poliacrilamida y agarosa. Isoelectroenfoque.
OBJETIVO: -Identificar aminoácidos y proteínas por medio de métodos basados en reacciones químicas.
 Química Biológica I TP : PROTEINAS Generalidades OBJETIVO: -Identificar aminoácidos y proteínas por medio de métodos basados en reacciones químicas. FUNDAMENTOS: Caracterización de las proteínas La caracterización
Química Biológica I TP : PROTEINAS Generalidades OBJETIVO: -Identificar aminoácidos y proteínas por medio de métodos basados en reacciones químicas. FUNDAMENTOS: Caracterización de las proteínas La caracterización
FACULTAD DE CIENCIAS NATURALES EXACTAS Y DE LA EDUCACIÓN DEPARTAMENTO DE QUÍMICA BIORGÁNICA
 FACULTAD DE CIENCIAS NATURALES EXACTAS Y DE LA EDUCACIÓN DEPARTAMENTO DE QUÍMICA BIORGÁNICA PRÁCTICA 3: PRUEBAS GENERALES PARA AMINOÁCIDOS Los aminoácidos constituyentes de las proteínas, contienen además
FACULTAD DE CIENCIAS NATURALES EXACTAS Y DE LA EDUCACIÓN DEPARTAMENTO DE QUÍMICA BIORGÁNICA PRÁCTICA 3: PRUEBAS GENERALES PARA AMINOÁCIDOS Los aminoácidos constituyentes de las proteínas, contienen además
RESULTADOS Y DISCUSIONES. El análisis por medio de electroforesis a demostrado ser uno de los
 39 RESULTADOS Y DISCUSIONES El análisis por medio de electroforesis a demostrado ser uno de los mejores métodos de separación para complejos proteicos, además de necesitar cantidades muy pequeñas de muestra.
39 RESULTADOS Y DISCUSIONES El análisis por medio de electroforesis a demostrado ser uno de los mejores métodos de separación para complejos proteicos, además de necesitar cantidades muy pequeñas de muestra.
TÉCNICAS INMUNOLÓGICAS. Bqca. Esp. Beda Elizabeth Mereles Rodríguez
 TÉCNICAS INMUNOLÓGICAS Bqca. Esp. Beda Elizabeth Mereles Rodríguez La medición de las interacciones Ag-Ac con fines diagnósticos se realizan por 2 vías Dx directo Utilización de Acs específicos para detectar
TÉCNICAS INMUNOLÓGICAS Bqca. Esp. Beda Elizabeth Mereles Rodríguez La medición de las interacciones Ag-Ac con fines diagnósticos se realizan por 2 vías Dx directo Utilización de Acs específicos para detectar
Proyecto de Fin de Cursos
 Universidad de la República Oriental del Uruguay Proyecto de Fin de Cursos ELECTROFORESIS EN GEL DE MOLÉCULAS DE ADN Noviembre de 2006 Carolina Etchart C.I. 3.757.708-8 Marcelo Lavagna C.I. 3.508.715-8
Universidad de la República Oriental del Uruguay Proyecto de Fin de Cursos ELECTROFORESIS EN GEL DE MOLÉCULAS DE ADN Noviembre de 2006 Carolina Etchart C.I. 3.757.708-8 Marcelo Lavagna C.I. 3.508.715-8
De los 92 elementos químicos que existen en la naturaleza 30 esenciales para organismos vivos.
 ELEMENTOS QUÍMICOS DE LA MATERIA VIVA Materia constituida por combinación de elementos químicos. De los 92 elementos químicos que existen en la naturaleza 30 esenciales para organismos vivos. ÁTOMOS ÁTOMO
ELEMENTOS QUÍMICOS DE LA MATERIA VIVA Materia constituida por combinación de elementos químicos. De los 92 elementos químicos que existen en la naturaleza 30 esenciales para organismos vivos. ÁTOMOS ÁTOMO
Separación Sólido-Líquido. Dra. María Victoria Miranda. Cátedra de Microbiología Industrial y Biotecnología. Facultad de Farmacia y Bioquímica.
 Separación Sólido-Líquido Dra. María Victoria Miranda Cátedra de Microbiología Industrial y Biotecnología Facultad de Farmacia y Bioquímica. UBA SOBRENADANTE Separación Sólido-Líquido FERMENTACIÓN SSL
Separación Sólido-Líquido Dra. María Victoria Miranda Cátedra de Microbiología Industrial y Biotecnología Facultad de Farmacia y Bioquímica. UBA SOBRENADANTE Separación Sólido-Líquido FERMENTACIÓN SSL
UNIDAD 5. AMINOÁCIDOS Y PROTEÍNAS
 UNIDAD 5. AMINOÁCIDOS Y PROTEÍNAS Dr en C. MPA MVZ Carlos Gutiérrez Olvera AMINOÁCIDOS: Como su nombre lo implica, los aminoácidos son moléculas orgánicas que contienen un grupo amino (NH2) en uno de los
UNIDAD 5. AMINOÁCIDOS Y PROTEÍNAS Dr en C. MPA MVZ Carlos Gutiérrez Olvera AMINOÁCIDOS: Como su nombre lo implica, los aminoácidos son moléculas orgánicas que contienen un grupo amino (NH2) en uno de los
Material elaborado por F. Agius, O. Borsani, P.Díaz, S. Gonnet, P. Irisarri, F. Milnitsky y J. Monza. Bioquímica. Facultad de Agronomía.
 AMINOACIDOS Las proteínas de bacterias, hongos, plantas y animales están constituidas a partir de las mismas 20 unidades o monómeros: los á-aminoácidos. Los aminoácidos tienen un grupo amino y un grupo
AMINOACIDOS Las proteínas de bacterias, hongos, plantas y animales están constituidas a partir de las mismas 20 unidades o monómeros: los á-aminoácidos. Los aminoácidos tienen un grupo amino y un grupo
AMINOÁCIDOS Y PROTEÍNAS
 4/6/15 DEPARTAMENTO DE BIOQUÍMICA ESFUNO EUTM AMINOÁCIDOS Y PROTEÍNAS ESTRUCTURA DE LOS AMINOÁCIDOS Grupo carboxilo Grupo amino Carbono α Cadena Lateral Ión dipolar o zwitterión Las proteínas tienen L-aminoácidos
4/6/15 DEPARTAMENTO DE BIOQUÍMICA ESFUNO EUTM AMINOÁCIDOS Y PROTEÍNAS ESTRUCTURA DE LOS AMINOÁCIDOS Grupo carboxilo Grupo amino Carbono α Cadena Lateral Ión dipolar o zwitterión Las proteínas tienen L-aminoácidos
Métodos para Inmunidad Viral
 Métodos para Inmunidad Viral Radioinmunoensayo (RIA) Técnica muy sensible basada en la competencia de unión al anticuerpo específico entre el antígeno a cuantificar y cantidades conocidas del antígeno
Métodos para Inmunidad Viral Radioinmunoensayo (RIA) Técnica muy sensible basada en la competencia de unión al anticuerpo específico entre el antígeno a cuantificar y cantidades conocidas del antígeno
qprotein (BCA) Kit para cuantificar proteinas totales PB-L Productos Bio-Lógicos
 qprotein () Kit para cuantificar proteinas totales PB-L http://www.pb-l.com.ar qprotein () Cat. no. RA03 CONTENIDO Componentes RA0301 RA0302 Buffer A 250 ml 500 ml Buffer B 5 ml 10 ml Proteína Patrón 5
qprotein () Kit para cuantificar proteinas totales PB-L http://www.pb-l.com.ar qprotein () Cat. no. RA03 CONTENIDO Componentes RA0301 RA0302 Buffer A 250 ml 500 ml Buffer B 5 ml 10 ml Proteína Patrón 5
Metodos de purificación
 Metodos de purificación Basado en las siguientes propiedades proteicas: Tamaño Solubilidad Carga Adsorción Afinidad CAROLINA VITA Característica Tamaño Solubidad Polaridad Carga Procedimientos Dialisis
Metodos de purificación Basado en las siguientes propiedades proteicas: Tamaño Solubilidad Carga Adsorción Afinidad CAROLINA VITA Característica Tamaño Solubidad Polaridad Carga Procedimientos Dialisis
BIOMOLÉCULAS. Son aquellas que se encuentran presentes tanto en la materia orgánica (viva) como en la materia inerte. Ellas son:
 Nombre Curso Fecha : : : Revisión FICHA DE BIOLOGÍA N 1 Profesora Verónica Abasto Córdova Biología 2 Medio BIOMOLÉCULAS Las biomoléculas son las moléculas constituyentes de los seres vivos. Están formadas
Nombre Curso Fecha : : : Revisión FICHA DE BIOLOGÍA N 1 Profesora Verónica Abasto Córdova Biología 2 Medio BIOMOLÉCULAS Las biomoléculas son las moléculas constituyentes de los seres vivos. Están formadas
Técnicas de Biología Molecular. Biol 3051L
 Técnicas de Biología Molecular Biol 3051L Objetivos El cortar el DNA con enzimas de restricción y hacer corridas de geles usando electroforesis es muchas veces el primer paso para estudiar un gen. En este
Técnicas de Biología Molecular Biol 3051L Objetivos El cortar el DNA con enzimas de restricción y hacer corridas de geles usando electroforesis es muchas veces el primer paso para estudiar un gen. En este
ESTRUCTURA Y PROPIEDADES DE PROTEÍNAS
 ESTRUCTURA Y PROPIEDADES DE PROTEÍNAS Purificación de la enzima lactato deshidrogenasa de músculo esquelético de pollo PARTE I. EXTRACCIÓN Y PRECIPITACIÓN POR SALADO. Las proteínas se purifican mediante
ESTRUCTURA Y PROPIEDADES DE PROTEÍNAS Purificación de la enzima lactato deshidrogenasa de músculo esquelético de pollo PARTE I. EXTRACCIÓN Y PRECIPITACIÓN POR SALADO. Las proteínas se purifican mediante
Area Química Biológica Curso: Bioquímica. Tema 6: PROTEINAS. Dra. Silvia M. Varas
 Area Química Biológica Curso: Bioquímica Tema 6: PROTEINAS Dra. Silvia M. Varas Las proteínas están formadas por unidades básicas que corresponden a los aminoácidos, los cuales se unen entre sí para formar
Area Química Biológica Curso: Bioquímica Tema 6: PROTEINAS Dra. Silvia M. Varas Las proteínas están formadas por unidades básicas que corresponden a los aminoácidos, los cuales se unen entre sí para formar
ACTIVIDAD ENZIMÁTICA. Dra. Lilian González Segura Departamento de Bioquímica Facultad de Química
 ACTIVIDAD ENZIMÁTICA Dra. Lilian González Segura Departamento de Bioquímica Facultad de Química Porqué la gran mayoría de las reacciones en los seres vivos necesitan ser catalizadas para que ocurran a
ACTIVIDAD ENZIMÁTICA Dra. Lilian González Segura Departamento de Bioquímica Facultad de Química Porqué la gran mayoría de las reacciones en los seres vivos necesitan ser catalizadas para que ocurran a
2. ESTRUCTURA Y PROPIEDADES DE PROTEÍNAS. 25 Agosto, 2009
 2. ESTRUCTURA Y PROPIEDADES DE PROTEÍNAS. 25 Agosto, 2009 El genoma haploide de un humano contiene 20,000-25,000 genes que codifican a proteínas. Transportadores Enzimas Receptores Estructurales Hormonas
2. ESTRUCTURA Y PROPIEDADES DE PROTEÍNAS. 25 Agosto, 2009 El genoma haploide de un humano contiene 20,000-25,000 genes que codifican a proteínas. Transportadores Enzimas Receptores Estructurales Hormonas
Biología Celular y Molecular. Guía de TP Nro. 5. Actividad proteolítica celular.
 Biología Celular y Molecular. Guía de TP Nro. 5 Actividad proteolítica celular. Introducción La actividad proteolítica secretada por las células es un elemento indispensable para la proliferación y migración
Biología Celular y Molecular. Guía de TP Nro. 5 Actividad proteolítica celular. Introducción La actividad proteolítica secretada por las células es un elemento indispensable para la proliferación y migración
Proteínas de la leche. Caseinato de sodio Una proteína extraída de la leche y usada para estabilizar la grasa en una emulsión Escala= 50 µm
 Proteínas de la leche Caseinato de sodio Una proteína extraída de la leche y usada para estabilizar la grasa en una emulsión Escala= 50 µm PROTEINAS En la leche, la proteína más importante es la caseína,
Proteínas de la leche Caseinato de sodio Una proteína extraída de la leche y usada para estabilizar la grasa en una emulsión Escala= 50 µm PROTEINAS En la leche, la proteína más importante es la caseína,
QUÍMICA BIOLÓGICA. Trabajo Práctico Nº2: Cinética Enzimática. Estudio cinético de la Glucosa-6-fosfato deshidrogenasa
 QUÍMICA BIOLÓGICA Trabajo Práctico Nº2: Cinética Enzimática Estudio cinético de la Glucosa-6-fosfato deshidrogenasa Las enzimas son catalizadores biológicos, en la mayoría de los casos de naturaleza proteica.
QUÍMICA BIOLÓGICA Trabajo Práctico Nº2: Cinética Enzimática Estudio cinético de la Glucosa-6-fosfato deshidrogenasa Las enzimas son catalizadores biológicos, en la mayoría de los casos de naturaleza proteica.
CROMATOGRAFIA. Dra. María del Rosario Torviso Química Orgánica I FFyB-UBA
 CROMATOGRAFIA Dra. María del Rosario Torviso Química Orgánica I FFyB-UBA 1 CROMATOGRAFIA Se basa en el principio general de distribución de un compuesto entre dos fases, una fija o estacionaria (FE) y
CROMATOGRAFIA Dra. María del Rosario Torviso Química Orgánica I FFyB-UBA 1 CROMATOGRAFIA Se basa en el principio general de distribución de un compuesto entre dos fases, una fija o estacionaria (FE) y
ENZIMAS-2005 CINÉTICA ENZIMÁTICA
 ENZIMAS-00 Las enzimas son catalizadores biológicos en su mayoría de naturaleza proteica (99,99%) y las ribosimas (fragmentos de RNA) (0,%). Las enzimas tienen tres propiedades bien definidas e inigualables
ENZIMAS-00 Las enzimas son catalizadores biológicos en su mayoría de naturaleza proteica (99,99%) y las ribosimas (fragmentos de RNA) (0,%). Las enzimas tienen tres propiedades bien definidas e inigualables
TÉCNICAS ELECTROFORÉTICAS
 1. Identificación Identificación de la Asignatura Asignatura Titulación: MÁSTER UNIVERSITARIO EN BIOLOGÍA MOLECULAR Y BIOTECNOLOGÍA Codigo: 4235 Curso: 1 Grupos: 1 Tipo: OPTATIVA Modalidad: Presencial
1. Identificación Identificación de la Asignatura Asignatura Titulación: MÁSTER UNIVERSITARIO EN BIOLOGÍA MOLECULAR Y BIOTECNOLOGÍA Codigo: 4235 Curso: 1 Grupos: 1 Tipo: OPTATIVA Modalidad: Presencial
ELECTROFORESIS AVANZADA
 Ref. ELECAVANZADA (4 prácticas) 1. OBJETIVO DEL EXPERIMENTO ELECTROFORESIS AVANZADA El objetivo de este experimento es introducir a los alumnos en el conocimiento de la teoría electroforética y familiarizarse
Ref. ELECAVANZADA (4 prácticas) 1. OBJETIVO DEL EXPERIMENTO ELECTROFORESIS AVANZADA El objetivo de este experimento es introducir a los alumnos en el conocimiento de la teoría electroforética y familiarizarse
SEMANA 29 PROPIEDADES FÍSICAS Y QUÍMICAS DE AMINOÁCIDOS Y PROTEÍNAS Elaborado por Lic. Fernando Andrade
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS UNIDAD DIDÁCTICA DE QUÍMICA, PRIMER AÑO PRACTICA DE LABORATORIO 2014 SEMANA 29 PROPIEDADES FÍSICAS Y QUÍMICAS DE AMINOÁCIDOS Y PROTEÍNAS
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS UNIDAD DIDÁCTICA DE QUÍMICA, PRIMER AÑO PRACTICA DE LABORATORIO 2014 SEMANA 29 PROPIEDADES FÍSICAS Y QUÍMICAS DE AMINOÁCIDOS Y PROTEÍNAS
Biocromatografía: intercambio iónico
 Biocromatografía: intercambio iónico Intercambio Iónico Columnas TSK-GEL El método más utilizado en la purificación de proteínas y otras moléculas que presenten carga eléctrica es la Cromatografía de Intercambio
Biocromatografía: intercambio iónico Intercambio Iónico Columnas TSK-GEL El método más utilizado en la purificación de proteínas y otras moléculas que presenten carga eléctrica es la Cromatografía de Intercambio
EL EMPLEO DE ANÁLISIS BIOQUÍMICOS Y MOLECULARES EN EL EXAMEN DHE MOLECULARES EN EL EXAMEN DHE
 X Curso de Formación sobre la Protección de las Obtenciones Vegetales para Países Iberoamericanos Montevideo (URUGUAY) 12 al 16 de Diciembre de 2011 EL EMPLEO DE ANÁLISIS BIOQUÍMICOS Y MOLECULARES EN EL
X Curso de Formación sobre la Protección de las Obtenciones Vegetales para Países Iberoamericanos Montevideo (URUGUAY) 12 al 16 de Diciembre de 2011 EL EMPLEO DE ANÁLISIS BIOQUÍMICOS Y MOLECULARES EN EL
