PREPARACIÓN PSU TEORÍA ATÓMICA PROF. ÁNGELA GAJARDO S. QUÍMICA ELECTIVO IV MEDIO 2016
|
|
|
- José Ignacio Martín Vázquez
- hace 6 años
- Vistas:
Transcripción
1 PREPARACIÓN PSU TEORÍA ATÓMICA PROF. ÁNGELA GAJARDO S. QUÍMICA ELECTIVO IV MEDIO 2016
2 I. ESTRUCTURA ATÓMICA 1.1 PARTÍCULAS SUBATÓMICAS Partícula subatómica Símbolo Carga fundamental (Q) Carga relativa Masa (kg) Ubicación en el átomo Electrón e - - 1,6 x ,11 x Corteza Protón p + + 1,6 x ,67 x Núcleo Neutrón n 0 0 1,67 x Núcleo
3 I. ESTRUCTURA ATÓMICA 1.2 MODELOS ATÓMICOS Los modelos atómicos científicos intentan interpretar la realidad de la estructura del átomo a partir de las propiedades observadas. La evolución de los modelos ha sido simultáneo al desarrollo y la observación científica. MODELO ATÓMICO DE DALTON La materia está formada por átomos. Los átomos son indivisibles. MODELO ATÓMICO DE THOMSON Forma Componentes Partículas Carga total Esférico Esfera con masa y carga positiva Electrones incrustados Neutra
4 I. ESTRUCTURA ATÓMICA 1.1I MODELOS ATÓMICOS MODELO ATÓMICO DE RUTHERFORD Componentes Partículas Carga Total Núcleo pequeño y muy masivo Corteza muy grande y muy poco masiva MODELO ATÓMICO DE BOHR Protones (carga positiva) y neutrones (sin carga, Rutherford predijo su existencia). Electrones (carga negativa). Muy separados unos de otros. Componentes Partículas Propiedades Núcleo Corteza Protones (carga positiva) y neutrones (sin carga). Electrones (carga negativa). Forman orbitas circulares y concéntricas que se van alejando del núcleo. Pequeño y masivo Neutra Neutra Cada órbita lleva asociada una cierta energía. Las órbitas externas tienen más energía que las internas.
5 MODELO ATÓMICO DE BOHR: ASPECTO CLAVE El electrón puede pasar de una órbita a otra. Si pasa de una más externa a otra más interna, emite energía, que se llama radiación. Para pasar de una orbita interna a otra más externa, el electrón necesita una energía de activación.
6 MODELO ATÓMICO ACTUAL BASES TEÓRICAS: - Sommerfield Órbitas elípticas, no circulares. - De Broglie Modelo onda-partícula. - Heisemberg Principio de incertidumbre. - Schrödinger Modelo de la probabilidad matemática. Componentes Partículas Propiedades Núcleo Corteza Protones (carga positiva) y neutrones (sin carga). Electrones (carga negativa). Solo se puede predecir la probabilidad de encontrarlos en una zona llamada orbital atómico. Pequeño y masivo. Cada orbital lleva asociada una cierta energía.
7
8 1.2 NÚMERO ATÓMICO Y NÚMERO MÁSICO NÚMERO ATÓMICO (Z): Número de protones (y por lo tanto, electrones) que tiene un átomo en el núcleo es lo que identifica a un elemento. Ej: 3 Li, 11 Na, 26 F. Átomo sin carga eléctrica Z coincide con el número de electrones del átomo. Átomo con carga eléctrica Z NO coincide con el número de electrones del átomo. NÚMERO MÁSICO (A): Número total de partículas que tiene un átomo en el núcleo. Expresa la composición nuclear que determina la masa atómica. Ej.: C 12, K 39, Xe 54. A = n de protones + n neutrones n de neutrones = A - Z
9
10 1.3 IONES Pueden ganar electrones para completar sus orbitales externos. LOS ÁTOMOS Pueden perder electrones de sus orbitales externos. Cuando ganan o pierden electrones quedan cargados eléctricamente UN ÁTOMO CARGADO ELÉCTRICAMENTE RECIBE EL NOMBRE DE IÓN - Si el número de electrones de un átomo supera a su número de protones, el átomo se denomina ión negativo o anión. - Si el número de electrones de un átomo es menor a su número de protones, el átomo se denomina ión positivo o catión.
11
12 1.4 ISÓTOPOS Átomo que pertenece al mismo elemento químico que otro, tiene su mismo número atómico, pero distinta masa atómica "los isótopos tienen el mismo número de protones que los átomos normales, pero diferente número de neutrones" EL HIDRÓGENO EN LA NATURALEZA Protio (hidrógeno natural) Deuterio Tritio 1 protón 1 protón 1 protón 1 electrón 1 electrón 1 electrón No tiene neutrones 1 neutrón 2 neutrones El deuterio y el tritio son isótopos del hidrógeno: los tres átomos tienen un portón y un electrón, pero se diferencian por el número de neutrones que tiene cada uno. Isótopos del Carbono
13 1.5 RADIOACTIVIDAD Algunos núcleos atómicos, de forma espontánea se rompen y se transforman en otros. Durante ese proceso de ruptura se emite radiación.
14 1.6 ÁTOMOS Y MOLÉCULAS Los átomos se unen entre sí por medio de enlaces químicos. Los compuestos químicos son agrupaciones de átomos, unidos mediante enlaces. Una molécula es la parte más pequeña de un compuesto que presenta todas las propiedades de dicho compuesto. Las moléculas de cualquier compuesto están formadas por varios átomos.
15
16 CAPA DE VALENCIA COMPORTAMIENTO QUÍMICO DE LOS ÁTOMOS
17 1.7 TABLA PERIÓDICA DE LOS ELEMENTOS Denominación: tabla periódica o sistema periódico de los elementos. Se organiza siguiendo un orden creciente de los números atómicos de los elementos, formando GRUPOS (columnas) y PERÍODOS (filas). La columnas están formadas por elementos que tienen propiedades semejantes. El orden y las propiedades guardan relación con la configuración electrónica de los elementos, sobre todo con sus electrones de valencia. Cada elemento ocupa una casilla en la tabla periódica. En ella se suelen escribir su número atómico, su masa atómica, la configuración de su capa de valencia, etc.
18
19 Cuando los elementos se ordenan en, aparece una repetición periódica de algunas propiedades físicas y químicas. LEY PERIÓDICA. Las propiedades químicas de los elementos s deben en gran parte a la configuración de la última capa de electrones (capa de valencia) Por ese motivo se ordenan los elementos en la tabla periódica. Columnas Grupos Misma configuración electrónica Filas Períodos Mismo número de capas n
20 PROPIEDADES PERIÓDICAS DE LOS ELEMENTOS
21
22
23
24 Configuración electrónica
25
26
27
28
29
30 EXTRA: TABLAS PERIÓDICAS MODERNAS
31
32
33 1.8 ENLACES QUÍMICOS Los átomos se unen entre sí formando moléculas. Las uniones entre átomos se llaman enlaces.
34 TIPOS DE ENLACES QUÍMICOS
35
36
EL ÁTOMO 1. El átomo. 2. Modelos atómicos. 3. Núcleo atómico. 4. Espectros atómicos. 5. Modelo atómico cuántico.
 EL ÁTOMO 1. El átomo. 2. Modelos atómicos. 3. Núcleo atómico. 4. Espectros atómicos. 5. Modelo atómico cuántico. Química 1º bachillerato El átomo 1 El átomo no es una partícula indivisible, sino que está
EL ÁTOMO 1. El átomo. 2. Modelos atómicos. 3. Núcleo atómico. 4. Espectros atómicos. 5. Modelo atómico cuántico. Química 1º bachillerato El átomo 1 El átomo no es una partícula indivisible, sino que está
Clase N 1. Modelo Atómico I
 Pre-Universitario Manuel Guerrero Ceballos Clase N 1 Modelo Atómico I ICAL ATACAMA Módulo Plan Común Modelos Atómicos Teoría Atómica De Dalton Los elementos están formados por partículas extremadamente
Pre-Universitario Manuel Guerrero Ceballos Clase N 1 Modelo Atómico I ICAL ATACAMA Módulo Plan Común Modelos Atómicos Teoría Atómica De Dalton Los elementos están formados por partículas extremadamente
Tema 5: El átomo y sus uniones.
 Tema 5: El átomo y sus uniones. 1. Teoría Atómica de Dalton. En 1803, John Dalton expone su Teoría Atómica que se basa en los siguientes puntos: Los elementos químicos están formados por partículas muy
Tema 5: El átomo y sus uniones. 1. Teoría Atómica de Dalton. En 1803, John Dalton expone su Teoría Atómica que se basa en los siguientes puntos: Los elementos químicos están formados por partículas muy
b) La zona externa del átomo se llama CORTEZA. y ahí es donde se mueven los ELECTRONES
 PREGUNTAS DE RESPUESTA BREVE 1. Completa las siguientes frases relativas a los átomos de los elementos: a) La parte del átomo en donde se puede considerar que se concentra toda su masa es el NÚCLEO y ahí
PREGUNTAS DE RESPUESTA BREVE 1. Completa las siguientes frases relativas a los átomos de los elementos: a) La parte del átomo en donde se puede considerar que se concentra toda su masa es el NÚCLEO y ahí
INTERACTIVEBOOK - Física y Química 4º ESO McGraw-Hill Education Dalton 1.2. Thomson: Descubrimiento del electrón. 1.3.
 El modelo de átomo INTERACTIVEBOOK - Física y Química 4º ESO McGraw-Hill Education INDICE 1. El modelo de átomo 1.1. Dalton 1.2. Thomson: Descubrimiento del electrón. 1.3. Rutherford: 1.3.1. Radioactividad
El modelo de átomo INTERACTIVEBOOK - Física y Química 4º ESO McGraw-Hill Education INDICE 1. El modelo de átomo 1.1. Dalton 1.2. Thomson: Descubrimiento del electrón. 1.3. Rutherford: 1.3.1. Radioactividad
Modelo atómico de Dalton(1808)
 El átomo Modelos atómicos Como no se podían ver los átomos los científicos crearon modelos para describirlos, éstos fueron evolucionando a lo largo de la historia a medida que se descubrieron nuevas cosas.
El átomo Modelos atómicos Como no se podían ver los átomos los científicos crearon modelos para describirlos, éstos fueron evolucionando a lo largo de la historia a medida que se descubrieron nuevas cosas.
2º Bachillerato. Química. Unidad 1 (Estructura atómica de la materia). Fotocopia 1.
 Partículas subatómicas Los átomos están formados por un núcleo (formado por protones y neutrones) rodeado por una nube de electrones, que se encuentran en la corteza. Entre núcleo y corteza hay espacio
Partículas subatómicas Los átomos están formados por un núcleo (formado por protones y neutrones) rodeado por una nube de electrones, que se encuentran en la corteza. Entre núcleo y corteza hay espacio
3 - Cómo podemos diferenciar un elemento químico de un compuesto, según la teoría de Dalton?
 TEORÍA ATÓMICA 1- A partir de los siguientes datos, cuántas veces es maor la masa del protón que la del electrón? Masa del protón =1,673 10-27 kg Masa del electrón =9,1 10-31 kg 2 - El modelo del átomo
TEORÍA ATÓMICA 1- A partir de los siguientes datos, cuántas veces es maor la masa del protón que la del electrón? Masa del protón =1,673 10-27 kg Masa del electrón =9,1 10-31 kg 2 - El modelo del átomo
Solucionario Cuaderno Estrategias y Ejercitación Modelo atómico de la materia I: estructura atómica, modelos atómicos y tipos de átomos
 Solucionario Cuaderno Estrategias y Ejercitación Modelo atómico de la materia I: estructura atómica, modelos atómicos y tipos de átomos Química Técnico Profesional Intensivo SCUACTC001TC83-A16V1 Ítem Alternativa
Solucionario Cuaderno Estrategias y Ejercitación Modelo atómico de la materia I: estructura atómica, modelos atómicos y tipos de átomos Química Técnico Profesional Intensivo SCUACTC001TC83-A16V1 Ítem Alternativa
Física y Química 3º E.S.O. 2013/14
 Física y Química 3º E.S.O. 2013/14 TEMA 3: La materia. Propiedades eléctricas y el átomo 1.- En la siguiente sopa de letras puedes encontrar los nombres de 13 elementos químicos. A O M O L P B A C E E
Física y Química 3º E.S.O. 2013/14 TEMA 3: La materia. Propiedades eléctricas y el átomo 1.- En la siguiente sopa de letras puedes encontrar los nombres de 13 elementos químicos. A O M O L P B A C E E
2.- Los átomos de un mismo elemento son iguales en masa y propiedades. Y los átomos de elementos diferentes son diferentes en masa y propiedades.
 FICHA 1 TEMA 3: ESTRUCTURA DE LA MATERIA PRIMEROS MODELOS ATÓMICOS La discusión sobre la continuidad o discontinuidad de la materia viene desde muy antiguo. Ya en la antigua Grecia había varias corrientes
FICHA 1 TEMA 3: ESTRUCTURA DE LA MATERIA PRIMEROS MODELOS ATÓMICOS La discusión sobre la continuidad o discontinuidad de la materia viene desde muy antiguo. Ya en la antigua Grecia había varias corrientes
Departamento de Física y Química. 2.- Deduce el número de neutrones, protones y electrones de los átomos siguientes:
 1.- Para el átomo de Galio, 69 31Ga ; deduce el número de protones, electrones y neutrones. 2.- Deduce el número de neutrones, protones y electrones de los átomos siguientes: U ; Hg ; Th ; He; Ne 235 200
1.- Para el átomo de Galio, 69 31Ga ; deduce el número de protones, electrones y neutrones. 2.- Deduce el número de neutrones, protones y electrones de los átomos siguientes: U ; Hg ; Th ; He; Ne 235 200
LiceoTolimense Química Séptimo 1 Periodo ESTRUCTURA INTERNA DE LA MATERIA
 ESTRUCTURA INTERNA DE LA MATERIA Lectura comprensiva Desde la antigüedad los filósofos se preguntaban de qué estaban formadas las cosas que los rodeaban. Primero pensaron que la materia era continua, es
ESTRUCTURA INTERNA DE LA MATERIA Lectura comprensiva Desde la antigüedad los filósofos se preguntaban de qué estaban formadas las cosas que los rodeaban. Primero pensaron que la materia era continua, es
PARTÍCULAS DEL ÁTOMO MODELOS ATÓMICOS. TEMA 7 Pág. 155 libro nuevo
 PARTÍCULAS DEL ÁTOMO MODELOS ATÓMICOS TEMA 7 Pág. 155 libro nuevo DESCUBRIMIENTO DEL ÁTOMO. PARTÍCULAS SUBATÓMICAS En la antigua Grecia ya había dos teorías sobre la materia: Teoría Atomística (siglo IV
PARTÍCULAS DEL ÁTOMO MODELOS ATÓMICOS TEMA 7 Pág. 155 libro nuevo DESCUBRIMIENTO DEL ÁTOMO. PARTÍCULAS SUBATÓMICAS En la antigua Grecia ya había dos teorías sobre la materia: Teoría Atomística (siglo IV
EXTRUCTURA ATOMICA ACTUAL
 ATOMOS Y ELEMENTOS TEMA 4 Química ATOMOS EXTRUCTURA ATOMICA ACTUAL PARTICULA UBICACION CARGA MASA PROTON NUCLEO + SI NEUTRON NUCLEO 0 SI ELECTRON ORBITAS - DESPRECIABLE La masa del átomo reside en el núcleo.
ATOMOS Y ELEMENTOS TEMA 4 Química ATOMOS EXTRUCTURA ATOMICA ACTUAL PARTICULA UBICACION CARGA MASA PROTON NUCLEO + SI NEUTRON NUCLEO 0 SI ELECTRON ORBITAS - DESPRECIABLE La masa del átomo reside en el núcleo.
Unidad I: Propiedades Periódicas: Masa y Enlace
 Unidad I: Propiedades Periódicas: Masa y Enlace 1. Nociones de teoría atómica moderna 2. Propiedades periódicas de los elementos 3. Enlace iónico y covalente 4. Masas atómicas y moleculares 1. Nociones
Unidad I: Propiedades Periódicas: Masa y Enlace 1. Nociones de teoría atómica moderna 2. Propiedades periódicas de los elementos 3. Enlace iónico y covalente 4. Masas atómicas y moleculares 1. Nociones
Modelo atómico de la materia.
 Modelo atómico de la materia. La Teoría Atómica se basa en la suposición (ratificada después por datos experimentales) de que la materia no es continua, sino que está formada por partículas distintas.
Modelo atómico de la materia. La Teoría Atómica se basa en la suposición (ratificada después por datos experimentales) de que la materia no es continua, sino que está formada por partículas distintas.
3.2. PARTÍCULAS SUBATÓMICAS.
 3.2. PARTÍCULAS SUBATÓMICAS. 3.2.1. PROTONES Y ELECTRONES. Aunque Dalton creía que los átomos eran indivisibles e inalterables, a lo largo del siglo XIX aparecieron cada vez más evidencias de que los átomos
3.2. PARTÍCULAS SUBATÓMICAS. 3.2.1. PROTONES Y ELECTRONES. Aunque Dalton creía que los átomos eran indivisibles e inalterables, a lo largo del siglo XIX aparecieron cada vez más evidencias de que los átomos
SEMANA 01 Estructura Atómica y Tabla Periódica. Licda. Lilian Judith Guzmán Melgar
 SEMANA 01 Estructura Atómica y Tabla Periódica Licda. Lilian Judith Guzmán Melgar 2016 ATOMO Es la partícula mas pequeña de un elemento que mantiene sus características. John Dalton formuló la TEORIA ATOMICA
SEMANA 01 Estructura Atómica y Tabla Periódica Licda. Lilian Judith Guzmán Melgar 2016 ATOMO Es la partícula mas pequeña de un elemento que mantiene sus características. John Dalton formuló la TEORIA ATOMICA
Estudio del átomo: 1. Átomos e isótopos 2. Modelos Atómicos 3. Teoría cuántica. Ing. Sol de María Jiménez González
 Estudio del átomo: 1. Átomos e isótopos 2. Modelos Atómicos 3. Teoría cuántica 1 Núcleo: protones y neutrones Los electrones se mueven alrededor. Característica Partículas Protón Neutrón Electrón Símbolo
Estudio del átomo: 1. Átomos e isótopos 2. Modelos Atómicos 3. Teoría cuántica 1 Núcleo: protones y neutrones Los electrones se mueven alrededor. Característica Partículas Protón Neutrón Electrón Símbolo
LA LA ESTRUCTURA DE LA MATERIA. 1.-Desarrollo histórico del concepto de átomo. Teoría de Demócrito. Teoría de Dalton. Componentes del átomo
 ANEXO AL TEMA 4 LA LA ESTRUCTURA DE LA MATERIA 1.-Desarrollo histórico del concepto de átomo Teoría de Demócrito Teoría de Dalton Modelo actual Componentes del átomo Concepto de ión 2.-Elememtos y compuestos
ANEXO AL TEMA 4 LA LA ESTRUCTURA DE LA MATERIA 1.-Desarrollo histórico del concepto de átomo Teoría de Demócrito Teoría de Dalton Modelo actual Componentes del átomo Concepto de ión 2.-Elememtos y compuestos
ESTRUCTURA ATÓMICA DE LA MATERIA. SISTEMA PERIÓDICO ESTRUCTURA ATÓMICA DE LA MATERIA
 ESTRUCTURA ATÓMICA DE LA MATERIA. SISTEMA PERIÓDICO ESTRUCTURA ATÓMICA DE LA MATERIA La teoría atómica de Dalton se mantuvo con éxito durante casi un siglo pero tuvo que ser abandonada a partir del descubrimiento
ESTRUCTURA ATÓMICA DE LA MATERIA. SISTEMA PERIÓDICO ESTRUCTURA ATÓMICA DE LA MATERIA La teoría atómica de Dalton se mantuvo con éxito durante casi un siglo pero tuvo que ser abandonada a partir del descubrimiento
FÍSICA Y QUÍMICA - 3º ESO ESTRUCTURA ATOMICA Y ENLACE 2
 FÍSICA Y QUÍMICA - 3º ESO ESTRUCTURA ATOMICA Y ENLACE 2 1. Define y explica los siguientes conceptos: número atómico, número másico e isótopos de un elemento químico. 2. Copia el siguiente párrafo y complétalo:
FÍSICA Y QUÍMICA - 3º ESO ESTRUCTURA ATOMICA Y ENLACE 2 1. Define y explica los siguientes conceptos: número atómico, número másico e isótopos de un elemento químico. 2. Copia el siguiente párrafo y complétalo:
5ª UNIDAD ELEMENTOS Y COMPUESTOS
 5ª UNIDAD ELEMENTOS Y COMPUESTOS 3º E.S.O. Grupo Apellidos: Nombre: INTRODUCCIÓN Comenzamos recordando los conceptos más importantes del tema anterior: Cómo son los átomos? Cómo están distribuidos los
5ª UNIDAD ELEMENTOS Y COMPUESTOS 3º E.S.O. Grupo Apellidos: Nombre: INTRODUCCIÓN Comenzamos recordando los conceptos más importantes del tema anterior: Cómo son los átomos? Cómo están distribuidos los
M. Eugenia Villaseca R. Licenciada y Profesora de Biología PUCV
 M. Eugenia Villaseca R. Licenciada y Profesora de Biología PUCV Comprender la utilidad de los modelos atómicos y de la teoría atómica para explicar los procesos de transformación físico-química de la materia
M. Eugenia Villaseca R. Licenciada y Profesora de Biología PUCV Comprender la utilidad de los modelos atómicos y de la teoría atómica para explicar los procesos de transformación físico-química de la materia
FÍSICA Y QUÍMICA TEMA 2: ESTRUCTURA ATÓMICA DE LA MATERIA
 Física y Química 3º Curso Educación Secundaria Obligatoria Curso académico 2016/2017 1 FÍSICA Y QUÍMICA TEMA 2: ESTRUCTURA ATÓMICA DE LA MATERIA Física y Química 3º Curso Educación Secundaria Obligatoria
Física y Química 3º Curso Educación Secundaria Obligatoria Curso académico 2016/2017 1 FÍSICA Y QUÍMICA TEMA 2: ESTRUCTURA ATÓMICA DE LA MATERIA Física y Química 3º Curso Educación Secundaria Obligatoria
La estructura atómica: el núcleo
 Tema 1 La estructura atómica: el núcleo Introducción. Modelos atómicos Composición del átomo. Partículas fundamentales Estructura del núcleo Estabilidad nuclear y energía de enlace nuclear Aplicaciones
Tema 1 La estructura atómica: el núcleo Introducción. Modelos atómicos Composición del átomo. Partículas fundamentales Estructura del núcleo Estabilidad nuclear y energía de enlace nuclear Aplicaciones
Contenidos. 1.- Primeras clasificaciones periódicas.
 LA TABLA PERIÓDICA. Contenidos 1.- Primeras clasificaciones periódicas. 1.1. Sistema periódico de Mendeleiev. 2.- La tabla periódica. 3.- Propiedades periódicas: 3.1. Tamaño de los átomos. Radios atómicos
LA TABLA PERIÓDICA. Contenidos 1.- Primeras clasificaciones periódicas. 1.1. Sistema periódico de Mendeleiev. 2.- La tabla periódica. 3.- Propiedades periódicas: 3.1. Tamaño de los átomos. Radios atómicos
ESQUEMA. De él cabe destacar el experimento que demostró que el modelo de Thompson era falso y los postulados que llevaron a que formulara su modelo:
 TEMA 2. ESTRUCTURA DE LA MATERIA.. MODELOS ATÓMICOS Dalton: Los átomos son indivisibles Thompson: Los átomos están formados por protones y neutrones. El átomo es una esfera de carga positiva y los electrones
TEMA 2. ESTRUCTURA DE LA MATERIA.. MODELOS ATÓMICOS Dalton: Los átomos son indivisibles Thompson: Los átomos están formados por protones y neutrones. El átomo es una esfera de carga positiva y los electrones
FÍSICA Y QUÍMICA 3º ESO ACTIVIDADES DE RECUPERACIÓN
 FÍSICA Y QUÍMICA 3º ESO ACTIVIDADES DE RECUPERACIÓN (PARTE 2) CURSO 2012/13 Nombre y apellidos: 1 LA CIENCIA Y SU MÉTODO. MEDIDA DE MAGNITUDES LOS ÁTOMOS Y SU COMPLEJIDAD 1. Qué explica el modelo atómico
FÍSICA Y QUÍMICA 3º ESO ACTIVIDADES DE RECUPERACIÓN (PARTE 2) CURSO 2012/13 Nombre y apellidos: 1 LA CIENCIA Y SU MÉTODO. MEDIDA DE MAGNITUDES LOS ÁTOMOS Y SU COMPLEJIDAD 1. Qué explica el modelo atómico
Un modelo atómico, por lo tanto consiste en representar de manera grafica, la dimensión atómica de la materia. El objetivo de estos modelos es que el
 Modelos atómicos Debido a que no se podían ver los átomos los científicos crearon modelos para describirlos, éstos fueron evolucionando a lo largo de la historia a medida que se descubrieron nuevas cosas.
Modelos atómicos Debido a que no se podían ver los átomos los científicos crearon modelos para describirlos, éstos fueron evolucionando a lo largo de la historia a medida que se descubrieron nuevas cosas.
El resultado es el Sistema Periódico. -En el sistema periódico los elementos están colocados por orden creciente de su número atómico (Z).
 Tema 2. La Tabla periódica -Desde hace tiempo los químicos han intentado ordenar los elementos de forma que queden agrupados aquellos que tienen propiedades químicas similares El resultado es el Sistema
Tema 2. La Tabla periódica -Desde hace tiempo los químicos han intentado ordenar los elementos de forma que queden agrupados aquellos que tienen propiedades químicas similares El resultado es el Sistema
1.5. TABLA PERIÓDICA.
 1.5. TABLA PERIÓDICA. 1.5.1. TABLA PERIÓDICA. La tabla periódica ordena todos los elementos conocidos según sus propiedades. Los últimos elementos, todavía no han recibido nombre oficial. El orden de los
1.5. TABLA PERIÓDICA. 1.5.1. TABLA PERIÓDICA. La tabla periódica ordena todos los elementos conocidos según sus propiedades. Los últimos elementos, todavía no han recibido nombre oficial. El orden de los
LA MATERIA. Características de los átomos
 LA MATERIA Características de los átomos Años más tarde del modelo atómico de Rutherford (1911) se descubrió una nueva partícula en el núcleo, el neutrón. Esta fue descubierta por Chadwick en 1932, y se
LA MATERIA Características de los átomos Años más tarde del modelo atómico de Rutherford (1911) se descubrió una nueva partícula en el núcleo, el neutrón. Esta fue descubierta por Chadwick en 1932, y se
ÁTOMOS Y RADIACTIVIDAD
 ÁTOMOS Y RADIACTIVIDAD 1 ATOMOS, MOLECULAS E IONES Atomo: Según Dalton un átomo se define como la cantidad básica de un elemento que puede intervenir en una combinación química. Los átomos están formados
ÁTOMOS Y RADIACTIVIDAD 1 ATOMOS, MOLECULAS E IONES Atomo: Según Dalton un átomo se define como la cantidad básica de un elemento que puede intervenir en una combinación química. Los átomos están formados
Átomos polielectrónicos Espín y configuraciones electrónicas Número y masa atómicos (isótopos) Tabla periódica y configuraciones electrónicas
 ESTRUCTURA ELECTRÓNICA Espín y configuraciones electrónicas Número y masa atómicos (isótopos) Tabla periódica y configuraciones electrónicas Átomos con un solo electrón: La energía depende solamente del
ESTRUCTURA ELECTRÓNICA Espín y configuraciones electrónicas Número y masa atómicos (isótopos) Tabla periódica y configuraciones electrónicas Átomos con un solo electrón: La energía depende solamente del
PORTAFOLIO DE EVIDENCIAS QUÍMICA I DE SEGUNDA OPORTUNIDAD I LEE DETENIDAMENTE CADA ENUNCIADO Y CONTESTA SEGÚN SE TE PIDA.
 PORTAFOLIO DE EVIDENCIAS QUÍMICA I DE SEGUNDA OPORTUNIDAD I LEE DETENIDAMENTE CADA ENUNCIADO Y CONTESTA SEGÚN SE TE PIDA. 1.- Ciencia que estudia las características y la composición de los materiales,
PORTAFOLIO DE EVIDENCIAS QUÍMICA I DE SEGUNDA OPORTUNIDAD I LEE DETENIDAMENTE CADA ENUNCIADO Y CONTESTA SEGÚN SE TE PIDA. 1.- Ciencia que estudia las características y la composición de los materiales,
El átomo: sus partículas elementales
 El átomo: sus partículas elementales Los rayos catódicos estaban constituidos por partículas cargadas negativamente ( a las que se llamo electrones) y que la relación carga/masa de éstas partículas era
El átomo: sus partículas elementales Los rayos catódicos estaban constituidos por partículas cargadas negativamente ( a las que se llamo electrones) y que la relación carga/masa de éstas partículas era
Integrantes :Natalia Castillo Carolina Cabello Laura Otálora Nicolás Osorio Asignatura : Química Curso : 2º año B
 Integrantes :Natalia Castillo Carolina Cabello Laura Otálora Nicolás Osorio Asignatura : Química Curso : 2º año B * Historia del Átomo: -El átomo en la antigüedad (pág. 3) -Leucipo y Demócrito (pág.4)
Integrantes :Natalia Castillo Carolina Cabello Laura Otálora Nicolás Osorio Asignatura : Química Curso : 2º año B * Historia del Átomo: -El átomo en la antigüedad (pág. 3) -Leucipo y Demócrito (pág.4)
MODELOS ATOMICOS. Solución Å; Ultravioleta; 1106 m/s
 MODELOS ATOMICOS 1. Calcular el valor del radio de la órbita que recorre el electrón del hidrogeno en su estado normal. Datos. h = 6 63 10 27 erg s, m(e ) = 9 1 10 28 gr, q(e ) = 4 8 10-10 u.e.e. Solución.
MODELOS ATOMICOS 1. Calcular el valor del radio de la órbita que recorre el electrón del hidrogeno en su estado normal. Datos. h = 6 63 10 27 erg s, m(e ) = 9 1 10 28 gr, q(e ) = 4 8 10-10 u.e.e. Solución.
1. Los elementos químicos
 RESUMEN de la UNIDAD 3. ELEMENTOS Y COMPUESTOS 1. Los elementos químicos La materia está formada por partículas denominadas átomos que, a su vez, están formados por otras partículas más pequeñas: protones,
RESUMEN de la UNIDAD 3. ELEMENTOS Y COMPUESTOS 1. Los elementos químicos La materia está formada por partículas denominadas átomos que, a su vez, están formados por otras partículas más pequeñas: protones,
UNIDAD 1: EL ÁTOMO Y EL SISTEMA PERIÓDICO
 UNIDAD 1: EL ÁTOMO Y EL SISTEMA PERIÓDICO 1. PRIMERAS TEORÍAS ATÓMICAS Demócrito, filósofo griego que vivió en el siglo IV a. C. propuso que, si se dividía la materia en trozos cada vez más pequeños, debería
UNIDAD 1: EL ÁTOMO Y EL SISTEMA PERIÓDICO 1. PRIMERAS TEORÍAS ATÓMICAS Demócrito, filósofo griego que vivió en el siglo IV a. C. propuso que, si se dividía la materia en trozos cada vez más pequeños, debería
NOMBRE: CURSO: HOJAS DE ACTIVIDADES FÍSICA Y QUÍMICA 3º DE ESO
 NOMBRE: URSO: HOJAS DE ATIVIDADES FÍSIA Y QUÍMIA 3º DE ESO Tema 4 ESTRUTURA DEL ÁTOMO Los trozos de una piedra partida en dos, incluso reducida a polvo, siguen siendo piedra, y cada uno de los fragmentos
NOMBRE: URSO: HOJAS DE ATIVIDADES FÍSIA Y QUÍMIA 3º DE ESO Tema 4 ESTRUTURA DEL ÁTOMO Los trozos de una piedra partida en dos, incluso reducida a polvo, siguen siendo piedra, y cada uno de los fragmentos
ESTRUCTURA DE LOS ATOMOS Ing. Alfredo Luis Rojas B.
 CAPITULO 4 ESTRUCTURA DE LOS ATOMOS Ing. Alfredo Luis Rojas B. Aproximadamente 400 a.c. el filosofo griego Democrito sugirió que toda la materia esta formada por partículas minúsculas, discretas e indivisibles,
CAPITULO 4 ESTRUCTURA DE LOS ATOMOS Ing. Alfredo Luis Rojas B. Aproximadamente 400 a.c. el filosofo griego Democrito sugirió que toda la materia esta formada por partículas minúsculas, discretas e indivisibles,
LA MATERIA: PROPIEDADES ELÉCTRICAS Y EL ÁTOMO
 FICH 1 DE REFUERO 1. Dado el siguiente átomo: 16 8O. a) Determina cuántos protones y neutrones tiene en el núcleo. b) Escribe la representación de un isótopo suyo. 2. Determina el número atómico y el número
FICH 1 DE REFUERO 1. Dado el siguiente átomo: 16 8O. a) Determina cuántos protones y neutrones tiene en el núcleo. b) Escribe la representación de un isótopo suyo. 2. Determina el número atómico y el número
ESTRUCTURA ATOMICA DESARROLLO HISTORICO
 ESTRUCTURA ATOMICA DESARROLLO HISTORICO MODELOS ATOMICOS Átomo: Partícula más pequeña de un elemento que retiene sus propiedades. DEMOCRITO Y LEUCIPO. En el Siglo V A.C. dos Filósofos Griegos Leucipo y
ESTRUCTURA ATOMICA DESARROLLO HISTORICO MODELOS ATOMICOS Átomo: Partícula más pequeña de un elemento que retiene sus propiedades. DEMOCRITO Y LEUCIPO. En el Siglo V A.C. dos Filósofos Griegos Leucipo y
Atomos, Moléculas e Iones. Basado en Capítulo 2 de Química (Chang, 2010) Dr. Hernández Castillo
 Atomos, Moléculas e Iones Basado en Capítulo 2 de Química (Chang, 2010) Dr. Hernández Castillo Atomo Grecia Demócrito Filosofía Química??? Materialismo monista atomos significaba indivisible Teoría Atómica
Atomos, Moléculas e Iones Basado en Capítulo 2 de Química (Chang, 2010) Dr. Hernández Castillo Atomo Grecia Demócrito Filosofía Química??? Materialismo monista atomos significaba indivisible Teoría Atómica
Como esta formada la materia?
 Como esta formada la materia? Demócrito, filósofo griego que vivió en el siglo IV a. C. propuso que, si se dividía la materia en trozos cada vez más pequeños, debería llegarse a una porción que ya no podría
Como esta formada la materia? Demócrito, filósofo griego que vivió en el siglo IV a. C. propuso que, si se dividía la materia en trozos cada vez más pequeños, debería llegarse a una porción que ya no podría
QUIMICA GENERAL. Docente : Raquel Villafrades Torres
 Universidad Pontificia Bolivariana QUIMICA GENERAL Docente : Raquel Villafrades Torres TEORIA ATOMICA DE DALTON (1808) BASES Ley de conservación de la masa: La masa total de las sustancias presentes después
Universidad Pontificia Bolivariana QUIMICA GENERAL Docente : Raquel Villafrades Torres TEORIA ATOMICA DE DALTON (1808) BASES Ley de conservación de la masa: La masa total de las sustancias presentes después
Con posterioridad el físico alemán Sommerfeld introdujo en el modelo la posibilidad de órbitas elípticas. Köningsberg, Munich, 1951
 4. El paso de una órbita a otra supone la absorción o emisión de radiación. El átomo sólo absorberá o emitirá la radiación justa para pasar de una órbita a otra. Las órbitas de los electrones son estables
4. El paso de una órbita a otra supone la absorción o emisión de radiación. El átomo sólo absorberá o emitirá la radiación justa para pasar de una órbita a otra. Las órbitas de los electrones son estables
Unidad 1 Estructura atómica de la materia. Teoría cuántica
 Unidad 1 Estructura atómica de la materia. Teoría cuántica 1.El átomo y la constitución de la materia DALTON NO ACEPTADO POR LOS FÍSICOS que creían en la idea de que los átomos se encontraban como disueltos
Unidad 1 Estructura atómica de la materia. Teoría cuántica 1.El átomo y la constitución de la materia DALTON NO ACEPTADO POR LOS FÍSICOS que creían en la idea de que los átomos se encontraban como disueltos
LA TEORIA ATOMICA John Dalton
 LA TEORIA ATOMICA En 1808, un científico inglés, el profesor John Dalton, formuló una definición precisa de las unidades indivisibles con las que está formada la materia y que llamamos átomos 1766-1844
LA TEORIA ATOMICA En 1808, un científico inglés, el profesor John Dalton, formuló una definición precisa de las unidades indivisibles con las que está formada la materia y que llamamos átomos 1766-1844
El carbono es el elemento básico para la vida. Todas las moléculas biológicas. importantes, con la excepción del agua, contienen carbono.
 3. EL CARBONO. 3.1. CARBONO. 3.1.1. ESTRUCTURA ELECTRÓNICA. El carbono es el elemento básico para la vida. Todas las moléculas biológicas importantes, con la excepción del agua, contienen carbono. Su número
3. EL CARBONO. 3.1. CARBONO. 3.1.1. ESTRUCTURA ELECTRÓNICA. El carbono es el elemento básico para la vida. Todas las moléculas biológicas importantes, con la excepción del agua, contienen carbono. Su número
Observa la imagen de la derecha. Puedes identificar el núcleo y la nube de electrones? Qué crees que representan las esferas azules, rojas y grises?
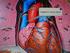 reflexiona Nuestro mundo está lleno de diversidad. Existe una variedad asombrosa en todos los materiales, sustancias y seres vivos que existen en la Tierra. Observa la imagen de la derecha. Incluso en
reflexiona Nuestro mundo está lleno de diversidad. Existe una variedad asombrosa en todos los materiales, sustancias y seres vivos que existen en la Tierra. Observa la imagen de la derecha. Incluso en
- Dalton: TEORIA ATÓMICA ( inicio del SIGLO XIX) - Descubrimiento del electrónjoseph John Thomson ( )
 REPASO QUÍMICA 01 - Dalton: TEORIA ATÓMICA ( inicio del SIGLO XIX) - Descubrimiento del electrónjoseph John Thomson (1856-1940) Modelo de Thompson Modelo del budín de pasas - EN 1895 WILHELM RONTGEN Descubre
REPASO QUÍMICA 01 - Dalton: TEORIA ATÓMICA ( inicio del SIGLO XIX) - Descubrimiento del electrónjoseph John Thomson (1856-1940) Modelo de Thompson Modelo del budín de pasas - EN 1895 WILHELM RONTGEN Descubre
Qué ocurriría si dividiéramos un trozo de materia muchas veces? Llegaríamos hasta una parte indivisible o podríamos seguir dividiendo sin parar?
 3 El átomo y los modelos atómicos El átomo a través de la historia Las primeras teorías atomistas Qué ocurriría si dividiéramos un trozo de materia muchas veces? Llegaríamos hasta una parte indivisible
3 El átomo y los modelos atómicos El átomo a través de la historia Las primeras teorías atomistas Qué ocurriría si dividiéramos un trozo de materia muchas veces? Llegaríamos hasta una parte indivisible
Ejercicios resueltos de 3º de E.S.O.
 Ejercicios resueltos de 3º de E.S.O. Estructura de la materia. Modelos atómicos Ejercicio resuelto nº 1 Si el número másico de un átomo es A = 30 y tiene 12 protones, calcula su número de neutrones. Resolución
Ejercicios resueltos de 3º de E.S.O. Estructura de la materia. Modelos atómicos Ejercicio resuelto nº 1 Si el número másico de un átomo es A = 30 y tiene 12 protones, calcula su número de neutrones. Resolución
MODELOS ATÓMICOS 2ª PARTE
 MODELOS ATÓMICOS 2ª PARTE Teoría Atómica de Joseph John Thomson Diseño Experimental de Joseph John Thomson (1856-1940) Utiliza Tubos de Rayos Catódicos, en los cuales estudia el comportamiento de los gases
MODELOS ATÓMICOS 2ª PARTE Teoría Atómica de Joseph John Thomson Diseño Experimental de Joseph John Thomson (1856-1940) Utiliza Tubos de Rayos Catódicos, en los cuales estudia el comportamiento de los gases
A su vez, una molécula está compuesta por átomos. Cada uno de ellos posee unas propiedades diferentes en el interior de la molécula que constituyen.
 Constitución de la materia. Supongamos que cualquier sustancia de la naturaleza la dividimos en partes cada vez más pequeñas, conservando cada una de ellas las propiedades de la sustancia inicial. Si seguimos
Constitución de la materia. Supongamos que cualquier sustancia de la naturaleza la dividimos en partes cada vez más pequeñas, conservando cada una de ellas las propiedades de la sustancia inicial. Si seguimos
QUÍMICA 2º BACH. TEMA 1. ESTRUCTURA ATÓMICA.
 Modelos atómicos QUÍMICA 2º BACH. TEMA 1. ESTRUCTURA ATÓMICA. Teoría atómica de Dalton: La materia está formada por átomos indivisibles. Los átomos de un elemento son distintos de los átomos de otro elemento
Modelos atómicos QUÍMICA 2º BACH. TEMA 1. ESTRUCTURA ATÓMICA. Teoría atómica de Dalton: La materia está formada por átomos indivisibles. Los átomos de un elemento son distintos de los átomos de otro elemento
INSTITUCION EDUCATIVA DIVERSIFICADO DE CHIA TALLER MODELOS ATOMICOS. GRADO OCTAVO Realizar cada una de las actividades propuestas de forma
 INSTITUCION EDUCATIVA DIVERSIFICADO DE CHIA TALLER MODELOS ATOMICOS. GRADO OCTAVO Realizar cada una de las actividades propuestas de forma responsable, la sustentación es oral e individual en la próxima
INSTITUCION EDUCATIVA DIVERSIFICADO DE CHIA TALLER MODELOS ATOMICOS. GRADO OCTAVO Realizar cada una de las actividades propuestas de forma responsable, la sustentación es oral e individual en la próxima
Colección de problemas Unidad 2
 Facultad de Química, UNAM Curso: Química General I Colección de problemas Unidad 2 1. Describe una contribución importante a la ciencia hecha por cada uno de los científicos siguientes: Dalton, Thomson,
Facultad de Química, UNAM Curso: Química General I Colección de problemas Unidad 2 1. Describe una contribución importante a la ciencia hecha por cada uno de los científicos siguientes: Dalton, Thomson,
Guía Temática de Química
 Guía Temática de Química Introducción a la Química Definición de química y de ciencias afines a ella Diferenciación de las ciencias afines a la química 1 Conceptos básicos de química y el método científico
Guía Temática de Química Introducción a la Química Definición de química y de ciencias afines a ella Diferenciación de las ciencias afines a la química 1 Conceptos básicos de química y el método científico
U N A M. Facultad de Ingeniería MODELO ATÓMICO DE J. J. THOMSON MODELO ATÓMICO DE ERNEST RUTHERFORD DESCUBRIMIENTO DEL PROTÓN Y DEL NEUTRON
 MODELO ATÓMICO DE J. J. THOMSON MODELO ATÓMICO DE ERNEST RUTHERFORD DESCUBRIMIENTO DEL PROTÓN Y DEL NEUTRON M. C. Q. Alfredo Velásquez Márquez Modelo Atómico de J. J. Thomson Electrones de Carga Negativa
MODELO ATÓMICO DE J. J. THOMSON MODELO ATÓMICO DE ERNEST RUTHERFORD DESCUBRIMIENTO DEL PROTÓN Y DEL NEUTRON M. C. Q. Alfredo Velásquez Márquez Modelo Atómico de J. J. Thomson Electrones de Carga Negativa
Química General UNEFA
 ESTRUCTURA ATOMICA El átomo se define como la unidad básica y estructural de la materia, en el cual podemos distinguir dos partes: el núcleo y la corteza. - El núcleo es la parte central del átomo y contiene
ESTRUCTURA ATOMICA El átomo se define como la unidad básica y estructural de la materia, en el cual podemos distinguir dos partes: el núcleo y la corteza. - El núcleo es la parte central del átomo y contiene
LOS COLORES DE LOS ELEMENTOS
 LOS COLORES DE LOS ELEMENTOS Expresiones tan comunes y sugestivas como "rojo cadmio", "verde esmeralda", "blanco de titanio" o "azul turquesa" relacionan muy directamente un color con un material. Como
LOS COLORES DE LOS ELEMENTOS Expresiones tan comunes y sugestivas como "rojo cadmio", "verde esmeralda", "blanco de titanio" o "azul turquesa" relacionan muy directamente un color con un material. Como
ALUMNO: AUTORA: Prof. Ma. Laura Sanchez
 ALUMNO: AUTORA: Prof. Ma. Laura Sanchez 1.1 Evolución de las teorías atómicas Desde la antigüedad se ha discutido acerca de cómo está formada la materia, especialmente si es infinitamente divisible, o
ALUMNO: AUTORA: Prof. Ma. Laura Sanchez 1.1 Evolución de las teorías atómicas Desde la antigüedad se ha discutido acerca de cómo está formada la materia, especialmente si es infinitamente divisible, o
Colegio Alberto Pérez Institución Teresiana Departamento de Ciencias Química Profesora Caterina González Poblete. Núcleo. (protones y neutrones)
 Colegio Alberto Pérez Institución Teresiana Departamento de Ciencias Química Profesora Caterina González Poblete EL ÁTOMO Núcleo Envoltura (electrones) (protones y neutrones) El átomo, como lo conocemos
Colegio Alberto Pérez Institución Teresiana Departamento de Ciencias Química Profesora Caterina González Poblete EL ÁTOMO Núcleo Envoltura (electrones) (protones y neutrones) El átomo, como lo conocemos
Núcleo Atómico. El núcleo es una masa muy compacta formada por protones y neutrones.
 Núcleo Atómico Profesor: Robinson Pino H. 1 COMPONENTES DEL NÚCLEO ATÓMICO El núcleo es una masa muy compacta formada por protones y neutrones. PROTÓN PROTÓN(p + ) Es una partícula elemental con carga
Núcleo Atómico Profesor: Robinson Pino H. 1 COMPONENTES DEL NÚCLEO ATÓMICO El núcleo es una masa muy compacta formada por protones y neutrones. PROTÓN PROTÓN(p + ) Es una partícula elemental con carga
Colegio San Lorenzo - Copiapó - Región de Atacama Per Laborem ad Lucem
 TEMARIO EXAMENES QUIMICA 2012 7º BASICO Descubrimiento del átomo: Quién lo descubrió y su significado Estructura atómica: Partes del átomo, características del núcleo y la corteza, cálculo del protón,
TEMARIO EXAMENES QUIMICA 2012 7º BASICO Descubrimiento del átomo: Quién lo descubrió y su significado Estructura atómica: Partes del átomo, características del núcleo y la corteza, cálculo del protón,
EL ÁTOMO CONTENIDOS. ANTECEDENTES HISTÓRICOS. ( ) MODELOS ATÓMICOS. RAYOS CATÓDICOS. MODELO DE THOMSON.
 EL ÁTOMO CONTENIDOS. 1.- Antecedentes históricos.( ) 2.- Partículas subatómicas. ( ) 3.- Modelo atómico de Thomsom. 4.- Los rayos X. 5.- La radiactividad. 6.- Modelo atómico de Rutherford. 7.- Radiación
EL ÁTOMO CONTENIDOS. 1.- Antecedentes históricos.( ) 2.- Partículas subatómicas. ( ) 3.- Modelo atómico de Thomsom. 4.- Los rayos X. 5.- La radiactividad. 6.- Modelo atómico de Rutherford. 7.- Radiación
TEMA 4 (I) ESTRUCTURA ATÓMICA.
 Estructura Atómica, Sistema Periódico y Enlace Químico. 1 TEMA 4 (I) ESTRUCTURA ATÓMICA. 1. DESCUBRIMIENTO DE LA ESTRUCTURA ATÓMICA. 1.- Qué experimentos condujeron a la idea del núcleo atómico? (3.12)
Estructura Atómica, Sistema Periódico y Enlace Químico. 1 TEMA 4 (I) ESTRUCTURA ATÓMICA. 1. DESCUBRIMIENTO DE LA ESTRUCTURA ATÓMICA. 1.- Qué experimentos condujeron a la idea del núcleo atómico? (3.12)
PROYECTO PLATAFORMA VIRTUAL PRUEBA SABER 11 COLEGIO ANDRES BELLO
 PROYECTO PLATAFORMA VIRTUAL PRUEBA SABER 11 COLEGIO ANDRES BELLO QUÍMICA PROFESORA: ADRIANA GUTIERREZ RIVAS GRADO 11 SAN JOSE DE CÚCUTA 20/07/12 1451. El elemento Q reacciona con el oxígeno formando el
PROYECTO PLATAFORMA VIRTUAL PRUEBA SABER 11 COLEGIO ANDRES BELLO QUÍMICA PROFESORA: ADRIANA GUTIERREZ RIVAS GRADO 11 SAN JOSE DE CÚCUTA 20/07/12 1451. El elemento Q reacciona con el oxígeno formando el
Una mezcla es un compuesto formado por varias sustancias con distintas propiedades
 COMPOSICIÓN DE LA MATERIA Mezclas homogéneas y heterogéneas Una mezcla es un compuesto formado por varias sustancias con distintas propiedades Algunos sistemas materiales como la leche a simple vista parecen
COMPOSICIÓN DE LA MATERIA Mezclas homogéneas y heterogéneas Una mezcla es un compuesto formado por varias sustancias con distintas propiedades Algunos sistemas materiales como la leche a simple vista parecen
UNIDAD 10.- LAS UNIONES ENTRE ÁTOMOS. Cuestiones de evaluación inicial. 2.- Cuántos protones y cuantos neutrones tiene el Carbono?
 UNIDAD 10.- LAS UNIONES ENTRE ÁTOMOS Cuestiones de evaluación inicial 1.- Cuántos elementos químicos conoces? 2.- Cuántos protones y cuantos neutrones tiene el Carbono? 3.- Qué es el sistema periódico?
UNIDAD 10.- LAS UNIONES ENTRE ÁTOMOS Cuestiones de evaluación inicial 1.- Cuántos elementos químicos conoces? 2.- Cuántos protones y cuantos neutrones tiene el Carbono? 3.- Qué es el sistema periódico?
Tema II: Estructura atómica y tabla periódica
 República Bolivariana de Venezuela Ministerio del Poder Popular para la Educación U.E. Colegio Santo Tomás de Villanueva Departamento de Ciencias Cátedra: Química Orgánica 5 Año Tema II: Estructura atómica
República Bolivariana de Venezuela Ministerio del Poder Popular para la Educación U.E. Colegio Santo Tomás de Villanueva Departamento de Ciencias Cátedra: Química Orgánica 5 Año Tema II: Estructura atómica
Configuración Electrónica
 Configuración Electrónica La configuración electrónica de un átomo indica la forma como están distribuidos los electrones entre los distintos orbitales atómicos. Según el Principio de Exclusión de Pauli,
Configuración Electrónica La configuración electrónica de un átomo indica la forma como están distribuidos los electrones entre los distintos orbitales atómicos. Según el Principio de Exclusión de Pauli,
Ficha de refuerzo de competencias 1
 . La estructura de la materia. Agrupaciones de átomos En esta ficha trabajarás... El átomo, partícula constituyente de la materia. Dentro del átomo: electrones, protones y neutrones. La teoría atómica
. La estructura de la materia. Agrupaciones de átomos En esta ficha trabajarás... El átomo, partícula constituyente de la materia. Dentro del átomo: electrones, protones y neutrones. La teoría atómica
SOLUCIONARIO EJERCICIOS PROPUESTOS
 Unidad 4 Los átomos y su complejidad EJERCICIOS PROPUESTOS 1. Argumenta cómo se explica la ley de la conservación de la masa en las reacciones químicas mediante la teoría atómica de Dalton. Calcula cuánto
Unidad 4 Los átomos y su complejidad EJERCICIOS PROPUESTOS 1. Argumenta cómo se explica la ley de la conservación de la masa en las reacciones químicas mediante la teoría atómica de Dalton. Calcula cuánto
Ejercicios y respuestas del apartado: Propiedades de los períodos y de los grupos. Electronegatividad
 Ejercicios y respuestas del apartado: Propiedades de los períodos y de los grupos. Electronegatividad Propiedades periódicas (1) La electronegatividad en la tabla periódica disminuye cuanto más a la (1)
Ejercicios y respuestas del apartado: Propiedades de los períodos y de los grupos. Electronegatividad Propiedades periódicas (1) La electronegatividad en la tabla periódica disminuye cuanto más a la (1)
ESTRUCTURA ATÓMICA - PREGUNTAS DE TEST
 ESTRUCTURA ATÓMICA - PREGUNTAS DE TEST Serie A: PARTICULAS SUBATOMICAS: Serie B- ESPECTROS: Serie C- COMPOSICION DEL ÁTOMO Serie D- ESTRUCTURA ELECTRÓNICA Serie E- ATOMO DE THOMPSON Serie F- DEFECTO DE
ESTRUCTURA ATÓMICA - PREGUNTAS DE TEST Serie A: PARTICULAS SUBATOMICAS: Serie B- ESPECTROS: Serie C- COMPOSICION DEL ÁTOMO Serie D- ESTRUCTURA ELECTRÓNICA Serie E- ATOMO DE THOMPSON Serie F- DEFECTO DE
Solucionario Cuaderno Estrategias y Ejercitación Modelo atómico de la materia II: números cuánticos y configuración electrónica
 Solucionario Cuaderno Estrategias y Ejercitación Modelo atómico de la materia II: números cuánticos y configuración electrónica Química Técnico Profesional Intensivo SCUACTC002TC83-A16V1 Ítem Alternativa
Solucionario Cuaderno Estrategias y Ejercitación Modelo atómico de la materia II: números cuánticos y configuración electrónica Química Técnico Profesional Intensivo SCUACTC002TC83-A16V1 Ítem Alternativa
PARTÍCULAS FUNDAMENTALES. NÚMEROS CUÁNTICOS. PROPIEDADES PERIÓDICAS.
 PARTÍCULAS FUNDAMENTALES. NÚMEROS CUÁNTICOS. PROPIEDADES PERIÓDICAS. PARTÍCULAS FUNDAMENTALES. CONCEPTOS PREVIOS De acuerdo con lo anterior, en un átomo hay tres partículas fundamentales: protones y neutrones,
PARTÍCULAS FUNDAMENTALES. NÚMEROS CUÁNTICOS. PROPIEDADES PERIÓDICAS. PARTÍCULAS FUNDAMENTALES. CONCEPTOS PREVIOS De acuerdo con lo anterior, en un átomo hay tres partículas fundamentales: protones y neutrones,
Colegio Pasionista de Quilpué Departamento de Ciencias Ciencias Naturales 8 año básico 2015 Miss. Cecilia Rojas Olguín. El átomo.
 Colegio Pasionista de Quilpué Departamento de Ciencias Ciencias Naturales 8 año básico 2015 Miss. Cecilia Rojas Olguín El átomo 06 de Marzo 2015 Objetivos de la clase Comprender el Modelo corpuscular de
Colegio Pasionista de Quilpué Departamento de Ciencias Ciencias Naturales 8 año básico 2015 Miss. Cecilia Rojas Olguín El átomo 06 de Marzo 2015 Objetivos de la clase Comprender el Modelo corpuscular de
Sistema Periódico de los elementos. 2º Bachillerato
 Sistema Periódico de los elementos 2º Bachillerato Índice 1. Clasificación de los elementos 2. Núcleo atómico 3. Configuración electrónica 4. La tabla periódica 5. Propiedades periódicas Tamaño y radio
Sistema Periódico de los elementos 2º Bachillerato Índice 1. Clasificación de los elementos 2. Núcleo atómico 3. Configuración electrónica 4. La tabla periódica 5. Propiedades periódicas Tamaño y radio
Elementos ordenados según su número atómico (Z, número de p + ) Hay 18 PERÍODOS
 TABLA PERIÓDICA Elementos ordenados según su número atómico (Z, número de p + ) Columnas Filas GRUPOS PERÍODOS Familias de elementos con propiedades comunes Hay 18 División principal Elementos representativos
TABLA PERIÓDICA Elementos ordenados según su número atómico (Z, número de p + ) Columnas Filas GRUPOS PERÍODOS Familias de elementos con propiedades comunes Hay 18 División principal Elementos representativos
TABLA PERIODICA Y PERIOCIDAD
 ENSAYO QUIMICA MODELOS ATOMICOS Y TABLA PERIODICA El mundo que hoy habitamos tiene infinidades de elementos que lo conforman, los océanos, la tierra, una mesa o hasta nosotros mismos estamos formados por
ENSAYO QUIMICA MODELOS ATOMICOS Y TABLA PERIODICA El mundo que hoy habitamos tiene infinidades de elementos que lo conforman, los océanos, la tierra, una mesa o hasta nosotros mismos estamos formados por
Tercero: una reacción química incluye sólo la separación combinación o reordenamiento de átomos sin crearlos o destruirlos.
 Coomppoonneennt teess ffuunnddaameennt taalleess ddeell áát toomoo El filósofo griego demócrito en el siglo V a.c. propuso la idea de que la materia estaba formada por partículas muy pequeñas indivisibles
Coomppoonneennt teess ffuunnddaameennt taalleess ddeell áát toomoo El filósofo griego demócrito en el siglo V a.c. propuso la idea de que la materia estaba formada por partículas muy pequeñas indivisibles
La tabla periódica es la estrella orientadora para la exploración en el capo de la química, la física, la mineralogía y la técnica.
 SISTEMA PERIÓDICO DE LOS ELEMENTOS La tabla periódica es la estrella orientadora para la exploración en el capo de la química, la física, la mineralogía y la técnica. Niels Bohr Principio de exclusión
SISTEMA PERIÓDICO DE LOS ELEMENTOS La tabla periódica es la estrella orientadora para la exploración en el capo de la química, la física, la mineralogía y la técnica. Niels Bohr Principio de exclusión
2. Cuál(es) de las siguientes propiedades periódicas aumenta(n) al incrementarse el número atómico en un grupo?
 Programa Estándar Anual Nº Guía práctica Teoría atómica III: tabla periódica y propiedades periódicas Ejercicios PSU 1. En un sistema periódico muy simplificado, como el que se muestra en la figura, los
Programa Estándar Anual Nº Guía práctica Teoría atómica III: tabla periódica y propiedades periódicas Ejercicios PSU 1. En un sistema periódico muy simplificado, como el que se muestra en la figura, los
Programa de Acceso Inclusivo, Equidad y Permanencia PAIEP U. de Santiago. Química
 Modelos atómicos Los filósofos de la antigüedad especularon sobre cómo estaba formada la materia. Demócrito (460-370 a.c) y otros filósofos anteriores a él, pensaban que el mundo material debería estar
Modelos atómicos Los filósofos de la antigüedad especularon sobre cómo estaba formada la materia. Demócrito (460-370 a.c) y otros filósofos anteriores a él, pensaban que el mundo material debería estar
Guía de Estudio para 1er Parcial Temas Selectos de Química
 Guía de Estudio para 1er Parcial Temas Selectos de Química 1. Menciona que científicos ordenaron los elementos conocidos en su época en triadas (grupos de tres), en octavas, por número atómico y quien
Guía de Estudio para 1er Parcial Temas Selectos de Química 1. Menciona que científicos ordenaron los elementos conocidos en su época en triadas (grupos de tres), en octavas, por número atómico y quien
INTRUDUCCIÓN ESTRUCTURA ATÓMICA
 LECTURA Nº 1: ESTRUCTURA ATÓMICA Resumen realizado con fines educativos por Ing. José Prado (UNEFA Núcleo Mérida) de: P. ANDER Y A. SONNESSA. (1970). Principios de Química. Editorial Limusa S.A. MAHAM,
LECTURA Nº 1: ESTRUCTURA ATÓMICA Resumen realizado con fines educativos por Ing. José Prado (UNEFA Núcleo Mérida) de: P. ANDER Y A. SONNESSA. (1970). Principios de Química. Editorial Limusa S.A. MAHAM,
ÁTOMO..su historia y su estudio
 ÁTOMO.su historia y su estudio LOS GRIEGOS Y SU APORTE 2000 años antes de Cristo, la civilización griega representada por varios filósofos, ya se preguntaban acerca de qué estaba formado el universo?...
ÁTOMO.su historia y su estudio LOS GRIEGOS Y SU APORTE 2000 años antes de Cristo, la civilización griega representada por varios filósofos, ya se preguntaban acerca de qué estaba formado el universo?...
J.J Thomson propone el primer modelo de átomo:
 MODELOS ATÓMICOS. DALTON En 1808, Dalton publicó sus ideas sobre el modelo atómico de la materia las cuales han servido de base a la química moderna. Los principios fundamentales de esta teoría son: 1.
MODELOS ATÓMICOS. DALTON En 1808, Dalton publicó sus ideas sobre el modelo atómico de la materia las cuales han servido de base a la química moderna. Los principios fundamentales de esta teoría son: 1.
3. El sistema periódico de los elementos. 3. El sistema periódico de los elementos. 3. El sistema periódico de los elementos
 3. El sistema periódico de los elementos Clasificación de los elementos químicos en el siglo XIX: los químicos de la época tenían una idea vaga de los átomos; no conocían p + ni e -. Clasificaban los elementos
3. El sistema periódico de los elementos Clasificación de los elementos químicos en el siglo XIX: los químicos de la época tenían una idea vaga de los átomos; no conocían p + ni e -. Clasificaban los elementos
FÍSICA Y QUÍMICA Solucionario ELECTRONES Y ENLACES
 FÍSICA Y QUÍMICA Solucionario ELECTRONES Y ENLACES 1.* Indicad cuántos electrones tienen en la última capa cada uno de estos elementos. a) C 4 f) O 6 k) K 1 b) F 7 g) P 5 l) S 6 c) Ne 8 h) H 1 m) He 8
FÍSICA Y QUÍMICA Solucionario ELECTRONES Y ENLACES 1.* Indicad cuántos electrones tienen en la última capa cada uno de estos elementos. a) C 4 f) O 6 k) K 1 b) F 7 g) P 5 l) S 6 c) Ne 8 h) H 1 m) He 8
Repartido nº3 Estructura electrónica y Tabla Periódica
 La periferia: Recordamos: Repartido nº3 Estructura electrónica y Tabla Periódica En la periferia se encuentran los electrones. La cantidad de electrones de un átomo equivale a la cantidad de protones,
La periferia: Recordamos: Repartido nº3 Estructura electrónica y Tabla Periódica En la periferia se encuentran los electrones. La cantidad de electrones de un átomo equivale a la cantidad de protones,
REFUERZO ESPECIAL CIENCIAS NATURALES. APRENDIZAJE ESPERADO: Afianzar los procesos básicos del área para su promoción al siguiente grado.
 REFUERZO ESPECIAL CIENCIAS NATURALES SÉPTIMO PERIODO IV IVON GÓMEZ APRENDIZAJE ESPERADO: Afianzar los procesos básicos del área para su promoción al siguiente grado. Apreciado estudiante: Las actividades
REFUERZO ESPECIAL CIENCIAS NATURALES SÉPTIMO PERIODO IV IVON GÓMEZ APRENDIZAJE ESPERADO: Afianzar los procesos básicos del área para su promoción al siguiente grado. Apreciado estudiante: Las actividades
SOLUCIONARIO Guía Estándar Anual
 SOLUCIONARIO Guía Estándar Anual El enlace químico SGUICES004CB33-A16V1 Ítem Alternativa Habilidad 1 E Reconocimiento 2 B Aplicación 3 C Comprensión 4 D Comprensión 5 D Aplicación 6 D Aplicación 7 D Comprensión
SOLUCIONARIO Guía Estándar Anual El enlace químico SGUICES004CB33-A16V1 Ítem Alternativa Habilidad 1 E Reconocimiento 2 B Aplicación 3 C Comprensión 4 D Comprensión 5 D Aplicación 6 D Aplicación 7 D Comprensión
