Para Diagnóstico In Vitro. Número de Catálogo. Volumen de Reactivo. Número de Lote. Condiciones de Almacenamiento. Fecha de Vencimiento
|
|
|
- Alfredo Ramírez Álvarez
- hace 5 años
- Vistas:
Transcripción
1 Servicio Técnico: Servicio al Cliente (EUA): Servicio al Cliente (UE): IdentiClone TCRD Gene Clonality Assay Para la Identificación de Reordenamientos Clonales de Genes Codificantes para la Cadena Delta del Receptor de la Célula T Para Diagnóstico In Vitro Simbología utilizada Para Diagnóstico In Vitro Número de Catálogo Volumen de Reactivo Número de Lote Condiciones de Almacenamiento Fecha de Vencimiento Representante Autorizado en la Unión Europea Fabricante Consulte las Instrucciones para su Uso Condiciones de almacenamiento: -65 C a -85ºC (Los controles de ADN pueden separarse del resto de los materiales del ensayo y mantenerse a una temperatura entre 2 C y 8 C) Nro. de Catálogo Productos Cantidad Reacciones IdentiClone TCRD Gene Clonality Assay MegaKit ABI Fluorescence Detection 330 Reacciones
2 Página 2 de 15 Contenidos 1. MARCA REGISTRADA USO PREVISTO RESUMEN Y DESCRIPCIÓN DEL ENSAYO PRINCIPIOS DEL PROCEDIMIENTO REACCIÓN EN CADENA DE LA POLIMERASA (PCR) DETECCIÓN DE FLUORESCENCIA DIFERENCIAL REACTIVOS COMPONENTES PRECAUCIONES Y ADVERTENCIAS ALMACENAMIENTO Y MANIPULACIÓN INSTRUMENTOS TERMOCICLADOR ABI 310, ABI 3100, Ó ABI RECOGIDA Y PREPARACIÓN DE LA MUESTRA PRECAUCIONES SUSTANCIAS QUE INTERFIEREN REQUERIMIENTOS DE LA MUESTRA Y SU MANIPULACIÓN PREPARACIÓN DE LA MUESTRA CONSERVACIÓN DE LA MUESTRA PROCEDIMIENTO DEL ENSAYO MATERIALES SUMINISTRADOS EN EL KIT MATERIALES REQUERIDOS PERO NO SUMINISTRADOS EN EL KIT PREPARACIÓN DE LOS REACTIVOS AMPLIFICACIÓN DETECCIÓN DE FLUORESCENCIA ABI CONTROL DE CALIDAD CONTROLES POSITIVOS RECOMENDADOS INTERPRETACIÓN DE LOS RESULTADOS ANÁLISIS INTERPRETACIÓN DE LA MUESTRA PROBLEMA LIMITACIONES DEL ENSAYO VALORES ESPERADOS TAMAÑO ESPERADO DE LOS PRODUCTOS AMPLIFICADOS RESULTADOS DE LA MUESTRA CARACTERÍSTICAS ANALÍTICAS BIBLIOGRAFÍA SERVICIO TÉCNICO Y AL CLIENTE ASPECTOS LEGALES... 15
3 Página 3 de Marca Registrada IdentiClone TCRD Gene Clonality Assay MegaKit ABI Fluorescence Detection 2. Uso Previsto El IdentiClone TCRD Gene Clonality Assay, es una prueba diagnóstica in vitro basada en la reacción en cadena de la polimerasa (PCR), diseñada para la identificación de reordenamientos clonales de genes codificantes para la cadena delta del receptor de la célula T en pacientes con sospechas de enfermedades linfoproliferativas. Específicamente, el TCRD Gene Clonality Assay puede utilizarse con los siguientes fines: Identificar clonalidad en enfermedades linfoproliferativas atípicas. Sustentar un diagnóstico diferencial entre lesiones reactivas y neoplasias hematológicas de células T, y de algunas de células B inmaduras. Determinar el linaje involucrado en enfermedades linfoproliferativas diferenciadas. Monitorizar y evaluar recurrencias de la enfermedad. 3. Resumen y descripción del ensayo Los reordenamientos de los genes que codifican los receptores antigénicos ocurren durante la ontogenia de los linfocitos T y B. Dichos reordenamientos genéticos generan productos que son únicos tanto en longitud como en secuencia genética para cada célula. Por lo tanto, los ensayos basados en la reacción en cadena de la polimerasa (PCR) se pueden utilizar para identificar poblaciones de linfocitos que derivan de una única célula mediante la detección del reordenamiento específico de los genes V-J, presente dentro del locus del receptor antigénico 1. El ensayo de PCR IdentiClone emplea múltiples oligonucleótidos iniciadores (cebadores) consenso que hibridan regiones genéticas conservadas dentro del gen codificante para la cadena delta del receptor de la célula T. Este ensayo se utiliza para la detección de una gran mayoría de neoplasias clonales de linfocitos T a partir de ADN. Los productos resultantes de la amplificación se pueden analizar mediante el uso de diferentes métodos de detección entre los que se incluyen la electroforesis en geles y la electroforesis capilar. El análisis de los reordenamientos genéticos también se puede realizar mediante técnicas basadas en Southern Blot (SB). Aunque el análisis mediante SB es muy fiable, está siendo reemplazado cada vez más por las técnicas de PCR debido a la mayor eficiencia y sensibilidad de estas últimas. Más aún, las técnicas de PCR son relativamente fáciles, menos laboriosas y requieren mucha menos cantidad de ADN de alto peso molecular que los ensayos de SB. Por otro lado, a menudo la PCR puede ser realizada en ADN extraído de muestras de tejido fijado y embebido en parafina, mientras que no ocurre lo mismo para SB, ya que con frecuencia el ADN en estas muestras está degradado. Debido a todo lo anterior, existe una gran necesidad de reemplazar el análisis mediante SB por técnicas fiables de PCR. El ensayo IdentiClone de InVivoScribe Technologies representa una nueva propuesta para la determinación diagnóstica de clonalidad basada en la PCR. Estos ensayos estandarizados fueron rigurosamente optimizados analizando muestras controles positivas y negativas empleando múltiples master mixes (mezclas de reacción). El desarrollo del ensayo fue seguido por un extenso proceso de validación que incluía la determinación analítica de más de 400 muestras clínicas clasificadas según la Clasificación Revisada Europea/Americana de Linfomas (REAL). Las determinaciones fueron hechas en más de 30 centros de diagnóstico destacados e independientes diseminados a través de toda Europa en el marco de un estudio de colaboración conocido como la Acción Concertada BIOMED-2. Los resultados del estudio BIOMED-2 se encuentran publicados en Leukemia, una revista especializada líder en el área 2. Los ensayos basados en la detección de fluorescencia ABI no son capaces de detectar de manera fiable poblaciones clonales que representen menos del 1% de la población total de linfocitos. Debe enfatizarse que los resultados de los ensayos moleculares de clonalidad deben interpretarse siempre en un contexto conjunto de datos clínicos, histológicos e inmunofenotípicos. El presente ensayo incluye 2 mezclas de reacción. La mezcla de reacción del Tubo TCRD (TCRD Tube) hibrida en las secuencias conservadas de las regiones variables, de diversidad, y de unión del locus de la cadena delta del receptor de la célula T. La mezcla de reacción Specimen Control Size Ladder (control de muestra con marcador de tamaño) hibrida con varios genes amplificando una serie de productos de aproximadamente 100, 200, 300, 400 y 600 pares de bases para asegurar que la calidad y cantidad de ADN inicial es la adecuada para generar un resultado válido. En todos nuestros
4 Página 4 de 15 ensayos de clonalidad se utiliza un único programa de termociclador y metodologías de detección similares con lo que se mejora la consistencia interna y facilita el entrenamiento en una gama amplia de ensayos diferentes. 4. Principios del Procedimiento 4.1. Reacción en Cadena de la Polimerasa (PCR) Los ensayos de PCR son utilizados de manera rutinaria para la identificación de poblaciones clonales de células T. Estos ensayos amplifican el ADN situado entre los cebadores que hibridan en las secuencias conservadas (FR) de las regiones variables (V), de las regiones de unión (J), y de diversidad (TCRD Tube). Estas regiones conservadas se encuentran a ambos lados dentro de un area de la region V-J donde ocurren los reordenamientos geneticos programados durante la maduración de todos los linfocitos T y B. Los genes de receptores antigénicos que sufren reordenamientos son aquellos genes que codifican las cadenas pesadas y livianas en las células B, y los genes que codifican para el receptor de células T en las células T. Cada célula B o T tiene un único reordenamiento V-J productivo con una longitud y secuencia nucleotídica característicos. Por lo tanto, cuando el ADN de una población normal o policlonal se amplifica utilizando cebadores que flanquean las regiones V-J, los productos generados forman una distribución normal o Gaussiana dentro de un rango de tamaños determinado. En un gel, esta distribución de productos se visualiza como un extendido. Esta distribución Gaussiana refleja la población heterogénea de reordenamientos V-J. (En ciertos casos, cuando el ADN de linfocitos no está presente, no se observa producto alguno). La amplificación del ADN de muestras que contienen una población clonal, genera uno o dos productos de amplificación prominentes (amplicones mayoritarios) dentro de un espectro minoritario de productos de amplificación policlonales de fondo. Figura 1. Representación simple de la organización de un gen reordenado que codifica para la cadena delta del receptor de la célula T en el cromosoma 14 (14q11.2). Las flechas negras indican las posiciones aproximadas de los cebadores. El número y especificidad de los cebadores se encuentran listados para la mezcla de reacción del Tubo TCRD. Debido a que los genes codificantes para el receptor antigénico son polimórficos (consisten en una población heterogénea de secuencias de ADN relacionadas) es difícil emplear un único conjunto de cebadores que hibriden en todas las regiones flanqueantes conservadas del reordenamiento V-J. Adicionalmente, la diversidad de la región N y las mutaciones somáticas, confieren aún más heterogeneidad a las secuencias de ADN de estas regiones. Por lo tanto, y para identificar la mayoría de los reordenamientos clonales posibles, es necesario emplear mezclas de reacción con varios cebadores que hibriden en varias regiones FR. Como se ha mencionado anteriormente, los reordenamientos clonales son identificados como productos prominentes de un tamaño concreto dentro de un fondo de productos minoritarios de tamaños diferentes que conforman una distribución Gaussiana alrededor de un reordenamiento de un tamaño promedio favorecido estadísticamente Detección de Fluorescencia Diferencial La detección diferencial de fluorescencia normalmente se utiliza para resolver los amplicones de diferentes tamaños utilizando un instrumento de electroforesis capilar. Los cebadores pueden ser marcados con diferentes moléculas fluorescentes (fluoróforos) de manera que puedan producir diferentes espectros de emisión tras la excitación por un láser
5 Página 5 de 15 en el instrumento de electroforesis capilar. De esta manera, marcadores fluorescentes diferentes pueden corresponderse con diferentes regiones amplificadas. Este sistema de detección proporciona una sensibilidad insuperada, una resolución capaz de discriminar diferencias de sólo un nucleótido, una detección diferencial de los productos y una cuantificación relativa. Con este sistema además, se evita el uso de geles de agarosa y poliacrilamida, así como de agentes carcinógenos como el bromuro de etidio. Más aún, la detección diferencial permite una interpretación exacta, reproducible y objetiva de los productos de amplificación específicos y el almacenamiento automático de los datos. La reproducibilidad intra- e inter-ensayo en la determinación del tamaño utilizando electroforesis capilar es de aproximadamente 1 a 2 nucleótidos. Esta reproducibilidad y sensibilidad junto con el archivo automático de los datos de las muestras posibilita el monitoreo, el seguimiento y la comparación de los datos de un determinado paciente a lo largo del tiempo. 5. Reactivos 5.1. Componentes Reacciones IdentiClone TCRD Gene Clonality Assay MegaKit ABI Fluorescence Detection 330 Reacciones Tabla 1 Reactivo Mezcla de Reacción (Master Mix) Mezcla Control de Amplificación de la Muestra Control Positivo de ADN Control Negativo (Normal) de ADN Número de Catálogo Componentes del reactivo (ingredientes activos) Cantidad Nro. de unidades Nro. de unidades TCRD Tube 6FAM & HEX Múltiples oligonucleótidos que hibridan en las regiones de entramado Vδ + Dδ + Jδ del gen de la cadena delta del receptor de la célula T. Specimen Control Size Ladder 6FAM Múltiples oligonucleótidos que hibridan en diferentes genes endógenos. IVS-0021 Clonal Control DNA 200 μg/ml de ADN en solución TE 1/ µl 1 5 IVS-0000 Polyclonal Control DNA 200 μg/ml de ADN en solución TE 1/10 Nota: No se ha utilizado conservante alguno en la fabricación de este producto. T de Conservación 1500 µl a -85 C 1500 µl a -85 C 100 µl a 8 C ó -65 a -85 C 2 a 8 C ó -65 a -85 C 5.2. Precauciones y Advertencias 1. Este producto es para Uso en Diagnóstico In Vitro 2. El kit de ensayo será usado como un conjunto. Ningún reactivo debe sustituirse por otro reactivo similar proveniente de otro fabricante. El realizar diluciones, reducir los volúmenes de las mezclas de amplificación o cualquier otra desviación del protocolo original pueden afectar la eficacia de este ensayo y/o anular cualquier sublicencia limitada que se adquiera con la compra de este ensayo. 3. Los materiales son estables hasta la fecha de caducidad que se indica en la etiqueta cuando son manipulados, conservados y almacenados de acuerdo a las instrucciones. No utilizar los productos una vez sobrepasada la fecha de caducidad 4. El cumplimiento riguroso de las instrucciones de uso y el seguimiento del protocolo asegurará un funcionamiento analítico y reproducibilidad óptimos. Debe asegurarse de que el programa del termociclador usado sea el correcto, ya que el uso de otros programas puede dar lugar a datos erróneos o inexactos, como resultados falsos positivos y falsos negativos. 5. No mezclar o combinar los reactivos procedentes de kits con diferentes números de lote. 6. Se recuerda al personal del laboratorio que deben usar todos los equipos de protección personal adecuados y trabajar de acuerdo a las buenas prácticas de laboratorio y a las recomendaciones universales para el trabajo con muestras biológicas. Las muestras deben ser manipuladas en instalaciones homologadas de contención de seguridad biológica y abiertas solamente en cabinas de seguridad biológica certificadas. Se recomienda el uso de agua destilada de grado biología molecular en la preparación del ADN de la muestra. 7. Debido a la sensibilidad analítica de este ensayo, se debe tener un cuidado extremo para prevenir la contaminación de los reactivos o de las mezclas de amplificación con las muestras, controles o materiales amplificados. Todos los reactivos deben ser cuidadosamente examinados para detectar cualquier signo de contaminación (por ej. Controles negativos que generen señales positivas). Se debe descartar inmediatamente cualquier reactivo con sospecha de contaminación.
6 Página 6 de Para minimizar las posibilidades de contaminación, se deben utilizar guantes limpios cuando se manipulen las muestras y los reactivos. Las áreas de trabajo y las pipetas se deben limpiar de forma rutinaria antes de empezar a realizar cualquier reacción de PCR. 9. El proceso de esterilización en autoclave no elimina la contaminación con ADN. El flujo de trabajo en el laboratorio de PCR debe ir siempre en una sola dirección entre las diferentes áreas de trabajo separadas; comenzando en el área de Preparación de las Mezclas de Reacción; siguiendo en el de la Preparación de la Muestra, pasando a continuación al de la Amplificación, y finalmente al de la Detección. No introducir ADN amplificado en las áreas designadas para la preparación de la muestra o de las mezclas de reacción. 10. Todas las pipetas, puntas y cualquier otro equipamiento utilizado en un área particular debe ser utilizado y mantenido dentro de esa área del laboratorio. 11. Con el objetivo de prevenir la contaminación cruzada, y/o con RNasas y DNasas, siempre que sea posible, se debe utilizar material plástico estéril y desechable Almacenamiento y Manipulación Si el producto no es usado de forma inmediata, el kit debe ser almacenado entre -65 C y -85 C. La temperatura de almacenamiento óptima para los controles de ADN es entre 2 C y 8 C, aunque también pueden ser almacenados entre -65 C y -85 C. Todos los reactivos y controles deben ser descongelados y agitados vigorosamente antes de usarse para asegurar que se han resuspendido completamente. La agitación excesiva puede causar roturas en el ADN y la separación de los cebadores de sus fluoróforos conjugados. Los materiales son estables hasta la fecha de caducidad indicada cuando son manipulados y almacenados de acuerdo a las instrucciones. No deben utilizarse pasada su fecha de caducidad. Debido a su alta concentración salina, las mezclas de reacción de PCR son sensibles a los ciclos de congelado/descongelado. En caso necesario, las mezclas de reacción se deben alicuotar en tubos estériles y herméticos, con tapa de rosca y junta de goma. 6. Instrumentos 6.1. Termociclador Uso ó Función: Amplificación de muestras de ADN Especificaciones y Características de Funcionamiento: Rango Térmico Mínimo: de 15 C a 96 C Velocidad Mínima de la Rampa: 0.8 C/seg Seguir los protocolos de instalación, operación, calibración y mantenimiento del fabricante. Ver la sección 8.4 Amplificación para el programa del termociclador ABI 310, ABI 3100, ó ABI 3130 Uso ó Función: Detección de los fragmentos y análisis Especificaciones y Características de Funcionamiento: Los siguientes instrumentos de electroforesis capilar cumplen con los requisitos de funcionamiento para este ensayo: ABI 310 Genetic Analyzer (1-capilar) ABI 3100 Avant Genetic Analyzer (4-capilares) ABI 3100 Genetic Analyzer (16-capilares) ABI 3130 Genetic Analyzer (4-capilares) ABI 3130XL Genetic Analyzer (16-capilares) Seguir los protocolos de instalación, operación, calibración y mantenimiento del fabricante. El instrumento ABI utilizado debe estar calibrado con el grupo de fluoróforos 6FAM, HEX, NED, y ROX. Emplear las condiciones asignadas por defecto para el polímero y tipo de capilar utilizado. Ver la sección 8.5 Detección de Fluorescencia ABI para la preparación de la muestra. 7. Recogida y Preparación de la Muestra 7.1. Precauciones Las muestras biológicas humanas pueden contener materiales potencialmente infecciosos. Todas las muestras deben manipularse de acuerdo con las normas estándar OSHA sobre patógenos de transmisión sanguínea o las normas de bioseguridad de nivel 2.
7 Página 7 de Sustancias que Interfieren Se sabe que las siguientes sustancias interfieren en la reacción de PCR: 1. Quelantes de cationes divalentes 2. Puntas de pipetas de retención baja 3. EDTA (no significativo a bajas concentraciones) 4. Heparina 7.3. Requerimientos de la Muestra y su manipulación Este ensayo analiza ADN genómico proveniente de las siguientes fuentes: 1. 5 ml de sangre periférica, biopsia de médula ósea, o aspirado de médula ósea anticoagulado con heparina o EDTA (conservado entre 2 C y 8 C y transportado a temperatura ambiente) 2. Un mínimo de 5mm cuadrados (5mm 3 ) de tejido (conservado y transportado congelado; o conservado y transportado en RPMI 1640 a temperatura ambiente o en hielo) 3. 2μg de ADN genómico (conservado entre 2 C y 8 C y transportado a temperatura ambiente) 4. Muestras o cortes de tejido fijados en formol y embebidos en parafina (conservados y transportados a temperatura ambiente) 7.4. Preparación de la Muestra Extraer el ADN genómico de las muestras de los pacientes tan pronto como sea posible. Resuspender el ADN a una concentración final de 100 μg a 400 μg por ml en TE 1/10 (1 mm Tris-HCl, ph 8.0; 0.1 mm EDTA) o en agua grado biología molecular o grado USP. Este ensayo es un sistema robusto. Un amplio rango de concentraciones de ADN será capaz de generar un resultado válido. Por lo tanto, generalmente no son necesarios la cuantificación y el ajuste de las concentraciones de ADN. El análisis de la muestra problema de ADN con el Specimen Control Size Ladder asegurará que existe ADN en cantidad y calidad suficientes para generar un resultado válido Conservación de la Muestra El ADN genómico debe conservarse entre 2 C y 8 C o entre -65 C y -85 C hasta el momento de su uso. 8. Procedimiento del Ensayo 8.1. Materiales Suministrados en el Kit Tabla 2 Número de Catálogo Descripción TCRD Tube 6FAM & HEX Specimen Control Size Ladder 6FAM IVS-0021 Clonal Control DNA IVS-0000 Polyclonal Control DNA 8.2. Materiales Requeridos pero No Suministrados en el Kit Tabla 3 Reactivo/Material Reactivos/Materiales y Proveedores Recomendados Notas ADN Polimerasa Agua Bi-Destilada Grado Biología Molecular o Agua Grado USP Pipetas Calibradas Termociclador Applied Biosystems: AmpliTaq Gold DNA Polymerase (Cat# N ) Rainin: Pipetas P-2, P-20, P-200, y P-1000 O pipetas SL-2, SL-20, SL-200, y SL-1000 Bio-Rad: MJ Research PTC-100 o PTC-200, PTC-220, PTC-240 Perkin-Elmer PE 9600 o PE 9700 El agua debe ser estéril y libre de DNasas y RNasas. Deben ser capaces de medir volúmenes exactos entre 1μl y 1000μl. Mezcladores Vortex Placas o tubos para PCR Estériles
8 Página 8 de 15 Reactivo/Material Reactivos/Materiales y Proveedores Recomendados Notas Puntas de pipetas con Estériles, libres de filtro Pirógenos/RNasas/DNasas Tubos para microcentrífuga Estériles Instrumento de Applied Biosystems: Electroforesis Capilar Series ABI 310, 3100, o 3130 ABI Formamida Hi-Di InVivoScribe Technologies: HI-Deionized Formamide (Cat# ) Applied Biosystems: Hi-Di Formamide (Cat# ) Estándares de tamaño ROX Set D de Calibración Espectral de Colorantes Polímero Solución tampón InVivoScribe Technologies: Hi-Di Formamide w/rox size standards for ABI 310 (Cat# ) Hi-Di Formamide w/rox size standards for ABI 3100 (Cat# ) Applied Biosystems: GeneScan - 400HD [ROX] (Cat# ) Applied Biosystems: Para instrumentos ABI 3100 y 3130: DS-30 Matrix Standard Kit (Dye Set D) (Cat# ) Para instrumentos ABI 310: NED Matrix Standard (Cat# ) Y Fluorescent Amidite Matrix Standards [6FAM, TET, HEX, TAMRA, ROX] (Cat# ) Applied Biosystems: Polímero POP-4: POP-4 for 310 Genetic Analyzers (Cat# ) POP-4 for 3100/3100-Avant Genetic Analyzers (Cat# ) POP-4 for 3130/3130XL Genetic Analyzers (Cat# ) Polímero POP-7: POP-7 for 3130/3130XL Genetic Analyzers (Cat# ) Applied Biosystems: 10X Genetic Analyzer Buffer with EDTA (Cat# ) Set de colorantes usados para realizar la calibración espectral del instrumento ABI para usarlo con 6FAM, HEX, NED, y ROX Diluir 1:10 con agua estéril antes de usar 8.3. Preparación de los Reactivos Todas las muestras desconocidas deben ser analizadas usando la mezcla de reacción del Specimen Control Size Ladder. Esto se hace para asegurar que no están presentes inhibidores de la amplificación y que hay ADN en cantidad y calidad suficientes para generar un resultado válido. Los resultados generados con un análisis único son válidos; no obstante, se recomienda realizar el análisis de cada muestra por duplicado siempre que sea posible. Si el análisis por duplicado genera resultados inconsistentes, es necesario volver a ensayar o analizar la muestra. Los controles positivo, negativo y blanco deben ser analizados para cada una de las mezclas de reacción. 1. Usando guantes, sacar las mezclas de reacción de reacción del congelador. Dejar que los tubos se descongelen completamente y entonces mezclar suavemente. 2. En una cabina de contención tomar una alícuota suficiente de cada mezcla de reacción y transferirla a tubos de microcentrífuga individuales, limpios y estériles. Los volúmenes de las alícuotas deben ser de 45μl para cada reacción. Se recomienda añadir una reacción extra por cada 15 reacciones, para compensar los errores de pipeteo. De esta manera, para cada mezcla de reacción (excepto para el Specimen Control Size Ladder), el número de reacciones (n) debe ser: n = 2 # de muestras (correr cada muestra por duplicado) + 1 control positivo de ADN (Ver sección 8.7 Controles Positivos Recomendados) + 1 control negativo de ADN (IVS-0000 Polyclonal Control DNA) + 1 control sin templado o blanco (agua) + 1 para compensar los errores de pipeteo n = 2 # de muestras + 4 Total Por lo tanto el volumen total de alícuota para cada mezcla de reacción debería ser n 45μl.
9 Para la mezcla de reacción del Specimen Control Size Ladder, el número de reacciones (m) debería ser: m = # de muestras (correr cada muestra por duplicado) + 1 control negativo de ADN (IVS-0000 Polyclonal Control DNA) + 1 control sin templado o blanco (agua) + 1 para compensar los errores de pipeteo m = # de muestras + 3 Total Página 9 de 15 Por lo tanto el volumen total de alícuota para la mezcla de reacción del Specimen Control Size Ladder debería ser m 45μl. 3. Añadir 1.25 unidades (o 0.25μl a 5 unidades/μl) de ADN polimerasa AmpliTaq Gold por reacción a cada mezcla de reacción. El total de polimerasa AmpliTaq Gold que es necesaria añadir a cada mezcla maestra de reacción deberá ser n 0.25μl, y m 0.25μl para la mezcla de reacción del Specimen Control Size Ladder. Mezclar suavemente con vortex. 4. Para cada reacción, alicuotar 45μl de la respectiva mezcla de reacción + ADN polimerasa en cada pocillo de una placa de PCR o tubo. 5. Añadir 5μl de la muestra correspondiente (muestra problema de ADN, control positivo de ADN, control negativo de ADN, o agua) en cada pocillo que contenga las respectivas mezclas de reacción. Mezclar suavemente con la pipeta varias veces. 6. Tapar los tubos o cubrir la placa de PCR. 7. Las muestras están ahora listas para ser amplificadas en un termociclador. Si la amplificación no puede realizarse inmediatamente después de la preparación de los reactivos, la placa de PCR o los tubos pueden ser conservados entre 2 C y 8 C por un período de hasta 24 horas. Guía Rápida: Para cada mezcla de reacción de reacción y n reacciones, mezclar: n 45μl Mezcla de Reacción n 0.25μl ADN polimerasa AmpliTaq Gold Vorterear suavemente para mezclar. Alicuotar 45μl de mezcla de reacción + solución de ADN polimerasa en cada reservorio de reacción. Agregar 5μl del respectivo Templado a cada reservorio. Volumen total de reacción = 50μl 8.4. Amplificación 1. Amplificar las muestras usando el siguiente programa de PCR: (Nota: Se recomienda usar la opción calculada para la medición de la temperatura con los termocicladores PTC BioRad MJ Research.) Programa Estándar para AmpliTaq Gold Paso 1: 95 C por 7 minutos Paso 2: 95 C por 45 segundos Paso 3: 60 C por 45 segundos Paso 4: 72 C por 90 segundos Paso 5: Ir a paso 2; repetir 34 veces Paso 6: 72 C por 10 minutos Paso 7: 15 C por tiempo indefinido 2. Retirar los tubos o la placa de amplificación del termociclador. Aunque el ADN amplificado es estable a temperatura ambiente durante largos períodos de tiempo, los productos de PCR deben almacenarse entre 2 C y 8 C hasta la detección. La detección debe realizarse dentro de los 30 días posteriores a la amplificación.
10 Página 10 de Detección de Fluorescencia ABI Por favor, tenga en cuenta, que en la detección de fluorescencia ABI es normal ver un pico de fluorescencia precedente que es un artefacto debido a la saturación de la señal en el método de detección que usa la plataforma ABI. Los picos precedentes suelen presentarse con una pendiente que se orienta hacia el lado derecho a menudo conectando con el pico real. Esto se hace realmente evidente en la mezcla de reacción del Specimen Control Size Ladder donde el pico de 96 nucleótidos tiene un pico precedente que aparece a los 84 nucleótidos. No se recomienda analizar mezclas de productos de PCR de diferentes mezclas de reacción, ya que esto resultará en una reducción global de la sensibilidad del ensayo. 1. En un tubo de microcentrífuga nuevo, mezclar una cantidad apropiada (para un total de 10μl por reacción de PCR) de Formamida Hi-Di con estándares de tamaño ROX a. Mezclar bien con vortex. 2. En una nueva placa de PCR de 96 pocillos, pipetear 10μl de Formamida Hi-Di con estándares de tamaño ROX en cada pocillo para cada reacción de PCR. 3. Añadir 1μl de cada reacción de PCR a los pocillos que contienen Formamida Hi-Di con estándares de tamaño ROX. Añadir sólo una muestra por pocillo. Mezclar con la pipeta. 4. Tapar los tubos o cubrir la placa de PCR. 5. Desnaturalizar las muestras con calor a 95ºC durante 2 minutos, seguido de un enfriamiento en hielo durante 5 minutos. 6. Preparar una hoja de muestras y la lista de inyección para las muestras a analizar. 7. Correr las muestras en el instrumento de electroforesis capilar siguiendo el manual del usuario b. 8. Los resultados son automáticamente mostrados como picos de tamaño y color específicos. Revisar el trazado y los controles y luego informar el resultado. (Ver debajo las secciones 9 Interpretación de los Resultados y 11 Valores Esperados). Nota a : Consulte las recomendaciones del inserto del producto de Applied Biosystems para mezclar la Formamida Hi-Di con los Estándares de Tamaño ROX para los diferentes instrumentos ABI. De manera alternativa, se pueden adquirir directamente las alícuotas ya mezcladas en InVivoScribe Technologies. Nota b : A medida que las muestras son corridas en el aparato, son fraccionadas, detectadas y analizadas por el instrumento. Cada electroforesis tiene una duración de minutos. Rutinariamente, los instrumentos de electroforesis capilar ABI son capaces de realizar 2 electroforesis por hora (para los instrumentos de 1, 4, y 16 capilares esta capacidad es igual a 48, 192, y 786 muestras por día, respectivamente), y de analizar y almacenar automáticamente los datos para su revisión o comparación con los de otros ensayos Control de Calidad En el kit se suministran controles positivos y negativos (o normales) y deben ser analizados cada vez que se desarrolla el ensayo para asegurar el desarrollo apropiado del mismo. Adicionalmente, se debe incluir un control sin ADN (por ej. agua) para controlar la posible contaminación de la mezcla de reacción o la contaminación cruzada de las reacciones de PCR debidas al empleo de técnicas asépticas inadecuadas. También se debe incluir un control de la solución tampón para asegurar que el tampón utilizado para resuspender las muestras no ha sido contaminado. Los valores de los controles positivos se encuentran en la sección 11.1 Tamaño Esperado de los Productos Amplificados. Controles adicionales y controles de sensibilidad (diluciones de los controles positivos en el control negativo) se encuentran disponibles en InVivoScribe Technologies Controles Positivos Recomendados Los tamaños de los productos amplificados mostrados en la tabla se obtuvieron usando una plataforma ABI Los tamaños de los productos amplificados obtenidos en su instrumento de electroforesis capilar específico pueden diferir en 1 a 4 nucleótidos (nt) de los que se encuentran en la tabla, dependiendo de la plataforma de detección y de la versión del programa de análisis utilizados. Una vez identificado, el tamaño del amplicón determinado en su plataforma específica será consistente entre diferentes electroforesis. Esta reproducibilidad es extremadamente útil cuando se hace un seguimiento de enfermedad recurrente. Nota: Color indica el color de los productos generados con la mezcla de reacción cuando se usan las asignaciones de color por defecto de los sistemas de detección de fluorescencia ABI. Tabla 4 Mezcla de Reacción Secuencia Blanco Color ADN Control Número de Catálogo TCRD Tube Vδ + Dδ + Jδ Azul + Verde Rango de Tamaños Válido --- Specimen Control Size Ladder Genes Múltiples Azul IVS-0021 Clonal Control DNA Rango de Tamaños Válido IVS-0000 Polyclonal Control DNA Tamaño del Producto en Nucleótidos a 158 (menor), , 200, 300, 400, 600 b 100, 200, 300, 400, 600 b
11 Página 11 de 15 Nota a : Un pico prominente de 90nt es visto en numerosas muestras normales. Nota b : Debido a que los fragmentos de PCR de menor tamaño son preferencialmente amplificados, es normal que el fragmento de 600nt presente una señal disminuida o que se pierda completamente. Durante los tiempos normales de electroforesis en los equipos ABI, el pico de 600nt puede no llegar a aparecer. Más aún, el tamaño de este pico puede diferir en 30nt cuando el tamaño del fragmento es calculado utilizando el estándar de tamaño GeneScan - 400HD [ROX]. 9. Interpretación de los Resultados Aunque un resultado positivo es altamente sugestivo de un proceso neoplásico, tanto los resultados positivos como los negativos deben interpretarse en un contexto global con toda la información clínica y los resultados de los ensayos del laboratorio. El rango de tamaños para cada una de las mezclas de reacción ha sido determinado analizando muestras control positivas y negativas. Para una interpretación exacta y significativa es importante tener en cuenta que se deben ignorar las bandas que aparezcan fuera del rango de tamaños válido para cada una de las mezclas de reacción Análisis 1. Muestras que no amplifican después de ser ensayadas repetidamente deber ser informadas como No se puede informar un resultado de esta muestra debido a que no se obtiene ADN en cantidad o calidad suficiente para su análisis. 2. Muestras que generan un resultado negativo deben ser repetidas si el control positivo de la reacción no amplificó. 3. Si las muestras analizadas por duplicado generan resultados diferentes, el ensayo debe ser repetido o vuelto a evaluar para aclarar un posible cambio de muestras. 4. Todos los controles del ensayo deben ser examinados previamente a la interpretación de los resultados de la muestra problema. Si los controles no generan los resultados correctos, el ensayo no es válido y las muestras no deben ser interpretadas. La siguiente tabla describe el análisis de cada uno de los controles y las acciones a seguir basándose en los resultados obtenidos. Tabla 5 Tipo de Control Resultado Esperado Resultado Aberrante Control Sin Templado No presenta amplificación, continuar con el análisis. Amplificación presente, repetir el ensayo. Control Policlonal Control Positivo (Este también puede ser un control de extracción si se añade un material control positivo a través de los procesos de extracción) Specimen Control Size Ladder (Este control de amplificación es esencial para muestras de calidad y cantidad desconocida.) El tamaño del producto es consistente con el tamaño esperado de acuerdo a la lista de la sección 11.1 Tamaño Esperado de los Productos Amplificados. No hay reordenamientos clonales presentes. Continuar con el análisis. El tamaño del producto es consistente con el tamaño esperado de acuerdo a la lista de la sección 11.1 Tamaño Esperado de los Productos Amplificados. Continuar con el análisis. Si todos los picos de 100, 200, 300, 400, y 600pb están presentes, continuar con el análisis. Debido a que los fragmentos de PCR de menor tamaño son preferencialmente amplificados, es normal que el fragmento de 600pb presente una señal disminuida o que se la pierda completamente. Continuar con el análisis. Presenta reordenamientos clonales, repetir el ensayo. Repetir el ensayo. Si no se observan picos, repetir el ensayo a menos que la muestra resulte positiva. Si sólo se observan 1, 2, o 3 picos, re-evaluar la muestra para determinar una posible degradación del ADN a menos que la muestra resulte positiva.
12 Página 12 de Interpretación de la Muestra Problema Cuando los controles generan los resultados esperados, las muestras clínicas deben ser interpretadas como se detalla a continuación: Uno o dos picos positivos prominentes a dentro del rango de tamaños válido se informa como: Positivo para la detección de un reordenamiento(s) clonal(es) del gen de la cadena delta del receptor de la célula T, consistente con la presencia de una población celular clonal. En un contexto global de criterios diagnósticos, las poblaciones celulares clonales pueden indicar la presencia de una neoplasia hematológica. La ausencia de picos positivos a dentro del rango de tamaños válido se informa como: Negativo para la detección de reordenamientos clonales del gen de la cadena delta del receptor de la célula T. Nota a : Los criterios para definir un pico positivo son los siguientes: Los productos generados de muestras al diagnóstico que caen dentro del rango de tamaños válido y tienen una amplitud de al menos tres veces la amplitud del tercer pico más grande del fondo policlonal, son consistentes con un pico positivo. Los productos generados de muestras recolectadas después del diagnóstico inicial que caen dentro del rango de tamaños válido y son: bien 1) de una amplitud de al menos tres veces la amplitud del tercer pico mas grande; o bien, 2) exceden la amplitud de los picos vecinos adyacentes y son idénticos en tamaño a los productos clonales amplificados previamente en muestras del mismo paciente usando la misma mezcla de reacción, son consistentes con un pico positivo. 10. Limitaciones del Ensayo Este ensayo no identifica el 100% de las poblaciones celulares clonales. Este ensayo no puede detectar de manera fiable una cantidad menor de 1 célula positiva por cada 100 células normales. Los resultados de las pruebas moleculares de clonalidad siempre deben ser interpretados en el contexto global de datos clínicos, histológicos e inmunofenotípicos. Los ensayos basados en la técnica de PCR están sujetos a interferencia por la degradación del ADN o por la inhibición de la PCR debida a EDTA, heparina y otros agentes. 11. Valores Esperados Tamaño Esperado de los Productos Amplificados Los tamaños de los productos amplificados mostrados en la tabla se obtuvieron usando una plataforma ABI Los tamaños de los productos amplificados obtenidos en su instrumento de electroforesis capilar específico pueden diferir en 1 a 4 nucleótidos (nt) de los que se encuentran en la tabla, dependiendo de la plataforma de detección y de la versión del programa de análisis utilizados. Una vez identificado, el tamaño del amplicón determinado en su plataforma específica será consistente entre diferentes electroforesis. Esta reproducibilidad es extremadamente útil cuando se hace un seguimiento de enfermedad recurrente. Nota: Color indica el color de los productos generados con la mezcla de reacción cuando se usan las asignaciones de color por defecto de los sistemas de detección de fluorescencia ABI. Tabla 6 Mezcla de Reacción Secuencia Blanco TCRD Tube Vδ + Dδ + Jδ Azul + Verde Rango de Tamaños Válido IVS-0000 Polyclonal Control DNA IVS-0021 Clonal Control DNA Specimen Control Genes Azul Rango de Tamaños Válido Size Ladder Múltiples IVS-0000 Polyclonal Control DNA Color ADN Control Número de Catálogo Tamaño del Producto en Nucleótidos a , (menor), , 200, 300, 400, 600 b 100, 200, 300, 400, 600 b Nota a : Un pico prominente de 90nt es visto en numerosas muestras normales. Nota b : Debido a que los fragmentos de PCR de menor tamaño son preferencialmente amplificados, es normal que el fragmento de 600nt presente una señal disminuida o que se pierda completamente. Durante los tiempos normales de electroforesis en los equipos ABI, el pico de 600nt puede no llegar a aparecer. Más aún, el tamaño de este pico puede diferir en 30nt cuando el tamaño del fragmento es calculado utilizando el estándar de tamaño GeneScan - 400HD [ROX].
13 Página 13 de Resultados de la Muestra Los resultados que se muestran a continuación fueron generados utilizando las mezclas de reacción indicadas. Los productos amplificados fueron resueltos en un instrumento ABI Para cada mezcla de reacción: El carril 1 muestra los datos generados al ensayar un control alternativo de ADN 100% clonal. El carril 2 muestra los datos generados al ensayar el control recomendado de ADN 100% clonal. El carril 3 muestra los datos generados al ensayar una dilución al 10% del control recomendado de ADN clonal. El carril 4 muestra los datos generados al ensayar el control de ADN policlonal, IVS-0000 Polyclonal Control DNA. Figura 2 Para la mezcla de reacción del Specimen Control Size Ladder: El panel 1 muestra los datos generados al ensayar un control negativo (agua). El panel 2 muestra los datos generados al ensayar el control positivo recomendado, IVS-0000 Polyclonal Control DNA. Los paneles 3 y 4 muestran los datos generados al ensayar dos controles diferentes de ADNs control 100% clonal. Figura 3
14 Página 14 de Características Analíticas El ensayo de Clonalidad del Gen TCRD, IdentiClone TCRD Gene Clonality Assay, es un procedimiento rápido y fiable, que es mucho más sensible que el análisis mediante Southern Blot (SB) para la detección de clonalidad en casos de sospecha de enfermedades linfoproliferativas. El diagnóstico final clínico-histopatológico se correlaciona muy bien con los resultados de PCR en un gran número de pacientes en comparación con los resultados de SB. Esto fue evidenciado por un trabajo relevante publicado en 2003 en la revista Leukemia por van Dongen et al. Tabla 7 Concordancia PCR/SB (Leukemia 2 ): IGH: 93% sensibilidad / 92% especificidad IGK: 90% sensibilidad / 90% especificidad IGL: 86% sensibilidad / 92% especificidad TCRB: 86% sensibilidad / 98% especificidad TCRG: 89% sensibilidad / 94% especificidad TCRD: 83% sensibilidad / 95% especificidad La exactitud diagnóstica de los ensayos IdentiClone fue determinada como de al menos un 89%. Usando los ensayos IdentiClone, no se detectaron resultados falsos positivos claros y se observó un alto nivel de precisión. Además, un claro beneficio de este ensayo fue que los resultados clonales generados por el mismo permitieron una detección subsecuente de reordenamientos genéticos específicos de paciente y de tumor para la detección de enfermedad mínima residual. 13. Bibliografía 1. Miller, JE, Wilson, SS, Jaye, DJ, Kronenberg, M. An automated semiquantitative B and T cell clonality assay. Mol. Diag. 1999, 4(2): Van Dongen, JJM et al. Design and standardization of PCR primers and protocols for detection of clonal immunoglobulin and T-cell receptor gene recombinations in suspect lymphoproliferations: Report of the BIOMED-2 Concerted Action BMH4-CT Leukemia 2003, 17(12): Servicio Técnico y al Cliente Fabricante Representante Autorizado y Asistencia Técnica en la UE InVivoScribe Technologies, Inc. InVivoScribe Technologies, SARL 6330 Nancy Ridge Drive, Suite 106 Le Forum Bât B San Diego, California Avenue de la Tramontane USA ZI Athelia IV La Ciotat, France Teléfono: Teléfono: +33 (0) Fax: Fax: +33 (0) Servicio Técnico: support@invivoscribe.com Servicio Técnico: support@invivoscribe.com Servicio al cliente: sales@invivoscribe.com Servicio al Cliente: sales-eu@invivoscribe.com Sitio Web: Sitio Web: Horario de atención: 7:00AM 5:00PM PST/PDT Horario de atención: 9:00AM 5:00PM CET/CEST Los representantes técnicos y de stención al cliente están disponibles de lunes a viernes para responder a todas sus preguntas, mediante consultas telefónicas, por correo electrónico o en la web.
15 Página 15 de Aspectos Legales Este es un producto de diagnóstico in vitro. La metodología empleada está protegida por las patentes número 5,296,351 y 5,418,134 de los Estados Unidos de América; por la patente número 626,601 de Australia y por la patente número 2,781,438 de Japón, todas las cuales están bajo licencia exclusiva de InVivoScribe Technologies ( IVS ). Esta metodología también requiere métodos de amplificación de ácidos nucleicos como la Reacción en Cadena de la Polimerasa (PCR). En determinados países, esta tecnología está o puede estar cubierta por derechos bajo patente de Hoffmann-LaRoche, Inc. y de F. Hoffmann-LaRoche Ltd. Ninguna licencia para el uso de la metodología de PCR cubierta por alguna de estas últimas patentes es otorgada al comprador, expresamente o por implicación, por la simple compra de estos productos. Como lo es para cualquier uso dentro de los Estados Unidos de América, Australia y Japón (incluyendo el envío de resultados a estos países): La adquisición de este producto incluye una sublicencia limitada para la práctica no comercial y sin fines de lucro de esta tecnología si, y solo si, el comprador está registrado en IVS exclusivamente como un usuario de productos IVS sin fines de lucro. Ninguna licencia para tal uso es otorgada por la simple compra de estos productos. Para solicitar un formulario de registro de usuario exclusivo de productos sin fines de lucro, para discutir los términos de una potencial sublicencia para realizar una práctica más amplia de estos métodos, o por otras inquietudes, por favor contacte con IVS mediante correo electrónico a: legal@invivoscribe.com, o por teléfono al número IdentiClone es una marca registrada de InVivoScribe Technologies. P/N Revisión B 2009/05
Para Diagnóstico In Vitro. Número de Catálogo. Volumen de Reactivo. Número de Lote. Condiciones de Almacenamiento. Fecha de Vencimiento
 Servicio Técnico: support@invivoscribe.com Servicio al Cliente (EUA): sales@invivoscribe.com Servicio al Cliente (UE): sales-eu@invivoscribe.com IdentiClone TCRG Gene Clonality Assay Para la Identificación
Servicio Técnico: support@invivoscribe.com Servicio al Cliente (EUA): sales@invivoscribe.com Servicio al Cliente (UE): sales-eu@invivoscribe.com IdentiClone TCRG Gene Clonality Assay Para la Identificación
IdentiClone BCL2/JH Translocation Assay Para la Identificación de Linfoma Folicular y de otros Linfomas y Leucemias Para Diagnóstico In Vitro
 Servicio Técnico: support@invivoscribe.com Servicio al Cliente (EUA): sales@invivoscribe.com Servicio al Cliente (UE): sales-eu@invivoscribe.com IdentiClone BCL2/JH Translocation Assay Para la Identificación
Servicio Técnico: support@invivoscribe.com Servicio al Cliente (EUA): sales@invivoscribe.com Servicio al Cliente (UE): sales-eu@invivoscribe.com IdentiClone BCL2/JH Translocation Assay Para la Identificación
Para Diagnóstico In Vitro. Número de Catálogo. Volumen de Reactivo. Número de Lote. Condiciones de Almacenamiento. Fecha de Vencimiento
 Servicio Técnico: support@invivoscribe.com Servicio al Cliente (EUA): sales@invivoscribe.com Servicio al Cliente (UE): sales-eu@invivoscribe.com IdentiClone IGH Gene Clonality Assay Para la Identificación
Servicio Técnico: support@invivoscribe.com Servicio al Cliente (EUA): sales@invivoscribe.com Servicio al Cliente (UE): sales-eu@invivoscribe.com IdentiClone IGH Gene Clonality Assay Para la Identificación
Para Diagnóstico In Vitro. Número de Catálogo. Volumen de Reactivo. Número de Lote. Condiciones de Almacenamiento. Fecha de Vencimiento
 Servicio Técnico: support@invivoscribe.com Servicio al Cliente (EUA): sales@invivoscribe.com Servicio al Cliente (UE): sales-eu@invivoscribe.com IdentiClone TCRG Gene Clonality Assay Para la Identificación
Servicio Técnico: support@invivoscribe.com Servicio al Cliente (EUA): sales@invivoscribe.com Servicio al Cliente (UE): sales-eu@invivoscribe.com IdentiClone TCRG Gene Clonality Assay Para la Identificación
IdentiClone BCL2/JH Gene Clonality Assay
 Instrucciones para su Uso IdentiClone BCL2/JH Gene Clonality Assay Para la Identificación de Linfoma Folicular y de otros Linfomas y Leucemias Para Diagnóstico In Vitro Fabricante: Invivoscribe Technologies,
Instrucciones para su Uso IdentiClone BCL2/JH Gene Clonality Assay Para la Identificación de Linfoma Folicular y de otros Linfomas y Leucemias Para Diagnóstico In Vitro Fabricante: Invivoscribe Technologies,
IdentiClone TCRB Gene Clonality Assay
 Instrucciones para su Uso IdentiClone TCRB Gene Clonality Assay Para la Identificación de Reordenamientos Clonales de Genes Codificantes para la Cadena Beta del Receptor de la Célula T Para Diagnóstico
Instrucciones para su Uso IdentiClone TCRB Gene Clonality Assay Para la Identificación de Reordenamientos Clonales de Genes Codificantes para la Cadena Beta del Receptor de la Célula T Para Diagnóstico
Código: KIT-001 Ver: 1. Pre-FRAXA. Sistema para la detección del número de repetidos CGG en el gene FMR1 PM F M M F M M M C. Reg.
 Pre-FRAXA Sistema para la detección del número de repetidos CGG en el gene FMR1 PM F M M F M M M C Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336 71 60. www.atgen.com.uy
Pre-FRAXA Sistema para la detección del número de repetidos CGG en el gene FMR1 PM F M M F M M M C Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336 71 60. www.atgen.com.uy
AMPLIFICACIÓN Y DETECCIÓN POR PCR DEL LOCUS HUMANO D1S80
 AMPLIFICACIÓN Y DETECCIÓN POR PCR DEL LOCUS HUMANO D1S80 Ref. PCR1 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir a los estudiantes en los principios y práctica de la Reacción
AMPLIFICACIÓN Y DETECCIÓN POR PCR DEL LOCUS HUMANO D1S80 Ref. PCR1 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir a los estudiantes en los principios y práctica de la Reacción
PCR gen 16S ARNr bacteriano
 PCR gen 16S ARNr bacteriano Ref. PCR16S 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir a los estudiantes en los principios y la práctica de la Reacción en Cadena de la Polimerasa
PCR gen 16S ARNr bacteriano Ref. PCR16S 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir a los estudiantes en los principios y la práctica de la Reacción en Cadena de la Polimerasa
TaqMan Roundup Ready Quantification Kit. Part No:
 TaqMan Roundup Ready Quantification Kit Part No: 4466335 1. Introducción Los organismos modificados genéticamente (OMG) se encuentran ampliamente distribuidos, siendo la soja y el maíz los vegetales que
TaqMan Roundup Ready Quantification Kit Part No: 4466335 1. Introducción Los organismos modificados genéticamente (OMG) se encuentran ampliamente distribuidos, siendo la soja y el maíz los vegetales que
EXTRACCIÓN DE ADN (Doyle & Doyle, 1987)
 EXTRACCIÓN DE ADN (Doyle & Doyle, 1987) MATERIALES Y REACTIVOS (Grado biología molecular a analítico) Cloroformo Alcohol Isoamilico Isopropanol. Etanol al 70%. Bloques de Hielo Microcentrifuga Bloque de
EXTRACCIÓN DE ADN (Doyle & Doyle, 1987) MATERIALES Y REACTIVOS (Grado biología molecular a analítico) Cloroformo Alcohol Isoamilico Isopropanol. Etanol al 70%. Bloques de Hielo Microcentrifuga Bloque de
ESTUDIO DE POLIMORFISMOS ALU HUMANOS POR PCR
 ESTUDIO DE POLIMORFISMOS ALU HUMANOS POR PCR Ref. PCRALU 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir a los estudiantes en los principios y práctica de la Reacción en Cadena
ESTUDIO DE POLIMORFISMOS ALU HUMANOS POR PCR Ref. PCRALU 1. OBJETIVO DEL EXPERIMENTO El objetivo de este experimento es introducir a los estudiantes en los principios y práctica de la Reacción en Cadena
Código: IDK-003 Ver: 1. Factor V Leiden
 Sistema para detección de la alteración G1691A en el gene que codifica para el Factor V de la coagulación humana Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336 71
Sistema para detección de la alteración G1691A en el gene que codifica para el Factor V de la coagulación humana Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336 71
SSI DERMATOPHYTE PCR KIT PRUEBA PCR DERMATOFITO
 SSI DERMATOPHYTE PCR KIT PRUEBA PCR DERMATOFITO 2 Prueba de PCR para la detección de dermatofitos y Trichophyton rubrum Para uso diagnóstico in vitro Aplicación La prueba de PCR para dermatofitos en uñas
SSI DERMATOPHYTE PCR KIT PRUEBA PCR DERMATOFITO 2 Prueba de PCR para la detección de dermatofitos y Trichophyton rubrum Para uso diagnóstico in vitro Aplicación La prueba de PCR para dermatofitos en uñas
Código: IDK-006 Ver: 1 MTHFR A1298C. Sistema para detección de la alteración A1298C en el gene de la Mutilen Tetrahidrofolato Reductasa
 Sistema para detección de la alteración A1298C en el gene de la Mutilen Tetrahidrofolato Reductasa Reg. MSP 21199 Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336
Sistema para detección de la alteración A1298C en el gene de la Mutilen Tetrahidrofolato Reductasa Reg. MSP 21199 Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336
Código: KIT-005 Ver: 1 MTHFR C677T
 Sistema para detección de la alteración C677T en el gene que codifica para la Metilen-tetrahidrofolato reductasa humana 1 Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598)
Sistema para detección de la alteración C677T en el gene que codifica para la Metilen-tetrahidrofolato reductasa humana 1 Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598)
Para Diagnóstico In Vitro. Número de Catálogo. Volumen de Reactivo. Número de Lote. Condiciones de Almacenamiento. Fecha de Vencimiento
 Servicio Técnico: support@invivoscribe.com Servicio al Cliente (EUA): sales@invivoscribe.com Servicio al Cliente (UE): sales-eu@invivoscribe.com IdentiClone TCRD Gene Clonality Assay Para la Identificación
Servicio Técnico: support@invivoscribe.com Servicio al Cliente (EUA): sales@invivoscribe.com Servicio al Cliente (UE): sales-eu@invivoscribe.com IdentiClone TCRD Gene Clonality Assay Para la Identificación
RESULTADOS Y DISCUSIÓN
 RESULTADOS Y DISCUSIÓN Extracción de ADN en sangre periférica La técnica de extracción por GeneClean empleada en este trabajo dio un buen rendimiento, ya que la cantidad de ADN y el nivel de purificación
RESULTADOS Y DISCUSIÓN Extracción de ADN en sangre periférica La técnica de extracción por GeneClean empleada en este trabajo dio un buen rendimiento, ya que la cantidad de ADN y el nivel de purificación
ESTUDIO DE REORDENAMIENTOS CLONALES EN LOS GENES DEL RECEPTOR DE CÉLULA T (TCR) MEDIANTE PCR
 Butlletí Nº Mes ESTUDIO DE REORDENAMIENTOS CLONALES EN LOS GENES DEL RECEPTOR DE CÉLULA T (TCR) MEDIANTE PCR El receptor de célula T El receptor de célula T (TCR), es un receptor de membrana, presente
Butlletí Nº Mes ESTUDIO DE REORDENAMIENTOS CLONALES EN LOS GENES DEL RECEPTOR DE CÉLULA T (TCR) MEDIANTE PCR El receptor de célula T El receptor de célula T (TCR), es un receptor de membrana, presente
Laboratorio de Ecología de Enfermedades Facultad de Ciencias Veterinarias Universidad Nacional del Litoral Santa Fe, Argentina. PCR en Tiempo Real
 Laboratorio de Ecología de Enfermedades Facultad de Ciencias Veterinarias Universidad Nacional del Litoral Santa Fe, Argentina PCR en Tiempo Real Dr. Lucas Monje Consejo Nacional de Investigaciones Científicas
Laboratorio de Ecología de Enfermedades Facultad de Ciencias Veterinarias Universidad Nacional del Litoral Santa Fe, Argentina PCR en Tiempo Real Dr. Lucas Monje Consejo Nacional de Investigaciones Científicas
CYP 2C9 A1075C CYP2C9*3
 CYP 2C9 A1075C Sistema para la detección de la mutación A1075C en el gene del citocromo P450 2C9. Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336 71 60. Info@atgen.com.uy
CYP 2C9 A1075C Sistema para la detección de la mutación A1075C en el gene del citocromo P450 2C9. Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2 336 71 60. Info@atgen.com.uy
- Las mezclas de amplificación se presentan en formato monotest en tubos de PCR de 0.2 ó 0.5 ml, identificadas con diferentes colores.
 ! El diagnóstico de los linfomas malignos es una de las áreas que más dificultad reviste dentro de la histopatología. Si bien muchos casos se diagnostican a través de los datos histomorfológicos e inmunohistoquímicos,
! El diagnóstico de los linfomas malignos es una de las áreas que más dificultad reviste dentro de la histopatología. Si bien muchos casos se diagnostican a través de los datos histomorfológicos e inmunohistoquímicos,
TRATAMIENTO PRONOSTICO DIAGNOSTICO
 Pruebas moleculares en oncología Diagnostico genético Pruebas moleculares en Enfermedades Hematológicas Pruebas moleculares en Infecciosas FarmacoGenomica. TRATAMIENTO PRONOSTICO DIAGNOSTICO. ACREDITACION
Pruebas moleculares en oncología Diagnostico genético Pruebas moleculares en Enfermedades Hematológicas Pruebas moleculares en Infecciosas FarmacoGenomica. TRATAMIENTO PRONOSTICO DIAGNOSTICO. ACREDITACION
DANAGENE BLOOD DNA KIT
 Ref. 0601 100 ml Ref. 0602 200 ml DANAGENE BLOOD DNA KIT 1.INTRODUCCION DANAGENE BLOOD DNA Kit provee un método para la extracción de ADN genómico de alta calidad a partir de sangre total o médula ósea.
Ref. 0601 100 ml Ref. 0602 200 ml DANAGENE BLOOD DNA KIT 1.INTRODUCCION DANAGENE BLOOD DNA Kit provee un método para la extracción de ADN genómico de alta calidad a partir de sangre total o médula ósea.
Validación de métodos, ensayos de aptitud y biometrología en OGM
 Validación de métodos, ensayos de aptitud y biometrología en OGM AMOUNT OF DNA 8 256 PCR Punto 9 Final 512 10 1,024 11 2,048 12 4,096 CYCLE No. de NUMBER ciclo 13 AMOUNT Copias OF de DNA ADN 8,192 140
Validación de métodos, ensayos de aptitud y biometrología en OGM AMOUNT OF DNA 8 256 PCR Punto 9 Final 512 10 1,024 11 2,048 12 4,096 CYCLE No. de NUMBER ciclo 13 AMOUNT Copias OF de DNA ADN 8,192 140
La Patología a Molecular y el Control de Calidad
 UNIDAD DIDÁCTICA 7: LOS PROCESOS EN ANATOMÍA PATOLÓGICA La Patología a Molecular y el Control de Calidad Asunción n Olmo Sevilla Master Diagnóstica S. L. Patología Molecular: Patología del futuro X Personal:
UNIDAD DIDÁCTICA 7: LOS PROCESOS EN ANATOMÍA PATOLÓGICA La Patología a Molecular y el Control de Calidad Asunción n Olmo Sevilla Master Diagnóstica S. L. Patología Molecular: Patología del futuro X Personal:
BIOLOGÍA MOLECULAR TOTAL DE PUNTOS: 90. País: ESPAÑA
 XII OLIMPIADA IBEROAMERICANA DE BIOLOGÍA SETIEMBRE 2018 LOJA-ECUADOR EXAMEN PRÁCTICO BIOLOGÍA MOLECULAR TOTAL DE PUNTOS: 90 TIEMPO PERMITIDO: 120 minutos País: ESPAÑA ESCRIBA EL CÓDIGO EN EL SIGUIENTE
XII OLIMPIADA IBEROAMERICANA DE BIOLOGÍA SETIEMBRE 2018 LOJA-ECUADOR EXAMEN PRÁCTICO BIOLOGÍA MOLECULAR TOTAL DE PUNTOS: 90 TIEMPO PERMITIDO: 120 minutos País: ESPAÑA ESCRIBA EL CÓDIGO EN EL SIGUIENTE
GENOTIPADO 1. MICROSATÉLITES
 GENOTIPADO 1. MICROSATÉLITES El uso de marcadores moleculares para la identificación de genotipos de interés mediante microsatélites es susceptible de ser analizadas a través de la instrumentación existente
GENOTIPADO 1. MICROSATÉLITES El uso de marcadores moleculares para la identificación de genotipos de interés mediante microsatélites es susceptible de ser analizadas a través de la instrumentación existente
Código: IDK-004 Ver: 1. Factor II 20210
 20210 Sistema para detección de la alteración G20210A en el gene que codifica para el de la coagulación humana PM 1 2 Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2
20210 Sistema para detección de la alteración G20210A en el gene que codifica para el de la coagulación humana PM 1 2 Valdense 3616. 11700. Montevideo. Uruguay. Teléfono (598) 2 336 83 01. Fax (598) 2
Protocolo de iniciación PCR. a tiempo real
 Protocolo de iniciación PCR a tiempo real CERTEST Biotec, S.L. Pol. Industrial Río Gállego II, Calle J, Nº 1, 50840, San Mateo de Gállego, Zaragoza (SPAIN) www.certest.es Protocolo de iniciación PCR a
Protocolo de iniciación PCR a tiempo real CERTEST Biotec, S.L. Pol. Industrial Río Gállego II, Calle J, Nº 1, 50840, San Mateo de Gállego, Zaragoza (SPAIN) www.certest.es Protocolo de iniciación PCR a
Protocolos de preparación de muestras
 Protocolos de preparación de muestras Contenido 1. TIPOS DE MUESTRA 2. PROTOCOLO DE PREPARACIÓN DE MUESTRA 2.1 Producto de PCR crudo (sin purificar). 2.2 Producto de PCR crudo en gel (sin purificar). 2.3
Protocolos de preparación de muestras Contenido 1. TIPOS DE MUESTRA 2. PROTOCOLO DE PREPARACIÓN DE MUESTRA 2.1 Producto de PCR crudo (sin purificar). 2.2 Producto de PCR crudo en gel (sin purificar). 2.3
KITS EDUCATIVOS DE BIOLOGÍA MOLECULAR
 KITS EDUCATIVOS DE BIOLOGÍA MOLECULAR Índice General Aula GENYCA. Flujo de trabajo. 3 Kits Educativos de Técnicas Básicas 5 P1-A. Extracción de ADN de Sangre 6 P1-B. Extracción de ADN en Columna 7 P2.
KITS EDUCATIVOS DE BIOLOGÍA MOLECULAR Índice General Aula GENYCA. Flujo de trabajo. 3 Kits Educativos de Técnicas Básicas 5 P1-A. Extracción de ADN de Sangre 6 P1-B. Extracción de ADN en Columna 7 P2.
Características de rendimiento
 Características de rendimiento Kit QIAamp DSP DNA FFPE Tissue, versión 1 60404 Administración de versiones Este documento es la versión 1, R3 de las Características del rendimiento del kit QIAamp DSP DNA
Características de rendimiento Kit QIAamp DSP DNA FFPE Tissue, versión 1 60404 Administración de versiones Este documento es la versión 1, R3 de las Características del rendimiento del kit QIAamp DSP DNA
IdentiClone BCL1/JH Translocation Assay Para la Identificación del Linfoma del Manto y de otros Linfomas y Leucemias Para Diagnóstico In Vitro
 Servicio Técnico: support@invivoscribe.com Servicio al Cliente (EUA): sales@invivoscribe.com Servicio al Cliente (UE): sales-eu@invivoscribe.com IdentiClone BCL1/JH Translocation Assay Para la Identificación
Servicio Técnico: support@invivoscribe.com Servicio al Cliente (EUA): sales@invivoscribe.com Servicio al Cliente (UE): sales-eu@invivoscribe.com IdentiClone BCL1/JH Translocation Assay Para la Identificación
Test Genéticos Moleculares
 CERPO Centro de Referencia Perinatal Oriente Facultad de Medicina, Universidad de Chile Test Genéticos Moleculares Dr. Guillermo Parrao Barrera Residente Medicina Materno Fetal Pontificia Universidad Católica
CERPO Centro de Referencia Perinatal Oriente Facultad de Medicina, Universidad de Chile Test Genéticos Moleculares Dr. Guillermo Parrao Barrera Residente Medicina Materno Fetal Pontificia Universidad Católica
3. MATERIALES Y MÉTODOS
 3. MATERIALES Y MÉTODOS El proceso general llevado a cabo en la presente tesis se ilustra en el siguiente esquema: Exudado uretral/ cervical y/o biopsias Extracción del ADN PCR Digestión Algoritmo computacional:
3. MATERIALES Y MÉTODOS El proceso general llevado a cabo en la presente tesis se ilustra en el siguiente esquema: Exudado uretral/ cervical y/o biopsias Extracción del ADN PCR Digestión Algoritmo computacional:
Ensayo rápido cuantitativo microfluidico para la detección de Dimero - D. Uso Exclusivo para la Atencion Medica Profesional
 Ensayo rápido cuantitativo microfluidico para la detección de Dimero - D Uso Exclusivo para la Atencion Medica Profesional INTRODUCCIÓN Cuando la fibrina en un coágulo sanguíneo se rompe por las enzimas
Ensayo rápido cuantitativo microfluidico para la detección de Dimero - D Uso Exclusivo para la Atencion Medica Profesional INTRODUCCIÓN Cuando la fibrina en un coágulo sanguíneo se rompe por las enzimas
VERSIÓN PARA EQUIPOS COBAS c501/c502 DE ROCHE
 VERSIÓN PARA EQUIPOS COBAS c501/c502 DE ROCHE EQUIPO ADICIONAL NO SUMINISTRADO: La preparación de los reactivos requiere el empleo de micropipetas o sistemas que permitan dispensar los volúmenes especificados.
VERSIÓN PARA EQUIPOS COBAS c501/c502 DE ROCHE EQUIPO ADICIONAL NO SUMINISTRADO: La preparación de los reactivos requiere el empleo de micropipetas o sistemas que permitan dispensar los volúmenes especificados.
DANAGENE SPIN GENOMIC DNA KIT
 DANAGENE SPIN GENOMIC DNA KIT Ref.0605.1 50 extracciones Ref.0605.2 250 extracciones Ref.0605.3 1000 extracciones 1. INTRODUCCION Este kit está designado para una rápida extracción y purificación de ADN
DANAGENE SPIN GENOMIC DNA KIT Ref.0605.1 50 extracciones Ref.0605.2 250 extracciones Ref.0605.3 1000 extracciones 1. INTRODUCCION Este kit está designado para una rápida extracción y purificación de ADN
PCR SIMULADA. Ref.PCR Simulada (4 prácticas) 1. OBJETIVO DEL EXPERIMENTO
 Ref.PCR Simulada (4 prácticas) 1. OBJETIVO DEL EXPERIMENTO PCR SIMULADA El objetivo de este experimento es introducir a los estudiantes en los principios y práctica de la Reacción en Cadena de la Polimerasa
Ref.PCR Simulada (4 prácticas) 1. OBJETIVO DEL EXPERIMENTO PCR SIMULADA El objetivo de este experimento es introducir a los estudiantes en los principios y práctica de la Reacción en Cadena de la Polimerasa
Hoja de protocolo del instrumento QIAsymphony SP
 Hoja de protocolo del instrumento QIAsymphony SP Protocolo DNA_Blood_200_V7_DSP Información general Para uso en diagnóstico in vitro. Este protocolo está indicado para la purificación de ADN mitocondrial
Hoja de protocolo del instrumento QIAsymphony SP Protocolo DNA_Blood_200_V7_DSP Información general Para uso en diagnóstico in vitro. Este protocolo está indicado para la purificación de ADN mitocondrial
- Las mezclas de amplificación se presentan en formato monotest en tubos de PCR de 0.2 0.5 ml, identificados con diferente color.
 ! El diagnóstico de los linfomas malignos es una de las áreas que más dificultad reviste dentro de la histopatología. Si bien muchos casos se diagnostican a través de los datos histomorfológicos e inmunohistoquímicos,
! El diagnóstico de los linfomas malignos es una de las áreas que más dificultad reviste dentro de la histopatología. Si bien muchos casos se diagnostican a través de los datos histomorfológicos e inmunohistoquímicos,
DANAGENE SPIN BLOOD DNA KIT
 DANAGENE SPIN BLOOD DNA KIT Ref. 0606.1 50 extracciones Ref. 0606.2 250 extracciones 1. INTRODUCCION Este kit está designado para una rápida extracción y purificación de ADN genómico de alta calidad a
DANAGENE SPIN BLOOD DNA KIT Ref. 0606.1 50 extracciones Ref. 0606.2 250 extracciones 1. INTRODUCCION Este kit está designado para una rápida extracción y purificación de ADN genómico de alta calidad a
PROCEDIMIENTO DE EVALUACIÓN Y ACREDITACIÓN DE LAS COMPETENCIAS PROFESIONALES CUESTIONARIO DE AUTOEVALUACIÓN PARA LAS TRABAJADORAS Y TRABAJADORES
 MINISTERIO DE EDUCACIÓN SECRETARÍA DE ESTADO DE EDUCACIÓN Y FORMACIÓN PROFESIONAL DIRECCIÓN GENERAL DE FORMACIÓN PROFESIONAL INSTITUTO NACIONAL DE LAS CUALIFICACIONES PROCEDIMIENTO DE EVALUACIÓN Y ACREDITACIÓN
MINISTERIO DE EDUCACIÓN SECRETARÍA DE ESTADO DE EDUCACIÓN Y FORMACIÓN PROFESIONAL DIRECCIÓN GENERAL DE FORMACIÓN PROFESIONAL INSTITUTO NACIONAL DE LAS CUALIFICACIONES PROCEDIMIENTO DE EVALUACIÓN Y ACREDITACIÓN
TECNICAS DE BIOLOGIA MOLECULAR
 Química Biológica Patológica TECNICAS DE BIOLOGIA MOLECULAR IV- Parte Aplicadas al diagnóstico de Enfermedades Genéticas Tema:1 (1) Dra. Silvia Varas qbpatologica.unsl@gmail.com TIPO DE MUTACION DEFINE
Química Biológica Patológica TECNICAS DE BIOLOGIA MOLECULAR IV- Parte Aplicadas al diagnóstico de Enfermedades Genéticas Tema:1 (1) Dra. Silvia Varas qbpatologica.unsl@gmail.com TIPO DE MUTACION DEFINE
Material complementario UD 5
 Material complementario UD 5 Componentes de la PCR ADN molde que es el que se quiere replicar. Oligonucleótidos iniciadores, primers o cebadores: - Son oligonucleótidos monocatenarios cuya secuencia es
Material complementario UD 5 Componentes de la PCR ADN molde que es el que se quiere replicar. Oligonucleótidos iniciadores, primers o cebadores: - Son oligonucleótidos monocatenarios cuya secuencia es
PCR Múltiplex. Listeria monocytogenes
 PCR Múltiplex Listeria monocytogenes PCR-múltiplex En una sola reacción de PCR se amplifican al mismo tiempo 2 o más genes Condiciones similares de PCR para los genes amplificar: Desnaturalización Alineamiento
PCR Múltiplex Listeria monocytogenes PCR-múltiplex En una sola reacción de PCR se amplifican al mismo tiempo 2 o más genes Condiciones similares de PCR para los genes amplificar: Desnaturalización Alineamiento
4. TIPADO GENÉTICO DE BACTERIAS PATÓGENAS MEDIANTE ELECTROFORESIS EN CAMPOS PULSADOS (PFGE) Materiales - Bacterias crecidas en placas de agar
 4. TIPADO GENÉTICO DE BACTERIAS PATÓGENAS MEDIANTE ELECTROFORESIS EN CAMPOS PULSADOS (PFGE) Materiales - Bacterias crecidas en placas de agar - Agarosa de grado molecular - Agarosa de bajo punto de fusión
4. TIPADO GENÉTICO DE BACTERIAS PATÓGENAS MEDIANTE ELECTROFORESIS EN CAMPOS PULSADOS (PFGE) Materiales - Bacterias crecidas en placas de agar - Agarosa de grado molecular - Agarosa de bajo punto de fusión
TP Nro 6 Validación de Métodos Analíticos
 TP Nro 6 Validación de Métodos Analíticos 1. Introducción: La validación de un método es el procedimiento por medio del cual se definen los requerimientos analíticos y se confirma que el método en consideración
TP Nro 6 Validación de Métodos Analíticos 1. Introducción: La validación de un método es el procedimiento por medio del cual se definen los requerimientos analíticos y se confirma que el método en consideración
Ficha descriptiva SERVICIOS CENTRALES DEL CENTRO DE APOYO TECNOLÓGICO DE LA URJC. Nombre de la UNIDAD/Técnica: Genómica y Citometría de Flujo.
 Página 1 de 5 Nombre de la UNIDAD/Técnica: Genómica y Citometría de Flujo. Responsable: José Antonio Mas Gutiérrez Teléfono: 914 888 645 / 914 887 184 Email joseantonio.mas@urjc.es Principios de la Técnica
Página 1 de 5 Nombre de la UNIDAD/Técnica: Genómica y Citometría de Flujo. Responsable: José Antonio Mas Gutiérrez Teléfono: 914 888 645 / 914 887 184 Email joseantonio.mas@urjc.es Principios de la Técnica
Diagnóstico molecular más allá de la simplicidad. Idylla. Sistema de diagnóstico molecular completamente automatizado
 Diagnóstico molecular más allá de la simplicidad Idylla TM Sistema de diagnóstico molecular completamente automatizado Idylla TM Nunca habia sido tan fácil volverse molecular Facilidad de uso El sistema
Diagnóstico molecular más allá de la simplicidad Idylla TM Sistema de diagnóstico molecular completamente automatizado Idylla TM Nunca habia sido tan fácil volverse molecular Facilidad de uso El sistema
KIT PARA ANÁLISIS MOLECULAR DEL GEN IgH Nº CAT. MAD BP-2/5 (20 DETERMINACIONES)
 KIT PARA ANÁLISIS MOLECULAR DEL GEN IgH Nº CAT. MAD-003994BP-2/5 (20 DETERMINACIONES) El diagnóstico de los linfomas malignos es una de las áreas que más dificultad reviste dentro de la histopatología.
KIT PARA ANÁLISIS MOLECULAR DEL GEN IgH Nº CAT. MAD-003994BP-2/5 (20 DETERMINACIONES) El diagnóstico de los linfomas malignos es una de las áreas que más dificultad reviste dentro de la histopatología.
FIND-IT Bronquitis Infecciosa Aviar
 FIND-IT Bronquitis Infecciosa Aviar Sistema para la detección del virus de Bronquitis Infeccioso Aviar por Transcripción Reversa y PCR en Tiempo Real en un solo paso. FBIA 50 Bronquitis Infecciosa Aviar:
FIND-IT Bronquitis Infecciosa Aviar Sistema para la detección del virus de Bronquitis Infeccioso Aviar por Transcripción Reversa y PCR en Tiempo Real en un solo paso. FBIA 50 Bronquitis Infecciosa Aviar:
Técnicas del ADN recombinante Introducción
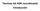 Técnicas del ADN recombinante Introducción Estructura primaria del ADN Enzimas de restricción (ER) Son enzimas (endonucleasas) de origen bacteriano que reconocen y cortan secuencias específicas (4-8 pb)
Técnicas del ADN recombinante Introducción Estructura primaria del ADN Enzimas de restricción (ER) Son enzimas (endonucleasas) de origen bacteriano que reconocen y cortan secuencias específicas (4-8 pb)
A03 Apéndice de la Guía para la Calificación Revision 5.14 April 6, 2016
 A03 Apéndice de la Guía para la Calificación Revision 5.14 April 6, 2016 Nombre del Laboratorio: Nombre del Apéndice: Apéndice Número: Asesor: Fecha: A03 Apéndice de la Guía para la calificación NOTAS
A03 Apéndice de la Guía para la Calificación Revision 5.14 April 6, 2016 Nombre del Laboratorio: Nombre del Apéndice: Apéndice Número: Asesor: Fecha: A03 Apéndice de la Guía para la calificación NOTAS
Progensa PCA3 Urine Specimen Transport Kit
 Urine Specimen Transport Kit Instrucciones del médico Para uso de diagnóstico in vitro. Para exportación de EE.UU. únicamente. Instrucciones 1. Se recomienda que el paciente beba agua abundantemente (aproximadamente
Urine Specimen Transport Kit Instrucciones del médico Para uso de diagnóstico in vitro. Para exportación de EE.UU. únicamente. Instrucciones 1. Se recomienda que el paciente beba agua abundantemente (aproximadamente
Instrucciones de uso. BAG Cycler Check. Kit de para la validación de la uniformidad de la temperatura en los termocicladores
 Instrucciones de uso BAG Cycler Check Kit de para la validación de la uniformidad de la temperatura en los termocicladores listo para usar, prealicuotado REF 7104 (10 tests) REF 71044 (4 tests) Contenidos
Instrucciones de uso BAG Cycler Check Kit de para la validación de la uniformidad de la temperatura en los termocicladores listo para usar, prealicuotado REF 7104 (10 tests) REF 71044 (4 tests) Contenidos
REF IMG Determinación de la informatividad de los polimorfismos en quimeras hematopoyéticas mediante PCR a tiempo real
 Determinación de la informatividad de los polimorfismos en quimeras hematopoyéticas mediante PCR a tiempo real REF IMG-116-26 Fabricado por: Instituto de Medicina Genómica SL Agustín Escardino 9, Parc
Determinación de la informatividad de los polimorfismos en quimeras hematopoyéticas mediante PCR a tiempo real REF IMG-116-26 Fabricado por: Instituto de Medicina Genómica SL Agustín Escardino 9, Parc
TEMA 14 NUEVAS TECNOLOGÍAS PARA EL ESTUDIO DE LAS ENFERMEDADES INFECCIOSAS: MÉTODOS GENÉTICOS
 TEMA 14 NUEVAS TECNOLOGÍAS PARA EL ESTUDIO DE LAS ENFERMEDADES INFECCIOSAS: MÉTODOS GENÉTICOS Tema 14. Nuevas tecnologías para el estudio de enfermedades infecciosas: métodos genéticos Métodos genéticos
TEMA 14 NUEVAS TECNOLOGÍAS PARA EL ESTUDIO DE LAS ENFERMEDADES INFECCIOSAS: MÉTODOS GENÉTICOS Tema 14. Nuevas tecnologías para el estudio de enfermedades infecciosas: métodos genéticos Métodos genéticos
REAL TIME PCR DETECTION KITS
 REAL TIME PCR DETECTION KITS REAL TIME PCR KITS Compañía Certest Biotec es una empresa enfocada en el desarrollo y fabricación de productos de diagnóstico in vitro con aplicaciones humanas, veterinarias
REAL TIME PCR DETECTION KITS REAL TIME PCR KITS Compañía Certest Biotec es una empresa enfocada en el desarrollo y fabricación de productos de diagnóstico in vitro con aplicaciones humanas, veterinarias
11. MÉTODOS PARA LA DETECCIÓN DEL ROTAVIRUS. Actualmente existen diversos métodos en el mercado que pueden utilizarse
 11. MÉTODOS PARA LA DETECCIÓN DEL ROTAVIRUS Actualmente existen diversos métodos en el mercado que pueden utilizarse para el diagnóstico de rotavirus, las cuales pueden realizarse directamente a partir
11. MÉTODOS PARA LA DETECCIÓN DEL ROTAVIRUS Actualmente existen diversos métodos en el mercado que pueden utilizarse para el diagnóstico de rotavirus, las cuales pueden realizarse directamente a partir
HBsAg CONFIRMATORY TEST Para la confirmación de muestras positivas con el UMELISA HBsAg PLUS
 HBsAg CONFIRMATORY TEST Para la confirmación de muestras positivas con el UMELISA HBsAg PLUS INTERES CLÍNICO Con el descubrimiento del antígeno de superficie del virus de la Hepatitis B (1) se crearon
HBsAg CONFIRMATORY TEST Para la confirmación de muestras positivas con el UMELISA HBsAg PLUS INTERES CLÍNICO Con el descubrimiento del antígeno de superficie del virus de la Hepatitis B (1) se crearon
DANAGENE microspin DNA KIT
 Ref. 0607.1 50 extracciones Ref. 0607.2 250 extracciones 1.INTRODUCCION DANAGENE microspin DNA KIT Este kit permite una eficiente extracción de ADN genómico y mitocondrial a partir de muestras de pequeño
Ref. 0607.1 50 extracciones Ref. 0607.2 250 extracciones 1.INTRODUCCION DANAGENE microspin DNA KIT Este kit permite una eficiente extracción de ADN genómico y mitocondrial a partir de muestras de pequeño
1. OBTENCIÓN DE ADN DE BACTERIAS PATÓGENAS
 1. OBTENCIÓN DE ADN DE BACTERIAS PATÓGENAS Existen diferentes métodos para la obtención de ADN bacteriano que varían en duración y complejidad del procedimiento en función de la calidad del ADN que queramos
1. OBTENCIÓN DE ADN DE BACTERIAS PATÓGENAS Existen diferentes métodos para la obtención de ADN bacteriano que varían en duración y complejidad del procedimiento en función de la calidad del ADN que queramos
PROCEDIMIENTO DE EVALUACIÓN Y ACREDITACIÓN DE LAS COMPETENCIAS PROFESIONALES CUESTIONARIO DE AUTOEVALUACIÓN PARA LAS TRABAJADORAS Y TRABAJADORES
 MINISTERIO DE EDUCACIÓN SECRETARÍA DE ESTADO DE EDUCACIÓN Y FORMACIÓN PROFESIONAL DIRECCIÓN GENERAL DE FORMACIÓN PROFESIONAL INSTITUTO NACIONAL DE LAS CUALIFICACIONES PROCEDIMIENTO DE EVALUACIÓN Y ACREDITACIÓN
MINISTERIO DE EDUCACIÓN SECRETARÍA DE ESTADO DE EDUCACIÓN Y FORMACIÓN PROFESIONAL DIRECCIÓN GENERAL DE FORMACIÓN PROFESIONAL INSTITUTO NACIONAL DE LAS CUALIFICACIONES PROCEDIMIENTO DE EVALUACIÓN Y ACREDITACIÓN
12.359,04 IMPORTE MAXIMO LOTE 1: ,92 IMPORTE MAXIMO LOTE 2: IMPORTE MAXIMO LOTE 3: ,54 REACTIVOS PARA AISLAMIENTO DE ACIDOS NUCLEICOS
 HOSPITAL RAMON Y CAJAL RAZON SOCIAL: SUMINISTROS - PETICION DE OFERTAS C.I.F.: SERVICIO DE GENETICA MEDICA DOMICILIO: LOCALIDAD: TRAMITA: HOSPITAL RAMON Y CAJAL TELEFONO/FAX: Nº DE COMPRA: CONCURSO ABIERTO
HOSPITAL RAMON Y CAJAL RAZON SOCIAL: SUMINISTROS - PETICION DE OFERTAS C.I.F.: SERVICIO DE GENETICA MEDICA DOMICILIO: LOCALIDAD: TRAMITA: HOSPITAL RAMON Y CAJAL TELEFONO/FAX: Nº DE COMPRA: CONCURSO ABIERTO
PARVOVIRUS B19 oligomix Alert kit
 CARACTERÍSTICAS DEL KIT búsqueda del ADN de Parvovirus B19 ÍNDICE USO PREVISTO pág. 1 PRESENTACIÓN DEL KIT pág. 1 CARACTERÍSTICAS DEL KIT pág. 2 OTROS PRODUCTOS REQUERIDOS pág. 2 MATERIAL PROVISTO EN EL
CARACTERÍSTICAS DEL KIT búsqueda del ADN de Parvovirus B19 ÍNDICE USO PREVISTO pág. 1 PRESENTACIÓN DEL KIT pág. 1 CARACTERÍSTICAS DEL KIT pág. 2 OTROS PRODUCTOS REQUERIDOS pág. 2 MATERIAL PROVISTO EN EL
RT- PCR diagnóstica del Cotton leafroll dwarf virus (CLRDV) en plantas de algodón
 RT- PCR diagnóstica del Cotton leafroll dwarf virus (CLRDV) en plantas de algodón La identificación rápida y precisa de los patógenos que afectan a los cultivos de interés agronómico es crítica para predecir
RT- PCR diagnóstica del Cotton leafroll dwarf virus (CLRDV) en plantas de algodón La identificación rápida y precisa de los patógenos que afectan a los cultivos de interés agronómico es crítica para predecir
REF : IMG Determinación de la informatividad de los polimorfismos en quimeras hematopoyéticas mediante PCR a tiempo real
 Determinación de la informatividad de los polimorfismos en quimeras hematopoyéticas mediante PCR a tiempo real REF : IMG-116-24 Fabricado por: Instituto de Medicina Genómica SL Agustín Escardino 9, Parc
Determinación de la informatividad de los polimorfismos en quimeras hematopoyéticas mediante PCR a tiempo real REF : IMG-116-24 Fabricado por: Instituto de Medicina Genómica SL Agustín Escardino 9, Parc
HBsAg CONFIRMATORY TEST INTERÉS CLÍNICO
 HBsAg CONFIRMATORY TEST Para la confirmación de muestras positivas con el UMELISA HBsAg PLUS. INTERÉS CLÍNICO Con el descubrimiento del antígeno de superficie del virus de la Hepatitis B (1) se crearon
HBsAg CONFIRMATORY TEST Para la confirmación de muestras positivas con el UMELISA HBsAg PLUS. INTERÉS CLÍNICO Con el descubrimiento del antígeno de superficie del virus de la Hepatitis B (1) se crearon
Universidad Nacional Autónoma de México Secretaría de Educación Abierta y Continua Laboratorio de Biología Molecular y Genómica Facultad de Ciencias
 Agenda del Curso Teórico-Práctico de Genética Forense Universidad Nacional Autónoma de México Secretaría de Educación Abierta y Continua Laboratorio de Biología Molecular y Genómica Facultad de Ciencias
Agenda del Curso Teórico-Práctico de Genética Forense Universidad Nacional Autónoma de México Secretaría de Educación Abierta y Continua Laboratorio de Biología Molecular y Genómica Facultad de Ciencias
BETA - GLOBIN oligomix Alert kit control externo de calidad del ADN extraído
 ÍNDICE USO PREVISTO pág. 1 PRESENTACIÓN DEL KIT pág. 1 CARACTERÍSTICAS DEL KIT pág. 2 OTROS PRODUCTOS REQUERIDOS pág. 2 MATERIAL PROVISTO EN EL KIT pág. 2 MATERIAL REQUERIDO NO PROVISTO EN EL KIT pág.
ÍNDICE USO PREVISTO pág. 1 PRESENTACIÓN DEL KIT pág. 1 CARACTERÍSTICAS DEL KIT pág. 2 OTROS PRODUCTOS REQUERIDOS pág. 2 MATERIAL PROVISTO EN EL KIT pág. 2 MATERIAL REQUERIDO NO PROVISTO EN EL KIT pág.
SOLICITUD DEL SERVICIO DE SECUENCIACION CENTRO DE DETECCION BIOMOLECULAR EN ENFERMEDADES EMERGENTES/BUAP
 SOLICITUD DEL SERVICIO DE SECUENCIACION CENTRO DE DETECCION BIOMOLECULAR EN ENFERMEDADES EMERGENTES/BUAP Usuario: Institución: Fecha: Departamento: e-mail: Teléfono: Ext.: Investigador Principal: e-mail:
SOLICITUD DEL SERVICIO DE SECUENCIACION CENTRO DE DETECCION BIOMOLECULAR EN ENFERMEDADES EMERGENTES/BUAP Usuario: Institución: Fecha: Departamento: e-mail: Teléfono: Ext.: Investigador Principal: e-mail:
DANAGENE SALIVA KIT. Ref Extracciones / Ref Extracciones
 DANAGENE SALIVA KIT Ref.0603.4 50 Extracciones / Ref.0603.41 160 Extracciones 1.INTRODUCCION Este kit provee un método para la extracción de ADN genómico de alta calidad a partir de muestras de saliva
DANAGENE SALIVA KIT Ref.0603.4 50 Extracciones / Ref.0603.41 160 Extracciones 1.INTRODUCCION Este kit provee un método para la extracción de ADN genómico de alta calidad a partir de muestras de saliva
Reacción en cadena de la polimerasa (PCR)
 Curso: Biología Molecular y Genómica Enero 2014. Conceptos elementales sobre la técnica de reacción en cadena de la polimerasa (PCR) Dr. Juan Venegas Hermosilla Programa de Biología Celular y Molecular
Curso: Biología Molecular y Genómica Enero 2014. Conceptos elementales sobre la técnica de reacción en cadena de la polimerasa (PCR) Dr. Juan Venegas Hermosilla Programa de Biología Celular y Molecular
ANÁLISIS DE LA EXPRESIÓN GÉNICA
 ANÁLISIS DE LA EXPRESIÓN GÉNICA qpcr (PCR en tiempo real) Northern blot Western blot Gen reportero - Northern blot - Aporta información sobre la presencia de un transcrito, su abundancia y su tamaño -
ANÁLISIS DE LA EXPRESIÓN GÉNICA qpcr (PCR en tiempo real) Northern blot Western blot Gen reportero - Northern blot - Aporta información sobre la presencia de un transcrito, su abundancia y su tamaño -
REACCIÓN EN CADENA DE LA POLIMERASA (PCR)
 REACCIÓN EN CADENA DE LA POLIMERASA (PCR) Microbiología General Microbiología M de los Alimentos Licenciatura en Bioquímica i Ingeniería en alimentos c Microbiología r 2015 Licenciatura en Biotecnología
REACCIÓN EN CADENA DE LA POLIMERASA (PCR) Microbiología General Microbiología M de los Alimentos Licenciatura en Bioquímica i Ingeniería en alimentos c Microbiología r 2015 Licenciatura en Biotecnología
Técnico Superior en Laboratorio Clínico y Biomédico
 CICLO FORMATIVO DE GRADO SUPERIOR Técnico Superior en Laboratorio Clínico y Biomédico EXTRACTO DE LA PROGRAMACIÓN DEL MODULO "BIOLOGIA MOLECULAR" CURSO ACADÉMICO 2018/ 19 PROFESORA DEL MODULO Carmen Méndez
CICLO FORMATIVO DE GRADO SUPERIOR Técnico Superior en Laboratorio Clínico y Biomédico EXTRACTO DE LA PROGRAMACIÓN DEL MODULO "BIOLOGIA MOLECULAR" CURSO ACADÉMICO 2018/ 19 PROFESORA DEL MODULO Carmen Méndez
50 kits de recolección de muestras con torunda multitest Aptima (N.º de catálogo PRD-03546) Cada kit contiene:
 Uso previsto El kit de recolección de muestras con torunda se utiliza con los ensayos Aptima. El kit de recolección de muestras con torunda multitest Aptima se utiliza para que médico y paciente puedan
Uso previsto El kit de recolección de muestras con torunda se utiliza con los ensayos Aptima. El kit de recolección de muestras con torunda multitest Aptima se utiliza para que médico y paciente puedan
Aspectos técnicos para establecer el límite de la detección mediante amplificación por PCR
 Aspectos técnicos para establecer el límite de la detección mediante amplificación por PCR Martha Graciela Rocha Munive Centro Nacional de Investigación y capacitación ambiental Instituto Nacional de Ecología
Aspectos técnicos para establecer el límite de la detección mediante amplificación por PCR Martha Graciela Rocha Munive Centro Nacional de Investigación y capacitación ambiental Instituto Nacional de Ecología
GMO Extraction Kit. Part No:
 GMO Extraction Kit Part No: 4466336 1. Contenido del kit La siguiente tabla muestra los reactivos incluidos en el kit: Reactivos Lysis Buffer 1 Lysis Buffer 2 Wash Buffer 1 Wash Buffer 2 H 2 O Proteinase
GMO Extraction Kit Part No: 4466336 1. Contenido del kit La siguiente tabla muestra los reactivos incluidos en el kit: Reactivos Lysis Buffer 1 Lysis Buffer 2 Wash Buffer 1 Wash Buffer 2 H 2 O Proteinase
MATERIALES Y MÉTODOS. Muestras
 MATERIALES Y MÉTODOS Muestras Las muestras de sangre con el bacilo M. tuberculosis se obtuvieron de 2 pacientes con tuberculosis diagnosticada por clínica, laboratorio y con cultivo positivo como controles
MATERIALES Y MÉTODOS Muestras Las muestras de sangre con el bacilo M. tuberculosis se obtuvieron de 2 pacientes con tuberculosis diagnosticada por clínica, laboratorio y con cultivo positivo como controles
DANAGENE microrna KIT
 DANAGENE microrna KIT Ref.0804 1.INTRODUCCION Este kit provee un método rápido y eficiente para la extracción y purificación de moléculas pequeñas de ARN (
DANAGENE microrna KIT Ref.0804 1.INTRODUCCION Este kit provee un método rápido y eficiente para la extracción y purificación de moléculas pequeñas de ARN (
Práctica: Electroforesis de DNA y transferencia a membranas de celulosa o nylon.
 Biología Celular y Molecular para Medicina Jorge Contreras Pineda Práctica: Electroforesis de DNA y transferencia a membranas de celulosa o nylon. GENERALIDADES La electroforesis es una técnica de laboratorio
Biología Celular y Molecular para Medicina Jorge Contreras Pineda Práctica: Electroforesis de DNA y transferencia a membranas de celulosa o nylon. GENERALIDADES La electroforesis es una técnica de laboratorio
qprotein (BCA) Kit para cuantificar proteinas totales PB-L Productos Bio-Lógicos
 qprotein () Kit para cuantificar proteinas totales PB-L http://www.pb-l.com.ar qprotein () Cat. no. RA03 CONTENIDO Componentes RA0301 RA0302 Buffer A 250 ml 500 ml Buffer B 5 ml 10 ml Proteína Patrón 5
qprotein () Kit para cuantificar proteinas totales PB-L http://www.pb-l.com.ar qprotein () Cat. no. RA03 CONTENIDO Componentes RA0301 RA0302 Buffer A 250 ml 500 ml Buffer B 5 ml 10 ml Proteína Patrón 5
BIOFOOD Kits Kits para detección e identificación de especies de vertebrados en alimentos usando secuencias génicas (Ref )
 Fabricado por: BIOTOOLS B&M Labs, S.A. Valle de Tobalina - 52 - Nave 39 28021 Madrid Spain Tel. (34) 91 710 00 74 Fax (34) 91 505 31 18 e-mail: info@biotools.eu www.biotools.eu BIOFOOD Kits Kits para detección
Fabricado por: BIOTOOLS B&M Labs, S.A. Valle de Tobalina - 52 - Nave 39 28021 Madrid Spain Tel. (34) 91 710 00 74 Fax (34) 91 505 31 18 e-mail: info@biotools.eu www.biotools.eu BIOFOOD Kits Kits para detección
PLANIFICACIÓN DE ASIGNATURA
 PLANIFICACIÓN DE ASIGNATURA I IDENTIFICACION GENERAL DE LA ASIGNATURA CARRERA BIOQUIMICA DEPARTAMENTO BIOLOGIA ASIGNATURA BIOLOGIA MOLECULAR II CÓDIGO 1681 PRERREQUISITOS Biología Molecular I CREDITOS
PLANIFICACIÓN DE ASIGNATURA I IDENTIFICACION GENERAL DE LA ASIGNATURA CARRERA BIOQUIMICA DEPARTAMENTO BIOLOGIA ASIGNATURA BIOLOGIA MOLECULAR II CÓDIGO 1681 PRERREQUISITOS Biología Molecular I CREDITOS
FluoroSpheres Code No. K0110
 FluoroSpheres Code No. K0110 6a edición Perlas de calibración para monitoreo diario del citómetro de flujo. Contiene reactivos para 40 calibraciones. (105798-004) SSK0110CE_02/ES/2015.12 p. 1/8 Contenidos
FluoroSpheres Code No. K0110 6a edición Perlas de calibración para monitoreo diario del citómetro de flujo. Contiene reactivos para 40 calibraciones. (105798-004) SSK0110CE_02/ES/2015.12 p. 1/8 Contenidos
INDICACIONES TRADOS. Orina. control hcg. Juego de. hcg Orina. etapas de embarazo. temprano. Cuando se. hcg Orina. tamponada con.
 Instrucciones para uso profesional INDICACIONES El Juego de control hcg Orina se utiliza con la prueba de QuickVue+ hcg Combo, prueba de QuickVue hcg Orina o Combo y prueba de RapidVue hcg. Estos controles
Instrucciones para uso profesional INDICACIONES El Juego de control hcg Orina se utiliza con la prueba de QuickVue+ hcg Combo, prueba de QuickVue hcg Orina o Combo y prueba de RapidVue hcg. Estos controles
PREPARACIÓN DE MEDIOS DE CULTIVO
 Introducción Clasificación de los medios de cultivo Almacenamiento de los medios de cultivo Trabajo Práctico Nº 6 PREPARACIÓN DE MEDIOS DE CULTIVO Objetivo Fundamento Procedimiento Resultados Bibliografía
Introducción Clasificación de los medios de cultivo Almacenamiento de los medios de cultivo Trabajo Práctico Nº 6 PREPARACIÓN DE MEDIOS DE CULTIVO Objetivo Fundamento Procedimiento Resultados Bibliografía
DECK control interno de calidad del ADN extraído
 ELITechGroup S.p.A. C.so Svizzera, 185 10149 Torino ITALY Oficinas: Tel. +39-011 976 19 Fax +39-011 936 76 11 E. mail: emd.support@elitechgroup.com Sitio WEB: www.elitechgroup.com -20 C PRINCIPIO DEL MÉTODO
ELITechGroup S.p.A. C.so Svizzera, 185 10149 Torino ITALY Oficinas: Tel. +39-011 976 19 Fax +39-011 936 76 11 E. mail: emd.support@elitechgroup.com Sitio WEB: www.elitechgroup.com -20 C PRINCIPIO DEL MÉTODO
ELECTROPHORESIS 4 detección electroforética de ADN
 ÍNDICE USO PREVISTO pág. 1 PRINCIPIO DEL MÉTODO pág. 2 DESCRIPCIÓN DEL KIT pág. 2 MATERIAL PROVISTO EN EL KIT pág. 2 MATERIAL REQUERIDO NO PROVISTO EN EL KIT pág. 3 OTROS PRODUCTOS REQUERIDOS pág. 3 ADVERTENCIAS
ÍNDICE USO PREVISTO pág. 1 PRINCIPIO DEL MÉTODO pág. 2 DESCRIPCIÓN DEL KIT pág. 2 MATERIAL PROVISTO EN EL KIT pág. 2 MATERIAL REQUERIDO NO PROVISTO EN EL KIT pág. 3 OTROS PRODUCTOS REQUERIDOS pág. 3 ADVERTENCIAS
QUANTIMIX LIONPROBES KIT
 Fabricado por: BIOTOOLS B&M Labs, S.A. Valle de Tobalina - 52 - Nave 39 28021 Madrid España Tel. 91 710 00 74 Fax 93 843 78 84 e-mail: info@biotools.eu www.biotools.eu QUANTIMIX LIONPROBES KIT Kit LIONPROBES
Fabricado por: BIOTOOLS B&M Labs, S.A. Valle de Tobalina - 52 - Nave 39 28021 Madrid España Tel. 91 710 00 74 Fax 93 843 78 84 e-mail: info@biotools.eu www.biotools.eu QUANTIMIX LIONPROBES KIT Kit LIONPROBES
3. Tipo de poder adjudicador: Administración Pública. Principal actividad ejercida: Sanidad
 Ref: 47/04449.9/8 ANUNCIO DE LICITACIÓN DEL CONTRATO DE SUMINISTRO DE REACTIVOS, FUNGIBLES, ACCESORIOS PARA ANALIZADORES GENETICOS, TERMOCICLADORES Y PCR CUANTITATIVO TIEMPO REAL CON DESTINO AL HOSPITAL
Ref: 47/04449.9/8 ANUNCIO DE LICITACIÓN DEL CONTRATO DE SUMINISTRO DE REACTIVOS, FUNGIBLES, ACCESORIOS PARA ANALIZADORES GENETICOS, TERMOCICLADORES Y PCR CUANTITATIVO TIEMPO REAL CON DESTINO AL HOSPITAL
