Miopatías estructurales congénitas
|
|
|
- Bernardo Mariano Ortega Escobar
- hace 7 años
- Vistas:
Transcripción
1 miopatías Miopatías estructurales congénitas Ricardo Erazo-Torricelli Introducción. Las miopatías congénitas son un grupo heterogéneo de enfermedades que comparten clínica de inicio precoz y alteraciones histopatológicas musculares específicas. El estudio genético permite determinar la mutación causal en la mayoría de los casos. Existe heterogeneidad fenotípica y genotípica, lo que se ilustra al observar que un genotipo puede expresarse en más de una forma clinicopatológica y un fenotipo puede estar causado por diferentes mutaciones genéticas. Desarrollo. En esta revisión, se detallan las características de las principales miopatías congénitas que permiten su identificación clínica, patológica y genética. Se describen los hallazgos de la biopsia muscular que constituyen el principal pilar diagnóstico. Se enfatiza y se detalla la importancia del diagnóstico diferencial, descartando otras patologías que se presentan con hipotonía en la lactancia o el período neonatal. Se destacan las formas neonatales graves (nemalínica, miotubular ligada al X) que se deben identificar precozmente para establecer el pronóstico y brindar un consejo genético adecuado. Se subrayan las mutaciones del gen rianodina (RYR1) por su asociación a la hipertermia maligna y las mutaciones de la selenoproteína 1 (SEPN1) y la miopatía nemalínica por su asociación a hipoventilación nocturna. Conclusiones. El conocimiento profundo de las miopatías estructurales congénitas facilita la confirmación diagnóstica de la miopatía congénita, lo que permite la aplicación oportuna de medidas relacionadas con la respiración y la alimentación de los casos más graves y con la optimización de la función motora en todos los pacientes con miopatía congénita. Palabras clave. Atrofia fibras tipo 1. Hipotonía. Biopsia muscular. Central core. Centronuclear. Miopatías congénitas. Miotubular. Nemalínica. Servicio de Neurología Pediátrica. Hospital Luis Calvo Mackenna. Providencia, Santiago, Chile. Correspondencia: Dr. Ricardo Erazo Torricelli. Carlos Silva Vildósola, 8085-I. La Reina, Santiago, Chile. ricardoerazo@yahoo.com Declaración de intereses: El autor declara la inexistencia de conflictos de interés en relación con este artículo. Aceptado tras revisión externa: Cómo citar este artículo: Erazo-Torricelli R. Miopatías estructurales congénitas. Rev Neurol 2013; 57 (Supl 1): S Revista de Neurología Introducción Las miopatías congénitas son un grupo heterogéneo de enfermedades que tienen en común una expresión clínica precoz (en los primeros meses de vida) y una biopsia muscular con alteraciones estructurales específicas de la fibra muscular [1]. Son genéticamente heterogéneas. Una entidad específica puede estar asociada a mutaciones en más de un gen y muchos de los genes causales pueden asociarse a más de un fenotipo clinicopatológico [2-4]. La presentación clínica de las miopatías congénitas es característica: hipotonía desde el nacimiento o los primeros meses de vida, debilidad muscular proximal, reflejos osteotendinosos disminuidos, diparesia facial y trastornos respiratorios y alimentarios o ambos en los casos más graves. La oftalmoparesia es también un signo relevante y su presencia orienta a tipos específicos de miopatía congénita [4-6]. El curso de las miopatías es no progresivo o lentamente progresivo. En la actualidad, las miopatías congénitas pueden clasificarse, de acuerdo con las alteraciones patológicas del músculo observadas con microscopía óptica y electrónica, en miopatías con acumulación de proteínas (nemalínica y otras), miopatías con cores, miopatías con núcleos centrales y miopatías con variación del tamaño de las fibras [3,7]. Avances recientes sugieren que una anomalía en el acoplamiento excitación-contracción muscular puede ser un tema común en todas las miopatías congénitas, a través de filamentos contráctiles malformados como ocurre en las miopatías nemalínicas o por alteración de la homeostasis del calcio en la tríada (el componente funcional más pequeño de la fibra muscular que incluye el túbulo T y el retículo sarcoplásmico), en el caso de la miopatía miotubular/ centronuclear y la miopatía con cores [7]. En esta revisión, se va a realizar una descripción de cada una de las principales miopatías congénitas y se van a detallar todos los avances alcanzados en la última década en la genética de estas enfermedades, su correlación con la clínica y la histopatología y la descripción de nuevos cuadros clinicopatológicos que expanden el universo de las miopatías congénitas. Rev Neurol 2013; 57 (Supl 1): S53-S64 S53
2 R. Erazo-Torricelli Tabla I. Miopatías congénitas y genes asociados (modificado de [4]). Herencia Gen Proteína Histología Miopatía nemalínica De novo/dominante autosómica recesiva rara o dominante Autosómica dominante Autosómica dominante ACTA 1 NEB TPM3 TPM2 TNNT1 CFL2 KBTBP 13 α-actina Nebulina Tropomiosina 3 β-tropomiosina 2 Troponina lenta Cofilina 2 Familia BTB/Kelch Rod sarcoplasma Rod intranuclear Caps DCTF Cuerpos cebra Core-rods Rod sarcoplasma core y rods Rod sarcoplasma DCTF Rod sarcoplasma caps Rod sarcoplasma Core y rod Core y rod Miopatía con cores Central core Minicore Autosómica dominante RYR1 RYR1 SEPN1 RYR1 Receptor de rianodina 1 Receptor de rianodina 1 Selenoproteína N1 Receptor de rianodina Central core núcleos centrales Central core núcleos centrales Multiminicores Multiminicores Miopatía centronuclear Recesiva ligada X Autosómica dominante MTM1 DNM2 BIN1 RYR1 Miotubularina Dinamina 2 Anfifisina Receptor de rianodina 1 Núcleos centrales Núcleos centrales Núcleos centrales Núcleos centrales Clínica Las miopatías congénitas tienen elementos clínicos comunes, aunque pueden diferenciarse entre sí en algunos aspectos. Coinciden en un inicio precoz en los primeros meses de vida, algunas desde el primer día de vida con trastornos respiratorios graves, se trata por ejemplo de la miopatía miotubular y la miopatía nemalínica grave. Las miopatías congénitas leves pueden expresarse en la edad escolar e incluso en la edad adulta. El signo cardinal de las miopatías congénitas es la hipotonía. Es de inicio precoz y casi siempre es detectable en el recién nacido, aún en los casos no graves. Si bien la hipotonía es generalizada, está más marcada en las cinturas y la musculatura cervical. La diparesia facial y la cefaloparesia son signos característicos. La oftalmoparesia/ptosis palpebral se observa en general en los casos de miopatía miotubular y centronuclear, pero también puede estar presente en casos de miopatía nemalínica y multicore/minicore. La debilidad muscular es más prominente en la musculatura proximal y cervical. Los reflejos osteotendinosos suelen estar disminuidos o abolidos. Se asocian trastornos de succión/ deglución y, en los más graves (miopatía miotubular y forma neonatal de miopatía nemalínica), existe debilidad de la musculatura respiratoria que lleva a una dependencia de la ventilación mecánica prolongada o permanente desde el nacimiento. Clasificación Las miopatías congénitas se clasifican actualmente de acuerdo con la alteración estructural/histoquímica del músculo y en relación con la mutación genética causal (Tabla 1) [2]. Los tres tipos clínicos clásicos son las miopatías nemalínicas, con cores y con núcleos centrales [2,4,6], pero se debe agregar la miopatía con desproporción congénita del tipo de fibras, en la que la única alteración es la atrofia de las fibras de tipo 1, hallazgo observado en las demás miopatías pero asociado a otras alteraciones patológicas específicas. Miopatías nemalínicas Las miopatías nemalínicas o miopatías con agregados (acúmulos) de proteínas [2] son un grupo heterogéneo de miopatías que tienen en común la pre- S54 Rev Neurol 2013; 57 (Supl 1): S53-S64
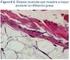
3 Miopatías sencia de bastoncillos o rods en las fibras musculares esqueléticas y se ven rojas con la tinción de tricrómico de Gomori modificado (Fig. 1) [8,9]. En ocasiones, es necesaria la inclusión plástica de toluidina o un análisis con microscopía electrónica para visualizarlas cuando las inclusiones nemalínicas son escasas o pequeñas. Shy et al [10] documentaron el primer caso de miopatía con inclusiones citoplasmáticas, al que denominaron nemalínico por su parecido con los hilos (nema en griego) y esta denominación se mantiene hasta hoy. La microscopía electrónica permite identificar los cuerpos nemalínicos en la banda Z del sarcómero y comprobar que están formados principalmente por acúmulos de α-actinina, aunque también contienen tropomiosina, nebulina, actina y miotilina [11,12]. Los cuerpos nemalínicos pueden aparecer también en el núcleo o estar ahí de manera exclusiva [13]. Muchos defectos genéticos se han relacionado con la presencia de cuerpos nemalínicos en el músculo. El espectro clínico de las miopatías nemalínicas en muy amplio, aunque estén causadas por el mismo defecto genético y van de cuadros graves a leves. El término miopatía nemalínica se utiliza para los casos congénitos de inicio precoz. Los casos de inicio en la edad adulta se denominan miopatías con rods. También se observan rods en las miopatías por defectos del receptor de rianodina (RYR1), que en este caso se llaman miopatías rod-core [14]. Respecto a la herencia de las miopatías nemalínicas, ésta es siempre autosómica y varía entre la autosómica dominante (AD) y la autosómica recesiva (AR), con la excepción de casos aislados de mutación nueva dominante. Hay siete mutaciones genéticas descritas y seis de ellas codifican proteínas de los filamentos finos del sarcómero o asociadas a ellos [15]. Las mutaciones dominantes del gen que codifican la α-actina (ACTA1) y las recesivas que codifican la nebulina (NEB) son las más frecuentes [16]. Clínica La clínica de las miopatías nemalínicas es por lo general de inicio neonatal, pero hay casos de inicio en la niñez e incluso en la edad adulta. La debilidad es generalizada y simétrica, con predilección por los músculos proximales y flexores del cuello. La afectación de la musculatura respiratoria es frecuente, en ocasiones más grave que el resto de la musculatura, por lo que puede haber pacientes ambulantes con insuficiencia ventilatoria significativa [15]. La creatincinasa (CK) está en rangos normales o levemente altos. No hay relación entre las miopatías Figura 1. Biopsia muscular. Tinción de Gomori modificada: cuerpos nemalínicos sarcoplásmicos en la periferia de las fibras. nemalínicas y la hipertermia maligna, aun en los casos de miopatía rod-core por mutación del RYR. Se han definido cinco categorías clínicas de miopatía nemalínica [17]: Forma congénita grave: pacientes sin movimientos o con respiración espontánea al nacer, o con contracturas graves o fracturas al nacer. Forma congénita intermedia: pacientes con movimientos y respiración espontánea al nacer pero que posteriormente son incapaces de alcanzar la marcha o una respiración independiente. Forma congénita típica: con debilidad simétrica, hitos motores retrasados pero alcanzados y curso no progresivo o lentamente progresivo. Forma leve de inicio en la niñez. Forma de inicio en la adultez. El Consorcio Internacional de Miopatía Nemalínica añadió una sexta categoría: otras miopatías nemalínicas con asociaciones inusuales, es decir aquellas que no coinciden con los otros cinco tipos. En un momento más reciente, se ha descrito la miopatía nemalínica esporádica de inicio tardío (SLONM), caracterizada por insuficiencia respiratoria, headdrop o camptocormia y de origen autoinmune [18]. Subtipos de miopatía nemalínica según el defecto genético Miopatía nemalínica causada por una mutación del gen de α-tropomiosina lenta TPM3 (NEM1) Hay casos de mutación del TPM3 dominante de expresión leve y otra recesiva expresada como formas Rev Neurol 2013; 57 (Supl 1): S53-S64 S55
4 R. Erazo-Torricelli intermedias de miopatía nemalínica [19]. La biopsia muscular muestra cuerpos nemalínicos casi en exclusiva en las fibras tipo 1 atróficas. La mutación del TPM3 puede producir exclusivamente desproporción del tipo de fibras [20]. Miopatía nemalínica causada por una mutación del gen nebulina NEB (NEM2) La mutación del NEB es recesiva y produce por lo general la forma típica de miopatía nemalínica, aunque también puede producir formas graves, intermedias y leves [21]. Desde el punto de vista clínico, se observa debilidad de los músculos axiales y de cinturas. Recientemente, se ha descrito una forma clínica en exclusiva distal con biopsia muscular que puede no mostrar cuerpos nemalínicos [22,23]. Existe la miopatía rod-core por mutación del NEB [14]. Miopatía nemalínica por mutación en el gen α-actina ACTA1 (NEM3) La clínica de la miopatía nemalínica por mutación del gen ACTA1 es en general grave, a veces expresada con ausencia de movimientos y respiración espontánea al nacer. Con menos frecuencia, se observan formas intermedias, leves o típicas de miopatías nemalínicas. Los ACTA1 son generalmente dominantes de novo, por lo que no hay riesgo de recurrencia de la enfermedad, excepto en casos muy infrecuentes de mosaicismo en unas pocas familias [24]. Estas mutaciones pueden expresarse raramente como miopatía de cuerpos cebra, de clínica no grave [25]. Cuando los ACTA1 son recesivos corresponden a mutaciones null expresadas casi siempre por una miopatía nemalínica grave con grado de afectación cardíaca dependiente del grado de expresión de la α-actina cardíaca [26]. La biopsia muscular de algunos pacientes con mutación del ACTA1 no muestra cuerpos nemalínicos, en cambio se detectan cores o sólo desproporción del tipo de fibras [15]. Cuando los cuerpos nemalínicos se ubican en el núcleo en lugar del sarcoplasma, se presentan casi siempre cuadros graves de mal pronóstico [15]. Miopatía nemalínica causada por una mutación en el gen β-tropomiosina TPM2 (NEM4) Mutaciones dominantes del gen TPM2 se asocian a cuadros leves y típicos de miopatía nemalínica así como a casos de artrogriposis distal [27,28] o a casos de síndrome de Escobar asociado a una miopatía nemalínica. Las mutaciones dominantes se asocian también a una cap myopathy [29,30]. La mutación homocigótica recesiva sin sentido de la troponina lenta TPNN1 produce miopatía nemalínica en los niños de la comunidad amish [31]. Miopatía nemalínica causada por una mutación en la repetición Kelch y en dominio BTB (POZ) que contiene KBTBD13 (NEM6) Mutaciones del KBTBD13 se han descrito recientemente como causa de miopatías nemalínicas de herencia dominante. Esta miopatía produce clínica de inicio en la infancia temprana y destaca alteraciones posturales que provocan caídas [32]. Miopatía nemalínica por mutación del gen cofilina-2 CFL2 (NEM7) Hay sólo dos pacientes descritos con una mutación del gen CFL2 que, a diferencia de la miopatía nemalínica clásica, no mostraron diparesia facial [33]. Miopatías con cores Bajo esta denominación, se agrupa un tipo heterogéneo de miopatías que presentan en la biopsia muscular un defecto común focal en la tinción oxidativa de la fibra muscular. Según la característica del defecto, se han denominado central core, multicores, minicores y multiminicores [34,35]. En 1956, Shy y Magee describieron los primeros casos de miopatía central core (CCD) [36]. El nombre se acuñó al describir una carencia de actividad oxidativa en el core debida a la ausencia de mitocondrias en ese sector de la fibra muscular (Fig. 2) [37]. Con posterioridad, Engel describió la miopatía multicore, que en la actualidad se denomina enfermedad multiminicore (MmD). Hace poco se ha determinado con más exactitud la alteración genética de las miopatías con cores, al detectar varias mutaciones en el gen del receptor de la rianodina (RYR1) en la CCD [38], involucrado en la homeostasis del calcio y el mecanismo excitacióncontracción (EC) y al identificar el gen de la selenoproteína N (SEPN1) en la miopatía minimulticore (MmD) [39], cuyo producto también está involucrado, entre otras funciones, en la homeostasis del calcio. La presentación clínica de la CCD de herencia dominante se evidencia en la lactancia por hipotonía o en la infancia temprana por retraso motor [40]. Los casos más graves se expresan como secuencia de acinesia fetal [41,42]. Enfermedad central core (CCD) La miopatía o CCD se produce por mutaciones dominantes en el gen RYR1, en el cromosoma 19q13.1 S56 Rev Neurol 2013; 57 (Supl 1): S53-S64
5 Miopatías [43]. Además de en la MCC, el gen RYR1 se ha implicado con la susceptibilidad a presentar hipertermia maligna (HM), un cuadro grave potencialmente letal desencadenado por anestésicos volátiles y relajantes musculares [44]. La relación entre la CCD y la HM se sospechaba desde hacía muchos años debido a la superposición clinicopatológica entre ambos cuadros [45]. En la actualidad, hay 200 mutaciones del RYR1 descritas relacionadas con la HM, la CCD y la MmD [43,46,47], pero también con la miopatía centronuclear y una desproporción congénita del tipo de fibras [48,49]. La mayoría de las mutaciones del RYR1 relacionadas con la HM y la CCD son dominantes missense [50]. En cambio, las mutaciones recesivas del RYR1 se asocian a la miopatía multiminicore [51]. La presentación clínica clásica de la CCD se caracteriza por una hipotonía y debilidad muscular proximal desde los primeros meses de vida. Si se expresa en la infancia predomina el retraso motor [40]. Existen casos muy graves de acinesia fetal y también cuadros leves de inicio en la edad adulta [41,42]. Mialgias, calambres e intolerancia al ejercicio pueden ser signos asociados o la única manifestación de la enfermedad [45,52]. La distribución típica de la debilidad se da en la cintura pelviana y la musculatura axial [40]. Es destacable que la diplejía o paresia facial no se observa en la CCD [50]. La afectación bulbar y respiratoria es infrecuente en la CCD dominante relacionada con el RYR1, pero puede existir en casos neonatales graves [41,42]. Las alteraciones ortopédicas son frecuentes en la CCD por mutación del RYR1, en especial luxación de caderas, escoliosis y deformidades de los pies [50]. La artrogriposis es rara, pero se observa en el síndrome de King-Denborough, cuadro que está asociado a la HM y hace poco que se ha confirmado como genéticamente alélico con la CCD [53,54]. En nuestro centro, hemos diagnosticado a tres hermanos con esta patología, dos de ellos con artrogriposis generalizada, insuficiencia respiratoria y hernia diafragmática. Casi todos los pacientes con CCD alcanzan la marcha independiente. La mayoría de casos son no progresivos o sólo lentamente progresivos en la edad adulta. La relación entre CCD e HM es compleja. No todos los casos de CCD tienen susceptibilidad de sufrir HM. Sin embargo, hay que considerar los niños con esta enfermedad como altamente susceptibles de presentar hipertermia maligna con la anestesia general [50]. La CK puede estar normal pero puede estar elevada unas 6 a 14 veces [50]. Figura 2. a) Biopsia muscular: NADH. Se observa un defecto de tinción (cores) en el centro de las fibras; b) Tinción H-E. Destaca un defecto de tinción en la mayoría de las fibras. Aumento del tejido conectivo. b a Enfermedad multiminicore (MmD) La miopatía o enfermedad multiminicore se clasifica clínicamente en forma clásica, forma con oftalmoplejía externa, forma moderada con afectación de manos y forma neonatal grave [50]. La forma clásica de la enfermedad multiminicore se debe a una mutación recesiva del gen que codifica la selenoproteína, el SEPN1 [39,55,56], y se caracteriza por una espina rígida de inicio temprano, escoliosis e insuficiencia respiratoria [39]. Destaca la dificultad de alimentación y el retraso del crecimiento. Hallazgos frecuentes son voz aguda, diparesia facial e indemnidad de la musculatura extraocular, excepto en las formas graves [50,55,56]. La debilidad muscular axial es relevante en el tronco y los flexores del cuello, con incapacidad de lograr sostén cefálico [57]. La debilidad también está en la musculatura de la cintura escapular. La esco- Rev Neurol 2013; 57 (Supl 1): S53-S64 S57
6 R. Erazo-Torricelli liosis y la insuficiencia respiratoria aparecen en la segunda década de la vida [50]. Es típica la discordancia entre la gravedad de la afectación respiratoria y la escasa debilidad de la muscular segmentaria [56,58]. La hipertermia maligna no se ha descrito en pacientes con MmD producida por mutación del SEPN1, pero sí en pacientes con mutación del RYR1 sin debilidad muscular [59]. La histopatología de la miopatía de la CCD se define como zonas extensas con reducción de la actividad oxidativa en el eje central de la fibra muscular (central cores), mientras que la característica de la miopatía multiminicore (MmD) consiste en múltiples áreas focales que afectan sólo a unos pocos sarcómeros (minicores) con una reducción de la actividad oxidativa [60]. En las CCD relacionadas con la mutación del RYR1 los cores pueden ser centrales, periféricos o haber más de uno por fibra [60]. La miopatía o enfermedad multiminicore (MmD) por mutación del SEPN1 muestra histopatología con cores menos definidos, pequeños y evidenciados por zonas de tinción irregular (multiminicores) [55,57]. Cuando la MmD se debe a una mutación del RYR1 se observan lesiones más grandes llamadas multicores [55,57]. Los central cores se ubican en las fibras de tipo 1 y los minicores se observan en ambos tipos de fibras (1 y 2) [40,60]. Sin embargo, la diferenciación del tipo de fibras puede ser indistinguible en la miopatía central core por mutación del RYR1, pues suele haber predominio o existencia exclusiva de fibras de tipo 1 [49,60,61]. En ocasiones, puede encontrarse sólo desproporción del tipo de fibras en mutaciones de los genes RYR1 y SEPN1 [49,61]. Puede haber asociación de cores con núcleos centrales en mutaciones del RYR1 [46]. Puede observarse un aumento del tejido adiposo y conectivo en mutaciones de los genes SEPN1 y RYR1, que simulen un pattern de distrofia muscular [39]. En la microscopía electrónica, se evidencia una ausencia de mitocondrias en los cores [50]. Los cores de la CCD y la MmD pueden no estar presentes cuando la biopsia muscular se practica a una edad muy temprana [50]. Miopatías centronucleares Las miopatías centronucleares (MCN) son enfermedades hereditarias caracterizadas por una alta incidencia de núcleos que conforman hileras en la parte central de la fibra muscular [5]. De acuerdo con la herencia y la presentación clínica, se clasifican en tres tipos: Herencia recesiva ligada al X o miopatía miotubular: forma grave de inicio prenatal o neonatal causada por una mutación del gen MTM1. Forma clásica autosómica dominante o esporádica de miopatía centronuclear: de presentación leve, moderada o grave producida por una mutación del gen DMN2. Cuadros recesivos con fenotipo moderado o grave producidos por mutaciones en el gen BIN1 [62]. Los tres genes de las MCN participan en la remodelación y el tráfico de membrana y también en la función de los túbulos T de acuerdo con descripciones recientes de disfunción de estos orgánulos en las MCN [62]. Las miopatías centronucleares se describieron en los años 60. Los primeros casos fueron adultos con oftalmoplejía externa y recién nacidos varones con forma grave de herencia recesiva ligada al X. La miopatía miotubular recesiva ligada al X (XLMTM) está causada por la mutación del gen MTM1, que codifica la proteína miotubularina 1 (MTM1) [63]. Existen formas esporádicas y autosómicas, identificadas por dos genes autosómicos, el gen DNM2, que codifica la dinamina 2, forma autosómica dominante (AD) de la MCN [64], y el gen BIN1, que codifica la anfifisina 2, que causa la MCN autosómica recesiva [65]. Además, hay casos familiares sin gen identificado y formas esporádicas. Finalmente, se ha descrito una MCN producida por mutación en el gen RYR1 en la que se asocia presencia de núcleos internalizados y áreas de desorganización miofibrilar. Se expresa en el período neonatal y constituye la MCN relacionada con una mutación del RYR1 austosómica recesiva [46]. Signos clínicos y neuropatológicos de las MCN Miopatía miotubular recesiva ligada al X En 1966, Spiro et al [66] describieron una miopatía con alteraciones morfológicas musculares similares a la etapa miotubular del desarrollo embrionario muscular. Fardeau restringió esta denominación a la forma recesiva ligada al X (XLMTM) que afecta a pacientes de sexo masculino [1]. Los niños con XLMTM presentan hipotonía y debilidad muscular generalizada grave desde el nacimiento, casi siempre asociada a una insuficiencia respiratoria grave y dificultad de deglución grave. Con frecuencia se dan polihidroamnios, movimientos fetales disminuidos y costillas finas. La diplejía facial, la oftalmoparesia externa y la ptosis palpebral son signos muy frecuentes. El pronóstico de esta enfermedad es muy desfavorable, con fallecimiento en los pri- S58 Rev Neurol 2013; 57 (Supl 1): S53-S64
7 Miopatías meros meses de vida en la mayoría de los casos, aunque una pequeña proporción de casos muestra una forma menos grave con supervivencia hasta la niñez e incluso la edad adulta. Pocos niños alcanzan la marcha independiente y autonomía completa [67,68]. En nuestro centro neuromuscular, hemos atendido a cuatro niños con la forma menos grave de XLMTM. Todos han alcanzado la marcha independiente. Uno presentó peliosis hepática de curso letal [69]. La evolución clásica de los niños que sobreviven es la dependencia al ventilador mecánico y alimentación por gastrostomía. La histología muestra una gran proporción de fibras atróficas, núcleos centrales, disminución de actividad de la ATPasa miofibrilar y aumento de la actividad enzimática oxidativa en el centro de las fibras [70] (Fig. 3). En la microscopía electrónica, destaca escasez de miofibrillas en la periferia de las fibras, importante acumulación de mitocondrias y ausencia de miofilamentos. El estudio inmunohistoquímico permite marcar un canal de calcio de los túbulos T y el receptor de rianodina 1 (RYR1) utilizando anticuerpos específicos. La desmina se marca positiva en el núcleo y sarcolema de las fibras. Recientemente, se ha observado una tinción en collar de las fibras musculares en casos esporádicos con la forma menos grave de XLMTM [64,70,71]. En nuestro centro neuromuscular (Clínica Alemana), hemos encontrado esta alteración histopatológica en dos hermanos con XLMTM (Fig. 4). MCN relacionada con una mutación AD del gen DMN2 La MCN de herencia AD por mutación del gen DMN2 se expresan clínicamente con un espectro amplio desde formas leves del adulto hasta formas graves del lactante [64]. Sin embargo, la presentación clásica es un fenotipo leve de inicio tardío en la infancia o edad adulta temprana [64]. Existe una gran variabilidad clínica en los casos con mutación del DMN2. La presentación pediátrica se caracteriza por hipotonía y debilidad generalizada, diparesia facial, ptosis palpebral y oftalmoparesia. La biopsia muscular muestra tres alteraciones típicas como son una importante centralización e internalización nuclear, un predominio y atrofia de las fibras de tipo 1 y una disposición radial de las cadenas sarcoplásmicas con gran actividad oxidativa central [64,70]. Esta tríada histopatológica sólo se ve en las MCN por mutación del gen DNM2 [70], pero puede estar ausente en pacientes muy pequeños [72]. MCN por mutación AR del gen BIN1 Corresponden a un grupo pequeño de pacientes Figura 3. a) Biopsia muscular, tinción hematoxilina-eosina: fibras atróficas con núcleos centrales; b) Tinción NADH: aumento de la tinción en el centro de las fibras, con halo claro periférico. a Figura 4. a y b) Biopsia de ambos niños, hematoxilina-eosina: núcleos centrales en numerosas fibras; c) Biopsia del recién nacido (ATPasa 4.6) que muestra tinción en collar en varias fibras; d) Biopsia del hermano. Tinción NADH: se observa la tinción en collar en especial en las fibras más atróficas (tipo 1). a c con MCN, pero se han descrito varias formas clínicas moderadas y graves [65]. La debilidad y la atrofia muscular generalizada, la diparesia facial y la oftalmoparesia están casi siempre presentes [70]. La biopsia muscular de la MCN relacionada con el gen BIN1 muestra fibras de tipo 1 atróficas con núcleos centrales [62,70]. b b d Rev Neurol 2013; 57 (Supl 1): S53-S64 S59
8 R. Erazo-Torricelli Figura 5. a) Biopsia muscular, tinción hematoxilina-eosina: fibras con múltiples núcleos internos; b y c) Tinción COX y NADH respectivamente: defectos de tinción en fibras. Figura 6. Biopsia muscular, tinción NADH: se observa una importante atrofia de las fibras de tipo 1, un 50% más pequeñas que las de tipo 2, característico de la desproporción congénita del tipo de fibras. a b c Miopatía congénita por mutación del gen RYR1 con múltiples núcleos internos y desorganización miofibrilar Se denomina así la miopatía congénita relacionada con una mutación del gen RYR1 y se expresa clínicamente por hipotonía desde el nacimiento, debilidad muscular axial y proximal, diparesia facial, ptosis palpebral, oftalmoplejía externa, afectación respiratoria ocasional y contracturas [46]. La biopsia muscular muestra una internalización nuclear múltiple inusual asociada a extensas áreas con defecto de actividad de la ATPasa y actividad oxidativa irregular [46,62]. En uno de estos pacientes, se detectó una mutación heterocigótica del gen RYR1 y posteriormente se detectó en siete pacientes no relacionados una mutación del gen RYR1 recesiva [46]. En nuestra unidad neuromuscular (Hospital Luis Calvo Mackenna), hemos estudiado a dos hermanos con hipotonía, debilidad generalizada, diplejía facial, oftalmoparesia y trastorno de alimentación desde el período neonatal, con múltiples núcleos internos en biopsia muscular compatibles con la distrofia miotónica. En la adolescencia, una nueva biopsia muscular mostró múltiples núcleos internos más defecto de tinción con ATPasa y NADH, lo que planteó una miopatía CN con cores (Fig. 5). Miopatías con desproporción del tipo de fibras (DCTF) Las miopatías con DCTF constituyen más un síndrome que una entidad definida [73]. Se caracterizan por una importante atrofia de las fibras de tipo 1, sin otras alteraciones de la patología muscular [73]. Cuando la diferencia de tamaño entre las fibras de tipo 1 y 2 resulta modesta, se pueden incluir un S60 Rev Neurol 2013; 57 (Supl 1): S53-S64
9 Miopatías Tabla II. Diagnóstico diferencial de las miopatías congénitas (hipotonía del recién nacido y lactante). Modificado de [3]. Diferencias clínicas Diferencias de laboratorio Distrofia muscular congénita Indemnidad facial CK elevada Hiperlaxitud distal (C. VI) RM cerebro: leucodistrofia, displasia cortical Hipertrofia gemelar (α-dg) Biopsia muscular: pattern distrófico Distrofia miotónica congénita Diplejía facial Biopsia muscular: puede ser similar al MTM1 Miotonía materna Estudio genético de la DM1 Madre asintomática Miopatías metabólicas Visceromegalia Lactato, amonio o ácidos orgánicos elevados Cardiomegalia (Pompe) Resonancia cerebral anormal Biopsia muscular: depósito glicógeno, lípidos Fibras rojas rasgadas o COX(-) (mitocondrial) Síndromes miasténicos congénitos Ptosis, oftalmoplejía Estimulación repetitiva: EMG de fibra única Debilidad musculatura bulbar Anticuerpos anti-r acetilcolina maternos Paresia facial Atrofia muscular espinal Hipotonía grave, arreflexia EMG con denervación Indemnidad facial Test del gen SMN1 Fasciculaciones linguales Neuropatía hipomielinizante congénita Alteraciones sensitivas EMG: denervación VCN enlentecida Biopsia de nervio Síndrome de Prader-Willi Hipotonía grave (predominio axial) Test de metilación del cromosoma 15 Ojos almendrados, manos/pies pequeños Trastornos bulbares (deglución) considerable número de patologías centrales y periféricas [73]. En 1973, Brooke describió la desproporción del tipo de fibras como entidad independiente [74]. El hallazgo posterior de múltiples patologías centrales, metabólicas y periféricas extendió el concepto de DCTF como hallazgo inespecífico [75]. Sin embargo, hay pacientes con DCTF y mutaciones genéticas identificadas que mantienen sus características patológicas a través del tiempo, lo que apoya su denominación como entidad clínica independiente y explica el consenso actual existente respecto a su validación como miopatías congénitas DCTF [76]. Aunque se considera la DCTF como una miopatía de segundo orden por no ser específica [73], se han definido elementos para hacer posible su diagnóstico. Así, debe existir clínica categórica de miopatía y en la biopsia deben observarse fibras de tipo 1 al menos un 35-40% más pequeñas que las de tipo 2 [73] (Fig. 6). En estos pacientes, se han encontrado mutaciones genéticas específicas [73]. Hay varias mutaciones relacionadas con la miopatía por desproporción del tipo de fibras que en orden de frecuencia son de los genes TPM3, RYR1 y ACTA1 [73]. Diagnóstico diferencial de las miopatías congénitas El diagnóstico de las miopatías congénitas se apoya de modo importante en los signos clínicos [77]. La histopatología es fundamental para la confirmación diagnóstica y también el estudio genético. La imagenología muscular es de gran ayuda para diferenciar las miopatías congénitas [78]. El diagnóstico diferencial se basa fundamentalmente en el descarte de cuadros expresados por hipotonía (Tabla II) [79,80]. La miopatía nemalínica presenta diplejía facial y paladar ojival. El sello clínico de la miopatía centronuclear (DMN2) es la oftalmoplejía externa. Cuando la cefaloparesia es muy grave después del año de vida hay que considerar la distrofia muscular congénita head-drop por mutación del gen LMNA [81]. La miopatía central core no presenta diparesia facial y se asocia con luxación de caderas, escoliosis y contracturas. Debe diferenciarse de las distrofias musculares congénitas [80,82]. La presencia de polihidroamnios y movimientos fetales disminuidos predice una enfermedad neuromuscular grave como la miopatía nemalínica, la distrofia miotónica neonatal y, en recién nacidos varones, la miopatía miotubular (XLMTM) [80]. Los cuadros neonatales gra- Rev Neurol 2013; 57 (Supl 1): S53-S64 S61
10 R. Erazo-Torricelli ves o rápidamente progresivos del lactante obligan a descartar una miopatía mitocondrial por depleción del ADNmt, en especial por mutación en la timidincinasa 2 (TK2) [83]. Conclusiones Las miopatías congénitas constituyen un grupo heterogéneo clinicopatológico de entidades no progresivas o de progresión lenta cuyo diagnóstico se basa fundamentalmente en la clínica y el estudio histopatológico y genético. En la última década, se han hecho enormes progresos en la identificación genética de las diversas miopatías, aunque aún hay varios cuadros no bien definidos y no asociados a ninguna mutación genética conocida. El diagnóstico certero de las miopatías estructurales congénitas permite establecer pronóstico y estrategia de manejo/rehabilitación adecuados y posibilita la elaboración de un consejo genético eficaz, para lo que es indispensable el diagnóstico precoz. La tarea actual es continuar avanzando en el conocimiento de las miopatías congénitas para lograr terapias eficaces en el futuro. Bibliografía 1. Sewry CA. Pathological defects in congenital myopathies. J Muscle Res Cell Motil 2008; 29: Goebel. HH. Congenital myopathies. Introduction. Semin Pediatr Neurol 2011; 18: North KN. Clinical approach to congenital myopathies. Semin Pediatr Neurol 2011; 18: Nance JR, Dowling JJ, Gibbs EM, Bönnemann CG. Congenital myopathies: an update. Curr Neurol Neurosci Rep 2012; 12: Fardeau M, Tome FMS. Congenital myopathies. In Engel AG, Franzini-Armstrong C, eds. Myology. 3 ed. New York: McGraw- Hill; p Taratuto AL. Congenital myopathies and related disorders. Curr Opin Neurol 2002; 15: North KN. What is new in congenital myopathies? Neuromuscul Disord 2008; 18: Lake BD, Wilson J. Zebra body myopathy. Clinical, histochemical and ultraestructural studies. J Neurol Sci 1975; 24: Gonatas NK. The fine structure of the rod-like bodies in nemaline myopathy and their relation to the Z-discs. J Neuropathol Exp Neurol 1966; 25: Shy GM, Engel WK, Somers JE, Wanco T. Nemaline myopathy. A new congenital myopathy. Brain 1963; 86: Ilkovski B, Cooper ST, Nowak K, Ryan MM, Yang N, Schnei CH, et al. Nemaline myopathy caused by mutations in the muscle alpha-skeletal-actin gen. Am J Hum Genet 2001; 68: Yamaguchi M, Robson RM, Stromer MH, Dahl DS, Oda T. Nemaline myopathy rod bodies. Structure and composition. J Neurol Sci 1986; 56: Goebel HH, Warlo I. Nemaline myopathy with intranuclear rods-intranuclear rod myopathy. Neuromuscul Disord 1997; 7: Romero NR, Lehtokari VL, Quijano-Roy S, Monnier N, Claeys KG, Carlier LY, et al. Rod-core myopathy caused by mutations in the nebulin gene. Neurology 2009; 73: Wallgren-Pettersson C, Sewry CA, Nowak KJ, Laing NG. Nemaline myopathies. Semin Pediatr Neurol 2011; 18: Wallgren-Pettersson C, Pelin K, Nowak KJ, Muntoni F, Romero NB, Goebel HH, et al. Genotype-phenotype correlations in nemaline myopathy caused by mutations in the genes for nebulin and skeletal muscle α-actin. Neuromuscul Disord 2004; 14: Ryan MM, Schnell C, Strickland CD, Schield LK, Ianaccone S, Laing NG, et al. Nemaline myopathy: a clinical study of 143 patients. Ann Neurol 2001; 50: Chahin N, Selcen D, Engel AG. Sporadic late-onset nemaline myopathy. Neurology 2005; 65: Tan P, Briner J, Boltshauser E, Davis MR, Wilton SD, North K, et al. Homozygosity for a nonsense mutation in the alphatropomyosin slow gene TPM3 in a patient with severe infantile nemaline myopathy. Neuromuscul Disord 1999; 9: Clarke NF, Kolski H, Dye DE, Lim E, Smith RL, Patel R, et al. Mutations in TPM3 are a common cause of congenital fiber type disproportion. Ann Neurol 2008; 63: Lehtokari VL, Pelin K, Sandbacka M, Ranta S, Donner K, Muntoni F, et al. Identification of 45 novel mutations in the nebulin gene associated with autosomal recessive nemaline myopathy. Hum Mutat 2006; 27: Wallgren-Pettersson C, Lehtokari VL, Kalimo H, Paetau A, Nuutinen E, Hackman P, et al. Distal myopathy caused by homozygous missense mutations in the nebulin gene. Brain 2007; 130: Lehtokari VL, Pelin K, Herzegfalvi A, Karcagi V, Pouget J, Franques J, et al. Nemaline myopathy caused by mutations in the nebulin gen may present as a distal myopathy. Neuromuscul Disord 2011; 8: Laing NG, Dye DE, Wallgren-Pettersson C, Richard G, Monnier N, Lillis S, et al. Mutations and polymorphisms of the skeletal muscle alpha-actin gene (ACTA1). Hum Mutat 2009; 30: Sewry CA, Holton J, Dick DJ, Jacques T, Muntoni F, Hanna M, et al. Zebra body myopathy resolved. Neuromuscul Disord 2009; 19: Nowak KJ, Sewry CA, Navarro C, Squier W, Reina C, Ricoy JR, et al. Nemaline myopathy caused by absence of alpha-skeletal muscle actin. Ann Neurol 2007; 61: Donner K, Ollikainen M, Ridanpaa M, Christen HJ, Goebel HH, De Viser M, et al. Mutations in the β-tropomiosyn (TPM2) gene a rare cause of nemaline myopathy. Neuromuscul Disord 2002; 12: Sung SS, Brassington AM, Grannatt K, Rutherford A, Whitby FG, Krakoviak PA, et al. Mutations in genes encoding fast-twitch contractile proteins cause distal arthrogryposis syndromes. Am J Hum Genet 2003; 72: Tajsharghi H, Ohlsson M, Lindberg C, Oldfors A. Congenital myopathy with nemaline rods and cap structures caused by a mutation in the β-tropomyosin gene (TPM2). Arch Neurol 2007; 64: Tajsharghi H, Ohlsson M, Lindberg C, Oldfors A. Myopathies associated with tropomyosin mutations. Neuromuscul Disord 2012; 11: Johnston JJ, Kelley RI, Crawford TO, Morton DH, Agarwala R, Koch T, et al. A novel nemaline myopathy in the Amish caused by a mutation in troponin. Am J Hum Genet 2000; 67: Sambuughin N, Yau KS, Olivé M, Duff RM, Bayarsaikhan M, Lu S, et al. Dominant mutations in KBTBD13, a member of the BTB/Kelch family, cause nemaline myopathy with cores. Am J Hum Genet 2010; 87: Agrawal PB, Greenleaf RS, Lehtokari VL, Wallgren-Pettersson C, Wallefeld W, Laing G, et al. Nemaline myopathy with minicores caused by mutation of the CFL2 gene encoding the skeletal muscle acting-binding proteins, cofilin 2. Am J Hum Genet 2007; 80: Jungbluth H. Multi-minicore disease. Orphanet J Rare Dis 2007; 2: 31. S62 Rev Neurol 2013; 57 (Supl 1): S53-S64
11 Miopatías 35. Jungbluth H. Central core disease. Orphanet J Rare Dis 2007; 2: Magee KR, Shy GM. A new congenital non-progressive myopathy. Brain 1956; 79: Dubowitz V, Pearse AG. Oxidative enzime and phosphorilase in central core disease of muscle. Lancet 1960; 2: Zhang I, Chen Hs, Kanna VK, De Leon S, Phillips MS, Schappert K, et al. A mutation in the human ryanodine receptor gen associated with central core disease. Nat Genet 1993; 5: Ferreiro A, Quijano-Roy S, Pichereau C, Moghadaszadeh B, Goemans N, Bonnemann C, et al. Mutations of the selenoprotein N gen which is implicated in rigid spine muscular dystrophy, cause the classical phenotype of multiminicore disease: reassessing the nosology of early-onset myopathy. Am J Hum Genet 2002; 71: Dubowitz V. Muscle disorders in childhood. 2 ed. London: W.B. Saunders; Romero NB, Monnier N, Viollet L Cortey A, Chevallay M, LeRoy JP, et al. Dominant and recessive central core disease associated with RYR1 mutations and fetal akinesia. Brain 2003; 126: Hernández-Lain A, Husson I, Monnier N, Farnoux G, Brochere C, Lacene E, et al. De novo RYR1 heterozigous mutation (14898T) causing letal core-rod myopathy in twins. Eur J Med Genet 2011; 54: Wu S, Ibarra MC, Malicdan MC, Murayama K, Ichihara Y, Kikuchi H, et al. Central core disease is due to RYR1 mutations in more than 90% of patients. Brain 2006; 129: Denborough MA, Dennett X, Anderson RM. Central core disease and malignant hyperpyrexia. BMJ 1973; 1: Shuaib A, Paasuke RT, Brownell KW. Central core disease. Clinical features in 13 patients. Medicine (Baltimore) 1987; 66: Bevilacqua JA, Monnier N, Bitoun M, Eymard B Ferreiro A, Monges S, et al. Recessive RYR1 mutations cause unusual congenital myopathy with prominent nuclear internalization and large areas of myofibrillar disorganization. Neuropathol Appl Neurobiol 2011; 37: Tilgen N, Zorzato F, Halliger-Keller B, Muntoni F, Sewry C, Palmucci LM, et al. Identification of four novel mutations in the C-terminal spanning domain of the ryanodine receptor 1: association with central core disease and alteration of calcium homeostasis. Hum Mol Genet 2001; 10: Wilmshurst JM, Lillis S, Zhou H, Pillay K, Henderson H, Kress W, et al. RYR1 mutations are a common cause of congenital myopathies with central nuclei. Ann Neurol 2010; 68: Clarke NF, Waddell LB, Cooper ST, Perry M, Smith RL, Komberg AJ, et al. Recessive mutations in RYR1 are a common cause of congenital fiber type disproportion. Hum Mutat 2010; 31: E Jungbluth N, Sewry C, Muntoni F. Core myopathies. Semin Pediatr Neurol 2011; 18: Jungbluth N, Zhou H, Hartley L, Halliger-Keller B, Messina S, Longman C, et al. Minicore myopathy with ophthalmoplegia caused by mutations in the ryanodine receptor type 1 gene. Neurology 2005; 65: Bethlem J, Van Gool J, Hulsmann WC, Meijer AE. Familial non-progressive myopathy with muscle cramps after exercise. A new disease associated with cores in the muscle fibres. Brain 1966; 89: D Arcy CE, Bjorksten A, Yiu EM, Bankier A, Gillies R, McLead CA, et al. King-Demborough caused by a novel mutation in the ryanodine receptor gene. Neurology 2008; 71: Dowling JJ, Lillis S, Amburgey K, Zhou H, Al-Sarraj S, Buk SJ, et al. King-Demborough syndrome with and without mutations in the skeletal muscle ryanodine receptor (RYR1) gene. Neuromuscul Disord 2011; 21: Ferreiro A, Stournet B, Chateau D, Romero NB Laroche C, Odent S, et al. Multi-minicore disease searching for boundaries: phenotype analysis of 38 cases. Ann Neurol 2000; 48: Jungbluth H, Sewry C, Brown SC, Manzur AY, Mercuri E, Bushby, et al. Mini-core myopathy in children: a clinical and histopathological study of 19 cases. Neuromuscul Disord 2000; 10: D Amico A, Haliloglu G, Richard P, Talim B, Maugenre S, Ferreiro A, et al. Two patients with dropp head syndrome due to mutations in LMNA or SEPN1 genes. Neuromuscul Disord 2005; 15: Rowe PW, Eagle M, Pollit C, Bullock RE, Bushby KM. Multicore myopathy: respiratory failure and paraespinal muscle contractures are important complications. Dev Med Child Neurol 2000; 42: Tosch V, Vasli N, Krets C, Nicot AS, Gasnier C, Dondaine N, et al. Novel molecular diagnostic approaches for X-linked centronuclear (myotubular) myopathy reveal intronic mutations. Neuromuscul Disord 2010; 20: Dubowitz V, Sewry CA. Muscle biopsy: a practical approach. 3 ed. London: W.B. Saunders; Sewry CA, Muller C, Davis M, Dwyer JS, Dove J, Evans G, et al. The spectrum of pathology in central core disease. Neuromuscul Disord 2002; 12: Romero NB, Bitoun M. Centronuclear myopathies. Semin Pediat Neurol 2011; 18: Laporte J, Hu IJ,Krets C, Mandel JL, Kioschis P, Cov JF, et al. A gene mutated in a X-linked myotubular myopathy defines a new putative tyrosine phosphatase family conserved in yeast. Nat Genet 1996; 13: Bitoun M, Mangenre S, Jeannet PY, Lacen E, Ferrer X, Laforet P, et al. Mutations in dynamin 2 causes dominant centronuclear myopathy. Nat Genet 2005; 37: Nicot AS, Toussaint A, Tosch B, Kretz M, Wallgren-Petersson E, Iwarsson E, et al. Mutations in anphiphysin2 (BIN1) disrupt interaction with dynamin 2 and causes a dominant centro - nuclear myopathy. Nat Genet 2007; 39: Spiro AJ, Shy GM, Gonatas NK. Myotubular myopathy. Persistence of fetal muscle in an adolescent boy. Arch Neurol 1966; 14: Biancalana V, Caron O, Gallati S, Baas F, Kress W, Novelli G. Characterization of mutations in 77 patients with X-linked myotubular myopathy including a family with very mild phenotype. Hum Genet 2003; 112: Chanzy S, Routon MC, Moretti S, De Genes C, Mselati JC. Unusual good prognosis for X-linked myotubular myopathy. Arch Pediatr 2003; 10: Karger B, Varchmin-Schultheiss K, Fechner G. Fatal hepatic haemorrhage in a child peliosis hepatitis versus maltreatment. Int J Legal Med 2005; 119: Romero NB. Centronuclear myopathies: a widening concept. Neuromuscul Disord 2010; 20: Bevilacqua JA, Bitoun M, Biancalana V, Oldfors A, Stoltenburg G, Claeys KG, et al. Necklace fibers, a new histological marker of late-onset MTM1-related centronuclear myopathy. Acta Neuropathol 2009; 117: Bitoun M, Bevilacqua JA, Eymard B, Prudhon B, Fardeau M, Guicheney P, et al. New centronuclear myopathy due to a novel dynamin 2 mutation. Neurology 2009; 72: Clarke NF. Congenital fiber-type disproportion. Semin Pediatr Neurol 2011; 18: Brooke MH, Engel WK. The histographic analysis of human muscle with regard to fiber types. 4. Children s biopsies. Neurology 1969; 19: Dubowitz V. Congenital fibre type disproportion: a pathology in search of a disease. In Dubowitz V, ed. Muscle disorders of childhood. 2 ed. London: Bailliere Tindall; Clarke NF. Congenital fibre type disproportion a syndrome at the crossroads of the congenital myopathies. Neuromuscul Disord 2011; 21: Cabello A, Ricoy-Campo JR. Miopatías congénitas. Rev Neurol 2003; 37: Quijano-Roy S, Carlier RY, Fischer D. Muscle imaging in congenital myopathies. Semin Pediat Neurol 2011; 18: Alfonso I, Papazian O, Valencia P. Hipotonía neonatal generalizada. Rev Neurol 2003; 37: Rev Neurol 2013; 57 (Supl 1): S53-S64 S63
12 R. Erazo-Torricelli 80. Erazo-Torricelli R. Hipotonía neonatal. Rev Neurol 2000; 31: Quijano-Roy S, Mbieleu M, Bonnemann C, Jeannet PY, Colomer J, Clarcke LF, et al. De novo LMNA mutations cause a new form of congenital muscular dystrophy. Ann Neurol 2008; 64: Erazo-Torricelli R. Actualización en distrofias musculares. Rev Neurol 2004; 39: Oskoui M, Davidzon D, Pascual J, Erazo R, Gurgel-Giannetti J, Krisna S, et al. Clinical spectrum of mitocondrial DNA depletion due to mutation in thymidin kinase two gene. Arch Neurol 2006; 63: Structural congenital myopathies Introduction. Congenital myopathies are a heterogeneous group of diseases that share clinical early onset and specific hystopathological alterations in muscle. Genetic studies allow to determine the causative mutation in most cases. Genotypic and phenotypic heterogeneity exists, which is illustrated by noting that a genotype can be expressed in more than one clinicopathologic way and a phenotype may be caused by different genetic mutations. Development. In this review we detail the characteristics of major congenital myopathies that allow clinical, pathological and genetic identification. We describe the findings of muscle biopsy that are the mainstay diagnosis. We emphasize and detail the importance of differential diagnosis by ruling out other diseases that present with hypotonia in infancy or neonatal period. We highlight the severe neonatal forms (nemaline, X-linked myotubular) to be identified early to establish prognosis and provide appropriate genetic counseling. We emphasize mutations of ryanodine gene (RYR1) through its association with malignant hyperthermia and mutations of selenoprotein 1 (SEPN1) and nemaline by its association with nocturnal hypoventilation. Conclusions. The deep knowledge of structural congenital myopathies facilitates diagnostic confirmation of congenital myopathy, allowing the timely implementation of measures related to breathing and feeding in more severe cases and the optimization of motor function in all patients with myopathy congenital. Key words. Center core. Centronuclear. Congenital myopathies. Hypotonia. Muscle biopsy. Myotubular. Nemaline. Type 1 fiber atrophy. S64 Rev Neurol 2013; 57 (Supl 1): S53-S64
MIOPATÍAS CONGENITAS:
 MIOPATÍAS CONGENITAS: Características clínicas y mecanismos fisiopatológicos Marcos Madruga Garrido Sección de Neuropediatría Unidad Funcional Multidisciplinar de Patología Neuromuscular en la Infancia
MIOPATÍAS CONGENITAS: Características clínicas y mecanismos fisiopatológicos Marcos Madruga Garrido Sección de Neuropediatría Unidad Funcional Multidisciplinar de Patología Neuromuscular en la Infancia
Tracción desde decúbito pull to sit. Mínimo retraso a los 2 meses.
 Evaluación del lactante hipotónico Salvador Ibáñez Micó Servicio de Pediatría Hospital Santa Lucía. Cartagena Introducción Período neonatal: descartar enfermedadades sistémicas (sepsis, insuficiencia cardíaca).
Evaluación del lactante hipotónico Salvador Ibáñez Micó Servicio de Pediatría Hospital Santa Lucía. Cartagena Introducción Período neonatal: descartar enfermedadades sistémicas (sepsis, insuficiencia cardíaca).
ENFERMEDADES DE LA MOTONEURONA Y ESCLEROSIS LATERAL AMIOTROFICA
 ENFERMEDADES DE LA MOTONEURONA Y ESCLEROSIS LATERAL AMIOTROFICA Clase de neurología. Dr. Jaume Coll i Cantí UAB. 2011 ELA (ESCLEROSIS LATERAL AMIOTRÓFICA) es la más común de las enfermedades de la neurona
ENFERMEDADES DE LA MOTONEURONA Y ESCLEROSIS LATERAL AMIOTROFICA Clase de neurología. Dr. Jaume Coll i Cantí UAB. 2011 ELA (ESCLEROSIS LATERAL AMIOTRÓFICA) es la más común de las enfermedades de la neurona
HIPOTONÍA NEONATAL. Dr. Ricardo Erazo T.
 HIPOTONÍA NEONATAL Dr. Ricardo Erazo T. I. Definición. La hipotonía se define como la disminución del tono muscular en reposo y se expresa por la típica posición en rana, con marcada abducción de caderas
HIPOTONÍA NEONATAL Dr. Ricardo Erazo T. I. Definición. La hipotonía se define como la disminución del tono muscular en reposo y se expresa por la típica posición en rana, con marcada abducción de caderas
CURSO DE ACTUALIZACIÓN EN MIASTENIA GRAVIS de Febrero de 2012 Colegio Oficial de Médicos Valladolid
 CURSO DE ACTUALIZACIÓN EN MIASTENIA GRAVIS 21-22 de Febrero de 2012 Colegio Oficial de Médicos Valladolid MIASTENIA GRAVIS DIAGNÓSTICO CLÍNICO Mª Isabel Yugueros Fernández NEUROLOGÍA DIAGNÓSTICO MIASTENIA
CURSO DE ACTUALIZACIÓN EN MIASTENIA GRAVIS 21-22 de Febrero de 2012 Colegio Oficial de Médicos Valladolid MIASTENIA GRAVIS DIAGNÓSTICO CLÍNICO Mª Isabel Yugueros Fernández NEUROLOGÍA DIAGNÓSTICO MIASTENIA
GUÍA SOBRE ATROFIA MUSCULAR ESPINAL
 GUÍA SOBRE ATROFIA MUSCULAR ESPINAL Teleton 05_atrofia mus.indd 1 ÍNDICE 3... Qué es la atrofia muscular espinal? 3... Cómo se adquiere? 3... Cómo se manifiesta? 6... Cómo se realiza el diagnóstico? 7...
GUÍA SOBRE ATROFIA MUSCULAR ESPINAL Teleton 05_atrofia mus.indd 1 ÍNDICE 3... Qué es la atrofia muscular espinal? 3... Cómo se adquiere? 3... Cómo se manifiesta? 6... Cómo se realiza el diagnóstico? 7...
DIAGNOSTICO DIFERENCIALY ALGORITMO DE LAS DISTROFIAS MUSCULARES
 I CURSO DE FORMACION DE ENFERMEDADES NEUROMUSCULARES DIAGNOSTICO DIFERENCIALY ALGORITMO DE LAS DISTROFIAS MUSCULARES Dra Carmen Paradas Unidad de Enfermedades Neuromusculares Hospital U. Virgen del Rocio,
I CURSO DE FORMACION DE ENFERMEDADES NEUROMUSCULARES DIAGNOSTICO DIFERENCIALY ALGORITMO DE LAS DISTROFIAS MUSCULARES Dra Carmen Paradas Unidad de Enfermedades Neuromusculares Hospital U. Virgen del Rocio,
Lactante Hipotónico. Dra. P. López Esteban Neurofisiología Clínica. marzo de 2016
 Lactante Hipotónico Dra. P. López Esteban Neurofisiología Clínica marzo de 2016 Es realmente necesaria la electromiografía en el diagnostico de las enfermedades musculares en el momento actual? Origen
Lactante Hipotónico Dra. P. López Esteban Neurofisiología Clínica marzo de 2016 Es realmente necesaria la electromiografía en el diagnostico de las enfermedades musculares en el momento actual? Origen
Lactante Hipotónico. Dra. P. López Esteban Neurofisiología Clínica. 22 de marzo de 2012
 Lactante Hipotónico Dra. P. López Esteban Neurofisiología Clínica 22 de marzo de 2012 Es realmente necesaria la electromiografía en el diagnostico de las enfermedades musculares en el momento actual? Origen
Lactante Hipotónico Dra. P. López Esteban Neurofisiología Clínica 22 de marzo de 2012 Es realmente necesaria la electromiografía en el diagnostico de las enfermedades musculares en el momento actual? Origen
Paciente con aumento de enzimas musculares sintomáticos
 Paciente con aumento de enzimas musculares sintomáticos Dr. Andrés Nascimento Osorio Unidad de patología Neuromuscular, Servicio de Neurología. Hospital Sant Joan de Déu. U.B. Barcelona-Spain Aumento de
Paciente con aumento de enzimas musculares sintomáticos Dr. Andrés Nascimento Osorio Unidad de patología Neuromuscular, Servicio de Neurología. Hospital Sant Joan de Déu. U.B. Barcelona-Spain Aumento de
Clasificación y Definición Actual de las Miocardiopatías. Módulo Miocardiopatías SCOB 2003 Dr. A. J. Pasca
 Clasificación y Definición Actual de las Miocardiopatías Módulo Miocardiopatías SCOB 2003 Dr. A. J. Pasca Enfermedad de las proteínas contráctiles del sarcómero Thierfelder, Cell 1994 INCIDENCIA 0.2%
Clasificación y Definición Actual de las Miocardiopatías Módulo Miocardiopatías SCOB 2003 Dr. A. J. Pasca Enfermedad de las proteínas contráctiles del sarcómero Thierfelder, Cell 1994 INCIDENCIA 0.2%
EXPLORACION NEUROFISIOLOGICA DEL LACTANTE HIPOTONICO. Dra. P. López Esteban Neurofisiología Clínica
 EXPLORACION NEUROFISIOLOGICA DEL LACTANTE HIPOTONICO Neurofisiología Clínica Es realmente necesaria la electromigrafía en el diagnostico de las enfermedades musculares en el momento actual?? Origen Periférico
EXPLORACION NEUROFISIOLOGICA DEL LACTANTE HIPOTONICO Neurofisiología Clínica Es realmente necesaria la electromigrafía en el diagnostico de las enfermedades musculares en el momento actual?? Origen Periférico
Hipotonía en el recién nacido
 Hipotonía en el recién nacido García Díaz MF, García González V, LombrañaÁlvarez E, García Mozo R, García GarcíaE, Moreno Pavón B. Sº de Pediatría, Hospital de Cabueñes, Gijón Caso clínico RN mujer, sin
Hipotonía en el recién nacido García Díaz MF, García González V, LombrañaÁlvarez E, García Mozo R, García GarcíaE, Moreno Pavón B. Sº de Pediatría, Hospital de Cabueñes, Gijón Caso clínico RN mujer, sin
Utilidad de la resonancia magnética en el diagnóstico de las enfermedades musculares hereditarias
 Utilidad de la resonancia magnética en el diagnóstico de las enfermedades musculares hereditarias Dres. Jorge Díaz J (1)., Lionel Suazo R (1)., Claudia Castiglioni T (2)., Jorge A. Bevilacqua R (3). 1.
Utilidad de la resonancia magnética en el diagnóstico de las enfermedades musculares hereditarias Dres. Jorge Díaz J (1)., Lionel Suazo R (1)., Claudia Castiglioni T (2)., Jorge A. Bevilacqua R (3). 1.
Esclerosis lateral amiotrófica i maneig multidisciplinar
 Esclerosis lateral amiotrófica i maneig multidisciplinar M.A. Rubio Servicio de Neurología. Hospital del Mar. Parc de Salut Mar Mayo 2017 180 160 140 120 100 80 60 40 20 0 Lou Gehrig's Runs diagnosis
Esclerosis lateral amiotrófica i maneig multidisciplinar M.A. Rubio Servicio de Neurología. Hospital del Mar. Parc de Salut Mar Mayo 2017 180 160 140 120 100 80 60 40 20 0 Lou Gehrig's Runs diagnosis
Patología de la unión neuromuscular y del músculo estriado. Juan de Dios Arrebola Benítez Medicina Interna
 Patología de la unión neuromuscular y del músculo estriado Juan de Dios Arrebola Benítez Medicina Interna Distribución de los tejidos corporales en el adulto Funciones del músculo estriado Mantenimiento
Patología de la unión neuromuscular y del músculo estriado Juan de Dios Arrebola Benítez Medicina Interna Distribución de los tejidos corporales en el adulto Funciones del músculo estriado Mantenimiento
Técnicas de Histoquímica e Inmunohistoquímica. en Patología Neuromuscular: utilidad. diagnóstica
 Técnicas de Histoquímica e Inmunohistoquímica en Patología Neuromuscular: utilidad diagnóstica Soraya Barrera Cabañeros ( TEAP) Servicio de Anatomía Patológica y Neuropatología. Hospital Meixoeiro Complexo
Técnicas de Histoquímica e Inmunohistoquímica en Patología Neuromuscular: utilidad diagnóstica Soraya Barrera Cabañeros ( TEAP) Servicio de Anatomía Patológica y Neuropatología. Hospital Meixoeiro Complexo
26 1. FACTORES QUE MODIFICAN LOS PATRONES DE HERENCIA MONOGENICA
 Tema 26 1. FACTORES QUE MODIFICAN LOS PATRONES DE HERENCIA MONOGENICA Heterogeneidad alélica y/o de locus Penetrancia incompleta Expresividad Variable Anticipación Sello genómico Pleiotropía Mutaciones
Tema 26 1. FACTORES QUE MODIFICAN LOS PATRONES DE HERENCIA MONOGENICA Heterogeneidad alélica y/o de locus Penetrancia incompleta Expresividad Variable Anticipación Sello genómico Pleiotropía Mutaciones
DISTROFIAS MUSCULARES
 Las distrofias musculares son enfermedades genéticas que causan debilidad y degeneración progresiva del músculo. La palabra distrofia viene del griego dis que significa difícil o defectuoso y trof de nutrición.
Las distrofias musculares son enfermedades genéticas que causan debilidad y degeneración progresiva del músculo. La palabra distrofia viene del griego dis que significa difícil o defectuoso y trof de nutrición.
CASOS CLÍNICOS PARA DIFERENCIAR EL SISTEMA NERVIOSO CENTRAL DEL PERIFÉRICO
 CASOS CLÍNICOS PARA DIFERENCIAR EL SISTEMA NERVIOSO CENTRAL DEL PERIFÉRICO Daniel Sanchez Masian Neurology/Neurosurgery Unit Animal Health Trust Lanwades Park, Kentford Newmarket, Suffolk CB8 7UU Las enfermedades
CASOS CLÍNICOS PARA DIFERENCIAR EL SISTEMA NERVIOSO CENTRAL DEL PERIFÉRICO Daniel Sanchez Masian Neurology/Neurosurgery Unit Animal Health Trust Lanwades Park, Kentford Newmarket, Suffolk CB8 7UU Las enfermedades
Ataxias. Jorge Luis Palacios Espichán MIR 3 Análisis Clínicos. XX JORNADA de FORMACIÓN INTERHOSPITALARIA del LABORATORIO CLÍNICO
 XX JORNADA de FORMACIÓN INTERHOSPITALARIA del LABORATORIO CLÍNICO LABORATORIO CLÍNICO EN EL DIAGNÓSTICO DE LAS ENFERMEDADES NEUROLÓGICAS Ataxias Jorge Luis Palacios Espichán MIR 3 Análisis Clínicos Ataxia
XX JORNADA de FORMACIÓN INTERHOSPITALARIA del LABORATORIO CLÍNICO LABORATORIO CLÍNICO EN EL DIAGNÓSTICO DE LAS ENFERMEDADES NEUROLÓGICAS Ataxias Jorge Luis Palacios Espichán MIR 3 Análisis Clínicos Ataxia
CONTRIBUCIÓN DE LA ANATOMÍA PATOLÓGICA AL DIAGNÓSTICO DE LAS ENFERMEDADES MUSCULARES
 CONTRIBUCIÓN DE LA ANATOMÍA PATOLÓGICA AL DIAGNÓSTICO DE LAS ENFERMEDADES MUSCULARES IX Curso de Enfermedades Musculares en la Infancia y Adolescencia Mercedes García Villanueva Servicio de Anatomía Patológica
CONTRIBUCIÓN DE LA ANATOMÍA PATOLÓGICA AL DIAGNÓSTICO DE LAS ENFERMEDADES MUSCULARES IX Curso de Enfermedades Musculares en la Infancia y Adolescencia Mercedes García Villanueva Servicio de Anatomía Patológica
I CURSO DE FORMACION EN ENFERMEDADES NEUROMUSCULARES PRUEBAS DIAGNÓSTICAS. CUÁL Y PARA QUÉ.
 I CURSO DE FORMACION EN ENFERMEDADES NEUROMUSCULARES PRUEBAS DIAGNÓSTICAS. CUÁL Y PARA QUÉ. Dr. Jordi Díaz Manera Unidad de Enfermedades Neuromusculares Servicio de Neurología Hospital de la Santa Creu
I CURSO DE FORMACION EN ENFERMEDADES NEUROMUSCULARES PRUEBAS DIAGNÓSTICAS. CUÁL Y PARA QUÉ. Dr. Jordi Díaz Manera Unidad de Enfermedades Neuromusculares Servicio de Neurología Hospital de la Santa Creu
30 SEP Día Mundial de la Distrofia Muscular de Cinturas (LGMD) Qué es la Distrofia Muscular de Cinturas (LGMD)?
 30 SEP Día Mundial de la Distrofia Muscular de Cinturas (LGMD) Qué es la Distrofia Muscular de Cinturas (LGMD)? Un término usado para un GRUPO de enfermedades neuromusculares raras que se heredan y causan
30 SEP Día Mundial de la Distrofia Muscular de Cinturas (LGMD) Qué es la Distrofia Muscular de Cinturas (LGMD)? Un término usado para un GRUPO de enfermedades neuromusculares raras que se heredan y causan
Indice General. Introducción. Capítulo 1. - Parte 1. - PROCESOS MÉDICOS CRONICOS
 Indice General Capítulo 1. - Introducción 17 Parte 1. - PROCESOS MÉDICOS CRONICOS Capítulo 2. - Artritis reumaloide j uvenil Signos y síntomas. Diagnóstico diferencial Estudios de laboratorio Curso Conducta
Indice General Capítulo 1. - Introducción 17 Parte 1. - PROCESOS MÉDICOS CRONICOS Capítulo 2. - Artritis reumaloide j uvenil Signos y síntomas. Diagnóstico diferencial Estudios de laboratorio Curso Conducta
DISCAPACIDADES DE ETIOLOGIA GENETICA: PROYECCIONES DE ATENCION INTEGRAL. Prof. Dra. Aracely Lantigua Cruz CUBA 2004
 DISCAPACIDADES DE ETIOLOGIA GENETICA: PROYECCIONES DE ATENCION INTEGRAL Prof. Dra. Aracely Lantigua Cruz CUBA 2004 GENOMA HUMANO 30 000 A 50 000 GENES NUCLEARES Y EL ADN MITOCONDRIAL. MUTACIONES DE ESTOS
DISCAPACIDADES DE ETIOLOGIA GENETICA: PROYECCIONES DE ATENCION INTEGRAL Prof. Dra. Aracely Lantigua Cruz CUBA 2004 GENOMA HUMANO 30 000 A 50 000 GENES NUCLEARES Y EL ADN MITOCONDRIAL. MUTACIONES DE ESTOS
Consideraciones genéticas en la enfermedad de Fabry. Dra. Mónica López Rodríguez Servicio Medicina Interna
 Consideraciones genéticas en la enfermedad de Fabry Dra. Mónica López Rodríguez Servicio Medicina Interna 1 DEFINICIÓN GENÉTICA La Genética es el estudio de la herencia, el proceso en el cual un padre
Consideraciones genéticas en la enfermedad de Fabry Dra. Mónica López Rodríguez Servicio Medicina Interna 1 DEFINICIÓN GENÉTICA La Genética es el estudio de la herencia, el proceso en el cual un padre
1 Congreso Argentino de Medicina Interna Pediátrica
 1 Congreso Argentino de Medicina Interna Pediátrica Hospital pediátrico de alta complejidad. 3 nivel de atención. Atiende pacientes de todo el país y países limítrofes. 9 salas de internación con entre
1 Congreso Argentino de Medicina Interna Pediátrica Hospital pediátrico de alta complejidad. 3 nivel de atención. Atiende pacientes de todo el país y países limítrofes. 9 salas de internación con entre
Recomendaciones para anestesia en pacientes afectados por Miopatía distal de Welander
 orphananesthesia Recomendaciones para anestesia en pacientes afectados por Miopatía distal de Welander Nombre de la enfermedad: miopatía distal de Welander CIE 10: G71.0 Sinónimos: miopatía distal tipo
orphananesthesia Recomendaciones para anestesia en pacientes afectados por Miopatía distal de Welander Nombre de la enfermedad: miopatía distal de Welander CIE 10: G71.0 Sinónimos: miopatía distal tipo
Síndrome periódico asociado a la criopirina (CAPS)
 www.printo.it/pediatric-rheumatology/ar/intro Síndrome periódico asociado a la criopirina (CAPS) Versión de 2016 1. QUÉ SON LOS CAPS 1.1 En qué consiste? El síndrome periódico asociado a la criopirina
www.printo.it/pediatric-rheumatology/ar/intro Síndrome periódico asociado a la criopirina (CAPS) Versión de 2016 1. QUÉ SON LOS CAPS 1.1 En qué consiste? El síndrome periódico asociado a la criopirina
Función pulmonar en pacientes con Disquinesia Ciliar Primaria (DCP)
 Función pulmonar en pacientes con Disquinesia Ciliar Primaria (DCP) Dr Sergio Scigliano Centro Respiratorio Hospital de Niños Ricardo Gutiérrez Buenos Aires, Argentina sergioscigliano@gmail.com Disquinesia
Función pulmonar en pacientes con Disquinesia Ciliar Primaria (DCP) Dr Sergio Scigliano Centro Respiratorio Hospital de Niños Ricardo Gutiérrez Buenos Aires, Argentina sergioscigliano@gmail.com Disquinesia
CURSO DE ENTRENADOR NACIONAL DE CLUB
 CURSO DE ENTRENADOR NACIONAL DE CLUB Área de ciencias biológicas: Fisiología Tema 3: Fisiología Muscular Profesora Lic. CCAFyD Prudencia Guerrero Cruz Máster en Educación Física y salud Máster en Alto
CURSO DE ENTRENADOR NACIONAL DE CLUB Área de ciencias biológicas: Fisiología Tema 3: Fisiología Muscular Profesora Lic. CCAFyD Prudencia Guerrero Cruz Máster en Educación Física y salud Máster en Alto
Fisiología y Envejecimiento Sistema muscular
 Tema 7 * Clasificación. * Funciones. * Anatomofisiología del músculo esquelético. * Mecanismo general de la contracción muscular. 1 Clasificación Los músculos se pueden clasificar según 3 criterios: 1.
Tema 7 * Clasificación. * Funciones. * Anatomofisiología del músculo esquelético. * Mecanismo general de la contracción muscular. 1 Clasificación Los músculos se pueden clasificar según 3 criterios: 1.
Fisiología del Músculo. Dr. Ricardo Curcó
 Fisiología del Músculo Dr. Ricardo Curcó Músculo Estriado Liso Esquelético Cardíaco Músculo Liso Músculo esquelético Es el músculo bajo control voluntario. Cada fibra muscular se encuentra inervado por
Fisiología del Músculo Dr. Ricardo Curcó Músculo Estriado Liso Esquelético Cardíaco Músculo Liso Músculo esquelético Es el músculo bajo control voluntario. Cada fibra muscular se encuentra inervado por
Escuela Universitaria de Tecnología Médica - Escuela de Parteras Facultad de Medicina Universidad de la República. UTI Biología Celular y Tisular
 Escuela Universitaria de Tecnología Médica - Escuela de Parteras Facultad de Medicina Universidad de la República UTI Biología Celular y Tisular Tejido Muscular Lic. Valentina Lagos Departamento de Histología
Escuela Universitaria de Tecnología Médica - Escuela de Parteras Facultad de Medicina Universidad de la República UTI Biología Celular y Tisular Tejido Muscular Lic. Valentina Lagos Departamento de Histología
Síndromes de denervación muscular en el hombro. Hallazgos en RM.
 Síndromes de denervación muscular en el hombro. Hallazgos en RM. Juan Félix Molina Granados, Jaume Pomés Tallo*, Esther Domínguez Franjo, Xavier Tomás Batlle*, Monserrat del Amo Conill*. Unidad Central
Síndromes de denervación muscular en el hombro. Hallazgos en RM. Juan Félix Molina Granados, Jaume Pomés Tallo*, Esther Domínguez Franjo, Xavier Tomás Batlle*, Monserrat del Amo Conill*. Unidad Central
Avances genéticos en las distrofinopatias. Jesús Molano Unidad de Genética Molecular INGEMM Hospital Universitario La Paz Madrid
 Avances genéticos en las distrofinopatias Jesús Molano Unidad de Genética Molecular INGEMM Hospital Universitario La Paz Madrid Distrofias musculares hereditarias Definición: Grupo de enfermedades hereditarias
Avances genéticos en las distrofinopatias Jesús Molano Unidad de Genética Molecular INGEMM Hospital Universitario La Paz Madrid Distrofias musculares hereditarias Definición: Grupo de enfermedades hereditarias
SÍNDROME DE RETT EN ESPAÑA: ANÁLISIS DE MUTACIONES Y CORRELACIONES CLÍNICAS
 SÍNDROME DE RETT EN ESPAÑA: ANÁLISIS DE MUTACIONES Y CORRELACIONES CLÍNICAS E. Monrós, J. Armstrong, E. Aibar, P. Poo, I. Canós y M. Pineda Sección de Genética y Servicio de Neurología. Hospital Sant Joan
SÍNDROME DE RETT EN ESPAÑA: ANÁLISIS DE MUTACIONES Y CORRELACIONES CLÍNICAS E. Monrós, J. Armstrong, E. Aibar, P. Poo, I. Canós y M. Pineda Sección de Genética y Servicio de Neurología. Hospital Sant Joan
 Página 1 de 5 ISBN: 978-84-692-76778 COMUNICACIONES Nº 1843. Gastritis colágena: presentación de un caso Ayman Gaafar [1], Leire Andrés [1], Giovanni de Petris [2], José Ignacio López [1] (1) Servicio
Página 1 de 5 ISBN: 978-84-692-76778 COMUNICACIONES Nº 1843. Gastritis colágena: presentación de un caso Ayman Gaafar [1], Leire Andrés [1], Giovanni de Petris [2], José Ignacio López [1] (1) Servicio
PICADILLO CLINICA MEDICA A
 PICADILLO CLINICA MEDICA A HISTORIA CLÍNICA n Un hombre de 61 años es evaluado por una historia de 10 meses de debilidad generalizada. n No presenta mialgia ni otro Ipo de dolor. n Su antecedente personal
PICADILLO CLINICA MEDICA A HISTORIA CLÍNICA n Un hombre de 61 años es evaluado por una historia de 10 meses de debilidad generalizada. n No presenta mialgia ni otro Ipo de dolor. n Su antecedente personal
Síndrome de Sjögren en pediatría: diagnóstico y manejo
 María del Pilar Gómez, Juan Pablo Rojas Síndrome de Sjögren en pediatría: diagnóstico y manejo R E P O R T E D E C A S O Síndrome de Sjögren en pediatría: diagnóstico y manejo Sjögren's syndrome in children:
María del Pilar Gómez, Juan Pablo Rojas Síndrome de Sjögren en pediatría: diagnóstico y manejo R E P O R T E D E C A S O Síndrome de Sjögren en pediatría: diagnóstico y manejo Sjögren's syndrome in children:
Diagnóstico de ELA. Lucía Galán Dávila Unidad de ELA Hospital Clínico San Carlos Madrid
 Diagnóstico de ELA Lucía Galán Dávila Unidad de ELA Hospital Clínico San Carlos Madrid La Esclerosis Lateral Amiotrófica es una enfermedad neurodegenerativa rápidamente progresiva que afecta predominantemente
Diagnóstico de ELA Lucía Galán Dávila Unidad de ELA Hospital Clínico San Carlos Madrid La Esclerosis Lateral Amiotrófica es una enfermedad neurodegenerativa rápidamente progresiva que afecta predominantemente
Esclerosis Múltiple. Enfermedad autoinmune dirigida contra componentes de la mielina - glucoproteína mielínica - proteína básica mielina
 Esclerosis Múltiple Esclerosis Múltiple Enfermedad autoinmune dirigida contra componentes de la mielina - glucoproteína mielínica - proteína básica mielina Se caracteriza por la triada: inflamación, desmielinización
Esclerosis Múltiple Esclerosis Múltiple Enfermedad autoinmune dirigida contra componentes de la mielina - glucoproteína mielínica - proteína básica mielina Se caracteriza por la triada: inflamación, desmielinización
Diagnóstico electrofisiológico. Valor del estudio electromiografico. El estudio electrofisiológico del sistema nervioso periférico (SNP) debe
 Diagnóstico electrofisiológico. Valor del estudio electromiografico. El estudio electrofisiológico del sistema nervioso periférico (SNP) debe considerarse como una prolongación de la exploración neurológica
Diagnóstico electrofisiológico. Valor del estudio electromiografico. El estudio electrofisiológico del sistema nervioso periférico (SNP) debe considerarse como una prolongación de la exploración neurológica
Árboles genealógicos. Ejercicios de genética
 Árboles genealógicos Ejercicios de genética Qué tipos de problemas podemos resolver? Y más importante aún cómo lo hacemos? Para qué sirve? Identificación de características de origen genético en humanos
Árboles genealógicos Ejercicios de genética Qué tipos de problemas podemos resolver? Y más importante aún cómo lo hacemos? Para qué sirve? Identificación de características de origen genético en humanos
TEJIDO MUSCULAR ESTRIADO ESQUELÉTICO
 19 TEJIDO MUSCULAR ESTRIADO ESQUELÉTICO ESTRUCTURA DEL TEMA: 19.1. Generalidades. 19.2. célula muscular estriada esquelética. 19.3. Células satélites. 19.4. Heterogeneidad de las fibras musculares estriadas
19 TEJIDO MUSCULAR ESTRIADO ESQUELÉTICO ESTRUCTURA DEL TEMA: 19.1. Generalidades. 19.2. célula muscular estriada esquelética. 19.3. Células satélites. 19.4. Heterogeneidad de las fibras musculares estriadas
EL ÁCIDO LÁCTICO EN EL DIAGNÓSTICO DIFERENCIAL DE LAS MIOPATÍAS METABÓLICAS. Pilar Carrasco Salas R2 Análisis Clínicos
 EL ÁCIDO LÁCTICO EN EL DIAGNÓSTICO DIFERENCIAL DE LAS MIOPATÍAS METABÓLICAS Pilar Carrasco Salas R2 Análisis Clínicos Introducción El ácido láctico es uno de los productos finales de la glucolisis Metabolismo
EL ÁCIDO LÁCTICO EN EL DIAGNÓSTICO DIFERENCIAL DE LAS MIOPATÍAS METABÓLICAS Pilar Carrasco Salas R2 Análisis Clínicos Introducción El ácido láctico es uno de los productos finales de la glucolisis Metabolismo
Universidad Centroccidental Lisandro Alvarado Decanato de Ciencias Veterinarias Área de Anatomía Microscópica y Embriología Veterinarias
 Universidad Centroccidental Lisandro Alvarado Decanato de Ciencias Veterinarias Área de Anatomía Microscópica y Embriología Veterinarias TEJIDO MUSCULAR M.V María Teresa Colmenárez Pérez DCV - UCLA- 2016
Universidad Centroccidental Lisandro Alvarado Decanato de Ciencias Veterinarias Área de Anatomía Microscópica y Embriología Veterinarias TEJIDO MUSCULAR M.V María Teresa Colmenárez Pérez DCV - UCLA- 2016
Hallazgos en Resonancia Magnética en la Hipertermia Maligna
 Hallazgos en Resonancia Magnética en la Hipertermia Maligna Poster no.: S-0669 Congreso: SERAM 2012 Tipo del póster: Presentación Electrónica Educativa Autores: B. Sanchez Cordon 1, G. Liaño Esteso 2,
Hallazgos en Resonancia Magnética en la Hipertermia Maligna Poster no.: S-0669 Congreso: SERAM 2012 Tipo del póster: Presentación Electrónica Educativa Autores: B. Sanchez Cordon 1, G. Liaño Esteso 2,
Mecánica de la contracción muscular. Depto. Biofísica Facultad de Medicina
 Mecánica de la contracción muscular Depto. Biofísica Facultad de Medicina Objetivo Estudiar los mecanismos involucrados en la contracción muscular esquelética. Para ello trataremos sobre: - Aspectos de
Mecánica de la contracción muscular Depto. Biofísica Facultad de Medicina Objetivo Estudiar los mecanismos involucrados en la contracción muscular esquelética. Para ello trataremos sobre: - Aspectos de
Fisología del Músculo Normal. Dr. Ramón Mauricio Coral Vázquez Escuela Superior de Medicina Instituto Politécnico Nacional
 Fisología del Músculo Normal Dr. Ramón Mauricio Coral Vázquez Escuela Superior de Medicina Instituto Politécnico Nacional Proteínas musculares asociadas a miopatías Mitocondria Coral-Vázquez RM, et al.
Fisología del Músculo Normal Dr. Ramón Mauricio Coral Vázquez Escuela Superior de Medicina Instituto Politécnico Nacional Proteínas musculares asociadas a miopatías Mitocondria Coral-Vázquez RM, et al.
TUMORES DE PARTES BLANDAS EN EL NIÑO
 TUMORES DE PARTES BLANDAS EN EL NIÑO INTRODUCCION Es una patología menos frecuente que en la edad adulta Se trata casi siempre de extirpe benigna, como son las lipomas, hemangiomas, etc. Dado que son raros
TUMORES DE PARTES BLANDAS EN EL NIÑO INTRODUCCION Es una patología menos frecuente que en la edad adulta Se trata casi siempre de extirpe benigna, como son las lipomas, hemangiomas, etc. Dado que son raros
SÍNDROME DE SJOGREN-LARSSON
 SÍNDROME DE SJOGREN-LARSSON QUÉ ES EL SÍNDROME DE SJOGREN-LARSSON (SLS)? El Síndrome de Sjögren-Larsson (SLS) es un error congénito del metabolismo de los lípidos (grasas), causado por mutaciones en el
SÍNDROME DE SJOGREN-LARSSON QUÉ ES EL SÍNDROME DE SJOGREN-LARSSON (SLS)? El Síndrome de Sjögren-Larsson (SLS) es un error congénito del metabolismo de los lípidos (grasas), causado por mutaciones en el
y según tipo, acianóticas, siendo comunicación interventricular en mayor proporción, y su tratamiento prevalece el
 Características epidemiológicas y clínicas de las cardiopatías congénitas en menores de 5 a os del Hospital Almanzor Aguinaga Asen o. Enero Diciembre 2012. 1,a 1,2,b 1,2,c RESUMEN Material y Métodos: quirúrgico.
Características epidemiológicas y clínicas de las cardiopatías congénitas en menores de 5 a os del Hospital Almanzor Aguinaga Asen o. Enero Diciembre 2012. 1,a 1,2,b 1,2,c RESUMEN Material y Métodos: quirúrgico.
IMPACTO DEL CRIBADO NEONATAL SOBRE LA AFECTACIÓN N RESPIRATORIA EN FQ. Carmen Antelo Landeira Unidad de Fibrosis Quística
 IMPACTO DEL CRIBADO NEONATAL SOBRE LA AFECTACIÓN N RESPIRATORIA EN FQ Carmen Antelo Landeira Unidad de Fibrosis Quística Cribado Neonatal de FQ ORENSTEIN DM. Am J Dis Child 1977;131:973-5 16 parejas de
IMPACTO DEL CRIBADO NEONATAL SOBRE LA AFECTACIÓN N RESPIRATORIA EN FQ Carmen Antelo Landeira Unidad de Fibrosis Quística Cribado Neonatal de FQ ORENSTEIN DM. Am J Dis Child 1977;131:973-5 16 parejas de
Mecánica de la Contracción Muscular
 Mecánica de la Contracción Muscular Dpto. Biofísica Facultad de Enfermería UTI: Locomotor ESFUNO Objetivos de la Clase Analizar algunos aspectos de la biofísica del músculo esquelético que permitan entender
Mecánica de la Contracción Muscular Dpto. Biofísica Facultad de Enfermería UTI: Locomotor ESFUNO Objetivos de la Clase Analizar algunos aspectos de la biofísica del músculo esquelético que permitan entender
ATROFIA MUSCULAR ESPINAL INFANTIL
 ATROFIA MUSCULAR ESPINAL INFANTIL E Tizzano Ferrari Servicio de Genética. Hospital de La Santa Cruz y San Pablo. Barcelona. E Tizzano Ferrari. Atrofia muscular espinal infantil. Protoc diagn ter pediatr.
ATROFIA MUSCULAR ESPINAL INFANTIL E Tizzano Ferrari Servicio de Genética. Hospital de La Santa Cruz y San Pablo. Barcelona. E Tizzano Ferrari. Atrofia muscular espinal infantil. Protoc diagn ter pediatr.
Esencialmente las personas con problemas de baja estatura se pueden agrupar dentro de dos categorías:
 Fundamentación y Objetivos de una fisioterapia específica para pacientes con Displasias Oseas: Prevención y Tratamientos. FUNDAMENTACIÓN Esencialmente las personas con problemas de baja estatura se pueden
Fundamentación y Objetivos de una fisioterapia específica para pacientes con Displasias Oseas: Prevención y Tratamientos. FUNDAMENTACIÓN Esencialmente las personas con problemas de baja estatura se pueden
Criterios diagnósticos para la Esclerosis Múltiple. Evolución de los criterios de Mc Donald.
 Criterios diagnósticos para la Esclerosis Múltiple. Evolución de los criterios de Mc Donald. Poster no.: S-0890 Congreso: SERAM 2012 Tipo del póster: Presentación Electrónica Educativa Autores: A. Joaquín
Criterios diagnósticos para la Esclerosis Múltiple. Evolución de los criterios de Mc Donald. Poster no.: S-0890 Congreso: SERAM 2012 Tipo del póster: Presentación Electrónica Educativa Autores: A. Joaquín
1-Tipos de Músculos Esquelético Liso Cardíaco
 FISIOLOGÍA MUSCULAR 1-Tipos de Músculos Esquelético Liso Cardíaco ultiunitario: cada fibra se comporta Como una unidad funcional Unitario: sincicio funcional Control voluntario por SNMS. Sin actividad
FISIOLOGÍA MUSCULAR 1-Tipos de Músculos Esquelético Liso Cardíaco ultiunitario: cada fibra se comporta Como una unidad funcional Unitario: sincicio funcional Control voluntario por SNMS. Sin actividad
Tema 7: Tejido Muscular
 Universidad la República Escuela de Salud Licenciatura en Enfermería Asignatura: Histología Tema 7: Tejido Muscular Unidad de Histología Mg Bárbara Cuevas Montuschi Tejido Muscular Tejido Muscular Estriado
Universidad la República Escuela de Salud Licenciatura en Enfermería Asignatura: Histología Tema 7: Tejido Muscular Unidad de Histología Mg Bárbara Cuevas Montuschi Tejido Muscular Tejido Muscular Estriado
Temas actuales: genética mitocondrial. Bioinformática Elvira Mayordomo
 Temas actuales: genética mitocondrial Bioinformática 11-3-16 Elvira Mayordomo Dos tipos de DNA DNA mitocondrial (mtdna): Se obtiene por vía materna En los humanos es muy corto (16.569 bp) Se conoce mucho
Temas actuales: genética mitocondrial Bioinformática 11-3-16 Elvira Mayordomo Dos tipos de DNA DNA mitocondrial (mtdna): Se obtiene por vía materna En los humanos es muy corto (16.569 bp) Se conoce mucho
PASO 2. Capítulo 3: Tejido Muscular
 PASO 2. Capítulo 3: Tejido Muscular Objetivos 1. Definir el tejido muscular. 2. Nombrar los elementos estructurales y su organización en este tejido. 3. Identificar los criterios utilizados para clasificar
PASO 2. Capítulo 3: Tejido Muscular Objetivos 1. Definir el tejido muscular. 2. Nombrar los elementos estructurales y su organización en este tejido. 3. Identificar los criterios utilizados para clasificar
ANALISIS CLINICO E HISTOPATOLOGICO DE 14 CASOS DE SINDROME DE ALPORT
 ANALISIS CLINICO E HISTOPATOLOGICO DE 14 CASOS DE SINDROME DE ALPORT 1,3 Ballesteros A., 2 Carpio D., 4 Romero C 1 Ardiles L., 1 Mezzano S. 1 Nefrología, Instituto de Medicina e 2 Instituto de Anatomía,
ANALISIS CLINICO E HISTOPATOLOGICO DE 14 CASOS DE SINDROME DE ALPORT 1,3 Ballesteros A., 2 Carpio D., 4 Romero C 1 Ardiles L., 1 Mezzano S. 1 Nefrología, Instituto de Medicina e 2 Instituto de Anatomía,
1. QUÉ SON LAS ENFERMEDADES NEUROMUSCULARES?
 UNIDAD 4. DISCAPACIDAD MOTORA LAS ENFERMEDADES NEUROMUSCULARES. CONTENIDO 1.1 QUÉ SON LAS ENFERMEDADES NEUROMUSCULARES?... 1 1.2. Síntomas... 2 1.3. EPIDEMIOLOGÍA... 3 1.4. causas o etiología... 3 a) Enfermedades
UNIDAD 4. DISCAPACIDAD MOTORA LAS ENFERMEDADES NEUROMUSCULARES. CONTENIDO 1.1 QUÉ SON LAS ENFERMEDADES NEUROMUSCULARES?... 1 1.2. Síntomas... 2 1.3. EPIDEMIOLOGÍA... 3 1.4. causas o etiología... 3 a) Enfermedades
Síndrome de Ehlers-Danlos
 Síndrome de Ehlers-Danlos es el nombre por el que se conocen un grupo heterogéneo de enfermedades hereditarias del tejido conectivo, caracterizadas por hiperlaxitud articular, hiperextensibilidad de la
Síndrome de Ehlers-Danlos es el nombre por el que se conocen un grupo heterogéneo de enfermedades hereditarias del tejido conectivo, caracterizadas por hiperlaxitud articular, hiperextensibilidad de la
ENFERMEDADES HEREDITARIAS EN ANIMALES que son las enfermedades hereditarias?
 ENFERMEDADES HEREDITARIAS EN ANIMALES que son las enfermedades hereditarias? Las enfermedades hereditarias son aquellas que se transmiten mediante el proceso de la herencia, es decir de los progenitores
ENFERMEDADES HEREDITARIAS EN ANIMALES que son las enfermedades hereditarias? Las enfermedades hereditarias son aquellas que se transmiten mediante el proceso de la herencia, es decir de los progenitores
Hallazgos en RM del sindrome del espacio cuadrilateral. Descripición de dos casos y revisión de la literatura
 Hallazgos en RM del sindrome del espacio cuadrilateral. Descripición de dos casos y revisión de la literatura Poster no.: S-1099 Congreso: SERAM 2014 Tipo del póster: Presentación Electrónica Educativa
Hallazgos en RM del sindrome del espacio cuadrilateral. Descripición de dos casos y revisión de la literatura Poster no.: S-1099 Congreso: SERAM 2014 Tipo del póster: Presentación Electrónica Educativa
ENFERMEDADES DEGENERATIVAS DEL SISTEMA NERVIOSO CENTRAL
 ENFERMEDADES DEGENERATIVAS DEL SISTEMA NERVIOSO CENTRAL Introducción El término degenerativo se aplica a las enfermedades del sistema nervioso que cursan con alteraciones de las células neuronales. Estos
ENFERMEDADES DEGENERATIVAS DEL SISTEMA NERVIOSO CENTRAL Introducción El término degenerativo se aplica a las enfermedades del sistema nervioso que cursan con alteraciones de las células neuronales. Estos
ESPACIO PÁRKINSON CONOCE LA ENFERMEDAD 1 Qué es el párkinson? Causas, diagnóstico y evolución
 ESPACIO PÁRKINSON CONOCE LA ENFERMEDAD 1 Qué es el párkinson? Causas, diagnóstico y evolución Espacio Párkinson 2017 es un proyecto puesto en marcha por la Federación Española de Párkinson con el objetivo
ESPACIO PÁRKINSON CONOCE LA ENFERMEDAD 1 Qué es el párkinson? Causas, diagnóstico y evolución Espacio Párkinson 2017 es un proyecto puesto en marcha por la Federación Española de Párkinson con el objetivo
Tiene a su cargo el movimiento del cuerpo y el cambio de tamaño y forma de los órganos internos.
 Tejido muscular Tiene a su cargo el movimiento del cuerpo y el cambio de tamaño y forma de los órganos internos. Este tejido se caracteriza por poseer conjuntos de células especializadas largas, cuya función
Tejido muscular Tiene a su cargo el movimiento del cuerpo y el cambio de tamaño y forma de los órganos internos. Este tejido se caracteriza por poseer conjuntos de células especializadas largas, cuya función
09/11/2010. Grado Medicina. Genética 1 er Curso. Genética clínica y consejo genético
 Grado Medicina Genética 1 er Curso TEMA 10 GENÉTICA CLÍNICA. 10.1 Genética clínica y consejo genético. 10.2 Enfermedades de herencia autosómica. 10.3 Enfermedades de herencia ligada al cromosoma X. 10.4
Grado Medicina Genética 1 er Curso TEMA 10 GENÉTICA CLÍNICA. 10.1 Genética clínica y consejo genético. 10.2 Enfermedades de herencia autosómica. 10.3 Enfermedades de herencia ligada al cromosoma X. 10.4
Recomendaciones para anestesia en pacientes que sufren de Enfermedad multiminicore (Multiminicore Disease)
 orphananesthesia Recomendaciones para anestesia en pacientes que sufren de Enfermedad multiminicore (Multiminicore Disease) Nombre de la enfermedad: Enfermedad multiminicore (Multiminicore Disease) IDC
orphananesthesia Recomendaciones para anestesia en pacientes que sufren de Enfermedad multiminicore (Multiminicore Disease) Nombre de la enfermedad: Enfermedad multiminicore (Multiminicore Disease) IDC
ULTRAESTRUCTURA Y ORGANIZACIÓN DE LOS SARCÓMEROS
 Clasificación del músculo MODO DE CONTROL ANATÓMICA HISTOLÓGICA Voluntario Esquelético Estriado Involuntario Cardíaco Visceral Liso Propiedades básicas del músculo Transforma la energía a química en energía
Clasificación del músculo MODO DE CONTROL ANATÓMICA HISTOLÓGICA Voluntario Esquelético Estriado Involuntario Cardíaco Visceral Liso Propiedades básicas del músculo Transforma la energía a química en energía
Aportación del patólogo al diagnóstico de las enfermedades musculares
 Aportación del patólogo al diagnóstico de las enfermedades musculares X Curso de Enfermedades Musculares en la Infancia y Adolescencia Mercedes García Villanueva Servicio de Anatomía Patológica Hospital
Aportación del patólogo al diagnóstico de las enfermedades musculares X Curso de Enfermedades Musculares en la Infancia y Adolescencia Mercedes García Villanueva Servicio de Anatomía Patológica Hospital
E.A.Torrigiani. Villa María, 15 de agosto 2014
 E.A.Torrigiani Villa María, 15 de agosto 2014 Descripta en 1916 por Guillain, Barré y Strohl Enfermedad adquirida y autoinmune Polirradiculoneuropatía desmielinizante inflamatoria aguda: AIDP Debilidad
E.A.Torrigiani Villa María, 15 de agosto 2014 Descripta en 1916 por Guillain, Barré y Strohl Enfermedad adquirida y autoinmune Polirradiculoneuropatía desmielinizante inflamatoria aguda: AIDP Debilidad
Caso 2: 1ª RM: aumento de señal en la corteza cerebral en difusión y FLAIR, con ganglios de la base normales. 2ª RM: aparece aumento de señal en
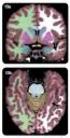 RESULTADOS: En todos los casos encontramos alteraciones características a nivel cortical y/o en los ganglios basales en fases iniciales de la enfermedad. Caso 1: 1ª RM: aumento de señal en T2, FLAIR y
RESULTADOS: En todos los casos encontramos alteraciones características a nivel cortical y/o en los ganglios basales en fases iniciales de la enfermedad. Caso 1: 1ª RM: aumento de señal en T2, FLAIR y
PATOLOGÍA QUIRÚRGICA Jornadas Cien8ficas 82º Reunión Mensual. Jueves 26 de Abril del 2012
 PATOLOGÍA QUIRÚRGICA Jornadas Cien8ficas 82º Reunión Mensual Jueves 26 de Abril del 2012 Caso Nº 3 Dr. Ishtvan Torres CASO Nº N1100208 Dr. Isthvan Torres Cadáver de sexo masculino de 47 años de edad. Se
PATOLOGÍA QUIRÚRGICA Jornadas Cien8ficas 82º Reunión Mensual Jueves 26 de Abril del 2012 Caso Nº 3 Dr. Ishtvan Torres CASO Nº N1100208 Dr. Isthvan Torres Cadáver de sexo masculino de 47 años de edad. Se
Tejido Muscular. La célula o fibra muscular es la unidad estructural y funcional del tejido muscular
 Tejido Muscular La célula o fibra muscular es la unidad estructural y funcional del tejido muscular Cuando decimos fibra muscular no nos estamos refiriendo a un tipo de fibra extracelular, como es el caso
Tejido Muscular La célula o fibra muscular es la unidad estructural y funcional del tejido muscular Cuando decimos fibra muscular no nos estamos refiriendo a un tipo de fibra extracelular, como es el caso
POLINEUROPATIA Y DOLOR NEUROPATICO
 POLINEUROPATIA Y DOLOR NEUROPATICO DR MARIO FUENTEALBA UDEC - HGGB CONTENIDO DIAGNOSTICO DE POLINEUROPATIA ESTUDIO DE POLINEUROPATIA FISIOPATOLOGIA DOLOR NEUROPATICO MANEJO DE DOLOR NEUROPATICO EPIDEMIOLOGIA
POLINEUROPATIA Y DOLOR NEUROPATICO DR MARIO FUENTEALBA UDEC - HGGB CONTENIDO DIAGNOSTICO DE POLINEUROPATIA ESTUDIO DE POLINEUROPATIA FISIOPATOLOGIA DOLOR NEUROPATICO MANEJO DE DOLOR NEUROPATICO EPIDEMIOLOGIA
Departamento de Estadísticas y Gestión de la Información Página 1
 Departamento de Estadísticas y Gestión de la Información Página 1 MORTALIDAD INFANTIL 2009 SERVICIO DE SALUD METROPOLITANO ORIENTE Informe preparado por el Dpto. de Estadísticas y Gestión de la Información
Departamento de Estadísticas y Gestión de la Información Página 1 MORTALIDAD INFANTIL 2009 SERVICIO DE SALUD METROPOLITANO ORIENTE Informe preparado por el Dpto. de Estadísticas y Gestión de la Información
Docente: Dra. M. Gloria Pinto Alumno: Juan Pablo Silva Ramo: Fisiopatología Fecha :
 Docente: Dra. M. Gloria Pinto Alumno: Juan Pablo Silva Ramo: Fisiopatología Fecha : 22-06-2011 Las enfermedades neurodegenerativas, son trastornos del sistema nervioso central marcados por una pérdida
Docente: Dra. M. Gloria Pinto Alumno: Juan Pablo Silva Ramo: Fisiopatología Fecha : 22-06-2011 Las enfermedades neurodegenerativas, son trastornos del sistema nervioso central marcados por una pérdida
Aspectos clínicos y moleculares de la miotonía congénita.
 Aspectos clínicos y moleculares de la miotonía congénita. Jesús Molano Unidad de Genética Molecular Instituto de Genética Médica y Molecular (INGEMM) Hospital Universitario La Paz Miotonía: Disminución
Aspectos clínicos y moleculares de la miotonía congénita. Jesús Molano Unidad de Genética Molecular Instituto de Genética Médica y Molecular (INGEMM) Hospital Universitario La Paz Miotonía: Disminución
ENFERMEDAD WILSON. Esperanza Castejón Sesión extrahospitalaria
 ENFERMEDAD WILSON Esperanza Castejón Sesión extrahospitalaria COBRE Oligoelemento esencial en el organismo Hígado: Regula, distribuye y excreta el cobre Proteína reguladora del cobre : ATP7A : intestino
ENFERMEDAD WILSON Esperanza Castejón Sesión extrahospitalaria COBRE Oligoelemento esencial en el organismo Hígado: Regula, distribuye y excreta el cobre Proteína reguladora del cobre : ATP7A : intestino
La enfermedad renal crónica: Prevalencia y valor pronóstico
 La enfermedad renal crónica: Prevalencia y valor pronóstico Dr Jose Luis Górriz Servicio de Nefrologia Hospital Universitario Dr Peset Valencia. España Concepto de enfermedad renal crónica (ERC) de las
La enfermedad renal crónica: Prevalencia y valor pronóstico Dr Jose Luis Górriz Servicio de Nefrologia Hospital Universitario Dr Peset Valencia. España Concepto de enfermedad renal crónica (ERC) de las
Episodios paroxísticos no epilépticos
 Episodios paroxísticos no epilépticos Sara Sánchez-García Óscar García Campos Alfonso Verdú Pérez Carmen Villaizán Pérez Julio 2014 1 Episodios paroxísticos no epilépticos Grupo de trastornos, síndromes
Episodios paroxísticos no epilépticos Sara Sánchez-García Óscar García Campos Alfonso Verdú Pérez Carmen Villaizán Pérez Julio 2014 1 Episodios paroxísticos no epilépticos Grupo de trastornos, síndromes
Trombocitemia: neoplasia mieloproliferativa caracterizada por trombocitosis-ver Trombocitemia Esencial (TE).
 TROMBOCITOSIS DEFINICIONES Trombocitosis: recuento de plaquetas > 450 x 10 9 / L Trombocitosis Primaria: trombocitosis causada por una alteración en las células hematopoyéticas; el nivel sérico de trombopoyetina
TROMBOCITOSIS DEFINICIONES Trombocitosis: recuento de plaquetas > 450 x 10 9 / L Trombocitosis Primaria: trombocitosis causada por una alteración en las células hematopoyéticas; el nivel sérico de trombopoyetina
CONSULTA DE ENFERMEDADES RARAS
 CONSULTA DE ENFERMEDADES RARAS PRESENTACIÓN DEL PROBLEMA Las llamadas Enfermedades Raras, también conocidas como Enfermedades Minoritarias o Enfermedades Metabólicas Hereditarias son un grupo de enfermedades
CONSULTA DE ENFERMEDADES RARAS PRESENTACIÓN DEL PROBLEMA Las llamadas Enfermedades Raras, también conocidas como Enfermedades Minoritarias o Enfermedades Metabólicas Hereditarias son un grupo de enfermedades
REHABILITACIÓN EN NEONATOLOGÍA ALTO RIESGO NEUROLÓGICO. Angélica Duque Villalobos Medico Fisiatra Fundación Clínica Valle Del Lili
 REHABILITACIÓN EN NEONATOLOGÍA ALTO RIESGO NEUROLÓGICO Angélica Duque Villalobos Medico Fisiatra Fundación Clínica Valle Del Lili NEURODESARROLLO Serie de mecanismos que involucran los procesos biológicos
REHABILITACIÓN EN NEONATOLOGÍA ALTO RIESGO NEUROLÓGICO Angélica Duque Villalobos Medico Fisiatra Fundación Clínica Valle Del Lili NEURODESARROLLO Serie de mecanismos que involucran los procesos biológicos
Genes y cáncer TEMA 9
 TEMA 9 Genes y cáncer Antecedentes históricos Modelos experimentales Causas multifactoriales Protooncogenes y genes supresores de tumores Reordenaciones cromosómicas y cáncer Mutaciones puntuales y cáncer
TEMA 9 Genes y cáncer Antecedentes históricos Modelos experimentales Causas multifactoriales Protooncogenes y genes supresores de tumores Reordenaciones cromosómicas y cáncer Mutaciones puntuales y cáncer
TIPOS DE TEJIDO MUSCULAR
 CARACTERISTICAS UNIVERSALES DEL TEJIDO MUSCULAR Excitabilidad Las células musculares pueden producir corrientes eléctricas Contractibilidad Las células musculares se pueden acortar Extensibilidad Las células
CARACTERISTICAS UNIVERSALES DEL TEJIDO MUSCULAR Excitabilidad Las células musculares pueden producir corrientes eléctricas Contractibilidad Las células musculares se pueden acortar Extensibilidad Las células
Capítulo 1 Definición
 Capítulo 1 Definición El 1 de diciembre de 1999, se estableció la definición de enfermedad rara para todas aquellas patologías cuya cifra de prevalencia se encuentra por debajo de 5 casos por cada 10.000
Capítulo 1 Definición El 1 de diciembre de 1999, se estableció la definición de enfermedad rara para todas aquellas patologías cuya cifra de prevalencia se encuentra por debajo de 5 casos por cada 10.000
Ejercicio Muscular. Universidad Nacional La Matanza
 Ejercicio Muscular Universidad Nacional La Matanza División funcional Músculo: Haz muscular (fascículo) Fibra (célula) Fibrilla Sarcómero Filamentos finos Filamentos gruesos Hazdefibras Fibra muscular
Ejercicio Muscular Universidad Nacional La Matanza División funcional Músculo: Haz muscular (fascículo) Fibra (célula) Fibrilla Sarcómero Filamentos finos Filamentos gruesos Hazdefibras Fibra muscular
Una mujer de 25 anos expresa la hemophilia A de forma leve, la evaluación genética revela
 1. Una mujer de 25 anos expresa la hemophilia A de forma leve, la evaluación genética revela que ella es una portadora heterocigotica para la mutación del gen del facto VIII de los sgtes enunciados explica
1. Una mujer de 25 anos expresa la hemophilia A de forma leve, la evaluación genética revela que ella es una portadora heterocigotica para la mutación del gen del facto VIII de los sgtes enunciados explica
Epilepsia 360º. Te garantizamos la máxima utilidad clínica
 Epilepsia 360º Te garantizamos la máxima utilidad clínica Epilepsia 360º la aproximación más completa y coste-eficaz para el análisis de fenotipos heterogéneos o inespecíficos Utilizamos la más eficaz
Epilepsia 360º Te garantizamos la máxima utilidad clínica Epilepsia 360º la aproximación más completa y coste-eficaz para el análisis de fenotipos heterogéneos o inespecíficos Utilizamos la más eficaz
IMPORTANCIA DE LA FISIOTERAPIA EN NIÑOS CON DISPLASIAS ÓSEAS
 IMPORTANCIA DE LA FISIOTERAPIA EN NIÑOS CON DISPLASIAS ÓSEAS Centro de Fisioterapia Ogíjares Mª Carmen Aguilar Hernánz Inmaculada Puertas Torres Mª Dolores García Espejo DEFINICIÓN DE DISPLASIAS ÓSEAS:
IMPORTANCIA DE LA FISIOTERAPIA EN NIÑOS CON DISPLASIAS ÓSEAS Centro de Fisioterapia Ogíjares Mª Carmen Aguilar Hernánz Inmaculada Puertas Torres Mª Dolores García Espejo DEFINICIÓN DE DISPLASIAS ÓSEAS:
Enfermedades Neuromusculares en Niños
 Vol. 14 N 2 Abril 2003 Enfermedades Neuromusculares en Niños Dra. Karin Kleinsteuber S., Dra. Claudia Castiglio Unidad de Neurología Infantil Clínica Las Condes Introducción El enorme progreso que ha experimentado
Vol. 14 N 2 Abril 2003 Enfermedades Neuromusculares en Niños Dra. Karin Kleinsteuber S., Dra. Claudia Castiglio Unidad de Neurología Infantil Clínica Las Condes Introducción El enorme progreso que ha experimentado
ESTIMULACIÓN MÚLTIPLE TEMPRANA. Dra. Carmen Montserrat Gómez Juárez R4 Medicina de Rehabilitación
 ESTIMULACIÓN MÚLTIPLE TEMPRANA Dra. Carmen Montserrat Gómez Juárez R4 Medicina de Rehabilitación Con los avances en la atención del recién nacido se ha logrado una tasa creciente de supervivencia entre
ESTIMULACIÓN MÚLTIPLE TEMPRANA Dra. Carmen Montserrat Gómez Juárez R4 Medicina de Rehabilitación Con los avances en la atención del recién nacido se ha logrado una tasa creciente de supervivencia entre
