MODULO III SECCION 3 SISTEMAS DISPERSOS HETEROGENEOS. Mercedes Fernández Arévalo
|
|
|
- Virginia Paz Cabrera
- hace 7 años
- Vistas:
Transcripción
1 MODULO III SECCION 3 SISTEMAS DISPERSOS HETEROGENEOS Mercedes Fernández Arévalo
2 SISTEMAS DISPERSOS HETEROGÉNEOS Sistemas en el que una sustancia está dispersada,, en forma de unidades discretas, en el seno de otra en la cuál es insoluble. Ambas sustancias pueden estar en forma de sólido, líquido o gas. Son sistemas termodinámicamente inestables Componentes: 1. Fase interna, dispersada, discontinua (FI) 2. Fase externa, dispersante, continua, medio de dispersión (FE) 3. Interfase (4. Estabilizante)
3 SISTEMAS DISPERSOS HETEROGÉNEOS CLASIFICACIÓN: 1. Según afinidad por el medio de dispersión: Liofílicas Liofóbicas Interacción mucho menor, estabilizándose por otros mecanismos (cargas eléctrica, ) Interacción fuerte con las moléculas de la FE
4 SISTEMAS DISPERSOS HETEROGÉNEOS CLASIFICACIÓN: 1. Según afinidad por el medio de dispersión: Liofílicas Liofóbicas 2. Según el tamaño de la FI: Clasificación de Ostwald
5 CLASIFICACIÓN DE OSTWALD FI Ø part. > 0.1 µm Dispersiones groseras 0.1 µm m > Ø part. > µm Coloides Ø part. < µm Soluciones verdades 5
6 SISTEMAS DISPERSOS HETEROGÉNEOS CLASIFICACIÓN: 1. Según afinidad por el medio de dispersión: Liofílicas Liofóbicas 2. Según el tamaño de la FI: Clasificación de Ostwald 3. Según el estado de agregación de ambas fases
7 ESTADO DE AGREGACIÓN DE LA MATERIA FE FI TIPO DE SISTEMA EJEMPLO Gas Sólido Aerosol Humo Gas Líquido Aerosol Niebla Líquido Sólido Suspensión, sol. colidal Susp., tinta Líquido Líquido Emulsión Leche Líquido Gas Espuma E. de afeitar Sólido Sólido Sol sólido Perlas Sólido Líquido Emul.. sólida Mantequilla Sólido Gas Espuma sólida 7
8 SISTEMAS DISPERSOS HETEROGÉNEOS Propiedades cinéticas: 1. Movimiento Browniano 2. Difusión 3. Presión Osmótica 4. Sedimentación 5. Viscosidad 8
9 SISTEMAS DISPERSOS HETEROGÉNEOS 1. Movimiento Browniano Movimiento errático observado en partículas menores de 5µm. La velocidad de las partículas es inversamente proporcional a su tamaño y a la viscosidad del medio 2-5 µm 2. Difusión 9
10 SISTEMAS DISPERSOS HETEROGÉNEOS 2. Difusión Las partículas difunden espontáneamente desde zonas de mayor a menor concentración, hasta que la concentración de todo el sistema es homogénea. Resulta directamente del mocimiento Browniano Ley de Frick dq = - DS (dc/dx) dt D - coeficiente de difusión S - área del plano C - concentración x - distancia t - tiempo q - cantidad de sustancia dq/dt = -DS (dc/dx) si S = 1 dq/dt = -D (dc/dx) D = constante dq/dt - dc/dx 10
11 SISTEMAS DISPERSOS HETEROGÉNEOS 3. Ósmosis Cuando las partículas no pueden difundir en el sistema por la presencia de una membrana semipermeable, son las moléculas del solvente las que se mueven desde la zona de menor a la de mayor concentración. Ecuación de Van't Hoff Π = crt Π - Presión osmótica c - concentración (g/l) R - constante de los gases T - Temperatura absoluta 11
12 SISTEMAS DISPERSOS HETEROGÉNEOS 4. Sedimentación V= f(ø, g, δ, η) Gravedad Ley de Stoke v = 2r 2 (D - d) g / 9η v - velocidad de sedimentación r - radio de la partícula g - fuerza de la gravedad D - densidad de la partícula d - densidad del medio η - viscosidad del medio 2-5 µm Movimiento Browniano Equilibrio de sedimentation Fuerza de gravedad neutralizada por el movimiento Browniano 12
13 SISTEMAS DISPERSOS HETEROGÉNEOS 4. Sedimentación Ley de Stoke v = 2r 2 (D - d) g / 9η 13
14 Ejemplo: SISTEMAS DISPERSOS HETEROGÉNEOS 4. Sedimentación Determine la viscosidad absoluta de un jarabe usando una bola de acero de 0.2 cm de radio. La densidad de la bola es de 2.33 g / cc y la densidad del jarabe es 1.33 g / cc a 250 ºC. La velocidad de caída de la bola es de 4.35 cm / s. v = 2r 2 (D - d) g / 9η η = 2r 2 (D - d) g / 9v = 2 (0.2)(0.2) [ ] 980 / 9(4.35) = 2.0 poise 14
15 4. Sedimentación Ejemplo: SISTEMAS DISPERSOS HETEROGÉNEOS Determine la velocidad de sedimentación de un sulfuro en agua. El diámetro medio de partícula es de 5.5 µm. Las densidades del sulfuro y del agua a 250 ºC son 1.96 y g/cc, respectivamente. La viscosidad del agua a 250 ºC es poise. v = 2r 2 (D - d) g / 9η = 2 (5.5*10-4 )(5.5*10-4 )( ) *980 / 9( ) = 7.1*10-3 cm/s 15
16 4. Sedimentación Ejemplo: SISTEMAS DISPERSOS HETEROGÉNEOS Si la altura de la botella de la suspensión anterior del sulfuro es de 10 cm, cuánto tardará el sistema en sedimentar completamente? v = 7.1*10-3 cm/s 1/x = 7.1*10-3 /10 x = 1408 s = ap. 24 min. Sedimenta demasiado rápidamente. Convendría aumentar la viscosidad para reducir la velocidad de sedimentación. 16
17 SISTEMAS DISPERSOS HETEROGÉNEOS 4. Sedimentación Ejemplo: Del ejemplo anterior, calcule el tamaño medio de partícula del sulfuro v = 2r 2 (D - d) g / 9η r 2 = v 9η / 2 (D - d) g = (0.0071)(9)( ) / 2( )980 r = 5.5*10-4 cm diámetro medio = 11*10-4 cm 17
18 SISTEMAS DISPERSOS HETEROGÉNEOS 4. Sedimentación Ejemplo: Cuál deberá ser la viscosidad del sistema anterior para reducir su velocidad de sedimentación desde cm/s a cm/s? v = 2r2 (D - d) g / 9η η = 2r 2 (D - d)g / 9v = 2 (5.5*10-4 ) 2 ( )(980) / 9( ) = poise 18
19 SISTEMAS DISPERSOS HETEROGÉNEOS 4. Sedimentación Ley de Stoke v = 2r 2 (D - d) g / 9η Otro factor importante es la DENSIDAD. Es posible modificar la densidad de la dispersión adicionando sustancias no iónicas Ejemplos: SORBITOL PVP GLICERINA AZUCAR PEG 19
20 SISTEMAS DISPERSOS HETEROGÉNEOS REOLOGÍA Propiedades de flujo (Φ) y deformación de las dispersiones cuando se someten a una presión (tensión, compresión o cizalla (τ) (fuerza por unidad de área: F/A) CIZALLA VELOCIDAD DE CIZALLA τ (F/A) D (dv/dx) Fluidez = Φ = 1/η 20
21 τ Fuerza de cizalla F/A SISTEMAS DISPERSOS HETEROGÉNEOS Bingham (plástico ideal) τ = τ o + η D Pseudoplástico: aclaramiento por cizalla (>τ <η >Φ) η Fluidez = Φ = 1/η Newtoniano: τ = η D (η y Φ = ctes.) Dilatante (>τ >η <Φ) (Φ 0) Velocidad de cizalla dv/dx dx D
22 τ SISTEMAS DISPERSOS HETEROGÉNEOS Fluidez = Φ = 1/η Fuerza de cizalla F/A Pseudoplástico con Fuerza de ruptura y Comportamiento tixotrópico Velocidad de cizalla dv/dx dx D
23 SISTEMAS DISPERSOS HETEROGÉNEOS * Se obtienen al dispersar una sustancia en el seno de otra en la cuál es insoluble. * Son sistemas termodinámicamente inestables * Componentes: 1. Fase interna, dispersada, discontinua (FI) 2. Fase externa, dispersante, continua, medio de dispersión (FE) 3. Interfase (4. Estabilizante)
24 SISTEMAS DISPERSOS HETEROGÉNEOS TERMODINÁMICAMENTE INESTABLES 1. FUERZAS DE INTERACCIONES MOLECULARES * FENÓMENOS SUPERFICIALES * FENÓMENOS INTERFACIALES 2. FUERZAS DE INTERACCIONES PARTICULARES POTENCIAL ELECTROCINÉTICO
25 1. FUERZAS DE INTERACCIONES MOLECULARES Moléculas de Agua Las moléculas del agua presentan una disposición característica. Tiene la posibilidad de formar puentes de H, lo que le confieren al agua propiedades especiales. Las moléc. de agua experimentan una gran atracción unas por otras. + - O H H + - O + H H + Esto causa alta tensión superficial, baja presión de vapor, alto calor específico, alto calor de vaporización y alto punto de ebullición.
26 1. FUERZAS DE INTERACCIONES MOLECULARES Tensión Superficial Una moléc. de agua en el interior de la soluc. está sometida a fuerzas de atracción en todas las direcciones. En la superficie, las mólec. están atraídas sólo hacia los lados y hacia abajo, mateniéndolas fuertemente unidas. Esto causa la tensión superfical. γ: relación inversa con la T y la P
27 1. FUERZAS DE INTERACCIONES MOLECULARES Tensión Superficial El cristal tiene molóculas polares, por lo que puede formar puentes de H. Atrae moléculas de agua. Algunas son empujadas hacia arriba, curvando así la superficie del agua. cristal plastico Las gotas de agua son redondas porque todas las moléculas situadas en su superficie experimentan una atracción neta hacia el interior.
28 Tensión superficial γ Superficie líquido - gas Fuerza resultante de las interacciones inter- moleculares,, que tienden a reducir al máximo la razón área superficial / volumen Menor superficie = menor energía asociada (esfera) Energía Superficial = Tensión superficial * área superficial Energía por unidad de área (mj/m 2 ; mn/m)
29 Tensión superficial γ Formación de superficie? Vapor Superficie Líquido 29
30 Tensión superficial γ Formación de superficie? Vapor REGION INTERFACIAL Liquido 30
31 Tensión superficial γ Formación de superficie? Vapor Liquido Las moleculas en el interior son estables (expuestas a un campo de fuerza simetrico) 31
32 Tensión superficial γ Formación de superficie? Las moleculas en la interfase son inestables,, se ven empujadas hacia el interior, para minimizar el area interfacial 32
33 Tensión superficial γ Expansión de la interfase Formación de superficie? 33
34 Tensión superficial γ Expansión de la interfase... Formación de superficie? 34
35 Tensión superficial γ Expansión de la interfase... Formación de superficie? 35
36 Tensión superficial γ Expansión de la interfase... Formación de superficie? W = Trabajo realizado para expandir la supercie A A = Incremento de superficie 36
37 Tensión superficial γ Aumento de superficie? Desfavorable! No existe un potencial molecular compensado en la superficie Por tanto, la creación de más superfice siempre estará acompañada de un aumento en la energía libre del sistema ( G A > 0) Así que la formación de nueva superficie siempre es un proceso termodinámicamente desfavorable 37
38 Tensión superficial γ - Superficie ALGUNAS ECUACIONES Tensión superficial (σ or γ) - incremento de energía libre como resultado de la formación de 1 unidad de superfice (cm 2, m 2 ) G σ = ; σ >0 Α p,t (siempre positivo!) La formación de superficie ( A) implica siempre un aumento en la energía libre ( G) G Α = σ Α >0 38
39 Tensión superficial γ - Superficie ALGUNAS ECUACIONES... EXPRESIÓN MATEMÁTICA: W = G G = γ A γ: : constante de proporcionalidad entre el trabajo que es necesario aplicar para crear nueva superficie y el área de la misma Newton / metro (SI) Más frecuente: dinas / cm (CGS) 39
40 Tensiones de superficie Interfases Gas / Liq. Gas / Sol. Liq.. / Sol. Liq.1 / Liq.2 Sol.1 / Sol.2 Tension superficial Tension interfacial 40
41 Tensión interfacial γ12 Sustancias inmiscibles: diferencia entre fuerzas de cohesión y fuerzas atractivas entre dos moléculas diferentes F atrac.. (mol. polar - m. polar) >>>> F atrac.. (m. polar - m. apolar) La fuerza resultante cerca de la interfase está dirigida hacia el interior. Por el contrario, la resultante en el interior es nula. Para aumentar la superficie de contacto total (desplazar moléculas del interior al exterior), es necesario un aporte neto de energía (ENERGÍA LIBRE INTERFACIAL) Sistema termodinámicamente inestable
42 Tensión interfacial γ12 SISTEMAS LIQUIDO-LIQUIDO 42
43 Tensión interfacial γ12 SISTEMAS LIQUIDO-LIQUIDO Aceite y agua Agitación? 43
44 Tensión interfacial γ12 SISTEMAS LIQUIDO-LIQUIDO Aceite y agua La agitación distribuye el aceite a través del agua. Qué pasa cuando cesa la agitación? 44
45 Tensión interfacial γ12 SISTEMAS LIQUIDO-LIQUIDO Aceite y agua Cuando la agitación cesa,, la acción de la energía libre interfacial hará que: 1. Las gotas de aceite se vuelvan esféricas 45
46 Tensión interfacial γ12 SISTEMAS LIQUIDO-LIQUIDO Aceite y agua Cuando la agitación cesa,, la acción de la energía libre interfacial hará que: 1. Las gotas de aceite se vuelvan esféricas 2. La acción de la gravedad empice a actuar sobre las gotas esféricas de aceite. 46
47 Tensión interfacial γ12 SISTEMAS LIQUIDO-LIQUIDO Aceite y agua Cuando la agitación cesa,, la acción de la energía libre interfacial hará que: 1. Las gotas de aceite se vuelvan esféricas 2. La acción de la gravedad empice a actuar sobre las gotas esféricas de aceite. 3. Las gotas coalescen para reducir la energía libre por reducción de la 47 tension interfacial.
48 Tensión interfacial γ12 SISTEMAS SOLIDO-LIQUIDO 48
49 Tensión interfacial γ12 Trabajo de COHESION (W 11 ) (mj/m 2 ): Energía necesaria para separar 2 superficies identicas desde el contacto hasta una separacion infinita liquido γ L SISTEMAS SOLIDO-LIQUIDO Trabajo de cohesion WC = γ + γ = 2 γ L L L liquido γ L γ L liquido 49
50 Tensión interfacial γ12 GRADO DE AFINIDAD SISTEMAS SOLIDO-LIQUIDO γ LS Trabajo de ADHESION (W 12 ) (mj/m 2 ): Energia necesaria para separar 2 superficies diferentes desde el contacto hasta una separacion infinita liquido γ Trabajo de adhesion WA = γ + γ - L S S solido γ = γ + γ LS L S - WA γ LS liquido γ L γ S solido 50
51 Tensión interfacial γ12 SISTEMAS SOLIDO-LIQUIDO DIFUSIÓN DE UN LÍQUIDO SOBRE UN SÓLIDO SÓLO OCURRIRÁ SI EL TRABAJO SE ADHESIÓN SUPERA AL DE COHESIÓN WA > WC S = Spreading Coefficient S = WA - WC Si S > 0, el líquido difundirá sobre el sólido permitiendo generar el sistema 51
52 Tensión interfacial γ12
53 Tensión interfacial γ12 Por qué las gotas adquieren una forma esférica? La tendendia del sistema es reducir su energía libre.. El resultado es adoptar una configuración con la que presente la menor área superficial posible.. Y la esfera es la forma geométrica que permite una superficie menor para un volumen dado.
54 Tensión interfacial γ12 Por qué la tensión superficial del agua es mayor que la del aceite? La tensión superficial deriva de las interacciones entre las moléculas de una fase. El agua es polar, y las interacciones intermoleculares entre moléculas polares son mayores que las interacciones entre moléculas no polares.
55 Tensión interfacial γ12 Por qué la tensión interfacial es menor que las tensiones superficiales? Por el trabajo de adhesión Cuando dos fases condensadas (2 líquidos) están en contacto, la interacción a través de de la interfaz es mayor que la que existe entre una fase condensada y un gas.
56 Tensión interfacial γ12 Fuerzas moleculares en la interfaz Liquido / Gas? Sin embargo, la baja densidad que hay en el gas hace que existan pocas moléculas para interaccionar. La interacción a través de la interfase es posible. 56
57 Tensión interfacial γ12 Fuerzas moleculares en la interfaz Liq.1 / Liq.2? La densidad elevada de la fase liquida vecina significa que existen suficientes moleculas cerca para interacturar. La interacción a través de la interfase es posible. El resultado es que la fuerza neta de atraccion en las moleculas de la interfase es menor. 57
58 Tensión interfacial γ12 Por qué los tensioactivos disminuyen la tensión en la interfaz? Las moléculas tensioactivas son anfifílicas Polar region Nonpolar region
59 Tensión interfacial γ12 Las moléculas anfifílicas se localizan, preferentemente, en la interfaz. Esto hace que disminuya la diferencia entre las dos fases.
60 Tensión interfacial γ12 Las moléculas anfifílicas se localizan, preferentemente, en la interfaz. Esto hace que disminuya la diferencia entre las dos fases.
61 SISTEMAS DISPERSOS HETEROGÉNEOS TERMODINÁMICAMENTE INESTABLES 1. FUERZAS DE INTERACCIONES MOLECULARES * FENÓMENOS SUPERFICIALES * FENÓMENOS INTERFACIALES 2. FUERZAS DE INTERACCIONES PARTICULARES POTENCIAL ELECTROCINÉTICO
62 2. FUERZAS DE INTERACCIONES PARTICULARES La mayoría de las partículas de un SDH (sean iónicas o no) presentan una carga eléctrica superficial desarrollada por distintos mecanismos: 1. Disociación de grupos ionógenos 2. Adsorción de iones (aniones: < hidratación - > movilidad) 3. Electrificación por fricción,... REGLA DE COHEN: la fase de > constante dieléctrica se carga positivamente POTENCIAL ELECTROCINÉTICO
63 2. FUERZAS DE INTERACCIONES PARTICULARES S D SUPERFICIE DOBLE CAPA ELÉCTRICA 63
64 2. FUERZAS DE INTERACCIONES PARTICULARES S DOBLE CAPA ELÉCTRICA D Capa difusa de contraiones en posiciones menos estrictas. Capa de Stern Capa monomolecular de contraiones del medio en contacto con la superficie, en posiciones muy determinadas. A partir de aquí, la concentración de iones va disminuyendo. Punto de neutralidad A partir de donde la carga eléctrica de la partícula no se hace sentir más 64
65 2. FUERZAS DE INTERACCIONES PARTICULARES S D > ζ Mayor repulsión interpaticular DOBLE CAPA ELÉCTRICA No se puede medir directamente la carga de la partícula Potencial Z (ζ) Diferencia del potencial que hay entre la zona de separación de la capa fija y la capa difusa y el punto de neutralidad. Se estima en función de la movilidad electroforética 65
66 2. FUERZAS DE INTERACCIONES PARTICULARES DOBLE CAPA ELÉCTRICA ESTABILIDAD DE LOS SDH? 66
67 2. FUERZAS DE INTERACCIONES PARTICULARES TEORÍA DLVO: (Deryagin y Landau, Verwey y Overbeek) Energía potencial total + Repulsión - Atracción Mínimo primario Agregación tipo coagulado (IRREVERSIBLE) Máximo primario Mínimo secundario Agregación tipo floculado (REDISPERSABLE) Distancia entre las partículas
68 2. FUERZAS DE INTERACCIONES PARTICULARES TEORÍA DLVO: (Deryagin y Landau, Verwey y Overbeek) Energía potencial total + Repulsión - Atracción Mínimo primario Máximo primario Mínimo secundario Distancia entre las partículas La curva de energía potencial se puede modificar variando la concentración de electrolitos. ESTABILIZACIÓN DE SDH.
69 CLASIFICACIÓN DE OSTWALD FI Ø part. > 0.1 µm Dispersiones groseras 0.1 µm m > Ø part. > µm Coloides Ø part. < µm Soluciones verdades 69
70 Coloides Son dispersiones en las que el tamaño de FI es superior al de moléculas pero demasiado pequeñas para que les afecte la gravedad. (sólo mov. Browniano) Tamaño: Å 0.1 µm µm
71 Coloides Tipo de coloide FI FE Ejemplo Fog Aerosol Liquid Gas Fog Aerosol Solid Gas Smoke Foam Gas Liquid Whipped Cream Solid foam Gas Solid Marshmallow Emulsion Liquid Liquid Milk Solid emulsion Liquid Solid Butter Sol Solid Liquid Paint; cell fluid Solid sol Solid Solid Opal
72 Coloides Tipo de coloide FI FE Ejemplo Aerosol Liquid Gas Aerosol Solid Gas Foam Gas Liquid Solid foam Gas Solid Emulsion Liquid Liquid Solid emulsion Liquid Solid Sol Solid Liquid Solid sol Solid Solid Fog Gas Smoke Whipped Cream Marshmallow Milk Butter Paint; cell fluid Opal
73 Coloides Tipo de coloide FI FE Ejemplo Aerosol Liquid Gas Aerosol Solid Gas Foam Gas Liquid Solid foam Gas Solid Emulsion Liquid Liquid Solid emulsion Liquid Solid Sol Solid Liquid Solid sol Solid Solid Fog Gas Smoke Whipped Cream Marshmallow Milk Butter Paint; cell fluid Opal
74 Coloides Tipo de coloide FI FE Ejemplo Aerosol Liquid Gas Aerosol Solid Gas Foam Gas Liquid Solid foam Gas Solid Emulsion Liquid Liquid Solid emulsion Liquid Solid Sol Solid Liquid Solid sol Solid Solid Fog Gas Smoke Whipped Cream Marshmallow Milk Butter Paint; cell fluid Opal
75 Coloides Tipo de coloide FI FE Ejemplo Aerosol Liquid Gas Aerosol Solid Gas Foam Gas Liquid Solid foam Gas Solid Emulsion Liquid Liquid Solid emulsion Liquid Solid Sol Solid Liquid Solid sol Solid Solid Fog Gas Smoke Whipped Cream Marshmallow Milk Butter Paint Opal, pearl
76 < 1 nm > 100 nm SOLUCIONES COLOIDES SUSPENSIONES Atomos simples, moléc.. pequeñas, iones. Transparente Movim.. molecular Nunca sedimenta Agregados de átomos, moléc.. o iones. Transp. ef. Tyndall Mov.. browniano Coagulación (sedim.) Grupos de part., partículas (de minerales (arena)) Translúcido Mov.. por gravedad USANDO SANGRE ENTERA A MODO DE EJEMPLO: Comp. dtos.. en agua: sales, glucosa, gases Prot. plasmáticas: albúminas, globulinas, fibrinógeno Cél.. sanguíneas: glób.. rojos, blancos, plaquetas
77 < 1 nm > 100 nm SOLUCIONES COLOIDES SUSPENSIONES DIFRACCIÓN EN TODAS DIRECCIONES DIFRACCIÓN EN FORMA DE BARRA
78 Coloides Tipos de coloides 1. SOLUCIONES VERDADERAS DE MACROMOLÉCULAS 2. DISPERSIONES COLOIDALES (SOLES) 3. COLOIDES DE ASOCIACIÓN El elemento común entre las tres clases de coloides es el hecho de que son sostenidos en la dispersión por interacciones electrostáticas con las moléculas de agua. Las tres clases de coloides diferencian en su composición química.
79 Coloides 1. SOLUCIONES VERDADERAS DE MACROMOLÉCULAS Se caracterizan por una fuerte interacción con el agua, por lo que generan el coloide espontáneamente cuando se introducen en el medio. - Termodinámicamente estables - Liofílicos (reversibles) - Ej.: prot., MC, goma de tragacanto,,... Moléculas grandes con grupos funcionales que producen enlaces de hidrógeno con las moléculas de agua.
80 2. DISPERSIONES COLOIDALES = SOLES = Suspensiones coloidales Termodinámicamente inestables Liofóbicos (irreversibles) Fase dispersa polimérica = LATEX Coloides Reticulación química o física que atrapa al dte. = GEL Doble capa eléctrica Las arcillas forman una carga negativa en su superficie cuando están en contacto con agua, y permanecen en la suspensión por la interacción electrostática entre su carga superficial negativa y la carga positiva de cationes del agua.
81 3. COLOIDES DE ASOCIACIÓN Termodinámicamente estables Liofílicos (reversibles) Ej.: tensioactivos que forman micelas Coloides Agregados de moléculas anfifílicas CMC (Concentración por encima de la cuál se empiezan a formar las micelas) Interacción electrostática de las cabezas polares de las micelas con el agua
82 Coloides 3. COLOIDES DE ASOCIACIÓN Concentration del tensioactivo por debajo de la CMC Concentration del tensioactivo por encima de la CMC 82
83 Coloides 3. COLOIDES DE ASOCIACIÓN CAMBIOS DE PROPIEDADES Magnitud de la propiedad CMC TENSIÓN SUPERFICIAL Concentración del tensioactivo 83
84 Coloides 3. COLOIDES DE ASOCIACIÓN CAMBIOS DE PROPIEDADES Magnitud de la propiedad CMC TENSIÓN SUPERFICIAL SOLUBILIDAD DE UN SOLUTO APOLAR Concentración del tensioactivo 84
85 Soluto apolar Concentration del tensioactivo por debajo de la CMC Concentration del tensioactivo por encima 85 de la CMC
86 Coloides Métodos de obtención 1. Métodos de condensación 2. Métodos de dispersión 3. Adición simple de la fase dispersa al medio de dispersión
87 Coloides Métodos de obtención 1. Métodos de condensación Crecimiento de partículas hasta tamaño coloidal: se parte de una solución verdadera y por reacción química se obtienen partículas insolubles de tamaño coloidal
88 Coloides Métodos de obtención 2. Métodos de dispersión Se parte de partículas mayores de tamaño coloidal: - Dispersión mecánica: molino coloidal (actúa por cizalla) - Dispersión eléctrica: arco voltaico entre dos electrodos del metal que se quiere dispersar
89 Coloides Métodos de obtención 3. Adición simple de la FI al medio de dispersión (Para sustancias que forman espontáneamente soluciones coloidales) Ejemplos: proteínas (albúmina, hemoglobina,...) polisacáridos (almidón, MC, dextrinas,...)
90 Coloides Métodos de eliminación de coloides Las partículas coloidales son demasiado pequeñas para ser separadas por métodos físicos (e.g. filtración). Se puede provocar la coagulación de las partículas coloidales (aumentan de tamaño) hasta que puedan ser eliminadas por filtración. 90
91 Coloides Métodos de eliminación de coloides MÉTODOS DE COAGULACIÓN Calentamiento (se facilita la colisión entre las partículas y su atracción entre ellas) Adición de electrolitos (neutralización de las cargas superficiales de las partículas coloidales) Diálisis: uso de membranas semipermeables que separan iones de partículas coloidales. 91
SISTEMA DISPERSO. Fase interna, discontinua o dispersa. Fase externa, continua o dispersante
 SISTEMA DISPERSO Fase interna, discontinua o dispersa Fase externa, continua o dispersante Tipos de sistema disperso TIPO DE DISPERSION TAMAÑO DE PARTICULA EJEMPLO Molecular (disolución) Coloidal < 1 nm
SISTEMA DISPERSO Fase interna, discontinua o dispersa Fase externa, continua o dispersante Tipos de sistema disperso TIPO DE DISPERSION TAMAÑO DE PARTICULA EJEMPLO Molecular (disolución) Coloidal < 1 nm
Coloides en la vida diaria
 COLOIDES 2017 Por qué la leche es blanca? Por qué se corta si la dejamos fuera de la heladera? Por qué para preparar mayonesa hay que batir? Por qué la receta lleva huevo? Por qué la clara de huevo es
COLOIDES 2017 Por qué la leche es blanca? Por qué se corta si la dejamos fuera de la heladera? Por qué para preparar mayonesa hay que batir? Por qué la receta lleva huevo? Por qué la clara de huevo es
SUSPENSIONES. Mercedes Fernández Arévalo
 Mercedes Fernández Arévalo CLASIFICACIÓN DE OSTWALD FI Ø part. > 0.1 µm Dispersiones groseras 0.1 µm m > Ø part. > 0.001 µm Coloides Ø part. < 0.1 µm Soluciones verdades ESTADO DE AGREGACIÓN DE LA MATERIA
Mercedes Fernández Arévalo CLASIFICACIÓN DE OSTWALD FI Ø part. > 0.1 µm Dispersiones groseras 0.1 µm m > Ø part. > 0.001 µm Coloides Ø part. < 0.1 µm Soluciones verdades ESTADO DE AGREGACIÓN DE LA MATERIA
Interacciones a nivel de la interfase y otros fenómenos interfaciales. Capítulo 3: Propiedades físicoquímicas de sistemas dispersos
 Interacciones a nivel de la interfase y otros fenómenos interfaciales Capítulo 3: Propiedades físicoquímicas de sistemas dispersos Lunes, 7 de septiembre de 2009 Las fuerzas de interacción entre interfases
Interacciones a nivel de la interfase y otros fenómenos interfaciales Capítulo 3: Propiedades físicoquímicas de sistemas dispersos Lunes, 7 de septiembre de 2009 Las fuerzas de interacción entre interfases
Soluciones y dispersiones
 COLOIDES 2016 Soluciones y dispersiones Soluciones verdaderas Mezcla de especies dispersadas como moléculas individuales Soluto y disolvente con pesos moleculares comparables DG < 0: Termodinam. estables
COLOIDES 2016 Soluciones y dispersiones Soluciones verdaderas Mezcla de especies dispersadas como moléculas individuales Soluto y disolvente con pesos moleculares comparables DG < 0: Termodinam. estables
Tema 2: Dispersiones (1) Material preparado por VChan 1
 MATERIA: Cualquier cosa que ocupa espacio y tiene masa. Es todo lo que nos rodea. 2.1 Proceso de disolución Velocidad de disolución Material preparado por: Licda. Victoria Chan Escuela de Química/ ITCR
MATERIA: Cualquier cosa que ocupa espacio y tiene masa. Es todo lo que nos rodea. 2.1 Proceso de disolución Velocidad de disolución Material preparado por: Licda. Victoria Chan Escuela de Química/ ITCR
C O L O I D E S Y SUSPENCIONES
 C O L O I D E S Y SUSPENCIONES 1 C O L O I D E S SOLUCIÓN IDEAL SUSPENSIÓN COLOIDAL CRISTALES PRECIPITADOS HOMOGÉNEA SEMI-HOMOGÉNEA HETEROGÉNEA Fase dispersa : Partículas (sólidos) suspendidas en un medio
C O L O I D E S Y SUSPENCIONES 1 C O L O I D E S SOLUCIÓN IDEAL SUSPENSIÓN COLOIDAL CRISTALES PRECIPITADOS HOMOGÉNEA SEMI-HOMOGÉNEA HETEROGÉNEA Fase dispersa : Partículas (sólidos) suspendidas en un medio
1. MATERIA Y SU ASPECTO
 1. MATERIA Y SU ASPECTO El aspecto de un sistema material puede variar según el método de observación. Algunos sistemas materiales como la leche, la sangre o la mantequilla a simple vista parecen uniformes,
1. MATERIA Y SU ASPECTO El aspecto de un sistema material puede variar según el método de observación. Algunos sistemas materiales como la leche, la sangre o la mantequilla a simple vista parecen uniformes,
Disoluciones. Qué es una mezcla? Concepto de Mezcla 12/05/2014
 Disoluciones Profesora: Karina Oñate Fuentes Asignatura: Química- Plan común Nivel: 2º año medio Qué es una mezcla? Los compuestos químicos pueden unirse para reaccionar o mezclarse. En el primer caso
Disoluciones Profesora: Karina Oñate Fuentes Asignatura: Química- Plan común Nivel: 2º año medio Qué es una mezcla? Los compuestos químicos pueden unirse para reaccionar o mezclarse. En el primer caso
FACULTAD DE MEDICINA LICENCIATURA EN NUTRICIÓN FISICOQUÍMICA SEPTIEMBRE 2015
 UNIVERSIDAD AUTÓNOMA DEL ESTADO DE MÉXICO FACULTAD DE MEDICINA LICENCIATURA EN NUTRICIÓN FISICOQUÍMICA SEPTIEMBRE 2015 ESTADOS DE DISPERSIÓN Dra. en C.A.R.N YAMEL LIBIEN JIMÉNEZ SEPTIEMBRE 2015 OBJETIVO
UNIVERSIDAD AUTÓNOMA DEL ESTADO DE MÉXICO FACULTAD DE MEDICINA LICENCIATURA EN NUTRICIÓN FISICOQUÍMICA SEPTIEMBRE 2015 ESTADOS DE DISPERSIÓN Dra. en C.A.R.N YAMEL LIBIEN JIMÉNEZ SEPTIEMBRE 2015 OBJETIVO
UNIVERSIDAD CENTRAL DE VENEZUELA ESCUELA DE AGRONOMÍA FACULTAD DE AGRONOMÍA DEPARTAMENTO DE QUIMÍCA Y TECNOLOGÍA CÁTEDRA QUÍMICA ANALÍTICA
 UNIVERSIDAD CENTRAL DE VENEZUELA ESCUELA DE AGRONOMÍA FACULTAD DE AGRONOMÍA DEPARTAMENTO DE QUIMÍCA Y TECNOLOGÍA CÁTEDRA QUÍMICA ANALÍTICA Venezuela-Maracay Contenido: Importancia. Qué es un coloide? Clasificación
UNIVERSIDAD CENTRAL DE VENEZUELA ESCUELA DE AGRONOMÍA FACULTAD DE AGRONOMÍA DEPARTAMENTO DE QUIMÍCA Y TECNOLOGÍA CÁTEDRA QUÍMICA ANALÍTICA Venezuela-Maracay Contenido: Importancia. Qué es un coloide? Clasificación
Tema 18. Tema 18 (II) Disoluciones Tipos de disoluciones Tipos de disoluciones Propiedades físicas de las disoluciones
 Tema 18 (II) 18.1 Tipos de disoluciones 18.2 Propiedades físicas de las disoluciones Disoluciones 18.3 Macromoléculas y coloides 1 2 18.1 Tipos de disoluciones Una DISOLUCIÓN es una mezcla homogénea de
Tema 18 (II) 18.1 Tipos de disoluciones 18.2 Propiedades físicas de las disoluciones Disoluciones 18.3 Macromoléculas y coloides 1 2 18.1 Tipos de disoluciones Una DISOLUCIÓN es una mezcla homogénea de
Estabilidad de los Sistemas Coloidales
 Capítulo 5 Estabilidad de los Sistemas Coloidales SISTEMAS COLOIDALES en FARMACIA c Dr. Licesio J. Rodríguez ljr@usal.es - http://www3.usal.es/licesio/ Departamento de Química física - Facultad de Farmacia
Capítulo 5 Estabilidad de los Sistemas Coloidales SISTEMAS COLOIDALES en FARMACIA c Dr. Licesio J. Rodríguez ljr@usal.es - http://www3.usal.es/licesio/ Departamento de Química física - Facultad de Farmacia
CAPITULO 4. LA OPERACIÓN UNITARIA COMO PROCESO DE TRANSFERENCIA DE MASA, ENERGÍA Y/O CANTIDAD DE MOVIMIENTO PROF. JOSE MAYORGA
 UNIVERSIDAD DE LOS ANDES FACULTAD DE INGENIERIA INGENIERIA QUIMICA INTRODUCCIÓN A LA INGENIERIA QUIMICA CAPITULO 4. LA OPERACIÓN UNITARIA COMO PROCESO DE TRANSFERENCIA DE MASA, ENERGÍA Y/O CANTIDAD DE
UNIVERSIDAD DE LOS ANDES FACULTAD DE INGENIERIA INGENIERIA QUIMICA INTRODUCCIÓN A LA INGENIERIA QUIMICA CAPITULO 4. LA OPERACIÓN UNITARIA COMO PROCESO DE TRANSFERENCIA DE MASA, ENERGÍA Y/O CANTIDAD DE
M A T E R I A L E S. Sistemas dispersivos
 M A T E R I A L E S Sistemas dispersivos I FISICOQUIMICA DE SUPERFICIES SUPERFICIE: es la superficie de contacto entre un gas y una fase condensada (líquido o sólido). INTERFASE: es la superficie de contacto
M A T E R I A L E S Sistemas dispersivos I FISICOQUIMICA DE SUPERFICIES SUPERFICIE: es la superficie de contacto entre un gas y una fase condensada (líquido o sólido). INTERFASE: es la superficie de contacto
M A T E R I A L E S. Sistemas dispersivos
 M A T E R I A L E S Sistemas dispersivos I FISICOQUIMICA DE SUPERFICIES SUPERFICIE: es la superficie de contacto entre un gas y una fase condensada (líquido o sólido). INTERFASE: es la superficie de contacto
M A T E R I A L E S Sistemas dispersivos I FISICOQUIMICA DE SUPERFICIES SUPERFICIE: es la superficie de contacto entre un gas y una fase condensada (líquido o sólido). INTERFASE: es la superficie de contacto
REOLOGÍA (Bingham 1920)
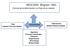 REOLOGÍA (Bingham 1920) Ciencia de la deformación y el flujo de la materia Flujo Líquidos Viscosos Ideales Viscoelasticidad Deformación Sólidos Elásticos Ideales Ingeniería Procesos industriales Polímeros
REOLOGÍA (Bingham 1920) Ciencia de la deformación y el flujo de la materia Flujo Líquidos Viscosos Ideales Viscoelasticidad Deformación Sólidos Elásticos Ideales Ingeniería Procesos industriales Polímeros
14/08/2017. Mezcla Es la unión física de 2 o más sustancias
 Compilado por: Ing. Nelson Velásquez MATERIA Sustancias Formadas por el mismo tipo de átomos o moléculas. Responden a una sola fórmula definida. Mezclas Formadas por distintos tipos de átomos y moléculas,
Compilado por: Ing. Nelson Velásquez MATERIA Sustancias Formadas por el mismo tipo de átomos o moléculas. Responden a una sola fórmula definida. Mezclas Formadas por distintos tipos de átomos y moléculas,
Una mezcla es un compuesto formado por varias sustancias con distintas propiedades
 COMPOSICIÓN DE LA MATERIA Mezclas homogéneas y heterogéneas Una mezcla es un compuesto formado por varias sustancias con distintas propiedades Algunos sistemas materiales como la leche a simple vista parecen
COMPOSICIÓN DE LA MATERIA Mezclas homogéneas y heterogéneas Una mezcla es un compuesto formado por varias sustancias con distintas propiedades Algunos sistemas materiales como la leche a simple vista parecen
Propiedades funcionales
 Propiedades funcionales Se define como: toda propiedad no nutricional que influencia la utilidad de un ingrediente en un alimento. La mayor parte de las propiedades funcionales influyen sobre el carácter
Propiedades funcionales Se define como: toda propiedad no nutricional que influencia la utilidad de un ingrediente en un alimento. La mayor parte de las propiedades funcionales influyen sobre el carácter
Clasificación de la materia
 Clasificación de la materia La materia puede estar en forma de sustancias puras o mezclas. Materia Sustancias Puras Mezclas Elemento Compuesto Homogéneas Heterogéneas Disoluciones Coloides Suspensiones
Clasificación de la materia La materia puede estar en forma de sustancias puras o mezclas. Materia Sustancias Puras Mezclas Elemento Compuesto Homogéneas Heterogéneas Disoluciones Coloides Suspensiones
TEMA 6 MEZCLAS Y DISOLUCIONES
 TEMA 6 MEZCLAS Y DISOLUCIONES 1 Contenidos: 1. Tipos de disoluciones 2. El proceso de disolución 3. Formas de expresar la concentración. 4. Solubilidad. Factores que afectan a la solubilidad 5. Propiedades
TEMA 6 MEZCLAS Y DISOLUCIONES 1 Contenidos: 1. Tipos de disoluciones 2. El proceso de disolución 3. Formas de expresar la concentración. 4. Solubilidad. Factores que afectan a la solubilidad 5. Propiedades
REPÚBLICA BOLIVARIANA DE VENEZUELA MINISTERIO DEL PODER POPULAR PARA LA DEFENSA UNIVERSIDAD NACIONAL EXPERIMENTAL POLITÉCNICA DE LA FUERZA ARMADA
 REPÚBLICA BOLIVARIANA DE VENEZUELA MINISTERIO DEL PODER POPULAR PARA LA DEFENSA UNIVERSIDAD NACIONAL EXPERIMENTAL POLITÉCNICA DE LA FUERZA ARMADA NACIONAL NÚCLEO FALCÓN SEDE PUNTO FIJO CATEDRA: FISICOQUIMICA
REPÚBLICA BOLIVARIANA DE VENEZUELA MINISTERIO DEL PODER POPULAR PARA LA DEFENSA UNIVERSIDAD NACIONAL EXPERIMENTAL POLITÉCNICA DE LA FUERZA ARMADA NACIONAL NÚCLEO FALCÓN SEDE PUNTO FIJO CATEDRA: FISICOQUIMICA
Coloides y Suspensiones Osmosis y Diálisis. SEMANA 10 Licda. Lilian Judith Guzmán Melgar
 Coloides y Suspensiones Osmosis y Diálisis SEMANA 10 Licda. Lilian Judith Guzmán Melgar SUSPENSIONES Las suspensiones son mezclas heterogéneas formadas por una fase sólida (polvo o pequeñas partículas
Coloides y Suspensiones Osmosis y Diálisis SEMANA 10 Licda. Lilian Judith Guzmán Melgar SUSPENSIONES Las suspensiones son mezclas heterogéneas formadas por una fase sólida (polvo o pequeñas partículas
Tema 2: Fuerzas intermoleculares
 Tema 2: Fuerzas intermoleculares Fuerzas intermoleculares: ion dipolo, dipolo dipolo, dispersión de London y puentes de hidrógeno. Gases ideales y reales. Propiedades de los ĺıquidos. Presión de vapor.
Tema 2: Fuerzas intermoleculares Fuerzas intermoleculares: ion dipolo, dipolo dipolo, dispersión de London y puentes de hidrógeno. Gases ideales y reales. Propiedades de los ĺıquidos. Presión de vapor.
líquido sólido Interfase sólido-líquido
 INTERFASES La mayoría de los procesos fisicoquímicos naturales y artificiales ocurren en sistemas heterogéneos en donde las diferentes fases que las componen están separadas por una interfase, definida
INTERFASES La mayoría de los procesos fisicoquímicos naturales y artificiales ocurren en sistemas heterogéneos en donde las diferentes fases que las componen están separadas por una interfase, definida
El primer caso es un ejemplo de mezcla heterogénea porque aprecias los componentes que la forman.
 Otras disoluciones por Cristina Andrade Guevara Figura 1. Glass of water Figura 3. Glass of water Supón que tienes un vaso con agua y le agregas aserrín. Durante algún tiempo, las partículas de aserrín
Otras disoluciones por Cristina Andrade Guevara Figura 1. Glass of water Figura 3. Glass of water Supón que tienes un vaso con agua y le agregas aserrín. Durante algún tiempo, las partículas de aserrín
Tema 8: Disoluciones y sus propiedades
 Tema 8: Disoluciones y sus propiedades Francisco G. Calvo-Flores Contenidos 8-1 Disoluciones y tipos 8-2 Unidades de concentración 8-3 Disoluciones ideales y no ideales 8-4 Formación de disoluciones: equilibrio
Tema 8: Disoluciones y sus propiedades Francisco G. Calvo-Flores Contenidos 8-1 Disoluciones y tipos 8-2 Unidades de concentración 8-3 Disoluciones ideales y no ideales 8-4 Formación de disoluciones: equilibrio
DEPARTAMENTO DE BIOQUÍMICA ESFUNO EUTM AGUA Y SOLUCIONES
 DEPARTAMENTO DE BIOQUÍMICA ESFUNO EUTM AGUA Y SOLUCIONES La molécula de agua La molécula de agua Líquido, sólido o gaseoso: existen los tres en la tierra Solvente Universal: por lo que es casi imposible
DEPARTAMENTO DE BIOQUÍMICA ESFUNO EUTM AGUA Y SOLUCIONES La molécula de agua La molécula de agua Líquido, sólido o gaseoso: existen los tres en la tierra Solvente Universal: por lo que es casi imposible
Fuerzas intermoleculares y líquidos y sólidos
 Fuerzas intermoleculares y líquidos y sólidos Capítulo 11 Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display. Una fase es la parte homógenea de un sistema en contacto
Fuerzas intermoleculares y líquidos y sólidos Capítulo 11 Copyright The McGraw-Hill Companies, Inc. Permission required for reproduction or display. Una fase es la parte homógenea de un sistema en contacto
SISTEMAS MATERIALES. Departamento de Física y Química 2º ESO
 SISTEMAS MATERIALES Departamento de Física y Química 2º ESO 0. Mapa conceptual MATERIA Sustancias puras Mezclas Heterogéneas Homogéneas Sistemas coloidales Técnicas de separación Disoluciones Soluto Disolvente
SISTEMAS MATERIALES Departamento de Física y Química 2º ESO 0. Mapa conceptual MATERIA Sustancias puras Mezclas Heterogéneas Homogéneas Sistemas coloidales Técnicas de separación Disoluciones Soluto Disolvente
FUERZAS INTERMOLECULARES
 FUERZAS INTERMOLECULARES Dentro de una molécula, los átomos están unidos mediante fuerzas intramoleculares (enlaces iónicos, metálicos o covalentes, principalmente). Estas son las fuerzas que se deben
FUERZAS INTERMOLECULARES Dentro de una molécula, los átomos están unidos mediante fuerzas intramoleculares (enlaces iónicos, metálicos o covalentes, principalmente). Estas son las fuerzas que se deben
Aprendizajes esperados
 Disoluciones II Aprendizajes esperados Identificar diluciones. Identificar los factores que afectan la solubilidad. Definir propiedades coligativas. Pregunta oficial PSU Al bajar gradualmente la temperatura,
Disoluciones II Aprendizajes esperados Identificar diluciones. Identificar los factores que afectan la solubilidad. Definir propiedades coligativas. Pregunta oficial PSU Al bajar gradualmente la temperatura,
TRATADO DE TECNOLOGÍA FARMACÉUTICA (VOL. I) HACIA UNA QUÍMICA PARA EL SIGLO XXI
 TRATADO DE TECNOLOGÍA FARMACÉUTICA (VOL. I) HACIA UNA QUÍMICA PARA EL SIGLO XXI Proyecto editorial BiBlioteca de Químicas director: Carlos Seoane Prado catedrático de Química orgánica universidad complutense
TRATADO DE TECNOLOGÍA FARMACÉUTICA (VOL. I) HACIA UNA QUÍMICA PARA EL SIGLO XXI Proyecto editorial BiBlioteca de Químicas director: Carlos Seoane Prado catedrático de Química orgánica universidad complutense
Tema 5.-Propiedades de transporte
 Tema 5.- Propiedades de transporte Tema 5.-Propiedades de transporte 5.1-Teoría cinética de los gases 5.2.-Difusión 5.3.-Sedimentación 5.4.-Viscosidad 5.5.-Electroforesis 5.1-Teoría cinética de los gases
Tema 5.- Propiedades de transporte Tema 5.-Propiedades de transporte 5.1-Teoría cinética de los gases 5.2.-Difusión 5.3.-Sedimentación 5.4.-Viscosidad 5.5.-Electroforesis 5.1-Teoría cinética de los gases
Tema 5.- Propiedades de transporte
 Tema 5.- Propiedades de transporte Tema 5.-Propiedades de transporte 5.1-Teoría cinética de los gases 5.2.-Difusión 5.3.-Sedimentación 5.4.-Viscosidad 5.5.-Electroforesis 5.1-Teoría cinética de los gases
Tema 5.- Propiedades de transporte Tema 5.-Propiedades de transporte 5.1-Teoría cinética de los gases 5.2.-Difusión 5.3.-Sedimentación 5.4.-Viscosidad 5.5.-Electroforesis 5.1-Teoría cinética de los gases
Teoría Cinético-Molecular. Fuerzas Intermoleculares y Líquidos y Sólidos. Fase. Fuerzas 18/08/2011
 Fuerzas Intermoleculares y Líquidos y Sólidos Teoría Cinético-Molecular Gases (moleculas bien separadas) Líquidos y Sólidos (moléculas bien cercanas) Qué es una fase? Basado en Capítulo 11 de Química (Chang,
Fuerzas Intermoleculares y Líquidos y Sólidos Teoría Cinético-Molecular Gases (moleculas bien separadas) Líquidos y Sólidos (moléculas bien cercanas) Qué es una fase? Basado en Capítulo 11 de Química (Chang,
Clasificación de los sistemas dispersos según el tamaño de las partículas de la fase interna
 Clasificación de los sistemas dispersos según el tamaño de las partículas de la fase interna Denominación Características Ejemplo Disoluciones Tamaño de partícula de la fase dispersa menor de 1 nm. La
Clasificación de los sistemas dispersos según el tamaño de las partículas de la fase interna Denominación Características Ejemplo Disoluciones Tamaño de partícula de la fase dispersa menor de 1 nm. La
A continuación se detallan cada una de las propiedades coligativas:
 PREGUNTA (Técnico Profesional) Se prepara una solución con 2 mol de agua y 0,5 mol de un electrolito no volátil. Al respecto, cuál es la presión de vapor a 25 ºC de esta solución, si la presión del agua
PREGUNTA (Técnico Profesional) Se prepara una solución con 2 mol de agua y 0,5 mol de un electrolito no volátil. Al respecto, cuál es la presión de vapor a 25 ºC de esta solución, si la presión del agua
PSU MÓDULO COMÚN QUÍMICA PROPIEDADES COLIGATIVAS
 DEPARTAMENTO DE CIENCIAS PSU_MÓDULO COMÚN DE QUÍMICA PSU MÓDULO COMÚN QUÍMICA PROPIEDADES COLIGATIVAS Corresponden a las nuevas propiedades del solvente, debido que el soluto altera al solvente puro en
DEPARTAMENTO DE CIENCIAS PSU_MÓDULO COMÚN DE QUÍMICA PSU MÓDULO COMÚN QUÍMICA PROPIEDADES COLIGATIVAS Corresponden a las nuevas propiedades del solvente, debido que el soluto altera al solvente puro en
Energías de Interacción
 Química General e Inorgánica A Energías de Interacción Tema 7 Fuerzas intermoleculares Fuerzas intermoleculares son fuerzas de atracción entre las moléculas Fuerzas intramoleculares mantienen juntos a
Química General e Inorgánica A Energías de Interacción Tema 7 Fuerzas intermoleculares Fuerzas intermoleculares son fuerzas de atracción entre las moléculas Fuerzas intramoleculares mantienen juntos a
S.E.P. S.E.I.T DIRECCION GENERAL DE INSTITUTOS TECNOLOGICOS
 S.E.P. S.E.I.T DIRECCION GENERAL DE INSTITUTOS TECNOLOGICOS NOMBRE DE LA ASIGNATURA: FISICOQUIMICA I (4-2-10) NIVEL: LICENCIATURA CARRERA: INGENIERIA BIOQUIMICA CLAVE: BQC-9314 TEMARIO: NUM. TEMAS SUBTEMAS
S.E.P. S.E.I.T DIRECCION GENERAL DE INSTITUTOS TECNOLOGICOS NOMBRE DE LA ASIGNATURA: FISICOQUIMICA I (4-2-10) NIVEL: LICENCIATURA CARRERA: INGENIERIA BIOQUIMICA CLAVE: BQC-9314 TEMARIO: NUM. TEMAS SUBTEMAS
PROGRAMA ACADÉMICO SEMILLERO DE QUÍMICA
 PROGRAMA ACADÉMICO SEMILLERO DE QUÍMICA UNIDAD 1: MATERIA Y MEDICIÓN CLASE TEMAS SUBTEMAS JUSTIFICACIÓN 1 2 3 MATERIA Y MEDICIÓN La química. Ramas de la química. La materia. Estados de la Materia Clasificación
PROGRAMA ACADÉMICO SEMILLERO DE QUÍMICA UNIDAD 1: MATERIA Y MEDICIÓN CLASE TEMAS SUBTEMAS JUSTIFICACIÓN 1 2 3 MATERIA Y MEDICIÓN La química. Ramas de la química. La materia. Estados de la Materia Clasificación
ESTADOS DE AGREGACIÓN DE LA MATERIA FLUIDOS
 FLUIDOS LÍQUIDOS ESTADOS DE AGREGACIÓN DE LA MATERIA FLUIDOS CONCEPTO DE FLUIDO Los líquidos y los gases son fluidos porque las partículas están dispuestas de forma más desordenada que en los sólidos,
FLUIDOS LÍQUIDOS ESTADOS DE AGREGACIÓN DE LA MATERIA FLUIDOS CONCEPTO DE FLUIDO Los líquidos y los gases son fluidos porque las partículas están dispuestas de forma más desordenada que en los sólidos,
Tema 2: Dispersiones III parte Propiedades Coligativas. Propiedades de las disoluciones. Material preparado por: Licda.
 Tema 2: Dispersiones III parte Propiedades de las disoluciones Material preparado por: Licda. Victoria Chan Propiedades de las Disoluciones Propiedades constitutivas: propiedades físicas que dependen de
Tema 2: Dispersiones III parte Propiedades de las disoluciones Material preparado por: Licda. Victoria Chan Propiedades de las Disoluciones Propiedades constitutivas: propiedades físicas que dependen de
GAS GAS GASESOSA GAS LIQUIDO LIQUIDA LIQUIDO LIQUIDO LIQUIDA LIQUIDO SOLIDO SOLIDA SOLIDO LIQUIDO LIQUIDA SOLIDO SOLIDO SOLIDA
 Resumen química segundo modulo SEMANA 7 (AGUA, SOLUCIONES, DENSIDAD Y UNIDADES RELATIVAS) AGUA: forma puentes de hidrogeno muy fuertes Punto de ebullición 100 C y fusión 0 Densidad 1g/mL Calor especifico
Resumen química segundo modulo SEMANA 7 (AGUA, SOLUCIONES, DENSIDAD Y UNIDADES RELATIVAS) AGUA: forma puentes de hidrogeno muy fuertes Punto de ebullición 100 C y fusión 0 Densidad 1g/mL Calor especifico
Tema 4. Fuerzas intermoleculares
 Tema 4: Fuerzas intermoleculares Química para biólogos Slide 1 of 35 Contenidos 4-1 Electronegatividad 4-2 Polaridad de enlace y molécula: momento dipolar 4-3 Fuerzas intermoleclares 4-4 Puentes de hidrógeno
Tema 4: Fuerzas intermoleculares Química para biólogos Slide 1 of 35 Contenidos 4-1 Electronegatividad 4-2 Polaridad de enlace y molécula: momento dipolar 4-3 Fuerzas intermoleclares 4-4 Puentes de hidrógeno
COMPOSICIÓN QUÍMICA DE LA MATERIA VIVA
 COMPOSICIÓN QUÍMICA DE LA MATERIA VIVA ELEMENTOS QUÍMICOS: 110 BIOELEMENTOS ( Elementos biogénicos): 25-30 Forman parte de la materia viva, aunque no son exclusivos de ella No son los más abundantes, pero
COMPOSICIÓN QUÍMICA DE LA MATERIA VIVA ELEMENTOS QUÍMICOS: 110 BIOELEMENTOS ( Elementos biogénicos): 25-30 Forman parte de la materia viva, aunque no son exclusivos de ella No son los más abundantes, pero
Conductividad en presencia de campo eléctrico
 6. Fenómenos de transporte Fenómenos de transporte Conductividad térmicat Viscosidad Difusión n sedimentación Conductividad en presencia de campo eléctrico UAM 01-13. Química Física. Transporte CT V 1
6. Fenómenos de transporte Fenómenos de transporte Conductividad térmicat Viscosidad Difusión n sedimentación Conductividad en presencia de campo eléctrico UAM 01-13. Química Física. Transporte CT V 1
UNIDAD 1 La materia y sus cambios
 UNIDAD 1 La materia y sus cambios Tema 1.2 Composición de la materia. Sustancias y mezclas. Mezclas homogéneas, heterogéneas y coloides. Introducción a las disoluciones: no saturadas, saturadas y sobresaturadas.
UNIDAD 1 La materia y sus cambios Tema 1.2 Composición de la materia. Sustancias y mezclas. Mezclas homogéneas, heterogéneas y coloides. Introducción a las disoluciones: no saturadas, saturadas y sobresaturadas.
Profesor: Carlos Gutiérrez Arancibia. Temas a tratar: - - Sustancias Puras - Mezclas - Enlaces Químicos - Fuerzas Intermoleculares
 Profesor: Carlos Gutiérrez Arancibia Temas a tratar: - - Sustancias Puras - Mezclas - Enlaces Químicos - Fuerzas Intermoleculares A. Sustancia Pura: SUSTANCIAS PURAS Y MEZCLAS Una sustancia pura es un
Profesor: Carlos Gutiérrez Arancibia Temas a tratar: - - Sustancias Puras - Mezclas - Enlaces Químicos - Fuerzas Intermoleculares A. Sustancia Pura: SUSTANCIAS PURAS Y MEZCLAS Una sustancia pura es un
CÁTEDRA: FÍSICO-QUÍMICA
 CÁTEDRA: FÍSICO-QUÍMICA UNIDAD 2 Tema E Tensión Superficial Bibliografía: Glasstone, Barrow D. Tensión superficial. Tensión superficial. Energía superficial. Unidades. Mojabilidad y humectación. Ángulo
CÁTEDRA: FÍSICO-QUÍMICA UNIDAD 2 Tema E Tensión Superficial Bibliografía: Glasstone, Barrow D. Tensión superficial. Tensión superficial. Energía superficial. Unidades. Mojabilidad y humectación. Ángulo
Base molecular de la vida. TEMA 6 LIBRO (Pág. 131)
 Base molecular de la vida TEMA 6 LIBRO (Pág. 131) GUIÓN TEMA Bioelementos Biomoléculas inorgánicas Agua Sales minerales Ósmosis Biomoléculas orgánicas Glúcidos Lípidos Proteínas Ácidos nucleicos Bioelementos
Base molecular de la vida TEMA 6 LIBRO (Pág. 131) GUIÓN TEMA Bioelementos Biomoléculas inorgánicas Agua Sales minerales Ósmosis Biomoléculas orgánicas Glúcidos Lípidos Proteínas Ácidos nucleicos Bioelementos
Tema 5: Disoluciones. (Químic General) Disoluciones 6 de noviembre de / 38
 Tema 5: Disoluciones Tipos de disoluciones. Concentración. Solubilidad de gases. Diagramas de fases de dos componentes. Propiedades coligativas: presión osmótica, disminución del punto de fusión y aumento
Tema 5: Disoluciones Tipos de disoluciones. Concentración. Solubilidad de gases. Diagramas de fases de dos componentes. Propiedades coligativas: presión osmótica, disminución del punto de fusión y aumento
PROPIEDADES Y FUNCIONES BIOLÓGICAS
 EL PROPIEDADES Y FUNCIONES BIOLÓGICAS MOLÉCULA DE AGUA LA MOLÉCULA DE AGUA 104,5º δ = densidad de carga Enlace covalente Puentes de H Aunque es eléctricamente neutra, las moléculas de agua tienen carácter
EL PROPIEDADES Y FUNCIONES BIOLÓGICAS MOLÉCULA DE AGUA LA MOLÉCULA DE AGUA 104,5º δ = densidad de carga Enlace covalente Puentes de H Aunque es eléctricamente neutra, las moléculas de agua tienen carácter
Universidad Nacional Experimental Francisco de Miranda Área de Tecnología Complejo Docente El Sabino Programa Ingeniería Química Cátedra: Fenómeno de
 Universidad Nacional Experimental Francisco de Miranda Área de Tecnología Complejo Docente El Sabino Programa Ingeniería Química Cátedra: Fenómeno de Transporte INTRODUCCION Los fluidos son de gran interés
Universidad Nacional Experimental Francisco de Miranda Área de Tecnología Complejo Docente El Sabino Programa Ingeniería Química Cátedra: Fenómeno de Transporte INTRODUCCION Los fluidos son de gran interés
Tema 2 Dispersiones (1)
 Tema 2 Dispersiones (1) 2.1 Velocidad de disolución Material preparado por: Licda. Victoria Chan Escuela de Química/ ITCR MATERIA:Cualquier cosa que ocupa espacio y tiene masa. Es todo lo que nos rodea.
Tema 2 Dispersiones (1) 2.1 Velocidad de disolución Material preparado por: Licda. Victoria Chan Escuela de Química/ ITCR MATERIA:Cualquier cosa que ocupa espacio y tiene masa. Es todo lo que nos rodea.
Repaso de Sistemas de concentración molar
 Repaso de Sistemas de concentración molar Prof. José A. Pérez Química Analítica 1 Unidades de Concentración molaridad, molalidad, % masa, % volumen, %masa/volumen, partes por mil (ppmil), partes por millón
Repaso de Sistemas de concentración molar Prof. José A. Pérez Química Analítica 1 Unidades de Concentración molaridad, molalidad, % masa, % volumen, %masa/volumen, partes por mil (ppmil), partes por millón
Transferencia de Momentum
 Transferencia de Momentum 1740-2 2014-02-06 3ª. Contenido Aspectos básicos de fluidos Esfuerzo cortante (Stress); Diferencia entre fluido y sólido; Definición de fluido; Ley de la viscosidad de Newton;
Transferencia de Momentum 1740-2 2014-02-06 3ª. Contenido Aspectos básicos de fluidos Esfuerzo cortante (Stress); Diferencia entre fluido y sólido; Definición de fluido; Ley de la viscosidad de Newton;
UNIVERSIDAD AUTÓNOMA CHAPINGO DEPARTAMENTO DE INGENIERÍA AGROINDUSTRIAL FICHA CURRICULAR. Fisicoquímica
 1. Datos generales UNIVERSIDAD AUTÓNOMA CHAPINGO DEPARTAMENTO DE INGENIERÍA AGROINDUSTRIAL FICHA CURRICULAR Departamento Nombre del programa Licenciatura Línea curricular Procesos Unitarios Asignatura
1. Datos generales UNIVERSIDAD AUTÓNOMA CHAPINGO DEPARTAMENTO DE INGENIERÍA AGROINDUSTRIAL FICHA CURRICULAR Departamento Nombre del programa Licenciatura Línea curricular Procesos Unitarios Asignatura
Equilibrio físico. Prof. Jesús Hernández Trujillo. Facultad de Química, UNAM. Equilibrio físico/j. Hdez. T p.
 Equilibrio físico/j. Hdez. T p. 1/34 Equilibrio físico Prof. Jesús Hernández Trujillo jesus.hernandezt@gmail.com Facultad de Química, UNAM Equilibrio físico/j. Hdez. T p. 2/34 Interacciones intermoleculares
Equilibrio físico/j. Hdez. T p. 1/34 Equilibrio físico Prof. Jesús Hernández Trujillo jesus.hernandezt@gmail.com Facultad de Química, UNAM Equilibrio físico/j. Hdez. T p. 2/34 Interacciones intermoleculares
Disoluciones Químicas
 Disoluciones Químicas Las disoluciones son mezclas homogéneas de dos o más sustancias, es decir, cuyos componentes no se pueden distinguir a simple vista. Siempre que se esta en presencia de una mezcla
Disoluciones Químicas Las disoluciones son mezclas homogéneas de dos o más sustancias, es decir, cuyos componentes no se pueden distinguir a simple vista. Siempre que se esta en presencia de una mezcla
Dispersiones Alimenticias
 Los Sistemas Alimenticios se dividen en dos grupos principales: a).- TEJIDOS COMESTIBLES INTACTOS: Son aquellos que no han sido modificados mecánicamente por el hombre. Dentro de estos tenemos: El tejido
Los Sistemas Alimenticios se dividen en dos grupos principales: a).- TEJIDOS COMESTIBLES INTACTOS: Son aquellos que no han sido modificados mecánicamente por el hombre. Dentro de estos tenemos: El tejido
Fundamentos de Química. Horario de Tutorías
 Fundamentos de Química Segundo Cuatrimestre Horario de Tutorías Martes 12:00-14:00 16:00-19:00 Edificio 24B.Tercera Planta 14/02/2006 Tema 11: Propiedades de las disoluciones 11.1 Definición de disolución
Fundamentos de Química Segundo Cuatrimestre Horario de Tutorías Martes 12:00-14:00 16:00-19:00 Edificio 24B.Tercera Planta 14/02/2006 Tema 11: Propiedades de las disoluciones 11.1 Definición de disolución
EL AGUA Y LAS SALES MINERALES
 EL AGUA Y LAS SALES MINERALES 1. EL AGUA DE LA MATERIA VIVA El agua es la molécula más abundante de la materia viva La cantidad de agua en los seres vivos es variable Según el tipo de tejido: más agua
EL AGUA Y LAS SALES MINERALES 1. EL AGUA DE LA MATERIA VIVA El agua es la molécula más abundante de la materia viva La cantidad de agua en los seres vivos es variable Según el tipo de tejido: más agua
SOLUCIONES. Coordinadora de Enseñanza de Bioquímica y Biología Molecular. Fac. de Medicina. UNAM
 SOLUCIONES M. en C. Alicia Cea Bonilla Coordinadora de Enseñanza de Bioquímica y Biología Molecular. Fac. de Medicina. UNAM 1 Qué es una solución? Es una mezcla homogénea de dos o más sustancias. La sustancia
SOLUCIONES M. en C. Alicia Cea Bonilla Coordinadora de Enseñanza de Bioquímica y Biología Molecular. Fac. de Medicina. UNAM 1 Qué es una solución? Es una mezcla homogénea de dos o más sustancias. La sustancia
TEMA 1: LA NATURALEZA BÁSICA DE LA MATERIA QUÉ ELEMENTOS INTEGRAN LA MATERIA VIVA?
 TEMA 1: LA NATURALEZA BÁSICA DE LA MATERIA QUÉ ELEMENTOS INTEGRAN LA MATERIA VIVA? Concepto de Bioquímica Concepto de Bioelemento Los bioelementos, también conocidos como elementos biogénicos, son los
TEMA 1: LA NATURALEZA BÁSICA DE LA MATERIA QUÉ ELEMENTOS INTEGRAN LA MATERIA VIVA? Concepto de Bioquímica Concepto de Bioelemento Los bioelementos, también conocidos como elementos biogénicos, son los
QUÉ ES LA TEMPERATURA?
 1 QUÉ ES LA TEMPERATURA? Nosotros experimentamos la temperatura todos los días. Cuando estamos en verano, generalmente decimos Hace calor! y en invierno Hace mucho frío!. Los términos que frecuentemente
1 QUÉ ES LA TEMPERATURA? Nosotros experimentamos la temperatura todos los días. Cuando estamos en verano, generalmente decimos Hace calor! y en invierno Hace mucho frío!. Los términos que frecuentemente
Para la solución de algunos de los ejercicios propuestos, se adjunta una parte del sistema periódico hasta el elemento Nº 20.
 Programa Estándar Anual Nº Guía práctica Disoluciones I: mezclas, disoluciones y unidades porcentuales de concentración Ejercicios PSU Para la solución de algunos de los ejercicios propuestos, se adjunta
Programa Estándar Anual Nº Guía práctica Disoluciones I: mezclas, disoluciones y unidades porcentuales de concentración Ejercicios PSU Para la solución de algunos de los ejercicios propuestos, se adjunta
cromatografía 03/07/2012 INTRODUCCIÓN Etapas de un análisis cuantitativo Curso: Química Analítica II Loreto Ascar 2012 Proceso Analítico
 cromatografía Curso: Química Analítica II Loreto Ascar 2012 INTRODUCCIÓN Cómo determinar un analito en una muestra problema? X Proceso Analítico Etapas de un análisis cuantitativo Elección del método Obtención
cromatografía Curso: Química Analítica II Loreto Ascar 2012 INTRODUCCIÓN Cómo determinar un analito en una muestra problema? X Proceso Analítico Etapas de un análisis cuantitativo Elección del método Obtención
Enlace Químico: Compuestos Químicos
 Enlace Químico: Compuestos Químicos Contenidos Introducción. Enlace Iónico. Enlace Covalente. S 8 Enlace Metálico. Introducción. En general los objetos están formados por conjuntos de átomos iguales (elementos)
Enlace Químico: Compuestos Químicos Contenidos Introducción. Enlace Iónico. Enlace Covalente. S 8 Enlace Metálico. Introducción. En general los objetos están formados por conjuntos de átomos iguales (elementos)
Escuela del Petróleo - Química
 Escuela del Petróleo - Química 2012 1 Unidad 2 1) Sistema Materiales 2) Materiales Homogéneos y Heterogéneos. a. Separación de las fases b. Sustancia Pura 3) extensivas e intensivas 4) Sistemas dispersos
Escuela del Petróleo - Química 2012 1 Unidad 2 1) Sistema Materiales 2) Materiales Homogéneos y Heterogéneos. a. Separación de las fases b. Sustancia Pura 3) extensivas e intensivas 4) Sistemas dispersos
El agua y las sales minerales
 El agua y las sales minerales El agua El agua es la molécula más abundante de la materia viva La cantidad de agua en los seres vivos es variable Según el tipo de tejido: más agua cuanto más actividad metabólica
El agua y las sales minerales El agua El agua es la molécula más abundante de la materia viva La cantidad de agua en los seres vivos es variable Según el tipo de tejido: más agua cuanto más actividad metabólica
INTRODUCCIÓN A LA TECNOLOGÍA DE MEMBRANAS. Raúl Moliner Salvador. Unidad de Medio Ambiente. 15 Octubre 2009, Castellón de la Plana.
 INTRODUCCIÓN A LA TECNOLOGÍA DE MEMBRANAS Raúl Moliner Salvador. Unidad de Medio Ambiente. 15 Octubre 2009, Castellón de la Plana. Estructura de la presentación 1. Definición y clasificación de las membranas.
INTRODUCCIÓN A LA TECNOLOGÍA DE MEMBRANAS Raúl Moliner Salvador. Unidad de Medio Ambiente. 15 Octubre 2009, Castellón de la Plana. Estructura de la presentación 1. Definición y clasificación de las membranas.
Agua y Soluciones SEMANA 07. Licda. Lilian Judith Guzmán M.
 Agua y Soluciones SEMANA 07 Licda. Lilian Judith Guzmán M. AGUA El agua es el compuesto químico más abundante en los seres vivos y en nuestro planeta, lo cual lo hace ser uno de los compuestos más extraordinarios.
Agua y Soluciones SEMANA 07 Licda. Lilian Judith Guzmán M. AGUA El agua es el compuesto químico más abundante en los seres vivos y en nuestro planeta, lo cual lo hace ser uno de los compuestos más extraordinarios.
SEGUNDO DE BACHILLERATO QUÍMICA. a A + b B c C + d D
 TEMA 5. CINÉTICA QUÍMICA a A + b B c C + d D 1 d[a] 1 d[b] 1 d[c] 1 d[d] mol v = = = + = + a dt b dt c dt d dt L s El signo negativo en la expresión de velocidad es debido a que los reactivos desaparecen,
TEMA 5. CINÉTICA QUÍMICA a A + b B c C + d D 1 d[a] 1 d[b] 1 d[c] 1 d[d] mol v = = = + = + a dt b dt c dt d dt L s El signo negativo en la expresión de velocidad es debido a que los reactivos desaparecen,
Química General. Clase 3 FECHA: 19/05
 Química General Clase 3 FECHA: 19/05 Unidad 3 Enlaces químicos Uniones iónicas, uniones covalentes Enlace iónico. Concepto. Condiciones. Formación de compuestos iónicos. Estructura de los compuestos iónicos.
Química General Clase 3 FECHA: 19/05 Unidad 3 Enlaces químicos Uniones iónicas, uniones covalentes Enlace iónico. Concepto. Condiciones. Formación de compuestos iónicos. Estructura de los compuestos iónicos.
BLOQUE I: LA BASE MOLECULAR Y FÍSICO-QUÍMICA DE LA VIDA. Tema 2.- Componentes químicos de la célula: biomoléculas inorgánicas
 BLOQUE I: LA BASE MOLECULAR Y FÍSICO-QUÍMICA DE LA VIDA Tema 2.- Componentes químicos de la célula: biomoléculas inorgánicas Tema 2.- Componentes químicos de la célula: biomoléculas inorgánicas A.- Los
BLOQUE I: LA BASE MOLECULAR Y FÍSICO-QUÍMICA DE LA VIDA Tema 2.- Componentes químicos de la célula: biomoléculas inorgánicas Tema 2.- Componentes químicos de la célula: biomoléculas inorgánicas A.- Los
Velocidad es la variación de la concentración de una de las sustancias de la reacción con el tiempo. Su unidad es: mol L 1 s 1.
 Cinética es el estudio de la velocidad a la que tienen lugar las reacciones químicas. Los resultados sólo pueden obtenerse por vía experimental y de ellos puede predecirse el camino por el que transcurren
Cinética es el estudio de la velocidad a la que tienen lugar las reacciones químicas. Los resultados sólo pueden obtenerse por vía experimental y de ellos puede predecirse el camino por el que transcurren
Propiedades de la materia. Características de sólidos, líquidos y gases
 Propiedades de la materia Características de sólidos, líquidos y gases Fluidos Líquidos Ej: H 2 O Estados de la materia Gases Ej: O 2 Amorfos Ej: caucho Cristalinos Ej: sal, azúcar Sólidos Metálicos Enlace
Propiedades de la materia Características de sólidos, líquidos y gases Fluidos Líquidos Ej: H 2 O Estados de la materia Gases Ej: O 2 Amorfos Ej: caucho Cristalinos Ej: sal, azúcar Sólidos Metálicos Enlace
Unidad 2. La materia
 Física y Química Unidad 2: La materia Unidad 2. La materia Índice de contenido 1. Estados de agregación de la materia...3 2. Cambios de estado...4 3. Clasificación de la materia...6 3.1.- Métodos de separación
Física y Química Unidad 2: La materia Unidad 2. La materia Índice de contenido 1. Estados de agregación de la materia...3 2. Cambios de estado...4 3. Clasificación de la materia...6 3.1.- Métodos de separación
Unidad 2 Enlace Químico
 Unidad 2 Enlace Químico OPCIÓN A 1. Defina: Resonancia: Concepto propuesto por Pauling para explicar las situaciones en las que ninguna de las posibles estructuras de Lewis de una molécula explica la estructura
Unidad 2 Enlace Químico OPCIÓN A 1. Defina: Resonancia: Concepto propuesto por Pauling para explicar las situaciones en las que ninguna de las posibles estructuras de Lewis de una molécula explica la estructura
CRISTALOQUÍMICA TEMA 9 POLIMORFISMO Y TRANSFORMACIONES POLIMÓRFICAS. TRANSFORMACIONES ORDEN - DESORDEN ÍNDICE
 CRISTALOQUÍMICA TEMA 9 POLIMORFISMO Y TRANSFORMACIONES POLIMÓRFICAS. TRANSFORMACIONES ORDEN - DESORDEN 9.1 Introducción 9.2 Estabilidad y equilibrio ÍNDICE 9.3 Concepto de polimorfismo y de transformación
CRISTALOQUÍMICA TEMA 9 POLIMORFISMO Y TRANSFORMACIONES POLIMÓRFICAS. TRANSFORMACIONES ORDEN - DESORDEN 9.1 Introducción 9.2 Estabilidad y equilibrio ÍNDICE 9.3 Concepto de polimorfismo y de transformación
EQUILIBRIO DE INTERFASES Y CINÉTICA FÍSICA 1637 DEPARTAMENTO DE FISICOQUÍMICA. 6o. NÚMERO DE HORAS/SEMANA Teoría 3 Práctica 3 CRÉDITOS 9
 EQUILIBRIO DE INTERFASES Y CINÉTICA FÍSICA 1637 DEPARTAMENTO DE FISICOQUÍMICA UBICACIÓN SEMESTRE 6o. TIPO DE ASIGNATURA TEÓRICO-PRÁCTICA NÚMERO DE HORAS/SEMANA Teoría 3 Práctica 3 CRÉDITOS 9 Este curso
EQUILIBRIO DE INTERFASES Y CINÉTICA FÍSICA 1637 DEPARTAMENTO DE FISICOQUÍMICA UBICACIÓN SEMESTRE 6o. TIPO DE ASIGNATURA TEÓRICO-PRÁCTICA NÚMERO DE HORAS/SEMANA Teoría 3 Práctica 3 CRÉDITOS 9 Este curso
1. Los estados de la materia
 1. Los estados de la materia Propiedades La materia que nos rodea aparece ante nosotros con muy diversos aspectos. Presenta distintas formas, colores, dureza, fluidez pero en general, consideramos que
1. Los estados de la materia Propiedades La materia que nos rodea aparece ante nosotros con muy diversos aspectos. Presenta distintas formas, colores, dureza, fluidez pero en general, consideramos que
Propiedades fisicoquímicas y funcionales de los alimentos 2015
 TRABAJO PRÁCTICO N 2: EMULSIONES DETERMINACIÓN DE LA ESTABILIDAD DE EMULSIONES POR CONDUCTIMETRÍA, MICROSCOPÍA Y TURBIDIMETRÍA. OBJETIVOS: 1. Determinar la estabilidad de emulsiones por conductimetría,
TRABAJO PRÁCTICO N 2: EMULSIONES DETERMINACIÓN DE LA ESTABILIDAD DE EMULSIONES POR CONDUCTIMETRÍA, MICROSCOPÍA Y TURBIDIMETRÍA. OBJETIVOS: 1. Determinar la estabilidad de emulsiones por conductimetría,
QUÍMICA I. TEMA 10 Equilibrio de solubilidad. Tecnólogo en Minería
 QUÍMICA I TEMA 10 Equilibrio de solubilidad Tecnólogo en Minería O b j e t i v o Examinar las propiedades físicas de las disoluciones y compararlas con las de sus componentes Disoluciones acuosas de sustancias
QUÍMICA I TEMA 10 Equilibrio de solubilidad Tecnólogo en Minería O b j e t i v o Examinar las propiedades físicas de las disoluciones y compararlas con las de sus componentes Disoluciones acuosas de sustancias
MOLÉCULAS POLAReS Y NO POLAReS
 MOLÉCULAS POLAReS Y NO POLAReS Una molécula polar presenta distribución asimétrica de las cargas eléctricas debido a la diferencia de electronegatividad de los átomos que la forman. Presenta dos zonas
MOLÉCULAS POLAReS Y NO POLAReS Una molécula polar presenta distribución asimétrica de las cargas eléctricas debido a la diferencia de electronegatividad de los átomos que la forman. Presenta dos zonas
1. La materia: sustancias puras y mezclas
 RESUMEN de la UNIDAD 3. DIVERSIDAD DE LA MATERIA 1. La materia: sustancias puras y mezclas La principal clasificación que se hace de la materia es en sustancias puras y mezclas. Las sustancias puras tienen
RESUMEN de la UNIDAD 3. DIVERSIDAD DE LA MATERIA 1. La materia: sustancias puras y mezclas La principal clasificación que se hace de la materia es en sustancias puras y mezclas. Las sustancias puras tienen
FÍSICA Y QUÍMICA 2º ESO Tema 2: LA MATERIA Mezclas y Soluciones. Sustancias puras y mezclas
 Sustancias puras y mezclas La materia que nos rodea es, en la mayoría de los casos, una mezcla de sustancias. Los científicos han intentado clasificar las sustancias desde el principio de los tiempos.
Sustancias puras y mezclas La materia que nos rodea es, en la mayoría de los casos, una mezcla de sustancias. Los científicos han intentado clasificar las sustancias desde el principio de los tiempos.
1.5 Métodos de separación de mezclas Decantación, filtración, extracción, cristalización, destilación, cromatografía.
 1.5 Métodos de separación de mezclas Decantación, filtración, extracción, cristalización, destilación, cromatografía. 1 Para tomar apuntes MÉTODO DE SEPARACIÓN PROPIEDAD(ES) EN LAS QUE SE BASA MEZCLAS
1.5 Métodos de separación de mezclas Decantación, filtración, extracción, cristalización, destilación, cromatografía. 1 Para tomar apuntes MÉTODO DE SEPARACIÓN PROPIEDAD(ES) EN LAS QUE SE BASA MEZCLAS
UNIDADES DE ESTUDIO Y SUS CONTENIDOS Unidad 1: PROPIEDADES DE LOS FLUIDOS PUROS.
 1. DATOS INFORMATIVOS ASIGNATURA: QUÌMICA-FÌSICA DEPARTAMENTO: CIENCIAS EXACTAS ELEMENTO DE COMPETENCIA: CÓDIGO: EXCT-22318 CARRERAS: PETROQUÌMICA NRC 4548 NIVEL: QUINTO ÁREA DEL CONOCIMIENTO: QUÌMICA
1. DATOS INFORMATIVOS ASIGNATURA: QUÌMICA-FÌSICA DEPARTAMENTO: CIENCIAS EXACTAS ELEMENTO DE COMPETENCIA: CÓDIGO: EXCT-22318 CARRERAS: PETROQUÌMICA NRC 4548 NIVEL: QUINTO ÁREA DEL CONOCIMIENTO: QUÌMICA
Disoluciones. Química General II 2011
 Disoluciones Química General II 2011 Disolución Es una mezcla homogénea de dos o mas sustancias. Componentes: Soluto: Sustancia (s) presente (s) en menor cantidad en una disolución, son las sustancias
Disoluciones Química General II 2011 Disolución Es una mezcla homogénea de dos o mas sustancias. Componentes: Soluto: Sustancia (s) presente (s) en menor cantidad en una disolución, son las sustancias
UNIVERSIDAD DE ANTIOQUIA FACULTAD DE QUÍMICA FARMACÉUTICA LABORATORIO DE QUÍMICA GENERAL Profesor: Jaime O. Pérez DEYMER GÓMEZ CORREA:
 UNIVERSIDAD DE ANTIOQUIA FACULTAD DE QUÍMICA FARMACÉUTICA LABORATORIO DE QUÍMICA GENERAL Profesor: Jaime O. Pérez Práctica: SOLUCIONES 1 Fecha: 9/Marzo/2010 DEYMER GÓMEZ CORREA: 1 042 091 432 OBJETIVOS
UNIVERSIDAD DE ANTIOQUIA FACULTAD DE QUÍMICA FARMACÉUTICA LABORATORIO DE QUÍMICA GENERAL Profesor: Jaime O. Pérez Práctica: SOLUCIONES 1 Fecha: 9/Marzo/2010 DEYMER GÓMEZ CORREA: 1 042 091 432 OBJETIVOS
TEMA 2 La materia y sus propiedades QUÉ ES LA MATERIA? ESTADOS DE LA MATERIA CAMBIOS DE ESTADO MODELO CINÉTICO-MOLECULAR
 TEMA 2 La materia y sus propiedades QUÉ ES LA MATERIA? ESTADOS DE LA MATERIA CAMBIOS DE ESTADO MODELO CINÉTICO-MOLECULAR 1. QUÉ ES LA MATERIA? El universo que conocemos, puede definirse en términos de
TEMA 2 La materia y sus propiedades QUÉ ES LA MATERIA? ESTADOS DE LA MATERIA CAMBIOS DE ESTADO MODELO CINÉTICO-MOLECULAR 1. QUÉ ES LA MATERIA? El universo que conocemos, puede definirse en términos de
FÍSICA Y QUÍMICA Versión impresa ELECTRONES Y ENLACES
 FÍSICA Y QUÍMICA Versión impresa ELECTRONES Y ENLACES Niveles de energía Modelo atómico actual Orbitales Configuración electrónica Tabla periódica Cada electrón puede encontrarse con más probabilidad en
FÍSICA Y QUÍMICA Versión impresa ELECTRONES Y ENLACES Niveles de energía Modelo atómico actual Orbitales Configuración electrónica Tabla periódica Cada electrón puede encontrarse con más probabilidad en
Para que se cristaliza una sustancia?
 OPERACIONES UNITARIAS DE SEPARACION Y ESTABILIZACION Teóricos Prof. G. Picó 2016 CRISTALIZACION 245 Para que se cristaliza una sustancia? - Eliminar el solvente (agua) y otros cosolutos. - Se incrementa
OPERACIONES UNITARIAS DE SEPARACION Y ESTABILIZACION Teóricos Prof. G. Picó 2016 CRISTALIZACION 245 Para que se cristaliza una sustancia? - Eliminar el solvente (agua) y otros cosolutos. - Se incrementa
FUERZAS INTERMOLECULARES
 FUERZAS INTERMOLECULARES FUERZAS INTRAMOLECULARES: Fuerzas que se dan en el interior de las moléculas :Enlace Químico. FUERZAS INTERMOLECULARES: Interacciones entre moléculas. Mantienen unidas las moléculas
FUERZAS INTERMOLECULARES FUERZAS INTRAMOLECULARES: Fuerzas que se dan en el interior de las moléculas :Enlace Químico. FUERZAS INTERMOLECULARES: Interacciones entre moléculas. Mantienen unidas las moléculas
BLOQUE I: LA BASE MOLECULAR Y FÍSICO-QUÍMICA DE LA VIDA. Tema 2.- Componentes químicos de la célula: biomoléculas inorgánicas
 BLOQUE I: LA BASE MOLECULAR Y FÍSICO-QUÍMICA DE LA VIDA Tema 2.- Componentes químicos de la célula: biomoléculas inorgánicas Tema 2.- Componentes químicos de la célula: biomoléculas inorgánicas A.- Los
BLOQUE I: LA BASE MOLECULAR Y FÍSICO-QUÍMICA DE LA VIDA Tema 2.- Componentes químicos de la célula: biomoléculas inorgánicas Tema 2.- Componentes químicos de la célula: biomoléculas inorgánicas A.- Los
1. Fuerza. Leyes de Newton (Gianc )
 Tema 1: Mecánica 1. Fuerza. Leyes de Newton. 2. Movimiento sobreamortiguado. 3. Trabajo y energía. 4. Diagramas de energía. 5. Hidrostática: presión. 6. Principio de Arquímedes. 7. Hidrodinámica: ecuación
Tema 1: Mecánica 1. Fuerza. Leyes de Newton. 2. Movimiento sobreamortiguado. 3. Trabajo y energía. 4. Diagramas de energía. 5. Hidrostática: presión. 6. Principio de Arquímedes. 7. Hidrodinámica: ecuación
