TEMA 1: Bioelementos, agua y sales minerales
|
|
|
- Elena Ortíz Díaz
- hace 6 años
- Vistas:
Transcripción
1 BIOLOGÍA DE 2º DE BACHILLERATO TEMA 1: Bioelementos, agua y sales minerales Composición de los seres vivos: bioelementos y biomoléculas El agua Estructura Propiedades físico-químicas Funciones biológicas Disoluciones acuosas de las sales minerales. Difusión, ósmosis y diálisis ORIENTACIONES 1. Definir qué es un bioelemento y enumerar los más importantes. Destacar las propiedades físico-químicas del carbono. 2. Conocer la estructura molecular del agua y relacionarla con sus propiedades físico-químicas. Resaltar su papel biológico como disolvente, reactivo químico, termo-regulador y en función de su densidad y tensión superficial. 3. Reconocer el papel del agua y de las disoluciones salinas en los equilibrios osmóticos y ácidobase.
2 INTRODUCCIÓN Sistema material : Conjunto de partes o elementos organizados que interaccionan entre sí Los seres vivos son sistemas materiales que se caracterizan por: 1. Estar compuestos de elementos químicos denominados bioelementos, que se asocian en biomoléculas, con distintos niveles de complejidad y de las que hay que citar como específicas de los seres vivos, las biomoléculas orgánicas, que son todas compuestos del carbono y que presentan una gran variedad de funciones y formas. 2. Presentar un elevado grado de organización, que se puede estructurar en niveles cada vez más complejos, formados por moléculas con una elevada especialización funcional que se agrupan e interactúan dando lugar a las células procariotas, a los orgánulos de las células eucariotas, a las células eucariotas, a la agrupación de estas células en tejidos, órganos, aparatos y sistemas que originan los organismos pluricelulares. Los seres vivos individuales se organizan en poblaciones que interactúan con otras, formando comunidades que interactúan con el medio y originan ecosistemas que constituyen la Biosfera.
3 Célula: Unidad anatómica y fisiológica de los seres vivos. Tejido: Conjunto de células, con características semejantes, que desempeñan análoga misión. Órgano: Resultado de la agrupación de tejidos en una estructura especializada con una función concreta. Aparato: Conjunto de órganos, dispuestos unos a continuación de otros, que realizan sus funciones coordinadas para desempeñar una función más amplia del organismo. Sistema: Conjunto de formaciones de un mismo tejido, repartidas por todo el organismo, que se coordinan para realizar una función amplia en el individuo. Especie: Conjunto de seres vivos, con características morfológicas y fisiológicas similares, que pueden cruzarse entre sí dando descendencia fértil. Población: Conjunto de individuos de la misma especie que viven en un área determinada. Comunidad: Conjunto de poblaciones. Ecosistema: Comunidad o Biocenosis mas su medio ambiente o Biotopo.
4 3. Según el nivel de organización al que hayan llegado y a otras características como los tipos de nutrición que realicen, los seres vivos se clasifican en cinco Reinos: Móneras, al que pertenecen organismos unicelulares procariotas con nutrición autótrofa y heterótrofa. Protoctístas, al que pertenecen organismos unicelulares eucariotas y pluricelulares sencillos, con nutrición autótrofa y heterótrofa. Fungi u Hongos formado por organismos unicelulares eucariotas o pluricelulares heterótrofos. Vegetal formado por seres vivos pluricelulares, eucariotas con tejidos, órganos, aparatos y sistemas y con nutrición autótrofa. Animal, al que pertenecen organismos pluricelulares eucariotas con tejidos, órganos, aparatos y sistemas y nutrición heterótrofa. 4. Una gran diversidad, debido a las mutaciones, reproducción sexual e interacciones con el medio ambiente, que hace que exista una selección natural hacia formas de vida cada vez más especializadas, y una evolución en el tiempo y en el espacio, colonizándose todos los hábitat del Planeta. 5. Ser capaces de intercambiar materia y energía con el medio (Función de nutrición), dar respuesta frente a estímulos (Función de relación), generar descendientes que perpetúan la vida en el espacio y en el tiempo (Función de reproducción).
5 1. COMPOSICIÓN DE LOS S.VIVOS: BIOELEMENTOS Y BIOMOLÉCULAS Concepto de bioelemento. Los bioelementos son los átomos que están presentes en los sistemas vivos. Existen unos 70, incluidos en la tabla periódica, de los cuales 25 están presentes en todos los seres vivos y el resto en determinados grupos. Los bioelementos principales están en una abundancia del 96%, los secundarios con un 3.9% aproximadamente y los oligoelementos con menos del 0.1% Propiedades de los bioelementos más abundantes: 1. Tienen capas electrónicas externas incompletas, por lo que tienden a formar enlaces covalentes (comparten electrones para completar su última capa) estables y originar biomoléculas. 2. Poseen número atómico bajo, por lo cual los electrones de enlace quedan próximos al núcleo y las moléculas originadas son estables. 3. Originan moléculas polares (moléculas con una distribución asimétrica de sus electrones) y por ello, solubles en agua. Esto es debido a que el oxígeno y nitrógeno son muy electronegativos. Esta propiedad permite el movimiento en el medio interno, los intercambios con el medio externo, y las reacciones químicas. 4. Pueden incorporarse fácilmente a los seres vivos.
6 Propiedades físico-químicas del carbono 1. El átomo de carbono tiene cuatro electrones de valencia en su capa externa, lo cual facilita que pueda formar consigo mismo enlaces sencillos, dobles y triples, y esto le hace esencial para formar la estructura básica de las moléculas orgánicas. 2. Su configuración tetraédrica posibilita la formación de moléculas con estructuras variadas y complejas responsables de la diversidad morfológica y funcional de los seres vivos. 3. Forma enlaces covalentes con otros átomos como O, H, N, S, lo que permite que las moléculas presenten grupos funcionales que confieren propiedades específicas. 4. Los enlaces de las moléculas del carbono se pueden romper y formar sin excesiva dificultad, lo que permite la liberación o acumulación de energía y por tanto las reacciones de oxidación reducción del metabolismo celular. 5. La combinación del carbono con el oxígeno (CO2) es un gas fácil de intercambiar con el medio.
7 Clasificación de los bioelementos Los bioelementos se clasifican según su abundancia en: Bioelementos primarios: C, H, O, N, P y S. Forman aproximadamente el 96% de la materia viva. Son los constituyentes de las biomoléculas orgánicas y además el P interviene en procesos de intercambio de energía. Bioelementos secundarios: Na+, K+, Ca2+, Mg2+, Cl-...Constituyen aproximadamente el 3,9% de la materia viva y son necesarios para la vida de la célula. Oligoelementos. Se encuentran en cantidades inferiores al 0,1 %. Son imprescindibles porque desempeñan funciones esenciales en diferentes procesos bioquímicos y fisiológicos. Algunos como Fe, Mn, Cu, Zn, I,.. son esenciales para la mayoría de los organismos. Otros como Si, F, Cr, Li, sólo están presentes en determinados grupos de organismos.
8 Funciones de los bioelementos. Estructural o plástica: C, H, O, N, P y S. Constituyen las biomoléculas orgánicas. Funciones específicas: - Calcio. Forma parte de estructuras esqueléticas y en forma iónica participa en la contracción muscular y en la coagulación de la sangre - Magnesio. Es necesario para la actuación de muchas enzimas y forma parte de la clorofila. - Hierro. Es responsable del transporte de oxígeno de la hemoglobina, y forma parte de otros complejos proteicos como los citocromos de la cadena respiratoria, que participan en reacciones de oxido-reducción. - Sodio, potasio y cloro. Crean gradientes de membrana y participan en la transmisión del impulso nervioso. - Cinc. Actúa como cofactor de muchas enzimas. - Litio. Actúa sobre los neurotransmisores. Puede prevenir estados depresivos. - Yodo. Necesario para la síntesis de la hormona tiroxina. - Cobalto. Forma parte de la vitamina B12. - Flúor. Participa en la constitución de huesos y dientes. - Manganeso. Actúa como catalizador en muchas reacciones químicas. Participa en la fotolisis del agua durante la fotosíntesis. - Cu++ actúa con las enzimas de oxidación y en el transporte de oxígeno al formar la hemocianina de Artrópodos y moluscos.
9 1.1. BIOMOLÉCULAS Concepto Son moléculas formadas al combinarse los bioelementos y que constituyen los seres vivos Clasificación 1.2. EL AGUA Es el compuesto mayoritario en los seres vivos (65 al 95 %). Su abundancia en el ser vivo queda en relación con: -La actividad metabólica. -Composición del medio interno Estructura química del agua La molécula de agua está formada por 2 átomos de hidrógeno y uno de oxígeno unidos mediante enlaces covalentes polares; aunque es eléctricamente neutra por tener igual número de protones y electrones, los electrones compartidos son atraídos más fuertemente por el átomo de oxígeno, por su mayor electronegatividad, que por los átomos de hidrógeno. Esto convierte a la molécula de agua en un dipolo, con dos cargas negativas en el átomo de oxígeno y una positiva en cada átomo de hidrógeno.
10 Una consecuencia de su carácter dipolar es la formación de enlaces de hidrógeno entre los dipolos, que hace que presente una estructura en forma de red responsable de que se encuentre en estado líquido a temperatura ambiente y de las demás propiedades físicoquímicas. El agua presenta unas características muy importantes, una de ellas se refiere a su estructura molecular, ya que adopta forma espacial de "V", donde el oxígeno se sitúa en el vértice y los hidrógenos en los extremos. El ángulo que forma la V es de y la distancia entre los átomos de hidrógeno y el oxígeno es de 0 96 Å.
11 Propiedades físico-químicas del agua a) Derivadas de su polaridad. - Elevada constante dieléctrica, que le confiere una elevada capacidad disolvente y dispersante de sustancias polares y anfipáticas. La constante dieléctrica es la tendencia a disminuir las atracciones interiónicas. Esto provoca: Separación de compuestos iónicos en iones individuales, rodeándolos por dipolos de agua que impiden su unión ( solvatación). Formación de puentes de hidrógeno con otras moléculas que contienen grupos funcionales polares, originando su disolución o dispersión. Debido a esta propiedad, el agua desempeña estas funciones biológicas: 1. Transporte de sustancias. 2. Medio donde ocurren las reacciones bioquímicas. 3. Interviene en reacciones de hidrólisis. 4. Regula el estado líquido y coloidal del protoplasma celular.
12 b) Propiedades derivadas de la existencia de enlaces de hidrógeno - Ser líquida a temperatura ambiente lo que hace que sea el constituyente mayoritario de los seres vivos, siendo el medio en que se dan las reacciones químicas del metabolismo, el vehículo de transporte de sustancias, el soporte y sostén de células sin pared, etc. - Elevada tensión superficial. Las moléculas de agua de la superficie experimentan fuerzas de atracción hacia el interior del líquido. Esto favorece que dicha superficie oponga una gran resistencia a ser traspasada, a romperse. Esta propiedad permite el desplazamiento de los organismos que viven en la superficie. - Elevada fuerza de cohesión. Los enlaces de hidrógeno mantienen fuertemente unidas a unas moléculas con otras y esta propiedad hace que el agua sea casi incompresible y confiere al agua las siguientes funciones: Dar volumen a las células, sostén a animales sin esqueleto, emisión de pseudópodos Turgencia a las plantas. Función amortiguadora o mecánica. - Elevada fuerza de adhesión. Las moléculas de agua tienen la capacidad de adherirse (formar enlaces por puentes de hidrógeno con otras moléculas polares) a las paredes de conductos de diámetro pequeño, lo que permite ascender en contra de la gravedad. Este fenómeno se conoce como capilaridad y contribuye, por ejemplo, a la ascensión de savia bruta a través de los vasos leñosos. - Elevado calor específico. El calor específico Ce, se define como la cantidad de calor que hay que suministrar a un gramo de una sustancia para que aumente su temperatura 1º centígrado. En el agua el Ce es muy alto, 1 caloría / g C, lo que implica que el agua se va a comportar como un buen amortiguador de cambios bruscos de la temperatura, ya que antes de enfriarse o de calentarse tiene que perder o ganar mucho calor respectivamente. El agua puede absorber gran cantidad de calor sin elevar mucho la temperatura, porque esta energía tiene que romper los puentes de hidrógeno entre las moléculas. Esto la convierte en un amortiguador térmico, con función termorreguladora.
13 - Elevado calor de vaporización. Cuando el agua pasa de estado líquido a gaseoso necesita absorber mucho calor para romper los enlaces de hidrógeno. Cuando el agua se evapora en la superficie de un ser vivo, absorbe calor del organismo actuando como regulador térmico, colabora así en la refrigeración de los organismos - Escasa densidad en estado sólido. En estado sólido el agua presenta todos sus posibles enlaces de hidrógeno, cuatro por cada molécula, formando un retículo que ocupa mayor volumen que en estado líquido, por lo que es menos denso. Esta propiedad permite la vida acuática en climas fríos, ya que al descender la temperatura se forma una capa de hielo en la superficie, que flota y protege al agua líquida. - Alta conductividad. Esto facilita la distribución del calor por toda la masa de agua lo que evita que se acumule en una determinada zona de un organismo - Bajo grado de ionización. En el agua existe una pequeñísima cantidad de moléculas ionizadas (disociadas en sus iones) una de cada moléculas de agua. Debido a eso, si al agua se añade un ácido o una base, aunque sea poca cantidad, estos niveles varían bruscamente. Por ello en el transcurso de la evolución, seres vivos han adquirido mecanismos que mantienen constante el ph: los sistemas tampón, formados por sales minerales en disolución. Los iones de las moléculas de agua permiten las reacciones químicas de hidrólisis necesarias para el metabolismo y la digestión.
14 Funciones biológicas del agua Las propiedades del agua, que dependen de la estructura de la molécula, determinan el papel fundamental del agua en los seres vivos. Entre las funciones ya citadas, destacaremos: a) Gran capacidad de disolvente para sustancias polares como ácidos, bases y sales y para sustancias orgánicas que presentan una acusada polaridad como los glúcidos. b) Función termorreguladora. Los enlaces de hidrógeno entre las moléculas del agua tienden a dificultar su movimiento, de modo que para una determinada cantidad de calor la temperatura del agua sube o baja muy lentamente. c) Actúa como transportador de sustancias tanto alimenticias como de desecho, dentro del organismo y entre éste y su medio. d) El agua interviene en muchas reacciones metabólicas fundamentales como la hidrólisis y la fotosíntesis. e) Termoaislante, permite la vida en zonas frías. Debido a su baja densidad en estado sólido. f) Da forma y volumen a las células debido a su elevada fuerza de cohesión. g) Es el medio en el que se dan las reacciones químicas de los seres vivos. h) Movimiento de ascenso de la savia bruta por los vasos de los vegetales
15 DISOLUCIONES ACUOSAS DE SALES MINERALES Concepto y tipos de sales minerales son compuestos químicos que se encuentran en los seres vivos en forma sólida (precipitadas), en forma líquida (disueltas) en forma de iones o asociadas a sustancias orgánicas formando parte de las fosfoproteínas, fosfolípidos, etc Funciones: a.- Estructurales. Las realizan las sales minerales que se encuentran en forma sólida y constituyen estructuras de sostén, protección y apoyo en los seres vivos. Ejemplos. CaCO3 del caparazón de los moluscos, Ca3(PO4)2 de los huesos del esqueleto, SiO2 de las algas diatomeas. b.- Reguladoras u homeostáticas Las realizan las sales minerales disueltas que se 23encuentran en forma de cationes: Mg2+, Ca2+, Na+, K+ o de aniones: Cl, SO, PO, HPO, H2PO, NO HCO, CO Regulación del ph. En 1909, Sörensen estableció el concepto de ph de una disolución para valorar cuantitativamente su grado de acidez y, de igual forma, el de poh para valorar cuantitativamente el grado de alcalinidad o basicidad. El agua pura posee la capacidad de disociarse en iones, se disocian en H+ y OH-, lo que hace que en realidad sea una mezcla de tres especies: agua molecular (H2O), protones hidratados (H3O+) e iones hidroxilo (OH-).
16 ph = -log [H+] ó ph = -log [H3O+] Esta disociación es muy débil en el agua pura, y el producto iónico a 25 C es: Kw = [H+] [OH-]= 1,0 x moles/litro Como en el agua pura la concentración de hidrogeniones y de hidroxilos es la misma, [H3O+] = [OH ] = 10-7 moles/litro Cuando en una disolución ocurre esto decimos que es de tipo neutro, cuando el ph de una disolución es menor que 7, se debe a que en ella la [H3O+] es mayor que la [OH ], y en este caso decimos que la disolución es de tipo ácido. Cuando el ph es mayor que 7, se debe a que la [H3O+] es menor que la [OH ], y en este caso decimos que la disolución es de tipo básico o alcalino. Las sustancias que al disolverse en agua provocan un aumento de los iones H3O+ reciben el nombre de ácidos, son aquellas sustancias responsables de que el ph disminuya. Existen otras que al disolverse en agua provocan el efecto contrario, es decir un aumento de los iones OH, estas sustancias se denominan bases y son las responsables de que el ph aumente. La actividad biológica se produce a un determinado valor de ph. Los organismos vivos no soportan variaciones de ph mayores de unas décimas, ya que las variaciones de ph afectan a la estabilidad de las macromoléculas (desnaturalización de proteínas, desnaturalización del ADN ). Por esta razón los seres vivos han desarrollado los sistemas tampón. Así, reacciones químicas que se verifican en los organismos producen variaciones de ph y algunas sales minerales disueltas contribuyen a disminuir esas variaciones, manteniendo el ph constante. Estas sales minerales disueltas constituyen los sistemas tampón, amortiguadores o buffer, consisten en un conjunto de sustancias relacionadas entre sí (acido debil y su base conjugada), capaces de mantener el ph constante y por tanto, se oponen automáticamente a los cambios de ph captando o cediendo H+ del medio.
17 - En el medio extracelular (sangre) actúa el sistema tampón bicarbonato. En el plasma sanguíneo, el CO2 procedente del metabolismo celular se combina de forma reversible con H2O, dando H2CO3. Este ácido carbónico es un ácido débil que puede disociarse en los iones H+ y HCO3(bicarbonato) que es su base conjugada, una sal. Si el medio es básico, la reacción se desplaza hacia la derecha, y si es ácido hacia la izquierda. En un medio basico: CO2 + H2O CO3H2 CO3H- + H+ asi el PH disminuye CO3H2 CO3H- + H+ asi el PH aumenta En un medio acido: CO2 + H2O Ante una acidosis en la sangre (exceso de H+), el bicarbonato se une al exceso de H+, dando ácido carbónico que se descompone inmediatamente en CO2 y H2O. - El principal sistema tampón intracelular es el tampón fosfato. En el sistema tampón fosfato las dos especies son: H 2PO4- y H+ + HPO42En un medio basico: 1H PO + H O ácido debil HPO 2- + H O 4 3 base conjugada (sal) + En un medio ácido: 1H PO + H O HPO 24 + H O 3 +
18 Regulan el estado físico del protoplasma celular, favoreciendo la dispersión de moléculas de gran tamaño como las proteínas. Regulación de la presión osmótica y el volumen celular. La presencia de sales en el medio interno celular es determinante para que se verifique la entrada o salida de agua a través de la membrana mediante procesos de ósmosis. La ósmosis es un fenómeno en el que se produce el paso o difusión de un disolvente a través
19 de una membrana semipermeable (permite el paso de disolventes, pero no de solutos) desde una disolución más diluida a otra más concentrada. Los medios acuosos separados por membranas semipermeables pueden tener distintas concentraciones, y se denominan: - Hipertónicos, los que tienen una elevada concentración de solutos con respecto a otros en que la concentración es menor. - Hipotónicos, los que contienen una concentración de solutos baja con respecto a otros que la tienen superior. Las moléculas de agua difunden desde medios hipotónicos hacia los hipertónicos provocando un aumento de presión sobre la cara de la membrana del compartimento hipotónico, denominada presión osmótica. Como consecuencia los dos medios serán isotónicos. Las membranas celulares se comportan como membranas semipermeables, o selectivamente permeables: - Cuando el medio externo celular es hipertónico con respecto al medio interno, sale agua de la célula por ósmosis (a esto se le denomina plasmólisis); entonces, disminuye el volumen celular y aumenta la presión osmótica en el interior celular. - Cuando el medio externo celular es hipotónico con respecto al medio interno, se produce entrada de agua en la célula, lo que ocasiona: aumento del volumen celular y disminución de la presión osmótica en el interior celular. En el caso de las células animales puede producirse estallido celular o hemólisis. En células bacterianas y vegetales, que presentan paredes rígidas, se produce turgencia celular. - Cuando el contenido celular es isotónico con respecto al medio externo, no se produce intercambio de agua entre ambos lados de la membrana.
20 Específicas: Algunos cationes como el Mg 2+, Mn 2+, Zn+, Cu+, etc., actúan como cofactores enzimáticos y son necesarios para la actividad de determinados enzimas. Otros cationes como el ión ferroso-férrico (Fe2+ - Fe3+) de la hemoglobina transporta el oxígeno en la sangre. El ión Ca2+ interviene en la contracción muscular y en la coagulación de la sangre. Los cationes Na+, K+, Cl-, participan en la transmisión del impulso nervioso.
21 PROPIEDADES DE LAS DISOLUCIONES VERDADERAS Para comprender muchos de los fenómenos que ocurren en el interior de los organismos, y por tanto, de sus células, es fundamental conocer las propiedades de las disoluciones. Son principalmente la difusión, la ósmosis y la diálisis. - Difusión: es el proceso de la repartición homogénea (uniforme) de las partículas de un fluido (gas o líquido) en el seno de otro fluido al ponerlos en contacto. Ejemplo: la absorción del O2 de los pulmones a la sangre. Al final la difusión se detiene cuando se igualan las concentraciones de dichas partículas en ambos fluidos. -Diálisis: es el proceso de separación de partículas según su masa molecular (tamaño), gracias a una membrana semipermeable que tan solo deja pasar agua y otras moléculas pequeñas pero no las grandes. Una aplicación clínica muy usada en individuos con insuficiencia renal (sus riñones no funcionan bien y los desechos se acumulan en el cuerpo) es la hemodiálisis, que permite separar la urea y otros desechos de baja masa molecular de la sangre, sin alterar la concentración de las proteínas sanguíneas que tienen una masa molecular elevada.
22 - Osmosis: es el proceso por el que se produce el paso del disolvente (en los seres vivos es el agua) a través de una membrana semipermeable entre dos disoluciones de diferente concentración; este paso de disolvente se produce desde la disolución más diluida hacia la más concentrada, hasta que las dos concentraciones alcanzan el equilibrio, igualándose las concentraciones. VOCABULARIO Ácido. Apolar. Base. Capilaridad. Hidrólisis. Hipertónico. Hipotónico. Isotónico. Plasmólisis. Polar. PH. Sistema tampón. Turgencia.
23 CUESTIONES DE SELECTIVIDAD 1.- Defina bioelemento y biomolécula [0,4]. Cite cuatro ejemplos de bioelementos y cuatro de biomoléculas [0,8] e indique la importancia biológica de cada uno de los ejemplos [0,8]. 2.-Describa [0,5] y dibuje [0,3] la estructura de la molécula de agua. Enumere cuatro propiedades físico-químicas del agua y relaciónelas con sus funciones biológicas [1,2].Explique el tipo de enlace que se establece entre las moléculas de agua. 3.- En las zonas polares, donde las temperaturas son muy bajas, Cómo es posible que los ecosistemas marinos se mantengan con vida en las épocas con temperaturas por debajo de 0º? Razone la respuesta. 4.- Un sistema de conservación de alimentos muy utilizado desde antiguo consiste en añadir una considerable cantidad de sal al alimento (salazón) para preservarlo del ataque de microorganismos que puedan alterarlo. Explique de forma razonada este hecho [1]. 5.- La hoja de una planta al sol tiene generalmente menos temperatura que las rocas de su entorno. A qué propiedad físico-química del agua se debe este hecho? Razone la respuesta [1]. 6.- En el Mar Muerto existe una elevada salinidad. Explique razonadamente por qué el número de especies en el Mar Muerto es menor que en otros mares [1]. 7.-En relación con la imagen adjunta, responda las siguientes cuestiones: a).- Identifique la sustancia representada [0,2] y explique los criterios utilizados para identificarla [0,3]. Qué tipo de enlace se establece entre ambas moléculas? [0,2]. Explique una consecuencia biológica de la existencia de estos enlaces [0,3]. b).-indique cinco funciones que realiza esta sustancia en los seres vivos [1]
24 8.-El contenido salino interno de los glóbulos rojos presentes en la sangre es del 0,9%. Qué le pasaría a un organismo, si se le inyectara en la sangre una solución salina que hiciera que la concentración final de sales en sangre fuese del 2,2%? [0,5]. Y si la concentración final fuese del 0,01%? [0,5]. Razone las respuestas. 9.-Se introducen células animales en tres tubos de ensayo: el tubo A tiene una solución hipertónica, el B una hipotónica y el C una isotónica. Exponga razonadamente lo que les ocurrirá a las células en cada uno de los tubos 10.- Qué ocurre cuando células que carecen de pared celular se colocan en una solución muy concentrada de sales? [0,5]. Sucedería lo mismo si se colocasen en agua destilada? [0,5]. Razone las respuestas Las plantas herbáceas mantienen su turgencia y la posición erecta gracias al agua, al tiempo que resuelven problemas de transporte de nutrientes. Dé una explicación razonada a estos hechos [1] La inclusión de glóbulos rojos en un medio hipotónico se utiliza como paso previo para obtener membranas celulares puras. Dé una explicación razonada del porqué de este procedimiento [1] Por qué una célula animal muere en un medio hipotónico y sin embargo una célula vegetal no? Dé una explicación razonada a este hecho [1] Qué ocurriría si introducimos un pez marino en agua dulce? [0,5]. Y si introducimos un pez de agua dulce en agua de mar? [0,5]. Razone las respuestas Al añadir un ácido a una disolución de CLNa se produce un gran descenso del valor del ph. Sin embargo si añadimos la misma cantidad al plasma sanguíneo apenas hay cambios. Proponga una explicación razonada a este hecho y explique las consecuencias de los cambios bruscos de ph en los seres vivos. 16.-Cogemos hojas de lechuga, se cubren con un paño húmedo y se guardan en el frigorífico a 4ºC permaneciendo turgentes durante mucho tiempo, sin embrago al aliñar con aceite, sal y vinagre pierden la turgencia. Razonar la respuesta
BIOLOGÍA DE 2º DE BACHILLERATO 1. BASE FÍSICO QUIMICA DE LA VIDA.
 BIOLOGÍA DE 2º DE BACHILLERATO 1. BASE FÍSICO QUIMICA DE LA VIDA. 1.1.- Composición de los seres vivos: bioelementos y biomoléculas. 1.2.- El agua. 1.2.1. Estructura. 1.2.2. Propiedades físico-químicas.
BIOLOGÍA DE 2º DE BACHILLERATO 1. BASE FÍSICO QUIMICA DE LA VIDA. 1.1.- Composición de los seres vivos: bioelementos y biomoléculas. 1.2.- El agua. 1.2.1. Estructura. 1.2.2. Propiedades físico-químicas.
EL AGUA Y LAS SALES MINERALES
 EL AGUA Y LAS SALES MINERALES 1. EL AGUA DE LA MATERIA VIVA El agua es la molécula más abundante de la materia viva La cantidad de agua en los seres vivos es variable Según el tipo de tejido: más agua
EL AGUA Y LAS SALES MINERALES 1. EL AGUA DE LA MATERIA VIVA El agua es la molécula más abundante de la materia viva La cantidad de agua en los seres vivos es variable Según el tipo de tejido: más agua
Niveles de Organización Conceptos, átomos y enlaces
 Niveles de Organización Conceptos, átomos y enlaces Cómo se organiza la materia viva? NIVELES DE ORGANIZACIÓN ÁTOMO MOLÉCULA (ELEMENTO- COMPUESTO) MACROMOLÉCULA CÉLULA TEJIDO ÓRGANO SISTEMA ORGANISMO MULTICELULAR
Niveles de Organización Conceptos, átomos y enlaces Cómo se organiza la materia viva? NIVELES DE ORGANIZACIÓN ÁTOMO MOLÉCULA (ELEMENTO- COMPUESTO) MACROMOLÉCULA CÉLULA TEJIDO ÓRGANO SISTEMA ORGANISMO MULTICELULAR
Tema 1. Introducción. Bioelementos y Biomoléculas Inorgánicas
 Tema 1. Introducción. Bioelementos y Biomoléculas Inorgánicas 1. Concepto de Biología: Es la ciencia que estudia todos los fenómenos y procesos relacionados con los seres vivos. 2. Características de los
Tema 1. Introducción. Bioelementos y Biomoléculas Inorgánicas 1. Concepto de Biología: Es la ciencia que estudia todos los fenómenos y procesos relacionados con los seres vivos. 2. Características de los
Bioelementos y Biomoléculas 1-Moléculas inorganicas : Agua
 Bioelementos y Biomoléculas 1-Moléculas inorganicas : Agua Técnico Professor: Verónica en masoterapia Pantoja. Lic. MSP. Objetivos Reconocer los bioelementos en los seres vivos Reconocer el agua como biomolécula
Bioelementos y Biomoléculas 1-Moléculas inorganicas : Agua Técnico Professor: Verónica en masoterapia Pantoja. Lic. MSP. Objetivos Reconocer los bioelementos en los seres vivos Reconocer el agua como biomolécula
Profesor(a): C.D. María Isabel Pérez Aguilar
 Área Académica: Biología Básica Tema: Bioelementos Profesor(a): C.D. María Isabel Pérez Aguilar Periodo: Enero- Julio 2012 Abstract Bioelements Bioelements are the essential components of life. This topic
Área Académica: Biología Básica Tema: Bioelementos Profesor(a): C.D. María Isabel Pérez Aguilar Periodo: Enero- Julio 2012 Abstract Bioelements Bioelements are the essential components of life. This topic
EL AGUA Y LAS SALES MINERALES. El agua es el elemento y principio de las cosas. Tales de Mileto
 EL AGUA Y LAS SALES MINERALES El agua es el elemento y principio de las cosas. Tales de Mileto 1. EL AGUA DE LA MATERIA VIVA El agua es la molécula más abundante de la materia viva La cantidad de agua
EL AGUA Y LAS SALES MINERALES El agua es el elemento y principio de las cosas. Tales de Mileto 1. EL AGUA DE LA MATERIA VIVA El agua es la molécula más abundante de la materia viva La cantidad de agua
Bioelementos y biomoléculas 1-Moleculas inorganicas Sales minerales. Verónica Pantoja. Lic. MSP.
 Bioelementos y biomoléculas 1-Moleculas inorganicas Sales minerales Professor: Kinesiologia Verónica Pantoja. Lic. MSP. 1.Precipitadas Formando estructuras sólidas, insolubles, con función esquelética.
Bioelementos y biomoléculas 1-Moleculas inorganicas Sales minerales Professor: Kinesiologia Verónica Pantoja. Lic. MSP. 1.Precipitadas Formando estructuras sólidas, insolubles, con función esquelética.
SALES MINERALES , CO 3. Aniones: Cl -, PO 4. , NO 3, Cationes: Na +, Ca 2+, Mg 2+, Fe 2+, Fe 3+, K +
 SALES MINERALES Aniones: Cl -, PO 4 3-, CO 3 2-, NO 3, Cationes: Na +, Ca 2+, Mg 2+, Fe 2+, Fe 3+, K + SALES PRECIPITADAS Vieira SALES PRECIPITADAS: CaCO 3 Exoesqueleto de Ca Sales de Ca: caparazones
SALES MINERALES Aniones: Cl -, PO 4 3-, CO 3 2-, NO 3, Cationes: Na +, Ca 2+, Mg 2+, Fe 2+, Fe 3+, K + SALES PRECIPITADAS Vieira SALES PRECIPITADAS: CaCO 3 Exoesqueleto de Ca Sales de Ca: caparazones
UD 1. LA MATERIA VIVA: BIOELEMENTOS Y BIOMOLÉCULAS. ANEXO: Tipos de enlaces y formas de representar las moléculas
 UD 1. LA MATERIA VIVA: BIOELEMENTOS Y BIOMOLÉCULAS. ANEXO: Tipos de enlaces y formas de representar las moléculas 1. BIOELEMENTOS O ELEMENTOS BIOGÉNICOS Son los elementos químicos que se encuentran en
UD 1. LA MATERIA VIVA: BIOELEMENTOS Y BIOMOLÉCULAS. ANEXO: Tipos de enlaces y formas de representar las moléculas 1. BIOELEMENTOS O ELEMENTOS BIOGÉNICOS Son los elementos químicos que se encuentran en
LOS COMPONENTES QUÍMICOS DE LA CÉLULA
 LOS COMPONENTES QUÍMICOS DE LA CÉLULA 1. Los enlaces químicos Unen elementos para formar moléculas o estas entre sí. COVALENTES (Se comparten electrones) NO POLARES (Entre elementos de igual electronegatividad
LOS COMPONENTES QUÍMICOS DE LA CÉLULA 1. Los enlaces químicos Unen elementos para formar moléculas o estas entre sí. COVALENTES (Se comparten electrones) NO POLARES (Entre elementos de igual electronegatividad
BIOLOGÍA 2º BACHILLERATO 1. BASE FISICO QUÍMICA DE LA VIDA (2) Clara Benhamú BIOELEMENTOS
 PROGRAMACIÓN: BLOQUE I. CUÁL ES LA COMPOSICIÓN DE LOS SERES VIVOS? LAS MOLÉCULAS DE LA VIDA Base físico-química 1. Composición de los seres vivos: bioelementos y biomoléculas. 2. El agua. 2.1. Estructura.
PROGRAMACIÓN: BLOQUE I. CUÁL ES LA COMPOSICIÓN DE LOS SERES VIVOS? LAS MOLÉCULAS DE LA VIDA Base físico-química 1. Composición de los seres vivos: bioelementos y biomoléculas. 2. El agua. 2.1. Estructura.
Las propiedades tan peculiares que presenta la molécula de agua son debidas a su estructura molecular. Ésta tiene las siguientes características:
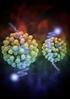 MOLÉCULAS INORGÁNICAS: AGUA Y SALES MINERALES El agua. Estructura de la molécula y carácter dipolar. Enlaces por puentes de H y estructura reticular del agua líquida. Propiedades fisicoquímicas del agua;
MOLÉCULAS INORGÁNICAS: AGUA Y SALES MINERALES El agua. Estructura de la molécula y carácter dipolar. Enlaces por puentes de H y estructura reticular del agua líquida. Propiedades fisicoquímicas del agua;
EL AGUA Y LAS SALES MINERALES
 EL AGUA Y LAS SALES MINERALES El agua es el componente molecular más abundante en los seres vivos. La cantidad varía con la edad de los animales: Por ejemplo en el embrión el porcentaje aproximado es del
EL AGUA Y LAS SALES MINERALES El agua es el componente molecular más abundante en los seres vivos. La cantidad varía con la edad de los animales: Por ejemplo en el embrión el porcentaje aproximado es del
Elementos químicos - compuestos moleculares - nivel celular (bioelementos) - (biomoléculas) - (procariota-eucariota)
 NIVELES DE ORGANIZACIÓN DE LOS SERES VIVOS Esta organización hace referencia a cómo se estructuran los diferentes componentes materiales hasta llegar al nivel celular, y posteriormente su distinción entre
NIVELES DE ORGANIZACIÓN DE LOS SERES VIVOS Esta organización hace referencia a cómo se estructuran los diferentes componentes materiales hasta llegar al nivel celular, y posteriormente su distinción entre
Niveles de organización biológica. La composición de los seres vivos
 Niveles de organización biológica. La composición de los seres vivos Imagen de Fondo bajo licencia Creative Commons, autor: René Ehrtardt. Animación ADN de dominio público, fuente:wikipedia Con este tema
Niveles de organización biológica. La composición de los seres vivos Imagen de Fondo bajo licencia Creative Commons, autor: René Ehrtardt. Animación ADN de dominio público, fuente:wikipedia Con este tema
1. Concepto de sistema tampón. Cita algunos ejemplos biológicos de tampones inorgánicos.
 VALENCIA (COMUNIDAD VALENCIANA) / JUNIO 00. COU / BIOLOGIA / BIOMOLECULAS / OPCION A / EJERCICIO 1 OPCION A 1. Concepto de sistema tampón. Cita algunos ejemplos biológicos de tampones inorgánicos. La actividad
VALENCIA (COMUNIDAD VALENCIANA) / JUNIO 00. COU / BIOLOGIA / BIOMOLECULAS / OPCION A / EJERCICIO 1 OPCION A 1. Concepto de sistema tampón. Cita algunos ejemplos biológicos de tampones inorgánicos. La actividad
Guía Bioelementos y biomoléculas inorgánicas Profesor Gustavo Arriagada Bustamante Primero medio. Unidad 1. Estructura y función de los seres vivos.
 Guía Bioelementos y biomoléculas inorgánicas Profesor Gustavo Arriagada Bustamante Primero medio. Unidad 1. Estructura y función de los seres vivos. Nombre: Curso: Fecha: Objetivos Identificar las principales
Guía Bioelementos y biomoléculas inorgánicas Profesor Gustavo Arriagada Bustamante Primero medio. Unidad 1. Estructura y función de los seres vivos. Nombre: Curso: Fecha: Objetivos Identificar las principales
Organización básica del cuerpo humano
 Organización básica del cuerpo humano I. Niveles de organización del cuerpo humano El ser humano es un organismo extremadamente complejo. Existen diferentes niveles de complejidad o de organización en
Organización básica del cuerpo humano I. Niveles de organización del cuerpo humano El ser humano es un organismo extremadamente complejo. Existen diferentes niveles de complejidad o de organización en
1.2. PROPIEDADES FÍSICO QUÍMICAS Y FUNCIONES BIOLÓGICAS DEL AGUA
 1. EL AGUA Es el componente mayoritario de todos los seres vivos, representando por término medio un 70% de su peso total. Está en continua renovación. El contenido en agua varía según el tipo de organismo,
1. EL AGUA Es el componente mayoritario de todos los seres vivos, representando por término medio un 70% de su peso total. Está en continua renovación. El contenido en agua varía según el tipo de organismo,
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2010 QUÍMICA TEMA 3: ENLACES QUÍMICOS
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 010 QUÍMICA TEMA : ENLACES QUÍMICOS Junio, Ejercicio, Opción A Reserva 1, Ejercicio, Opción A Reserva, Ejercicio, Opción B Reserva, Ejercicio, Opción B Septiembre,
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 010 QUÍMICA TEMA : ENLACES QUÍMICOS Junio, Ejercicio, Opción A Reserva 1, Ejercicio, Opción A Reserva, Ejercicio, Opción B Reserva, Ejercicio, Opción B Septiembre,
IES Atenea (S.S. de los Reyes) Departamento de Física y Química. PAU Química. Septiembre Fase específica OPCIÓN A
 1 PAU Química. Septiembre 2010. Fase específica OPCIÓN A Cuestión 1A. Considere las sustancias: cloruro de potasio, agua, cloro y sodio. a) Indique el tipo de enlace que presenta cada una de ellas. b)
1 PAU Química. Septiembre 2010. Fase específica OPCIÓN A Cuestión 1A. Considere las sustancias: cloruro de potasio, agua, cloro y sodio. a) Indique el tipo de enlace que presenta cada una de ellas. b)
NÚCLEO TEMÁTICO 1. La materia es todo aquello que nos rodea, ocupa un lugar en el espacio y tiene masa.
 BIOQUÍMICA NÚCLEO TEMÁTICO 1 Introducción Bioquímica: es una rama de la química y es la ciencia que estudia los componentes químicos de los seres vivos, especialmente las proteínas, carbohidratos, lípidos
BIOQUÍMICA NÚCLEO TEMÁTICO 1 Introducción Bioquímica: es una rama de la química y es la ciencia que estudia los componentes químicos de los seres vivos, especialmente las proteínas, carbohidratos, lípidos
TEMA 1.LA MATERIA VIVA. AGUA Y SALES MINERALES.
 TEMA 1.LA MATERIA VIVA. AGUA Y SALES MINERALES. 1. Los bioelementos. Los elementos más abundantes en la corteza terrestre (O, Si, Al, Fe, etc.) no son los que forman la mayor parte de la materia viva (C,
TEMA 1.LA MATERIA VIVA. AGUA Y SALES MINERALES. 1. Los bioelementos. Los elementos más abundantes en la corteza terrestre (O, Si, Al, Fe, etc.) no son los que forman la mayor parte de la materia viva (C,
BIOMOLÉCULAS. Son moléculas fundamentales para la constitución y funcionamiento de todo ser vivo. Se clasifican en dos grupos:
 FICHA N 2 UNIDAD III: CÉLULAS A ORGANISMOS Profesora Verónica Abasto Córdova Ciencias Naturales 8 Básico Nombre : Curso : Fecha : Revisión BIOMOLÉCULAS Son moléculas fundamentales para la constitución
FICHA N 2 UNIDAD III: CÉLULAS A ORGANISMOS Profesora Verónica Abasto Córdova Ciencias Naturales 8 Básico Nombre : Curso : Fecha : Revisión BIOMOLÉCULAS Son moléculas fundamentales para la constitución
Las funciones de los seres vivos. Fisiología celular
 Las funciones de los seres vivos Fisiología celular La célula, como unidad funcional de los seres vivos, está capacitada para llevar a cabo las funciones características de éstos: nutrición, reproducción
Las funciones de los seres vivos Fisiología celular La célula, como unidad funcional de los seres vivos, está capacitada para llevar a cabo las funciones características de éstos: nutrición, reproducción
Una mezcla es un compuesto formado por varias sustancias con distintas propiedades
 COMPOSICIÓN DE LA MATERIA Mezclas homogéneas y heterogéneas Una mezcla es un compuesto formado por varias sustancias con distintas propiedades Algunos sistemas materiales como la leche a simple vista parecen
COMPOSICIÓN DE LA MATERIA Mezclas homogéneas y heterogéneas Una mezcla es un compuesto formado por varias sustancias con distintas propiedades Algunos sistemas materiales como la leche a simple vista parecen
I) Biomoléculas 3) El agua I-3 EL AGUA
 I-3 EL AGUA IMPORTANCIA DEL AGUA PARA LOS SERES VIVOS El agua es el líquido más abundante de la corteza y uno de los pocos líquidos naturales. No es de extrañar entonces que el agua sea una sustancia esencial
I-3 EL AGUA IMPORTANCIA DEL AGUA PARA LOS SERES VIVOS El agua es el líquido más abundante de la corteza y uno de los pocos líquidos naturales. No es de extrañar entonces que el agua sea una sustancia esencial
Tema 1. Introducción
 Tema 1. Introducción - Bioquímica: concepto, y objetivos - Importancia de la Bioquímica en la Lic. De Farmacia - Composición química del cuerpo humano: Bioelementos Bioelementos primarios o principales
Tema 1. Introducción - Bioquímica: concepto, y objetivos - Importancia de la Bioquímica en la Lic. De Farmacia - Composición química del cuerpo humano: Bioelementos Bioelementos primarios o principales
EJERCICIOS DE BIOQUÍMICA: BIOELEMENTOS. AGUA Y SALES MINERALES
 EJERCICIOS DE BIOQUÍMICA: BIOELEMENTOS. AGUA Y SALES MINERALES 1) El siguiente cuadro representa el % de agua de ciertos organismos, qué deduces de ello? Por qué crees que es tan bajo el % de agua en las
EJERCICIOS DE BIOQUÍMICA: BIOELEMENTOS. AGUA Y SALES MINERALES 1) El siguiente cuadro representa el % de agua de ciertos organismos, qué deduces de ello? Por qué crees que es tan bajo el % de agua en las
TEMA Nº 1.- COMPONENTES DE LA MATERIA VIVA. AGUA Y SALES MINERALES
 Componentes de la materia viva. Agua y sales minerales 5 TEMA Nº 1.- COMPONENTES DE LA MATERIA VIVA. AGUA Y SALES MINERALES INTRODUCCIÓN Etimológicamente, el término biología proviene del griego (bios=vida,
Componentes de la materia viva. Agua y sales minerales 5 TEMA Nº 1.- COMPONENTES DE LA MATERIA VIVA. AGUA Y SALES MINERALES INTRODUCCIÓN Etimológicamente, el término biología proviene del griego (bios=vida,
Tema 7: Características generales de los seres vivos
 Tema 7: Características generales de los seres vivos Constituyentes químicos Bioelementos-Elementos biogénicos: elementos que forman a los seres vivos. Primarios: (98%) C,H,O;N;P y S. Secundarios: Ca,
Tema 7: Características generales de los seres vivos Constituyentes químicos Bioelementos-Elementos biogénicos: elementos que forman a los seres vivos. Primarios: (98%) C,H,O;N;P y S. Secundarios: Ca,
Profesor: Carlos Gutiérrez Arancibia. Temas a tratar: - - Sustancias Puras - Mezclas - Enlaces Químicos - Fuerzas Intermoleculares
 Profesor: Carlos Gutiérrez Arancibia Temas a tratar: - - Sustancias Puras - Mezclas - Enlaces Químicos - Fuerzas Intermoleculares A. Sustancia Pura: SUSTANCIAS PURAS Y MEZCLAS Una sustancia pura es un
Profesor: Carlos Gutiérrez Arancibia Temas a tratar: - - Sustancias Puras - Mezclas - Enlaces Químicos - Fuerzas Intermoleculares A. Sustancia Pura: SUSTANCIAS PURAS Y MEZCLAS Una sustancia pura es un
SOLUCIONARIO Guía Estándar Anual
 SOLUCIONARIO Guía Estándar Anual El enlace químico SGUICES004CB33-A16V1 Ítem Alternativa Habilidad 1 E Reconocimiento 2 B Aplicación 3 C Comprensión 4 D Comprensión 5 D Aplicación 6 D Aplicación 7 D Comprensión
SOLUCIONARIO Guía Estándar Anual El enlace químico SGUICES004CB33-A16V1 Ítem Alternativa Habilidad 1 E Reconocimiento 2 B Aplicación 3 C Comprensión 4 D Comprensión 5 D Aplicación 6 D Aplicación 7 D Comprensión
J. L. Sánchez Guillén. IES Pando - Oviedo Departamento de Biología y Geología 1
 J. L. Sánchez Guillén IES Pando - Oviedo Departamento de Biología y Geología 1 El agua es la molécula más abundante en los medios orgánicos. Un 70% del peso celular está formado por moléculas de agua.
J. L. Sánchez Guillén IES Pando - Oviedo Departamento de Biología y Geología 1 El agua es la molécula más abundante en los medios orgánicos. Un 70% del peso celular está formado por moléculas de agua.
La organización del cuerpo humano. Punto 1: Los niveles de organización.
 La organización del cuerpo humano Punto 1: Los niveles de organización. ATOMO MOLECULA Unidad constituyente más pequeña de la materia ordinaria. Conjunto de al menos dos átomos enlazados covalentes que
La organización del cuerpo humano Punto 1: Los niveles de organización. ATOMO MOLECULA Unidad constituyente más pequeña de la materia ordinaria. Conjunto de al menos dos átomos enlazados covalentes que
Agua, carbohidratos y Lípidos
 Agua, carbohidratos y Lípidos Biomoléculas Inorgánicas Características del agua El agua es el principal e imprescindible componente del cuerpo humano. Aproximadamente el 60 % de este agua se encuentra
Agua, carbohidratos y Lípidos Biomoléculas Inorgánicas Características del agua El agua es el principal e imprescindible componente del cuerpo humano. Aproximadamente el 60 % de este agua se encuentra
O Un elemento químico es una sustancia que no puede dividirse en otras sustancias por medios químicos comunes. Actualmente los químicos reconocen 92
 BIOELEMENTOS BIOELEMENTOS O La vida se compone de materia, que es todo lo que ocupa espacio y tiene masa. La materia, en forma tan diversas como una roca, madera, metal y aire, se compone de elementos
BIOELEMENTOS BIOELEMENTOS O La vida se compone de materia, que es todo lo que ocupa espacio y tiene masa. La materia, en forma tan diversas como una roca, madera, metal y aire, se compone de elementos
TRANSPORTE A TRAVÉS DE LA MEMBRANA CELULAR
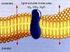 TRANSPORTE A TRAVÉS DE LA MEMBRANA CELULAR Introducción Compartimientos Acuosos separados por Barreras Biológicas Organelos selectivos, autocatalíticos, autoreproductivos, competitivos, adaptativos...
TRANSPORTE A TRAVÉS DE LA MEMBRANA CELULAR Introducción Compartimientos Acuosos separados por Barreras Biológicas Organelos selectivos, autocatalíticos, autoreproductivos, competitivos, adaptativos...
Composición química de los seres vivos
 Composición química de los seres vivos Elementos químicos de la materia viva BIOELEMENTOS Se clasifican por su abundancia En proporcion superior al 96% PRIMARIOS En una proporción aprox. 3,9% SECUNDARIOS
Composición química de los seres vivos Elementos químicos de la materia viva BIOELEMENTOS Se clasifican por su abundancia En proporcion superior al 96% PRIMARIOS En una proporción aprox. 3,9% SECUNDARIOS
TEMA 8 La Tierra un planeta habitado
 TEMA 8 La Tierra un planeta habitado La vida en la Tierra Características que permiten la vida en la Tierra: 1. La distancia al sol: rotación/traslación, inclinación eje terrestre. Luz y calor 2. Presencia
TEMA 8 La Tierra un planeta habitado La vida en la Tierra Características que permiten la vida en la Tierra: 1. La distancia al sol: rotación/traslación, inclinación eje terrestre. Luz y calor 2. Presencia
I) Biomoléculas 2) El agua I-2 EL AGUA
 I-2 EL AGUA IMPRTANCIA DEL AGUA PARA LS SERES VIVS El agua es el líquido más abundante de la corteza y uno de los pocos líquidos naturales. No es de extrañar entonces que el agua sea una sustancia esencial
I-2 EL AGUA IMPRTANCIA DEL AGUA PARA LS SERES VIVS El agua es el líquido más abundante de la corteza y uno de los pocos líquidos naturales. No es de extrañar entonces que el agua sea una sustancia esencial
EL AGUA Y LAS SALES MINERALES. ( Cataratas de Yosemite en California)
 EL AGUA Y LAS SALES MINERALES ( Cataratas de Yosemite en California) EL AGUA ES LA BIOMOLÉCULA MÁS ABUNDANTE EN LOS SERES VIVOS La vida surgió en el agua y depende para su existencia de la presencia de
EL AGUA Y LAS SALES MINERALES ( Cataratas de Yosemite en California) EL AGUA ES LA BIOMOLÉCULA MÁS ABUNDANTE EN LOS SERES VIVOS La vida surgió en el agua y depende para su existencia de la presencia de
Biomoléculas orgánicas: Carbohidratos y Lípidos. Propiedad Intelectual Cpech
 Biología Biomoléculas orgánicas: Carbohidratos y Lípidos Repaso Biomoléculas. Biomoléculas inorgánicas: Moléculas que no presentan carbono en su estructura. Biomoléculas orgánicas: Moléculas que presentan
Biología Biomoléculas orgánicas: Carbohidratos y Lípidos Repaso Biomoléculas. Biomoléculas inorgánicas: Moléculas que no presentan carbono en su estructura. Biomoléculas orgánicas: Moléculas que presentan
LA ORGANIZACIÓN DEL CUERPO HUMANO
 LA ORGANIZACIÓN DEL CUERPO HUMANO RICARDO, ALBERTO, PABLO Y JORGE 1º Los niveles de organización Todos los seres vivos estamos dotados de un conjunto de estructuras con sus funciones específicas. Ordenados
LA ORGANIZACIÓN DEL CUERPO HUMANO RICARDO, ALBERTO, PABLO Y JORGE 1º Los niveles de organización Todos los seres vivos estamos dotados de un conjunto de estructuras con sus funciones específicas. Ordenados
Pág ª) Qué es un ser vivo? Un ser formado por células que es capaz de desempeñar las tres funciones vitales:
 TEMA 1 Pág. 160 1ª) Qué es un ser vivo? Un ser formado por células que es capaz de desempeñar las tres funciones vitales: Pág. 10 2ª ) Qué reinos de seres vivos habitan en la tierra? Moneras, protoctistas,
TEMA 1 Pág. 160 1ª) Qué es un ser vivo? Un ser formado por células que es capaz de desempeñar las tres funciones vitales: Pág. 10 2ª ) Qué reinos de seres vivos habitan en la tierra? Moneras, protoctistas,
FÍSICA Y QUÍMICA Solucionario ELECTRONES Y ENLACES
 FÍSICA Y QUÍMICA Solucionario ELECTRONES Y ENLACES 1.* Indicad cuántos electrones tienen en la última capa cada uno de estos elementos. a) C 4 f) O 6 k) K 1 b) F 7 g) P 5 l) S 6 c) Ne 8 h) H 1 m) He 8
FÍSICA Y QUÍMICA Solucionario ELECTRONES Y ENLACES 1.* Indicad cuántos electrones tienen en la última capa cada uno de estos elementos. a) C 4 f) O 6 k) K 1 b) F 7 g) P 5 l) S 6 c) Ne 8 h) H 1 m) He 8
Pág ª) Qué es un ser vivo? Un ser formado por células que es capaz de desempeñar las tres funciones vitales:
 TEMA 1 Pág. 160 1ª) Qué es un ser vivo? Un ser formado por células que es capaz de desempeñar las tres funciones vitales: Pág. 10 2ª ) Qué reinos de seres vivos habitan en la tierra? Moneras, protoctistas,
TEMA 1 Pág. 160 1ª) Qué es un ser vivo? Un ser formado por células que es capaz de desempeñar las tres funciones vitales: Pág. 10 2ª ) Qué reinos de seres vivos habitan en la tierra? Moneras, protoctistas,
BLOQUE II. ORGANIZACIÓN Y FISIOLOGÍA CELULAR
 I.E.S. Flavio Irnitano El Saucejo (Sevilla) Curso 2.015 2.016 Departamento de Biología y Geología NIVEL: 2º Bachillerato MATERIA: BIOLOGÍA BLOQUE II. ORGANIZACIÓN Y FISIOLOGÍA CELULAR 3. CÉLULA EUCARIÓTICA.
I.E.S. Flavio Irnitano El Saucejo (Sevilla) Curso 2.015 2.016 Departamento de Biología y Geología NIVEL: 2º Bachillerato MATERIA: BIOLOGÍA BLOQUE II. ORGANIZACIÓN Y FISIOLOGÍA CELULAR 3. CÉLULA EUCARIÓTICA.
ENLACES QUÍMICOS. Los enlaces químicos, son las fuerzas que mantienen unidos a los átomos.
 1. Generalidades de los enlaces químicos ENLACES QUÍMICOS Los enlaces químicos, son las fuerzas que mantienen unidos a los átomos. Cuando los átomos se enlazan entre sí, ceden, aceptan o comparten electrones.
1. Generalidades de los enlaces químicos ENLACES QUÍMICOS Los enlaces químicos, son las fuerzas que mantienen unidos a los átomos. Cuando los átomos se enlazan entre sí, ceden, aceptan o comparten electrones.
BIOLOGIA GENERAL Y METODOLOGIA DE LAS CIENCIAS Trabajo Práctico Nº 1:
 BIOLOGIA GENERAL Y METODOLOGIA DE LAS CIENCIAS Trabajo Práctico Nº 1: - 1 - NIVELES DE ORGANIZACIÓN Y BIOMOLÉCULAS Objetivos: Comprender como la materia se va organizando en diferentes niveles. Diferenciar
BIOLOGIA GENERAL Y METODOLOGIA DE LAS CIENCIAS Trabajo Práctico Nº 1: - 1 - NIVELES DE ORGANIZACIÓN Y BIOMOLÉCULAS Objetivos: Comprender como la materia se va organizando en diferentes niveles. Diferenciar
JUNIO FASE GENERAL QUÍMICA. OPCIÓN A
 JUNIO 2011. FASE GENERAL 1. (2,5 puntos) QUÍMICA. OPCIÓN A La nitroglicerina, C 3 H 5 N 3 O 9 (l), descompone a 1 atm y 25 ºC para formar N 2 (g), CO 2 (g), H 2 O(l) y O 2 (g), desprendiendo 1541,4 kj/mol
JUNIO 2011. FASE GENERAL 1. (2,5 puntos) QUÍMICA. OPCIÓN A La nitroglicerina, C 3 H 5 N 3 O 9 (l), descompone a 1 atm y 25 ºC para formar N 2 (g), CO 2 (g), H 2 O(l) y O 2 (g), desprendiendo 1541,4 kj/mol
IES Atenea (S.S. de los Reyes) Departamento de Física y Química. PAU Química. Septiembre 2006 PRIMERA PARTE
 1 PAU Química. Septiembre 2006 PRIMERA PARTE Cuestión 1. La configuración electrónica del último nivel energético de un elemento es 4s 2 4p 3. De acuerdo con este dato: a) Deduzca la situación de dicho
1 PAU Química. Septiembre 2006 PRIMERA PARTE Cuestión 1. La configuración electrónica del último nivel energético de un elemento es 4s 2 4p 3. De acuerdo con este dato: a) Deduzca la situación de dicho
Interacciones químicas de no enlace. Fuerzas de van der Waals
 Interacciones químicas de no enlace IES La Magdalena. Avilés. Asturias En el mundo material, además de los enlaces entre átomos existen otras interacciones, más débiles, pero lo suficientemente intensas
Interacciones químicas de no enlace IES La Magdalena. Avilés. Asturias En el mundo material, además de los enlaces entre átomos existen otras interacciones, más débiles, pero lo suficientemente intensas
QUÍMICA BIOINORGÁNICA. Corteza O Si Al Fe Ca Mg Na K Ti H B. Océanos O H Cl Na Mg Ca K C Br B Sr. Seres humanos H O C N Na K Ca Mg P S Cl
 Química Inorgánica Química bioinorgánica 1 QUÍMICA BIOINORGÁNICA La química bioinorgánica es el estudio de los elementos inorgánicos que se utilizan en biología. La materia viviente está basada en estructuras
Química Inorgánica Química bioinorgánica 1 QUÍMICA BIOINORGÁNICA La química bioinorgánica es el estudio de los elementos inorgánicos que se utilizan en biología. La materia viviente está basada en estructuras
TEMA 7: LA MEMBRANA PLASMÁTICA.
 TEMA 7: LA MEMBRANA PLASMÁTICA. 1.-La membrana plasmática como unidad estructural. 2.- Características de la membrana plasmática. 2.1. Estructura y composición. 2.2. Propiedades de la membrana plasmática.
TEMA 7: LA MEMBRANA PLASMÁTICA. 1.-La membrana plasmática como unidad estructural. 2.- Características de la membrana plasmática. 2.1. Estructura y composición. 2.2. Propiedades de la membrana plasmática.
GUÍA PARA EXAMEN DE REGULARIZACIÓN DE QUÍMICA 1
 GUÍA PARA EXAMEN DE REGULARIZACIÓN DE QUÍMICA 1 1.- Ciencia que estudia la composición, estructura de la materia y sus transformaciones. R= Química 2.-Es todo lo que tiene masa y posee inercia R= Materia
GUÍA PARA EXAMEN DE REGULARIZACIÓN DE QUÍMICA 1 1.- Ciencia que estudia la composición, estructura de la materia y sus transformaciones. R= Química 2.-Es todo lo que tiene masa y posee inercia R= Materia
SESIÓN 3 LA QUÍMICA DE LA VIDA
 Biología SESIÓN 3 LA QUÍMICA DE LA VIDA 1. Las Bases Químicas De La Vida Los organismos vivos y el mundo en el que viven están sometidos a las leyes de la física y de la química. En los organismos vivos
Biología SESIÓN 3 LA QUÍMICA DE LA VIDA 1. Las Bases Químicas De La Vida Los organismos vivos y el mundo en el que viven están sometidos a las leyes de la física y de la química. En los organismos vivos
TEMA 1: SERES VIVOS Y MATERIA PRIMA
 1. Características de los seres vivos TEMA 1: SERES VIVOS Y MATERIA PRIMA La Biología se define como la ciencia que estudia a los seres vivos. Los seres vivos están formados por moléculas que individualmente
1. Características de los seres vivos TEMA 1: SERES VIVOS Y MATERIA PRIMA La Biología se define como la ciencia que estudia a los seres vivos. Los seres vivos están formados por moléculas que individualmente
Biología 2 Segundo de Media. Proyecto 1 Agosto/Sept Prof.: Lic. Manuel B. Noboa G.
 Biología 2 Segundo de Media. Proyecto 1 Agosto/Sept. 2016. Prof.: Lic. Manuel B. Noboa G. Unidad Nº 1: Las funciones vitales: Nutrición Animal y Vegetal. Cómo puedes describir las funciones vitales de
Biología 2 Segundo de Media. Proyecto 1 Agosto/Sept. 2016. Prof.: Lic. Manuel B. Noboa G. Unidad Nº 1: Las funciones vitales: Nutrición Animal y Vegetal. Cómo puedes describir las funciones vitales de
OBJETIVO.- Diferenciar los distintos tipos de enlace químico para establecer las propiedades de cada compuesto.
 OBJETIVO.- Diferenciar los distintos tipos de enlace químico para establecer las propiedades de cada compuesto. 1. Generalidades de los enlaces químicos Los enlaces químicos, son las fuerzas que mantienen
OBJETIVO.- Diferenciar los distintos tipos de enlace químico para establecer las propiedades de cada compuesto. 1. Generalidades de los enlaces químicos Los enlaces químicos, son las fuerzas que mantienen
Unidad I: Propiedades Periódicas: Masa y Enlace
 Unidad I: Propiedades Periódicas: Masa y Enlace 1. Nociones de teoría atómica moderna 2. Propiedades periódicas de los elementos 3. Enlace iónico y covalente 4. Masas atómicas y moleculares 1. Nociones
Unidad I: Propiedades Periódicas: Masa y Enlace 1. Nociones de teoría atómica moderna 2. Propiedades periódicas de los elementos 3. Enlace iónico y covalente 4. Masas atómicas y moleculares 1. Nociones
TEMA 8 SISTEMA PERIÓDICO Y ENLACES
 TEMA 8 SISTEMA PERIÓDICO Y ENLACES 1. LA TABLA PERIÓDICA Elementos químicos son el conjunto de átomos que tienen en común su número atómico, Z. Hoy conocemos 111 elementos diferentes. Los elementos que
TEMA 8 SISTEMA PERIÓDICO Y ENLACES 1. LA TABLA PERIÓDICA Elementos químicos son el conjunto de átomos que tienen en común su número atómico, Z. Hoy conocemos 111 elementos diferentes. Los elementos que
UNIDAD 1. D. Borja Blanco Vives. Profesor de Biología y Geología 4ºESO
 UNIDAD 1. D. Borja Blanco Vives. Profesor de Biología y Geología 4ºESO 1. LA COMPOSICIÓN DE LOS SERES VIVOS. Todos los seres vivos están formados por: - materia inorgánica: agua y sales minerales - materia
UNIDAD 1. D. Borja Blanco Vives. Profesor de Biología y Geología 4ºESO 1. LA COMPOSICIÓN DE LOS SERES VIVOS. Todos los seres vivos están formados por: - materia inorgánica: agua y sales minerales - materia
El agua es la molécula más abundante en l o s m e d i o s orgánicos. Un 70% del. está formado por moléculas de agua.
 EL AGUA EL AGUA El agua es la molécula más abundante en l o s m e d i o s orgánicos. Un 70% del peso celular está formado por moléculas de agua. El agua es la molécula más abundante en l o s m e d i o
EL AGUA EL AGUA El agua es la molécula más abundante en l o s m e d i o s orgánicos. Un 70% del peso celular está formado por moléculas de agua. El agua es la molécula más abundante en l o s m e d i o
ANDALUCÍA / JUNIO 2000 LOGSE / QUÍMICA / OPCIÓN A /EXAMEN COMPLETO OPCIÓN A
 OPCIÓN A 1. ormule o nombre los siguientes compuestos: a) Óxido de cromo (III) b) osfato de calcio c) Ácido benzoico d) BaSO 4 e) KNO 3 f) CH 3 CH 2 OH 2. Razone qué cantidad de las siguientes sustancias
OPCIÓN A 1. ormule o nombre los siguientes compuestos: a) Óxido de cromo (III) b) osfato de calcio c) Ácido benzoico d) BaSO 4 e) KNO 3 f) CH 3 CH 2 OH 2. Razone qué cantidad de las siguientes sustancias
Valor 3 puntos. 42. a. Diferenciación. b. Mutaciones. c. Recombinación. d. Herencia.
 Valor 3 puntos Las alteraciones que se producen en el material cromosómico ó genético de las células y que son capaces de transmitirse a la descendencia se denominan: 42. a. Diferenciación. b. Mutaciones.
Valor 3 puntos Las alteraciones que se producen en el material cromosómico ó genético de las células y que son capaces de transmitirse a la descendencia se denominan: 42. a. Diferenciación. b. Mutaciones.
La Célula. Membrana celular. UNIVERSIDAD NACIONAL DE GRAL. SAN MARTÍN ECyT BIOLOGÍA. Biología I
 La Célula. Membrana celular UNIVERSIDAD NACIONAL DE GRAL. SAN MARTÍN ECyT BIOLOGÍA Biología I Los seres vivos están formados por células Organismos unicelulares: bacterias, plantas (algas unicelulares),
La Célula. Membrana celular UNIVERSIDAD NACIONAL DE GRAL. SAN MARTÍN ECyT BIOLOGÍA Biología I Los seres vivos están formados por células Organismos unicelulares: bacterias, plantas (algas unicelulares),
ENLACE QUÍMICO 2º BACH EJERCICIOS DE ENLACE QUÍMICO DEL LIBRO 28. H-CHO H C = O : CH 3 OH H C O H H H H C O C H H H CH 3 OCH 3
 EJERCICIOS DE ENLACE QUÍMICO DEL LIBRO 28. -CO C = O : C 3 O C O C 3 OC 3 C O C a) La longitud de enlace CO es menor en el formaldehido, ya que tiene un doble enlace. b) El metanol puede formar enlaces
EJERCICIOS DE ENLACE QUÍMICO DEL LIBRO 28. -CO C = O : C 3 O C O C 3 OC 3 C O C a) La longitud de enlace CO es menor en el formaldehido, ya que tiene un doble enlace. b) El metanol puede formar enlaces
Tema VI: Transporte Celular
 República Bolivariana de Venezuela Ministerio del Poder Popular para la Educación U.E. Colegio Santo Tomás de Villanueva Departamento de Ciencias Cátedra: Ciencias Biológicas 3 Año Tema VI: Transporte
República Bolivariana de Venezuela Ministerio del Poder Popular para la Educación U.E. Colegio Santo Tomás de Villanueva Departamento de Ciencias Cátedra: Ciencias Biológicas 3 Año Tema VI: Transporte
2x = x = M. 100 = α = % NOCl eq K C =
 1 Universidad de Castilla la Mancha Selectividad Septiembre.013 Opción A SEPTIEMBRE 013 1.- El cloruro de nitrosilo es un gas utilizado en la síntesis de productos farmacéuticos. Se descompone a altas
1 Universidad de Castilla la Mancha Selectividad Septiembre.013 Opción A SEPTIEMBRE 013 1.- El cloruro de nitrosilo es un gas utilizado en la síntesis de productos farmacéuticos. Se descompone a altas
Las que tienen relación con el de tamaño: LAS PROPIEDADES PERIÓDICAS. Se pueden separar en dos grupos: PERIODICIDAD
 LAS PROPIEDADES PERIÓDICAS Se pueden separar en dos grupos: 1- Las que tienen relación con el de tamaño: Los radios atómicos y los radios iónicos o cristalinos. La densidad. (ρ) El punto de fusión y ebullición.
LAS PROPIEDADES PERIÓDICAS Se pueden separar en dos grupos: 1- Las que tienen relación con el de tamaño: Los radios atómicos y los radios iónicos o cristalinos. La densidad. (ρ) El punto de fusión y ebullición.
COMPLEJO EDUCACIONAL JOAQUIN EDWARDS BELLO GUÍA REFORZAMIENTO 1 MEDIO
 COMPLEJO EDUCACIONAL JOAQUIN EDWARDS BELLO GUÍA REFORZAMIENTO 1 MEDIO NOMBRE: PJE. TOTAL: FECHA: CURSO: 1 MEDIO PJE. OBTENIDO: CALIFICACION: ASIGNATURA: BIOLOGIA UNIDAD: I - II OBJETIVO (S): CONTENIDO
COMPLEJO EDUCACIONAL JOAQUIN EDWARDS BELLO GUÍA REFORZAMIENTO 1 MEDIO NOMBRE: PJE. TOTAL: FECHA: CURSO: 1 MEDIO PJE. OBTENIDO: CALIFICACION: ASIGNATURA: BIOLOGIA UNIDAD: I - II OBJETIVO (S): CONTENIDO
PRUEBA DE ADMISIÓN 2012
 Nº Prueba I. Datos generales del postulante: Nombre completo: Edad: Colegio de procedencia: Nº Solicitud: Dirección: Nº Tel/ Cel.: Correo Electrónico E-mail: Carrera de interés: (Puede anotar más de una)
Nº Prueba I. Datos generales del postulante: Nombre completo: Edad: Colegio de procedencia: Nº Solicitud: Dirección: Nº Tel/ Cel.: Correo Electrónico E-mail: Carrera de interés: (Puede anotar más de una)
Biología General y Metodología de las Ciencias 2016 BIOMOLÉCULAS
 BIOMOLÉCULAS Objetivos: Reconocer los distintos niveles de organización de la materia. Diferenciar las propiedades constreñimiento, emergentes y colectivas. Identificar las principales Biomoléculas según
BIOMOLÉCULAS Objetivos: Reconocer los distintos niveles de organización de la materia. Diferenciar las propiedades constreñimiento, emergentes y colectivas. Identificar las principales Biomoléculas según
5ª UNIDAD ELEMENTOS Y COMPUESTOS
 5ª UNIDAD ELEMENTOS Y COMPUESTOS 3º E.S.O. Grupo Apellidos: Nombre: INTRODUCCIÓN Comenzamos recordando los conceptos más importantes del tema anterior: Cómo son los átomos? Cómo están distribuidos los
5ª UNIDAD ELEMENTOS Y COMPUESTOS 3º E.S.O. Grupo Apellidos: Nombre: INTRODUCCIÓN Comenzamos recordando los conceptos más importantes del tema anterior: Cómo son los átomos? Cómo están distribuidos los
FISIOLOGÍA GENERAL Jesús Merino Pérez y María José Noriega Borge
 INTRODUCCIÓN AL ESTUDIO DE LA FISIOLOGÍA La Fisiología General es una parte de las Ciencias Fisiológicas encargada de estudiar las bases de funcionamiento de los seres vivos. Apoyándose en las leyes y
INTRODUCCIÓN AL ESTUDIO DE LA FISIOLOGÍA La Fisiología General es una parte de las Ciencias Fisiológicas encargada de estudiar las bases de funcionamiento de los seres vivos. Apoyándose en las leyes y
ESCUELA SUPERIOR POLITÉCNICA DEL LITORAL BIOLOGIA (2005) I TERMINO PRIMERA EVALUACION
 ESCUELA SUPERIOR POLITÉCNICA DEL LITORAL BIOLOGIA (2005) I TERMINO PRIMERA EVALUACION Nombre:... Paralelo:. Firma:. # Matrícula: No utilizar corrector ni hacer tachones, automáticamente queda anulada la
ESCUELA SUPERIOR POLITÉCNICA DEL LITORAL BIOLOGIA (2005) I TERMINO PRIMERA EVALUACION Nombre:... Paralelo:. Firma:. # Matrícula: No utilizar corrector ni hacer tachones, automáticamente queda anulada la
-aproximadamente 60% del organismo humano. -componente mas abundante en la mayoría de los alimentos
 EL AGUA -aproximadamente 60% del organismo humano -componente mas abundante en la mayoría de los alimentos -responsable del carácter apetecible de muchos alimentos y también de la aptitud al deterioro
EL AGUA -aproximadamente 60% del organismo humano -componente mas abundante en la mayoría de los alimentos -responsable del carácter apetecible de muchos alimentos y también de la aptitud al deterioro
Actualización en Medio Interno Conceptos básicos
 Actualización en Medio Interno Conceptos básicos Bioquímica Lucrecia Drago Bioquímica M. Fernanda Pontoriero Ácidos Moléculas capaces de liberar H + HCl H + + Cl H 2 CO 3 H + + HCO 3 Bases Moléculas capaces
Actualización en Medio Interno Conceptos básicos Bioquímica Lucrecia Drago Bioquímica M. Fernanda Pontoriero Ácidos Moléculas capaces de liberar H + HCl H + + Cl H 2 CO 3 H + + HCO 3 Bases Moléculas capaces
MC I Medio. El Agua y los iones. Manuel Mallol Simmonds
 El Agua y los iones MC I Medio El agua es una molécula ampliamente estudiada bajo los prismas de diferentes ciencias naturales. En la biología, el agua permite la existencia y desarrollo de la vida tal
El Agua y los iones MC I Medio El agua es una molécula ampliamente estudiada bajo los prismas de diferentes ciencias naturales. En la biología, el agua permite la existencia y desarrollo de la vida tal
Material elaborado por F. Agius, O. Borsani, P.Díaz, S. Gonnet, P. Irisarri, F. Milnitsky y J. Monza. Bioquímica. Facultad de Agronomía.
 AMINOACIDOS Las proteínas de bacterias, hongos, plantas y animales están constituidas a partir de las mismas 20 unidades o monómeros: los á-aminoácidos. Los aminoácidos tienen un grupo amino y un grupo
AMINOACIDOS Las proteínas de bacterias, hongos, plantas y animales están constituidas a partir de las mismas 20 unidades o monómeros: los á-aminoácidos. Los aminoácidos tienen un grupo amino y un grupo
TEMA 9 LAS FUNCIONES VITALES Y LA NUTRICIÓN VEGETAL. Asignatura: Ciencias de la Naturaleza de 2º ESO Profesor: David Leunda San Miguel
 TEMA 9 LAS FUNCIONES VITALES Y LA NUTRICIÓN VEGETAL Asignatura: Ciencias de la Naturaleza de 2º ESO Profesor: David Leunda San Miguel 1-.Las funciones vitales: introducción Existen 1.800.000 especies de
TEMA 9 LAS FUNCIONES VITALES Y LA NUTRICIÓN VEGETAL Asignatura: Ciencias de la Naturaleza de 2º ESO Profesor: David Leunda San Miguel 1-.Las funciones vitales: introducción Existen 1.800.000 especies de
Componentes químicos de
 Componentes químicos de las célulasc Componentes químicos Las células están compuestas por una enorme cantidad y variedad de moléculas que pueden clasificarse en: Componentes inorgánicos Componentes orgánicos
Componentes químicos de las célulasc Componentes químicos Las células están compuestas por una enorme cantidad y variedad de moléculas que pueden clasificarse en: Componentes inorgánicos Componentes orgánicos
LA CÉLULA Y LA BASE FÍSICO-QUÍMICA DE LA VIDA
 LA CÉLULA Y LA BASE FÍSICO-QUÍMICA DE LA VIDA 7. PAREDES CELULARES Y MEMBRANA PLASMÁTICA. ORGÁNULOS MICROTUBULARES 1. Membrana plasmática: (jun 97 B4) a) Dibuja un diagrama rotulado de la membrana plasmática
LA CÉLULA Y LA BASE FÍSICO-QUÍMICA DE LA VIDA 7. PAREDES CELULARES Y MEMBRANA PLASMÁTICA. ORGÁNULOS MICROTUBULARES 1. Membrana plasmática: (jun 97 B4) a) Dibuja un diagrama rotulado de la membrana plasmática
La célula. Unidad Los seres vivos están formados por células
 La célula Unidad Los seres vivos están formados por células Definición de célula. Es la unidad anatómico y funcional de todo ser vivo. Tiene función de autoconservación y autorreproducción. Es por esto,
La célula Unidad Los seres vivos están formados por células Definición de célula. Es la unidad anatómico y funcional de todo ser vivo. Tiene función de autoconservación y autorreproducción. Es por esto,
Actividad introductoria: Aplicación en la industria de las fuerzas intermoleculares.
 Grado 10 Ciencias - Unidad 3 Cómo se relacionan los componentes del mundo? Tema Cómo afectan las fuerzas intermoleculares las propiedades de los compuestos? Curso: Nombre: Actividad introductoria: Aplicación
Grado 10 Ciencias - Unidad 3 Cómo se relacionan los componentes del mundo? Tema Cómo afectan las fuerzas intermoleculares las propiedades de los compuestos? Curso: Nombre: Actividad introductoria: Aplicación
Bloque 5 Ponte en forma 2. Qué representa la estructura de Lewis? La estructura de Lewis representa los electrones externos o de valencia de un átomo.
 Bloque 5 Ponte en forma 2. Qué representa la estructura de Lewis? La estructura de Lewis representa los electrones externos o de valencia de un átomo. 3. Marca con una X el inciso que muestre la estructura
Bloque 5 Ponte en forma 2. Qué representa la estructura de Lewis? La estructura de Lewis representa los electrones externos o de valencia de un átomo. 3. Marca con una X el inciso que muestre la estructura
Los enlaces C F son polares pero la geometría tetraédrica
 1 PAU Química. Modelo 2010 PRIMERA PARTE Cuestión 1. Dadas las siguientes sustancias: CO 2, CF 4, H 2 CO y HF: a) Escriba las estructuras de Lewis de sus moléculas. b) Explique sus geometrías por la teoría
1 PAU Química. Modelo 2010 PRIMERA PARTE Cuestión 1. Dadas las siguientes sustancias: CO 2, CF 4, H 2 CO y HF: a) Escriba las estructuras de Lewis de sus moléculas. b) Explique sus geometrías por la teoría
QUÍMICA.SEPTIEMBRE (FE). OPCIÓN A
 1. (2,5 puntos) QUÍMICA.SEPTIEMBRE (FE). OPCIÓN A Las entalpías estándar de combustión del C(s), H 2 (g) y propano gas, C 3 H 8 (g), son -394, -286 y -2220 kj/mol, respectivamente: i. Calcule la entalpía
1. (2,5 puntos) QUÍMICA.SEPTIEMBRE (FE). OPCIÓN A Las entalpías estándar de combustión del C(s), H 2 (g) y propano gas, C 3 H 8 (g), son -394, -286 y -2220 kj/mol, respectivamente: i. Calcule la entalpía
JUNIO FASE ESPECÍFICA. QUÍMICA. OPCIÓN A
 JUNIO 2011. FASE ESPECÍFICA. QUÍMICA. OPCIÓN A 1. (2,5 puntos) Disponemos de los pares redox (Fe 2+ /Fe) y (O 2 /H 2 O), con potenciales estándar de reducción 0,44 V y +1,23 V, respectivamente. Con ellos
JUNIO 2011. FASE ESPECÍFICA. QUÍMICA. OPCIÓN A 1. (2,5 puntos) Disponemos de los pares redox (Fe 2+ /Fe) y (O 2 /H 2 O), con potenciales estándar de reducción 0,44 V y +1,23 V, respectivamente. Con ellos
EJERCICIOS RESUELTOS DE ENLACE QUIMICO
 EJERCICIOS RESUELTOS DE ENLACE QUIMICO 1. a) Qué tipo de enlace presenta el compuesto formado por F y Ca? b) Formule dicho compuesto a) Considerando los números atómicos del F (Z=9) y el Ca (Z=20) se desarrollan
EJERCICIOS RESUELTOS DE ENLACE QUIMICO 1. a) Qué tipo de enlace presenta el compuesto formado por F y Ca? b) Formule dicho compuesto a) Considerando los números atómicos del F (Z=9) y el Ca (Z=20) se desarrollan
MEMBRANA CELULAR: Modelo de organización, Transporte a través de membrana
 MEMBRANA CELULAR: Modelo de organización, Transporte a través de membrana Componentes de la membrana celular Modelo Mosaico Fluido Glúcidos Proteínas Colesterol Fosfolípidos Componentes de la membrana
MEMBRANA CELULAR: Modelo de organización, Transporte a través de membrana Componentes de la membrana celular Modelo Mosaico Fluido Glúcidos Proteínas Colesterol Fosfolípidos Componentes de la membrana
Los elementos químicos
 Los elementos químicos Física y Química Las primeras clasificaciones de los elementos Oxford University Press España, S. A. Física y Química 3º ESO 2 Un elemento químico es un tipo de materia constituido
Los elementos químicos Física y Química Las primeras clasificaciones de los elementos Oxford University Press España, S. A. Física y Química 3º ESO 2 Un elemento químico es un tipo de materia constituido
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE.
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 000 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE http://emestrada.wordpress.com Complete los siguientes equilibrios ácido-base identificando, de forma razonada, los
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 000 QUÍMICA TEMA 6: EQUILIBRIOS ÁCIDO-BASE http://emestrada.wordpress.com Complete los siguientes equilibrios ácido-base identificando, de forma razonada, los
3. OTROS ELEMENTOS. Iones y oligoelementos. Mencionar algunas de sus funciones e ilustrar algún ejemplo.
 TEMA 2. ELEMENTOS BIOGÉNICOS. GUIÓN. (1 sesión) 1. ELEMENTOS BIOGÉNICOS. -Concepto. 2. BIOELEMENTOS PRIMARIOS -RAZÓNES DE LA ABUNDANCIA DE C, H, O y N. 3. OTROS ELEMENTOS. Iones y oligoelementos. Mencionar
TEMA 2. ELEMENTOS BIOGÉNICOS. GUIÓN. (1 sesión) 1. ELEMENTOS BIOGÉNICOS. -Concepto. 2. BIOELEMENTOS PRIMARIOS -RAZÓNES DE LA ABUNDANCIA DE C, H, O y N. 3. OTROS ELEMENTOS. Iones y oligoelementos. Mencionar
COLEGIO SAN JOSÉ - Hijas de María Auxiliadora C/ Emilio Ferrari, 87 - Madrid Departamento de Ciencias Naturales
 TEMA 1. ELEMENTOS Y COMPUESTOS EJERCICIOS Y SOLUCIONES 4. El sistema periódico 1. Escribe la configuración electrónica de los 3 primeros elementos alcalinotérreos y explica razonadamente si estos elementos
TEMA 1. ELEMENTOS Y COMPUESTOS EJERCICIOS Y SOLUCIONES 4. El sistema periódico 1. Escribe la configuración electrónica de los 3 primeros elementos alcalinotérreos y explica razonadamente si estos elementos
SOLUCIONES EJERCICIOS DE ENLACE QUÍMICO. 1º BCT
 SOLUCIOES EJERCICIOS DE ELACE QUÍMICO. 1º CT 1. La teoría de la repulsión de los pares electrónicos de la capa de valencia (TRPECV) dice que los pares electrónicos que rodean al átomo central se disponen
SOLUCIOES EJERCICIOS DE ELACE QUÍMICO. 1º CT 1. La teoría de la repulsión de los pares electrónicos de la capa de valencia (TRPECV) dice que los pares electrónicos que rodean al átomo central se disponen
FÍSICA Y QUÍMICA - 3º ESO ESTRUCTURA ATOMICA Y ENLACE 2
 FÍSICA Y QUÍMICA - 3º ESO ESTRUCTURA ATOMICA Y ENLACE 2 1. Define y explica los siguientes conceptos: número atómico, número másico e isótopos de un elemento químico. 2. Copia el siguiente párrafo y complétalo:
FÍSICA Y QUÍMICA - 3º ESO ESTRUCTURA ATOMICA Y ENLACE 2 1. Define y explica los siguientes conceptos: número atómico, número másico e isótopos de un elemento químico. 2. Copia el siguiente párrafo y complétalo:
Explicación de las propiedades y los estados de agregación en los compuestos químicos en función de los tipos de enlace. vs.
 Explicación de las propiedades y los estados de agregación en los compuestos químicos en función de los tipos de enlace. vs. Usar las propiedades y los estados de agregación en los compuestos químicos
Explicación de las propiedades y los estados de agregación en los compuestos químicos en función de los tipos de enlace. vs. Usar las propiedades y los estados de agregación en los compuestos químicos
