Curso: Introducción a la Investigación Clínica.
|
|
|
- Raúl Alarcón Zúñiga
- hace 5 años
- Vistas:
Transcripción
1 Curso: Introducción a la Investigación Clínica. 25/12/2012 Medimar Solutions, LLC 1 Este curso tiene dos Módulos. El primer módulo explica las leyes por las que se rige la Investigación Clínica. Estas leyes están contenidas en el Código de Regulaciones Federales de la FDA. El segundo módulo explica las Buenas Prácticas Clínicas y la Conferencia Internacional de Armonización. 25/12/2012 Medimar Solutions, LLC 2 1
2 Antes de comenzar el curso baje a su computadora el Libro de texto (versión electrónica incluida en el precio del curso). que encuentra bajo handouts. Para preguntas y comentarios durante el curso comuníquese directamente con la profesora al correo electrónico: mgarcia@medimarsolutions.com 25/12/2012 Medimar Solutions, LLC 3 Primer módulo: Código de Regulaciones Federales de la FDA que aplican a la Investigación de nuevos medicamentos. 25/12/2012 Medimar Solutions, LLC 4 2
3 Al concluir este módulo los alumnos serán capaces de: Describir qué es la Investigación Clínica. Identificar los pasos en el proceso de investigación de nuevos productos medicinales. Conocer cuáles son las entidades que toman parte en el proceso de Investigación Clínica. Identificar las funciones y responsabilidades de la FDA. Conocer los Productos bajo la jurisdicción de la FDA. Identificar los datos históricos más relevantes que condujeron a la regulación del proceso de Investigación. Identificar los capítulos del Título 21 Código de Regulaciones Federales que rigen la investigación de nuevos productos medicinales. Describir los estados de desarrollo de una droga. Identificar las fases de la Investigación Clínica. Conocer qué es un IND y en cuáles circunstancias esta debe ser presentada a la FDA. Describir los elementos claves componen una IND. Describir qué es un NDA y sus tipos. Al concluir este curso los alumnos serán capaces de: Conocer qué son los IRB. Identificar las responsabilidades de los IRB. Conocer los tipos de IRB. Identificar funciones y operaciones de los IRB. Conocer los requisitos de membrecía de los IRB. Conocer los criterios de aprobación y re-aprobación de estudios Conocer cuales son los Documentos que deben ser revisados por el IRB antes del inicio y durante la conducción de un estudio en un sitio de Investigación. Conocer el propósito del Consentimiento informado. Conocer los requisitos generales del consentimiento Informado. Identificar los elementos básicos y adicionales del consentimiento Informado. Conocer qué es la forma de declaración financiera y quienes están obligados a completarla. Conocer las obligaciones del sponsor y los investigadores en relación a la declaración financiera. 3
4 Al concluir este curso los alumnos serán capaces de: Conocer las responsabilidades del sponsor en relación al producto bajo investigación. Identificar Efectos adversos y Efectos Adversos Serios Conocer las responsabilidades del Investigador en relación a la identificación y reporte de Efectos adversos y Efectos Adversos Serios. Conocer las responsabilidades del sponsor en relación a la identificación y reporte de Efectos adversos y Efectos Adversos Serios. Conocer los requisitos que deben cumplir los documentos y las firmas electrónicas para que estos sean considerados equivalentes a los documentos en papel y a las firmas por escrito. Al concluir cada segmento de este módulo, el alumno debe tomar un examen. Cada examen puede ser tomado dos veces. Para obtener el certificado al final del curso, el alumno debe obtener al menos un resultado de 70%. 4
5 Segundo módulo: Buenas Prácticas Clínicas y Conferencia Internacional de Armonización. 25/12/2012 Medimar Solutions, LLC 1 Al concluir este módulo los alumnos serán capaces de: Conocer qué son las Buenas Prácticas Clínicas (GCP). Conocer los eventos históricos que tuvieron como consecuencia la creación de documentos éticos. Identificar las estipulaciones del Código de Núremberg. Conocer la Declaración de Helsinki y sus objetivos. Identificar los principios básicos del Reporte de Belmont. Conocer las responsabilidades de los Investigadores en relación a las GCP. Conocer las responsabilidades del sponsor en relación a las GCP. Conocer qué es La Conferencia Internacional de Armonización (International Conference of Harmonization, ICH por sus siglas en inglés). Conocer cómo está formado el Comité Directivo de la ICH. Conocer cuáles son las funciones de la Secretaría de la ICH. 1
6 Al concluir este curso los alumnos serán capaces de: Identificar los pasos y actividades en el proceso de Armonización. Identificar los tópicos seleccionados para la Armonización. Conocer las diferencias entre las normativas de la ICH y las regulaciones de la FDA. Conocer los objetivos de las normativas E2 y E6 de la ICH. Conocer las secciones de la Normativa E6 de la ICH. Conocer los tópicos de la Normativa E2 que han sido seleccionados para la armonización Al concluir este módulo, el alumno debe tomar un examen. El examen puede ser tomado dos veces. Para obtener el certificado al final del curso, el alumno debe obtener al menos un resultado de 70%. 2
Curso: Manejo del Sitio de Investigación Clínica.
 Curso: Manejo del Sitio de Investigación Clínica. 25/12/2012 Medimar Solutions, LLC 1 Este curso tiene dos Módulos. El primer módulo explica las actividades que deben realizarse antes del inicio de un
Curso: Manejo del Sitio de Investigación Clínica. 25/12/2012 Medimar Solutions, LLC 1 Este curso tiene dos Módulos. El primer módulo explica las actividades que deben realizarse antes del inicio de un
CONTENIDO SECCIÓN I DEFINICIÓN Y ALCANCES DE LA INVESTIGACIÓN CLÍNICA
 CONTENIDO SECCIÓN I DEFINICIÓN Y ALCANCES DE LA INVESTIGACIÓN CLÍNICA Capítulo 1... 25 La Ciencia Y El Método Científico... 25 Introducción... 25 Conocimiento Científico Y Sentido Común... 26 Clasificación
CONTENIDO SECCIÓN I DEFINICIÓN Y ALCANCES DE LA INVESTIGACIÓN CLÍNICA Capítulo 1... 25 La Ciencia Y El Método Científico... 25 Introducción... 25 Conocimiento Científico Y Sentido Común... 26 Clasificación
Título: Informe para Certificación de Comités de Ética Acreditados. Nombre del Comité de Ética de la investigación
 del Reporte Nombre del Comité de Ética de la investigación Aspecto Revisado Documentación General Revisado SI NO NA Comentarios/Hallazgos/ Recomendaciones/Observa ciones/ Requerimientos (Hacer referencia
del Reporte Nombre del Comité de Ética de la investigación Aspecto Revisado Documentación General Revisado SI NO NA Comentarios/Hallazgos/ Recomendaciones/Observa ciones/ Requerimientos (Hacer referencia
Certificación en Buenas Prácticas Clínicas Resolución 2378 del Capítulo Regulatorio de CROs - AVANZAR Octubre 12 de 2016
 Certificación en Buenas Prácticas Clínicas Resolución 2378 del 2008 Capítulo Regulatorio de CROs - AVANZAR Octubre 12 de 2016 Objetivo Abrir un espacio de diálogo entre el capítulo de Regulatorio de CROs
Certificación en Buenas Prácticas Clínicas Resolución 2378 del 2008 Capítulo Regulatorio de CROs - AVANZAR Octubre 12 de 2016 Objetivo Abrir un espacio de diálogo entre el capítulo de Regulatorio de CROs
FACULTAD DE CIENCIAS BIOMÉDICAS - UNIVERSIDAD AUSTRAL. Programas de Posgrados Curso de Buenas Prácticas en Investigación Clínica
 FACULTAD DE CIENCIAS BIOMÉDICAS - UNIVERSIDAD AUSTRAL Programas de Posgrados Curso de Buenas Prácticas en Investigación Clínica INSCRIPCION ABIERTA InicioMartes 10 de agosto de 2010 Directores: Dr. Celso
FACULTAD DE CIENCIAS BIOMÉDICAS - UNIVERSIDAD AUSTRAL Programas de Posgrados Curso de Buenas Prácticas en Investigación Clínica INSCRIPCION ABIERTA InicioMartes 10 de agosto de 2010 Directores: Dr. Celso
Comités de Ética en Investigación (CEIs)
 Comités de Ética en Investigación (CEIs) 1. CONCEPTO 2.ORIGEN 3.PRINCIPIOS 4.FUNCIONES 5. FORMACIÓN 6.NORMATIVAS 7. CEI-IICS Uno de los principios fundamentales de toda investigación científica que involucra
Comités de Ética en Investigación (CEIs) 1. CONCEPTO 2.ORIGEN 3.PRINCIPIOS 4.FUNCIONES 5. FORMACIÓN 6.NORMATIVAS 7. CEI-IICS Uno de los principios fundamentales de toda investigación científica que involucra
Monitoreo de Estudios Clínicos. Guillermo Casteller
 Monitoreo de Estudios Clínicos Guillermo Casteller Objetivos Enumerar las actividades principales que deben realizarse durante las visitas de monitoreo: preparación, conducción, post monitoreo y seguimiento
Monitoreo de Estudios Clínicos Guillermo Casteller Objetivos Enumerar las actividades principales que deben realizarse durante las visitas de monitoreo: preparación, conducción, post monitoreo y seguimiento
AVAL DEL CONIS DE CURSO DE BUENAS PRÁCTICAS DE INVESTIGACIÓN (INVESTIGACIÓN OBSERVACIONAL Y EPIDEMIOLÓGICA)
 AVAL DEL CONIS DE CURSO DE BUENAS PRÁCTICAS DE INVESTIGACIÓN (INVESTIGACIÓN OBSERVACIONAL Y EPIDEMIOLÓGICA) 1. PROPÓSITO Y ALCANCE Disponer de un procedimiento para que el CONIS brinde el aval a los cursos
AVAL DEL CONIS DE CURSO DE BUENAS PRÁCTICAS DE INVESTIGACIÓN (INVESTIGACIÓN OBSERVACIONAL Y EPIDEMIOLÓGICA) 1. PROPÓSITO Y ALCANCE Disponer de un procedimiento para que el CONIS brinde el aval a los cursos
HOSPITAL JUÁREZ DE MÉXICO ORGANISMO DESCENTRALIZADO POLÍTICAS DE SEGURIDAD DEL PACIENTE QUE PARTICIPA EN PROTOCOLOS DE INVESTIGACIÓN CIENTÍFICA
 HOSPITAL JUÁREZ DE MÉXICO ORGANISMO DESCENTRALIZADO POLÍTICAS DE SEGURIDAD DEL PACIENTE QUE PARTICIPA EN PROTOCOLOS DE CIENTÍFICA Diciembre 2014 ÍNDICE HOJA Propósito 2 Definiciones 2 Marco Jurídico 2
HOSPITAL JUÁREZ DE MÉXICO ORGANISMO DESCENTRALIZADO POLÍTICAS DE SEGURIDAD DEL PACIENTE QUE PARTICIPA EN PROTOCOLOS DE CIENTÍFICA Diciembre 2014 ÍNDICE HOJA Propósito 2 Definiciones 2 Marco Jurídico 2
Guías de BUENA PRÁCTICA CLINICA
 CURSO BUENAS PRACTICAS CLINICAS Guías de BUENA PRÁCTICA CLINICA Desirée Sáenz Campos, MD, MSc, PhD. Catedrática, Escuela de Medicina UCR. Area de Medicamentos y Terapéutica Clínica, CCSS. Etica en Investigación:
CURSO BUENAS PRACTICAS CLINICAS Guías de BUENA PRÁCTICA CLINICA Desirée Sáenz Campos, MD, MSc, PhD. Catedrática, Escuela de Medicina UCR. Area de Medicamentos y Terapéutica Clínica, CCSS. Etica en Investigación:
Sección Ensayos Clínicos Agencia Nacional de Medicamentos Instituto de Salud Pública de Chile
 Regulación de Ensayos Clínicos en Chile Sección Ensayos Clínicos Agencia Nacional de Medicamentos Instituto de Salud Pública de Chile 11/mayo/2012 Marco legal y normativa Constitución Política del Estado
Regulación de Ensayos Clínicos en Chile Sección Ensayos Clínicos Agencia Nacional de Medicamentos Instituto de Salud Pública de Chile 11/mayo/2012 Marco legal y normativa Constitución Política del Estado
Qué es un Ensayo Clínico?
 Qué es un Ensayo Clínico? E.U, MSc Macarena Manríquez Mimica Coordinadora Estudios Clínicos ISP, Novartis, MSD Profesora Instructor Universidad de los Andes Tópicos a tratar Definición de un Ensayo Clínico
Qué es un Ensayo Clínico? E.U, MSc Macarena Manríquez Mimica Coordinadora Estudios Clínicos ISP, Novartis, MSD Profesora Instructor Universidad de los Andes Tópicos a tratar Definición de un Ensayo Clínico
FORMULARIO PARA LA PRESENTACION DE PROYECTOS DE INVESTIGACION
 FORMULARIO PARA LA PRESENTACION DE PROYECTOS DE INVESTIGACION SR. PRESIDENTE DEL COMITÉ DE ÉTICA EN INVESTIGACIÓN MEDICO ESPECIALIZADO ALEXANDER FLEMING DEL INSTITUTO S / D Por la presente envío para revisión
FORMULARIO PARA LA PRESENTACION DE PROYECTOS DE INVESTIGACION SR. PRESIDENTE DEL COMITÉ DE ÉTICA EN INVESTIGACIÓN MEDICO ESPECIALIZADO ALEXANDER FLEMING DEL INSTITUTO S / D Por la presente envío para revisión
Principios de Buenas Prácticas Clínicas en Investigación - Regulaciones Internacionales
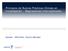 Principios de Buenas Prácticas Clínicas en Investigación - Regulaciones Internacionales Janssen / GCO-Chile/ Country Manager Buenas Prácticas Clínicas BPC (GCP) Estándar unificado para el diseño, la realización,
Principios de Buenas Prácticas Clínicas en Investigación - Regulaciones Internacionales Janssen / GCO-Chile/ Country Manager Buenas Prácticas Clínicas BPC (GCP) Estándar unificado para el diseño, la realización,
Curso especialista en gestión administrativa de ensayos clinicos (Clinical Trial Assistant-CTA)
 i Curso especialista en gestión administrativa de ensayos clinicos (Clinical Trial Assistant-CTA) CURSO - 2013 1 CURSO ESPECIALISTA EN GESTIÓN ADMINISTRATIVA DE EN- SAYOS CLÍNICOS (CTA) PRESENTACIÓN Si
i Curso especialista en gestión administrativa de ensayos clinicos (Clinical Trial Assistant-CTA) CURSO - 2013 1 CURSO ESPECIALISTA EN GESTIÓN ADMINISTRATIVA DE EN- SAYOS CLÍNICOS (CTA) PRESENTACIÓN Si
Red de Comités de Ética en Investigación: Fortalezas de trabajar en Red
 I CURSO INTERNACIONAL CONCEPTOS BÁSICOS SOBRE INVESTIGACIÓN Y BIENESTAR DE ANIMALES Red de Comités de Ética en Investigación: Fortalezas de trabajar en Red Fredy A Canchihuamán, MD MPH PhD Coordinador
I CURSO INTERNACIONAL CONCEPTOS BÁSICOS SOBRE INVESTIGACIÓN Y BIENESTAR DE ANIMALES Red de Comités de Ética en Investigación: Fortalezas de trabajar en Red Fredy A Canchihuamán, MD MPH PhD Coordinador
Comité de Ética de Protocolos de Investigación
 INFORMES DEL INVESTIGADOR Sr. Investigador: Para cumplir con los requisitos que exige la ANMAT, se deberán remitir al CEPI, cuando corresponda, los informes que se detallan a continuación: Hoja de firmas
INFORMES DEL INVESTIGADOR Sr. Investigador: Para cumplir con los requisitos que exige la ANMAT, se deberán remitir al CEPI, cuando corresponda, los informes que se detallan a continuación: Hoja de firmas
Perspectiva general. FHI, Currículo de capacitación sobre ética de la investigación. Diapositiva 1
 Perspectiva general Principios de la ética de la investigación Fundamentos de la ética de la investigación Realización responsable de la investigación Supervisión de la investigación Problemas especiales
Perspectiva general Principios de la ética de la investigación Fundamentos de la ética de la investigación Realización responsable de la investigación Supervisión de la investigación Problemas especiales
Introducción a la Ética de la Investigación. Rodrigo A. Salinas Departamento de Ciencias Neurológicas Universidad de Chile
 Introducción a la Ética de la Investigación Rodrigo A. Salinas Departamento de Ciencias Neurológicas Universidad de Chile Código de Nüremberg 1. El consentimiento voluntario del sujeto humano es absolutamente
Introducción a la Ética de la Investigación Rodrigo A. Salinas Departamento de Ciencias Neurológicas Universidad de Chile Código de Nüremberg 1. El consentimiento voluntario del sujeto humano es absolutamente
RESPONSABILIDADES DEL INVESTIGADOR SEGÚN GCP-ICH
 RESPONSABILIDADES DEL INVESTIGADOR SEGÚN GCP-ICH Lic. Eugenia Farré Phoenix Cuyo - 7 y 8nov13 Calificaciones y acuerdos del investigador Formación académica CV Matrícula Profesional Experiencia comprobable
RESPONSABILIDADES DEL INVESTIGADOR SEGÚN GCP-ICH Lic. Eugenia Farré Phoenix Cuyo - 7 y 8nov13 Calificaciones y acuerdos del investigador Formación académica CV Matrícula Profesional Experiencia comprobable
Documentos básicos sobre la ética en la experimentación humana
 REQUERIMIENTOS ÉTICOS Y LEGALES EN LA INVESTIGACIÓN CON MEDICAMENTOS. LOS COMITÉS ÉTICOS DE INVESTIGACIÓN CLÍNICA Rosa Morros Pedrós Dept. Farmacologia, Toxicologia i Terapèutica Universitat Autònoma de
REQUERIMIENTOS ÉTICOS Y LEGALES EN LA INVESTIGACIÓN CON MEDICAMENTOS. LOS COMITÉS ÉTICOS DE INVESTIGACIÓN CLÍNICA Rosa Morros Pedrós Dept. Farmacologia, Toxicologia i Terapèutica Universitat Autònoma de
Curso especialista en Coordinación de Investigación Clinica en ensayos clinicos (CIC - Study Coordinator)
 Curso especialista en Coordinación de Investigación Clinica en ensayos clinicos (CIC - Study Coordinator) CURSO 2016 CURSO ESPECIALISTA EN COORDINACIÓN DE INVESTIGACIÓN CLÍNICA EN ENSAYOS CLÍNICOS (CIC-STUDY
Curso especialista en Coordinación de Investigación Clinica en ensayos clinicos (CIC - Study Coordinator) CURSO 2016 CURSO ESPECIALISTA EN COORDINACIÓN DE INVESTIGACIÓN CLÍNICA EN ENSAYOS CLÍNICOS (CIC-STUDY
Tema: PROCEDIMIENTOS POSTERIORES A LA EVALUACIÓN No. de POE : 5.4 Fecha de Escritura: Sept-Oct 2015 Aprobado por: CECIC
 Comité de Ética de CER Investigaciones Clínicas Vicente López 1441 Quilmes, Buenos Aires Tel. 011 3530-8535 Tema: PROCEDIMIENTOS POSTERIORES A LA EVALUACIÓN No. de POE : 5.4 Fecha de Escritura: Sept-Oct
Comité de Ética de CER Investigaciones Clínicas Vicente López 1441 Quilmes, Buenos Aires Tel. 011 3530-8535 Tema: PROCEDIMIENTOS POSTERIORES A LA EVALUACIÓN No. de POE : 5.4 Fecha de Escritura: Sept-Oct
BUENAS PRACTICAS CLINICAS (BPC) Y NORMAS ICH (CONFERENCIA INTERNACIONAL DE ARMONIZACION) JESÚS FRÍAS INIESTA
 CAPÍTULO 17 BUENAS PRACTICAS CLINICAS (BPC) Y NORMAS ICH (CONFERENCIA INTERNACIONAL DE ARMONIZACION) JESÚS FRÍAS INIESTA Servicio de Farmacología Clínica Hospital Universitario La Paz Departamento de Farmacología
CAPÍTULO 17 BUENAS PRACTICAS CLINICAS (BPC) Y NORMAS ICH (CONFERENCIA INTERNACIONAL DE ARMONIZACION) JESÚS FRÍAS INIESTA Servicio de Farmacología Clínica Hospital Universitario La Paz Departamento de Farmacología
Preparación de una Auditoría en los Ensayos Clínicos. D. Manuel Román Martínez Servicio de Farmacología Clínica Hospital Universitario de la Princesa
 Preparación de una Auditoría en los Ensayos Clínicos. D. Manuel Román Martínez Servicio de Farmacología Clínica Hospital Universitario de la Princesa Índice Introducción Procedimiento de la Auditoría.
Preparación de una Auditoría en los Ensayos Clínicos. D. Manuel Román Martínez Servicio de Farmacología Clínica Hospital Universitario de la Princesa Índice Introducción Procedimiento de la Auditoría.
Aspectos ETICOS Regulaciones y marco legal internacional
 Aspectos ETICOS Regulaciones y marco legal internacional Desirée Sáenz Campos MD, MSc, PhD. Catedrática, Escuela de Medicina UCR. Area de Medicamentos y Terapéutica Clínica, CCSS. Ética en la investigación
Aspectos ETICOS Regulaciones y marco legal internacional Desirée Sáenz Campos MD, MSc, PhD. Catedrática, Escuela de Medicina UCR. Area de Medicamentos y Terapéutica Clínica, CCSS. Ética en la investigación
Requisitos de Presentación de Protocolos de Investigación al Comité de Bioética de la Investigación del ICGES
 Requisitos de Presentación de Protocolos de Investigación al Comité de Bioética de la Investigación del ICGES Aspectos Generales: Todos los documentos que se presentan para evaluación al CBI-ICGES deben
Requisitos de Presentación de Protocolos de Investigación al Comité de Bioética de la Investigación del ICGES Aspectos Generales: Todos los documentos que se presentan para evaluación al CBI-ICGES deben
Actualización Sobre la Regla Común de los EEUU de América
 Actualización Sobre la Regla Común de los EEUU de América II Curso Internacional Sobre Aspectos Éticos para la Investigación en Salud para los Comités de Ética en Investigación de EsSalud Sergio G. Litewka
Actualización Sobre la Regla Común de los EEUU de América II Curso Internacional Sobre Aspectos Éticos para la Investigación en Salud para los Comités de Ética en Investigación de EsSalud Sergio G. Litewka
Investigación con Seres Humanos (HRP Estándares, intenciones y elementos medibles
 Investigación con Seres Humanos (HRP Estándares, intenciones y elementos medibles Estándar HRP.1 POLITICA 104/14 Los lideres del hospital son responsables de la protección de los seres humanos que participan
Investigación con Seres Humanos (HRP Estándares, intenciones y elementos medibles Estándar HRP.1 POLITICA 104/14 Los lideres del hospital son responsables de la protección de los seres humanos que participan
REGULACIÓN INTERNACIONAL DE ÉTICA EN INVESTIGACIÓN
 REGULACIÓN INTERNACIONAL DE ÉTICA EN INVESTIGACIÓN Med. Patricia Socualaya Sotomayor OBJETIVO Revisar los siguientes documentos: Código de Núremberg Reporte Belmont Declaración de Helsinki Código de Regulaciones
REGULACIÓN INTERNACIONAL DE ÉTICA EN INVESTIGACIÓN Med. Patricia Socualaya Sotomayor OBJETIVO Revisar los siguientes documentos: Código de Núremberg Reporte Belmont Declaración de Helsinki Código de Regulaciones
COMISIÓN FEDERAL PARA LA PROTECCIÓN CONTRA RIESGOS SANITARIOS COMISIÓN DE AUTORIZACIÓN SANITARIA LA REGULACIÓN DE LOS ENSAYOS CLÍNICOS EN MÉXICO
 COMISIÓN FEDERAL PARA LA PROTECCIÓN CONTRA RIESGOS SANITARIOS COMISIÓN DE AUTORIZACIÓN SANITARIA LA REGULACIÓN DE LOS ENSAYOS CLÍNICOS EN MÉXICO DRA. ELIZABETH ROJAS SERAFIN ENSAYOS CLÍNICOS 1 CONTENIDO
COMISIÓN FEDERAL PARA LA PROTECCIÓN CONTRA RIESGOS SANITARIOS COMISIÓN DE AUTORIZACIÓN SANITARIA LA REGULACIÓN DE LOS ENSAYOS CLÍNICOS EN MÉXICO DRA. ELIZABETH ROJAS SERAFIN ENSAYOS CLÍNICOS 1 CONTENIDO
PROCEDIMIENTO OPERATIVO DE ACCESO AL COMITÉ ÉTICO CIENTÍFICO. Servicio de Salud Talcahuano
 PROCEDIMIENTO OPERATIVO DE ACCESO AL COMITÉ ÉTICO CIENTÍFICO Servicio de Salud Talcahuano INDICE I- MARCO LEGAL II- DOCUMENTACIÓN REQUERIDA PARA PRESENTAR AL COMITÉ ÉTICO CIENTÍFICO III- REVISIÓN Y RESPUESTAS
PROCEDIMIENTO OPERATIVO DE ACCESO AL COMITÉ ÉTICO CIENTÍFICO Servicio de Salud Talcahuano INDICE I- MARCO LEGAL II- DOCUMENTACIÓN REQUERIDA PARA PRESENTAR AL COMITÉ ÉTICO CIENTÍFICO III- REVISIÓN Y RESPUESTAS
Ministerio de Salud Presidencia de la Nación
 COMISION DE INVESTIGACIONES BIOMÉDICAS EN SERES HUMANOS CONSEJO FEDERAL DE SALUD 16 de noviembre de 2007 Ministerio de Salud Presidencia de la Nación 1. GUÍA A DE BUENAS PRÁCTICAS CLÍNICAS DE INVESTIGACIÓN
COMISION DE INVESTIGACIONES BIOMÉDICAS EN SERES HUMANOS CONSEJO FEDERAL DE SALUD 16 de noviembre de 2007 Ministerio de Salud Presidencia de la Nación 1. GUÍA A DE BUENAS PRÁCTICAS CLÍNICAS DE INVESTIGACIÓN
Prof. Dra. Ingrid Strusberg Reumatóloga Directora Instituto Médico Strusberg Prof. Adjunta Cátedra de Semiología. UHMI Nº 2. FCM.
 Prof. Dra. Ingrid Strusberg Reumatóloga Directora Instituto Médico Strusberg Prof. Adjunta Cátedra de Semiología. UHMI Nº 2. FCM. UNC Doctora en Medicina y Cirugía Magister en Investigación Clínica Farmacológica
Prof. Dra. Ingrid Strusberg Reumatóloga Directora Instituto Médico Strusberg Prof. Adjunta Cátedra de Semiología. UHMI Nº 2. FCM. UNC Doctora en Medicina y Cirugía Magister en Investigación Clínica Farmacológica
HONDURAS. Legislación local de Investigación. Honduras no tiene regulación específica para el tema de investigaciones clínicas.
 HONDURAS Legislación local de Investigación Honduras no tiene regulación específica para el tema de investigaciones clínicas. En el aspecto legislativo, cuenta con: 1. La Secretaria de salud. 2. El Código
HONDURAS Legislación local de Investigación Honduras no tiene regulación específica para el tema de investigaciones clínicas. En el aspecto legislativo, cuenta con: 1. La Secretaria de salud. 2. El Código
Manual Operativo del Comité Ético Científico de la Universidad de Iberoamérica CEC-UNIBE. Universidad de Iberoamérica
 Manual Operativo del Comité Ético Científico de la Universidad de Iberoamérica CEC-UNIBE Universidad de Iberoamérica 2016 1. Introducción Los países en desarrollo, y en especial aquellos donde la medicina
Manual Operativo del Comité Ético Científico de la Universidad de Iberoamérica CEC-UNIBE Universidad de Iberoamérica 2016 1. Introducción Los países en desarrollo, y en especial aquellos donde la medicina
Buenas Prácticas Clínicas
 VI Conferencia Panamericana para la Armonización n de la Reglamentación n Farmacéutica (CPARF) Grupo de Trabajo Buenas Prácticas Clínicas Resultados y perspectivas Fortalecimiento de las Autoridades Reguladoras
VI Conferencia Panamericana para la Armonización n de la Reglamentación n Farmacéutica (CPARF) Grupo de Trabajo Buenas Prácticas Clínicas Resultados y perspectivas Fortalecimiento de las Autoridades Reguladoras
De la Bioética a la Ética Clínica
 De la Bioética a la Ética Clínica Hospital de Sagunto. Mayo 2013 1.- Bioética e investigación. n. Aspectos básicos b 2.- Aspectos éticos aplicables a la investigación n clínica 3.- Comités s de ética e
De la Bioética a la Ética Clínica Hospital de Sagunto. Mayo 2013 1.- Bioética e investigación. n. Aspectos básicos b 2.- Aspectos éticos aplicables a la investigación n clínica 3.- Comités s de ética e
CURSO TEORICO- PRÁCTICO DE ETICA EN INVESTIGACIÓN CLINICA. FUNDACIÓN CIDEA
 CURSO TEORICO- PRÁCTICO DE ETICA EN INVESTIGACIÓN CLINICA. FUNDACIÓN CIDEA Coordinación Académica: -MAGLIO, Ignacio. -BELLO, María Alejandra Cuerpo docente: Expertos -BOLAÑOS, Carlos -SAIDON, Patricia
CURSO TEORICO- PRÁCTICO DE ETICA EN INVESTIGACIÓN CLINICA. FUNDACIÓN CIDEA Coordinación Académica: -MAGLIO, Ignacio. -BELLO, María Alejandra Cuerpo docente: Expertos -BOLAÑOS, Carlos -SAIDON, Patricia
Norma/Política Protección de participantes en investigación
 01.01 de / Modificación: 01/01 : Responsables de la Gestión de la norma/política: Dra Karin KOPITOWSKI karin.kopitowski@hospitalitaliano.org.ar Dr. Adrian GADANO adrian.gadano@hospitalitaliano.org.ar Capítulo
01.01 de / Modificación: 01/01 : Responsables de la Gestión de la norma/política: Dra Karin KOPITOWSKI karin.kopitowski@hospitalitaliano.org.ar Dr. Adrian GADANO adrian.gadano@hospitalitaliano.org.ar Capítulo
HACIA UNA RED NACIONAL DE BIOETICA EN EL PERU
 HACIA UNA RED NACIONAL DE BIOETICA EN EL PERU Méd. Gabriela Minaya M. Directora General Oficina General de Investigación y Transferencia Tecnológica Ética en Investigación Por qué existe la Ética en Investigación?
HACIA UNA RED NACIONAL DE BIOETICA EN EL PERU Méd. Gabriela Minaya M. Directora General Oficina General de Investigación y Transferencia Tecnológica Ética en Investigación Por qué existe la Ética en Investigación?
Características de los EECC en proyectos europeos y aspectos prácticos a tener en cuenta
 Características de los EECC en proyectos europeos y aspectos prácticos a tener en cuenta Silvia Jiménez Jorge Investigadora- Gestora de proyecto UICEC H. Universitario Virgen del Rocío www.jornadasaludinvestiga.es
Características de los EECC en proyectos europeos y aspectos prácticos a tener en cuenta Silvia Jiménez Jorge Investigadora- Gestora de proyecto UICEC H. Universitario Virgen del Rocío www.jornadasaludinvestiga.es
Instituto Cardiovascular de Buenos Aires MANUAL DE NORMAS Y PROCEDIMIENTOS
 HOJA: 1 de 6 1. OBJETIVO Este procedimiento describe los métodos que utilizará este Comité de Ética (CEI-ICBA) para organizar la tarea de recepción y distribución de documentación previa a las reuniones
HOJA: 1 de 6 1. OBJETIVO Este procedimiento describe los métodos que utilizará este Comité de Ética (CEI-ICBA) para organizar la tarea de recepción y distribución de documentación previa a las reuniones
Curso: BPC Excelencia en la gestión de la Investigación Clínica
 Curso: BPC Excelencia en la gestión de la Investigación Clínica Fecha: Miércoles del 02 de mayo al 27 de junio de 2018. Horario: de 12:00 a 14:00hs. Lugar: Bvar. Artigas 1565 (ex 1555) Sindicato Médico
Curso: BPC Excelencia en la gestión de la Investigación Clínica Fecha: Miércoles del 02 de mayo al 27 de junio de 2018. Horario: de 12:00 a 14:00hs. Lugar: Bvar. Artigas 1565 (ex 1555) Sindicato Médico
IV DIPLOMADO EN INVESTIGACIÓN CLÍNICA y MONITOREO DE ENSAYOS CLÍNICOS 2009
 IV DIPLOMADO EN INVESTIGACIÓN CLÍNICA y MONITOREO DE ENSAYOS CLÍNICOS 2009 1. INFORMACION GENERAL 1.1. DIPLOMA: Diplomado en Investigación Clínica 1.2. TITULO: Monitor de Ensayos Clínicos 1.3. REQUISITOS:
IV DIPLOMADO EN INVESTIGACIÓN CLÍNICA y MONITOREO DE ENSAYOS CLÍNICOS 2009 1. INFORMACION GENERAL 1.1. DIPLOMA: Diplomado en Investigación Clínica 1.2. TITULO: Monitor de Ensayos Clínicos 1.3. REQUISITOS:
Family Health International
 Perspectiva general Principios de la ética de la Fundamentos de la ética de la Realización responsable de la Supervisión de la Problemas especiales en Diapositiva 1 Principios de ética de la Objetivos
Perspectiva general Principios de la ética de la Fundamentos de la ética de la Realización responsable de la Supervisión de la Problemas especiales en Diapositiva 1 Principios de ética de la Objetivos
Diciembre 2015 Versión 1.0 Hoja: A. En idioma español;
 LA DOCUMENTACIÓN DEBERÁ PRESENTARSE, DE ACUERDO A LO SIGUIENTE: A. En idioma español; Toda la documentación deberá presentarse únicamente en idioma español. Los documentos que acompañen a las solicitudes
LA DOCUMENTACIÓN DEBERÁ PRESENTARSE, DE ACUERDO A LO SIGUIENTE: A. En idioma español; Toda la documentación deberá presentarse únicamente en idioma español. Los documentos que acompañen a las solicitudes
SALA CIENCIAS DE LA SALUD
 PROCEDIMIENTO PARA EL SOMETIMIENTO DE PROYECTOS DE INVESTIGACIÓN A EVALUACIÓN POR EL COMITÉ DE ÉTICA EN INVESTIGACIÓN SALA CIENCIAS DE LA SALUD El proceso mediante el cual se somete un trabajo de investigación
PROCEDIMIENTO PARA EL SOMETIMIENTO DE PROYECTOS DE INVESTIGACIÓN A EVALUACIÓN POR EL COMITÉ DE ÉTICA EN INVESTIGACIÓN SALA CIENCIAS DE LA SALUD El proceso mediante el cual se somete un trabajo de investigación
COMITÉS DE ÉTICA EN INVESTIGACIÓN (CEI)
 COMITÉS DE ÉTICA EN INVESTIGACIÓN (CEI) Objetivo: Enfatizar el papel de los CEI como clave en la gestión de la calidad de la investigación, además de compartir a los asistentes los programas que imparte
COMITÉS DE ÉTICA EN INVESTIGACIÓN (CEI) Objetivo: Enfatizar el papel de los CEI como clave en la gestión de la calidad de la investigación, además de compartir a los asistentes los programas que imparte
Numero Fecha Autor Aprobado por I.Hernandez, V.Gómez, J. Garza
 I. PROPÓSITO I.1.Describir los procesos mediante el investigador mantiene informados de los eventos adversos inesperados, serios, no serios así como de otros resultados inesperados que podrían afectar
I. PROPÓSITO I.1.Describir los procesos mediante el investigador mantiene informados de los eventos adversos inesperados, serios, no serios así como de otros resultados inesperados que podrían afectar
Red Nacional de Investigaciones Clínicas para el Tratamiento de las Drogas
 Red Nacional de Investigaciones Clínicas para el Tratamiento de las Drogas Institutos Nacionales de Salud Departamento de Salud y Servicios Humanos de los Estados Unidos INTRODUCCIÓN La Red de Investigaciones
Red Nacional de Investigaciones Clínicas para el Tratamiento de las Drogas Institutos Nacionales de Salud Departamento de Salud y Servicios Humanos de los Estados Unidos INTRODUCCIÓN La Red de Investigaciones
SELECCION UNICA. Seleccione la opción correcta con relación al enunciado * LA OPCION CORRECTA SE HA SEÑALADO CON LETRA COLOR ROJO
 SEMINARIO INTERNACIONAL SOBRE INVESTIGACIÓN CON SERES HUMANOS Y DERECHOS FUNDAMENTALES CLAVE DE RESPUESTA PRUEBA ESCRITA PARA OBTENCIÓN DEL CERTIFICADO EN BUENAS PRÁCTICAS CLÍNICAS SELECCION UNICA. Seleccione
SEMINARIO INTERNACIONAL SOBRE INVESTIGACIÓN CON SERES HUMANOS Y DERECHOS FUNDAMENTALES CLAVE DE RESPUESTA PRUEBA ESCRITA PARA OBTENCIÓN DEL CERTIFICADO EN BUENAS PRÁCTICAS CLÍNICAS SELECCION UNICA. Seleccione
OBJETIVOS A QUIÉN VA DIRIGIDO
 INTRODUCCIÓN La normativa de Buena Práctica Clínica (BPC) es un estándar internacional de calidad científica y ética dirigida al diseño, realización, registro y redacción de informes de ensayos que implican
INTRODUCCIÓN La normativa de Buena Práctica Clínica (BPC) es un estándar internacional de calidad científica y ética dirigida al diseño, realización, registro y redacción de informes de ensayos que implican
ESTADO ACTUAL Y PERSPECTIVA
 ESTADO ACTUAL Y PERSPECTIVA DEL REGISTRO PARA LOS COMITÉS DE ÉTICA EN INVESTIGACIÓN M en C. Areli Cerón Sánchez Dirección Operativa Comisión Nacional de Bioética CDMX_CMN EVOLUCIÓN DEL CEI Adición de Art.
ESTADO ACTUAL Y PERSPECTIVA DEL REGISTRO PARA LOS COMITÉS DE ÉTICA EN INVESTIGACIÓN M en C. Areli Cerón Sánchez Dirección Operativa Comisión Nacional de Bioética CDMX_CMN EVOLUCIÓN DEL CEI Adición de Art.
Norma/Política Requisitos para los patrocinantes de investigación en humanos
 01.01 Norma/Política 146/14 de / Modificación: 01/01 : Capítulo JCI 5a edición: HRP 3 Responsables de la Gestión de la política: Dra. Karin KOPITOWSKI karin.kopitowski@hispitalitaliano.org.ar Dr. Adrian
01.01 Norma/Política 146/14 de / Modificación: 01/01 : Capítulo JCI 5a edición: HRP 3 Responsables de la Gestión de la política: Dra. Karin KOPITOWSKI karin.kopitowski@hispitalitaliano.org.ar Dr. Adrian
Lista de Procedimientos de Operación Estándar
 Lista de Procedimientos de Operación Estándar Número Procedimiento 1. Autoridad bajo la cual el Comité de la Clínica del Bajío CLINBA, S.C., está establecido y autorizado. 2. Acerca del Comité de la Clínica
Lista de Procedimientos de Operación Estándar Número Procedimiento 1. Autoridad bajo la cual el Comité de la Clínica del Bajío CLINBA, S.C., está establecido y autorizado. 2. Acerca del Comité de la Clínica
Comité de Bioética Universidad Tecnológica de Pereira (CBE-UTP)
 Comité de Bioética Universidad Tecnológica de Pereira (CBE-UTP) Qué es el CBE-UTP? Es una organización independiente, interdisciplinaria y pluralista, integrada por profesionales médicos, científicos y
Comité de Bioética Universidad Tecnológica de Pereira (CBE-UTP) Qué es el CBE-UTP? Es una organización independiente, interdisciplinaria y pluralista, integrada por profesionales médicos, científicos y
Ministerio de Salud Secretaría de Políticas, Regulación e Institutos A.N.M.A.T.
 BUENOS AIRES, 29 Feb 2008 VISTO la Disposición N 5330/97, la Disposición N 2124/05, el Expediente Nº 1-0047-0000-024488-07-9 del Registro de la Administración Nacional de Medicamentos, Alimentos y Tecnología
BUENOS AIRES, 29 Feb 2008 VISTO la Disposición N 5330/97, la Disposición N 2124/05, el Expediente Nº 1-0047-0000-024488-07-9 del Registro de la Administración Nacional de Medicamentos, Alimentos y Tecnología
I. Hernández, V. Gómez, J. Garza
 I. PROPÓSITO I.1.Describir el proceso mediante el cual todos los protocolos de investigación son evaluados de acuerdo a los lineamientos del Comité. I.2. El proceso inicia con el sometimiento de la papelería
I. PROPÓSITO I.1.Describir el proceso mediante el cual todos los protocolos de investigación son evaluados de acuerdo a los lineamientos del Comité. I.2. El proceso inicia con el sometimiento de la papelería
Manual para Usuarios Procesos y Procedimientos
 2012 ComitédeBioética,UniversidadSanFranciscodeQuito ElComitédeRevisiónInstitucionaldelaUSFQ TheInstitutionalReviewBoardoftheUSFQ ManualparaUsuarios ProcesosyProcedimientos Unaguíacompletaquerespondelaspreguntasmásfrecuentes:
2012 ComitédeBioética,UniversidadSanFranciscodeQuito ElComitédeRevisiónInstitucionaldelaUSFQ TheInstitutionalReviewBoardoftheUSFQ ManualparaUsuarios ProcesosyProcedimientos Unaguíacompletaquerespondelaspreguntasmásfrecuentes:
Autorización de investigaciones clínicas. con productos sanitarios FORMULARIO DE DATOS BÁSICOS DE LA SOLICITUD
 ANEXO B Autorización de investigaciones clínicas con productos sanitarios FORMULARIO DE DATOS BÁSICOS DE LA SOLICITUD I. DATOS DE IDENTIFICACIÓN DE LA INVESTIGACIÓN CLÍNICA I. Nº EXPTE. (no cumplimentar):
ANEXO B Autorización de investigaciones clínicas con productos sanitarios FORMULARIO DE DATOS BÁSICOS DE LA SOLICITUD I. DATOS DE IDENTIFICACIÓN DE LA INVESTIGACIÓN CLÍNICA I. Nº EXPTE. (no cumplimentar):
Reglamento General de Actividades de Investigación
 INSTITUTO NACIONAL DE SALUD DEL NIÑO OFICINA EJECUTIVA DE APOYO A LA INVESTIGACIÓN Y DOCENCIA ESPECIALIZADA Reglamento General de Actividades de Investigación Base Legal Ley N 26842 - Ley General de Salud
INSTITUTO NACIONAL DE SALUD DEL NIÑO OFICINA EJECUTIVA DE APOYO A LA INVESTIGACIÓN Y DOCENCIA ESPECIALIZADA Reglamento General de Actividades de Investigación Base Legal Ley N 26842 - Ley General de Salud
Que por Disposición A.N.M.A.T. Nº 5330/97 se aprobó el Régimen de Buenas Prácticas de Investigación en Estudios de Farmacología Clínica.
 Administración Nacional de Medicamentos, Alimentos y Tecnología Médica SALUD PUBLICA Disposición 1067/2008 Modificación de la Disposición Nº 5330/97 por la que se aprobara el Régimen de Buenas Prácticas
Administración Nacional de Medicamentos, Alimentos y Tecnología Médica SALUD PUBLICA Disposición 1067/2008 Modificación de la Disposición Nº 5330/97 por la que se aprobara el Régimen de Buenas Prácticas
REPÚBLICA DE PANAMÁ MINISTERIO DE SALUD. DECRETO EJECUTIVO No (De 27 de agosto de 2007 ) EL PRESIDENTE DE LA REPÚBLICA,
 1 REPÚBLICA DE PANAMÁ MINISTERIO DE SALUD DECRETO EJECUTIVO No. 340 (De 27 de agosto de 2007 ) "Por el cual se modifica el Capítulo V del Título II del Decreto Ejecutivo 178 de 12 de julio de 2001, Que
1 REPÚBLICA DE PANAMÁ MINISTERIO DE SALUD DECRETO EJECUTIVO No. 340 (De 27 de agosto de 2007 ) "Por el cual se modifica el Capítulo V del Título II del Decreto Ejecutivo 178 de 12 de julio de 2001, Que
Normas de buena práctica clínica (BPC)
 Normas de buena práctica clínica (BPC) 17.Sep - 31.Oct Cód. @19-18 Edición 2018 Tipo de actividad Cursos Online Fecha 17.Sep - 31.Oct Idiomas Español- castellano Validez académica 30 horas DIRECCIÓN Iciar
Normas de buena práctica clínica (BPC) 17.Sep - 31.Oct Cód. @19-18 Edición 2018 Tipo de actividad Cursos Online Fecha 17.Sep - 31.Oct Idiomas Español- castellano Validez académica 30 horas DIRECCIÓN Iciar
CURSO REGULACION SANITARIA DE PRODUCTOS BIOLOGICOS Y BIOTECNOLOGICOS
 CURSO REGULACION SANITARIA DE PRODUCTOS BIOLOGICOS Y BIOTECNOLOGICOS 1.- Introducción Programa General Fase Virtual de Autoaprendizaje y Fase Presencial Edición 2017 Los medicamentos biológicos y biotecnológicos
CURSO REGULACION SANITARIA DE PRODUCTOS BIOLOGICOS Y BIOTECNOLOGICOS 1.- Introducción Programa General Fase Virtual de Autoaprendizaje y Fase Presencial Edición 2017 Los medicamentos biológicos y biotecnológicos
Preguntas frecuentes sobre la participación en ensayos clínicos
 Preguntas frecuentes sobre la participación en ensayos clínicos Escoger participar en un ensayo clínico es una decisión personalmente importante. Las preguntas frecuentes siguientes proporcionan información
Preguntas frecuentes sobre la participación en ensayos clínicos Escoger participar en un ensayo clínico es una decisión personalmente importante. Las preguntas frecuentes siguientes proporcionan información
UNIDAD DE ÉTICA Y SEGURIDAD EN INVESTIGACIÓN
 UNIDAD DE ÉTICA Y SEGURIDAD EN INVESTIGACIÓN Andrea Leisewitz MSc Bioethics PhD Bio. Celular y Molecular MSc innovación Profesor Asistente Facultad de Medicina Ética y Seguridad en Investigación 2018 ALV;
UNIDAD DE ÉTICA Y SEGURIDAD EN INVESTIGACIÓN Andrea Leisewitz MSc Bioethics PhD Bio. Celular y Molecular MSc innovación Profesor Asistente Facultad de Medicina Ética y Seguridad en Investigación 2018 ALV;
RESPONSABILIDAD DE LOS INVESTIGADORES Y LOS COMITES DE ETICA EN LOS PAISES SUBDESARROLLADOS
 RESPONSABILIDAD DE LOS INVESTIGADORES Y LOS COMITES DE ETICA EN LOS PAISES SUBDESARROLLADOS SOLEDAD DIAZ Instituto Chileno de Medicina Reproductiva () Santiago, Chile, 2006 CUESTIONES ETICAS FUNDAMENTALES
RESPONSABILIDAD DE LOS INVESTIGADORES Y LOS COMITES DE ETICA EN LOS PAISES SUBDESARROLLADOS SOLEDAD DIAZ Instituto Chileno de Medicina Reproductiva () Santiago, Chile, 2006 CUESTIONES ETICAS FUNDAMENTALES
Norma/Política Información al paciente y familia sobre el acceso a investigación
 01.01 Información al paciente y familia sobre el acceso a investigación de / Modificación: 01/01 : Responsables de la Gestión de la norma/política: Dra Karin KOPITOWSKI karin.kopitowski@hospitalitaliano.org.ar
01.01 Información al paciente y familia sobre el acceso a investigación de / Modificación: 01/01 : Responsables de la Gestión de la norma/política: Dra Karin KOPITOWSKI karin.kopitowski@hospitalitaliano.org.ar
Curs de normes de Bona Pràctica Clínica per a Investigadors i col laboradors d assaigs clínics. Esther Cucurull Barcelona, 3 de maig de 2011
 Curs de normes de Bona Pràctica Clínica per a Investigadors i col laboradors d assaigs clínics Esther Cucurull Barcelona, 3 de maig de 2011 Normas de Buena Práctica Clínica Estándar internacional ético
Curs de normes de Bona Pràctica Clínica per a Investigadors i col laboradors d assaigs clínics Esther Cucurull Barcelona, 3 de maig de 2011 Normas de Buena Práctica Clínica Estándar internacional ético
LA INVESTIGACION CLINICA DE LA FAMILIA A A LA Z
 LA INVESTIGACION CLINICA DE LA FAMILIA A A LA Z Grupo de Promotores del Muhammad Ali Parkinson Center Phoenix, Arizona QUE ES LA INVESTIGACION CLINICA? La investigación clínica incluye Estudios Clínicos
LA INVESTIGACION CLINICA DE LA FAMILIA A A LA Z Grupo de Promotores del Muhammad Ali Parkinson Center Phoenix, Arizona QUE ES LA INVESTIGACION CLINICA? La investigación clínica incluye Estudios Clínicos
DIPLOMA DE POSTÍTULO EN INVESTIGACIÓN CLÍNICA XIV Y CERTIFICADO DE MONITOR DE ENSAYOS CLÍNICOS VERSIÓN
 XIV VERSIÓN DIPLOMA DE POSTÍTULO EN INVESTIGACIÓN CLÍNICA Y CERTIFICADO DE MONITOR DE ENSAYOS CLÍNICOS DIPLOMA DE POSTÍTULO EN INVESTIGACIÓN CLÍNICA Y CERTIFICADO DE MONITOR DE ENSAYOS CLÍNICOS, XIV VERSIÓN
XIV VERSIÓN DIPLOMA DE POSTÍTULO EN INVESTIGACIÓN CLÍNICA Y CERTIFICADO DE MONITOR DE ENSAYOS CLÍNICOS DIPLOMA DE POSTÍTULO EN INVESTIGACIÓN CLÍNICA Y CERTIFICADO DE MONITOR DE ENSAYOS CLÍNICOS, XIV VERSIÓN
C) Información del centro
 Hoja: 1 de 4 A) Información del trámite No. de ingreso Fecha ingreso Fecha atención Establecimiento (Razón Social del Solicitante o Promovente) XX3300912X000X día de mes de año día de mes de año (Indicará
Hoja: 1 de 4 A) Información del trámite No. de ingreso Fecha ingreso Fecha atención Establecimiento (Razón Social del Solicitante o Promovente) XX3300912X000X día de mes de año día de mes de año (Indicará
REQUISITOS PARA PRESENTACION DE PROTOCOLOS DE INVESTIGACION CON SUJETOS HUMANOS ANTE LA JUNTA DE REVISION INSTITUCIONAL
 REQUISITOS PARA PRESENTACION DE PROTOCOLOS DE INVESTIGACION CON SUJETOS HUMANOS ANTE LA JUNTA DE REVISION INSTITUCIONAL UNIVERSIDAD INTERAMERICANA DE PUERTO RICO JUNTA DE REVISIÓN INSTITUCIONAL OFICINA
REQUISITOS PARA PRESENTACION DE PROTOCOLOS DE INVESTIGACION CON SUJETOS HUMANOS ANTE LA JUNTA DE REVISION INSTITUCIONAL UNIVERSIDAD INTERAMERICANA DE PUERTO RICO JUNTA DE REVISIÓN INSTITUCIONAL OFICINA
Aspectos éticos de la investigación biomédica
 Aspectos éticos de la investigación biomédica Pedro Gorrotxategi Gorrotxategi Marzo 2012 1 Evolución histórica de la ética en la investigación (I) Investigación Dilemas morales Los propios médicos se responsabilizaban
Aspectos éticos de la investigación biomédica Pedro Gorrotxategi Gorrotxategi Marzo 2012 1 Evolución histórica de la ética en la investigación (I) Investigación Dilemas morales Los propios médicos se responsabilizaban
DIPLOMA DE POSTÍTULO EN INVESTIGACIÓN CLÍNICA XII Y CERTIFICADO DE MONITOR DE ENSAYOS CLÍNICOS VERSIÓN
 XII VERSIÓN DIPLOMA DE POSTÍTULO EN INVESTIGACIÓN CLÍNICA Y CERTIFICADO DE MONITOR DE ENSAYOS CLÍNICOS DIPLOMA DE POSTÍTULO EN INVESTIGACIÓN CLÍNICA Y CERTIFICADO DE MONITOR DE ENSAYOS CLÍNICOS, XII VERSIÓN
XII VERSIÓN DIPLOMA DE POSTÍTULO EN INVESTIGACIÓN CLÍNICA Y CERTIFICADO DE MONITOR DE ENSAYOS CLÍNICOS DIPLOMA DE POSTÍTULO EN INVESTIGACIÓN CLÍNICA Y CERTIFICADO DE MONITOR DE ENSAYOS CLÍNICOS, XII VERSIÓN
Impacto de las supervisiones en en el Derecho de las Personas en Investigación
 Impacto de las supervisiones en en el Derecho de las Personas en Investigación Foro Internacional de Ensayos Clínicos, Salud Pública y Derechos Humanos Fredy A. Canchihuamán, MD MPH PhD Presidente Comité
Impacto de las supervisiones en en el Derecho de las Personas en Investigación Foro Internacional de Ensayos Clínicos, Salud Pública y Derechos Humanos Fredy A. Canchihuamán, MD MPH PhD Presidente Comité
DIPLOMA DE POSTÍTULO EN INVESTIGACIÓN CLÍNICA XIII Y CERTIFICADO DE MONITOR DE ENSAYOS CLÍNICOS VERSIÓN
 XIII VERSIÓN DIPLOMA DE POSTÍTULO EN INVESTIGACIÓN CLÍNICA Y CERTIFICADO DE MONITOR DE ENSAYOS CLÍNICOS DIPLOMA DE POSTÍTULO EN INVESTIGACIÓN CLÍNICA Y CERTIFICADO DE MONITOR DE ENSAYOS CLÍNICOS, XII VERSIÓN
XIII VERSIÓN DIPLOMA DE POSTÍTULO EN INVESTIGACIÓN CLÍNICA Y CERTIFICADO DE MONITOR DE ENSAYOS CLÍNICOS DIPLOMA DE POSTÍTULO EN INVESTIGACIÓN CLÍNICA Y CERTIFICADO DE MONITOR DE ENSAYOS CLÍNICOS, XII VERSIÓN
PROGRAMA CURSO BUENAS PRÁCTICAS EN INVESTIGACIÓN BIOMÉDICA (INVESTIGACIÓN OBSERVACIONAL E INTERVENCIONAL)
 PROGRAMA CURSO BUENAS PRÁCTICAS EN INVESTIGACIÓN BIOMÉDICA (INVESTIGACIÓN OBSERVACIONAL E INTERVENCIONAL) 1. Características Horas virtuales: 18 horas divididas en 6 módulos Horas presenciales: 7 horas.
PROGRAMA CURSO BUENAS PRÁCTICAS EN INVESTIGACIÓN BIOMÉDICA (INVESTIGACIÓN OBSERVACIONAL E INTERVENCIONAL) 1. Características Horas virtuales: 18 horas divididas en 6 módulos Horas presenciales: 7 horas.
COMISIÓN DE AUTORIZACIÓN SANITARIA ENSAYOS CLÍNICOS HOMOCLAVE ENMIENDA A LOS DOCUMENTOS PREVIAMENTE AUTORIZADOS
 Hoja 1 de 5 ENMIENDA A LOS S PREVIAMENTE AUTORIZADOS Identificador ROSA 1) Formato de solicitud Formato de Autorizaciones, Certificados y Visitas, solicitud de autorización de protocolo de Llenar las siguientes
Hoja 1 de 5 ENMIENDA A LOS S PREVIAMENTE AUTORIZADOS Identificador ROSA 1) Formato de solicitud Formato de Autorizaciones, Certificados y Visitas, solicitud de autorización de protocolo de Llenar las siguientes
LA COOPERACIÓN ENTRE LA PROFESIÓN MÉDICA Y LA INDUSTRIA FARMACÉUTICA
 Declaración Conjunta 3 del CPME y de la EFPIA sobre LA COOPERACIÓN ENTRE LA PROFESIÓN MÉDICA Y LA INDUSTRIA FARMACÉUTICA Introducción 1. La profesión médica, representada por el Comité Permanente de Médicos
Declaración Conjunta 3 del CPME y de la EFPIA sobre LA COOPERACIÓN ENTRE LA PROFESIÓN MÉDICA Y LA INDUSTRIA FARMACÉUTICA Introducción 1. La profesión médica, representada por el Comité Permanente de Médicos
Universidad Interamericana de Puerto Rico Junta de Revisión Institucional Oficina Central del Sistema UIPR JRI 2014
 Universidad Interamericana de Puerto Rico Junta de Revisión Institucional Oficina Central del Sistema UIPR JRI 2014 45 CFR PARTE A BELMONT REPORT DOCUMENTO NORMATIVO: A-IRB-013-2000R Política Institucional
Universidad Interamericana de Puerto Rico Junta de Revisión Institucional Oficina Central del Sistema UIPR JRI 2014 45 CFR PARTE A BELMONT REPORT DOCUMENTO NORMATIVO: A-IRB-013-2000R Política Institucional
CÓDIGO DE ÉTICA PARA LA INVESTIGACIÓN
 www.uladech.edu.pe RECTORADO CÓDIGO DE ÉTICA PARA LA INVESTIGACIÓN VERSIÓN 001 Aprobado por acuerdo del Consejo Universitario con Resolución N 0108-2016-CU-ULADECH Católica, de fecha 25 de enero de 2016
www.uladech.edu.pe RECTORADO CÓDIGO DE ÉTICA PARA LA INVESTIGACIÓN VERSIÓN 001 Aprobado por acuerdo del Consejo Universitario con Resolución N 0108-2016-CU-ULADECH Católica, de fecha 25 de enero de 2016
SOLICITUD ACREDITACIÓN COMITÉ ÉTICO CIENTÍFICO (CEC)
 Fecha SOLICITUD ACREDITACIÓN COMITÉ ÉTICO CIENTÍFICO (CEC) I.- IDENTIFICACIÓN DE LA INSTITUCIÓN EN QUE SE CONSTITUYE EL CEC RAZON SOCIAL RUT DIRECCIÓN TELÉFONO CORREO ELECTRÓNICO II.- IDENTIFICACIÓN REPRESENTANTE
Fecha SOLICITUD ACREDITACIÓN COMITÉ ÉTICO CIENTÍFICO (CEC) I.- IDENTIFICACIÓN DE LA INSTITUCIÓN EN QUE SE CONSTITUYE EL CEC RAZON SOCIAL RUT DIRECCIÓN TELÉFONO CORREO ELECTRÓNICO II.- IDENTIFICACIÓN REPRESENTANTE
D-10 REGLAMENTO DE BIOÉTICA. Código: D-10 REGLAMENTO DE BIOÉTICA. Fecha efectiva 18/04/2016. Página: 1 de 13. Versión: 00
 UNIVERSIDAD METROPOLITANA DE EDUCACIÓN, CIENCIA Y TECNOLOGÍA REGLAMENTO DE BIOÉTICA Código: D-10 Versión: 00 Fecha efectiva 18/04/2016 Página: 1 de 13 D-10 REGLAMENTO DE BIOÉTICA 1 Por medio del cual se
UNIVERSIDAD METROPOLITANA DE EDUCACIÓN, CIENCIA Y TECNOLOGÍA REGLAMENTO DE BIOÉTICA Código: D-10 Versión: 00 Fecha efectiva 18/04/2016 Página: 1 de 13 D-10 REGLAMENTO DE BIOÉTICA 1 Por medio del cual se
Cuáles son sus papeles y obligaciones?
 Science at the heart of medicine Cuáles son sus papeles y obligaciones? Ruth Macklin, PhD Ruth Macklin, PhD El Papel de los Comités El papel principal de los comités de ética es proteger los derechos y
Science at the heart of medicine Cuáles son sus papeles y obligaciones? Ruth Macklin, PhD Ruth Macklin, PhD El Papel de los Comités El papel principal de los comités de ética es proteger los derechos y
Anexo 3 Criterios y requisitos que debe reunir la documentación que acompaña al protocolo de investigación para su evaluación por la CNIC
 Anexo 3 Criterios y requisitos que debe reunir la documentación que acompaña al protocolo de investigación para su evaluación por la CNIC Página 1 de 7 Clave: 2800-003-004 Criterios y requisitos que debe
Anexo 3 Criterios y requisitos que debe reunir la documentación que acompaña al protocolo de investigación para su evaluación por la CNIC Página 1 de 7 Clave: 2800-003-004 Criterios y requisitos que debe
Cuando los riesgos previsibles son extremos, la decisión ética es en general bastante fácil de tomar. Si los riesgos son muy grandes, se rechaza la
 Cuando los riesgos previsibles son extremos, la decisión ética es en general bastante fácil de tomar. Si los riesgos son muy grandes, se rechaza la experimentación. Si los riesgo son muy pequeños, y la
Cuando los riesgos previsibles son extremos, la decisión ética es en general bastante fácil de tomar. Si los riesgos son muy grandes, se rechaza la experimentación. Si los riesgo son muy pequeños, y la
Curso: Buenas Prácticas Clínicas. Modalidad: híbrida Del 16 de agosto al 30 de setiembre de 2017 PROGRAMA
 En coordinación con la Vicerrectoría de Investigación Curso: Buenas Prácticas Clínicas (Para investigadores y CEC que se involucrarán en investigación intervencional en humanos) Modalidad: híbrida Del
En coordinación con la Vicerrectoría de Investigación Curso: Buenas Prácticas Clínicas (Para investigadores y CEC que se involucrarán en investigación intervencional en humanos) Modalidad: híbrida Del
Farmacovigilancia Proactiva de la prolongación del intervalo QTc en hospitales de la ciudad de Buenos Aires.
 UNIVERSIDAD DE BUENOS AIRES Secretaría de Ciencia y Técnica Proyectos de Investigación Científica o de Innovación Tecnológica Programación Científica 2010-2012 Farmacovigilancia Proactiva de la prolongación
UNIVERSIDAD DE BUENOS AIRES Secretaría de Ciencia y Técnica Proyectos de Investigación Científica o de Innovación Tecnológica Programación Científica 2010-2012 Farmacovigilancia Proactiva de la prolongación
Metodología de la Investigación. Dra. Rosalilia Garcia Kavanagh
 Metodología de la Investigación Dra. Rosalilia Garcia Kavanagh Unidad 5.- Ética del Investigador 5.1.- Conceptos 5.2.- Revisión de Códigos Internacionales EVALUACION FINAL Conocimiento de lo que el ser
Metodología de la Investigación Dra. Rosalilia Garcia Kavanagh Unidad 5.- Ética del Investigador 5.1.- Conceptos 5.2.- Revisión de Códigos Internacionales EVALUACION FINAL Conocimiento de lo que el ser
Guía para la Industria
 148 Guía para la Industria Estudios para Evaluar la Seguridad de Residuos de Medicamentos Veterinarios en Alimentos Humanos: Estudio de Toxicidad del Desarrollo VICH GL32 GUIA FINAL (Esta versión de la
148 Guía para la Industria Estudios para Evaluar la Seguridad de Residuos de Medicamentos Veterinarios en Alimentos Humanos: Estudio de Toxicidad del Desarrollo VICH GL32 GUIA FINAL (Esta versión de la
Características del Ensayo clínico. El Ensayo clínico controlado (aleatorizado, randomizado) El Ensayo Clínico Controlado (ECC)
 El Ensayo clínico controlado (aleatorizado, randomizado) la nueva lógica de la terapéutica El Ensayo Clínico Controlado (ECC) Establece y compara la eficacia de las intervenciones Patrón de oro Paradigma
El Ensayo clínico controlado (aleatorizado, randomizado) la nueva lógica de la terapéutica El Ensayo Clínico Controlado (ECC) Establece y compara la eficacia de las intervenciones Patrón de oro Paradigma
Versión 1. Elaborada Marzo de Fecha de entrada en vigencia: Adaptado por: Firma Fecha Posición
 UNIVERSIDAD DE PANAMÁ COMITÉ DE BIOÉTICA DE LA INVESTIGACIÓN, CBIUP PROTOCOLO OPERATIVO ESTÁNDAR TÍTULO: Requisitos de Presentación de Protocolos de Investigación u otros documentos por primera vez al
UNIVERSIDAD DE PANAMÁ COMITÉ DE BIOÉTICA DE LA INVESTIGACIÓN, CBIUP PROTOCOLO OPERATIVO ESTÁNDAR TÍTULO: Requisitos de Presentación de Protocolos de Investigación u otros documentos por primera vez al
en desacuerdo con el Estado miembro evaluador (4) los plazos para evaluar y autorizar, que, según nuestro punto de vista, son poco
 Declaración del Grupo Europeo de Ética de la Ciencia y las Nuevas Tecnologías (GEE) sobre la Propuesta de Regulación del Parlamento Europeo y el Consejo sobre Ensayos Clínicos de Medicamentos para Uso
Declaración del Grupo Europeo de Ética de la Ciencia y las Nuevas Tecnologías (GEE) sobre la Propuesta de Regulación del Parlamento Europeo y el Consejo sobre Ensayos Clínicos de Medicamentos para Uso
