USO DE LA BALANZA TERMOGRAVIMÉTRICA PARA LA DETERMINACIÓN DE VELOCIDADES DE REACCIÓN. CASO: DESCOMPOSICIÓN DEL CARBONATO DE CALCIO
|
|
|
- José Ignacio Botella Juárez
- hace 8 años
- Vistas:
Transcripción
1 USO DE LA BALANZA TERMOGRAVIMÉTRICA PARA LA DETERMINACIÓN DE VELOCIDADES DE REACCIÓN. CASO: DESCOMPOSICIÓN DEL CARBONATO DE CALCIO ERWIN FERNÁNDEZ RICO OMAR FABIAN GARCIA AFANADOR UNIVERSIDAD INDUSTRIAL DE SANTANDER FACULTAD DE INGENIERÍAS FISICOQUÍMICAS ESCUELA DE INGENIERÍA QUÍMICA BUCARAMANGA 27
2 USO DE LA BALANZA TERMOGRAVIMÉTRICA PARA LA DETERMINACIÓN DE VELOCIDADES DE REACCIÓN. CASO: DESCOMPOSICIÓN DEL CARBONATO DE CALCIO ERWIN FERNÁNDEZ RICO OMAR FABIAN GARCIA AFANADOR Trabajo de grado presentado como requisito para optar al título de Ingeniero Químico Director ÁLVARO RAMÍREZ GARCÍA Ingeniero Químico PhD UNIVERSIDAD INDUSTRIAL DE SANTANDER FACULTAD DE INGENIERÍAS FISICOQUÍMICAS ESCUELA DE INGENIERÍA QUÍMICA BUCARAMANGA 27
3
4
5 AGRADECIMIENTOS Al Doctor Alvaro Ramírez García por su confianza en nosotros y por el tiempo dedicado a este proyecto. A Huguinho, esto es como si fuera suyo. A Eduardo, Wilson, Martha, Linita, Guillermo y Chucho, las personas que trabajan en la escuela. Nos tienen paciencia y nos aconsejan. A Paola, Ciro, Porras que estuvieron presentes mientras se escribía esto. Al profesor Grosso y al profesor Henao que nos dieron otra perspectiva para nuestro trabajo. A nuestros amigos, imposible nombrarlos, son muchos. A la señora Angela, que nos soporto en su casa. A la familia de Huguinho en piedecuesta que siempre nos recibieron. Y a todo aquel que en algún momento fue importante.
6 Con mucho cariño a mi madre Angela Afanador y mi hermano Cesar Garcia, que con mucho esfuerzo, dedicación y paciencia hicieron que se cumpliera mi sueño de ser Ingeniero Químico. OMAR.
7 Para Camila, mi bebe hermosa, que en estos ocho años de vida le ha tocado compartirme con la universidad. A mis amigos, me tomare el atrevimiento de nombrar a algunos muy specialmente, Pedro Ferrada,Fabio Molano, Manuel Valero, William Serrano, Zaira Milena Perez, Carlos Zarate, Ivan Mantilla, Carlos el chori Gonzalez, Jose Posada, Carlos Gordillo, Diego Camargo, Jair Ruiz,Ferney Ortiz, Edwar Arenas, Hugo Acosta, Andrea Carolina Acosta y Omar Garcia A todas las entidades universitarias en las que he participado, La Sub Veinte CALSV, al Centro de Estudios de Ingeniería Química, los Toros UIS Rugby Club, los Ositos Cariñositos de Ingequimica, el Combo de Alvarito, Producciones la primera inc., barra los Busca Huecos de Igequimica. A las personas que en el 22 ayudaron a tomar la decisión de retirarme por un tiempo de la universidad, de no ser asi, no creo que hubiese terminado. A Nadia, la mujer que amo, en quien pienso a cada momento y a quien me gustaría tener por siempre a mi lado, pero como no se puede, créame que la tendré siempre en un rincón de mi corazón. CALSV#2.
8 INTRODUCCION CONTENIDO Pág. CAPITULO I CONCEPTOS BÁSICOS Técnicas termoanalíticas Termogravimetría Factores que afectan las curvas termogravimétricas Aplicaciones de la termogravimetría Descomposición térmica Temperatura de descomposición Carbonato de calcio Velocidad de reacción Energía de activación Determinación experimental de E a y A por medio de termogravimetría Modelamiento de la balanza termogravimétrica como un 7 reactor discontinúo. Método integral Modelo matemático de Kissinger Modelo matemático de Coast-Redfern 1 CAPITULO II MÉTODOLOGIA EXPERIMENTAL 12 CAPITULO III RESULTADOS Y ANALISIS 14
9 3.1. CURVAS TERMOGRAVIMÉTRICAS GENERADAS PARA LA 14 DESCOMPOSICIÓN DEL CaCO DETERMINACIÓN DEL ORDEN DE REACCIÓN EMPLEANDO EL 15 MÉTODO INTEGRAL 3.3. DETERMINACION DE LA ENERGÍA DE ACTIVACIÓN Y FACTOR DE 16 FRECUENCIA EMPLEANDO EL MÉTODO INTEGRAL 3.4. DETERMINACIÓN DE LA ENERGÍA DE ACTIVACIÓN EMPLEANDO 17 EL MODELO MATEMÁTICO DE KISSINGER 3.5. DETERMINACIÓN DE LA ENERGÍA DE ACTIVACIÓN Y FACTOR 18 DE FRECUENCIA EMPLEANDO EL MODELO MATEMÁTICO DE COAST-REDFERN 3.6. VELOCIDAD DE REACCIÓN PROPUESTA EMPLEANDO ELMÉTODO 19 INTEGRAL 3.7. VELOCIDAD DE REACCIÓN PROPUESTA EMPLEANDO EL MODELO 2 DE KISSINGER 3.8. VELOCIDAD DE REACCIÓN PROPUESTA EMPLENADO EL MODELO 2 DE COAST-REDFER CAPITULO IV CONCLUSIONES 21 REFERENCIAS BIBLIOGRAFICAS 22
10 LISTA DE TABLAS Tabla Nombre pág. 1 Especificaciones del carbonato de calcio empleado en los 13 experimentos 2 Tiempo empleado en cada rutina de experimentos según la 12 velocidad de calentamiento (β) 3 Factor de correlación lineal (R 2 ) obtenido en el calulo de E a 16 y A 4 Energía de activación E a (kj/mol) calculada a diferente β 16 y orden de reacción 5 Factor de frecuencia A (1/min) calculada a diferente β y orden 17 de reacción 6 Temperatura en el punto de inflexión (T m ) a diferentes β 18 7 Energía de activación E a (kj/mol) y factor de correlación lineal 18 (R 2 ) obtenidos empleando el modelo de Kissinger 8 Resultados del modelo de Coast-Redfern a diferentes 19 velocidades de calentamiento
11 LISTA DE FIGURAS FIGURA NOMBRE pág 1 Curvas termogravimétricas 2 a. %W pérdida Vs T (ºC) b. %W pérdida Vs t (min) 2 Evolución de la pérdida en peso de carbonato (%W) 14 respecto al tiempo (min) para diferentes β 3 Evolución de la pérdida en peso de carbonato (%W) 15 respecto a la temperatura (K) para diferentes β
12 LISTA DE ANEXOS ANEXO NOMBRE pág. A Método integral 25 B Modelo matemático de Kissinger 42 C Modelo matemático de Coast-Redfern 43
13 RESUMEN TITULO :USO DE LA BALANZA TERMOGRAVIMÉTRICA PARA LA DETERMINACION DE VELOCIDADES DE REACCIÓN. CASO: DESCOMPOSICION DEL CARBONATO DE CALCIO * Autores: ERWIN FERNANDEZ RICO ** OMAR FABIAN GARCIA AFANADOR Palabras claves: CaCO 3, termogravimetria, energía de activación, factor de frecuencia, velocidad de reacción. DESCRIPCIÓN: Las curvas termogravimétricas obtenidas usando la balanza termogravimétrica permiten obtener parámetros cinéticos como la energía de activación (E a ) y el factor de frecuencia (A) que se requieren para calcular la constante de velocidad de reacción (k) cuando se sigue el modelo propuesto por Arrhenius. Estos parámetros deben ser calculados experimentalmente ya que actualmente solo las teorías mecano-cuánticas permiten su evaluación con cierta precisión. Las curvas termogravimétricas para la reacción de descomposición del carbonato de calcio han sido medidas para cinco diferentes velocidades de calentamiento (β). Los parámetros cinéticos y la velocidad de reacción fueron evaluadas a partir de las curvas termogravimétricas usando el modelo de Kissinger, Coast y las ecuaciones derivadas a partir de balances molares asumiendo que la balanza termogravimétrica se comporta como un reactor discontinuo. La velocidad de calentamiento (β) afecta la evaluación del cálculo de la energía de activaciòn y el factor de frecuencia. * Proyecto de grado ** FACULTAD DE INGENIERIAS FISICOQUIMICAS, ESCUELA DE INGENIERIA QUIMICA Director: Ph D. Alvaro Ramírez Garcia
14 ABSTRACT TITLE: USING THE THERMOGRAVIMETRIC ANALYSER TO DETERMINE REACTION RATES. CASE: CALCIUM CARBONATE DECOMPOSITION * Authors: ERWIN FERNANDEZ RICO ** OMAR FABIAN GARCIA AFANADOR Keywords: CaCO 3, termogravimetry, activation energy, frecuency factor, reaction rates. DESCRIPTION The themogravimetric curves obtained using a thermogravimetric analyser allow us to obtain kinetics parameters such as the activation energy (E a ) and the frecuency factor (A) which are required in order to calculate the rate constant (k) when the Arrhenius model is used. These parameters have to be determined experimentally because for the time being only quantic theories allow to predict their evaluation with some accuracy. The thermogravimetric curves of the thermal decomposition reaction of calcium carbonate have been measured at five different heating rates (β). The kinetics parameters and the reaction rate were evaluated from analysis of the thermogravimetry curves by using the Kissinger, Coast and the equations derived assuming that the thermogravimetric analyser behaves like a batch reactor. The heating rate (β) affects the activation energy and the frecuency factor evaluation. * Undergraduate Thesis Work ** FACULTAD DE INGENIERIAS FISICOQUIMICAS, ESCUELA DE INGENIERIA QUIMICA Director: Ph D. Alvaro Ramírez Garcia
15 INTRODUCCION El diseño y desarrollo de nuevos materiales están transformando nuestras vidas. Estos materiales deben ser caracterizados y es de vital importancia conocer su desempeño ante diferentes atmósferas (estudios de corrosión) y los limites en los que pueden ser empleados (estabilidad térmica). La balanza termogravimétrica permite llevar a cabo estos y otros estudios de manera sencilla. Las curvas termogravimétricas de la reacción de descomposición térmica del carbonato de calcio han sido medidas para cinco velocidades diferentes de calentamiento (β). Los parámetros cinéticos y la velocidad de reacción fueron evaluados a partir de estas curvas. El primer capítulo describe la técnica de termogravimetría y sus aplicaciones; conceptos cinéticos como velocidad de reacción, energía de activación y factor de frecuencia así como una breve explicación de los modelos de Kissinger, y Coast, usados previamente en otros estudios. De igual manera se muestran las ecuaciones obtenidas cuando se modela la balanza termogravimétrica como un reactor discontinúo. En el segundo capítulo se muestra un diagrama de bloques en el cual se presenta la métodología del trabajo experimental. En el tercer capítulo se muestran los resultados de cálculo del orden de reacción, energía de activación y el factor de frecuencia para cada uno de los modelos propuestos y su respectiva discusión. Finalmente en el cuarto capítulo se presentan las principales conclusiones.
16 CAPITULO I CONCEPTOS BÁSICOS 1.1. TÉCNICAS TERMOANALÍTICAS Las técnicas termoanalíticas tales como termogravimetría, termovolumetría y análisis térmicos diferenciales están siendo empleadas en la investigación de reacciónes químicas en el estado liquido y sólido a temperaturas elevadas. Estas técnicas conllevan la medición continua de un cambio en una propiedad física (masa, volumen o capacidad calorífica) a medida que la temperatura se incrementa a una velocidad de calentamiento determinada [5] Termogravimetría. Por medio de esta técnica se estudia el cambio en la masa de una muestra mientras que esta es sometida a una rutina de calentamiento, la cual es generalmente una función lineal del tiempo. La técnica termogravimétrica es inherentemente cuantitativa y por consiguiente poderosa. Sin embargo, la técnica no permite obtener información química (energía de activación, factor de frecuencia, orden de reacción ) directamente a partir de las curvas obtenidas por lo que se requiere un tratamiento en los datos obtenidos a fin de adquirir información valiosa. La sensibilidad de la balanza termogravimétrica de uso en laboratorios tanto en la determinación de diferencias de peso como en el control de la temperatura es la clave para el análisis de procesos de descomposición, como es el caso objeto de este trabajo. 2
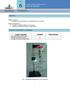
17 La Figura 1 muestra curvas termogravimétricas para la descomposición de carbonato de calcio obtenidas por la balanza termogravimétrica TG 25 para una velocidad de calentamiento β = 12ºC/min %W T a %W t b Figura 1. Curvas termogravimétricas. a. %W pérdida Vs T (ºC). b. %W pérdida Vs t (min). 3
18 Se observa una pequeña pérdida de peso en el intervalo de temperatura hasta 2 o C ó en los primeros 15 minutos que los autores atribuyen a pérdida de humedad. En las curvas termogravimétricas se observan varias regiones: inicialmente, una pequeña disminución, que como ya se anotó, puede corresponder a la humedad de la muestra; sigue una región de peso constante en la que posiblemente no ocurre reacción; se observa luego una región en la que inicia la pérdida en peso, que seguramente corresponde a el inicio de la reacción; a continuación se observa un segmento casi lineal de pérdida en peso; la pendiente es un indicativo de la velocidad de reacción; en el último segmento de la curva se observa peso constante y corresponde a la región en la que la reacción no ocurre por agotamiento de reactivo Factores que afectan las curvas termogravimétricas Varios factores influencian la forma de la curva termogravimétrica entre ellos: la velocidad de calentamiento (β), la cantidad de muestra y la naturaleza y velocidad de flujo del gas de arrastre. En esta investigación se estudia la influencia de β en la determinación de la energía de activación y el factor de frecuencia Aplicaciones de la termogravimetría La capacidad de la termogravimetría para generar datos cuantitativos de casi toda clase de materiales ha permitido llevar a cabo estudios en los campos de la ciencia y tecnología. Las áreas en las que se ha aplicado la termogravimetría incluyen: 4
19 Estabilidad térmica: Relativa a materiales que pueden descomponerse en diferentes atmósferas. Las curvas termogravimétricas pueden ayudar a explicar los mecanismos de descomposición. Estudios cinéticos: Por medio de las curvas termogravimétricas es posible obtener parámetros cinéticos como la energía de activación (E a ) y el factor de frecuencia (A) requeridos para calcular la constante de velocidad de reacción (k) cuando se sigue el modelo propuesto por Arrhenius a partir de los datos de perdida de peso. Caracterización de materiales: Termogravimetría y análisis diferencial térmico pueden ser utilizados para identificar materiales y en procesos de control de calidad. Estudios de corrosión: Permite estudiar los fenómenos de corrosión que se presentan cuando se someten los materiales a oxidación o cuando estos reacciónan bajo atmósferas reactivas de gases o vapores. Simulación de procesos industriales: Debido a que el horno de la balanza termogravimétrica puede ser considerado como un mini reactor, es posible modelar y extrapolar las condiciones de operación a un reactor industrial Descomposición térmica Es una reacción química en la que una sustancia se descompone en al menos dos sustancias químicas cuando es sometida a calentamiento. La reacción es endotérmica ya que requiere el suministro de energía térmica para romper los enlaces químicos en la muestra a descomponer [16]. 5
20 1.3. TEMPERATURA DE DESCOMPOSICIÓN La temperatura o intervalo de temperatura al que una sustancia se descompone en sus constituyentes se conoce como temperatura de descomposición. Sin embargo, para algunos compuestos, esta temperatura puede disminuir cuando la descomposición se lleva a cabo en presencia de otras sustancias o según la atmósfera bajo la cual se efectué la reacción [16] Carbonato de calcio El carbonato de calcio es un mineral abundante que representa un 4% de la corteza terrestre. Como mineral inorgánico es ampliamente utilizado debido a sus usos en la industria de papel, plásticos, pinturas, metalúrgica, etc. La cinética de descomposición del carbonato de calcio es el ejemplo más popular en las investigaciones de análisis térmico. Esto se debe principalmente a la importancia tecnológica del compuesto y a la aparente simplicidad de la reacción [11]. La descomposición térmica del carbonato de calcio sigue la siguiente reacción endotérmica: CaCO 3() s CaO () s + CO 2() g : H =178kJ.mol 1 (1) El conocimiento del proceso y el control de la descomposición del carbonato es importante ya que permite el diseño de reactores y la optimización en cuanto a los recursos energéticos necesarios para la obtención de CaO y CO Velocidad de reacción La velocidad de desaparición de la especie A, r A, depende de la temperatura y la composición y en el caso de muchas reacciónes se puede escribir como el 6
21 producto de una constante de velocidad (k) y una función de las concentraciones (actividades) de las diversas especies que participan en la reacción: [ ][ fn( C A,C B,...)] (2) r A = k ( T) La ecuación algebraica que relaciona r A con las concentraciones de las especies se denomina expresión cinética o ley de velocidad. La velocidad especifica de reacción, -r A, se toma como referencia a una especie dada de las reacciónes y normalmente debe llevar el subíndice correspondiente a esa especie [4]. La constante de velocidad de reacción k no es una verdadera constante; solo es independiente de las concentraciones de las especies que intervienen en la reacción. La cantidad k depende marcadamente de la temperatura. Este supuesto es válido en la mayor parte de las reacciónes de laboratorio e industriales y ha funcionado de forma muy aceptable [4]. Fue el gran químico Arrhenius quien primero sugirió que la dependencia de la constante de velocidad de reacción, k, respecto a la temperatura se podía correlacionar con una ecuación del tipo kt ( )= Ae E / RT (3) Donde: A=factor de frecuencia o preexponencial E=energía de activación, J.mol -1 o cal.mol -1 R=constante de los gases = J/mol.K = 1.987cal/mol.K T= temperatura absoluta, K Se ha verificado experimentalmente que la ecuación (3) llamada ecuación de Arrhenius, es valida para la mayoría de las constantes de velocidad de reacción 7
22 hasta donde permite la precisión experimental, dentro de intervalos de temperatura relativamente amplios [4] Energía de activación La energía de activación E a se ha considerado como la energía mínima que deben poseer las moléculas de los reactivos para que ocurra la reacción. Algunos sugieren que E a no es más que un parámetro empírico que correlaciona la velocidad de reacción específica con la temperatura [9]. No obstante, la postulación de la ecuación de Arrhenius sigue siendo el paso individual más importante en cinética química y conserva su utilidad hoy, casi un siglo después. Existe una regla práctica que dice que la velocidad de reacción se duplica por cada aumento de 1ºC en la temperatura. Sin embargo, esto solo es cierto para una combinación especifica de energía de activación y temperatura. Por ejemplo, si la energía de activación es de 53.6 kj/mol, la velocidad solo se duplicará si la temperatura se eleva de 3 a 31 K [4]. Cuanto mayor es la energía de activación, más sensible a la temperatura es la velocidad de reacción. Aunque todavía no es posible predecir la energía de activación a priori se han iniciado proyectos de investigación importantes para calcular energías de activación a partir de primeros principios [4] Determinación experimental de E a y A por medio de termogravimetría Estudios previos para la descomposición de carbonato de calcio han sido reportados [8] [1] [11] [12] [13] [14] y en ellos se ha establecido que las condiciones experimentales afectan los parámetros cinéticos [2]. 8
23 Modelamiento de la balanza termogravimétrica como un reactor discontinúo. Método integral. A partir del balance molar para un reactor discontinuo se obtiene una relación que nos permite encontrar A y E a para cualquier orden de reacción (n). En esta relación no se tienen en cuenta consideraciones fenomenológicas en cuanto a transferencia de masa y energía como otros autores lo han hecho. Una vez calculado A y E a se podrá encontrar la constante de velocidad k siguiendo el modelo propuesto por Arrhenius y finalmente con el orden de reacción quedará determinada la velocidad de reacción para cualquier sistema. Balance molar para un reactor discontinúo: dx A rav = N A (4) dt A V=cte kt ()C n dx A = C A A dt (5) k(t) = A e E a RT E a RT A e C n dx A = C A A dt (6) Para n= con C A =1 9
24 dx A dt E a RT = A e (7) dx A ln = ln A (8) dt RT Para n = 1 dx A dt = A e E a RT ( 1 X A ) (9) X t dx A = A ( 1 X A ) X E a e RT dt (1) ln 1 X E a RT = A e t (11) 1 X 1 1 X E a RT ln = A e (12) t 1 X ln 1 1 X ln = ln A E a t 1 X RT (13) Para n 1 dx A dt E a RT = A e ( 1 X A ) n (14) X 1 E a e X t dx RT = A ( 1 X A ) n dt (15)
25 ( 1 X) n +1 ( n +1 ) n +1 ( ) ( ) 1 X n +1 E a RT = A te (16) Para to=, X = n +1 ( 1 X) n +1 ( ) 1 * 1 E t = A a RT e (17) ( ) ( n+ 1 1 X ) 1 = ln A ( n + 1) t RT ln (18) Con las ecuaciones (8), (13) y (18) para cualquier orden de reacción (n) es posible calcular la velocidad de reacción y el factor de frecuencia para una velocidad de calentamiento (β) preestablecida. Otros autores [11] [13] [14] han desarrollado modelos que incluyen efectos diversos como la velocidad de calentamiento y los fenómenos de transferencia de masa y energía Modelo matemático de Kissinger La deducción y una explicación detallada del método se encuentra en [12]. Kissinger propone la ecuación (19) para calcular la energía de activación en función de la velocidad de calentamiento. En el trabajo de Kissinger se muestra que aunque el valor de conversión en el punto de inflexión cambia con la velocidad de calentamiento, la pendiente de la curva de ln(β/t 2 m ) frente a 1/T m, es constante, por lo cual se concluye que para efectos de utilización de la ecuación (19), el segundo término se considera globalmente constante y podría decirse que en el cálculo de la energía de activación según la ecuación de Kissinger, no intervienen 11
26 el orden de reacción n, ni la conversión. De esta forma, según el modelo conduce al valor de E a sin un conocimiento previo del mecanismo de reacción. ln β 2 = ln AE a n(1 x) n 1 E a (19) T m RT m Donde: β=velocidad de calentamiento (ºC/min), x=conversión, T m =Temperatura en el punto de inflexión, n=orden de reacción, A=factor de frecuencia y E a =energía de activación. E a Modelo matemático de Coast-Redfern El método propuesto por Coast [12] asume un orden de reacción n= 2/3 y una cinética de degradación que incluye efectos relacionados a la contracción de volumen que sufre el carbonato al ser sometido a calentamiento. Hasta el momento es el método más usado como referencia en estudios hechos por otros autores [13]. El modelo matemático propuesto se presenta a continuación: Donde: ln g(x) = ln( AR ) E a T 2 βe a RT (2) g(x) = 1 1 x ( ) 1 3 Función que incluye efectos en la contracción de volumen que sufre el carbonato al ser sometido a calentamiento. 12
27 β=velocidad de calentamiento (ºC/min), x=conversión, T=Temperatura, A=factor de frecuencia y E a =energía de activación. Al graficar ln g(x) contra 1/T se obtiene una línea recta de cuya pendiente se T 2 puede calcular la energía de activación y con el punto de corte se obtiene el factor de frecuencia. 13
28 CAPITULO II MÉTODOLOGIA EXPERIMENTAL MONTAJE DE LA MUESTRA DE CARBONATO DE CALCIO (CaCO 3 ) VARIACION DE LA RATA DE CALENTAMIENTO (β) 8ºC/min 1ºC/min 12ºC/min 25ºC/min 4ºC/min OBTENCION DE LAS CURVAS TERMOGRAVIMÉTRICAS DETERMINACION DE LOS PARAMETROS CINETICOS CALCULO DE LA VELOCIDAD DE REACCIÓN 14
29 El carbonato de calcio grado analítico fue suministrado por Laboratorios Merck (Bogotá, Colombia); Las especificaciones del CaCO 3 se presentan en la Tabla 1. Tabla 1. Especificaciones del carbonato de calcio empleado en los experimentos CARBONATO DE CALCIO (CaCO 3 ) Número CAS Densidad específica (2ºC) 2.93 g/cm 3 Punto de descomposición 825 ºC Se realizaron cinco pruebas a distintas velocidades de calentamiento como se indica en la Tabla 2. Tabla 2. Tiempo empleado en cada rutina de experimentos según la velocidad de calentamiento (ß). ß (ºC/min) Tiempo de experimento (min) Para todos los experimentos se emplearon alrededor de 1 mg de muestra; se trabajo con Nitrógeno (1 cm 3 /min) como gas de arrastre de CO 2 y para generar una atmósfera inerte durante la descomposición del carbonato. Una vez cargada la muestra en el portamuestra de la balanza se fijo una temperatura inicial de To = 3ºC y una temperatura final de Tf = 1ºC a fin de garantizar la descomposición completa del CaCO 3. Con las curvas termogravimétricas generadas y las ecuaciones (8), (13), (18), (19) y (2) se calcularon los parámetros cinéticos para la descomposición del carbonato de calcio. Estos parámetros y los resultados obtenidos se muestran en el siguiente capítulo. 15
30 CAPITULO III RESULTADOS Y ANALISIS 3.1. CURVAS TERMOGRAVIMÉTRICAS GENERADAS PARA LA DESCOMPOSICION DEL CaCO 3. En la Figura 2 se observa la pérdida de peso con respecto al tiempo para la descomposición del carbonato a diferentes velocidades de calentamiento (β). %W Vs Tiempo 1 %w ºC/min 1 ºC/min 12 ºC/min 25 ºC/min 4 ºC/min t Figura 2. Evolución de la pérdida en peso de carbonato (%w) respecto al tiempo (min) para diferentes β. Como se observa en la Figura 2 a medida que se incrementa la velocidad de calentamiento, aumenta la velocidad de descomposición del carbonato de calcio como se collige del menor tiempo de descomposición y de la mayor pendiente de 16
31 la curva. Este comportamiento también se aprecia en la Figura que muestra la evolución de %W Vs T para diferentes β. %W Vs TEMPERATURA 1 %W ºC/min 1 ºC/min 12ºC/min 25 ºC/min 4 ºC/min T Figura 3. Evolución de la pérdida en peso de carbonato (%W) respecto a la temperatura (ºC) para diferentes β. La Figura 3 muestra que para la misma muestra de carbonato existe una temperatura de descomposición diferente a cada velocidad de calentamiento y como ya se había establecido en trabajos previos a esta investigación las condiciones experimentales influencian la forma de las curvas termogravimétricas y por ende al cálculo de los parámetros cinéticos [2]. Obsérvese un retraso en el proceso a medida que aumenta la velocidad de calentamiento DETERMINACION DEL ORDEN DE REACCIÓN EMPLEANDO EL MÉTODO INTEGRAL Utilizando las ecuaciones (8), (13) y (18) del método integral, se calculo el coeficiente de correlación lineal (R 2 ) para diferentes ordenes de reacción como se reporta en la Tabla 3. 17
32 Tabla 3. Factor de correlación lineal (R 2 ) obtenido en el calculo de E a y A. β (ºC/min) ORDEN DE REACCIÓN (n) ,994 1,,9997,9978,9825 1,9878,9988,9971,9914, ,9947,9967,9953,9912,977 25,9864,9977,9967,9864,9813 4,9673,936,97,912,8724 Obsérvese que n=.5 presenta la mejor correlación de datos experimentales. Para n=.6 también se obtiene una buena correlación; se anota que n=.66 es el valor más utilizado en la literatura [12]. En el Anexo B se muestra en detalle el procedimiento que se siguió para calcular estos valores DETERMINACION DE LA ENERGÍA DE ACTIVACIÓN Y FACTOR DE FRECUENCIA EMPLEANDO EL MÉTODO INTEGRAL. Los datos obtenidos de E a y A para el método integral son presentados en la Tabla 4 y Tabla 5 respectivamente. Tabla 4. Energía de activación E a (kj/mol) calculada a diferente β y orden de reacción. β (K/min) ORDEN DE REACCIÓN , , , , , , , , , , , , ,17 188, , , , , , ,
33 4 151, ,686 11,524 13, ,2699 Tabla 5. Factor de frecuencia A (1/min) calculada a diferente β y orden de reacción. β (ºC/min) ORDEN DE REACCIÓN ,66E+9 2,75E+8 5,95E+8 2,99E+9 6,72E ,39E+8 1,9E+7 4,87E+7 3,46E+8 3,E ,37E+9 4,6E+7 8,55E+7 3,4E+8 2,13E ,5E+9 5,24E+7 8,43E+7 1,66E+9 7,88E+9 4 6,5E+6 7,3E+3 8,9E+4 1,39E+5 4,69E+6 Como se observa en la Tabla 4 y Tabla 5 y a partir de los coeficientes de correlación reportados en la Tabla 3 el método integral se ajusta mejor a bajas velocidades de calentamiento (β) y los valores obtenidos de E a y A están en un rango aceptable de datos para el orden de reacción establecido anteriormente. En el Anexo B se muestra en detalle el procedimiento que se siguió para calcular estos valores DETERMINACION DE LA ENERGÍA DE ACTIVACIÓN EMPLEANDO EL MODELO MATEMÁTICO DE KISSINGER Para la determinación del punto de inflexión requerido en este método se grafico d(%w ) dt Vs T y la temperatura T a la cual d(%w ) = valor máximo, corresponde a la dt temperatura en el punto de inflexión T m. 19
34 El Anexo C muestra en detalle el procedimiento que se siguió para calcular la energía de activación empleando la ecuación (19) y correlacionando los datos de las curvas termogravimétricas. La Tabla 6 reporta los valores obtenidos de T m para cada β estudiado en la descomposición del carbonato de calcio. Tabla 6. Temperatura en el punto de inflexión (T m ) a diferentes β. β (ºC/min) Tm (K) La Tabla 7 reporta el valor E a y el coeficiente de correlación lineal (R 2 ) obtenido al ajustar los datos obtenidos en la Tabla 6. Tabla 7. Energía de activación E a (kj/mol) y factor de correlación lineal (R 2 ) obtenidos empleando el modelo de Kissinger. Factor de E a (kj/mol) correlación R 2 25,6,9516 Como se observa en la Tabla 7, el método de Kissinger permite obtener un valor de E a sin un conocimiento previo del orden de reacción. Sin embargo, al emplear este método no es posible calcular A si no se conoce con anterioridad el valor de n. 2
35 Cabe resaltar que el valor reportado en la Tabla 7 es empleado como criterio de comparación a los valores de E a presentados en la Tabla 4 y Tabla 8. 21
36 3.5. DETERMINACION DE LA ENERGÍA DE ACTIVACIÓN Y FACTOR DE FRECUENCIA EMPLEANDO EL MODELO MATEMÁTICO DE COAST REDFERN En el Anexo D se muestra en detalle el procedimiento que se siguió para calcular E a y A empleando el modelo matemático de Coast-Redfern. La Tabla 8 muestra los valores de E a, A y el factor de correlación lineal (R 2 ) cuando se empleo el modelo matemático de Coast-Redfern quienes emplean un orden de reacción n=.66 y sugieren que para el calculo de los parámetros cinéticos se debe trabajar en un intervalo de conversiones de [.11.26] [12]. Tabla 8. Resultados del modelo de Coast-Redfern a diferentes velocidades de calentamiento. β (ºC/min) (kj/mol) A (1/min) Factor de correlación R ,4359 2,71E+8, ,3823 1,25E+8, ,5424 5,12E+6, ,6364 5,9E+7, ,37 1,5E+3,9993 Obsérvese que al igual que en el método integral los datos de las curvas termogravimétricas se ajustan mejor a bajas velocidades de calentamiento. Los valores de E a y A calculados utilizando tanto el modelo integral como el de Coast-Redfern (n=.66) difieren debido a que el modelo de Coast-Redfern incluye una función que corrige los efectos de contracción de volumen que sufre el carbonato de calcio al descomponerse [12] [1]. 22
37 3.6. VELOCIDAD DE REACCIÓN PROPUESTA EMPLEANDO EL MÉTODO INTEGRAL Para el método integral se propone que la velocidad de reacción para la descomposición no isotérmica del carbonato de calcio sea determinada por: r Ca CO = e RT [ C a CO 3 ] VELOCIDAD DE REACCIÓN PROPUESTA EMPLEANDO EL MODELO DE KISSINGER Para el modelo estudiado se propone que la velocidad de reacción para la descomposición no isotérmica del carbonato de calcio sea determinada por: 25.6 rc a CO 3 = Ae RT [ C a CO 3 ] n 3.8. VELOCIDAD DE REACCIÓN PROPUESTA EMPLEANDO EL MODELO DE COAST-REDFERN Para el modelo de Coast-Redfern se propone que la velocidad de reacción para la descomposición no isotérmica del carbonato de calcio sea determinada por: rc a CO 3 = e RT [ C a CO 3 ].66 23
38 CAPITULO IV CONCLUSIONES 1. La termogravimetría es una técnica sencilla y eficaz para realizar estudios cinéticos en reacciónes de descomposición en fase sólida. 2. El método integral de tratamiento de datos experimentales condujo a calcular un orden de reacción n=.5 (el valor reportado en la literatura [12] n=.66 también tiene una buena correlación); podría decirse que el orden de reacción esta en un intervalo [.5-.6]. 3. Para el calculo de la energía de activación se utilizaron los ecuaciones propuestos por Kissinger (19) y Coast-Redfern (2). Los valores calculados con los datos experimentales están en el intervalo de valores publicados en la literatura [12] 4. El tratamiento de los datos experimentales permite ajustar ecuaciones de velocidad de reacción de orden [;.5;.66; 1; 2] todas con correlaciones altas mayores de.95. El criterio utilizado para escoger n=.5 fue el de mejor (mayor) correlación. Esta conclusión es valida a bajas velocidades de calentamiento, menores que 25ºC/min. A velocidades de calentamiento de 4ºC/min se predice con buena correlación (R 2 =.96) para orden ; para otros ordenes la correlación es mas baja [.87;.9]. 24
39 REFERENCIAS BIBLIOGRAFICAS [1] Butt, J. (198). Reaction kinetics and reactor design Englewood Cliffs, Prentice Hall. [2] Cho, S. W., S.-M. Joo, et al. (26). "Kinetics Analysis of the Decomposition of Calcium Carbonate using Danyang Limestone." Material Science Forum (26): [3] Flynn, J. and L. Wall (1966). "A quick, direct method for the determination of activation energy from thermogravimetric data." Polymer letters 4(1966): [4] Fogler, H. S. (21). Elementos de ingeniería de las reacciónes químicas. Ciudad de México, Prentice Hall. [5] Freeman, E. and B. Carrol (1957). "The application of thermoanalytical techniques to reaction kinetics. The thermogravimetric evaluation of the kinetics of decomposition of calcium oxalate monohydrate." Chemistry department, Rutgers University 62(1957): 394. [6] Gao, Z., I. Amasaki, et al. (24). "Assesment of the error of the pre-exponential factor obtained from the isoconversional measurement of polymer degradation." Polymer degradation and stability 83(24): [7] Gotor, F. J., M. Macias, et al. (2). "Comparative study of the kinetics of the thermal decomposition of synthetic and natural siderite samples." Physic chemical minerals 27(2): [8] Gunasekaran, S. and G. Anbalagan (27). "Thermal decomposition of natural dolomite." Material Science 3(4): [9] Karplus, M., R. N. Porter, et al. (1978). Chemical physics 55(5). [1] L' vov, B. and V. Ugolkov (23). "Peculiarities of CaCO3, SrCO3 and BaCO3 decomposition in CO2 as a proof their primary dissociative evaporation " Thermochimica acta 41(1-2): [11] L' vov, B., V. Ugolkov, et al. (22). "Decomposition kinetics of calcite: a new approach to the old problem." Thermochimica aca 39(1-2): [12] Ozawa, T. (1965). "A new method of analyzing thermograimetric data." Electrotechnical Laboratory 38(11):
40 [13] Rao, R. T. (1996). "Kinetics of calcium carbonate decomposition " Chem. Eng. Technol 19(1996): [14] Satterfield, C. and F. Feakes (1959). "Kinetics of the thermal decomposition of calcium carbonate." A.I.Ch.E 5(1): [15] Zsako, J. and E. H. Arz (1972). "Kinetic analysis of thermogravimetric data." Journal of Thermal Analysis and Calorimetry 6(1974): [16] 26
41 ANEXO A: MÉTODO INTEGRAL CALCULO DE LOS PARAMETROS CINETICO PARA ORDEN.5 ln ( ) ( n+ 1 1 X ) 1 = ln A ( n + 1) t RT Graficando entonces, ( ) ( + X n 1 1 ) ( n + 1) t ln m * R E a = y 1 1 b A = e vs. T 1 obtenemos una línea de la forma y = mx + b, Velocidad de calentamiento 8 K/min W inicial 1,967 mg T t % W W X dx/dt 1/T LN(((1-X)^- n+1)-1)/(- n+1)*t (K) (min) %g (mg) (1/min) (1/K) (1/min) ,55 1,879785,273399,798146, , ,14 1,763138,375911,155613, , ,6 1,73792, ,139319, , ,9 1,62723, ,182266, , ,98 1, ,932288, , , ,82 1,398994,12369, , , ,371 1, ,163759,37369, , ,56 1,413852,2739, , , ,35 9,799145, ,5691,1645-4, ,67 9,55989, ,6913, , ,5 9,157445, , , , ,82 8, ,592688, , , ,66 8, , ,17168, , ,14 7,819238, , , , , KJ/mol Ao ,6 1/min 27
42 LN[((1-X)^(-n+1))-1)/(-n+1)*t] {1/min},1, ,1 4,1 6,1 8 1/T {1/K},11,11 2,11 4,11 6 y = x + 19,432 R 2 = 1 Velocidad de calentamiento 1 K/min W inicial 14,434 mg T (K) t (min) % W (%) W (mg) X dx/dt (1/min) 1/T (1/K) LN(((1-X)^-n+1)- 1)/(-n+1)*t (1/min) ,95 13,993763,329286, , , ,33 13,942722, ,157415, , ,5 13,78447, ,21233, , ,38 13,622892,982432, , , ,89 13,477426, ,377463,1645-4, ,95 13,127723, ,491388, , ,48 12,771232, , , , ,37 12,322358, ,787746, , ,52 11, , , , , ,94 11,155196, ,116811,175-3, ,69 1, , , ,9971-2, ,13 9,545242, ,14838, , Ao 163,96394 KJ/mol ,53 1/min 28
43 LN[((1-X)^(-n+1))-1)/(-n+1)*t] {1/min},98,1,12,14,16,18,11, /T {1/K} y = x + 16,779 R 2 =,9988 Velocidad de calentamiento 12 K/min W inicial 11,3 mg T (K) t (min) % W %g W (mg) X dx/dt (1/min) 1/T (1/K) LN(((1-X)^-n+1)- 1)/(-n+1)*t (1/min) ,13 1,823739,21927,541738, , ,8 1,78734, ,81268, , ,32 1,734396,41379, , , ,62 1,657186,573753, ,1929-5, ,61 1,545783, ,248772, , ,17 1,386951,11775, , , ,18 1,167454, ,49271, , ,47 9,868541,233444, , , ,88 9,472564, ,884187, , ,27 8,96481, , , , ,57 8,335371, , ,11-3, ,617,737538, , , Ao 174,46929 KJ/mol ,97 1/min 29
44 LN[((1-X)^(-n+1))-1)/(-n+1)*t] {1/min},95,1,15,11, /T {1/K} y = -2985x + 17,659 R 2 =,9967 Velocidad de calentamiento 25 K/min W inicial 7,475 mg T K t min % W %g W mg X dx/dt 1/min 1/T 1/K LN(((1-X)^-n+1)- 1)/(-n+1)*t 1/min ,79 7,39825,18247,11197, , ,92 7,24477, , , , ,1 7,18725,843432, , , ,46 6,836635,174164, ,9971-3, ,94 6,349265, , , , ,54 5,571865, , , , LN[((1-X)^(-n+1))-1)/(-n+1)*t] {1/min}, ,9 6,9 8,1,1 2,1 4,1 6,1 8,11 y = -2132x + 17,776 R 2 =,9977 Ao 177,14828 KJ/mol ,5 1/min 1/T {1/K} 3
45 Velocidad de calentamiento 4 K/min W inicial 9,621 mg T (K) t (min) % W % W (mg) X dx/dt (1/min) 1/T (1/K) LN(((1-X)^-n+1)- 1)/(-n+1)*t (1/min) ,49 9, ,786821,245881, , ,34 9, , ,368822, , ,8 9, , ,639292, , ,45 9, , ,154953,1645-5, ,45 9, , ,491763, , ,76 8,635896, , , , ,25 7, ,531248, ,9473-2, LN[((1-X)^(-n+1))-1)/(-n+1)*t] {1/min},8-1,9,1,11,12, /T {1/K} y = -1372x + 8,952 R 2 =,936 Ao 18,6868 KJ/mol 737, /min CALCULO DE LOS PARAMETROS CINETICO PARA ORDEN.66 ln ( ) ( n+ 1 1 X ) 1 = ln A ( n + 1) t RT Graficando entonces, ( ) ( + X n 1 1 ) ( n + 1) t ln m * R E a = y 1 1 b A = e vs. T 1 obtenemos una línea de la forma y = mx + b, Velocidad de calentamiento 8 K/min W inicial 1,967 mg 31
46 LN[((1-X)^(-n+1))-1)/(-n+1)*t] {1/min},1, ,1 4,1 6,1 8,11,11 2,11 4,11 6 y = x + 2,24 R 2 =,9997 Ao 19,15788 KJ/mol ,3 1/min 1/T {1/K} Velocidad de calentamiento 1 K/min W inicial 14,434 mg LN[((1-X)^(-n+1))-1)/(-n+1)*t] {1/min},98,1,12,14,16,18,11, /T {1/K} y = -2572x + 17,73 R 2 =,9971 Ao 171,3568 KJ/mol ,92 1/min Velocidad de calentamiento 12 K/min W inicial 11,3 mg Ao 179,1748 KJ/mol ,64 1/min 32
47 LN[((1-X)^(-n+1))-1)/(-n+1)*t] {1/min},95,1,15,11, /T {1/K} y = x + 18,265 R 2 =,9953 Velocidad de calentamiento 25 K/min W inicial 7,475 mg LN[((1-X)^(-n+1))-1)/(-n+1)*t] {1/min}, ,9 6,9 8,1,1 2,1 4,1 6,1 8,11 y = x + 18,285 R 2 =,9967 Ao 181, KJ/mol ,73 1/min 1/T {1/K} Velocidad de calentamiento 4 K/min W inicial 9,621 mg Ao 11,8678 KJ/mol 894, /min 33
48 LN[((1-X)^(-n+1))-1)/(-n+1)*t] {1/min},8-1,9,1,11,12, /T {1/K} y = x + 9,943 R 2 =,97 Graficando m * R E a = y 1 CALCULO DE LOS PARAMETROS CINETICO PARA ORDEN dx ln dt A = ln A RT dx A 1 ln vs. obtenemos una línea de la forma y = mx + b, entonces, dt T b A = e Velocidad de calentamiento 8 K/min W inicial 1,967 mg,1,12,14,16,18,11,112,114,116-1 LN(dX/dt) [1/min] y = -228x + 21,228 R 2 =, ,5592 KJ/mol Ao 1.65E+9 1/min /T [1/K] Velocidad de calentamiento 1 K/min W inicial 14,434 mg 34
49 LN(dX/dt) [1/min] -,5,98,1,12,14,16,18,11, ,5-2 -2,5-3 -3,5-4 -4,5-5 1/T [1/K] y = x + 19,641 R 2 =,9878 Ao 18, KJ/mol /min Velocidad de calentamiento 12 K/min W inicial 11,3 mg,95,1,15,11,115-1 LN(dX/dt) [1/min] y = x + 21,587 R 2 =,9947 Ao 195,19692 KJ/mol /min /T [1/K] Velocidad de calentamiento 25 K/min W inicial 7,475 mg Ao 197, KJ/mol /min 35
50 LN(dX/dt) [1/min] -,5,9,95,1,15, ,5-2 -2,5-3 -3,5-4 -4,5-5 1/T [1/K] y = x + 21,126 R 2 =,9864 Velocidad de calentamiento 4 K/min W inicial 9,621 mg,85-1,95,15,115,125 LN(dX/dt) [1/min] y = x + 15,616 R 2 =,9673 Ao 151,61414 KJ/mol 65269,14 1/min /T [1/K] CALCULO DE LOS PARAMETROS CINETICO PARA ORDEN 1 1 X 1 ln ln = ln A t X 1 RT 1 Graficando 1 X 1 ln ln vs. obtenemos una línea de la forma y = mx + b, t 1 X T m * R b entonces, E a = y A = e 1 36
51 Velocidad de calentamiento 8 K/min W inicial 1,967 mg LN((-1/t)*LN(1-X)) [1/min],1,1,1,11,11,11,11,11, y = x + 21,819 R 2 =,9978 Ao 22, KJ/mol /min -7 1/T [1/K] Velocidad de calentamiento 1 K/min W inicial 14,434 mg LN((-1/t)*LN(1-X)) [1/min],98,1,12,14,16,18,11, y = x + 19,662 R 2 =, Ao 186,3464 KJ/mol /min -6 1/T [1/K] Velocidad de calentamiento 12 K/min W inicial 11,3 mg Ao 188, KJ/mol /min 37
52 LN((-1/t)*LN(1-X)) [1/min],95,1,15,11, y = x + 19,533 R 2 =, /T [1/K] Velocidad de calentamiento 25 K/min W inicial 7,475 mg LN((-1/t)*LN(1-X)) [1/min],9,95,1,15, y = -2469x + 21,229 R 2 =,9864 Ao 24, KJ/mol /min -6 1/T [1/K] Velocidad de calentamiento 4 K/min W inicial 9,621 mg Ao 13,459 KJ/mol ,674 1/min 38
53 LN((-1/t)*LN(1-X)) [1/min],8-1,9,1,11,12, y = x + 11,845 R 2 =, /T [1/K] CALCULO DE LOS PARAMETROS CINETICO PARA ORDEN 2 ln ( ) ( n+ 1 1 X ) 1 = ln A ( n + 1) t RT Graficando entonces, ( ) ( + X n 1 1 ) ( n + 1) t ln m * R E a = y 1 1 b A = e vs. T 1 obtenemos una línea de la forma y = mx + b, Velocidad de calentamiento 8 K/min W inicial 1,967 mg LN[((1-X)^(-n+1))-1)/(-n+1)*t] {1/min},1, ,1 4,1 6,1 8,11,11 2,11 4,11 6 y = x + 27,233 R 2 =,9825 Ao 242, KJ/mol 6,71648E+11 1/min 1/T {1/K} 39
54 Velocidad de calentamiento 1 K/min W inicial 14,434 mg LN[((1-X)^(-n+1))-1)/(-n+1)*t] {1/min},98,1,12,14,16,18,11, /T {1/K} y = x + 26,426 R 2 =,9599 Ao 237,9511 KJ/mol 2,99686E+11 1/min Velocidad de calentamiento 12 K/min W inicial 11,3 mg LN[((1-X)^(-n+1))-1)/(-n+1)*t] {1/min},95,1,15,11, /T {1/K} y = -2652x + 23,783 R 2 =,977 Ao 22,48728 KJ/mol /min Velocidad de calentamiento 25 K/min W inicial 7,475 mg Ao 216,5797 KJ/mol /min 4
55 LN[((1-X)^(-n+1))-1)/(-n+1)*t] {1/min}, ,9 6,9 8,1,1 2,1 4,1 6,1 8,11 y = -265x + 22,788 R 2 =,9813 1/T {1/K} Velocidad de calentamiento 4 K/min W inicial 9,621 mg LN[((1-X)^(-n+1))-1)/(-n+1)*t] {1/min},8-1,9,1,11,12, /T {1/K} y = x + 1,734 R 2 =,8754 Ao 121,92481 KJ/mol 45889, /min 41
56 ANEXO B: MODELO MATEMATICO DE KISSINGER A Rn ln β = T ln 2 E m ( 1 X ) a n 1 RT m Graficando m * R E a = 1 ln β 2 T m vs. T 1 obtenemos una línea de la forma y = mx + b, entonces, BETA K/min Tm K Ln (B/Tm^2) 1/Tm 1/K ,671226, ,589215, , , , , , ,97276 LN(BETA/Tm^2) [1/K*min] -1-1,2,96,98,1,12,14-1,4-1,6-1, ,2-11,4-11,6-11,8-12 y = -2473x + 13,654 R 2 =,8435 1/T [1/K] 25,6522 KJ/mol 42
57 ANEXO C: MODELO MATEMATICO DE COAST ( X ) F A R ln = ln T E 2 β a RT F 1 ( X ) = 1 ( 1 X ) 3 ( X ) F Graficando ln 2 T m * R entonces, E a = y 1 1 vs. obtenemos una línea de la forma T A = m ( e E β ) R a y = mx + b, Velocidad de calentamiento 8 K/min W inicial 1,967 mg LN(F(X)/T^2) [1/K^2] -2,1,1,1,11,11,11,11,11, /T [1/K] y = x + 13,995 R 2 =,9998 A 235, KJ/mol /min Velocidad de calentamiento 1 K/min W inicial 14,434 mg A 233, KJ/mol /min 43
58 LN(F(X)/T^2) [1/K^2],98-2,1,12,14,16,18,11, /T [1/K] y = -2871x + 13,5 R 2 =,9998 Velocidad de calentamiento 12 K/min W inicial 11,3 mg LN(F(X)/T^2) [1/K^2],95-2,1,15,11, /T [1/K] y = x + 9,7481 R 2 =,9982 A 27, KJ/mol /min Velocidad de calentamiento 25 K/min W inicial 7,475 mg A 231, KJ/mol ,7 1/min 44
59 LN(F(X)/T^2) [1/K^2] -2,9,95,1,15, /T [1/K] y = x + 11,21 R 2 =,9993 Velocidad de calentamiento 4 K/min W inicial 9,621 mg,8,9,1,11,12,13 LN(F(X)/T^2) [1/K^2] y = x -,8731 R 2 =,9298 A 131,36954 KJ/mol 159, /min -25 1/T [1/K] 45
1. INTRODUCCIÓN 1.1 INGENIERÍA
 1. INTRODUCCIÓN 1.1 INGENIERÍA Es difícil dar una explicación de ingeniería en pocas palabras, pues se puede decir que la ingeniería comenzó con el hombre mismo, pero se puede intentar dar un bosquejo
1. INTRODUCCIÓN 1.1 INGENIERÍA Es difícil dar una explicación de ingeniería en pocas palabras, pues se puede decir que la ingeniería comenzó con el hombre mismo, pero se puede intentar dar un bosquejo
ESTADOS DE AGREGACIÓN DE LA MATERIA
 ESADOS DE AGREGACIÓN DE LA MAERIA. Propiedades generales de la materia La materia es todo aquello que tiene masa y volumen. La masa se define como la cantidad de materia de un cuerpo. Se mide en kg. El
ESADOS DE AGREGACIÓN DE LA MAERIA. Propiedades generales de la materia La materia es todo aquello que tiene masa y volumen. La masa se define como la cantidad de materia de un cuerpo. Se mide en kg. El
CAPITULO 4 FLUIDIZACIÓN EMPLEANDO VAPOR SOBRECALENTADO. Potter [10], ha demostrado en una planta piloto que materiales sensibles a la
![CAPITULO 4 FLUIDIZACIÓN EMPLEANDO VAPOR SOBRECALENTADO. Potter [10], ha demostrado en una planta piloto que materiales sensibles a la CAPITULO 4 FLUIDIZACIÓN EMPLEANDO VAPOR SOBRECALENTADO. Potter [10], ha demostrado en una planta piloto que materiales sensibles a la](/thumbs/26/7800050.jpg) 34 CAPITULO 4 FLUIDIZACIÓN EMPLEANDO VAPOR SOBRECALENTADO 4.1 Lecho fluidizado con vapor sobrecalentado Potter [10], ha demostrado en una planta piloto que materiales sensibles a la temperatura pueden
34 CAPITULO 4 FLUIDIZACIÓN EMPLEANDO VAPOR SOBRECALENTADO 4.1 Lecho fluidizado con vapor sobrecalentado Potter [10], ha demostrado en una planta piloto que materiales sensibles a la temperatura pueden
Unidad IV: Cinética química
 63 Unidad IV: Cinética química El objetivo de la cinética química es el estudio de las velocidades de las reacciones químicas y de los factores de los que dependen dichas velocidades. De estos factores,
63 Unidad IV: Cinética química El objetivo de la cinética química es el estudio de las velocidades de las reacciones químicas y de los factores de los que dependen dichas velocidades. De estos factores,
Determinación del equivalente eléctrico del calor
 Determinación del equivalente eléctrico del calor Julieta Romani Paula Quiroga María G. Larreguy y María Paz Frigerio julietaromani@hotmail.com comquir@ciudad.com.ar merigl@yahoo.com.ar mapaz@vlb.com.ar
Determinación del equivalente eléctrico del calor Julieta Romani Paula Quiroga María G. Larreguy y María Paz Frigerio julietaromani@hotmail.com comquir@ciudad.com.ar merigl@yahoo.com.ar mapaz@vlb.com.ar
LABORATORIO DE MECÁNICA LEY DE HOOKE
 No 6 LABORATORIO DE MECÁNICA LEY DE HOOKE DEPARTAMENTO DE FÍSICA Y GEOLOGÍA UNIVERSIDAD DE PAMPLONA FACULTAD DE CIENCIAS BÁSICAS Objetivos Objetivo General: Estudiar experimentalmente el comportamiento
No 6 LABORATORIO DE MECÁNICA LEY DE HOOKE DEPARTAMENTO DE FÍSICA Y GEOLOGÍA UNIVERSIDAD DE PAMPLONA FACULTAD DE CIENCIAS BÁSICAS Objetivos Objetivo General: Estudiar experimentalmente el comportamiento
DRAFT. Trabajo, Calor y Primer Principio de la Termodinámica.
 DRAFT Trabajo, Calor y Primer Principio de la Termodinámica. J.V. Alvarez Departmento de Fisica de la Materia Condensada, Universidad Autonoma de Madrid. 28049 Madrid, Spain. (Dated: October 10, 2007)
DRAFT Trabajo, Calor y Primer Principio de la Termodinámica. J.V. Alvarez Departmento de Fisica de la Materia Condensada, Universidad Autonoma de Madrid. 28049 Madrid, Spain. (Dated: October 10, 2007)
TRABAJO PRACTICO ESTERILIZACION
 TRABAJO PRACTICO ESTERILIZACION Introducción La esterilización es un proceso de suma importancia para la industria de las fermentaciones. Para comenzar la explicación de este tema es conveniente dejar
TRABAJO PRACTICO ESTERILIZACION Introducción La esterilización es un proceso de suma importancia para la industria de las fermentaciones. Para comenzar la explicación de este tema es conveniente dejar
Estudiar experimentalmente el comportamiento de resortes y bandas elásticas.
 No 6 LABORATORIO DE FISICA PARA LAS CIENCIAS DE LA VIDA DEPARTAMENTO DE FISICA Y GEOLOGIA UNIVERSIDAD DE PAMPLONA FACULTAD DE CIENCIAS BÁSICAS Objetivos Estudiar experimentalmente el comportamiento de
No 6 LABORATORIO DE FISICA PARA LAS CIENCIAS DE LA VIDA DEPARTAMENTO DE FISICA Y GEOLOGIA UNIVERSIDAD DE PAMPLONA FACULTAD DE CIENCIAS BÁSICAS Objetivos Estudiar experimentalmente el comportamiento de
Caída de Presión en Tubos de Diferente Diámetro
 Caída de Presión en Tubos de Diferente Diámetro Laboratorio de Operaciones Unitarias Equipo 4 Primavera 2008 México D.F., 12 de marzo de 2008 Alumnos: Arlette Mayela Canut Noval arlettecanut@hotmail.com
Caída de Presión en Tubos de Diferente Diámetro Laboratorio de Operaciones Unitarias Equipo 4 Primavera 2008 México D.F., 12 de marzo de 2008 Alumnos: Arlette Mayela Canut Noval arlettecanut@hotmail.com
Circuito RC, Respuesta a la frecuencia.
 Circuito RC, Respuesta a la frecuencia. A.M. Velasco (133384) J.P. Soler (133380) O.A. Botina (13368) Departamento de física, facultad de ciencias, Universidad Nacional de Colombia Resumen. Se armó un
Circuito RC, Respuesta a la frecuencia. A.M. Velasco (133384) J.P. Soler (133380) O.A. Botina (13368) Departamento de física, facultad de ciencias, Universidad Nacional de Colombia Resumen. Se armó un
Circuito RL, Respuesta a la frecuencia.
 Circuito RL, Respuesta a la frecuencia. A.M. Velasco (133384) J.P. Soler (133380) O.A. Botina (133268) Departamento de física, facultad de ciencias, Universidad Nacional de Colombia Resumen. Se estudia
Circuito RL, Respuesta a la frecuencia. A.M. Velasco (133384) J.P. Soler (133380) O.A. Botina (133268) Departamento de física, facultad de ciencias, Universidad Nacional de Colombia Resumen. Se estudia
Potenciales de optimización de reacciones de laboratorio -
 Potenciales de optimización de reacciones de laboratorio - Reglas básicas para síntesis sostenibles En el curso de la investigación sobre algunas reaccione incluidas en NOP se han podido identificar algunos
Potenciales de optimización de reacciones de laboratorio - Reglas básicas para síntesis sostenibles En el curso de la investigación sobre algunas reaccione incluidas en NOP se han podido identificar algunos
Covarianza y coeficiente de correlación
 Covarianza y coeficiente de correlación Cuando analizábamos las variables unidimensionales considerábamos, entre otras medidas importantes, la media y la varianza. Ahora hemos visto que estas medidas también
Covarianza y coeficiente de correlación Cuando analizábamos las variables unidimensionales considerábamos, entre otras medidas importantes, la media y la varianza. Ahora hemos visto que estas medidas también
III. DIFUSION EN SOLIDOS
 Metalografía y Tratamientos Térmicos III - 1 - III. DIFUSION EN SOLIDOS III.1. Velocidad de procesos en sólidos Muchos procesos de producción y aplicaciones en materiales de ingeniería están relacionados
Metalografía y Tratamientos Térmicos III - 1 - III. DIFUSION EN SOLIDOS III.1. Velocidad de procesos en sólidos Muchos procesos de producción y aplicaciones en materiales de ingeniería están relacionados
Circuitos RLC resonantes acoplados
 Pág. 1 Circuitos RLC resonantes acoplados Cano, Ramiro Díaz, Federico Trebisacce, Carlos cramirocano@.com.ar Facil7@hotmail.com trevicjt@hotmail.com Universidad Favaloro, Facultad de Ingeniería Bs. As.
Pág. 1 Circuitos RLC resonantes acoplados Cano, Ramiro Díaz, Federico Trebisacce, Carlos cramirocano@.com.ar Facil7@hotmail.com trevicjt@hotmail.com Universidad Favaloro, Facultad de Ingeniería Bs. As.
A ÁLISIS ESTADÍSTICO DE LA DEGRADACIÓ TÉRMICA DEL POLIURETA O RESUME
 X Congreso Galego de Estatística e Investigación de Operacións Pontevedra, 3 4 5 de novembro de 2011 A ÁLISIS ESTADÍSTICO DE LA DEGRADACIÓ TÉRMICA DEL POLIURETA O Javier Tarrío-Saavedra 1, Fernando Barbadillo
X Congreso Galego de Estatística e Investigación de Operacións Pontevedra, 3 4 5 de novembro de 2011 A ÁLISIS ESTADÍSTICO DE LA DEGRADACIÓ TÉRMICA DEL POLIURETA O Javier Tarrío-Saavedra 1, Fernando Barbadillo
2. SISTEMAS LINEALES DE PRIMER ORDEN (I)
 2. SISTEMAS LINEALES DE PRIMER ORDEN (I) 2.1 INTRODUCCIÓN DOMINIO TIEMPO Un sistema lineal de primer orden con una variable de entrada, " x ( ", y una variable salida, " y( " se modela matemáticamente
2. SISTEMAS LINEALES DE PRIMER ORDEN (I) 2.1 INTRODUCCIÓN DOMINIO TIEMPO Un sistema lineal de primer orden con una variable de entrada, " x ( ", y una variable salida, " y( " se modela matemáticamente
Los gases combustibles pueden servir para accionar motores diesel, para producir electricidad, o para mover vehículos.
 PIRÓLISIS 1. Definición La pirólisis se define como un proceso termoquímico mediante el cual el material orgánico de los subproductos sólidos se descompone por la acción del calor, en una atmósfera deficiente
PIRÓLISIS 1. Definición La pirólisis se define como un proceso termoquímico mediante el cual el material orgánico de los subproductos sólidos se descompone por la acción del calor, en una atmósfera deficiente
ENERGÍA ELÉCTRICA. Central térmica
 ENERGÍA ELÉCTRICA. Central térmica La central térmica de Castellón (Iberdrola) consta de dos bloques de y 5 MW de energía eléctrica, y utiliza como combustible gas natural, procedente de Argelia. Sabiendo
ENERGÍA ELÉCTRICA. Central térmica La central térmica de Castellón (Iberdrola) consta de dos bloques de y 5 MW de energía eléctrica, y utiliza como combustible gas natural, procedente de Argelia. Sabiendo
TEMA 1 Conceptos básicos de la termodinámica
 Bases Físicas y Químicas del Medio Ambiente TEMA 1 Conceptos básicos de la termodinámica La termodinámica es el estudio de la transformación de una forma de energía en otra y del intercambio de energía
Bases Físicas y Químicas del Medio Ambiente TEMA 1 Conceptos básicos de la termodinámica La termodinámica es el estudio de la transformación de una forma de energía en otra y del intercambio de energía
DESARROLLO DE UNA HERAMIENTA COMPUTACIONAL PARA EL DIMENSIONAMIENTO DE GASODUCTOS Y REDES DE DISTRIBUCIÓN DE GAS
 DESARROLLO DE UNA HERAMIENTA COMPUTACIONAL PARA EL DIMENSIONAMIENTO DE GASODUCTOS Y REDES DE DISTRIBUCIÓN DE GAS PROPONENTES GERMÁN JOAQUÍN LÓPEZ FORERO Ingeniero Químico de la Universidad Nacional de
DESARROLLO DE UNA HERAMIENTA COMPUTACIONAL PARA EL DIMENSIONAMIENTO DE GASODUCTOS Y REDES DE DISTRIBUCIÓN DE GAS PROPONENTES GERMÁN JOAQUÍN LÓPEZ FORERO Ingeniero Químico de la Universidad Nacional de
Cifras significativas e incertidumbre en las mediciones
 Unidades de medición Cifras significativas e incertidumbre en las mediciones Todas las mediciones constan de una unidad que nos indica lo que fue medido y un número que indica cuántas de esas unidades
Unidades de medición Cifras significativas e incertidumbre en las mediciones Todas las mediciones constan de una unidad que nos indica lo que fue medido y un número que indica cuántas de esas unidades
5. RESULTADOS. 5.1 Resultados obtenidos de Visual Basic.
 5. RESULTADOS. 5.1 Resultados obtenidos de Visual Basic. Para poder obtener los resultados que arrojan las ecuaciones programadas de sobrepresión, es necesaria la creación de una base de datos que contenga
5. RESULTADOS. 5.1 Resultados obtenidos de Visual Basic. Para poder obtener los resultados que arrojan las ecuaciones programadas de sobrepresión, es necesaria la creación de una base de datos que contenga
Capítulo 10. Estudio de un caso con parámetros reales: acuífero de Borden
 Capítulo 10. Estudio de un caso con parámetros reales: acuífero de Borden Tras la realización de muchos casos sintéticos y un estudio detallado de todos los parámetros que intervienen en el problema y
Capítulo 10. Estudio de un caso con parámetros reales: acuífero de Borden Tras la realización de muchos casos sintéticos y un estudio detallado de todos los parámetros que intervienen en el problema y
HOJA INFORMATIVA DE HORTICULTURA
 HOJA INFORMATIVA DE HORTICULTURA COSECHA Y POST-COSECHA: Importancia y fundamentos Alejandro R. Puerta Ing. Agr. Agosto 2002 La cosecha y post - cosecha es una etapa de fundamental importancia en el proceso
HOJA INFORMATIVA DE HORTICULTURA COSECHA Y POST-COSECHA: Importancia y fundamentos Alejandro R. Puerta Ing. Agr. Agosto 2002 La cosecha y post - cosecha es una etapa de fundamental importancia en el proceso
Estudio de polimorfismo en drogas farmacéuticas. Daniel Vega
 Estudio de polimorfismo en drogas farmacéuticas. Daniel Vega Departamento Física de la Materia Condensada Comisión Nacional de Energía Atómica Escuela de Ciencia y Tecnología - UNSAM Polimorfismo afecta
Estudio de polimorfismo en drogas farmacéuticas. Daniel Vega Departamento Física de la Materia Condensada Comisión Nacional de Energía Atómica Escuela de Ciencia y Tecnología - UNSAM Polimorfismo afecta
Control Estadístico del Proceso. Ing. Claudia Salguero Ing. Alvaro Díaz
 Control Estadístico del Proceso Ing. Claudia Salguero Ing. Alvaro Díaz Control Estadístico del Proceso Es un conjunto de herramientas estadísticas que permiten recopilar, estudiar y analizar la información
Control Estadístico del Proceso Ing. Claudia Salguero Ing. Alvaro Díaz Control Estadístico del Proceso Es un conjunto de herramientas estadísticas que permiten recopilar, estudiar y analizar la información
FUNDAMENTOS DE DISEÑO DE REACTORES 3.1 ECUACIÓN GENERAL DE BALANCE DE MASA
 C A P Í T U L O 3 FUNDAMENTOS DE DISEÑO DE REACTORES 3.1 ECUACIÓN GENERAL DE BALANCE DE MASA Todos los procesos de tratamiento de aguas residuales se pueden analizar por medio de una caja negra y balances
C A P Í T U L O 3 FUNDAMENTOS DE DISEÑO DE REACTORES 3.1 ECUACIÓN GENERAL DE BALANCE DE MASA Todos los procesos de tratamiento de aguas residuales se pueden analizar por medio de una caja negra y balances
Física de los Procesos Biológicos Curso 2005/6
 Bibliografía: ísica, Kane, Tema 8 ísica de los Procesos Biológicos Curso 2005/6 Grupo 3 TEMA 2 BIOMECÁNICA 2.1 SÓIDO DEORMABE Parte 1 Introducción Vamos a estudiar como los materiales se deforman debido
Bibliografía: ísica, Kane, Tema 8 ísica de los Procesos Biológicos Curso 2005/6 Grupo 3 TEMA 2 BIOMECÁNICA 2.1 SÓIDO DEORMABE Parte 1 Introducción Vamos a estudiar como los materiales se deforman debido
Completar: Un sistema material homogéneo constituido por un solo componente se llama.
 IES Menéndez Tolosa 3º ESO (Física y Química) 1 Completar: Un sistema material homogéneo constituido por un solo componente se llama. Un sistema material homogéneo formado por dos o más componentes se
IES Menéndez Tolosa 3º ESO (Física y Química) 1 Completar: Un sistema material homogéneo constituido por un solo componente se llama. Un sistema material homogéneo formado por dos o más componentes se
CAPITULO 5. PROCESO DE SECADO. El secado se describe como un proceso de eliminación de substancias volátiles (humedad)
 CAPITULO 5. PROCESO DE SECADO. 5.1 Descripción general del proceso de secado. El secado se describe como un proceso de eliminación de substancias volátiles (humedad) para producir un producto sólido y
CAPITULO 5. PROCESO DE SECADO. 5.1 Descripción general del proceso de secado. El secado se describe como un proceso de eliminación de substancias volátiles (humedad) para producir un producto sólido y
Introducción a los sistemas de control
 Introducción a los sistemas de control Sistema Un sistema es una combinación de componentes que actúan juntos y realizan un objetivo determinado A un sistema se le puede considerar como una caja negra
Introducción a los sistemas de control Sistema Un sistema es una combinación de componentes que actúan juntos y realizan un objetivo determinado A un sistema se le puede considerar como una caja negra
CAPITULO 4 FLUIDIZACIÓN EMPLEANDO VAPOR SOBRECALENTADO. 4.1 Comparación del proceso de sacado con vapor sobrecalentado y aire.
 CAPITULO 4 FLUIDIZACIÓN EMPLEANDO VAPOR SOBRECALENTADO. 4.1 Comparación del proceso de sacado con vapor sobrecalentado y aire. El proceso de secado es una de las operaciones más importantes en la industria
CAPITULO 4 FLUIDIZACIÓN EMPLEANDO VAPOR SOBRECALENTADO. 4.1 Comparación del proceso de sacado con vapor sobrecalentado y aire. El proceso de secado es una de las operaciones más importantes en la industria
ESTUDIO PRELIMINAR DE ALGUNOS FACTORES INFLUYENTES EN EL RENDIMIENTO ACADÉMICO DE ALUMNOS DEL GRUPO EXECUTIVE FISIOTERAPIA
 ESTUDIO PRELIMINAR DE ALGUNOS FACTORES INFLUYENTES EN EL RENDIMIENTO ACADÉMICO DE ALUMNOS DEL GRUPO EXECUTIVE FISIOTERAPIA Autores: Noemí Díaz Matas; Carlos Martín Saborido; Raquel Díaz-Meco Conde; Silvia
ESTUDIO PRELIMINAR DE ALGUNOS FACTORES INFLUYENTES EN EL RENDIMIENTO ACADÉMICO DE ALUMNOS DEL GRUPO EXECUTIVE FISIOTERAPIA Autores: Noemí Díaz Matas; Carlos Martín Saborido; Raquel Díaz-Meco Conde; Silvia
SÍNTESIS Y PERSPECTIVAS
 SÍNTESIS Y PERSPECTIVAS Los invitamos a observar, a identificar problemas, pero al mismo tiempo a buscar oportunidades de mejoras en sus empresas. REVISIÓN DE CONCEPTOS. Esta es la última clase del curso.
SÍNTESIS Y PERSPECTIVAS Los invitamos a observar, a identificar problemas, pero al mismo tiempo a buscar oportunidades de mejoras en sus empresas. REVISIÓN DE CONCEPTOS. Esta es la última clase del curso.
Aproximación local. Plano tangente. Derivadas parciales.
 Univ. de Alcalá de Henares Ingeniería de Telecomunicación Cálculo. Segundo parcial. Curso 004-005 Aproximación local. Plano tangente. Derivadas parciales. 1. Plano tangente 1.1. El problema de la aproximación
Univ. de Alcalá de Henares Ingeniería de Telecomunicación Cálculo. Segundo parcial. Curso 004-005 Aproximación local. Plano tangente. Derivadas parciales. 1. Plano tangente 1.1. El problema de la aproximación
Dirección de Planificación Universitaria Dirección de Planificación Universitaria 0819-07289 Panamá, Rep. de Panamá 0819-07289 Panamá, Rep.
 Comparación de las tasas de aprobación, reprobación, abandono y costo estudiante de dos cohortes en carreras de Licenciatura en Ingeniería en la Universidad Tecnológica de Panamá Luzmelia Bernal Caballero
Comparación de las tasas de aprobación, reprobación, abandono y costo estudiante de dos cohortes en carreras de Licenciatura en Ingeniería en la Universidad Tecnológica de Panamá Luzmelia Bernal Caballero
MÓDULO 3 CURVAS DE INFILTRACIÓN
 MÓDULO 3 CURVAS DE INFILTRACIÓN Autores: Dr. Ing. Roberto Pizarro T. Ing. Juan Pablo Flores V. Ing. Claudia Sangüesa P. Ing. Enzo Martínez A. 1. INTRODUCCIÓN La infiltración el agua posee un rol fundamental
MÓDULO 3 CURVAS DE INFILTRACIÓN Autores: Dr. Ing. Roberto Pizarro T. Ing. Juan Pablo Flores V. Ing. Claudia Sangüesa P. Ing. Enzo Martínez A. 1. INTRODUCCIÓN La infiltración el agua posee un rol fundamental
INTRODUCCIÓN A LA TERMODINÁMICA QUÍMICA. La mecánica cuántica estudia la estructura atómica, los enlaces en moléculas y la espectroscopia.
 INTRODUCCIÓN A LA TERMODINÁMICA QUÍMICA 1. Qué es la Química Física? "La química física estudia los principios que gobiernan las propiedades el comportamiento de los sistemas químicos" El estudio de los
INTRODUCCIÓN A LA TERMODINÁMICA QUÍMICA 1. Qué es la Química Física? "La química física estudia los principios que gobiernan las propiedades el comportamiento de los sistemas químicos" El estudio de los
Capítulo 5. Estudio de la influencia de la relajación sobre el proceso de la cristalización eutéctica
 Capítulo 5 Estudio de la influencia de la relajación sobre el proceso de la cristalización eutéctica Estudio de la influencia de la relajación sobre el proceso de la cristalización eutectica 5.1. Tratamiento
Capítulo 5 Estudio de la influencia de la relajación sobre el proceso de la cristalización eutéctica Estudio de la influencia de la relajación sobre el proceso de la cristalización eutectica 5.1. Tratamiento
SEDO: SOFTWARE EDUCATIVO DE MATEMÁTICA NUMÉRICA. Lic. Maikel León Espinosa. mle@uclv.edu.cu
 EDU082 Resumen SEDO: SOFTWARE EDUCATIVO DE MATEMÁTICA NUMÉRICA Lic. Maikel León Espinosa mle@uclv.edu.cu Departamento de Ciencia de la Computación Universidad Central Marta Abreu de Las Villas Carretera
EDU082 Resumen SEDO: SOFTWARE EDUCATIVO DE MATEMÁTICA NUMÉRICA Lic. Maikel León Espinosa mle@uclv.edu.cu Departamento de Ciencia de la Computación Universidad Central Marta Abreu de Las Villas Carretera
Modificación y parametrización del modulo de Solicitudes (Request) en el ERP/CRM Compiere.
 UNIVERSIDAD DE CARABOBO FACULTAD DE CIENCIA Y TECNOLOGÍA DIRECCION DE EXTENSION COORDINACION DE PASANTIAS Modificación y parametrización del modulo de Solicitudes (Request) en el ERP/CRM Compiere. Pasante:
UNIVERSIDAD DE CARABOBO FACULTAD DE CIENCIA Y TECNOLOGÍA DIRECCION DE EXTENSION COORDINACION DE PASANTIAS Modificación y parametrización del modulo de Solicitudes (Request) en el ERP/CRM Compiere. Pasante:
Lubricantes a base de Polyalkylene Glycol (PAG) usados con HFC134a (R134a)
 LUBRICANTES SINTÉTICOS PARA SISTEMAS DE AIRE ACONDICIONADO ( SL AIR FREEZE LUBRICANT A & B ) Introducción En los países industrializados, la producción del refrigerante CFC12 (R12) cesó desde 1995 debido
LUBRICANTES SINTÉTICOS PARA SISTEMAS DE AIRE ACONDICIONADO ( SL AIR FREEZE LUBRICANT A & B ) Introducción En los países industrializados, la producción del refrigerante CFC12 (R12) cesó desde 1995 debido
CAPITULO I. Introducción. En la actualidad, las empresas están tomando un papel activo en cuanto al uso de sistemas y
 CAPITULO I Introducción 1.1 Introducción En la actualidad, las empresas están tomando un papel activo en cuanto al uso de sistemas y redes computacionales. La tecnología ha ido evolucionando constantemente
CAPITULO I Introducción 1.1 Introducción En la actualidad, las empresas están tomando un papel activo en cuanto al uso de sistemas y redes computacionales. La tecnología ha ido evolucionando constantemente
UNIDAD 2. Contenido de Humedad del Agua en el Suelo
 UNIDAD 2. Contenido de Humedad del Agua en el Suelo CONTENIDO Índice de Ilustraciones y Tablas... 2 2.1. Contenido de Humedad del Suelo... 3 2.2. Retención de agua en el suelo... 6 2.3. Determinación del
UNIDAD 2. Contenido de Humedad del Agua en el Suelo CONTENIDO Índice de Ilustraciones y Tablas... 2 2.1. Contenido de Humedad del Suelo... 3 2.2. Retención de agua en el suelo... 6 2.3. Determinación del
Capítulo 2 Tratamiento Contable de los Impuestos. 2.1 Normas Internacionales de Contabilidad
 Capítulo 2 Tratamiento Contable de los Impuestos 2.1 Normas Internacionales de Contabilidad Las Normas Internacionales de Contabilidad (NIC) o International Financial Reporting Standard (IFRS) son los
Capítulo 2 Tratamiento Contable de los Impuestos 2.1 Normas Internacionales de Contabilidad Las Normas Internacionales de Contabilidad (NIC) o International Financial Reporting Standard (IFRS) son los
No hay resorte que oscile cien años...
 No hay resorte que oscile cien años... María Paula Coluccio y Patricia Picardo Laboratorio I de Física para Biólogos y Geólogos Depto. de Física, FCEyN, UBA - 1999 Resumen: En el presente trabajo nos proponemos
No hay resorte que oscile cien años... María Paula Coluccio y Patricia Picardo Laboratorio I de Física para Biólogos y Geólogos Depto. de Física, FCEyN, UBA - 1999 Resumen: En el presente trabajo nos proponemos
CAPÍTULO 5. CONCLUSIONES
 CAPÍTULO 5. CONCLUSIONES Este trabajo ha tenido como objetivos el análisis y modelado del proceso de purificación de estireno mediante adsorción en alúmina y el análisis del cambio de escala del sistema,
CAPÍTULO 5. CONCLUSIONES Este trabajo ha tenido como objetivos el análisis y modelado del proceso de purificación de estireno mediante adsorción en alúmina y el análisis del cambio de escala del sistema,
TEMA 5 ESTUDIOS CORRELACIONALES.
 TEMA 5 ESTUDIOS CORRELACIONALES. 1. INTRODUCCIÓN. 2. CONCEPTO DE CORRELACIÓN. 3. CASOS EN LOS QUE SE UTILIZA LA INVESTIGACIÓN CORRELACIONAL. 4. LIMITACIONES DE LOS ESTUDIOS CORRELACIONALES 1 1. INTRODUCCIÓN.
TEMA 5 ESTUDIOS CORRELACIONALES. 1. INTRODUCCIÓN. 2. CONCEPTO DE CORRELACIÓN. 3. CASOS EN LOS QUE SE UTILIZA LA INVESTIGACIÓN CORRELACIONAL. 4. LIMITACIONES DE LOS ESTUDIOS CORRELACIONALES 1 1. INTRODUCCIÓN.
LOS RETOS DE LA ENSEÑANZA EN LA INGENIERÍA 1
 LOS RETOS DE LA ENSEÑANZA EN LA INGENIERÍA 1 Horacio Ramírez de Alba* En este escrito se presenta un panorama de la profesión de la ingeniería y su relación con el desarrollo del país, y a partir de ello
LOS RETOS DE LA ENSEÑANZA EN LA INGENIERÍA 1 Horacio Ramírez de Alba* En este escrito se presenta un panorama de la profesión de la ingeniería y su relación con el desarrollo del país, y a partir de ello
ANÁLISIS TÉRMICO. Consultoría de Calidad y Laboratorio S.L. RPS-Qualitas
 ANÁLISIS TÉRMICO Introducción. El término Análisis Térmico engloba una serie de técnicas en las cuales, algún parámetro físico del sistema es medido de manera continua en función de la temperatura, mientras
ANÁLISIS TÉRMICO Introducción. El término Análisis Térmico engloba una serie de técnicas en las cuales, algún parámetro físico del sistema es medido de manera continua en función de la temperatura, mientras
ENERGÍA INTERNA PARA GASES NO IDEALES.
 DEPARTAMENTO DE FISICA UNIERSIDAD DE SANTIAGO DE CHILE ENERGÍA INTERNA PARA GASES NO IDEALES. En el caso de los gases ideales o cualquier cuerpo en fase no gaseosa la energía interna es función de la temperatura
DEPARTAMENTO DE FISICA UNIERSIDAD DE SANTIAGO DE CHILE ENERGÍA INTERNA PARA GASES NO IDEALES. En el caso de los gases ideales o cualquier cuerpo en fase no gaseosa la energía interna es función de la temperatura
El plan de clase sobre el efecto invernadero y el sistema climático global
 Para los docentes El plan de clase sobre el efecto invernadero y el sistema climático global El siguiente plan de clase se diseñó para ser usado con la sección de Cambio Climático del sitio web La evidencia
Para los docentes El plan de clase sobre el efecto invernadero y el sistema climático global El siguiente plan de clase se diseñó para ser usado con la sección de Cambio Climático del sitio web La evidencia
CÁLCULO DEL CAUDAL DEL CIRCUITO PRIMARIO UTILIZANDO LA CAÍDA DE PRESIÓN DEL GENERADOR DE VAPOR DE LA CENTRAL NUCLEAR ATUCHA 2
 CÁLCULO DEL CAUDAL DEL CIRCUITO PRIMARIO UTILIZANDO LA CAÍDA DE PRESIÓN DEL GENERADOR DE VAPOR DE LA CENTRAL NUCLEAR ATUCHA 2 Luis Lencina Hugo Ballesteros 2014 ESSS CONFERENCE AND USER MEETING INTRODUCCIÓN
CÁLCULO DEL CAUDAL DEL CIRCUITO PRIMARIO UTILIZANDO LA CAÍDA DE PRESIÓN DEL GENERADOR DE VAPOR DE LA CENTRAL NUCLEAR ATUCHA 2 Luis Lencina Hugo Ballesteros 2014 ESSS CONFERENCE AND USER MEETING INTRODUCCIÓN
1. Fundamento teórico
 1 1. Fundamento teórico Los métodos espectroscópicos atómicos y moleculares figuran entre los métodos analíticos instrumentales más utilizados. La espectroscopia molecular basada en la radiación ultravioleta,
1 1. Fundamento teórico Los métodos espectroscópicos atómicos y moleculares figuran entre los métodos analíticos instrumentales más utilizados. La espectroscopia molecular basada en la radiación ultravioleta,
Equipos de medición. Intervalos de calibración e interpretación de Certificados de Calibración
 Equipos de medición. Intervalos de calibración e interpretación de Certificados de Calibración Equipos de Medición. Intervalos de calibración e interpretación de Certificados de Calibración Disertante:
Equipos de medición. Intervalos de calibración e interpretación de Certificados de Calibración Equipos de Medición. Intervalos de calibración e interpretación de Certificados de Calibración Disertante:
TEMA 4 INTRODUCCIÓN AL ANÁLISIS VOLUMÉTRICO
 TEMA 4 INTRODUCCIÓN AL ANÁLISIS VOLUMÉTRICO Las valoraciones se emplean extensivamente en Química Analítica para la cuantificación de diversas especies químicas. En este tema se describen los principios
TEMA 4 INTRODUCCIÓN AL ANÁLISIS VOLUMÉTRICO Las valoraciones se emplean extensivamente en Química Analítica para la cuantificación de diversas especies químicas. En este tema se describen los principios
ESTUDIO DE SEGURIDAD DEL SECTOR COMERCIAL
 C CÁMARA DE COMERCIO DE COSTA RICA ESTUDIO DE SEGURIDAD DEL SECTOR COMERCIAL MEDICIÓN ANUAL 2012 ESTUDIO DE SEGURIDAD DEL SECTOR COMERCIAL MEDICION ANUAL DEL 2012 LOS COSTOS DE LA INSEGURIDAD DEL SECTOR
C CÁMARA DE COMERCIO DE COSTA RICA ESTUDIO DE SEGURIDAD DEL SECTOR COMERCIAL MEDICIÓN ANUAL 2012 ESTUDIO DE SEGURIDAD DEL SECTOR COMERCIAL MEDICION ANUAL DEL 2012 LOS COSTOS DE LA INSEGURIDAD DEL SECTOR
CAPÍTULO 7 7. CONCLUSIONES
 CAPÍTULO 7 7. CONCLUSIONES 7.1. INTRODUCCIÓN 7.2. CONCLUSIONES PARTICULARES 7.3. CONCLUSIONES GENERALES 7.4. APORTACIONES DEL TRABAJO DE TESIS 7.5. PROPUESTA DE TRABAJOS FUTUROS 197 CAPÍTULO 7 7. Conclusiones
CAPÍTULO 7 7. CONCLUSIONES 7.1. INTRODUCCIÓN 7.2. CONCLUSIONES PARTICULARES 7.3. CONCLUSIONES GENERALES 7.4. APORTACIONES DEL TRABAJO DE TESIS 7.5. PROPUESTA DE TRABAJOS FUTUROS 197 CAPÍTULO 7 7. Conclusiones
MODELOS DE INVENTARIO
 MODELOS DE INVENTARIO Los modelos de inventarios son métodos que ayudan a reducir o minimizar los niveles de inventario requeridos en la producción. Existen varios métodos que nos ayudan a conseguir dicho
MODELOS DE INVENTARIO Los modelos de inventarios son métodos que ayudan a reducir o minimizar los niveles de inventario requeridos en la producción. Existen varios métodos que nos ayudan a conseguir dicho
QUE DA. Parte 1. nosotros). Tienes gripa,
 LAS VUELTAS QUE DA LA GRIPA Parte 1 Hola! mi nombre es Carolina y vivo en Colombia. Me gusta mucho ir al colegio, pero desde hace dos días no he podido ir porque me siento muy enferma. Tengo tos, me duele
LAS VUELTAS QUE DA LA GRIPA Parte 1 Hola! mi nombre es Carolina y vivo en Colombia. Me gusta mucho ir al colegio, pero desde hace dos días no he podido ir porque me siento muy enferma. Tengo tos, me duele
Capitulo 3. Primer Año de Operaciones
 Capitulo 3 Primer Año de Operaciones Área de producción La empresa, como se había mencionado anteriormente, contaba hasta antes de asumir la administración de ella con cinco períodos de operación. La información
Capitulo 3 Primer Año de Operaciones Área de producción La empresa, como se había mencionado anteriormente, contaba hasta antes de asumir la administración de ella con cinco períodos de operación. La información
CARACTERÍSTICAS DEL ESTADO VÍTREO BAJO LA AMPLIA DENOMINACIÓN GENÉRICA DE VIDRIOS O DE CUERPOS VÍTREOS QUEDA COMPRENDIDA UNA GRAN VARIEDAD
 CARACTERÍSTICAS DEL ESTADO VÍTREO BAJO LA AMPLIA DENOMINACIÓN GENÉRICA DE VIDRIOS O DE CUERPOS VÍTREOS QUEDA COMPRENDIDA UNA GRAN VARIEDAD DE SUSTANCIAS QUE, AUNQUE A TEMPERATURA AMBIENTE TIENEN LA APARIENCIA
CARACTERÍSTICAS DEL ESTADO VÍTREO BAJO LA AMPLIA DENOMINACIÓN GENÉRICA DE VIDRIOS O DE CUERPOS VÍTREOS QUEDA COMPRENDIDA UNA GRAN VARIEDAD DE SUSTANCIAS QUE, AUNQUE A TEMPERATURA AMBIENTE TIENEN LA APARIENCIA
La relación entre la altura de caída y el tiempo que tarda en rebotar 6 veces una pelota
 La relación entre la altura de caída y el tiempo que tarda en rebotar 6 veces una pelota INTRODUCCIÓN En este experimento voy a relacionar el tiempo que tarda una pelota en rebotar 6 veces desde distintas
La relación entre la altura de caída y el tiempo que tarda en rebotar 6 veces una pelota INTRODUCCIÓN En este experimento voy a relacionar el tiempo que tarda una pelota en rebotar 6 veces desde distintas
Dr. José Vicente García Pérez. Resumen
 Estudio de la Aplicación de Ultrasonidos de Alta Intensidad en Sistemas Sólido-Líquido y Sólido-Gas. Influencia en la Cinética de Transporte de Materia y en la Estructura de los Productos Autor César Ozuna
Estudio de la Aplicación de Ultrasonidos de Alta Intensidad en Sistemas Sólido-Líquido y Sólido-Gas. Influencia en la Cinética de Transporte de Materia y en la Estructura de los Productos Autor César Ozuna
Control de la temperatura ambiente en un invernadero tipo venlo, mediante el uso del microcontrolador 8031
 Control de la temperatura ambiente en un invernadero tipo venlo, mediante el uso del microcontrolador 8031 GENARO CALDERÓN RODRÍGUEZ HÉCTOR HORACIO OCHOA NARANJO FACULTAD DE INGENIERÍA MECANICA Y ELÉCTRICA
Control de la temperatura ambiente en un invernadero tipo venlo, mediante el uso del microcontrolador 8031 GENARO CALDERÓN RODRÍGUEZ HÉCTOR HORACIO OCHOA NARANJO FACULTAD DE INGENIERÍA MECANICA Y ELÉCTRICA
CAPITULO 4 JUSTIFICACION DEL ESTUDIO. En este capítulo se presenta la justificación del estudio, supuestos y limitaciones de
 CAPITULO 4 JUSTIFICACION DEL ESTUDIO En este capítulo se presenta la justificación del estudio, supuestos y limitaciones de estudios previos y los alcances que justifican el presente estudio. 4.1. Justificación.
CAPITULO 4 JUSTIFICACION DEL ESTUDIO En este capítulo se presenta la justificación del estudio, supuestos y limitaciones de estudios previos y los alcances que justifican el presente estudio. 4.1. Justificación.
Joaquín Bernal Méndez Dpto. Física Aplicada III 1
 TERMODINÁMICA Tm Tema 7: 7Cn Conceptos ptsfndmntls Fundamentales Fundamentos Físicos de la Ingeniería 1 er Curso Ingeniería Industrial Dpto. Física Aplicada III 1 Índice Introducción Sistema y entorno
TERMODINÁMICA Tm Tema 7: 7Cn Conceptos ptsfndmntls Fundamentales Fundamentos Físicos de la Ingeniería 1 er Curso Ingeniería Industrial Dpto. Física Aplicada III 1 Índice Introducción Sistema y entorno
CAPÍTULO 4 ESTUDIO DE MERCADO. en el mercado. Por medio de la ley de la demanda, se determina que al subir el precio de un
 CAPÍTULO 4 ESTUDIO DE MERCADO 4.1. DEMANDA DEL PROYECTO La demanda es la cantidad de bienes o servicios que los compradores intentan adquirir en el mercado. Por medio de la ley de la demanda, se determina
CAPÍTULO 4 ESTUDIO DE MERCADO 4.1. DEMANDA DEL PROYECTO La demanda es la cantidad de bienes o servicios que los compradores intentan adquirir en el mercado. Por medio de la ley de la demanda, se determina
Unidad 6 Cálculo de máximos y mínimos
 Unidad 6 Cálculo de máimos y mínimos Objetivos Al terminar la unidad, el alumno: Utilizará la derivada para decidir cuándo una función es creciente o decreciente. Usará la derivada para calcular los etremos
Unidad 6 Cálculo de máimos y mínimos Objetivos Al terminar la unidad, el alumno: Utilizará la derivada para decidir cuándo una función es creciente o decreciente. Usará la derivada para calcular los etremos
Ecuaciones de primer grado con dos incógnitas
 Ecuaciones de primer grado con dos incógnitas Si decimos: "las edades de mis padres suman 120 años", podemos expresar esta frase algebraicamente de la siguiente forma: Entonces, Denominamos x a la edad
Ecuaciones de primer grado con dos incógnitas Si decimos: "las edades de mis padres suman 120 años", podemos expresar esta frase algebraicamente de la siguiente forma: Entonces, Denominamos x a la edad
TIPO DE CAMBIO, TIPOS DE INTERES Y MOVIMIENTOS DE CAPITAL
 TIPO DE CAMBIO, TIPOS DE INTERES Y MOVIMIENTOS DE CAPITAL En esta breve nota se intentan analizar las relaciones existentes en el sector español entre tipo de cambio, tasa de inflación y tipos de interés,
TIPO DE CAMBIO, TIPOS DE INTERES Y MOVIMIENTOS DE CAPITAL En esta breve nota se intentan analizar las relaciones existentes en el sector español entre tipo de cambio, tasa de inflación y tipos de interés,
Álgebra Lineal Ma1010
 Álgebra Lineal Ma1010 Mínimos Cuadrados Departamento de Matemáticas ITESM Mínimos Cuadrados Álgebra Lineal - p. 1/34 En esta sección veremos cómo se trabaja un sistema inconsistente. Esta situación es
Álgebra Lineal Ma1010 Mínimos Cuadrados Departamento de Matemáticas ITESM Mínimos Cuadrados Álgebra Lineal - p. 1/34 En esta sección veremos cómo se trabaja un sistema inconsistente. Esta situación es
Laboratorio Física I
 Laboratorio Física I Guía Pedro Miranda y Fabián Juárez 1. Informes de laboratorio 1.1. Introducción Uno de los elementos más utilizados en la comunicación de conocimientos es el informe. El propósito
Laboratorio Física I Guía Pedro Miranda y Fabián Juárez 1. Informes de laboratorio 1.1. Introducción Uno de los elementos más utilizados en la comunicación de conocimientos es el informe. El propósito
FUNCIONES DE UNA VARIABLE Julián de la Horra Departamento de Matemáticas U.A.M.
 FUNCIONES DE UNA VARIABLE Julián de la Horra Departamento de Matemáticas U.A.M. 1 Introducción Una de las primeras necesidades que surgen en las Ciencias Experimentales es la de poder expresar los valores
FUNCIONES DE UNA VARIABLE Julián de la Horra Departamento de Matemáticas U.A.M. 1 Introducción Una de las primeras necesidades que surgen en las Ciencias Experimentales es la de poder expresar los valores
Colegio Alexander von Humboldt - Lima. Tema: La enseñanza de la matemática está en un proceso de cambio
 Refo 07 2004 15 al 19 de noviembre 2004 Colegio Alexander von Humboldt - Lima Tema: La enseñanza de la matemática está en un proceso de cambio La enseñanza de la matemática debe tener dos objetivos principales:
Refo 07 2004 15 al 19 de noviembre 2004 Colegio Alexander von Humboldt - Lima Tema: La enseñanza de la matemática está en un proceso de cambio La enseñanza de la matemática debe tener dos objetivos principales:
Los estados financieros proporcionan a sus usuarios información útil para la toma de decisiones
 El ABC de los estados financieros Importancia de los estados financieros: Aunque no lo creas, existen muchas personas relacionadas con tu empresa que necesitan de esta información para tomar decisiones
El ABC de los estados financieros Importancia de los estados financieros: Aunque no lo creas, existen muchas personas relacionadas con tu empresa que necesitan de esta información para tomar decisiones
CORRELACIÓN Y PREDICIÓN
 CORRELACIÓN Y PREDICIÓN 1. Introducción 2. Curvas de regresión 3. Concepto de correlación 4. Regresión lineal 5. Regresión múltiple INTRODUCCIÓN: Muy a menudo se encuentra en la práctica que existe una
CORRELACIÓN Y PREDICIÓN 1. Introducción 2. Curvas de regresión 3. Concepto de correlación 4. Regresión lineal 5. Regresión múltiple INTRODUCCIÓN: Muy a menudo se encuentra en la práctica que existe una
Optimizar recursos y asegurar cumplimiento metrológico Buenos Aires 7 de Agosto 2015 EXPOFYBI
 Optimizar recursos y asegurar cumplimiento metrológico Buenos Aires 7 de Agosto 2015 EXPOFYBI Operación que establece, una relación entre los valores y sus incertidumbres de medida asociadas obtenidas
Optimizar recursos y asegurar cumplimiento metrológico Buenos Aires 7 de Agosto 2015 EXPOFYBI Operación que establece, una relación entre los valores y sus incertidumbres de medida asociadas obtenidas
ISOTERMA DE ADSORCIÓN DE ÁCIDO OXÁLICO SOBRE CARBÓN ACTIVO. Eva Mª Talavera Rodríguez y Francisco A. Ocaña Lara
 ISOTERMA DE ADSORCIÓN DE ÁCIDO OXÁLICO SOBRE CARBÓN ACTIVO Eva Mª Talavera Rodríguez y Francisco A. Ocaña Lara 1. Objetivos 1.- Verificar la adsorción de las moléculas de un soluto en una disolución líquida
ISOTERMA DE ADSORCIÓN DE ÁCIDO OXÁLICO SOBRE CARBÓN ACTIVO Eva Mª Talavera Rodríguez y Francisco A. Ocaña Lara 1. Objetivos 1.- Verificar la adsorción de las moléculas de un soluto en una disolución líquida
Estudio de la evaporación
 Estudio de la evaporación Volumen del líquido Tipo de líquido Superficie del recipiente Altura del recipiente Forma del recipiente Presencia de una sal disuelta Introducción Todos hemos observado que una
Estudio de la evaporación Volumen del líquido Tipo de líquido Superficie del recipiente Altura del recipiente Forma del recipiente Presencia de una sal disuelta Introducción Todos hemos observado que una
1.4.- D E S I G U A L D A D E S
 1.4.- D E S I G U A L D A D E S OBJETIVO: Que el alumno conozca y maneje las reglas empleadas en la resolución de desigualdades y las use para determinar el conjunto solución de una desigualdad dada y
1.4.- D E S I G U A L D A D E S OBJETIVO: Que el alumno conozca y maneje las reglas empleadas en la resolución de desigualdades y las use para determinar el conjunto solución de una desigualdad dada y
Evaluación de la capacidad óptima de medida y alcance de la acreditación de un laboratorio de calibración
 Evaluación de la capacidad óptima de medida y alcance de la acreditación de un laboratorio de calibración Fernández Pareja, Mª Teresa te_fer@topografia.upm.es Departamento de Ingeniería Topográfica y Cartografía
Evaluación de la capacidad óptima de medida y alcance de la acreditación de un laboratorio de calibración Fernández Pareja, Mª Teresa te_fer@topografia.upm.es Departamento de Ingeniería Topográfica y Cartografía
La presente tesis pretende que los estudiantes observen la teoría de las acciones de control
 CAPÍTULO V. CONCLUSIONES. La presente tesis pretende que los estudiantes observen la teoría de las acciones de control de forma virtual al mismo tiempo analicen físicamente los sistemas electrónicos cuando
CAPÍTULO V. CONCLUSIONES. La presente tesis pretende que los estudiantes observen la teoría de las acciones de control de forma virtual al mismo tiempo analicen físicamente los sistemas electrónicos cuando
Guía de Preparación de Muestras para PLASTICOS para el Software de Formulación de Datacolor
 Guía de Preparación de Muestras para PLASTICOS para el Software de Formulación de Datacolor 1. Generalidades 2. Qué se necesita para comenzar? 3. Qué hacer para sistemas opacos y translúcidos? 4. Qué hacer
Guía de Preparación de Muestras para PLASTICOS para el Software de Formulación de Datacolor 1. Generalidades 2. Qué se necesita para comenzar? 3. Qué hacer para sistemas opacos y translúcidos? 4. Qué hacer
LA MEDIDA Y SUS ERRORES
 LA MEDIDA Y SUS ERRORES Magnitud, unidad y medida. Magnitud es todo aquello que se puede medir y que se puede representar por un número. Para obtener el número que representa a la magnitud debemos escoger
LA MEDIDA Y SUS ERRORES Magnitud, unidad y medida. Magnitud es todo aquello que se puede medir y que se puede representar por un número. Para obtener el número que representa a la magnitud debemos escoger
CAPÍTULO 10 Aplicaciones de la Derivada a Funciones Económicas
 CAPÍTULO 10 Aplicaciones de la Derivada a Funciones Económicas Introducción En la economía, la variación de alguna cantidad con respecto a otra puede ser descrita por un concepto promedio o por un concepto
CAPÍTULO 10 Aplicaciones de la Derivada a Funciones Económicas Introducción En la economía, la variación de alguna cantidad con respecto a otra puede ser descrita por un concepto promedio o por un concepto
Por otro lado podemos enunciar los objetivos más específicos de nuestro estudio:
 RESUMEN La empresa familiar es aquella cuya administración, dirección y control está en manos de una familia. Sus miembros toman decisiones estratégicas y operativas, asumiendo por completo la responsabilidad
RESUMEN La empresa familiar es aquella cuya administración, dirección y control está en manos de una familia. Sus miembros toman decisiones estratégicas y operativas, asumiendo por completo la responsabilidad
DESARROLLO DE MATERIAL MULTIMEDIA MULTIDISCIPLINAR
 DESARROLLO DE MATERIAL MULTIMEDIA MULTIDISCIPLINAR Mª Luisa García, Mª Antonia Egea, Marta Espina, Mª Angeles Salvadó, Oriol Valls, Mª José García-Celma GIDAIF (Grup d Innovació Docent en Anàlisi Instrumental
DESARROLLO DE MATERIAL MULTIMEDIA MULTIDISCIPLINAR Mª Luisa García, Mª Antonia Egea, Marta Espina, Mª Angeles Salvadó, Oriol Valls, Mª José García-Celma GIDAIF (Grup d Innovació Docent en Anàlisi Instrumental
Facultad de Economía Claudia Montserrat Martínez Stone CAPITULO IV EVALUACIÓN FINANCIERA
 CAPITULO IV EVALUACIÓN FINANCIERA 56 4.1.- Criterios de Evaluación Financiera La Evaluación de un Proyecto debe tener como base el análisis con el que se mide la rentabilidad económica, en el que principalmente
CAPITULO IV EVALUACIÓN FINANCIERA 56 4.1.- Criterios de Evaluación Financiera La Evaluación de un Proyecto debe tener como base el análisis con el que se mide la rentabilidad económica, en el que principalmente
Química Biológica I TP 1: ESPECTROFOTOMETRIA
 Química Biológica I TP 1: ESPECTROFOTOMETRIA OBJETIVOS: - Reforzar el aprendizaje del uso del espectrofotómetro. - Realizar espectro de absorción de sustancias puras: soluciones de dicromato de potasio.
Química Biológica I TP 1: ESPECTROFOTOMETRIA OBJETIVOS: - Reforzar el aprendizaje del uso del espectrofotómetro. - Realizar espectro de absorción de sustancias puras: soluciones de dicromato de potasio.
Solubilidad. y se representa por.
 Solubilidad Solubilidad. La solubilidad mide la cantidad máxima de soluto capaz de disolverse en una cantidad definida de disolvente, a una temperatura determinada, y formar un sistema estable que se denomina
Solubilidad Solubilidad. La solubilidad mide la cantidad máxima de soluto capaz de disolverse en una cantidad definida de disolvente, a una temperatura determinada, y formar un sistema estable que se denomina
UNIVERSIDAD DE ANTIOQUIA FACULTAD DE INGENIERÍA DEPARTAMENTO DE INGENIERÍA QUÍMICA LABORATORIO DE OPERACIONES UNITARIAS II TRANSFERENCIA DE CALOR
 UNIVERSIDAD DE ANTIOQUIA FACULTAD DE INGENIERÍA DEPARTAMENTO DE INGENIERÍA QUÍMICA LABORATORIO DE OPERACIONES UNITARIAS II TRANSFERENCIA DE CALOR INFORME INTERCAMBIADOR DE PLACAS María Claudia Romero,
UNIVERSIDAD DE ANTIOQUIA FACULTAD DE INGENIERÍA DEPARTAMENTO DE INGENIERÍA QUÍMICA LABORATORIO DE OPERACIONES UNITARIAS II TRANSFERENCIA DE CALOR INFORME INTERCAMBIADOR DE PLACAS María Claudia Romero,
Indicadores para la generación de conocimiento acerca de la evaluación de la calidad de las instituciones educativas
 Indicadores para la generación de conocimiento acerca de la evaluación de la calidad de las instituciones educativas Por Antonio Millán Arellano Nov 25 de 2006 Resumen El uso de indicadores es cada día
Indicadores para la generación de conocimiento acerca de la evaluación de la calidad de las instituciones educativas Por Antonio Millán Arellano Nov 25 de 2006 Resumen El uso de indicadores es cada día
LOS GASES Y SUS LEYES DE
 EMA : LOS GASES Y SUS LEYES DE COMBINACIÓN -LAS LEYES DE LOS GASES En el siglo XII comenzó a investigarse el hecho de que los gases, independientemente de su naturaleza, presentan un comportamiento similar
EMA : LOS GASES Y SUS LEYES DE COMBINACIÓN -LAS LEYES DE LOS GASES En el siglo XII comenzó a investigarse el hecho de que los gases, independientemente de su naturaleza, presentan un comportamiento similar
INDICADORES PRESENTADO POR: LUIS DARÍO TÉLLEZ RAMÍREZ
 PRESENTADO POR: LUIS DARÍO TÉLLEZ RAMÍREZ CONTENIDO GENERALIDADES DE LA MEDICIÓN CLASIFICACIÓN DE FORMULACIÓN O AJUSTE DE GENERALIDADES DE LA MEDICIÓN EN EL SECTOR PÚBLICO La medición consiste en revisar
PRESENTADO POR: LUIS DARÍO TÉLLEZ RAMÍREZ CONTENIDO GENERALIDADES DE LA MEDICIÓN CLASIFICACIÓN DE FORMULACIÓN O AJUSTE DE GENERALIDADES DE LA MEDICIÓN EN EL SECTOR PÚBLICO La medición consiste en revisar
Aportaciones de los libros de texto del área de Ciencias de la Naturaleza a la competencia científica en el dominio de la combustión
 Aportaciones de los libros de texto del área de Ciencias de la Naturaleza a la competencia científica en el dominio de la combustión JOSÉ ANTONIO RUEDA SERÓN Y ÁNGEL BLANCO LÓPEZ Universidad de Málaga.
Aportaciones de los libros de texto del área de Ciencias de la Naturaleza a la competencia científica en el dominio de la combustión JOSÉ ANTONIO RUEDA SERÓN Y ÁNGEL BLANCO LÓPEZ Universidad de Málaga.
