PROCEDIMIENTO ENUMERACION POR METODO SERIE DE TUBOS MULTIPLES (NMP) DE BACILLUS CEREUS EN ALIMENTOS. PRT Página 1 de 15
|
|
|
- Marcos Silva Sáez
- hace 6 años
- Vistas:
Transcripción
1 PRT Página 1 de OBJETIVO Detectar el número de células viables de Bacillus cereus en el alimentos con baja contaminación. 2. CAMPO DE APLICACION Y ALCANCE Aplicar este procedimiento en alimentos en los que se espera detectar < 10 células / g o ml. Este método es recomendable en muestras deshidratadas, alimentos con alto contenido de almidón en donde el recuento no es recomendado. 3. FUNDAMENTO Bacillus cereus es un bacilo Gram positivo, aerobio-anaerobio facultativo. Es formador de esporas, las que se encuentran en la tierra, polvo y por esta razón es un frecuente contaminante de alimentos. La intoxicación alimentaria provocada por B. cereus puede ocurrir cuando los alimentos son preparados con mucha anticipación sin la refrigeración adecuada. Alimentos con una enumeración >10 6 ufc/g pueden provocar intoxicación alimentaria. El fundamento del método se basa en proporcionar una etapa de enriquecimiento selectivo por la adición de Polimixina B y por la capacidad del microorganismo para precipitar la lecitina de la yema de huevo que contiene el medio y su característica de no fermentar el manitol, estas 2 propiedades son utilizadas para diferenciar las colonias de B. cereus en el medio de cultivo MYP. La adición de la polimixina es actuar como un inhibidor del desarrollo de otros bacilos facultativos ambientales. 4. REFERENCIAS 4.1. Food and Drug Administration "Bacteriological Analytical Manual" online, enero 2001, carpeta TERMINOLOGIA No Aplica. 6. MATERIALES, INSUMOS Y EQUIPOS 6.1. Materiales Pipetas estériles de 1, 5 y 10 ml graduadas en 0,1 ml Propipetas Placas Petri estériles 15 x 100 mm Asas desechables de nicrom o platino de aro 2 mm y 3 mm de diámetro Tubos estériles de 13 x 100 mm y tubos de 16 x 125 mm Jarra anaerobiosis, Anaerogen o Gas Pack con generador de H 2 + CO 2 y catalizador Rastrillos estériles Lápiz marcador
2 PRT Página 2 de Mecheros Tubos estériles 13 x 100 mm Tubos 16 x 125 mm Gradilla para tinción 6.2 Medios de Cultivo y Reactivos Caldo soya tripticasa con polimixina Solución de polimixina B al 0,15 % Agar Manitol-Yema de huevo y Polimixina (MYP) Agar Tirosina Agar nutritivo para Bacillus cereus Caldo Glucosa-Rojo fenol Caldo Nitrato Caldo Voges Proskauer (VP modificado) Caldo lisozima Solución de Polimixina B 0.1% para agar MYP Solución de α naftol 0,5% en ácido acético 5N Solución de ácido sulfanílico 0,8% en ácido acético 5N Solución de α naftol 5% en etanol Solución de KOH al 40% Emulsión de Yema de Huevo al 50% Reactivos para tinción de Gram Zinc en polvo Agua de dilución debutterfield en tubos con 9 ml ± 0,2 ml y frascos de 450 ml ± 5mL Cristales creatina Solución de tinción Fucsina básica Metanol Medio movilidad B cereus Agar soya tripticasa sangre de cordero 6.3 Equipos Estufas de incubación reguladas a 30º ± 2 C y 35º ± 2º C Refrigerador Vortex Contador de colonias Microscopio
3 PRT Página 3 de 15 7 DESARROLLO DEL PROCESO 7.1 Recepción de la muestra en el laboratorio Recibir la dilución 10-1 de la muestra procesada en el laboratorio de Recepción de muestras según PRT Preparar a partir de dilución 10-1 diluciones seriadas hasta 10-3, transfiriendo 1 ml a 9 ml de diluyente Si es necesario realizar diluciones adicionales si se sospecha de una población de B. cereus que excede 10 3 / g Anotar en la hoja de registro la inscripción de muestras del laboratorio, N, fecha de recepción, naturaleza de la muestra, fecha de análisis, analista y todos lo datos solicitados por el registro En el caso de muestras de brotes de ETA, anotar la información adicional que se disponga, si la hay El período transcurrido entre la preparación del homogeneizado de la muestra y la siembra no debe superar los 20 minutos. 7.2 Siembra recuento de células viables de Bacillus cereus Inocular 3 tubos de caldo soya tripticasa con polimixina al 0,15 % con 1 ml de la dil 10-1 cada uno Inocular 3 tubos de caldo soya tripticasa con polimixina al 0,15 % con 1 ml de la dil 10-2 cada uno Inocular 3 tubos de caldo soya tripticasa con polimixina al 0,15 % con 1 ml de la dil 10-3 cada uno Incubar los tubos por 48 ± 2 h a 30 C. y observe un denso desarrollo, el cual es típico para B. cereus. 7.3 Lectura Enumeración presuntiva células viables B. cereus Registre la combinación de tubos positivos en la hoja de Registro de análisis del laboratorio RG De cada tubo positivo sembrar por separado en estría en placas agar MYP Incube las placas h a 30 C.
4 PRT Página 4 de Traspaso Seleccionar las placas de agar MYP que presenten desarrollo de colonias rosadas (manitol negativas y una zona de precipitación alrededor de la colonia (lecitinasa positiva) Traspasar al menos 1 o más colonias que presenten las características del punto a agar nutritivo tendido para realizar la confirmación de B. cereus En caso de no tener colonias aisladas, proceder como sigue: Tomar una porción de cultivo con asa Sembrar por aislamiento en una placa de agar MYP previamente seca Incubar las placas invertidas a 30º C ± 2 C por 24 a 48 horas Registrar las características de este cultivo en la hoja de Registro de análisis del laboratorio RG Traspasar al menos 1 o más colonias que presenten las características del punto a agar nutritivo tendido para realizar la confirmación de B. cereus Realizar pruebas bioquímicas a las colonias seleccionadas 7.5 Pruebas Confirmativas Del agar nutritivo tendido realizar Gram y observar microscópicamente. B. cereus aparece como bacilo largo Gram positivo, en cadenas cortas a largas; de esporas elipsoidales de disposición central o subterminal y el esporangio no engrosado A partir del cultivo de agar nutritivo tendido transferir con asa de 3 mm a tubos de 13 x 100 mm que contienen 0,5 ml de agua de dilución buffer fosfato, suspenda el cultivo y mezcle en vortex. Use esta suspensión para inocular los siguientes medios confirmatorios: Prueba de Fermentación de glucosa: Inocular con asa de 2 mm la suspensión de cultivo en 3 ml de caldo glucosa rojo fenol e incubar en anaerobiosis por 24 horas a 35 C ± 2 C Prueba VP modificado: Inocular en 5mL de medio VP con la suspensión de cultivo utilizando asa de 3mm de diámetro. Incubar por 48±2 h a 35 C Prueba lisozima: Inocular en 2,5 ml de caldo nutritivo que contenga 0,001% de lisozima con la suspensión de cultivo utilizando asa de 2 mm. También inocular en 2,5 ml de caldo nutritivo como control positivo. Incubar por 24 horas a 35 C ± 2 C.
5 PRT Página 5 de Prueba tirosina: Inocular en toda la superficie del agar tirosina tendido la suspensión de cultivo con asa de 3 mm, Incubar por 48 horas a 35 C ± 2 C. Incubar los tubos que no presenten crecimiento hasta por 7 días antes de considerar el resultado como negativo Prueba de reducción de nitratos a nitritos: Inocular en 5 ml de caldo nitrato con la suspensión del cultivo, utilizando asa de 3 mm. Incubar por 24 horas a 35 C ± 2 C Agar MYP: puede ser omitido si los resultados son determinantes en las placas de agar MYP original o inicial en las cuales además no se observan interferentes de otros microorganismos presentes. Si no es así dividir la placa en 6-8 secciones iguales y rotular cada sección e inocular tocando suavemente con asa de 2 mm la suspensión del cultivo en la superficie del agar en un área de 4 cm 2 de agar. (Por esta forma pueden ser ensayados seis o más cultivos por placa).incubar a 35 C ± 2 C por 24 horas. 7.6 Pruebas adicionales para diferenciar otros miembros del B. cereus: B. mycoides, B, thuringiensis y B. anthracis Prueba de la motilidad: Inocular en medio BC motilidad en picadura en el centro del tubo con asa de 3 mm con cultivo de una suspensión de 24 horas. Incubar 18 a 24 horas a 30 C y examinar crecimiento a lo largo de la línea de inoculación. Alternativamente, añada 0,2 ml de agua destilada estéril a la superficie de agar nutritivo tendido e inocule con asa de 3 mm del cultivo de una suspensión. Incubar 6 a 8 horas a 30 C ± 2 C y suspenda con asa de 3 mm el líquido a acumulado en la base del agar tendido en una gota de agua estéril sobre un portaobjeto, ponga un cubreobjeto y observe al microscopio Desarrollo rizoidal: en agar nutritivo (18 a 20 ml) en placa, dejar secar completamente a temperatura ambiente por 1 a 2 días. Inocular suspensión del cultivo con asa de 2 mm suavemente sólo tocando la superficie de la parte central del agar en la placa. Permitir que el inóculo sea absorbido. Incubar a 30 C ± 2 C por 48 a 72 horas Actividad hemolítica: en una placa de agar soya tripticase con sangre de cordero dividir la placa en 6-8 secciones iguales y rotular cada sección e inocular tocando suavemente con asa de 2 mm la suspensión del cultivo de 24 h en la superficie del agar en un área de 4 cm 2 de, se pueden hacer cuñas de agar.incubar a 35 C ± 2 C por 24 horas Prueba de cristales de proteína tóxicos: inocular en agar nutritivo tendido con asa de 3 mm una suspensión de un cultivo de 24 h.incubar a 30 C ± 2 C por 24 h y luego dejar a temperatura ambiente por 2 a 3 días. Preparar extendido o frotis con agua destilada estéril en un porta objeto. Secar al aire y fijar suavemente con la llama de un mechero Bunsen. En un soporte de tinción inundar con metanol, dejar tendido por 30 segundos, elimine el metanol y secar al aire. Ubicar nuevamente el porta objeto en el soporte de tinción e inundar completamente con fucsina básica al 0,5 % o con colorante TB carbolfucsina tinción de ZN. Calentar deslizando desde abajo con un pequeño mechero Bunsen hasta que se desprenda vapor. Esperar 1 a 2 min y repita este paso,
6 PRT Página 6 de 15 dejar tendido 30 segundos, elimine el colorante y enjuagar profundamente con agua corriente. Dejar secar y examinar al microscopio en inmersión. 7.7 Lectura de las pruebas bioquímicas En caldo Fermentación de glucosa, agitar vigorosamente el tubo y observar desarrollo por incremento de la turbiedad y viraje del indicador de rojo a amarillo, lo que indica que el ácido ha sido producido anaeróbicamente desde la glucosa, un cambio parcial de color rojo a naranjado/ amarillo puede ocurrir incluso en los tubos de control sin inóculo debido a la reducción de ph por la exposición del medio a CO 2 formado en la jarra de anaerobiosis. Asegúrese de usar apropiados controles positivos y negativos para distinguir reacciones falso-positivo La prueba en VP para la producción de acetilmetil-carbinol es positiva al pipetear 1 ml y transferirlo a tubos de 16 x 125 mm, luego añadir 0,6 ml de solución de alfa-naftol al 5% en etanol y 0,2 ml de NaOH al 40%.Agitar y se puede añadir unos pocos cristales de creatina. Después de una hora a temperatura ambiente se puede observar la aparición de color rosado intenso o violeta lo que indica que la reacción es positiva En caldo lisozima observar desarrollo por la presencia de turbidez como resultado positivo. Observar desarrollo en caldo lisozima como en caldo nutritivo de control. Si la lectura fuese negativa incubar por 24 horas adicionales antes de descartar En el agar tirosina observar una zona clara en el medio cerca o alrededor de desarrollo de B. cereus, lo que indica que la tirosina ha sido descompuesta. Los tubos que presenten desarrollo pero sin evidencia de hidrólisis de la tirosina incubar por un total de 7 días antes de considerar la prueba como negativa En caldo nitrato observar la parición color rojo anaranjado al agregar 0,25 ml de ácido sulfanílico al 0,8 % en ácido acético 5 N y 0,25 ml de α naftol al 0,5% en ácido acético 5N, un cambio de color a anaranjado indica que la prueba es positiva, si no aparece color naranjo dentro de 10 minutos, indica que la prueba es negativa y se debe agregar polvo de Zn, no debe observarse cambios para interpretar la prueba como positiva, de lo contrario si al agregar Zinc en polvo se presenta coloración anaranjada, se debe interpretar la prueba como negativa En agar MYP observar la producción de lecitinasa indicada por una zona de precipitación alrededor de las colonias. El manitol no es fermentado por lo tanto las colonias son rosadas Interpretación de los resultados: B. cereus es un bacilo Gram positivo con esporas, produce lecitinasa y no fermenta manitol en agar MYP, crece y produce ácido en condiciones anaeróbicas a partir de la glucosa, reduce nitratos a nitritos, produce acetilmetil-carbinol, descompone la tirosina, y crece en presencia de lisozima la 0,001%.
7 PRT Página 7 de Estas características básicas son compartidas con otros miembros del grupo Bacillus cereus, incluyendo las cepas rizoidales de B. mycoides, los cristales de B. thuringiensis patógenos para insectos, y B. anthracis patógeno de mamíferos Pruebas adicionales: Prueba de la motilidad, los microorganismos móviles producen desarrollo difuso en el medio de cultivo. Los inmóviles crecen sólo en la línea de inoculación. Si realiza la prueba en agar tendido en la observación al microscopio se distinguen microorganismos móviles. La mayoría de las cepas de B. cereus y B. thuringiensis son móviles, unas pocas cepas de B. cereus son inmóviles El desarrollo rizoidal se manifiesta por el crecimiento en arborización o desarrollo similar a raíces que se extienden por varios centímetros del centro de la inoculación y es característico de B. mycoides Actividad hemolítica en B. cereus es fuerte y marcada produciendo 2 a 4 mm de zona de β.- hemólisis (hemólisis completa) alrededor de las colonias. (Seis o más colonias pueden ser testeadas en cada placa) En la prueba de cristales tóxicos de proteína se observan esporas libres y los cristales se observan como formas tetragonales y se tiñen en forma muy oscura. Los cristales son usualmente más pequeños que las esporas Interpretación resultados pruebas adicionales: B. cereus es móvil, presenta una marcada β- hemólisis, no presenta desarrollo rizoidal y no produce cristales tóxicos de proteína. 7.8 Cálculo y expresión de resultados Anotar lo resultados de las pruebas bioquímicas y morfológicas en RG Confirmar como B. cereus las colonias que cumplen con los puntos y Realizar el cálculo de NMP de B. cereus / g o ml de muestra basado sobre el número de tubos cada dilución que obtuvo confirmación de al menos una colonia de B. cereus. 7.9 Informe de resultados El resultado se expresa en NMP de Bacillus cereus por g o ml de producto analizado según corresponda.
8 PRT Página 8 de 15 8 REGISTROS 8.1 Registro resultados de análisis enumeración de Bacillus cereus en alimentos 8.2 Registro control esterilidad medios de cultivo laboratorio ensayos de esporulados 8.3 Registro cepa control positivo y control negativo análisis Bacillus cereus 9 ANEXOS Anexo N 1 Tabla diferencial de grupo Bacillus cereus. Anexo N 2 Preparación Medios de cultivo. Anexo N 3 Preparación Reactivos. Anexo N 4 Registro resultados de análisis enumeración de Bacillus cereus en alimentos RG Anexo N 5 Registro cepa control positivo y control negativo análisis Bacillus cereus RG Anexo N 6 Registro control esterilidad medios de cultivo laboratorio ensayos esporulados RG
9 PRT Página 9 de 15 ANEXO N 1-PRT TABLA DIFRENCIAL GRUPO BACILLUS CEREUS Table 1. Differential characteristics of large-celled Group I Bacillus species Feature B. cereus B. thuringiensis B. mycoides B. anthracis B. megaterium Gram reaction + (a) Catalase Motility +/- (b) +/- - (c) - +/- Reduction of nitrate + +/ (d) Tyrosine decomposed + + +/- - (d) +/- Lysozyme-resistant Egg yolk reaction Anaerobic utilization of glucose VP reaction Acid produced from mannitol Hemolysis (Sheep RBC) (d) - Known pathogenicity (e) /characteristic a +, % of strains are positive. b +/-, 50-50% of strains are positive. c -, % of strains are negative. d -, Most strains are negative. e See Section H, Limitations of method for B. cereus. produces enterotoxins endotoxin crystals pathogenic to insects rhizoidal growth pathogenic to animals and humans
10 PRT Página 10 de 15 ANEXO N 2-PRT PREPARACION MEDIOS DE CULTIVO Agar soya tripticase con sangre de cordero Fórmula: Peptona tripticasa Peptona phytone Na Cl Agar Agua destilada 15 g 5 g 5 g 15 g 1 L Calentar hasta disolver. Autoclavar 15 min a 121 C, ph final 7,3 ± 0,2 C. Enfriar a 50 C y añadir 5 ml de sangre de cordero desfibrinada a 100 ml de agar base. Mezclar y dispensar 20 ml en placas Petri de 15 x 100 mm. Medio motilidad para Bacillus cereus Fórmula: Tripticasa Extracto de levadura Dextrosa Na 2 HPO 4 Agar Agua destilada 10 g 2,5 g 5 g 2,5 g 3 g 1 L Calentar con agitación hasta disolver. Dispensar 100 ml en frascos Schott de 250 ml. Autoclavar por 15 min a a121 C. El ph final 7,4 ± 0.2. Enfriar a 50 C. Dispensar asépticamente 2 ml en tubos estériles de 13 x 100 mm. Almacenar a temperatura ambiente 2 días antes de su uso.
11 PRT Página 11 de 15 Caldo soya tripticasa con Polimixina B. Fórmula: Peptona tripticasa Petona fitona Na Cl K 2 HPO 4 Glucosa Agua destilada 17 g 3 g 5 g 2,5 g 2,5 g 1 L Calentar con constante agitación hasta disolver. Dispensar porciones de 15 ml en tubos de 20 x 150 mm. Autoclavar por 15 minutos a 121 C. Solución de Polimixina B al 0,15 % Disolver unidades de sulfato de polimixina B en 33.3 ml de agua destilada. Esterilizar por filtración. Almacenar en la oscuridad a 4 C hasta su uso. Antes de usar, añadir 0,1 ml de la solución de polimixina B al 0,15% a 15 ml del caldo de soya tripticasa. Mezclar.
12 PRT Página 12 de 15 ANEXO N 3-PRT PREPARACIÓN REACTIVOS Solución Lisozima Disolver 0.1 g de lisozima en 65 ml de HCl 0,01 N estéril. Calentar hasta ebullición por 20 min. Diluir a 100 ml con HCl 0,01 N. Alternativamente, disolver 0,1 g de lisozima en 100 ml de agua destilada. Esterilizar por filtración a través de membrana filtrante de 0,45 µm. Confirmar esterilidad antes de usar. Añadir 1 ml de solución lisozima a 99 ml de caldo nutritivo. Mezclar y dispensar 2,5 ml a tubos estériles de 13 x 100 mm. Suspensión Tirosina Suspender 0,5 g de L- tirosina en 10 ml de agua destilada en tubos de 20 x 150 mm. Mezclar con Vortex. Autoclavar 15 min a 121 C. A 100 ml de agar base agregar los 190 ml de la suspensión de tirosina. Mezclar bien invirtiendo el tubo 2 ó 3 veces. En forma aséptica dispensar 3,5 ml en tubos de 13 x 100 mm y mezclar. Tender los tubos y enfriar rápidamente para prevenir la separación de la tirosina. Solución de Fucsina Básica Disolver 0,5 g de fucsina básica en 20 ml de etanol al 95%. Diluir a 100 ml con agua destilada. Filtrar si es necesario con papel filtro Whatman N 3 para remover colorante sin disolver. También se puede usar TB carbolfucsina ZN.
13 PRT Página 13 de 15 Anexo N 4 Registro resultados de análisis enumeración de Bacillus cereus en alimentos. Fecha de recepción:... N :...Analista:...Incubadora... Tipo demuestra:...hora análisis...observaciones:... Diluciones Partida Diluyente Recuento en placa Agar MYP Enumeración (NMP) CST con polimixina al 0,15% Pruebas bioquímicas Colonia 1 Colonia 2 Colonia 3 Colonia 4 Colonia 5 Observaciones Agar MYP: Lecitinasa Fermetación Manitol Gram Ferm. Glucosa en anaerobiosis Reducción nitratos a nitritos Desarrollo en lisozima Lisis Tirosina Voges Proskauer Hemólisis Motilidad Desarrollo rizoidal Cristales tóxicos proteico Recuento Confirmado:...Fecha Informe:...
14 PRT Página 14 de 15 Anexo N 5 Registro cepa control positivo y control negativo análisis Bacillus cereus. Responsable: Fecha Informe: Fecha Pruebas Partida Control positivo Cepa Control negativo Cepa Control esterilidad Agar MYP Glucosa en Anaerobiosis Reducción de Nitratos Desarrollo en Lizosima Lisis Tirosina Voges Proskahuer Pruebas adicionales Desarrollo Rizoidal Hemólisis Movilidad Cristales tóxicos proteico Manitol Lecitinasa Lectura Manitol Lecitinasa Lectura
15 PRT Página 15 de 15 Anexo N 6 Registro control esterilidad medios de cultivo laboratorio ensayos esporulados Fecha/Lote Caldo soya Tripticase con polimixina Agar MYP Agar TSC Buffer fosfato Butterfield Agua Peptonada 0,1% Agar Nutritivo Agar Sangre Caldo soya Tripticase Caldo Cerebro Corazón Caldo Cerebro Corazó n almidón Caldo Cooked Meat Caldo Tioglicolato Medio Medio fermentació Duncan Spray Strong Fecha Lectura
PROCEDIMIENTO DETECCIÓN Y ENUMERACIÓN POR NUMERO MAS PROBABLE (NMP) CON ETAPA DE PRE- ENRIQUECIMIENTO DE ENTEROBACTERIACEAE EN ALIMENTOS
 Página 1 de 5 1. OBJETIVO Estimar el número de Enterobacteriaceae presentes en el alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos de consumo humano
Página 1 de 5 1. OBJETIVO Estimar el número de Enterobacteriaceae presentes en el alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a todas las muestras de alimentos de consumo humano
PROCEDIMIENTO RECUENTO DE COLIFORMES EN MEDIO SÓLIDO
 PRT-712.03-008 Página 1 de 6 1. OBJETIVO Este método es utilizado para realizar recuento de bacterias del grupo coliformes, como indicador sanitario. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento
PRT-712.03-008 Página 1 de 6 1. OBJETIVO Este método es utilizado para realizar recuento de bacterias del grupo coliformes, como indicador sanitario. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento
NMP PARA LA DETERMINACION DE COLIFORMES Y Escherichia coli EN ALIMENTOS BASADO EN BAM on line
 COLIFORMES Y Escherichia coli EN ME-712.02-004 Página 1 de 9 1. OBJETIVO Estimar la densidad de bacterias del grupo coliformes, como indicador sanitario en alimentos. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar
COLIFORMES Y Escherichia coli EN ME-712.02-004 Página 1 de 9 1. OBJETIVO Estimar la densidad de bacterias del grupo coliformes, como indicador sanitario en alimentos. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar
Objetivos. S Determinar la presencia de bacterias coliformes en una muestra de agua
 Análisis del agua S Objetivos S Determinar la presencia de bacterias coliformes en una muestra de agua Introducción S Las tres pruebas básicas para determinar la presencia de bacterias coliformes (asociada
Análisis del agua S Objetivos S Determinar la presencia de bacterias coliformes en una muestra de agua Introducción S Las tres pruebas básicas para determinar la presencia de bacterias coliformes (asociada
QUÉ CONTIENE UN MEDIO? Aquellos requerimientos nutricionales que los microorganismos necesitan para crecer. Depende del ambiente en donde viven.
 OBJETIVOS u Diferenciar entre ciertos tipos de medios u Conocer actividades bioquímicas de las bacterias u Conocer los procesos bioquímicos de fermentación u Descibir los patrones de fermentación de carbohidratos
OBJETIVOS u Diferenciar entre ciertos tipos de medios u Conocer actividades bioquímicas de las bacterias u Conocer los procesos bioquímicos de fermentación u Descibir los patrones de fermentación de carbohidratos
PRÁCTICO N 3. Técnicas para la observación, aislamiento y conservación de microorganismos
 PRÁCTICO N 3 Técnicas para la observación, aislamiento y conservación de microorganismos Objetivos Conocer el manejo del microscopio óptico, sus partes y utilidad en el laboratorio de microbiología. Conocer
PRÁCTICO N 3 Técnicas para la observación, aislamiento y conservación de microorganismos Objetivos Conocer el manejo del microscopio óptico, sus partes y utilidad en el laboratorio de microbiología. Conocer
AISLAMIENTO DE MICROORGANISMOS
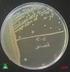 PRÁCTICA5 AISLAMIENTO DE MICROORGANISMOS Introducción En la naturaleza, la mayoría de los microorganismos no se encuentran aislados, sino integrados en poblaciones mixtas. Para llevar a cabo el estudio
PRÁCTICA5 AISLAMIENTO DE MICROORGANISMOS Introducción En la naturaleza, la mayoría de los microorganismos no se encuentran aislados, sino integrados en poblaciones mixtas. Para llevar a cabo el estudio
PROCEDIMIENTO DETECCION Vibrio cholerae EN AGUAS POR TECNICA DE MEMBRANA FILTRANTE. PRT Página 1 de 8
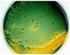 PRT-712.02-062 Página 1 de 8 1. OBJETIVO Detectar la presencia de Vibrio cholerae en aguas. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a muestras de aguas claras que no contengan residuos,
PRT-712.02-062 Página 1 de 8 1. OBJETIVO Detectar la presencia de Vibrio cholerae en aguas. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a muestras de aguas claras que no contengan residuos,
PROCEDIMIENTO NMP PARA LA DETERMINACION DE COLIFORMES FECALES EN AGUAS POR METODO A-1 PRT-712.02-006
 Página 1 de 6 1. OBJETIVO Este análisis se realiza para estimar la densidad de coliformes fecales en agua, con una incubación de 24 hrs. por lo cual se obtienen resultados en menor tiempo que el método
Página 1 de 6 1. OBJETIVO Este análisis se realiza para estimar la densidad de coliformes fecales en agua, con una incubación de 24 hrs. por lo cual se obtienen resultados en menor tiempo que el método
PRACTICA 2 TINCION DE GRAM
 PRACTICA 2 TINCION DE GRAM OBJETIVOS DE APRENDIZAJE: Cuando haya completado este experimento, usted debe comprender: 1. La base teórica y química de los procedimientos de tinción diferencial. 2. La base
PRACTICA 2 TINCION DE GRAM OBJETIVOS DE APRENDIZAJE: Cuando haya completado este experimento, usted debe comprender: 1. La base teórica y química de los procedimientos de tinción diferencial. 2. La base
PROCEDIMIENTO RECUENTO DE AREOBIOS MESOFILOS EN LECHE UHT
 PRT- 712.02-078 Página 1 de 9 1. OBJETIVO Conocer la calidad microbiológica de la leche sometida a ultra alta temperatura de acuerdo a lo establecido en el Reglamento Sanitario de los Alimentos. 2. CAMPO
PRT- 712.02-078 Página 1 de 9 1. OBJETIVO Conocer la calidad microbiológica de la leche sometida a ultra alta temperatura de acuerdo a lo establecido en el Reglamento Sanitario de los Alimentos. 2. CAMPO
RECOPILADO POR: EL PROGRAMA UNIVERSITARIO DE ALIMENTOS
 NMX-F-187-1978. DETERMINACIÓN DEL NÚMERO MÁS PROBABLE DE GÉRMENES. METHOD OF TEST FOR GERMS MOST PROBABLE NUMBER. NORMAS MEXICANAS. DIRECCIÓN GENERAL DE NORMAS. PREFACIO En la elaboración de esta Norma
NMX-F-187-1978. DETERMINACIÓN DEL NÚMERO MÁS PROBABLE DE GÉRMENES. METHOD OF TEST FOR GERMS MOST PROBABLE NUMBER. NORMAS MEXICANAS. DIRECCIÓN GENERAL DE NORMAS. PREFACIO En la elaboración de esta Norma
LABORATORIO DE MICROBIOLOGÍA EXPERIMENTAL Grupo 2 (10:00 13:00 hrs) Semestre Profesores: Guadalupe Tsuzuki Reyes y Rosalba Esquivel-Cote
 Semana 2 Semana 1 LABORATORIO DE EXPERIMENTAL Grupo 2 (10:00 13:00 hrs) Semestre 2013-2 Profesores: Guadalupe Tsuzuki Reyes y Rosalba Esquivel-Cote CALENDARIO DE ACTIVIDADES UNIDAD Lunes 28 ENERO Miércoles
Semana 2 Semana 1 LABORATORIO DE EXPERIMENTAL Grupo 2 (10:00 13:00 hrs) Semestre 2013-2 Profesores: Guadalupe Tsuzuki Reyes y Rosalba Esquivel-Cote CALENDARIO DE ACTIVIDADES UNIDAD Lunes 28 ENERO Miércoles
PROCEDIMIENTO RECUENTO DE E COLI EN ALIMENTOS UTILIZANDO AGAR VRB-MUG
 PRT-712.02-037 Página 1 de 8 1. OBJETIVO Enumerar los microorganismos E. coli presentes en una muestra de alimento 2. CAMPO DE APLICACIÓN Y ALCANCE Muestras de alimentos que se requiera realizar método
PRT-712.02-037 Página 1 de 8 1. OBJETIVO Enumerar los microorganismos E. coli presentes en una muestra de alimento 2. CAMPO DE APLICACIÓN Y ALCANCE Muestras de alimentos que se requiera realizar método
PROCEDIMIENTO RECUENTO DE LACTOBACILLUS BULGARICUS Y STREPTOCOCCUS THERMOPHILUS EN YOGURT. APHA 17 Edición, modificado. PRT-712.02-047 Página 1 de 8
 PRT-712.02-047 Página 1 de 8 1. OBJETIVO Conocer el número de Lactobacillus bulgaricus y Streptococcus thermophilus (microorganismos característicos del yogurt) presentes en una muestra de yogurt. 2. CAMPO
PRT-712.02-047 Página 1 de 8 1. OBJETIVO Conocer el número de Lactobacillus bulgaricus y Streptococcus thermophilus (microorganismos característicos del yogurt) presentes en una muestra de yogurt. 2. CAMPO
Título de la gráfica: Crecimiento/ No crecimiento
 Resultados de la semana anterior (TSB) Título de la gráfica: # tubo TSB 1-24 Crecimiento/ No crecimiento Descripción del crecimiento Resultados de la semana anterior (TSA slant) Título de la gráfica: tubo
Resultados de la semana anterior (TSB) Título de la gráfica: # tubo TSB 1-24 Crecimiento/ No crecimiento Descripción del crecimiento Resultados de la semana anterior (TSA slant) Título de la gráfica: tubo
1. LEVINE EMB AGAR FOTO 6. Medios de cultivo Levine EMG Agar.
 1. LEVINE EMB AGAR. El Agar EMB Levine es un medio selectivo y diferencial, adecuado para el crecimiento de Enterobacterias. Es un medio adecuado para la búsqueda y diferenciación de bacilos entéricos,
1. LEVINE EMB AGAR. El Agar EMB Levine es un medio selectivo y diferencial, adecuado para el crecimiento de Enterobacterias. Es un medio adecuado para la búsqueda y diferenciación de bacilos entéricos,
RECOPILADO POR: EL PROGRAMA UNIVERSITARIO DE ALIMENTOS
 NMX-F-310-1978. DETERMINACIÓN DE CUENTA DE STAPHYLOCOCCUS AUREUS COAGULASA POSITIVA, EN ALIMENTOS. METHOD OF TEST FOR COUNT OF STAPHYLOCOCCUS AUREUS IN FOOD. NORMAS MEXICANAS. DIRECCIÓN GENERAL DE NORMAS.
NMX-F-310-1978. DETERMINACIÓN DE CUENTA DE STAPHYLOCOCCUS AUREUS COAGULASA POSITIVA, EN ALIMENTOS. METHOD OF TEST FOR COUNT OF STAPHYLOCOCCUS AUREUS IN FOOD. NORMAS MEXICANAS. DIRECCIÓN GENERAL DE NORMAS.
PROCEDIMIENTO METODO DE RECUENTO EN PLACA DIRECTO STAPHYLOCOCCUS AUREUS BAM ON LINE 2001
 PRT-712.02-024 Página 1 de 13 1. OBJETIVO Detectar el número de unidades formadoras de colonias (ufc.) de S. aureus presentes en muestras de alimentos y agua 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este
PRT-712.02-024 Página 1 de 13 1. OBJETIVO Detectar el número de unidades formadoras de colonias (ufc.) de S. aureus presentes en muestras de alimentos y agua 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este
PROCEDIMIENTO DE METODO CUALITATIVO DE DETECCION DE SHIGELLA SPP EN MATRIZ AGUA
 PRT-712.02-065 Página 1 de 5 1. OBJETIVO Detectar en forma cualitativa la presencia de Shigella spp en muestras de aguas. 2. CAMPO DE APLICACIÓN Y ALCANCE Este procedimiento es aplicable a las muestras
PRT-712.02-065 Página 1 de 5 1. OBJETIVO Detectar en forma cualitativa la presencia de Shigella spp en muestras de aguas. 2. CAMPO DE APLICACIÓN Y ALCANCE Este procedimiento es aplicable a las muestras
DEGRADACIÓN DE LA LACTOSA POR LACTOBACILUS HASTA ÁCIDO LÁCTICO
 DEGRADACIÓN DE LA LACTOSA POR LACTOBACILUS HASTA ÁCIDO LÁCTICO I. INTRODUCCIÓN Los organismos aerobios así como los anaerobios rompen la molécula de glucosa para su catalización, este camino es usado,
DEGRADACIÓN DE LA LACTOSA POR LACTOBACILUS HASTA ÁCIDO LÁCTICO I. INTRODUCCIÓN Los organismos aerobios así como los anaerobios rompen la molécula de glucosa para su catalización, este camino es usado,
Universidad Nacional de Ingeniería UNI Norte. Métodos de detección de contaminación microbiana
 Universidad Nacional de Ingeniería UNI Norte Curso: Un enfoque práctico para la inocuidad de los alimentos Métodos de detección de contaminación microbiana iciar el explorador Internet Explorer.lnk Facilitadoras
Universidad Nacional de Ingeniería UNI Norte Curso: Un enfoque práctico para la inocuidad de los alimentos Métodos de detección de contaminación microbiana iciar el explorador Internet Explorer.lnk Facilitadoras
Petrifilm. Placas para Recuento de E. coli y Coliformes. Guía de Interpretación. E. coli : E. coli es capaz de crecer en medios conteniendo
 Guía de Interpretación Petrifilm Placas para Recuento de E. coli y Coliformes Esta guía sirve para familiarizarse con los resultados obtenidos en las placas M Petrifilm para Recuento de E. coli y Coliformes
Guía de Interpretación Petrifilm Placas para Recuento de E. coli y Coliformes Esta guía sirve para familiarizarse con los resultados obtenidos en las placas M Petrifilm para Recuento de E. coli y Coliformes
PRACTICA Núm. 17 COLIFORMES TOTALES Y FECALES EN AGUA DE CONSUMO HUMANO
 PRACTICA Núm. 17 COLIFORMES TOTALES Y FECALES EN AGUA DE CONSUMO HUMANO I. OBJETIVO Investigar la presencia de bacterias del grupo Coliforme en agua de consumo humano mediante la técnica del Número Más
PRACTICA Núm. 17 COLIFORMES TOTALES Y FECALES EN AGUA DE CONSUMO HUMANO I. OBJETIVO Investigar la presencia de bacterias del grupo Coliforme en agua de consumo humano mediante la técnica del Número Más
DETERMINACIÓN DIOXIDO DE AZUFRE TOTAL EN ALIMENTOS DESHIDRATADOS Método Monier-Williams modificado ME
 DETERMINACIÓN DIOXIDO DE AZUFRE TOTAL EN ALIMENTOS DESHIDRATADOS Página 1 de 6 1. OBJETIVO Determinar dióxido de azufre total en alimentos deshidratados por método Monier-Williams modificado. 2. CAMPO
DETERMINACIÓN DIOXIDO DE AZUFRE TOTAL EN ALIMENTOS DESHIDRATADOS Página 1 de 6 1. OBJETIVO Determinar dióxido de azufre total en alimentos deshidratados por método Monier-Williams modificado. 2. CAMPO
PROCEDIMIENTO ENUMERACION LISTERIA MONOCYTOGENES EN ALIMENTOS ISO 11290-2. MODIFICADO. PRT-712.02-093 Página 1 de 20
 PRT-712.02-093 Página 1 de 20 1. OBJETIVO Determinar el número de unidades formadoras de colonias (UFC) de Listeria monocytogenes en matrices de alimentos. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicable a
PRT-712.02-093 Página 1 de 20 1. OBJETIVO Determinar el número de unidades formadoras de colonias (UFC) de Listeria monocytogenes en matrices de alimentos. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicable a
BIORREACTRES. Estudios básicos y aplicados sobre procesos de fermentación
 BIORREACTRES Ing. en Alimentos Estudios básicos y aplicados sobre procesos de fermentación Mg. Anahí V. Cuellas Docente investigadora Universidad Nacional de Quilmes TRABAJO PRACTICO Obtención de enzimas
BIORREACTRES Ing. en Alimentos Estudios básicos y aplicados sobre procesos de fermentación Mg. Anahí V. Cuellas Docente investigadora Universidad Nacional de Quilmes TRABAJO PRACTICO Obtención de enzimas
MICROBIOLOGIA APLICADA Manual de Laboratorio APENDICE C PREPARACION DE SOLUCIONES Y REACTIVOS
 APENDICE C PREPARACION DE SOLUCIONES Y REACTIVOS 200 1. AGUA DE DILUCION CON SOLUCION BUFFER. Solución I Disolver 34 g de fosfato monobásico de potasio (KH 2 PO 4 ) en 500 ml de agua destilada. Ajustar
APENDICE C PREPARACION DE SOLUCIONES Y REACTIVOS 200 1. AGUA DE DILUCION CON SOLUCION BUFFER. Solución I Disolver 34 g de fosfato monobásico de potasio (KH 2 PO 4 ) en 500 ml de agua destilada. Ajustar
APÉNDICE G. Identificación bioquímica de enterobacterias por el sistema API 20E
 APÉNDICE G Identificación bioquímica de enterobacterias por el sistema API 20E OBJETIVO: - Establecer la metodología en la identificación de enterobacterias por medio de pruebas bioquímicas estandarizadas
APÉNDICE G Identificación bioquímica de enterobacterias por el sistema API 20E OBJETIVO: - Establecer la metodología en la identificación de enterobacterias por medio de pruebas bioquímicas estandarizadas
PRÁCTICAS DE MICROBIOLOGÍA CLÍNICA (CURSO )
 PRÁCTICAS DE MICROBIOLOGÍA CLÍNICA (CURSO 2012 2013) PRÁCTICAS A REALIZAR ANÁLISIS CUALITATIVO DE ORINA PRUEBA DE BAUER KIRBY (ANTIBIOGRAMA) PRUEBA DE EPSILON (DETERMINACIÓN DE LA CMI) ANÁLISIS CUALITATIVO
PRÁCTICAS DE MICROBIOLOGÍA CLÍNICA (CURSO 2012 2013) PRÁCTICAS A REALIZAR ANÁLISIS CUALITATIVO DE ORINA PRUEBA DE BAUER KIRBY (ANTIBIOGRAMA) PRUEBA DE EPSILON (DETERMINACIÓN DE LA CMI) ANÁLISIS CUALITATIVO
DANAGENE BLOOD DNA KIT
 Ref. 0601 100 ml Ref. 0602 200 ml DANAGENE BLOOD DNA KIT 1.INTRODUCCION DANAGENE BLOOD DNA Kit provee un método para la extracción de ADN genómico de alta calidad a partir de sangre total o médula ósea.
Ref. 0601 100 ml Ref. 0602 200 ml DANAGENE BLOOD DNA KIT 1.INTRODUCCION DANAGENE BLOOD DNA Kit provee un método para la extracción de ADN genómico de alta calidad a partir de sangre total o médula ósea.
Miel de abejas - Determinación de Clostridium sulfitoreductores
 Vencimiento consulta pública: 2007.09.07 PROYECTO DE NORMA EN CONSULTA PUBLICA NCh3123.c2007 Miel de abejas - Determinación de Clostridium sulfitoreductores - Método de recuento Preámbulo El Instituto
Vencimiento consulta pública: 2007.09.07 PROYECTO DE NORMA EN CONSULTA PUBLICA NCh3123.c2007 Miel de abejas - Determinación de Clostridium sulfitoreductores - Método de recuento Preámbulo El Instituto
TRANSFERENCIAS ASÉPTICAS
 Introducción Objetivo Procedimiento Trabajo Práctico Nº 3 TRANSFERENCIAS ASÉPTICAS Resultados Observaciones Bibliografía INTRODUCCIÓN La inoculación de medios de cultivo y la manipulación de cultivos microbianos
Introducción Objetivo Procedimiento Trabajo Práctico Nº 3 TRANSFERENCIAS ASÉPTICAS Resultados Observaciones Bibliografía INTRODUCCIÓN La inoculación de medios de cultivo y la manipulación de cultivos microbianos
DETERMINACION DE BACTERIAS COLIFORMES: COLIMETRIA
 DETERMINACION DE BACTERIAS COLIFORMES: COLIMETRIA En esta práctica, vamos a centrarnos en determinar las bacterias coliformes presentes en un agua mediante el Método de los tubos múltiples ó colimetria
DETERMINACION DE BACTERIAS COLIFORMES: COLIMETRIA En esta práctica, vamos a centrarnos en determinar las bacterias coliformes presentes en un agua mediante el Método de los tubos múltiples ó colimetria
8. PRUEBAS DE SUSCEPTIBILIDAD PARA Mycobacterium tuberculosis. Estudios científicos han determinado que al menos el 1 % de los bacilos tuberculosos
 8. PRUEBAS DE SUSCEPTIBILIDAD PARA Mycobacterium tuberculosis. Estudios científicos han determinado que al menos el 1 % de los bacilos tuberculosos de un paciente determinado son resistentes in Vitro a
8. PRUEBAS DE SUSCEPTIBILIDAD PARA Mycobacterium tuberculosis. Estudios científicos han determinado que al menos el 1 % de los bacilos tuberculosos de un paciente determinado son resistentes in Vitro a
USO: MEDIO ENRIQUECIDO QUE PERMITE EL CRECIMIENTO DE MICROORGANISMOS EXIGENTES COMO HAEMOPHILUS, NEISSERIA Y LISTERIA.
 AGAR CHOCOLATE SUPLEMENTADO USO: MEDIO ENRIQUECIDO QUE PERMITE EL CRECIMIENTO DE MICROORGANISMOS EXIGENTES COMO HAEMOPHILUS, NEISSERIA Y LISTERIA. AGAR 10.0 g FOSFATO DIPOTASICO ALMIDON DE 1.0 g FOSFATO
AGAR CHOCOLATE SUPLEMENTADO USO: MEDIO ENRIQUECIDO QUE PERMITE EL CRECIMIENTO DE MICROORGANISMOS EXIGENTES COMO HAEMOPHILUS, NEISSERIA Y LISTERIA. AGAR 10.0 g FOSFATO DIPOTASICO ALMIDON DE 1.0 g FOSFATO
Taxonomía bacteriana
 Página 1 Unidad Temática 5 Taxonomía bacteriana (Guía de estudio) Benintende, S; Sánchez, C., Sterren, M. Y Musante, C Objetivo El objetivo de la Taxonomía bacteriana es dar un ordenamiento de las unidades
Página 1 Unidad Temática 5 Taxonomía bacteriana (Guía de estudio) Benintende, S; Sánchez, C., Sterren, M. Y Musante, C Objetivo El objetivo de la Taxonomía bacteriana es dar un ordenamiento de las unidades
INFORME DE RESULTADOS
 INFORME DE RESULTADOS Los análisis realizados al producto con Aloe vera, se desarrollaron de acuerdo a lo establecido en CCAYAC-P-062, para determinar la dilución correspondiente con las 3 cepas analizadas
INFORME DE RESULTADOS Los análisis realizados al producto con Aloe vera, se desarrollaron de acuerdo a lo establecido en CCAYAC-P-062, para determinar la dilución correspondiente con las 3 cepas analizadas
NORMA Oficial Mexicana NOM-112-SSA1-1994, Bienes y servicios. Determinación de bacterias coliformes. Técnica del número más probable.
 10-19-95 NORMA Oficial Mexicana NOM-112-SSA1-1994, Bienes y servicios. Determinación de bacterias coliformes. Técnica del número más probable. Al margen un sello con el Escudo Nacional, que dice: Estados
10-19-95 NORMA Oficial Mexicana NOM-112-SSA1-1994, Bienes y servicios. Determinación de bacterias coliformes. Técnica del número más probable. Al margen un sello con el Escudo Nacional, que dice: Estados
PRÁCTICA Nº 2 OPERACIONES COMUNES EN UN LABORATORIO
 PRÁCTICA Nº 2 OPERACIONES COMUNES EN UN LABORATORIO OBJETIVO Utilizar el material de laboratorio en las operaciones más comunes realizadas en un laboratorio de química. I. ASPECTOS TEÓRICOS Una vez conocido
PRÁCTICA Nº 2 OPERACIONES COMUNES EN UN LABORATORIO OBJETIVO Utilizar el material de laboratorio en las operaciones más comunes realizadas en un laboratorio de química. I. ASPECTOS TEÓRICOS Una vez conocido
RepublicofEcuador EDICTOFGOVERNMENT±
 RepublicofEcuador EDICTOFGOVERNMENT± Inordertopromotepubliceducationandpublicsafety,equaljusticeforal, abeterinformedcitizenry,theruleoflaw,worldtradeandworldpeace, thislegaldocumentisherebymadeavailableonanoncommercialbasis,asit
RepublicofEcuador EDICTOFGOVERNMENT± Inordertopromotepubliceducationandpublicsafety,equaljusticeforal, abeterinformedcitizenry,theruleoflaw,worldtradeandworldpeace, thislegaldocumentisherebymadeavailableonanoncommercialbasis,asit
PREPARACION DE MEDIOS DE CULTIVO
 PREPARACION DE MEDIOS DE CULTIVO MEDIOS DE CULTIVO Un medio de cultivo es un conjunto de nutrientes, factores de crecimiento y otros componentes que crean las condiciones necesarias para el desarrollo
PREPARACION DE MEDIOS DE CULTIVO MEDIOS DE CULTIVO Un medio de cultivo es un conjunto de nutrientes, factores de crecimiento y otros componentes que crean las condiciones necesarias para el desarrollo
RECONOCIMIENTO DE LOS PRINCIPIOS INMEDIATOS QUE HAY EN UN ALIMENTO
 RECONOCIMIENTO DE LOS PRINCIPIOS INMEDIATOS QUE HAY EN UN ALIMENTO Fundamento Los alimentos se diferencian entre sí por las sustancias o principios inmediatos que contienen y por la cantidad de cada uno
RECONOCIMIENTO DE LOS PRINCIPIOS INMEDIATOS QUE HAY EN UN ALIMENTO Fundamento Los alimentos se diferencian entre sí por las sustancias o principios inmediatos que contienen y por la cantidad de cada uno
Bacillus cereus. Introducción.
 Bacillus cereus Introducción. Es un bacilo formador de esporas responsable de intoxicaciones alimentarias, siendo su hábitat natural el suelo, contamina con frecuencia cereales, leche, budines, cremas
Bacillus cereus Introducción. Es un bacilo formador de esporas responsable de intoxicaciones alimentarias, siendo su hábitat natural el suelo, contamina con frecuencia cereales, leche, budines, cremas
RepublicofEcuador EDICTOFGOVERNMENT±
 RepublicofEcuador EDICTOFGOVERNMENT± Inordertopromotepubliceducationandpublicsafety,equaljusticeforal, abeterinformedcitizenry,theruleoflaw,worldtradeandworldpeace, thislegaldocumentisherebymadeavailableonanoncommercialbasis,asit
RepublicofEcuador EDICTOFGOVERNMENT± Inordertopromotepubliceducationandpublicsafety,equaljusticeforal, abeterinformedcitizenry,theruleoflaw,worldtradeandworldpeace, thislegaldocumentisherebymadeavailableonanoncommercialbasis,asit
ANEXO 1 Medios de cultivo y reconstitución de cepas
 conservamos 31 ANEXO 1 Medios de cultivo y reconstitución de cepas Agar tripticasa de soya (TSA) -Triptona, digestión pancreática de caseína -Peptona de soya, digestión pancreática de harina de soya -Cloruro
conservamos 31 ANEXO 1 Medios de cultivo y reconstitución de cepas Agar tripticasa de soya (TSA) -Triptona, digestión pancreática de caseína -Peptona de soya, digestión pancreática de harina de soya -Cloruro
Trabajo Práctico N 3. Reconocimiento de sustancias ácidas, básicas y neutras. mediante el empleo de indicadores químicos.
 Trabajo Práctico N 3 Reconocimiento de sustancias ácidas, básicas y neutras mediante el empleo de indicadores químicos. Objetivos: Diferenciar mediante el empleo de indicadores u el cambio de color de
Trabajo Práctico N 3 Reconocimiento de sustancias ácidas, básicas y neutras mediante el empleo de indicadores químicos. Objetivos: Diferenciar mediante el empleo de indicadores u el cambio de color de
UNIVERSIDAD TECNOLOGICA NACIONAL
 UNIVERSIDAD TECNOLOGICA NACIONAL FACULTAD REGIONAL ROSARIO DEPARTAMENTO DE INGENIERIA QUIMICA CATEDRA DE BIOTECNOLOGIA Trabajo práctico n 3 Siembra y recuento de microorganismos. 2009 Jefe de Cátedra:
UNIVERSIDAD TECNOLOGICA NACIONAL FACULTAD REGIONAL ROSARIO DEPARTAMENTO DE INGENIERIA QUIMICA CATEDRA DE BIOTECNOLOGIA Trabajo práctico n 3 Siembra y recuento de microorganismos. 2009 Jefe de Cátedra:
DESCRIPCION DE BIOCOUNTER
 DESCRIPCION DE BIOCOUNTER BIOCOUNTER es un Laminocultivo para Control Microbiológico Industrial utilizado ampliamente en el campo alimentario y áreas relacionadas. El análisis microbiológico realizado
DESCRIPCION DE BIOCOUNTER BIOCOUNTER es un Laminocultivo para Control Microbiológico Industrial utilizado ampliamente en el campo alimentario y áreas relacionadas. El análisis microbiológico realizado
PROCEDIMIENTO RECUENTO DE MICROORGANISMOS HETEROTROFOS EN PLACA. METODO STANDARD METHODS FOR EXAMINATION OF WATER AND WASTEWATER
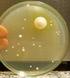 PRT- 712.02-072 Página 1 de 15 1. OBJETIVO Conocer el número de microorganismos heterotróficos viables que contiene una muestra de agua de diálisis para verificar la calidad bacteriológica especificada
PRT- 712.02-072 Página 1 de 15 1. OBJETIVO Conocer el número de microorganismos heterotróficos viables que contiene una muestra de agua de diálisis para verificar la calidad bacteriológica especificada
PROCEDIMIENTO RECUENTO DE CLOSTRIDIUM PERFRINGENS PRT-712.04-034
 Página 1 de 15 1. OBJETIVO Detectar el número de unidades formadoras de colonias de Clostridium perfringens en alimentos. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a los alimentos en
Página 1 de 15 1. OBJETIVO Detectar el número de unidades formadoras de colonias de Clostridium perfringens en alimentos. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicar este procedimiento a los alimentos en
MICROBIOLOGÍA DE ALIMENTOS. Resumen de las prácticas de Microbiología de Alimentos
 MICROBIOLOGÍA DE ALIMENTOS Resumen de las prácticas de Microbiología de Alimentos 1 Ingeniero Técnico Agrícola Industrias Agrarias y Alimentarias CURSO 2004-2005 Profesora: Cristina Solano Goñi e-mail:
MICROBIOLOGÍA DE ALIMENTOS Resumen de las prácticas de Microbiología de Alimentos 1 Ingeniero Técnico Agrícola Industrias Agrarias y Alimentarias CURSO 2004-2005 Profesora: Cristina Solano Goñi e-mail:
MGA LÍMITES MICROBIANOS
 EL TEXTO EN COLOR ROJO HA SIDO MODIFICADO Con fundamento en el numeral 4.11.1 de la Norma Oficial Mexicana NOM-001-SSA1-2010, se publica el presente proyecto a efecto de que los interesados, a partir del
EL TEXTO EN COLOR ROJO HA SIDO MODIFICADO Con fundamento en el numeral 4.11.1 de la Norma Oficial Mexicana NOM-001-SSA1-2010, se publica el presente proyecto a efecto de que los interesados, a partir del
2. Observación de hongos de interés industrial
 2. Observación de hongos de interés industrial En esta práctica se realizarán observaciones en fresco de varios hongos de interés industrial. 2.1 Preparaciones para el estudio microscópico de los aislados
2. Observación de hongos de interés industrial En esta práctica se realizarán observaciones en fresco de varios hongos de interés industrial. 2.1 Preparaciones para el estudio microscópico de los aislados
TEMA 12. Pruebas de sensibilidad a los antimicrobianos
 TEMA 12 Pruebas de sensibilidad a los antimicrobianos Tema 12. Pruebas de sensibilidad a los antimicrobianos 1. Nacimiento de la era de los antibióticos 2. Pruebas de sensibilidad a los antimicrobianos
TEMA 12 Pruebas de sensibilidad a los antimicrobianos Tema 12. Pruebas de sensibilidad a los antimicrobianos 1. Nacimiento de la era de los antibióticos 2. Pruebas de sensibilidad a los antimicrobianos
PRACTICA Núm. 21 RECUENTO DE INDICADORES DE CONTAMINACION FECAL EN AGUA MEDIANTE FILTRACION POR MEMBRANA
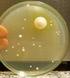 PRAICA Núm. 21 RECUENTO DE INDICADORES DE CONTAMINACION FECAL EN AGUA MEDIANTE FILTRACION POR MEMBRANA I. OBJETIVO Efectuar el recuento de Indicadores de contaminación fecal en diferentes tipos de agua.
PRAICA Núm. 21 RECUENTO DE INDICADORES DE CONTAMINACION FECAL EN AGUA MEDIANTE FILTRACION POR MEMBRANA I. OBJETIVO Efectuar el recuento de Indicadores de contaminación fecal en diferentes tipos de agua.
NMX-F-254-1977. CUENTA DE ORGANISMOS COLIFORMES. COLIFORM ORGANISMS COUNT. NORMAS MEXICANAS. DIRECCIÓN GENERAL DE NORMAS.
 NMX-F-54-977. CUENTA DE ORGANISMOS COLIFORMES. COLIFORM ORGANISMS COUNT. NORMAS MEXICANAS. DIRECCIÓN GENERAL DE NORMAS. PREFACIO. En la elaboración de la presente Norma participaron los siguientes Organismos:
NMX-F-54-977. CUENTA DE ORGANISMOS COLIFORMES. COLIFORM ORGANISMS COUNT. NORMAS MEXICANAS. DIRECCIÓN GENERAL DE NORMAS. PREFACIO. En la elaboración de la presente Norma participaron los siguientes Organismos:
UNIVERSIDAD NACIONAL DE COLOMBIA FACULTAD DE MEDICINA DEPARTAMENTO DE MICROBIOLOGIA PRACTICAS DE LABORATORIO COCOS GRAM POSITIVOS
 UNIVERSIDAD NACIONAL DE COLOMBIA FACULTAD DE MEDICINA DEPARTAMENTO DE MICROBIOLOGIA PRACTICAS DE LABORATORIO COCOS GRAM POSITIVOS Maye Bernal Rivera Introducción Los cocos gram positivos excluyendo las
UNIVERSIDAD NACIONAL DE COLOMBIA FACULTAD DE MEDICINA DEPARTAMENTO DE MICROBIOLOGIA PRACTICAS DE LABORATORIO COCOS GRAM POSITIVOS Maye Bernal Rivera Introducción Los cocos gram positivos excluyendo las
GUÍA REALIZACIÓN DE CULTIVOS MICROBIOLÓGICOS
 ESCUELA DE SALUD GUÍA REALIZACIÓN DE CULTIVOS MICROBIOLÓGICOS DIRIGIDO A ALUMNOS DE: Técnico de laboratorio Clínico y Banco de Sangre Técnico de Enfermería Técnico de Radiodiagnóstico y Radioterapia Informática
ESCUELA DE SALUD GUÍA REALIZACIÓN DE CULTIVOS MICROBIOLÓGICOS DIRIGIDO A ALUMNOS DE: Técnico de laboratorio Clínico y Banco de Sangre Técnico de Enfermería Técnico de Radiodiagnóstico y Radioterapia Informática
Técnicas de monitoreo para la detección de microorganismos en el medio ambiente
 Técnicas de monitoreo para la detección de microorganismos en el medio ambiente Gloria Alicia Figueroa Aguilar Condiciones Ambientales REQUISITO: El laboratorio debe asegurarse que las condiciones ambientales,
Técnicas de monitoreo para la detección de microorganismos en el medio ambiente Gloria Alicia Figueroa Aguilar Condiciones Ambientales REQUISITO: El laboratorio debe asegurarse que las condiciones ambientales,
Cuenta en placa de bacterias
 Análisis Microbiológico de Alimentos. 2ª ed. Facultad de Química,. México. Cuenta en placa de bacterias OBJETIVOS Realizar adecuadamente la técnica de cuenta en placa para diversos grupos microbianos de
Análisis Microbiológico de Alimentos. 2ª ed. Facultad de Química,. México. Cuenta en placa de bacterias OBJETIVOS Realizar adecuadamente la técnica de cuenta en placa para diversos grupos microbianos de
METODO DE FILTRACIÓN POR MEMBRANA PARA DETERMINACION DE COLIFORMES Y E. coli EN AGUA
 PRT-712.03-009 Página 1 de 7 1. OBJETIVO Este método se utiliza para medir la calidad sanitaria del agua potable. 2. CAMPO DE APLICACIÓN Y ALCANCE Se aplica a agua clorada o agua naturales de muy baja
PRT-712.03-009 Página 1 de 7 1. OBJETIVO Este método se utiliza para medir la calidad sanitaria del agua potable. 2. CAMPO DE APLICACIÓN Y ALCANCE Se aplica a agua clorada o agua naturales de muy baja
UNIVERSIDAD INTERAMERICANA DE PUERTO RICO RECINTO DE ARECIBO DEPARTAMENTO DE CIENCIAS Y TECNOLOGÍA BIOL 3405: LABORATORIO DE INMUNOLOGÍA
 UNIVERSIDAD INTERAMERICANA DE PUERTO RICO RECINTO DE ARECIBO DEPARTAMENTO DE CIENCIAS Y TECNOLOGÍA BIOL 3405: LABORATORIO DE INMUNOLOGÍA I. TÍTULO Dilución II. OBJETIVOS Repasar el concepto de dilución
UNIVERSIDAD INTERAMERICANA DE PUERTO RICO RECINTO DE ARECIBO DEPARTAMENTO DE CIENCIAS Y TECNOLOGÍA BIOL 3405: LABORATORIO DE INMUNOLOGÍA I. TÍTULO Dilución II. OBJETIVOS Repasar el concepto de dilución
PROCEDIMIENTO PARA IDENTIFICACION BIOQUIMICA DE CEPAS DE LISTERIA MONOCYTOGENES AISLADAS EN ALIMENTOS Y AMBIENTE
 PRT-712.03-086 Página 1 de 15 1. OBJETIVO Obtener confirmación mediante la caracterización bioquímica de cepas aisladas y presuntivas de Listeria monocytogenes. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicable
PRT-712.03-086 Página 1 de 15 1. OBJETIVO Obtener confirmación mediante la caracterización bioquímica de cepas aisladas y presuntivas de Listeria monocytogenes. 2. CAMPO DE APLICACIÓN Y ALCANCE Aplicable
CONTROL HIGIENICO DE PRODUCTOS NO OBLIGATORIAMENTE ESTERILES. FUENTE: Centro de Documentación e Información del Ministerio de Economía - Argentina
 CONTROL HIGIENICO DE PRODUCTOS NO OBLIGATORIAMENTE ESTERILES FUENTE: Centro de Documentación e Información del Ministerio de Economía - Argentina En este artículo se especifican los ensayos necesarios
CONTROL HIGIENICO DE PRODUCTOS NO OBLIGATORIAMENTE ESTERILES FUENTE: Centro de Documentación e Información del Ministerio de Economía - Argentina En este artículo se especifican los ensayos necesarios
o Solución de KOH al 0,01% Disolver el colorante en el alcohol, y añadir la solución de KOH
 OBSERVACIÓN DE LAS BACTERIAS TINCIÓN SENCILLA 1.- Material necesario Cultivo bacteriano de 24 horas, en medio sólido Portaobjetos limpios y desengrasados Frasco lavador con agua de grifo o destilada Asa
OBSERVACIÓN DE LAS BACTERIAS TINCIÓN SENCILLA 1.- Material necesario Cultivo bacteriano de 24 horas, en medio sólido Portaobjetos limpios y desengrasados Frasco lavador con agua de grifo o destilada Asa
PRACTICA No.9 REACCIONES QUIMICAS I
 PRACTICA No.9 REACCIONES QUIMICAS I INTRODUCCION: Las transformaciones de la materia se conocen como REACCIONES QUIMICAS. En ellas se opera un cambio en la estructura íntima de las sustancias reaccionantes
PRACTICA No.9 REACCIONES QUIMICAS I INTRODUCCION: Las transformaciones de la materia se conocen como REACCIONES QUIMICAS. En ellas se opera un cambio en la estructura íntima de las sustancias reaccionantes
Placas Petrifilm. para el Recuento de Coliformes. Guía de interpretación
 Placas Petrifilm para el Recuento de Coliformes Guía de interpretación Esta guía lo familiarizará con los resultados de las Placas Petrifilm TM para Recuento de Coliformes. Para mayor información, contacte
Placas Petrifilm para el Recuento de Coliformes Guía de interpretación Esta guía lo familiarizará con los resultados de las Placas Petrifilm TM para Recuento de Coliformes. Para mayor información, contacte
ESTUDIO MICROSCÓPICO DE LAS BACTERIAS DEL YOGUR
 ESTUDIO MICROSCÓPICO DE LAS BACTERIAS DEL YOGUR 1- Prepara un portaobjetos bien limpio con una gota de agua. 2 - Coge una porción pequeña de yogur con un palillo o una aguja enmangada y hacer una extensión
ESTUDIO MICROSCÓPICO DE LAS BACTERIAS DEL YOGUR 1- Prepara un portaobjetos bien limpio con una gota de agua. 2 - Coge una porción pequeña de yogur con un palillo o una aguja enmangada y hacer una extensión
UNIVERSIDAD DE MAYORES PRÁCTICAS DE MICROBIOLOGÍA DEPARTAMENTO DE BIOMEDICINA Y BIOTECNOLOGÍA MICROBIOLOGÍA I
 UNIVERSIDAD DE MAYORES PRÁCTICAS DE MICROBIOLOGÍA DEPARTAMENTO DE BIOMEDICINA Y BIOTECNOLOGÍA MICROBIOLOGÍA I DRAS. MARÍA LUISA ORTIZ Y ANA PEDREGOSA 1 PRÁCTICAS DE MICROBIOLOGÍA DEPARTAMENTO DE BIOMEDICINA
UNIVERSIDAD DE MAYORES PRÁCTICAS DE MICROBIOLOGÍA DEPARTAMENTO DE BIOMEDICINA Y BIOTECNOLOGÍA MICROBIOLOGÍA I DRAS. MARÍA LUISA ORTIZ Y ANA PEDREGOSA 1 PRÁCTICAS DE MICROBIOLOGÍA DEPARTAMENTO DE BIOMEDICINA
F-CGPEGI-CC-01/REV-00
 F-CGPEGI-CC-01/REV-00 UNIVERSIDAD AUTONOMA DE YUCATAN FACULTAD DE MEDICINA LABORATORIO DE CIENCIAS FISIOLOGICAS MANUAL DE PREPARACIÓN DE REACTIVOS RESPONSABLE DEL LABORATORIO DE CIENCIAS FISIOLOGICAS Q.
F-CGPEGI-CC-01/REV-00 UNIVERSIDAD AUTONOMA DE YUCATAN FACULTAD DE MEDICINA LABORATORIO DE CIENCIAS FISIOLOGICAS MANUAL DE PREPARACIÓN DE REACTIVOS RESPONSABLE DEL LABORATORIO DE CIENCIAS FISIOLOGICAS Q.
UNIVERSIDAD AUTONOMA DE CHIAPAS FACULTAD DE CIENCIAS QUIMICAS CAMPUS IV OCOZOCOAUTLA DE ESPINOZA. LABORATORIO DE BIOLOGIA CELULAR
 UNIVERSIDAD AUTONOMA DE CHIAPAS FACULTAD DE CIENCIAS QUIMICAS CAMPUS IV OCOZOCOAUTLA DE ESPINOZA. LABORATORIO DE BIOLOGIA CELULAR Catedrático: Dra. Ana Olivia cañas Urbina. PRACTICA No. 3: TINCIONES Equipo:
UNIVERSIDAD AUTONOMA DE CHIAPAS FACULTAD DE CIENCIAS QUIMICAS CAMPUS IV OCOZOCOAUTLA DE ESPINOZA. LABORATORIO DE BIOLOGIA CELULAR Catedrático: Dra. Ana Olivia cañas Urbina. PRACTICA No. 3: TINCIONES Equipo:
Dr. Oscar Gutiérrez Coronado Microbiologia Práctica No. 1 Preparación y esterilización de materiales y medios de cultivo
 Dr. Oscar Gutiérrez Coronado Microbiologia Práctica No. 1 Preparación y esterilización de materiales y medios de cultivo Objetivos. Que el alumno conozca los principios generales de las técnicas de esterilización
Dr. Oscar Gutiérrez Coronado Microbiologia Práctica No. 1 Preparación y esterilización de materiales y medios de cultivo Objetivos. Que el alumno conozca los principios generales de las técnicas de esterilización
PROCEDIMIENTO RECUENTO MOHOS Y LEVADURAS EN ALIMENTOS NORMA ISO 7954. 1. OBJETIVO Conocer el número de Mohos y Levaduras que contiene un alimento.
 PRT- 712.02-031 Página 1 de 14 1. OBJETIVO Conocer el número de Mohos y Levaduras que contiene un alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Este procedimiento se aplica a todos los alimentos de consumos
PRT- 712.02-031 Página 1 de 14 1. OBJETIVO Conocer el número de Mohos y Levaduras que contiene un alimento. 2. CAMPO DE APLICACIÓN Y ALCANCE Este procedimiento se aplica a todos los alimentos de consumos
INSTRUMENTOS BÁSICOS DE UN LABORATORIO
 INSTRUMENTOS BÁSICOS DE UN LABORATORIO Trasfondo y Contenido En un laboratorio se utiliza una amplia variedad de instrumentos o herramientas que, en su conjunto, se denominan material de laboratorio. Pueden
INSTRUMENTOS BÁSICOS DE UN LABORATORIO Trasfondo y Contenido En un laboratorio se utiliza una amplia variedad de instrumentos o herramientas que, en su conjunto, se denominan material de laboratorio. Pueden
Aplicación a escala de laboratorio
 Aplicación a escala de laboratorio Índice de contenidos Velcorin Aplicación a escala de laboratorio págs. 3 5 Introducción pág. 3 Medidas de precaución pág. 3 Método de trabajo (sensorial) pág. 4 Método
Aplicación a escala de laboratorio Índice de contenidos Velcorin Aplicación a escala de laboratorio págs. 3 5 Introducción pág. 3 Medidas de precaución pág. 3 Método de trabajo (sensorial) pág. 4 Método
PRACTICA Nº 6 GLUCÓSIDOS CARDIOTÓNICOS Y SAPONINAS
 PRACTICA Nº 6 GLUCÓSIDOS CARDIOTÓNICOS Y SAPONINAS GLICÓSIDOS CARDIOTÓNICOS La valoración de glicósidos se puede realizar por los siguientes métodos: Por pesada directa del glicósido aislado, Por colorimetría,
PRACTICA Nº 6 GLUCÓSIDOS CARDIOTÓNICOS Y SAPONINAS GLICÓSIDOS CARDIOTÓNICOS La valoración de glicósidos se puede realizar por los siguientes métodos: Por pesada directa del glicósido aislado, Por colorimetría,
PRÁCTICA No. 7 DETERMINACIÓN DE COLIFORMES TOTALES Y FECALES EN AGUA RESIDUAL POR EL MÉTODO DEL NUMERO MAS PROBABLE (NMP)
 PRÁCTICA No. 7 DETERMINACIÓN DE COLIFORMES TOTALES Y FECALES EN AGUA RESIDUAL POR EL MÉTODO DEL NUMERO MAS PROBABLE (NMP) I. OBJETIVO Determinar la presencia de coliformes totales y fecales en el efluente
PRÁCTICA No. 7 DETERMINACIÓN DE COLIFORMES TOTALES Y FECALES EN AGUA RESIDUAL POR EL MÉTODO DEL NUMERO MAS PROBABLE (NMP) I. OBJETIVO Determinar la presencia de coliformes totales y fecales en el efluente
PRÁCTICA HIGIENE, INSPECCIÓN Y CONTROL DE LA MIEL
 PRÁCTICA HIGIENE, INSPECCIÓN Y CONTROL DE LA MIEL Determinación del contenido de humedad Determinación gravimétrica del contenido de sólidos insolubles en agua Conductividad eléctrica Determinación del
PRÁCTICA HIGIENE, INSPECCIÓN Y CONTROL DE LA MIEL Determinación del contenido de humedad Determinación gravimétrica del contenido de sólidos insolubles en agua Conductividad eléctrica Determinación del
DETERMINACION DE CAFEÍNA EN TE, CAFÉ Y YERBA MATE Basado en Método AOAC Modificado
 ME-711.02-008 Página 1 de 5 1. OBJETIVO Determinar el contenido de cafeína en fruitivos como té, café o yerba mate por método Bailey y Andrews. 2. CAMPO DE APLICACIÓN Y ALCANCE El método es aplicable a
ME-711.02-008 Página 1 de 5 1. OBJETIVO Determinar el contenido de cafeína en fruitivos como té, café o yerba mate por método Bailey y Andrews. 2. CAMPO DE APLICACIÓN Y ALCANCE El método es aplicable a
RECOPILADO POR: EL PROGRAMA UNIVERSITARIO DE ALIMENTOS
 NMX-F-312-1978. DETERMINACIÓN DE REDUCTORES DIRECTOS Y TOTALES EN ALIMENTOS. METHOD OF TEST FOR TOTAL AND DIRECT REDUCING SUBSTANCES IN FOOD. NORMAS MEXICANAS. DIRECCIÓN GENERAL DE NORMAS. PREFACIO En
NMX-F-312-1978. DETERMINACIÓN DE REDUCTORES DIRECTOS Y TOTALES EN ALIMENTOS. METHOD OF TEST FOR TOTAL AND DIRECT REDUCING SUBSTANCES IN FOOD. NORMAS MEXICANAS. DIRECCIÓN GENERAL DE NORMAS. PREFACIO En
Logros. Crecimiento bacteriano. Crecimiento. Finalidad de las bacterias
 Fisiología bacteriana Dr. Juan C. Salazar jcsalazar@med.uchile.cl Programa de Microbiología y Micología ICBM, Facultad de Medicina Finalidad de las bacterias Logros Crecimiento Cómo lo hacen? Herramientas
Fisiología bacteriana Dr. Juan C. Salazar jcsalazar@med.uchile.cl Programa de Microbiología y Micología ICBM, Facultad de Medicina Finalidad de las bacterias Logros Crecimiento Cómo lo hacen? Herramientas
RECOPILADO POR: EL PROGRAMA UNIVERSITARIO DE ALIMENTOS
 NMX-F-304-1977. MÉTODO GENERAL DE INVESTIGACIÓN DE SALMONELLA EN ALIMENTOS. GENERAL RESEARCH METHOD FOR THE DETERMINATION OF SALMONELLA IN FOODS. NORMAS MEXICANAS. DIRECCIÓN GENERAL DE NORMAS. PREFACIO.
NMX-F-304-1977. MÉTODO GENERAL DE INVESTIGACIÓN DE SALMONELLA EN ALIMENTOS. GENERAL RESEARCH METHOD FOR THE DETERMINATION OF SALMONELLA IN FOODS. NORMAS MEXICANAS. DIRECCIÓN GENERAL DE NORMAS. PREFACIO.
PREPARACIÓN DE MEDIOS DE CULTIVO
 Introducción Clasificación de los medios de cultivo Almacenamiento de los medios de cultivo Trabajo Práctico Nº 6 PREPARACIÓN DE MEDIOS DE CULTIVO Objetivo Fundamento Procedimiento Resultados Bibliografía
Introducción Clasificación de los medios de cultivo Almacenamiento de los medios de cultivo Trabajo Práctico Nº 6 PREPARACIÓN DE MEDIOS DE CULTIVO Objetivo Fundamento Procedimiento Resultados Bibliografía
Preparación de agua de dilución :
 La determinación de la Demanda Bioquímica de Oxígeno es una prueba en la que se determina los requerimientos relativos de oxígeno en aguas contaminadas tal como aguas residuales domésticas e industriales,,
La determinación de la Demanda Bioquímica de Oxígeno es una prueba en la que se determina los requerimientos relativos de oxígeno en aguas contaminadas tal como aguas residuales domésticas e industriales,,
Asignatura: Procesamiento De Lácteos AG Ing. Elvis Cruz
 Universidad Nacional Autónoma De Honduras Centro Universitario Regional Del Centro UNAH-CURC Departamento De Agroindustria Ingeniería Agroindustrial Asignatura: Procesamiento De Lácteos AG - 422 Ing. Elvis
Universidad Nacional Autónoma De Honduras Centro Universitario Regional Del Centro UNAH-CURC Departamento De Agroindustria Ingeniería Agroindustrial Asignatura: Procesamiento De Lácteos AG - 422 Ing. Elvis
CURSO DE EXTENSIÓN TEÓRICO PRÁCTICO HERRAMIENTAS EFICIENTES PARA LA IDENTIFICACIÓN DE LEVADURAS DE INTERÉS AGROINDUSTRIAL
 LIBRO DE MEMORIAS 2 CURSO DE EXTENSIÓN TEÓRICO PRÁCTICO HERRAMIENTAS EFICIENTES PARA LA IDENTIFICACIÓN DE LEVADURAS DE INTERÉS AGROINDUSTRIAL Santiago de Cali, 23 al 28 de agosto de 2010 3 Libro de memorias
LIBRO DE MEMORIAS 2 CURSO DE EXTENSIÓN TEÓRICO PRÁCTICO HERRAMIENTAS EFICIENTES PARA LA IDENTIFICACIÓN DE LEVADURAS DE INTERÉS AGROINDUSTRIAL Santiago de Cali, 23 al 28 de agosto de 2010 3 Libro de memorias
PET-RPLA KIT para DETECCIÓN de TOXINAS. Código: TD0930
 PET-RPLA KIT para DETECCIÓN de TOXINAS Código: TD0930 Kit para detección de enterotoxina tipo A de Clostridium perfringens en muestras fecales o en filtrados de cultivos por aglutinación pasiva de látex
PET-RPLA KIT para DETECCIÓN de TOXINAS Código: TD0930 Kit para detección de enterotoxina tipo A de Clostridium perfringens en muestras fecales o en filtrados de cultivos por aglutinación pasiva de látex
Ejemplos de recolección, conservación, envase y transporte de muestras de alimentos MANEJO EN EL MUESTRAS CONSERVACIÓN
 VI. Ejemplos de recolección, conservación, envase y transporte de muestras de alimentos RECOLECCIÓN Y Y DESECHO sólidos o mezcla de dos alimentos Realice cortes o tomar porciones de los alimentos utilizando
VI. Ejemplos de recolección, conservación, envase y transporte de muestras de alimentos RECOLECCIÓN Y Y DESECHO sólidos o mezcla de dos alimentos Realice cortes o tomar porciones de los alimentos utilizando
PRÁCTICA No. 4 Métodos de cultivo y descripción morfológica de hongos Introducción
 PRÁCTICA No. 4 Métodos de cultivo y descripción morfológica de hongos Objetivos. Que el alumno aprenda las técnicas de cultivo y manipulación de diferentes tipos de hongos. Que el estudiante conozca las
PRÁCTICA No. 4 Métodos de cultivo y descripción morfológica de hongos Objetivos. Que el alumno aprenda las técnicas de cultivo y manipulación de diferentes tipos de hongos. Que el estudiante conozca las
Placas Petrifilm. para el Recuento de E. coli/coliformes. Guía de interpretación
 Placas Petrifilm para el Recuento de E. coli/coliformes Guía de interpretación Esta guía lo familiarizará con los resultados de las Placas Petrifilm TM para el Recuento de E.coli/Coliformes. Para mayor
Placas Petrifilm para el Recuento de E. coli/coliformes Guía de interpretación Esta guía lo familiarizará con los resultados de las Placas Petrifilm TM para el Recuento de E.coli/Coliformes. Para mayor
PROCEDIMIENTO EVALUACION DE MEDIOS DE CULTIVO PRT-712.00-105
 PRT712.00105 28102008 10012012 Página 1 de 25 1. OBJETIVO Asegurar la calidad de los medios de cultivos preparados en la Sección Microbiología de utilizados en los análisis microbiológicos de alimentos
PRT712.00105 28102008 10012012 Página 1 de 25 1. OBJETIVO Asegurar la calidad de los medios de cultivos preparados en la Sección Microbiología de utilizados en los análisis microbiológicos de alimentos
Conceptos básicos para la toma, muestra, transporte, conservación y almacenamiento de muestras.
 Conceptos básicos para la toma, muestra, transporte, conservación y almacenamiento de muestras. A continuación se muestran los conceptos básicos para una buena toma de muestras cualquier información relevante,
Conceptos básicos para la toma, muestra, transporte, conservación y almacenamiento de muestras. A continuación se muestran los conceptos básicos para una buena toma de muestras cualquier información relevante,
RepublicofEcuador EDICTOFGOVERNMENT±
 RepublicofEcuador EDICTOFGOVERNMENT± Inordertopromotepubliceducationandpublicsafety,equaljusticeforal, abeterinformedcitizenry,theruleoflaw,worldtradeandworldpeace, thislegaldocumentisherebymadeavailableonanoncommercialbasis,asit
RepublicofEcuador EDICTOFGOVERNMENT± Inordertopromotepubliceducationandpublicsafety,equaljusticeforal, abeterinformedcitizenry,theruleoflaw,worldtradeandworldpeace, thislegaldocumentisherebymadeavailableonanoncommercialbasis,asit
UNIVERSIDAD TECNOLOGICA NACIONAL
 UNIVERSIDAD TECNOLOGICA NACIONAL FACULTAD REGIONAL ROSARIO DEPARTAMENTO DE INGENIERIA QUIMICA CATEDRA DE BIOTECNOLOGIA Trabajo práctico n 1 Preparación de medios de cultivo 2009 Jefe de Cátedra: Ing. Eduardo
UNIVERSIDAD TECNOLOGICA NACIONAL FACULTAD REGIONAL ROSARIO DEPARTAMENTO DE INGENIERIA QUIMICA CATEDRA DE BIOTECNOLOGIA Trabajo práctico n 1 Preparación de medios de cultivo 2009 Jefe de Cátedra: Ing. Eduardo
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS UNIDAD DIDACTICA QUIMICA PRIMER AÑO PRACTICAS DE LABORATORIO QUIMICA 2010
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS UNIDAD DIDACTICA QUIMICA PRIMER AÑO PRACTICAS DE LABORATORIO QUIMICA 2010 CARBOHIDRATOS ELABORADO POR: LICDA. LUCRECIA CASASOLA DE LEIVA
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS UNIDAD DIDACTICA QUIMICA PRIMER AÑO PRACTICAS DE LABORATORIO QUIMICA 2010 CARBOHIDRATOS ELABORADO POR: LICDA. LUCRECIA CASASOLA DE LEIVA
PRACTICA #5 BIOLOGIA CELULAR VETERINARIA SOLUCIONES HIPERTONICAS E HIPOTONICAS
 PRACTICA #5 BIOLOGIA CELULAR VETERINARIA SOLUCIONES HIPERTONICAS E HIPOTONICAS OBJETIVO: Observar el efecto de las soluciones con diferente concentración de soluto en células sanguíneas. FUNDAMENTO: Todas
PRACTICA #5 BIOLOGIA CELULAR VETERINARIA SOLUCIONES HIPERTONICAS E HIPOTONICAS OBJETIVO: Observar el efecto de las soluciones con diferente concentración de soluto en células sanguíneas. FUNDAMENTO: Todas
FERMENTACIONES Y METANOGENESIS
 CUARTA PARTE EN PROCESOS DE FERMENTACION, energía de sustratos orgánicos es transferida a ATP exclusivamente por fosforilación a nivel de sustrato. Como las fermentaciones no requieren de oxígeno y éstas
CUARTA PARTE EN PROCESOS DE FERMENTACION, energía de sustratos orgánicos es transferida a ATP exclusivamente por fosforilación a nivel de sustrato. Como las fermentaciones no requieren de oxígeno y éstas
NORMA VENEZOLANA COVENIN 3718:2001. AISLAMIENTO E IDENTIFICACIÓN DE Listeria monocytogenes EN ALIMENTOS FONDONORMA
 NORMA VENEZOLANA COVENIN 3718:2001 AISLAMIENTO E IDENTIFICACIÓN DE Listeria monocytogenes EN ALIMENTOS FONDONORMA PRÓLOGO La presente norma fue elaborada de acuerdo a las directrices del Comité Técnico
NORMA VENEZOLANA COVENIN 3718:2001 AISLAMIENTO E IDENTIFICACIÓN DE Listeria monocytogenes EN ALIMENTOS FONDONORMA PRÓLOGO La presente norma fue elaborada de acuerdo a las directrices del Comité Técnico
Anexo Conservar a 4 o C.
 Anexo 1 Purificación de ADN viral 1. Partir de un sobrenadante de un cultivo celular infectado y clarificado. 2. Concentrar las formas brotantes de los baculovirus por centrifugación (centrifugrar 1,5
Anexo 1 Purificación de ADN viral 1. Partir de un sobrenadante de un cultivo celular infectado y clarificado. 2. Concentrar las formas brotantes de los baculovirus por centrifugación (centrifugrar 1,5
