RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Zoladex 3,6 mg (Goserelina)
|
|
|
- Ramón Vidal Carrizo
- hace 6 años
- Vistas:
Transcripción
1 Nombre del producto: DCI Forma farmacéutica: Fortaleza: Presentación: RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Zoladex 3,6 mg (Goserelina) Implante SC 3,6 mg/implante Estuche por una jeringa precargada de Poliestireno/PEAD con implante estéril de 3,6 mg. Titular del Registro Sanitario, país: AstraZeneca UK Limited, Reino Unido. Fabricante, país: Número de Registro Sanitario: 1038 Fecha de Inscripción: 15 de abril de 1998 Composición: Cada implante contiene: Goserelina (eq. a 3,77 mg de acetato de goserelina) Plazo de validez: Condiciones de almacenamiento: Indicaciones terapéuticas: Zoladex está indicado: AstraZeneca UK Limited, Reino Unido. 3,6 mg 36 meses Almacenar por debajo de 25 ºC. Para el tratamiento del cáncer de próstata en las siguientes situaciones. Para el tratamiento del cáncer de próstata metastásico, donde Zoladex ha demostrado beneficios de supervivencia comparables a las castraciones quirúrgicas. Para el tratamiento del cáncer de próstata localmente avanzado, como una alternativa a la castración quirúrgica, donde Zoladex ha demostrado beneficios de supervivencia comparables a un agente antiandrogénico. Como terapia adyuvante a la radioterapia en los pacientes con un cáncer de próstata localmente avanzado o localizado de alto riesgo, donde Zoladex ha demostrado una mejor supervivencia sin enfermedad y supervivencia global. Como terapia neoadyuvante antes de la radioterapia en los pacientes con un cáncer de próstata localmente avanzado o localizado de alto riesgo, donde Zoladex ha demostrado una mejor supervivencia sin enfermedad. Como terapia adyuvante a la prostatectomía radical en los pacientes con un cáncer de próstata localmente avanzado con alto riesgo de progresión de la enfermedad, donde Zoladex ha demostrado una mejor supervivencia sin enfermedad. Cáncer de mama avanzado en mujeres pre y perimenopáusicas, para quienes el tratamiento de manipulación hormonal sea apropiado.
2 Zoladex 3,6 mg está indicado como una alternativa a la quimioterapia en el estándar de atención para las mujeres pre y perimenopáusicas con cáncer de mama temprano positivo por receptores de estrógeno (RE). Endometriosis: En el manejo de la endometriosis, Zoladex alivia los síntomas, incluido el dolor, y reduce el tamaño y la cantidad de las lesiones endometriales. Adelgazamiento del endometrio: Zoladex está indicado para disminuir el grosor del endometrio uterino antes de la ablación o resección endometrial. Fibromas uterinos: Junto con una terapia con hierro para el mejoramiento hematológico de las pacientes anémicas con fibromas, antes de la cirugía. Reproducción asistida: Regulación en disminución de la hipófisis como preparación para la superovulación. Contraindicaciones: Hipersensibilidad severa conocida al principio activo o a cualquiera de los excipientes de este producto. Embarazo y lactancia. Precauciones: Ver Advertencias. Advertencias especiales y precauciones de uso: Zoladex no está indicado para el tratamiento de los niños, ya que no se ha establecido la seguridad y eficacia en este grupo de pacientes. Existe un mayor riesgo de depresión incidente (que puede ser severa) en los pacientes sometidos a un tratamiento con agonistas de la hormona liberadora de gonadotropina (GnRH, por sus siglas en inglés), como la goserelina. Se debe informar a los pacientes lo correspondiente y, si aparecen los síntomas, se debe administrar el tratamiento según sea apropiado. La terapia de privación de andrógenos puede prolongar el intervalo QT. En aquellos pacientes con una historia de prolongación del QT o con factores de riesgo para tal prolongación y en los pacientes que reciben productos medicinales concomitantes que podrían prolongar el intervalo QT, los médicos deben valorar la razón beneficio riesgo, incluido el potencial de Torsades de pointes antes de iniciar Zoladex. Se ha reportado lesión en el sitio de inyección con Zoladex, incluidos eventos de dolor, hematoma, hemorragia y lesión vascular. Se debe monitorear a los pacientes afectados por signos o síntomas de hemorragia abdominal. En casos muy infrecuentes, el error en la administración ha resultado en lesión vascular y choque hemorrágico que requirió transfusiones sanguíneas y la intervención quirúrgica. Se debe tomar cuidado especial cuando se administra Zoladex a pacientes con un IMC bajo y/o que reciben medicaciones de anticoagulación completa. Hombres Deberá considerarse cuidadosamente el uso de Zoladex en los hombres con un riesgo particular de desarrollar obstrucción ureteral o compresión de la médula espinal y estos pacientes deben observarse cuidadosamente durante el primer mes de tratamiento. Si se presenta o desarrolla la compresión medular o alteración de la función renal debido a obstrucción ureteral, se deberá establecer el tratamiento específico estandarizado para el tratamiento de estas complicaciones. Debe considerarse el uso inicial de un agente antiandrogénico (ej. acetato de ciproterona 300 mg al día por tres días antes y tres semanas después de iniciar Zoladex) al inicio de la terapia con análogos de la hormona liberadora de la hormona luteinizante (LHRH), ya que
3 se ha reportado que previene las posibles secuelas del aumento inicial del nivel de la testosterona sérica. El uso de los agonistas de la LHRH puede reducir la densidad mineral ósea. En los hombres, los datos preliminares sugieren que el uso de un bisfosfonato en combinación con un agonista de la LHRH puede reducir la pérdida del mineral óseo. Es necesario tener un cuidado especial en los pacientes con factores de riesgo adicionales para la osteoporosis (ej. abusadores crónicos de bebidas alcohólicas, fumadores, terapia a largo plazo con agentes anticonvulsivos o corticosteroides, antecedentes familiares de osteoporosis). Es necesario monitorear cuidadosamente a los pacientes con depresión conocida y a los pacientes con hipertensión. Se ha visto una disminución de la tolerancia a la glucosa en los hombres que reciben agonistas de la LHRH. Esto puede manifestarse como diabetes o pérdida del control glicémico en los pacientes con una diabetes mellitus preexistente. Por lo tanto, debe considerarse el monitoreo de los niveles de la glucosa sanguínea. En un estudio farmacoepidemiológico de agonistas de la LHRH usados para el tratamiento del cáncer de próstata, se observó la presencia de infarto de miocardio e insuficiencia cardiaca. El riesgo pareciera aumentar cuando se usan en combinación con agentes antiandrogénicos. Mujeres Indicación en el cáncer de mama Disminución de la densidad mineral ósea: La utilización de agonistas de la LHRH puede causar una disminución de la densidad mineral ósea. Después de dos años de tratamiento para el cáncer de mama temprano, la pérdida promedio de densidad mineral ósea fue 6,2% y 11,5% en el cuello femoral y la espina lumbar, respectivamente. Se demostró que esta pérdida fue parcialmente reversible en el seguimiento al año de haber suspendido el tratamiento, con una recuperación de 3,4% y 6,4% respecto a los valores en la línea de base en el cuello femoral y la espina lumbar, respectivamente, aunque esta recuperación se basó en datos muy limitados. En la mayoría de las mujeres, los datos disponibles actualmente sugieren que hay recuperación de la pérdida ósea al suspender el tratamiento. Los datos preliminares sugieren que el uso de Zoladex en combinación con el tamoxifeno en las pacientes con cáncer de mama puede reducir la pérdida de la densidad mineral ósea. Indicaciones benignas Pérdida de la densidad mineral ósea: El uso de agonistas de la LHRH puede causar una reducción de la densidad mineral ósea, con un promedio de 1% por mes durante un período de tratamiento de seis meses. Cada reducción del 10% de la densidad mineral ósea se asocia a un riesgo de fractura dos a tres veces mayor. En la mayoría de las mujeres, los datos disponibles actualmente sugieren que la pérdida ósea se recupera después de suspender el tratamiento. En las pacientes tratadas con Zoladex para la endometriosis, se ha demostrado que al agregar una terapia hormonal de reemplazo se reduce la pérdida de la densidad mineral ósea y los síntomas vasomotores. No hay datos específicos para los pacientes con una osteoporosis establecida o con factores de riesgo para la osteoporosis (ej. abusadores crónicos de bebidas alcohólicas, fumadores, terapia a largo plazo con agentes que reducen la densidad mineral ósea, como los anticonvulsivos o corticosteroides, antecedentes familiares de osteoporosis, desnutrición, ej. anorexia nerviosa). Debido a que la disminución de la densidad mineral ósea probablemente será más nociva en estos pacientes, debe considerarse el tratamiento con Zoladex en forma individual para cada paciente y debe iniciarse solo si los beneficios del
4 tratamiento superan los riesgos, tras una evaluación muy cuidadosa. Deben considerarse medidas adicionales para contrarrestar la pérdida de la densidad mineral ósea. Sangrado por abstinencia Al inicio del tratamiento con Zoladex, algunas mujeres presentan sangrado vaginal, de duración e intensidad variables. Si hubiera sangrado vaginal, generalmente se presenta en el primer mes después de iniciar el tratamiento. Tal sangrado probablemente representa un sangrado por abstinencia de estrógeno y se espera que ceda espontáneamente. Si el sangrado continúa, debe investigarse la causa. No hay datos clínicos sobre los efectos en el tratamiento de las condiciones ginecológicas benignas con Zoladex por períodos mayores de seis meses. El uso de Zoladex puede causar un aumento de la resistencia del cuello uterino y se debe tener cuidado al dilatar el cérvix. En la reproducción asistida, Zoladex debe administrarse solamente como parte de un esquema de reproducción asistida bajo la supervisión de un especialista con experiencia en esta área. Al igual que con otros agonistas de la LHRH, hay reportes de casos del síndrome de hiperestimulación ovárica (OHSS, por sus siglas en inglés) asociado al uso de Zoladex 3,6 mg en combinación con gonadotropina. El ciclo de estimulación debe monitorearse cuidadosamente para identificar a las pacientes con riesgo de desarrollar un OHSS. Siempre que sea posible, no debe usarse la gonadotrofina coriónica humana (hcg) si existe un riesgo de OHSS. Se recomienda usar Zoladex con cuidado en el tratamiento de fertilización en las pacientes con un síndrome de ovario poliquístico, ya que puede aumentar el reclutamiento folicular. Las mujeres fértiles deben usar métodos anticonceptivos no hormonales durante el tratamiento con Zoladex y hasta que se reinicie la menstruación después de suspender el tratamiento con Zoladex. Es necesario monitorear cuidadosamente a los pacientes con depresión conocida y a los pacientes con hipertensión. El tratamiento con Zoladex puede causar reacciones positivas en las pruebas antidopaje. Efectos indeseables: Se calcularon las siguientes categorías de frecuencia para las reacciones medicamentosas adversas (ADR, por sus siglas en inglés), con base en los reportes de los ensayos clínicos con Zoladex y las fuentes postcomercialización. Las reacciones adversas observadas con mayor frecuencia fueron rubor, sudoración y reacciones en el sitio de la inyección. Se usó la siguiente convención para la clasificación de la frecuencia: muy comunes ( 1/10), comunes ( 1/100 a <1/10), poco comunes ( 1/1000 a <1/100), infrecuentes ( 1/ a <1/1,000), muy infrecuentes (<1/10 000) y desconocidas (no pueden estimarse a partir de los datos disponibles). Cuadro: Reacciones medicamentosas adversas con Zoladex 3,6 mg, presentadas según la clase de sistemas y órganos de MedDRA CLASE DE SISTEMAS Y ÓRGANOS FRECUENCIA HOMBRES MUJERES Neoplasmas benignos, Muy infrecuentes Tumor pituitario Tumor pituitario
5 CLASE DE SISTEMAS Y FRECUENCIA HOMBRES MUJERES ÓRGANOS malignos y no especificados (incluye quistes y pólipos) Se desconoce N/A Degeneración de fibroma uterino Trastornos del sistemapoco comunes Hipersensibilidad ahipersensibilidad inmune medicamentos medicamentos a Infrecuentes Reacción anafiláctica Reacción anafiláctica Trastornos endocrinos Trastornos del metabolismo y la nutrición Muy infrecuentes Hemorragia pituitaria Hemorragia pituitaria Comunes Tolerancia a lan/a glucosa alterada a Poco comunes N/A Hipercalcemia Trastornos psiquiátricos Muy comunes Libido disminuida b Libido disminuida b Comunes Cambios en el ánimo, Cambios en el ánimo, depresión depresión Muy infrecuentes Trastorno psicótico Trastorno psicótico Trastornos del sistemacomunes Parestesias Parestesias nervioso Compresión de lan/a médula espinal N/A Cefalea Trastornos cardiacos Comunes Insuficiencia cardiaca, f infarto del miocardio f N/A Desconocido Prolongación QT Prolongación QT Trastornos vasculares Muy comunes Rubor b Rubor b Comunes Presión arterialpresión anormal c anormal c arterial Trastornos cutáneos y de tejidos subcutáneos Muy comunes Hiperhidrosis b Hiperhidrosis, b acné i Comunes Sarpullido d Sarpullido, d alopecia g Muy comunes Hiperhidrosis b Hiperhidrosis,b acné i Comunes Sarpullido d Sarpullido,d alopecia g Se desconoce Alopecia h Ver comunes
6 CLASE DE SISTEMAS Y FRECUENCIA HOMBRES MUJERES ÓRGANOS Comunes Dolor óseo e N/A Ver poco comunes Artralgia Poco comunes Artralgia Ver comunes Poco comunes Obstrucción ureteral N/A Muy comunes Disfunción eréctil N/A N/A Sequedad vulvovaginal N/A Agrandamiento de mamas Comunes Ginecomastia N/A Poco comunes Sensibilidad en lasn/a mamas Infrecuentes N/A Quiste ovárico N/A Síndrome de hiperestimulación ovárica (con el uso concomitante de gonadotropinas) Se desconoce N/A Sangrado por abstinencia (ver la sección 4.4) Trastornos generales y en el sitio de la administración Muy comunes Ver comunes Reacción en el sitio de la inyección Comunes Reacción en el sitio de la inyección N/A Ver muy comunes Recrudecimiento del tumor, dolor tumoral (al iniciar el tratamiento) Investigaciones Comunes Disminución de la densidad ósea (ver la sección 4.4), aumento de peso Disminución de la densidad ósea (ver la sección 4.4), aumento de peso a. Se ha observado una disminución de la tolerancia a la glucosa en los hombres que reciben agonistas de la LHRH. Esto podría manifestarse como diabetes o pérdida del control glicémico en personas con diabetes mellitus preexistente.
7 b. Estos son efectos farmacológicos que rara vez requieren retirar el tratamiento. c. Estos efectos pueden manifestarse como hipotensión o hipertensión; se han visto ocasionalmente en pacientes que reciben Zoladex. Los cambios generalmente son transitorios y se resuelven conforme continúa el tratamiento o al suspender la terapia con Zoladex. Rara vez estos cambios han sido suficientes para requerir una intervención médica, lo que incluye retirar el tratamiento con Zoladex. d. Por lo general, estos efectos son leves y con frecuencia ceden sin descontinuar la terapia. e. Inicialmente, los pacientes con cáncer de próstata pueden presentar un aumento temporal del dolor óseo, lo que puede manejarse sintomáticamente. f. Se observó en un estudio farmacoepidemiológico de agonistas de la LHRH usados para el tratamiento del cáncer de próstata. El riesgo parece aumentar cuando se usan en combinación con agentes antiandrogénicos. g. Se ha reportado la pérdida del cabello en las mujeres, incluidas las pacientes más jóvenes bajo tratamiento para condiciones benignas. Este efecto generalmente es leve, pero ocasionalmente puede ser severo. h. En particular, la pérdida del vello corporal, un efecto esperado del nivel de andrógenos disminuido. i. En la mayoría de los casos, se reportó el acné en el primer mes después de iniciar Zoladex. Experiencia postcomercialización Se ha reportado una cantidad pequeña de casos de cambios en el recuento sanguíneo, disfunción hepática, embolia pulmonar y neumonía intersticial asociados a Zoladex. Además, se han reportado las siguientes reacciones medicamentosas adversas en mujeres que reciben el tratamiento para indicaciones ginecológicas benignas: acné, cambios en los vellos corporales, piel seca, aumento de peso, aumento del colesterol sérico, síndrome de hiperestimulación ovárica (si se usa en forma concomitante con gonadotropinas), vaginitis, secreción vaginal, nerviosismo, trastorno del sueño, cansancio, edema periférico, mialgias, contracciones en las pantorrillas, náuseas, vómito, diarrea, estreñimiento, quejas abdominales, alteraciones de la voz. Inicialmente, las pacientes con cáncer de mama pueden presentar un aumento temporal de los signos y síntomas, lo que puede manejarse sintomáticamente. Rara vez, las pacientes con cáncer de mama con metástasis han desarrollado hipercalcemia al iniciar la terapia. En presencia de síntomas indicativos de hipercalcemia (ej. sed), debe excluirse la hipercalcemia. Rara vez, algunas mujeres pueden iniciar la menopausia durante el tratamiento con los análogos de la LHRH y la menstruación podría no reanudarse tras la suspensión del tratamiento. No se sabe si este es un efecto del tratamiento con Zoladex o un reflejo de su condición ginecológica. Posología y método de administración: Adultos Un implante de Zoladex 3,6 mg inyectado por vía subcutánea en la pared anterior del abdomen, cada 28 días (4 semanas). No se requiere ajustar la dosis en los pacientes con insuficiencia renal o hepática ni en los adultos mayores. La endometriosis debe tratarse solo por un período de seis meses, ya que a la fecha no hay información clínica para períodos de tratamiento más prolongados. No deben darse cursos repetidos, debido a la posibilidad de pérdida de la densidad del mineral óseo. En las
8 pacientes que reciben Zoladex para el tratamiento de la endometriosis, se ha demostrado que la pérdida de densidad del mineral óseo y los síntomas vasomotores se reducen con una terapia de reemplazo hormonal (un agente estrogénico y un agente progestágeno diariamente). Para el adelgazamiento del endometrio: usar un tratamiento de cuatro a ocho semanas. Podría ser necesario un segundo implante en las pacientes con un útero grande o para mayor flexibilidad en la fecha de la cirugía. Para las mujeres que están anémicas como resultado de los fibromas uterinos: Puede administrarse un implante de Zoladex 3,6 mg con suplementos de hierro por hasta tres meses antes de la cirugía. Reproducción asistida: Zoladex 3,6 mg se administra para regular en disminución la glándula pituitaria, lo que se define con la disminución de los niveles de estradiol en el suero similares a los observados en la fase folicular temprana (aproximadamente 150 pmol/l). Esto generalmente requerirá entre 7 y 21 días. Una vez que se ha alcanzado la regulación en disminución de la pituitaria, se inicia la superovulación (estimulación controlada de los ovarios) con gonadotropina. La disminución de la actividad pituitaria que se logra con un agonista de depósito es más consistente, lo que sugiere que en algunos casos podría existir una mayor necesidad de gonadotropina. En la etapa apropiada del desarrollo folicular, se suspende la gonadotropina y se administra gonadotropina coriónica humana (hcg) para inducir la ovulación. Las técnicas para el monitoreo del tratamiento, la obtención de los oocitos y la fertilización se realizan según la práctica habitual de cada clínica. Niños Zoladex no está indicado para los niños. Para una administración correcta de Zoladex, seguir las indicaciones en la tarjeta de instrucciones. Interacción con otros productos medicinales y otras formas de interacción: Ya que el tratamiento de privación de andrógenos puede prolongar el intervalo QT, el uso concomitante de Zoladex con los productos medicinales que se saben prolongan el intervalo QT o productos medicinales capaces de inducir Torsades de pointes, tales como los productos medicinales antiarrítmicos de la clase IA (por ejemplo, quinidina, disopiramida) o la clase III (por ejemplo, amiodarone, sotalol, dofetilida, ibutilida), metadona, moxifloxacina, antipsicóticos, etc. debe evaluarse cuidadosamente. Uso en Embarazo y lactancia: Embarazo: Zoladex no debe usarse durante el embarazo, ya que el uso concurrente de agonistas de la LHRH se asocia a un riesgo teórico de aborto o anormalidad fetal. Es necesario examinar cuidadosamente a las mujeres potencialmente fértiles para excluir el embarazo antes de comenzar el tratamiento. Se deben emplear métodos anticonceptivos no hormonales durante la terapia hasta el reinicio de los ciclos menstruales (ver también la advertencia sobre el tiempo hasta el reinicio de los ciclos menstruales). Se deberá excluir el embarazo antes de emplear Zoladex en la reproducción asistida. Cuando se administra Zoladex para este propósito, no existe evidencia clínica que sugiera una asociación causal entre Zoladex y alguna anormalidad posterior en el desarrollo del oocito, el embarazo o su resultado. Lactancia: No se recomienda la administración de Zoladex durante la lactancia. Efectos sobre la conducción de vehículos/maquinarias: No hay evidencias de que Zoladex afecte la capacidad para conducir vehículos u operar maquinaria.
9 Sobredosis: No hay mucha experiencia de sobredosis en los seres humanos. Cuando Zoladex se ha administrado antes de tiempo o cuando se ha administrado una dosis mayor a la planeada originalmente, no se han observado efectos adversos clínicamente significativos. Los ensayos en animales sugieren que con las dosis más altas de Zoladex no habrá más reacciones fuera de los efectos terapéuticos deseados con respecto a las concentraciones de las hormonas sexuales y sobre el tracto reproductor. En caso de sobredosis, la condición debe manejarse en forma sintomática. Propiedades farmacodinámicas: Grupo farmacoterapéutico: Análogos de la hormona liberadora de gonadotropinas, Código ATC: L02AE03 Zoladex (D-Ser (Bu t ) 6 Azgli 10 LHRH) es un análogo sintético de la hormona liberadora de la hormona luteinizante (LHRH) de origen natural. Durante la administración crónica de Zoladex, se produce una inhibición de la secreción de la hormona luteinizante de la glándula pituitaria, lo que causa la disminución de las concentraciones de testosterona sérica en los hombres y de las concentraciones del estradiol sérico en las mujeres. Este efecto es reversible al suspender la terapia. Inicialmente, al igual que otros agonistas de lalhrh, Zoladex puede aumentar transitoriamente las concentraciones de la testosterona sérica en los hombres y del estradiol sérico en las mujeres. En los hombres, aproximadamente a los 21 días después de la inyección del primer implante, las concentraciones de testosterona disminuyen hasta el rango de castración y permanecen suprimidas con el tratamiento continuo cada 28 días. Esta inhibición causa la regresión del tumor prostático y una mejoría sintomática en la mayoría de los pacientes. En los ensayos clínicos comparativos, se ha demostrado que Zoladex produce resultados de supervivencia similares a los obtenidos con castraciones quirúrgicas en los pacientes con cáncer de próstata metastásico. En un análisis combinado de dos ensayos aleatorios controlados que compararon la monoterapia con bicalutamida 150 mg versus la castración (predominantemente en forma de Zoladex), no hubo ninguna diferencia significativa en la supervivencia global entre los pacientes con un cáncer de próstata localmente avanzado tratados con bicalutamida y los tratados con castración (razón de riesgo = 1,05 [intervalo de confianza: 0,81 a 1,36]). Sin embargo, no se pudo concluir estadísticamente la equivalencia de los dos tratamientos. En los ensayos comparativos, se ha demostrado que Zoladex mejora la supervivencia sin enfermedad y la supervivencia global cuando se usa como terapia adyuvante a la radioterapia en pacientes con cáncer de próstata localizado de alto riesgo (T 1-T 2 y antígeno prostático de al menos 10 ng/ml o una puntuación Gleason de al menos 7) o localmente avanzado (T 3-T 4). No se ha establecido la duración óptima de la terapia adyuvante; un ensayo comparativo demostró que 3 años de Zoladex adyuvante proporciona una mejoría de supervivencia significativa en comparación con solo la radioterapia. Se ha demostrado que la administración de Zoladex neoadyuvante antes de la radioterapia mejora la supervivencia sin enfermedad en los pacientes con un cáncer de próstata localmente avanzado o localizado de alto riesgo. Después de la prostatectomía, la administración de Zoladex adyuvante en los pacientes que se encuentra tienen una diseminación extraprostática del tumor puede mejorar los períodos de supervivencia sin enfermedad, pero no hay una mejoría significativa en la supervivencia salvo que los pacientes tengan evidencias de compromiso ganglionar al momento de la cirugía. Los pacientes con una enfermedad localmente avanzada cuya clasificación se haya establecido patológicamente deben tener factores de riesgo adicionales, tales como un antígeno prostático de al menos 10 ng/l o una puntuación Gleason de al menos 7, antes de
10 considerar la administración de Zoladex adyuvante. No hay evidencias de mejores resultados clínicos con el uso de Zoladex neoadyuvante antes de la prostatectomía radical. En las mujeres, las concentraciones del estradiol sérico se suprimen alrededor de los 21 días después de la inyección del primer implante y se mantienen suprimidas a niveles comparables a los observados en mujeres postmenopáusicas con un tratamiento continuo cada 28 días. Dicha supresión se asocia a una respuesta del cáncer de mama avanzado hormonodependiente, la endometriosis, los fibromas uterinos y la supresión del desarrollo folicular dentro del ovario. En la mayoría de las pacientes, causará el adelgazamiento del endometrio y amenorrea. Las pacientes pueden iniciar la menopausia durante el tratamiento con análogos de la LHRH. Raramente, algunas mujeres no recuperan los ciclos menstruales al suspender la terapia. Se ha demostrado que Zoladex, en combinación con hierro, induce amenorrea y mejora las concentraciones de la hemoglobina y los parámetros hematológicos asociados en las mujeres anémicas con fibromas. La combinación produjo una concentración media de la hemoglobina de 1 g/dl por encima de lo obtenido con solo la terapia con hierro. Propiedades farmacocinéticas (Absorción, distribución, biotransformación, eliminación): La biodisponibilidad de Zoladex es prácticamente completa. La administración de un implante cada cuatro semanas garantiza el mantenimiento de concentraciones eficaces, sin acumulación tisular. Zoladex se une poco a las proteínas y tiene una vida media de eliminación sérica de dos a cuatro horas en los sujetos con una función renal normal. La vida media aumenta en los pacientes con una función renal alterada. Para el compuesto administrado mensualmente bajo una formulación de implante, este cambio tendrá un efecto mínimo. Por lo tanto, no es necesario ajustar la dosis en estos pacientes. No hay ningún cambio farmacocinético significativo en los pacientes con insuficiencia hepática. Información preclínica sobre la seguridad Después de la administración repetida y a largo plazo de Zoladex, se ha observado un aumento en la incidencia de tumores pituitarios benignos en ratas machos. Aunque este hallazgo es similar al observado anteriormente en esta especie tras la castración quirúrgica, no se ha establecido su relevancia en los seres humanos. En los ratones, la administración repetida y a largo plazo con múltiplos de la dosis para los seres humanos produjo cambios histológicos en algunas regiones del sistema digestivo, que se manifestaron con hiperplasia de las células de los islotes pancreáticos y una proliferación benigna en la región pilórica del estómago, lo que también se ha reportado como una lesión espontánea en esta especie. Se desconoce cuál es la relevancia clínica de estos hallazgos. Instrucciones de uso, manipulación y destrucción del remanente no utilizable del producto: Usar en la forma indicada por el médico. Utilizar sólo si el sobre está intacto. Usar inmediatamente después de abrir el sobre. Eliminar la jeringa en un dispositivo recolector aprobado para objetos punzantes. Fecha de aprobación/ revisión del texto: 31 de enero de 2017.
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO ZOLADEX LA 10,8 mg (Goserelina) Implante SC
 Nombre del producto: RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO ZOLADEX LA 10,8 mg (Goserelina) Forma farmacéutica: Fortaleza: Presentación: Titular del Registro Sanitario, país: Fabricante, país: Implante
Nombre del producto: RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO ZOLADEX LA 10,8 mg (Goserelina) Forma farmacéutica: Fortaleza: Presentación: Titular del Registro Sanitario, país: Fabricante, país: Implante
FICHA TECNICA. ZOLADEX TRIMESTRAL 10,8 está indicado en el tratamiento del cáncer de próstata, cuando la terapia hormonal está indicada.
 FICHA TECNICA 1.- NOMBRE DEL MEDICAMENTO ZOLADEX TRIMESTRAL 10,8 Goserelina 2.- COMPOSICION CUALITATIVA Y CUANTITATIVA Cada jeringa precargada contiene un implante con: Principio Activo: Acetato de Goserelina,
FICHA TECNICA 1.- NOMBRE DEL MEDICAMENTO ZOLADEX TRIMESTRAL 10,8 Goserelina 2.- COMPOSICION CUALITATIVA Y CUANTITATIVA Cada jeringa precargada contiene un implante con: Principio Activo: Acetato de Goserelina,
FICHA TÉCNICA. Cada implante en jeringa precargada contiene 3,6 mg de goserelina (como acetato).
 1 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Zoladex 3,6 mg implante en jeringa precargada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada implante en jeringa precargada contiene 3,6 mg de goserelina (como
1 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Zoladex 3,6 mg implante en jeringa precargada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada implante en jeringa precargada contiene 3,6 mg de goserelina (como
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. Menopur 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Menopur 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principios activos: 1 Ampolla con la sustancia seca contiene Menotropina (Gonadotropina menopáusica humana, hmg)
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Menopur 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principios activos: 1 Ampolla con la sustancia seca contiene Menotropina (Gonadotropina menopáusica humana, hmg)
Forma farmacéutica Vía de administración. Contenido (Concentración) Estado miembro. Nombre. Dinamarca. Vantas 50 mg Implante Subcutánea 50 mg
 ANEXO I RELACIÓN DE LOS NOMBRES DEL MEDICAMENTO, FORMA FARMACÉUTICA, DOSIS, VÍA DE ADMINISTRACIÓN, SOLICITANTE, TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN EN LOS ESTADOS MIEMBROS Estado miembro Dinamarca
ANEXO I RELACIÓN DE LOS NOMBRES DEL MEDICAMENTO, FORMA FARMACÉUTICA, DOSIS, VÍA DE ADMINISTRACIÓN, SOLICITANTE, TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN EN LOS ESTADOS MIEMBROS Estado miembro Dinamarca
ANÁLISIS DE DUPLICIDADES DEL SUBGRUPO TERAPÉUTICO L02 - TERAPIA ENDOCRINA
 ANÁLISIS DE ES DEL SUBGRUPO TERAPÉUTICO L02 - TERAPIA ENDOCRINA Clasificación ATC L02A: HORMONAS Y AGENTES RELACIONADOS L02AB PROGESTÁGENOS L02AE ANÁLOGOS DE LA HORMONA LIBERADORA DE GONADOTROPINAS. Histrelina
ANÁLISIS DE ES DEL SUBGRUPO TERAPÉUTICO L02 - TERAPIA ENDOCRINA Clasificación ATC L02A: HORMONAS Y AGENTES RELACIONADOS L02AB PROGESTÁGENOS L02AE ANÁLOGOS DE LA HORMONA LIBERADORA DE GONADOTROPINAS. Histrelina
DIRECCION REGULACION DE LA SALUD CENTRO NACIONAL DE FARMACOVIGILANCIA
 DIRECCION REGULACION DE LA SALUD CENTRO NACIONAL DE FARMACOVIGILANCIA Comunicación sobre cambios en la información de seguridad de Sibutramina para profesionales sanitarios Mayo de 2010 NOTA INFORMATIVA
DIRECCION REGULACION DE LA SALUD CENTRO NACIONAL DE FARMACOVIGILANCIA Comunicación sobre cambios en la información de seguridad de Sibutramina para profesionales sanitarios Mayo de 2010 NOTA INFORMATIVA
ANASTROZOL COMPRIMIDOS RECUBIERTOS 1 mg. COMPOSICIÓN Cada comprimido recubierto contiene: Excipientes: Según lo aprobado en Registro
 ANASTROZOL COMPRIMIDOS RECUBIERTOS 1 mg COMPOSICIÓN Cada comprimido recubierto contiene: Anastrozol 1 mg Excipientes: Según lo aprobado en Registro CLASIFICACION TERAPEUTICA Antineoplásico INDICACIONES
ANASTROZOL COMPRIMIDOS RECUBIERTOS 1 mg COMPOSICIÓN Cada comprimido recubierto contiene: Anastrozol 1 mg Excipientes: Según lo aprobado en Registro CLASIFICACION TERAPEUTICA Antineoplásico INDICACIONES
MEGAPLEX 160mg. Nombre Comercial. Megaplex 160mg. Nombre Genérico. Acetato de Megestrol 160mg. Concentración. 160mg. Denominación Común Internacional
 MEGAPLE 160mg 1. Identificación del Medicamento Nombre Comercial Megaplex 160mg Nombre Genérico Acetato de Megestrol 160mg Concentración 160mg Denominación Común Internacional Acetato de Megestrol N Registro
MEGAPLE 160mg 1. Identificación del Medicamento Nombre Comercial Megaplex 160mg Nombre Genérico Acetato de Megestrol 160mg Concentración 160mg Denominación Común Internacional Acetato de Megestrol N Registro
LABORATORIOS NORMON, S.A. AMBROXOL NORMON 15 mg/5 ml Jarabe EFG
 1. NOMBRE DEL MEDICAMENTO 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada 5 ml de jarabe contienen: AMBROXOL (D.C.I.) hidrocloruro 15 mg Excipientes, ver apartado 6.1. 3. FORMA FARMACEUTICA Jarabe. 4. DATOS
1. NOMBRE DEL MEDICAMENTO 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada 5 ml de jarabe contienen: AMBROXOL (D.C.I.) hidrocloruro 15 mg Excipientes, ver apartado 6.1. 3. FORMA FARMACEUTICA Jarabe. 4. DATOS
No. el alcohol no altera el mecanismo de acción o los efectos del Andanza.
 GUÍA SOBRE 1 1. Qué es Es un fármaco aprobado para su uso como adyuvante, del plan alimentario hipocalórico y la práctica de ejercicio, en el manejo del sobrepeso y la obesidad en adolescentes y adultos.
GUÍA SOBRE 1 1. Qué es Es un fármaco aprobado para su uso como adyuvante, del plan alimentario hipocalórico y la práctica de ejercicio, en el manejo del sobrepeso y la obesidad en adolescentes y adultos.
Hipersensibilidad conocida a penciclovir, famciclovir o a los otros componentes de la formulación, por ejemplo propilenglicol.
 1. NOMBRE DEL MEDICAMENTO Penciclovir Beecham bomba dosificadora Penciclovir Beecham crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio activo: Penciclovir al 1% DCI: penciclovir 3. FORMA FARMACÉUTICA
1. NOMBRE DEL MEDICAMENTO Penciclovir Beecham bomba dosificadora Penciclovir Beecham crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio activo: Penciclovir al 1% DCI: penciclovir 3. FORMA FARMACÉUTICA
LLD Abreviado de Zoloft. Todo medicamento debe conservarse fuera del alcance de los niños.
 LLD Abreviado de Zoloft Versión: 19.0 Fecha: 20 de febrero de 2015 Aprobación ARCSA: 23 febrero de 2016 Todo medicamento debe conservarse fuera del alcance de los niños. 1. Presentación: Sertralina que
LLD Abreviado de Zoloft Versión: 19.0 Fecha: 20 de febrero de 2015 Aprobación ARCSA: 23 febrero de 2016 Todo medicamento debe conservarse fuera del alcance de los niños. 1. Presentación: Sertralina que
Información del Documento Original
 ANTECEDENTES Que mediante escrito No. 2015108841 del 21/08/2015, el señor Jorge Emilio Solano Rozo, actuando en calidad de representante legal de Laboratorios Chalver De Colombia S.A. con domicilio en
ANTECEDENTES Que mediante escrito No. 2015108841 del 21/08/2015, el señor Jorge Emilio Solano Rozo, actuando en calidad de representante legal de Laboratorios Chalver De Colombia S.A. con domicilio en
PRINCIPIO Y FIN DE LA VIDA REPRODUCTIVA. Cambios puberales y menopausia.
 PRINCIPIO Y FIN DE LA VIDA REPRODUCTIVA Cambios puberales y menopausia. Definiciones Adrenarquia: Incremento de la secreción de andrógenos por las glándulas adrenales. Ocurre entre los 5 y los 20 años.
PRINCIPIO Y FIN DE LA VIDA REPRODUCTIVA Cambios puberales y menopausia. Definiciones Adrenarquia: Incremento de la secreción de andrógenos por las glándulas adrenales. Ocurre entre los 5 y los 20 años.
RECURRENCIA POST PROSTATECTOMÍA RADICAL. Dra. Beatriz Cuendias Abreu Hospital Hermanos Ameijeiras
 RECURRENCIA POST PROSTATECTOMÍA RADICAL Dra. Beatriz Cuendias Abreu Hospital Hermanos Ameijeiras ELEMENTOS A CONSIDERAR Definición Tipo de recurrencia Investigaciones Manejo terapéutico MOMENTO PARA REALIZAR
RECURRENCIA POST PROSTATECTOMÍA RADICAL Dra. Beatriz Cuendias Abreu Hospital Hermanos Ameijeiras ELEMENTOS A CONSIDERAR Definición Tipo de recurrencia Investigaciones Manejo terapéutico MOMENTO PARA REALIZAR
FICHA TÉCNICA. Por vial liofilizado: Principio activo: Pamoato de triptorelina (D.C.I.) (equivalente a triptorelina)... 0,01125 g*
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Decapeptyl Trimestral 11,25 mg, inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por vial liofilizado: Principio activo: Pamoato de triptorelina (D.C.I.) (equivalente
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Decapeptyl Trimestral 11,25 mg, inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por vial liofilizado: Principio activo: Pamoato de triptorelina (D.C.I.) (equivalente
Alivio de los sofocos que aparecen durante la menopausia como consecuencia de la deprivación estrogénica.
 1. NOMBRE DEL MEDICAMENTO Normosoy 40 mg cápsulas duras 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada cápsula contiene: 290 mg de extracto etanólico 85% V/V seco de semillas de Glycine max (L.) Merr.
1. NOMBRE DEL MEDICAMENTO Normosoy 40 mg cápsulas duras 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada cápsula contiene: 290 mg de extracto etanólico 85% V/V seco de semillas de Glycine max (L.) Merr.
Vacuna frente al papilomavirus humano. (Comentarios a las fichas técnicas)
 Vacuna frente al papilomavirus humano (Comentarios a las fichas técnicas) Prof. Ángel Gil de Miguel, Catedrático de Medicina Preventiva y Salud Pública, Universidad Rey Juan Carlos, Comunidad de Madrid
Vacuna frente al papilomavirus humano (Comentarios a las fichas técnicas) Prof. Ángel Gil de Miguel, Catedrático de Medicina Preventiva y Salud Pública, Universidad Rey Juan Carlos, Comunidad de Madrid
CENAVUL Suspensión inyectable
 Camí Pedra Estela s/n 43205 Reus Telf. 977 75 72 73 Fax. 977 75 13 98 www.cenavisa.com E-mail: cenavisa@cenavisa.com FICHA TÉCNICA: CENAVUL Suspensión inyectable Reg. nº: 2145 ESP FICHA TÉCNICA (RESUMEN
Camí Pedra Estela s/n 43205 Reus Telf. 977 75 72 73 Fax. 977 75 13 98 www.cenavisa.com E-mail: cenavisa@cenavisa.com FICHA TÉCNICA: CENAVUL Suspensión inyectable Reg. nº: 2145 ESP FICHA TÉCNICA (RESUMEN
ANASTROZOL 1 mg Tabletas
 ANASTROZOL 1 mg Tabletas ANASTROZOL 1 mg Tabletas Anticanceroso COMPOSICIÓN: Cada tableta contiene: Anastrozol...1 mg Excipientes c.s. ACCIÓN FARMACOLÓGICA: Anastrozol es un inhibidor no esteroidal de
ANASTROZOL 1 mg Tabletas ANASTROZOL 1 mg Tabletas Anticanceroso COMPOSICIÓN: Cada tableta contiene: Anastrozol...1 mg Excipientes c.s. ACCIÓN FARMACOLÓGICA: Anastrozol es un inhibidor no esteroidal de
FICHA TÉCNICA. Principio activo: Triptorelina (D.C.I.) (en forma de acetato)..3,75 mg*
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Decapeptyl 3,75 mg, inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA - Por vial liofilizado: Principio activo: Triptorelina (D.C.I.) (en forma de acetato)..3,75
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Decapeptyl 3,75 mg, inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA - Por vial liofilizado: Principio activo: Triptorelina (D.C.I.) (en forma de acetato)..3,75
AMENORREA SECUNDARIA. Dra. Ma. Susana Apablaza H. Gíneco-Obstetra Ginecóloga Infanto-Juvenil Unidad Adolescencia Clínica Alemana Temuco
 AMENORREA SECUNDARIA Dra. Ma. Susana Apablaza H. Gíneco-Obstetra Ginecóloga Infanto-Juvenil Unidad Adolescencia Clínica Alemana Temuco Definición: Ausencia de menstruación en una mujer que ya ha menstruado
AMENORREA SECUNDARIA Dra. Ma. Susana Apablaza H. Gíneco-Obstetra Ginecóloga Infanto-Juvenil Unidad Adolescencia Clínica Alemana Temuco Definición: Ausencia de menstruación en una mujer que ya ha menstruado
ANDROPAUSIA Qué es eso?
 Conoce usted el significado? ANDROPAUSIA Qué es eso? Cambios hormonales debidos a disminución de los valores de testosterona que tienen lugar en los hombres de edad media relacionados con el proceso de
Conoce usted el significado? ANDROPAUSIA Qué es eso? Cambios hormonales debidos a disminución de los valores de testosterona que tienen lugar en los hombres de edad media relacionados con el proceso de
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Dolovet vet 2,4 g polvo para uso oral. 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Principio(s) activo(s): Ketoprofeno
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Dolovet vet 2,4 g polvo para uso oral. 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Principio(s) activo(s): Ketoprofeno
ENOXPRIM. Solución inyectable. Solución inyectable estéril, libre de pirógenos, contenida en jeringas pre-llenadas listas para usarse.
 ENOXPRIM Solución inyectable ENOXAPARINA FORMA FARMACÉUTICA Y FORMULACIÓN Cada jeringa contiene: Enoxaparina sódica 20 mg 40 mg Equivalente a 2,000 U.I. 4,000 U.I. Agua inyectable, c.b.p. 0.2 ml 0.4 ml
ENOXPRIM Solución inyectable ENOXAPARINA FORMA FARMACÉUTICA Y FORMULACIÓN Cada jeringa contiene: Enoxaparina sódica 20 mg 40 mg Equivalente a 2,000 U.I. 4,000 U.I. Agua inyectable, c.b.p. 0.2 ml 0.4 ml
Taller de actualización en anticoncepción 2016 ANTICONCEPCIÓN CON SOLO. atención primaria GESTÁGENOS. Raquel Rodríguez Rodríguez
 Curso de actualización en Taller de actualización en anticoncepción 2016 ginecología y anticoncepción en ANTICONCEPCIÓN CON SOLO atención primaria GESTÁGENOS Raquel Rodríguez Rodríguez Supresión del pico
Curso de actualización en Taller de actualización en anticoncepción 2016 ginecología y anticoncepción en ANTICONCEPCIÓN CON SOLO atención primaria GESTÁGENOS Raquel Rodríguez Rodríguez Supresión del pico
FICHA TECNICA. Acamprosato 333 mg Para consultar la lista completa de excipientes, ver sección 6.1
 FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO ZULEX 333 mg, Comprimidos recubiertos 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Acamprosato 333 mg Para consultar la lista completa de excipientes, ver sección 6.1
FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO ZULEX 333 mg, Comprimidos recubiertos 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Acamprosato 333 mg Para consultar la lista completa de excipientes, ver sección 6.1
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 ACICLOVIR 5% Crema CREMA ANTIVIRAL Página 1 ACICLOVIR 5% Crema Crema Principio Activo Aciclovir Excipientes necesarios
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 ACICLOVIR 5% Crema CREMA ANTIVIRAL Página 1 ACICLOVIR 5% Crema Crema Principio Activo Aciclovir Excipientes necesarios
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 GRISEOFULVINA 125 mg/5 ml SUSPENSION ANTIMICÓTICO Página 1 GRISEOFULVINA 125 mg/5 ml Suspensión Principio Activo
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 GRISEOFULVINA 125 mg/5 ml SUSPENSION ANTIMICÓTICO Página 1 GRISEOFULVINA 125 mg/5 ml Suspensión Principio Activo
1. NOMBRE DEL MEDICAMENTO. GONAPEPTYL Diario 0,1 mg/ml solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 1. NOMBRE DEL MEDICAMENTO GONAPEPTYL Diario 0,1 mg/ml solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada jeringa precargada de 1 ml de solución inyectable contiene 100 microgramos de acetato
1. NOMBRE DEL MEDICAMENTO GONAPEPTYL Diario 0,1 mg/ml solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada jeringa precargada de 1 ml de solución inyectable contiene 100 microgramos de acetato
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Glucosamina KERN PHARMA 1.500 mg polvo para solución oral EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada sobre
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Glucosamina KERN PHARMA 1.500 mg polvo para solución oral EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada sobre
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Lonactene (carbetocina) Solución para inyección IM, IV
 Nombre del producto: RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Lonactene (carbetocina) Forma farmacéutica: Fortaleza: Presentación: Solución para inyección IM, IV 100 µg/ml Estuche por una ampolleta
Nombre del producto: RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Lonactene (carbetocina) Forma farmacéutica: Fortaleza: Presentación: Solución para inyección IM, IV 100 µg/ml Estuche por una ampolleta
1. NOMBRE DEL PRODUCTO FARMACÉUTICO
 1. NOMBRE DEL PRODUCTO FARMACÉUTICO Andriol Testocaps 40 mg cápsulas 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada cápsula contiene 40,0 mg de undecanoato de testosterona, que es equivalente a 25,3 mg
1. NOMBRE DEL PRODUCTO FARMACÉUTICO Andriol Testocaps 40 mg cápsulas 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada cápsula contiene 40,0 mg de undecanoato de testosterona, que es equivalente a 25,3 mg
FICHA TÉCNICA. Excipientes con efecto conocido 1,38 g de sacarosa y 1,10 g glucosa. Para consultar la lista completa de excipientes ver sección 6.1.
 1. NOMBRE DEL MEDICAMENTO FICHA TÉCNICA STREPSILS pastillas para chupar sabor menta 2.- COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por pastilla para chupar: Amilmetacresol, 0,6 mg Alcohol 2,4-diclorobencílico,
1. NOMBRE DEL MEDICAMENTO FICHA TÉCNICA STREPSILS pastillas para chupar sabor menta 2.- COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por pastilla para chupar: Amilmetacresol, 0,6 mg Alcohol 2,4-diclorobencílico,
Guía Evaluación y tratamiento del Hirsutismo en mujeres premenopausicas
 Guía Evaluación y tratamiento del Hirsutismo en mujeres premenopausicas Martin K, Chang J, Ehrmann D, Ibanez L, Lobo R, Rosenfiel R, Shapiro J, Montori V, Swiglo B. The Endocrine Society, 2008 Dras P.
Guía Evaluación y tratamiento del Hirsutismo en mujeres premenopausicas Martin K, Chang J, Ehrmann D, Ibanez L, Lobo R, Rosenfiel R, Shapiro J, Montori V, Swiglo B. The Endocrine Society, 2008 Dras P.
FICHA TÉCNICA. LORATADINA KERN PHARMA está indicado para el tratamiento sintomático de rinitis alérgica y urticaria idiopática crónica.
 FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO LORATADINA KERN PHARMA 10 mg comprimidos EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 10 mg de loratadina. Lista de excipientes,
FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO LORATADINA KERN PHARMA 10 mg comprimidos EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 10 mg de loratadina. Lista de excipientes,
FARMACOS QUE ACTUAN EN EL SISTEMA REPRODUCTOR
 FARMACOS QUE ACTUAN EN EL SISTEMA REPRODUCTOR CLASE DE FARMACOS Durante la adolescencia inicias la toma de decisiones importantes, algunas de las cuales pueden influir a todo lo largo de tu vida. La elección
FARMACOS QUE ACTUAN EN EL SISTEMA REPRODUCTOR CLASE DE FARMACOS Durante la adolescencia inicias la toma de decisiones importantes, algunas de las cuales pueden influir a todo lo largo de tu vida. La elección
FICHA TÉCNICA. Por sobre: Acetato de calcio, 2,5 g (equivale a 635 mg de calcio), almidón de maíz, manitol (E421)
 FICHA TÉCNICA 1.- NOMBRE DEL MEDICAMENTO ROYEN 500 mg cápsula dura. ROYEN 2,5 g polvo para suspensión oral. 2.- COMPOSICIÓN CUALITATIVA Y CUANTITATIVA ROYEN 500 mg cápsula dura. Por cápsula: Acetato de
FICHA TÉCNICA 1.- NOMBRE DEL MEDICAMENTO ROYEN 500 mg cápsula dura. ROYEN 2,5 g polvo para suspensión oral. 2.- COMPOSICIÓN CUALITATIVA Y CUANTITATIVA ROYEN 500 mg cápsula dura. Por cápsula: Acetato de
1 comprimido de mg contiene los siguientes principios activos:
 1. NOMBRE DEL MEDICAMENTO Rennie Refluxine Comprimidos masticables 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 comprimido de 3.486 mg contiene los siguientes principios activos: Carbonato cálcico 1.250
1. NOMBRE DEL MEDICAMENTO Rennie Refluxine Comprimidos masticables 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 comprimido de 3.486 mg contiene los siguientes principios activos: Carbonato cálcico 1.250
FICHA TÉCNICA. Parches Sor Virginia Extracto de Capsicum frutescens 2,59%
 Página: 1 de 1 ÍNDICE: 1. NOMBRE DEL MEDICAMENTO 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 3. FORMA FARMACÉUTICA 4. DATOS CLÍNICOS: 4.1 Indicaciones terapéuticas 4.2 Posología y forma de administración
Página: 1 de 1 ÍNDICE: 1. NOMBRE DEL MEDICAMENTO 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 3. FORMA FARMACÉUTICA 4. DATOS CLÍNICOS: 4.1 Indicaciones terapéuticas 4.2 Posología y forma de administración
1. Es lo mismo menopausia y climaterio?
 1. Es lo mismo menopausia y climaterio? El término menopausia hace referencia al último periodo menstrual, es decir, tiene una fecha concreta. Se considera que la menopausia está establecida cuando transcurre
1. Es lo mismo menopausia y climaterio? El término menopausia hace referencia al último periodo menstrual, es decir, tiene una fecha concreta. Se considera que la menopausia está establecida cuando transcurre
FICHA TÉCNICA TOXOIDES TETÁNICO Y DIFTÉRICO (TD)
 1. DENOMINACIÓN DISTINTIVA. 2. DENOMINACIÓN GENÉRICA. Toxoides tetánico y diftérico 3. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA. Toxoide diftérico Toxoide tetánico Vehículo cbp 3 5 Lf 10 20 Lf 0.5 ml 4.
1. DENOMINACIÓN DISTINTIVA. 2. DENOMINACIÓN GENÉRICA. Toxoides tetánico y diftérico 3. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA. Toxoide diftérico Toxoide tetánico Vehículo cbp 3 5 Lf 10 20 Lf 0.5 ml 4.
Neevia docconverter 5.1
 CJIPlrTVLO 5 JI:JffICO:NCEqr[IO/OS 01{llLPS ANTICONCEPTIVOS ORALES La píldora fue inventada en Puerto Rico en 1956; 40 años mas tarde es consíderada uno de los avances más grandes del siglo XX. 16 Los
CJIPlrTVLO 5 JI:JffICO:NCEqr[IO/OS 01{llLPS ANTICONCEPTIVOS ORALES La píldora fue inventada en Puerto Rico en 1956; 40 años mas tarde es consíderada uno de los avances más grandes del siglo XX. 16 Los
Anexo III. Modificaciones a las secciones relevantes de la ficha técnica o resumen de las características del producto y los prospectos
 Anexo III Modificaciones a las secciones relevantes de la ficha técnica o resumen de las características del producto y los prospectos Nota: Estas modificaciones a las secciones relevantes de la Ficha
Anexo III Modificaciones a las secciones relevantes de la ficha técnica o resumen de las características del producto y los prospectos Nota: Estas modificaciones a las secciones relevantes de la Ficha
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. MAGNESIUM PYRE 64 mg comprimidos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO MAGNESIUM PYRE 64 mg comprimidos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 64 mg de magnesio (en forma de 550 mg de cloruro de magnesio,
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO MAGNESIUM PYRE 64 mg comprimidos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 64 mg de magnesio (en forma de 550 mg de cloruro de magnesio,
3. CRIPTORQUIDIA, HIPOGONADISMO HIPOGONADOTROPO Y DESARROLLO SEXUAL
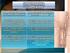 3. CRIPTORQUIDIA, HIPOGONADISMO HIPOGONADOTROPO Y DESARROLLO SEXUAL 3.1. Fisiopatología La criptorquidia es un hallazgo muy frecuente en los niños varones con SPW, algunos autores describen una incidencia
3. CRIPTORQUIDIA, HIPOGONADISMO HIPOGONADOTROPO Y DESARROLLO SEXUAL 3.1. Fisiopatología La criptorquidia es un hallazgo muy frecuente en los niños varones con SPW, algunos autores describen una incidencia
SÍNDROME DE OVARIOS POLIQUÍSTICOS
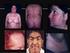 SÍNDROME DE OVARIOS POLIQUÍSTICOS Dr. Eric Saucedo de la Llata El Síndrome de Ovarios Poliquísticos (SOP) es la enfermedad endocrina (glandular) más común de las mujeres. Tiene una frecuencia del 5 al
SÍNDROME DE OVARIOS POLIQUÍSTICOS Dr. Eric Saucedo de la Llata El Síndrome de Ovarios Poliquísticos (SOP) es la enfermedad endocrina (glandular) más común de las mujeres. Tiene una frecuencia del 5 al
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. Auxina E-50, Auxina E-200, Auxina E-400 Vitamina E (Acetato de dl-? -tocoferol)
 1. NOMBRE DEL MEDICAMENTO Auxina E-50, Auxina E-200, Auxina E-400 Vitamina E (Acetato de dl-? -tocoferol) FICHA TÉCNICA 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por cápsula: Principio Activo:?? Auxina
1. NOMBRE DEL MEDICAMENTO Auxina E-50, Auxina E-200, Auxina E-400 Vitamina E (Acetato de dl-? -tocoferol) FICHA TÉCNICA 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Por cápsula: Principio Activo:?? Auxina
Clasificación de las crisis epilépticas para la programación terapéutica Farmacocinética de los fármacos antiepilépticos...
 Índice Parte 1 - Bases para la terapéutica con fármacos antiepilépticos Clasificación de las crisis epilépticas para la programación terapéutica... 19 Clasificación de las Crisis Epilépticas (1981)...
Índice Parte 1 - Bases para la terapéutica con fármacos antiepilépticos Clasificación de las crisis epilépticas para la programación terapéutica... 19 Clasificación de las Crisis Epilépticas (1981)...
Oxicodona. . Agonista puro opioide de los receptores mu, Kappa y delta, con efecto analgésico, ansiolítico y sedante.
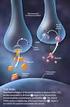 Oxicodona 1. Grupo Farmacoterapéutico:. Agonista puro opioide de los receptores mu, Kappa y delta, con efecto analgésico, ansiolítico y sedante. 2.- Formas farmacéuticas registradas:. Comprimidos de 10mg
Oxicodona 1. Grupo Farmacoterapéutico:. Agonista puro opioide de los receptores mu, Kappa y delta, con efecto analgésico, ansiolítico y sedante. 2.- Formas farmacéuticas registradas:. Comprimidos de 10mg
GUINV016B2-A16V1. Guía: Mensajeros químicos y sexualidad
 Biología GUINV016B2-A16V1 Guía: Mensajeros químicos y sexualidad Biología - Segundo Medio Sección 1 Observando y reflexionando Actividad A Junto con tu compañero(a), analiza la siguiente noticia y responde
Biología GUINV016B2-A16V1 Guía: Mensajeros químicos y sexualidad Biología - Segundo Medio Sección 1 Observando y reflexionando Actividad A Junto con tu compañero(a), analiza la siguiente noticia y responde
FICHA TÉCNICA. Bicalutamida Zentiva 50 mg comprimidos recubiertos con película EFG
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Bicalutamida Zentiva 50 mg comprimidos recubiertos con película EFG 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 50 mg de bicalutamida. Excipientes:
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Bicalutamida Zentiva 50 mg comprimidos recubiertos con película EFG 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 50 mg de bicalutamida. Excipientes:
ANEXO CONDICIONES O RESTRICCIONES A IMPLEMENTAR EN LOS ESTADOS MIEMBROS EN RELACIÓN CON LA UTILIZACIÓN SEGURA Y EFICAZ DEL MEDICAMENTO
 ANEXO CONDICIONES O RESTRICCIONES A IMPLEMENTAR EN LOS ESTADOS MIEMBROS EN RELACIÓN CON LA UTILIZACIÓN SEGURA Y EFICAZ DEL MEDICAMENTO CONDICIONES O RESTRICCIONES A IMPLEMENTAR EN LOS ESTADOS MIEMBROS
ANEXO CONDICIONES O RESTRICCIONES A IMPLEMENTAR EN LOS ESTADOS MIEMBROS EN RELACIÓN CON LA UTILIZACIÓN SEGURA Y EFICAZ DEL MEDICAMENTO CONDICIONES O RESTRICCIONES A IMPLEMENTAR EN LOS ESTADOS MIEMBROS
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Nombre del producto: Ovidrel 250 µg/0.5 ml (Coriogonadotropina alfa) Forma farmacéutica: Solución para inyección SC. Fortaleza: Presentación: Titular del registro
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Nombre del producto: Ovidrel 250 µg/0.5 ml (Coriogonadotropina alfa) Forma farmacéutica: Solución para inyección SC. Fortaleza: Presentación: Titular del registro
INFORMACIÓN PARA EL PRESCRIPTOR ELONVA Corifolitropina alfa 100 mcg/0,5 ml mcg/0,5 ml Solución Inyectable - Vía subcutánea VENTA BAJO RECETA
 INFORMACIÓN PARA EL PRESCRIPTOR ELONVA Corifolitropina alfa 100 mcg/0,5 ml - 150 mcg/0,5 ml Solución Inyectable - Vía subcutánea VENTA BAJO RECETA FORMULA: Cada jeringa prellenada de ELONVA 100 mcg/0,5
INFORMACIÓN PARA EL PRESCRIPTOR ELONVA Corifolitropina alfa 100 mcg/0,5 ml - 150 mcg/0,5 ml Solución Inyectable - Vía subcutánea VENTA BAJO RECETA FORMULA: Cada jeringa prellenada de ELONVA 100 mcg/0,5
Sección 9: Antiparkinsonianos
 201 Sección 9: Antiparkinsonianos 9.1 Fármacos utilizados en el parkinsonismo...202 9.2 Fármacos utilizados en el temblor esencial y trastornos relacionados...204 202 9.1 Fármacos utilizados en el parkinsonismo
201 Sección 9: Antiparkinsonianos 9.1 Fármacos utilizados en el parkinsonismo...202 9.2 Fármacos utilizados en el temblor esencial y trastornos relacionados...204 202 9.1 Fármacos utilizados en el parkinsonismo
FICHA TÉCNICA. Vispring 500 microgramos/ml colirio en solución en envases unidosis
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Vispring 500 microgramos/ml colirio en solución en envases unidosis 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de colirio en solución contiene: Tetrizolina
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Vispring 500 microgramos/ml colirio en solución en envases unidosis 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de colirio en solución contiene: Tetrizolina
FICHA TÉCNICA. El comprimido es redondo, blanco y marcado con el código NL 1.5 en una cara.
 1. NOMBRE DEL MEDICAMENTO NorLevo 1500 microgramos comprimido. FICHA TÉCNICA 2. COMPOSICIÓN CUANTITATIVA Y CUALITATIVA Cada comprimido contiene 1500 microgramos de levonorgestrel. Excipientes: Lactosa
1. NOMBRE DEL MEDICAMENTO NorLevo 1500 microgramos comprimido. FICHA TÉCNICA 2. COMPOSICIÓN CUANTITATIVA Y CUALITATIVA Cada comprimido contiene 1500 microgramos de levonorgestrel. Excipientes: Lactosa
FICHA DE INFORMACIÓN AL PACIENTE: ESPIRONOLACTONA
 FICHA DE INFORMACIÓN AL PACIENTE: ESPIRONOLACTONA 1.- QUÉ ES Y PARA QUE SE UTILIZA 1.1 Acción: Diurético y antihipertensivo, por alteración del mecanismo de funcionamiento renal con aumento de la eliminación
FICHA DE INFORMACIÓN AL PACIENTE: ESPIRONOLACTONA 1.- QUÉ ES Y PARA QUE SE UTILIZA 1.1 Acción: Diurético y antihipertensivo, por alteración del mecanismo de funcionamiento renal con aumento de la eliminación
DlSPOSIeIOM NI 6 3 9 6
 ~desakt S~de'1J~, ~~e'l~,4, n, 1/(,,4. 7, DlSPOSIeIOM NI 6 3 9 6 BUENOS AIRES, O 2 NOV 2012 VISTO el Expediente NO 1-0047-0000-010532-12-6 del Registro de la Administración Nacional de Medicamentos, Alimentos
~desakt S~de'1J~, ~~e'l~,4, n, 1/(,,4. 7, DlSPOSIeIOM NI 6 3 9 6 BUENOS AIRES, O 2 NOV 2012 VISTO el Expediente NO 1-0047-0000-010532-12-6 del Registro de la Administración Nacional de Medicamentos, Alimentos
FICHA TÉCNICA. Cada implante en jeringa precargada contiene 10,8 mg de goserelina (como acetato).
 1 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Zoladex Trimestral 10,8 mg implante en jeringa precargada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada implante en jeringa precargada contiene 10,8 mg de goserelina
1 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Zoladex Trimestral 10,8 mg implante en jeringa precargada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada implante en jeringa precargada contiene 10,8 mg de goserelina
Tratamiento: Iniciar tratamiento según el esquema terapéutico (Anexo 3) de todas las pacientes menores de años, que no tengan exploración patoló
 P R O C E S O S hemorragias uterinas anormales Definición funcional Proceso por el cual, tras una anamnesis específica realizada a una mujer que consulta debido a un sangrado anormal a través de los genitales,
P R O C E S O S hemorragias uterinas anormales Definición funcional Proceso por el cual, tras una anamnesis específica realizada a una mujer que consulta debido a un sangrado anormal a través de los genitales,
FASE FOLICULAR. Fase Tardía y Ovulación
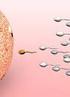 FASE FOLICULAR Fase Tardía y Ovulación Aumento importante de LH (6-10 veces) Inicio 2 días antes ovulación Pico máximo a 16 horas antes de ovulación Aumento importante FSH (2-3 veces) LH efecto de producción
FASE FOLICULAR Fase Tardía y Ovulación Aumento importante de LH (6-10 veces) Inicio 2 días antes ovulación Pico máximo a 16 horas antes de ovulación Aumento importante FSH (2-3 veces) LH efecto de producción
FICHA TÉCNICA. La duración estimada del tratamiento será de dos semanas.
 FICHA TÉCNICA 1. NOMBRE DE LA ESPECIALIDAD UVALETTE 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Contenido por comprimido recubierto: - 120,00 mg de extracto seco etanólico al 30%, de planta entera de Taraxacum
FICHA TÉCNICA 1. NOMBRE DE LA ESPECIALIDAD UVALETTE 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Contenido por comprimido recubierto: - 120,00 mg de extracto seco etanólico al 30%, de planta entera de Taraxacum
FICHA TÉCNICA. KETOISDIN 400 mg óvulos está indicado en adultos para el tratamiento local de
 1. NOMBRE DEL MEDICAMENTO KETOISDIN 400 mg óvulos FICHA TÉCNICA 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada óvulo contiene: 400 mg de ketoconazol Excipientes con efecto conocido: Butilhidroxianisol
1. NOMBRE DEL MEDICAMENTO KETOISDIN 400 mg óvulos FICHA TÉCNICA 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada óvulo contiene: 400 mg de ketoconazol Excipientes con efecto conocido: Butilhidroxianisol
INFORMACION PARA PRESCRIBIR AMPLIA
 INFORMACION PARA PRESCRIBIR AMPLIA 1. Nombre Comercial: PAMORELIN 2. Nombre Genérico: PAMOATO DE TRIPTORELINA 3. Forma Farmacéutica y Formulación: Suspensión. Cada frasco ámpula con liofilizado contiene:
INFORMACION PARA PRESCRIBIR AMPLIA 1. Nombre Comercial: PAMORELIN 2. Nombre Genérico: PAMOATO DE TRIPTORELINA 3. Forma Farmacéutica y Formulación: Suspensión. Cada frasco ámpula con liofilizado contiene:
Tratamiento de EPOC y oxigenoterapia
 Tratamiento de EPOC y oxigenoterapia Dr. Chih Hao Chen Ku Farmacología Clínica Hospital San Juan de Dios Universidad de Costa Rica Componentes del manejo 1. Valorar y monitorizar la enfermedad 2. Reducir
Tratamiento de EPOC y oxigenoterapia Dr. Chih Hao Chen Ku Farmacología Clínica Hospital San Juan de Dios Universidad de Costa Rica Componentes del manejo 1. Valorar y monitorizar la enfermedad 2. Reducir
LEXATUSSIN Dextrometorfano Bromhidrato 15 mg / 5 ml Jarabe
 LEXATUSSIN Dextrometorfano Bromhidrato 15 mg / 5 ml Jarabe LEXATUSSIN (Dextrometorfano Bromhidrato 15 mg/5 ml) Jarabe COMPOSICIÓN: Cada 100 ml de Jarabe contiene: Dextrometorfano Bromhidrato monohidrato...
LEXATUSSIN Dextrometorfano Bromhidrato 15 mg / 5 ml Jarabe LEXATUSSIN (Dextrometorfano Bromhidrato 15 mg/5 ml) Jarabe COMPOSICIÓN: Cada 100 ml de Jarabe contiene: Dextrometorfano Bromhidrato monohidrato...
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 COMPLEJO B COMPRIMIDOS RECUBIERTOS VITAMINA Página 1 COMPLEJO B Comprimidos Recubiertos Principio Activo Tiamina
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 COMPLEJO B COMPRIMIDOS RECUBIERTOS VITAMINA Página 1 COMPLEJO B Comprimidos Recubiertos Principio Activo Tiamina
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSCTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSCTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Cellufresh 5 mg/ml colirio en solución en envase unidosis 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de solución
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSCTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Cellufresh 5 mg/ml colirio en solución en envase unidosis 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de solución
1. NOMBRE DEL MEDICAMENTO. VALSEDAN 150 mg, Comprimidos recubiertos Extracto de Valeriana officinalis 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 1. NOMBRE DEL MEDICAMENTO VALSEDAN 150 mg, Comprimidos recubiertos Extracto de Valeriana officinalis 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene: Principio activo: Extracto seco
1. NOMBRE DEL MEDICAMENTO VALSEDAN 150 mg, Comprimidos recubiertos Extracto de Valeriana officinalis 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene: Principio activo: Extracto seco
Son hormonas contenidas en substancias líquidas que se aplican intramuscularmente en el glúteo o nalga, por medio de una jeringa.
 Qué son los hormonales inyectables? Son hormonas contenidas en substancias líquidas que se aplican intramuscularmente en el glúteo o nalga, por medio de una jeringa. Existen inyectables de dos tipos: Combinados
Qué son los hormonales inyectables? Son hormonas contenidas en substancias líquidas que se aplican intramuscularmente en el glúteo o nalga, por medio de una jeringa. Existen inyectables de dos tipos: Combinados
MIOMATOSIS UTERINA. Dra. Martha Gabriela García Sandoval
 Dra. Martha Gabriela García Sandoval Los leiomiomas algunas veces conocidos como miomas o fibromas son tumores benignos que se encuentran con gran frecuencia en el utero. 75% presentan miomas diagnosticados
Dra. Martha Gabriela García Sandoval Los leiomiomas algunas veces conocidos como miomas o fibromas son tumores benignos que se encuentran con gran frecuencia en el utero. 75% presentan miomas diagnosticados
FICHA TECNICA. ANASTROZOL NORMON 1 mg comprimidos recubiertos con película EFG
 FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO ANASTROZOL NORMON 1 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 1 mg de anastrozol. Excipientes:
FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO ANASTROZOL NORMON 1 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 1 mg de anastrozol. Excipientes:
RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO TOLFEDINE 4% 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA. INGREDIENTES ACTIVOS: Ácido tolfenámico... 4,00 g EXCIPIENTES:
RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO TOLFEDINE 4% 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA. INGREDIENTES ACTIVOS: Ácido tolfenámico... 4,00 g EXCIPIENTES:
Hormonas del cuerpo humano
 Hormonas del cuerpo humano Las hormonas son sustancias químicas producidas por las glándulas, tejidos especializados y neuronas que equilibran las funciones biológicas del cuerpo, como el metabolismo,
Hormonas del cuerpo humano Las hormonas son sustancias químicas producidas por las glándulas, tejidos especializados y neuronas que equilibran las funciones biológicas del cuerpo, como el metabolismo,
GINECOLOGÍA COLON/RECTO. por DR. MARIANA CARMONA
 GINECOLOGÍA COLON/RECTO por DR. MARIANA CARMONA La robótica ha revolucionado la cirugía ginecológica en los últimos años, siendo el Da Vinci una de sus máximas expresiones gracias a las numerosas ventajas
GINECOLOGÍA COLON/RECTO por DR. MARIANA CARMONA La robótica ha revolucionado la cirugía ginecológica en los últimos años, siendo el Da Vinci una de sus máximas expresiones gracias a las numerosas ventajas
AutorSPCosteoporVar.FT.doc FICHA TÉCNICA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO OSTEOPOR 830 mg comprimidos recubiertos. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Complejo de oseína-hidroxiapatita (COH) 830 mg, compuesto por: 75 mg de péptidos
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO OSTEOPOR 830 mg comprimidos recubiertos. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Complejo de oseína-hidroxiapatita (COH) 830 mg, compuesto por: 75 mg de péptidos
FICHA TÉCNICA. Bicalutamida ratiopharm 50 mg comprimidos recubiertos con película EFG
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Bicalutamida ratiopharm 50 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un comprimido contiene 50 mg de bicalutamida Excipientes
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Bicalutamida ratiopharm 50 mg comprimidos recubiertos con película EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un comprimido contiene 50 mg de bicalutamida Excipientes
CLIMATERIO Y MENOPAUSIA
 CLIMATERIO Y MENOPAUSIA 4to año de Medicina 21 de diciembre de 2010 Año 52 de la Revolución Dr.C. Miguel Sarduy Nápoles Profesor Titular Universidad Médica de La Habana CLIMATERIO Y MENOPAUSIA Sumario
CLIMATERIO Y MENOPAUSIA 4to año de Medicina 21 de diciembre de 2010 Año 52 de la Revolución Dr.C. Miguel Sarduy Nápoles Profesor Titular Universidad Médica de La Habana CLIMATERIO Y MENOPAUSIA Sumario
Curso Superior Bianual de Especialización en Endocrinología Ginecológica y Reproductiva
 Sociedad Argentina de Endocrinología Ginecológica y Reproductiva Ia y IIa Cátedra Ginecología Universidad Nacional de Córdoba Curso Superior Bianual de Especialización en Endocrinología Ginecológica y
Sociedad Argentina de Endocrinología Ginecológica y Reproductiva Ia y IIa Cátedra Ginecología Universidad Nacional de Córdoba Curso Superior Bianual de Especialización en Endocrinología Ginecológica y
1. NOMBRE DEL MEDICAMENTO. Orgametril 5 mg comprimidos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 1. NOMBRE DEL MEDICAMENTO Orgametril 5 mg comprimidos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 5 mg de linestrenol. Excipientes: lactosa monohidrato, 71 mg. Para consultar la
1. NOMBRE DEL MEDICAMENTO Orgametril 5 mg comprimidos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 5 mg de linestrenol. Excipientes: lactosa monohidrato, 71 mg. Para consultar la
ANEXO III MODIFICACIONES DEL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Y DEL PROSPECTO
 ANEXO III MODIFICACIONES DEL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Y DEL PROSPECTO 25 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO DE LOS MEDICAMENTOS QUE CONTENGAN BROMOCRIPTINA 4.2 Posología y forma
ANEXO III MODIFICACIONES DEL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Y DEL PROSPECTO 25 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO DE LOS MEDICAMENTOS QUE CONTENGAN BROMOCRIPTINA 4.2 Posología y forma
FICHA TÉCNICA 1.- NOMBRE DEL MEDICAMENTO. Bicalutamida ratiopharm 50 mg comprimidos recubiertos con película EFG
 FICHA TÉCNICA 1.- NOMBRE DEL MEDICAMENTO Bicalutamida ratiopharm 50 mg comprimidos recubiertos con película EFG 2.- COMPOSICION CUALITATIVA Y CUANTITATIVA Un comprimido contiene 50 mg de bicalutamida Excipientes:
FICHA TÉCNICA 1.- NOMBRE DEL MEDICAMENTO Bicalutamida ratiopharm 50 mg comprimidos recubiertos con película EFG 2.- COMPOSICION CUALITATIVA Y CUANTITATIVA Un comprimido contiene 50 mg de bicalutamida Excipientes:
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 INDOMETACINA 25 mg COMPRIMIDOS RECUBIERTOS ANTIINFLAMATORIO ANTIRREUMÁTICO Página 1 INDOMETACINA 25 mg Comprimidos
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 INDOMETACINA 25 mg COMPRIMIDOS RECUBIERTOS ANTIINFLAMATORIO ANTIRREUMÁTICO Página 1 INDOMETACINA 25 mg Comprimidos
FOLLETO DE INFORMACION AL PACIENTE. ABRAXANE LIOFILIZADO PARA SUSPENSIÓN INYECTABLE 100 mg
 FOLLETO INFORMACION AL PACIENTE ABRAXANE LIOFILIZADO PARA SUSPENSIÓN INYECTABLE 100 mg NANOPARTICULAS DE PACLITAXEL LIGADO A ALBÚMINA Leer esta Información para el paciente antes de empezar a recibir ABRAXANE
FOLLETO INFORMACION AL PACIENTE ABRAXANE LIOFILIZADO PARA SUSPENSIÓN INYECTABLE 100 mg NANOPARTICULAS DE PACLITAXEL LIGADO A ALBÚMINA Leer esta Información para el paciente antes de empezar a recibir ABRAXANE
1. NOMBRE DEL MEDICAMENTO 2. COMPOSICIÓN CUANTITATIVA Y CUALITATIVA 3. FORMA FARMACÉUTICA 4. DATOS CLÍNICOS
 POSTINOR 750 microgramos comprimidos. 1. NOMBRE DEL MEDICAMENTO 2. COMPOSICIÓN CUANTITATIVA Y CUALITATIVA Cada comprimido contiene 750 microgramos de levonorgestrel. Excipientes en el apartado 6.1. Comprimidos.
POSTINOR 750 microgramos comprimidos. 1. NOMBRE DEL MEDICAMENTO 2. COMPOSICIÓN CUANTITATIVA Y CUALITATIVA Cada comprimido contiene 750 microgramos de levonorgestrel. Excipientes en el apartado 6.1. Comprimidos.
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO LAMBDALINA 40 mg/g crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 g de crema contiene 40 mg de lidocaína Excipientes:
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO LAMBDALINA 40 mg/g crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 g de crema contiene 40 mg de lidocaína Excipientes:
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 PARACETAMOL 125 mg / 5 ml JARABE ANALGÉSICO ANTIPIRÉTICO Página 1 PARACETAMOL 125 mg / 5 ml Jarabe Principio Activo
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 PARACETAMOL 125 mg / 5 ml JARABE ANALGÉSICO ANTIPIRÉTICO Página 1 PARACETAMOL 125 mg / 5 ml Jarabe Principio Activo
Estradiol (DCI)... 2 mg (en forma de hemihidrato)
 1. NOMBRE DEL PRODUCTO ESTIREL 2 mg 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Estradiol (DCI)... 2 mg (en forma de hemihidrato) 3. FORMA FARMACEUTICA Comprimidos recubiertos 4. DATOS CLINICOS 4.1 Indicaciones
1. NOMBRE DEL PRODUCTO ESTIREL 2 mg 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Estradiol (DCI)... 2 mg (en forma de hemihidrato) 3. FORMA FARMACEUTICA Comprimidos recubiertos 4. DATOS CLINICOS 4.1 Indicaciones
FICHA TÉCNICA. Una vez reconstituida la solución contiene 1,875 mg/ml de triptorelina base (3,75 mg en 2 ml de volumen total).
 agencia española de medicamentos y productos sanitarios FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Decapeptyl mensual 3,75 mg, polvo y disolvente para suspensión inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
agencia española de medicamentos y productos sanitarios FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Decapeptyl mensual 3,75 mg, polvo y disolvente para suspensión inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 MEBENDAZOL 100 mg COMPRIMIDOS RECUBIERTOS ANTIHELMÍNTICO Página 1 MEBENDAZOL 100 mg Comprimidos Recubiertos Principio
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 MEBENDAZOL 100 mg COMPRIMIDOS RECUBIERTOS ANTIHELMÍNTICO Página 1 MEBENDAZOL 100 mg Comprimidos Recubiertos Principio
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO. CUNISER 500 Gonadotropina sérica equina (PMSG), en polvo y disolvente para solución inyectable.
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO CUNISER 500 Gonadotropina sérica equina (PMSG), en polvo y disolvente para solución inyectable. 2. COMPOSICIÓN CUALITATIVA
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO CUNISER 500 Gonadotropina sérica equina (PMSG), en polvo y disolvente para solución inyectable. 2. COMPOSICIÓN CUALITATIVA
TERAPÉUTICA FARMACOLÓGICA EN ATENCIÓN PRIMARIA
 MÓDULO I Sesión 1 ASPECTOS BÁSICOS DE FARMACOLOGÍA. Fecha: 12-Mar-11 Farmacología Básica. 1.- Definiciones en farmacología. 2.- Concepto de receptor. 3.- Mecanismos de acción de los fármacos. 4.- Variantes
MÓDULO I Sesión 1 ASPECTOS BÁSICOS DE FARMACOLOGÍA. Fecha: 12-Mar-11 Farmacología Básica. 1.- Definiciones en farmacología. 2.- Concepto de receptor. 3.- Mecanismos de acción de los fármacos. 4.- Variantes
FICHA TECNICA. P R A M O X Pramocaína
 FICHA TECNICA P R A M O X Pramocaína 1. NOMBRE DEL MEDICAMENTO PRAMOX Gel PRAMOX Crema PRAMOX Emulsión 2. COMPOSICION CUALITATIVA Y CUANTITATIVA PRAMOX Gel y Crema :. Cada 100 g contienen: Pramocaína (DCI)
FICHA TECNICA P R A M O X Pramocaína 1. NOMBRE DEL MEDICAMENTO PRAMOX Gel PRAMOX Crema PRAMOX Emulsión 2. COMPOSICION CUALITATIVA Y CUANTITATIVA PRAMOX Gel y Crema :. Cada 100 g contienen: Pramocaína (DCI)
FICHA DE INFORMACIÓN AL PACIENTE: CITALOPRAM
 FICHA DE INFORMACIÓN AL PACIENTE: CITALOPRAM 1.1 Acción: Antidepresivo. 1.- QUÉ ES Y PARA QUE SE UTILIZA 1.2 Cómo actúa este fármaco: Inhibe la recaptación de serotonina a nivel de la membrana neuronal,
FICHA DE INFORMACIÓN AL PACIENTE: CITALOPRAM 1.1 Acción: Antidepresivo. 1.- QUÉ ES Y PARA QUE SE UTILIZA 1.2 Cómo actúa este fármaco: Inhibe la recaptación de serotonina a nivel de la membrana neuronal,
Documento Resumen: Procedimiento para la ILVE
 Documento Resumen: Procedimiento para la 1. Elaboración de la historia clínica Implica: Determinar el estado de embarazo. La realización del examen físico. Efectuar análisis de laboratorio. 1.1 Determinar
Documento Resumen: Procedimiento para la 1. Elaboración de la historia clínica Implica: Determinar el estado de embarazo. La realización del examen físico. Efectuar análisis de laboratorio. 1.1 Determinar
9º Congreso de la Sociedad Española de Contracepción
 9º Congreso de la Sociedad Española de Contracepción 1ª Reunión Iberoamericana de Contracepción Hospital Gineco-Obstétrico Eusebio Hernández La Habana, Cuba Clínica Mediterránea Médica Valencia, Castelló,
9º Congreso de la Sociedad Española de Contracepción 1ª Reunión Iberoamericana de Contracepción Hospital Gineco-Obstétrico Eusebio Hernández La Habana, Cuba Clínica Mediterránea Médica Valencia, Castelló,

 Full version is >>> HERE
Full version is >>> HERE