UNIVERSIDAD NACIONAL DE FRONTERA CEPREUNF CICLO REGULAR tenemos: corrosión, acidez,
|
|
|
- Pablo de la Cruz Castillo
- hace 5 años
- Vistas:
Transcripción
1 Curso: QUÍMICA Semana 01 Tema: MATERIA Y ENERGIA MATERIA: Es toda realidad objetiva que tiene masa, ocupa un lugar en el espacio e impresiona a nuestros sentidos. Por ejemplo, el agua, el aire, las frutas, la tinta, madera, etc. PROPIEDADES DE LA MATERIA: a. Por su Naturaleza: Son aquellas que nos proporcionan información de la forma como una sustancia se comporta o distingue de las demás, pero que no nos sirven para identificar qué clase de materia es. Pueden ser: 1. Generales: Comunes a todo tipo de materia, estas son: extensión, inercia, indestructibilidad, divisibilidad, dilatación, porosidad (discontinuidad), impenetrabilidad, ponderabilidad (peso), atracción, color, olor, sabor. 2. Específicas: Comunes a determinado conjunto de sustancia, tenemos: para sólidos (dureza, maleabilidad, ductibilidad, tenacidad, elasticidad) y para fluidos (gases y líquidos) estas son: (tensión superficial, viscosidad, compresibilidad, expansibilidad). b. Propiedades Particulares: Aquellas que dependen de cada tipo de sustancia y que sirven para diferenciarlas unas de otras, estas son: 1. Físicas: Aquellas que pueden medirse sin alterar la estructura o composición de la materia, tenemos: temperatura, punto fusión, punto ebullición, densidad, color, índice de refracción, solubilidad, etc 2. Químicas: Son aquellas que describen el comportamiento de una sustancia en las reacciones químicas. Así tenemos: que a la intemperie el Hierro se oxida, mientras el oro no; el oxígeno es comburente, el nitrógeno no, etc. dentro de este grupo tenemos: corrosión, acidez, inflamabilidad, combustibilidad, electronegatividad, poder reductor, etc. c. Por la cantidad de masa: 1. Extensivas: Aquellas que dependen de la cantidad de masa. Tenemos: volumen, inercia, impenetrabilidad, tenacidad, calor ganado o perdido, etc. 2. Intensivas: Aquellas que no dependen de la cantidad de masa. Tenemos: temperatura, densidad, color, acidez, dureza, etc. ESTADOS DE AGREGACIÓN DE LA MATERIA: En el universo la materia se encuentra en cuatro estados. Los que pueden interactuar entre ellos. Sus principales características son: Sólido: Las fuerzas de cohesión son mayores que las de repulsión, tienen forma y volumen definido. Ejemplo: madera, hielo, ladrillo, alambre, etc. Líquido: Las fuerzas de cohesión y repulsión son parecidas, tienen volumen definido y toman la forma del recipiente que los contiene. Ejemplo: agua, aceite, alcohol, etc. Gaseoso: Las fuerzas de repulsión son mayores que las de cohesión, no tienen forma ni volumen definido, ocupando todo el volumen del recipiente que los contiene. Ejemplo: aire, propano, oxígeno, etc. Plasmático: Se halla a elevadas temperaturas (mayores a 10 millones de grados Kelvin); es el más abundante del universo, se encuentra en las estrellas como el sol, núcleo de los cometas, etc. Los cambios de estado que sufre la materia y el correspondiente nombre de cada uno son: DOCENTE Ing. Carlos Salazar 1
2 Proceso exotérmico con Desprendimiento de calor Sublimación Sólido concebible de un material. Por lo tanto son partículas, las moléculas, los átomos, los protones, neutrones, electrones, fotones, etc. Solidificación Fusión Líquido Licuación o Vaporización Condensación Gaseoso Ionización Plasmático Deposición Proceso endotérmico con Absorción de calor La materia se puede dividir en: Materia Cuerpo Partícula Molécula Átomo Partículas Sub atómicas Hasta el grado de molécula la materia conserva sus propiedades características y se puede llegar a ella mediante medios mecánicos y físicos. Para obtener átomos tenemos que usar medios químicos. CAMBIOS DE LA MATERIA: a. Físicos: Son aquellos que ocurren sin que se produzca alteración en la composición química de la materia. Se cambia la forma, el tamaño, el estado de agregación, el estado de movimiento. Ejemplo: cambios de estado, doblar un alambre, disolver azúcar en agua, etc. b. Químicos: Son aquellos en los que se altera la composición química de la materia. Ejemplo: oxidación de un clavo, digestión de los alimentos, fermentaciones, fotosíntesis, quemar un papel, etc. c. Nucleares: Aquellos en los cuales se modifica la constitución del núcleo de los átomos. En ellos hay un gran desprendimiento de energía y pérdida lenta de masa. Ejemplo: fusión y fisión nuclear. ALOTROPIA: Propiedad de ciertos elementos de hallarse en un mismo estado físico en 2 ó más formas distintas. Ejemplo: O 2 O 3 (Oxígeno Ozono); S 4 S 8 (Azufre rombico y monoclínico); P 4 P 12 (Fósforo blanco y rojo) GRADO DE DIVISIÓN DE LA MATERIA: El concepto de partícula es amplio y lo usamos mucho en química, abarca desde una pequeña porción de materia hasta la más ínfima porción SISTEMA: Es una porción limitada de materia que tiene fronteras y que se aísla para su estudio. Pueden ser: a. Abiertos: Cuando hay transferencia de masa y energía entre el sistema y el medio ambiente. En estos hay que limitar el sistema a lo que tenemos en estudio. b. Cerrados: Cuando no hay transferencia de masa pero si de energía con el medio ambiente. c. Aislados: Cuando no hay transferencia de masa y energía con el medio ambiente. Los sistemas se clasifican en: a. Homogéneos: Aquellos en donde todos los puntos de su masa presentan las mismas propiedades físicas y químicas. Ejemplo: solución de NaCl, agua pura, aire, etc. b. Heterogéneos: Aquellos que están formados por dos ó más fases que pueden estar en un mismo o diversos estados de agregación. Ejemplo: agua con aceite, granito con arena, etc. FASE: Es cada una de las partes homogéneas que forman un sistema material. Por el número de fases los sistemas pueden ser: monofásicos, difásicos, trifásicos, etc. COMPONENTE: Es cada una de las sustancias (simples o compuestas) que están presentes en un sistema. DOCENTE Ing. Carlos Salazar 2
3 Ejemplos: 1. En un vaso a medio llenar se tiene agua y aceite cuántas fases y componentes hay? Aceite Se tiene: H2O 2 fases y 2 componentes 2. En un recipiente cerrado se tiene agua, alcohol, hielo y aceite hasta sus ¾ partes, cuántas fases y componentes hay? Vapores de agua, alcohol y aceite Aceite Hielo Agua y alcohol SUSTANCIAS PURAS: Toda sustancia homogénea con características físicas y químicas propias. Pueden ser: a. Elementos: Sustancias simples formadas por un solo tipo de átomos no pueden ser separados en otras más simples. Estos son los 109 elementos químicos oficialmente reconocidos. A las moléculas formadas por átomos iguales como el H2, O2, N2, P4, etc se les llama sustancias elementales. b. Compuestos: Sustancias formadas por átomos de elementos diferentes, se pueden separar por procesos químicos. Se les representa mediante fórmulas. Ejemplo: agua (H2O); alcohol etílico (C2H5OH), ácido sulfúrico (H2SO4); etc. Se tiene: 4 fases y 3 componentes MÉTODOS DE SEPARACIÓN DE MEZCLAS: CLASIFICACIÓN DE LA MATERIA: 1. Filtración: Nos permite separa sólidos insolubles de un líquido. Ejemplo: arena de agua. 2. Decantación: Nos permite separa líquidos inmiscibles como agua con aceite o sólidos muy finos de líquidos aprovechando su diferencia de densidad como en el agua turbia; a esta también se le llama sedimentación. MEZCLA: Sistema formado por dos ó más sustancias en cantidades variables, donde cada componente conserva sus propiedades. No tienen fórmula y pueden ser: a. Homogéneas: Cuando las sustancias que la constituyen forman una sola fase. Ejemplo: agua azucarada, bronce, gasolina, vinagre, oro de 18 kilates, etc. b. Heterogéneas: Aquellos sistemas que presentan dos ó más fases. Ejemplo: agua-hielo, aceite-agua, arenacemento, etc. pueden ser: Agregados: como ensalada de frutas Suspensiones: como néctar de frutas Coloides: como la mayonesa. 3. Cristalización: Nos permite separa un sólido soluble de un líquido como la sal del agua, se puede acelerar calentando la solución o colocándola en un depósito de gran área. 4. Destilación: Se utiliza para separar líquidos miscibles, aprovechando su diferente temperatura de ebullición. Pueden ser: simple (separación de 2 líquidos, como agua y alcohol etílico) y fraccionada (separación de tres o más componentes, como el petróleo). 5. Tamizado: Técnica que nos permite separar sólidos de diferente diámetro, como el usado en las canteras para separar piedras grandes, piedra mediana, confitillo, arena gruesa y arena fina. 6. Centrifugación: Se utiliza para separar sólidos suspendidos en un líquido mediante la aplicación de una fuerza centrífuga. DOCENTE Ing. Carlos Salazar 3
4 7. Licuación: Técnica usada para separar mezclas gaseosas, como nitrógeno del oxígeno. ENERGÍA: Es la capacidad que tiene la materia para efectuar trabajo o transferir calor. LEY DE CONSERVACIÓN MATERIA - ENERGÍA: Fue enunciada por Albert Einstein, dice: la materia y la energía no se crean ni se destruyen, sólo se transforman. Dicha interconversión se expresa mediante la ecuación: E = mv 2 Dónde: E = Energía, en joule m = Masa, en kilogramos v = velocidad de la luz = 3 x 10 8 m/s Ejemplo: Cuál es la cantidad de energía, en joule, que se obtiene al desintegrase 2 gramos de Hidrógeno. Cuando un cuerpo está en movimiento, está sujeto a los dos tipos de energía; luego, su energía total estará dada por la expresión: E = Ec + Ep Otras formas de energía son: radiante, nuclear, química, luminosa, eléctrica, eolica, sonora, hidráulica, etc. CALOR: Es una forma de energía, se mide frecuentemente en calorías. En el S.I la unidad de medida es el joule. 1 joule = 1kg x CALOR ESPECÍFICO (c.e): Es la cantidad de calor necesario para elevar la temperatura de un gramo de sustancia en un grado centígrado (o grado Kelvin) sin cambio de fase. c.e = Q m t 2 m 2 s = 10 7 ergios E = (2g x 1 ) (3 x 10 8 Kg 1000g m s ) 2 = 6 x Joule El c.e de una sustancia difiere del estado (sólido, líquido o gaseoso) en que se encuentre. Ejercicio: Qué masa en gramos de una sustancia radiactiva se desintegra cuando se libero 9 x 1010 joule. CLASES DE ENERGÍA: 1. Cinética: Es aquella que posee la materia debido a su estado de movimiento. Se expresa mediante: Dónde: m = Masa del cuerpo v = Velocidad del cuerpo 2. Potencial: Es aquella que posee la materia por la posición (altura) en la que se encuentra. Se calcula mediante: E = mgh Dónde: g: Aceleración de la gravedad h: altura Ejemplo: c.e; H2O (Hielo) = 2,09; J/g C H2O ( Liquida) = 4,18 J/g C CAPACIDAD CALORÍFICA (C): Es la cantidad de calor necesaria para elevar la temperatura de una masa de sustancia en 1 C. Esto es: C = m.ce Conocido el calor específico de una sustancia, se puede determinar la energía liberada o absorbida, aplicando: Q = C x T = m. c.e. T Además, en todo sistema en el que se tiene varios objetos, cuando se llega al equilibrio térmico se cumple: Q Ganado = Q perdido E = Ec + Ep DOCENTE Ing. Carlos Salazar 4
5 CUESTIONARIO 1. Marque verdadero o falso según corresponda: I. La materia se clasifica en mezclas y sustancias. II. La sustancia se caracteriza por tener características definidas. III. La mezcla homogénea se puede separar por decantación. IV. Una mezcla heterogénea se separa por métodos físicos a) VVFV b) VVVV c) FFFF d) FFVV e) VFVF 2. Con respecto a las sustancias marque verdadero o falso según corresponda I. Todos los compuestos son iónicos II. Algunos compuestos están formados por moléculas III. Los elementos están formados por un solo tipo de átomos a) FVV b) FFF c) VFV d) VFF e) FFV 3. Seleccione mezclas homogéneas: I) Gasolina II) acero III) arena IV) jugo de frutas a) I, IV b) I,III c) II,III d) III,IV e) I,II 4. La alternativa que contiene una sustancia elemental y una mezcla, respectivamente es: a) Ozono aire b) alcohol éter c) gasolina diamante d) cuarzo azufre e) vino fósforo 5. La propiedad de la materia que indica la presencia de espacios vacíos en ella se denomina y es una propiedad a) Extensión particular b) discontinuidad - particular c) discontinuidad general d) divisibilidad general e) indestructibilidad general 6. La es la capacidad que tienen algunos sólidos de ser transformados en hilos y es una propiedad a) Ductibilidad general b) ductibilidad particular c) maleabilidad particular d) elasticidad general e) elasticidad general 7. La materia se caracteriza por presentar fuerzas de cohesión de igual magnitud que las fuerzas de repulsión, y presenta fluidez. a) Sólida b) líquida c) gaseosa d) plasmática e) amorfa 8. El término licuación se emplea cuando un... pasa al estado... a) sólido líquido b) gas líquido c) vapor líquido d) líquido gas e) líquido vapor 9. Cuál de los siguientes cambios es químico? a) Fusión de un metal DOCENTE Ing. Carlos Salazar 5
6 b) combustión de leña e) desintegración del uranio c) sublimación de la naftalina d) evaporación del agua 10. En el párrafo: El azufre es un sólido amarillo pálido, que tiene dos formas alotrópicas, se quema en el aire para formar SO2. Al calentarse a 180 C toma coloración marrón. Funde a 113 C y no es soluble en el agua. Cuántas propiedades son físicas y cuántas químicas. a) 0, 6 b) 4, 2 c) 5, 1 d) 2, 4 e) 3, Si un profesor de química le solicita separar el aceite y azúcar de una mezcla de aceite y azúcar disuelto en agua; qué métodos de separación utilizaría? a) decantación y destilación b) destilación y filtración b) cristalización y filtración d) filtración y centrifugación e) decantación y cristalización 12. Una solución acuosa de sacarosa con aceite en un vaso de precipitado a medio llenar formar un sistema de... fases y... componentes a) 3, 3 b) 2, 3 c) 2, 2 d) 3, 2 e) 3, Etanol, cloroformo, agua y 2 cubitos de hielo se mezclan en un sistema cerrado y aislado, entonces el número de fases y componentes es: a) 4, 4 b) 5, 4 c) 3, 4 d) 4, 3 e) 3,3 14. Cuál será la energía en Joule liberada cuando se descomponen 5 mg de material radiactivo? a) 4,5x10 11 b) 5,0x10-10 c) 4,5x10 17 d) 1,5x10 14 e) 1,5x Calcular la masa en mg desintegrada en un proceso nuclear, si se liberaron 9x1012 J. a) 1x10 11 b) 1x10 9 c) 1x10 10 d) 1x10 2 e) 1x Calcule el calor específico en J/g C del oro si para variar la temperatura en 100 C de una muestra de 10g de este metal se necesitaron 129J. a) 1,20x10-2 b) 2,09x10-1 c) 1,29x10-1 d) 7,75x10-1 e) 7,75x Calcular la capacidad calorífica en kj/ C de 50 g de agua si el ce agua = 1cal g -1 C -1 a) 5,00x10-3 b) 5,00x10-2 c) 2,09x10-1 d) 5,00x10 3 e) 2,09x Calcular el calor en kj absorbido cuando un recipiente de 100g de vidrio pírex se calentó desde 25 C hasta 95 C. ( ce vidrio pírex = 0.8Jg-1 C-1) DOCENTE Ing. Carlos Salazar 6
7 a) 7,2x10 1 b) 5,06x10-1 c) 5,6x10 0 d) 3,6x10 1 e) 7,7x Una plancha de hierro (ce= 0,106 cal/g C) de 100g se calentó desde 20 C hasta 120 C. Calcule el calor ganado en calorías. a) 1,42x10 4 b) 1,10x10 4 c) 1,06x10 3 d) 1,76x10 3 e) 1,62x A un termo que contenía 50mL de agua a 80 C se agregaron 30mL de agua a 8 C rápidamente se cerró herméticamente. Cuál será la temperatura de equilibrio en C de la mezcla? a) 53 b) 25 c) 66 d) 78 e) Cuando doblo una barra de vidrio, esta llega a romperse, Por qué? a) Es transparente b) Es Frágil c) Es barata d) Es insignificante e) Solo se usa para las ventanas 22. Evalué lo que corresponde a la alotropía e indique (V) o falso (F) Es propiedad de algunos compuestos químicos Es propiedad de cada elemento químico Los alótropos poseen propiedades diferentes a pesar de contener átomos del mismo elemento. H y H2 son alótropos del H a) FFVF b) FVVF c) FVVV d) VVFF e) FFVV 23. Cuál es el máximo responsable de todos los procesos de oxidación y corrosión que se dan en los materiales expuestos a su acción? a) Nitrógeno b) Oxígeno c) Carbono d) Hidrógeno e) aire 24. La atracción de molécula - molécula se llama: a) gravedad b) gravitación c) cohesión d) afinidad e) adhesión 25. El cobre se transforma en hilos por la: a) masa b) ductilidad c) volumen d) maleabilidad e) elasticidad 26. Mide la cantidad de materia: a) Volumen b) Masa c) Extensión d) Peso e) Todas 27. Una Jarra vacía pesa 25 g, si se llena totalmente de agua pesará 125 g. Si en vez de agua se llena totalmente con aceite pesaría 105 g. Calcular la densidad del aceite a) 0.8 g/cm 3 b) 1.8 g/cm 3 c) 0.08 g/cm 3 DOCENTE Ing. Carlos Salazar 7
8 d) 0.18 g/cm 3 e) g/cm No es evidencia de un cambio químico a) Cambio de color b) Formación de un precipitado c) Evaporación de una sustancia líquida d) Desprendimiento de un gas e) Desprendimiento de calor 29. Indique la relación incorrecta. a) mayonesa: mezcla heterogénea b) vinagre: mezcla homogénea c) salmuera: mezcla homogénea d) jugo de fresas: mezcla homogénea e) mermelada: mezcla heterogénea 30. Señale la sustancia compuesta ternaria de mayor atomicidad. a) SCl 2 b) Fe 3O 4 c) C 2H 5OH d) H 2CO 3 e) CH 3CH 3 EVALUACIÓN 1. Indique la relación correcta entre el proceso realizado y el tipo de partícula obtenido, que verifican la discontinuidad de la materia: 1. Molienda ( ) Moléculas o Iones 2. Disolución ( ) Electrones, protones y neutrones 3. Electrolisis ( ) partículas 4. Reacción nuclear ( ) Átomos a) 1,2,3,4 b) 3,1,2,4 c) 4,2,1,2 d) 2, 4, 1,3 e) 2, 1, 3,4 2. Indique la secuencia correcta: ( ) Todo compuesto químico es una sustancia. ( ) Toda sustancia es un compuestos químico. ( ) El agua de mar es una mezcla. ( ) Las aguas duras son sustancias químicas. a) VFVF b) VFFF c) VVFF d) VVVF e) FFVV 3. El número de proposiciones correctas es: I. El estado de agregación de un cuerpo depende de las condiciones de presión y temperatura. II. Los estados fundamentales de la materia son sólido, líquido, gaseoso y coloidal. III. Existen sistemas heterogéneos donde hay una sola sustancia. IV. El volumen y la masa son propiedades físicas. V. El aire es una sustancia compuesta. a) 5 b) 3 c) 1 d) 2 e) 4 4. Indicar la secuencia correcta: Las prop. Físicas se pueden medir sin modificar la identidad de la sustancia. Las prop. Físicas pueden ser extensivas e intensivas. La inflamabilidad es una propiedad química. a) VVF b) FVV c) VFV d) VFF e) VVV DOCENTE Ing. Carlos Salazar 8
9 5. Cierto investigador, después de sintetizar y analizar un nuevo compuesto químico encontró que: su densidad es 1,75 g/ml; posee gran conductividad eléctrica, es muy soluble en agua, tiene gran resistencia a la oxidación ambiental, es blando y de color azul. En el orden dado identifíquelas como físicas (F) o químicas (Q): a) FFFQFF b) FQFQFF c) FQFQFQ d) FQQQFF e) FQFQQF 6. Cuando Se mezcla KI(ac) con Pb(NO3)2(ac) ocurre un cambio químico; formándose una nueva sustancia, el precipitado de PbI2. Esta sustancia es un sólido, de color amarillo a la temperatura de 25 C, tiene una masa de 2,5g y su densidad aproximada es 1,8g/cm3. El orden de propiedades extensivas e intensivas del PbI2 respectivamente son: a) I,E,I,I b) I,I,E,I c) I,E,E,I d) E,I,E,I e) I,I,E,E 7. Se mezclan con agitación en recipiente cerrado a 0 C y presión atmosférica las siguientes sustancias puras: hielo, agua y azúcar; luego se calienta hasta 25 C manteniendo la agitación. Que proposiciones son correctas: I. La mezcla inicial antes de agitar tiene 4 fases. II. La mezcla luego de agitarse a 0 C tiene 2 fases. III. La mezcla luego de agitarse a 25 C tiene 2 fases. 8. Por destilación de una solución se obtiene un líquido que destila a temperatura constante (80 C). En el fondo del recipiente queda un residuo sólido amarillento que se disuelve en agua, respecto a esto podemos afirmar que son ciertos: 1. Es un fenómeno físico 2. Es un fenómeno químico 3. La solubilidad es una prop. Física 4. El líquido es una sust. Pura. a) 1,2 y 3 b) 1y 4 c) 2,3 y 4 d) 1,2y 4 e) 1,3 y 4 9. Suponiendo que la 1ra bomba atómica contenía 12kg de material fisionable y durante la explosión se liberó 1,08x1013 KJ, cuál es el porcentaje de material fisionable que se convirtió en energía? a) 1% b) 5% c) 10% d) 20% e) 50% 10. Para operar una máquina térmica se requieren 9,0x1010J. Cuántas de estas máquinas se podrán operar con la energía obtenida de la transformación del 10% de una muestra de 1g de U 235? a) 1 b) 10 c) 25 d) 100 e) 75 a) I b) I y II c) I y III d) II y III e) III DOCENTE Ing. Carlos Salazar 9
10 DOCENTE Ing. Carlos Salazar 10
TALLER DE AUTOEVALUACIÓN DE PERIODO
 TALLER DE AUTOEVALUACIÓN DE PERIODO I. Relaciona la columna de la izquierda con la de la derecha escribiendo dentro del paréntesis la letra que corresponda a la respuesta correcta. 1.-Es un ejemplo de
TALLER DE AUTOEVALUACIÓN DE PERIODO I. Relaciona la columna de la izquierda con la de la derecha escribiendo dentro del paréntesis la letra que corresponda a la respuesta correcta. 1.-Es un ejemplo de
Materia. La materia es cualquier sustancia que tenga masa y ocupe un espacio.
 Materia La materia es cualquier sustancia que tenga masa y ocupe un espacio. Propiedades fundamentales de la materia Generales o extensivas Específicas o intensivas Físicas Químicas Propiedades generales
Materia La materia es cualquier sustancia que tenga masa y ocupe un espacio. Propiedades fundamentales de la materia Generales o extensivas Específicas o intensivas Físicas Químicas Propiedades generales
TEMA 1: MATERIA, CLASIFICACIÓN Y ESTADOS DE AGREGACIÓN CLASIFICACIÓN Y ESTADOS DE AGREGACIÓN
 TEMA 1: MATERIA, CLASIFICACIÓN Y ESTADOS DE AGREGACIÓN CLASIFICACIÓN Y ESTADOS DE AGREGACIÓN Reconoce e identifica las diferentes clases de materia. 1. Completa el siguiente esquema: 2. Indique si los
TEMA 1: MATERIA, CLASIFICACIÓN Y ESTADOS DE AGREGACIÓN CLASIFICACIÓN Y ESTADOS DE AGREGACIÓN Reconoce e identifica las diferentes clases de materia. 1. Completa el siguiente esquema: 2. Indique si los
La Materia y sus Cambios
 La Materia y sus Cambios 1. Química 2. Concepto de Materia y Energía 3. Estados de la Materia 4. Propiedades de la Materia 5. Composición de la Materia 6. Métodos de Separación de Mezclas 1. Química Química:
La Materia y sus Cambios 1. Química 2. Concepto de Materia y Energía 3. Estados de la Materia 4. Propiedades de la Materia 5. Composición de la Materia 6. Métodos de Separación de Mezclas 1. Química Química:
ESTADOS DE AGREGACIÓN DE LA MATERIA
 LA MATERIA LA MATERIA Materia es todo aquello que ocupa un lugar en el espacio y tiene masa. La madera, el agua, el corcho, la sal,.. Son clases diferentes de materia. Las clases de materia que se utilizan
LA MATERIA LA MATERIA Materia es todo aquello que ocupa un lugar en el espacio y tiene masa. La madera, el agua, el corcho, la sal,.. Son clases diferentes de materia. Las clases de materia que se utilizan
Curso Química General I. Apuntes Unidad 1
 Curso Química General I Apuntes Unidad 1 MATERIA Todo aquello que ocupa un lugar en el espacio, tiene una energía medible y está sujeto a cambios en el tiempo y a interacciones con aparatos de medida.
Curso Química General I Apuntes Unidad 1 MATERIA Todo aquello que ocupa un lugar en el espacio, tiene una energía medible y está sujeto a cambios en el tiempo y a interacciones con aparatos de medida.
PROPIEDADES DE LA MATERIA. Prof. Jackeline Ruttell torres Química Febrero 2017
 PROPIEDADES DE LA MATERIA Prof. Jackeline Ruttell torres Química Febrero 2017 DEFINICIONES IMPORTANTES Sustancia: materia con composición uniforme y constante Ej. Agua siempre posee dos átomos de hidrógeno
PROPIEDADES DE LA MATERIA Prof. Jackeline Ruttell torres Química Febrero 2017 DEFINICIONES IMPORTANTES Sustancia: materia con composición uniforme y constante Ej. Agua siempre posee dos átomos de hidrógeno
Materia es todo aquello que tiene masa y ocupa un lugar en el espacio (tiene volumen). La ciencia que estudia la materia es la Química.
 Alfonso García Materia es todo aquello que tiene masa y ocupa un lugar en el espacio (tiene volumen). La ciencia que estudia la materia es la Química. Un sistema material es una porción de materia. Ejemplos:
Alfonso García Materia es todo aquello que tiene masa y ocupa un lugar en el espacio (tiene volumen). La ciencia que estudia la materia es la Química. Un sistema material es una porción de materia. Ejemplos:
TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS
 TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS 1. LA MATERIA Y SU ASPECTO Los sistemas materiales, formados por una o varias sustancias, pueden clasificarse en: - Sistemas materiales heterogéneos: presentan
TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS 1. LA MATERIA Y SU ASPECTO Los sistemas materiales, formados por una o varias sustancias, pueden clasificarse en: - Sistemas materiales heterogéneos: presentan
Es una ciencia porque tiene un objeto de estudio (la materia), y un método (el método experimental).
 Objetivos: La Química es una ciencia que estudia la materia en sentido general, su estructura, sus propiedades y las reacciones que transforman sustancias en otras. Es una ciencia porque tiene un objeto
Objetivos: La Química es una ciencia que estudia la materia en sentido general, su estructura, sus propiedades y las reacciones que transforman sustancias en otras. Es una ciencia porque tiene un objeto
Departamento de Electrónica y Automática Facultad de Ingeniería UNSJ BIOINGENIERÍA DEPARTAMENTO DE ELECTRÓNICA Y AUTOMÁTICA
 Departamento de Electrónica y Automática Facultad de Ingeniería UNSJ BIOINGENIERÍA DEPARTAMENTO DE ELECTRÓNICA Y AUTOMÁTICA FACULTAD DE INGENIERÍA UNIVERSIDAD NACIONAL DE SAN JUAN Guía de Trabajo Practico
Departamento de Electrónica y Automática Facultad de Ingeniería UNSJ BIOINGENIERÍA DEPARTAMENTO DE ELECTRÓNICA Y AUTOMÁTICA FACULTAD DE INGENIERÍA UNIVERSIDAD NACIONAL DE SAN JUAN Guía de Trabajo Practico
Elemento. Un elemento químico, o solamente elemento, es una sustancia formada por átomos con el mismo número n. de protones
 Elemento Un elemento químico, o solamente elemento, es una sustancia formada por átomos con el mismo número n de protones en el núcleo. n Este número n se conoce como el número n atómico del elemento.
Elemento Un elemento químico, o solamente elemento, es una sustancia formada por átomos con el mismo número n de protones en el núcleo. n Este número n se conoce como el número n atómico del elemento.
CURSO INTRODUCTORIO DE QUÍMICA
 CURSO INTRODUCTORIO DE QUÍMICA UNIDAD II. S MATERIALES INTRODUCCIÓN Se llama sistema material a una porción limitada de materia, dentro del universo, que se separa real o imaginariamente, para su estudio.
CURSO INTRODUCTORIO DE QUÍMICA UNIDAD II. S MATERIALES INTRODUCCIÓN Se llama sistema material a una porción limitada de materia, dentro del universo, que se separa real o imaginariamente, para su estudio.
Escuela del Petróleo - Química
 Escuela del Petróleo - Química 2012 1 Unidad 2 1) Sistema Materiales 2) Materiales Homogéneos y Heterogéneos. a. Separación de las fases b. Sustancia Pura 3) extensivas e intensivas 4) Sistemas dispersos
Escuela del Petróleo - Química 2012 1 Unidad 2 1) Sistema Materiales 2) Materiales Homogéneos y Heterogéneos. a. Separación de las fases b. Sustancia Pura 3) extensivas e intensivas 4) Sistemas dispersos
SISTEMAS MATERIALES. Qué ejemplos podés dar de un mismo cuerpo formado por distintos materiales y de distintos cuerpos formados por un mismo material?
 SISTEMAS MATERIALES Lic. Lidia Iñigo Se denomina MATERIA a todo lo que forma los distintos objetos o cuerpos que nos rodean, ya sean inertes o seres vivos. La materia se caracteriza por ocupar un lugar
SISTEMAS MATERIALES Lic. Lidia Iñigo Se denomina MATERIA a todo lo que forma los distintos objetos o cuerpos que nos rodean, ya sean inertes o seres vivos. La materia se caracteriza por ocupar un lugar
1 TEMA 11: La materia CRA Sexma de La Sierra. CoNoTiC. *Esquema conceptual: 11. LA MATERIA
 1 TEMA 11: La materia CRA Sexma de La Sierra. CoNoTiC *Esquema conceptual: 11. LA MATERIA 2 TEMA 11: La materia CRA Sexma de La Sierra. CoNoTiC 1. La materia y sus propiedades A través de los sentidos
1 TEMA 11: La materia CRA Sexma de La Sierra. CoNoTiC *Esquema conceptual: 11. LA MATERIA 2 TEMA 11: La materia CRA Sexma de La Sierra. CoNoTiC 1. La materia y sus propiedades A través de los sentidos
Materia. Mezclas Son aquellas que están formados por 2 o más sustancias.
 Qué es la materia? Materia Sustancias Puras Son aquellas que tienen una composición y propiedades DEFINIDAS. Mezclas Son aquellas que están formados por 2 o más sustancias. Elementos No se pueden separar
Qué es la materia? Materia Sustancias Puras Son aquellas que tienen una composición y propiedades DEFINIDAS. Mezclas Son aquellas que están formados por 2 o más sustancias. Elementos No se pueden separar
RESPUESTAS DE LOS EJERCICIOS DE APLICACIÓN DEL LIBRO UN ACERCAMIENTO A LA QUÍMICA CAPÍTULO N 1: LOS SISTEMAS MATERIALES
 RESPUESTAS DE LOS EJERCICIOS DE APLICACIÓN DEL LIBRO UN ACERCAMIENTO A LA QUÍMICA ACLARACIÓN: Las respuestas que pudieren faltar de algunos ejercicios serán agregadas en futuras actualizaciones. CAPÍTULO
RESPUESTAS DE LOS EJERCICIOS DE APLICACIÓN DEL LIBRO UN ACERCAMIENTO A LA QUÍMICA ACLARACIÓN: Las respuestas que pudieren faltar de algunos ejercicios serán agregadas en futuras actualizaciones. CAPÍTULO
ESTADOS DE AGREGACIÒN DE LA MATERIA
 Materia Materia es todo aquello que constituye a los cuerpos, ocupa un espacio, tiene masa y energía. Se presenta en tres estados de agregación molecular: gaseosa, líquida y sólida. Está formada por átomos
Materia Materia es todo aquello que constituye a los cuerpos, ocupa un espacio, tiene masa y energía. Se presenta en tres estados de agregación molecular: gaseosa, líquida y sólida. Está formada por átomos
COLEGIO ROSARIO DE SANTODOMINGO BANCO DE PREGUNTAS QUIMICA GRADO 10
 COLEGIO ROSARIO DE SANTODOMINGO BANCO DE PREGUNTAS QUIMICA GRADO 10 NOTA: ALGUNAS DE LAS PREGUNTAS PRESENTES EN ESTE CUESTIONARIO SON PREGUNTAS LIBERADAS POR EL ICFES ENTRE LOS AÑOS DE 2009 A 2011. Como
COLEGIO ROSARIO DE SANTODOMINGO BANCO DE PREGUNTAS QUIMICA GRADO 10 NOTA: ALGUNAS DE LAS PREGUNTAS PRESENTES EN ESTE CUESTIONARIO SON PREGUNTAS LIBERADAS POR EL ICFES ENTRE LOS AÑOS DE 2009 A 2011. Como
Web-page:
 GUÍA - PARALELO CEPRE UNI ESTADOS DE AGREGACIÓN MOLECULAR SÓLIDOS Y LÍQUIDOS I. Colocar (A) si la propiedad corresponde a un sólido amorfo y (C) si la propiedad corresponde a un sólido cristalino: 1. Poseen
GUÍA - PARALELO CEPRE UNI ESTADOS DE AGREGACIÓN MOLECULAR SÓLIDOS Y LÍQUIDOS I. Colocar (A) si la propiedad corresponde a un sólido amorfo y (C) si la propiedad corresponde a un sólido cristalino: 1. Poseen
INSTITUCIÓN EDUCATIVA COLEGIO ARTÍSTICO RAFAEL CONTRERAS NAVARRO Esp. Jesús Alonso Paba León
 INSTITUCIÓN EDUCATIVA COLEGIO ARTÍSTICO RAFAEL CONTRERAS NAVARRO Esp. Jesús Alonso Paba León GUÍA No 1: MATERIA Y ENERGÍA GRADOS: DÉCIMO 1 Y 2 OBJETIVO: Reconocer la estructura y las diferentes propiedades
INSTITUCIÓN EDUCATIVA COLEGIO ARTÍSTICO RAFAEL CONTRERAS NAVARRO Esp. Jesús Alonso Paba León GUÍA No 1: MATERIA Y ENERGÍA GRADOS: DÉCIMO 1 Y 2 OBJETIVO: Reconocer la estructura y las diferentes propiedades
Departamento Ciencias. Física y Química MATERIA. se clasifica en. SUSTANCIAS PURAS pueden ser. por métodos. físicos originan. Compuestos.
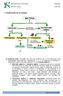 1. Clasificación de la materia MATERIA se clasifica en MEZCLAS pueden ser por métodos físicos originan SUSTANCIAS PURAS pueden ser Heterogéneas Homogéneas Compuestos como las Disoluciones formados por
1. Clasificación de la materia MATERIA se clasifica en MEZCLAS pueden ser por métodos físicos originan SUSTANCIAS PURAS pueden ser Heterogéneas Homogéneas Compuestos como las Disoluciones formados por
La materia se puede definir como todo aquello que tiene masa y ocupa un volumen.
 Tema 2: LA MATERIA Que es la materia? La materia se puede definir como todo aquello que tiene masa y ocupa un volumen. Clasificación de la materia (criterio: separación) Mezclas Sustancias puras Composición
Tema 2: LA MATERIA Que es la materia? La materia se puede definir como todo aquello que tiene masa y ocupa un volumen. Clasificación de la materia (criterio: separación) Mezclas Sustancias puras Composición
Unidad I Sub-Unidad 1.1. MATERIA Y ENERGÍA
 DEFINICIONES: Materia es todo lo que tiene masa y ocupa un lugar en el espacio; Masa es la cantidad de materia que tiene un cuerpo; Volumen es el espacio ocupado por la masa Estados de la materia en relación
DEFINICIONES: Materia es todo lo que tiene masa y ocupa un lugar en el espacio; Masa es la cantidad de materia que tiene un cuerpo; Volumen es el espacio ocupado por la masa Estados de la materia en relación
EVALUACIÓN SUMATIVA FINAL Primera Unidad: Agua, compuesto indispensable.
 EVALUACIÓN SUMATIVA FINAL Primera Unidad: Agua, compuesto indispensable. 1. ( ) Tipo de materia cuyos componentes conservan sus propiedades y se encuentran en proporción variable. a) un elemento b) una
EVALUACIÓN SUMATIVA FINAL Primera Unidad: Agua, compuesto indispensable. 1. ( ) Tipo de materia cuyos componentes conservan sus propiedades y se encuentran en proporción variable. a) un elemento b) una
Nivel Inicial - Serie 1
 Nivel Inicial - Aclaración para esta y para futuras series de ejercitación: Utiliza tu tabla periódica (o la provista por la OAQ en su sitio web oaq.fcen.uba.ar) para obtener las masas atómicas que pudieras
Nivel Inicial - Aclaración para esta y para futuras series de ejercitación: Utiliza tu tabla periódica (o la provista por la OAQ en su sitio web oaq.fcen.uba.ar) para obtener las masas atómicas que pudieras
INTRUCCIONES PARA LA RECUPERACIÓN
 INTRUCCIONES PARA LA RECUPERACIÓN Se entrega una relación de actividades. Dichas actividades deberán ser entregadas antes de la fecha límite de entrega, pudiéndose ser consultado el profesor cuantas veces
INTRUCCIONES PARA LA RECUPERACIÓN Se entrega una relación de actividades. Dichas actividades deberán ser entregadas antes de la fecha límite de entrega, pudiéndose ser consultado el profesor cuantas veces
CLASIFICACIONES DE LA MATERIA. Estados de la materia Sustancias puras Elementos Compuestos Mezclas Propiedades de la materia.
 CLASIFICACIONES DE LA MATERIA Estados de la materia Sustancias puras Elementos Compuestos Mezclas Propiedades de la materia. LA MATERIA Es todo aquello que ocupa un sitio en el espacio, se puede tocar,
CLASIFICACIONES DE LA MATERIA Estados de la materia Sustancias puras Elementos Compuestos Mezclas Propiedades de la materia. LA MATERIA Es todo aquello que ocupa un sitio en el espacio, se puede tocar,
TEMA 3: Composición de la Materia
 TEMA 3: Composición de la Materia 1. Mezclas homogéneas y heterogéneas Una mezcla es una composición de varias sustancias con distintas propiedades. Distinguimos dos tipos de mezclas: Mezclas homogéneas:
TEMA 3: Composición de la Materia 1. Mezclas homogéneas y heterogéneas Una mezcla es una composición de varias sustancias con distintas propiedades. Distinguimos dos tipos de mezclas: Mezclas homogéneas:
UNIVERSIDAD NACIONAL AGRARIA LA MOLINA CENTRO DE ESTUDIOS PREUNIVERSITARIOS PRIMER SEMINARIO DE QUÍMICA
 UNIVERSIDAD NACIONAL AGRARIA LA MOLINA CENTRO DE ESTUDIOS PREUNIVERSITARIOS PRIMER SEMINARIO DE QUÍMICA UNIDAD 1: LA MATERIA 1. Indicar si los enunciados son verdaderos( V) o falsos( F ) : ( ) A la materia
UNIVERSIDAD NACIONAL AGRARIA LA MOLINA CENTRO DE ESTUDIOS PREUNIVERSITARIOS PRIMER SEMINARIO DE QUÍMICA UNIDAD 1: LA MATERIA 1. Indicar si los enunciados son verdaderos( V) o falsos( F ) : ( ) A la materia
INSTITUCIÓN EDUCATIVA GIO MANUEL FERNANDEZ DE NOVOA do con calidad, aseguramos el futu. Guía de Estudio. Grado: 5º.
 INSTITUCIÓN EDUCATIVA COLEG GIO MANUEL FERNANDEZ DE NOVOA Formand do con calidad, aseguramos el futu uro Guía de Estudio Nombre: Fecha: Tema: El atomo, Grado: 5º. Asignatura: Ciencias Naturales. El átomo,
INSTITUCIÓN EDUCATIVA COLEG GIO MANUEL FERNANDEZ DE NOVOA Formand do con calidad, aseguramos el futu uro Guía de Estudio Nombre: Fecha: Tema: El atomo, Grado: 5º. Asignatura: Ciencias Naturales. El átomo,
BANCO DE PREGUNTAS DE QUÍMICA PRIMER PARCIAL - GESTION I/2010
 UNIVERSIDAD MAYOR DE SAN SIMON FACULTAD DE CIENCIAS Y TECNOLOGIA DEPARTAMENTO DE QUIMICA CURSO PREFACULTATIVO BANCO DE PREGUNTAS DE QUÍMICA PRIMER PARCIAL - GESTION I/2010 1.- Cuántas de las siguientes
UNIVERSIDAD MAYOR DE SAN SIMON FACULTAD DE CIENCIAS Y TECNOLOGIA DEPARTAMENTO DE QUIMICA CURSO PREFACULTATIVO BANCO DE PREGUNTAS DE QUÍMICA PRIMER PARCIAL - GESTION I/2010 1.- Cuántas de las siguientes
La materia y los cambios químicos 4. Sustancias puras y mezclas
 4. Sustancias puras y mezclas Materia Sustancias puras Formadas por un único tipo de componente Mezclas Formada por dos o más sustancias puras Elementos Formados por la misma clase de átomos Compuestos
4. Sustancias puras y mezclas Materia Sustancias puras Formadas por un único tipo de componente Mezclas Formada por dos o más sustancias puras Elementos Formados por la misma clase de átomos Compuestos
Una mezcla es un compuesto formado por varias sustancias con distintas propiedades
 COMPOSICIÓN DE LA MATERIA Mezclas homogéneas y heterogéneas Una mezcla es un compuesto formado por varias sustancias con distintas propiedades Algunos sistemas materiales como la leche a simple vista parecen
COMPOSICIÓN DE LA MATERIA Mezclas homogéneas y heterogéneas Una mezcla es un compuesto formado por varias sustancias con distintas propiedades Algunos sistemas materiales como la leche a simple vista parecen
LA MATERIA. - Masa - Volumen -Energía - Carga eléctrica. Propiedades generales
 TEMA 2 La Materia LA MATERIA Propiedades generales - Masa - Volumen -Energía - Carga eléctrica Propiedades características - Densidad - Punto de fusión - Punto de ebullición -Conductividad eléctrica -
TEMA 2 La Materia LA MATERIA Propiedades generales - Masa - Volumen -Energía - Carga eléctrica Propiedades características - Densidad - Punto de fusión - Punto de ebullición -Conductividad eléctrica -
1) Indicar si las siguientes propiedades son extensivas o intensivas:
 Sistemas Materiales Guía de Ejercitación 1) Indicar si las siguientes propiedades son extensivas o intensivas: a) Volumen b) Densidad c) Olor d) Pto. de fusión e) Presión f) Sabor g) Pto. de ebullición
Sistemas Materiales Guía de Ejercitación 1) Indicar si las siguientes propiedades son extensivas o intensivas: a) Volumen b) Densidad c) Olor d) Pto. de fusión e) Presión f) Sabor g) Pto. de ebullición
Qué es la materia? Todo lo que nos rodea, incluidos nosotros mismos, está formado por un componente común: la Materia.
 Qué es la materia? Todo lo que nos rodea, incluidos nosotros mismos, está formado por un componente común: la Materia. Los distintos medios, aire, agua y muro, son materia pero poseen distinta composición,
Qué es la materia? Todo lo que nos rodea, incluidos nosotros mismos, está formado por un componente común: la Materia. Los distintos medios, aire, agua y muro, son materia pero poseen distinta composición,
FÍSICA Y QUÍMICA 2º ESO Tema 2: LA MATERIA Mezclas y Soluciones. Sustancias puras y mezclas
 Sustancias puras y mezclas La materia que nos rodea es, en la mayoría de los casos, una mezcla de sustancias. Los científicos han intentado clasificar las sustancias desde el principio de los tiempos.
Sustancias puras y mezclas La materia que nos rodea es, en la mayoría de los casos, una mezcla de sustancias. Los científicos han intentado clasificar las sustancias desde el principio de los tiempos.
2. LOS ESTADOS DE LA MATERIA. Nuria Montiel Guardiola - 1 -
 1. LA MATERIA La materia es todo aquello que existe, tiene masa y ocupa lugar en un espacio. Las cosas materiales se pueden medir y contar y las cosas inmateriales no. 2. LOS ESTADOS DE LA MATERIA Nuria
1. LA MATERIA La materia es todo aquello que existe, tiene masa y ocupa lugar en un espacio. Las cosas materiales se pueden medir y contar y las cosas inmateriales no. 2. LOS ESTADOS DE LA MATERIA Nuria
LA MATERIA Y SU DIVERSIDAD
 LA MATERIA Y SU DIVERSIDAD La materia es todo aquello que tiene masa y ocupa un espacio, es decir, tiene volumen. Propiedades generales La masa y el volumen, son comunes a toda la materia y no nos sirven
LA MATERIA Y SU DIVERSIDAD La materia es todo aquello que tiene masa y ocupa un espacio, es decir, tiene volumen. Propiedades generales La masa y el volumen, son comunes a toda la materia y no nos sirven
Nombre del alumno: No. De lista Fecha:
 GUIA DE EXAMEN EXTRAORDINARIO CIENCIAS III (QUÍMICA) TERCER GRADO Nombre del alumno: Grupo Titular: Ing. Sonia Castañeda Rocha No. De lista Fecha: I.- SUBRAYA LA RESPUESTA CORRECTA 1.- Qué método de separación
GUIA DE EXAMEN EXTRAORDINARIO CIENCIAS III (QUÍMICA) TERCER GRADO Nombre del alumno: Grupo Titular: Ing. Sonia Castañeda Rocha No. De lista Fecha: I.- SUBRAYA LA RESPUESTA CORRECTA 1.- Qué método de separación
CURSO DE NIVELACIÓN EN QUÍMICA INTRODUCCIÓN A LA QUÍMICA
 U.N.P.S.J.B. FACULTAD DE CIENCIAS NATURALES SEDE TRELEW CURSO DE NIVELACIÓN EN QUÍMICA INTRODUCCIÓN A LA QUÍMICA AÑO 2016 Lic. Maite L. Domínguez Ing. Sebastián Polacco Ing Ruth Salomón LA MATERIA MATERIA:
U.N.P.S.J.B. FACULTAD DE CIENCIAS NATURALES SEDE TRELEW CURSO DE NIVELACIÓN EN QUÍMICA INTRODUCCIÓN A LA QUÍMICA AÑO 2016 Lic. Maite L. Domínguez Ing. Sebastián Polacco Ing Ruth Salomón LA MATERIA MATERIA:
ELEMENTOS DE TERMODINAMICA
 ESCUELA DE QUÍMICA DEPARTAMENTO DE QUÍMICA GENERAL QUÍMICA GENERAL II RESOLUCIÓN HOJA DE TRABAJO UNIDAD I ELEMENTOS DE TERMODINAMICA 3. Resuelva los siguientes problemas; copie el enunciado, deje constancia
ESCUELA DE QUÍMICA DEPARTAMENTO DE QUÍMICA GENERAL QUÍMICA GENERAL II RESOLUCIÓN HOJA DE TRABAJO UNIDAD I ELEMENTOS DE TERMODINAMICA 3. Resuelva los siguientes problemas; copie el enunciado, deje constancia
U.D. 2 LA MATERIA. Para describir un cuerpo o un sistema material, necesitamos conocer sus propiedades. Así, distinguimos entre:
 U.D. 2 LA MATERIA 1. Propiedades de la materia La materia, o sistema material, es todo lo que posee una propiedad fundamental llamada masa, y que ocupa un espacio, es decir, un volumen. Para describir
U.D. 2 LA MATERIA 1. Propiedades de la materia La materia, o sistema material, es todo lo que posee una propiedad fundamental llamada masa, y que ocupa un espacio, es decir, un volumen. Para describir
PROBLEMAS MEZCLAS Y DISOLUCIONES
 PROBLEMAS MEZCLAS Y DISOLUCIONES 1. Clasifica como homogéneos o heterogéneos los siguientes sistemas materiales: un trozo de cobre, agua salada, hierro oxidado, una ensalada. 2. Al mezclar dos sistemas
PROBLEMAS MEZCLAS Y DISOLUCIONES 1. Clasifica como homogéneos o heterogéneos los siguientes sistemas materiales: un trozo de cobre, agua salada, hierro oxidado, una ensalada. 2. Al mezclar dos sistemas
SISTEMAS MATERIALES. Departamento de Física y Química 2º ESO
 SISTEMAS MATERIALES Departamento de Física y Química 2º ESO 0. Mapa conceptual MATERIA Sustancias puras Mezclas Heterogéneas Homogéneas Sistemas coloidales Técnicas de separación Disoluciones Soluto Disolvente
SISTEMAS MATERIALES Departamento de Física y Química 2º ESO 0. Mapa conceptual MATERIA Sustancias puras Mezclas Heterogéneas Homogéneas Sistemas coloidales Técnicas de separación Disoluciones Soluto Disolvente
Unidad 2. La materia
 Física y Química Unidad 2: La materia Unidad 2. La materia Índice de contenido 1. Estados de agregación de la materia...3 2. Cambios de estado...4 3. Clasificación de la materia...6 3.1.- Métodos de separación
Física y Química Unidad 2: La materia Unidad 2. La materia Índice de contenido 1. Estados de agregación de la materia...3 2. Cambios de estado...4 3. Clasificación de la materia...6 3.1.- Métodos de separación
ORGANIZACIÓN BLOQUE 5
 ORGANIZACIÓN BLOQUE 5 FECHA ACTIVIDAD TEMA 4-8 de abril 017 3-4/mayo/017 8 al 19 mayo /017 Revisión de apuntes y practicas de laboratorio Revision de apuntes y Pruebas tipo Enlace Situación de problema
ORGANIZACIÓN BLOQUE 5 FECHA ACTIVIDAD TEMA 4-8 de abril 017 3-4/mayo/017 8 al 19 mayo /017 Revisión de apuntes y practicas de laboratorio Revision de apuntes y Pruebas tipo Enlace Situación de problema
ACTIVIDAD DE INTERPRETASCION EN LA MEDICION
 1 ACTIVIDAD DE INTERPRETASCION EN LA MEDICION 1. El sulfuro de hierro es una sustancia sólida a temperatura ambiente y está compuesta de hierro y azufre. Estas sustancias tienen las siguientes propiedades:
1 ACTIVIDAD DE INTERPRETASCION EN LA MEDICION 1. El sulfuro de hierro es una sustancia sólida a temperatura ambiente y está compuesta de hierro y azufre. Estas sustancias tienen las siguientes propiedades:
1. MATERIA Y SU ASPECTO
 1. MATERIA Y SU ASPECTO El aspecto de un sistema material puede variar según el método de observación. Algunos sistemas materiales como la leche, la sangre o la mantequilla a simple vista parecen uniformes,
1. MATERIA Y SU ASPECTO El aspecto de un sistema material puede variar según el método de observación. Algunos sistemas materiales como la leche, la sangre o la mantequilla a simple vista parecen uniformes,
Termoquímica. Química General II era Unidad
 Termoquímica Química General II 2011 1era Unidad Termodinámica Es el estudio científico de la conversión del calor a otras formas de energía Energía Es la capacidad de efectuar un trabajo. Algunas formas
Termoquímica Química General II 2011 1era Unidad Termodinámica Es el estudio científico de la conversión del calor a otras formas de energía Energía Es la capacidad de efectuar un trabajo. Algunas formas
MODULO 2. Primera mirada con ojos de químico. El Mundo que nos rodea. Química
 MODULO 2 El Mundo que nos rodea Primera mirada con ojos de químico Química Materia (propiedades, transformaciones, combinaciones) Ramas Se divide estudia Ciencia Experimental Química: General Inorgánica
MODULO 2 El Mundo que nos rodea Primera mirada con ojos de químico Química Materia (propiedades, transformaciones, combinaciones) Ramas Se divide estudia Ciencia Experimental Química: General Inorgánica
INTRODUCCIÓN DISOLUCIONES
 QUIMICA COMUN INTRODUCCIÓN DISOLUCIONES EBULLICIÓN V/S EVAPORACIÓN Ambos conceptos tienen relación con la presión de vapor. La presión de vapor es la fuerza que tienen las moléculas de un líquido para
QUIMICA COMUN INTRODUCCIÓN DISOLUCIONES EBULLICIÓN V/S EVAPORACIÓN Ambos conceptos tienen relación con la presión de vapor. La presión de vapor es la fuerza que tienen las moléculas de un líquido para
UNIDAD 6 - LA MATERIA
 UNIDAD 6 - LA MATERIA La materia es todo lo que pesa y ocupa un lugar en el espacio. A través de los sentidos (vista, oído, tacto, gusto y olfato) recibimos y percibimos información sobre todo lo que nos
UNIDAD 6 - LA MATERIA La materia es todo lo que pesa y ocupa un lugar en el espacio. A través de los sentidos (vista, oído, tacto, gusto y olfato) recibimos y percibimos información sobre todo lo que nos
Sólido Líquido Gaseoso
 1.1 Conceptos sobre la materia y la energía Todo lo que nos rodea, incluidos nosotros mismos, está formado por un componente común: la materia. Normalmente, para referirnos a los objetos usamos términos
1.1 Conceptos sobre la materia y la energía Todo lo que nos rodea, incluidos nosotros mismos, está formado por un componente común: la materia. Normalmente, para referirnos a los objetos usamos términos
Estados de la materia en relación a cambios de la temperatura del ambiente
 Todo lo que nos rodea, incluidos nosotros mismos, está formado por un componente común: la materia. Normalmente, para referirnos a los objetos usamos términos como materia, masa, peso, volumen. Para clarificar
Todo lo que nos rodea, incluidos nosotros mismos, está formado por un componente común: la materia. Normalmente, para referirnos a los objetos usamos términos como materia, masa, peso, volumen. Para clarificar
Estado Características Cambio físico
 Materia Todas las sustancias pueden existir, al menos en principio, en los tres estados: sólido, líquido y gaseoso, tal como lo muestra la figura, los gases difieren de los sólidos y de los líquidos en
Materia Todas las sustancias pueden existir, al menos en principio, en los tres estados: sólido, líquido y gaseoso, tal como lo muestra la figura, los gases difieren de los sólidos y de los líquidos en
Materia: FÍSICA Y QUÍMICA 3º E.S.O Curso
 ACTIVIDADES FÍSICA Y QUÍMICA 3º ESO PROGRAMA DE REFUERZO. PRIMERA PARTE 1.-Calcular el tanto por ciento en peso y en volumen de una disolución que se prepara al disolver 40 ml de ácido nítrico cuya densidad
ACTIVIDADES FÍSICA Y QUÍMICA 3º ESO PROGRAMA DE REFUERZO. PRIMERA PARTE 1.-Calcular el tanto por ciento en peso y en volumen de una disolución que se prepara al disolver 40 ml de ácido nítrico cuya densidad
INSTITUCIÓN EDUCATIVA FE Y ALEGRÍA NUEVA GENERACIÓN
 INSTITUCIÓN EDUCATIVA FE Y ALEGRÍA NUEVA GENERACIÓN Formando para el amor y la vida - AREA CIENCIAS NATURALES: QUIMICA - FISICA Tema: La Materia, Energía y Sonido Tiempo: 2 periodos académicos Grado: Quinto
INSTITUCIÓN EDUCATIVA FE Y ALEGRÍA NUEVA GENERACIÓN Formando para el amor y la vida - AREA CIENCIAS NATURALES: QUIMICA - FISICA Tema: La Materia, Energía y Sonido Tiempo: 2 periodos académicos Grado: Quinto
EVALUACIÓN SUMATIVA. Observa los siguientes esquemas y responde lo que abajo se pregunta:
 EVALUACIÓN SUMATIVA Observa los siguientes esquemas y responde lo que abajo se pregunta: A B En cuál de los dos esquemas se está representando a nivel molecular un cambio físico y en cuál un cambio químico?
EVALUACIÓN SUMATIVA Observa los siguientes esquemas y responde lo que abajo se pregunta: A B En cuál de los dos esquemas se está representando a nivel molecular un cambio físico y en cuál un cambio químico?
ACTIVIDADES DE PENDIENTES DE FÍSICA Y QUÍMICA DE 3º ESO
 ACTIVIDADES DE PENDIENTES DE FÍSICA Y QUÍMICA DE 3º ESO 1. a) Qué es la Ciencia? Qué es la Física? Qué es la Química? b) Señala qué procesos se estudian la Física y cuáles estudia la Química: a. Descenso
ACTIVIDADES DE PENDIENTES DE FÍSICA Y QUÍMICA DE 3º ESO 1. a) Qué es la Ciencia? Qué es la Física? Qué es la Química? b) Señala qué procesos se estudian la Física y cuáles estudia la Química: a. Descenso
Métodos de separación de sistemas materiales sencillos
 Métodos de separación de sistemas materiales sencillos SISTEMAS MATERIALES Mezclas Separación física Sustancias Puras no Son uniformes? si si Pueden descomponerse por reacciones químicas? no Mezclas heterogéneas
Métodos de separación de sistemas materiales sencillos SISTEMAS MATERIALES Mezclas Separación física Sustancias Puras no Son uniformes? si si Pueden descomponerse por reacciones químicas? no Mezclas heterogéneas
I Unidad Ciencia que estudia la materia Objetivos Contenidos Procedimientos. Que es la química
 CONTENIDOS ANUALES OCTAVO I Unidad Ciencia que estudia la materia Objetivos Contenidos Procedimientos 1. Reconocer el campo de estudio de la Química y sus aplicaciones en el mejoramiento de la calidad
CONTENIDOS ANUALES OCTAVO I Unidad Ciencia que estudia la materia Objetivos Contenidos Procedimientos 1. Reconocer el campo de estudio de la Química y sus aplicaciones en el mejoramiento de la calidad
DIVERSIDAD DE LA MATERIA TEMA 3
 DIVERSIDAD DE LA MATERIA TEMA 3 Cómo se presenta la materia Sistema homogéneos Sistemas materiales que tienen el mismo aspecto en cualquiera de sus partes. Ejemplo: agua, leche, gelatina Sistemas heterogéneos
DIVERSIDAD DE LA MATERIA TEMA 3 Cómo se presenta la materia Sistema homogéneos Sistemas materiales que tienen el mismo aspecto en cualquiera de sus partes. Ejemplo: agua, leche, gelatina Sistemas heterogéneos
Nombre y apellidos:...
 1 Señala las opciones correctas: a) El conocimiento científico surge de la necesidad de dar respuesta a un problema basado en hechos a los que se quiere dar explicación. b) El conocimiento científico es
1 Señala las opciones correctas: a) El conocimiento científico surge de la necesidad de dar respuesta a un problema basado en hechos a los que se quiere dar explicación. b) El conocimiento científico es
MATERIA: ES TODO LO QUE TIENE MASA Y VOLUMEN.
 MATERIA: ES TODO LO QUE TIENE MASA Y VOLUMEN. CLASIFICACIÓN DE LA MATERIA: SEGÚN: A. ESTADO DE AGREGACIÓN. B. COMPOSICIÓN. A. ESTADO DE AGREGACIÓN. SE REFIERE A LA FORMA DE INTERACCIÓN ENTRE LAS MOLÉCULAS
MATERIA: ES TODO LO QUE TIENE MASA Y VOLUMEN. CLASIFICACIÓN DE LA MATERIA: SEGÚN: A. ESTADO DE AGREGACIÓN. B. COMPOSICIÓN. A. ESTADO DE AGREGACIÓN. SE REFIERE A LA FORMA DE INTERACCIÓN ENTRE LAS MOLÉCULAS
La materia, las fuerzas y la energía
 La materia, las fuerzas y la energía Nombre:... Curso: 5º PRIMARIA 1. Definición, unidad y aparato que se usa para medirlo. Masa: Volumen: Une con flechas los siguientes conceptos con su definición. Materia
La materia, las fuerzas y la energía Nombre:... Curso: 5º PRIMARIA 1. Definición, unidad y aparato que se usa para medirlo. Masa: Volumen: Une con flechas los siguientes conceptos con su definición. Materia
Selección Múltiple: Encierre en un círculo la alternativa que consideres correcta
 REFUERZO SIMCE 2013 N 1 Este refuerzo entra en las pruebas parciales y globales. Se aplicara el reglamento de evaluación en caso de no entrega en la fecha oportuna. Selección Múltiple: Encierre en un círculo
REFUERZO SIMCE 2013 N 1 Este refuerzo entra en las pruebas parciales y globales. Se aplicara el reglamento de evaluación en caso de no entrega en la fecha oportuna. Selección Múltiple: Encierre en un círculo
CLASE Nº 1 ESTRUCTURA DE LA MATERIA
 UNIVERSIDAD NACIONAL EXPERIMENTAL POLITECNICA ANTONIO JOSÉ DE SUCRE VICERRECTORADO BARQUISIMETO DEPARTAMENTO DE INGENIERÍA QUÍMICA QUÍMICA GENERAL CLASE Nº 1 ESTRUCTURA DE LA MATERIA Noviembre, 2010 1
UNIVERSIDAD NACIONAL EXPERIMENTAL POLITECNICA ANTONIO JOSÉ DE SUCRE VICERRECTORADO BARQUISIMETO DEPARTAMENTO DE INGENIERÍA QUÍMICA QUÍMICA GENERAL CLASE Nº 1 ESTRUCTURA DE LA MATERIA Noviembre, 2010 1
CAMBIOS DE LA MATERIA
 CAMBIOS DE LA MATERIA Propiedades generales: Son aquellas cuyo valor no sirve para identificar una sustancia. Ejemplos: la masa, el volumen y la temperatura a la que se encuentra un cuerpo. Propiedades
CAMBIOS DE LA MATERIA Propiedades generales: Son aquellas cuyo valor no sirve para identificar una sustancia. Ejemplos: la masa, el volumen y la temperatura a la que se encuentra un cuerpo. Propiedades
1.5 Métodos de separación de mezclas Decantación, filtración, extracción, cristalización, destilación, cromatografía.
 1.5 Métodos de separación de mezclas Decantación, filtración, extracción, cristalización, destilación, cromatografía. 1 Para tomar apuntes MÉTODO DE SEPARACIÓN PROPIEDAD(ES) EN LAS QUE SE BASA MEZCLAS
1.5 Métodos de separación de mezclas Decantación, filtración, extracción, cristalización, destilación, cromatografía. 1 Para tomar apuntes MÉTODO DE SEPARACIÓN PROPIEDAD(ES) EN LAS QUE SE BASA MEZCLAS
Todo lo que vemos es materia
 Todo lo que vemos es materia CLASIFICACIÓN DE LA MATERIA La materia se presenta en la naturaleza en forma de sustancias puras y mezclas, de modo que podemos establecer la siguiente clasificación: CLASIFICACIÓN
Todo lo que vemos es materia CLASIFICACIÓN DE LA MATERIA La materia se presenta en la naturaleza en forma de sustancias puras y mezclas, de modo que podemos establecer la siguiente clasificación: CLASIFICACIÓN
IES ALONSO QUESADA Física y Química 3º ESO Trabajo Científico. Estados de la materia. Clasificación de la materia.
 IES ALONSO QUESADA Física y Química 3º ESO Trabajo Científico. Estados de la materia. Clasificación de la materia. 1) Contesta las siguientes preguntas: a - Cuáles son los pasos del método científico?.
IES ALONSO QUESADA Física y Química 3º ESO Trabajo Científico. Estados de la materia. Clasificación de la materia. 1) Contesta las siguientes preguntas: a - Cuáles son los pasos del método científico?.
Soluciones y unidades de concentración
 MATERIA Soluciones y unidades de concentración MEZCLAS SISTEMAS HETEROGÉNEOS Leche Arena Sal y azúcar SISTEMAS HOMOGÉNEOS Sal en agua Aire Acero COMPUESTOS Agua Etanol Benceno SUSTANCIAS PURAS ELEMENTOS
MATERIA Soluciones y unidades de concentración MEZCLAS SISTEMAS HETEROGÉNEOS Leche Arena Sal y azúcar SISTEMAS HOMOGÉNEOS Sal en agua Aire Acero COMPUESTOS Agua Etanol Benceno SUSTANCIAS PURAS ELEMENTOS
Soluciones y unidades de concentración
 Soluciones y unidades de concentración Dra. Dra. Patricia Patricia Satti, Satti, UNRN UNRN MATERIA MEZCLAS SUSTANCIAS PURAS SISTEMAS HETEROGÉNEOS Leche Arena Sal y azúcar SISTEMAS HOMOGÉNEOS Sal en agua
Soluciones y unidades de concentración Dra. Dra. Patricia Patricia Satti, Satti, UNRN UNRN MATERIA MEZCLAS SUSTANCIAS PURAS SISTEMAS HETEROGÉNEOS Leche Arena Sal y azúcar SISTEMAS HOMOGÉNEOS Sal en agua
1 UNIVERSIDAD DON BOSCO DEPARTAMENTO DE CIENCIAS BÁSICAS QUIMICA GENERAL CICLO I
 1 UNIVERSIDAD DON BOSCO DEPARTAMENTO DE CIENCIAS BÁSICAS QUIMICA GENERAL CICLO I - 2009 DISCUSIÓN DE PROBLEMAS Nº 1 UNIDAD No. 1: GENERALIDADES SOBRE LA MATERIA OBJETIVOS: El estudiante al resolver esta
1 UNIVERSIDAD DON BOSCO DEPARTAMENTO DE CIENCIAS BÁSICAS QUIMICA GENERAL CICLO I - 2009 DISCUSIÓN DE PROBLEMAS Nº 1 UNIDAD No. 1: GENERALIDADES SOBRE LA MATERIA OBJETIVOS: El estudiante al resolver esta
Materia: FÍSICA Y QUÍMICA Curso
 ACTIVIDADES DE REFUERZO FÍSICA Y QUÍMICA 3º ESO. JUNIO 2015. 1.- Realizar las configuraciones electrónicas de todos los elementos de los tres primeros periodos de la tabla periódica. 2.- Razonar cuales
ACTIVIDADES DE REFUERZO FÍSICA Y QUÍMICA 3º ESO. JUNIO 2015. 1.- Realizar las configuraciones electrónicas de todos los elementos de los tres primeros periodos de la tabla periódica. 2.- Razonar cuales
PROPUESTA DE PRUEBA FINAL (sumativa)
 PROPUESTA DE PRUEBA FINAL (sumativa) 1. ( ) Una mezcla está formada por dos o más sustancias diferentes que a) conservan sus propiedades. b) pierden sus propiedades. c) adquieren propiedades nuevas. d)
PROPUESTA DE PRUEBA FINAL (sumativa) 1. ( ) Una mezcla está formada por dos o más sustancias diferentes que a) conservan sus propiedades. b) pierden sus propiedades. c) adquieren propiedades nuevas. d)
EJERCICIOS TEMA 2. LA MATERIA Y SUS PROPIEDADES.
 EJERCICIOS TEMA 2. LA MATERIA Y SUS PROPIEDADES. 1. La materia puede presentarse en tres estados de agregación. Cuáles son? 2. Cómo son la forma y el volumen de un sólido? Y de un líquido? Y de un gas?
EJERCICIOS TEMA 2. LA MATERIA Y SUS PROPIEDADES. 1. La materia puede presentarse en tres estados de agregación. Cuáles son? 2. Cómo son la forma y el volumen de un sólido? Y de un líquido? Y de un gas?
LA MATERIA: ESTADOS DE AGREGACIÓN
 LA MATERIA: ESTADOS DE AGREGACIÓN 1. PROPIEDADES DE LA MATERIA Materia: es todo aquello que existe, tiene masa y ocupa un volumen, los distintos tipos de materia se llaman sustancias. El sistema material
LA MATERIA: ESTADOS DE AGREGACIÓN 1. PROPIEDADES DE LA MATERIA Materia: es todo aquello que existe, tiene masa y ocupa un volumen, los distintos tipos de materia se llaman sustancias. El sistema material
DEPARTAMENTO DE FÍSICA Y QUÍMICA RECUPERACIÓN DE MATERIA PENDIENTE DE FÍSICA Y QUÍMICA. ZnO SO2. KH SnH4 BeO. HgH2 FeH3. PbO AgH HCl.
 FORMULACIÓN 1. Escribe o formula. Óxido de disodio Óxido de cloro (V) Dióxido de nitrógeno Hidruro de magnesio Hidruro de hierro (III) Trióxido de dialuminio Hidruro de plata Cloruro de cobre (II) Óxido
FORMULACIÓN 1. Escribe o formula. Óxido de disodio Óxido de cloro (V) Dióxido de nitrógeno Hidruro de magnesio Hidruro de hierro (III) Trióxido de dialuminio Hidruro de plata Cloruro de cobre (II) Óxido
SUSTANCIA QUÍMICA mercurio oxígeno
 ELEMENTO O SUSTANCIA ELEMENTAL: Sustancia formada por un mismo tipo de átomos, por ejemplo: Hg, H 2, Cu, O 2 SUSTANCIA QUÍMICA mercurio oxígeno COMPUESTO O SUSTANCIA COMPUESTA: Sustancia formada por dos
ELEMENTO O SUSTANCIA ELEMENTAL: Sustancia formada por un mismo tipo de átomos, por ejemplo: Hg, H 2, Cu, O 2 SUSTANCIA QUÍMICA mercurio oxígeno COMPUESTO O SUSTANCIA COMPUESTA: Sustancia formada por dos
IES SIERRA DEL AGUA ACTIVIDADES DE FÍSICA Y QUÍMICA DE ALUMNOS PENDIENTES DE 3º DE ESO
 IES SIERRA DEL AGUA ACTIVIDADES DE FÍSICA Y QUÍMICA DE ALUMNOS PENDIENTES DE 3º DE ESO Tema 1: Medida y método científico. 1. Transforme las siguientes magnitudes al S.I de unidades: a) 228 Gm b) 436 ns
IES SIERRA DEL AGUA ACTIVIDADES DE FÍSICA Y QUÍMICA DE ALUMNOS PENDIENTES DE 3º DE ESO Tema 1: Medida y método científico. 1. Transforme las siguientes magnitudes al S.I de unidades: a) 228 Gm b) 436 ns
UNIDAD 1 La materia y sus cambios
 UNIDAD 1 La materia y sus cambios Tema 1.3 Propiedades características de las sustancias: físicas, organolépticas, químicas; intensivas y extensivas. NMLV 1 Propiedades de las sustancias Organolépticas
UNIDAD 1 La materia y sus cambios Tema 1.3 Propiedades características de las sustancias: físicas, organolépticas, químicas; intensivas y extensivas. NMLV 1 Propiedades de las sustancias Organolépticas
Tiempo (minutos) Temperatura (ºC)
 EXAMEN FINAL 3º ESO. FÍSICA Y QUÍMICA. 1.- Al calentar un cierto sólido se ha obtenido la siguiente tabla de datos: Tiempo (minutos) 0 2 4 6 10 12 16 18 20 Temperatura (ºC) -5 0 5 10 20 20 20 25 30 Representa
EXAMEN FINAL 3º ESO. FÍSICA Y QUÍMICA. 1.- Al calentar un cierto sólido se ha obtenido la siguiente tabla de datos: Tiempo (minutos) 0 2 4 6 10 12 16 18 20 Temperatura (ºC) -5 0 5 10 20 20 20 25 30 Representa
LA MATERIA Y SUS PROPIEDADES
 LA MATERIA Y SUS PROPIEDADES Todas las cosas que nos rodean, tu ropa, el aire que respiras, el agua que bebes.. están hechas con materia. Propiedades de la materia Toda la materia tiene masa y volumen.
LA MATERIA Y SUS PROPIEDADES Todas las cosas que nos rodean, tu ropa, el aire que respiras, el agua que bebes.. están hechas con materia. Propiedades de la materia Toda la materia tiene masa y volumen.
La materia Materia es todo lo que tiene masa y ocupa un lugar en el espacio. La materia está formada por átomos y moléculas. Todo lo que nos rodea e i
 La materia Materia es todo lo que tiene masa y ocupa un lugar en el espacio. La materia está formada por átomos y moléculas. Todo lo que nos rodea e incluso nosotros mismos estamos hechos por materia.
La materia Materia es todo lo que tiene masa y ocupa un lugar en el espacio. La materia está formada por átomos y moléculas. Todo lo que nos rodea e incluso nosotros mismos estamos hechos por materia.
Agua y Soluciones SEMANA 07. Licda. Lilian Judith Guzmán M.
 Agua y Soluciones SEMANA 07 Licda. Lilian Judith Guzmán M. AGUA El agua es el compuesto químico más abundante en los seres vivos y en nuestro planeta, lo cual lo hace ser uno de los compuestos más extraordinarios.
Agua y Soluciones SEMANA 07 Licda. Lilian Judith Guzmán M. AGUA El agua es el compuesto químico más abundante en los seres vivos y en nuestro planeta, lo cual lo hace ser uno de los compuestos más extraordinarios.
ACTIVIDADES PARA LOS ALUMNOS CON LA ASIGNATURA DE FÍSICA Y QUÍMICA DE 3º PENDIENTE
 ACTIVIDADES PARA LOS ALUMNOS CON LA ASIGNATURA DE FÍSICA Y QUÍMICA DE 3º PENDIENTE Los alumnos que hallan suspendido la asignatura de Física y Química de 3º deberán entregar, el día del examen de la asignatura,
ACTIVIDADES PARA LOS ALUMNOS CON LA ASIGNATURA DE FÍSICA Y QUÍMICA DE 3º PENDIENTE Los alumnos que hallan suspendido la asignatura de Física y Química de 3º deberán entregar, el día del examen de la asignatura,
FÍSICA Y QUÍMICA TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS
 Física y Química 3º Curso Educación Secundaria Obligatoria Curso académico 2015/2016 1 FÍSICA Y QUÍMICA TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS Física y Química 3º Curso Educación Secundaria Obligatoria
Física y Química 3º Curso Educación Secundaria Obligatoria Curso académico 2015/2016 1 FÍSICA Y QUÍMICA TEMA 3: MEZCLAS, DISOLUCIONES Y SUSTANCIAS PURAS Física y Química 3º Curso Educación Secundaria Obligatoria
La materia. Capitulo 2
 La materia Capitulo 2 Que es la materia Aquello que ocupe espacio y posea masa. Puede que se vea o no. Se presenta en tres estados básicos: Solido Liquido Gas Solidos Su volumen y forma son definidos No
La materia Capitulo 2 Que es la materia Aquello que ocupe espacio y posea masa. Puede que se vea o no. Se presenta en tres estados básicos: Solido Liquido Gas Solidos Su volumen y forma son definidos No
1º ESO IES MURIEDAS Bonifacio San Millán
 1º ESO IES MURIEDAS Bonifacio San Millán En las mezclas se aprecia, a simple vista, que están formadas por varios componentes En las mezclas NO se aprecia, a simple vista, que están formadas por varios
1º ESO IES MURIEDAS Bonifacio San Millán En las mezclas se aprecia, a simple vista, que están formadas por varios componentes En las mezclas NO se aprecia, a simple vista, que están formadas por varios
