FíSICA MODERNA. Maestría en Ciencias (Materiales) Otoño 2013 Dra. Lilia Meza Montes Instituto de Física Luis Rivera Terrazas
|
|
|
- Arturo Romero Aguirre
- hace 7 años
- Vistas:
Transcripción
1 FíSICA MODERNA Maestría en Ciencias (Materiales) Otoño 2013 Dra. Lilia Meza Montes Instituto de Física Luis Rivera Terrazas
2 Parte I. Introducción a la Mecánica Cuántica 1. Orígenes de las ideas cuánticas
3 Situación de la física a finales del siglo XIX Universo MATERIA Partículas puntuales Energía E Momentum p Leyes de Newton Ley de Lorentz r F carga = RADIACIÓN Ondas electromagnéticas Frecuencia Angular ω Vector de onda k Leyes de Maxwell r r r q( E+ v B) velocidad campos
4 Estructura Atómica John Dalton ( ): - Cada elemento químico se compone de átomos de un tipo único - No puede ser alterado o destruido por medios químicos - Se combinan para formar sustancias Avogrado (1811) Dos gases con igual V, P, T contienen el mismo número de moléculas.
5 Átomos Neutros formados por igual número de cargas + y Thomson (1897) Descubre electrón modelo de jalea Rutherford Modelo planetario - +
6 Radiación: ondas electromagnéticas λ k Frecuencia ω=2π/t Vector de onda Vector de onda k=2π/λ E Campo eléctrico B Campo magnético
7 1cm 0.1mm Microondas λ 1 micra 0.001mm Infrarrojo Ultravioleta 1 nanómetro Rayos X suaves
8 Ondas electromagnéticas.ppt
9 Fenómenos que no encontraban explicación en este marco teórico Radiación de cuerpo negro Efecto fotoeléctrico Efecto Compton
10 Radiación de cuerpo negro Cuerpos calientes emiten (absorben) radiación λ e Intensidad dependen de T Ejemplo: metal rojo->amarillo->blanco T ambiente: Infrarrojo MODELO Cuerpo Negro: absorbe toda la radiación que incide sobre él
11 Espectro de un cuerpo negro Depende de T
12 Teoría clásica: Densidad de energía 1884, Boltzmann. Ciclo de Carnot (radiación como sustancia), leyes de la termodinámica Ley de Stefan-Boltzmann: Energía emitida por unidad de tiempo por unidad de área u ( T ) = at a= erg / K cm Pero no depende de la frecuencia (o longitud de onda)
13 Ley de Rayleigh-Jeans Fines de siglo XIX Densidad(conteo) de longitudes de onda posibles x su energía Densidad de ondas: Modelo cavidad cúbica λ posibles: nodos en la pared ( υ) dυ = 2 8πυ c G 3 dυ
14 Comparación clásica-cuántica
15 Ley de Rayleigh-Jeans Teorema de equipartición: energía promedio por grado de libertad kt/2 (oscilador armónico: 2) ε = kt Fórmula de Rayleigh-Jeans Pero u( υ) dυ = εg( υ) dυ = υ u 8π 2 ktυ dυ 3 c Experimentos: u 0 Catástrofe ultravioleta
16 Ley de Wien Leyes de termodinámica y radiación Ley de desplazamiento Ley de Wien λ max T = cmK u( υ) dυ = 8π kβe 3 c υ dυ βυ /T 3 υ u 0 Pero discrepancias 11 υ / T > 10 / sk
17 Resultados clásicos Leyes Rayleigh-Jeans Ley de Wien 8π 2 u( υ) dυ = ktυ dυ 3 c u( υ) dυ = 8π kβe 3 c υ dυ βυ /T 3 F(x), x=ν/t
18 Planck (1900) x>>1 Wien x<1 R-J 1 1) ( ) ( = x e k x F β β υ υ υ π υ υ βυ υ d e dv c h d u T kt h 3 / / ) ( = s J h = Constante de Planck
19 Cuantización de la energía Osciladores isotrópicos irradian energía solo en Múltiplos de unidad básica de energía Energía promedio ε = n= 0 n= 0 = υf( x) = e hν ε e n e hν / kt 1 ε / kt ε / kt n n ε nhυ n = n = 0,1,2,
20 EFECTO FOTOELÉCTRICO
21 Efecto fotoeléctrico 1887, Hertz Al incidir luz (Vis-UV) en el metal (alcalino) emisión de electrones (fotocorriente) Explicación: Einstein, 1905 No sólo la energía de osciladores está cuantizada, la radiación se transporta en cuantos de luz (fotones)
22 Experimento Luz (intensidad I, frecuencia ν) incide sobre un metal placa colectora Luz incidente placa emisora vacío El metal emite electrones que forman fotocorriente Potencial retardador V: frena los electrones amperímetro Se mide la fotocorriente generada
23 Efecto fotoeléctrico
24 Resultados experimentales Fotocorriente Fotocorriente 2I I 3I Vo I=cte ν 1 ν 2 ν 1 Vo ν=cte V V Electrones absorben energía de onda luminosa Tiempo de emisión <10-9 s (teoría clásica: acumulación de energía llevaría más tiempo) Aumento de intensidad I aumenta corriente pero mismo Vo (teoría clásica: mayor intensidad mayor energía de fotoelectrones) ν aumenta mayor energía de fotoelectrones
25 Energía cinética vs. frecuencia Na m = E = h( ν 0) υ ν max max Energía cinética máxima del fotoelectrón (ev) Incremento lineal de la energía cinética del electrón eyectado Constante de Planck Pendiente es una constante, llamada ahora de Planck Frecuencia Hz x10 14 ν 0
26 Modelo metal 1905, Einstein Energía está cuantizada (quantum de luz=fotón, hν) Un electrón absorbe un cuanto (un solo fotón) Esta energía =vencer atracción de metal (función de trabajo Φ=hv 0 ) + energía cinética - Ek =0 E=hv E k =hv-hv 0 Máxima E de electrones 1 2 mv 2 max φ = hυ 0 = E = hυ φ max E max =ev 0 E mínima para que electrones puedan escapar
27 Función de trabajo Característica del metal Cs K Na Li Ca Cu Ag Pt Φ (ev) eV = E que adquiere un electrón en una diferencia de potencial de 1 V = (1.602x10-19 C)(1V)=1.602x10-19 J Fotones Intensidad I ~ número de fotones Mayor I más fotoelectrones mayor fotocorriente E = hν como ν = c / λ E= hc λ Energía de fotón depende de frecuencia ( o long. de onda)
28 1/cm ev EFECTO COMPTON, 1923
29 Dispersión de electrones exteriores del átomo de carbono Cristal + cámara de ionización = Espectrómetro ( mide la longitud de onda) Electrones de capas interiores: corrimiento pequeño porque están ligados y átomo recula como un todo
30 Resultados experimentales Intensidad de radiación detectada vs longitud de onda θ λ' λ= λ (1 cosθ ) c Corrimiento Compton Mínimo en θ=0 Máximo en θ=π imgqua/compdat.gif
31
32 Teoría: fotón se comporta como partícula con momento Momento del fotón hν/c Velocidad de la luz c p Momento del electrón p Conservación de momentum total (inicial=final) Componente x Componente y fotón λ Inicial Final electrón hν hν ' + 0= cosθ+ p cosφ c c hν ' 0= senθ + p senφ c λ (1)
33 Teoría: fotón se comporta como partícula Conservación de energía Relatividad especial E = = E m k 2 0 c + m c 4 + Combinando ecuaciones (1) y (2) 0 p 2 2 c 2 hν + m c fotón E k 0 = 2 = hν λ' λ= hν ' + E hν ' h m c 0 electrón k + m c 0 (1 cosθ ) 2 (2) Longitud de onda de Compton λ c =2.425x10-12 cm
34 Comportamiento dual En la escala subatómica, las leyes son diferentes: comportamiento cuántico Cantidades tienen valores discretos: energía, momento, por ejemplo, NO toman cualquier valor, ESTÁN CUANTIZADAS Formalismo matemático diferente (otras ecuaciones): MECÁNICA CUÁNTICA Fotón (fenómenos ondulatorios) también se comporta como partícula. Y las partículas?
35 Electrones: doble rendija Patrón de interferencia similar al de una onda Introduction to Quantum Mechanics, S. M. Blinder
36 Difracción de rayos X en cristales Haz incidente Haz difractado Cristal
37 Difracción de Rayos X y electrones: similares Rayos X Electrones Escalados para comparación
38 Onda o partícula? Los objetos (fotones, electrones ) tienen comportamiento dual Corpuscular Ondulatorio El comportamiento específico depende de las circunstancias particulares del fenómeno observado
MATERIA MOLÉCULAS ÁTOMOS PARTÍCULAS SUBATÓMICAS. Partícula Masa (g) Carga (Coulombs) Carga unitaria. Electrón
 MATERIA MOLÉCULAS ÁTOMOS PARTÍCULAS SUBATÓMICAS Partícula Masa (g) Carga (Coulombs) Carga unitaria Electrón 9.10939 10-28 -1.6022 10-19 -1 Protón 1.67262 10-24 +1.6022 10-19 +1 Neutrón 1.67493 10-24 0
MATERIA MOLÉCULAS ÁTOMOS PARTÍCULAS SUBATÓMICAS Partícula Masa (g) Carga (Coulombs) Carga unitaria Electrón 9.10939 10-28 -1.6022 10-19 -1 Protón 1.67262 10-24 +1.6022 10-19 +1 Neutrón 1.67493 10-24 0
Unidad 1 Estructura atómica de la materia. Teoría cuántica
 Unidad 1 Estructura atómica de la materia. Teoría cuántica 1.El átomo y la constitución de la materia DALTON NO ACEPTADO POR LOS FÍSICOS que creían en la idea de que los átomos se encontraban como disueltos
Unidad 1 Estructura atómica de la materia. Teoría cuántica 1.El átomo y la constitución de la materia DALTON NO ACEPTADO POR LOS FÍSICOS que creían en la idea de que los átomos se encontraban como disueltos
EXTRUCTURA ATOMICA ACTUAL
 ATOMOS Y ELEMENTOS TEMA 4 Química ATOMOS EXTRUCTURA ATOMICA ACTUAL PARTICULA UBICACION CARGA MASA PROTON NUCLEO + SI NEUTRON NUCLEO 0 SI ELECTRON ORBITAS - DESPRECIABLE La masa del átomo reside en el núcleo.
ATOMOS Y ELEMENTOS TEMA 4 Química ATOMOS EXTRUCTURA ATOMICA ACTUAL PARTICULA UBICACION CARGA MASA PROTON NUCLEO + SI NEUTRON NUCLEO 0 SI ELECTRON ORBITAS - DESPRECIABLE La masa del átomo reside en el núcleo.
Radiación. Cuerpo Negro Espectros Estructura del Atomo Espectroscopia Efecto Doppler. L. Infante 1
 Radiación Cuerpo Negro Espectros Estructura del Atomo Espectroscopia Efecto Doppler L. Infante 1 Cuerpo Negro: Experimento A medida que el objeto se calienta, se hace más brillante ya que emite más radiación
Radiación Cuerpo Negro Espectros Estructura del Atomo Espectroscopia Efecto Doppler L. Infante 1 Cuerpo Negro: Experimento A medida que el objeto se calienta, se hace más brillante ya que emite más radiación
Tema 11: Física Cuántica
 Tema 11: Física Cuántica 11.1 Introducción. 11. Limitaciones de la Física Clásica. 11.3 Efecto fotoeléctrico. 11.4 Dualidad onda-corpúsculo; hipótesis de De Broglie 11.5 Principio de indeterminación de
Tema 11: Física Cuántica 11.1 Introducción. 11. Limitaciones de la Física Clásica. 11.3 Efecto fotoeléctrico. 11.4 Dualidad onda-corpúsculo; hipótesis de De Broglie 11.5 Principio de indeterminación de
M. Eugenia Villaseca R. Licenciada y Profesora de Biología PUCV
 M. Eugenia Villaseca R. Licenciada y Profesora de Biología PUCV Comprender la utilidad de los modelos atómicos y de la teoría atómica para explicar los procesos de transformación físico-química de la materia
M. Eugenia Villaseca R. Licenciada y Profesora de Biología PUCV Comprender la utilidad de los modelos atómicos y de la teoría atómica para explicar los procesos de transformación físico-química de la materia
Velocidad de la Luz. c = (2,9979 ± 0,0001) x 10 8 m/s
 Velocidad de la Luz Métodos fallidos, como el de Galileo Galilei en 1667. Método astronómico de Olaf Roemer en 1675, concluye que c > 2 x 10 8 m/s (periodo de eclipse de satélites de Jupiter). Método de
Velocidad de la Luz Métodos fallidos, como el de Galileo Galilei en 1667. Método astronómico de Olaf Roemer en 1675, concluye que c > 2 x 10 8 m/s (periodo de eclipse de satélites de Jupiter). Método de
PRUEBAS DE ACCESO A LA UNIVERSIDAD MATERIAS DE MODALIDAD: FASES GENERAL Y ESPECÍFICA
 PRUEBAS DE ACCESO A LA UNIVERSIDAD MATERIAS DE MODALIDAD: FASES GENERAL Y ESPECÍFICA CURSO 2012-2013 CONVOCATORIA: JULIO MATERIA: FÍSICA De las dos opciones propuestas, sólo hay que desarrollar una opción
PRUEBAS DE ACCESO A LA UNIVERSIDAD MATERIAS DE MODALIDAD: FASES GENERAL Y ESPECÍFICA CURSO 2012-2013 CONVOCATORIA: JULIO MATERIA: FÍSICA De las dos opciones propuestas, sólo hay que desarrollar una opción
leyes de la radiación Dpto. de Ingeniería Cartográfica Carlos Pinilla Ruiz Ingeniería Técnica en Topografía lección 2 Teledetección
 lección 2 1 sumario 2 Fuentes de radiación. El cuerpo negro. Leyes de la radiación. Terminología radiométrica. fuentes de radiación 3 Energía radiante: es la energía transportada por una onda electromagnética.
lección 2 1 sumario 2 Fuentes de radiación. El cuerpo negro. Leyes de la radiación. Terminología radiométrica. fuentes de radiación 3 Energía radiante: es la energía transportada por una onda electromagnética.
Robert A. MILLIKAN ( )
 Robert A. MILLIKAN (1906 1914) Modelo atómico de Rutherford - Todo átomo está formado por un núcleo y corteza. - El núcleo, muy pesado, y de muy pequeño tamaño, formado por un número de protones igual
Robert A. MILLIKAN (1906 1914) Modelo atómico de Rutherford - Todo átomo está formado por un núcleo y corteza. - El núcleo, muy pesado, y de muy pequeño tamaño, formado por un número de protones igual
INDICE 22. La carga eléctrica Resumen, preguntas, problemas 23. El campo eléctrico Resumen, preguntas, problemas Resumen, preguntas, problemas
 INDICE 22. La carga eléctrica 22-1. las propiedades de la materia con carga 646 22-2. la conservación y cuantización de la carga 652 22-3. la ley de Colulomb 654 22-4. las fuerzas en las que intervienen
INDICE 22. La carga eléctrica 22-1. las propiedades de la materia con carga 646 22-2. la conservación y cuantización de la carga 652 22-3. la ley de Colulomb 654 22-4. las fuerzas en las que intervienen
J.J Thomson propone el primer modelo de átomo:
 MODELOS ATÓMICOS. DALTON En 1808, Dalton publicó sus ideas sobre el modelo atómico de la materia las cuales han servido de base a la química moderna. Los principios fundamentales de esta teoría son: 1.
MODELOS ATÓMICOS. DALTON En 1808, Dalton publicó sus ideas sobre el modelo atómico de la materia las cuales han servido de base a la química moderna. Los principios fundamentales de esta teoría son: 1.
Cuerpo negro. Un cuerpo que absorbe toda la radiación que incide en él se llama Cuerpo Negro Ideal(CNI). R =σt 4
 Equilibrio térmico Cuando luz incide sobre un cuerpo, parte de ésta es reflejada y otra parte es absorbida por el cuerpo. La luz absorbida aumenta la energía interna del cuerpo, aumentando su temperatura.
Equilibrio térmico Cuando luz incide sobre un cuerpo, parte de ésta es reflejada y otra parte es absorbida por el cuerpo. La luz absorbida aumenta la energía interna del cuerpo, aumentando su temperatura.
PRUEBAS DE ACCESO A LA UNIVERSIDAD MATERIAS DE MODALIDAD: FASES GENERAL Y ESPECÍFICA
 PRUEBAS DE ACCESO A LA UNIVERSIDAD MATERIAS DE MODALIDAD: FASES GENERAL Y ESPECÍFICA CURSO 013 014 CONVOCATORIA: PROBLEMAS OPCIÓN A MATERIA: FÍSICA De las dos opciones propuestas, sólo hay que desarrollar
PRUEBAS DE ACCESO A LA UNIVERSIDAD MATERIAS DE MODALIDAD: FASES GENERAL Y ESPECÍFICA CURSO 013 014 CONVOCATORIA: PROBLEMAS OPCIÓN A MATERIA: FÍSICA De las dos opciones propuestas, sólo hay que desarrollar
Ejercicios de Física cuántica y nuclear. PAU (PAEG)
 1. Las longitudes de onda del espectro visible están comprendidas, aproximadamente, entre 390 nm en el violeta y 740 nm en el rojo. Qué intervalo aproximado de energías, en ev, corresponde a los fotones
1. Las longitudes de onda del espectro visible están comprendidas, aproximadamente, entre 390 nm en el violeta y 740 nm en el rojo. Qué intervalo aproximado de energías, en ev, corresponde a los fotones
EL ÁTOMO CONTENIDOS. ANTECEDENTES HISTÓRICOS. ( ) MODELOS ATÓMICOS. RAYOS CATÓDICOS. MODELO DE THOMSON.
 EL ÁTOMO CONTENIDOS. 1.- Antecedentes históricos.( ) 2.- Partículas subatómicas. ( ) 3.- Modelo atómico de Thomsom. 4.- Los rayos X. 5.- La radiactividad. 6.- Modelo atómico de Rutherford. 7.- Radiación
EL ÁTOMO CONTENIDOS. 1.- Antecedentes históricos.( ) 2.- Partículas subatómicas. ( ) 3.- Modelo atómico de Thomsom. 4.- Los rayos X. 5.- La radiactividad. 6.- Modelo atómico de Rutherford. 7.- Radiación
LAS LEYES DE LA RADIACIÓN EN LA TIERRA Y EN EL ESPACIO OBJETIVO RESUMEN. GENERACIÓN DE LINEAS: Leyes de Kirchhoff
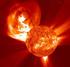 LAS LEYES DE LA RADIACIÓN EN LA TIERRA Y EN EL ESPACIO OBJETIVO Aproximarnos a los procesos que absorben y generan radiación electromagnética en la Tierra y en el espacio. Basada en presentación de Tabaré
LAS LEYES DE LA RADIACIÓN EN LA TIERRA Y EN EL ESPACIO OBJETIVO Aproximarnos a los procesos que absorben y generan radiación electromagnética en la Tierra y en el espacio. Basada en presentación de Tabaré
TEMA 4: OPTICA. Cómo puede un buceador estimar la profundidad a la que se encuentra?
 Cómo puede un buceador estimar la profundidad a la que se encuentra? http://www.buceando.es/ Física A qué distancia podemos distinguir los ojos de un gato montés? Soy daltónico? La luz: naturaleza dual
Cómo puede un buceador estimar la profundidad a la que se encuentra? http://www.buceando.es/ Física A qué distancia podemos distinguir los ojos de un gato montés? Soy daltónico? La luz: naturaleza dual
Ondas. Prof. Jesús Hernández Trujillo Facultad de Química, UNAM. Ondas/J. Hdez. T p. 1
 Ondas Prof. Jesús Hernández Trujillo Facultad de Química, UNAM Ondas/J. Hdez. T p. 1 Introducción Definición: Una onda es una perturbación que se propaga en el tiempo y el espacio Ejemplos: Ondas en una
Ondas Prof. Jesús Hernández Trujillo Facultad de Química, UNAM Ondas/J. Hdez. T p. 1 Introducción Definición: Una onda es una perturbación que se propaga en el tiempo y el espacio Ejemplos: Ondas en una
Programa de Acceso Inclusivo, Equidad y Permanencia PAIEP U. de Santiago. Química
 Modelos atómicos Los filósofos de la antigüedad especularon sobre cómo estaba formada la materia. Demócrito (460-370 a.c) y otros filósofos anteriores a él, pensaban que el mundo material debería estar
Modelos atómicos Los filósofos de la antigüedad especularon sobre cómo estaba formada la materia. Demócrito (460-370 a.c) y otros filósofos anteriores a él, pensaban que el mundo material debería estar
XIII OLIMPIADA CHILENA DE FISICA 2005 Sociedad Chilena de Física
 XIII OLIMPIADA CHILENA DE FISICA 2005 Sociedad Chilena de Física PRUEBA EXPERIMENTAL A NOMBRE: RUT: CURSO: NUMERO TOTAL DE PAGINAS ESCRITAS: PUNTAJE TOTAL La constante de Planck de la física cuántica y
XIII OLIMPIADA CHILENA DE FISICA 2005 Sociedad Chilena de Física PRUEBA EXPERIMENTAL A NOMBRE: RUT: CURSO: NUMERO TOTAL DE PAGINAS ESCRITAS: PUNTAJE TOTAL La constante de Planck de la física cuántica y
PAAU (LOXSE) Setembro 2003
 PAAU (LOXSE) Setembro 2003 Código: 22 FÍSICA Elegir y desarrollar una de las dos opciones propuestas. Puntuación máxima: Problemas 6 puntos (1,5 cada apartado) Cuestiones 4 puntos (1 cada cuestión, teórica
PAAU (LOXSE) Setembro 2003 Código: 22 FÍSICA Elegir y desarrollar una de las dos opciones propuestas. Puntuación máxima: Problemas 6 puntos (1,5 cada apartado) Cuestiones 4 puntos (1 cada cuestión, teórica
MODELOS ATOMICOS. Solución Å; Ultravioleta; 1106 m/s
 MODELOS ATOMICOS 1. Calcular el valor del radio de la órbita que recorre el electrón del hidrogeno en su estado normal. Datos. h = 6 63 10 27 erg s, m(e ) = 9 1 10 28 gr, q(e ) = 4 8 10-10 u.e.e. Solución.
MODELOS ATOMICOS 1. Calcular el valor del radio de la órbita que recorre el electrón del hidrogeno en su estado normal. Datos. h = 6 63 10 27 erg s, m(e ) = 9 1 10 28 gr, q(e ) = 4 8 10-10 u.e.e. Solución.
Comportamiento Electrónico de los Materiales. Tema 1. Fundamentos Físicos de la Estructura Electrónica del Átomo
 Comportamiento Electrónico de los Materiales Tema 1. Fundamentos Físicos de la Estructura Electrónica del Átomo 1.1 Fundamentos de la Estructura Atómica de la Materia1. 1.1.1 Historia: Se tiene conocimiento
Comportamiento Electrónico de los Materiales Tema 1. Fundamentos Físicos de la Estructura Electrónica del Átomo 1.1 Fundamentos de la Estructura Atómica de la Materia1. 1.1.1 Historia: Se tiene conocimiento
MODELO ATÓMICO DE DALTON 1808
 ESTRUCTURA ATÓMICA MODELO ATÓMICO DE DALTON 1808 Sienta las bases para la estequiometría de composición y la estequiometría de reacción. 1. Un elemento se compone de partículas extremadamente pequeñas,
ESTRUCTURA ATÓMICA MODELO ATÓMICO DE DALTON 1808 Sienta las bases para la estequiometría de composición y la estequiometría de reacción. 1. Un elemento se compone de partículas extremadamente pequeñas,
EFECTO FOTOELÉCTRICO
 EFECTO FOTOELÉCTRICO Objetivo: Analizar el efecto fotoeléctrico y obtener la constante de Planck Introducción: La emisión y absorción de luz fue tema de investigación del físico Max Planck. Cuando Planck
EFECTO FOTOELÉCTRICO Objetivo: Analizar el efecto fotoeléctrico y obtener la constante de Planck Introducción: La emisión y absorción de luz fue tema de investigación del físico Max Planck. Cuando Planck
Teoría Cuántica y la estructura electrónica de los Átomos
 EN EL INTERIOR DEL ATOMO TEMA 3 Química General e Inorgánica A Teoría Cuántica y la estructura electrónica de los Átomos 1 LO QUE SABEMOS EXTRUCTURA ATOMICA ACTUAL PARTICULA UBICACION CARGA MASA PROTON
EN EL INTERIOR DEL ATOMO TEMA 3 Química General e Inorgánica A Teoría Cuántica y la estructura electrónica de los Átomos 1 LO QUE SABEMOS EXTRUCTURA ATOMICA ACTUAL PARTICULA UBICACION CARGA MASA PROTON
FISICA CUANTICA. Dr. Mario Piris Silvera. Instittuto Superior de Ciencias y Tecnología Nucleares. Editorial ISCTN, 1999.
 FISICA CUANTICA Dr. Mario Piris Silvera Instittuto Superior de Ciencias y Tecnología Nucleares Editorial ISCTN, 1999. La Habana, Cuba Índice general 1. Cuantos de luz. 9 1.1. Cuerpo Negro. Hipótesis de
FISICA CUANTICA Dr. Mario Piris Silvera Instittuto Superior de Ciencias y Tecnología Nucleares Editorial ISCTN, 1999. La Habana, Cuba Índice general 1. Cuantos de luz. 9 1.1. Cuerpo Negro. Hipótesis de
Física P.A.U. FÍSICA MODERNA 1 FÍSICA MODERNA. 1. Se hará una lista con los datos, pasándolos al Sistema Internacional si no lo estuviesen.
 Física P.A.U. FÍSICA MODERNA FÍSICA MODERNA INTRODUCCIÓN RECOMENDACIONES. Se hará una lista con los datos, pasándolos al Sistema Internacional si no lo estuviesen. 2. Se hará otra lista con las incógnitas.
Física P.A.U. FÍSICA MODERNA FÍSICA MODERNA INTRODUCCIÓN RECOMENDACIONES. Se hará una lista con los datos, pasándolos al Sistema Internacional si no lo estuviesen. 2. Se hará otra lista con las incógnitas.
FÍSICA y QUÍMICA. Número cuántico Secundario (SUBNIVEL) l. Número cuántico Magnético (ORBITAL, como si fuera una caja) m.
 TEMA 1: ESTRUCTURA DE LA MATERIA. MODELOS ATÓMICOS 1. Modelo Atómico de RUTHERFORD a. Modelo predecesor de Thomson. b. Modelo atómico de Rutherford. c. Virtudes y defectos del Modelo de Rutherford. 2.
TEMA 1: ESTRUCTURA DE LA MATERIA. MODELOS ATÓMICOS 1. Modelo Atómico de RUTHERFORD a. Modelo predecesor de Thomson. b. Modelo atómico de Rutherford. c. Virtudes y defectos del Modelo de Rutherford. 2.
- Marie Curie. - Joseph Thomson. - Ernest Rutherford. - Max Planck. - Albert Einstein. - Niels Bohr. - Louis de Broglie. - Werner Heisenberg
 - Marie Curie - Joseph Thomson - Ernest Rutherford - Max Planck - Albert Einstein - Niels Bohr - Louis de Broglie - Werner Heisenberg - Wolfgang Pauli - Arnorld Sommerfeld Autores (Orden Alfabético): Celia
- Marie Curie - Joseph Thomson - Ernest Rutherford - Max Planck - Albert Einstein - Niels Bohr - Louis de Broglie - Werner Heisenberg - Wolfgang Pauli - Arnorld Sommerfeld Autores (Orden Alfabético): Celia
TEMA 2 LA CORTEZA ELECTRÓNICA
 Orígenes de la teoría cuántica TEMA 2 LA CORTEZA ELECTRÓNICA Había una grave dificultad con el modelo del átomo de Rutherford. De acuerdo con todos los principios de la física conocidos en 1911, el átomo
Orígenes de la teoría cuántica TEMA 2 LA CORTEZA ELECTRÓNICA Había una grave dificultad con el modelo del átomo de Rutherford. De acuerdo con todos los principios de la física conocidos en 1911, el átomo
UNIDAD VIII: RADIACION TERMICA. Introducción. Ley de KIRCHOFF. Ley de PLANCK. Transporte de calor por radiación.
 UNIDAD VIII: RADIACION TERMICA Ley de KIRCHOFF. Ley de PLANCK. Transporte de calor por radiación. Introducción La temperatura de un cuerpo que esta más caliente que su entorno tiende a decrecer con el
UNIDAD VIII: RADIACION TERMICA Ley de KIRCHOFF. Ley de PLANCK. Transporte de calor por radiación. Introducción La temperatura de un cuerpo que esta más caliente que su entorno tiende a decrecer con el
Ejercicios de exámenes de Selectividad FÍSICA MODERNA: EFECTO FOTOELÉCTRICO
 Ejercicios de exámenes de Selectividad FÍSICA MODERNA: EFECTO FOTOELÉCTRICO 1. Un haz de luz monocromática de longitud de onda en el vacío 450 nm incide sobre un metal cuya longitud de onda umbral, para
Ejercicios de exámenes de Selectividad FÍSICA MODERNA: EFECTO FOTOELÉCTRICO 1. Un haz de luz monocromática de longitud de onda en el vacío 450 nm incide sobre un metal cuya longitud de onda umbral, para
Clase N 1. Modelo Atómico I
 Pre-Universitario Manuel Guerrero Ceballos Clase N 1 Modelo Atómico I ICAL ATACAMA Módulo Plan Común Modelos Atómicos Teoría Atómica De Dalton Los elementos están formados por partículas extremadamente
Pre-Universitario Manuel Guerrero Ceballos Clase N 1 Modelo Atómico I ICAL ATACAMA Módulo Plan Común Modelos Atómicos Teoría Atómica De Dalton Los elementos están formados por partículas extremadamente
Física 2º Bachillerato. Orientaciones Generales.
 Física 2º Bachillerato. Orientaciones Generales. Recomendaciones generales 1. Prestar especial atención a las magnitudes vectoriales y las unidades 2. Ningún problema suele requerir un tratamiento matemático
Física 2º Bachillerato. Orientaciones Generales. Recomendaciones generales 1. Prestar especial atención a las magnitudes vectoriales y las unidades 2. Ningún problema suele requerir un tratamiento matemático
Preuniversitario Esperanza Joven Curso Física Intensivo, Módulo Común. Ondas III; La luz
 Preuniversitario Esperanza Joven Curso Física Intensivo, Módulo Común Guía 11 Ondas III; La luz Nombre: Fecha: Naturaleza de la luz 1. Teoría corpuscular: Newton formula que la luz estaba formada por pequenos
Preuniversitario Esperanza Joven Curso Física Intensivo, Módulo Común Guía 11 Ondas III; La luz Nombre: Fecha: Naturaleza de la luz 1. Teoría corpuscular: Newton formula que la luz estaba formada por pequenos
Tema 2. La radiación electromagnética (REM) Teledetección 2º Curso de IT en Topografía EPS Jaén
 Tema 2. La radiación electromagnética (REM) Teledetección 2º Curso de IT en Topografía EPS Jaén 1. Movimiento ondulatorio 2. La radiación electromagnética (REM) 3. El espectro electromagnético 4. Terminología
Tema 2. La radiación electromagnética (REM) Teledetección 2º Curso de IT en Topografía EPS Jaén 1. Movimiento ondulatorio 2. La radiación electromagnética (REM) 3. El espectro electromagnético 4. Terminología
ESTRUCTURA DEL ÁTOMO. MODELOS DE RUTHERFORD Y DE BOHR-SOMMERFELD
 ESTRUCTURA DEL ÁTOMO. MODELOS DE RUTHERFORD Y DE BOHR-SOMMERFELD De todas las partículas subatómicas elementales, ay tres que interesan fundamentalmente, pues son necesarias para construir un modelo atómico
ESTRUCTURA DEL ÁTOMO. MODELOS DE RUTHERFORD Y DE BOHR-SOMMERFELD De todas las partículas subatómicas elementales, ay tres que interesan fundamentalmente, pues son necesarias para construir un modelo atómico
Departamento de Física y Química
 1 PAU Física, septiembre 2011 OPCIÓN A Cuestión 1.- Un espejo esférico convexo, proporciona una imagen virtual de un objeto que se encuentra a 3 m del espejo con un tamaño 1/5 del de la imagen real. Realice
1 PAU Física, septiembre 2011 OPCIÓN A Cuestión 1.- Un espejo esférico convexo, proporciona una imagen virtual de un objeto que se encuentra a 3 m del espejo con un tamaño 1/5 del de la imagen real. Realice
QUÍMICA 2º BACH. TEMA 1. ESTRUCTURA ATÓMICA.
 Modelos atómicos QUÍMICA 2º BACH. TEMA 1. ESTRUCTURA ATÓMICA. Teoría atómica de Dalton: La materia está formada por átomos indivisibles. Los átomos de un elemento son distintos de los átomos de otro elemento
Modelos atómicos QUÍMICA 2º BACH. TEMA 1. ESTRUCTURA ATÓMICA. Teoría atómica de Dalton: La materia está formada por átomos indivisibles. Los átomos de un elemento son distintos de los átomos de otro elemento
Problemas. Cuestiones. Física 2º Bach. Física moderna 20/05/09 DEPARTAMENTO DE FÍSICA E QUÍMICA. Nombre: [2 PUNTOS /UNO]
![Problemas. Cuestiones. Física 2º Bach. Física moderna 20/05/09 DEPARTAMENTO DE FÍSICA E QUÍMICA. Nombre: [2 PUNTOS /UNO] Problemas. Cuestiones. Física 2º Bach. Física moderna 20/05/09 DEPARTAMENTO DE FÍSICA E QUÍMICA. Nombre: [2 PUNTOS /UNO]](/thumbs/49/25535199.jpg) Física 2º Bach. Física moderna 20/05/09 DEPARTAMENTO DE FÍSICA E QUÍMICA Problemas Nombre: [2 PUNTOS /UNO] 1. Al iluminar una célula fotoeléctrica con radiación electromagnética de longitud de onda 185
Física 2º Bach. Física moderna 20/05/09 DEPARTAMENTO DE FÍSICA E QUÍMICA Problemas Nombre: [2 PUNTOS /UNO] 1. Al iluminar una célula fotoeléctrica con radiación electromagnética de longitud de onda 185
Módulo 5: La luz. Ondas electromagnéticas
 Módulo 5: La luz 1 Ondas electromagnéticas Partículas cargadas eléctricamente (cargas) en movimiento forman una corriente eléctrica Una corriente eléctrica que cambia (debida al movimiento) crea un campo
Módulo 5: La luz 1 Ondas electromagnéticas Partículas cargadas eléctricamente (cargas) en movimiento forman una corriente eléctrica Una corriente eléctrica que cambia (debida al movimiento) crea un campo
Radiación electromagnética Naturaleza de la luz Teoría cuántica Espectros atómicos Modelo de Bohr
 ESTRUCTURA ELECTRÓNICA Número de Avogadro Radiación electromagnética Naturaleza de la luz Teoría cuántica Espectros atómicos Modelo de Bohr Número de Avogadro Amadeo Avogadro (1776-1856, italiano) Descubrió
ESTRUCTURA ELECTRÓNICA Número de Avogadro Radiación electromagnética Naturaleza de la luz Teoría cuántica Espectros atómicos Modelo de Bohr Número de Avogadro Amadeo Avogadro (1776-1856, italiano) Descubrió
Colegio Pasionista de Quilpué Departamento de Ciencias Ciencias Naturales 8 año básico 2015 Miss. Cecilia Rojas Olguín. El átomo.
 Colegio Pasionista de Quilpué Departamento de Ciencias Ciencias Naturales 8 año básico 2015 Miss. Cecilia Rojas Olguín El átomo 06 de Marzo 2015 Objetivos de la clase Comprender el Modelo corpuscular de
Colegio Pasionista de Quilpué Departamento de Ciencias Ciencias Naturales 8 año básico 2015 Miss. Cecilia Rojas Olguín El átomo 06 de Marzo 2015 Objetivos de la clase Comprender el Modelo corpuscular de
3. Física de la luz, fenómenos ópticos y su reproducción por com
 3. Física de la luz, fenómenos ópticos y su reproducción por computador Tercera sesión 3 de agosto de 2010 Contenido 1 ¾Qué es la luz? 2 La luz Naturaleza de la luz Teoría corpuscular Trabajos preliminares
3. Física de la luz, fenómenos ópticos y su reproducción por computador Tercera sesión 3 de agosto de 2010 Contenido 1 ¾Qué es la luz? 2 La luz Naturaleza de la luz Teoría corpuscular Trabajos preliminares
o el descubrimiento del fotón y del carácter cuántico del mundo microscópico.
 El efecto fotoeléctrico, o el descubrimiento del fotón y del carácter cuántico del mundo microscópico. Qué es el efecto foto-eléctrico: es el fenómeno que consiste en que los metales liberan electrones
El efecto fotoeléctrico, o el descubrimiento del fotón y del carácter cuántico del mundo microscópico. Qué es el efecto foto-eléctrico: es el fenómeno que consiste en que los metales liberan electrones
Solución de los problemas del Capítulo 1
 Nota: los valores de las constantes que puede necesitar para los cálculos están dados en la bibliografía de referencia. Complete la siguiente tabla Qué información mínima se necesita para caracterizar
Nota: los valores de las constantes que puede necesitar para los cálculos están dados en la bibliografía de referencia. Complete la siguiente tabla Qué información mínima se necesita para caracterizar
ESTRUCTURA DEL ÁTOMO - RESUMEN
 TEMA 1 ESTRUCTURA DEL ÁTOMO - RESUMEN 1. DESCUBRIMIENTO DE LA ESTRUCTURA ATÓMICA (ideas generales) Dalton: consideraba que un átomo no podía romperse en trozos más pequeños. El primer indicio de que el
TEMA 1 ESTRUCTURA DEL ÁTOMO - RESUMEN 1. DESCUBRIMIENTO DE LA ESTRUCTURA ATÓMICA (ideas generales) Dalton: consideraba que un átomo no podía romperse en trozos más pequeños. El primer indicio de que el
Las estructura electrónica de los átomos
 Las estructura electrónica de los átomos Al preguntarnos por las diferencias entre las propiedades químicas y físicas de los elementos, así como, su forma de enlazarse y la forma en la cual emiten o absorben
Las estructura electrónica de los átomos Al preguntarnos por las diferencias entre las propiedades químicas y físicas de los elementos, así como, su forma de enlazarse y la forma en la cual emiten o absorben
INDICE. Volumen 1 Mecánica
 INDICE Volumen 1 Mecánica 1 1. Unidades cantidades físicas y vectores 1.1. La naturaleza de la física 2 1.2. Como resolver problemas en física 3 1.3. Estándares y unidades 5 1.4. Consistencia y conversiones
INDICE Volumen 1 Mecánica 1 1. Unidades cantidades físicas y vectores 1.1. La naturaleza de la física 2 1.2. Como resolver problemas en física 3 1.3. Estándares y unidades 5 1.4. Consistencia y conversiones
El modelo cuántico de átomo
 El modelo cuántico de átomo IES La Magdalena. Avilés. Asturias En los últimos años del s. XIX y principios del XX el estudio de la interacción entre la materia y las ondas electromagnéticas llevó a la
El modelo cuántico de átomo IES La Magdalena. Avilés. Asturias En los últimos años del s. XIX y principios del XX el estudio de la interacción entre la materia y las ondas electromagnéticas llevó a la
El e c t r o m a g n e t i s m o. Eduardo Bonda Álvaro Suárez Marcelo Vachetta
 El e c t r o m a g n e t i s m o Cuántica y Relatividad Eduardo Bonda Álvaro Suárez Marcelo Vachetta índice Índice Prólogo...9 Capítulo 1 - Campo Eléctrico...11 Introducción... 11 Elektron... 11 Carga
El e c t r o m a g n e t i s m o Cuántica y Relatividad Eduardo Bonda Álvaro Suárez Marcelo Vachetta índice Índice Prólogo...9 Capítulo 1 - Campo Eléctrico...11 Introducción... 11 Elektron... 11 Carga
1. Estructura Atómica
 1. Estructura Atómica 1.1 Modelos atómicos: de Dalton a Rutherford 1.1.1 Modelo atómico de Dalton 1.1.2 Modelo atómico de Thomson 1.1.3 Modelo atómico de Rutherford 1.2 Modelo atómico de Bohr 1.2.1 Espectro
1. Estructura Atómica 1.1 Modelos atómicos: de Dalton a Rutherford 1.1.1 Modelo atómico de Dalton 1.1.2 Modelo atómico de Thomson 1.1.3 Modelo atómico de Rutherford 1.2 Modelo atómico de Bohr 1.2.1 Espectro
Practica nº n 5: Fenómenos de Difracción.
 Facultad de Farmacia Universidad de Granada Departamento de Química Física Practica nº n 5: Fenómenos de Difracción. OBJETIVOS 1.Observar los fenómenos de difracción Rendija simple Rendija doble 2.Calcular
Facultad de Farmacia Universidad de Granada Departamento de Química Física Practica nº n 5: Fenómenos de Difracción. OBJETIVOS 1.Observar los fenómenos de difracción Rendija simple Rendija doble 2.Calcular
PAAU (LOXSE) Setembro 2004
 PAAU (LOXSE) Setembro 004 Código: FÍSICA Elegir y desarrollar una de las dos opciones propuestas. Puntuación máxima: Problemas 6 puntos (1,5 cada apartado) Cuestiones 4 puntos (1 cada cuestión, teórica
PAAU (LOXSE) Setembro 004 Código: FÍSICA Elegir y desarrollar una de las dos opciones propuestas. Puntuación máxima: Problemas 6 puntos (1,5 cada apartado) Cuestiones 4 puntos (1 cada cuestión, teórica
VIBRACIÓN Y ONDAS. Se denomina rayo a la línea perpendicular a los frentes de onda, como se muestra en la figura.
 VIBRACIÓN Y ONDAS DEFINICIÓN DE ONDA Una partícula realiza un movimiento vibratorio cuando realiza una oscilación alrededor del punto de equilibrio. Un ejemplo de movimiento vibratorio lo constituye la
VIBRACIÓN Y ONDAS DEFINICIÓN DE ONDA Una partícula realiza un movimiento vibratorio cuando realiza una oscilación alrededor del punto de equilibrio. Un ejemplo de movimiento vibratorio lo constituye la
Ejercicios de Física cuántica y nuclear. PAEG
 1. Las longitudes de onda del espectro visible están comprendidas, aproximadamente, entre 390 nm en el violeta y 740 nm en el rojo. Qué intervalo aproximado de energías, en ev, corresponde a los fotones
1. Las longitudes de onda del espectro visible están comprendidas, aproximadamente, entre 390 nm en el violeta y 740 nm en el rojo. Qué intervalo aproximado de energías, en ev, corresponde a los fotones
QUIMICA GENERAL. Docente : Raquel Villafrades Torres
 Universidad Pontificia Bolivariana QUIMICA GENERAL Docente : Raquel Villafrades Torres TEORIA ATOMICA DE DALTON (1808) BASES Ley de conservación de la masa: La masa total de las sustancias presentes después
Universidad Pontificia Bolivariana QUIMICA GENERAL Docente : Raquel Villafrades Torres TEORIA ATOMICA DE DALTON (1808) BASES Ley de conservación de la masa: La masa total de las sustancias presentes después
ESTRUCTURA DE LA MATERIA
 ESTRUCTURA DE LA MATERIA CONTENIDOS. 1.- Radiación electromagnética y espectros atómicos. 1.1. Espectros atómicos. 1.2. Series espectrales. 1.3. Ley de Rygberg ( ). 2.- Orígenes de la teoría cuántica.
ESTRUCTURA DE LA MATERIA CONTENIDOS. 1.- Radiación electromagnética y espectros atómicos. 1.1. Espectros atómicos. 1.2. Series espectrales. 1.3. Ley de Rygberg ( ). 2.- Orígenes de la teoría cuántica.
EL EFECTO FOTOELÉCTRICO
 1 EL EFECTO FOTOELÉCTRICO M.A. Rodríguez-Meza 1 y J.L. Cervantes-Cota Depto. De Física, Instituto Nacional de Investigaciones Nucleares Apdo. Postal 18-1027, México D.F. 11801, México Resumen Presentamos
1 EL EFECTO FOTOELÉCTRICO M.A. Rodríguez-Meza 1 y J.L. Cervantes-Cota Depto. De Física, Instituto Nacional de Investigaciones Nucleares Apdo. Postal 18-1027, México D.F. 11801, México Resumen Presentamos
FUNDAMENTOS DE ENERGÍA SOLAR
 FUNDAMENTOS DE ENERGÍA SOLAR Dr. Ricardo Guerrero Lemus 1 DUALIDAD ONDA/PARTÍCULA DE LA LUZ: A partir de finales del siglo XVII empezó a prevalecer el punto de vista mecánico de Newton por el que la luz
FUNDAMENTOS DE ENERGÍA SOLAR Dr. Ricardo Guerrero Lemus 1 DUALIDAD ONDA/PARTÍCULA DE LA LUZ: A partir de finales del siglo XVII empezó a prevalecer el punto de vista mecánico de Newton por el que la luz
IEO-394 Semiconductores. Juan E. Martínez P. Docente. UdeA
 IEO-394 Semiconductores Juan E. Martínez P. Docente. UdeA Bandas de Energía Y Corrientes de Portadores en Semiconductores. PARTICION DE LOS NIVELES DE ENERGIA A medida que se traen juntos N átomos Cada
IEO-394 Semiconductores Juan E. Martínez P. Docente. UdeA Bandas de Energía Y Corrientes de Portadores en Semiconductores. PARTICION DE LOS NIVELES DE ENERGIA A medida que se traen juntos N átomos Cada
Ejercicios de Ondas Mecánicas y Ondas Electromagnéticas.
 Ejercicios de Ondas Mecánicas y Ondas Electromagnéticas. 1.- Determine la velocidad con que se propagación de una onda a través de una cuerda sometida ala tensión F, como muestra la figura. Para ello considere
Ejercicios de Ondas Mecánicas y Ondas Electromagnéticas. 1.- Determine la velocidad con que se propagación de una onda a través de una cuerda sometida ala tensión F, como muestra la figura. Para ello considere
Un modelo atómico, por lo tanto consiste en representar de manera grafica, la dimensión atómica de la materia. El objetivo de estos modelos es que el
 Modelos atómicos Debido a que no se podían ver los átomos los científicos crearon modelos para describirlos, éstos fueron evolucionando a lo largo de la historia a medida que se descubrieron nuevas cosas.
Modelos atómicos Debido a que no se podían ver los átomos los científicos crearon modelos para describirlos, éstos fueron evolucionando a lo largo de la historia a medida que se descubrieron nuevas cosas.
Índice general. Introducción 1
 Índice general Introducción 1 1. La atmósfera 3 1.1. Introducción........................ 4 1.2. Composición de la atmósfera............... 4 1.3. La estructura de la atmósfera.............. 8 1.3.1. La
Índice general Introducción 1 1. La atmósfera 3 1.1. Introducción........................ 4 1.2. Composición de la atmósfera............... 4 1.3. La estructura de la atmósfera.............. 8 1.3.1. La
MODELOS ATÓMICOS 2ª PARTE
 MODELOS ATÓMICOS 2ª PARTE Teoría Atómica de Joseph John Thomson Diseño Experimental de Joseph John Thomson (1856-1940) Utiliza Tubos de Rayos Catódicos, en los cuales estudia el comportamiento de los gases
MODELOS ATÓMICOS 2ª PARTE Teoría Atómica de Joseph John Thomson Diseño Experimental de Joseph John Thomson (1856-1940) Utiliza Tubos de Rayos Catódicos, en los cuales estudia el comportamiento de los gases
Prueba experimental. Constante de Planck y comportamiento de un LED
 Prueba experimental. Constante de Planck y comportamiento de un LED Objetivo. Se va a construir un circuito eléctrico para alimentar LEDs de diferentes colores y obtener un valor aproximado de la constante
Prueba experimental. Constante de Planck y comportamiento de un LED Objetivo. Se va a construir un circuito eléctrico para alimentar LEDs de diferentes colores y obtener un valor aproximado de la constante
3. TRANSFORMADORES. Su misión es aumentar o reducir el voltaje de la corriente manteniendo la potencia. n 2 V 1. n 1 V 2
 3. TRANSFORMADORES Un transformador son dos arrollamientos (bobina) de hilo conductor, magnéticamente acoplados a través de un núcleo de hierro común (dulce). Un arrollamiento (primario) está unido a una
3. TRANSFORMADORES Un transformador son dos arrollamientos (bobina) de hilo conductor, magnéticamente acoplados a través de un núcleo de hierro común (dulce). Un arrollamiento (primario) está unido a una
I.E.S. Virgen del Puerto Química 2º Bachillerato 2016/2017
 UD. 1 ESTRUCTURA ATÓMICA 1. INTRODUCCIÓN Dalton Thomson Rutherford Bohr Schrödinger (El concepto de átomo surge en la Grecia clásica, pero hasta principios del siglo XIX no se formula la primera teoría
UD. 1 ESTRUCTURA ATÓMICA 1. INTRODUCCIÓN Dalton Thomson Rutherford Bohr Schrödinger (El concepto de átomo surge en la Grecia clásica, pero hasta principios del siglo XIX no se formula la primera teoría
TEMA 2 ESTRUCTURA ELECTRÓNICA DE LOS ÁTOMOS
 TEMA 2 ESTRUCTURA ELECTRÓNICA DE LOS ÁTOMOS MARÍA PILAR RUIZ OJEDA BORJA MUÑOZ LEOZ Contenidos: 1. Introducción 2. Modelo de Thomson 3. Modelo de Rutherford 4. La luz y las ondas electromagnéticas 5. Dispersión
TEMA 2 ESTRUCTURA ELECTRÓNICA DE LOS ÁTOMOS MARÍA PILAR RUIZ OJEDA BORJA MUÑOZ LEOZ Contenidos: 1. Introducción 2. Modelo de Thomson 3. Modelo de Rutherford 4. La luz y las ondas electromagnéticas 5. Dispersión
El espectro electromagnético y los colores
 Se le llama espectro visible o luz visible a aquella pequeña porción del espectro electromagnético que es captada por nuestro sentido de la vista. La luz visible está formada por ondas electromagnéticas
Se le llama espectro visible o luz visible a aquella pequeña porción del espectro electromagnético que es captada por nuestro sentido de la vista. La luz visible está formada por ondas electromagnéticas
DEPARTAMENTO DE FÍSICA COLEGIO "LA ASUNCIÓN"
 COLEGIO "LA ASUNCIÓN" 1(8) Ejercicio nº 1 La ecuación de una onda armónica es: Y = 0 02 sen (4πt πx) Estando x e y expresadas en metros y t en segundos: a) Halla la amplitud, la frecuencia, la longitud
COLEGIO "LA ASUNCIÓN" 1(8) Ejercicio nº 1 La ecuación de una onda armónica es: Y = 0 02 sen (4πt πx) Estando x e y expresadas en metros y t en segundos: a) Halla la amplitud, la frecuencia, la longitud
CAPITULO I: La Luz CAPITULO I: LA LUZ 1
 CAPITULO I: La Luz CAPITULO I: LA LUZ 1 1.- La luz 1.1.- El nanómetro 1.2.- El espectro visible 1.3.- Naturaleza de la luz 1.4.- Fuentes de luz 2.- La Materia y la luz 2.1.- Fórmula R.A.T. 22-2.2. Absorción
CAPITULO I: La Luz CAPITULO I: LA LUZ 1 1.- La luz 1.1.- El nanómetro 1.2.- El espectro visible 1.3.- Naturaleza de la luz 1.4.- Fuentes de luz 2.- La Materia y la luz 2.1.- Fórmula R.A.T. 22-2.2. Absorción
PROPIEDADES DE LOS RAYOS X I
 CAPÍTULO.. RADIACIÓN ELECTROMAGNÉTICA Los rayos X son radiación electromagnética de la misma aturaleza que la luz pero de longitud de onda mucho más corta. La unidad de medida en la región de los rayos
CAPÍTULO.. RADIACIÓN ELECTROMAGNÉTICA Los rayos X son radiación electromagnética de la misma aturaleza que la luz pero de longitud de onda mucho más corta. La unidad de medida en la región de los rayos
PORTAFOLIO DE EVIDENCIAS QUÍMICA I DE SEGUNDA OPORTUNIDAD I LEE DETENIDAMENTE CADA ENUNCIADO Y CONTESTA SEGÚN SE TE PIDA.
 PORTAFOLIO DE EVIDENCIAS QUÍMICA I DE SEGUNDA OPORTUNIDAD I LEE DETENIDAMENTE CADA ENUNCIADO Y CONTESTA SEGÚN SE TE PIDA. 1.- Ciencia que estudia las características y la composición de los materiales,
PORTAFOLIO DE EVIDENCIAS QUÍMICA I DE SEGUNDA OPORTUNIDAD I LEE DETENIDAMENTE CADA ENUNCIADO Y CONTESTA SEGÚN SE TE PIDA. 1.- Ciencia que estudia las características y la composición de los materiales,
UNIVERSIDAD REGIONAL AMAZÓNICA IKIAM Carrera en Ingeniería en Ciencias del Agua. Syllabus de asignatura Secundo Semestre 1. INFORMACIÓN GENERAL
 UNIVERSIDAD REGIONAL AMAZÓNICA IKIAM Carrera en Ingeniería en Ciencias del Agua Syllabus de asignatura Secundo Semestre 1. INFORMACIÓN GENERAL Asignatura: Unidad Curricular Nivel Campos de formación Pre-requisitos
UNIVERSIDAD REGIONAL AMAZÓNICA IKIAM Carrera en Ingeniería en Ciencias del Agua Syllabus de asignatura Secundo Semestre 1. INFORMACIÓN GENERAL Asignatura: Unidad Curricular Nivel Campos de formación Pre-requisitos
Introducción a Física de Partículas y Cosmología
 Introducción a Física de Partículas y Cosmología del siglo XX Parte 1/4 Fernando Marchesano CERN (agradecimientos a Rolf Landua y Ángel Uranga por material original) Advertencia Estas charlas sobre Física
Introducción a Física de Partículas y Cosmología del siglo XX Parte 1/4 Fernando Marchesano CERN (agradecimientos a Rolf Landua y Ángel Uranga por material original) Advertencia Estas charlas sobre Física
Tema 9: ÓPTICA FÍSICA.
 2º BACHILLERATO FÍSICA Parte IV: ÓPTICA. Tema 9: ÓPTICA FÍSICA. 9.1. Naturaleza de la luz. 9.2. Ecuaciones de Maxwell. 9.3. Ondas electromagnéticas. 9.4. Dispersión. Reflexión y refracción. 9.5. Propiedades
2º BACHILLERATO FÍSICA Parte IV: ÓPTICA. Tema 9: ÓPTICA FÍSICA. 9.1. Naturaleza de la luz. 9.2. Ecuaciones de Maxwell. 9.3. Ondas electromagnéticas. 9.4. Dispersión. Reflexión y refracción. 9.5. Propiedades
LiceoTolimense Química Séptimo 1 Periodo ESTRUCTURA INTERNA DE LA MATERIA
 ESTRUCTURA INTERNA DE LA MATERIA Lectura comprensiva Desde la antigüedad los filósofos se preguntaban de qué estaban formadas las cosas que los rodeaban. Primero pensaron que la materia era continua, es
ESTRUCTURA INTERNA DE LA MATERIA Lectura comprensiva Desde la antigüedad los filósofos se preguntaban de qué estaban formadas las cosas que los rodeaban. Primero pensaron que la materia era continua, es
radiación Transferencia de Calor p. 1/1
 Transferencia de Calor p. 1/1 radiación la radiación térmica corresponde a la parte del espectro electromagnético con logitudes de onda por encima del bajo UV y el visible hasta las microondas... Transferencia
Transferencia de Calor p. 1/1 radiación la radiación térmica corresponde a la parte del espectro electromagnético con logitudes de onda por encima del bajo UV y el visible hasta las microondas... Transferencia
FÍSICA MODERNA: Teoría Cuántica
 FÍSICA MODERNA: Teoría Cuántica 1. Primeras teorías sobre la naturaleza de la luz. 1 1.1 Triunfo de la teoría ondulatoria. Ondas electromagnéticas:. Efecto fotoeléctrico. 3.1 Leyes del efecto fotoeléctrico:
FÍSICA MODERNA: Teoría Cuántica 1. Primeras teorías sobre la naturaleza de la luz. 1 1.1 Triunfo de la teoría ondulatoria. Ondas electromagnéticas:. Efecto fotoeléctrico. 3.1 Leyes del efecto fotoeléctrico:
5.1. Magnitudes radiométricas
 5. Radiometría y fotometría 5.1. Magnitudes radiométricas y fotométricas tricas 1 5. Radiometría y fotometría. 2 Magnitudes radiométricas y fotométricas tricas Radiometría rama de la Física dedicada a
5. Radiometría y fotometría 5.1. Magnitudes radiométricas y fotométricas tricas 1 5. Radiometría y fotometría. 2 Magnitudes radiométricas y fotométricas tricas Radiometría rama de la Física dedicada a
El átomo: sus partículas elementales
 El átomo: sus partículas elementales Los rayos catódicos estaban constituidos por partículas cargadas negativamente ( a las que se llamo electrones) y que la relación carga/masa de éstas partículas era
El átomo: sus partículas elementales Los rayos catódicos estaban constituidos por partículas cargadas negativamente ( a las que se llamo electrones) y que la relación carga/masa de éstas partículas era
Estructura de la materia y Sistema Periódico
 Estructura de la materia y Sistema Periódico 1 - Respecto el número cuántico «n» que aparece en el modelo atómico de Bohr indicar de manera razonada cuáles de las siguientes frases son correctas y cuáles
Estructura de la materia y Sistema Periódico 1 - Respecto el número cuántico «n» que aparece en el modelo atómico de Bohr indicar de manera razonada cuáles de las siguientes frases son correctas y cuáles
Interacción de neutrones con la materia. Laura C. Damonte 2014
 Interacción de neutrones con la materia Laura C. Damonte 2014 Interacción de neutrones con la materia La interacción de los neutrones con la materia tiene interés tanto experimental y teórico como también
Interacción de neutrones con la materia Laura C. Damonte 2014 Interacción de neutrones con la materia La interacción de los neutrones con la materia tiene interés tanto experimental y teórico como también
Estas partículas son estudiadas por J.J. Thomson que las caracterizó determinando el tipo de carga que poseían y su relación carga/masa.
 página 1/12 Partículas en el átomo Los experimentos de Volta y más tarde otros que pusieron de manifiesto la existencia de partículas cargadas en la materia llevaron a la investigación que obligó a replantearse
página 1/12 Partículas en el átomo Los experimentos de Volta y más tarde otros que pusieron de manifiesto la existencia de partículas cargadas en la materia llevaron a la investigación que obligó a replantearse
Calibración de un espectrómetro y medición de longitudes de onda de las líneas de un espectro.
 Calibración de un espectrómetro y medición de longitudes de onda de las líneas de un espectro. Objetivo Obtener la curva de calibración de un espectrómetro de red de difracción. Determinar la longitud
Calibración de un espectrómetro y medición de longitudes de onda de las líneas de un espectro. Objetivo Obtener la curva de calibración de un espectrómetro de red de difracción. Determinar la longitud
Implementación de un sistema básico para Espectroscopia de gases atómicos ABSTRACT KEY WORDS RESUMEN
 Implementación de un sistema básico para Espectroscopia de gases atómicos Heriberto Peña Pedraza Facultad de Ciencias Básicas. Departamento de Física Universidad de Pamplona Grupo de Investigaciones Ópticas
Implementación de un sistema básico para Espectroscopia de gases atómicos Heriberto Peña Pedraza Facultad de Ciencias Básicas. Departamento de Física Universidad de Pamplona Grupo de Investigaciones Ópticas
TEORÍAS SOBRE LA NATURALEZA DE LA LUZ
 TEORÍAS SOBRE LA NATURALEZA DE LA LUZ Desde el siglo XVII han sido dos las teorías físicas que han tratado de explicar la naturaleza de la luz. Durante mucho tiempo los defensores de una y otra mantuvieron
TEORÍAS SOBRE LA NATURALEZA DE LA LUZ Desde el siglo XVII han sido dos las teorías físicas que han tratado de explicar la naturaleza de la luz. Durante mucho tiempo los defensores de una y otra mantuvieron
SESIÓN 11 PROPIEDADES ONDULATORIAS DE LA LUZ
 SESIÓN 11 PROPIEDADES ONDULATORIAS DE LA LUZ I. CONTENIDOS: 1. Naturaleza de las ondas luminosas. 2. Difracción de la luz. 3. Interferencia: elementos y características. 4. Polarización: elementos y características.
SESIÓN 11 PROPIEDADES ONDULATORIAS DE LA LUZ I. CONTENIDOS: 1. Naturaleza de las ondas luminosas. 2. Difracción de la luz. 3. Interferencia: elementos y características. 4. Polarización: elementos y características.
Como esta formada la materia?
 Como esta formada la materia? Demócrito, filósofo griego que vivió en el siglo IV a. C. propuso que, si se dividía la materia en trozos cada vez más pequeños, debería llegarse a una porción que ya no podría
Como esta formada la materia? Demócrito, filósofo griego que vivió en el siglo IV a. C. propuso que, si se dividía la materia en trozos cada vez más pequeños, debería llegarse a una porción que ya no podría
LA RIOJA / JUNIO 04. LOGSE / FÍSICA / EXAMEN COMPLETO
 LA RIOJA / JUNIO 0. LOGSE / FÍSICA / EXAMEN COMPLEO EXAMEN COMPLEO El alumno elegirá una sola de las opciones de problemas, así como cuatro de las cinco Cuestiones propuestas. No deben resolverse problemas
LA RIOJA / JUNIO 0. LOGSE / FÍSICA / EXAMEN COMPLEO EXAMEN COMPLEO El alumno elegirá una sola de las opciones de problemas, así como cuatro de las cinco Cuestiones propuestas. No deben resolverse problemas
ESPECTROFOTOMETRÍA UV-VISIBLE. Mª Luisa Fernández de Córdova Universidad de Jaén
 ESPECTROFOTOMETRÍA UV-VISIBLE 1. Propiedades de la luz 2. Absorción de luz 2.1. Fenómeno de la absorción 2.2. Espectros de absorción molecular 2.3. Tipos de transiciones electrónicas 3. Ley de Lambert-Beer
ESPECTROFOTOMETRÍA UV-VISIBLE 1. Propiedades de la luz 2. Absorción de luz 2.1. Fenómeno de la absorción 2.2. Espectros de absorción molecular 2.3. Tipos de transiciones electrónicas 3. Ley de Lambert-Beer
PAAU (LOXSE) Setembro 2002
 PAAU (LOXSE) Setembro 00 Código: FÍSICA Elegir y desarrollar una de las dos opciones propuestas. Puntuación máxima: Problemas 6 puntos (1,5 cada apartado) Cuestiones 4 puntos (1 cada cuestión, teórica
PAAU (LOXSE) Setembro 00 Código: FÍSICA Elegir y desarrollar una de las dos opciones propuestas. Puntuación máxima: Problemas 6 puntos (1,5 cada apartado) Cuestiones 4 puntos (1 cada cuestión, teórica
GALICIA/ JUNIO 01. LOGSE / FÍSICA / EXAMEN COMPLETO
 Desarrollar una de las dos opciones propuestas. Cada problema puntúa 3 (1,5 cada apartado) y cada cuestión teórica o práctica 1. OPCIÓN 1 Un cilindro macizo y homogéneo de 3 kg de masa y 0,1 m de radio
Desarrollar una de las dos opciones propuestas. Cada problema puntúa 3 (1,5 cada apartado) y cada cuestión teórica o práctica 1. OPCIÓN 1 Un cilindro macizo y homogéneo de 3 kg de masa y 0,1 m de radio
PROGRAMA DE ASIGNATURA. ASIGNATURA: Física Experimental V AÑO: 2013 CARÁCTER: Obligatoria CARRERA/s: Licenciatura en Física
 PROGRAMA DE ASIGNATURA ASIGNATURA: Física Experimental V AÑO: 2013 CARÁCTER: Obligatoria CARRERA/s: Licenciatura en Física RÉGIMEN: cuatrimestral CARGA HORARIA: 120 hs. UBICACIÓN en la CARRERA: cuarto
PROGRAMA DE ASIGNATURA ASIGNATURA: Física Experimental V AÑO: 2013 CARÁCTER: Obligatoria CARRERA/s: Licenciatura en Física RÉGIMEN: cuatrimestral CARGA HORARIA: 120 hs. UBICACIÓN en la CARRERA: cuarto
Thompson (1898) Rutherford (1911) Bohr (1913) Schrödinger (1926) NUMEROS CUANTICOS
 Thompson (1898) Modelo Atómico Rutherford (1911) Bohr (1913) Propiedad corpuscular de las onda (PLANCK) Propiedad ondulatoria de las partículas (De Broglie) Schrödinger (1926) Números cuánticos 1 NUMEROS
Thompson (1898) Modelo Atómico Rutherford (1911) Bohr (1913) Propiedad corpuscular de las onda (PLANCK) Propiedad ondulatoria de las partículas (De Broglie) Schrödinger (1926) Números cuánticos 1 NUMEROS
EL ÁTOMO. Se supuso que estas partículas deberían estar en todos los átomos. Thomson las llamó electrones.
 ANTECEDENTES HISTÓRICOS. () EL ÁTOMO Leucipo y Demócrito. Proponen la Discontinuidad de la materia. Dalton. Formula la primera Teoría atómica. Volta, Davy, Faraday, Berzelius, descubren la Naturaleza eléctrica
ANTECEDENTES HISTÓRICOS. () EL ÁTOMO Leucipo y Demócrito. Proponen la Discontinuidad de la materia. Dalton. Formula la primera Teoría atómica. Volta, Davy, Faraday, Berzelius, descubren la Naturaleza eléctrica
Diagrama de correlación de enlaces moleculares Antienlace : rojo 1s similar a 2s
 Redes Cristalinas Ciencia de Materiales Ing. en Mecatrónica Otoño 2009 Lilia Meza Montes-IFUAP Diagrama de correlación de enlaces moleculares Antienlace : rojo 1s similar a 2s Sólidos cristalinos y amorfos
Redes Cristalinas Ciencia de Materiales Ing. en Mecatrónica Otoño 2009 Lilia Meza Montes-IFUAP Diagrama de correlación de enlaces moleculares Antienlace : rojo 1s similar a 2s Sólidos cristalinos y amorfos
