Cabergolina 05 feb 2013 CDS Version 13.0 PREPARADO POR PFIZER INC PFIZER VENEZUELA, S.A. Fecha de vigencia de la ficha técnica: 05 de febrero de 2013
|
|
|
- Miguel Gil Alcaraz
- hace 7 años
- Vistas:
Transcripción
1 PREPARADO POR PFIZER INC PFIZER VENEZUELA, S.A. Fecha de vigencia de la ficha técnica: 05 de febrero de 2013 Fecha de la ficha técnica sustituida: 23 de julio de 2008 CABERGOLINA DOCUMENTO LOCAL DE PRODUCTO VERSION
2 1. NOMBRE DEL MEDICAMENTO DOSTINEX 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Disponible en comprimidos que contienen 0.5 mg de cabergolina cada uno 3. FORMA FARMACÉUTICA Comprimidos 4. DATOS CLÍNICOS 4.1 Indicaciones terapéuticas Inhibición/supresión de la lactancia fisiológica: DOSTINEX está indicado para 1) la inhibición de la lactancia fisiológica inmediatamente después del parto y 2) la supresión de la lactancia establecida. Tratamiento de trastornos hiperprolactinémicos (Consulte las secciones 4.3 Contraindicaciones y 4.4 Advertencias y precauciones especiales de uso - Tratamiento a largo plazo). DOSTINEX está indicado para el tratamiento de trastornos hiperprolactinémicos, lo que incluye disfunciones como amenorrea, oligomenorrea, anovulación y galactorrea. DOSTINEX también está indicado para pacientes con adenomas de hipófisis secretores de la hormona prolactina (micro y macroprolactinomas), hiperprolactinemia idiopática o síndrome de la silla turca vacía con hiperprolactinemia asociada, que representan las patologías básicas subyacentes que contribuyen a las manifestaciones clínicas descritas anteriormente. 4.2 Posología y vía de administración General: Los comprimidos DOSTINEX se administran por vía oral. Debido a que la tolerabilidad de los agentes dopaminérgicos se incrementa al ingerir alimentos, se recomienda que DOSTINEX se administre con las comidas. En pacientes que no toleran los medicamentos dopaminérgicos, se puede reducir la probabilidad de que sufran eventos adversos si se comienza el tratamiento con dosis reducidas de DOSTINEX (por ej., 0.25 mg una vez por semana) y, luego se, incrementan gradualmente hasta alcanzar la posología terapéutica. En caso de que los eventos 2
3 adversos sean graves o persistan, la reducción temporal de la posología seguida de un incremento más gradual (por ej., incrementos de 0.25 mg por semana cada dos semanas) puede aumentar la tolerabilidad. Inhibición/supresión de la lactancia fisiológica: Para inhibir la lactancia: la dosis recomendada es de 1 mg (dos comprimidos de 0.5 mg) en una única dosis el primer día posterior al parto. Para suprimir la lactancia establecida: la posología recomendada es de 0.25 mg (medio comprimido de 0.5 mg) cada 12 horas durante 2 días (1 mg en total). (Consulte la sección 4.4 Advertencias y precauciones especiales de uso Inhibición/supresión de la lactancia fisiológica). Tratamiento de trastornos hiperprolactinémicos: (Consulte las secciones 4.3 Contraindicaciones y 4.4 Advertencias y precauciones especiales de uso - Tratamiento a largo plazo). La posología inicial recomendada de DOSTINEX es de 0.5 mg por semana administrados en una o dos dosis por semana (medio comprimido de 0.5 mg; por ej., lunes y jueves). La dosis semanal deberá incrementarse gradualmente, preferentemente mediante la adición de 0.5 mg por semana a intervalos mensuales hasta lograr una respuesta óptima al tratamiento. Generalmente, la posología terapéutica es de 1 mg por semana, pero puede variar de 0.25 mg a 2 mg por semana. Se han administrado posologías de hasta 4.5 mg por semana en pacientes con trastornos hiperprolactinémicos. (Consulte la sección 4.4 Advertencias y precauciones especiales de uso Tratamiento de trastornos hiperprolactinémicos). La dosis semanal puede administrarse en una sola dosis o puede dividirse en dos o más dosis por semana, según la tolerabilidad del paciente. Se aconseja la división de la dosis semanal en varias dosis cuando es superior a 1 mg por semana. Durante la incrementación de la dosis, se debe evaluar a los pacientes para determinar la mínima dosis efectiva que logra el efecto terapéutico. Se aconseja verificar los niveles séricos de prolactina a intervalos mensuales ya que una vez que se alcanza la posología terapéutica, se observa una normalización de los niveles séricos de prolactina en un plazo de 2 a 4 semanas. Al interrumpir la administración de DOSTINEX, suele observarse la recurrencia de hiperprolactinemia. Sin embargo, en algunos pacientes se ha observado la supresión permanente de los niveles de prolactina durante varios meses. En la mayoría de las mujeres, los ciclos ovulatorios persisten durante al menos 6 meses luego de interrumpir la administración de DOSTINEX. Pacientes con insuficiencia hepática grave: 3
4 Se deben considerar dosis más bajas de DOSTINEX en pacientes con insuficiencia hepática grave. (Consulte la sección 4.4 Advertencias y precauciones especiales de uso Insuficiencia hepática). Niños: No se ha establecido la seguridad y eficacia en pacientes menores de 16 años. Ancianos: No se ha estudiado formalmente la administración de DOSTINEX en ancianos con trastornos hiperprolactinémicos. 4.3 Contraindicaciones Hipersensibilidad a la cabergolina, a cualquier otro componente del medicamento o a cualquier alcaloide ergotínico. Antecedentes de trastornos fibróticos pulmonares, pericárdicos y retroperitoneales. (Consulte la sección 4.4 Advertencias y precauciones especiales de uso Fibrosis/valvulopatía). Tratamiento a largo plazo: Evidencia anatómica de la valvulopatía cardíaca de cualquier válvula como lo determina el ecocardiograma pretratamiento mostrando el engrosamiento de la valva de las válvulas, restricción de válvulas, estenosis-restricción mixta de las válvulas. (Consulte la sección 4.4 Advertencias y precauciones especiales de uso Fibrosis/valvulopatía). 4.4 Advertencias y precauciones especiales de uso General: Como con otros derivados de ergot, deben tomarse precauciones cuando se administra DOSTINEX a pacientes que padecen enfermedad cardiovascular grave, síndrome de Raymund, úlcera péptica o hemorragia gastrointestinal, o con antecedentes de trastornos mentales graves, particularmente psicóticos. Insuficiencia hepática: Deben considerarse dosis más bajas para pacientes con insuficiencia hepática grave que hayan recibido tratamiento prolongado con DOSTINEX. En comparación con los voluntarios normales y con aquellos con menor grado de insuficiencia hepática, se ha observado un incremento de AUC en pacientes con insuficiencia hepática grave (clasificación de Child-Pugh, clase C) que recibieron una única dosis de 1 mg. 4
5 Hipotensión postural: Se puede producir hipotensión postural luego de la administración de cabergolina. Debe tenerse cuidado al administrar DOSTINEX en concomitancia con otros medicamentos que se sabe que disminuyen la presión arterial. Fibrosis/valvulopatía: Como con otros derivados de ergot, se han notificado derrames pleurales/fibrosis pulmonar y valvulopatía luego de la administración prolongada de cabergolina. Algunos de los informes eran de pacientes tratados anteriormente con agonistas dopaminérgicos ergóticos. Por consiguiente, DOSTINEX no debe administrarse en pacientes con antecedentes, signos actuales o síntomas clínicos de trastornos respiratorios o cardíacos relacionados con el tejido fibrótico. Se ha determinado que la velocidad de sedimentación globular (VSG) aumenta de manera anormal en asociación con derrames pleurales/fibrosis. Se recomienda el examen de rayos X de pecho en los casos en los que la inexplicable VSG aumente a valores anormales. Las mediciones de la creatinina sérica también se pueden utilizar para ayudar a diagnosticar el trastorno fibrótico. Luego del diagnóstico de derrames pleurales/fibrosis pulmonar o valvulopatía, se ha notificado que la interrupción de la administración de cabergolina ha resultado en una mejoría de los signos y síntomas. (Consulte la sección 4.3 Contraindicaciones). Los resultados de un extenso estudio de cohorte retrospectivo en varios países europeos entre personas enfermas de Parkinson demostraron que al ser comparadas con personas recientemente tratadas con levodopa, las personas que habían cambiado la pergolida por cabergolina presentaron mayores riesgos de sufrir regurgitación valvular cardíaca (RVC) que los recientemente tratados con cabergolina que nunca habían consumido pergolida. (Consulte las secciones 4.8 Reacciones adversas y 5.1 Propiedades farmacodinámicas). Tratamiento a largo plazo: Antes de iniciar el tratamiento a largo plazo: Todos los pacientes deben someterse a una evaluación cardiovascular, incluido un ecocardiograma para evaluar la presencia potencial de la enfermedad valvular asintomática. También es adecuado realizar investigaciones iniciales de la velocidad de sedimentación globular u otros marcadores inflamatorios, función pulmonar/rayos X de pecho y función renal antes de comenzar la terapia. En pacientes con insuficiencia valvular, se desconoce si el tratamiento con cabergolina puede empeorar la enfermedad subyacente. Si se detecta la enfermedad valvular fibrótica, el paciente no debe tratarse con cabergolina (consulte la sección 4.3 Contraindicaciones). Durante el tratamiento a largo plazo: 5
6 Los trastornos fibróticos pueden tener un inicio insidioso y los pacientes deben ser monitoreados regularmente por posibles manifestaciones de fibrosis progresiva. Por consiguiente, durante el tratamiento, se le debe prestar atención a los signos y síntomas de: Enfermedad pleuropulmonar tales como disnea, dificultad para respirar, tos permanente o dolor de pecho. Insuficiencia renal u obstrucción vascular ureteral/abdominal que pueden ocurrir con dolor lumbar/en el costado y edema de extremidades inferiores como así también cualquier sensibilidad o masa abdominal posible que puede indicar fibrosis retroperitoneal. Insuficiencia cardíaca: los casos de fibrosis valvular y pericárdica han solido manifestarse como insuficiencia cardíaca. Por consiguiente, se debe descartar la fibrosis valvular (y pericarditis constrictiva) si ocurren tales síntomas. Resulta esencial el monitoreo de diagnóstico clínico para el desarrollo de trastornos fibróticos, según sea adecuado. Después del comienzo del tratamiento, el primer ecocardiograma debe ocurrir en un plazo de 3 a 6 meses; posteriormente, la frecuencia del monitoreo ecocardiográfico debe determinarse por una evaluación clínica individual adecuada con un énfasis particular en los signos y síntomas antes mencionados, pero debe ocurrir como mínimo cada 6 a 12 meses. La cabergolina se debe discontinuar si un ecocardiograma revela una insuficiencia valvular nueva o empeorada, restricción valvular o engrosamiento de la valva de las válvulas (consulte la sección 4.3 Contraindicaciones). La necesidad de otro monitoreo clínico (p. ej.: examen físico con auscultación cardíaca, rayos X, tomografía computada) se debe determinar en forma individual. Se deben llevar a cabo investigaciones adecuadas adicionales tales como velocidad de sedimentación globular y mediciones de la creatinina sérica si son necesarias para respaldar el diagnóstico de un trastorno fibrótico. Somnolencia/inicio repentino del sueño: La cabergolina ha sido vinculada con la somnolencia. Los agonistas dopaminérgicos pueden asociarse con episodios de inicio repentino del sueño en pacientes que padecen Parkinson. Es posible considerar la disminución de la posología o la suspensión del tratamiento. (Consulte la sección 4.7 Efectos sobre la capacidad para conducir y usar máquinas). Inhibición/supresión de la lactancia fisiológica: Como con otros derivados de ergot, no debe administrarse DOSTINEX a mujeres con hipertensión inducida por el embarazo, por ejemplo, preeclampsia o hipertensión 6
7 postparto, a menos que se considere que el beneficio potencial supera la posibilidad de riesgo. En mujeres lactantes tratadas para la supresión de la lactancia establecida no debe excederse una única dosis de 0.25 mg de DOSTINEX para evitar una posible hipotensión postural. (Consulte la sección 4.2 Posología y método de administración Inhibición/supresión de la lactancia fisiológica y el inciso anterior: Hipotensión postural). Tratamiento de trastornos hiperprolactinémicos: Se indica una evaluación completa de la glándula pituitaria antes de iniciar el tratamiento con DOSTINEX. DOSTINEX restablece la ovulación y fertilidad en mujeres con hipogonadismo hiperprolactinémico. Debido a que el embarazo puede ocurrir antes de la reiniciación de la menstruación, se recomienda hacer una prueba de embarazo al menos cada 4 semanas durante el período de amenorrea y, luego de que se reinicia la menstruación, cada vez que el período menstrual se retrase más de 3 días. Debe aconsejarse a las mujeres que deseen evitar un embarazo que usen un método de anticoncepción mecánica durante el tratamiento con DOSTINEX y luego de la interrupción de este hasta que se repita la anovulación. Como medida preventiva, las mujeres que queden embarazadas deben ser controladas para detectar signos de agrandamiento de la glándula pituitaria ya que durante la gestación se pueden expandir los tumores pituitarios preexistentes. Psiquiátrico: Se han informado trastornos de control de impulsos tales como el juego patológico, aumento de la líbido e hipersexualidad en pacientes tratados con agonistas dopaminérgicos, incluido DOSTINEX. Esto generalmente ha sido reversible luego de una reducción de la dosis o discontinuación del tratamiento. 4.5 Interacciones medicamentosas y de otro género No hay información disponible sobre la interacción entre la cabergolina y otros alcaloides ergotínicos. Por ende, no se recomienda el uso concomitante de estos medicamentos durante el tratamiento prolongado con DOSTINEX. Debido a que DOSTINEX produce el efecto terapéutico mediante la estimulación directa de los receptores dopaminérgicos, no debe administrarse en concomitancia con medicamentos antagonistas de la dopamina (por ejemplo, fenotiazinas, butirofenonas, tioxantenos, metoclopramida) ya que podrían reducir el efecto hipoprolactinémico de DOSTINEX. Como con otros derivados de ergot, DOSTINEX no debe administrarse con antibióticos macrólidos (como la eritromicina) debido al aumento de la biodisponibilidad sistémica de la cabergolina. 7
8 4.6 Embarazo y lactancia Los estudios con cabergolina en animales no han demostrado efectos teratogénicos o efectos en el funcionamiento reproductivo en su totalidad. Sin embargo, no existen estudios adecuados y debidamente controlados en mujeres embarazadas. DOSTINEX debe administrarse durante el embarazo solo si es claramente necesario. Si se produce la concepción durante el tratamiento con DOSTINEX, debe considerarse la interrupción del tratamiento, luego de una evaluación minuciosa de los riesgos y beneficios para la madre y el feto. Debe evitarse el embarazo durante al menos un mes luego de la interrupción del tratamiento con DOSTINEX debido a la prolongada semivida del medicamento y a la cantidad limitada de información en cuanto a la exposición en el útero, aunque el consumo de DOSTINEX entre 0.5 y 2 mg por semana para tratar trastornos hiperprolactinémicos no parece estar asociado a un aumento del riesgo de aborto, nacimiento prematuro, embarazo múltiple o anomalías congénitas. (Consulte la sección 4.4 Advertencias y precauciones especiales de uso Tratamiento de trastornos hiperprolactinémicos). En las ratas, la cabergolina o sus metabolitos se eliminan en la leche. No hay información sobre la eliminación en la leche materna de los seres humanos. Sin embargo, se aconseja que las madres no amamanten en caso de que DOSTINEX no haya producido la inhibición/supresión de la lactancia. Debido a que impide la lactancia, DOSTINEX no se debe administrar a mujeres con trastornos hiperprolactinémicos que deseen amamantar a sus hijos. 4.7 Efectos sobre la capacidad para conducir y usar máquinas Se debe informar a los pacientes tratados con cabergolina y que experimenten somnolencia que deben abstenerse de conducir o realizar actividades en las que la falta de concentración pueda ponerlos a ellos o a otras personas en peligro de lesiones o muerte (por ej. al operar máquinas), a menos que los pacientes hayan superado tales situaciones de somnolencia. (Consulte la sección 4.4 Advertencias especiales y precauciones de uso Somnolencia/inicio repentino del sueño). 4.8 Reacciones adversas Inhibición/supresión de la lactancia: Aproximadamente el 14% de las mujeres tratadas en ensayos clínicos con una única dosis de 1 mg de DOSTINEX para la inhibición de la lactancia fisiológica ha informado al menos un evento adverso. Los eventos adversos notificados fueron transitorios y de leves a moderados en gravedad. Los eventos adversos más frecuentes fueron mareos/vértigo, dolor de cabeza, náuseas y dolor abdominal. También se notificaron palpitaciones, dolor epigástrico, somnolencia (consulte la sección 4.4 Advertencias y precauciones especiales de uso Somnolencia/inicio repentino del sueño y la sección 4.7 Efectos 8
9 sobre la capacidad para conducir y usar máquinas), epistaxis y hemianopsia transitoria. Puede producirse una disminución asintomática de la presión arterial ( 20 mmhg de presión sistólica y 10 mmhg de diastólica) durante los primeros 3 a 4 días posteriores al parto. Se han observado eventos adversos en aproximadamente 14% de las mujeres en edad lactante tratadas con 0.25 mg de DOSTINEX cada 12 horas durante 2 días para la supresión de la lactancia. La mayoría de los eventos adversos fueron transitorios y de leves a moderados en gravedad. Los eventos adversos más frecuentes fueron mareos/vértigo, dolor de cabeza, náuseas, somnolencia (consulte la sección 4.4 Advertencias y precauciones especiales de uso Somnolencia/inicio repentino del sueño y la sección 4.7 Efectos sobre la capacidad para conducir y usar máquinas) y dolor abdominal. También se notificaron vómitos, síncope, astenia y sofocos. Trastornos hiperprolactinémicos: La información obtenida en un ensayo clínico controlado de 6 meses de tratamiento, con dosis de entre 1 y 2 mg por semana administrados en dos dosis semanales, indica un 68% de incidencia de eventos adversos durante el tratamiento con DOSTINEX. Generalmente, los eventos adversos fueron de leves a moderados en gravedad, con apariciones durante las primeras dos semanas de tratamiento principalmente. La mayoría desapareció con la continuación del tratamiento. El 14% de los pacientes notificaron haber sufrido eventos adversos graves al menos una vez durante el tratamiento. Se interrumpió el tratamiento debido a los eventos adversos en, aproximadamente, el 3% de los pacientes. A menudo, los eventos adversos disminuyeron normalmente a los pocos días, luego de la interrupción del tratamiento con DOSTINEX. Los eventos adversos más comunes (de mayor a menor frecuencia) fueron: náuseas, dolor de cabeza, mareos/vértigo, dolor abdominal/dispepsia/gastritis, astenia/cansancio, estreñimiento, vómitos, dolor en las mamas, sofocos, depresión y parestesia. General: Generalmente, los eventos adversos están relacionados con la dosis. (Consulte la sección 4.2 Posología y método de administración: General). Generalmente, DOSTINEX produce un efecto hipotensor en pacientes con terapia prolongada. Sin embargo, raramente se ha notificado hipotensión postural (consulte la sección 4.4 Advertencias y precauciones especiales de uso: También se notificaron hipotensión postural e Inhibición/supresión de la lactancia fisiológica) o desmayos. Al ser derivado de ergot, DOSTINEX puede actuar como vasoconstrictor. Se han notificado vasoespasmos digitales y calambres en las piernas. 9
10 Son poco frecuentes las alteraciones en las pruebas estándar de laboratorio durante el tratamiento prolongado con DOSTINEX. Se ha observado un descenso en los valores de hemoglobina en mujeres amenorréicas durante los primeros meses luego de la reanudación de la menstruación. Seguimiento posterior a la comercialización: Se han notificado los siguientes eventos relacionados con la cabergolina: agresión, alopecía, aumento de las creatinfosfoquinasas, delirios, disnea, edema, fibrosis, función hepática anormal, reacción de hipersensibilidad, trastornos de control de impulsos tales como hipersexualidad, aumento de la líbido y juego patológico, pruebas de función hepática anormales, trastornos psicóticos, erupción, alteraciones respiratorias, insuficiencia respiratoria y valvulopatía. (Consulte la sección 4.3 Contraindicaciones y sección 4.4 Advertencias y precauciones especiales de uso Fibrosis/Valvulopatía y Psiquiátrico). La prevalencia de insuficiencia valvular asintomática es significativamente mayor que aquella de los agonistas dopaminérgicos no derivados del cornezuelo. (Consulte la sección 4.3 Contraindicaciones y sección 4.4 Advertencias y precauciones especiales de uso Fibrosis/Valvulopatía). 4.9 Sobredosis Es posible que los síntomas de sobredosis sean aquellos de sobrestimulación de los receptores dopaminérgicos; por ejemplo, náuseas, vómitos, malestar gástrico, hipotensión postural, confusión/psicosis o alucinaciones. Deben tomarse medidas de respaldo para eliminar el medicamento sin absorber y mantener la presión arterial, si es necesario. Además, se aconseja la administración de medicamentos antagonistas de la dopamina. 5. PROPIEDADES FARMACOLÓGICAS 5.1 Propiedades farmacodinámicas DOSTINEX es un derivado de ergot dopaminérgico provisto de una fuerte y prolongada capacidad de reducir la prolactina (PRL). Actúa mediante la estimulación directa de los receptores D 2 de la dopamina de las células lactotropas pituitarias. De esta manera, inhibe la secreción de la PRL. En las ratas, el compuesto disminuye la secreción de PRL con dosis orales de 3 a 25 mcg/kg e in vitro con una concentración de 45 pg/ml. Además, DOSTINEX produce un efecto dopaminérgico central mediante la estimulación del receptor D 2 con dosis orales mayores que las que reducen efectivamente los niveles séricos de PRL. La larga duración del efecto reductor de la PRL del DOSTINEX probablemente se deba a su permanencia prolongada en el órgano diana conforme lo sugiere la eliminación lenta de la radioactividad total proveniente de la pituitaria luego de una única dosis oral en las ratas (t ½ de aproximadamente 60 horas). 10
11 Se han estudiado los efectos farmacodinámicos de DOSTINEX en voluntarios saludables, mujeres con fiebre puerperal y pacientes con trastornos hiperprolactinémicos. Luego de la administración de una única dosis de DOSTINEX (de 0.3 a 1.5 mg), se ha observado una disminución significativa de los niveles séricos de PRL en los grupos estudiados. El efecto es rápido (en un plazo de 3 horas posteriores a la administración) y prolongado (de 7 a 28 días en los voluntarios saludables y pacientes con trastornos hiperprolactinémicos, y de 14 a 21 días en las mujeres con fiebre puerperal). La disminución de la PRL depende de la dosis tanto en términos de la magnitud del efecto como de la duración de la acción. En cuanto a los efectos de DOSTINEX en el sistema endocrino no relacionados con el efecto antiprolactinémico, la información disponible en humanos confirma los hallazgos experimentales en animales que indican que el compuesto evaluado presenta una acción selectiva y que no produce efectos en la secreción basal de otras hormonas pituitarias o del cortisol. Los efectos farmacodinámicos de DOSTINEX no relacionados con el efecto del tratamiento solo se asocian a la disminución de la presión arterial. El máximo efecto hipotensor de DOSTINEX con una única dosis generalmente ocurre durante las primeras 6 horas luego de la ingesta del medicamento y depende de la dosis tanto en términos del límite de disminución como de la frecuencia. Fibrosis y valvulopatía Se realizó un estudio de cohorte retrospectivo en varios países utilizando registros de práctica general y sistemas de conexión de registros en el Reino Unido, Italia y Holanda para evaluar la asociación entre el nuevo uso de agonistas dopaminérgicos incluida la cabergolina (n = 27,812) para la enfermedad de Parkinson, la hiperprolactinemia, la insuficiencia valvular cardíaca (CVR), otras fibrosis y otros eventos cardiopulmonares en un máximo de 12 años de seguimiento. En el análisis limitado a personas con hiperprolactinemia tratados con agonistas dopaminérgicos (n=8,386), cuando se los compara con el no uso (n=15,147), las personas expuestas a la cabergolina no tuvieron un riesgo elevado de CVR. (Consulte la sección 4.4 Advertencias y precauciones especiales de uso Fibrosis/Valvulopatía y sección 4.8 Reacciones adversas). 5.2 Propiedades farmacodinámicas Se han estudiado los perfiles farmacocinético y metabólico de DOSTINEX en voluntarios saludables de ambos sexos y en pacientes mujeres con trastornos hiperprolactinémicos. Luego de la administración oral del compuesto etiquetado, la radioactividad se absorbió rápidamente en el tracto gastrointestinal y se observó que el pico de radioactividad en plasma fue entre 0.5 y 4 horas. Diez días después de la administración, se recuperó entre el 18 y el 72% de la dosis radioactiva en orina y heces, respectivamente. El medicamento intacto en orina representó entre el 2 y 3% de la dosis. 11
12 En la orina, el principal metabolito identificado fue el 6-alil-8 -carboxi-ergolina, que representó entre el 4 y 6% de la dosis. En la orina, se identificaron tres metabolitos adicionales, los cuales representaron en total menos del 3% de la dosis. Se ha determinado que los metabolitos son mucho menos potentes que DOSTINEX en la inhibición in vitro de la secreción de prolactina. La biotransformación de DOSTINEX también se estudió en el plasma de los voluntarios varones saludables tratados con [ 14 C]- cabergolina: se demostró una biotransformación rápida y extensa de la cabergolina. La baja excreción urinaria de DOSTINEX intacto fue confirmada también en estudios con el producto no radioactivo. La semivida de eliminación de DOSTINEX, estimada con las velocidades de excreción urinaria, es amplia (de 63 a 68 horas en voluntarios saludables, mediante radioinmunoensayo, y de 79 a 115 horas en pacientes con trastornos hiperprolactinémicos, mediante el método de cromatografía líquida de alta resolución). Con base en la semivida de eliminación, el estado de equilibrio se debe alcanzar después de 4 semanas, como fue confirmado por los niveles promedios de los picos plasmáticos de DOSTINEX, obtenidos después de una dosis única (37 8 pg/ml) y después de una pauta posológica múltiple durante 4 semanas ( pg/ml). Los estudios in vitro mostraron que el medicamento en concentraciones de 0.1 a 10 ng/ml se encuentra unido a las proteínas plasmáticas entre un 41 y 42%. Los alimentos no parecen afectar la absorción y disposición de DOSTINEX. 5.3 Datos preclínicos de seguridad Casi todos los hallazgos en la serie de estudios de seguridad preclínicos son una consecuencia de los efectos dopaminérgicos centrales o de la inhibición prolongada de la PRL en especies (roedores) que tienen una fisiología hormonal específica diferente a la del ser humano. Los estudios de seguridad preclínicos de DOSTINEX indican un margen de seguridad amplio para este compuesto en roedores y en monos, así como la carencia de potencial teratogénico, mutagénico o carcinogénico. 6. DATOS FARMACÉUTICOS 6.1 Lista de excipientes Leucina. Llactosa anhidra. 6.2 Incompatibilidades No se aplica. 6.3 Vida útil 12
13 24 meses 6.4 Precauciones especiales para el almacenamiento Mantener a 25 C 6.5 Naturaleza y contenido del envase La caja de cartón contiene un frasco de vidrio color ámbar con tapa a rosca 6.6 Precauciones especiales para el desecho de los medicamentos consumidos o los materiales residuales que provienen de dichos medicamentos y otras manipulaciones de los medicamentos No se aplica. 13
ANEXO III MODIFICACIONES DEL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Y DEL PROSPECTO
 ANEXO III MODIFICACIONES DEL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Y DEL PROSPECTO 42 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO DE LOS MEDICAMENTOS QUE CONTENGAN CABERGOLINA 4.2 Posología y forma
ANEXO III MODIFICACIONES DEL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Y DEL PROSPECTO 42 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO DE LOS MEDICAMENTOS QUE CONTENGAN CABERGOLINA 4.2 Posología y forma
FOLLETO DE INFORMACIÓN AL PROFESIONAL. DOSTINEX Comprimidos 0.5 mg (Cabergolina)
 FOLLETO DE INFORMACIÓN AL PROFESIONAL DOSTINEX Comprimidos 0.5 mg (Cabergolina) 1. NOMBRE DEL MEDICAMENTO DOSTINEX 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Los comprimidos de DOSTINEX contienen 0,5 mg
FOLLETO DE INFORMACIÓN AL PROFESIONAL DOSTINEX Comprimidos 0.5 mg (Cabergolina) 1. NOMBRE DEL MEDICAMENTO DOSTINEX 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Los comprimidos de DOSTINEX contienen 0,5 mg
DOSTINEX 0.5 mg (Cabergolina) Tabletas
 DOSTINEX 0.5 mg (Cabergolina) Tabletas 1. NOMBRE DEL PRODUCTO FARMACÉUTICO DOSTINEX 0.5 mg Tabletas 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada tableta de DOSTINEX contiene: 0.5 mg de cabergolina Excipiente(s)
DOSTINEX 0.5 mg (Cabergolina) Tabletas 1. NOMBRE DEL PRODUCTO FARMACÉUTICO DOSTINEX 0.5 mg Tabletas 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada tableta de DOSTINEX contiene: 0.5 mg de cabergolina Excipiente(s)
FICHA TÉCNICA. Cada comprimido contiene 0,5 mg de cabergolina. Excipientes con efecto conocido: cada comprimido contiene 75,85 mg de lactosa anhidra.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Dostinex 0,5 mg comprimidos. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 0,5 mg de cabergolina. Excipientes con efecto conocido: cada comprimido
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Dostinex 0,5 mg comprimidos. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 0,5 mg de cabergolina. Excipientes con efecto conocido: cada comprimido
Ministerio de Salud Secretaría de Política, Regulación y Relaciones Sanitarias A.N.M.A.T.
 BUENOS AIRES, 07 Sep 2007 VISTO la Resolución del ex Ministerio de Salud y Acción Social N 706/93, la Disposición N 5904/96, el Expediente N 1-0047-0000-014095-07-9 del registro de esta Administración
BUENOS AIRES, 07 Sep 2007 VISTO la Resolución del ex Ministerio de Salud y Acción Social N 706/93, la Disposición N 5904/96, el Expediente N 1-0047-0000-014095-07-9 del registro de esta Administración
ANEXO III MODIFICACIONES DEL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Y DEL PROSPECTO
 ANEXO III MODIFICACIONES DEL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Y DEL PROSPECTO 25 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO DE LOS MEDICAMENTOS QUE CONTENGAN BROMOCRIPTINA 4.2 Posología y forma
ANEXO III MODIFICACIONES DEL RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO Y DEL PROSPECTO 25 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO DE LOS MEDICAMENTOS QUE CONTENGAN BROMOCRIPTINA 4.2 Posología y forma
Hipersensibilidad conocida a penciclovir, famciclovir o a los otros componentes de la formulación, por ejemplo propilenglicol.
 1. NOMBRE DEL MEDICAMENTO Penciclovir Beecham bomba dosificadora Penciclovir Beecham crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio activo: Penciclovir al 1% DCI: penciclovir 3. FORMA FARMACÉUTICA
1. NOMBRE DEL MEDICAMENTO Penciclovir Beecham bomba dosificadora Penciclovir Beecham crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio activo: Penciclovir al 1% DCI: penciclovir 3. FORMA FARMACÉUTICA
LABORATORIOS NORMON, S.A. AMBROXOL NORMON 15 mg/5 ml Jarabe EFG
 1. NOMBRE DEL MEDICAMENTO 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada 5 ml de jarabe contienen: AMBROXOL (D.C.I.) hidrocloruro 15 mg Excipientes, ver apartado 6.1. 3. FORMA FARMACEUTICA Jarabe. 4. DATOS
1. NOMBRE DEL MEDICAMENTO 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada 5 ml de jarabe contienen: AMBROXOL (D.C.I.) hidrocloruro 15 mg Excipientes, ver apartado 6.1. 3. FORMA FARMACEUTICA Jarabe. 4. DATOS
INFORMACION PARA PRESCRIBIR AMPLIA
 INFORMACION PARA PRESCRIBIR AMPLIA 1. Nombre Comercial: ANUAR ASF 2. Nombre Genérico: CABERGOLINA 3. Forma Farmacéutica y Formulación: Comprimidos. Cada comprimido contiene: Cabergolina... 0.5 mg Excipiente
INFORMACION PARA PRESCRIBIR AMPLIA 1. Nombre Comercial: ANUAR ASF 2. Nombre Genérico: CABERGOLINA 3. Forma Farmacéutica y Formulación: Comprimidos. Cada comprimido contiene: Cabergolina... 0.5 mg Excipiente
PROSPECTO: INFORMACIÓN PARA EL USUARIO. Cabergolina Teva 0,5 mg comprimidos EFG Cabergolina
 PROSPECTO: INFORMACIÓN PARA EL USUARIO Cabergolina Teva 0,5 mg comprimidos EFG Cabergolina Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento, porque contiene información importante
PROSPECTO: INFORMACIÓN PARA EL USUARIO Cabergolina Teva 0,5 mg comprimidos EFG Cabergolina Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento, porque contiene información importante
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. MAGNESIUM PYRE 64 mg comprimidos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO MAGNESIUM PYRE 64 mg comprimidos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 64 mg de magnesio (en forma de 550 mg de cloruro de magnesio,
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO MAGNESIUM PYRE 64 mg comprimidos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 64 mg de magnesio (en forma de 550 mg de cloruro de magnesio,
Alivio de los sofocos que aparecen durante la menopausia como consecuencia de la deprivación estrogénica.
 1. NOMBRE DEL MEDICAMENTO Normosoy 40 mg cápsulas duras 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada cápsula contiene: 290 mg de extracto etanólico 85% V/V seco de semillas de Glycine max (L.) Merr.
1. NOMBRE DEL MEDICAMENTO Normosoy 40 mg cápsulas duras 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada cápsula contiene: 290 mg de extracto etanólico 85% V/V seco de semillas de Glycine max (L.) Merr.
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 ACICLOVIR 5% Crema CREMA ANTIVIRAL Página 1 ACICLOVIR 5% Crema Crema Principio Activo Aciclovir Excipientes necesarios
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 ACICLOVIR 5% Crema CREMA ANTIVIRAL Página 1 ACICLOVIR 5% Crema Crema Principio Activo Aciclovir Excipientes necesarios
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 ERGOTAMINA + CAFEÍNA 1/100 mg COMPRIMIDOS RECUBIERTOS ANALGÉSICO, ANTIMIGRAÑOSO Página 1 ERGOTAMINA + CAFEÍNA 1/100
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 ERGOTAMINA + CAFEÍNA 1/100 mg COMPRIMIDOS RECUBIERTOS ANALGÉSICO, ANTIMIGRAÑOSO Página 1 ERGOTAMINA + CAFEÍNA 1/100
FICHA TÉCNICA. Tratamiento de la incontinencia urinaria asociada a la insuficiencia del esfínter uretral en la perra.
 DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO CONTINENZA 40 mg/ml jarabe 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene: Sustancia activa:
DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO CONTINENZA 40 mg/ml jarabe 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene: Sustancia activa:
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 INDOMETACINA 25 mg COMPRIMIDOS RECUBIERTOS ANTIINFLAMATORIO ANTIRREUMÁTICO Página 1 INDOMETACINA 25 mg Comprimidos
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 INDOMETACINA 25 mg COMPRIMIDOS RECUBIERTOS ANTIINFLAMATORIO ANTIRREUMÁTICO Página 1 INDOMETACINA 25 mg Comprimidos
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 METRONIDAZOL 500 mg TABLETA VAGINAL ANTIPARASITARIO - ANTIPROTOZOARIO Página 1 METRONIDAZOL 500 mg Tableta Vaginal
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 METRONIDAZOL 500 mg TABLETA VAGINAL ANTIPARASITARIO - ANTIPROTOZOARIO Página 1 METRONIDAZOL 500 mg Tableta Vaginal
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Emeprid 1 mg/ml solución oral para perros y gatos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Emeprid 1 mg/ml solución oral para perros y gatos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada
Cuidado de la enfermera a pacientes con complicaciones de preeclampsia eclampsia, síndrome de Hellp
 Cuidado de la enfermera a pacientes con complicaciones de preeclampsia eclampsia, síndrome de Hellp Enf. María Guadalupe Vega Jefe de Piso Unidad de Terapia Intensiva Hospital General Las Américas, Ecatepec
Cuidado de la enfermera a pacientes con complicaciones de preeclampsia eclampsia, síndrome de Hellp Enf. María Guadalupe Vega Jefe de Piso Unidad de Terapia Intensiva Hospital General Las Américas, Ecatepec
RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO PARACETAMOL SP, 300 mg/ml Solución para administración en agua de bebida, para cerdos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO PARACETAMOL SP, 300 mg/ml Solución para administración en agua de bebida, para cerdos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
FICHA TECNICA. (1) Equivalente a 185,2 mg de hidróxido de magnesio.
 FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO 2. COMPOSICION Por 5 ml: Principios activos: Gel de hidróxido alumínico... 350 mg Hidróxido magnésico... 20 mg Por comprimido: Principio activo: Hidróxido alumínico...
FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO 2. COMPOSICION Por 5 ml: Principios activos: Gel de hidróxido alumínico... 350 mg Hidróxido magnésico... 20 mg Por comprimido: Principio activo: Hidróxido alumínico...
Unidad Coordinadora Nacional de Farmacovigilancia. Comunicación a profesionales sanitarios sobre AGONISTAS DOPAMINÉRGICOS ERGÓTICOS Alerta No 7
 1 Diciembre 2008 Unidad Coordinadora Nacional de Farmacovigilancia. Comunicación a profesionales sanitarios sobre AGONISTAS DOPAMINÉRGICOS ERGÓTICOS Alerta No 7 Una alternativa a la levodopa es el uso
1 Diciembre 2008 Unidad Coordinadora Nacional de Farmacovigilancia. Comunicación a profesionales sanitarios sobre AGONISTAS DOPAMINÉRGICOS ERGÓTICOS Alerta No 7 Una alternativa a la levodopa es el uso
LABORATORIOS NORMON, S.A.
 1. NOMBRE DEL MEDICAMENTO normoval 250 mg comprimidos recubiertos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto de normoval contiene: 250 mg de extracto hidroalcohólico seco de raíz
1. NOMBRE DEL MEDICAMENTO normoval 250 mg comprimidos recubiertos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido recubierto de normoval contiene: 250 mg de extracto hidroalcohólico seco de raíz
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Ginkokán 40 mg comprimidos Extracto de Ginkgo biloba EGb 761 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Ginkokán 40 mg comprimidos Extracto de Ginkgo biloba EGb 761 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido
FICHA TÉCNICA. KETOISDIN 400 mg óvulos está indicado en adultos para el tratamiento local de
 1. NOMBRE DEL MEDICAMENTO KETOISDIN 400 mg óvulos FICHA TÉCNICA 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada óvulo contiene: 400 mg de ketoconazol Excipientes con efecto conocido: Butilhidroxianisol
1. NOMBRE DEL MEDICAMENTO KETOISDIN 400 mg óvulos FICHA TÉCNICA 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada óvulo contiene: 400 mg de ketoconazol Excipientes con efecto conocido: Butilhidroxianisol
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 CALCIO-500 D COMPRIMIDOS RECUBIERTOS SUPLEMENTO MINERAL Página 1 CALCIO-500 D Comprimidos Recubiertos Principio
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 CALCIO-500 D COMPRIMIDOS RECUBIERTOS SUPLEMENTO MINERAL Página 1 CALCIO-500 D Comprimidos Recubiertos Principio
FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO. 1. NOMBRE DEL MEDICAMENTO Dextrometorfano Hidrobromuro Farmalider 15 mg cápsulas blandas
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Dextrometorfano Hidrobromuro Farmalider 15 mg cápsulas blandas 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Dextrometorfano
FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Dextrometorfano Hidrobromuro Farmalider 15 mg cápsulas blandas 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Dextrometorfano
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Lactulosa Level 667,5 mg/ml solución oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 mililitro de solución oral contiene
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Lactulosa Level 667,5 mg/ml solución oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 mililitro de solución oral contiene
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 METRONIDAZOL 500 mg COMPRIMIDOS RECUBIERTOS ANTIPARASITARIO - ANTIPROTOZOARIO Página 1 METRONIDAZOL 500 mg Comprimidos
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 METRONIDAZOL 500 mg COMPRIMIDOS RECUBIERTOS ANTIPARASITARIO - ANTIPROTOZOARIO Página 1 METRONIDAZOL 500 mg Comprimidos
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO VECOXAN 2,5 mg/ml SUSPENSION ORAL TERNEROS Y CORDEROS Diclazurilo 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO VECOXAN 2,5 mg/ml SUSPENSION ORAL TERNEROS Y CORDEROS Diclazurilo 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Mupirocina ISDIN 20 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene 20 mg de mupirocina. Para consultar
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Mupirocina ISDIN 20 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene 20 mg de mupirocina. Para consultar
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. PRODELION 25-50 microgramos comprimidos. PRODELION 150 microgramos comprimidos
 agencia española de medicamentos y productos sanitarios FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO PRODELION 25-50 microgramos comprimidos PRODELION 75 microgramos comprimidos PRODELION 150 microgramos comprimidos
agencia española de medicamentos y productos sanitarios FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO PRODELION 25-50 microgramos comprimidos PRODELION 75 microgramos comprimidos PRODELION 150 microgramos comprimidos
FICHA TÉCNICA. Por sobre: Acetato de calcio, 2,5 g (equivale a 635 mg de calcio), almidón de maíz, manitol (E421)
 FICHA TÉCNICA 1.- NOMBRE DEL MEDICAMENTO ROYEN 500 mg cápsula dura. ROYEN 2,5 g polvo para suspensión oral. 2.- COMPOSICIÓN CUALITATIVA Y CUANTITATIVA ROYEN 500 mg cápsula dura. Por cápsula: Acetato de
FICHA TÉCNICA 1.- NOMBRE DEL MEDICAMENTO ROYEN 500 mg cápsula dura. ROYEN 2,5 g polvo para suspensión oral. 2.- COMPOSICIÓN CUALITATIVA Y CUANTITATIVA ROYEN 500 mg cápsula dura. Por cápsula: Acetato de
FICHA TECNICA DE URINORM BENZBROMARONA 1. DENOMINACIÓN DEL MEDICAMENTO. URINORM, 100 mg, comprimidos. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TECNICA DE URINORM BENZBROMARONA 1. DENOMINACIÓN DEL MEDICAMENTO URINORM, 100 mg, comprimidos. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene: Benzbromarona (D.C.I.)...100 mg
FICHA TECNICA DE URINORM BENZBROMARONA 1. DENOMINACIÓN DEL MEDICAMENTO URINORM, 100 mg, comprimidos. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene: Benzbromarona (D.C.I.)...100 mg
Psicofàrmacos. Escuela de parteras 2013
 Psicofàrmacos Escuela de parteras 2013 Psicofàrmacos Fàrmacos que actùan sobre las funciones cerebrales como sedantes o estimulantes, lo que produce cambios en la percepciòn, estado de ànimo, conciencia
Psicofàrmacos Escuela de parteras 2013 Psicofàrmacos Fàrmacos que actùan sobre las funciones cerebrales como sedantes o estimulantes, lo que produce cambios en la percepciòn, estado de ànimo, conciencia
FICHA TÉCNICA. NORPROLAC 75 microgramos comprimidos
 agencia española de medicamentos y productos sanitarios FICHA TÉCNICA NORPROLAC 25-50 microgramos comprimidos NORPROLAC 75 microgramos comprimidos 1. NOMBRE DEL MEDICAMENTO NORPROLAC 25-50 microgramos
agencia española de medicamentos y productos sanitarios FICHA TÉCNICA NORPROLAC 25-50 microgramos comprimidos NORPROLAC 75 microgramos comprimidos 1. NOMBRE DEL MEDICAMENTO NORPROLAC 25-50 microgramos
CENAVUL Suspensión inyectable
 Camí Pedra Estela s/n 43205 Reus Telf. 977 75 72 73 Fax. 977 75 13 98 www.cenavisa.com E-mail: cenavisa@cenavisa.com FICHA TÉCNICA: CENAVUL Suspensión inyectable Reg. nº: 2145 ESP FICHA TÉCNICA (RESUMEN
Camí Pedra Estela s/n 43205 Reus Telf. 977 75 72 73 Fax. 977 75 13 98 www.cenavisa.com E-mail: cenavisa@cenavisa.com FICHA TÉCNICA: CENAVUL Suspensión inyectable Reg. nº: 2145 ESP FICHA TÉCNICA (RESUMEN
Prospecto: Información para el usuario. Pramipexol Zentiva 0,18 mg comprimidos EFG. Pramipexol
 Prospecto: Información para el usuario Pramipexol Zentiva 0,18 mg comprimidos EFG Pramipexol Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento. - Conserve este prospecto, ya que
Prospecto: Información para el usuario Pramipexol Zentiva 0,18 mg comprimidos EFG Pramipexol Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento. - Conserve este prospecto, ya que
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 SUPOSITORIO BRONQUIAL LACTANTE SUPOSITORIO ANALGÉSICO, EXPECTORANTE BALSÁMICO Página 1 SUPOSITORIO BRONQUIAL LACTANTE
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 SUPOSITORIO BRONQUIAL LACTANTE SUPOSITORIO ANALGÉSICO, EXPECTORANTE BALSÁMICO Página 1 SUPOSITORIO BRONQUIAL LACTANTE
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO RIMADYL SOLUCIÓN INYECTABLE PARA BOVIN0 50 mg/ml 2. COMPOSICIÓN CUALITATIVA
DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO RIMADYL SOLUCIÓN INYECTABLE PARA BOVIN0 50 mg/ml 2. COMPOSICIÓN CUALITATIVA
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 COMPLEJO B COMPRIMIDOS RECUBIERTOS VITAMINA Página 1 COMPLEJO B Comprimidos Recubiertos Principio Activo Tiamina
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 COMPLEJO B COMPRIMIDOS RECUBIERTOS VITAMINA Página 1 COMPLEJO B Comprimidos Recubiertos Principio Activo Tiamina
FICHA TECNICA. P R A M O X Pramocaína
 FICHA TECNICA P R A M O X Pramocaína 1. NOMBRE DEL MEDICAMENTO PRAMOX Gel PRAMOX Crema PRAMOX Emulsión 2. COMPOSICION CUALITATIVA Y CUANTITATIVA PRAMOX Gel y Crema :. Cada 100 g contienen: Pramocaína (DCI)
FICHA TECNICA P R A M O X Pramocaína 1. NOMBRE DEL MEDICAMENTO PRAMOX Gel PRAMOX Crema PRAMOX Emulsión 2. COMPOSICION CUALITATIVA Y CUANTITATIVA PRAMOX Gel y Crema :. Cada 100 g contienen: Pramocaína (DCI)
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 BROMHEXINA 4 mg/5 ml JARABE MUCOLÍTICO, EXPECTORANTE Página 1 BROMHEXINA 4 mg/5 ml Jarabe Principio Activo Bromhexina
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 BROMHEXINA 4 mg/5 ml JARABE MUCOLÍTICO, EXPECTORANTE Página 1 BROMHEXINA 4 mg/5 ml Jarabe Principio Activo Bromhexina
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Glucosamina KERN PHARMA 1.500 mg polvo para solución oral EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada sobre
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Glucosamina KERN PHARMA 1.500 mg polvo para solución oral EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada sobre
FICHA DE INFORMACIÓN AL PACIENTE: Ranitidina
 FICHA DE INFORMACIÓN AL PACIENTE: Ranitidina 1.- QUÉ ES Y PARA QUE SE UTILIZA 1.1 Acción: Antiúlcera péptica, antisecretor gástrico, antagonista de los receptores H2 de la histamina. 1.2 Cómo actúa este
FICHA DE INFORMACIÓN AL PACIENTE: Ranitidina 1.- QUÉ ES Y PARA QUE SE UTILIZA 1.1 Acción: Antiúlcera péptica, antisecretor gástrico, antagonista de los receptores H2 de la histamina. 1.2 Cómo actúa este
1. NOMBRE DEL MEDICAMENTO 2. COMPOSICIÓN CUANTITATIVA Y CUALITATIVA 3. FORMA FARMACÉUTICA 4. DATOS CLÍNICOS
 POSTINOR 750 microgramos comprimidos. 1. NOMBRE DEL MEDICAMENTO 2. COMPOSICIÓN CUANTITATIVA Y CUALITATIVA Cada comprimido contiene 750 microgramos de levonorgestrel. Excipientes en el apartado 6.1. Comprimidos.
POSTINOR 750 microgramos comprimidos. 1. NOMBRE DEL MEDICAMENTO 2. COMPOSICIÓN CUANTITATIVA Y CUALITATIVA Cada comprimido contiene 750 microgramos de levonorgestrel. Excipientes en el apartado 6.1. Comprimidos.
FICHA DE INFORMACIÓN AL PACIENTE: Simvastatina
 FICHA DE INFORMACIÓN AL PACIENTE: Simvastatina 1.- QUÉ ES Y PARA QUE SE UTILIZA 1.1 Acción: Hipolipemiante, inhibidor de la enzima hidroximetil-glutaril-coa-reductasa.. 1.2 Cómo actúa este fármaco: Inhibe
FICHA DE INFORMACIÓN AL PACIENTE: Simvastatina 1.- QUÉ ES Y PARA QUE SE UTILIZA 1.1 Acción: Hipolipemiante, inhibidor de la enzima hidroximetil-glutaril-coa-reductasa.. 1.2 Cómo actúa este fármaco: Inhibe
Para la lista completa de excipientes, véase la sección Indicaciones de uso, especificando las especies de destino
 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Metacam 2 mg/ml solución inyectable para gatos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un ml contiene: Sustancia activa: Meloxicam Excipientes: Etanol 2 mg
1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Metacam 2 mg/ml solución inyectable para gatos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un ml contiene: Sustancia activa: Meloxicam Excipientes: Etanol 2 mg
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Pramipexol Normon 0,26 mg comprimidos de liberación prolongada EFG. Pramipexol Normon 0,52 mg comprimidos de liberación prolongada EFG. Pramipexol Normon 1,05 mg
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Pramipexol Normon 0,26 mg comprimidos de liberación prolongada EFG. Pramipexol Normon 0,52 mg comprimidos de liberación prolongada EFG. Pramipexol Normon 1,05 mg
Sección 9: Antiparkinsonianos
 201 Sección 9: Antiparkinsonianos 9.1 Fármacos utilizados en el parkinsonismo...202 9.2 Fármacos utilizados en el temblor esencial y trastornos relacionados...204 202 9.1 Fármacos utilizados en el parkinsonismo
201 Sección 9: Antiparkinsonianos 9.1 Fármacos utilizados en el parkinsonismo...202 9.2 Fármacos utilizados en el temblor esencial y trastornos relacionados...204 202 9.1 Fármacos utilizados en el parkinsonismo
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 COTRIMOXAZOL 200/40/5 ml SUSPENSIÓN ANTIINFECCIOSO-ANTIBACTERIANO Página 1 COTRIMOXAZOL 200/40/5 ml Suspensión Principio
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 COTRIMOXAZOL 200/40/5 ml SUSPENSIÓN ANTIINFECCIOSO-ANTIBACTERIANO Página 1 COTRIMOXAZOL 200/40/5 ml Suspensión Principio
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. REACTINE Levocabastina 0,5mg/ml colirio en suspensión. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO REACTINE Levocabastina 0,5mg/ml colirio en suspensión. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene: Levocabastina (como hidrocloruro) equivalente
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO REACTINE Levocabastina 0,5mg/ml colirio en suspensión. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene: Levocabastina (como hidrocloruro) equivalente
FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO
 FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO Hodernal 800 mg/ml solución oral Parafina líquida 1. NOMBRE DEL MEDICAMENTO Hodernal 800 mg/ml solución oral. 2. COMPOSICIÓN CUANTITATIVA Y CUALITATIVA
FICHA TÉCNICA O RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO Hodernal 800 mg/ml solución oral Parafina líquida 1. NOMBRE DEL MEDICAMENTO Hodernal 800 mg/ml solución oral. 2. COMPOSICIÓN CUANTITATIVA Y CUALITATIVA
N H S-CCDS-MK4117-MTL
 DESALEX 5 mg Tabletas Recubiertas DESALEX 5 mg Tabletas Orodispersables DESALEX 0,5 mg/ml Jarabe DESALEX 0,25 mg/ 0,5 ml Solución Gotas 1 DESCRIPCIÓN DEL PRODUCTO Desalex 5 mg tabletas recubiertas, Desalex
DESALEX 5 mg Tabletas Recubiertas DESALEX 5 mg Tabletas Orodispersables DESALEX 0,5 mg/ml Jarabe DESALEX 0,25 mg/ 0,5 ml Solución Gotas 1 DESCRIPCIÓN DEL PRODUCTO Desalex 5 mg tabletas recubiertas, Desalex
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. Lacovin 20 mg/ml solución cutánea. Lacovin 50 mg/ml solución cutánea.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Lacovin 20 mg/ml solución cutánea. Lacovin 50 mg/ml solución cutánea. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de Lacovin 20 mg/ml solución cutánea contiene
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Lacovin 20 mg/ml solución cutánea. Lacovin 50 mg/ml solución cutánea. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de Lacovin 20 mg/ml solución cutánea contiene
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. Cabergolina Teva 0,5 mg comprimidos EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Cabergolina Teva 0,5 mg comprimidos EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 0,5 mg de cabergolina. Excipientes con efecto conocido:
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Cabergolina Teva 0,5 mg comprimidos EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene 0,5 mg de cabergolina. Excipientes con efecto conocido:
PROSPECTO: INFORMACIÓN PARA EL USUARIO. ACETILCISTEÍNA BEXAL 100 mg polvo para solución oral EFG
 PROSPECTO: INFORMACIÓN PARA EL USUARIO ACETILCISTEÍNA BEXAL 100 mg polvo para solución oral EFG Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento. Conserve este prospecto, ya
PROSPECTO: INFORMACIÓN PARA EL USUARIO ACETILCISTEÍNA BEXAL 100 mg polvo para solución oral EFG Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento. Conserve este prospecto, ya
Principio activo / Dósis: Metoclopramida 0,2 % Linea de Desarrollo: Aparato Digestivo
 Principio activo / Dósis: Metoclopramida 0,2 % Linea de Desarrollo: Aparato Digestivo FÓRMULA: Metoclopramida (como clorhidrato) 100ml x 0,20 g. Amarillo de tartrazina como colorante c.s. 1 / 22 Metoclopramida
Principio activo / Dósis: Metoclopramida 0,2 % Linea de Desarrollo: Aparato Digestivo FÓRMULA: Metoclopramida (como clorhidrato) 100ml x 0,20 g. Amarillo de tartrazina como colorante c.s. 1 / 22 Metoclopramida
LLD Abreviado de Zoloft. Todo medicamento debe conservarse fuera del alcance de los niños.
 LLD Abreviado de Zoloft Versión: 19.0 Fecha: 20 de febrero de 2015 Aprobación ARCSA: 23 febrero de 2016 Todo medicamento debe conservarse fuera del alcance de los niños. 1. Presentación: Sertralina que
LLD Abreviado de Zoloft Versión: 19.0 Fecha: 20 de febrero de 2015 Aprobación ARCSA: 23 febrero de 2016 Todo medicamento debe conservarse fuera del alcance de los niños. 1. Presentación: Sertralina que
FICHA TECNICA. Tratamiento de la intoxicación por Amanita phalloides.
 FICHA TECNICA 1 - NOMBRE DEL MEDICAMENTO Legalon SIL 2 - COMPOSICION CUALITATIVA Y CUANTITATIVA Un vial para infusión con 598,5 mg de producto liofilizado contiene: 528,5 mg de silibinina-c-2',3- dihidrogenosuccinato
FICHA TECNICA 1 - NOMBRE DEL MEDICAMENTO Legalon SIL 2 - COMPOSICION CUALITATIVA Y CUANTITATIVA Un vial para infusión con 598,5 mg de producto liofilizado contiene: 528,5 mg de silibinina-c-2',3- dihidrogenosuccinato
PROSPECTO PARA el liberador del lote Ecuphar NV: ACTIMARBO 80 MG COMPRIMIDOS SABOR PARA PERROS
 DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS PROSPECTO PARA el liberador del lote Ecuphar NV: ACTIMARBO 80 MG COMPRIMIDOS SABOR PARA PERROS 1. NOMBRE O RAZÓN SOCIAL Y DOMICILIO O SEDE SOCIAL DEL TITULAR DE
DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS PROSPECTO PARA el liberador del lote Ecuphar NV: ACTIMARBO 80 MG COMPRIMIDOS SABOR PARA PERROS 1. NOMBRE O RAZÓN SOCIAL Y DOMICILIO O SEDE SOCIAL DEL TITULAR DE
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO. VECOXAN 2,5 mg/ml SUSPENSION ORAL TERNEROS Y CORDEROS Diclazurilo
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO VECOXAN 2,5 mg/ml SUSPENSION ORAL TERNEROS Y CORDEROS Diclazurilo 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO VECOXAN 2,5 mg/ml SUSPENSION ORAL TERNEROS Y CORDEROS Diclazurilo 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada
PAROXETINA COMPRIMIDOS CON RECUBRIMIENTO ENTÉRICO 12,5mg-25mg
 PAROXETINA COMPRIMIDOS CON RECUBRIMIENTO ENTÉRICO 12,5mg-25mg Lea cuidadosamente este folleto antes de la administración de este medicamento, contiene información importante acerca de su tratamiento. Si
PAROXETINA COMPRIMIDOS CON RECUBRIMIENTO ENTÉRICO 12,5mg-25mg Lea cuidadosamente este folleto antes de la administración de este medicamento, contiene información importante acerca de su tratamiento. Si
Anexo III. Modificaciones a las secciones relevantes de la ficha técnica o resumen de las características del producto y los prospectos
 Anexo III Modificaciones a las secciones relevantes de la ficha técnica o resumen de las características del producto y los prospectos Nota: Estas modificaciones a las secciones relevantes de la Ficha
Anexo III Modificaciones a las secciones relevantes de la ficha técnica o resumen de las características del producto y los prospectos Nota: Estas modificaciones a las secciones relevantes de la Ficha
Anexo II. Modificaciones a las secciones pertinentes de la ficha técnica y el prospecto
 Anexo II Modificaciones a las secciones pertinentes de la ficha técnica y el prospecto 6 Para los medicamentos que contienen los inhibidores de la enzima convertidora de angiotensina (IECA) benazepril,
Anexo II Modificaciones a las secciones pertinentes de la ficha técnica y el prospecto 6 Para los medicamentos que contienen los inhibidores de la enzima convertidora de angiotensina (IECA) benazepril,
Para consultar la lista completa de excipientes, ver sección 6.1.
 1. NOMBRE DEL MEDICAMENTO Betahistina NORMON 8 mg comprimidos EFG. Betahistina NORMON 16 mg comprimidos EFG. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido de Betahistina NORMON 8 mg contiene
1. NOMBRE DEL MEDICAMENTO Betahistina NORMON 8 mg comprimidos EFG. Betahistina NORMON 16 mg comprimidos EFG. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido de Betahistina NORMON 8 mg contiene
Prospecto: información para el usuario. Memantina Cinfa 10 mg comprimidos recubiertos con película EFG Memantina hidrocloruro
 Prospecto: información para el usuario Memantina Cinfa 10 mg comprimidos recubiertos con película EFG Memantina hidrocloruro Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento,
Prospecto: información para el usuario Memantina Cinfa 10 mg comprimidos recubiertos con película EFG Memantina hidrocloruro Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento,
PROSPECTO: I FORMACIÓ PARA EL USUARIO. Pramipexol Apotex 0,18 mg comprimidos EFG. (Pramipexol)
 PROSPECTO: I FORMACIÓ PARA EL USUARIO Pramipexol Apotex 0,18 mg comprimidos EFG (Pramipexol) Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento Conserve este prospecto, ya que
PROSPECTO: I FORMACIÓ PARA EL USUARIO Pramipexol Apotex 0,18 mg comprimidos EFG (Pramipexol) Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento Conserve este prospecto, ya que
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. IDEOS UNIDIA 1000 mg/880 UI granulado efervescente 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO IDEOS UNIDIA 1000 mg/880 UI granulado efervescente 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada sobre de 8 g contiene : Calcio elemento... 1000 mg ó25 mmol equivalente
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO IDEOS UNIDIA 1000 mg/880 UI granulado efervescente 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada sobre de 8 g contiene : Calcio elemento... 1000 mg ó25 mmol equivalente
FICHA TÉCNICA. ENTEROSTREP SP 500mg/g polvo para administración en agua de bebida para conejos
 FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO ENTEROSTREP SP 500mg/g polvo para administración en agua de bebida para conejos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada g contiene: Sustancia
FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO ENTEROSTREP SP 500mg/g polvo para administración en agua de bebida para conejos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada g contiene: Sustancia
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. RESINCALCIO polvo para suspensión oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO RESINCALCIO polvo para suspensión oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada 100 g de polvo para suspensión oral contienen 99,75 g de poliestireno sulfonato
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO RESINCALCIO polvo para suspensión oral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada 100 g de polvo para suspensión oral contienen 99,75 g de poliestireno sulfonato
Prospecto: información para el usuario
 Prospecto: información para el usuario Dostinex 0,5 mg comprimidos Cabergolina Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento. - Conserve este prospecto, ya que puede tener
Prospecto: información para el usuario Dostinex 0,5 mg comprimidos Cabergolina Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento. - Conserve este prospecto, ya que puede tener
ARIPIPRAZOL En adolescentes contrastorno Bipolar I
 ARIPIPRAZOL En adolescentes contrastorno Bipolar I Información para profesionales sanitarios Preguntas frecuentes Disponible en la web de la AEMPS www.aemps.gob.es Información sobre prevención de riesgos
ARIPIPRAZOL En adolescentes contrastorno Bipolar I Información para profesionales sanitarios Preguntas frecuentes Disponible en la web de la AEMPS www.aemps.gob.es Información sobre prevención de riesgos
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO ULCERGOLD 370 mg/g PASTA ORAL PARA EQUINO 2. COMPOSICIÓN CUALITATIVA Y
DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO ULCERGOLD 370 mg/g PASTA ORAL PARA EQUINO 2. COMPOSICIÓN CUALITATIVA Y
FICHA TÉCNICA. Vispring 500 microgramos/ml colirio en solución en envases unidosis
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Vispring 500 microgramos/ml colirio en solución en envases unidosis 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de colirio en solución contiene: Tetrizolina
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Vispring 500 microgramos/ml colirio en solución en envases unidosis 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml de colirio en solución contiene: Tetrizolina
4.2 Indicaciones de uso, especificando las especies a las que va destinado
 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Loxicom 5 mg/ml solución inyectable para perros y gatos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene: Principio activo: Meloxicam Excipientes:
1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Loxicom 5 mg/ml solución inyectable para perros y gatos 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene: Principio activo: Meloxicam Excipientes:
Cada ml contiene levocabastina (como hidrocloruro) equivalente a 0,5 mg de levocabastina.
 1. NOMBRE DEL MEDICAMENTO Bilina 0,5 mg/ml colirio en suspensión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene levocabastina (como hidrocloruro) equivalente a 0,5 mg de levocabastina. Excipiente
1. NOMBRE DEL MEDICAMENTO Bilina 0,5 mg/ml colirio en suspensión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada ml contiene levocabastina (como hidrocloruro) equivalente a 0,5 mg de levocabastina. Excipiente
Prospecto: información para el paciente. Memantina Kern Pharma 10 mg/ml solución oral EFG Hidrocloruro de memantina
 Prospecto: información para el paciente Memantina Kern Pharma 10 mg/ml solución oral EFG Hidrocloruro de memantina Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento porque contiene
Prospecto: información para el paciente Memantina Kern Pharma 10 mg/ml solución oral EFG Hidrocloruro de memantina Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento porque contiene
Enfermedad de Kawasaki
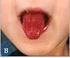 www.printo.it/pediatric-rheumatology/ar/intro Enfermedad de Kawasaki Versión de 2016 2. DIAGNÓSTICO Y TRATAMIENTO 2.1 Cómo se diagnostica? El diagnóstico de la enfermedad de Kawasaki se realiza en base
www.printo.it/pediatric-rheumatology/ar/intro Enfermedad de Kawasaki Versión de 2016 2. DIAGNÓSTICO Y TRATAMIENTO 2.1 Cómo se diagnostica? El diagnóstico de la enfermedad de Kawasaki se realiza en base
Documento Local de Producto
 1 Documento Local de Producto Título del Documento : Difenoxilato HCl / atropina sulfato Última fecha de Revisión: Abr-1998 Fecha efectiva: Julio-20-2011 Versión CDS: 3.0 1. NOMBRE DEL PRODUCTO MEDICINAL
1 Documento Local de Producto Título del Documento : Difenoxilato HCl / atropina sulfato Última fecha de Revisión: Abr-1998 Fecha efectiva: Julio-20-2011 Versión CDS: 3.0 1. NOMBRE DEL PRODUCTO MEDICINAL
Las definiciones básicas (ACC/AHA)
 Las definiciones básicas (ACC/AHA) Qué es la? Cuáles son sus modalidades y criterios de diagnóstico? Qué significa IC con fracción de eyección reducida o preservada? El American College of Cardiology y
Las definiciones básicas (ACC/AHA) Qué es la? Cuáles son sus modalidades y criterios de diagnóstico? Qué significa IC con fracción de eyección reducida o preservada? El American College of Cardiology y
CRONODINE (Diltiazem clorhidrato)
 CRONODINE (Diltiazem clorhidrato) 1. NOMBRE DEL MEDICAMENTO: CRONODINE 120 mg y 240 mg 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA: CRONODINE 120: Diltiazem (DCI) clorhidrato 120 mg CRONODINE 240: Diltiazem
CRONODINE (Diltiazem clorhidrato) 1. NOMBRE DEL MEDICAMENTO: CRONODINE 120 mg y 240 mg 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA: CRONODINE 120: Diltiazem (DCI) clorhidrato 120 mg CRONODINE 240: Diltiazem
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. ACICLOVIR COMBIX 800 mg Comprimidos EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO ACICLOVIR COMBIX 800 mg Comprimidos EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido de 800 mg contiene: Aciclovir (DCI) 800 mg. 3. FORMA FARMACÉUTICA
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO ACICLOVIR COMBIX 800 mg Comprimidos EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido de 800 mg contiene: Aciclovir (DCI) 800 mg. 3. FORMA FARMACÉUTICA
1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO. Pexion 100 mg comprimidos para perros Pexion 400 mg comprimidos para perros
 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Pexion 100 mg comprimidos para perros Pexion 400 mg comprimidos para perros 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un comprimido contiene: Sustancia activa:
1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Pexion 100 mg comprimidos para perros Pexion 400 mg comprimidos para perros 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un comprimido contiene: Sustancia activa:
TECNOLOGÍA EN SALUD DE INTERÉS Deferasirox
 TECNOLOGÍA EN SALUD DE INTERÉS Deferasirox 1. RESUMEN Título del reporte: Evaluación de efectividad y seguridad de deferasirox en Hemosiderosis Transfusional Información general de la tecnología: deferasirox
TECNOLOGÍA EN SALUD DE INTERÉS Deferasirox 1. RESUMEN Título del reporte: Evaluación de efectividad y seguridad de deferasirox en Hemosiderosis Transfusional Información general de la tecnología: deferasirox
MÓDULO 2. TRATAMIENTO DE LAS PLANTAS MEDICINALES
 CURSO FITOTERAPIA MÓDULO 2. TRATAMIENTO DE LAS PLANTAS MEDICINALES Página 2 TEMA 2.6 TOXICIDAD Y PRECAUCIONES TOXICIDAD Una droga se define como tóxica cuando produce un efecto lesivo sobre nuestra biología,
CURSO FITOTERAPIA MÓDULO 2. TRATAMIENTO DE LAS PLANTAS MEDICINALES Página 2 TEMA 2.6 TOXICIDAD Y PRECAUCIONES TOXICIDAD Una droga se define como tóxica cuando produce un efecto lesivo sobre nuestra biología,
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO VETMEDIN 5 mg COMPRIMIDOS MASTICABLES PARA PERROS 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un comprimido masticable
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO VETMEDIN 5 mg COMPRIMIDOS MASTICABLES PARA PERROS 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un comprimido masticable
3. FORMA FARMACÉUTICA Solución oral. La solución es transparente, de color marrón y con olor característico.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO FERPLEX 40 mg Solución Oral 2. COMPOSICIÓN CUANTITATIVA Y CUALITATIVA Cada vial de 15 ml de solución oral contiene: Hierro proteinsuccinilato 800 mg, equivalente
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO FERPLEX 40 mg Solución Oral 2. COMPOSICIÓN CUANTITATIVA Y CUALITATIVA Cada vial de 15 ml de solución oral contiene: Hierro proteinsuccinilato 800 mg, equivalente
AMENORREA SECUNDARIA. Dra. Ma. Susana Apablaza H. Gíneco-Obstetra Ginecóloga Infanto-Juvenil Unidad Adolescencia Clínica Alemana Temuco
 AMENORREA SECUNDARIA Dra. Ma. Susana Apablaza H. Gíneco-Obstetra Ginecóloga Infanto-Juvenil Unidad Adolescencia Clínica Alemana Temuco Definición: Ausencia de menstruación en una mujer que ya ha menstruado
AMENORREA SECUNDARIA Dra. Ma. Susana Apablaza H. Gíneco-Obstetra Ginecóloga Infanto-Juvenil Unidad Adolescencia Clínica Alemana Temuco Definición: Ausencia de menstruación en una mujer que ya ha menstruado
Pacientes de edad avanzada: debe considerarse la conveniencia de ampliar el intervalo de dosificación (Ver Propiedades Famacocinéticas).
 FT290191-B+2 1. NOMBRE DEL MEDICAMENTO DARVON 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Dextropropoxifeno (D.C.I.) napsilato 100 mg. 3. FORMA FARMACÉUTICA Cápsulas para administración por vía oral. 4.
FT290191-B+2 1. NOMBRE DEL MEDICAMENTO DARVON 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Dextropropoxifeno (D.C.I.) napsilato 100 mg. 3. FORMA FARMACÉUTICA Cápsulas para administración por vía oral. 4.
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 DEPARTAMENTO MEDICAMENTOS VETERINARIOS DE RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO LIBEO 10 mg COMPRIMIDOS MASTICABLES PARA PERROS 2. COMPOSICIÓN CUALITATIVA
DEPARTAMENTO MEDICAMENTOS VETERINARIOS DE RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO LIBEO 10 mg COMPRIMIDOS MASTICABLES PARA PERROS 2. COMPOSICIÓN CUALITATIVA
La osmolaridad calculada de la solución es de 307 mosm/l y el ph de 4,5-7,0. El contenido teórico en sodio y en cloruro es de 154 mmol/l.
 1. NOMBRE DEL MEDICAMENTO Fleboflex Salina Fisiológica Grifols Solución para perfusión Cloruro de sodio 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada 100 ml de solución contienen: Cloruro de sodio (D.C.I.),
1. NOMBRE DEL MEDICAMENTO Fleboflex Salina Fisiológica Grifols Solución para perfusión Cloruro de sodio 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada 100 ml de solución contienen: Cloruro de sodio (D.C.I.),
INTRODUCCIÓN. Otras investigaciones mostraron que el incremento de la glicemia basal en ayunas en hipertiroideos fue más alta que en normales (4,5,6).
 INTRODUCCIÓN La alteración en el metabolismo de la glucosa ha sido descrita en pacientes con hipertiroidismo; muchas investigaciones se han realizado al respecto, siendo sus resultados controversiales.
INTRODUCCIÓN La alteración en el metabolismo de la glucosa ha sido descrita en pacientes con hipertiroidismo; muchas investigaciones se han realizado al respecto, siendo sus resultados controversiales.
Información sobre prevención de riesgos autorizada por la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS)_Agosto_2016
 KEYTRUDA (pembrolizumab) Información para pacientes Keytruda es un medicamento biológico Información sobre prevención de riesgos autorizada por la Agencia Española de Medicamentos y Productos Sanitarios
KEYTRUDA (pembrolizumab) Información para pacientes Keytruda es un medicamento biológico Información sobre prevención de riesgos autorizada por la Agencia Española de Medicamentos y Productos Sanitarios
LEXATUSSIN Dextrometorfano Bromhidrato 15 mg / 5 ml Jarabe
 LEXATUSSIN Dextrometorfano Bromhidrato 15 mg / 5 ml Jarabe LEXATUSSIN (Dextrometorfano Bromhidrato 15 mg/5 ml) Jarabe COMPOSICIÓN: Cada 100 ml de Jarabe contiene: Dextrometorfano Bromhidrato monohidrato...
LEXATUSSIN Dextrometorfano Bromhidrato 15 mg / 5 ml Jarabe LEXATUSSIN (Dextrometorfano Bromhidrato 15 mg/5 ml) Jarabe COMPOSICIÓN: Cada 100 ml de Jarabe contiene: Dextrometorfano Bromhidrato monohidrato...
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO. Principio activo: 18,42 mg de benazepril (equivalente a 20 mg de benazepril hidrocloruro)
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO BENAKOR 20 mg COMPRIMIDOS PARA PERROS 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene: Principio
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO BENAKOR 20 mg COMPRIMIDOS PARA PERROS 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido contiene: Principio
La bradicinesia se define como la lentitud para iniciar y continuar los movimientos, así como dificultad para ajustar la posición corporal.
 1 CIE-10: VI Enfermedades del sistema nervioso G00-G99 Enfermedad de Parkinson G20 GPC Diagnóstico y tratamiento de la enfermedad de Parkinson inicial en el primer nivel de atención Definición La enfermedad
1 CIE-10: VI Enfermedades del sistema nervioso G00-G99 Enfermedad de Parkinson G20 GPC Diagnóstico y tratamiento de la enfermedad de Parkinson inicial en el primer nivel de atención Definición La enfermedad
Cada comprimido de Pramipexol Actavis 0,18 mg contiene 0,18 mg de pramipexol base (como 0,25 mg de dihidrocloruro de pramipexol monohidrato).
 1. NOMBRE DEL MEDICAMENTO Pramipexol Actavis 0,18 mg comprimidos EFG Pramipexol Actavis 0,7 mg comprimidos EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido de Pramipexol Actavis 0,18 mg contiene
1. NOMBRE DEL MEDICAMENTO Pramipexol Actavis 0,18 mg comprimidos EFG Pramipexol Actavis 0,7 mg comprimidos EFG 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada comprimido de Pramipexol Actavis 0,18 mg contiene
FARMACIA CLÍNICA MEDICAMENTOS EN CIRCUNSTANCIAS ESPECIALES
 FARMACIA CLÍNICA MEDICAMENTOS EN CIRCUNSTANCIAS ESPECIALES Carlos Raposo MEDICAMENTOS Y SU EXCRECIÓN EN LECHE MATERNA Variables que condicionan la excreción MEDICAMENTO Peso molecular (Pm) Grado de ionización
FARMACIA CLÍNICA MEDICAMENTOS EN CIRCUNSTANCIAS ESPECIALES Carlos Raposo MEDICAMENTOS Y SU EXCRECIÓN EN LECHE MATERNA Variables que condicionan la excreción MEDICAMENTO Peso molecular (Pm) Grado de ionización
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. 2. COMPOSICIÓN CUALITATIVA y CUANTITATIVA 3. FORMA FARMACÉUTICA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ketoconazol Abamed 2% crema 2. COMPOSICIÓN CUALITATIVA y CUANTITATIVA Composición por gramo: Ketoconazol (DOE)... 20 mg Para excipientes véase sección 6.1 3. FORMA
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Ketoconazol Abamed 2% crema 2. COMPOSICIÓN CUALITATIVA y CUANTITATIVA Composición por gramo: Ketoconazol (DOE)... 20 mg Para excipientes véase sección 6.1 3. FORMA
