Departamento de Ingeniería Metalúrgica Universidad de Santiago de Chile
|
|
|
- Jesús de la Fuente Segura
- hace 6 años
- Vistas:
Transcripción
1 CAPÍTULO 18: SÓLIDOS CRISTALINOS INTRODUCCIÓN El hecho que los sólidos cristalinos tengan un orden de largo alcance requiere que cada uno de los átomos o moléculas, cualquiera que sea la unidad base del material, deben tener idénticos alrededores dentro del sólido. Un modo simple de interpretar la estructura cristalina es considerar que ella consiste en un arreglo tridimensional de puntos en el espacio (red de puntos), donde cada punto de la red tiene idénticos alrededores. Asociados con cada uno de estos puntos de la red hay un solo átomo o idénticos grupos de átomos, dependiendo del sólido considerado. Hay sólo 14 modos diferentes de arreglar puntos de red en el espacio de tal forma que cada punto tenga idénticos alrededores. Así, cada uno de los miles de materiales cristalinos se puede describir por uno de estos arreglos de puntos más el grupo de átomos asociado. El tamaño y la complejidad del grupo de átomos varía, pues para la mayoría de los materiales el grupo consiste sólo de unos pocos átomos. La fig. ilustra como la red de puntos es combinada con un grupo de átomos para generar un arreglo periódico es de átomos. Figura 1: Red de puntos + grupos de átomos = Arreglo periódico de átomos Las 14 diferentes redes de puntos se conocen como "redes de Bravais". Ellas son descritas con mayor facilidad por medio de la "celdilla unitaria" o pequeño paralelepípedo que representa la simetría de toda la red de Bravais. La celdilla unitaria queda definida por vectores de traslación de red (vectores que conectan puntos de la red). Un ejemplo de una celdilla unitaria de la forma más general, definida por los tres vectores de red a, b y c se muestran en la Fig. 4 Capítulo 18: Sólidos Cristalinos 221
2 Figura 2: Celdilla unitaria definida por los vectores de red a, b, c. Las magnitudes de a, b y c se conocen como los parámetros de la red. La repetición de la celdilla unitaria en las tres dimensiones generará la red de Bravais. Los tres vectores de traslación de red que especifican la celdilla unitaria definen un sistema de coordenadas conocido como "sistema cristalino". Las 14 redes de Bravais pueden ser definidas sólo por 7 sistemas cristalinos diferentes, como se ve en la Tabla II y las celdillas unitarias de las redes de Bravais se muestran en la fig. 5. Tabla II : Características de los siete sistemas cristalinos diferentes. SISTEMA Ejes y ángulos entre ejes Ejemplos TRICLÍNICO Tres ejes de diferentes longitudes B (OH) Y en ángulos diferentes a 90º Al 2 O 5 A # b # c. α # β # 8 # 90º. MONOCLÍNICO Tres ejes de diferentes longitudes y KNO 2 Dos ángulos a 90º y una diferente KCLO a 90º ORTORRÓMBICO Tres ejes de diferentes longitudes y Fe C Los tres ángulos a 90º FeS 2 a # b # c α # β # 8 # 90º. TETRAGONAL Dos ejes iguales a los tres ángulos TiO 2 Rectos. KIO 4 a # b # c α # β # 8 # 90º. CÚBICO Tres ejes iguales y los tres ángulos Cu, Ag rectos a # b # c α # β # 8 # 90º. Ni, NaCl Capítulo 18: Sólidos Cristalinos 222
3 HEXAGONAL Dos ejes iguales y un ángulo de 120º Zn, Mg Un tercer eje en ángulo recto. a = b # c α = β= 90º 8 = 120º. ROMBOÉDRICO Tres ejes iguales inclinados en Sb, Bi Ángulos no rectos e iguales A = b = c α = β = 8 # 90º Figura : Las 14 redes de puntos ilustradas por sus celdillas unitarias (1) Triclínico simple (2) Monoclínico simple () Monoclínico centrado en la base (4) Ortorrómbico simple (5) Ortorrómbico centrado en la base (6) Ortorrómbico centrado en el cuerpo (7) Ortorrómbico de caras centradas (8) Hexagonal Capítulo 18: Sólidos Cristalinos 22
4 (9) Romboédrico (10) Tetragonal simple (11) Tetragonal centrado en el cuerpo (12) Cúbico Simple (1) Cúbico de cuerpo centrado (14) Cúbico de caras centradas SISTEMA CÚBICO Aunque los metales tienen celdillas unitarias que son relativamente simples en concepto, no encontramos elementos metálicos con la red cúbica primitiva o simple de la fig. (). Esto se puede explicar si colocamos un átomo en cada punto de la red de la figura 7 y definimos el concepto de "Número de Coordinación" (NC) como la cantidad de átomos más cercanos a uno tomado como centro, vemos que para la red cúbica simple cada átomo tiene sólo seis vecinos y por lo tanto, su NC = 6. Recordemos que cuando se reúnen átomos hay una liberación de energía y un número de coordinación mayor generalmente proporciona una estructura más estable liberando más energía. Así el NC para el sistema cúbico de cuerpo centrado (bcc) es 8 y para el sistema cúbico de caras centradas (fcc) y para el hexagonal compacto (hcp) es 12. Figura 4: Red cúbica primitiva. El espacio está dividido en tres conjuntos de planos paralelos igualmente espaciados. Los ejes de referencia x, y y z son mutuamente perpendiculares. Cada punto de intersección es equivalente. Para visualizar el arreglo de átomos se utilizan dos tipos de modelos, uno en que el átomo es considerado como un punto y el otro en que se presentan como esferas duras inelásticas. Otro concepto importante es el factor de empaquetamiento atómico (FEA). Capítulo 18: Sólidos Cristalinos 224
5 18.. FACTOR DE EMPAQUETAMIENTO ATÓMICO (F.E.A.) SISTEMA CÚBICO SIMPLE (c.s.) En la figura 4 se aprecia que a la estructura cúbica simple le corresponde un átomo por celdilla unitaria (1/8) de átomo por vértice) y el parámetro a = 2 r, así el F.E.A. será: Nº de átomos por celdilla unitaria x volumen de un átomo Volumen ocupado = volumen de la celdilla unitaria a=2r 4 1 x π r % volumen ocupado = a 4 π r x 100 = (2 r) x 100 = 52.4% SISTEMA CÚBICO DE CUERPO CENTRADO (b.c.c.) A la estructura cúbica de cuerpo centrado (b.c.c) le corresponden 2 átomos por celdilla unitaria y el parámetro (A) (B) (C) (C) Figura 5: Representación esquemática de la estructura b.c.c. (A). Su equipamiento atómico (B) Número de átomos en la estructura b.c.c. (C) Capítulo 18: Sólidos Cristalinos 225
6 4 2 x π r % volumen ocupado = a 4 r a = x 100 = 8 π r 4 x 100 = 8 π r 64 r x 100 = 8 π x 100 = 68% Los metales Fe α, Cr, Li, Mo, W, Na y otros (ver tabla I) cristalizan en el sistema b.c.c SISTEMA CÚBICO DE CARAS CENTRADAS (f.c.c.) En el sistema cúbico de caras centradas (fcc) a la celdilla unitaria le corresponden 4 átomos (1/8 de átomo por cada vértice y 1/2 átomo en cada cara). La constante de red 4 r "a que está relacionada con el radio atómico "r" por: a = como se ve en la figura 6. 2 (A) (B) Figura 6: Representación esquemática de la estructura fcc (A). Su empaquetamiento atómico (B). Número de átomos Capítulo 18: Sólidos Cristalinos 226
7 a = % 4 r 2 volumen ocupado = 4 x 4 p a r x 100 = 16 p r 64 r 2 2 x 100 = p 2 x 100 = 74.1% El Fe γ, Al, Au, Pb, Cu, Ag, Ni cristalizan en el sistema f.c.c SISTEMA HEXAGONAL SIMPLE (h.s.) La estructura h.s. contiene 1/2 átomo en cada vértice totalizando átomos por celdilla unitaria fig. 7. Los elementos que poseen esta estructura son: O, H, N, Se, Te, Po. Figura 7: Representación esquemática de una celdilla unitaria hexagonal simple (h.s.) SISTEMA HEXAGONAL COMPACTO (h.c.p.) Esta estructura posee átomos más que la estructura hs y están ubicados en los intersticios formados entre átomos de las capas adyacentes como se ve en la Fig. 8. Los elementos que poseen esta estructura son: Co, Mg, Be, Ti. Capítulo 18: Sólidos Cristalinos 227
8 A B Figura 8: Ilustración esquemática del sistema hexagonal compacto (A) ubicación de dos átomos del centro. (B) modelo espacial de la estructura hcp ENLACE METÁLICO Un tipo de enlace atómico primario es el enlace metálico, que se presenta en los metales sólidos. En metales en estado sólido, los átomos se encuentran empaquetados relativamente muy juntos en una ordenación sistemática o estructura cristalina. Por ejemplo, la disposición de los átomos de cobre en el cristal de cobre se muestra en la Fig. 9 (a). En esta estructura los átomos están tan juntos que sus electrones externos de valencia son atraídos por los núcleos de sus numerosos vecinos. En el caso del cobre sólido, cada átomo está rodeado por otros doce átomos más próximos. Los electrones de valencia no están, por tanto, asociados férreamente a núcleo particular alguno y así, es posible que se extiendan entre los átomos en forma de una nube electrónica de carga de baja densidad, o "gas electrónico". Los metales sólidos son, por consiguiente, visualizados como constituidos por núcleos de iones positivos (átomos sin sus electrones de valencia) y electrones de valencia dispersados en forma de una nube electrónica que cubre una gran extensión de espacio (Fig. 9b) Capítulo 18: Sólidos Cristalinos 228
9 (a) (b) Figura 9: (a) Muestra la disposición atómica en un cristal de cobre metálico. Cada átomo de cobre se coordina con otros 12 átomos de cobre, dando lugar a una estructura cristalina llamada estructura cúbica centrada en las caras. Los átomos se mantienen juntos por un "gas electrónico" de electrones de valencia deslocalizados, (b) Diagrama esquemático bidimensional de átomos enlazados metálicamente. Los círculos con signos positivos en su interior representan núcleos iónicos positivos, y las nubes de carga en torno a los núcleos iónicos representan los electrones de valencia dispersados. Débilmente enlazados a los núcleos de iones positivos pueden moverse fácilmente en el metal cristalino y, por esto, son llamados, frecuentemente, "electrones libres". Las altas conductividades térmicas y eléctricas de los metales se basan en la teoría de que algunos electrones son libres para moverse a través de la celda cristalina del metal. La mayoría de los metales pueden ser deformados considerablemente sin fracturas debido a que los átomos de metal se pueden deslizar unos sobre otros sin distorsionar completamente la estructura de enlace metálico. Los átomos en un enlace metálico sólido se mantienen juntos por enlace metálico para lograr un estado de más baja energía (o más estable). Para el enlace metálico no hay restricciones sobre pares electrónicos como en el enlace covalente o sobre la neutralidad de carga como en el enlace iónico. En el enlace metálico los electrones de valencia más externos de los átomos son compartidos por muchos átomos circundantes y de este modo, en general, el enlace metálico no resulta direccional SOLUCIONES SÓLIDAS Algunos metales utilizados comercialmente son puros, como el Cu, pero en muchos casos se le adicionan a otros metales con el fin de mejorar o cambiar sus propiedades. En el latón, al Cu se le agrega Zn para formar una solución sólida sustitucional en la cual el Cu (que se encuentra en mayor cantidad) se le denomina como el solvente, y el Capítulo 18: Sólidos Cristalinos 229
10 Zn (que se encuentra en menor cantidad) es el soluto. Lo mismo sucede con el Sn añadido al Cu y recibe el nombre de bronce. Las soluciones sólidas de los metales se forman más fácilmente cuando los átomos de solvente y soluto tienen dimensiones y estructuras electrónicas semejantes. En el latón los átomos de Zn sustituyen a los átomos de Cu en la estructura cristalina con una distribución al azar de las dos clases de átomos como se ve en la Fig. 10 Figura 10: Solución sólida sustitucional con distribución al azar. Cu Zn Figura 11: Solución sólida sustitucional con distribución ordenada cuando los átomos de soluto sustituyen en forma ordenada a los átomos del solvente tenemos una solución sólida sustitucional ordenada. Cuando en una solución sólida un átomo de dimensiones pequeñas se ubica en los intersticios que dejan el retículado de átomos de mayor tamaño se denomina como solución sólida intersticial. Ejemplo: átomos de carbono en la red del Feγ. Capítulo 18: Sólidos Cristalinos 20
11 Figura 12: Solución sólida intersticial de C en la red cristalina del Feγ DEFECTOS CRISTALINOS Hasta aquí hemos visto una regularidad en los arreglos atómicos de los materiales, pero en realidad, en los materiales reales existen varios tipos de inperfecciones cristalinas. Los defectos o imperfecciones se pueden considerar como una parte integral de la estructura de la materia y se pueden clasificar de acuerdo a su geometría como se aprecia en la tabla II. Tabla II: CLASIFICACIÓN DE LOS DEFECTOS Número de Tipo Nombre Dimensiones 0 de Punto vacancia, intersticial, de vacancia e intersticial, impureza sustitucional, impureza intersticial. 1 de Línea Dislocación de borde, helicoidal y mixta. 2 de Superficie Borde de grano, borde de macla de Volumen Huecos, porosidades inclusión DEFECTOS PUNTUALES El más simple es la vacancia que involucra la ausencia de un átomo centro del metal (Fig. 1 a y b) tales defectos pueden ser consecuencia de un empaquetamiento imperfecto durante la cristalización original o pueden resultar de vibraciones térmicas de los átomos a temperaturas elevadas. Capítulo 18: Sólidos Cristalinos 21
12 DEFECTOS DE SCHOTTKY Se presentan en compuestos que deben mantener un balance de carga. Involucran vacancias de pares de iones de cargas opuestas (c). Tanto los defectos de Shottky como las vacancias facilitan la difusión atómica. DEFECTOS INTERSTICIALES Se trata de que un átomo extra puede ser alojado dentro de una estructura cristalina produciendo distorsión atómica (d) DEFECTOS DE FRENKEL Un ión es desplazado en la red a un sitio intersticial (e). Las estructuras compactas tienen menos intersticiales y defectos de Frenkel, que vacancias y defectos de Schottky porque se necesita una energía adicional para forzar a los átomos hacia las intersticios. Figura 1: Representación de defectos puntuales DEFECTOS LINEALES El tipo más común de defecto lineal dentro de un cristal es una dislocación de borde. La mitad superior del cristal contiene ocho celdillas unitarias al igual que la mitad inferior, cuando se cuentan a lo largo del eje x. La distinción importante en que las ocho celdillas de la parte superior están comprimidas en el mismo espacio que es ocupado por siete celdillas en la mitad inferior del cristal. Esto crea un medio plano extra en la parte superior y constituye una dislocación de borde. Los planos atómicos más cercanos a la dislocación sufren la mayor cantidad de distorsión. La dislocación se considera positiva si el medio plano se encuentra en la parte superior (1) y negativa si se encuentra en la parte inferior del cristal (T) Capítulo 18: Sólidos Cristalinos 22
13 Figura 14: Representación de dislocaciones de borde o de cuña DISLOCACIÓN HELICOIDAL O DE TORNILLO Este tipo de dislocación se muestra en forma esquemática en la Fig. 15 y consiste en un desplazamiento de la mitad del cristal de tal forma que se produce una rampla. Si se hace un recorrido en la dirección contraria a los punteros del reloj, comenzando en el punto o, se terminaría el recorrido en el punto z, que se encuentra en un nivel superior. Si el recorrido en el punto z, que se encuentra en un nivel superior. Si el recorrido se efectúa en la dirección de los punteros se finalizaría en el punto, en un nivel por debajo del punto de partida. Figura 15: Dislocaciones de tornillo. Durante la cristalización se pueden originar dislocaciones de ambos tipos, pero se producen en forma más común durante la deformación plástica de los metales y aleaciones DEFECTOS DE SUPERFICIE Las imperfecciones cristalinas pueden extenderse en dos dimensiones. Como una frontera. La frontera más obvia es la superficie externa. A pesar que podemos visualizar Capítulo 18: Sólidos Cristalinos 2
14 una superficie simplemente como la terminación de la estructura cristalina, debemos apreciar el hecho de que los átomos en la superficie no son del todo comparables a los átomos dentro del cristal. Los átomos en la superficie tienen vecinos, sólo en un lado como se ve en la Fig. 16, por lo tanto, estos átomos tienen energía más alta que los internos. Figura 16: Átomos en la superficie (esquemático). Debido a que estos átomos no están totalmente rodeados por vecinos, poseen más energía que los átomos internos. CONTORNO DE GRANOS O LÍMITES DE GRANOS Aún cuando un material como el cobre en un alambre eléctrico, puede contener sólo una fase, esto es, sólo una estructura f.cc. dicho material contiene muchos cristales de varias orientaciones. A estos cristales individuales se les llama granos. La forma de un grano en un sólido está controlada usualmente por la presencia de los granos que lo rodea. Dentro de cualquier grano particular todas las celdillas unitarias están arregladas con una orientación y un patrón. Sin embargo, en el límite entre dos granos adyacentes, hay una zona de transición la cual no está alineada con ninguno de los granos, como se ve en la fig. 17. Cuando se observa un metal con un microscopio metalográfico, y a pesar de que no podemos ver los átomos individuales, podemos localizar con rapidez las fronteras de grano, si el metal ha sido atacado previamente. Primero se pule el metal hasta que se obtenga una superficie plana como espejo y luego se ataca químicamente por un corto período de tiempo. Los átomos en el área de transición entre un grano y el siguiente se disolverá más fácilmente que otros átomos, y dejará una línea que puede ser vista con el microscopio (Figura 18). Capítulo 18: Sólidos Cristalinos 24
15 Figura 17: Limite de grano nótese el área de desorden en la frontera. Figura 18: Observación de límite de granos con un microscopio metalográfico La falta de coincidencia en la orientación de granos adyacentes produce un empaquetamiento de átomos menos eficientes a lo largo de la frontera y que tienen una energía mayor que aquellos dentro de los granos. La mayor energía de los átomos en los límites de grano es importante para la modelación de los cambios de fase polimórficos. El menor empaquetamiento atómico a lo largo del límite favorece la difusión atómica y la falta de coincidencia entre granos adyacentes modifica la evolución de los movimientos de las dislocaciones. De esta manera el límite de grano modifica la deformación plástica de un material. A temperaturas normales los límites de grano interfieren con el deslizamiento. Por lo tanto, un material de grano fino es más resistente que uno de grano grueso. Capítulo 18: Sólidos Cristalinos 25
16 DEFECTOS DE VOLUMEN Se pueden presentar como inclusiones de material extraño, como restos de escoria atrapada por el metal, o huecos o poros producidos por burbujas de gas que no pueden escapar a la superficie durante la solidificación. Figura 19: Defectos de volumen Capítulo 18: Sólidos Cristalinos 26
Estructuras Cristalinas. Julio Alberto Aguilar Schafer
 Estructuras Cristalinas Julio Alberto Aguilar Schafer Modelo del estado líquido los metales Modelo del paso del estado líquido al estado sólido de los metales Equilibrio líquido-vapor Presión de vapor
Estructuras Cristalinas Julio Alberto Aguilar Schafer Modelo del estado líquido los metales Modelo del paso del estado líquido al estado sólido de los metales Equilibrio líquido-vapor Presión de vapor
MODIFICACIÓN DE LAS PROPIEDADES DE LOS METALES CONTENIDOS
 MODIFICACIÓN DE LAS PROPIEDADES DE LOS METALES CONTENIDOS Generalidades Estructura interna de los metales. Defectos en la estructura cristalina Soluciones sólidas Mecanismos de endurecimiento de los metales
MODIFICACIÓN DE LAS PROPIEDADES DE LOS METALES CONTENIDOS Generalidades Estructura interna de los metales. Defectos en la estructura cristalina Soluciones sólidas Mecanismos de endurecimiento de los metales
Física del Estado Sólido REDES CRISTALINAS. Dr. Andrés Ozols. Facultad de Ingeniería Universidad de Buenos Aires. Dr. A. Ozols 1
 Física del Estado Sólido REDES CRISTALINAS Dr. Andrés Ozols Facultad de Ingeniería Universidad de Buenos Aires 2009 Dr. A. Ozols 1 ÁTOMOS EN SÓLIDOS Dr. A. Ozols 2 ORDEN CRISTALINO y FORMA René Just Hauy
Física del Estado Sólido REDES CRISTALINAS Dr. Andrés Ozols Facultad de Ingeniería Universidad de Buenos Aires 2009 Dr. A. Ozols 1 ÁTOMOS EN SÓLIDOS Dr. A. Ozols 2 ORDEN CRISTALINO y FORMA René Just Hauy
IMPERFECCIONES EN SÓLIDOSS
 IMPERFECCIONES EN SÓLIDOSS UN ORDENAMIENTO PERFECTO DE LOS ÁTOMOS EN LOS MATERIALES CRISTALINOS SOLAMENTE PUEDE OCURRIR A UNA TEMPERATURA DE 0 K. TAL SÓLIDO IDEAL NO EXISTE: TODOS TIENEN GRAN NÚMERO DE
IMPERFECCIONES EN SÓLIDOSS UN ORDENAMIENTO PERFECTO DE LOS ÁTOMOS EN LOS MATERIALES CRISTALINOS SOLAMENTE PUEDE OCURRIR A UNA TEMPERATURA DE 0 K. TAL SÓLIDO IDEAL NO EXISTE: TODOS TIENEN GRAN NÚMERO DE
CRISTALOGRAFIA. Es un sólido compuesto de átomos, iones o moléculas ordenados de una cierta forma y que se repite en tres dimensiones.
 CRISTALOGRAFIA CRISTAL SÓLIDO MONOCRISTALINO SÓLIDO POLICRISTALINO Es un sólido compuesto de átomos, iones o moléculas ordenados de una cierta forma y que se repite en tres dimensiones. Región donde el
CRISTALOGRAFIA CRISTAL SÓLIDO MONOCRISTALINO SÓLIDO POLICRISTALINO Es un sólido compuesto de átomos, iones o moléculas ordenados de una cierta forma y que se repite en tres dimensiones. Región donde el
Tema 3. Solidificación, defectos y difusión en sólidos
 Tema 3. Solidificación, defectos y difusión en sólidos 2. Defectos a) Defectos puntuales b) Dislocaciones c) Defectos superficiales 3. Difusión en sólidos a) Generalidades b) Mecanismos de difusión c)
Tema 3. Solidificación, defectos y difusión en sólidos 2. Defectos a) Defectos puntuales b) Dislocaciones c) Defectos superficiales 3. Difusión en sólidos a) Generalidades b) Mecanismos de difusión c)
UNIDAD 3. MODIFICACIÓN DE LAS PROPIEDADES DE LOS METALES
 UNIDAD 3. MODIFICACIÓN DE LAS PROPIEDADES DE LOS METALES 1. GENERALIDADES... Pág. 49 2. ESTRUCTURA INTERNA DE LOS METALES... Pág. 49 2.1. Estructuras cristalinas... Pág. 49 2.2. Estructura cristalina cúbica
UNIDAD 3. MODIFICACIÓN DE LAS PROPIEDADES DE LOS METALES 1. GENERALIDADES... Pág. 49 2. ESTRUCTURA INTERNA DE LOS METALES... Pág. 49 2.1. Estructuras cristalinas... Pág. 49 2.2. Estructura cristalina cúbica
TEMA 1: ESTRUCTURA INTERNA DE LOS MATERIALES
 PERIODO Departamento de Tecnología. IES Nuestra Señora de la Almudena Mª Jesús Saiz TEMA 1: ESTRUCTURA INTERNA DE LOS MATERIALES El átomo: Toda la materia está compuesta por átomos y éstos por partículas
PERIODO Departamento de Tecnología. IES Nuestra Señora de la Almudena Mª Jesús Saiz TEMA 1: ESTRUCTURA INTERNA DE LOS MATERIALES El átomo: Toda la materia está compuesta por átomos y éstos por partículas
TEMA 4. IMPERFECIONES EN SÓLIDOS
 TEMA 4. IMPERFECIONES EN SÓLIDOS En el Tema 3 se ha descrito el SÓLIDO CRISTALINO mediante la aproximación del CRISTAL IDEAL, que tomamos como modelo de perfección cristalina Los sólidos cristalinos reales
TEMA 4. IMPERFECIONES EN SÓLIDOS En el Tema 3 se ha descrito el SÓLIDO CRISTALINO mediante la aproximación del CRISTAL IDEAL, que tomamos como modelo de perfección cristalina Los sólidos cristalinos reales
Diagrama de correlación de enlaces moleculares Antienlace : rojo 1s similar a 2s
 Redes Cristalinas Ciencia de Materiales Ing. en Mecatrónica Otoño 2009 Lilia Meza Montes-IFUAP Diagrama de correlación de enlaces moleculares Antienlace : rojo 1s similar a 2s Sólidos cristalinos y amorfos
Redes Cristalinas Ciencia de Materiales Ing. en Mecatrónica Otoño 2009 Lilia Meza Montes-IFUAP Diagrama de correlación de enlaces moleculares Antienlace : rojo 1s similar a 2s Sólidos cristalinos y amorfos
Estructura de los Sólidos
 Estructura de los Sólidos Estructura Cristalina OBJETIVOS a) Definir sólidos cristalinos y amorfos b) Definir estructura cristalina c) Describir las diferentes estructuras cristalinas d) Utilizar índices
Estructura de los Sólidos Estructura Cristalina OBJETIVOS a) Definir sólidos cristalinos y amorfos b) Definir estructura cristalina c) Describir las diferentes estructuras cristalinas d) Utilizar índices
Síntesis y Caracterización Estructural de los Materiales Ángel Carmelo Prieto Colorado
 Síntesis y Caracterización Estructural de los Materiales Ángel Carmelo Prieto Colorado Física de la Materia Condensada, Cristalografía y Mineralogía. Facultad de Ciencias. Universidad de Valladolid. Estructura
Síntesis y Caracterización Estructural de los Materiales Ángel Carmelo Prieto Colorado Física de la Materia Condensada, Cristalografía y Mineralogía. Facultad de Ciencias. Universidad de Valladolid. Estructura
Estructura Interna de los Materiales
 TEMA III Estructura Interna de los Materiales LECCIÓN 3 Estructura Cristalina y Amorfa 1 3.1 ESTADOS DE LA MATERIA Ciencia y Tecnología de los Materiales La materia puede presentarse en tres estados: gaseoso,
TEMA III Estructura Interna de los Materiales LECCIÓN 3 Estructura Cristalina y Amorfa 1 3.1 ESTADOS DE LA MATERIA Ciencia y Tecnología de los Materiales La materia puede presentarse en tres estados: gaseoso,
Tema 2.- Estructura de la Materia
 BLOQUE II.- ESTRUCTURA Estructura de la Materia * James F. Shackerlford Introducción a la Ciencia de Materiales para Ingenieros. Cuarta edición. Ed. Prentice Hall (1998) * Pat L. Mangonon Ciencia de Materiales:
BLOQUE II.- ESTRUCTURA Estructura de la Materia * James F. Shackerlford Introducción a la Ciencia de Materiales para Ingenieros. Cuarta edición. Ed. Prentice Hall (1998) * Pat L. Mangonon Ciencia de Materiales:
METALES. 1.- Materiales CRISTALINOS y la deformación plástica
 METALES 1.- Materiales CRISTALINOS y la deformación plástica esfuerzo El ensayo de tracción s = F/A 0 s f, resistencia a la fluencia s T, resistencia a la tracción s T, resistencia a la ruptura s= Ke n
METALES 1.- Materiales CRISTALINOS y la deformación plástica esfuerzo El ensayo de tracción s = F/A 0 s f, resistencia a la fluencia s T, resistencia a la tracción s T, resistencia a la ruptura s= Ke n
TEMA 1. ESTRUCTURA INTERNA DE LOS MATERIALES.
 TEMA 1. ESTRUCTURA INTERNA DE LOS MATERIALES. INDICE. 1. EL ATOMO. 2. FUERZAS Y ENERGIAS DE INTERACCION ENTRE ATOMOS. 3. ESTRUCTURA ELECTRÓNICA REACTIVIDAD QUIMICA. 4. TIPOS DE ENLACES ATOMICOS Y MOLECULARES.
TEMA 1. ESTRUCTURA INTERNA DE LOS MATERIALES. INDICE. 1. EL ATOMO. 2. FUERZAS Y ENERGIAS DE INTERACCION ENTRE ATOMOS. 3. ESTRUCTURA ELECTRÓNICA REACTIVIDAD QUIMICA. 4. TIPOS DE ENLACES ATOMICOS Y MOLECULARES.
ALEACIONES 1. INTRODUCCION 2. CLASIFICACION 3. SOLUCIONES SÓLIDAS 4. FASES INTERMEDIAS 5. SOLUCIONES SÓLIDAS ORDENADAS M.V.M.G ALEACIONES 1
 ALEACIONES 1. INTRODUCCION 2. CLASIFICACION 3. SOLUCIONES SÓLIDAS 4. FASES INTERMEDIAS 5. SOLUCIONES SÓLIDAS ORDENADAS 2007-08 ALEACIONES 1 INTRODUCCIÓN Una aleación es la combinación de dos o más metales,
ALEACIONES 1. INTRODUCCION 2. CLASIFICACION 3. SOLUCIONES SÓLIDAS 4. FASES INTERMEDIAS 5. SOLUCIONES SÓLIDAS ORDENADAS 2007-08 ALEACIONES 1 INTRODUCCIÓN Una aleación es la combinación de dos o más metales,
MATERIALES METALICOS 2do Ingeniería Mecánica. Diagramas de Equilibrio de Fases
 MATERIALES METALICOS 2do Ingeniería Mecánica Diagramas de Equilibrio de Fases Ing. Víctor Gómez Universidad Tecnológica Nacional Facultad Regional Tucumán Aleaciones Ø Aleación: Sustancia que tiene propiedades
MATERIALES METALICOS 2do Ingeniería Mecánica Diagramas de Equilibrio de Fases Ing. Víctor Gómez Universidad Tecnológica Nacional Facultad Regional Tucumán Aleaciones Ø Aleación: Sustancia que tiene propiedades
Estructuras Cristalinas más usuales de Metales Puros (y de sus soluciones sólidas) Cristales metálicos
 Estructuras Cristalinas más usuales de Metales Puros (y de sus soluciones sólidas) Reglas generales Para un cristal al equilibrio químico, los átomos se ordenarán en forma regular y compacta, de manera
Estructuras Cristalinas más usuales de Metales Puros (y de sus soluciones sólidas) Reglas generales Para un cristal al equilibrio químico, los átomos se ordenarán en forma regular y compacta, de manera
TEMA 8 ESTRUCTURA CRISTALINA
 Tema 8. Estructura cristalina 1 TEMA 8 ESTRUCTURA CRISTALINA Los sólidos pueden clasificarse: 1.- Por su ordenación: 1a. Sólidos amorfos: tienen una estructura desordenada. Sus átomos o moléculas se colocan
Tema 8. Estructura cristalina 1 TEMA 8 ESTRUCTURA CRISTALINA Los sólidos pueden clasificarse: 1.- Por su ordenación: 1a. Sólidos amorfos: tienen una estructura desordenada. Sus átomos o moléculas se colocan
UNE RAFAEL MARÍA BARALT PROGRAMA DE INGENIERÍA Y TECNOLOGÍA INGENIERÍA EN MTTO MECÁNICO SOLIDIFICACIÓN. Elaborado por: Ing. Roger Chirinos.
 UNE RAFAEL MARÍA BARALT PROGRAMA DE INGENIERÍA Y TECNOLOGÍA INGENIERÍA EN MTTO MECÁNICO SOLIDIFICACIÓN Elaborado por: Ing. Roger Chirinos. MSc Cabimas, Noviembre de 2013 SOLIDIFICACIÓN Fundamentos básicos
UNE RAFAEL MARÍA BARALT PROGRAMA DE INGENIERÍA Y TECNOLOGÍA INGENIERÍA EN MTTO MECÁNICO SOLIDIFICACIÓN Elaborado por: Ing. Roger Chirinos. MSc Cabimas, Noviembre de 2013 SOLIDIFICACIÓN Fundamentos básicos
TEMA 8 SISTEMA PERIÓDICO Y ENLACES
 TEMA 8 SISTEMA PERIÓDICO Y ENLACES 1. LA TABLA PERIÓDICA Elementos químicos son el conjunto de átomos que tienen en común su número atómico, Z. Hoy conocemos 111 elementos diferentes. Los elementos que
TEMA 8 SISTEMA PERIÓDICO Y ENLACES 1. LA TABLA PERIÓDICA Elementos químicos son el conjunto de átomos que tienen en común su número atómico, Z. Hoy conocemos 111 elementos diferentes. Los elementos que
Capítulo 2 La estructura de los sólidos cristalinos
 Capítulo 2 La estructura de los sólidos cristalinos TEMA 2: La estructura de los sólidos cristalinos 1. Los enlaces interatómicos 2. La estructura cristalina 3. Estructuras de empaquetamiento compacto
Capítulo 2 La estructura de los sólidos cristalinos TEMA 2: La estructura de los sólidos cristalinos 1. Los enlaces interatómicos 2. La estructura cristalina 3. Estructuras de empaquetamiento compacto
Materiales de Construcción
 Juan Antonio Polanco Madrazo Soraya Diego Cavia Carlos Thomas García DPTO. DE CIENCIA E INGENIERÍA DEL TERRENO Y DE LOS MATERIALES Este tema se publica bajo Licencia: CreaCve Commons BY- NC- ND 4.0 La
Juan Antonio Polanco Madrazo Soraya Diego Cavia Carlos Thomas García DPTO. DE CIENCIA E INGENIERÍA DEL TERRENO Y DE LOS MATERIALES Este tema se publica bajo Licencia: CreaCve Commons BY- NC- ND 4.0 La
Contenido. 5. Estructura cristalina. Omar De la Peña-Seaman IFUAP Física del Estado Sólido Maestría (Física) 1/51 51
 Contenido 5. Estructura cristalina 1 / Omar De la Peña-Seaman IFUAP Física del Estado Sólido Maestría (Física) 1/51 51 Contenido: Tema 05 5. Estructura cristalina 5.1 Arreglo periódico de átomos: bases,
Contenido 5. Estructura cristalina 1 / Omar De la Peña-Seaman IFUAP Física del Estado Sólido Maestría (Física) 1/51 51 Contenido: Tema 05 5. Estructura cristalina 5.1 Arreglo periódico de átomos: bases,
3. La estructura de sólidos cristalinos 3.1 Conceptos fundamentales 3.2 Celda unitaria 3.3 Redes de Bravias 3.4 Estructuras cristalinas 3.
 Contenido 3. La estructura de sólidos cristalinos 3.1 Conceptos fundamentales 3.2 Celda unitaria 3.3 Redes de Bravias 3.4 Estructuras cristalinas 3.5 Volumen y densidad 3.6 Direcciones y planos cristalográficos
Contenido 3. La estructura de sólidos cristalinos 3.1 Conceptos fundamentales 3.2 Celda unitaria 3.3 Redes de Bravias 3.4 Estructuras cristalinas 3.5 Volumen y densidad 3.6 Direcciones y planos cristalográficos
ESTRUCTURA DE LOS MATERIALES 2. 25/02/2012 Elaboró Ing. Efrén Giraldo T. 1
 ESTRUCTURA DE LOS MATERIALES 2 25/02/2012 Elaboró Ing. Efrén Giraldo T. 1 FACTOR DE EMPAQUETAMIENTO FEA = (No de átomos por celda. Vol de un átomo) / V (celda) 25/02/2012 Elaboró Ing. Efrén Giraldo T.
ESTRUCTURA DE LOS MATERIALES 2 25/02/2012 Elaboró Ing. Efrén Giraldo T. 1 FACTOR DE EMPAQUETAMIENTO FEA = (No de átomos por celda. Vol de un átomo) / V (celda) 25/02/2012 Elaboró Ing. Efrén Giraldo T.
CRISTALOQUÍMICA TEMA 9 POLIMORFISMO Y TRANSFORMACIONES POLIMÓRFICAS. TRANSFORMACIONES ORDEN - DESORDEN ÍNDICE
 CRISTALOQUÍMICA TEMA 9 POLIMORFISMO Y TRANSFORMACIONES POLIMÓRFICAS. TRANSFORMACIONES ORDEN - DESORDEN 9.1 Introducción 9.2 Estabilidad y equilibrio ÍNDICE 9.3 Concepto de polimorfismo y de transformación
CRISTALOQUÍMICA TEMA 9 POLIMORFISMO Y TRANSFORMACIONES POLIMÓRFICAS. TRANSFORMACIONES ORDEN - DESORDEN 9.1 Introducción 9.2 Estabilidad y equilibrio ÍNDICE 9.3 Concepto de polimorfismo y de transformación
Solidificación e Imperfecciones. en Sólidos
 Preguntas definitivas Capítulo 2 Solidificación e Imperfecciones en Sólidos Ciencia de Materiales 28 PREGUNTA 2.1 Cuándo suele presentar interés el uso de un metal en estado puro?. Justifícalo. Pon un
Preguntas definitivas Capítulo 2 Solidificación e Imperfecciones en Sólidos Ciencia de Materiales 28 PREGUNTA 2.1 Cuándo suele presentar interés el uso de un metal en estado puro?. Justifícalo. Pon un
Longitud y energía de enlace
 Longitud y energía de enlace ENLACES QUIMICOS Los enlaces interatómicos se clasifican en: Enlaces iónicos Enlaces covalentes Enlaces metálicos ENLACE IÓNICO: Transferencia de electrones Li F El litio le
Longitud y energía de enlace ENLACES QUIMICOS Los enlaces interatómicos se clasifican en: Enlaces iónicos Enlaces covalentes Enlaces metálicos ENLACE IÓNICO: Transferencia de electrones Li F El litio le
IMPERFECCIONES CRISTALINAS ANA QUIGUANTAR EDWIN RODRIGUES JEISON CORDOBA
 IMPERFECCIONES CRISTALINAS ANA QUIGUANTAR EDWIN RODRIGUES JEISON CORDOBA CORPORACION UNIVERSITARIA AUTONOMA DE NARIÑO FACULTAD DE INGENIERIA MECANICA SEGUNDO SEMESTRE CIENCIA DE LOS MATERIALES SAN JUAN
IMPERFECCIONES CRISTALINAS ANA QUIGUANTAR EDWIN RODRIGUES JEISON CORDOBA CORPORACION UNIVERSITARIA AUTONOMA DE NARIÑO FACULTAD DE INGENIERIA MECANICA SEGUNDO SEMESTRE CIENCIA DE LOS MATERIALES SAN JUAN
Tema 20 Propiedades eléctricas de los materiales.
 Tema 20 Propiedades eléctricas de los materiales. Las propiedades eléctricas miden la respuesta del material cuando se le aplica un campo eléctrico. Conductividad eléctrica R i = V ; R= resistencia del
Tema 20 Propiedades eléctricas de los materiales. Las propiedades eléctricas miden la respuesta del material cuando se le aplica un campo eléctrico. Conductividad eléctrica R i = V ; R= resistencia del
ESTRUCTURAS CRISTALINAS (P2)
 ESTRUCTURAS CRISTALINAS (P2) Objetivos - Visualización de estructuras de sólidos mediante el uso de modelos - Estudio de redes cristalinas basadas en ordenamientos de esferas de igual tamaño - Identificación
ESTRUCTURAS CRISTALINAS (P2) Objetivos - Visualización de estructuras de sólidos mediante el uso de modelos - Estudio de redes cristalinas basadas en ordenamientos de esferas de igual tamaño - Identificación
DEFECTOS E IMPERFECCIONES CRISTALINAS
 DEFECTOS E IMPERFECCIONES CRISTALINAS Realmente no existen cristales perfectos sino que contienen varios tipos de imperfecciones y defectos, que afectan a muchas de sus propiedades físicas y mecánicas
DEFECTOS E IMPERFECCIONES CRISTALINAS Realmente no existen cristales perfectos sino que contienen varios tipos de imperfecciones y defectos, que afectan a muchas de sus propiedades físicas y mecánicas
Estructura Atómica y Cristalina. Departamento de Tecnología IES San José
 1. INTRODUCCIÓN. Las propiedades y comportamiento de los materiales dependen, principalmente de su constitución y de su estructura. Por ello estudiaremos la disposición geométrica de los átomos y las interacciones
1. INTRODUCCIÓN. Las propiedades y comportamiento de los materiales dependen, principalmente de su constitución y de su estructura. Por ello estudiaremos la disposición geométrica de los átomos y las interacciones
PORTAFOLIO DE EVIDENCIAS QUÍMICA I DE SEGUNDA OPORTUNIDAD I LEE DETENIDAMENTE CADA ENUNCIADO Y CONTESTA SEGÚN SE TE PIDA.
 PORTAFOLIO DE EVIDENCIAS QUÍMICA I DE SEGUNDA OPORTUNIDAD I LEE DETENIDAMENTE CADA ENUNCIADO Y CONTESTA SEGÚN SE TE PIDA. 1.- Ciencia que estudia las características y la composición de los materiales,
PORTAFOLIO DE EVIDENCIAS QUÍMICA I DE SEGUNDA OPORTUNIDAD I LEE DETENIDAMENTE CADA ENUNCIADO Y CONTESTA SEGÚN SE TE PIDA. 1.- Ciencia que estudia las características y la composición de los materiales,
ENLACE QUÍMICO 2º BACH EJERCICIOS DE ENLACE QUÍMICO DEL LIBRO 28. H-CHO H C = O : CH 3 OH H C O H H H H C O C H H H CH 3 OCH 3
 EJERCICIOS DE ENLACE QUÍMICO DEL LIBRO 28. -CO C = O : C 3 O C O C 3 OC 3 C O C a) La longitud de enlace CO es menor en el formaldehido, ya que tiene un doble enlace. b) El metanol puede formar enlaces
EJERCICIOS DE ENLACE QUÍMICO DEL LIBRO 28. -CO C = O : C 3 O C O C 3 OC 3 C O C a) La longitud de enlace CO es menor en el formaldehido, ya que tiene un doble enlace. b) El metanol puede formar enlaces
Actividad: Cómo son las configuraciones electrónicas?
 Cómo son las configuraciones electrónicas de los elementos que forman una familia? Nivel: 2º Medio Subsector: Ciencias químicas Unidad temática: Actividad: Cómo son las configuraciones electrónicas? En
Cómo son las configuraciones electrónicas de los elementos que forman una familia? Nivel: 2º Medio Subsector: Ciencias químicas Unidad temática: Actividad: Cómo son las configuraciones electrónicas? En
Los elementos químicos
 Los elementos químicos Física y Química Las primeras clasificaciones de los elementos Oxford University Press España, S. A. Física y Química 3º ESO 2 Un elemento químico es un tipo de materia constituido
Los elementos químicos Física y Química Las primeras clasificaciones de los elementos Oxford University Press España, S. A. Física y Química 3º ESO 2 Un elemento químico es un tipo de materia constituido
OBJETIVO.- Diferenciar los distintos tipos de enlace químico para establecer las propiedades de cada compuesto.
 OBJETIVO.- Diferenciar los distintos tipos de enlace químico para establecer las propiedades de cada compuesto. 1. Generalidades de los enlaces químicos Los enlaces químicos, son las fuerzas que mantienen
OBJETIVO.- Diferenciar los distintos tipos de enlace químico para establecer las propiedades de cada compuesto. 1. Generalidades de los enlaces químicos Los enlaces químicos, son las fuerzas que mantienen
FÍSICA Y QUÍMICA Solucionario ELECTRONES Y ENLACES
 FÍSICA Y QUÍMICA Solucionario ELECTRONES Y ENLACES 1.* Indicad cuántos electrones tienen en la última capa cada uno de estos elementos. a) C 4 f) O 6 k) K 1 b) F 7 g) P 5 l) S 6 c) Ne 8 h) H 1 m) He 8
FÍSICA Y QUÍMICA Solucionario ELECTRONES Y ENLACES 1.* Indicad cuántos electrones tienen en la última capa cada uno de estos elementos. a) C 4 f) O 6 k) K 1 b) F 7 g) P 5 l) S 6 c) Ne 8 h) H 1 m) He 8
1817: Döbreiner. Triadas de elementos con propiedades semejantes. 1865: Newlands. Ley de las octavas. Ordenó 55 elementos.
 Evolución histórica de la Tabla Periódica 1817: Döbreiner. Triadas de elementos con propiedades semejantes. 1865: Newlands. Ley de las octavas. Ordenó 55 elementos. 1869: Mendeleev y Meyer: las propiedades
Evolución histórica de la Tabla Periódica 1817: Döbreiner. Triadas de elementos con propiedades semejantes. 1865: Newlands. Ley de las octavas. Ordenó 55 elementos. 1869: Mendeleev y Meyer: las propiedades
Estructura Cristalina de Sólidos
 Estructura Cristalina de Sólidos Relación entre estructura periódica y propiedades Bibliografía: 1. Solid State Physics. Ashcroft and Mermin. 2. Solid State Chemistry. West. 3. Química del Estado Sólido.
Estructura Cristalina de Sólidos Relación entre estructura periódica y propiedades Bibliografía: 1. Solid State Physics. Ashcroft and Mermin. 2. Solid State Chemistry. West. 3. Química del Estado Sólido.
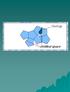 Caso de varios vectores primitivos de un mismo arreglo. Base o Motivo: Átomo o conjunto de átomos que se asocian con un punto de la malla Malla o Lattice: Es un arreglo infinito de puntos en el espacio,
Caso de varios vectores primitivos de un mismo arreglo. Base o Motivo: Átomo o conjunto de átomos que se asocian con un punto de la malla Malla o Lattice: Es un arreglo infinito de puntos en el espacio,
El Modelo Moderno y resultados de nuestro interés
 CLASES 3 Y 4 ESTRUCTURA ELECTRÓNICA DE LOS ELEMENTOS AL ESTADO FUNDAMENTAL. TABLA PERIÓDICA. ELECTRONEGATIVIDAD. El Modelo Moderno y resultados de nuestro interés Así es como el Modelo Moderno (MM) reemplazó
CLASES 3 Y 4 ESTRUCTURA ELECTRÓNICA DE LOS ELEMENTOS AL ESTADO FUNDAMENTAL. TABLA PERIÓDICA. ELECTRONEGATIVIDAD. El Modelo Moderno y resultados de nuestro interés Así es como el Modelo Moderno (MM) reemplazó
Siete sistemas y catorce retículos
 ESTRUCTURA CRISTALINA - PERFECCION Siete sistemas y catorce retículos Celda unitaria c a b Constantes reticulares o parámetros reticulares Longitud de los bordes Ángulos entre los ejes cristalográficos
ESTRUCTURA CRISTALINA - PERFECCION Siete sistemas y catorce retículos Celda unitaria c a b Constantes reticulares o parámetros reticulares Longitud de los bordes Ángulos entre los ejes cristalográficos
FÍSICA Y QUÍMICA 3º ESO ACTIVIDADES DE RECUPERACIÓN
 FÍSICA Y QUÍMICA 3º ESO ACTIVIDADES DE RECUPERACIÓN (PARTE 2) CURSO 2012/13 Nombre y apellidos: 1 LA CIENCIA Y SU MÉTODO. MEDIDA DE MAGNITUDES LOS ÁTOMOS Y SU COMPLEJIDAD 1. Qué explica el modelo atómico
FÍSICA Y QUÍMICA 3º ESO ACTIVIDADES DE RECUPERACIÓN (PARTE 2) CURSO 2012/13 Nombre y apellidos: 1 LA CIENCIA Y SU MÉTODO. MEDIDA DE MAGNITUDES LOS ÁTOMOS Y SU COMPLEJIDAD 1. Qué explica el modelo atómico
Materiales: Estructura interna y propiedades
 Materiales: Estructura interna y propiedades Para satisfacer esa curiosidad que muestra el protagonista de nuestra historia, va a hacer como los detectives de algunas películas: mirar los materiales con
Materiales: Estructura interna y propiedades Para satisfacer esa curiosidad que muestra el protagonista de nuestra historia, va a hacer como los detectives de algunas películas: mirar los materiales con
Capítulo 2 La estructura de los sólidos cristalinos
 Capítulo 2 La estructura de los sólidos cristalinos TEMA 2: La estructura de los sólidos cristalinos 1. Los enlaces interatómicos 2. La estructura cristalina 3. Estructuras cristalinas compactas 4. Direcciones
Capítulo 2 La estructura de los sólidos cristalinos TEMA 2: La estructura de los sólidos cristalinos 1. Los enlaces interatómicos 2. La estructura cristalina 3. Estructuras cristalinas compactas 4. Direcciones
PRIMERAS CLASIFICACIONES PERIÓDICAS
 LA TABLA PERIÓDICA PRIMERAS CLASIFICACIONES PERIÓDICAS Cuando a principios del siglo XIX se midieron las masas atómicas de una gran cantidad de elementos, se observó que ciertas propiedades variaban periódicamente
LA TABLA PERIÓDICA PRIMERAS CLASIFICACIONES PERIÓDICAS Cuando a principios del siglo XIX se midieron las masas atómicas de una gran cantidad de elementos, se observó que ciertas propiedades variaban periódicamente
Profesor: Carlos Gutiérrez Arancibia. Temas a tratar: - - Sustancias Puras - Mezclas - Enlaces Químicos - Fuerzas Intermoleculares
 Profesor: Carlos Gutiérrez Arancibia Temas a tratar: - - Sustancias Puras - Mezclas - Enlaces Químicos - Fuerzas Intermoleculares A. Sustancia Pura: SUSTANCIAS PURAS Y MEZCLAS Una sustancia pura es un
Profesor: Carlos Gutiérrez Arancibia Temas a tratar: - - Sustancias Puras - Mezclas - Enlaces Químicos - Fuerzas Intermoleculares A. Sustancia Pura: SUSTANCIAS PURAS Y MEZCLAS Una sustancia pura es un
Física y Química 3º ESO
 1. Física y Química. Ciencias de la medida forman parte de las necesitan Ciencias de la naturaleza medir las propiedades de los cuerpos que se dividen en para lo cual se emplean lo que siempre conlleva
1. Física y Química. Ciencias de la medida forman parte de las necesitan Ciencias de la naturaleza medir las propiedades de los cuerpos que se dividen en para lo cual se emplean lo que siempre conlleva
La tabla periódica es la estrella orientadora para la exploración en el capo de la química, la física, la mineralogía y la técnica.
 SISTEMA PERIÓDICO DE LOS ELEMENTOS La tabla periódica es la estrella orientadora para la exploración en el capo de la química, la física, la mineralogía y la técnica. Niels Bohr Principio de exclusión
SISTEMA PERIÓDICO DE LOS ELEMENTOS La tabla periódica es la estrella orientadora para la exploración en el capo de la química, la física, la mineralogía y la técnica. Niels Bohr Principio de exclusión
Técnico Profesional QUÍMICA
 Programa Técnico Profesional QUÍMICA Geometría molecular Nº Ejercicios PSU 1. La siguiente figura muestra la estructura del gas metano. C Al respecto, qué valor adopta el ángulo de enlace en este compuesto?
Programa Técnico Profesional QUÍMICA Geometría molecular Nº Ejercicios PSU 1. La siguiente figura muestra la estructura del gas metano. C Al respecto, qué valor adopta el ángulo de enlace en este compuesto?
Tema 2 Estructuras Cristalinas
 Tema 2 Estructuras Cristalinas Para poder comprender las propiedades de los materiales, y poder por tanto seleccionar el material idóneo para una aplicación específica, se hace necesario comprender la
Tema 2 Estructuras Cristalinas Para poder comprender las propiedades de los materiales, y poder por tanto seleccionar el material idóneo para una aplicación específica, se hace necesario comprender la
Docente: Raquel Villafrades Torres. Química General
 Propiedades Periódicas Docente: Raquel Villafrades Torres Química General UPB Introducción Las propiedades periódicas son aquellas que varían de forma regular por la posición que ocupan los elementos en
Propiedades Periódicas Docente: Raquel Villafrades Torres Química General UPB Introducción Las propiedades periódicas son aquellas que varían de forma regular por la posición que ocupan los elementos en
Estructura cristalina: Índices de Miller. Y en términos de grado de compacidad? Volumen de átomos= Volumen de la celda= ( ) 3
 1 Cuántos átomos hay en una celda unidad? Vértices 1/8 Caras 1/2 Número total de átomos en la celda unidad: 8 en los vértices: 8 x 1/8 = 1 6 en las caras: 6 x 1/2 = 3 Total: 4 átomos Y en términos de grado
1 Cuántos átomos hay en una celda unidad? Vértices 1/8 Caras 1/2 Número total de átomos en la celda unidad: 8 en los vértices: 8 x 1/8 = 1 6 en las caras: 6 x 1/2 = 3 Total: 4 átomos Y en términos de grado
ESTRUCTURA Y CRISTALIZACION DE LOS METALES
 Materiales Metálicos 2do. Ingeniería Mecánica ESTRUCTURA Y CRISTALIZACION DE LOS METALES Ing. Víctor Gómez U. T. N Facultad Regional Tucumán METALURGIA FISICA Es la ciencia que se ocupa de estudiar las
Materiales Metálicos 2do. Ingeniería Mecánica ESTRUCTURA Y CRISTALIZACION DE LOS METALES Ing. Víctor Gómez U. T. N Facultad Regional Tucumán METALURGIA FISICA Es la ciencia que se ocupa de estudiar las
La presencia del estado sólido en la materia que nos rodea es constante. El arreglo de sus moléculas o iones es uniforme.
 2.7 ESTRUCTURA DE LOS MATERIALES. 2.7.1 ESTADO SÓLIDO (CRISTALINO). La presencia del estado sólido en la materia que nos rodea es constante. El arreglo de sus moléculas o iones es uniforme. En los gases
2.7 ESTRUCTURA DE LOS MATERIALES. 2.7.1 ESTADO SÓLIDO (CRISTALINO). La presencia del estado sólido en la materia que nos rodea es constante. El arreglo de sus moléculas o iones es uniforme. En los gases
Propiedades Periódicas y Propiedades de los elementos
 Propiedades Periódicas y Propiedades de los elementos Se denominan propiedades periódicas, aquellas que tienen una tendencia de variación de acuerdo a la ubicación de los elementos en la tabla periódica.
Propiedades Periódicas y Propiedades de los elementos Se denominan propiedades periódicas, aquellas que tienen una tendencia de variación de acuerdo a la ubicación de los elementos en la tabla periódica.
GEOMETRÍA DE LOS CRISTALES I
 CAPÍTULO 4 GEOMETRÍA DE LOS CRISTALES I 4.1 REDES Conjuntos de puntos imaginarios que tienen una relación fija en el espacio constituyendo un armazón sobre el cual el cristal se construye. En la Figura
CAPÍTULO 4 GEOMETRÍA DE LOS CRISTALES I 4.1 REDES Conjuntos de puntos imaginarios que tienen una relación fija en el espacio constituyendo un armazón sobre el cual el cristal se construye. En la Figura
Características de los materiales sólidos
 Características de los materiales sólidos Los materiales sólidos metálicos presentan una serie de propiedades que les otorgan la característica de ser una fuente importante de aplicaciones tecnológicas.
Características de los materiales sólidos Los materiales sólidos metálicos presentan una serie de propiedades que les otorgan la característica de ser una fuente importante de aplicaciones tecnológicas.
CAPITULO II. DISPOSITIVOS SEMICONDUCTORES.
 CAPITULO II. DISPOSITIVOS SEMICONDUCTORES. Tema 4. SEMICONDUCTORES. Las características físicas que permiten distinguir entre un aislante, un semiconductor y un metal, están determinadas por la estructura
CAPITULO II. DISPOSITIVOS SEMICONDUCTORES. Tema 4. SEMICONDUCTORES. Las características físicas que permiten distinguir entre un aislante, un semiconductor y un metal, están determinadas por la estructura
Tema 9. SOLIDOS COVALENTES
 Tema 9. SOLIDOS COVALENTES Introducción Estructuras de no-metales Boro Carbono Fósforo Arsénico, Antimonio y Bismuto Selenio y Telurio Estructuras de óxidos Estructuras basadas en tetraedros Estructuras
Tema 9. SOLIDOS COVALENTES Introducción Estructuras de no-metales Boro Carbono Fósforo Arsénico, Antimonio y Bismuto Selenio y Telurio Estructuras de óxidos Estructuras basadas en tetraedros Estructuras
A su vez, una molécula está compuesta por átomos. Cada uno de ellos posee unas propiedades diferentes en el interior de la molécula que constituyen.
 Constitución de la materia. Supongamos que cualquier sustancia de la naturaleza la dividimos en partes cada vez más pequeñas, conservando cada una de ellas las propiedades de la sustancia inicial. Si seguimos
Constitución de la materia. Supongamos que cualquier sustancia de la naturaleza la dividimos en partes cada vez más pequeñas, conservando cada una de ellas las propiedades de la sustancia inicial. Si seguimos
Enlace Químico. Colegio San Esteban Diácono Departamento de Ciencias Química Iº Medio Prof. Juan Pastrián / Sofía Ponce de León
 Enlace Químico Colegio San Esteban Diácono Departamento de Ciencias Química Iº Medio Prof. Juan Pastrián / Sofía Ponce de León Objetivos u u u u u Comprender la interacción entre átomos a partir de su
Enlace Químico Colegio San Esteban Diácono Departamento de Ciencias Química Iº Medio Prof. Juan Pastrián / Sofía Ponce de León Objetivos u u u u u Comprender la interacción entre átomos a partir de su
Una mezcla es un compuesto formado por varias sustancias con distintas propiedades
 COMPOSICIÓN DE LA MATERIA Mezclas homogéneas y heterogéneas Una mezcla es un compuesto formado por varias sustancias con distintas propiedades Algunos sistemas materiales como la leche a simple vista parecen
COMPOSICIÓN DE LA MATERIA Mezclas homogéneas y heterogéneas Una mezcla es un compuesto formado por varias sustancias con distintas propiedades Algunos sistemas materiales como la leche a simple vista parecen
Explicación de las propiedades y los estados de agregación en los compuestos químicos en función de los tipos de enlace. vs.
 Explicación de las propiedades y los estados de agregación en los compuestos químicos en función de los tipos de enlace. vs. Usar las propiedades y los estados de agregación en los compuestos químicos
Explicación de las propiedades y los estados de agregación en los compuestos químicos en función de los tipos de enlace. vs. Usar las propiedades y los estados de agregación en los compuestos químicos
IEO-394 Semiconductores. Juan E. Martínez P. Docente. UdeA
 IEO-394 Semiconductores Juan E. Martínez P. Docente. UdeA Bandas de Energía Y Corrientes de Portadores en Semiconductores. PARTICION DE LOS NIVELES DE ENERGIA A medida que se traen juntos N átomos Cada
IEO-394 Semiconductores Juan E. Martínez P. Docente. UdeA Bandas de Energía Y Corrientes de Portadores en Semiconductores. PARTICION DE LOS NIVELES DE ENERGIA A medida que se traen juntos N átomos Cada
2. ESTRUCTURA DE LOS SÓLIDOS CRISTALINOS
 . ESTRUCTURA DE LOS SÓLIDOS CRISTALINOS MATERIALES 1/14 ÍNDICE 1. CONCEPTOS GENERALES. CELDILLA CRISTALINA. SISTEMAS CRISTALINOS. REDES DE BRAVAIS 4. DENSIDAD Y FACTOR DE EMPAQUETAMIENTO 5. ESTRUCTURAS
. ESTRUCTURA DE LOS SÓLIDOS CRISTALINOS MATERIALES 1/14 ÍNDICE 1. CONCEPTOS GENERALES. CELDILLA CRISTALINA. SISTEMAS CRISTALINOS. REDES DE BRAVAIS 4. DENSIDAD Y FACTOR DE EMPAQUETAMIENTO 5. ESTRUCTURAS
SOLUCIONARIO Guía Estándar Anual
 SOLUCIONARIO Guía Estándar Anual El enlace químico SGUICES004CB33-A16V1 Ítem Alternativa Habilidad 1 E Reconocimiento 2 B Aplicación 3 C Comprensión 4 D Comprensión 5 D Aplicación 6 D Aplicación 7 D Comprensión
SOLUCIONARIO Guía Estándar Anual El enlace químico SGUICES004CB33-A16V1 Ítem Alternativa Habilidad 1 E Reconocimiento 2 B Aplicación 3 C Comprensión 4 D Comprensión 5 D Aplicación 6 D Aplicación 7 D Comprensión
DIFUSIÓN UNIVERSIDAD TECNOLÓGICA DE PEREIRA TECNOLOGIA MECANICA
 DIFUSIÓN UNIVERSIDAD TECNOLÓGICA DE PEREIRA TECNOLOGIA MECANICA 1 CONTENIDO Concepto de difusión Mecanismos de difusión Difusión en régimen permanente y en régimen transitório Fatores que influeyen en
DIFUSIÓN UNIVERSIDAD TECNOLÓGICA DE PEREIRA TECNOLOGIA MECANICA 1 CONTENIDO Concepto de difusión Mecanismos de difusión Difusión en régimen permanente y en régimen transitório Fatores que influeyen en
LA TABLA PERIÓDICA. Cuestiones generales. Propiedades periódicas
 Cuestiones generales. LA TABLA PERIÓDICA. 1.- Indica el nombre, símbolo, nombre del grupo a que pertenece y periodo de los elementos de números atómicos 3, 9, 16, 19, 38 y 51. 2.- a) Indica el nombre,
Cuestiones generales. LA TABLA PERIÓDICA. 1.- Indica el nombre, símbolo, nombre del grupo a que pertenece y periodo de los elementos de números atómicos 3, 9, 16, 19, 38 y 51. 2.- a) Indica el nombre,
Unidad 3 Curso: Química General 1 Mtra. Norma Mónica López.
 Unidad 3 Curso: Química General 1 Mtra. Norma Mónica López. Interacciones eléctricas De atracción +, - De repulsión +, + ó -,- Entre Átomos de una misma molécula Moléculas vecinas 2 ENLACE QUÍMICO Siempre
Unidad 3 Curso: Química General 1 Mtra. Norma Mónica López. Interacciones eléctricas De atracción +, - De repulsión +, + ó -,- Entre Átomos de una misma molécula Moléculas vecinas 2 ENLACE QUÍMICO Siempre
QUÍMICA FUNDAMENTAL. Tabla Periódica
 QUÍMICA FUNDAMENTAL Tabla Periódica 1 TEMAS DE ESTUDIO Construcción de la Tabla Periódica con base en la configuración electrónica Propiedades periódicas de los elementos 2 ANTECEDENTES HISTÓRICOS: ELEMENTOS
QUÍMICA FUNDAMENTAL Tabla Periódica 1 TEMAS DE ESTUDIO Construcción de la Tabla Periódica con base en la configuración electrónica Propiedades periódicas de los elementos 2 ANTECEDENTES HISTÓRICOS: ELEMENTOS
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2010 QUÍMICA TEMA 3: ENLACES QUÍMICOS
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 010 QUÍMICA TEMA : ENLACES QUÍMICOS Junio, Ejercicio, Opción A Reserva 1, Ejercicio, Opción A Reserva, Ejercicio, Opción B Reserva, Ejercicio, Opción B Septiembre,
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 010 QUÍMICA TEMA : ENLACES QUÍMICOS Junio, Ejercicio, Opción A Reserva 1, Ejercicio, Opción A Reserva, Ejercicio, Opción B Reserva, Ejercicio, Opción B Septiembre,
III. DIFUSION EN SOLIDOS
 Metalografía y Tratamientos Térmicos III - 1 - III. DIFUSION EN SOLIDOS III.1. Velocidad de procesos en sólidos Muchos procesos de producción y aplicaciones en materiales de ingeniería están relacionados
Metalografía y Tratamientos Térmicos III - 1 - III. DIFUSION EN SOLIDOS III.1. Velocidad de procesos en sólidos Muchos procesos de producción y aplicaciones en materiales de ingeniería están relacionados
PROPIEDADES PERIÓDICAS DE LOS ELEMENTOS. LA TABLA PERIÓDICA.
 PROPIEDADES PERIÓDICAS DE LOS ELEMENTOS. LA TABLA PERIÓDICA. A partir de la posición de los elementos en la tabla periódica formando grupos y períodos podemos deducir la evolución de algunas propiedades
PROPIEDADES PERIÓDICAS DE LOS ELEMENTOS. LA TABLA PERIÓDICA. A partir de la posición de los elementos en la tabla periódica formando grupos y períodos podemos deducir la evolución de algunas propiedades
ENLACES QUÍMICOS. Los enlaces químicos, son las fuerzas que mantienen unidos a los átomos.
 1. Generalidades de los enlaces químicos ENLACES QUÍMICOS Los enlaces químicos, son las fuerzas que mantienen unidos a los átomos. Cuando los átomos se enlazan entre sí, ceden, aceptan o comparten electrones.
1. Generalidades de los enlaces químicos ENLACES QUÍMICOS Los enlaces químicos, son las fuerzas que mantienen unidos a los átomos. Cuando los átomos se enlazan entre sí, ceden, aceptan o comparten electrones.
UNIDAD 1: LA MATERIA CRISTALINA
 UNIDAD 1: LA MATERIA CRISTALINA CONCEPTOS MATERIA CRISTALINA: Aquella cuyas partículas están perfectamente ordenadas en el espacio, ocupando posiciones fijas y a distancias regulares unas de otras, formando
UNIDAD 1: LA MATERIA CRISTALINA CONCEPTOS MATERIA CRISTALINA: Aquella cuyas partículas están perfectamente ordenadas en el espacio, ocupando posiciones fijas y a distancias regulares unas de otras, formando
ACTIVIDAD ACUMULATIVA
 1 Primer Semestre ACTIVIDAD ACUMULATIVA ENLACE QUÍMICO ESTRUCTURA DE LEWIS NOMBRE: NOTA (ACUMULATIVA): CURSO: 1º MEDIO PUNTAJE: FECA: Objetivos: 1. Comprender los aspectos esenciales del modelo atómico
1 Primer Semestre ACTIVIDAD ACUMULATIVA ENLACE QUÍMICO ESTRUCTURA DE LEWIS NOMBRE: NOTA (ACUMULATIVA): CURSO: 1º MEDIO PUNTAJE: FECA: Objetivos: 1. Comprender los aspectos esenciales del modelo atómico
Química Inorgánica Bloque d 1. BLOQUE d
 Química Inorgánica Bloque d 1 BLOQUE d Los elementos del bloque d están ubicados entre los grupos 2 y 13 de la tabla periódica y se los suele llamar metales de transición. elemento de transición: es un
Química Inorgánica Bloque d 1 BLOQUE d Los elementos del bloque d están ubicados entre los grupos 2 y 13 de la tabla periódica y se los suele llamar metales de transición. elemento de transición: es un
Tabla Periódica y Propiedades Periódicas
 Tabla Periódica y Propiedades Periódicas Primeras clasificaciones periódicas. Fines S. XVIII Metales y no metales. 1829, Döbereiner Tríadas de comportamiento químico similar. A principios del siglo XIX
Tabla Periódica y Propiedades Periódicas Primeras clasificaciones periódicas. Fines S. XVIII Metales y no metales. 1829, Döbereiner Tríadas de comportamiento químico similar. A principios del siglo XIX
Las que tienen relación con el de tamaño: LAS PROPIEDADES PERIÓDICAS. Se pueden separar en dos grupos: PERIODICIDAD
 LAS PROPIEDADES PERIÓDICAS Se pueden separar en dos grupos: 1- Las que tienen relación con el de tamaño: Los radios atómicos y los radios iónicos o cristalinos. La densidad. (ρ) El punto de fusión y ebullición.
LAS PROPIEDADES PERIÓDICAS Se pueden separar en dos grupos: 1- Las que tienen relación con el de tamaño: Los radios atómicos y los radios iónicos o cristalinos. La densidad. (ρ) El punto de fusión y ebullición.
1.1 Definición de semiconductor
 Índice 1.- Introducción 1.1- Definición 1.2-Modelo de bandas de energía 1.3- Materiales intrínseco y extrínseco 2.-Tipos de materiales semiconductores 2.1- Estequiométricos (aislantes) 2.2- Imperfecciones
Índice 1.- Introducción 1.1- Definición 1.2-Modelo de bandas de energía 1.3- Materiales intrínseco y extrínseco 2.-Tipos de materiales semiconductores 2.1- Estequiométricos (aislantes) 2.2- Imperfecciones
PREGUNTAS PRUEBAS PAU MATERIALES
 PREGUNTAS PRUEBAS PAU MATERIALES JUNIO 2010 FE Opción A Defina brevemente las siguientes propiedades que presentan los compuestos metálicos: a) Elasticidad (0,5 puntos) b) Tenacidad (0,5 puntos) c) Maleabilidad
PREGUNTAS PRUEBAS PAU MATERIALES JUNIO 2010 FE Opción A Defina brevemente las siguientes propiedades que presentan los compuestos metálicos: a) Elasticidad (0,5 puntos) b) Tenacidad (0,5 puntos) c) Maleabilidad
Unidad I: Propiedades Periódicas: Masa y Enlace
 Unidad I: Propiedades Periódicas: Masa y Enlace 1. Nociones de teoría atómica moderna 2. Propiedades periódicas de los elementos 3. Enlace iónico y covalente 4. Masas atómicas y moleculares 1. Nociones
Unidad I: Propiedades Periódicas: Masa y Enlace 1. Nociones de teoría atómica moderna 2. Propiedades periódicas de los elementos 3. Enlace iónico y covalente 4. Masas atómicas y moleculares 1. Nociones
La estructura cristalina de los metales
 La estructura cristalina de los metales Moisés Hinojosa* INTRODUCCIÓN Dentro del universo de los materiales para ingeniería, los metales ocupan un lugar preponderante. En nuestra región, la industria metal-mecánica
La estructura cristalina de los metales Moisés Hinojosa* INTRODUCCIÓN Dentro del universo de los materiales para ingeniería, los metales ocupan un lugar preponderante. En nuestra región, la industria metal-mecánica
LA TABLA PERIÓDICA. 1
 LA TABLA PERIÓDICA. 1 Clasificación de Mendeleiev Clasificó lo 63 elementos conocidos utilizando el criterio de masa atómica creciente, ya que no se conocía el concepto de número atómico puesto que no
LA TABLA PERIÓDICA. 1 Clasificación de Mendeleiev Clasificó lo 63 elementos conocidos utilizando el criterio de masa atómica creciente, ya que no se conocía el concepto de número atómico puesto que no
3.1. Estructura atómica
 3.1. Estructura atómica Átomo Protones (+) Núcleo Neutrones (sin carga) Corteza Electrones (-) *Z Número atómico = Número de protones. Cuando el átomo está en estado neutro, Z también es equivalente al
3.1. Estructura atómica Átomo Protones (+) Núcleo Neutrones (sin carga) Corteza Electrones (-) *Z Número atómico = Número de protones. Cuando el átomo está en estado neutro, Z también es equivalente al
TEMA 3: DIAGRAMAS DE EQUILIBRIO
 TEMA 3: DIAGRAMAS DE EQUILIBRIO 1.- Aleaciones Características Los metales puros tienen poca aplicación en la industria. La mayoría de ellos se combinan con otros metales o no metales para mejorar sus
TEMA 3: DIAGRAMAS DE EQUILIBRIO 1.- Aleaciones Características Los metales puros tienen poca aplicación en la industria. La mayoría de ellos se combinan con otros metales o no metales para mejorar sus
Enlaces Primarios o fuertes Secundarios o débiles
 Capítulo III MET 2217 Tipos de enlaces atómicos y moleculares Enlaces Primarios o fuertes Secundarios o débiles Enlaces primarios Iónico Actúan fuerzas intermoleculares relativamente grandes, electrostáticas.
Capítulo III MET 2217 Tipos de enlaces atómicos y moleculares Enlaces Primarios o fuertes Secundarios o débiles Enlaces primarios Iónico Actúan fuerzas intermoleculares relativamente grandes, electrostáticas.
Resolución de ejercicios PRÁCTICO 12
 Resolución de ejercicios PRÁCTIC 12 1) a) bservando la estructura de Lewis de la molécula BeH 2 podemos decir que el átomo de Be se une a dos átomos de H mediante dos enlaces simples. Una hibridación de
Resolución de ejercicios PRÁCTIC 12 1) a) bservando la estructura de Lewis de la molécula BeH 2 podemos decir que el átomo de Be se une a dos átomos de H mediante dos enlaces simples. Una hibridación de
Tema 1.3 Estados de agregación de la materia. Tema 1.4 Composición de la materia
 Tema 1.3 Estados de agregación de la materia Tema 1.4 Composición de la materia 1 MATERIA Todo aquello que ocupa un lugar en el espacio, tiene una energía medible y está sujeto a cambios en el tiempo y
Tema 1.3 Estados de agregación de la materia Tema 1.4 Composición de la materia 1 MATERIA Todo aquello que ocupa un lugar en el espacio, tiene una energía medible y está sujeto a cambios en el tiempo y
Química Inorgánica Ingeniería Química
 Química Inorgánica Ingeniería Química Examen final 28 de enero de 2005 Contesta a las siguientes cuestiones. Utiliza para ello el espacio proporcionado. Si te hiciera falta más espacio utiliza la cara
Química Inorgánica Ingeniería Química Examen final 28 de enero de 2005 Contesta a las siguientes cuestiones. Utiliza para ello el espacio proporcionado. Si te hiciera falta más espacio utiliza la cara
Contenido. 3.- Carga nuclear efectiva y reactividad. 4.- Propiedades periódicas:
 LA TABLA PERIÓDICA Contenido Primeras clasificaciones periódicas. 1.1. Sistema periódico de Mendeleiev. 2.- La tabla periódica. 2.1. Ley de Moseley. 3.- Carga nuclear efectiva y reactividad. 4.- Propiedades
LA TABLA PERIÓDICA Contenido Primeras clasificaciones periódicas. 1.1. Sistema periódico de Mendeleiev. 2.- La tabla periódica. 2.1. Ley de Moseley. 3.- Carga nuclear efectiva y reactividad. 4.- Propiedades
Estudio del átomo: 1. Átomos e isótopos 2. Modelos Atómicos 3. Teoría cuántica. Ing. Sol de María Jiménez González
 Estudio del átomo: 1. Átomos e isótopos 2. Modelos Atómicos 3. Teoría cuántica 1 Núcleo: protones y neutrones Los electrones se mueven alrededor. Característica Partículas Protón Neutrón Electrón Símbolo
Estudio del átomo: 1. Átomos e isótopos 2. Modelos Atómicos 3. Teoría cuántica 1 Núcleo: protones y neutrones Los electrones se mueven alrededor. Característica Partículas Protón Neutrón Electrón Símbolo
Propiedades magnéticas
 Propiedades magnéticas Fuerzas magnéticas Las fuerzas magnéticas se generan mediante el movimiento de partículas cargadas Eléctricamente; existen junto a las fuerzas electrostáticas. Distribuciones del
Propiedades magnéticas Fuerzas magnéticas Las fuerzas magnéticas se generan mediante el movimiento de partículas cargadas Eléctricamente; existen junto a las fuerzas electrostáticas. Distribuciones del
DEPARTAMENTO DE TECNOLOGÍA Actividades complementarias Curso: 1º Bach. Profesor: José Jiménez R. Tema 12: Materiales Metálicos: Metales ferrosos
 PARTAMENTO 1.- Determinar, en %, el factor de empaquetamiento de una: a) Red cúbica centrada en el cuerpo (BCC). b) Red cúbica centrada en las caras (FCC). 2.- El hierro a 20 ºC cristaliza en una red BCC
PARTAMENTO 1.- Determinar, en %, el factor de empaquetamiento de una: a) Red cúbica centrada en el cuerpo (BCC). b) Red cúbica centrada en las caras (FCC). 2.- El hierro a 20 ºC cristaliza en una red BCC
