Estructura Cristalina de Sólidos
|
|
|
- Santiago Arroyo Santos
- hace 8 años
- Vistas:
Transcripción
1 Estructura Cristalina de Sólidos Relación entre estructura periódica y propiedades Bibliografía: 1. Solid State Physics. Ashcroft and Mermin. 2. Solid State Chemistry. West. 3. Química del Estado Sólido. Smart y Moore Federico Williams fwilliams@qi.fcen.uba.ar primer cuatrimestre 2014
2 Sólidos Cristalinos Estuctura Cristalina: arreglo periódico de átomos que se repite en el espacio. Dependiendo del carácter del enlace químico los sólidos pueden ser metálicos, iónicos o covalentes. En este último caso existen las redes covalentes tridimensionales y los sólidos moleculares o poliméricos (N 2, O 2, H 2 O, C 60, grafito, polietileno, etc.). Cr: Metálico ClCs: iónico C (diamante): covalente polietileno: covalente Objetivos: 1.Describir la estructura cristalina de la materia: Redes de Bravais, Indices de Miller, Empaquetamientos Compactos, Covalencia y Defectos. 2.Describir cómo se puede determinar experimentalmente la estructura cristalina de sólidos: Difracción de rayos X.
3 Red de Bravais La descripción de todo sólido cristalino utiliza el concepto de red de Bravais que especifica el arreglo periódico en el que se ordenan las unidades repetitivas del cristal. Estas unidades pueden ser átomos individuales, grupos de átomos, moléculas, iones, etc. pero la red de Bravais especifica la geometría de la estructura periódica independientemente de lo que las unidades son y se define como: a) Una red de Bravais es un arreglo infinito de puntos con un arreglo y orientación tal que se ve exactamente igual desde cualquier punto donde se mira al arreglo. b) Una red de Bravais consiste de todos los puntos cuyas posiciones vienen dadas por: R a n b n c donde a, b, c son los vectores de la red y n a, n b, n c son números enteros. n a b c R naa nbb R1 3a 2b R 2a b 2
4 El conjunto de puntos en la figura (a) no es una red de Bravais porque los entornos alrededor de los puntos 1 y 2 son distintos. Sin embargo si consideramos los puntos de a pares (b) entonces si formamos una red de Bravais. Arreglos periódicos de objetos se pueden dividir en grupos idénticos que ocupan sitios en una Red de Bravais. Los grupos de objetos son el motivo y la combinación red de Bravais + motivo espeficia la estructura cristalina. El conjunto de vectores de red para cualquier red de Bravais no es único, existen infinitas posibilidades no equivalentes. Por ejemplo, la siguiente figura ilustra varias opciones de pares de vectores para una red de Bravais bidimensional:
5 En una dimensión existe solo una red de Bravais posible a En dos dimensiones existen cinco redes de Bravais posibles
6 En tres dimensiones existen 14 redes de Bravais posibles (7 sistemas cristalinos basados en 6 parámetros) cúbico tetragonal 4 tipos de celdas unidades: P: primitivo I: centrado en el cuerpo F: centrado en las caras C: centrado en los lados monoclínico ortorrómbico triclínico trigonal hexagonal
7 Celda unidad primitiva Se llama celda unidad primitiva o celda primitiva al volumen que llena todo el espacio sin solaparse consigo mismo ni dejando espacios vacíos a partir de traslaciones de todos los vectores de la red de Bravais. La celda primitiva contiene un punto de la red exactamente. El volumen de la celda primitiva es único (es la inversa de la densidad de puntos de la red), pero la forma de la celda primitiva no lo es: La celda primitiva no refleja claramente la simetría de la red, si solo vemos la celda primitiva en la siguiente red cúbica (indicada por las líneas sólidas) no es sencillo reconocer que la red es cúbica.
8 Celda unidad convencional (no primitiva) Se llama celda unidad convencional o simplemente celda unidad al volumen que llena todo el espacio sin solaparse consigo mismo ni dejando espacios vacíos a partir de traslaciones de un subconjunto de vectores de la red de Bravais. Estas celdas que contienen más de un punto de la red y por lo tanto son no primitivas. Las celdas convencionales no primitivas se usan para mostrar la simetría de la red y contienen un múltiplo entero de celdas primitivas. Para el caso de la red de Bravais cúbica centrada en las caras (fcc), la celda convencional tiene cuatro veces el volumen de la celda primitiva y contiene cuatro puntos de la red. Combinaciones lineales de los vectores de red primitivos generan todos los puntos en la red, mientras que las mismas combinaciones de los vectores convencionales generan solo un cuarto de los sitios.
9 Celda de Wigner-Seitz La celda de Wigner-Seitz es una celda primitiva especial, por lo tanto contiene solo un punto de la red. Se llama celda de Wigner-Seitz a la región del espacio que está más cerca a un punto de la red de Bravais. Para construir la celda de Wigner-Seitz se debe conectar un punto de la red de Bravais con otros puntos de la red de Bravais y bisectar cada una de estas líneas con un plano perpendicular. El poliedro más pequeño limitado por estos planos que contiene al punto original es la celda de Wigner-Seitz. Celda de Wigner-Seitz en dos dimensiones: Celda de Wigner-Seitz de la red de Bravais cúbica centrada en las caras: La celda de Wigner-Seitz se utiliza en la descripción de las propiedades electrónicas de un cristal.
10 Estructura cristalina: red de Bravais más un motivo Hasta ahora solo describimos las redes (arreglo tridimensional de puntos). Para describir la estructura del cristal debemos considerar el arreglo de los átomos en el espacio. La Estructura cristalina es el arreglo periódico de átomos en un cristal y puede describirse asociando a cada punto de la red de Bravais un grupo de átomos llamado Motivo (o Base). Un motivo es un conjunto de uno a más átomos que tiene la misma estequeometría que el material. Por lo tanto la estructura del cristal siempre se construye a partir de una red y un motivo. a celda unidad Motivo r 1 En cualquier motivo compuesto por J átomos, se necesitan J vectores r j que especifican las posiciones de cada átomo en el motivo con respecto al punto (0,0,0) de la red de Bravais. Los vectores r j se escriben en función de los vectores de la red con coordenadas fraccionales (x j, y j, z j ) menores que 1. r j x j a y j b Por lo tanto la posición de cada átomo en el cristal se puede especificar por la suma del vector de red R y el vector del motivo r j z j c
11 Ejemplo es dos dimensiones: el motivo consiste de dos átomos (unidos por la línea llena) localizados en las celdas primitivas de la red de Bravais. Cr: el motivo es un átomo de Cr localizado en cada punto de la red cúbica I centrada en el cuerpo CsCl: el motivo contiene dos átomos, el átomo de Cl en (0,0,0) y el átomo de Cs (1/2,1/2,1/2). Cuando el motivo se coloca en todos los vértices de una red cúbica P, se genera la estructura cristalina del CsCl.
12 Estructura cristalina = Red + motivo diamante: la estructura es una red cúbica F centrada en las caras con dos átomos en el motivo relacionados por un desplazamiento de (1/4, 1/4,1/4). NaCl: la estructura es una red cúbica F centrada en las caras con dos átomos en el motivo relacionados por un desplazamiento de (1/2, 0, 0). Todas las estructuras cristalinas consisten de una de las 14 redes de Bravais más el motivo (conjunto de átomos) que decoran cada punto de la red.
13 Índices de Miller Son índices para planos definidos por los valores recíprocos (h k l) de las intercepciones en los ejes (1/h 1/k 1/l). Para nombrar planos que intersecta un eje en todos sus puntos, trasladarlo en una unidad de red en la dirección normal al plano.
14 El índice de Milles (hkl) no representa solo un plano, sino al conjunto de todos los planos de la red paralelos e idénticos. plano de red (122) Para determinar los índices de Miller se puede contar el numero de espacios que cruzamos al pasar a lo largo del borde de cada celda. El conjunto de planos indistinguibles pertenecen a la misma familia de planos. Las familias de planos idénticos se escriben {h k l}. Por ejemplo, en la estructura cúbica los planos (100), (010), (001), (100), (010), (001) pertenecen a la familia {100}.
15 Direcciones Las direcciones se indican con el símbolo [uvw] que describe todas las direcciones paralelas e idénticas. La direccion [uvw] es el vector que apunta desde el origen de la red al punto de la red con coordenadas u, v y w.
16 Representación visual de la estructura de cristales Modelos de poliedros: Cada poliedro sólido representa un átomo electropositivo y sus ligandos de coordinación (los vecinos más cercanos electronegativos). El átomo metálico esté en el centro del poliedro y sus ligandos en los vértices. Poliedros comúnmente usados incluyen: tetraedro, octaedro, pirámide cuadrada, prisma trigonal y el cubo. Estructura del Mo 4 O 11. En el modelo de esferas duras, las esferas grandes representan al O y las pequeñas al Mo. El modelo del poliedro muestra que la estructura se puede pensar como capas de grupos octaédricos (MoO 6 ) separadas por capas de grupos tetraédricos (MoO 4 ).
17 Arreglos basados en empaquetamiento compactos Una manera de describir las estructuras cristalinas asume que todos los átomos de una estructura cristalina están en los sitios de una estructura correspondiente a un empaquetamiento compacto o en sitios intersticiales bien definidos. Las estructuras de muchos cristales se pueden describir en términos del empaquetamiento compacto de esferas que representan a los átomos o iones. Empaquetamiento hexagonal compacto (hcp) A B A Empaquetamiento cúbico compacto (ccp) La fracción de volumen total ocupado por las esferas (cuando se tocan) es igual para ambas estructuras a (este es el máximo valor posible para empaquetamiento de esferas).
18
19 Estructuras de empaquetamiento compacto hcp y ccp ABABAB genera un empaquetamiento hexagonal compacto hcp La celda unidad que muestra la simetría total del arreglo es hexagonal, es decir a b, c 1.63 a, a b 90º, g 120º 2 átomos en la celda unidad: (0, 0, 0) (1/3, 2/3, 1/2) ABCABC genera un empaquetamiento cúbico compacto ccp La celda unidad que muestra la simetría total del arreglo es cúbica centrada en las caras (fcc), es decir a b c, a b g 90º 4 átomos en la celda unidad: (0, 0, 0) (0, 1/2, 1/2), (1/2, 0, 1/2), (1/2, 1/2, 0) Coordinaciones locales en (a) fcc (b) hcp Ambas estructuras hcp y fcc tienen coordinación 12 y densidades idénticas. La configuración de los vecinos difiere pero el número de vecinos es el mismo.
20 Empaquetamiento no compactos: cúbico centrado en el cuerpo (bcc) Algunos metales muestran estructura cúbica centrada en el cuerpo (bcc). Ocupa el 68% del Espacio. Número de coordinación 6 a 1a y 8 a 0,866a, entonces se la describe como coordinación 8+6. Número de coordinación y fracción de espacio ocupado en empaquetamientos de esferas: Ningún elemento tiene esta estructura Solo un elemento Pa tiene esta estructura Solo un elemento a-po. As, Sb, Bi y P tienen versiones distorsionadas. bcc Empaquetamientos compactos hcp y fcc
21 Sitios intersticiales Existen un número bien definido de posiciones intersticiales en los espacios entre los sitios de los empaquetamientos compactos. La estructura fcc tiene 4 sitios octaédricos por celda unidad; uno está en el centro y el resto está en los puntos medios de todos los bordes de la celda. También existen 8 sitios tetraédricos por celda unidad en las posiciones ( 1/4, 1/4, 1/4). 3 de los 6 primeros vecinos de los sitios octaédricos están en una misma capa compacta y los otros 3 están en la siguiente. Un átomo que ocupe la posición octaédrica intersticial se encontrará a la mitad de la distancia entre dos capas (a la misma distancia de los 6 ligandos). 3 de los 4 primeros vecinos de los sitios tetraédricos están en una misma capa y el cuarto está en otra. Esperamos que el átomo intersticial ocupe una posición equidistante entre los cuatro ligandos. Dado que esta posición no es equidistante entre los dos planos compactos, los sitios tetraédricos que se encuentran por arriba (T ) y por debajo (T ) de un plano central de referencia son distintos. En las estructuras hcp y fcc por cada sitio en el empaquetamiento compacto existen 1 sitio intersticial octaédrico y 2 sitios intersticiales tetraédricos (T y T ). En la estructura bcc por cada sitio en el empaquetamiento compacto existen 6 sitios equivalentes pseudo-tetraédricos y 3 pseudo-octaédricos.
22 Empaquetamiento compactos en sólidos metálicos fcc = Elementos metálicos La atracción entre los electrones de valencia deslocalizados y los átomos cargados positivamente es isotrópica. Por lo tanto, el enlace metálico forma estructuras cristalinas basadas en empaquetamiento compactos que maximizan el espacio ocupado y el número de coordinación (número de primeros vecinos). La mayoría de los metales elementales cristalizan en las estructuras fcc (cúbica centrada en las caras), hcp (empaquetamiento hexagonal compacto) o bcc (cúbica centrada en el cuerpo). Los empaquetamiento compactos fcc y hcp tienen 12 primeros vecinos y los segundos vecinos se encuentran un 41% más alejados. Mientras que en la estructura bcc hay 8 primeros vecinos y 6 segundos vecinos solo un 15% más alejados, esto genera átomos con un número de coordinación efectivo de 8+6 (14) en esta estructura. Polimorfismo: Algunos metales existen en diferentes tipos de estructura a temperatura y presión ambientes. Muchos metales adoptan diferentes estructuras a diferente temperatura y presión. No todos los metales dan empaquetamiento compacto debido a efectos residuales de direccionalidad de los orbitales.
23 Empaquetamiento compactos en estructuras iónicas Materiales en los que los aniones son más grandes que los cationes se pueden describir como un empaquetamiento compacto de aniones en el que los cationes ocupan sitios intersticiales. Estructuras típicas AB n 1:1 NaCl (fcc, todos los huecos O h ) NiAs (hcp, todos los huecos O h ) ZnS blenda (fcc, ½ huecos T) ZnS wurtzita (hcp, ½ huecos T) CsCl (bcc, cúbico no compacto) 1:2 CaF 2 fluorita (fcc de Ca, F ocupa todos los huecos T) CdCl 2 (fcc, ½ huecos O h por capas (100% en una capa, 0% en la siguiente)) CdI 2 (hcp, ½ huecos O h por capas) TiO 2 (hcp, ½ huecos O h en cada capa) 1:3 SrCl 3 (fcc, 2/3 Oh) o BiCl 3 (hcp, 2/3 Oh) 2:3 Al 2 O 3 (fcc, 2/3 Oh)
24 Principios de Laves Principio Espacial: El espacio se usa en la forma mas eficiente Principio de Simetría: Se adopta la mayor simetría posible Principio de Conexión: Existirán el mayor numero de conexiones posibles entre los componentes (maximiza el número de coordinación) Metales y gases inertes: dan estructuras compactas Desviaciones: Metales BCC Interacciones Preferidas, Disminución de la simetría, Reducción del número de coordinación, Disminución de la eficiencia en el llenado del espacio Compuestos Iónicos tienden a seguir los principios, pero se alteran por interacciones de uniones direccionales, diferencia de tamaño y estequiometria. Regla de la relación de radios para estructuras iónicas Los cationes se rodean con la mayor cantidad de aniones posibles (y viceversa) para maximizar la interacción electrostática (considerando a los iones como esferas cargadas no-polarizables e incompresibles). La estructura del compuesto depende de la relación r / r. (1) un catión debe estar en contacto con sus vecinos aniones y (2) aniones vecinos pueden o no estar en contacto. estable estable inestable aumenta r / r aumenta la coordinación
25 Cálculo de los radios límite coordinación relación de radios Estructura tipo Trigonal, <r+/r-<0.225 Tetraédrica, <r+/r-<0.414 ZnS Octaédrica, <r+/r-<0.732 NaCl Cúbica, <r+/r-<1 CsCl
26 Ionicidad y diagramas de Mooser-Pearson La regla de la relación de radios no siempre es buena para predecir la estructura adoptada por ciertos compuestos. Mooser y Pearson proponen un modelo que está basado en el carácter covalente de los enlaces y por lo tanto en su direccionalidad. Dos factores afectan el grado de covalencia de la unión: (1) el n promedio de los átomos y (2) la diferencia de electronegatividades Dx. A mayor grado de covalencia, menor coordinación y mayor direccionalidad.
27
28 CsCl Red: Cúbica - P (Primitiva) Motivo Cl en (0,0,0); Cs en (1/2,1/2,1/2) 1 CsCl en la celda unitaria Coordinación: 8:8 (cúbica). Dos redes cúbicas primitivas interpenetradas
29 NaCl CCP Cl con Na en todos los huecos octaédricos Red: fcc Motivo: Cl en (0,0,0); Na en (1/2,0,0) 4 NaCl en la celda unidad Coordinación: 6:6 (octaédrica)
30 NiAs empaquetamiento hcp de aniones As donde cationes Ni ocupan todos los huecos octaédricos. los átomos de As también tiene coordinación 6 estando en posiciones de prisma trigonal.
31 ZnS (blenda) CCP S 2- con Zn 2+ en la mitad de los sitios tetraédricos (solo T+ {o T-} llenos) Red: fcc r c /r a = 0,225 4 ZnS en la celda unidad Motivo: S en (0,0,0); Zn en (1/4,1/4,1/4) Coordinación: 4:4 (tetraédrica). Los sitios del catión y anión son topologicamente idénticos
32 ZnS (wurtzita) HCP S 2- con Zn 2+ en la mitad de los sitios tetraédricos (sólo T+{o T-} llenos) Red: Hexagonal - P Motivo: 2S en (1/3,2/3,3/8) y (2/3,1/3,1/2+3/8); 2 Zn en (1/3,2/3,0) y (2/3,1/3,1/2) 2 ZnS en la celda unidad Coordinación: 4:4 (tetraédrica)
33 Rutilo (TiO 2 ) empaquetamiento hcp de O con Ti ocupando la mitad de los hueco octaédricos en cada capa Celda Unidad: Primitiva Tetragonal (a = b c) 2 TiO 2 por celda unidad Motivo: 2 Ti en (0, 0, 0); (1/2, 1/2, 1/2) y 4 O en ± (0.3, 0.3, 0); (0.8, 0.2, 1/2), (0.2, 0.8, 1/2) Ti: 6 (coordinación octaédrica) O: 3 (coordinación trigonal plana) TiO 6 octaedros comparten aristas en cadenas a lo largo del eje c Cadenas que comparten las aristas estan unidas por los vértices
34 CaF 2 (fluorita) fcc Ca 2+ con F - en huecos tetraédricos Coord Ca 2+ = 8; F - = 4 r C /r A = formulas por celda unidad bcc F con Ca 2+ en ½ de huecos cúbicos CsCl ocupa todos los cúbicos
35 MgAl 2 O 4 (espinela) La estructura de espinela con la composición AB 2 O 4 es cúbica, con una red fcc de O 2- y cationes bivalentes y trivalentes ocupando 1/8 de los sitios tetraédricos y ½ de los sitios octaédricos en la celda unidad de 32 O 2- (8 unidades fórmula). En las Espinelas inversas,b[abo 4 ], los cationes B ocupan 8 sitios tetraédricos y los restantes junto con los cationes A los 16 sitios octaédricos. Magnetita; Fe 3+ ( Fe 2+ Fe 3+ )O 4 Espinela; Mg 2+ ( Al 2 3+ )O 4 Cromita; Fe 3+ (Cr 2 3+ )O 4 Jacobsita; Fe 3+ ( Mn 2+ Fe 3+ )O 4
36 ReO 3 Red : Cubica Primitiva 1 ReO 3 p or celda uni dad Moti vo : Re en (0, 0, 0); 3O en (1/2, 0, 0), (0, 1/2, 0), (0, 0, 1/2) Re: 6 ( coordinacion octaedrica ) O: 2 ( cordinacion lineal ) ReO 6 octaedros comparten solo los vertices Puede considerarse como oxido ccp con 1/4 de los sitios c cp vacantes ( en el centr o de la celda). Vease la celda unidad expresada con el origen en O Muestra un fcc de atomos de O defectuoso (falta O en una cara) Ejemplos: WO 3, AlF 3, ScF 3, FeF 3, CoF 3, Sc(OH) 3
37 Estructura cúbica ABO 3 (perovskitas) Red: Cúbica Primitiva (estructura ideal) 1 CaTiO 3 por celda unidad Motivo de la Celda: Ti en (0, 0, 0); Ca en (1/2, 1/2, 1/2); 3O en (1/2, 0, 0), (0, 1/2, 0), (0, 0, 1/2) Ca coordinación 12 por O (cuboctaédrico) Ti coordinación 6 por O (octaédrico) O octaedro distorsionado (4xCa + 2xTi) TiO 6 octaedros comparten solo los vértices El Ca llena el sitio vacante ccp in ReO 3, arreglo CaO 3 ccp con ¼ de huecos octaédricos (definidos por 6O) llenos con Ti
38 Anion T + T - O Structure ccp - - Full NaCl ccp Full - - Blenda, ZnS ccp Full Full - Antifluorita ccp - - ½ CdCl 2 hcp - - Full NiAs hcp Full - - Wurtzita, ZnS hcp - - 1/2 CdI 2 ccp 1/8 1/8 1/2 Spinela, MgAl 2 O 4 hcp 1/8 1/8 1/2 Olivine, Mg 2 SiO 4 hcp - - 2/3 Corundum, Al 2 O 3 ccp AO /4 Perovskita, CaTiO 3 ccp (¾ only) - - 1/4 ReO 3
39 diamante: la estructura es una red cúbica fcc centrada en las caras con dos átomos en el motivo relacionados por un desplazamiento de (1/4, 1/4,1/4). Tiene átomos de C en todas las posiciones fcc y en la mitad de los sitios tetraédricos
40 Grafito = apilamiento en capas hexagonales desplazados Contamos Átomos en Celdas de 3D Átomos en diferentes posiciones de la celda se comparten por diferente número de celdas unitarias Átomos en vértices se comparten por 8 celdas 1/8 átomo por celda Átomo en arista compartido por 4 celdas 1/4 átomo por celda Átomo en cara compartido por 2 celdas 1/2 átomo por celda Átomo en el cuerpo único a 1 celda 1 átomo por celda
41 Defectos Defectos extendidos: como las dislocaciones y los bordes de grano afectan las propiedades mecánicas, de conducción y de reactividad. Defectos puntuales: son defectos en posiciones atómicas aisladas, pueden deberse a la presencia de un átomo extraño en un sitio específico o a una vacante donde normalmente se esperaría un átomo. Afectan las propiedades químicas (reactividad) y físicas (ópticas, conducción, electrónicas, magnéticas) del sólido. Defectos extrínsecos: se crean cuando un átomo extraño se inserta dentro de la red. Defectos intrínsecos: son inherentes al cristal y por lo tanto no cambian la composición del mismo. Existen dos tipos de defectos intrínsecos: Defectos de Schottky: consisten en vacantes en la red (una vacante catiónica y una aniónica). El número de vacantes catiónicas y aniónicas es la misma para preservar la electroneutralidad. Defectos de Frenkel: un átomo o ion que se traslada a una posición intersticial crea una vacante. Generalmente son defectos catiónicos, excepto en el caso de compuestos de estructura fluorita donde los defectos son aniónicos.
42 Defectos puntuales intrínsecos defecto de Schottky estructura ideal defecto de Frenkel n S ~ N exp(-dh S / 2kT) T = 0 K n F ~ (N N int ) 1/2 exp(-dh F / 2kT) No cambian la composición global Forman parte de la estructura del cristal N: número de sitios en la red N int : número de sitios intersticiales Schottky (vacancias de a pares en la red manteniendo la electroneutralidad) Frenkel (vacancias por desplazamiento: un ión se desplaza a un sitio intersticial) La presencia de defectos Schottky o Frenkel en un cristal depende del valor de DH predominando el defecto con el menor valor de DH. En algunos cristales es posible hallar ambos defectos.
43 La concentración de defectos Se requiere energía para crear un defecto, por lo tanto es un proceso endotérmico. Los defectos existen en cristales hasta a muy bajas temperaturas (en una concentración muy pequeña) aunque cueste energía debido al aumento de entropía configuracional. si DH = 5x10-19 J n s /N = 6.12 x T = 300 K n s /N = 6.37 x 10-8 T = 1000 K
44 Defectos puntuales extrínsecos 1:1 1:2 Igual valencia Diferente valencia Ca 2+ en ZrO 2 Crea huecos en la red de O Cambian la composición global Entran átomos extraños (dopado) Se igualan las cargas, se crean vacancias Influencia en la conductividad (props. eléctricas)
TEMA 8 ESTRUCTURA CRISTALINA
 Tema 8. Estructura cristalina 1 TEMA 8 ESTRUCTURA CRISTALINA Los sólidos pueden clasificarse: 1.- Por su ordenación: 1a. Sólidos amorfos: tienen una estructura desordenada. Sus átomos o moléculas se colocan
Tema 8. Estructura cristalina 1 TEMA 8 ESTRUCTURA CRISTALINA Los sólidos pueden clasificarse: 1.- Por su ordenación: 1a. Sólidos amorfos: tienen una estructura desordenada. Sus átomos o moléculas se colocan
Estructura Interna de los Materiales
 TEMA III Estructura Interna de los Materiales LECCIÓN 3 Estructura Cristalina y Amorfa 1 3.1 ESTADOS DE LA MATERIA Ciencia y Tecnología de los Materiales La materia puede presentarse en tres estados: gaseoso,
TEMA III Estructura Interna de los Materiales LECCIÓN 3 Estructura Cristalina y Amorfa 1 3.1 ESTADOS DE LA MATERIA Ciencia y Tecnología de los Materiales La materia puede presentarse en tres estados: gaseoso,
Consideraciones sobre estructuras representativas
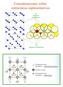 Consideraciones sobre estructuras representativas CONSIDERACIONES SOBRE ESTRUCTURAS REPRESENTATIVAS: En el empacamiento compacto hcp y ccp el número de coordinación es 12 Los elementos metálicos son los
Consideraciones sobre estructuras representativas CONSIDERACIONES SOBRE ESTRUCTURAS REPRESENTATIVAS: En el empacamiento compacto hcp y ccp el número de coordinación es 12 Los elementos metálicos son los
ESTRUCTURAS CRISTALINAS (P2)
 ESTRUCTURAS CRISTALINAS (P2) Objetivos - Visualización de estructuras de sólidos mediante el uso de modelos - Estudio de redes cristalinas basadas en ordenamientos de esferas de igual tamaño - Identificación
ESTRUCTURAS CRISTALINAS (P2) Objetivos - Visualización de estructuras de sólidos mediante el uso de modelos - Estudio de redes cristalinas basadas en ordenamientos de esferas de igual tamaño - Identificación
LABORATORIO DE ESTADO SÓLIDO Y SEMICONDUCTORES 1.1. PRÁCTICA N o 1 REDES DE BRAVAIS Y ESTRUCTURAS CRISTALINAS
 LABORATORIO DE ESTADO SÓLIDO Y SEMICONDUCTORES 1.1 PRÁCTICA N o 1 REDES DE BRAVAIS Y ESTRUCTURAS CRISTALINAS 1. INTRODUCCIÓN 1.1 Red de Bravais y celda primitiva unidad Uno de los conceptos fundamentales
LABORATORIO DE ESTADO SÓLIDO Y SEMICONDUCTORES 1.1 PRÁCTICA N o 1 REDES DE BRAVAIS Y ESTRUCTURAS CRISTALINAS 1. INTRODUCCIÓN 1.1 Red de Bravais y celda primitiva unidad Uno de los conceptos fundamentales
Estructura de los Sólidos
 Estructura de los Sólidos Estructura Cristalina OBJETIVOS a) Definir sólidos cristalinos y amorfos b) Definir estructura cristalina c) Describir las diferentes estructuras cristalinas d) Utilizar índices
Estructura de los Sólidos Estructura Cristalina OBJETIVOS a) Definir sólidos cristalinos y amorfos b) Definir estructura cristalina c) Describir las diferentes estructuras cristalinas d) Utilizar índices
Tema 2.- Estructura de la Materia
 BLOQUE II.- ESTRUCTURA Estructura de la Materia * James F. Shackerlford Introducción a la Ciencia de Materiales para Ingenieros. Cuarta edición. Ed. Prentice Hall (1998) * Pat L. Mangonon Ciencia de Materiales:
BLOQUE II.- ESTRUCTURA Estructura de la Materia * James F. Shackerlford Introducción a la Ciencia de Materiales para Ingenieros. Cuarta edición. Ed. Prentice Hall (1998) * Pat L. Mangonon Ciencia de Materiales:
1.-La Cristalografía. 2.-Simetría
 1.-La Cristalografía La Cristalografía es la ciencia que se ocupa de los sólidos cristalinos y describe su estructura interna, es decir, como están distribuidos los átomos en su interior. También estudia
1.-La Cristalografía La Cristalografía es la ciencia que se ocupa de los sólidos cristalinos y describe su estructura interna, es decir, como están distribuidos los átomos en su interior. También estudia
TEMA 5: INTROD. AL ESTADO SÓLIDO
 ESTADO SÓLIDO Figuras p1143 y p1146, Tipler 5ª Ed SEMICONDUCTORES Figuras p1141 y p1160, Tipler 5ª Ed DISPOSITIVOS http://axxon.com.ar/zap/c-zapping0127.htm Enlace químico: fuerza que mantiene unidos los
ESTADO SÓLIDO Figuras p1143 y p1146, Tipler 5ª Ed SEMICONDUCTORES Figuras p1141 y p1160, Tipler 5ª Ed DISPOSITIVOS http://axxon.com.ar/zap/c-zapping0127.htm Enlace químico: fuerza que mantiene unidos los
Química Inorgánica-63.13- Dra.Silvia E. Jacobo. Sólidos. Estructuras Cristalinas
 Sólidos Estructuras Cristalinas Ordenamientos atómicos En gases no hay orden En líquidos hay orden de corto alcance En sólidos hay orden de largo alcance El ordenamiento está determinado por el tipo de
Sólidos Estructuras Cristalinas Ordenamientos atómicos En gases no hay orden En líquidos hay orden de corto alcance En sólidos hay orden de largo alcance El ordenamiento está determinado por el tipo de
Estructura atómica de superficies
 Estructura atómica de superficies El número de coordinación de los átomos en una superficie es mucho menor que el número de coordinación de los átomos en el sólido. Uno puede pensar que forma una superficie
Estructura atómica de superficies El número de coordinación de los átomos en una superficie es mucho menor que el número de coordinación de los átomos en el sólido. Uno puede pensar que forma una superficie
Sobre la estructura periódica de los sólidos elementales
 Sobre la estructura periódica de los sólidos elementales Gonzalo Gutiérrez * gonzalo@fisica.ciencias.uchile.cl 3 Agosto 2004 Las diferentes propiedades de los materiales se reflejan con mucha claridad
Sobre la estructura periódica de los sólidos elementales Gonzalo Gutiérrez * gonzalo@fisica.ciencias.uchile.cl 3 Agosto 2004 Las diferentes propiedades de los materiales se reflejan con mucha claridad
Tema 2 Estructuras Cristalinas
 Tema 2 Estructuras Cristalinas Para poder comprender las propiedades de los materiales, y poder por tanto seleccionar el material idóneo para una aplicación específica, se hace necesario comprender la
Tema 2 Estructuras Cristalinas Para poder comprender las propiedades de los materiales, y poder por tanto seleccionar el material idóneo para una aplicación específica, se hace necesario comprender la
SÓLIDOS I. Tipos de sólidos. Sólidos cristalinos: los átomos, iones o moléculas se empaquetan en forma ordenada.
 SÓLIDOS I Tipos de sólidos Sólidos cristalinos: los átomos, iones o moléculas se empaquetan en forma ordenada. Sólidos amorfos: no presentan estructuras ordenadas. 1 Sólidos cristalinos Hay posiciones
SÓLIDOS I Tipos de sólidos Sólidos cristalinos: los átomos, iones o moléculas se empaquetan en forma ordenada. Sólidos amorfos: no presentan estructuras ordenadas. 1 Sólidos cristalinos Hay posiciones
SÓLIDOS INORGÁNICOS. Tema 6. FUNDAMENTOS
 SÓLIDOS INORGÁNICOS Tema 6. Fundamentos Tema 7. Sólidos metálicos Tema 8. Sólidos iónicos Tema 9. Sólidos covalentes Tema 10. Sólidos moleculares Tema 11. Defectos y no-estequiometría Tema 12. Propiedades
SÓLIDOS INORGÁNICOS Tema 6. Fundamentos Tema 7. Sólidos metálicos Tema 8. Sólidos iónicos Tema 9. Sólidos covalentes Tema 10. Sólidos moleculares Tema 11. Defectos y no-estequiometría Tema 12. Propiedades
Introducción a la Física del Estado Sólido
 Semana 1. Estructura cristalina. Definición de arreglos periódicos. Tipos de redes. Clasificación de simetrías. Índices de planos cristalinos. Ejemplos de estructuras cristalinas simples. Cristales no
Semana 1. Estructura cristalina. Definición de arreglos periódicos. Tipos de redes. Clasificación de simetrías. Índices de planos cristalinos. Ejemplos de estructuras cristalinas simples. Cristales no
TEMA 8: SÓLIDOS INORGÁNICOS. 2.- Redes bidimensionales y tridimensionales
 TEMA 8: SÓLIDOS INORGÁNICOS 1.- Tipos de sólidos 2.- Redes bidimensionales y tridimensionales 3.- Celda unidad y sus parámetros: - nº de átomos / celda - nº de coordinación (NC) - fracción de volumen ocupado
TEMA 8: SÓLIDOS INORGÁNICOS 1.- Tipos de sólidos 2.- Redes bidimensionales y tridimensionales 3.- Celda unidad y sus parámetros: - nº de átomos / celda - nº de coordinación (NC) - fracción de volumen ocupado
4. El ClNa cristaliza en el sistema cúbico con parámetro [a]=5.631å. Calcular su densidad sabiendo que su masa molecular es 58.45 uma.
![4. El ClNa cristaliza en el sistema cúbico con parámetro [a]=5.631å. Calcular su densidad sabiendo que su masa molecular es 58.45 uma. 4. El ClNa cristaliza en el sistema cúbico con parámetro [a]=5.631å. Calcular su densidad sabiendo que su masa molecular es 58.45 uma.](/thumbs/28/12696458.jpg) Síntesis y Caracterización Estructural de los Materiales: Bases Cristalográficas. 1. Dibuje en las celdas fundamentales cúbicas adjuntas (a = 3 Å): a. Las filas reticulares de índices de Weiss [02-1],
Síntesis y Caracterización Estructural de los Materiales: Bases Cristalográficas. 1. Dibuje en las celdas fundamentales cúbicas adjuntas (a = 3 Å): a. Las filas reticulares de índices de Weiss [02-1],
Estado Sólido. Estado Sólido. Estado Sólido. Estado Sólido - + Sólidos cristalinos y sólidos amorfos
 Sólidos cristalinos y sólidos amorfos Sólidos cristalinos: presentan un ordenamiento regular en el espacio Sólidos amorfos: no presentan el ordenamiento típico de los cristalinos Región cristalina Región
Sólidos cristalinos y sólidos amorfos Sólidos cristalinos: presentan un ordenamiento regular en el espacio Sólidos amorfos: no presentan el ordenamiento típico de los cristalinos Región cristalina Región
GRUPOS PUNTUALES. 4.- Si un plano de simetría contiene un eje de orden n, existen n planos que contienen el eje. formando entre ellos ángulos de
 GRUPOS PUNTUALES Existen algunas relaciones entre elementos de simetría que pueden ser útiles a la hora de deducir cuales son los conjuntos de estos que forman grupo. 1.- Todos los elementos de simetría
GRUPOS PUNTUALES Existen algunas relaciones entre elementos de simetría que pueden ser útiles a la hora de deducir cuales son los conjuntos de estos que forman grupo. 1.- Todos los elementos de simetría
Teoría de repulsión de pares electrónicos de la capa de Valencia
 Teoría de repulsión de pares electrónicos de la capa de Valencia La estructura del Lewis muestra las moléculas en dos dimensiones generalmente con una representación plana de ellos y los pares de electrones
Teoría de repulsión de pares electrónicos de la capa de Valencia La estructura del Lewis muestra las moléculas en dos dimensiones generalmente con una representación plana de ellos y los pares de electrones
El H solo necesita 2 electrones en su capa de valencia como el He.
 Tema II. Enlace químico Concepto de enlace químico y modelos de enlace Un enlace químico se caracteriza por una situación de mínima energía, respecto a los átomos de partida que lo forman, de ahí que la
Tema II. Enlace químico Concepto de enlace químico y modelos de enlace Un enlace químico se caracteriza por una situación de mínima energía, respecto a los átomos de partida que lo forman, de ahí que la
En la figura 1.1 puede verse el cuarzo cristalino y no cristalino respectivamente.
 TEMA 3.- ESTRUCTURA CRISTALINA. 1.- Introducción. Conceptos fundamentales. Se han descrito los enlaces atómicos determinados por la configuración electrónica de los átomos individuales. Ahora se va a tratar
TEMA 3.- ESTRUCTURA CRISTALINA. 1.- Introducción. Conceptos fundamentales. Se han descrito los enlaces atómicos determinados por la configuración electrónica de los átomos individuales. Ahora se va a tratar
Tipos de estructuras. Introducción a la Ciencia de Materiales. M. Bizarro F. M. Sánchez
 Tipos de estructuras Empaquetamiento compacto Son estructuras formadas por átomos de igual tamaño que se unen mediante enlace metálico (esferas duras) A B A : A B C : FCC vs HCP El factor de empaquetamiento
Tipos de estructuras Empaquetamiento compacto Son estructuras formadas por átomos de igual tamaño que se unen mediante enlace metálico (esferas duras) A B A : A B C : FCC vs HCP El factor de empaquetamiento
ESTRUCTURA DE LA MATERIA QCA 09 ANDALUCÍA
 1.- Considere el elemento cuya configuración electrónica es 1s 2 2s 2 2p 6 3s 2 3p 4. a) De qué elemento se trata? b) Justifique el periodo y el grupo del sistema periódico a los que pertenece. c) Cuál
1.- Considere el elemento cuya configuración electrónica es 1s 2 2s 2 2p 6 3s 2 3p 4. a) De qué elemento se trata? b) Justifique el periodo y el grupo del sistema periódico a los que pertenece. c) Cuál
La geometría molecular viene dada por la distribución de los átomos periféricos unidos al átomo central.
 Estructuras moleculares: Modelo VSPR (RPECV) Las estructuras de Lewis son útiles para establecer la distribución de los pares electrónicos en las moléculas pero no aportan nada sobre su previsible geometría.
Estructuras moleculares: Modelo VSPR (RPECV) Las estructuras de Lewis son útiles para establecer la distribución de los pares electrónicos en las moléculas pero no aportan nada sobre su previsible geometría.
El enlace covalente se explica mediante la Teoría del Orbital Molecular (TOM).(Bueno para moléculas sencillas, complicado para las complejas).
 . Aplicación de la Teoría de Grupos. Moléculas triatómicas lineales y angulares. Moléculas mono y bidimensionales. Moléculas poliédricas sencillas. Objetivos: Recordar los conceptos generales del enlace
. Aplicación de la Teoría de Grupos. Moléculas triatómicas lineales y angulares. Moléculas mono y bidimensionales. Moléculas poliédricas sencillas. Objetivos: Recordar los conceptos generales del enlace
Estructura de sólidos
 Estructura de sólidos Química Inorgánica - 2006 Tipos de estructuras cristalinas cristal enlace características molecular covalente-baja energía cristales blandos, bajo p.f. red covalente covalente cristales
Estructura de sólidos Química Inorgánica - 2006 Tipos de estructuras cristalinas cristal enlace características molecular covalente-baja energía cristales blandos, bajo p.f. red covalente covalente cristales
Tema 4. Cristaloquímica. Descripción estructural y
 Tema 4. Cristaloquímica. Descripción estructural y estructuras tipos Qué objetivos tiene la Cristaloquímica? Las fases cristalinas son componentes esenciales de los materiales, y especificamente de los
Tema 4. Cristaloquímica. Descripción estructural y estructuras tipos Qué objetivos tiene la Cristaloquímica? Las fases cristalinas son componentes esenciales de los materiales, y especificamente de los
Tema 1: Sólidos cristalinos Curso 2016/17
 Física del Estado Sólido I Tema 1: Sólidos cristalinos Curso 2016/17 Qué es un cristal? Un cristal ideal está formado por una distribución periódica tridimensional de átomos Desde hace siglos se observó
Física del Estado Sólido I Tema 1: Sólidos cristalinos Curso 2016/17 Qué es un cristal? Un cristal ideal está formado por una distribución periódica tridimensional de átomos Desde hace siglos se observó
ACTIVIDADES DA UNIDADE 14: O ENLACE QUÍMICO
 ACTIVIDADES DA UNIDADE 14: O ENLACE QUÍMICO 1 Puede formarse un enlace iónico entre átomos de un mismo elemento químico? Por qué? No. El enlace químico se produce entre átomos con valores muy diferentes
ACTIVIDADES DA UNIDADE 14: O ENLACE QUÍMICO 1 Puede formarse un enlace iónico entre átomos de un mismo elemento químico? Por qué? No. El enlace químico se produce entre átomos con valores muy diferentes
Estructuras Cristalinas
 Estructuras Cristalinas Bibliografía: Solid State Chemistry: An introduction, L. Smart and E. Moore. 1992 Solid State Chemistry and its applications, A.R. West. 1984 1 Enlace en Cerámicos Iónico Mezcla
Estructuras Cristalinas Bibliografía: Solid State Chemistry: An introduction, L. Smart and E. Moore. 1992 Solid State Chemistry and its applications, A.R. West. 1984 1 Enlace en Cerámicos Iónico Mezcla
Cap. 24 La Ley de Gauss
 Cap. 24 La Ley de Gauss Una misma ley física enunciada desde diferentes puntos de vista Coulomb Gauss Son equivalentes Pero ambas tienen situaciones para las cuales son superiores que la otra Aquí hay
Cap. 24 La Ley de Gauss Una misma ley física enunciada desde diferentes puntos de vista Coulomb Gauss Son equivalentes Pero ambas tienen situaciones para las cuales son superiores que la otra Aquí hay
CAP. 1:ESTRUCTURAS CRISTALINAS
 CAP. 1:ESTRUCTURAS CRISTALINAS Sólidos cristalinos: amorfos: Disposiciones periódicas en el espacio Disposición al azar Situaciones intermedias: (no periódicas pero ordenadas) Estructuras moduladas Casicristales
CAP. 1:ESTRUCTURAS CRISTALINAS Sólidos cristalinos: amorfos: Disposiciones periódicas en el espacio Disposición al azar Situaciones intermedias: (no periódicas pero ordenadas) Estructuras moduladas Casicristales
TEMA 5: INTRODUCCIÓN A LA SIMETRÍA MOLECULAR
 Tema 5 Simetría Molecular 1 TEMA 5: INTRODUCCIÓN A LA SIMETRÍA MOLECULAR La simetría de una molécula determina muchas de sus propiedades e incluso determina cómo se producen algunas reacciones. El estudio
Tema 5 Simetría Molecular 1 TEMA 5: INTRODUCCIÓN A LA SIMETRÍA MOLECULAR La simetría de una molécula determina muchas de sus propiedades e incluso determina cómo se producen algunas reacciones. El estudio
ESTRUCTURAS CARACTERÍSTICAS
 ESTRUCTURAS CARACTERÍSTICAS En este capítulo se describen algunas estructuras muy simples que permitirán analizar la disposición de los átomos de diversos compuestos característicos en los que el enlace
ESTRUCTURAS CARACTERÍSTICAS En este capítulo se describen algunas estructuras muy simples que permitirán analizar la disposición de los átomos de diversos compuestos característicos en los que el enlace
Los sólidos iónicos. Estructuras características de los sólidos iónicos
 Los sólidos iónicos Los compuestos iónicos suelen presentar una serie de características físicas que los distinguen de los covalentes. Así, los sólidos iónicos como el cloruro sódico y el nitrato de potasio
Los sólidos iónicos Los compuestos iónicos suelen presentar una serie de características físicas que los distinguen de los covalentes. Así, los sólidos iónicos como el cloruro sódico y el nitrato de potasio
Aplicación de programas 3D en la docencia universitaria. Estudio de estructuras cristalinas
 Aplicación de programas 3D en la docencia universitaria. Estudio de estructuras cristalinas F. Parres García; J.E. Crespo Amoros; S. Sanchez Caballero; M.A. Sellés Cantó; E. Perez Bernabeu Escuela Politçecnica
Aplicación de programas 3D en la docencia universitaria. Estudio de estructuras cristalinas F. Parres García; J.E. Crespo Amoros; S. Sanchez Caballero; M.A. Sellés Cantó; E. Perez Bernabeu Escuela Politçecnica
ESTRUCTURA Y CRISTALIZACION DE LOS METALES
 Materiales Metálicos 2do. Ingeniería Mecánica ESTRUCTURA Y CRISTALIZACION DE LOS METALES Ing. Víctor Gómez U. T. N Facultad Regional Tucumán METALURGIA FISICA Es la ciencia que se ocupa de estudiar las
Materiales Metálicos 2do. Ingeniería Mecánica ESTRUCTURA Y CRISTALIZACION DE LOS METALES Ing. Víctor Gómez U. T. N Facultad Regional Tucumán METALURGIA FISICA Es la ciencia que se ocupa de estudiar las
III. DIFUSION EN SOLIDOS
 Metalografía y Tratamientos Térmicos III - 1 - III. DIFUSION EN SOLIDOS III.1. Velocidad de procesos en sólidos Muchos procesos de producción y aplicaciones en materiales de ingeniería están relacionados
Metalografía y Tratamientos Térmicos III - 1 - III. DIFUSION EN SOLIDOS III.1. Velocidad de procesos en sólidos Muchos procesos de producción y aplicaciones en materiales de ingeniería están relacionados
TEMA 1: NOCIONES DE ESTADO SÓLIDO. La importancia de la estructura, el enlace y los estados electrónicos sobre las propiedades del material
 TEMA 1: NOCIONES DE ESTADO SÓLIDO La importancia de la estructura, el enlace y los estados electrónicos sobre las propiedades del material Sólido: Substancias elásticas rígidas, es decir, substancias que
TEMA 1: NOCIONES DE ESTADO SÓLIDO La importancia de la estructura, el enlace y los estados electrónicos sobre las propiedades del material Sólido: Substancias elásticas rígidas, es decir, substancias que
DEFECTOS E IMPERFECCIONES CRISTALINAS
 DEFECTOS E IMPERFECCIONES CRISTALINAS Realmente no existen cristales perfectos sino que contienen varios tipos de imperfecciones y defectos, que afectan a muchas de sus propiedades físicas y mecánicas
DEFECTOS E IMPERFECCIONES CRISTALINAS Realmente no existen cristales perfectos sino que contienen varios tipos de imperfecciones y defectos, que afectan a muchas de sus propiedades físicas y mecánicas
MODELO RPECV (REPULSION ENTRE PARES DE ELECTRONES DE LA CAPA DE VALENCIA)
 MODELO RPECV (REPULSION ENTRE PARES DE ELECTRONES DE LA CAPA DE VALENCIA) Con este Modelo puede deducirse la estructura de un gran número de compuestos covalentes de elementos representativos. Basándonos
MODELO RPECV (REPULSION ENTRE PARES DE ELECTRONES DE LA CAPA DE VALENCIA) Con este Modelo puede deducirse la estructura de un gran número de compuestos covalentes de elementos representativos. Basándonos
 El carbono y sus propiedades 1.-Definición El carbón es un combustible sólido de origen vegetal. El carbón o carbón mineral es una roca sedimentaria de color negro, muy rica en carbono, utilizada como
El carbono y sus propiedades 1.-Definición El carbón es un combustible sólido de origen vegetal. El carbón o carbón mineral es una roca sedimentaria de color negro, muy rica en carbono, utilizada como
INTRODUCCIÓN AL ENLACE IÓNICO
 INTRODUCCIÓN AL ENLACE IÓNICO AUTORIA SILVIA GARCÍA SEPÚLVEDA TEMÁTICA FÍSICA Y QUÍMICA ETAPA BACHILLERATO Resumen A continuación voy a pasar a describir como se lleva a cabo el estudio del enlace químico,
INTRODUCCIÓN AL ENLACE IÓNICO AUTORIA SILVIA GARCÍA SEPÚLVEDA TEMÁTICA FÍSICA Y QUÍMICA ETAPA BACHILLERATO Resumen A continuación voy a pasar a describir como se lleva a cabo el estudio del enlace químico,
35 Facultad de Ciencias Universidad de Los Andes Mérida-Venezuela. Potencial Eléctrico
 q 1 q 2 Prof. Félix Aguirre 35 Energía Electrostática Potencial Eléctrico La interacción electrostática es representada muy bien a través de la ley de Coulomb, esto es: mediante fuerzas. Existen, sin embargo,
q 1 q 2 Prof. Félix Aguirre 35 Energía Electrostática Potencial Eléctrico La interacción electrostática es representada muy bien a través de la ley de Coulomb, esto es: mediante fuerzas. Existen, sin embargo,
Operaciones Morfológicas en Imágenes Binarias
 Operaciones Morfológicas en Imágenes Binarias Introducción La morfología matemática es una herramienta muy utilizada en el procesamiento de i- mágenes. Las operaciones morfológicas pueden simplificar los
Operaciones Morfológicas en Imágenes Binarias Introducción La morfología matemática es una herramienta muy utilizada en el procesamiento de i- mágenes. Las operaciones morfológicas pueden simplificar los
TEMA 9 EL ENLACE IÓNICO Y LOS SÓLIDOS IÓNICOS
 TEMA 9 EL ENLACE IÓNICO Y LOS SÓLIDOS IÓNICOS Son aquellos en los que los iones constituyentes están unidos entre sí por fuerzas electrostáticas. Algunas de sus propiedades características son las siguientes:
TEMA 9 EL ENLACE IÓNICO Y LOS SÓLIDOS IÓNICOS Son aquellos en los que los iones constituyentes están unidos entre sí por fuerzas electrostáticas. Algunas de sus propiedades características son las siguientes:
Electrólisis. Electrólisis 12/02/2015
 Electrólisis Dr. Armando Ayala Corona Electrólisis La electrolisis es un proceso mediante el cual se logra la disociación de una sustancia llamada electrolito, en sus iones constituyentes (aniones y cationes),
Electrólisis Dr. Armando Ayala Corona Electrólisis La electrolisis es un proceso mediante el cual se logra la disociación de una sustancia llamada electrolito, en sus iones constituyentes (aniones y cationes),
TRABAJO PRÁCTICO: MODELOS EXTREMOS DE SUSTANCIA
 1 Complemento TRABAJO PRÁCTICO: S EXTREMOS DE SUSTANCIA FUNDAMENTOS TEÓRICOS BÁSICOS Todas las sustancias pueden considerarse formadas por un conjunto de unidades estructurales o fundamentales. La clase
1 Complemento TRABAJO PRÁCTICO: S EXTREMOS DE SUSTANCIA FUNDAMENTOS TEÓRICOS BÁSICOS Todas las sustancias pueden considerarse formadas por un conjunto de unidades estructurales o fundamentales. La clase
Ilustración 15.1. El número de coordinación en el NaCl es 6:6. Cada ion esta rodeado por seis iones que tienen carga opuesta a él.
 ENLACE IÓNICO Tú sabes que existen sustancias que forman sólidos cristalinos con altos puntos de fusión, que no conducen la corriente en estado sóliso pero se vuelven buenos conductores al fundirlos o
ENLACE IÓNICO Tú sabes que existen sustancias que forman sólidos cristalinos con altos puntos de fusión, que no conducen la corriente en estado sóliso pero se vuelven buenos conductores al fundirlos o
Sólidos Iónicos El enlace Iónico (1)
 1 Sólidos Iónicos El enlace Iónico (1) 2 * Huheey, J. E., Keiter, R. L., Keiter, E. A., Inorganic Chemistry: Principles of Structure and Reactivity, 4ª Ed., Harper Collins, 1993. Capítulo 4. * Douglas,
1 Sólidos Iónicos El enlace Iónico (1) 2 * Huheey, J. E., Keiter, R. L., Keiter, E. A., Inorganic Chemistry: Principles of Structure and Reactivity, 4ª Ed., Harper Collins, 1993. Capítulo 4. * Douglas,
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2009 QUÍMICA TEMA 3: ENLACES QUÍMICOS
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2009 QUÍMICA TEMA : ENLACES QUÍMICOS Junio, Ejercicio 2, Opción B Reserva 2, Ejercicio 2, Opción A Reserva, Ejercicio 2, Opción A Reserva, Ejercicio, Opción B
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2009 QUÍMICA TEMA : ENLACES QUÍMICOS Junio, Ejercicio 2, Opción B Reserva 2, Ejercicio 2, Opción A Reserva, Ejercicio 2, Opción A Reserva, Ejercicio, Opción B
ESTRUCTURA CRISTALINA
 SOLIDOS ESTRUCTURA CRISTALINA Dr. Andres Ozols 2005 Dr. A. Ozols 1 ALCANCE del ORDEN ATOMICO Estructura de corto alcance Estructura de alcance intermedio Estructura de largo alcance Dr. A. Ozols 2 TIPOS
SOLIDOS ESTRUCTURA CRISTALINA Dr. Andres Ozols 2005 Dr. A. Ozols 1 ALCANCE del ORDEN ATOMICO Estructura de corto alcance Estructura de alcance intermedio Estructura de largo alcance Dr. A. Ozols 2 TIPOS
Sólidos Arreglos y celdas unitarias. Ramón L. Hernández Castillo Enero 2012
 Sólidos Arreglos y celdas unitarias Ramón L. Hernández Castillo Enero 2012 Importancia de estudiar los sólidos cristalinos La mayoría de los compuestos inorgánicos son sólidos Casi todos los elementos
Sólidos Arreglos y celdas unitarias Ramón L. Hernández Castillo Enero 2012 Importancia de estudiar los sólidos cristalinos La mayoría de los compuestos inorgánicos son sólidos Casi todos los elementos
PARÁBOLA. 1) para la parte positiva: 2) para la parte negativa: 3) para la parte positiva: 4) para la parte negativa:
 Página 90 5 LA PARÁBOLA 5.1 DEFINICIONES La parábola es el lugar geométrico 4 de todos los puntos cuyas distancias a una recta fija, llamada, y a un punto fijo, llamado foco, son iguales entre sí. Hay
Página 90 5 LA PARÁBOLA 5.1 DEFINICIONES La parábola es el lugar geométrico 4 de todos los puntos cuyas distancias a una recta fija, llamada, y a un punto fijo, llamado foco, son iguales entre sí. Hay
De cualquier manera, solo estudiaremos en esta unidad los compuestos inorgánicos.
 Unidad 3 Ácidos, Hidróxidos y Sales: óxidos básicos, óxidos ácidos, hidróxidos, hidrácidos o ácidos binarios, ácidos ternarios, sales binarias, ternarias y cuaternarias. Formación y nomenclatura. Enlaces
Unidad 3 Ácidos, Hidróxidos y Sales: óxidos básicos, óxidos ácidos, hidróxidos, hidrácidos o ácidos binarios, ácidos ternarios, sales binarias, ternarias y cuaternarias. Formación y nomenclatura. Enlaces
ENTREACTO GEOMETRICO TOPOLOGICO
 ENTREACTO GEOMETRICO TOPOLOGICO ION CLORO ION SODIO ION OXIGENO ION HIDROGENO NEGATIVO POSITIVO NEGATIVO POSITIVO MODELO CON ESFERAS RIGIDAS ELECTRICAMENTE CARGADAS LOS TAMAÑOS RELATIVOS DE ANIONES Y CATIONES
ENTREACTO GEOMETRICO TOPOLOGICO ION CLORO ION SODIO ION OXIGENO ION HIDROGENO NEGATIVO POSITIVO NEGATIVO POSITIVO MODELO CON ESFERAS RIGIDAS ELECTRICAMENTE CARGADAS LOS TAMAÑOS RELATIVOS DE ANIONES Y CATIONES
Potencial eléctrico. du = - F dl
 Introducción Como la fuerza gravitatoria, la fuerza eléctrica es conservativa. Existe una función energía potencial asociada con la fuerza eléctrica. Como veremos, la energía potencial asociada a una partícula
Introducción Como la fuerza gravitatoria, la fuerza eléctrica es conservativa. Existe una función energía potencial asociada con la fuerza eléctrica. Como veremos, la energía potencial asociada a una partícula
Física de Semiconductores Curso 2007
 Física de Semiconductores Curso 007 Ing. Electrónica- P00 Ing. Electrónica/Electricista P88 3er. Año, V cuat. Trabajo Práctico Nro. 3: Bloque Sólidos: Semiconductores intrínsecos Objetivos: Estudiar las
Física de Semiconductores Curso 007 Ing. Electrónica- P00 Ing. Electrónica/Electricista P88 3er. Año, V cuat. Trabajo Práctico Nro. 3: Bloque Sólidos: Semiconductores intrínsecos Objetivos: Estudiar las
QUÍMICA INORGÁNICA I 9/1/17. El enlace iónico. Iones. Rafael Moreno Esparza
 QUÍMICA INORGÁNICA I Rafael Moreno Esparza 0 El enlace iónico Procedencia: La fuerza electrostática que mantiene unidos a dos átomos. Los átomos tratan de tener 8 electrones en la capa de valencia Los
QUÍMICA INORGÁNICA I Rafael Moreno Esparza 0 El enlace iónico Procedencia: La fuerza electrostática que mantiene unidos a dos átomos. Los átomos tratan de tener 8 electrones en la capa de valencia Los
El agua como disolvente
 hidrofobicas El agua como disolvente El elevado momento dipolar del agua y su facilidad para formar puentes de hidrógeno hacen que el agua sea un excelente disolvente. Una molécula o ión es soluble en
hidrofobicas El agua como disolvente El elevado momento dipolar del agua y su facilidad para formar puentes de hidrógeno hacen que el agua sea un excelente disolvente. Una molécula o ión es soluble en
ESTATICA: TIPOS DE MAGNITUDES: CARACTERÍSTICAS DE UN VECTOR. Rama de la física que estudia el equilibrio de los cuerpos.
 ESTATICA: Rama de la física que estudia el equilibrio de los cuerpos. TIPOS DE MAGNITUDES: MAGNITUD ESCALAR: Es una cantidad física que se especifica por un número y una unidad. Ejemplos: La temperatura
ESTATICA: Rama de la física que estudia el equilibrio de los cuerpos. TIPOS DE MAGNITUDES: MAGNITUD ESCALAR: Es una cantidad física que se especifica por un número y una unidad. Ejemplos: La temperatura
Ing. Fredy Velázquez Soto
 Ing. Fredy Velázquez Soto TIPOS DE SÓLIDOS Sólidos cristalinos Los átomos, iones o moléculas se empaquetan en un arreglo ordenado Sólidos covalentes ( diamante, cristales de cuarzo), sólidos metálicos,
Ing. Fredy Velázquez Soto TIPOS DE SÓLIDOS Sólidos cristalinos Los átomos, iones o moléculas se empaquetan en un arreglo ordenado Sólidos covalentes ( diamante, cristales de cuarzo), sólidos metálicos,
Talento Matemático 2002/2003. Real Academia de Ciencias
 Volvemos al hermoso tema de la simetría. Además de la imágenes de multitud de objetos y de seres vivos que poseen simetrías recuerdas en qué consistía una simetría desde el punto de vista matemático?,
Volvemos al hermoso tema de la simetría. Además de la imágenes de multitud de objetos y de seres vivos que poseen simetrías recuerdas en qué consistía una simetría desde el punto de vista matemático?,
Operación de Microsoft Excel
 Representación gráfica de datos Generalidades Excel puede crear gráficos a partir de datos previamente seleccionados en una hoja de cálculo. El usuario puede incrustar un gráfico en una hoja de cálculo,
Representación gráfica de datos Generalidades Excel puede crear gráficos a partir de datos previamente seleccionados en una hoja de cálculo. El usuario puede incrustar un gráfico en una hoja de cálculo,
UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUÍMICAS FUNDAMENTOS ESPECTROSCOPICOS ORBITALES ATÓMICOS
 UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUÍMICAS FUNDAMENTOS ESPECTROSCOPICOS Integrantes: Walter Bermúdez Lizbeth Sánchez Curso: Jueves 10:00 a 12:00 ORBITALES ATÓMICOS 1.- Definición de
UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUÍMICAS FUNDAMENTOS ESPECTROSCOPICOS Integrantes: Walter Bermúdez Lizbeth Sánchez Curso: Jueves 10:00 a 12:00 ORBITALES ATÓMICOS 1.- Definición de
SIMETRÍA. http://www.chem.ox.ac.uk/courses/molecular_symmetry/part2.html http://www.chem.ox.ac.uk/vrchemistry/sym/splash.html
 SIMETRÍA Elementos y operaciones de simetría Grupos puntuales de simetría Modelo de repulsión de pares de electrones de la capa de valencia (VSEPR) Simetría de las moléculas Tablas de caracteres http://www.chem.ox.ac.uk/courses/molecular_symmetry/part2.html
SIMETRÍA Elementos y operaciones de simetría Grupos puntuales de simetría Modelo de repulsión de pares de electrones de la capa de valencia (VSEPR) Simetría de las moléculas Tablas de caracteres http://www.chem.ox.ac.uk/courses/molecular_symmetry/part2.html
4. Estructura atómica, enlaces y Ordenamiento atómico de los metales
 4. Estructura atómica, enlaces y Ordenamiento atómico de los metales Atomo Unidad estructural básica de todos los materiales. En nuestro modelo, los átomos están constituidos por tres partículas subatómicas
4. Estructura atómica, enlaces y Ordenamiento atómico de los metales Atomo Unidad estructural básica de todos los materiales. En nuestro modelo, los átomos están constituidos por tres partículas subatómicas
ESTADO SOLIDO. Propiedades 03/07/2012. Fuerte interacción entre partículas
 ESTADO SOLIDO Propiedades Fuerte interacción entre partículas Ocupan posiciones relativamente fijas las partículas vibran Tienen forma propia y definida Son prácticamente incompresibles No difunden entre
ESTADO SOLIDO Propiedades Fuerte interacción entre partículas Ocupan posiciones relativamente fijas las partículas vibran Tienen forma propia y definida Son prácticamente incompresibles No difunden entre
Tema 9. SOLIDOS COVALENTES
 Tema 9. SOLIDOS COVALENTES Introducción Estructuras de no-metales Boro Carbono Fósforo Arsénico, Antimonio y Bismuto Selenio y Telurio Estructuras de óxidos Estructuras basadas en tetraedros Estructuras
Tema 9. SOLIDOS COVALENTES Introducción Estructuras de no-metales Boro Carbono Fósforo Arsénico, Antimonio y Bismuto Selenio y Telurio Estructuras de óxidos Estructuras basadas en tetraedros Estructuras
Física P.A.U. ELECTROMAGNETISMO 1 ELECTROMAGNETISMO. F = m a
 Física P.A.U. ELECTOMAGNETISMO 1 ELECTOMAGNETISMO INTODUCCIÓN MÉTODO 1. En general: Se dibujan las fuerzas que actúan sobre el sistema. Se calcula la resultante por el principio de superposición. Se aplica
Física P.A.U. ELECTOMAGNETISMO 1 ELECTOMAGNETISMO INTODUCCIÓN MÉTODO 1. En general: Se dibujan las fuerzas que actúan sobre el sistema. Se calcula la resultante por el principio de superposición. Se aplica
Tema 3. Relaciones periódicas entre los elementos
 Tema 3. Relaciones periódicas entre los elementos. Desarrollo de la tabla periódica. Clasificación de los elementos. Variaciones periódicas de propiedades físicas: carga nuclear efectiva, radio atómico,
Tema 3. Relaciones periódicas entre los elementos. Desarrollo de la tabla periódica. Clasificación de los elementos. Variaciones periódicas de propiedades físicas: carga nuclear efectiva, radio atómico,
Ablandamiento de agua mediante el uso de resinas de intercambio iónico.
 Ablandamiento de agua por intercambio iónica página 1 Ablandamiento de agua mediante el uso de resinas de intercambio iónico. (Fuentes varias) Algunos conceptos previos: sales, iones y solubilidad. Que
Ablandamiento de agua por intercambio iónica página 1 Ablandamiento de agua mediante el uso de resinas de intercambio iónico. (Fuentes varias) Algunos conceptos previos: sales, iones y solubilidad. Que
Química I. Objetivos de aprendizaje del tema
 Tema 3 Estados de la materia Objetivos de aprendizaje del tema Al finalizar el tema serás capaz de: Distinguir los estados físicos de la materia. Explicar los cambios de la materia en estado gaseoso identificando
Tema 3 Estados de la materia Objetivos de aprendizaje del tema Al finalizar el tema serás capaz de: Distinguir los estados físicos de la materia. Explicar los cambios de la materia en estado gaseoso identificando
ESTADO SOLIDO Al contrario de lo que sucede con los estados líquido y gaseoso, una sustancia en estado sólido posee forma definida y rigidez.
 ESTADO SOLIDO Al contrario de lo que sucede con los estados líquido y gaseoso, una sustancia en estado sólido posee forma definida y rigidez. Por rigidez se entiende que la energía de las atracciones intermoleculares
ESTADO SOLIDO Al contrario de lo que sucede con los estados líquido y gaseoso, una sustancia en estado sólido posee forma definida y rigidez. Por rigidez se entiende que la energía de las atracciones intermoleculares
Líneas Equipotenciales
 Líneas Equipotenciales A.M. Velasco (133384) J.P. Soler (133380) O.A. Botina (133268) Departamento de física, facultad de ciencias, Universidad Nacional de Colombia Resumen. En esta experiencia se estudia
Líneas Equipotenciales A.M. Velasco (133384) J.P. Soler (133380) O.A. Botina (133268) Departamento de física, facultad de ciencias, Universidad Nacional de Colombia Resumen. En esta experiencia se estudia
Corresponde a la operación que consiste en no hacer nada. Todos los objetos poseen al menos este elemento
 ELEMENTOS Y OPERACIONES DE SIMETRÍA Identidad (E) Corresponde a la operación que consiste en no hacer nada. Todos los objetos poseen al menos este elemento Eje de simetría (Cn) Eje que pasa por el objeto
ELEMENTOS Y OPERACIONES DE SIMETRÍA Identidad (E) Corresponde a la operación que consiste en no hacer nada. Todos los objetos poseen al menos este elemento Eje de simetría (Cn) Eje que pasa por el objeto
Divisibilidad y números primos
 Divisibilidad y números primos Divisibilidad En muchos problemas es necesario saber si el reparto de varios elementos en diferentes grupos se puede hacer equitativamente, es decir, si el número de elementos
Divisibilidad y números primos Divisibilidad En muchos problemas es necesario saber si el reparto de varios elementos en diferentes grupos se puede hacer equitativamente, es decir, si el número de elementos
Tecnología de Materiales
 Tecnología de Materiales 1.1.-Introducción: Los materiales son sustancias de las que cualquier cosa o producto está compuesto. Desde el comienzo de la civilización, los materiales junto con la energía
Tecnología de Materiales 1.1.-Introducción: Los materiales son sustancias de las que cualquier cosa o producto está compuesto. Desde el comienzo de la civilización, los materiales junto con la energía
Definición de vectores
 Definición de vectores Un vector es todo segmento de recta dirigido en el espacio. Cada vector posee unas características que son: Origen: O también denominado Punto de aplicación. Es el punto exacto sobre
Definición de vectores Un vector es todo segmento de recta dirigido en el espacio. Cada vector posee unas características que son: Origen: O también denominado Punto de aplicación. Es el punto exacto sobre
Apoyo para la preparación de los estudios de Ingeniería y Arquitectura Física (Preparación a la Universidad) Unidad 4: Vectores
 Apoyo para la preparación de los estudios de Ingeniería y Arquitectura Física (Preparación a la Universidad) Unidad 4: Vectores Universidad Politécnica de Madrid 5 de marzo de 2010 2 4.1. Planificación
Apoyo para la preparación de los estudios de Ingeniería y Arquitectura Física (Preparación a la Universidad) Unidad 4: Vectores Universidad Politécnica de Madrid 5 de marzo de 2010 2 4.1. Planificación
ESTRUCTURA * MOLÉCULAS COVALENTES (TRPECV) * METALES * COMPUESTOS IÓNICOS
 REPARTIDO 4 2007 ESTRUCTURA * MOLÉCULAS COVALENTES (TRPECV) * METALES * COMPUESTOS IÓNICOS Bibliografía: - Química, La Ciencia Central, T.L.Brown, H.E.LeMay, Jr., B. Bursten. Ed. Prentice-Hall, México,
REPARTIDO 4 2007 ESTRUCTURA * MOLÉCULAS COVALENTES (TRPECV) * METALES * COMPUESTOS IÓNICOS Bibliografía: - Química, La Ciencia Central, T.L.Brown, H.E.LeMay, Jr., B. Bursten. Ed. Prentice-Hall, México,
6. VECTORES Y COORDENADAS
 6. VECTORES Y COORDENADAS Página 1 Traslaciones. Vectores Sistema de referencia. Coordenadas. Punto medio de un segmento Ecuaciones de rectas. Paralelismo. Distancias Página 2 1. TRASLACIONES. VECTORES
6. VECTORES Y COORDENADAS Página 1 Traslaciones. Vectores Sistema de referencia. Coordenadas. Punto medio de un segmento Ecuaciones de rectas. Paralelismo. Distancias Página 2 1. TRASLACIONES. VECTORES
3.1 DEFINICIÓN. Figura Nº 1. Vector
 3.1 DEFINICIÓN Un vector (A) una magnitud física caracterizable mediante un módulo y una dirección (u orientación) en el espacio. Todo vector debe tener un origen marcado (M) con un punto y un final marcado
3.1 DEFINICIÓN Un vector (A) una magnitud física caracterizable mediante un módulo y una dirección (u orientación) en el espacio. Todo vector debe tener un origen marcado (M) con un punto y un final marcado
PRINCIPIOS TEÓRICOS ENLACE QUÍMICO TIPOS DE ENLACES
 TABLA DE CONTENIDOS Carátula 1 Tabla de Contenidos 3 Introducción 4 Objetivos 5 Principios Teóricos 6 6 Tipos de Enlaces 6 Enlace Iónico 7 Estructuras de los compuestos iónicos 8 Enlace Covalente 11 Enlace
TABLA DE CONTENIDOS Carátula 1 Tabla de Contenidos 3 Introducción 4 Objetivos 5 Principios Teóricos 6 6 Tipos de Enlaces 6 Enlace Iónico 7 Estructuras de los compuestos iónicos 8 Enlace Covalente 11 Enlace
 Diapositiva 1 Para presentar los semiconductores, es útil empezar revisando los conductores. Hay dos perspectivas desde las que se puede explorar la conducción: 1) podemos centrarnos en los dispositivos
Diapositiva 1 Para presentar los semiconductores, es útil empezar revisando los conductores. Hay dos perspectivas desde las que se puede explorar la conducción: 1) podemos centrarnos en los dispositivos
Cómo se unen los átomos
 Nivel: 2.º Medio Subsector: Ciencias químicas Unidad temática: Los cuerpos presentan aspectos y propiedades diferentes según el tipo de átomos que los componen y según la forma en que estos se unen. Pensemos
Nivel: 2.º Medio Subsector: Ciencias químicas Unidad temática: Los cuerpos presentan aspectos y propiedades diferentes según el tipo de átomos que los componen y según la forma en que estos se unen. Pensemos
CAPÍTULO II. FUENTES Y DETECTORES ÓPTICOS. Uno de los componentes clave en las comunicaciones ópticas es la fuente de
 CAPÍTULO II. FUENTES Y DETECTORES ÓPTICOS. 2.1 INTRODUCCIÓN. Uno de los componentes clave en las comunicaciones ópticas es la fuente de luz monocromática. En sistemas de comunicaciones ópticas, las fuentes
CAPÍTULO II. FUENTES Y DETECTORES ÓPTICOS. 2.1 INTRODUCCIÓN. Uno de los componentes clave en las comunicaciones ópticas es la fuente de luz monocromática. En sistemas de comunicaciones ópticas, las fuentes
2.1.- ESTRUCTURA DEL ÁTOMO
 2.1.- ESTRUCTURA DEL ÁTOMO El átomo está formado por un núcleo, que contiene nuetrones y protones, el que a su vez esta rodeado por electrones. La carga eléctrica de un átomo es nula. Número atómico es
2.1.- ESTRUCTURA DEL ÁTOMO El átomo está formado por un núcleo, que contiene nuetrones y protones, el que a su vez esta rodeado por electrones. La carga eléctrica de un átomo es nula. Número atómico es
4 Estructuras de los sólidos
 4 Estructuras de los sólidos 4.1 Comparación entre las propiedades de sólidos, líquidos y gases 4.2 Fuerzas entre moléculas y iones 4.3 Estructuras de los cristales 4.4 Sólidos metálicos 4.5 Sólidos iónicos
4 Estructuras de los sólidos 4.1 Comparación entre las propiedades de sólidos, líquidos y gases 4.2 Fuerzas entre moléculas y iones 4.3 Estructuras de los cristales 4.4 Sólidos metálicos 4.5 Sólidos iónicos
Lecturas previas a las clases del 14 y 20 de diciembre (Tema 20)
 Lecturas previas a las clases del 14 y 20 de diciembre (Tema 20) La lectura de los epígrafes que se indican y del resumen que sigue es indispensable para las clases magistrales del 14 y 20 de diciembre
Lecturas previas a las clases del 14 y 20 de diciembre (Tema 20) La lectura de los epígrafes que se indican y del resumen que sigue es indispensable para las clases magistrales del 14 y 20 de diciembre
Tema 4 Orbítales Moleculares. Hibridación
 Tema 4 Orbítales Moleculares Orbital atómico s, p (d y f) Los orbitales atómicos se mezclan para formar nuevos orbitales híbridos hibridación o hibridización orbitales híbridos sp 3, sp 2 y sp Se altera
Tema 4 Orbítales Moleculares Orbital atómico s, p (d y f) Los orbitales atómicos se mezclan para formar nuevos orbitales híbridos hibridación o hibridización orbitales híbridos sp 3, sp 2 y sp Se altera
TEMA 1: REPRESENTACIÓN GRÁFICA. 0.- MANEJO DE ESCUADRA Y CARTABON (Repaso 1º ESO)
 TEMA 1: REPRESENTACIÓN GRÁFICA 0.- MANEJO DE ESCUADRA Y CARTABON (Repaso 1º ESO) Son dos instrumentos de plástico transparente que se suelen usar de forma conjunta. La escuadra tiene forma de triángulo
TEMA 1: REPRESENTACIÓN GRÁFICA 0.- MANEJO DE ESCUADRA Y CARTABON (Repaso 1º ESO) Son dos instrumentos de plástico transparente que se suelen usar de forma conjunta. La escuadra tiene forma de triángulo
Traslación de puntos
 LECCIÓN CONDENSADA 9.1 Traslación de puntos En esta lección trasladarás figuras en el plano de coordenadas definirás una traslación al describir cómo afecta un punto general (, ) Una regla matemática que
LECCIÓN CONDENSADA 9.1 Traslación de puntos En esta lección trasladarás figuras en el plano de coordenadas definirás una traslación al describir cómo afecta un punto general (, ) Una regla matemática que
CRISTALOQUÍMICA TEMA 6 ESTRUCTURAS CRISTALINAS. Empaquetados compactos. Coordinación
 CRISTALOQUÍMICA TEMA 6 ESTRUCTURAS CRISTALINAS Empaquetados compactos. Coordinación ÍNDICE 6.1 Introducción 6.2 Estructuras cristalinas 6.3 Enlace en las estructuras cristalinas 6.4 Cristales iónicos 6.5
CRISTALOQUÍMICA TEMA 6 ESTRUCTURAS CRISTALINAS Empaquetados compactos. Coordinación ÍNDICE 6.1 Introducción 6.2 Estructuras cristalinas 6.3 Enlace en las estructuras cristalinas 6.4 Cristales iónicos 6.5
TEMA: CAMPO ELÉCTRICO
 TEMA: CAMPO ELÉCTRICO C-J-06 Una carga puntual de valor Q ocupa la posición (0,0) del plano XY en el vacío. En un punto A del eje X el potencial es V = -120 V, y el campo eléctrico es E = -80 i N/C, siendo
TEMA: CAMPO ELÉCTRICO C-J-06 Una carga puntual de valor Q ocupa la posición (0,0) del plano XY en el vacío. En un punto A del eje X el potencial es V = -120 V, y el campo eléctrico es E = -80 i N/C, siendo
a De los siguientes cuerpos geométricos, di cuáles son poliedros y cuáles no. Razona tu respuesta.
 POLIEDROS Ejercicio nº 1.- a De los siguientes cuerpos geométricos, di cuáles son poliedros y cuáles no. Razona tu respuesta. b Cuál es la relación llamada fórmula de Euler que hay entre el número de caras,
POLIEDROS Ejercicio nº 1.- a De los siguientes cuerpos geométricos, di cuáles son poliedros y cuáles no. Razona tu respuesta. b Cuál es la relación llamada fórmula de Euler que hay entre el número de caras,
ELECTROQUÍMICA. 1. Procesos electroquímicos (pila). 2. Potenciales normales de electrodo. 3. Ecuación de Nernst. 4. Electrolisis. 5. Leyes de Faraday.
 ELECTROQUÍMICA 1. Procesos electroquímicos (pila). 2. Potenciales normales de electrodo. 3. Ecuación de Nernst. 4. Electrolisis. 5. Leyes de Faraday. Química 2º bachillerato Electroquímica 1 0. CONOCIMIENTOS
ELECTROQUÍMICA 1. Procesos electroquímicos (pila). 2. Potenciales normales de electrodo. 3. Ecuación de Nernst. 4. Electrolisis. 5. Leyes de Faraday. Química 2º bachillerato Electroquímica 1 0. CONOCIMIENTOS
