ENTREACTO GEOMETRICO TOPOLOGICO
|
|
|
- Mario Peña Sevilla
- hace 5 años
- Vistas:
Transcripción
1 ENTREACTO GEOMETRICO TOPOLOGICO
2 ION CLORO ION SODIO ION OXIGENO ION HIDROGENO NEGATIVO POSITIVO NEGATIVO POSITIVO
3 MODELO CON ESFERAS RIGIDAS ELECTRICAMENTE CARGADAS LOS TAMAÑOS RELATIVOS DE ANIONES Y CATIONES SON DETERMINANTES PARA DEFINIR EL ARREGLO ESPACIAL MAS ESTABLE
4 4310 TRES ESFERAS TANGENTES FORMAN UN HUECO EN EL QUE, OTRA ESFERA PUEDE TAMBIEN SER TANGENTE, SI LAS DIMENSIONES SON: Sen /a = sen /b b/a = sen / sen (R + r)/2r = sen30/sen120 = 0.5/0.866 = (R + r) = (2R) (R + r) = R 1 + r/r = R R + r r/r = R/r = 6.46 HUGO TORRENS
5 4312 CUATRO ESFERAS TANGENTES FORMAN UN HUECO EN EL QUE, OTRA ESFERA PUEDE TAMBIEN SER TANGENTE, SI LAS DIMENSIONES SON: sen /a = sen /b b/a = sen / sen 2R/(2R + 2r) = sen45/sen90 = /1 = R = (2R) (2r) 1 = r/R ( )/ = r/r 2R R + r 90 0 r/r = R/r = HUGO TORRENS
6 CINCO ESFERAS TANGENTES FORMAN UN HUECO EN EL QUE, OTRA ESFERA PUEDE TAMBIEN SER TANGENTE, SI LAS DIMENSIONES SON: 4314 sen /a = sen /b b/a = sen / sen (R + r)/2r = sen54/sen72 = 0.809/0.951 = R + r = 0.851(2R)=1.7R 1 + r/r= 1.7 r/r =.7 B c A b a C r/r = 0.7 R/r = 1.42 HUGO TORRENS
7 SEIS ESFERAS TANGENTES FORMAN UN HUECO EN EL QUE, OTRA ESFERA PUEDE TAMBIEN SER TANGENTE, SI LAS DIMENSIONES SON: 4315 sen /a = sen /b b/a = sen / sen (R + r)/2r = sen60/sen60 = 1 R + r = 2R 1 + r/r= 2 r/r = 1 B c A b a C r/r = 1 = R/r HUGO TORRENS
8 r/r =.1547 R/r = r/r =.4142 R/r = r/r =.7 R/r = 1.42 r/r = 1 R/r = 1 HUGO TORRENS
9 RELACION DE RADIOS Y ESTRUCTURA
10 RELACION DE RADIOS Y ESTRUCTURA
11 TRES TIPOS DE PLANOS OBTENIDOS AL ORDENAS ESFERAS CON DISTINTOS EMPAQUES.
12 4307 HUECO TETRAEDRICO HUGO TORRENS
13 4307 HUECO OCTAEDRICO HUGO TORRENS
14 HUGO TORRENS 4308
15 HUGO TORRENS 4301
16 HUGO TORRENS 4302
17 HUGO TORRENS 4303
18 HUGO TORRENS 4304
19 HUGO TORRENS 4305
20 HUGO TORRENS 4317
21 HUGO TORRENS 4318
22 4306 LA SIGUIENTE FIGURA MUESTRA CRISTALES CASI PERFECTOS DE CLORURO DE SODIO, CRECIDOS EN AGUA PURA Y QUE, A LA VISTA, LUCEN COMO UN POLVO BLANCO... NaCl CON MICROSCOPIO ELECTRONICO DE BARRIDO HUGO TORRENS
23 ARREGLO DE ESFERAS RIGIDAS: LA CAPA A ES UNICA Y LA CAPA B OCUPA LOS HUECOS QUE FORMA LA A. LA TERCERA CAPA PUEDE ESCOGER OCUPAR UN HUECO QUE LA UBICA SOBRE LA PRIMERA CAPA O UN HUECO QUE LA UBICA EN UNA TERCERA CAPA C. HUECOS OCTAÉDRICOS Y HUECOS TETRAÉDRICOS.
24 EL HUECO TETRAÉDRICO APARECE ENTRE UNA ESFERA SOBRE EL TRIÁNGULO QUE FORMAN OTRAS TRES. EL HUECO TETRAÉDRICO PUEDE ACOMODAR UNA ESFERA DE RADIO IGUAL O INFERIOR A 0.225R.
25 HUECOS EN ESTRUCTURAS EMPAQUETADAS EL HUECO OCTAÉDRICO APARECE ENTRE DOS TRIÁNGULOS DE ESFERAS QUE ESTÁN OPUESTOS ENTRE SÍ. LOS SEIS ÁTOMOS QUE LO FORMAN SE DISPONEN EN LOS VÉRTICES DE UN OCTAEDRO. UN HUECO DE ESTAS CARACTERÍSTICAS PUEDE ACOMODAR OTRA ESFERA DE RADIO 0.414R.
26 ARREGLO DE ESFERAS RIGIDAS: EN CADA UNO DE ESTOS ARREGLOS, LOS HUECOS ENTRE LAS ESFERAS SON DISTINTOS
27 HUGO TORRENS 4340
28
29 * * * * * * * * * *
30 SI PERMITIMOS QUE LAS ESFERAS TENGAN CARGA, TENDRIAMOS QUE LOS ARREGLOS ESTABLES SON AQUELLOS QUE MAXIMIZAN ATRACCION Y MINIMIZAN REPULSION ESTABLE METAESTABLE INESTABLE
31 TETRAOXIDO DE Fe(II, III) CLORURO DE HIERRO (III) Fe 2 O 4 FeCl 3
32 ELRADIO IONICO DEPENDE DEL NUMERO DE COORDINACION
33 RELACION DE RADIOS r/r CRISTAL NC=8 CsCl, CaF2 NC=6 NaCl, RUTILO NC=4 WURTZITA, BLENDA NC=3
34 RELACION DE RADIOS X = r A / r B POLIEDRO COORDINACION NC=4 ZnS NC=6 NaCl, TIO 2 NC=8 CsCl, CaF 2
35 Estructura cristalina Ejemplo Antifluorita K 2 O, K 2 S, Li 2 O, Na 2 O, Na 2 Se, Na 2 S Cloruro de cesio CsCl, CaS, TlSb, CsCN, CuZn Fluorita CaF 2, UO 2, BaCl 2, HgF 2, PbO 2 Arseniuro de níquel NiAs, NiS, FeS, PtSn, CoS Perovskita CaTiO 3, BaTiO 3, SrTiO 3 Cloruro de sodio NaCl, LiCl, KBr, RbI, AgCl, AgBr, MgO, CaO, TiO, FeO, NiO, SnAs, UC, ScN Rutilo TiO 2, MnO 2, SnO 2, WO 2, MgF 2, NiF 2 Blenda ZnS, CuCl, CdS, HgS, GaP, InAs Wurtzita ZnS, ZnO, BeO, MnS, AgI, AlN, SiC, NH 4 F
36 ESTRUCTURAS CRISTALINAS MAS COMUNES
37 CRISTALES MAS COMUNES ESTRUCTURA DEL CLORURO DE SODIO NUMERO DE COORDINACION 6
38 HUGO TORRENS
39 CRISTALES MAS COMUNES ESTRUCTURA DEL CLORURO DE CESIO NÚMERO DE COORDINACIÓN: 8 POR CADA IÓN DE CESIO EXISTEN 8 IONES DE CLORURO, Y POR CADA IÓN DE CLORURO EXISTEN 8 IONES DE CESIO.
40 HUGO TORRENS 4322
41 CRISTALES MAS COMUNES ZnS ESTRUCTURA DE LA BLENDA DE ZINC a) NÚMERO DE COORDINACIÓN 4
42 HUGO TORRENS BLENDA DE ZINC ZnS
43 CRISTALES MAS COMUNES ZnS ESTRUCTURA DE WURTZITA b) NÚMERO DE COORDINACIÓN 4
44 HUGO TORRENS WURTZITA
45 CRISTALES MAS COMUNES BLENDA DE ZINC WURTZITA
46 CRISTALES MAS COMUNES ESTRUCTURA DE LA FLUORITA CaF 2 LOS NÚMEROS DE COORDINACIÓN SON 8 PARA EL CATIÓN Y 4 PARA EL ANIÓN
47 HUGO TORRENS FLUORITA CaF 2
48 CRISTALES MAS COMUNES ESTRUCTURA DEL RUTILO TiO 2 LOS NÚMEROS DE COORDINACIÓN SON 6 PARA EL CATIÓN Y 3 PARA EL ANIÓN
49 HUGO TORRENS RUTILO TiO 2
50 CRISTALES MAS COMUNES ESTRUCTURA TIPO PEROVSKITA COMPUESTOS ABX
51 CRISTALES MAS COMUNES ESTRUCTURA HEXAGONAL COMPACTA Ejemplos: He, N, Be, Mg, Co, Zn, Sc, Ti, etc
52 HUGO TORRENS CARBONATO DE CALCIO CALCITA
53 HUGO TORRENS CARBONATO DE CALCIO ARAGONITA
54 CARBONATO DE CALCIO CALCITA
55
56 HUGO TORRENS CRISTOBALITA SiO 2
57 HUGO TORRENS
58 Redes de Bravais
Los sólidos iónicos. Estructuras características de los sólidos iónicos
 Los sólidos iónicos Los compuestos iónicos suelen presentar una serie de características físicas que los distinguen de los covalentes. Así, los sólidos iónicos como el cloruro sódico y el nitrato de potasio
Los sólidos iónicos Los compuestos iónicos suelen presentar una serie de características físicas que los distinguen de los covalentes. Así, los sólidos iónicos como el cloruro sódico y el nitrato de potasio
CUAL DE LAS SIGUIENTES CARACTERISTICAS DEFINEN MEJOR A UN COMPUESTO IONICO?
 CUAL DE LAS SIGUIENTES CARACTERISTICAS DEFINEN MEJOR A UN COMPUESTO IONICO? A) FORMA CRISTALES B) FUNDE A ALTAS TEMPERATURAS C) CONDUCE ELECTRICIDAD EN DISOLUCION D) ES INCOLORO E) ES DURO 5- CUÁL DE LOS
CUAL DE LAS SIGUIENTES CARACTERISTICAS DEFINEN MEJOR A UN COMPUESTO IONICO? A) FORMA CRISTALES B) FUNDE A ALTAS TEMPERATURAS C) CONDUCE ELECTRICIDAD EN DISOLUCION D) ES INCOLORO E) ES DURO 5- CUÁL DE LOS
Tipos de estructuras. Introducción a la Ciencia de Materiales. M. Bizarro F. M. Sánchez
 Tipos de estructuras Empaquetamiento compacto Son estructuras formadas por átomos de igual tamaño que se unen mediante enlace metálico (esferas duras) A B A : A B C : FCC vs HCP El factor de empaquetamiento
Tipos de estructuras Empaquetamiento compacto Son estructuras formadas por átomos de igual tamaño que se unen mediante enlace metálico (esferas duras) A B A : A B C : FCC vs HCP El factor de empaquetamiento
Cristal iónico. Cristal iónico
 Cristal iónico Cristal iónico: sustancia sólida cuya estructura puede representarse como un arreglo infinito y regular de iones cargados opuestamente. La red se mantiene principalmente por fuerzas electrostáticas
Cristal iónico Cristal iónico: sustancia sólida cuya estructura puede representarse como un arreglo infinito y regular de iones cargados opuestamente. La red se mantiene principalmente por fuerzas electrostáticas
ESTRUCTURAS CARACTERÍSTICAS
 ESTRUCTURAS CARACTERÍSTICAS En este capítulo se describen algunas estructuras muy simples que permitirán analizar la disposición de los átomos de diversos compuestos característicos en los que el enlace
ESTRUCTURAS CARACTERÍSTICAS En este capítulo se describen algunas estructuras muy simples que permitirán analizar la disposición de los átomos de diversos compuestos característicos en los que el enlace
Estructura de sólidos
 Estructura de sólidos Química Inorgánica - 2006 Tipos de estructuras cristalinas cristal enlace características molecular covalente-baja energía cristales blandos, bajo p.f. red covalente covalente cristales
Estructura de sólidos Química Inorgánica - 2006 Tipos de estructuras cristalinas cristal enlace características molecular covalente-baja energía cristales blandos, bajo p.f. red covalente covalente cristales
QUIMICA DE MATERIALES 1.2. NATURALEZA DE LA UNION QUIMICA
 QUIMICA DE MATERIALES 1.2. NATURALEZA DE LA UNION QUIMICA ENLACE COVALENTE Los electrones están compartidos por los átomos IONICO Uno o más electrones son transferidos entre los átomos, formando iones
QUIMICA DE MATERIALES 1.2. NATURALEZA DE LA UNION QUIMICA ENLACE COVALENTE Los electrones están compartidos por los átomos IONICO Uno o más electrones son transferidos entre los átomos, formando iones
Consideraciones sobre estructuras representativas
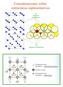 Consideraciones sobre estructuras representativas CONSIDERACIONES SOBRE ESTRUCTURAS REPRESENTATIVAS: En el empacamiento compacto hcp y ccp el número de coordinación es 12 Los elementos metálicos son los
Consideraciones sobre estructuras representativas CONSIDERACIONES SOBRE ESTRUCTURAS REPRESENTATIVAS: En el empacamiento compacto hcp y ccp el número de coordinación es 12 Los elementos metálicos son los
ESTRUCTURA DE SÓLIDOS
 Estructura de sólidos 1 ESTRUCTURA DE SÓLIDOS La mayoría de los compuestos inorgánicos se presentan como sólidos en un arreglo ordenado de átomos, iones o moléculas. Los sólidos pueden ser: cristalinos:
Estructura de sólidos 1 ESTRUCTURA DE SÓLIDOS La mayoría de los compuestos inorgánicos se presentan como sólidos en un arreglo ordenado de átomos, iones o moléculas. Los sólidos pueden ser: cristalinos:
ENLACE IÓNICO. Dra. Silvia Elena Castillo Blum
 ENLACE IÓNICO Dra. Silvia Elena Castillo Blum Enlace Químico ENLACE IÓNICO ENLACE COVALENTE ENLACE METÁLICO 2 Definición IUPAC Hay un enlace químico entre dos átomos o grupos de átomos cuando las fuerzas
ENLACE IÓNICO Dra. Silvia Elena Castillo Blum Enlace Químico ENLACE IÓNICO ENLACE COVALENTE ENLACE METÁLICO 2 Definición IUPAC Hay un enlace químico entre dos átomos o grupos de átomos cuando las fuerzas
Estructuras Cristalinas
 Estructuras Cristalinas Bibliografía: Solid State Chemistry: An introduction, L. Smart and E. Moore. 1992 Solid State Chemistry and its applications, A.R. West. 1984 1 Enlace en Cerámicos Iónico Mezcla
Estructuras Cristalinas Bibliografía: Solid State Chemistry: An introduction, L. Smart and E. Moore. 1992 Solid State Chemistry and its applications, A.R. West. 1984 1 Enlace en Cerámicos Iónico Mezcla
Tema 4. Cristaloquímica. Descripción estructural y
 Tema 4. Cristaloquímica. Descripción estructural y estructuras tipos Qué objetivos tiene la Cristaloquímica? Las fases cristalinas son componentes esenciales de los materiales, y especificamente de los
Tema 4. Cristaloquímica. Descripción estructural y estructuras tipos Qué objetivos tiene la Cristaloquímica? Las fases cristalinas son componentes esenciales de los materiales, y especificamente de los
ENLACE QUÍMICO. 2º Bachillerato
 ENLACE QUÍMICO 2º Bachillerato Índice 1. Enlace químico 2. Enlace iónico 3. Enlace covalente 4. Fuerzas intermoleculares 5. Enlace metálico 2 1. Enlace químico 1.1. Concepto de enlace químico. 1.2. Caracterización
ENLACE QUÍMICO 2º Bachillerato Índice 1. Enlace químico 2. Enlace iónico 3. Enlace covalente 4. Fuerzas intermoleculares 5. Enlace metálico 2 1. Enlace químico 1.1. Concepto de enlace químico. 1.2. Caracterización
Esquema del tema. Tema 4: Enlace iónico. Un poco de empirismo
 Esquema del tema Modelo iónico Características de los compuestos iónicos Corrigiendo el modelo iónico: Polarización y Módulo 12555- Química Inorgánica Título: Ingeniería Química Responsable: Juan José
Esquema del tema Modelo iónico Características de los compuestos iónicos Corrigiendo el modelo iónico: Polarización y Módulo 12555- Química Inorgánica Título: Ingeniería Química Responsable: Juan José
TEMA 8: SÓLIDOS INORGÁNICOS. 2.- Redes bidimensionales y tridimensionales
 TEMA 8: SÓLIDOS INORGÁNICOS 1.- Tipos de sólidos 2.- Redes bidimensionales y tridimensionales 3.- Celda unidad y sus parámetros: - nº de átomos / celda - nº de coordinación (NC) - fracción de volumen ocupado
TEMA 8: SÓLIDOS INORGÁNICOS 1.- Tipos de sólidos 2.- Redes bidimensionales y tridimensionales 3.- Celda unidad y sus parámetros: - nº de átomos / celda - nº de coordinación (NC) - fracción de volumen ocupado
Tema 8. Sólidos iónicos
 Tema 8. Sólidos iónicos Definiciones Estructuras iónicas Derivadas de CCP Derivadas de HCP Derivadas de empaquetamientos no compactos Racionalización de las estructuras iónicas Principios de Laves Reglas
Tema 8. Sólidos iónicos Definiciones Estructuras iónicas Derivadas de CCP Derivadas de HCP Derivadas de empaquetamientos no compactos Racionalización de las estructuras iónicas Principios de Laves Reglas
Sólidos Arreglos y celdas unitarias. Ramón L. Hernández Castillo Enero 2012
 Sólidos Arreglos y celdas unitarias Ramón L. Hernández Castillo Enero 2012 Importancia de estudiar los sólidos cristalinos La mayoría de los compuestos inorgánicos son sólidos Casi todos los elementos
Sólidos Arreglos y celdas unitarias Ramón L. Hernández Castillo Enero 2012 Importancia de estudiar los sólidos cristalinos La mayoría de los compuestos inorgánicos son sólidos Casi todos los elementos
Ilustración 15.1. El número de coordinación en el NaCl es 6:6. Cada ion esta rodeado por seis iones que tienen carga opuesta a él.
 ENLACE IÓNICO Tú sabes que existen sustancias que forman sólidos cristalinos con altos puntos de fusión, que no conducen la corriente en estado sóliso pero se vuelven buenos conductores al fundirlos o
ENLACE IÓNICO Tú sabes que existen sustancias que forman sólidos cristalinos con altos puntos de fusión, que no conducen la corriente en estado sóliso pero se vuelven buenos conductores al fundirlos o
TEMA 20. INTRODUCCIÓN AL ESTUDIO DE LOS SÓLIDOS NO MOLECULARES.
 TEMA 20. INTRODUCCIÓN AL ESTUDIO DE LOS SÓLIDOS NO MOLECULARES. TEMA 20.1. ENLACE EN SÓLIDOS NO MOLECULARES. ASPECTOS ENERGÉTICOS Y ESTRUCTURALES. POLARIZACIÓN EN EL ENLACE. TEMA 20. 2. APROXIMACIÓN AL
TEMA 20. INTRODUCCIÓN AL ESTUDIO DE LOS SÓLIDOS NO MOLECULARES. TEMA 20.1. ENLACE EN SÓLIDOS NO MOLECULARES. ASPECTOS ENERGÉTICOS Y ESTRUCTURALES. POLARIZACIÓN EN EL ENLACE. TEMA 20. 2. APROXIMACIÓN AL
Sólidos Iónicos El enlace Iónico (1)
 1 Sólidos Iónicos El enlace Iónico (1) 2 * Huheey, J. E., Keiter, R. L., Keiter, E. A., Inorganic Chemistry: Principles of Structure and Reactivity, 4ª Ed., Harper Collins, 1993. Capítulo 4. * Douglas,
1 Sólidos Iónicos El enlace Iónico (1) 2 * Huheey, J. E., Keiter, R. L., Keiter, E. A., Inorganic Chemistry: Principles of Structure and Reactivity, 4ª Ed., Harper Collins, 1993. Capítulo 4. * Douglas,
Continuo movimiento al azar. Largas, desiguales
 Gas Fuerzas Orden Distancias Propiedades Despreciables frente a la agitación térmica Continuo movimiento al azar Largas, desiguales Volúmenes variables, fluidos, bajas densidades, se difunden con rapidez
Gas Fuerzas Orden Distancias Propiedades Despreciables frente a la agitación térmica Continuo movimiento al azar Largas, desiguales Volúmenes variables, fluidos, bajas densidades, se difunden con rapidez
CAPITULO 4 SISTEMAS IONICOS
 CAPITULO 4 SISTEMAS IONICOS 1 CUÁL DE LAS SIGUIENTES REACCIONES OCURRE EN SENTIDO INVERSO AL INDICADO? A) HCl + NaBr HBr + NaCl B) CsF + LiBr CsBr + LiF C) CaO + SrS CaS + SrO D) CaSO 4 + 2LiF Li 2 SO
CAPITULO 4 SISTEMAS IONICOS 1 CUÁL DE LAS SIGUIENTES REACCIONES OCURRE EN SENTIDO INVERSO AL INDICADO? A) HCl + NaBr HBr + NaCl B) CsF + LiBr CsBr + LiF C) CaO + SrS CaS + SrO D) CaSO 4 + 2LiF Li 2 SO
Igual número de cationes y aniones. Ejemplos: cloruro de sodio (NaCl), cloruro de cesio (CsCl), blenda (ZnS), etc.
 6. MATERIALES CERÁMICOS 6.1 Estructura de los cerámicos Enlace atómico: parcial o totalmente iónico Iones metálicos: cationes (ceden sus electrones, +), aniones (aceptan electrones, - ). Estructuras cristalinas,
6. MATERIALES CERÁMICOS 6.1 Estructura de los cerámicos Enlace atómico: parcial o totalmente iónico Iones metálicos: cationes (ceden sus electrones, +), aniones (aceptan electrones, - ). Estructuras cristalinas,
CÚBICA SIMPLE HEXAGONAL ROMBOÉDRICA
 Formas de las celdas CÚBICA SIMPLE HEXAGONAL ROMBOÉDRICA TRICLÍNICA 1 1 2 3 4 C 2 3 4 5 6 5 6 7 B 8 3 1 5 2 8 A 8 6 4 Capa a Capa b Capa a Los cationes (más pequeños) ocupan los huecos formados por el
Formas de las celdas CÚBICA SIMPLE HEXAGONAL ROMBOÉDRICA TRICLÍNICA 1 1 2 3 4 C 2 3 4 5 6 5 6 7 B 8 3 1 5 2 8 A 8 6 4 Capa a Capa b Capa a Los cationes (más pequeños) ocupan los huecos formados por el
Enlace iónico. elemento poco. elemento muy + electronegativo. compuesto iónico (sal) electronegativo
 Enlace iónico Enlace iónico Necesitamos un nuevo modelo para explicar ciertas peculiaridades (Li2O). Este nuevo modelo es el enlace iónico Se forma por transferencia de electrones (no hay reparto equitativo,
Enlace iónico Enlace iónico Necesitamos un nuevo modelo para explicar ciertas peculiaridades (Li2O). Este nuevo modelo es el enlace iónico Se forma por transferencia de electrones (no hay reparto equitativo,
Ing. Fredy Velázquez Soto
 Ing. Fredy Velázquez Soto TIPOS DE SÓLIDOS Sólidos cristalinos Los átomos, iones o moléculas se empaquetan en un arreglo ordenado Sólidos covalentes ( diamante, cristales de cuarzo), sólidos metálicos,
Ing. Fredy Velázquez Soto TIPOS DE SÓLIDOS Sólidos cristalinos Los átomos, iones o moléculas se empaquetan en un arreglo ordenado Sólidos covalentes ( diamante, cristales de cuarzo), sólidos metálicos,
qwertyuiopasdfghjklzxcvbnmqwertyui opasdfghjklzxcvbnmqwertyuiopasdfgh jklzxcvbnmqwertyuiopasdfghjklzxcvb nmqwertyuiopasdfghjklzxcvbnmqwer
 qwertyuiopasdfghjklzxcvbnmqwertyui opasdfghjklzxcvbnmqwertyuiopasdfgh jklzxcvbnmqwertyuiopasdfghjklzxcvb nmqwertyuiopasdfghjklzxcvbnmqwer Cuestionario de Química 4 tyuiopasdfghjklzxcvbnmqwertyuiopas dfghjklzxcvbnmqwertyuiopasdfghjklzx
qwertyuiopasdfghjklzxcvbnmqwertyui opasdfghjklzxcvbnmqwertyuiopasdfgh jklzxcvbnmqwertyuiopasdfghjklzxcvb nmqwertyuiopasdfghjklzxcvbnmqwer Cuestionario de Química 4 tyuiopasdfghjklzxcvbnmqwertyuiopas dfghjklzxcvbnmqwertyuiopasdfghjklzx
Sólidos Iónicos El enlace Iónico (3)
 1 Sólidos Iónicos El enlace Iónico (3) 2 Efecto del tamaño de los iones sobre el retículo cristalino Determinar el tamaño de los iones implica fijar límites para el anión y el catión. Considerar cierto
1 Sólidos Iónicos El enlace Iónico (3) 2 Efecto del tamaño de los iones sobre el retículo cristalino Determinar el tamaño de los iones implica fijar límites para el anión y el catión. Considerar cierto
Cl Electrones de valencia: Cl: 7 3 = 21 P: 5 Total 26 Tres enlaces sencillos: - 6 Electrones restantes: 20
 ESTRUCTURAS DE LEWIS PARA EL ENLACE COVALENTE.- Lewis sugirió que los átomos comparten electrones para alcanzar la configuración de gas noble y tener así una estructura más estable. Salvo en el caso de
ESTRUCTURAS DE LEWIS PARA EL ENLACE COVALENTE.- Lewis sugirió que los átomos comparten electrones para alcanzar la configuración de gas noble y tener así una estructura más estable. Salvo en el caso de
Tema Tema 18 (I) Estados de agregación de la materia El estado sólido Estructura cristalina
 Tema 18 (I) Estados de agregación de la materia 18.1 El estado sólido 18.2 Estructura cristalina 18.3 Tipos de cristales 18.4 El estado líquido 18.5 Propiedades particulares del agua 1 2 18.1 El estado
Tema 18 (I) Estados de agregación de la materia 18.1 El estado sólido 18.2 Estructura cristalina 18.3 Tipos de cristales 18.4 El estado líquido 18.5 Propiedades particulares del agua 1 2 18.1 El estado
RESPUESTAS DE LOS EJERCICIOS DE APLICACIÓN DEL LIBRO UN ACERCAMIENTO A LA QUÍMICA CAPÍTULO N 6: REACCIONES Y LAS ECUACIONES QUÍMICAS.
 RESPUESTAS DE LOS EJERCICIOS DE APLICACIÓN DEL LIBRO UN ACERCAMIENTO A LA QUÍMICA ACLARACIÓN: Las respuestas que pudieren faltar de algunos ejercicios serán agregadas en futuras actualizaciones. CAPÍTULO
RESPUESTAS DE LOS EJERCICIOS DE APLICACIÓN DEL LIBRO UN ACERCAMIENTO A LA QUÍMICA ACLARACIÓN: Las respuestas que pudieren faltar de algunos ejercicios serán agregadas en futuras actualizaciones. CAPÍTULO
ANALISIS CUALITATIVO DE CATIONES
 ANALISIS CUALITATIVO DE CATIONES Olimpiada Veracruzana de Química 1 Dividimos a los cationes en 5 grupos: Reactivo 1 er Grupo Pb +2, Ag + y Hg +2 2. HCl 2º Grupo Hg +2, Cu +2, Cd +2, Bi +3, As +3, As +5,
ANALISIS CUALITATIVO DE CATIONES Olimpiada Veracruzana de Química 1 Dividimos a los cationes en 5 grupos: Reactivo 1 er Grupo Pb +2, Ag + y Hg +2 2. HCl 2º Grupo Hg +2, Cu +2, Cd +2, Bi +3, As +3, As +5,
Contenido. Minerales
 Contenido Minerales metales Mena, ganga, ley mineral Tipo de minerales Estructura de los materiales Tipo de enlaces: iónico, covalente, metálico, van der Waals, hidrógeno 1 Minerales Minerales sustancia
Contenido Minerales metales Mena, ganga, ley mineral Tipo de minerales Estructura de los materiales Tipo de enlaces: iónico, covalente, metálico, van der Waals, hidrógeno 1 Minerales Minerales sustancia
! Introducción a los sólidos iónicos! Qué elementos los forman?! Qué tipos de fuerzas mantienen la cohesión del cristal?
 Tema 8. Sólidos iónicos Estructura del NaCl Contenidos! Introducción a los sólidos iónicos! Qué elementos los forman?! Qué tipos de fuerzas mantienen la cohesión del cristal?! Propiedades de los sólidos
Tema 8. Sólidos iónicos Estructura del NaCl Contenidos! Introducción a los sólidos iónicos! Qué elementos los forman?! Qué tipos de fuerzas mantienen la cohesión del cristal?! Propiedades de los sólidos
ísica y uímica FORMULACIÓN Y NOMENCLATURA Nombre Óxido de bario Óxido de sodio Óxido de plata Fórmula
 Formula los siguientes compuestos: EJERCICIOS DE RECAPITULACIÓN Óxido de bario Óxido de sodio Óxido de plata BaO Na 2 O Ag 2 O Óxido de aluminio Al 2 O 3 Óxido de níquel (III) Ni 2 O 3 Óxido de cloro (VII)
Formula los siguientes compuestos: EJERCICIOS DE RECAPITULACIÓN Óxido de bario Óxido de sodio Óxido de plata BaO Na 2 O Ag 2 O Óxido de aluminio Al 2 O 3 Óxido de níquel (III) Ni 2 O 3 Óxido de cloro (VII)
01 Minerales y estructuras
 01 Minerales y estructuras Año 2017 15/08/2017 1 Contenido Minerales metales Mena, ganga, ley mineral Tipo de minerales Estructura de los materiales Tipo de enlaces: iónico, covalente, metálico, van der
01 Minerales y estructuras Año 2017 15/08/2017 1 Contenido Minerales metales Mena, ganga, ley mineral Tipo de minerales Estructura de los materiales Tipo de enlaces: iónico, covalente, metálico, van der
Tema 14.- Definición, Clasificación y Conformado
 BLOQUE V.- MATERIALES CERÁMICOS Tema 14.- Definición, y Conformado William D. Callister, Jr Introducción a la Ciencia e Ingeniería de los Materiales. Tomo **. Ed. Reverté James F. Shackerlford Introducción
BLOQUE V.- MATERIALES CERÁMICOS Tema 14.- Definición, y Conformado William D. Callister, Jr Introducción a la Ciencia e Ingeniería de los Materiales. Tomo **. Ed. Reverté James F. Shackerlford Introducción
ENLACE IÓNICO O ELECTROVALENTE
 ENLACE IÓNICO O ELECTROVALENTE Servicios Educativos Integrales Caracterizado por: o Cesión de electrones por parte de un metal a un no metal o Formación de iones de carga contraria, metal (+) y no metal
ENLACE IÓNICO O ELECTROVALENTE Servicios Educativos Integrales Caracterizado por: o Cesión de electrones por parte de un metal a un no metal o Formación de iones de carga contraria, metal (+) y no metal
Química Inorgánica-63.13- Dra.Silvia E. Jacobo. Sólidos. Estructuras Cristalinas
 Sólidos Estructuras Cristalinas Ordenamientos atómicos En gases no hay orden En líquidos hay orden de corto alcance En sólidos hay orden de largo alcance El ordenamiento está determinado por el tipo de
Sólidos Estructuras Cristalinas Ordenamientos atómicos En gases no hay orden En líquidos hay orden de corto alcance En sólidos hay orden de largo alcance El ordenamiento está determinado por el tipo de
Ejercicios tabla periódica. Enlace 4º ESO
 1. a) Indica la configuración electrónica de los átomos de los elementos A, B y C cuyos números atómicos son respectivamente: 12, 17 y 19. b) Escribe la configuración electrónica del ion más estable de
1. a) Indica la configuración electrónica de los átomos de los elementos A, B y C cuyos números atómicos son respectivamente: 12, 17 y 19. b) Escribe la configuración electrónica del ion más estable de
INTRODUCCIÓN A LA ELECTROQUÍMICA
 INTRODUCCIÓN A LA ELECTROQUÍMICA I. Q. Luis F. Farrera G. Departamento de Fisicoquímica Facultad de Química UNAM La electroquímica es la interrelación que se establece entre los sistemas químicos y los
INTRODUCCIÓN A LA ELECTROQUÍMICA I. Q. Luis F. Farrera G. Departamento de Fisicoquímica Facultad de Química UNAM La electroquímica es la interrelación que se establece entre los sistemas químicos y los
Unidad 3 Termodinámica Inorgánica. Química Inorgánica I. Compuestos iónicos Energía de red cristalina (U 0 ) Ciclo de Born-Haber
 Unidad 3 Termodinámica Inorgánica N N N N N N Química Inorgánica I Compuestos iónicos Energía de red cristalina (U 0 ) Ciclo de Born-aber Sigfrido Escalante Tovar mar-2016 [Co(L) 2 Cl 2 ]: dicloro bis-zoxazolamina
Unidad 3 Termodinámica Inorgánica N N N N N N Química Inorgánica I Compuestos iónicos Energía de red cristalina (U 0 ) Ciclo de Born-aber Sigfrido Escalante Tovar mar-2016 [Co(L) 2 Cl 2 ]: dicloro bis-zoxazolamina
SUSTANCIAS NATURALES CON ENLACE QUÍMICO IÓNICO
 SUSTANCIAS NATURALES CON ENLACE QUÍMICO IÓNICO AUTOR JAVIER RUIZ HIDALGO TEMÁTICA ENLACE QUÍMICO ETAPA BACHILLERATO Resumen En este trabajo he querido buscar imágenes de minerales, para poder utilizarlas
SUSTANCIAS NATURALES CON ENLACE QUÍMICO IÓNICO AUTOR JAVIER RUIZ HIDALGO TEMÁTICA ENLACE QUÍMICO ETAPA BACHILLERATO Resumen En este trabajo he querido buscar imágenes de minerales, para poder utilizarlas
ESTRUCTURES CARACTERÍSTIQUES
 ESTRUCTURES CARACTERÍSTIQUES En aquest capítol es descriuen algunes estructures molt simples que permeten analitzar la disposició dels àtoms de diversos compostos característics en el que l enllaç responsable
ESTRUCTURES CARACTERÍSTIQUES En aquest capítol es descriuen algunes estructures molt simples que permeten analitzar la disposició dels àtoms de diversos compostos característics en el que l enllaç responsable
QUÍMICA INORGÁNICA I 9/1/17. El enlace iónico. Iones. Rafael Moreno Esparza
 QUÍMICA INORGÁNICA I Rafael Moreno Esparza 0 El enlace iónico Procedencia: La fuerza electrostática que mantiene unidos a dos átomos. Los átomos tratan de tener 8 electrones en la capa de valencia Los
QUÍMICA INORGÁNICA I Rafael Moreno Esparza 0 El enlace iónico Procedencia: La fuerza electrostática que mantiene unidos a dos átomos. Los átomos tratan de tener 8 electrones en la capa de valencia Los
Naturaleza del enlace químico Enlace iónico Enlace covalente Enlaces intermoleculares Enlace metálico
 Naturaleza del enlace químico Enlace iónico Enlace covalente Enlaces intermoleculares Enlace metálico Naturaleza del enlace químico Los átomos tienden a adquirir la máxima estabilidad y esto se consigue
Naturaleza del enlace químico Enlace iónico Enlace covalente Enlaces intermoleculares Enlace metálico Naturaleza del enlace químico Los átomos tienden a adquirir la máxima estabilidad y esto se consigue
UNIDAD IV. 4.6 Índices de Miller. Direcciones y Planos compactos. e ** Para Sistema cubico y hexagonal.
 Fundamentos de Metalurgia y Materiales UNIDAD IV 4.6 Índices de Miller. Direcciones y Planos compactos. e ** Para Sistema cubico y hexagonal. 4.7 Huecos Intersticiales. Huecos Tetraédricos y Octaédricos.
Fundamentos de Metalurgia y Materiales UNIDAD IV 4.6 Índices de Miller. Direcciones y Planos compactos. e ** Para Sistema cubico y hexagonal. 4.7 Huecos Intersticiales. Huecos Tetraédricos y Octaédricos.
Estructura Cristalina de Sólidos
 Estructura Cristalina de Sólidos Relación entre estructura periódica y propiedades Bibliografía: 1. Solid State Physics. Ashcroft and Mermin. 2. Solid State Chemistry. West. 3. Química del Estado Sólido.
Estructura Cristalina de Sólidos Relación entre estructura periódica y propiedades Bibliografía: 1. Solid State Physics. Ashcroft and Mermin. 2. Solid State Chemistry. West. 3. Química del Estado Sólido.
Estructura Interna de los Materiales
 TEMA III Estructura Interna de los Materiales LECCIÓN 3 Estructura Cristalina y Amorfa 1 3.1 ESTADOS DE LA MATERIA Ciencia y Tecnología de los Materiales La materia puede presentarse en tres estados: gaseoso,
TEMA III Estructura Interna de los Materiales LECCIÓN 3 Estructura Cristalina y Amorfa 1 3.1 ESTADOS DE LA MATERIA Ciencia y Tecnología de los Materiales La materia puede presentarse en tres estados: gaseoso,
Ácidos y bases. Definiciones ácido-base
 Ácidos y bases Definiciones ácido-base Definición de Arrhenihus Sevate August Arrhenius 1858-1927 Ácido Aquella sustancia, que en solución acuosa, libera iones Hidrógeno (H 3 O + (ac)) Base HCl (ac) +
Ácidos y bases Definiciones ácido-base Definición de Arrhenihus Sevate August Arrhenius 1858-1927 Ácido Aquella sustancia, que en solución acuosa, libera iones Hidrógeno (H 3 O + (ac)) Base HCl (ac) +
ENLACE QUÍMICO II. 5.- De los compuestos iónicos KBr y NaBr, cuál será el más duro y cuál el de mayor temperatura de fusión?. Por qué?.
 ENLACE QUÍMICO II 1.- Representa las estructuras de Lewis indicando geometría molecular y momento dipolar de las siguientes moléculas: CO 2, H 2 S y O 2. 2.- De las siguientes moléculas: F 2, CS 2, C 2
ENLACE QUÍMICO II 1.- Representa las estructuras de Lewis indicando geometría molecular y momento dipolar de las siguientes moléculas: CO 2, H 2 S y O 2. 2.- De las siguientes moléculas: F 2, CS 2, C 2
Compuestos Químicos. Capítulo 3 Sec. 3.1-3.6 Rosamil Rey, PhD CHEM 2115
 Compuestos Químicos Capítulo 3 Sec. 3.1-3.6 Rosamil Rey, PhD CHEM 2115 Tipos de enlaces Enlaces covalentes comparten electrones entre átomos y forman compuestos moleculares. Estos compuestos son representados
Compuestos Químicos Capítulo 3 Sec. 3.1-3.6 Rosamil Rey, PhD CHEM 2115 Tipos de enlaces Enlaces covalentes comparten electrones entre átomos y forman compuestos moleculares. Estos compuestos son representados
5) Cuando un metal y un no metal reaccionan el tiende a perder electrones y el tiende a ganar electrones.
 Enlaces y compuestos iónicos. Opción Múltiple. Revisión PSI Química Nombre Electrones de valencia Aniones y Cationes 1) Los Metales tienden a electrones y no metales tienden a electrones. A) ganar, ganar
Enlaces y compuestos iónicos. Opción Múltiple. Revisión PSI Química Nombre Electrones de valencia Aniones y Cationes 1) Los Metales tienden a electrones y no metales tienden a electrones. A) ganar, ganar
MANUAL DE PRÁCTICAS DE MATERIALES CERÁMICOS PROGRAMA EDUCATIVO: INGENIERÍA EN MATERIALES ELABORADO POR: DR. OSCAR FERNANDO PACHECO SALAZAR
 1 de 14 DE MATERIALES CERÁMICOS PROGRAMA EDUCATIVO: INGENIERÍA EN MATERIALES ELABORADO POR: DR. OSCAR FERNANDO PACHECO SALAZAR Calkiní, Campeche, Febrero 2018 Revisó Aprobó Autorizó Presidente de Academia
1 de 14 DE MATERIALES CERÁMICOS PROGRAMA EDUCATIVO: INGENIERÍA EN MATERIALES ELABORADO POR: DR. OSCAR FERNANDO PACHECO SALAZAR Calkiní, Campeche, Febrero 2018 Revisó Aprobó Autorizó Presidente de Academia
Síntesis y Caracterización Estructural de los Materiales. Grado en Física.
 El hierro (Fe) sufre una tranformación polimórfica a 912 ºC, pasando de una estructura cubica centrada en el cuerpo (I o bcc) a una estructura cubica centrada en todas las caras (F o fcc). Sabiendo que
El hierro (Fe) sufre una tranformación polimórfica a 912 ºC, pasando de una estructura cubica centrada en el cuerpo (I o bcc) a una estructura cubica centrada en todas las caras (F o fcc). Sabiendo que
Sólidos Covalentes. Tema 4: Estado Sólido. QUIMICA GENERAL Química Inorgánica Sólidos Covalentes
 Sólidos Covalentes Esta obra está licenciada bajo una Licencia Creative Commons Reconocimiento-NoComercial-SinObraDerivada 3.0 España Attribution-NonCommercial-NoDerivs 3.0 Unported CC BY-NC-ND 3.0 http://creativecommons.org/licenses/by-nc-nd/3.0/es/
Sólidos Covalentes Esta obra está licenciada bajo una Licencia Creative Commons Reconocimiento-NoComercial-SinObraDerivada 3.0 España Attribution-NonCommercial-NoDerivs 3.0 Unported CC BY-NC-ND 3.0 http://creativecommons.org/licenses/by-nc-nd/3.0/es/
Materiales-G704/G742. Jesús Setién Marquínez Jose Antonio Casado del Prado Soraya Diego Cavia Carlos Thomas García
 Materiales-G704/G742 Lección 3. Estructura cristalina y amorfa Jesús Setién Marquínez Jose Antonio Casado del Prado Soraya Diego Cavia Carlos Thomas García Departamento de Ciencia e Ingeniería del Terreno
Materiales-G704/G742 Lección 3. Estructura cristalina y amorfa Jesús Setién Marquínez Jose Antonio Casado del Prado Soraya Diego Cavia Carlos Thomas García Departamento de Ciencia e Ingeniería del Terreno
TEMA 4 (Parte I) EL ENLACE QUÍMICO. IÓNICO
 TEMA 4 (Parte I) EL ENLACE QUÍMICO. IÓNICO Mª PILAR RUIZ OJEDA BORJA MUÑOZ LEOZ Contenidos: 1. Introducción 2. Representaciones de Lewis. Regla del Octeto 3. El enlace Iónico 3.1. Redes iónicas 3.2. Energía
TEMA 4 (Parte I) EL ENLACE QUÍMICO. IÓNICO Mª PILAR RUIZ OJEDA BORJA MUÑOZ LEOZ Contenidos: 1. Introducción 2. Representaciones de Lewis. Regla del Octeto 3. El enlace Iónico 3.1. Redes iónicas 3.2. Energía
ENLACE QUÍMICO(II). ENLACE IÓNICO
 ENLACE QUÍMICO(II). ENLACE IÓNICO 11Na [Ne] 1s 1 Na + [Ne] 17 Cl [Ne] 3s 3p 5 Cl - [Ne] 3s 3p 6 Na + Cl Na + Cl NaCl sólido blanco p.f = 801ºC Ejemplo 4Li(s) + O (g) Li O(s) P.f= 1700ºC 3Li 1s s 1 Li 1s
ENLACE QUÍMICO(II). ENLACE IÓNICO 11Na [Ne] 1s 1 Na + [Ne] 17 Cl [Ne] 3s 3p 5 Cl - [Ne] 3s 3p 6 Na + Cl Na + Cl NaCl sólido blanco p.f = 801ºC Ejemplo 4Li(s) + O (g) Li O(s) P.f= 1700ºC 3Li 1s s 1 Li 1s
ESCRITURA DE FÓRMULAS I: COMPUESTOS BINARIOS
 ESCRITURA DE FÓRMULAS I: COMPUESTOS BINARIOS PSI QUÍMICA NOMBRE I. Complete la tabla. Litio NO METALES Nitrógeno Oxígeno Cloro METALES Calcio II. Escriba las fórmulas para los siguientes compuestos: 1.
ESCRITURA DE FÓRMULAS I: COMPUESTOS BINARIOS PSI QUÍMICA NOMBRE I. Complete la tabla. Litio NO METALES Nitrógeno Oxígeno Cloro METALES Calcio II. Escriba las fórmulas para los siguientes compuestos: 1.
INTRODUCCION AL EQUILIBRIO PRECIPITACIÓN - SOLUBILIZACIÓN
 INTRODUCCION AL EQUILIBRIO PRECIPITACIÓN - SOLUBILIZACIÓN Lo básico que debes saber de Química General 14-1 LA SOLUBILIDAD DE ELECTROLITOS FUERTES POCO SOLUBLES Compuesto Solubilidad Electrolito NaCl BaSO
INTRODUCCION AL EQUILIBRIO PRECIPITACIÓN - SOLUBILIZACIÓN Lo básico que debes saber de Química General 14-1 LA SOLUBILIDAD DE ELECTROLITOS FUERTES POCO SOLUBLES Compuesto Solubilidad Electrolito NaCl BaSO
Sólidos Iónicos El enlace Iónico
 1 Sólidos Iónicos El enlace Iónico 2 * Huheey, J. E., Keiter, R. L., Keiter, E. A., Inorganic Chemistry: Principles of Structure and Reactivity, 4ª Ed., Harper Collins, 1993. Capítulo 4. * Douglas, B.;
1 Sólidos Iónicos El enlace Iónico 2 * Huheey, J. E., Keiter, R. L., Keiter, E. A., Inorganic Chemistry: Principles of Structure and Reactivity, 4ª Ed., Harper Collins, 1993. Capítulo 4. * Douglas, B.;
El enlace iónico. Estudio energético de su formación: Energía reticular.
 El enlace iónico. Estudio energético de su formación: Energía reticular. Tomamos una sustancia iónica típica; el NaCl y se parte de un mol de átomos de Cl y Na separados una distancia tan grande que la
El enlace iónico. Estudio energético de su formación: Energía reticular. Tomamos una sustancia iónica típica; el NaCl y se parte de un mol de átomos de Cl y Na separados una distancia tan grande que la
1. a) Cómo se forman los iones negativos? b) Qué elementos tienden a formarlos y porqué? c) Cuál será el ión del azufre?
 Tema 5. ELEMENTOS Y COMPUESTOS 1. a) Cómo se forman los iones negativos? b) Qué elementos tienden a formarlos y porqué? c) Cuál será el ión del azufre? a) Los iones negativos, llamados aniones, se forman
Tema 5. ELEMENTOS Y COMPUESTOS 1. a) Cómo se forman los iones negativos? b) Qué elementos tienden a formarlos y porqué? c) Cuál será el ión del azufre? a) Los iones negativos, llamados aniones, se forman
Los compuestos químicos
 Los compuestos químicos Física y Química Compuestos formados por moléculas Oxford University Press España, S. A. Física y Química 3º ESO 2 Un compuesto químico es una sustancia pura formada por dos o más
Los compuestos químicos Física y Química Compuestos formados por moléculas Oxford University Press España, S. A. Física y Química 3º ESO 2 Un compuesto químico es una sustancia pura formada por dos o más
Tema 2: Fuerzas intermoleculares
 Tema 2: Fuerzas intermoleculares Fuerzas intermoleculares: ion dipolo, dipolo dipolo, dispersión de London y puentes de hidrógeno. Gases ideales y reales. Propiedades de los ĺıquidos. Presión de vapor.
Tema 2: Fuerzas intermoleculares Fuerzas intermoleculares: ion dipolo, dipolo dipolo, dispersión de London y puentes de hidrógeno. Gases ideales y reales. Propiedades de los ĺıquidos. Presión de vapor.
Para la casa 12. Predice si los siguientes elementos producirán aniones, cationes o no producirán ninguno
 Enlaces y compuestos iónicos- Revisión- Problemas PSI Química Nombre Electrones de valencia 1. Cuántos electrones de valencia tiene el Oxígeno? 2. Cuántos electrones de valencia tiene el Litio? 3. Cuántos
Enlaces y compuestos iónicos- Revisión- Problemas PSI Química Nombre Electrones de valencia 1. Cuántos electrones de valencia tiene el Oxígeno? 2. Cuántos electrones de valencia tiene el Litio? 3. Cuántos
FÍSICA Y QUÍMICA 4º DE ESO CURSO 16/ 17
 FÍSICA Y QUÍMICA 4º DE ESO CURSO 16/ 17 Alumno/a: 1. Completa la tabla, utilizando el SP: NOMBRE SÍMBOLO Z A P + e - N CARGA *catión *anión *carga 0 24 28 3+ 65 28 35 Cobre 63 29 0 33 75 36 18 16 2-29
FÍSICA Y QUÍMICA 4º DE ESO CURSO 16/ 17 Alumno/a: 1. Completa la tabla, utilizando el SP: NOMBRE SÍMBOLO Z A P + e - N CARGA *catión *anión *carga 0 24 28 3+ 65 28 35 Cobre 63 29 0 33 75 36 18 16 2-29
FÍSICA Y QUÍMICA cuaderno de ejercicios
 FÍSICA Y QUÍMICA cuaderno de ejercicios FORMULACIÓN y nomenclatura 1.** Determinen si las siguientes afirmaciones se refieren a metales o a no metales. 1.1. Presentan un brillo característico. 1.2. Los
FÍSICA Y QUÍMICA cuaderno de ejercicios FORMULACIÓN y nomenclatura 1.** Determinen si las siguientes afirmaciones se refieren a metales o a no metales. 1.1. Presentan un brillo característico. 1.2. Los
UD 2 ENLACE QUÍMICO Y FUERZAS INTERMOLECULARES FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS TERNARIOS
 FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS TERNARIOS Ácidos oxoácidos o ternarios Se formulan añadiendo una molécula de agua a los óxidos no metálicos. Óxidos no metálicos Cl 2 O SO Cl 2 O 3 SO 2 N 2 O 3
FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS TERNARIOS Ácidos oxoácidos o ternarios Se formulan añadiendo una molécula de agua a los óxidos no metálicos. Óxidos no metálicos Cl 2 O SO Cl 2 O 3 SO 2 N 2 O 3
Tema 9. Tema 9: Estados de agregación de la materia. 9.1 Características generales de los estados de agregación LARGO ALCANCE ORDEN ALCANCE
 Tema 9: Estados de agregación de la materia 9.1 Características generales de los estados de agregación Desde el punto de vista microscópico: 9.1 Características generales 9.2 Sólidos: estructura cristalina
Tema 9: Estados de agregación de la materia 9.1 Características generales de los estados de agregación Desde el punto de vista microscópico: 9.1 Características generales 9.2 Sólidos: estructura cristalina
Unidad 1: Estructura atómica de la materia
 ACTIVIDADES Unidad 1: Estructura atómica de la materia Para a realización de ditas actividades recoméndase seguir a seguinte páxina de internet do Ministerio de Educación e ciencia na cal se explica de
ACTIVIDADES Unidad 1: Estructura atómica de la materia Para a realización de ditas actividades recoméndase seguir a seguinte páxina de internet do Ministerio de Educación e ciencia na cal se explica de
Capítulo 2 La estructura de los sólidos cristalinos
 Capítulo 2 La estructura de los sólidos cristalinos TEMA 2: La estructura de los sólidos cristalinos 1. Los enlaces interatómicos 2. La estructura cristalina 3. Estructuras de empaquetamiento compacto
Capítulo 2 La estructura de los sólidos cristalinos TEMA 2: La estructura de los sólidos cristalinos 1. Los enlaces interatómicos 2. La estructura cristalina 3. Estructuras de empaquetamiento compacto
Complementos de Geología
 Master de Profesor de Educación Secundaria Obligatoria y Bachillerato, Formación Profesional y Enseñanzas de Idioma (Módulo Específico de Biología y Geología) Complementos de Geología Ángel Carmelo Prieto
Master de Profesor de Educación Secundaria Obligatoria y Bachillerato, Formación Profesional y Enseñanzas de Idioma (Módulo Específico de Biología y Geología) Complementos de Geología Ángel Carmelo Prieto
IES La Magdalena. Avilés. Asturias. Enlace Iónico
 IES La Magdalena. Avilés. Asturias Si enfrentamos un átomo al que le falten pocos electrones en su capa de valencia para adquirir la configuración de gas noble (muy electronegativo, tendencia a coger electrones),
IES La Magdalena. Avilés. Asturias Si enfrentamos un átomo al que le falten pocos electrones en su capa de valencia para adquirir la configuración de gas noble (muy electronegativo, tendencia a coger electrones),
EJERCICIOS Y PROBLEMAS DE REPASO PARA EL ALUMNADO QUE PROMOCIONA A PRIMERO DE BACHILLER Y QUIERE ESTUDIAR FÍSICA Y QUÍMICA
 EJERCICIOS Y PROBLEMAS DE REPASO PARA EL ALUMNADO QUE PROMOCIONA A PRIMERO DE BACHILLER Y QUIERE ESTUDIAR FÍSICA Y QUÍMICA 1.- El gas propano reacciona con el oxígeno según la siguiente reacción: C 3 H
EJERCICIOS Y PROBLEMAS DE REPASO PARA EL ALUMNADO QUE PROMOCIONA A PRIMERO DE BACHILLER Y QUIERE ESTUDIAR FÍSICA Y QUÍMICA 1.- El gas propano reacciona con el oxígeno según la siguiente reacción: C 3 H
Tipos de reacciones químicas
 Óxido Reducción Tipos de reacciones químicas Hay un intercambio de electrones entre dos compuestos: gana electrones CuSO 4 + Zn ZnSO 4 + Cu pierde electrones Óxido Reducción o Redox Un átomo de alguna
Óxido Reducción Tipos de reacciones químicas Hay un intercambio de electrones entre dos compuestos: gana electrones CuSO 4 + Zn ZnSO 4 + Cu pierde electrones Óxido Reducción o Redox Un átomo de alguna
Para qué se unen los átomos? Es la fuerza que mantiene unidos dos átomos cualesquiera.
 Es la fuerza que mantiene unidos dos átomos cualesquiera. Enlace iónico : Es la fuerza que mantiene unidos átomos de electronegatividades muy diferentes. Enlace cova1ente: Es la fuerza que mantiene unidos
Es la fuerza que mantiene unidos dos átomos cualesquiera. Enlace iónico : Es la fuerza que mantiene unidos átomos de electronegatividades muy diferentes. Enlace cova1ente: Es la fuerza que mantiene unidos
CRISTALOQUÍMICA TEMA 6 ESTRUCTURAS CRISTALINAS. Empaquetados compactos. Coordinación
 CRISTALOQUÍMICA TEMA 6 ESTRUCTURAS CRISTALINAS Empaquetados compactos. Coordinación ÍNDICE 6.1 Introducción 6.2 Estructuras cristalinas 6.3 Enlace en las estructuras cristalinas 6.4 Cristales iónicos 6.5
CRISTALOQUÍMICA TEMA 6 ESTRUCTURAS CRISTALINAS Empaquetados compactos. Coordinación ÍNDICE 6.1 Introducción 6.2 Estructuras cristalinas 6.3 Enlace en las estructuras cristalinas 6.4 Cristales iónicos 6.5
HCl. NaCl + CO. AgCl + NaNO. Al SO + H H SO. CaO + CO. Na2CO. ZnSO. Hg + CuCl. MgO ZnCl. REACCIONES QUíMICAS
 Dadas las siguientes reacciones químicas, contesta: Qué sustancias son reactivos? Cuáles son productos?. Ajústalas a) H + Cl HCl b) CH5OH + O c) HCl + NaHCO NaCl + CO d) NaCl + AgNO AgCl + NaNO e) CO +
Dadas las siguientes reacciones químicas, contesta: Qué sustancias son reactivos? Cuáles son productos?. Ajústalas a) H + Cl HCl b) CH5OH + O c) HCl + NaHCO NaCl + CO d) NaCl + AgNO AgCl + NaNO e) CO +
Oposiciones Secundaria Física y Química Antonio Abrisqueta García, 1999 Temario Específico Tema 44
 TEMAS DE FÍSICA Y QUÍMICA (Oposiciones de Enseñanza Secundaria) ------------------------------------------------------------------------------- TEMA 44 SUSTANCIAS IÓNICAS. ASPECTOS ENERGÉTICOS EN LA FORMACIÓN
TEMAS DE FÍSICA Y QUÍMICA (Oposiciones de Enseñanza Secundaria) ------------------------------------------------------------------------------- TEMA 44 SUSTANCIAS IÓNICAS. ASPECTOS ENERGÉTICOS EN LA FORMACIÓN
LABORATORIO DE ESTADO SÓLIDO Y SEMICONDUCTORES 1.1. PRÁCTICA N o 1 REDES DE BRAVAIS Y ESTRUCTURAS CRISTALINAS
 LABORATORIO DE ESTADO SÓLIDO Y SEMICONDUCTORES 1.1 PRÁCTICA N o 1 REDES DE BRAVAIS Y ESTRUCTURAS CRISTALINAS 1. INTRODUCCIÓN 1.1 Red de Bravais y celda primitiva unidad Uno de los conceptos fundamentales
LABORATORIO DE ESTADO SÓLIDO Y SEMICONDUCTORES 1.1 PRÁCTICA N o 1 REDES DE BRAVAIS Y ESTRUCTURAS CRISTALINAS 1. INTRODUCCIÓN 1.1 Red de Bravais y celda primitiva unidad Uno de los conceptos fundamentales
Tipos de reacciones químicas
 Tipos de reacciones químicas Dra. Patricia Satti, UNRN REACCIONES QUÍMICAS Óxido Reducción Hay un intercambio de electrones entre dos compuestos: gana electrones CuSO 4 + Zn ZnSO 4 + Cu pierde electrones
Tipos de reacciones químicas Dra. Patricia Satti, UNRN REACCIONES QUÍMICAS Óxido Reducción Hay un intercambio de electrones entre dos compuestos: gana electrones CuSO 4 + Zn ZnSO 4 + Cu pierde electrones
INTRODUCCIÓN AL ESTADO CRISTALINO
 INTRODUCCIÓN AL ESTADO CRISTALINO Se describen como materiales cristalinos aquellos materiales sólidos cuyos elementos constitutivos se repiten de manera ordenada y paralela y cuya distribución en el espacio
INTRODUCCIÓN AL ESTADO CRISTALINO Se describen como materiales cristalinos aquellos materiales sólidos cuyos elementos constitutivos se repiten de manera ordenada y paralela y cuya distribución en el espacio
Las fases condensadas
 1 Las fases condensadas 2 * Huheey, J. E., Keiter, R. L., Keiter, E. A., Inorganic Chemistry: Principles of Structure and Reactivity, 4ª Ed., Harper Collins, 1993. Capítulo 4 y 7. * Casabó i Gispert, J,
1 Las fases condensadas 2 * Huheey, J. E., Keiter, R. L., Keiter, E. A., Inorganic Chemistry: Principles of Structure and Reactivity, 4ª Ed., Harper Collins, 1993. Capítulo 4 y 7. * Casabó i Gispert, J,
EL ESTADO SÓLIDO CLASE I
 EL ESTADO SÓLIDO CLASE I CARACTERISTICAS DEL ESTADO SOLIDO Los átomos, iones o moléculas que componen un compuesto sólido están unidas entre sí por fuerzas intensas de cohesión, formando un todo compacto
EL ESTADO SÓLIDO CLASE I CARACTERISTICAS DEL ESTADO SOLIDO Los átomos, iones o moléculas que componen un compuesto sólido están unidas entre sí por fuerzas intensas de cohesión, formando un todo compacto
5ª UNIDAD ELEMENTOS Y COMPUESTOS
 5ª UNIDAD ELEMENTOS Y COMPUESTOS 3º E.S.O. Grupo Apellidos: Nombre: INTRODUCCIÓN Comenzamos recordando los conceptos más importantes del tema anterior: Cómo son los átomos? Cómo están distribuidos los
5ª UNIDAD ELEMENTOS Y COMPUESTOS 3º E.S.O. Grupo Apellidos: Nombre: INTRODUCCIÓN Comenzamos recordando los conceptos más importantes del tema anterior: Cómo son los átomos? Cómo están distribuidos los
Física y Química: guía interactiva para la resolución de ejercicios LA ESTRUCTURA DE LA MATERIA Y LA REACCIÓN QUÍMICA
 Física y Química: guía interactiva para la resolución de ejercicios LA ESTRUCTURA DE LA MATERIA Y LA REACCIÓN QUÍMICA I.E.S. Élaios Departamento de Física y Química EJERCICIO 1 El dióxido de carbono es
Física y Química: guía interactiva para la resolución de ejercicios LA ESTRUCTURA DE LA MATERIA Y LA REACCIÓN QUÍMICA I.E.S. Élaios Departamento de Física y Química EJERCICIO 1 El dióxido de carbono es
QUÍMICA INORGÁNICA AVANZADA SÓLIDOS
 QUÍMICA INORGÁNICA AVANZADA SÓLIDOS Prácticamente todos los elementos y compuestos inorgánicos son sólidos a temperatura ambiente. Su característica principal, comparado con otras fases del mismo material,
QUÍMICA INORGÁNICA AVANZADA SÓLIDOS Prácticamente todos los elementos y compuestos inorgánicos son sólidos a temperatura ambiente. Su característica principal, comparado con otras fases del mismo material,
Enlace químico. José Mariano Lucena Cruz 19 de mayo de 2010
 José Mariano Lucena Cruz chenalc@gmail.com 19 de mayo de 2010 El enlace químico La unión entre átomos, moléculas o iones constituye el llamado enlace químico. Su fundamento siempre es de tipo eléctrico.
José Mariano Lucena Cruz chenalc@gmail.com 19 de mayo de 2010 El enlace químico La unión entre átomos, moléculas o iones constituye el llamado enlace químico. Su fundamento siempre es de tipo eléctrico.
Estado Sólido. Tema ESTADO SÓLIDO. Teoría, Dra. Sandra Signorella. Profesora Titular Área Química General e Inorgánica. Año 2018
 Teoría, Dra. Sandra Signorella Profesora Titular Área Química General e Inorgánica Tema ESTDO SÓLIDO ño 2018 Estado Sólido Características generales Sólidos cristalinos y amorfos Tipos de sólidos Propiedades
Teoría, Dra. Sandra Signorella Profesora Titular Área Química General e Inorgánica Tema ESTDO SÓLIDO ño 2018 Estado Sólido Características generales Sólidos cristalinos y amorfos Tipos de sólidos Propiedades
COMPUESTOS DE COORDINACION (EO) (LA CA ) a (LN) n ] (EO+CA) [M m. d n ESTADO DE OXIDACION. a + n NUMERO DE COORDINACION GEOMETRIA HUGO TORRENS
![COMPUESTOS DE COORDINACION (EO) (LA CA ) a (LN) n ] (EO+CA) [M m. d n ESTADO DE OXIDACION. a + n NUMERO DE COORDINACION GEOMETRIA HUGO TORRENS COMPUESTOS DE COORDINACION (EO) (LA CA ) a (LN) n ] (EO+CA) [M m. d n ESTADO DE OXIDACION. a + n NUMERO DE COORDINACION GEOMETRIA HUGO TORRENS](/thumbs/84/89196657.jpg) MAGNETISMO COMPUESTOS DE COORDINACION [M m (EO) (LA CA ) a (LN) n ] (EO+CA) ESTADO DE OXIDACION d n a + n NUMERO DE COORDINACION GEOMETRIA HUGO TORRENS d 0 d 1 d 2 d 3 d 4 d 5 d 6 d 7 d 8 d 9 E HUGO TORRENS
MAGNETISMO COMPUESTOS DE COORDINACION [M m (EO) (LA CA ) a (LN) n ] (EO+CA) ESTADO DE OXIDACION d n a + n NUMERO DE COORDINACION GEOMETRIA HUGO TORRENS d 0 d 1 d 2 d 3 d 4 d 5 d 6 d 7 d 8 d 9 E HUGO TORRENS
9. LA ENERGÍA RETICULAR
 La energía reticular U (o energía de red) es la energía necesaria para separar totalmente los iones que forman una red cristalina hasta una distancia infinita donde ya no interactúan eléctricamente. También
La energía reticular U (o energía de red) es la energía necesaria para separar totalmente los iones que forman una red cristalina hasta una distancia infinita donde ya no interactúan eléctricamente. También
