Los sólidos iónicos. Estructuras características de los sólidos iónicos
|
|
|
- Héctor Villanueva Botella
- hace 7 años
- Vistas:
Transcripción
1 Los sólidos iónicos Los compuestos iónicos suelen presentar una serie de características físicas que los distinguen de los covalentes. Así, los sólidos iónicos como el cloruro sódico y el nitrato de potasio tienen puntos de fusión moderadamente altos y son solubles en disolventes polares, en particular en agua. Sin embargo existen excepciones como el CaF 2 el cual presenta un elevado punto de fusión pero es insoluble en agua. Los compuestos iónicos también presentan una baja conductividad eléctrica en el estado sólido pero se hacen buenos conductores de la electricidad cuando se funden o cuando se disuelven en disolventes polares como el agua. Los sólidos iónicos presentan estructuras con bajos números de coordinación, a diferencia de los sólidos metálicos, lo que explica su menor densidad. De hecho, la distinción entre un sólido iónico y uno covalente puede establecerse en función del número de coordinación, al que puede llegarse de forma experimental mediante técnicas de difracción de rayos X. Sin embargo, algunos sólidos covalentes como el diamante presentan también bajos números de coordinación, por lo que es necesario un criterio más específico para establecer un sólido como iónico. La clasificación de un sólido como iónico se basa en la comparación de sus propiedades con las que predice el modelo iónico. Este es un modelo límite del enlace entre átomos y se basa en considerar al sólido formado por una red de esferas cargadas con signos opuestos y que interaccionan entre sí mediante fuerzas de tipo coulombianas. Si los parámetros termodinámicos calculados para el sólido empleando el modelo iónico coinciden con los determinados experimentalmente, entonces el sólido presenta naturaleza iónica. No obstante, hay que indicar que en algunos casos particulares esta coincidencia numérica no implica siempre la existencia de un enlace iónico. Estructuras características de los sólidos iónicos Las estructuras que se describen en este apartado son los modelos que describen a un gran número de sólidos iónicos. Por ejemplo, la estructura de la sal de roca, que toma su nombre de la forma mineral del NaCl, es característica de muchos otros sólidos iónicos. Muchas de las estructuras pueden considerarse constituidas por redes formadas por iones positivos y negativos en las que se maximizan las fuerzas atractivas entre iones de signos opuestos y se minimizan las fuerzas repulsivas entre iones de la misma carga.
2 Tabla 3. Estructuras cristalinas modelo de compuestos ionicos Estructura cristalina Antifluorita Cloruro de cesio Ejemplo K 2O, K 2S,Li 2O, Na 2O, Na 2Se, Na 2S CsCl, CaS, TlSb, CsCN, CuZn Fluorita CaF 2, UO 2, BaCl 2, HgF 2, PbO 2 Arseniuro de níquel NiAs, NiS, FeS, PtSn, CoS Perovskita CaTiO 3, BaTiO 3, SrTiO 3 Sal de roca NaCl, LiCl, KBr, RbI, AgCl, AgBr, MgO, CaO, TiO, FeO, NiO, SnAs, UC, ScN Rutilo TiO 2, MnO 2, SnO 2, WO 2, MgF 2, NiF 2 Blenda Wurtzita ZnS, CuCl, CdS, HgS, GaP, InAs ZnS, ZnO, BeO, MnS, AgI, AlN, SiC, NH 4F La estructura del cloruro sódico Esta estructura está basada en un empaquetamiento cúbico compacto (centrado en las caras) de los aniones y en el que los cationes ocupan todos los huecos octaédricos. La interpretación opuesta es igualmente válida: estructura de empaquetamiento compacto de cationes con los aniones ocupando los huecos octaédricos. En cada celda unidad los iones de un tipo ocupan los vértices y los centros de las caras del cubo mientras que los de signo contrario se sitúan en los centros de las aristas y en el centro del cubo (Figura 6). Cada ion de un signo está rodeado de 6 iones de signo contrario, por lo que el número de coordinación del catión y del anión en este tipo de estructura de 6. Se dice que la estructura presenta coordinación (6,6), donde el primer dígito representa el número de coordinación del catión y el segundo el del anión. Los seis iones de signo contrario que rodean a un ion central se disponen en forma octaédrica. Este tipo de estructura es adoptada por la mayoría de los haluros alcalinos como los de Li, Na, K, Rb y el CsF. También es adoptada por los óxidos de Mg, Ca, Sr, Ba y Cd.
3 Figura 6. Estructura del NaCl La estructura del cloruro de cesio Esta estructura es menos común que la del cloruro de sodio y la presentan los compuestos como el CsCl, CsBr y CsI, así como otros compuestos formados por iones de radios similares a estos como los haluros de amonio (excepto el NH 4 Br). La estructura del cloruro de cesio presenta una celda unidad cúbica en la que cada vértice está ocupado por el anión y el centro del cubo se ocupa por el catión, o viceversa (Figura 7) (o viceversa), lo que conduce a una coordinación (8,8). Figura 7. Estructura del CsCl Las estructuras de la blenda y de la wurtzita (ZnS) El sulfuro de cinc cristaliza en dos formas polimórficas, la wurtzita y la blenda. La primera se basa en un empaquetamiento hexagonal de los aniones en el que los cationes ocupan la mitad de los huecos tetraédricos. La estructura de la blenda está basada en un empaquetamiento de los aniones de tipo cúbico centrado en las caras en el que los cationes ocupan la mitad de los huecos tetraédricos. En ambos tipos de estructuras se da la coordinación (4,4). Las dos estructuras se presentan en los óxidos y sulfuros de los metales divalentes como el Be, Zn, Mn, Cd, Hg.
4 Figura 8. Estructura de la blenda Estructura de la wurtzita La estructura de la fluorita (CaF 2 ) Esta estructura toma su nombre del mineral fluorita, CaF 2. Consiste en un empaquetamiento cúbico centrado en las caras de los cationes Ca 2+ en el que los aniones F - ocupan todos los huecos tetraédricos. La estructura de tipo antifluorita presenta una disposición de cationes y aniones inversa a la de la fluorita. En la estructura de tipo fluorita, los aniones están rodeados de 4 cationes vecinos dispuestos en un entorno tetraédrico. Los cationes están rodeados de 8 aniones que se disponen en un entorno cúbico. Por lo tanto, los números de coordinación para el catión y el anión son diferentes, 8:4 respectivamente, consistente con la estequiometría del compuesto (hay doble número de aniones que de cationes). Este tipo de estructura la presentan los fluoruros de Ca, Sr, Ba, Cd, Hg(II), Pb(II).
5 Figura 9. Estructura del CaF 2. La estructura del rutilo (TiO 2 ) Toma su nombre del mineral rutilo, un mineral de óxido de Ti(IV). Se basa en un empaquetamiento hexagonal compacto de los aniones en el que los cationes ocupan la mitad de los huecos octaédricos. Cada átomo de Ti está rodeado de seis átomos de oxígeno (disposición octaédrica) y cada átomo de oxígeno se rodea de tres átomos de titanio (disposición trigonal), de forma que la estructura de tipo rutilo presenta coordinación de 6:3. Esta estructura es la adoptada, entre otros, por el óxido de Sn(IV) o casiderita, el MnO 2 y el WO 2 y por los fluoruros del tipo MgF 2 y NiF 2. Figura 10. Estructura del TiO2 (rutilo) La estructura de tipo perovskita El mineral perovskita CaTiO 3 posee una estructura que es el prototipo de muchos sólidos de composición ABX 3, particularmente óxidos. En su forma idealizada, la estructura de perovskita es cúbica, con los átomos A ocupando el centro del cubo y rodeado de 12 átomos de tipo X y los átomos B ocupando los vértices del cubo y rodeado por 6 átomos de tipo X. La suma de las cargas de los iones positivos A y B debe ser de 6 (A 2+ B 4+, A 3+ B 3+,...). La estructura de tipo perovskita está relacionada con la de materiales que presentan
6 propiedades eléctricas muy interesantes como los sólidos piezoeléctricos, ferroeléctricos y los superconductores de alta temperatura. Figura 11. Estructura de la perovskita.
ESTRUCTURAS CARACTERÍSTICAS
 ESTRUCTURAS CARACTERÍSTICAS En este capítulo se describen algunas estructuras muy simples que permitirán analizar la disposición de los átomos de diversos compuestos característicos en los que el enlace
ESTRUCTURAS CARACTERÍSTICAS En este capítulo se describen algunas estructuras muy simples que permitirán analizar la disposición de los átomos de diversos compuestos característicos en los que el enlace
Tipos de estructuras. Introducción a la Ciencia de Materiales. M. Bizarro F. M. Sánchez
 Tipos de estructuras Empaquetamiento compacto Son estructuras formadas por átomos de igual tamaño que se unen mediante enlace metálico (esferas duras) A B A : A B C : FCC vs HCP El factor de empaquetamiento
Tipos de estructuras Empaquetamiento compacto Son estructuras formadas por átomos de igual tamaño que se unen mediante enlace metálico (esferas duras) A B A : A B C : FCC vs HCP El factor de empaquetamiento
Estructura de sólidos
 Estructura de sólidos Química Inorgánica - 2006 Tipos de estructuras cristalinas cristal enlace características molecular covalente-baja energía cristales blandos, bajo p.f. red covalente covalente cristales
Estructura de sólidos Química Inorgánica - 2006 Tipos de estructuras cristalinas cristal enlace características molecular covalente-baja energía cristales blandos, bajo p.f. red covalente covalente cristales
QUIMICA DE MATERIALES 1.2. NATURALEZA DE LA UNION QUIMICA
 QUIMICA DE MATERIALES 1.2. NATURALEZA DE LA UNION QUIMICA ENLACE COVALENTE Los electrones están compartidos por los átomos IONICO Uno o más electrones son transferidos entre los átomos, formando iones
QUIMICA DE MATERIALES 1.2. NATURALEZA DE LA UNION QUIMICA ENLACE COVALENTE Los electrones están compartidos por los átomos IONICO Uno o más electrones son transferidos entre los átomos, formando iones
Consideraciones sobre estructuras representativas
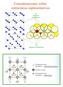 Consideraciones sobre estructuras representativas CONSIDERACIONES SOBRE ESTRUCTURAS REPRESENTATIVAS: En el empacamiento compacto hcp y ccp el número de coordinación es 12 Los elementos metálicos son los
Consideraciones sobre estructuras representativas CONSIDERACIONES SOBRE ESTRUCTURAS REPRESENTATIVAS: En el empacamiento compacto hcp y ccp el número de coordinación es 12 Los elementos metálicos son los
Sólidos Iónicos El enlace Iónico (1)
 1 Sólidos Iónicos El enlace Iónico (1) 2 * Huheey, J. E., Keiter, R. L., Keiter, E. A., Inorganic Chemistry: Principles of Structure and Reactivity, 4ª Ed., Harper Collins, 1993. Capítulo 4. * Douglas,
1 Sólidos Iónicos El enlace Iónico (1) 2 * Huheey, J. E., Keiter, R. L., Keiter, E. A., Inorganic Chemistry: Principles of Structure and Reactivity, 4ª Ed., Harper Collins, 1993. Capítulo 4. * Douglas,
ESTRUCTURA DE SÓLIDOS
 Estructura de sólidos 1 ESTRUCTURA DE SÓLIDOS La mayoría de los compuestos inorgánicos se presentan como sólidos en un arreglo ordenado de átomos, iones o moléculas. Los sólidos pueden ser: cristalinos:
Estructura de sólidos 1 ESTRUCTURA DE SÓLIDOS La mayoría de los compuestos inorgánicos se presentan como sólidos en un arreglo ordenado de átomos, iones o moléculas. Los sólidos pueden ser: cristalinos:
Estructuras Cristalinas
 Estructuras Cristalinas Bibliografía: Solid State Chemistry: An introduction, L. Smart and E. Moore. 1992 Solid State Chemistry and its applications, A.R. West. 1984 1 Enlace en Cerámicos Iónico Mezcla
Estructuras Cristalinas Bibliografía: Solid State Chemistry: An introduction, L. Smart and E. Moore. 1992 Solid State Chemistry and its applications, A.R. West. 1984 1 Enlace en Cerámicos Iónico Mezcla
Esquema del tema. Tema 4: Enlace iónico. Un poco de empirismo
 Esquema del tema Modelo iónico Características de los compuestos iónicos Corrigiendo el modelo iónico: Polarización y Módulo 12555- Química Inorgánica Título: Ingeniería Química Responsable: Juan José
Esquema del tema Modelo iónico Características de los compuestos iónicos Corrigiendo el modelo iónico: Polarización y Módulo 12555- Química Inorgánica Título: Ingeniería Química Responsable: Juan José
ENLACE IÓNICO. Dra. Silvia Elena Castillo Blum
 ENLACE IÓNICO Dra. Silvia Elena Castillo Blum Enlace Químico ENLACE IÓNICO ENLACE COVALENTE ENLACE METÁLICO 2 Definición IUPAC Hay un enlace químico entre dos átomos o grupos de átomos cuando las fuerzas
ENLACE IÓNICO Dra. Silvia Elena Castillo Blum Enlace Químico ENLACE IÓNICO ENLACE COVALENTE ENLACE METÁLICO 2 Definición IUPAC Hay un enlace químico entre dos átomos o grupos de átomos cuando las fuerzas
Tema 4. Cristaloquímica. Descripción estructural y
 Tema 4. Cristaloquímica. Descripción estructural y estructuras tipos Qué objetivos tiene la Cristaloquímica? Las fases cristalinas son componentes esenciales de los materiales, y especificamente de los
Tema 4. Cristaloquímica. Descripción estructural y estructuras tipos Qué objetivos tiene la Cristaloquímica? Las fases cristalinas son componentes esenciales de los materiales, y especificamente de los
TEMA 8: SÓLIDOS INORGÁNICOS. 2.- Redes bidimensionales y tridimensionales
 TEMA 8: SÓLIDOS INORGÁNICOS 1.- Tipos de sólidos 2.- Redes bidimensionales y tridimensionales 3.- Celda unidad y sus parámetros: - nº de átomos / celda - nº de coordinación (NC) - fracción de volumen ocupado
TEMA 8: SÓLIDOS INORGÁNICOS 1.- Tipos de sólidos 2.- Redes bidimensionales y tridimensionales 3.- Celda unidad y sus parámetros: - nº de átomos / celda - nº de coordinación (NC) - fracción de volumen ocupado
Para qué se unen los átomos? Es la fuerza que mantiene unidos dos átomos cualesquiera.
 Es la fuerza que mantiene unidos dos átomos cualesquiera. Enlace iónico : Es la fuerza que mantiene unidos átomos de electronegatividades muy diferentes. Enlace cova1ente: Es la fuerza que mantiene unidos
Es la fuerza que mantiene unidos dos átomos cualesquiera. Enlace iónico : Es la fuerza que mantiene unidos átomos de electronegatividades muy diferentes. Enlace cova1ente: Es la fuerza que mantiene unidos
Ing. Fredy Velázquez Soto
 Ing. Fredy Velázquez Soto TIPOS DE SÓLIDOS Sólidos cristalinos Los átomos, iones o moléculas se empaquetan en un arreglo ordenado Sólidos covalentes ( diamante, cristales de cuarzo), sólidos metálicos,
Ing. Fredy Velázquez Soto TIPOS DE SÓLIDOS Sólidos cristalinos Los átomos, iones o moléculas se empaquetan en un arreglo ordenado Sólidos covalentes ( diamante, cristales de cuarzo), sólidos metálicos,
Sólidos Arreglos y celdas unitarias. Ramón L. Hernández Castillo Enero 2012
 Sólidos Arreglos y celdas unitarias Ramón L. Hernández Castillo Enero 2012 Importancia de estudiar los sólidos cristalinos La mayoría de los compuestos inorgánicos son sólidos Casi todos los elementos
Sólidos Arreglos y celdas unitarias Ramón L. Hernández Castillo Enero 2012 Importancia de estudiar los sólidos cristalinos La mayoría de los compuestos inorgánicos son sólidos Casi todos los elementos
ENLACE QUÍMICO. 2º Bachillerato
 ENLACE QUÍMICO 2º Bachillerato Índice 1. Enlace químico 2. Enlace iónico 3. Enlace covalente 4. Fuerzas intermoleculares 5. Enlace metálico 2 1. Enlace químico 1.1. Concepto de enlace químico. 1.2. Caracterización
ENLACE QUÍMICO 2º Bachillerato Índice 1. Enlace químico 2. Enlace iónico 3. Enlace covalente 4. Fuerzas intermoleculares 5. Enlace metálico 2 1. Enlace químico 1.1. Concepto de enlace químico. 1.2. Caracterización
Tema 8. Sólidos iónicos
 Tema 8. Sólidos iónicos Definiciones Estructuras iónicas Derivadas de CCP Derivadas de HCP Derivadas de empaquetamientos no compactos Racionalización de las estructuras iónicas Principios de Laves Reglas
Tema 8. Sólidos iónicos Definiciones Estructuras iónicas Derivadas de CCP Derivadas de HCP Derivadas de empaquetamientos no compactos Racionalización de las estructuras iónicas Principios de Laves Reglas
Ejercicios tabla periódica. Enlace 4º ESO
 1. a) Indica la configuración electrónica de los átomos de los elementos A, B y C cuyos números atómicos son respectivamente: 12, 17 y 19. b) Escribe la configuración electrónica del ion más estable de
1. a) Indica la configuración electrónica de los átomos de los elementos A, B y C cuyos números atómicos son respectivamente: 12, 17 y 19. b) Escribe la configuración electrónica del ion más estable de
Cl Electrones de valencia: Cl: 7 3 = 21 P: 5 Total 26 Tres enlaces sencillos: - 6 Electrones restantes: 20
 ESTRUCTURAS DE LEWIS PARA EL ENLACE COVALENTE.- Lewis sugirió que los átomos comparten electrones para alcanzar la configuración de gas noble y tener así una estructura más estable. Salvo en el caso de
ESTRUCTURAS DE LEWIS PARA EL ENLACE COVALENTE.- Lewis sugirió que los átomos comparten electrones para alcanzar la configuración de gas noble y tener así una estructura más estable. Salvo en el caso de
CÚBICA SIMPLE HEXAGONAL ROMBOÉDRICA
 Formas de las celdas CÚBICA SIMPLE HEXAGONAL ROMBOÉDRICA TRICLÍNICA 1 1 2 3 4 C 2 3 4 5 6 5 6 7 B 8 3 1 5 2 8 A 8 6 4 Capa a Capa b Capa a Los cationes (más pequeños) ocupan los huecos formados por el
Formas de las celdas CÚBICA SIMPLE HEXAGONAL ROMBOÉDRICA TRICLÍNICA 1 1 2 3 4 C 2 3 4 5 6 5 6 7 B 8 3 1 5 2 8 A 8 6 4 Capa a Capa b Capa a Los cationes (más pequeños) ocupan los huecos formados por el
Ilustración 15.1. El número de coordinación en el NaCl es 6:6. Cada ion esta rodeado por seis iones que tienen carga opuesta a él.
 ENLACE IÓNICO Tú sabes que existen sustancias que forman sólidos cristalinos con altos puntos de fusión, que no conducen la corriente en estado sóliso pero se vuelven buenos conductores al fundirlos o
ENLACE IÓNICO Tú sabes que existen sustancias que forman sólidos cristalinos con altos puntos de fusión, que no conducen la corriente en estado sóliso pero se vuelven buenos conductores al fundirlos o
Enlace iónico. elemento poco. elemento muy + electronegativo. compuesto iónico (sal) electronegativo
 Enlace iónico Enlace iónico Necesitamos un nuevo modelo para explicar ciertas peculiaridades (Li2O). Este nuevo modelo es el enlace iónico Se forma por transferencia de electrones (no hay reparto equitativo,
Enlace iónico Enlace iónico Necesitamos un nuevo modelo para explicar ciertas peculiaridades (Li2O). Este nuevo modelo es el enlace iónico Se forma por transferencia de electrones (no hay reparto equitativo,
! Introducción a los sólidos iónicos! Qué elementos los forman?! Qué tipos de fuerzas mantienen la cohesión del cristal?
 Tema 8. Sólidos iónicos Estructura del NaCl Contenidos! Introducción a los sólidos iónicos! Qué elementos los forman?! Qué tipos de fuerzas mantienen la cohesión del cristal?! Propiedades de los sólidos
Tema 8. Sólidos iónicos Estructura del NaCl Contenidos! Introducción a los sólidos iónicos! Qué elementos los forman?! Qué tipos de fuerzas mantienen la cohesión del cristal?! Propiedades de los sólidos
Naturaleza del enlace químico Enlace iónico Enlace covalente Enlaces intermoleculares Enlace metálico
 Naturaleza del enlace químico Enlace iónico Enlace covalente Enlaces intermoleculares Enlace metálico Naturaleza del enlace químico Los átomos tienden a adquirir la máxima estabilidad y esto se consigue
Naturaleza del enlace químico Enlace iónico Enlace covalente Enlaces intermoleculares Enlace metálico Naturaleza del enlace químico Los átomos tienden a adquirir la máxima estabilidad y esto se consigue
Química Inorgánica-63.13- Dra.Silvia E. Jacobo. Sólidos. Estructuras Cristalinas
 Sólidos Estructuras Cristalinas Ordenamientos atómicos En gases no hay orden En líquidos hay orden de corto alcance En sólidos hay orden de largo alcance El ordenamiento está determinado por el tipo de
Sólidos Estructuras Cristalinas Ordenamientos atómicos En gases no hay orden En líquidos hay orden de corto alcance En sólidos hay orden de largo alcance El ordenamiento está determinado por el tipo de
Igual número de cationes y aniones. Ejemplos: cloruro de sodio (NaCl), cloruro de cesio (CsCl), blenda (ZnS), etc.
 6. MATERIALES CERÁMICOS 6.1 Estructura de los cerámicos Enlace atómico: parcial o totalmente iónico Iones metálicos: cationes (ceden sus electrones, +), aniones (aceptan electrones, - ). Estructuras cristalinas,
6. MATERIALES CERÁMICOS 6.1 Estructura de los cerámicos Enlace atómico: parcial o totalmente iónico Iones metálicos: cationes (ceden sus electrones, +), aniones (aceptan electrones, - ). Estructuras cristalinas,
UNIONES ENTRE ÁTOMOS. EL ENLACE QUÍMICO. Física y Química 3º de E.S.O. IES Isidra de Guzmán
 UNIONES ENTRE ÁTOMOS. EL ENLACE QUÍMICO Física y Química 3º de E.S.O. IES Isidra de Guzmán Introducción En la naturaleza, son muy pocos los átomos que se encuentran libres y aislados, sólo los átomos de
UNIONES ENTRE ÁTOMOS. EL ENLACE QUÍMICO Física y Química 3º de E.S.O. IES Isidra de Guzmán Introducción En la naturaleza, son muy pocos los átomos que se encuentran libres y aislados, sólo los átomos de
El enlace iónico. Estudio energético de su formación: Energía reticular.
 El enlace iónico. Estudio energético de su formación: Energía reticular. Tomamos una sustancia iónica típica; el NaCl y se parte de un mol de átomos de Cl y Na separados una distancia tan grande que la
El enlace iónico. Estudio energético de su formación: Energía reticular. Tomamos una sustancia iónica típica; el NaCl y se parte de un mol de átomos de Cl y Na separados una distancia tan grande que la
UNIDAD 3: EL ENLACE QUÍMICO
 UNIDAD 3: EL ENLACE QUÍMICO 1.- REGLA DEL OCTETO Casi todas las sustancias que encontramos en la naturaleza están formadas por átomos unidos. Las fuerzas que mantienen unidos los átomos en las distintas
UNIDAD 3: EL ENLACE QUÍMICO 1.- REGLA DEL OCTETO Casi todas las sustancias que encontramos en la naturaleza están formadas por átomos unidos. Las fuerzas que mantienen unidos los átomos en las distintas
Unidad 4 Enlace iónico y metálico
 Evaluación unidad 4. Enlace iónico y metálico CRITERIOS DE EVALUACIÓN. Utilizar el modelo de enlace correspondiente para explicar la formación de moléculas, de cristales y estructuras macroscópicas, y
Evaluación unidad 4. Enlace iónico y metálico CRITERIOS DE EVALUACIÓN. Utilizar el modelo de enlace correspondiente para explicar la formación de moléculas, de cristales y estructuras macroscópicas, y
SOLUCIONARIO Guía Técnico Profesional
 SOLUCIONARIO Guía Técnico Profesional El enlace químico SGUICTC004TC33-A16V1 Ítem Alternativa Habilidad 1 B Comprensión 2 E Comprensión 3 A Comprensión 4 A Comprensión 5 C Comprensión 6 D Aplicación 7
SOLUCIONARIO Guía Técnico Profesional El enlace químico SGUICTC004TC33-A16V1 Ítem Alternativa Habilidad 1 B Comprensión 2 E Comprensión 3 A Comprensión 4 A Comprensión 5 C Comprensión 6 D Aplicación 7
TEMA 1: ESTRUCTURA INTERNA DE LOS MATERIALES
 PERIODO Departamento de Tecnología. IES Nuestra Señora de la Almudena Mª Jesús Saiz TEMA 1: ESTRUCTURA INTERNA DE LOS MATERIALES El átomo: Toda la materia está compuesta por átomos y éstos por partículas
PERIODO Departamento de Tecnología. IES Nuestra Señora de la Almudena Mª Jesús Saiz TEMA 1: ESTRUCTURA INTERNA DE LOS MATERIALES El átomo: Toda la materia está compuesta por átomos y éstos por partículas
TEMA 4 (Parte I) EL ENLACE QUÍMICO. IÓNICO
 TEMA 4 (Parte I) EL ENLACE QUÍMICO. IÓNICO Mª PILAR RUIZ OJEDA BORJA MUÑOZ LEOZ Contenidos: 1. Introducción 2. Representaciones de Lewis. Regla del Octeto 3. El enlace Iónico 3.1. Redes iónicas 3.2. Energía
TEMA 4 (Parte I) EL ENLACE QUÍMICO. IÓNICO Mª PILAR RUIZ OJEDA BORJA MUÑOZ LEOZ Contenidos: 1. Introducción 2. Representaciones de Lewis. Regla del Octeto 3. El enlace Iónico 3.1. Redes iónicas 3.2. Energía
ENLACES QUÍMICOS. Enlace iónico
 ENLACES QUÍMICOS De los aproximadamente 90 elementos químicos que se encuentran en la naturaleza sólo en unos pocos casos, los gases nobles, sus átomos constituyen entidades individuales. En los demás
ENLACES QUÍMICOS De los aproximadamente 90 elementos químicos que se encuentran en la naturaleza sólo en unos pocos casos, los gases nobles, sus átomos constituyen entidades individuales. En los demás
ENLACE IÓNICO O ELECTROVALENTE
 ENLACE IÓNICO O ELECTROVALENTE Servicios Educativos Integrales Caracterizado por: o Cesión de electrones por parte de un metal a un no metal o Formación de iones de carga contraria, metal (+) y no metal
ENLACE IÓNICO O ELECTROVALENTE Servicios Educativos Integrales Caracterizado por: o Cesión de electrones por parte de un metal a un no metal o Formación de iones de carga contraria, metal (+) y no metal
Elementos Alcalinos:
 Elementos Alcalinos: Litio (Li) Sodio (Na) Potasio (K) Rubidio (Rb) Cesio (Cs) Francio (Fr) Berilio (Be) Magnesio (Mg) Calcio (Ca) Estroncio (Sr) Bario (Ba) Radio (Ra) 1 Propiedades físicas de los elementos
Elementos Alcalinos: Litio (Li) Sodio (Na) Potasio (K) Rubidio (Rb) Cesio (Cs) Francio (Fr) Berilio (Be) Magnesio (Mg) Calcio (Ca) Estroncio (Sr) Bario (Ba) Radio (Ra) 1 Propiedades físicas de los elementos
20.-/ a) Cu: Metálico ; BCl 3 : Covalente ; H 2 O: Covalente ; CsF: Iónico b) BCl 3 : Triangular plana y APOLAR ; H 2 O: Angular y POLAR.
 SOLUCIONES EL Y PROPIEDADES HOJA Nº 7 1.-/ a) Lineal b) Tetraédrica c) Angular d) Angular e) Piramidal trigonal 2.-/ a) Tetraédrica b) Tetraédrica c) Lineal d) Triangular e) Tetraédrica 3.-/ a) 769,2 kj/mol
SOLUCIONES EL Y PROPIEDADES HOJA Nº 7 1.-/ a) Lineal b) Tetraédrica c) Angular d) Angular e) Piramidal trigonal 2.-/ a) Tetraédrica b) Tetraédrica c) Lineal d) Triangular e) Tetraédrica 3.-/ a) 769,2 kj/mol
Tema 14.- Definición, Clasificación y Conformado
 BLOQUE V.- MATERIALES CERÁMICOS Tema 14.- Definición, y Conformado William D. Callister, Jr Introducción a la Ciencia e Ingeniería de los Materiales. Tomo **. Ed. Reverté James F. Shackerlford Introducción
BLOQUE V.- MATERIALES CERÁMICOS Tema 14.- Definición, y Conformado William D. Callister, Jr Introducción a la Ciencia e Ingeniería de los Materiales. Tomo **. Ed. Reverté James F. Shackerlford Introducción
SOLUCIONES BLOQUE 2. EL ÁTOMO: MODELOS, TABLA PERIÓDICA Y ENLACE QUÍMICO.
 SOLUCIONES BLOQUE 2. EL ÁTOMO: MODELOS, TABLA PERIÓDICA Y ENLACE QUÍMICO. Modelos Atómicos 1. Solución: Descubrimiento de los dos «tipos» de electricidad. Siglo XVIII. Descubrimiento del electrón. 1897.
SOLUCIONES BLOQUE 2. EL ÁTOMO: MODELOS, TABLA PERIÓDICA Y ENLACE QUÍMICO. Modelos Atómicos 1. Solución: Descubrimiento de los dos «tipos» de electricidad. Siglo XVIII. Descubrimiento del electrón. 1897.
Geometría molecular. Solo moléculas covalentes. 1.La geometría molecular se refiere a la organización tridimensional de los átomos en las moléculas.
 Tema 1. Propiedades generales. Geometría molecular. Propiedades generales de los elementos no metálicos. Propiedades generales de los óxidos y de los haluros a lo largo del sistema periódico. Variación
Tema 1. Propiedades generales. Geometría molecular. Propiedades generales de los elementos no metálicos. Propiedades generales de los óxidos y de los haluros a lo largo del sistema periódico. Variación
07/02/2015 EL ENLACE QUÍMICO. Tema 5
 EL ENLACE QUÍMICO Tema 5 Por qué se unen los átomos? Los átomos, moléculas e iones y se unen entre sí porque al hacerlo se llega a una situación de mínima energía, lo que equivale a decir de máxima estabilidad
EL ENLACE QUÍMICO Tema 5 Por qué se unen los átomos? Los átomos, moléculas e iones y se unen entre sí porque al hacerlo se llega a una situación de mínima energía, lo que equivale a decir de máxima estabilidad
ENLACE QUÍMICO II. 5.- De los compuestos iónicos KBr y NaBr, cuál será el más duro y cuál el de mayor temperatura de fusión?. Por qué?.
 ENLACE QUÍMICO II 1.- Representa las estructuras de Lewis indicando geometría molecular y momento dipolar de las siguientes moléculas: CO 2, H 2 S y O 2. 2.- De las siguientes moléculas: F 2, CS 2, C 2
ENLACE QUÍMICO II 1.- Representa las estructuras de Lewis indicando geometría molecular y momento dipolar de las siguientes moléculas: CO 2, H 2 S y O 2. 2.- De las siguientes moléculas: F 2, CS 2, C 2
QUÍMICA - 2º BACHILLERATO ENLACE QUÍMICO RESUMEN CONCEPTO DE ENLACE QUÍMICO
 Javier Robledano Arillo Química 2º Bachillerato Enlace Químico - 1 QUÍMICA - 2º BACHILLERATO ENLACE QUÍMICO RESUMEN CONCEPTO DE ENLACE QUÍMICO 1. Enlace químico: conjunto de fuerzas que mantienen unidos
Javier Robledano Arillo Química 2º Bachillerato Enlace Químico - 1 QUÍMICA - 2º BACHILLERATO ENLACE QUÍMICO RESUMEN CONCEPTO DE ENLACE QUÍMICO 1. Enlace químico: conjunto de fuerzas que mantienen unidos
Objetivo. Introducción. Palabras clave. Desarrollo. Química Unidad 8 Enlace químico. 1. Interacciones entre átomos
 Química Unidad 8 Enlace químico Objetivo Comprender los conceptos básicos de los modelos de enlace iónico, covalente y metálico. Introducción Los electrones cumplen un papel fundamental en la formación
Química Unidad 8 Enlace químico Objetivo Comprender los conceptos básicos de los modelos de enlace iónico, covalente y metálico. Introducción Los electrones cumplen un papel fundamental en la formación
Enlace Químico. Química General I 2012
 Enlace Químico Química General I 2012 Los electrones de valencia son los electrones del último orbital en un átomo, son los causantes de los enlaces químicos. Grupo e - configuración # de valencia 1A ns
Enlace Químico Química General I 2012 Los electrones de valencia son los electrones del último orbital en un átomo, son los causantes de los enlaces químicos. Grupo e - configuración # de valencia 1A ns
01 Minerales y estructuras
 01 Minerales y estructuras Año 2017 15/08/2017 1 Contenido Minerales metales Mena, ganga, ley mineral Tipo de minerales Estructura de los materiales Tipo de enlaces: iónico, covalente, metálico, van der
01 Minerales y estructuras Año 2017 15/08/2017 1 Contenido Minerales metales Mena, ganga, ley mineral Tipo de minerales Estructura de los materiales Tipo de enlaces: iónico, covalente, metálico, van der
Las fases condensadas (1)
 1 Las fases condensadas (1) 2 * Huheey, J. E., Keiter, R. L., Keiter, E. A., Inorganic Chemistry: Principles of Structure and Reactivity, 4ª Ed., Harper Collins, 1993. Capítulo 4 y 7. * Casabó i Gispert,
1 Las fases condensadas (1) 2 * Huheey, J. E., Keiter, R. L., Keiter, E. A., Inorganic Chemistry: Principles of Structure and Reactivity, 4ª Ed., Harper Collins, 1993. Capítulo 4 y 7. * Casabó i Gispert,
ENLACE QUÍMICO. TEMA 3 Pág. 271 libro (Unidad 13)
 ENLACE QUÍMICO TEMA 3 Pág. 271 libro (Unidad 13) CONCEPTO DE ENLACE QUÍMICO Concepto de enlace químico Las propiedades de las sustancias puras se deben a: Elementos de las que están constituidas Tipo de
ENLACE QUÍMICO TEMA 3 Pág. 271 libro (Unidad 13) CONCEPTO DE ENLACE QUÍMICO Concepto de enlace químico Las propiedades de las sustancias puras se deben a: Elementos de las que están constituidas Tipo de
Son las fuerzas de atracción que mantienen juntos a los átomos en los compuestos
 Son las fuerzas de atracción que mantienen juntos a los átomos en los compuestos ELECTRONEGATIVIDAD Los enlaces se clasifican en: iónico, covalente metálico. Enlace Iónico- resulta de la transferencia
Son las fuerzas de atracción que mantienen juntos a los átomos en los compuestos ELECTRONEGATIVIDAD Los enlaces se clasifican en: iónico, covalente metálico. Enlace Iónico- resulta de la transferencia
Estado Sólido. Estado Sólido. Estado Sólido. Estado Sólido - + Sólidos cristalinos y sólidos amorfos
 Sólidos cristalinos y sólidos amorfos Sólidos cristalinos: presentan un ordenamiento regular en el espacio Sólidos amorfos: no presentan el ordenamiento típico de los cristalinos Región cristalina Región
Sólidos cristalinos y sólidos amorfos Sólidos cristalinos: presentan un ordenamiento regular en el espacio Sólidos amorfos: no presentan el ordenamiento típico de los cristalinos Región cristalina Región
ÁCIDOS Y BASES DUROS Y BLANDOS.
 ÁCIDOS Y BASES DUROS Y BLANDOS. 4602 Pb(CH 3 COO) 2 + 2KI H 2 O PbI 2 + 2 K(CH 3 COO) 4603 2Na + H 2 O 2NaOH + H 2 ACIDOS Y BASES DUROS Y BLANDOS COMO PODEMOS SABER LA DIRECCION EN QUE OCURREN LAS SIGUIENTES
ÁCIDOS Y BASES DUROS Y BLANDOS. 4602 Pb(CH 3 COO) 2 + 2KI H 2 O PbI 2 + 2 K(CH 3 COO) 4603 2Na + H 2 O 2NaOH + H 2 ACIDOS Y BASES DUROS Y BLANDOS COMO PODEMOS SABER LA DIRECCION EN QUE OCURREN LAS SIGUIENTES
SOLUCIONARIO Guía Estándar Anual
 SOLUCIONARIO Guía Estándar Anual El enlace químico SGUICES004CB33-A16V1 Ítem Alternativa Habilidad 1 E Reconocimiento 2 B Aplicación 3 C Comprensión 4 D Comprensión 5 D Aplicación 6 D Aplicación 7 D Comprensión
SOLUCIONARIO Guía Estándar Anual El enlace químico SGUICES004CB33-A16V1 Ítem Alternativa Habilidad 1 E Reconocimiento 2 B Aplicación 3 C Comprensión 4 D Comprensión 5 D Aplicación 6 D Aplicación 7 D Comprensión
Enlace químico. José Mariano Lucena Cruz 19 de mayo de 2010
 José Mariano Lucena Cruz chenalc@gmail.com 19 de mayo de 2010 El enlace químico La unión entre átomos, moléculas o iones constituye el llamado enlace químico. Su fundamento siempre es de tipo eléctrico.
José Mariano Lucena Cruz chenalc@gmail.com 19 de mayo de 2010 El enlace químico La unión entre átomos, moléculas o iones constituye el llamado enlace químico. Su fundamento siempre es de tipo eléctrico.
1. Sistemas materiales: propiedades 2. Estados de agregación g de los sistemas materiales 3. Teoría cinético molecular
 UNIDAD 1: DIVERSIDAD Y UNIDAD DE ESTRUCTURA DE LA MATERIA 1. Sistemas materiales: propiedades 2. Estados de agregación g de los sistemas materiales 3. Teoría cinético molecular 4. Sustanciaspuras puras,
UNIDAD 1: DIVERSIDAD Y UNIDAD DE ESTRUCTURA DE LA MATERIA 1. Sistemas materiales: propiedades 2. Estados de agregación g de los sistemas materiales 3. Teoría cinético molecular 4. Sustanciaspuras puras,
PREGUNTAS DE TEST SOBRE ENLACES QUÍMICOS
 PREGUNTAS DE TEST SOBRE ENLACES QUÍMICOS )))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))) A - RADIOS ATÓMICOS: B - OTRAS PROPIEDADES PERIÓDICAS: E I, A E, ELECTRONEGATIVIDAD: C -
PREGUNTAS DE TEST SOBRE ENLACES QUÍMICOS )))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))))) A - RADIOS ATÓMICOS: B - OTRAS PROPIEDADES PERIÓDICAS: E I, A E, ELECTRONEGATIVIDAD: C -
GUÍA DE ESTUDIO SEMANA 2 ELECTRONEGATIVIDAD, UNIONES Y ENLACES QUIMICOS Elaborado por: Licda. Lilian Judith Guzmán Melgar
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MEDICAS, CUM UNIDAD DIDACTICA QUIMICA, PRIMER AÑO GUÍA DE ESTUDIO 2015 SEMANA 2 ELECTRONEGATIVIDAD, UNIONES Y ENLACES QUIMICOS Elaborado por:
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MEDICAS, CUM UNIDAD DIDACTICA QUIMICA, PRIMER AÑO GUÍA DE ESTUDIO 2015 SEMANA 2 ELECTRONEGATIVIDAD, UNIONES Y ENLACES QUIMICOS Elaborado por:
Estructura Cristalina de Sólidos
 Estructura Cristalina de Sólidos Relación entre estructura periódica y propiedades Bibliografía: 1. Solid State Physics. Ashcroft and Mermin. 2. Solid State Chemistry. West. 3. Química del Estado Sólido.
Estructura Cristalina de Sólidos Relación entre estructura periódica y propiedades Bibliografía: 1. Solid State Physics. Ashcroft and Mermin. 2. Solid State Chemistry. West. 3. Química del Estado Sólido.
EL ENLACE QUÍMICO. Son las fuerzas que mantienen unidos a los átomos entre sí para formar moléculas o iones.
 EL ENLACE QUÍMICO CONTENIDOS. 1.- El enlace químico. 1.1. Enlace iónico. Reacciones de ionización. 1.2. Enlace covalente. Modelo de Lewis. 2.- Justificación de la fórmula de los principales compuestos
EL ENLACE QUÍMICO CONTENIDOS. 1.- El enlace químico. 1.1. Enlace iónico. Reacciones de ionización. 1.2. Enlace covalente. Modelo de Lewis. 2.- Justificación de la fórmula de los principales compuestos
Los compuestos químicos
 Los compuestos químicos Física y Química Compuestos formados por moléculas Oxford University Press España, S. A. Física y Química 3º ESO 2 Un compuesto químico es una sustancia pura formada por dos o más
Los compuestos químicos Física y Química Compuestos formados por moléculas Oxford University Press España, S. A. Física y Química 3º ESO 2 Un compuesto químico es una sustancia pura formada por dos o más
ENLACE QUÍMICO. NaCl. Grafito: láminas de átomos de carbono
 NaCl Grafito: láminas de átomos de carbono Se denomina enlace químico al conjunto de fuerzas que mantienen unidos los átomos cuando forman moléculas o cristales, así como las fuerzas que mantienen unidas
NaCl Grafito: láminas de átomos de carbono Se denomina enlace químico al conjunto de fuerzas que mantienen unidos los átomos cuando forman moléculas o cristales, así como las fuerzas que mantienen unidas
Explicación de las propiedades y los estados de agregación en los compuestos químicos en función de los tipos de enlace. vs.
 Explicación de las propiedades y los estados de agregación en los compuestos químicos en función de los tipos de enlace. vs. Usar las propiedades y los estados de agregación en los compuestos químicos
Explicación de las propiedades y los estados de agregación en los compuestos químicos en función de los tipos de enlace. vs. Usar las propiedades y los estados de agregación en los compuestos químicos
Capítulo 2 La estructura de los sólidos cristalinos
 Capítulo 2 La estructura de los sólidos cristalinos TEMA 2: La estructura de los sólidos cristalinos 1. Los enlaces interatómicos 2. La estructura cristalina 3. Estructuras de empaquetamiento compacto
Capítulo 2 La estructura de los sólidos cristalinos TEMA 2: La estructura de los sólidos cristalinos 1. Los enlaces interatómicos 2. La estructura cristalina 3. Estructuras de empaquetamiento compacto
ENLACE QUÍMICO. TEMA 3 Pág. 271 libro (Unidad 13)
 ENLACE QUÍMICO TEMA 3 Pág. 271 libro (Unidad 13) CONCEPTO DE ENLACE QUÍMICO Concepto de enlace químico Propiedades de sustancias puras se deben a: Elementos de las que están constituidas Tipo de enlace
ENLACE QUÍMICO TEMA 3 Pág. 271 libro (Unidad 13) CONCEPTO DE ENLACE QUÍMICO Concepto de enlace químico Propiedades de sustancias puras se deben a: Elementos de las que están constituidas Tipo de enlace
1. Clasificación de sustancias por Plinio Sosa
 1. Clasificación de sustancias por Plinio Sosa a) Categorías límite Cómo agrupar tantas sustancias? Puede haber muchas maneras: por su color, por su textura, por su estado físico, por sus propiedades químicas
1. Clasificación de sustancias por Plinio Sosa a) Categorías límite Cómo agrupar tantas sustancias? Puede haber muchas maneras: por su color, por su textura, por su estado físico, por sus propiedades químicas
2. Teoría del enlace de valencia o teoría de deslocalización
 Los metales constituyen una extensa clase de sustancias que abarca cerca del ochenta por ciento de todos los elementos químicos conocidos. Tienen unas propiedades comunes que los caracterizan y que se
Los metales constituyen una extensa clase de sustancias que abarca cerca del ochenta por ciento de todos los elementos químicos conocidos. Tienen unas propiedades comunes que los caracterizan y que se
EJERCICIO DE EXAMEN DE QUÍMICA INORGÁNICA
 EJERCICIO DE EXAMEN DE QUÍMICA INORGÁNICA Las 6 preguntas siguientes se refieren a la tabla periódica que se presenta. Los símbolos han sido asignados arbitrariamente. D H B A E M G J L R X Y N P Q Z T
EJERCICIO DE EXAMEN DE QUÍMICA INORGÁNICA Las 6 preguntas siguientes se refieren a la tabla periódica que se presenta. Los símbolos han sido asignados arbitrariamente. D H B A E M G J L R X Y N P Q Z T
FÍSICA Y QUÍMICA 1º Bachillerato Ejercicios: El átomo y sus enlaces
 1(9) Ejercicio nº 1 Calcula el número atómico y el número másico, así como el número de protones, neutrones y electrones de los siguientes aniones: 35 1 80 1 1 31 3 17 Cl ; Br ; O ; P 35 8 15 Ejercicio
1(9) Ejercicio nº 1 Calcula el número atómico y el número másico, así como el número de protones, neutrones y electrones de los siguientes aniones: 35 1 80 1 1 31 3 17 Cl ; Br ; O ; P 35 8 15 Ejercicio
ENLACE QUÍMICO (0,8 puntos) (0,8 puntos) (0,4 puntos) Julio 2013 (0,8 puntos) (0,9 puntos) (0,3 puntos) Junio (1,2 puntos) (0,8 puntos)
 1 ENLACE QUÍMICO 1. Considere las especies químicas CO 2-3, CS 2, SiCl 4, NCl 3, y responda razonadamente a las siguientes cuestiones: a) Represente la estructura de Lewis de cada una de las especies químicas
1 ENLACE QUÍMICO 1. Considere las especies químicas CO 2-3, CS 2, SiCl 4, NCl 3, y responda razonadamente a las siguientes cuestiones: a) Represente la estructura de Lewis de cada una de las especies químicas
Tema 3. DEFECTOS EN LA ESTRUCTURA CRISTALINA. SOLIDIFICACIÓN DE ME-
 ÍNDICE Prólogo... 15 Tema 1. INTRODUCCIÓN A LA CIENCIA E INGENIERÍA DE MATERIALES... 17 1.1. Introducción... 19 1.2. Los materiales en la sociedad actual... 19 1.3. Propiedades de los materiales... 23
ÍNDICE Prólogo... 15 Tema 1. INTRODUCCIÓN A LA CIENCIA E INGENIERÍA DE MATERIALES... 17 1.1. Introducción... 19 1.2. Los materiales en la sociedad actual... 19 1.3. Propiedades de los materiales... 23
Sólidos Iónicos El enlace Iónico
 1 Sólidos Iónicos El enlace Iónico 2 * Huheey, J. E., Keiter, R. L., Keiter, E. A., Inorganic Chemistry: Principles of Structure and Reactivity, 4ª Ed., Harper Collins, 1993. Capítulo 4. * Douglas, B.;
1 Sólidos Iónicos El enlace Iónico 2 * Huheey, J. E., Keiter, R. L., Keiter, E. A., Inorganic Chemistry: Principles of Structure and Reactivity, 4ª Ed., Harper Collins, 1993. Capítulo 4. * Douglas, B.;
EJERCICIOS RESUELTOS DE ENLACE QUIMICO
 EJERCICIOS RESUELTOS DE ENLACE QUIMICO 1. a) Qué tipo de enlace presenta el compuesto formado por F y Ca? b) Formule dicho compuesto a) Considerando los números atómicos del F (Z=9) y el Ca (Z=20) se desarrollan
EJERCICIOS RESUELTOS DE ENLACE QUIMICO 1. a) Qué tipo de enlace presenta el compuesto formado por F y Ca? b) Formule dicho compuesto a) Considerando los números atómicos del F (Z=9) y el Ca (Z=20) se desarrollan
1- Enlaces entre átomos Por qué se unen los átomos? 2- Distintos tipos de enlaces 2.1- Enlace iónico Compuestos iónicos y sus propiedades 2.
 1- Enlaces entre átomos Por qué se unen los átomos? 2- Distintos tipos de enlaces 2.1- Enlace iónico 2.1.1- Compuestos iónicos y sus propiedades 2.2- Enlace covalente 2.2.1-Estructura de Lewis 2.2.2- Compuestos
1- Enlaces entre átomos Por qué se unen los átomos? 2- Distintos tipos de enlaces 2.1- Enlace iónico 2.1.1- Compuestos iónicos y sus propiedades 2.2- Enlace covalente 2.2.1-Estructura de Lewis 2.2.2- Compuestos
Tema 3. (Parte 1) Enlace químico y propiedades de las sustancias
 Tema 3. (Parte 1) Enlace químico y propiedades de las sustancias ÍNDICE 3.1. Enlace y estabilidad energética 3.2. Enlace iónico Energía de red Ciclo de Born-Haber Propiedades de las sustancias iónicas
Tema 3. (Parte 1) Enlace químico y propiedades de las sustancias ÍNDICE 3.1. Enlace y estabilidad energética 3.2. Enlace iónico Energía de red Ciclo de Born-Haber Propiedades de las sustancias iónicas
El enlace químico 3 ESO SEK-CATALUNYA
 El enlace químico 3 ESO SEK-CATALUNYA Contenidos Enlace químico Enlace metálico Propiedades de los metales Enlace iónico Propiedades de los compuestos iónicos Enlace covalente Propiedades de los compuestos
El enlace químico 3 ESO SEK-CATALUNYA Contenidos Enlace químico Enlace metálico Propiedades de los metales Enlace iónico Propiedades de los compuestos iónicos Enlace covalente Propiedades de los compuestos
EJERCICIOS DE SELECTIVIDAD DE QUÍMICA. TEMAS 1 Y 2
 EJERCICIOS DE SELECTIVIDAD DE QUÍMICA. TEMAS 1 Y 2 1.- a) Razone si una molécula de fórmula AB 2 debe ser siempre lineal. b) Justifique quién debe tener un punto de fusión mayor, el CsI o el CaO. c) Ponga
EJERCICIOS DE SELECTIVIDAD DE QUÍMICA. TEMAS 1 Y 2 1.- a) Razone si una molécula de fórmula AB 2 debe ser siempre lineal. b) Justifique quién debe tener un punto de fusión mayor, el CsI o el CaO. c) Ponga
Técnico Profesional QUÍMICA
 Programa Técnico Profesional QUÍMICA El enlace químico Nº Ejercicios PSU 1. Con respecto a la razón por la que se enlazan los átomos, cuál de las siguientes alternativas es correcta? A) Los átomos se enlazan
Programa Técnico Profesional QUÍMICA El enlace químico Nº Ejercicios PSU 1. Con respecto a la razón por la que se enlazan los átomos, cuál de las siguientes alternativas es correcta? A) Los átomos se enlazan
Colección de problemas Unidad 2
 Facultad de Química, UNAM Curso: Química General I Colección de problemas Unidad 2 1. Describe una contribución importante a la ciencia hecha por cada uno de los científicos siguientes: Dalton, Thomson,
Facultad de Química, UNAM Curso: Química General I Colección de problemas Unidad 2 1. Describe una contribución importante a la ciencia hecha por cada uno de los científicos siguientes: Dalton, Thomson,
GUÍA DE ESTUDIO PARA EL SEGUNDO PARCIAL DE QUÍMICA I Ciclo escolar
 1 ESCUELA PREPARATORIA OFI GUÍA DE ESTUDIO PARA EL SEGUNDO PARCIAL DE QUÍMICA I Ciclo escolar 2011-2012 Instrucción: Determina los valores de los números cuánticos correspondientes al electrón diferencial
1 ESCUELA PREPARATORIA OFI GUÍA DE ESTUDIO PARA EL SEGUNDO PARCIAL DE QUÍMICA I Ciclo escolar 2011-2012 Instrucción: Determina los valores de los números cuánticos correspondientes al electrón diferencial
n = = 1; 1234; 4; l l= = 0; 1; m m = = 0; 0 ; + 0; s 12; 2; = s s s = ½ ½
 ENLACE QUÍMICO 2012 6p 5d Energía 6s 4 f 5p 4d 5s 4s 4p 3d 3p 3s 2s 1s 2p nn == 4; 1; 2; 3; 0; 2; + 0; 2; ss = s= += +½ 1; ll == 1; 2; 3; 4; 0; m 2; 1; m == + 1; 0; 2; 1; s= +½ +½ ½ Enlaces según
ENLACE QUÍMICO 2012 6p 5d Energía 6s 4 f 5p 4d 5s 4s 4p 3d 3p 3s 2s 1s 2p nn == 4; 1; 2; 3; 0; 2; + 0; 2; ss = s= += +½ 1; ll == 1; 2; 3; 4; 0; m 2; 1; m == + 1; 0; 2; 1; s= +½ +½ ½ Enlaces según
INTRODUCCION AL EQUILIBRIO PRECIPITACIÓN - SOLUBILIZACIÓN
 INTRODUCCION AL EQUILIBRIO PRECIPITACIÓN - SOLUBILIZACIÓN Lo básico que debes saber de Química General 14-1 LA SOLUBILIDAD DE ELECTROLITOS FUERTES POCO SOLUBLES Compuesto Solubilidad Electrolito NaCl BaSO
INTRODUCCION AL EQUILIBRIO PRECIPITACIÓN - SOLUBILIZACIÓN Lo básico que debes saber de Química General 14-1 LA SOLUBILIDAD DE ELECTROLITOS FUERTES POCO SOLUBLES Compuesto Solubilidad Electrolito NaCl BaSO
IES La Magdalena. Avilés. Asturias. Enlace Iónico
 IES La Magdalena. Avilés. Asturias Si enfrentamos un átomo al que le falten pocos electrones en su capa de valencia para adquirir la configuración de gas noble (muy electronegativo, tendencia a coger electrones),
IES La Magdalena. Avilés. Asturias Si enfrentamos un átomo al que le falten pocos electrones en su capa de valencia para adquirir la configuración de gas noble (muy electronegativo, tendencia a coger electrones),
Tema 2: Fuerzas intermoleculares
 Tema 2: Fuerzas intermoleculares Fuerzas intermoleculares: ion dipolo, dipolo dipolo, dispersión de London y puentes de hidrógeno. Gases ideales y reales. Propiedades de los ĺıquidos. Presión de vapor.
Tema 2: Fuerzas intermoleculares Fuerzas intermoleculares: ion dipolo, dipolo dipolo, dispersión de London y puentes de hidrógeno. Gases ideales y reales. Propiedades de los ĺıquidos. Presión de vapor.
Introducción a los elementos metálicos y metalurgía
 Tema 7. Introducción a los elementos metálicos y Metalurgia. El enlace en los metales. Conductores y semiconductores. Los metales en la naturaleza. Preparación de la mena. Producción de los metales. La
Tema 7. Introducción a los elementos metálicos y Metalurgia. El enlace en los metales. Conductores y semiconductores. Los metales en la naturaleza. Preparación de la mena. Producción de los metales. La
Unidad 3. Átomos y moléculas
 Unidad 3. Átomos y moléculas Índice de contenido 1. Elementos y compuestos...2 1.1. Teoría atómica de Dalton...2 2.-El átomo...3 3.-Número atómico y número másico...4 4.-Isótopos, unidad de masa atómica
Unidad 3. Átomos y moléculas Índice de contenido 1. Elementos y compuestos...2 1.1. Teoría atómica de Dalton...2 2.-El átomo...3 3.-Número atómico y número másico...4 4.-Isótopos, unidad de masa atómica
TEMA 9 EL ENLACE IÓNICO Y LOS SÓLIDOS IÓNICOS
 TEMA 9 EL ENLACE IÓNICO Y LOS SÓLIDOS IÓNICOS Son aquellos en los que los iones constituyentes están unidos entre sí por fuerzas electrostáticas. Algunas de sus propiedades características son las siguientes:
TEMA 9 EL ENLACE IÓNICO Y LOS SÓLIDOS IÓNICOS Son aquellos en los que los iones constituyentes están unidos entre sí por fuerzas electrostáticas. Algunas de sus propiedades características son las siguientes:
TEMA 5. Elementos y compuestos 1 CLASIFICACIÓN DE LOS ELEMENTOS
 TEMA 5 Elementos y compuestos 1 CLASIFICACIÓN DE LOS ELEMENTOS La primera clasificación de los elementos fue la que distinguió entre metales y no metales y se basaba en el aspecto que presentaban los elementos
TEMA 5 Elementos y compuestos 1 CLASIFICACIÓN DE LOS ELEMENTOS La primera clasificación de los elementos fue la que distinguió entre metales y no metales y se basaba en el aspecto que presentaban los elementos
Enlace Químico: Enlace Iónico y Enlace Covalente. AUTHOR: VICENTE GUZMÁN BROTÓNS
 Ejercicio nº 1 De los compuestos iónicos KBr y NaBr, cuál será el más duro y cuál el de mayor temperatura de fusión? Por qué? Ejercicio nº 1 Coloca las siguientes moléculas por orden creciente de su polaridad:
Ejercicio nº 1 De los compuestos iónicos KBr y NaBr, cuál será el más duro y cuál el de mayor temperatura de fusión? Por qué? Ejercicio nº 1 Coloca las siguientes moléculas por orden creciente de su polaridad:
Unidad 9. Enlace químico ÍNDICE
 Unidad 9 Enlace químico 1 ÍNDICE 1. Átomos unidos por enlace químico. 2. Enlace iónico. Ciclo de Born-Haber. Energía de red. Estructura cristalina de los compuestos iónicos. Propiedades de los compuestos
Unidad 9 Enlace químico 1 ÍNDICE 1. Átomos unidos por enlace químico. 2. Enlace iónico. Ciclo de Born-Haber. Energía de red. Estructura cristalina de los compuestos iónicos. Propiedades de los compuestos
UNIDAD 3. MODIFICACIÓN DE LAS PROPIEDADES DE LOS METALES
 UNIDAD 3. MODIFICACIÓN DE LAS PROPIEDADES DE LOS METALES 1. GENERALIDADES... Pág. 49 2. ESTRUCTURA INTERNA DE LOS METALES... Pág. 49 2.1. Estructuras cristalinas... Pág. 49 2.2. Estructura cristalina cúbica
UNIDAD 3. MODIFICACIÓN DE LAS PROPIEDADES DE LOS METALES 1. GENERALIDADES... Pág. 49 2. ESTRUCTURA INTERNA DE LOS METALES... Pág. 49 2.1. Estructuras cristalinas... Pág. 49 2.2. Estructura cristalina cúbica
Numero másico (A). Suma del numero de protones y el numero de neutrones de un átomo.
 PROPIEDADES DE LOS MATERIALES. UNIDAD El Estado Solido. Estructura Atómica. Protón- partícula con carga positiva. Neutro-partícula con carga neutra. Electron-particula con carga negativa. Numero atómico
PROPIEDADES DE LOS MATERIALES. UNIDAD El Estado Solido. Estructura Atómica. Protón- partícula con carga positiva. Neutro-partícula con carga neutra. Electron-particula con carga negativa. Numero atómico
ENLACE QUÍMICO. + 2 y NF 3. Responda razonadamente:
 1 ENLACE QUÍMICO 1. Considere las especies químicas CS 2, SiCl 4, ICl + 2 y NF 3. Responda razonadamente: a) Represente la estructura de Lewis de cada una de las especies químicas propuestas. (0,8 puntos)
1 ENLACE QUÍMICO 1. Considere las especies químicas CS 2, SiCl 4, ICl + 2 y NF 3. Responda razonadamente: a) Represente la estructura de Lewis de cada una de las especies químicas propuestas. (0,8 puntos)
Tema 2: Fuerzas intermoleculares
 Tema 2: Fuerzas intermoleculares Fuerzas intermoleculares: definición y tratamiento general. Interacciones iónicas. Energía reticular. Moléculas polares. Puentes de Hidrógeno. Moléculas apolares. Gases
Tema 2: Fuerzas intermoleculares Fuerzas intermoleculares: definición y tratamiento general. Interacciones iónicas. Energía reticular. Moléculas polares. Puentes de Hidrógeno. Moléculas apolares. Gases
Maestro: Especialidad: Educación Primaria ENLACE QUÍMICO. Fundamentos y Didáctica de la Física y la Química
 Maestro: Especialidad: Educación Primaria ENLACE QUÍMICO Fundamentos y Didáctica de la Física y la Química Según la regla del octeto, una de las estructuras más estables de los elementos es tener ocho
Maestro: Especialidad: Educación Primaria ENLACE QUÍMICO Fundamentos y Didáctica de la Física y la Química Según la regla del octeto, una de las estructuras más estables de los elementos es tener ocho
Enlace químico Educación Secundaria Obligatoria Física y Química
 EL ENLACE QUÍMICO Hay tres maneras en que se unen los átomos: enlace iónico, enlace covalente y enlace metálico. Los enlaces entre átomos se producen porque éstos quieren cumplir la regla del octeto. La
EL ENLACE QUÍMICO Hay tres maneras en que se unen los átomos: enlace iónico, enlace covalente y enlace metálico. Los enlaces entre átomos se producen porque éstos quieren cumplir la regla del octeto. La
Las que tienen relación con el de tamaño: LAS PROPIEDADES PERIÓDICAS. Se pueden separar en dos grupos: PERIODICIDAD
 LAS PROPIEDADES PERIÓDICAS Se pueden separar en dos grupos: 1- Las que tienen relación con el de tamaño: Los radios atómicos y los radios iónicos o cristalinos. La densidad. (ρ) El punto de fusión y ebullición.
LAS PROPIEDADES PERIÓDICAS Se pueden separar en dos grupos: 1- Las que tienen relación con el de tamaño: Los radios atómicos y los radios iónicos o cristalinos. La densidad. (ρ) El punto de fusión y ebullición.
Compuestos Químicos. Capítulo 3 Sec. 3.1-3.6 Rosamil Rey, PhD CHEM 2115
 Compuestos Químicos Capítulo 3 Sec. 3.1-3.6 Rosamil Rey, PhD CHEM 2115 Tipos de enlaces Enlaces covalentes comparten electrones entre átomos y forman compuestos moleculares. Estos compuestos son representados
Compuestos Químicos Capítulo 3 Sec. 3.1-3.6 Rosamil Rey, PhD CHEM 2115 Tipos de enlaces Enlaces covalentes comparten electrones entre átomos y forman compuestos moleculares. Estos compuestos son representados
4º E.S.O. FÍSICA Y QUÍMICA 3. ENLACE QUÍMICO. Dpto. de Física y Química. R. Artacho
 4º E.S.O. FÍSICA Y QUÍMICA 3. ENLACE QUÍMICO R. Artacho Dpto. de Física y Química Índice CONTENIDOS 1. Enlace químico en las sustancias 2. Tipos de enlace entre átomos 3. Enlace iónico 4. Enlace covalente
4º E.S.O. FÍSICA Y QUÍMICA 3. ENLACE QUÍMICO R. Artacho Dpto. de Física y Química Índice CONTENIDOS 1. Enlace químico en las sustancias 2. Tipos de enlace entre átomos 3. Enlace iónico 4. Enlace covalente
UNIVERSIDAD NACIONAL AGRARIA LA MOLINA CENTRO DE ESTUDIOS PREUNIVERSITARIOS SEGUNDO SEMINARIO DE QUIMICA
 UNIVERSIDAD NACIONAL AGRARIA LA MOLINA CENTRO DE ESTUDIOS PREUNIVERSITARIOS SEGUNDO SEMINARIO DE QUIMICA 1. La configuración electrónica del átomo del elemento E es: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 1
UNIVERSIDAD NACIONAL AGRARIA LA MOLINA CENTRO DE ESTUDIOS PREUNIVERSITARIOS SEGUNDO SEMINARIO DE QUIMICA 1. La configuración electrónica del átomo del elemento E es: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 1
Colección de ejercicios UNIDAD 2
 Facultad de Química, UNAM Curso: Química General I Colección de ejercicios UNIDAD 2 1. Describe cuál fue la contribución al conocimiento de la estructura atómica hecha por cada uno de los siguientes científicos:
Facultad de Química, UNAM Curso: Química General I Colección de ejercicios UNIDAD 2 1. Describe cuál fue la contribución al conocimiento de la estructura atómica hecha por cada uno de los siguientes científicos:
