ENZIMAS & CINÉTICA ENZIMÁTICA
|
|
|
- Inés Godoy Ortiz de Zárate
- hace 6 años
- Vistas:
Transcripción
1 APUNTES DE BIOQUÍMICA 3 ENZIMAS & CINÉTICA ENZIMÁTICA 1 Julián A. Chamucero Millares 1 L os catalizadores son sustancias que se caracterizan por: 1. Aumentar la velocidad de una reacción química 2. No se alteran en el proceso [no se consumen] 3. No interfieren en el estado de equilibrio de la reacción. Es decir, no cambiar la dirección de la reacción. En los sistemas biológicos, la mayoría de las sustancias catalizadoras son proteínas que reciben el nombre de enzimas. Las enzimas y cualquier catalizador actúa sobre otras sustancias a las que llamamos sustratos. En el siguiente ejemplo observamos la reacción de descomposición del peróxido de hidrógeno: H H Esta reacción está favorecida termodinámicamente, puesto que su ΔG es negativo y por lo tanto la dirección de la reacción se encuentra desplazada hacia la izquierda; sin embargo, la descomposición de 1 mol de peróxido de hidrógeno a condiciones ambientales puede tardar mucho más de un año. No obstante, la adición de una molécula de ión férrico es capaz de acelerar la velocidad de la reacción hasta 1000 veces; más aún, la hemoglobina incrementa la tasa en un millón de veces. El ejemplo anterior nos permite concluir dos cosas: 1. Existen sustancias que aumentan la velocidad de una reacción, y 2. El hecho de que una reacción sea termodinámicamente favorable; es decir, que su ΔG sea negativo, no significa en absoluto que la reacción ocurra a gran velocidad. Cómo se estudian las velocidades de las reacciones? El estudio de las velocidades de las reacciones es el campo de aplicación de la cinética química. Ésta rama de la química utiliza modelos y ecuaciones matemáticas para evaluar la velocidad a la cual una serie de sustancias reaccionan para formar unos productos, veamos: Consideremos una reacción química simple, A B 1 Médico Interno. Internado énfasis en investigación. Laboratorio de Biomiméticos Instituto de Biotecnología. Universidad Nacional de Colombia. 2012
2 donde la velocidad es igual a la concentración de B por unidad de tiempo: es decir, a la velocidad de la formación del producto. Donde la velocidad es igual a menos la concentración de A por unidad de tiempo; es decir, la velocidad a la que se consume el reactante. Dado que estamos considerando una reacción irreversible, existe una proporción lineal en la que: O sea que la velocidad a la que se forma el producto es la misma a la que se consume el reactante, por lo que podemos obtener una constante K de velocidad: Por lo que al intentar conocer los determinantes de la velocidad de una reacción, lo que queremos averiguar en sí, son las variables que afectan la constante de velocidad. Entre dichas variables tenemos la temperatura y el ph de la solución; sin embargo, la más importante es la BARRERA ENERGÉTICA DEL ESTADO DE TRANSICIÓN. El estado de transición es una fase de la reacción química en la que los reactantes adoptan una configuración intermedia para transformarse luego en productos. La importancia del estado de transición radica en que presenta un valor de ΔG muy grande el cual deben superar los reactantes para continuar el curso de la reacción; esto quiere decir que cuanto más alto sea el ΔG del estado de transición, más lenta será la reacción. Para que los reactantes alcancen ese nivel de energía se requieren mínimo 3 cosas: 1. Una adecuada disposición de las moléculas 2. Colisiones eficientes entre las moléculas 3. Precisa energética de las colisiones 2 Consideremos ahora la misma reacción, pero ésta vez con la particularidad de ser reversible: A B Por lo que ahora, Estas demostraciones nos permiten tener un conocimiento básico de las velocidades de una reacción y de sus respectivas constantes de velocidad, empero, qué determina la velocidad de una reacción química? Primero que todo es importante conocer el significado del valor de K: Una k alta indica una reacción rápida Una k baja indica una reacción lenta Recordemos ahora que la energía libre del estado de transición se define por: ΔG ǂ = ΔH ǂ - T. ΔS ǂ Entonces si H es alto y S es bajo, el ΔG será mayor a cero, por ende la reacción será lenta. Esto nos indica que una reacción tendrá una constante de velocidad baja entre mayor sea la energética de las colisiones y
3 menor desorganización haya en el sistema; es decir, donde el movimiento de las moléculas tienda a la no aleatorización y disminuya entonces la adecuada disposición y las colisiones de las mismas. Cómo trabajan las enzimas? Las enzimas actúan en dos puntos críticos: 1. Disminuyen la barrera energética de la reacción 2. Aumentan la fracción de las moléculas reactantes Como hemos indicado, la barrera energética se define por: ΔG ǂ = ΔH ǂ - T. ΔS ǂ Modelos del mecanismo de acción de las enzimas Reconocemos ahora que las enzimas disminuyen el valor de ΔG ǂ [energía libre de Gibbs estándar del estado de transición] facilitando la formación de un estado similar al estado de transición. Para que ello sea posible, el sustrato se une a una región aminoacídica específica denominada sitio activo donde ocurre la formación de dicho estado. Para explicar la interacción del sustrato con el sitio activo de la enzima, se han planteado 2 modelos o hipótesis: 3 Y lo que debe hacer una enzima es permitir una reacomodación de los valores de entalpia y entropía para aumentar la velocidad de la reacción: Para disminuir ΔH, el sustrato adopta dentro del sitio activo de la enzima una configuración molecular diferente con menor energía. Para aumentar ΔS, la enzima ajusta la dirección de los sustratos para favorecer la colisión. 1. El primero de ellos fue postulado hacia el año 1894 por un bioquímico alemán llamado Emili Fischer. El pretendía explicar que el sustrato se une a la enzima del mismo modo que una llave encaja perfectamente en una cerradura; sin embargo, este modelo sólo explica la especificidad de las enzimas pero no responde a la pregunta de cómo se consigue formar un estado configuracional similar al del estado de transición. 2. Posteriormente Daniel Koshland proponía en 1958 un modelo diferente al que llamó del ajuste inducido. Esta hipótesis plantea que el sitio activo de la enzima induce al sustrato y a la misma enzima a
4 adoptar una configuración molecular diferente. Teniendo en cuenta esta modificación del modelo previo, la hipótesis del ajuste inducido explica tanto la especificidad como las características propias de la catálisis enzimática [disminución de la barrera energética]. residuos de aminoácidos importantes: a. La histidina que actúa como donadora de protones b. El glutamato que funciona como aceptor de protones Durante la catálisis se forma un compuesto intermediario de menor energía llamado enediol, ya que, el glutamato acepta un protón del carbono 2 [C 2 ] del gliceraldehido-3- fosfato y el residuo de histidina dona un protón al grupo carbonil del mismo G3P. 4 Ahora, si bien es cierto que la estructura completa de la enzima es importante, debido a que la secuencia completa de aminoácidos es la que permite el diseño específico de cada tipo de enzima, es el sitio activo quien juega el papel más substancial en la función catalítica de la enzima. Veamos 2 ejemplos para reconocer por qué. 1. Triosa fosfato isomerasa. Esta enzima como su nombre lo indica isomerisa las triosas fosfato. Un ejemplo es el cambio del gliceraldehido-3-fosfato a dihidroxiacetona-fosfato. El sitio activo de la enzima contiene 2 2. Serina proteasas. Las proteasas son enzimas que catalizan la hidrólisis de los enlaces peptídicos. Las serina proteasas son proteasas en las cuales el residuo de serina del sitio activo es el que juega el papel fundamental en la actividad catalítica. Dos ejemplos de esta clase de enzimas son la tripsina y la quimotripsina. El sitio activo de las enzimas está formado por los residuos aspartato, histidina y serina; ésta última se ubica justo
5 al lado del bolsillo donde se posará la cadena lateral del residuo de aminoácido en el cual la enzima corta el enlace peptídico. Ya que todas las serina proteasas tienen los mismos residuos en el sitio activo, éstas se diferencias por la característica del bolsillo que fija la cadena laretal del residuo específico para el que trabaja la enzima. La constante de velocidad de la reacción entre la enzima y el sustrato está dada por la suma entre la constante de disociación del complejo enzima sustrato en enzima y sustrato (K -1 ) y la constante de disociación del complejo en enzima y producto (K 2 ). K 1 [E][S] = K -1 [ES] + K 2 [ES] Sacamos factor común K 1 [E][S] = {[ES] (K- 1 +K 2 )} Despejamos la concentración del complejo enzima sustrato ( ) 5 Encontramos una constante de equilibrio general para toda la reacción Reemplazamos en la ecuación anterior ( ) (1) Despejamos y obtenemos la concentracion del complejo enzima sustrato en la constante de quilibrio en términos de la concentración de la enzima y el sustrato K M [ES] = [E] [S] (2) C inética enzimática La cinética enzimática estudia las velocidades de las reacciones catalizadas por enzimas. Consideremos lo siguiente: La reacción entre la enzima y el sustrato incluye la formación de un complejo enzima-sustrato E + S ES E+P K-1 K1 K2 Teniendo en cuenta que cuantificar la concentración del complejo enzima-sustrato es en términos prácticos algo imposible, consideremos que la concentración de la enzima después de la reacción es igual a la suma de la concentración de la enzima total menos la del complejo [E] f = [E] T [ES] (3) Reemplazamos esta ecuación en la igualdad número 2 K M [ES] = {[E] T [ES]}. [S]
6 K M [ES] = [E] T [S] [ES][S] Organizamos términos para obtener una formulación que nos permita calcular la concentración del complejo con valores que si podamos medir K M [ES] + [ES][S] = [E] T [S] [ES] (K M + [S]) = [E] T [S] (4) Ahora, partiendo que la reacción inicia desde el complejo enzima-sustrato ya formado, la velocidad de la reacción está dada por: v = K 2 [ES] Reemplazamos este término en la ecuación número 4 v = K 2 (5) Llegado el momento, hay un punto de saturación de la concentración total de la enzima por el sustrato, por lo que la reacción llega a su velocidad máxima: v max = K 2 [E] T Establecemos este término en la ecuación número 5 v = (6) Esta es la ecuación final del análisis de cinética enzimática y se denomina ecuación de Michaelis Menten y K M es la constante de Michaelis. Cuál es la interpretación de KM? Revisemos la siguiente fracción de la constante: Si K M tiene un valor mayor a cero [>0] nos indica que, K -1 >k 1, por lo que hay una disociación rápida del sustrato. De este modo, una primera aproximación a la constante de Michaelis es la de la afinidad por el sustrato, por lo que, entre más grande sea el valor de K M menor será la afinidad. No obstante, la interpretación real es que la K M constituye un valor numéricamente igual a la concentración del sustrato ([S]) a la que la la velocidad de la reacción es la mitad de la velocidad máxima; es decir, v max /2. Ejemplo: los valores de KM para la tripsina y la quimotripsina son: Tripsina: 1.5 x10-2 M Quimotripsina: 3 x10-4 M Esto quiere decir que se nececita una solución de sustrato en una concentración de 0,015 M para conseguir la mitad de la velocidad máxima de la reacción. Supongamos que la v max = 10 moles/s; o sea, que en un segundo la enzima cataliza 10 moles de sustrato. Cuando el sustrato alcanza una concentración de 0,015 M, la enzima cataliza la reacción de 5 moles de sustrato por segundo. Si comparamos los valores de K M para ambas enzimas, la tripsina requiere una concentración menor que la quimotripsina para conseguir la mitad de la velocidad máxima de la reacción. Para los diferentes estudios experimentales con enzimas, la tabulación y diagramación de los datos, se facilita el uso de una transformación algebráica de la ecuación de michaelis-menten. Al obtener los recíprocos a ambos lados de la igualdad y organizando los términos, obtenemos una ecuación que obedece a la formulación de línea recta: 6 y = (m) (x) + b
7 Esta igualdad se conoce como la ecuación de Lineweaver-Burk y permite hacer una gráfica en línea recta denominada representación doble-inversa que presenta: Una pendiente Una intercepción de sobre el eje (o sea el eje y) Una intercepción de sobre el eje de (o sea el eje x] 1. Inhibidor competitivo: se caracteriza por ser una molécula estructuralmente similar al sustrato original, por lo que, dependiendo de la concentración de uno y el otro, compiten por ocupar el sitio activo de la enzima. A mayor concentración del inhibidor, menor será la concentración de sustrato que sea catalizado por la enzima. La enzima dihidrofolato reductasa en una enzima encargada de participar en la síntesis de purinas y pirimidinas a partir de las reacciones con el dihidrofolato. Debido a que la síntesis del DNA y el RNA dependen de la formación de nucleótidos en los que participan las bases de purina y pirimidina, se desarrolló una molécula análoga al dihidrofolato conocida como metotrexate y que actualmente se usa entre otras cosas para el tratamiento quimioterapéutico del cáncer, con lo cual se inhibe la división celular por disminución de la síntesis de las bases constituyentes de los nucleótidos. 7 Inhibición enzimática Las enzimas son macromoléculas cuya función catalítica es susceptible de ser inhibida, existen dos grandes grupos de inhibidores: 1. Inhibidores reversibles 2. Inhibidores irreversibles La diferencia entre ellos radica en el tipo de enlace que forman con la enzima, el primero de ellos utiliza enlaces o fuerzas de interacción débiles, mientras que el segundo lo hace a travpes de enlaces covalentes. De acuerdo al sitio de unión del inhibidor, los inhibidores reversibles se dividen en 3 tipos: 2. Inhibición acompetitiva: en ella, el inhibidor se une exclusivamente al complejo enzima sustrato y por obvias razones en una región diferente al sitio activo de la enzima.
8 C aracterísticas cinéticas de los inhibidores Los experimentos que determinan las velocidades de reacciones catalizadas a diferentes concentraciones de sustrato y del inhibidor, permiten distinguir las características cinéticas de los diferentes tipos de inhibidores: 8 3. Inhibición no competitiva: en ella tanto el sustrato como el inhibidor pueden fijarse a la enzima y actúa disminuyendo el número de recambio de sustrato. 1. Inhibidor competitivo: ya que la molécula análoga desplaza al sustrato del sitio activo, la K M aparente aumenta, ya que hablando en términos del sustrato - se requiere mayor concentración del sustrato para alcanzar la mitad de la velocidad máxima de la reacción. Ahora, hablando en términos de la reacción en si, independientemente de qué molécula ocupe el sitio activo sea sustrato o inhibidor la velocidad máxima de la reacción se conseguirá cuando la concentración de alguna de las dos moléculas sature la concentración de enzima disponible, por lo que finalmente, la v max no cambia. 4. Inhibición mixta: se caracteriza porque el inhibidor puede unirse tanto a la enzima como al complejo enzima sustrato, prevenir la unión del sustrato o disminuir el recambio. 2. Inhibición acompetitiva: el inhibidor acompetitivo sólo se une al complejo enzima sustrato ya formado y bloquea la formación del producto. Ya que la enzima libre tiene ahora mayor concentración de sustrato disponible, la velocidad
9 máxima de la reacción es más fácil de alcanzar, por lo que el valor de v max disminuye. Si el valor de v max disminuye, significa que se requiere una concentración menor de sustrato para alcanzar la mitad de la velocidad máxima, por ende la K M aparente también disminuye. 4. Inhibición mixta:dado que actúa tanto en la enzima como en el complejo enzima sustrato, aumenta la K M y disminuye el valor de v max 9 3. Inhibición no competitiva: como mencionamos, el inhibidor no competitivo se une a una región diferente al sitio activo de la enzima por lo que no interfiere con la unión del sustrato y por ende la concentración para alcanzar la mitad de la velocidad máxima sigue siendo la misma y la K M no se ve alterada; sin embargo, como el inhibidor si retrasa el efecto catalítico, y la enzima demora en disociarse, hay menos enzimas libres para una concentración mayor de sustrato por lo que la velocidad máxima se alcanza más rápido y el valor de v max disminuye. En relación a los inhibidores irreversibles, en general son sustancias tóxicas que se unen de manera covalente al sitio activo de la enzima y bloquear su actividad catalítica. Los podemos dividir en: 1. Reactivos de grupo específico: son moléculas que reaccionan con cadenas laterales específicas de algunos residuos de aminoácidos en el sitio activo. 2. Sustratos análogos reactivos: son moléculas estructuralmente similares a los sustratos nativos pero que se unen de manera covalente al sitio activo de la enzima. 3. Inhibidores suicida: son moleculas similares al sustrato que se caracterizan por permitir una reacción catalítica; sin embargo, los productos resultan ser intermediarios tóxicos que se unen de manera covalente a la enzima y la inactivan.
10 M ecanismos de regulación enzimática Como cualquier otro mecanismo dentro de los seres vivos, la catálisis de las reacciones bioquímicas deben ocurrir en el lugar y el tiempo adecuados, por lo que se hace necesaria una regulación de la actividad enzimática. Se han descrito 5 mecanismos reguladores: 1. Control alostérico: ocurre en aquellas enzimas de naturaleza proteíca que contienen múltiples subunidades que actúan como sitio funcional y sitio de control. Presentan además una propiedad llamada cooperatividad de unión y que quiere decir que la unión de una molécula a un sitio control o funcional afecta la actividad de los demás sitios o subunidades. Si ese control cooperativo se da por la unión al sustrato, el mecanismo se denomina homoalosterismo; mientras que, si la cooperatividad es por otras moléculas diferentes al sustrato, la regulación es del tipo heteroalosterismo. Este tipo de enzimas no obedecen la cinética de Michaelis-Menten puesto que su comportamiento no se refiere a la unión de una sola molécula de sustrato al sitio activo sino de varias moléculas a los sitios funcionales. Un ejemplo clásico de enzima alostérica es la aspartato carbamoiltransferasa [ATCasa], una proteínas con estructura cuaternaria que incluye 6 unidades catalíticas unidad por 6 unidades reguladoras. La ATCasa cataliza la primera reacción de la biosíntesis de las pirimidinas que incluye la condensación del carbamoil fosfato y el aspartato para formar carbamoilaspartato. De la secuencia de la reacción de síntesis se obtiene un nucleótido de pirimida llamado citidin trifosfato [CTP] el cual cuando comienza a acumularse se une a uno de los sitios regulares de la enzima e inhibe su actividad indicando que ya se sintetizó la suficiente canditad de nucleotidos necesarios. 2. Diferentes formas de la enzima: hace referencia a las isozimas o isoenzimas, enzimas estructuralmente diferentes pero que catalizan la misma reacción; sin embargo, varían sus parámetros cinéticos y sus mecanismos de regulación. Dos ejemplos de esta clase de enzimas son la lactado deshidrogenasa, una enzima que participa en la glucólisis anaerobia y que presenta 2 isoenzimas, una en el músculo cardiaco y otra en el músculo esquelético y mostrándo diferente afinidad por la glucosa entre ambos tejidos. El segundo ejemplo lo constituye la glucoquinasa, una isoenzima de la hexoquinasa presente en el tejido hepático pero con menor afinidad por la glucosa para un adecuado control de los niveles de liberación de insulina y glucagón. 3. Modificaciones covalentes reversibles: es un elemento regulador abundante en los mecanismos de señalización intracelular e involucra la unión covalente reversible de grupos fosfato para la activación o inactivación de las enzimas. Una de las enzimas encargadas de la fosforilación [activación] de otras enzimas es la protein cinasa K que cataliza la reacción de transferencia de un grupo fosfato desde el ATP hacia un residuo de aminoácido de otra enzima. 4. Activación proteolítica: son enzimas que son sintetizadas en un estado inactivo o zimógenos y que requieren de un clivaje proteolítico para su activación. El tripsinógeno [el zimógeno de la tripsina] es sintetizado en el páncreas y secretado al duodeno donde es 10
11 activado por la enteroquinasa intestinal. 5. Síntesis de la enzima: es el control absoluto y está mediado por la expresión génica y la síntesis de mrna. Bibliografía 11 Mathews, C.K.; Van Holde, K.E.; Ahern K.G.(2002). Enzimas: catalizadores biológicos. Bioquímica. (pp )Pearson Education, S.A., Madrid. Nelson, D.L & Cox, M.M. (2008) Enzymes. Lehninger. Principles of Biochemistry. (pp ). W.H. Freeman and Compañy, New York. Berg, J.M.; Timoczko, J.L.; Stryer Lubert (2007) Enzymes: basic concepts and kinetics. Regulatory Strategies Lehninger. Principles of Biochemistry. (pp , ). W.H. Freeman and Compañy, New York.
Enzimas Departamento de Bioquímica Noviembre de 2005
 U.T.I. Biología Celular Enzimas Departamento de Bioquímica Noviembre de 2005 Enzimas A. Propiedades generales de las enzimas B. Principios fundamentales de su acción catalítica C. Introducción a la cinética
U.T.I. Biología Celular Enzimas Departamento de Bioquímica Noviembre de 2005 Enzimas A. Propiedades generales de las enzimas B. Principios fundamentales de su acción catalítica C. Introducción a la cinética
Cinética enzimática. La velocidad enzimática sigue una curva denominada hipérbola descripta por la Ecuación de Michaelis y Menten:
 Cinética enzimática Hemos visto que la concentración de sustrato es uno de los factores más importantes que determinan la velocidad de una reacción enzimática. La velocidad enzimática sigue una curva denominada
Cinética enzimática Hemos visto que la concentración de sustrato es uno de los factores más importantes que determinan la velocidad de una reacción enzimática. La velocidad enzimática sigue una curva denominada
Tema 10. Regulación de la actividad enzimática
 Tema 10. Regulación de la actividad enzimática Control de la actividad enzimática Regulación por cambios en la concentración de enzima Regulación alostérica Modificaciones covalentes reversibles Activación
Tema 10. Regulación de la actividad enzimática Control de la actividad enzimática Regulación por cambios en la concentración de enzima Regulación alostérica Modificaciones covalentes reversibles Activación
ENZIMAS. Kuhne en el año de 1876 les llamó enzima a los catalizadores que producían
 ENZIMAS Dr. Santiago René Anzaldúa Arce. Kuhne en el año de 1876 les llamó enzima a los catalizadores que producían fermentaciones de diversos compuestos, La palabra enzima significa en la levadura, pues
ENZIMAS Dr. Santiago René Anzaldúa Arce. Kuhne en el año de 1876 les llamó enzima a los catalizadores que producían fermentaciones de diversos compuestos, La palabra enzima significa en la levadura, pues
Licenciatura Ingeniería Bioquímica Industrial MANUAL DE PRÁCTICAS DEL LABORATORIO DE INGENIERÍA ENZIMÁTICA
 División de Ciencias Biológicas y de la Salud Departamento de Biotecnología Licenciatura Ingeniería Bioquímica Industrial MANUAL DE PRÁCTICAS DEL LABORATORIO DE INGENIERÍA ENZIMÁTICA Dr. Sergio Huerta
División de Ciencias Biológicas y de la Salud Departamento de Biotecnología Licenciatura Ingeniería Bioquímica Industrial MANUAL DE PRÁCTICAS DEL LABORATORIO DE INGENIERÍA ENZIMÁTICA Dr. Sergio Huerta
TEMA 11.- CINÉTICA ENZIMÁTICA
 TEMA 11.- CINÉTICA ENZIMÁTICA Introducción: Cinética enzimática. Ecuación de Michaelis-Menten. Ecuación de Lineweaver-Burk. Reacciones con múltiples substratos. Inhibición enzimática: - Reversible Competitiva.
TEMA 11.- CINÉTICA ENZIMÁTICA Introducción: Cinética enzimática. Ecuación de Michaelis-Menten. Ecuación de Lineweaver-Burk. Reacciones con múltiples substratos. Inhibición enzimática: - Reversible Competitiva.
Catálisis Enzimática MODELO DE MICHAELIS- MENTEN
 Catálisis Enzimática MODELO DE MICHAELIS- MENTEN Enzima - Sustrato La enzima dihidrofolato reductasa de E. coli con sus dos sustratos, dihidrofolato (derecha) y NADPH (izquierda), unidos al sitio activo.
Catálisis Enzimática MODELO DE MICHAELIS- MENTEN Enzima - Sustrato La enzima dihidrofolato reductasa de E. coli con sus dos sustratos, dihidrofolato (derecha) y NADPH (izquierda), unidos al sitio activo.
A B Ej. Cinética de primer orden
 Cinética enzimática A B Ej. Cinética de primer orden Concentración de A o B tiempo Reactivo Producto -da/dt = v = k [A] A=A 0 e- kt db/dt = v = k [A 0 ]-[B] B=A 0 + e kt Concentración en función del tiempo
Cinética enzimática A B Ej. Cinética de primer orden Concentración de A o B tiempo Reactivo Producto -da/dt = v = k [A] A=A 0 e- kt db/dt = v = k [A 0 ]-[B] B=A 0 + e kt Concentración en función del tiempo
ESTUDIOS CINÉTICOS SE MIDE LA VELOCIDAD DE LA REACCIÓN CATALIZADA. La velocidad de reacciones químicas: Para una reacción:
 ESTUDIOS CINÉTICOS SE MIDE LA VELOCIDAD DE LA REACCIÓN CATALIZADA La velocidad de reacciones químicas: Para una reacción: A B La velocidad depende de la concentración del reactante: v = k[a] k = constante
ESTUDIOS CINÉTICOS SE MIDE LA VELOCIDAD DE LA REACCIÓN CATALIZADA La velocidad de reacciones químicas: Para una reacción: A B La velocidad depende de la concentración del reactante: v = k[a] k = constante
Es la capacidad de realizar un trabajo. A pesar que existen varias formas de energía: química, luminosa, mecánica, etc., solo hay dos tipos básicos:
 Es la capacidad de realizar un trabajo. A pesar que existen varias formas de energía: química, luminosa, mecánica, etc., solo hay dos tipos básicos: Potencial: es la capacidad de realizar trabajo como
Es la capacidad de realizar un trabajo. A pesar que existen varias formas de energía: química, luminosa, mecánica, etc., solo hay dos tipos básicos: Potencial: es la capacidad de realizar trabajo como
Bioquímica Estructural y Metabólica. TEMA 5. Enzimología
 TEMA 5. Enzimas. Clasificación. Principios de la catálisis enzimá6ca. Energía de ac6vación. Velocidad de reacción y equilibrio de reacción. Ciné6ca enzimá6ca: ecuación de Michaelis- Menten. Ecuación de
TEMA 5. Enzimas. Clasificación. Principios de la catálisis enzimá6ca. Energía de ac6vación. Velocidad de reacción y equilibrio de reacción. Ciné6ca enzimá6ca: ecuación de Michaelis- Menten. Ecuación de
Es la capacidad de realizar un trabajo. En términos bioquímicos: representa la capacidad de cambio, ya que la vida depende de que la energía pueda
 Es la capacidad de realizar un trabajo. En términos bioquímicos: representa la capacidad de cambio, ya que la vida depende de que la energía pueda ser transformada de una forma a otra, cuyo estudio es
Es la capacidad de realizar un trabajo. En términos bioquímicos: representa la capacidad de cambio, ya que la vida depende de que la energía pueda ser transformada de una forma a otra, cuyo estudio es
EL CONTROL DE LAS ACTIVIDADES CELULARES
 EL CONTROL DE LAS ACTIVIDADES CELULARES LAS REACCIONES CELULARES BÁSICAS Todas las células llevan a cabo funciones vitales: Ingestión de nutrientes Eliminación de desperdicios Crecimiento Reproducción
EL CONTROL DE LAS ACTIVIDADES CELULARES LAS REACCIONES CELULARES BÁSICAS Todas las células llevan a cabo funciones vitales: Ingestión de nutrientes Eliminación de desperdicios Crecimiento Reproducción
III. Inhibición enzimática
 III. Inhibición enzimática Inhibidor: Efector que hace disminuir la actividad enzimática, a través de interacciones con el centro activo u otros centros específicos. Inhibidores Inhibidores Reversibles:
III. Inhibición enzimática Inhibidor: Efector que hace disminuir la actividad enzimática, a través de interacciones con el centro activo u otros centros específicos. Inhibidores Inhibidores Reversibles:
PROTEINAS COMO CATALIZADORES ENZIMAS
 PROTEINAS COMO CATALIZADORES ENZIMAS ENZIMAS son proteínas que catalizan reacciones químicas en los seres vivos. son catalizadores: sustancias que, sin consumirse en una reacción, aumentan notablemente
PROTEINAS COMO CATALIZADORES ENZIMAS ENZIMAS son proteínas que catalizan reacciones químicas en los seres vivos. son catalizadores: sustancias que, sin consumirse en una reacción, aumentan notablemente
CARACTERÍSTICAS DE LAS ENZIMAS
 BIOQUÍMICA I CARACTERÍSTICAS DE LAS ENZIMAS 1. Son los catalizadores de las reacciones químicas de los sistemas biológicos. 2. Tienen gran poder catalítico. 3. Poseen un elevado grado de especificidad
BIOQUÍMICA I CARACTERÍSTICAS DE LAS ENZIMAS 1. Son los catalizadores de las reacciones químicas de los sistemas biológicos. 2. Tienen gran poder catalítico. 3. Poseen un elevado grado de especificidad
Tema 7. Cinética Enzimática
 Tema 7 Cinética Enzimática 1 TEMA 7 CINÉTICA ENZIMÁTICA 1. DEFINICIONES CÓMO ACTÚAN LOS ENZIMAS? 2. CINÉTICA ENZIMÁTICA MODELO DE MICHAELIS-MENTEN REPRESENTACIONES 3. INHIBICIONES EN REACCIONES ENZIMÁTICAS
Tema 7 Cinética Enzimática 1 TEMA 7 CINÉTICA ENZIMÁTICA 1. DEFINICIONES CÓMO ACTÚAN LOS ENZIMAS? 2. CINÉTICA ENZIMÁTICA MODELO DE MICHAELIS-MENTEN REPRESENTACIONES 3. INHIBICIONES EN REACCIONES ENZIMÁTICAS
ESTRUCTURA DE LA TRIOSAFOSFATO ISOMERASA esta proteína es una eficiente enzima involucrada en la vía glucolítica.
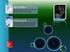 ESTRUCTURA DE LA TRIOSAFOSFATO ISOMERASA esta proteína es una eficiente enzima involucrada en la vía glucolítica. Características generales Cinética química Nomenclatura Centro activo Cofactores Factores
ESTRUCTURA DE LA TRIOSAFOSFATO ISOMERASA esta proteína es una eficiente enzima involucrada en la vía glucolítica. Características generales Cinética química Nomenclatura Centro activo Cofactores Factores
CINÉTICA QUÍMICA. Química General e Inorgánica Licenciatura en Ciencias Biológicas Profesorado en Biología Analista Biológico
 Química General e Inorgánica Licenciatura en Ciencias Biológicas Profesorado en Biología Analista Biológico CINÉTICA QUÍMICA La cinética química estudia la variación de la concentración de reactantes o
Química General e Inorgánica Licenciatura en Ciencias Biológicas Profesorado en Biología Analista Biológico CINÉTICA QUÍMICA La cinética química estudia la variación de la concentración de reactantes o
PROPEDÉUTICO DE ODONTOLOGÍA BIOQUÍMICA BÁSICA
 PROPEDÉUTICO DE ODONTOLOGÍA BIOQUÍMICA BÁSICA 2012 Dagmar Stojanovic de Malpica Ph D Escuela de Biología, Facultad de Ciencias, U.C.V. UNIDAD IV. ENZIMAS Relación entre el G o y la K eq en una reacción
PROPEDÉUTICO DE ODONTOLOGÍA BIOQUÍMICA BÁSICA 2012 Dagmar Stojanovic de Malpica Ph D Escuela de Biología, Facultad de Ciencias, U.C.V. UNIDAD IV. ENZIMAS Relación entre el G o y la K eq en una reacción
ENZIMAS. Las enzimas son proteínas con función catalítica
 ENZIMAS Las enzimas son proteínas con función catalítica Las enzimas son catalizadores biológicos que permiten que las reacciones metabólicas ocurran a gran velocidad en condiciones compatibles con la
ENZIMAS Las enzimas son proteínas con función catalítica Las enzimas son catalizadores biológicos que permiten que las reacciones metabólicas ocurran a gran velocidad en condiciones compatibles con la
CINÉTICA QUÍMICA. Dr. Hugo Cerecetto. Prof. Titular de Química
 CINÉTICA QUÍMICA Dr. Hugo Cerecetto Prof. Titular de Química Temario 2) La reacción química: - Nociones de Termoquímica y Termodinámica. Conceptos de entalpía y entropía de reacción. Energía libre. Espontaneidad
CINÉTICA QUÍMICA Dr. Hugo Cerecetto Prof. Titular de Química Temario 2) La reacción química: - Nociones de Termoquímica y Termodinámica. Conceptos de entalpía y entropía de reacción. Energía libre. Espontaneidad
METABOLISMO Y ENZIMAS
 DESAFÍO Nº 12 Profesora Verónica Abasto Córdova Biología 1 Medio Nombre del Estudiante : Curso : METABOLISMO Y ENZIMAS TIMBRE METABOLISMO En las clases anteriores, estudiamos los principios de la teoría
DESAFÍO Nº 12 Profesora Verónica Abasto Córdova Biología 1 Medio Nombre del Estudiante : Curso : METABOLISMO Y ENZIMAS TIMBRE METABOLISMO En las clases anteriores, estudiamos los principios de la teoría
ACCIÓN DE LOS INHIBIDORES COMPETITIVOS Y NO COMPETITIVOS SOBRE LA ACTIVIDAD ENZIMÁTICA
 ACCIÓN DE LOS INHIBIDORES COMPETITIVOS Y NO COMPETITIVOS SOBRE LA ACTIVIDAD ENZIMÁTICA I. INTRODUCCIÓN Una propiedad característica de las enzimas es su sensibilidad a diversos reactivos químicos que reaccionan
ACCIÓN DE LOS INHIBIDORES COMPETITIVOS Y NO COMPETITIVOS SOBRE LA ACTIVIDAD ENZIMÁTICA I. INTRODUCCIÓN Una propiedad característica de las enzimas es su sensibilidad a diversos reactivos químicos que reaccionan
Factores que afectan la velocidad de una reacción catalizada por enzimas
 Factores que afectan la velocidad de una reacción catalizada por enzimas Concentración de sustrato o sustratos (cofactores) Concentración de enzima Inhibidores Activadores ph Temperatura Regulación de
Factores que afectan la velocidad de una reacción catalizada por enzimas Concentración de sustrato o sustratos (cofactores) Concentración de enzima Inhibidores Activadores ph Temperatura Regulación de
6. Enzimas - Actividades
 I.E.S. Flavio Irnitano El Saucejo (Sevilla) Curso 2.015 2.016 Departamento de Biología y Geología NIVEL: 2º Bachillerato MATERIA: BIOLOGÍA 6.1. Concepto y estructura. BLOQUE I. CUÁL ES LA COMPOSICIÓN DE
I.E.S. Flavio Irnitano El Saucejo (Sevilla) Curso 2.015 2.016 Departamento de Biología y Geología NIVEL: 2º Bachillerato MATERIA: BIOLOGÍA 6.1. Concepto y estructura. BLOQUE I. CUÁL ES LA COMPOSICIÓN DE
FISIOLOGÍA GENERAL Jesús Merino Pérez y María José Noriega Borge
 ENZIMAS INTRODUCCIÓN Las enzimas son el grupo más variado y especializado de las proteínas, su función es actuar como catalizadores, permitiendo que las reacciones que transcurren en los seres vivos puedan
ENZIMAS INTRODUCCIÓN Las enzimas son el grupo más variado y especializado de las proteínas, su función es actuar como catalizadores, permitiendo que las reacciones que transcurren en los seres vivos puedan
ENZIMAS I TEMA Introducción
 TEMA 7 ENZIMAS I 1. Introducción 2. Las enzimas como catalizadores 3. Nomenclatura y clasificación de enzimas 4. Cofactores enzimáticos 5. Modelos de actuación de las enzimas 1. Introducción La vida depende
TEMA 7 ENZIMAS I 1. Introducción 2. Las enzimas como catalizadores 3. Nomenclatura y clasificación de enzimas 4. Cofactores enzimáticos 5. Modelos de actuación de las enzimas 1. Introducción La vida depende
Actividad: Cómo ocurren las reacciones químicas?
 Cinética química Cómo ocurren las reacciones químicas? Nivel: 3º Medio Subsector: Ciencias químicas Unidad temática: Cinética Actividad: Cómo ocurren las reacciones químicas? Qué es la cinética de una
Cinética química Cómo ocurren las reacciones químicas? Nivel: 3º Medio Subsector: Ciencias químicas Unidad temática: Cinética Actividad: Cómo ocurren las reacciones químicas? Qué es la cinética de una
UNIDAD 5. AMINOÁCIDOS Y PROTEÍNAS
 UNIDAD 5. AMINOÁCIDOS Y PROTEÍNAS Dr en C. MPA MVZ Carlos Gutiérrez Olvera AMINOÁCIDOS: Como su nombre lo implica, los aminoácidos son moléculas orgánicas que contienen un grupo amino (NH2) en uno de los
UNIDAD 5. AMINOÁCIDOS Y PROTEÍNAS Dr en C. MPA MVZ Carlos Gutiérrez Olvera AMINOÁCIDOS: Como su nombre lo implica, los aminoácidos son moléculas orgánicas que contienen un grupo amino (NH2) en uno de los
Click para ir al sitio web:
 Slide 1 / 63 New Jersey Center for Teaching and Learning Iniciativa de Ciencia Progresiva Este material está disponible gratuitamente en www.njctl.org y está pensado para el uso no comercial de estudiantes
Slide 1 / 63 New Jersey Center for Teaching and Learning Iniciativa de Ciencia Progresiva Este material está disponible gratuitamente en www.njctl.org y está pensado para el uso no comercial de estudiantes
SEGUNDO DE BACHILLERATO QUÍMICA. a A + b B c C + d D
 TEMA 5. CINÉTICA QUÍMICA a A + b B c C + d D 1 d[a] 1 d[b] 1 d[c] 1 d[d] mol v = = = + = + a dt b dt c dt d dt L s El signo negativo en la expresión de velocidad es debido a que los reactivos desaparecen,
TEMA 5. CINÉTICA QUÍMICA a A + b B c C + d D 1 d[a] 1 d[b] 1 d[c] 1 d[d] mol v = = = + = + a dt b dt c dt d dt L s El signo negativo en la expresión de velocidad es debido a que los reactivos desaparecen,
BLOQUE I: LAS MOLÉCULAS DE LA VIDA ENZIMAS. 2. Mecanismo de acción y cinética enzimática.
 ENZIMAS 1. Concepto y estructura. 2. Mecanismo de acción y cinética enzimática. 3. Regulación de la actividad enzimática: temperatura, ph, inhibidores. 4. Bibliografía. 5. Preguntas selectividad. Imagen
ENZIMAS 1. Concepto y estructura. 2. Mecanismo de acción y cinética enzimática. 3. Regulación de la actividad enzimática: temperatura, ph, inhibidores. 4. Bibliografía. 5. Preguntas selectividad. Imagen
EJERCICIOS DE TERMOQUÍMICA
 EJERCICIOS DE TERMOQUÍMICA En los exámenes de Acceso a la Universidad se proponen una serie de cuestiones (más teóricas) y problemas (prácticos) para resolver. En estos apuntes vamos a resolver ambos tipos
EJERCICIOS DE TERMOQUÍMICA En los exámenes de Acceso a la Universidad se proponen una serie de cuestiones (más teóricas) y problemas (prácticos) para resolver. En estos apuntes vamos a resolver ambos tipos
Similitudes y Diferencias entre los catalizadores inorgánico y las enzimas
 CINETICA ENZIATICA Enzimas: Determinan la pauta de las reacciones quimicas Intervienen en mecanismos de transduccion de Energia Estabilizan un estado de transicion Poseen alta especificidad de sustrato.
CINETICA ENZIATICA Enzimas: Determinan la pauta de las reacciones quimicas Intervienen en mecanismos de transduccion de Energia Estabilizan un estado de transicion Poseen alta especificidad de sustrato.
Bioenergética e introducción al metabolismo Departamento de Bioquímica Noviembre de 2005
 U.T.I. Biología Celular Bioenergética e introducción al metabolismo Departamento de Bioquímica Noviembre de 2005 Definiciones LA TERMODINAMICA ES LA CIENCIA QUE ESTUDIA LA ENERGIA Y SUS TRANSFORMACIONES
U.T.I. Biología Celular Bioenergética e introducción al metabolismo Departamento de Bioquímica Noviembre de 2005 Definiciones LA TERMODINAMICA ES LA CIENCIA QUE ESTUDIA LA ENERGIA Y SUS TRANSFORMACIONES
Bioquímica Termodinámica y bioenergética.
 Bioquímica Termodinámica y bioenergética. Facultad de Enfermería Universidad de la República ESFUNO 2014 Amalia Ávila Termodinámica y bioenergética Los organismos vivos no se encuentran en equilibrio con
Bioquímica Termodinámica y bioenergética. Facultad de Enfermería Universidad de la República ESFUNO 2014 Amalia Ávila Termodinámica y bioenergética Los organismos vivos no se encuentran en equilibrio con
UNIVERSIDAD PERUANA CAYETANO HEREDIA CENTRO FORMATIVO PREUNIVERSITARIO BIOLOGÍA METABOLISMO
 UNIVERSIDAD PERUANA CAYETANO HEREDIA CENTRO FORMATIVO PREUNIVERSITARIO BIOLOGÍA METABOLISMO METABOLISMO Ciclo interdependendiente, intercambio de E y materia. AUTOTROFOS FOTOSINTETICOS HETEROTROFOS Procesos
UNIVERSIDAD PERUANA CAYETANO HEREDIA CENTRO FORMATIVO PREUNIVERSITARIO BIOLOGÍA METABOLISMO METABOLISMO Ciclo interdependendiente, intercambio de E y materia. AUTOTROFOS FOTOSINTETICOS HETEROTROFOS Procesos
Ácidos nucléicos. Los ácidos nucleicos fueron descubiertos por Freidrich Miescher en Mirel Nervenis
 Ácidos nucléicos Los ácidos nucleicos fueron descubiertos por Freidrich Miescher en 1869 La información genética o genoma, está contenida en unas moléculas llamadas ácidos nucleicos. Existen dos tipos
Ácidos nucléicos Los ácidos nucleicos fueron descubiertos por Freidrich Miescher en 1869 La información genética o genoma, está contenida en unas moléculas llamadas ácidos nucleicos. Existen dos tipos
UNIDAD 2. CINÉTICA QUÍMICA
 UNIDAD 2. CINÉTICA QUÍMICA Introducción. Velocidad de reacción Cómo se producen las reacciones químicas Ecuación de la velocidad de reacción Factores que afectan a la velocidad de reacción Mecanismo de
UNIDAD 2. CINÉTICA QUÍMICA Introducción. Velocidad de reacción Cómo se producen las reacciones químicas Ecuación de la velocidad de reacción Factores que afectan a la velocidad de reacción Mecanismo de
Factores que afectan a la velocidad de una reacción.
 Factores que afectan a la elocidad de una reacción. Naturaleza de las sustancias. stado físico. Concentración de los reactios. l aumentar aumenta la elocidad. Temperatura. l aumentar aumenta la elocidad.
Factores que afectan a la elocidad de una reacción. Naturaleza de las sustancias. stado físico. Concentración de los reactios. l aumentar aumenta la elocidad. Temperatura. l aumentar aumenta la elocidad.
Son CATALIZADORES, es decir, disminuyen la energía de activación de las reacciones químicas. Son PROTEÍNAS con estructura tridimensional, que poseen
 Son CATALIZADORES, es decir, disminuyen la energía de activación de las reacciones químicas. Son PROTEÍNAS con estructura tridimensional, que poseen un centro activo en el que se acopla el sustrato para
Son CATALIZADORES, es decir, disminuyen la energía de activación de las reacciones químicas. Son PROTEÍNAS con estructura tridimensional, que poseen un centro activo en el que se acopla el sustrato para
Metabolismo. Forma de obtención de carbono. Corresponde a la actividad. participan sistemas multienzimáticos (rutas metabólicas) RUTAS METABÓLICAS
 Facultad de Ciencias de la Salud BIO160 Bioquímica i General Metabolismo METABOLISMO Corresponde a la actividad coordinada que ocurre dentro de una célula, en la cual participan sistemas multienzimáticos
Facultad de Ciencias de la Salud BIO160 Bioquímica i General Metabolismo METABOLISMO Corresponde a la actividad coordinada que ocurre dentro de una célula, en la cual participan sistemas multienzimáticos
Capítulo 4. Reacciones orgánicas.
 apítulo 4. Reacciones orgánicas. Una reacción química se puede definir como un proceso de interacción entre especies químicas en el que, como consecuencia de la ruptura y formación de enlaces, se origina
apítulo 4. Reacciones orgánicas. Una reacción química se puede definir como un proceso de interacción entre especies químicas en el que, como consecuencia de la ruptura y formación de enlaces, se origina
Proteínas Globulares: Hemoglobina. Proteínas Fibrosas: Colágeno
 Proteínas Globulares: Hemoglobina. Proteínas Fibrosas: Colágeno Tema 3 Proteínas Fibrosas y Proteínas Globulares Fibrosas Globulares Forma alargada Unidades repetidas de un solo tipo de estructura secundaria
Proteínas Globulares: Hemoglobina. Proteínas Fibrosas: Colágeno Tema 3 Proteínas Fibrosas y Proteínas Globulares Fibrosas Globulares Forma alargada Unidades repetidas de un solo tipo de estructura secundaria
Catálisis enzimática. Tema 8 (cont)
 Tema 8 (cont) Catálisis enzimática 1 Para entender las enzimas necesitamos dos propiedades termodinámicas de la reacción 1. Diferencia de E libre (ΔG) entre productos y reactantes. Se relaciona con la
Tema 8 (cont) Catálisis enzimática 1 Para entender las enzimas necesitamos dos propiedades termodinámicas de la reacción 1. Diferencia de E libre (ΔG) entre productos y reactantes. Se relaciona con la
ÁMINOACIDOS ESTRUCTURA
 Proteínas y Enzimas ÁMINAIDS ESTRUTURA N ADENA LATERAL N PLAR AMINÁIDS - LASIFIAIN AMINÁIDS - LASIFIAIN N ADENA LATERAL PLAR SIN ARGA ELETRIA AMINÁIDS - LASIFIAIN N ADENA LATERAL PLAR N ARGA ELETRIA N
Proteínas y Enzimas ÁMINAIDS ESTRUTURA N ADENA LATERAL N PLAR AMINÁIDS - LASIFIAIN AMINÁIDS - LASIFIAIN N ADENA LATERAL PLAR SIN ARGA ELETRIA AMINÁIDS - LASIFIAIN N ADENA LATERAL PLAR N ARGA ELETRIA N
CONVERGENCIA METABÓLICA. En el catabolismo aerobio existen tres fases principales:
 CONVERGENCIA METABÓLICA Rutas catabólicas En el catabolismo aerobio existen tres fases principales: - Fase I.- Transformación de Macromoléculas en sus Monómeros correspondientes. 1) Polisacáridos Monosacáridos
CONVERGENCIA METABÓLICA Rutas catabólicas En el catabolismo aerobio existen tres fases principales: - Fase I.- Transformación de Macromoléculas en sus Monómeros correspondientes. 1) Polisacáridos Monosacáridos
QUÍMICA FÍSICA II Grupo A. Tercer control, 10 de mayo de Escoged 2 de las 3 preguntas que os propongo, cada una de las preguntas vale 5 puntos.
 QUÍMICA FÍSICA II Grupo A. Tercer control, 10 de mayo de 2011 Escoged 2 de las 3 preguntas que os propongo, cada una de las preguntas vale 5 puntos. 1. Qué significado tienen los parámetros termodinámicos
QUÍMICA FÍSICA II Grupo A. Tercer control, 10 de mayo de 2011 Escoged 2 de las 3 preguntas que os propongo, cada una de las preguntas vale 5 puntos. 1. Qué significado tienen los parámetros termodinámicos
1.- CONCEPTO DE ENZIMA
 ENZIMAS 1.- CONCEPTO DE ENZIMA Los enzimas son catalizadores muy potentes y eficaces, Químicamente son proteínas Actúan en pequeña cantidad y se recuperan indefinidamente No llevan a cabo reacciones energéticamente
ENZIMAS 1.- CONCEPTO DE ENZIMA Los enzimas son catalizadores muy potentes y eficaces, Químicamente son proteínas Actúan en pequeña cantidad y se recuperan indefinidamente No llevan a cabo reacciones energéticamente
Generalidades de ENZIMAS
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,007 Generalidades de ENZIMAS Dr. Mynor Leiva 1 ENZIMAS Proteínas
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,007 Generalidades de ENZIMAS Dr. Mynor Leiva 1 ENZIMAS Proteínas
GLUCOSA: EXCELENTE COMBUSTIBLE Y PRECURSOR VERSÁTIL
 GLICÓLISIS GLUCOSA: EXCELENTE COMBUSTIBLE Y PRECURSOR VERSÁTIL GLICÓLISIS (GLYCOS = AZÚCAR + LÍSIS = RUPTURA) FASE PREPARATORIA O FASE DE GASTO DE ENERGÍA (ATP) Inversión de ATP aumenta el contenido de
GLICÓLISIS GLUCOSA: EXCELENTE COMBUSTIBLE Y PRECURSOR VERSÁTIL GLICÓLISIS (GLYCOS = AZÚCAR + LÍSIS = RUPTURA) FASE PREPARATORIA O FASE DE GASTO DE ENERGÍA (ATP) Inversión de ATP aumenta el contenido de
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2012 QUÍMICA TEMA 4: ENERGÍA DE LAS REACCIONES QUÍMICAS
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 1 QUÍMICA TEMA 4: ENERGÍA DE LAS REACCIONES QUÍMICAS Junio, Ejercicio 4, Opción A Junio, Ejercicio 6, Opción B Reserva 1, Ejercicio 3, Opción B Reserva, Ejercicio
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 1 QUÍMICA TEMA 4: ENERGÍA DE LAS REACCIONES QUÍMICAS Junio, Ejercicio 4, Opción A Junio, Ejercicio 6, Opción B Reserva 1, Ejercicio 3, Opción B Reserva, Ejercicio
Energía y metabolismo
 Energía y metabolismo Sesión 17 Introducción a la Biología Prof. Nelson A. Lagos Los sistemas vivos son abiertos y requieren energía para mantenerse La energía es la capacidad de hacer trabajo. Cinético
Energía y metabolismo Sesión 17 Introducción a la Biología Prof. Nelson A. Lagos Los sistemas vivos son abiertos y requieren energía para mantenerse La energía es la capacidad de hacer trabajo. Cinético
LA ENERGÍA EN LAS REACCIONES METABÓLICAS
 LA ENERGÍA EN LAS REACCIONES METABÓLICAS ENERGIA DE ACTIVACIÓN. CATALIZADORES ENERGIA DE ACTIVACIÓN. CATALIZADORES REACTIVOS PRODUCTOS ENERGIA DE ACTIVACIÓN. ENZIMAS Las ENZIMAS son proteínas que ACTÚAN
LA ENERGÍA EN LAS REACCIONES METABÓLICAS ENERGIA DE ACTIVACIÓN. CATALIZADORES ENERGIA DE ACTIVACIÓN. CATALIZADORES REACTIVOS PRODUCTOS ENERGIA DE ACTIVACIÓN. ENZIMAS Las ENZIMAS son proteínas que ACTÚAN
Tema 6. Termodinámica y cinética
 Tema 6. Termodinámica y cinética A) Termodinámica Por qué algunas reacciones químicas son espontáneas a ciertas temperaturas? Existe alguna forma de predecir si una reacción va a producirse en unas condiciones
Tema 6. Termodinámica y cinética A) Termodinámica Por qué algunas reacciones químicas son espontáneas a ciertas temperaturas? Existe alguna forma de predecir si una reacción va a producirse en unas condiciones
Lehninger, cap. 15, ps ; Mathews.- cap. 13, ps y cap.16. ps ; Stryer.- cap. 21, ps ; Voet.-cap. 15, ps
 BBM II. 2012/13 (R-T8-1) Tema 8.- Metabolismo del glucógeno: Metabolismo de polisacáridos de reserva. Degradación y Síntesis del glucógeno. Regulación metabólica y hormonal de la glucogenolisis y glucogénesis.
BBM II. 2012/13 (R-T8-1) Tema 8.- Metabolismo del glucógeno: Metabolismo de polisacáridos de reserva. Degradación y Síntesis del glucógeno. Regulación metabólica y hormonal de la glucogenolisis y glucogénesis.
Las enzimas. Interesante:
 Las enzimas Interesante: http://www.genomasur.com/lecturas/guia03.htm Las enzimas son catalizadores biológicos o biocatalizadores. Como tales: No se consumen en la reacción. No se alteran (sólo durante
Las enzimas Interesante: http://www.genomasur.com/lecturas/guia03.htm Las enzimas son catalizadores biológicos o biocatalizadores. Como tales: No se consumen en la reacción. No se alteran (sólo durante
Bioquímica. Carrera: IAC Participantes. Representantes de las academias de Ingeniería Ambiental. Academia de Ingeniería
 1.- DATOS DE LA ASIGNATURA Nombre de la asignatura: Carrera: Clave de la asignatura: Horas teoría-horas práctica-créditos Bioquímica Ingeniería Ambiental IAC - 0405 4-2-10 2.- HISTORIA DEL PROGRAMA Lugar
1.- DATOS DE LA ASIGNATURA Nombre de la asignatura: Carrera: Clave de la asignatura: Horas teoría-horas práctica-créditos Bioquímica Ingeniería Ambiental IAC - 0405 4-2-10 2.- HISTORIA DEL PROGRAMA Lugar
Tema 7. Actividad enzimática
 Tema 7. Actividad enzimática Definición, clasificación y nomenclatura de las enzimas Coenzimas y cofactores Mecanismos de la catálisis enzimática Centro activo y especificidad Tipos de catálisis Generalidades
Tema 7. Actividad enzimática Definición, clasificación y nomenclatura de las enzimas Coenzimas y cofactores Mecanismos de la catálisis enzimática Centro activo y especificidad Tipos de catálisis Generalidades
J. L. Sánchez Guillén. IES Pando - Oviedo Departamento de Biología y Geología
 J. L. Sánchez Guillén IES Pando - Oviedo Departamento de Biología y Geología METABOLISMO: Conjunto de procesos químicos que se producen en la célula, catalizados por enzimas y que tienen como objetivo
J. L. Sánchez Guillén IES Pando - Oviedo Departamento de Biología y Geología METABOLISMO: Conjunto de procesos químicos que se producen en la célula, catalizados por enzimas y que tienen como objetivo
Proteínas y Ácidos Nucleicos
 Proteínas y Ácidos Nucleicos Mapa conceptual Biomoléculas. Biomoléculas inorgánicas: Moléculas que no presentan carbono en su estructura. Biomoléculas orgánicas: Moléculas que presentan carbono en su estructura.
Proteínas y Ácidos Nucleicos Mapa conceptual Biomoléculas. Biomoléculas inorgánicas: Moléculas que no presentan carbono en su estructura. Biomoléculas orgánicas: Moléculas que presentan carbono en su estructura.
INTRODUCCION A LA BIOLOGIA CELULAR Y MOLECULAR
 INTRODUCCION A LA BIOLOGIA CELULAR Y MOLECULAR - Componentes químicos de la célula - Un poco de química 1 Un poco de química El 99% del peso de una célula corresponde a C, H, N y O. La sustancia más abundante
INTRODUCCION A LA BIOLOGIA CELULAR Y MOLECULAR - Componentes químicos de la célula - Un poco de química 1 Un poco de química El 99% del peso de una célula corresponde a C, H, N y O. La sustancia más abundante
GUÍA N 3: Equilibrio Químico y Cinética Química
 1 PRIMERA PARTE: Ejercicios de desarrollo. 1.- Defina los siguientes términos: a) Reacción irreversible b) Reacción reversible c) Equilibrio químico d) Constante de equilibrio e) Principio de Le Chatelier
1 PRIMERA PARTE: Ejercicios de desarrollo. 1.- Defina los siguientes términos: a) Reacción irreversible b) Reacción reversible c) Equilibrio químico d) Constante de equilibrio e) Principio de Le Chatelier
PLANIFICACIÓN DE ASIGNATURA
 PLANIFICACIÓN DE ASIGNATURA I IDENTIFICACION GENERAL DE LA ASIGNATURA CARRERA BIOQUÍMICA DEPARTAMENTO BiOLOGIA ASIGNATURA BIOQUIMICA I CÓDIGO PRERREQUISITOS Fisicoquímica II y Química Orgánica II CREDITOS
PLANIFICACIÓN DE ASIGNATURA I IDENTIFICACION GENERAL DE LA ASIGNATURA CARRERA BIOQUÍMICA DEPARTAMENTO BiOLOGIA ASIGNATURA BIOQUIMICA I CÓDIGO PRERREQUISITOS Fisicoquímica II y Química Orgánica II CREDITOS
Aplicación de los criterios de espontaneidad a una reacción química completa
 Algunas reflexiones sobre el equilibrio químico a partir de consideraciones termodinámicas Prof. Marisa García Dra. María Antonia Grompone 1 Introducción En los programas de Química del Bachillerato Diversificado
Algunas reflexiones sobre el equilibrio químico a partir de consideraciones termodinámicas Prof. Marisa García Dra. María Antonia Grompone 1 Introducción En los programas de Química del Bachillerato Diversificado
REACCIÓN QUÍMICA. ENERGÍA DE ACTIVACIÓN
 Enzimas REACCIÓN QUÍMICA. ENERGÍA DE ACTIVACIÓN Toda reacción química, sea exotérmica o endotérmica, requiere inicialmente una cantidad de energía, denominada energía de activación, para llevarse a cabo.
Enzimas REACCIÓN QUÍMICA. ENERGÍA DE ACTIVACIÓN Toda reacción química, sea exotérmica o endotérmica, requiere inicialmente una cantidad de energía, denominada energía de activación, para llevarse a cabo.
TEMA V. VELOCIDAD DE REACCIÓN. EQUILIBRIO QUÍMICO
 TEMA V. VELOCIDAD DE REACCIÓN. EQUILIBRIO QUÍMICO I. VELOCIDAD DE REACCIÓN. Hemos visto hasta ahora el efecto térmico que acompaña a la reacción química, así como la posibilidad de predecir la espontaneidad.
TEMA V. VELOCIDAD DE REACCIÓN. EQUILIBRIO QUÍMICO I. VELOCIDAD DE REACCIÓN. Hemos visto hasta ahora el efecto térmico que acompaña a la reacción química, así como la posibilidad de predecir la espontaneidad.
EQUILIBRIO QUÍMICO. Concentración. C ó D. Tiempo. Las concentraciones no cambian mucho con el tiempo. El Equilibrio es estable A+B C + D
 EQUILIBRIO QUÍMICO En química definimos equilibrio químico como el balance exacto entre dos procesos, uno de los cuales es opuesto a otro. Cuando ocurre una reacción química, los reactivos se va transformando
EQUILIBRIO QUÍMICO En química definimos equilibrio químico como el balance exacto entre dos procesos, uno de los cuales es opuesto a otro. Cuando ocurre una reacción química, los reactivos se va transformando
Biomoléculas orgánicas: Proteínas y Ácidos nucleicos. Propiedad Intelectual Cpech
 Biología Biomoléculas orgánicas: Proteínas y Ácidos nucleicos Repaso Moléculas orgánicas Carbohidratos Lípidos 1. Monosacáridos: glucosa 2. Disacáridos: maltosa 3. Polisacáridos: glucógeno 1. Ácidos grasos.
Biología Biomoléculas orgánicas: Proteínas y Ácidos nucleicos Repaso Moléculas orgánicas Carbohidratos Lípidos 1. Monosacáridos: glucosa 2. Disacáridos: maltosa 3. Polisacáridos: glucógeno 1. Ácidos grasos.
4. El esquema adjunto representa la estructura de una molécula denominada lisozima.
 BLOQUE I : La base físico-química de la materia 1. a. Nombre y formule un monosacárido que contenga seis átomos de carbono. b. Indica esquemáticamente una diferencia estructural existente entre el almidón
BLOQUE I : La base físico-química de la materia 1. a. Nombre y formule un monosacárido que contenga seis átomos de carbono. b. Indica esquemáticamente una diferencia estructural existente entre el almidón
BIOQUÍMICA-1º de Medicina Dpto. Biología Molecular Jesús Navas ENZIMAS
 Tema 6. ENZIMAS. Clasificación. Principios de la catálisis enzimática. Energía de activación. Velocidad de reacción y equilibrio de reacción. Cinética enzimática: ecuación de Michaelis- Menten. Ecuación
Tema 6. ENZIMAS. Clasificación. Principios de la catálisis enzimática. Energía de activación. Velocidad de reacción y equilibrio de reacción. Cinética enzimática: ecuación de Michaelis- Menten. Ecuación
LAS ENZIMAS ENZIMAS CLASIFICACIÓN ESTRUCTURA FUNCIÓN. Biocatalizadores. proteica. velocidad reacción. Energía activación. Inorgánica.
 LAS ENZIMAS ENZIMAS ESTRUCTURA puede ser FUNCIÓN CLASIFICACIÓN Holoenzima formada Estrictamente proteica Biocatalizadores actúan Ligasas Isomerasas Liasas Hidrolasas Transferasas Oxidorreductasas de naturaleza
LAS ENZIMAS ENZIMAS ESTRUCTURA puede ser FUNCIÓN CLASIFICACIÓN Holoenzima formada Estrictamente proteica Biocatalizadores actúan Ligasas Isomerasas Liasas Hidrolasas Transferasas Oxidorreductasas de naturaleza
Metabolismo glucídico y control de la Glicemia Bioquímica Facultad de Enfermería Universidad de la República
 Metabolismo glucídico y control de la Glicemia Bioquímica Facultad de Enfermería Universidad de la República ESFUNO 2014 Amalia Ávila Propiedades diferenciales y regulación de las distintas isoformas de
Metabolismo glucídico y control de la Glicemia Bioquímica Facultad de Enfermería Universidad de la República ESFUNO 2014 Amalia Ávila Propiedades diferenciales y regulación de las distintas isoformas de
CRISTALOQUÍMICA TEMA 9 POLIMORFISMO Y TRANSFORMACIONES POLIMÓRFICAS. TRANSFORMACIONES ORDEN - DESORDEN ÍNDICE
 CRISTALOQUÍMICA TEMA 9 POLIMORFISMO Y TRANSFORMACIONES POLIMÓRFICAS. TRANSFORMACIONES ORDEN - DESORDEN 9.1 Introducción 9.2 Estabilidad y equilibrio ÍNDICE 9.3 Concepto de polimorfismo y de transformación
CRISTALOQUÍMICA TEMA 9 POLIMORFISMO Y TRANSFORMACIONES POLIMÓRFICAS. TRANSFORMACIONES ORDEN - DESORDEN 9.1 Introducción 9.2 Estabilidad y equilibrio ÍNDICE 9.3 Concepto de polimorfismo y de transformación
N (g) 3 H (g) 2 NH (g)
 IES La Magdalena. Avilés. Asturias La cinética química estudia la velocidad a la que se producen las reacciones químicas, los factores que la modifican y el mecanismo (reacciones intermedias) a través
IES La Magdalena. Avilés. Asturias La cinética química estudia la velocidad a la que se producen las reacciones químicas, los factores que la modifican y el mecanismo (reacciones intermedias) a través
Un sistema se encuentra en un estado de equilibrio químico cuando su composición no varía con el tiempo.
 Un sistema se encuentra en un estado de equilibrio químico cuando su composición no varía con el tiempo. N 2 g 3 H 2 g 2 NH 3 g 2 NH 3 g N 2 g 3 H 2 g concentración H 2 N 2 NH 3 concentración NH 3 H 2
Un sistema se encuentra en un estado de equilibrio químico cuando su composición no varía con el tiempo. N 2 g 3 H 2 g 2 NH 3 g 2 NH 3 g N 2 g 3 H 2 g concentración H 2 N 2 NH 3 concentración NH 3 H 2
Tema 9 Parámetros que influyen en la velocidad de reacción enzimática
 Tema 9 Parámetros que influyen en la velocidad de reacción enzimática Factores que modifican la actividad enzimática Efecto del ph y la Tª Inhibidores Inhibición reversible Competitiva No competitiva Inhibición
Tema 9 Parámetros que influyen en la velocidad de reacción enzimática Factores que modifican la actividad enzimática Efecto del ph y la Tª Inhibidores Inhibición reversible Competitiva No competitiva Inhibición
CADENA RESPIRATORIA I. Dra. María Uxúa Alonso Fresán
 Universidad Autónoma del Estado de México Facultad de Medicina Veterinaria y Zootecnia Licenciatura en Medicina Veterinaria y Zootecnia Unidad de Aprendizaje de Bioquímica CADENA RESPIRATORIA I Dra. María
Universidad Autónoma del Estado de México Facultad de Medicina Veterinaria y Zootecnia Licenciatura en Medicina Veterinaria y Zootecnia Unidad de Aprendizaje de Bioquímica CADENA RESPIRATORIA I Dra. María
SÍNTESIS Y DEGRADACIÓN DE GLUCÓGENO
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, UNIDAD DIDÁCTICA: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,011 SÍNTESIS Y DEGRADACIÓN DE GLUCÓGENO Dr. Mynor A. Leiva Enríquez
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, UNIDAD DIDÁCTICA: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,011 SÍNTESIS Y DEGRADACIÓN DE GLUCÓGENO Dr. Mynor A. Leiva Enríquez
Fosforilación a nivel de sustrato. Fosforilación Oxidativa (Fosforilación a nivel de Cadena Respiratoria).
 Fosforilación a nivel de sustrato Fosforilación Oxidativa (Fosforilación a nivel de Cadena Respiratoria). La Fosforilación a nivel de sustrato es un mecanismo poco habitual de formación de ATP FOSFOGLICERATO
Fosforilación a nivel de sustrato Fosforilación Oxidativa (Fosforilación a nivel de Cadena Respiratoria). La Fosforilación a nivel de sustrato es un mecanismo poco habitual de formación de ATP FOSFOGLICERATO
ENZIMAS I TEMA 7. 1. Introducción
 TEMA 7 ENZIMAS I 1. Introducción 2. Las enzimas como catalizadores 3. Nomenclatura y clasificación de enzimas 4. Cofactores enzimáticos 5. Modelos de actuación de las enzimas 1. Introducción La vida depende
TEMA 7 ENZIMAS I 1. Introducción 2. Las enzimas como catalizadores 3. Nomenclatura y clasificación de enzimas 4. Cofactores enzimáticos 5. Modelos de actuación de las enzimas 1. Introducción La vida depende
Niveles de organización biológica. La composición de los seres vivos
 Niveles de organización biológica. La composición de los seres vivos Imagen de Fondo bajo licencia Creative Commons, autor: René Ehrtardt. Animación ADN de dominio público, fuente:wikipedia Con este tema
Niveles de organización biológica. La composición de los seres vivos Imagen de Fondo bajo licencia Creative Commons, autor: René Ehrtardt. Animación ADN de dominio público, fuente:wikipedia Con este tema
Compuestos ricos en energía. Dr. Juan Pablo Damián BMC Bioquímica, Facultad de Veterinaria
 Compuestos ricos en energía Dr. Juan Pablo Damián BMC Bioquímica, Facultad de Veterinaria ATP: moneda de energía entre catabolismo y anabolismo celular. Catabolismo ATP ADP + Pi Procesos endergónicos:
Compuestos ricos en energía Dr. Juan Pablo Damián BMC Bioquímica, Facultad de Veterinaria ATP: moneda de energía entre catabolismo y anabolismo celular. Catabolismo ATP ADP + Pi Procesos endergónicos:
Los nucleótidos están formados por una base nitrogenada, ribosa o desoxirribosa y un grupo fosfato.
 Introducción Los nucleótidos están formados por una base nitrogenada, ribosa o desoxirribosa y un grupo fosfato. Origen de los átomos que componen: Las bases púricas Base Nucleósido Nucleótido monofosfato
Introducción Los nucleótidos están formados por una base nitrogenada, ribosa o desoxirribosa y un grupo fosfato. Origen de los átomos que componen: Las bases púricas Base Nucleósido Nucleótido monofosfato
En el estudio de los mecanismos de acción farmacológica hay que distinguir.
 TEMA : ASPECTOS MOLECULARES DEL MECANISMO DE ACCIÓN DE LOS FÁRMACOS En el estudio de los mecanismos de acción farmacológica hay que distinguir. Fármacos de Acción Específica: son aquellos que han de interaccionar
TEMA : ASPECTOS MOLECULARES DEL MECANISMO DE ACCIÓN DE LOS FÁRMACOS En el estudio de los mecanismos de acción farmacológica hay que distinguir. Fármacos de Acción Específica: son aquellos que han de interaccionar
BIOSINTESIS DE AMINOÁCIDOS INTEGRANTES: ZACHARY FERNANDA CUELLAR CARDOZO PAOLA ANDREA CASTAÑO PAYA
 BIOSINTESIS DE AMINOÁCIDOS INTEGRANTES: ZACHARY FERNANDA CUELLAR CARDOZO PAOLA ANDREA CASTAÑO PAYA Aminoácidos Es una molécula orgánica con un grupo amino (-NH 2 ) y un grupo carboxilo (- COOH). Los aminoácidos
BIOSINTESIS DE AMINOÁCIDOS INTEGRANTES: ZACHARY FERNANDA CUELLAR CARDOZO PAOLA ANDREA CASTAÑO PAYA Aminoácidos Es una molécula orgánica con un grupo amino (-NH 2 ) y un grupo carboxilo (- COOH). Los aminoácidos
REGULACIÓN DE LA EXPRESIÓN GENÉTICA EN PROCARIOTES
 REGULACIÓN DE LA EXPRESIÓN GENÉTICA EN PROCARIOTES La regulación de la expresión de los genes surge de la necesidad de controlar la actividad de las enzimas o de las proteínas en general, en momentos precisos
REGULACIÓN DE LA EXPRESIÓN GENÉTICA EN PROCARIOTES La regulación de la expresión de los genes surge de la necesidad de controlar la actividad de las enzimas o de las proteínas en general, en momentos precisos
RESULTADO DE APRENDIZAJE:
 Explicar las reacciones químicas del ciclo de Krebs y su regulación RESULTADO DE APRENDIZAJE: Relacionar el metabolismo de las distintas macromoléculas alrededor del Ciclo de Krebs Las reacciones se llevan
Explicar las reacciones químicas del ciclo de Krebs y su regulación RESULTADO DE APRENDIZAJE: Relacionar el metabolismo de las distintas macromoléculas alrededor del Ciclo de Krebs Las reacciones se llevan
Energía Interna (E): Expresa la energía total de un sistema. Es la capacidad que tiene un sistema de desarrollar algún tipo de trabajo.
 Bioenergética Estudia el flujo de energía en los procesos biológicos, fisiológicos y bioquímicos. Se le conoce como la termodinámica aplicada a los sistemas biológicos. Conceptos básicos Energía Interna
Bioenergética Estudia el flujo de energía en los procesos biológicos, fisiológicos y bioquímicos. Se le conoce como la termodinámica aplicada a los sistemas biológicos. Conceptos básicos Energía Interna
Apuntes de Electroquímica
 En la región donde interaccionan electrodo y disolución pueden ocurrir dos tipos de reacciones: de oxidación o de reducción. La velocidad de una reacción elemental depende de la concentración de las especies
En la región donde interaccionan electrodo y disolución pueden ocurrir dos tipos de reacciones: de oxidación o de reducción. La velocidad de una reacción elemental depende de la concentración de las especies
SESIÓN 13 EQUILIBRIO QUÍMICO EN FASE GASEOSA
 I. CONTENIDOS: 1. Leyes de los gases. 2. Presión y temperatura. 3. Principio de Le Chatelier. 4. Constante de equilibrio. SESIÓN 13 EQUILIBRIO QUÍMICO EN FASE GASEOSA II. OBJETIVOS: Al término de la Sesión,
I. CONTENIDOS: 1. Leyes de los gases. 2. Presión y temperatura. 3. Principio de Le Chatelier. 4. Constante de equilibrio. SESIÓN 13 EQUILIBRIO QUÍMICO EN FASE GASEOSA II. OBJETIVOS: Al término de la Sesión,
Clave Genética y Síntesis de Proteínas
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,011 Clave Genética y Síntesis de Proteínas Dr. Mynor A. Leiva Enríquez
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,011 Clave Genética y Síntesis de Proteínas Dr. Mynor A. Leiva Enríquez
1.- Lactato, producido fundamentalmente mediante la glucólisis en el músculo esquelético y los eritrocitos
 Sustratos de la gluconeogénesis 1.- Lactato, producido fundamentalmente mediante la glucólisis en el músculo esquelético y los eritrocitos Durante el ejercicio intenso se movilizan las reservas de glucógeno
Sustratos de la gluconeogénesis 1.- Lactato, producido fundamentalmente mediante la glucólisis en el músculo esquelético y los eritrocitos Durante el ejercicio intenso se movilizan las reservas de glucógeno
Nutrición Vegetal. Absorción de sales minerales
 Nutrición Vegetal Absorción de sales minerales Absorción - Es el proceso mediante el cual un ión o molécula ingresa a una célula o un cuerpo a través de una membrana. No intervienen fuerzas intermoleculares.
Nutrición Vegetal Absorción de sales minerales Absorción - Es el proceso mediante el cual un ión o molécula ingresa a una célula o un cuerpo a través de una membrana. No intervienen fuerzas intermoleculares.
Biopolímero s (4831)
 Biopolímero s (4831) 4.3. Conceptos de catálisis química. 4.3.3. Ejemplos de tipos de catálisis. Aplicación a la catálisis enzimática Los iones metálicos como catalizadores Como se dijo anteriormente los
Biopolímero s (4831) 4.3. Conceptos de catálisis química. 4.3.3. Ejemplos de tipos de catálisis. Aplicación a la catálisis enzimática Los iones metálicos como catalizadores Como se dijo anteriormente los
FACULTAD DE CIENCIAS MEDICINA HUMANA Y CIENCIAS DE LA SALUD Escuela Profesional de Farmacia y Bioquímica SILABO
 FACULTAD DE CIENCIAS MEDICINA HUMANA Y CIENCIAS DE LA SALUD Escuela Profesional de Farmacia y Bioquímica SILABO 1. DATOS INFORMATIVOS 1.1 Asignatura : BIOQUÍMICA I 1.2 Código : 1902-19301 1.3 Área : Formativo
FACULTAD DE CIENCIAS MEDICINA HUMANA Y CIENCIAS DE LA SALUD Escuela Profesional de Farmacia y Bioquímica SILABO 1. DATOS INFORMATIVOS 1.1 Asignatura : BIOQUÍMICA I 1.2 Código : 1902-19301 1.3 Área : Formativo
INHIBICIÓN ENZIMÁTICA
 HBDORES HBCÓ EZMÁTCA TEMA Moléculas que disminuyen la V de reacción enzimática Afectan a la cinética de reacción al interferir con: - La formación del complejo ES - Con su disociación - Con ambos procesos
HBDORES HBCÓ EZMÁTCA TEMA Moléculas que disminuyen la V de reacción enzimática Afectan a la cinética de reacción al interferir con: - La formación del complejo ES - Con su disociación - Con ambos procesos
[ A ], [ B ]...: concentraciones molares de los reactivos en un momento dado.
![[ A ], [ B ]...: concentraciones molares de los reactivos en un momento dado. [ A ], [ B ]...: concentraciones molares de los reactivos en un momento dado.](/thumbs/49/25484895.jpg) VELOCIDAD MEDIA DE UNA REACCIÓN aa + b B c C + d D [ A] [ B] [ C] [ D] Vmedia = = = = a b c d A Velocidad de disminución de los reactivos: a Velocidad de aumento de los productos: ECUACIÓN DE VELOCIDAD
VELOCIDAD MEDIA DE UNA REACCIÓN aa + b B c C + d D [ A] [ B] [ C] [ D] Vmedia = = = = a b c d A Velocidad de disminución de los reactivos: a Velocidad de aumento de los productos: ECUACIÓN DE VELOCIDAD
Capítulo 12 REGULACIÓN DE LA EXPRESIÓN GÉNICA. Factores de Transcripción. Metilación. Procesamiento del ARN. Post-traduccional
 REGULACIÓN DE LA EXPRESIÓN GÉNICA - Mecanismos de Regulación Regulación Procariontes Eucariontes Operón Lactosa Operón Triptofano Transcripcional Procesamiento del ARN Traduccional Post-traduccional Factores
REGULACIÓN DE LA EXPRESIÓN GÉNICA - Mecanismos de Regulación Regulación Procariontes Eucariontes Operón Lactosa Operón Triptofano Transcripcional Procesamiento del ARN Traduccional Post-traduccional Factores
