Tema 1 INTRODUCCIÓN AL EMPLEO DE TÉCNICAS ESPECTROSCÓPICAS EN LA DILUCIDACIÓN DE ESTRUCTURAS ORGÁNICAS
|
|
|
- Domingo Aguilera Revuelta
- hace 5 años
- Vistas:
Transcripción
1 Tema 1 INTRODUCCIÓN AL EMPLEO DE TÉCNICAS ESPECTROSCÓPICAS EN LA DILUCIDACIÓN DE ESTRUCTURAS ORGÁNICAS 1. Usando los datos de la siguiente tabla que ilustra el efecto de la electronegatividad del heteroátomo sustituyente sobre el desplazamiento químico de protones indique: * Por definición 1 CH 3 F 4,26 ppm 2 CH 3 Cl 3,05 ppm 3 CH 3 Br 2,68 ppm 4 CH 3 I 2,16 ppm 5 CH 2 Cl 2 5,30 ppm 6 CHCl 3 7,27 ppm 7 CH 3 CCl 3 2,70 ppm 8 (CH 3 ) 4 C 0,86 ppm 9 (CH 3 ) 4 Si 0,00 ppm* a) Cómo varía el desplazamiento químico de los protones, en los compuestos 1 a 4, con la electronegatividad del halógeno? b) Cómo varía el desplazamiento químico con el número de halógenos vecinos, en los compuestos 2, 5 y 6? c) Comparando los compuestos 6 y 7, establecer cómo se modifica el corrimiento químico de un protón con la distancia de un átomo electronegativo. d) Explique por qué (CH 3 ) 4 Si absorbe a campos más altos (desplazamiento químico más bajo) que cualquier otra molécula de la Tabla. Podría imaginar una molécula cuyos protones tengan un desplazamiento químico a campos más altos que el TMS, es decir un valor negativo de 2. Cuántas señales de absorción RMN 1 H se observarían en el espectro de los siguientes compuestos? a) bromuro de t-butilo b) (CH 3 ) 3 C-CCl(CH 3 ) 2 c) 2-cloro-2-metoxipropano 3. Dadas las siguientes fórmulas moleculares determinar el índice de deficiencia de hidrógenos IDH (número de insaturacione y cierres de anillo) IDH = 2C H X + N donde C = cantidad de átomos de C; H = cantidad de átomos de H; X = cantidad de átomos de halógenos; N = cantidad de átomos de N. a. C 6 H 12 O; b. C 4 H 8 O 2 ; c. C 2 H 3 N; d. C 7 H 8 O; e. C 6 H 5 NO 2 4. Un compuesto desconocido de fórmula molecular C 5 H 11 Br tiene un espectro 1 H RMN consistente en dos líneas, una a 1,01 ppm (integral relativa 4,5) y la otra a ppm (integral relativa 1). Proponga la estructura de ese compuesto. 1
2 5. Proponer la estructura de los compuestos que responde a los siguientes datos: a) Un compuesto C 7 H 15 Cl tiene dos señales RMN 1 H a 1,08 y 1,59 con integración relativa 3:2, respectivamente. b) Un compuesto C 5 H 9 Cl 3 tiene tres señales RMN 1 H a 1,99; 4,31 y 6,55 con integración relativa 6:2:1, respectivamente. 6. Prediga el espectro 1 H RMN de CH 3 CHCl 2, analizando el modelo de multiplicidad para una serie equivalente de protones a en presencia de tres protones equivalentes adjuntos b. Incluya un análisis de la intensidad relativa de cada línea del modelo de partición. Asuma que las constantes de acoplamiento son aproximadamente las mismas que las encontradas en el bromuro de etilo. 7. Predecir el espectro 1 H RMN de los siguientes compuestos: a) (CH 3 ) 2 CH-I b) Cl 2 CH-CH 2 -Cl c) Cl-CH 2 -C(CH 3 ) 2 Cl d) CH 3 -O-CH 2 -CH 2 -CH 2 -O-CH 3 8. Proponer la estructura para los siguientes compuestos: a) C 4 H 8 Cl 2, 1 H RMN: (3H, d, J= 7,5 Hz); 2,15 (2H, c, J=7,5 Hz); 3,72 ( 2H, t, J=7,5 Hz); 4,27 (1H, sexteto, J=7,5 Hz). b) C 3 H 7 Br, 1 H RMN: 1,03 (3H, t, J=7 Hz); 1,88 (2H, sexteto, J=7 Hz); 3,40 (2H, t, J=7Hz). c) C 2 H 3 Cl 3, 1 H RMN: 3,98 (2H, d, J=7 Hz); 5,87 (1H, t, J=7 Hz). d) C 5 H 8 Br 4, 1 H RMN: 3,36 (s, la única línea del espectro). 9. El siguiente diagrama corresponde a la simulación de un espectro de 1 H RMN de un compuesto de fórmula molecular C 10 H 12 O 2. a) Ignorando la señal del TMS a δ = 0, cuántos grupos de señales hay en el espectro? b) Cuál es la multiplicidad (s, d, t, c, q) de la señal más apantallada del espectro? c) Qué unidad estructural corresponde al singulete a δ = 3.8 ppm? A) CH 3 C=O B) CH 2 C) O H D) O CH 3 E) C CH 3 F) C=C H 2
3 d) A partir de la separación de las líneas (J), qué señal está acoplada con el cuarteto a δ = 2.9 ppm? A) δ = 1.2 ppm B) δ = 3.8 ppm C) δ = 6.9 ppm D) δ = 7.9 ppm e) Utilizando el trazo de integración y la fórmula molecular, asigne un número entero de protones a cada una de las señales que se indican a continuación: 7.9 ppm; 6.9 ppm; 3.8 ppm; 2.9 ppm; 1.2 ppm g) Proponer una estructura para el compuesto. 10. Imagina que en tu mesada de laboratorio existen dos frascos rotulados como isómeros C 4 H 9 Br que contienen una sustancia líquida incolora. El espectro de 1 H RMN del compuesto A se presenta como un singulete a 1,63, y el espectro 1 H RMN del compuesto B se diagrama a continuación. Qué estructura esperaría para A y B? Espectro B Dos isómeros de un compuesto de fórmula molecular C 3 H 5 OCl, presentan en sus espectros de 1 H RMN tres señales: un singulete que integra para tres hidrógenos entre 3,5 y 4 ppm y sendos dobletes que integran cada uno para un hidrógeno entre 5 y 6,5 ppm. Al amplificar esta zona se pudo observar que para isómero A la constante de acoplamiento era de 7,0 Hz, mientras que para el isómero B era de 13,1 Hz. Proponer la estructura de ambos compuestos. 12. Un compuesto de fórmula molecular C 5 H 10 O presenta el siguiente espectro de 1 H RMN: 3
4 Mientras que otro de formula molecular C 7 H 14 O con propiedades fisicoquímicas muy similares responde al espectro: Proponer la estructura de ambos compuestos carbonílicos y dar una explicación de por qué en el segundo caso las señales a 1,3 ppm y 1,58 ppm se observan tan distorsionadas. 13. Proponer la estructura de una molécula oxigenada que posee cuatro átomos de carbono, que presenta en su espectro IR una notable banda de estiramiento -OH (3339 cm -1 ) y responde al siguiente espectro de 1 H RMN: 14. En qué solución el protón del grupo hidroxilo de etanol se presenta como un triplete? A) Etanol absoluto; B) Etanol en CDCl 3. Fundamenta tu respuesta. 15. Inequívocamente, los siguientes espectros de 1 H RMN corresponden a dos aldehídos como lo indica la presencia de los singuletes que se observan en zonas de campos bajos (alrededor de 10 ppm). Esto se confirma puesto que en los dos espectros IR se detectan bandas en la zona de cm -1 (estiramiento C-H de grupo H-C=O) y los típicos estiramientos C=O en la zona de 1700 cm -1. Además uno de ellos posee anillo aromático con un característico patrón de sustitución en posición para, mientras que el otro es un compuesto alifático. Proponer la estructura para cada uno de los aldehídos y asignar las señales presentes en cada uno de los espectros. 4
5 16. A diferencia de la señal de los aldehídos los hidrógenos ácidos no presentan picos agudos sino que, si se observan, se ven ensanchados y aún más desprotegidos (más de 11 ppm). Proponer las estructuras de los dos ácidos carboxílicos que se corresponden con los siguientes espectros de 1 H RMN sabiendo que sus PM son 74 y 178 respectivamente. 5
6 17. Asignar la estructura de un compuesto con propiedades ácidas cuya fórmula molecular es C 10 H 14 O (PM 150) y su espectro de 1 H RMN se grafica a continuación. El compuesto en cuestión presenta una ancha banda en la región del espectro IR comprendida entre los cm Se tienen tres viales sin etiqueta, cada uno de ellos contiene un isómero del triclorobenceno (1,2,3-triclorobenceno; 1,2,4-triclorobenceno y 1,3,5-triclorobenceno). Con el fin de identificar correctamente cada compuesto y poner la etiqueta correcta a cada vial, has registrado sus espectros de 13 C RMN. Qué espectro corresponde a cada compuesto si el espectro A presenta dos señales entre δ125 y 140 ppm, el B seis señales entre δ125 y 140 ppm y el C cuatro señales entre δ125 y 140 ppm? 19. Se tienen cuatro viales sin etiqueta, cada uno de ellos contiene un isómero del dicloropropano (1,1-dicloropropano; 2,2-dicloropropano; 1,2-dicloropropano y 1,3- dicloropropano). Con el fin de identificar correctamente cada compuesto y poner la etiqueta correcta a cada vial, has registrado sus espectros de 13 C y 1 H RMN. Qué espectro corresponde a cada compuesto si: a) El espectro de 13 C RMN A presenta tres señales entre δ0 y 60 ppm y el de 1 H RMN A tres señales entre δ0 y 5 ppm, siendo la señal más desapantallada un sexteto. b) El espectro de 13 C RMN B presenta dos señales entre δ0 y 70 ppm y el de 1 H RMN B un singulete a δ1.2 ppm. c) El espectro de 13 C RMN C presenta dos señales entre δ0 y 70 ppm y el de 1 H RMN C dos señales entre δ0 y 10 ppm, siendo la señal más desapantallada un triplete. d) El espectro de 13 C RMN D presenta tres señales entre δ0 y 70 ppm y el de 1 H RMN D tres señales entre δ0 y 10 ppm, siendo la señal más desapantallada un triplete. 6
7 20. El siguiente es el espectro de 13 C RMN, DEPT90 y DEPT135 de 2-metilciclopentanona. Asigna cada uno de los picos. 21. Los modernos espectrómetros de masas de alta resolución son capaces de distinguir iones que difieren tan solo en unas pocas milésimas de unidades de masa. Por lo tanto, se puede determinar la masa exacta de cualquier ión molecular o fragmento iónico. Esto es así tanto que las principales editoriales están aceptando las mediciones de HRMS (espectrometría de masa de alta resolución) para reemplazar los datos que se obtienen del análisis elemental. Compuestos con las siguientes fórmulas moleculares: C 7 H 14, C 6 H 10 O, C 5 H 6 O 2 y C 5 H 10 N 2 poseen la misma masa nominal, es decir, el mismo número entero redondeado, y por lo tanto los cuatro deberían presentar un ion molecular a m/z 98. Sin embargo si calculamos las masas atómicas de los elementos a partir de las masas exactas de sus isótopos naturales es factible distinguirlos y aproximarse a los valores experimentales que se obtienen por HRMS. Calcular el PM de los diferentes compuestos haciendo uso de los valores de masa tabulados. 1 H: 1, C: 12, N: 14, O: 15, S: 31, Cl: 34, Cl: 36, Br: 78, Br: 80,9163 7
8 22. Aplicando las reglas de fragmentación formula los cuatro cationes radicales que debieran dar origen a los picos de mayor abundancia en el EM del siguiente compuesto: 6-metil-1-fenilheptan-3-ona. 23. El ión molecular mostrado en la figura siguiente al fragmentarse rinde un pico muy intenso de m/z 70. Plantear el mecanismo de fragmentación por medio del cual se justifica su aparición. 24. El siguiente es el espectro de masas del 2-metilhexano. Representa las posibles estructuras delos fragmentos que dan lugar a los picos de m/z= 85,57 y Plantea la estructura del compuesto aromático que dio origen al siguiente espectro de masas. 8
9 26. Indica cuál de los siguientes espectros de masa corresponde a heptano y cuál a 2,2,3- trimetilbutano. Justificar la respuesta. 27. El siguiente es el espectro de masas de un compuesto monohalogenado. Formular su estructura. 23. Cuál de las siguientes moléculas dio origen espectro de masas que se ilustra a continuación? Asignar al menos tres picos, proponiendo las rutas de fragmentación adecuadas. 9
10 24. Cuál de los siguientes espectros corresponde a 1-pentanol y cuál a acetato de etilo? Asignar al menos dos picos proponiendo las rutas de fragmentación adecuadas para cada uno de ellos. 10
11 EJERCICIOS COMPLEMENTARIOS 1. Cuando 3-bromopropeno se deja reaccionar con HBr en presencia de peróxidos se forma un compuesto A que presenta el siguiente espectro RMN 1 H: 3,60 (4H, t, J=6 Hz); 1,38 (2H, quinteto, J=6 Hz). a) Teniendo en cuenta la reacción, qué estructura esperarías para el producto A? b) Utiliza los datos del espectro 1 H RMN para confirmar o refutar tu hipótesis. 2. Un hidrocarburo insaturado de fórmula molecular C 8 H 14 presenta el siguiente espectro de 1 H RMN. La molécula presenta un plano de simetría. Proponer la estructura para el mismo. 3. Los siguientes espectros de 1 H RMN corresponden a un par compuestos saponificables que como característica más notable de sus espectros IR presentan una banda en la zona de 1740 cm -1 atribuible a estiramientos C=O. Proponer la estructura de ambos compuestos sabiendo que sus fórmulas moleculares son C 4 H 8 O 2 y C 5 H 10 O 2. 11
12 4. Un compuesto carbonílico (banda a 1720 cm -1 en el espectro IR correspondiente a estiramiento C=O, probablemente de cetona), de fórmula molecular C 8 H 14 O (PM 126) presenta el siguiente espectro de 1 H RMN. Proponer una estructura que justifique la aparición de cada una de sus señales. 5. El siguiente es el espectro de un derivado hidroxilado en el anillo aromático de ácido cinámico, realizado en un espectrómetro Bruker operado a 400 MHz, utilizando CDCl 3 como disolvente y una gota de D 2 O. Determina la posición de hidroxilación en base a la asignación de las señales de los hidrógenos aromáticos. 12
13 6. Podrías indicar cuál de los espectros de 13 C RMN que se muestran a continuación corresponde al aminoácido leucina y cual a isoleucina? Justifica tu respuesta. 13
14 7. En la representación del espectro de 13 C RMN y DEPT135 (Distortionless Enhancement by Polarisation Transfer) del monoterpeno limoneno indica qué señales corresponden a carbonos cuaternarios, CH, CH 2 y cuáles a CH 3. 14
15 8. Haciendo uso de los espectros bidimensionales COSY (Correlated Spectroscopy) y HETCOR (Heteronuclear Correlated spectroscopy) asigna todas las señales de 1 H y 13 C RMN del compuesto 2-butenoato de etilo. 1 H RMN 13 C RMN 15
16 COSY HETCOR 16
Tema 1: INTRODUCCIÓN AL EMPLEO DE TÉCNICAS ESPECTROSCÓPICAS PARA LA DILUCIDACIÓN DE ESTRUCTURAS ORGÁNICAS.
 Tema 1: INTRODUCCIÓN AL EMPLEO DE TÉCNICAS ESPECTROSCÓPICAS PARA LA DILUCIDACIÓN DE ESTRUCTURAS ORGÁNICAS. 1. Usando los datos de la siguiente tabla que ilustra el efecto de la electronegatividad del heteroátomo
Tema 1: INTRODUCCIÓN AL EMPLEO DE TÉCNICAS ESPECTROSCÓPICAS PARA LA DILUCIDACIÓN DE ESTRUCTURAS ORGÁNICAS. 1. Usando los datos de la siguiente tabla que ilustra el efecto de la electronegatividad del heteroátomo
Problemas. Módulo 2. Espectroscopía de IR y RMN
 Problemas. Módulo 2. Espectroscopía de IR y RMN 1. Dadas las estructuras de cinco isómeros de fórmula molecular C 4 H 8 Oy los espectros IR identificados como A, B, C, D y E, indique de manera razonada
Problemas. Módulo 2. Espectroscopía de IR y RMN 1. Dadas las estructuras de cinco isómeros de fórmula molecular C 4 H 8 Oy los espectros IR identificados como A, B, C, D y E, indique de manera razonada
ESPECTROSCOPÍA EJEMPLOS DE ELUCIDACION ESTRUCTURAL DE COMPUESTOS. Elucidación estructural: Ejemplo 1 Dados los siguientes espectros:
 ESPECTROSCOPÍA EJEMPLOS DE ELUCIDACION ESTRUCTURAL DE COMPUESTOS Elucidación estructural: Ejemplo 1 Dados los siguientes espectros: 1) Empezaremos por encontrar la formula molecular, pues no la tenemos.
ESPECTROSCOPÍA EJEMPLOS DE ELUCIDACION ESTRUCTURAL DE COMPUESTOS Elucidación estructural: Ejemplo 1 Dados los siguientes espectros: 1) Empezaremos por encontrar la formula molecular, pues no la tenemos.
1. Responder a las siguientes cuestiones: a) Completar el siguiente esquema de síntesis explicando las reacciones que han tenido lugar (1 punto): N H
 MATERIAL DIDÁTI AUTRIZAD: L E PERMITE LA UTILIZAIÓN DE L D TEXT IGUIENTE: GARÍA FRAILE, A.; TE VILAR, E.: Análisis rgánico Editorial UNED. 1991. IBN: 84-362-2804-9. PRET, E.; BÜLMANN, P.; AFFLTER,.; ERRERA,
MATERIAL DIDÁTI AUTRIZAD: L E PERMITE LA UTILIZAIÓN DE L D TEXT IGUIENTE: GARÍA FRAILE, A.; TE VILAR, E.: Análisis rgánico Editorial UNED. 1991. IBN: 84-362-2804-9. PRET, E.; BÜLMANN, P.; AFFLTER,.; ERRERA,
MATERIAL DIDÁCTICO AUTORIZADO:
 MATERIAL DIDÁCTICO AUTORIZADO: SOLO SE PERMITE LA UTILIZACIÓN DE LOS DOS TEXTOS SIGUIENTES: GARCÍA FRAILE, A.; TESO VILAR, E.: Análisis Orgánico Editorial UNED. 1991. ISBN: 84-362-2804-9. PRETSCH, E.;
MATERIAL DIDÁCTICO AUTORIZADO: SOLO SE PERMITE LA UTILIZACIÓN DE LOS DOS TEXTOS SIGUIENTES: GARCÍA FRAILE, A.; TESO VILAR, E.: Análisis Orgánico Editorial UNED. 1991. ISBN: 84-362-2804-9. PRETSCH, E.;
Utilización de espectros de RMN para la deducción estructural de la Hidrobenzoína (1ª Parte)
 Utilización de espectros de RMN para la deducción estructural de la Hidrobenzoína (1ª Parte) Título: Utilización de espectros de RMN para la deducción estructural de la Hidrobenzoína (1ª Parte). Target:
Utilización de espectros de RMN para la deducción estructural de la Hidrobenzoína (1ª Parte) Título: Utilización de espectros de RMN para la deducción estructural de la Hidrobenzoína (1ª Parte). Target:
Resonancia Magnética Nuclear
 Clase 4 152.952 147.290 123.188 117.525 114.209 113.216 76.850 55.678 48.146 41.562 40.012 33.361 32.113 23.659 20.654 19.816 19.720 190 180 170 160 150 140 130 120 110 100 90 80 70 60 50 40 30 20 10 ppm
Clase 4 152.952 147.290 123.188 117.525 114.209 113.216 76.850 55.678 48.146 41.562 40.012 33.361 32.113 23.659 20.654 19.816 19.720 190 180 170 160 150 140 130 120 110 100 90 80 70 60 50 40 30 20 10 ppm
Espectrometría de masas
 Espectrometría de masas Información que puede obtenerse La masa molecular La fórmula molecular Algunas características estructurales del compuesto Espectrómetro de masas básico Técnica de Impacto de electrones
Espectrometría de masas Información que puede obtenerse La masa molecular La fórmula molecular Algunas características estructurales del compuesto Espectrómetro de masas básico Técnica de Impacto de electrones
PRÁCTICA DE ESPECTROSCOPIA INFRARROJA
 PRÁCTICA DE ESPECTROSCOPIA INFRARROJA PREPARACIÓN DE MUESTRAS Tu profesor te enseñará el manejo del equipo de infrarrojo y las técnicas de preparación de muestra: disolución, película, pastilla, y suspensión.
PRÁCTICA DE ESPECTROSCOPIA INFRARROJA PREPARACIÓN DE MUESTRAS Tu profesor te enseñará el manejo del equipo de infrarrojo y las técnicas de preparación de muestra: disolución, película, pastilla, y suspensión.
QUÍMICA ORGÁNICA SERIE DE EJERCICIOS Nº3 HALUROS DE ALQUILO,MÉTODOS DE ESTUDIO MOLÉCULAS, COMPUESTOS AROMÁTICOS
 QUÍMICA ORGÁNICA SERIE DE EJERCICIOS Nº3 HALUROS DE ALQUILO,MÉTODOS DE ESTUDIO MOLÉCULAS, COMPUESTOS AROMÁTICOS 1. Considerando que la reacción de 1-yodo-2-metilbutano cn CN - es de tipo SN2, indicar cómo
QUÍMICA ORGÁNICA SERIE DE EJERCICIOS Nº3 HALUROS DE ALQUILO,MÉTODOS DE ESTUDIO MOLÉCULAS, COMPUESTOS AROMÁTICOS 1. Considerando que la reacción de 1-yodo-2-metilbutano cn CN - es de tipo SN2, indicar cómo
QUÍMICA ORGÁNICA I (Parcial 1º)
 QUÍMICA ORGÁNICA I (Parcial 1º) 19-12-2013 Alumn@: DNI: 1 2 3 4 5 6 7 total calificación 1) Añadir los componentes que faltan (materiales de partida, reactivos o productos) de las siguientes reacciones:
QUÍMICA ORGÁNICA I (Parcial 1º) 19-12-2013 Alumn@: DNI: 1 2 3 4 5 6 7 total calificación 1) Añadir los componentes que faltan (materiales de partida, reactivos o productos) de las siguientes reacciones:
ESPECTROSCOPÍA DE RESONANCIA MAGNÉTICA NUCLEAR DE PROTONES
 ESPETROSOPÍA DE RESONANIA MAGNÉTIA NULEAR DE PROTONES La resonancia magnética nuclear es posible porque los núcleos de ciertos átomos, aquellos que tienen número de espín diferente de cero, (I ) se comportan
ESPETROSOPÍA DE RESONANIA MAGNÉTIA NULEAR DE PROTONES La resonancia magnética nuclear es posible porque los núcleos de ciertos átomos, aquellos que tienen número de espín diferente de cero, (I ) se comportan
ESPECTROSCOPIA INFRARROJA INTERPRETACIÓN BÁSICA Y TABLAS
 ESPECTROSCOPIA INFRARROJA INTERPRETACIÓN BÁSICA Y TABLAS RESONANCIA MAGNÉTICA PROTÓNICA REGLAS BÁSICAS DE INTERPRETACIÓN Y TABLAS REGLAS BÁSICAS DE INTERPRETACIÓN DE RESONANCIA MAGNÉTICA PROTÓNICA
ESPECTROSCOPIA INFRARROJA INTERPRETACIÓN BÁSICA Y TABLAS RESONANCIA MAGNÉTICA PROTÓNICA REGLAS BÁSICAS DE INTERPRETACIÓN Y TABLAS REGLAS BÁSICAS DE INTERPRETACIÓN DE RESONANCIA MAGNÉTICA PROTÓNICA
SISTEMAS PROTÓNICOS EN RESONANCIA MAGNÉTICO NUCLEAR DE 1 H. Fernando de J. Amézquita L. Diana Mendoza O. Universidad de Guanajuato
 SISTEMAS PROTÓNICOS EN RESONANCIA MAGNÉTICO NUCLEAR DE 1 H Fernando de J. Amézquita L. Diana Mendoza O. Universidad de Guanajuato Clasificación de los sistemas protónicos Sistema A2 Sistema AX Sistema
SISTEMAS PROTÓNICOS EN RESONANCIA MAGNÉTICO NUCLEAR DE 1 H Fernando de J. Amézquita L. Diana Mendoza O. Universidad de Guanajuato Clasificación de los sistemas protónicos Sistema A2 Sistema AX Sistema
TEMA 2: Resonancia Magnética Nuclear RMN-1H y 13C Fundamentos
 Fundamentos La Resonancia Magnética Nuclear (RMN) es la técnica que mayor información estructural proporciona. Ello se debe a que se observan los núcleos de los átomos y se puede conocer la influencia
Fundamentos La Resonancia Magnética Nuclear (RMN) es la técnica que mayor información estructural proporciona. Ello se debe a que se observan los núcleos de los átomos y se puede conocer la influencia
CALCULO DEL INDICE DE DEFICIENCIA DE HIDRÓGENOS IDH.
 Pag:1 Ya hemos visto cómo podemos averiguar la fórmula empírica y molecular de un compuesto. En este tema conoceremos varias técnicas analíticas que combinadas nos podrán ayudar a identificar la fórmula
Pag:1 Ya hemos visto cómo podemos averiguar la fórmula empírica y molecular de un compuesto. En este tema conoceremos varias técnicas analíticas que combinadas nos podrán ayudar a identificar la fórmula
VIBRACIONES CARACTERÍSTICAS DE ALGUNAS DE LAS FUNCIONES QUÍMICA-ORGÁNICAS MÁS IMPORTANTES.
 VIBRACIONES CARACTERÍSTICAS DE ALGUNAS DE LAS FUNCIONES QUÍMICA-ORGÁNICAS MÁS IMPORTANTES. ALCANOS NORMALES (LINEALES) En todos los alcanos normales o ramificados se espera encontrar solo estiramientos
VIBRACIONES CARACTERÍSTICAS DE ALGUNAS DE LAS FUNCIONES QUÍMICA-ORGÁNICAS MÁS IMPORTANTES. ALCANOS NORMALES (LINEALES) En todos los alcanos normales o ramificados se espera encontrar solo estiramientos
Tema 11: Química Orgánica
 M.P. Ruiz Ojeda y B. Muñoz Leoz Tema 11: Química Orgánica 1 Tema 11: Química Orgánica 1. Los alcanos tienen por fórmula general A) C n H 2n 4 B) C n H 2n 2 C) C n H 2n D) C n H 2n+2 E) C n H 2n+4 2. Los
M.P. Ruiz Ojeda y B. Muñoz Leoz Tema 11: Química Orgánica 1 Tema 11: Química Orgánica 1. Los alcanos tienen por fórmula general A) C n H 2n 4 B) C n H 2n 2 C) C n H 2n D) C n H 2n+2 E) C n H 2n+4 2. Los
EJERCICIOS DE INTERPRETACIÓN PARTE 2
 EJERCICIOS DE INTERPRETACIÓN PARTE 2 7 Ácido -Bromobutírico NMR 09 CH 3 CH 2 CH O C OH 3 1 Br 1 2 8 Feniletil Acetato NMR 14 5 O CH 2 CH 2 O C CH 3 3 2 2 9 Etil Succinato NMR 18 O O CH 3 CH 2 O C CH 2
EJERCICIOS DE INTERPRETACIÓN PARTE 2 7 Ácido -Bromobutírico NMR 09 CH 3 CH 2 CH O C OH 3 1 Br 1 2 8 Feniletil Acetato NMR 14 5 O CH 2 CH 2 O C CH 3 3 2 2 9 Etil Succinato NMR 18 O O CH 3 CH 2 O C CH 2
CALCULO DEL INDICE DE DEFICIENCIA DE HIDRÓGENOS IDH.
 Pag:1 CALCULO DEL INDICE DE DEFICIENCIA DE HIDRÓGENOS IDH. En química orgánica, el índice de deficiencia de hidrógeno (IDH) es utilizado para ayudar a dibujar estructuras químicas. La fórmula permite determinar
Pag:1 CALCULO DEL INDICE DE DEFICIENCIA DE HIDRÓGENOS IDH. En química orgánica, el índice de deficiencia de hidrógeno (IDH) es utilizado para ayudar a dibujar estructuras químicas. La fórmula permite determinar
Desplazamiento Químico. Dr. Jorge A. Palermo
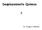 Desplazamiento Químico δ Dr. Jorge A. Palermo ν 0 = γ B 0 / 2π ECUACIÓN DE LARMOR E aumenta con B 0 Núcleo 1 2.35 Tesla 100 Mz 17.63 Tesla 750 Mz ν 0 aumenta con B 0 2 13 C 31 P 15.35 Mz 25.1 Mz 40.5 Mz
Desplazamiento Químico δ Dr. Jorge A. Palermo ν 0 = γ B 0 / 2π ECUACIÓN DE LARMOR E aumenta con B 0 Núcleo 1 2.35 Tesla 100 Mz 17.63 Tesla 750 Mz ν 0 aumenta con B 0 2 13 C 31 P 15.35 Mz 25.1 Mz 40.5 Mz
TALLER DE ESPECTROSCOPIA
 TALLER DE ESPECTROSCOPIA RESONANCIA MAGNÉTICA PROTONICA OBJETIVOS a) Que el alumno reciba la una orientación teórica básica sobre la técnica analítica denominada Resonancia Magnética Protonica b) El alumno
TALLER DE ESPECTROSCOPIA RESONANCIA MAGNÉTICA PROTONICA OBJETIVOS a) Que el alumno reciba la una orientación teórica básica sobre la técnica analítica denominada Resonancia Magnética Protonica b) El alumno
Espectrometría de masas. Complemento
 Espectrometría de masas Complemento Alcanos Se observan los iones moleculares, aunque con baja intensidad El patrónde fragmentación presenta picos que difieren en 14 unidades de masa (pérdida de CH 2
Espectrometría de masas Complemento Alcanos Se observan los iones moleculares, aunque con baja intensidad El patrónde fragmentación presenta picos que difieren en 14 unidades de masa (pérdida de CH 2
DETERMINACIÓN ESTRUCTURAL (Teoría) CURSO , GRUP A 9 de febrero Apellidos... Nombre...
 DETERMINAIÓN ESTRUTURAL (Teoría) URS 2003-2004, GRUP A 9 de febrero 2004 Apellidos... Nombre... 1.- Que diferencias espera encontrar entre el 3 - y el 3 -D. a) en sus espectros de masas. El ión molecular
DETERMINAIÓN ESTRUTURAL (Teoría) URS 2003-2004, GRUP A 9 de febrero 2004 Apellidos... Nombre... 1.- Que diferencias espera encontrar entre el 3 - y el 3 -D. a) en sus espectros de masas. El ión molecular
SANTIAGO V. LUIS C.U. Química Orgánica U.J.I. Despacho TC1424DD, 4º piso Dpto. Q. Inorgánica y Orgánica
 SANTIAGO V. LUIS C.U. Química Orgánica U.J.I. Despacho TC1424DD, 4º piso Dpto. Q. Inorgánica y Orgánica Tutorías: Martes, Miércoles, Jueves: 10:00-11:00 1 ELUCIDACIÓN ESTRUCTURAL EN COMPUESTOS ORGÁNICOS
SANTIAGO V. LUIS C.U. Química Orgánica U.J.I. Despacho TC1424DD, 4º piso Dpto. Q. Inorgánica y Orgánica Tutorías: Martes, Miércoles, Jueves: 10:00-11:00 1 ELUCIDACIÓN ESTRUCTURAL EN COMPUESTOS ORGÁNICOS
Información IR EM RMN UV DC
 Técnicas de determinación estructural Información IR EM RMN UV DC Fórmula molecular Grupos funcionales - XXX X - - XXX X XX X - Conectividad X X XXX X - Geometría/ - - XXX - X estereoquímica Quiralidad
Técnicas de determinación estructural Información IR EM RMN UV DC Fórmula molecular Grupos funcionales - XXX X - - XXX X XX X - Conectividad X X XXX X - Geometría/ - - XXX - X estereoquímica Quiralidad
FACTORES QUE AFECTAN AL DESPLAZAMIENTO QUIMICO (δ) EN RMN DE CARBONO-13
 Elucidación estructural: Resonancia Magnética Nuclear (desplazamiento de 13 C) FACTORES QUE AFECTAN AL DESPLAZAMIENTO QUIMICO (δ) EN RMN DE CARBONO-13 Los mismos factores que afectan al desplazamiento
Elucidación estructural: Resonancia Magnética Nuclear (desplazamiento de 13 C) FACTORES QUE AFECTAN AL DESPLAZAMIENTO QUIMICO (δ) EN RMN DE CARBONO-13 Los mismos factores que afectan al desplazamiento
clubdelquimico.blogspot.com
 clubdelquimico.blogspot.com Dadas las fórmulas siguientes: CH3OH, CH3CH2COOH, CH3COOCH3 y CH3CONH2 a. Diga cuál es el nombre del grupo funcional presente en cada una de las moléculas y nombre todos los
clubdelquimico.blogspot.com Dadas las fórmulas siguientes: CH3OH, CH3CH2COOH, CH3COOCH3 y CH3CONH2 a. Diga cuál es el nombre del grupo funcional presente en cada una de las moléculas y nombre todos los
ESPECTROMETRIA DE MASA
 ESPECTRMETRIA DE MASA 1.-Un compuesto de formula molecular C 10 H 14 tiene el siguiente espectro de masa a 70 ev. Proponga una estructura que justifique con ecuaciones apropiadas las dos señales intensas
ESPECTRMETRIA DE MASA 1.-Un compuesto de formula molecular C 10 H 14 tiene el siguiente espectro de masa a 70 ev. Proponga una estructura que justifique con ecuaciones apropiadas las dos señales intensas
Elucidación estructural: Resolución de problemas
 Objetivos: Elucidación estructural: Resolución de problemas Composición: átomos presentes y su proporción en la molécula, lo que se traduce en la obtención de una formula molecular. Composición elemental
Objetivos: Elucidación estructural: Resolución de problemas Composición: átomos presentes y su proporción en la molécula, lo que se traduce en la obtención de una formula molecular. Composición elemental
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2018 QUÍMICA TEMA 9: ORGÁNICA
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 018 QUÍMICA TEMA 9: ORGÁNICA Junio, Ejercicio 4, Opción A Reserva 1, Ejercicio 4, Opción A Reserva 1, Ejercicio 4, Opción B Reserva, Ejercicio 4, Opción A Reserva,
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 018 QUÍMICA TEMA 9: ORGÁNICA Junio, Ejercicio 4, Opción A Reserva 1, Ejercicio 4, Opción A Reserva 1, Ejercicio 4, Opción B Reserva, Ejercicio 4, Opción A Reserva,
Resonancia Magnética Nuclear
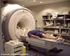 Resonancia Magnética Nuclear Por qué algunas señales aparecen como señales múltiples (multipletes)? Dos átomos que se encuentren contiguos interaccionan modificándose mutuamente. La forma de la señal depende
Resonancia Magnética Nuclear Por qué algunas señales aparecen como señales múltiples (multipletes)? Dos átomos que se encuentren contiguos interaccionan modificándose mutuamente. La forma de la señal depende
Tema 11: Química Orgánica
 Tema 11: Química Orgánica 1.Los alcanos tienen por formula general A) C n H 2n 4 B) C n H 2n 2 C) C n H 2n D) C n H 2n+2 E) C n H 2n+4 2.Los alquenos tienen por formula general A) C n H 2n 4 B) C n H 2n
Tema 11: Química Orgánica 1.Los alcanos tienen por formula general A) C n H 2n 4 B) C n H 2n 2 C) C n H 2n D) C n H 2n+2 E) C n H 2n+4 2.Los alquenos tienen por formula general A) C n H 2n 4 B) C n H 2n
Apellidos... Nombre. 1. Indique el número de señales y la multiplicidad que presentarán los compuestos siguientes en 1 H-RMN. Justificar.
 DETERMINACIN ESTRUCTURAL (5 de julio de 2005) Grupo A. TIP A Apellidos.... Nombre 1. Indique el número de señales y la multiplicidad que presentarán los compuestos siguientes en 1 H-RMN. Justificar. CH3
DETERMINACIN ESTRUCTURAL (5 de julio de 2005) Grupo A. TIP A Apellidos.... Nombre 1. Indique el número de señales y la multiplicidad que presentarán los compuestos siguientes en 1 H-RMN. Justificar. CH3
Asignaturas antecedentes y subsecuentes
 PROGRAMA DE ESTUDIOS Elucidación de Estructuras Moleculares Área a la que pertenece: AREA DE FORMACIÓN INTEGRAL PROFESIONAL Horas teóricas: 3 Horas practicas: 4 Créditos: 10 Clave: F0232 Ninguna. Asignaturas
PROGRAMA DE ESTUDIOS Elucidación de Estructuras Moleculares Área a la que pertenece: AREA DE FORMACIÓN INTEGRAL PROFESIONAL Horas teóricas: 3 Horas practicas: 4 Créditos: 10 Clave: F0232 Ninguna. Asignaturas
TEMA 5 ESPECTROSCOPÍA
 TEMA 5 ESPECTROSCOPÍA ORIGEN DEL PROBLEMA Durante el siglo XIX, antes que existieran las técnicas analíticas actuales, el químico orgánico podía determinar la fórmula molecular de una sustancia pura a
TEMA 5 ESPECTROSCOPÍA ORIGEN DEL PROBLEMA Durante el siglo XIX, antes que existieran las técnicas analíticas actuales, el químico orgánico podía determinar la fórmula molecular de una sustancia pura a
CH C C CH2 CH = CH2 O CH C - C = CH - C. QUÍMICA 2º DE BACHILLERATO QUÍMICA ORGÁNICA
 QUÍMICA ORGÁNICA QUÍMICA º DE BACHILLERATO 1. Indica el tipo de enlace y el tipo de hibridación que presenta cada átomo de carbono en los siguientes compuestos CH C - C = CH - C N CH C C CH CH = CH II
QUÍMICA ORGÁNICA QUÍMICA º DE BACHILLERATO 1. Indica el tipo de enlace y el tipo de hibridación que presenta cada átomo de carbono en los siguientes compuestos CH C - C = CH - C N CH C C CH CH = CH II
Resumen de la clase anterior
 Grupos Funcionales Resumen de la clase anterior sp 3 sp 2 sp Elemento de baja electronegatividad Capaz de hibridar electrones Carbono Hidrógeno Hidrocarburos Alifáticos Alicíclicos Aromáticos Alcanos Alquenos
Grupos Funcionales Resumen de la clase anterior sp 3 sp 2 sp Elemento de baja electronegatividad Capaz de hibridar electrones Carbono Hidrógeno Hidrocarburos Alifáticos Alicíclicos Aromáticos Alcanos Alquenos
Tema 1 INTRODUCCIÓN AL EMPLEO DE MÉTODOS ESPECTROMÉTRICOS PARA LA DILUCIDACIÓN DE ESTRUCTURAS ORGÁNICAS
 Tema 1 INTRODUCCIÓN AL EMPLEO DE MÉTODOS ESPECTROMÉTRICOS PARA LA DILUCIDACIÓN DE ESTRUCTURAS ORGÁNICAS Introducción a la espectroscopía de Resonancia Magnética nuclear (RMN). Fundamentación e instrumentación.
Tema 1 INTRODUCCIÓN AL EMPLEO DE MÉTODOS ESPECTROMÉTRICOS PARA LA DILUCIDACIÓN DE ESTRUCTURAS ORGÁNICAS Introducción a la espectroscopía de Resonancia Magnética nuclear (RMN). Fundamentación e instrumentación.
COLEGIO SAN JOSÉ - Hijas de María Auxiliadora C/ Emilio Ferrari, 87 - Madrid Departamento de Ciencias Naturales
 TEMA 3. FORMULACIÓN ORGÁNICA EJERCICIOS 3. Grupos funcionales 1. Se dan las siguientes moléculas utilizando su fórmula semidesarrollada. Indica a qué familia pertenecen y escribe la fórmula desarrollada
TEMA 3. FORMULACIÓN ORGÁNICA EJERCICIOS 3. Grupos funcionales 1. Se dan las siguientes moléculas utilizando su fórmula semidesarrollada. Indica a qué familia pertenecen y escribe la fórmula desarrollada
Ejercicios variados resueltos
 Ejercicios variados resueltos Programa de Acceso Inclusivo, Equidad y Permanencia 1. Cuál de los siguientes compuestos es isómero del CH 3 CH 2 COOH? a) CH 3 CO CH 2 OH b) CH 3 CH 2 CHO c) CH 2 =CH COOH
Ejercicios variados resueltos Programa de Acceso Inclusivo, Equidad y Permanencia 1. Cuál de los siguientes compuestos es isómero del CH 3 CH 2 COOH? a) CH 3 CO CH 2 OH b) CH 3 CH 2 CHO c) CH 2 =CH COOH
PROBLEMAS DE SELECTIVIDAD. TEMA 7: QUÍMICA ORGÁNICA
 PROBLEMAS DE SELECTIVIDAD. TEMA 7: QUÍMICA ORGÁNICA 2015 1) Dados los compuestos CH 3 CH 2 CH 2 Br y CH 3 CH 2 CH = CH 2, indica, escribiendo la reacción correspondiente: a) El que reacciona con H 2 O/H
PROBLEMAS DE SELECTIVIDAD. TEMA 7: QUÍMICA ORGÁNICA 2015 1) Dados los compuestos CH 3 CH 2 CH 2 Br y CH 3 CH 2 CH = CH 2, indica, escribiendo la reacción correspondiente: a) El que reacciona con H 2 O/H
TEMA 3.- APLICACIÓN DE LOS MÉTODOS FÍSICOS EN LA DETERMINACIÓN DE LA ESTRUCTURA.
 TEMA 3.- APLICACIÓ DE LS MÉTDS FÍSICS E LA DETERMIACIÓ DE LA ESTRUCTURA. Proponer los datos espectroscópicos del compuesto representado Se propone este ejercicio para familiarizarse con los datos espectroscópicos
TEMA 3.- APLICACIÓ DE LS MÉTDS FÍSICS E LA DETERMIACIÓ DE LA ESTRUCTURA. Proponer los datos espectroscópicos del compuesto representado Se propone este ejercicio para familiarizarse con los datos espectroscópicos
Fernando de J. Amézquita L. Diana Mendoza O.
 Tutorial para la interpretación de espectros de RMN Fernando de J. Amézquita L. Diana Mendoza O. Universidad de Guanajuato Introducción: Hemos preparado esta presentación con el objeto de facilitarle a
Tutorial para la interpretación de espectros de RMN Fernando de J. Amézquita L. Diana Mendoza O. Universidad de Guanajuato Introducción: Hemos preparado esta presentación con el objeto de facilitarle a
Tema 1 INTRODUCCIÓN AL EMPLEO DE MÉTODOS ESPECTROMÉTRICOS PARA LA DILUCIDACIÓN DE ESTRUCTURAS ORGÁNICAS
 Tema 1 INTRODUCCIÓN AL EMPLEO DE MÉTODOS ESPECTROMÉTRICOS PARA LA DILUCIDACIÓN DE ESTRUCTURAS ORGÁNICAS Introducción a la espectroscopía de Resonancia Magnética nuclear (RMN). Fundamentación e instrumentación.
Tema 1 INTRODUCCIÓN AL EMPLEO DE MÉTODOS ESPECTROMÉTRICOS PARA LA DILUCIDACIÓN DE ESTRUCTURAS ORGÁNICAS Introducción a la espectroscopía de Resonancia Magnética nuclear (RMN). Fundamentación e instrumentación.
ANÁLISIS INSTRUMENTAL_UII_PARTE DOS. Propiedades magnéticas de cuatro importantes núcleos que tienen un número cuántico de espín de ½
 RESONANCIA MAGNÉTICA NUCLEAR ANÁLISIS INSTRUMENTAL_UII_PARTE DOS Propiedades magnéticas de cuatro importantes núcleos que tienen un número cuántico de espín de ½ Desplazamiento químico Desdoblamiento spin-
RESONANCIA MAGNÉTICA NUCLEAR ANÁLISIS INSTRUMENTAL_UII_PARTE DOS Propiedades magnéticas de cuatro importantes núcleos que tienen un número cuántico de espín de ½ Desplazamiento químico Desdoblamiento spin-
PROBLEMAS DE SELECTIVIDAD. QUÍMICA ORGÁNICA
 PROBLEMAS DE SELECTIVIDAD. QUÍMICA ORGÁNICA 2017 1) Dado el siguiente compuesto CH 3 CH 2 CHOHCH 3 a) Justifique si presenta o no isomería óptica. b) Escriba la estructura de un isómero de posición y otro
PROBLEMAS DE SELECTIVIDAD. QUÍMICA ORGÁNICA 2017 1) Dado el siguiente compuesto CH 3 CH 2 CHOHCH 3 a) Justifique si presenta o no isomería óptica. b) Escriba la estructura de un isómero de posición y otro
HIDROCARBUROS AROMÁTICOS
 HIDROCARBUROS AROMÁTICOS Los hidrocarburos aromáticos son compuestos insaturados de un tipo especial. Originalmente recibieron el nombre de aromáticos debido al aroma que algunos poseen. Sin embargo no
HIDROCARBUROS AROMÁTICOS Los hidrocarburos aromáticos son compuestos insaturados de un tipo especial. Originalmente recibieron el nombre de aromáticos debido al aroma que algunos poseen. Sin embargo no
UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUÍMICAS
 UNIVERSIDAD CENTRAL DEL ECUADR FACULTAD DE CIENCIAS QUÍMICAS ÉTERES Y EPÓXIDS Cazar Irina Lenin Lombeida 12 de Julio del 2011 QUIMICA RGANICA II TEMA: QUIMICA RGANICA FRANCIS CAREY: EJERCICIS DE ÉTERES
UNIVERSIDAD CENTRAL DEL ECUADR FACULTAD DE CIENCIAS QUÍMICAS ÉTERES Y EPÓXIDS Cazar Irina Lenin Lombeida 12 de Julio del 2011 QUIMICA RGANICA II TEMA: QUIMICA RGANICA FRANCIS CAREY: EJERCICIS DE ÉTERES
Momento angular de espín
 Momento angular de espín 14 Ene 04 Reson 1 Estado de espín de un electrón: Ŝ 2 χ(σ) = s(s + 1) 2 χ(σ) Ŝ z χ(σ) = m s χ(σ) Donde s = 1/2 y hay dos orientaciones: m s = 1/2, 1/2 Estado de espín de un núcleo:
Momento angular de espín 14 Ene 04 Reson 1 Estado de espín de un electrón: Ŝ 2 χ(σ) = s(s + 1) 2 χ(σ) Ŝ z χ(σ) = m s χ(σ) Donde s = 1/2 y hay dos orientaciones: m s = 1/2, 1/2 Estado de espín de un núcleo:
SEGUNDO DE BACHILLERATO QUÍMICA. Simple C-C sp 3. Doble C=C sp 2. Triple C C
 TEMA 10. QUÍMICA ORGÁNICA PROPIEDADES GENERALES - Solubilidad: se disuelven generalmente en otros compuestos orgánicos, como éter, cloroformo o benceno - Estabilidad: suelen descomponerse a temperaturas
TEMA 10. QUÍMICA ORGÁNICA PROPIEDADES GENERALES - Solubilidad: se disuelven generalmente en otros compuestos orgánicos, como éter, cloroformo o benceno - Estabilidad: suelen descomponerse a temperaturas
TALLER DE ESPECTROSCOPIA
 TALLER DE ESPECTROSCOPIA I. OBJETIVOS a) Conocer los principios fundamentales que rigen la interacción energía-materia (radiación electromagnética-moléculas) en uno de los métodos espectroscópicos más
TALLER DE ESPECTROSCOPIA I. OBJETIVOS a) Conocer los principios fundamentales que rigen la interacción energía-materia (radiación electromagnética-moléculas) en uno de los métodos espectroscópicos más
TEMA 7: QUÍMICA DEL CARBONO EJERCICIOS DE SELECTIVIDAD 96/97
 TEMA 7: QUÍMICA DEL CARBONO EJERCICIOS DE SELECTIVIDAD 96/97 1. Complete las siguientes reacciones e indique de qué tipo son: a) CH 3 CH=CH 2 + HBr b) CH 3 CH 2 CH 2 OH + H 2 SO 4 c) C 6 H 6 (benceno)
TEMA 7: QUÍMICA DEL CARBONO EJERCICIOS DE SELECTIVIDAD 96/97 1. Complete las siguientes reacciones e indique de qué tipo son: a) CH 3 CH=CH 2 + HBr b) CH 3 CH 2 CH 2 OH + H 2 SO 4 c) C 6 H 6 (benceno)
CARACTERISTICAS QUE PRESENTA
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MEDICAS CUM UNIDAD DIDACTICA QUIMICA, PRIMER AÑO GUIA DE ESTUDIO 2015 SEMANA 15 INTRODUCCION A LA QUIMICA ORGÀNICA Elaborado por: Isabel Fratti
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MEDICAS CUM UNIDAD DIDACTICA QUIMICA, PRIMER AÑO GUIA DE ESTUDIO 2015 SEMANA 15 INTRODUCCION A LA QUIMICA ORGÀNICA Elaborado por: Isabel Fratti
Para un resorte: E p =1/2 K (r-r 0 ) 2
 El enlace en analogía con un resorte!! Para un resorte: E p =1/2 K (r-r 0 ) 2 Cual es la energía potencial cuando r=r 0?? Que pasa con la energía potencial del resorte cuando lo estiro? Graficando la ecuación
El enlace en analogía con un resorte!! Para un resorte: E p =1/2 K (r-r 0 ) 2 Cual es la energía potencial cuando r=r 0?? Que pasa con la energía potencial del resorte cuando lo estiro? Graficando la ecuación
Química Orgánica Grupos funcionales con oxígeno o nitrógeno
 Química rgánica Grupos funcionales con oxígeno o nitrógeno IES La Magdalena. Avilés. Asturias La parte carbonada constituye el esqueleto fundamental de las moléculas orgánicas. En esta estructura básica
Química rgánica Grupos funcionales con oxígeno o nitrógeno IES La Magdalena. Avilés. Asturias La parte carbonada constituye el esqueleto fundamental de las moléculas orgánicas. En esta estructura básica
Análisis avanzado de alimentos: Problemas
 Serie 2: Resonancia magnética nuclear Problema 1 En la figura se muestra el espectro de RMN 1 H del bromoetano. a) Deduzca la potencia del equipo en el que fue realizado. b) Asigne los desplazamientos
Serie 2: Resonancia magnética nuclear Problema 1 En la figura se muestra el espectro de RMN 1 H del bromoetano. a) Deduzca la potencia del equipo en el que fue realizado. b) Asigne los desplazamientos
Espectroscopía IR Parte II. Química Orgánica III Primer Semestre 2016 Facultad de CCQQ y Farmacia USAC
 Espectroscopía IR Parte II Química Orgánica III Primer Semestre 2016 Facultad de CCQQ y Farmacia USAC Grupos funcionales que presentan absorción en la región 4000-3000 cm En esta región se encuentran las
Espectroscopía IR Parte II Química Orgánica III Primer Semestre 2016 Facultad de CCQQ y Farmacia USAC Grupos funcionales que presentan absorción en la región 4000-3000 cm En esta región se encuentran las
Espectrometría de Masa
 Espectrometría de Masa La espectrometría de masa crea partículas cargadas (iones). Luego estos iones se analizan y pueden entregar información sobre el peso molecular de la molécula y acerca de su estructura
Espectrometría de Masa La espectrometría de masa crea partículas cargadas (iones). Luego estos iones se analizan y pueden entregar información sobre el peso molecular de la molécula y acerca de su estructura
CUESTIONES DE ORGÁNICA
 CUESTIONES DE ORGÁNICA 1.- Escriba la fórmula desarrollada de cada uno de los siguientes compuestos y nombre el grupo funcional que presentan. a) CH 3 CH 2 CHO b) CH 3 CH 2 CONH 2 c) CH 3 CH 2 COOCH 2
CUESTIONES DE ORGÁNICA 1.- Escriba la fórmula desarrollada de cada uno de los siguientes compuestos y nombre el grupo funcional que presentan. a) CH 3 CH 2 CHO b) CH 3 CH 2 CONH 2 c) CH 3 CH 2 COOCH 2
Introducción Espectroscopía RMN
 Introducción Espectroscopía RMN +½ -½ +½ -½ Espín Nuclear + + +1/2 1/2 Un núcleo se comporta como un imán diminuto En ausencia de Mext: distribución al azar + + + + + Un campo o externo provoca momentos
Introducción Espectroscopía RMN +½ -½ +½ -½ Espín Nuclear + + +1/2 1/2 Un núcleo se comporta como un imán diminuto En ausencia de Mext: distribución al azar + + + + + Un campo o externo provoca momentos
Seminarios RMN. satélites de 13 C. a) fac [Mo(CO) 3 (PMe 3 ) 3 ], b) mer [Mo(CO) 3 (PMe 3 ) 3 ].
![Seminarios RMN. satélites de 13 C. a) fac [Mo(CO) 3 (PMe 3 ) 3 ], b) mer [Mo(CO) 3 (PMe 3 ) 3 ]. Seminarios RMN. satélites de 13 C. a) fac [Mo(CO) 3 (PMe 3 ) 3 ], b) mer [Mo(CO) 3 (PMe 3 ) 3 ].](/thumbs/84/89973401.jpg) Licenciatura en Química. Universidad de Alcalá 3 Seminarios RMN 1 Describe los espectros de RMN de 1 que se espera observar para a) Ge Ge, b) Si 3 Si, c) P, d) P 4 y e) Si 3 P. Desprecia los satélites
Licenciatura en Química. Universidad de Alcalá 3 Seminarios RMN 1 Describe los espectros de RMN de 1 que se espera observar para a) Ge Ge, b) Si 3 Si, c) P, d) P 4 y e) Si 3 P. Desprecia los satélites
QUÍMICA ESTRUCTURAL II. ENLACE COVALENTE.
 QUÍMICA ESTRUCTURAL II. ENLACE COVALENTE. 1. Para las siguientes especies químicas: F 2, NaCl, CsF, H 2 S, AsH 3 y SiH 4, explica razonadamente: a) Cuáles tendrán enlaces covalentes puros. b) Cuáles tendrán
QUÍMICA ESTRUCTURAL II. ENLACE COVALENTE. 1. Para las siguientes especies químicas: F 2, NaCl, CsF, H 2 S, AsH 3 y SiH 4, explica razonadamente: a) Cuáles tendrán enlaces covalentes puros. b) Cuáles tendrán
Contenidos. Características del carbono Tipos de hibridación y enlace Formulación y nomenclatura de compuestos orgánicos
 QUIMICA ORGANICA Contenidos Características del carbono Tipos de hibridación y enlace Formulación y nomenclatura de compuestos orgánicos Características del Carbono Electronegatividad Enlace covalente
QUIMICA ORGANICA Contenidos Características del carbono Tipos de hibridación y enlace Formulación y nomenclatura de compuestos orgánicos Características del Carbono Electronegatividad Enlace covalente
QUÍMICA ESTRUCTURAL I-II
 QUÍMICA ESTRUCTURAL I-II 1. Para las siguientes especies químicas: F 2, NaCl, CsF, H 2 S, AsH 3 y SiH 4, explica razonadamente: a) Cuáles tendrán enlaces covalentes puros. b) Cuáles tendrán enlaces covalentes
QUÍMICA ESTRUCTURAL I-II 1. Para las siguientes especies químicas: F 2, NaCl, CsF, H 2 S, AsH 3 y SiH 4, explica razonadamente: a) Cuáles tendrán enlaces covalentes puros. b) Cuáles tendrán enlaces covalentes
ISOMERÍA. 2. CLASIFICACIÓN Existen 2 tipos básicos de isomería: estructural y espacial.
 UD. 8 ISOMERÍA y REACCIONES ORGÁNICAS ISOMERÍA (Cuando se formula un compuesto inorgánico, se hace referencia inequívocamente a un solo compuesto, mientras que, en química orgánica no suele suceder esto.
UD. 8 ISOMERÍA y REACCIONES ORGÁNICAS ISOMERÍA (Cuando se formula un compuesto inorgánico, se hace referencia inequívocamente a un solo compuesto, mientras que, en química orgánica no suele suceder esto.
UNIVERSIDAD DE PUERTO RICO RECINTO DE RÍO PIEDRAS DEPARTAMENTO DE QUÍMICA QUÍMICA ORGÁNICA II (QUIM 3032)
 QUÍMICA RGÁNICA II (QUIM 3032) PRIMER EXAMEN PARCIAL UNIVERSIDAD DE PUERT RIC RECINT DE RÍ PIEDRAS DEPARTAMENT DE QUÍMICA 25 DE FEBRER DE 2016 SECCIÓN: NMBRE: NÚM. DE ESTUDIANTE: El examen consta de 13
QUÍMICA RGÁNICA II (QUIM 3032) PRIMER EXAMEN PARCIAL UNIVERSIDAD DE PUERT RIC RECINT DE RÍ PIEDRAS DEPARTAMENT DE QUÍMICA 25 DE FEBRER DE 2016 SECCIÓN: NMBRE: NÚM. DE ESTUDIANTE: El examen consta de 13
ORGÁNICA I. 1.- Escribir y nombrar el compuesto obtenido por reacción entre a) el ácido acético y el 2-propanol. b) cloruro de acetilo con agua.
 ORGÁNICA I 1.- Escribir y nombrar el compuesto obtenido por reacción entre a) el ácido acético y el 2-propanol. b) cloruro de acetilo con agua. 2.- Escribir y nombrar el producto principal obtenido en
ORGÁNICA I 1.- Escribir y nombrar el compuesto obtenido por reacción entre a) el ácido acético y el 2-propanol. b) cloruro de acetilo con agua. 2.- Escribir y nombrar el producto principal obtenido en
TEMA VIII: PROBLEMAS DE QUIMICA ORGANICA
 TEMA VIII: PROBLEMAS DE QUIMICA ORGANICA 1. Complete las siguientes reacciones e indique de qué tipo son: a) = + HBr b) OH + H SO c) C 6 H 6 (benceno) + HNO H SO. a) Indique los grupos funcionales presentes
TEMA VIII: PROBLEMAS DE QUIMICA ORGANICA 1. Complete las siguientes reacciones e indique de qué tipo son: a) = + HBr b) OH + H SO c) C 6 H 6 (benceno) + HNO H SO. a) Indique los grupos funcionales presentes
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 2007 QUÍMICA TEMA 9: ORGÁNICA
 PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 007 QUÍMICA TEMA 9: ORGÁNICA Junio, Ejercicio 4, Opción B Reserva 1, Ejercicio 4, Opción A Reserva, Ejercicio 4, Opción B Reserva, Ejercicio 4, Opción A Reserva
PROBLEMAS RESUELTOS SELECTIVIDAD ANDALUCÍA 007 QUÍMICA TEMA 9: ORGÁNICA Junio, Ejercicio 4, Opción B Reserva 1, Ejercicio 4, Opción A Reserva, Ejercicio 4, Opción B Reserva, Ejercicio 4, Opción A Reserva
Introducción Espectroscopía RMN
 Introducción Espectroscopía RMN +½ -½ +½ -½ Espín Nuclear + + +1/2 1/2 Un núcleo se comporta como un imán diminuto En ausencia de Mext: distribución al azar + + + + + Un campo o externo provoca momentos
Introducción Espectroscopía RMN +½ -½ +½ -½ Espín Nuclear + + +1/2 1/2 Un núcleo se comporta como un imán diminuto En ausencia de Mext: distribución al azar + + + + + Un campo o externo provoca momentos
UNIDAD 1 (P.XIII) Objetivos
 UNIDAD 1 (P.XIII) Objetivos 1. Calcule el IDH en compuestos insaturados 2. Interprete el valor de IDH y proponga compuestos que cumplan un IDH determinado. 3. Dibuje las estructuras de resonancia de compuestos
UNIDAD 1 (P.XIII) Objetivos 1. Calcule el IDH en compuestos insaturados 2. Interprete el valor de IDH y proponga compuestos que cumplan un IDH determinado. 3. Dibuje las estructuras de resonancia de compuestos
EN QUÉ CONSISTE EL FENÓMENO DE LA ISOMERÍA?
 EN QUÉ CONSISTE EL FENÓMENO DE LA ISOMERÍA? DESEMPEÑO ESPERADO: EL ESTUDIANTE ENCUENTRA ISÓMEROS ESTRUCTURALES Y GEOMÉTRICOS, DIFERENCIÁNDOLOS A PARTIR DE SUS NOMBRES IUPAC. 1. INTRODUCCIÓN El alcohol
EN QUÉ CONSISTE EL FENÓMENO DE LA ISOMERÍA? DESEMPEÑO ESPERADO: EL ESTUDIANTE ENCUENTRA ISÓMEROS ESTRUCTURALES Y GEOMÉTRICOS, DIFERENCIÁNDOLOS A PARTIR DE SUS NOMBRES IUPAC. 1. INTRODUCCIÓN El alcohol
TEMA 8. ESTUDIO DE ALGUNAS FUNCIONES ORGÁNICAS
 TEMA 8. ESTUDIO DE ALGUNAS FUNCIONES ORGÁNICAS E2A.S2010 Indique los reactivos adecuados para realizar las siguientes transformaciones: a) CH 3 CH 2 COOH CH 3 CH 2 COOCH 3 b) CH 2 =CH CH 2 Cl CH 3 CH 2
TEMA 8. ESTUDIO DE ALGUNAS FUNCIONES ORGÁNICAS E2A.S2010 Indique los reactivos adecuados para realizar las siguientes transformaciones: a) CH 3 CH 2 COOH CH 3 CH 2 COOCH 3 b) CH 2 =CH CH 2 Cl CH 3 CH 2
UNIVERSIDA CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUIMCAS CARRERA DE QUIMICA FARMACEUTICA QUIMICA ORGANICA III
 Nombre: Laura Cadena Fecha: 26 de junio del 2011 Tema: UNIVERSIDA CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUIMCAS CARRERA DE QUIMICA FARMACEUTICA QUIMICA ORGANICA III FACOTRES QUE AFECTAN LA ACIDEZ DE
Nombre: Laura Cadena Fecha: 26 de junio del 2011 Tema: UNIVERSIDA CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUIMCAS CARRERA DE QUIMICA FARMACEUTICA QUIMICA ORGANICA III FACOTRES QUE AFECTAN LA ACIDEZ DE
Temario: Temario: SEMINARIO1 hora lectiva (2 grupos) martes y jueves. SEMINARIO1 hora lectiva (2 grupos) martes y jueves
 PROFESORES PARTICIPANTES: DRA. CAROLINA JULLIAN M. DR. ERNAN PESSOA M. COORDINADOR CATEDRA 2 horas lectivas SEMINARIO1 hora lectiva (2 grupos) martes y jueves Temario: ESPECTROSCOPIA NOMENCLATURA ESTRUCTURA
PROFESORES PARTICIPANTES: DRA. CAROLINA JULLIAN M. DR. ERNAN PESSOA M. COORDINADOR CATEDRA 2 horas lectivas SEMINARIO1 hora lectiva (2 grupos) martes y jueves Temario: ESPECTROSCOPIA NOMENCLATURA ESTRUCTURA
1010 DEPARTAMENTO DE FÍSICA Y QUÍMICA 2º Bachillerato QUÍMICA
 1.- Escribir y nombrar el compuesto obtenido por reacción entre: a) el ácido acético y el propan 2 ol; b) cloruro de acetilo con agua. (a) CH 3 COOH + CH 3 CHOH CH 3 CH 3 COO CH (CH 3 ) 2 + H 2 O; etanoato
1.- Escribir y nombrar el compuesto obtenido por reacción entre: a) el ácido acético y el propan 2 ol; b) cloruro de acetilo con agua. (a) CH 3 COOH + CH 3 CHOH CH 3 CH 3 COO CH (CH 3 ) 2 + H 2 O; etanoato
Nombre: 2. Clasifique los siguientes radicales en orden decreciente de estabilidad.
 Química Orgánica II (1411). Serie 1: Repaso. Reacciones de sustitución nucleofílica alifática y de eliminación Fecha de entrega: martes 09 de septiembre de 2014. Profesor: Javier Ordóñez Hernández Nombre:
Química Orgánica II (1411). Serie 1: Repaso. Reacciones de sustitución nucleofílica alifática y de eliminación Fecha de entrega: martes 09 de septiembre de 2014. Profesor: Javier Ordóñez Hernández Nombre:
ESPECTROSCOPÍA ESPECTROMETRIA DE MASAS
 ESPECTROSCOPÍA ESPECTROMETRIA DE MASAS La espectrometría de masas es una técnica experimental que permite la medición de iones derivados de moléculas. El espectrómetro de masas es un instrumento que permite
ESPECTROSCOPÍA ESPECTROMETRIA DE MASAS La espectrometría de masas es una técnica experimental que permite la medición de iones derivados de moléculas. El espectrómetro de masas es un instrumento que permite
Módulo 3. Parte 1: Organometálicos, alcoholes, fenoles y éteres.
 QUÍMICA RGÁNICA II. GRUP B Problemas Módulo 3. Parte 1: rganometálicos, alcoholes, fenoles y éteres. 1. rdene los siguientes compuestos de menor a mayor estado de oxidación. Determine en cada caso el número
QUÍMICA RGÁNICA II. GRUP B Problemas Módulo 3. Parte 1: rganometálicos, alcoholes, fenoles y éteres. 1. rdene los siguientes compuestos de menor a mayor estado de oxidación. Determine en cada caso el número
Unidad IV: Espectrometría de Masas. Química Orgánica III Primer Semestre 2016 Facultad de CC.QQ. Y Farmacia USAC
 Unidad IV: Espectrometría de Masas Química Orgánica III Primer Semestre 2016 Facultad de CC.QQ. Y Farmacia USAC Identificación de un compuesto Orgánico Determinación de Propiedades Físicas Apariencia Olor
Unidad IV: Espectrometría de Masas Química Orgánica III Primer Semestre 2016 Facultad de CC.QQ. Y Farmacia USAC Identificación de un compuesto Orgánico Determinación de Propiedades Físicas Apariencia Olor
Síntesis y caracterización espectroscópica del cloruro de oleoilo
 www.saber.ula.ve/avancesenquimica Avances en Química, 2 (1), 15-20 (2007) Nota Técnica Síntesis y caracterización espectroscópica del cloruro de oleoilo 15 Alfonso Rivas-Gil 1, Cristóbal Lárez V. 1 y Alí
www.saber.ula.ve/avancesenquimica Avances en Química, 2 (1), 15-20 (2007) Nota Técnica Síntesis y caracterización espectroscópica del cloruro de oleoilo 15 Alfonso Rivas-Gil 1, Cristóbal Lárez V. 1 y Alí
EXAMEN UD 8. ORGÁNICA OPCIÓN A
 EXAMEN UD 8. RGÁNICA PCIÓN A 1. Una sustancia tiene C, H y. Al calentarla con óxido de cobre (II) el carbono se oxida a C 2 y el hidrógeno a agua. A partir de un gramo de sustancia se forman 0,9776 g de
EXAMEN UD 8. RGÁNICA PCIÓN A 1. Una sustancia tiene C, H y. Al calentarla con óxido de cobre (II) el carbono se oxida a C 2 y el hidrógeno a agua. A partir de un gramo de sustancia se forman 0,9776 g de
Problemas de Química Física II. 3º de Químicas. RAMAN y POLIATOMICAS
 Problemas de Química Física II. 3º de Químicas RAMAN y POLIATOMICAS 1. Las primeras frecuencias del espectro Raman del N 2 son 19.908, 27.857, 35.812, 43.762, 51.721 y 59.622 cm -1. Sabiendo que estas
Problemas de Química Física II. 3º de Químicas RAMAN y POLIATOMICAS 1. Las primeras frecuencias del espectro Raman del N 2 son 19.908, 27.857, 35.812, 43.762, 51.721 y 59.622 cm -1. Sabiendo que estas
ANÁLISIS DE ESPECTROS
 EFECTOS DE CONJUGACIÓN Y TAMAÑO DE ANILLO EN C=O ALQUENOS Y AROMÁTICOS ( ESTIRAMIENTO C=C ) O-H 3600 N-H 3400 C-H 3000 C=N = 2250 C=C = 2150 C=O 1715 C=C 1650 C-O 1100 ANÁLISIS DE ESPECTROS CONJUGACIÓN
EFECTOS DE CONJUGACIÓN Y TAMAÑO DE ANILLO EN C=O ALQUENOS Y AROMÁTICOS ( ESTIRAMIENTO C=C ) O-H 3600 N-H 3400 C-H 3000 C=N = 2250 C=C = 2150 C=O 1715 C=C 1650 C-O 1100 ANÁLISIS DE ESPECTROS CONJUGACIÓN
Química Orgánica II (1411)
 Química Orgánica II (1411) Serie 1: Repaso y reacciones de sustitución nucleofílica alifática y de eliminación en haluros de alquilo y en sustratos Con buenos grupos salientes Fecha de entrega: 01 de abril
Química Orgánica II (1411) Serie 1: Repaso y reacciones de sustitución nucleofílica alifática y de eliminación en haluros de alquilo y en sustratos Con buenos grupos salientes Fecha de entrega: 01 de abril
UNIVERSIDAD DE ANTIOQUIA FACULTAD DE QUIMICA FARMACEUTICA CURSO DE FARMACOGNOSIA Y FITOQUIMICA PROFESOR ALEJANDRO MARTINEZ M.
 1. CONVENCIONES Y TERMINOS UNIVERSIDAD DE ANTIOQUIA FACULTAD DE QUIMICA FARMACEUTICA CURSO DE FARMACOGNOSIA Y FITOQUIMICA PROFESOR ALEJANDRO MARTINEZ M. Terminación inglesa ó término Terminación en español
1. CONVENCIONES Y TERMINOS UNIVERSIDAD DE ANTIOQUIA FACULTAD DE QUIMICA FARMACEUTICA CURSO DE FARMACOGNOSIA Y FITOQUIMICA PROFESOR ALEJANDRO MARTINEZ M. Terminación inglesa ó término Terminación en español
GUÍA DE EJERCICIOS CONCEPTOS FUNDAMENTALES
 GUÍA DE EJERCICIOS CONCEPTOS FUNDAMENTALES Área Resultados de aprendizaje Identifica, conecta y analiza conceptos básicos de química para la resolución de ejercicios, desarrollando pensamiento lógico y
GUÍA DE EJERCICIOS CONCEPTOS FUNDAMENTALES Área Resultados de aprendizaje Identifica, conecta y analiza conceptos básicos de química para la resolución de ejercicios, desarrollando pensamiento lógico y
6.1 Catalizador Espectroscopia infrarrojo (transformada de Fourier)
 VI. RESULTADOS 6.1 Catalizador 6.1.1 Espectroscopia infrarrojo (transformada de Fourier) El análisis realizado mediante esta técnica se le práctico al soporte (zeolita SAPO-34) calcinado. La principal
VI. RESULTADOS 6.1 Catalizador 6.1.1 Espectroscopia infrarrojo (transformada de Fourier) El análisis realizado mediante esta técnica se le práctico al soporte (zeolita SAPO-34) calcinado. La principal
ESTRUCTURAS DE RESONANCIA
 1 ESTRUCTURAS DE RESONANCIA HIBRIDOS DE RESONANCIA CUANDO SON POSIBLES DOS O MÁS ESTRUCTURAS PARA REPRESENTAR LOS ENLACES DE UNA MOLÉCULA Y SÓLO DIFIENREN EN LA COLOCACIÓN DE LOS ELECTRONES LA MOLÉCULA
1 ESTRUCTURAS DE RESONANCIA HIBRIDOS DE RESONANCIA CUANDO SON POSIBLES DOS O MÁS ESTRUCTURAS PARA REPRESENTAR LOS ENLACES DE UNA MOLÉCULA Y SÓLO DIFIENREN EN LA COLOCACIÓN DE LOS ELECTRONES LA MOLÉCULA
Nombre: Curso: Fecha:
 GUÍA ESTUDIO Nº1 PROPIEDADES DE HIDROCARBUROS Y FUNCIONES ORGÁNICAS PROPIEDADES DE LOS HIDROCARBUROS Propiedades de alcanos Subsector Profesor Química Paulina Gómez a) Propiedades físicas: Son menos densos
GUÍA ESTUDIO Nº1 PROPIEDADES DE HIDROCARBUROS Y FUNCIONES ORGÁNICAS PROPIEDADES DE LOS HIDROCARBUROS Propiedades de alcanos Subsector Profesor Química Paulina Gómez a) Propiedades físicas: Son menos densos
Espectrometría de Masas Interpretación de Espectros. Q. Georgina Duarte Lisci Facultad de Química UNAM
 Espectrometría de Masas Interpretación de Espectros Q Georgina Duarte Lisci Facultad de Química UAM egiones de Información en el Espectro de Masas %Abundancia Información General Series de Iones Información
Espectrometría de Masas Interpretación de Espectros Q Georgina Duarte Lisci Facultad de Química UAM egiones de Información en el Espectro de Masas %Abundancia Información General Series de Iones Información
Enseñanza de la Química CARACTERIZACIÓN DE BASES DE SCHIFF DERIVADAS DE 2-AMINOFENOL, USANDO RMN 1D Y 2D
 Recibido el 6-2-2009 87 Enseñanza de la Química ARATERIZAIÓN DE BASES DE SIFF DERIVADAS DE 2-AMINOFENOL, USANDO RMN D Y 2D *a a a a Sergio Zamorano, Juan amus, Andrea Orellana, Maribel Osorio RESUMEN En
Recibido el 6-2-2009 87 Enseñanza de la Química ARATERIZAIÓN DE BASES DE SIFF DERIVADAS DE 2-AMINOFENOL, USANDO RMN D Y 2D *a a a a Sergio Zamorano, Juan amus, Andrea Orellana, Maribel Osorio RESUMEN En
INSPECCIÓN DEL ESPECTRO
 IDROCARBUROS (ABSORCIONES C- ) ALCOOLES ÁCIDOS (ABSORCIONES O- ) AMINAS (ABSORCIONES N- ) O- 3600 N- 3400 C- 3000 C=N = 2250 C=C = 2150 C=O 1715 C=C 1650 C-O 1100 INSPECCIÓN DEL ESPECTRO Regiones Típicas
IDROCARBUROS (ABSORCIONES C- ) ALCOOLES ÁCIDOS (ABSORCIONES O- ) AMINAS (ABSORCIONES N- ) O- 3600 N- 3400 C- 3000 C=N = 2250 C=C = 2150 C=O 1715 C=C 1650 C-O 1100 INSPECCIÓN DEL ESPECTRO Regiones Típicas
Química Orgánica Compuestos orgánicos y reactividad
 Química Orgánica Compuestos orgánicos y reactividad IES La Magdalena. Avilés. Asturias El hecho de que el carbono posea una electronegatividad (2,55), intermedia entre el valor máximo (3,98 para el flúor)
Química Orgánica Compuestos orgánicos y reactividad IES La Magdalena. Avilés. Asturias El hecho de que el carbono posea una electronegatividad (2,55), intermedia entre el valor máximo (3,98 para el flúor)
QUÍMICA 2º BACHILLERATO
 1.-/ Complete las siguientes reacciones e indique el tipo de reacción (Adición, eliminación o sustitución) a que corresponden: a) CH 3 CH=CH 2 + H 2 O H2SO4 b) C 6 H 6 (benceno) + HNO 3 KOH c) CH 3 CHBrCH
1.-/ Complete las siguientes reacciones e indique el tipo de reacción (Adición, eliminación o sustitución) a que corresponden: a) CH 3 CH=CH 2 + H 2 O H2SO4 b) C 6 H 6 (benceno) + HNO 3 KOH c) CH 3 CHBrCH
Grupos funcionales Series homólogas
 Grupos funcionales Series homólogas Grupo funcional: Es un átomo o grupo de átomos unidos de manera característica y que determinan, preferentemente, las propiedades del compuesto en que están presentes.
Grupos funcionales Series homólogas Grupo funcional: Es un átomo o grupo de átomos unidos de manera característica y que determinan, preferentemente, las propiedades del compuesto en que están presentes.
