ENZIMAS. Son moléculas de naturaleza proteínica que aceleran las reacciones bioquímicas.
|
|
|
- Enrique Lara Coronel
- hace 6 años
- Vistas:
Transcripción
1 ENZIMAS
2 ENZIMAS Son moléculas de naturaleza proteínica que aceleran las reacciones bioquímicas. Son catalizadores biológicos que disminuyen la energía de activación de las reacciones que catalizan, de forma que se aceleran sustancialmente la tasa de reacción.
3 QUÉ ES UN CATALIZADOR? Es una molécula inorgánica u orgánica que incrementa notablemente la velocidad de las reacciones químicas sin ser modificada o consumida en la reacción.
4 Reacción enzimática simple E+S ES EP E : enzima libre S : sustrato ES : complejo enzima-sustrato EP: complejo enzima producto P : producto E+P
5 Cinética vs termodinámica Las reacciones proceden espontáneamente si hay un descenso en la energía libre cuando la temperatura y la presión se mantienen constantes. bioquímicas, que son termodinámicamente posibles, ocurren a velocidades despreciables, es decir son cinéticamente imposibles. Muchas reacciones De aquí la necesidad de la catálisis para incrementar sus velocidades. La catálisis en las células la llevan a cabo las enzimas.
6 Cinética vs termodinámica Lo que determina si una reacción es termodinámicamente posible es el valor del cambio en energía libre (ΔG). Lo que determina si una reacción es cinéticamente posible es el valor de su energía de activación (ΔG ).
7 El cambio negativo en energía libre (ΔG), o lo que es lo mismo el valor mayor de uno de la constante de equilibrio (Keq), nos dice que la reacción procede espontáneamente de S a P.
8 Relación entre la energía libre y la constante de equilibrio o ΔG = -RT ln Keq
9
10 Las enzimas, como cualquier catalizador incrementan notablemente la velocidad de las reacciones químicas al disminuir su energía de activación sin ser modificadas o consumidas en la reacción.
11 Reacción no catalizada Reacción catalizada
12 Necesidad de la biocatálisis Por qué la gran mayoría de las reacciones en los seres vivos necesitan ser catalizadas para que ocurran a una velocidad apreciable? Porque de lo contrario estarían todas en el equilibrio. Porque así la célula puede regular en forma diferencial su velocidad, regulando la actividad de los catalizadores de cada una de ellas.
13 Ventajas de inorgánicos las enzimas sobre los catalizadores Velocidades de reacción más elevadas, son más eficientes. ( ) Condiciones de reacción más suaves, (T<100 C, Presión atmosférica, ph fisiológico) Mayor especificidad de reacción, y (sustratos, reactivos, no subproductos) Capacidad para la regulación control alostérico, modificación covalente, [enzima]
14 QUÉ TANTO ACELERAN LAS ENZIMAS LAS VELOCIDADES DE LAS REACCIONES? La reacción en que una molécula de orotidina monofosfato (ácido orotidílico) pierde un CO2 ocurre 1017 veces más rápida cuando es catalizada por la enzima orotidina monofosfato descarboxilasa que cuando no es catalizada 1017 = CIEN MIL BILLONES DE VECES MÁS RÁPIDA Ácido orotidílico Ácido uridílico (UMP)
15
16 *Ejercicio 1. Aumento de la tasa de hidrólisis La ureasa aumenta la tasa de hidrólisis de la urea a ph 8.0 y 20 C por un factor de Una cantidad de ureasa puede hidrolizar completamente una cantidad dada de urea en 5.0 min a 20 C y ph 8.0. Cuánto tardará en hidrolizarse esta misma cantidad de urea en ausencia de la enzima y bajo las mismas condiciones? 9.5 x 108 años
17 Especificidad de la catálisis enzimática La catálisis enzimática requiere: Unión específica a la proteína de las moléculas de sustrato y de moléculas reguladoras. Reactividad específica de la proteína con el (los) sustrato (s).
18 Unión específica Las moléculas que van a reaccionar, llamadas sustratos, se unen a una región en la superficie llamada sitio activo.
19 Teorías de unión específica del sustrato Existen dos teorías para explicar la unión específica Teoría de la llave y la cerradura Teoría del ajuste inducido
20 Teoría de la llave y la cerradura
21 Teoría del ajuste inducido
22
23 Cambio conformacional de la hexocinasa inducido por su sustrato
24 ENZIMAS Apoenzima: Parte proteínica. Enzima Parte no proteínica: (holoenzima) Cofactores y coenzimas Grupo prostético: unión fuerte Resaltar que es covalente Cofactores: Uno o mas iones inorgánicos. Coenzimas: Moléculas orgánica o metaloorgánicas complejas Hemoglobina
25 COFACTORES Cofactores: Uno o mas iones inorgánicos.
26
27 Coenzimas: Moléculas orgánica o metaloorgánicas complejas
28 CLASIFICACIÓN DE LAS ENZIMAS 1. Deshidrogenasas, oxidasas, peroxidasas. 2. Transaminasas, cinasas, transacetilasas, metiltransferasas, aciltransferasas, glucosiltransferasas. 3. Esterasas, fosfatasas, glicosidasas, proteasas. 4. Descarboxilasas, aldehído liasas, cetoácido liasas. 5. Racemasas, epimerasas. 6.Sintetasas.
29
30 ALCOHOL DESHIDROGENASA EC Clase: 1 (oxidorreductasa) Subclase: 1 (actúa sobre un sustrato que posee un grupo CH-OH como donador de electrones) Subsubclase: 1 (NAD+ o NADP+ es la coenzima aceptor) Orden dentro de la subsubclase: 1 (primera enzima de este grupo)
31 CARACTERÍSTICAS DE LAS ENZIMAS Estereoespecificidad: sustratos quirales, las enzimas actúan sobre sustratos L o D, pero no sobre ambos. Las enzimas son estereoespecíficas porque forman varias interacciones entre aminoácidos del centro activo y los distintos grupos del sustrato. Especificidad geométrica: las enzimas son selectivas hacia la identidad de los grupos químicos situados en los sustratos. Sitio activo vacío Sitio activo ocupado Sitio activo: lugar donde se lleva a cabo la catálisis enzimática.
32 CARACTERÍSTICAS DE LAS ENZIMAS Sitio activo: lugar donde se lleva a cabo la catálisis enzimática. Sitio de unión a sustrato: Sitios químicos capaces de unirse al sustrato. Sitio alostérico: Lugar de unión a moléculas pequeñas, cuyo efecto es un cambio en el sitio activo o en el sitio de unión a sustrato, que modulan la actividad enzimática.
33 Ejercicio 2. Requerimiento del sitio activo La carboxipeptidasa, la cual remueve residuos de aminoácidos del extremo carboxilo de sus sustratos peptídicos, es un polipéptido de 307 aminoácidos. Los dos residuos de aminoácidos catalíticos son Arg145 y Glu270. a) Si la carboxipeptidasa fuera una α hélice, Qué tan lejos estarían los residuos Arg145 y Glu270? b) Explique cómo los dos residuos de aminoácidos pueden catalizar una reacción que ocurre en un espacio de pocos Å. a) 190 Å b) El plegamiento tridimensional de la enzima hace que los aminoácidos Arg145 y Glu270 queden cerca.
34 Unidades de actividad enzimática Actividad 1 unidad internacional (U) = 1 µmol de producto formado/min 1 katal = 1 mol de producto formado/s Actividad específica U/mg de proteína katal / mg proteína
35 Reacción catalizada enzimáticamente Reversible Irreversible simplificada
36 Parámetros enzimáticos Km (constante para cada enzima) = concentración de S a la que V0 es ½ Vmax. Es una medida de la afinidad de la enzima por S. Cuanto menor es Km, mayor es la afinidad de la enzima por S. Kcat (constante para cada enzima) = número de recambio = número de moléculas de sustrato convertidas en producto por molécula de enzima y unidad de tiempo, en condiciones saturantes del sustrato. Vmax Velocidad máxima teórica = la velocidad cuando todos los centros activos están ocupados con sustrato.
37 REPRESENTACIÓN GRÁFICA DE LA ECUACIÓN DE MICHAELIS-MENTEN
38 *Ejercicio 3 Una enzima que cataliza la reacción X Y se aisló de dos especies bacterianas diferentes. Las enzimas tienen el mismo valor de Vmax, pero diferente valor de Km para el sustrato X. La enzima A tiene un valor de Km de 2.0 mm, mientras que le enzima B tiene un valor de Km de 0.5 mm. En la siguiente gráfica se presenta la cinética de la reacción a la misma concentración de ambas enzimas Qué curva corresponde a la enzima A y cual a la enzima B? Enzima B Enzima A
39 ECUACIÓN DE MICHAELIS-MENTEN
40 La Vmax se alcanza cuando todos los centros activos están ocupados con el sustrato.
41 Unidades de los parámetros cinéticos
42 Velocidad máxima (Vmax) Es la velocidad límite a la que tiende la reacción catalizada por enzimas a concentraciones saturantes del sustrato, es decir cuando toda la enzima está como ES. Vmax = kcat[e]total Su valor cambia durante el proceso de purificación porque cambia la [E]
43 Constante catalítica (kcat) Sólo puede conocerse cuando se tiene a la enzima pura y por tanto se conoce su concentración. kcat = Vmax / [E]total o kcat = Vmax / [sitios activos] Si uno de los pasos es limitante de la velocidad, kcat es la constante de velocidad de este paso. A kcat también se le conoce como número de recambio, porque indica el número máximo de ciclos catalíticos por sitio activo y por unidad de tiempo.
44
45 *Ejercicio 4. Número de recambio La anhidrasa carbónica de los eritrocitos (Mr 30,000) cataliza la hidratación de CO2 y tiene uno de los mayores números de recambio que se conocen. H2O + CO2 H2CO3 Este es un proceso importante en el transporte de CO2 de los tejidos a los pulmones. Si 10.0 µg de anhidrasa carbónica cataliza la hidratación de 0.3 g de CO2 en un minuto a 37C a Vmax. Cuál es el número de recambio (Kcat) de la anhidrasa carbónica? Expresarlo en min-1 Kcat 2.0x107 min-1
46 Constante de Michaelis Menten (Km) En todos los casos es la concentración de sustrato a la que v = Vmax / 2
47
48 Constante de especificidad (Vmax/Km o kcat/km) Indica cuál es el mejor sustrato de una enzima (aquél que tenga la mayor constante de especificidad). Indica la eficiencia catalítica de la enzima a concentraciones de sustrato por debajo de los niveles de saturación. Representa el paso de unión de la enzima y el sustrato (cualquier factor que afecte esta constante está afectando el paso de unión).
49
50 Ejercicio 5. Constante de especificidad La enzima acetilcolinesterasa tiene un valor de Km para la acetilcolina de 9.5x10-5 M y un valor de Kcat de 1.4x104 s-1, mientras que la enzima catalasa tiene un valor de Km para el H2O2 de 2.5x10-2 M y un valor de Kcat de 1.0x107 s-1 Cuál de las dos enzimas está más próxima a la perfección catalítica (más específica)?
51 CINÉTICA ENZIMÁTICA
52 Transformaciones de la ecuación de velocidad de Michaelis Menten Lineal 1/v vs 1/[S] (Dobles recíprocos o Lineweaver-Burk) Sigmoidal v versus log S (semilogarítmica)
53 ECUACIÓN DE LINEWEAVER Y BURK
54 REPRESENTACIÓN GRÁFICA DE LINEWEAVER Y BURK Forma lineal de la ecuación de Michaelis-Menten, gráfica de dobles recíprocos.
55 Gráfica sigmoidal (velocidad inicial vs log [S])
56 *Ejercicio 6. Estimación de Vmax y Km por inspección Aunque los métodos gráficos dan una determinación exacta de la Vmax y Km de una reacción catalizada por una enzima, a veces estos valores pueden estimarse rápidamente inspeccionando los valores de Vo al incrementar [S]. Estimar Vmax y Km de la reacción catalizada enzimáticamente con los siguientes datos obtenidos: Vmax = 140 μmol/ml min Km = 1 x 10-5 M [S] (M) V0 (µmol/ml min) 2.5 X X X X X X X X
57 Ejercicio 7. Relación entre la velocidad de reacción y la concentración del sustrato. Ecuación de MichaelisMenten. Determina la fracción de Vmax que podría ser obtenida a las siguientes concentraciones de sustrato: 0.5 Km, 2 Km y 10 Km. 0.5 Km 2.0 Km 10 Km V0= 0.33 Vmax V0= 0.67 Vmax V0= 0.91 Vmax
58 Respuesta 0.5 Km 2.0 Km 10 Km V0= 0.33 Vmax V0= 0.67 Vmax V0= 0.91 Vmax
59 Factores que afectan la velocidad de una reacción catalizada por enzimas Concentración de sustrato o sustratos (cofactores) Concentración de enzima Inhibidores Activadores ph Temperatura
60 Regulación de la actividad enzimática por unión a la enzima de ligandos que no son sustrato INHIBIDOR : Molécula o ion que al unirse a la enzima produce una disminución en la velocidad de la reacción catalizada. ACTIVADOR: Molécula o ion que al unirse a la enzima produce un aumento en la velocidad de la reacción catalizada.
61
62 TIPOS DE INHIBIDORES ISOSTÉRICO El inhibidor se une al mismo sitio que el sustrato (sitio activo). ALOSTÉRICO El inhibidor se une a un sitio diferente al que se une el sustrato (sitio alostérico).
63 TIPOS DE INHIBIDORES COMPETITIVO El inhibidor se une a la enzima libre interfiriendo con la unión del sustrato. INCOMPETITIVO El inhibidor se une al complejo enzima-sustrato interfiriendo con la formación de producto. MIXTO El inhibidor se une tanto a la enzima libre como al complejo enzimas sustrato, interfiriendo la unión del sustrato y la formación del producto. NO COMPETITIVO Es un tipo especial de inhibidor mixto que se une con igual afinidad a la enzima libre y al complejo enzima-sustrato.
64 INHIBICIÓN COMPETITIVA El inhibidor se une a la enzima libre interfiriendo con la unión del sustrato Su efecto se contrarresta cuando [S]. Compiten con el sustrato por su sitio de unión. Reduce la concentración de enzima libre disponible.
65 Patrones de inhibición competitiva
66 INHIBICIÓN INCOMPETITIVA El inhibidor se une al complejo enzima-sustrato interfiriendo con la formación del producto) Inhibidores cuyo efecto NO se contrarresta incrementando la concentración del sustrato.
67 Patrones de inhibición incompetitiva
68 INHIBICIÓN MIXTA El inhibidor se une tanto a la enzima libre como al complejo enzima-sustrato, por lo tanto interfiere en la unión del sustrato y en la formación del producto
69 Patrones de inhibición mixta
70 INHIBICIÓN NO COMPETITIVA Es un tipo especial de inhibidor mixto que se une con igual afinidad a la enzima libre y al complejo enzima-sustrato
71 Patrones de inhibición no competitiva
72 EFECTO DE LOS INHIBIDORES SOBRE LOS PARÁMETROS CINÉTICOS Inhibidor competitivo Km, no cambia Vmax Inhibidor mixto Km, Vmax Inhibidor incompetitivo Km, Vmax Inhibidor no competitivo No cambia Km, Vmax
73 *Ejercicio 9. Inhibidores En la siguiente tabla se incluyen las velocidades iniciales de una reacción catalizada por una enzima que sigue cinética de Michaelis-Menten, medidas en ausencia (control), y en presencia de dos inhibidores diferentes (1 y 2), ambos a una concentración de 10 mm. Se usó la misma concentración de enzima en todas las determinaciones.
74 [S] (mm) Control V0 (µmol/ml s) Inhibidor 1 Inhibidor a) Presentar en un análisis gráfico de dobles recíprocos el patrón de inhibición. b) Determinar las constantes cinéticas (Km y Vmax) de la enzima en ausencia y presencia de los inhibidores. c) Para cada inhibidor determinar el tipo de inhibición.
75
76 Efecto del ph sobre la actividad de las enzimas Cambio en la ionización de los residuos de aminoácidos implicados en la unión del sustrato. Cambio en la ionización de residuos de aminoácidos implicados en la catálisis. Cambio en la ionización de grupos del sustrato. Cambio en la ionización de residuos de aminoácidos implicados en la estabilidad de la enzima.
77
78
79 Efecto de la temperatura sobre la velocidad de las reacciones catalizadas por enzimas La temperatura afecta la constante de velocidad de una reacción química como describe la ecuación de Arrhenius.
80
81 En las reacciones catalizadas por enzimas: La velocidad aumenta con la temperatura hasta que la enzima comienza a desnaturalizarse. No existe una temperatura óptima de reacción, depende de las condiciones en que midamos la reacción, especialmente del tiempo.
82 Mecanismos de regulación enzimática Regulación de la cantidad de la enzima Regulación de la actividad de la enzima preexistente
83 Mecanismos de regulación de la cantidad de enzima Regulación transcripcional Síntesis del ARNm Maduración y vida media del ARNm Regulación traduccional Síntesis de la proteína Regulación postraduccional Degradación de la proteína
84 Mecanismos de regulación de la actividad de la enzima Regulación por moléculas o iones. Sustratos, productos, cofactores. Inhibidores, activadores, ph. Regulación por modificación química Irreversible Zimógenos Reversible Adición de un grupo químico Oxidación-reducción de cisteínas Regulación por localización intracelular Isoenzimas
85
86
87
88
89
90 Regulación de la actividad enzimática por proteólisis limitada
91 Zimógenos Formas inactivas de enzimas que son convertidas a formas activas por proteólisis en sitios específicos. En general son enzimas proteolíticas que de sintetizarse activas producirían daños a la célula. Se activan una vez fuera de la célula que las produce (enzimas digestivas, enzimas implicadas en la coagulación sanguínea) o cuando deben llevar a la muerte celular (caso de las caspasa en la apoptosis).
92
93
94 Isoenzimas Proteínas que en un organismo catalizan la misma reacción pero están codificadas por genes diferentes. Difieren en sus propiedades cinéticas. Se expresan diferencialmente en diferentes tejidos, organelos o estados fisiológicos o patológicos.
95
96 Modificación química reversible por adición de un grupo
97
98 Modificación química reversible por oxidación-reducción de cisteínas vecinas
99 Cooperatividad enzimática
100 Enzimas con cooperatividad positiva La unión del sustrato es cada vez más fácil a medida que la enzima se satura más y más. Dependencia sigmoidal de la velocidad inicial vs [S]. Enzimas con cooperatividad negativa La unión del sustrato es cada vez más difícil a medida que la enzima se satura más y más. Dependencia hiperbólica de la velocidad inicial vs [S].
101 Cooperatividad positiva entre los sitios alostéricos La unión del efector alostérico (inhibidor o activador) es cada vez más fácil a medida que la enzima se satura más y más por este ligando. Dependencia sigmoidal de la velocidad inicial vs el efector alostérico.
102 MECANISMOS DE CATÁLISIS ENZIMÁTICA OBJETIVO: Disminución de la energía de activación de la reacción catalizada con respecto a la no catalizada
103 Tipos de catálisis enzimática CATÁLISIS ÁCIDO-BASE CATÁLISIS ELECTROSTÁTICA CATÁLISIS COVALENTE
104 Catálisis ácido-base La catálisis ácida general consiste en la transferencia de un protón desde un residuo de la enzima, que se comporta como un ácido de Brönsted, al sustrato o intermediarios de la reacción, disminuyéndose así la energía libre del estado de transición. La catálisis básica general consiste en la transferencia de un protón desde el sustrato o intermediarios de la reacción a un residuo de la enzima, que se comporta como una base de Brönsted, disminuyéndose así la energía libre del estado de transición. Si se dan ambos tipos de catálisis se tiene una catálisis ácido-base concertada.
105 Catálisis electrostática La enzima estabiliza intermediarios o estados de transición de la reacción por neutralización de cargas gracias a la disposición espacial en el sitio activo de residuos con carga opuesta. En otros casos la distribución de cargas en el sitio activo sirve para guiar a sustratos cargados o polares a sus sitios de unión.
106 Catálisis covalente La enzima forma transitoriamente un enlace covalente con el sustrato. La catálisis covalente consiste en tres pasos sucesivos: Ataque nucleofílico de la enzima sobre el sustrato (formación del enlace covalente). Toma de electrones por el catalizador u otro sustrato (formación del producto). Separación del producto de la enzima (ruptura del enlace covalente, generalmente por hidrólisis).
107 Mecanismo catalítico de la quimotripsina
108
109
110
111
112 Liberación del extremo amino de uno de los fragmentos en que se rompió la cadena polpeptídica
113
114
115
116 Liberación del extremo carboxilo del otro fragmento en que se rompió la cadena polipeptídica
117 CINÉTICA ENZIMÁTICA
118 Caracterización cinética de las enzimas Determinar la velocidad inicial de la reacción catalizada Variando la concentración de sustrato(s) y manteniendo la concentración de enzima constante. Variando la concentración de enzima y manteniendo la concentración de sustrato(s) constante. Determinar los parámetros o constantes cinéticas: Vmax, kcat, Km, Vmax/Km, kcat/km
119 VELOCIDAD DE REACCIÓN Velocidad de reacción: Cambio de concentración por unidad de tiempo.
120 Por qué medir la velocidad inicial? En el caso de las reacciones catalizadas por enzimas, hay dos razones que hacen muy conveniente medir velocidades iniciales: El producto es un inhibidor de la reacción. La enzima puede ser inestable en el medio de reacción.
121 INHIBICIÓN COMPETITIVA
122 Distribución de las especies de la enzima en ausencia de cooperatividad
123 Distribución de las especies de la enzima en caso de cooperatividad extrema
124 Cooperatividad de unión
125 Curvas de saturación sigmoidal por inhibidores y activadores
126 Saturación sigmoidal por el sustrato (cooperatividad positiva)
127 Constantes o parámetros cinéticos Son las constantes que aparecen en las ecuaciones de velocidad. Están formadas por constantes de velocidad de los pasos que constituyen la reacción catalizada.
128 Efecto del ph sobre la estabilidad vs efectos sobre la actividad de las enzimas
129 Interés del estudio de los efectos del ph sobre la velocidad de las reacciones catalizadas
130 Los H+ son inhibidores y/o activadores
131
132 Enzimas alostéricas con cooperatividad positiva de unión Son enzimas oligoméricas que poseen varios sitios activos y sitios alostéricos y exhiben una cinética de saturación por sus sustratos y/o efectores alostéricos de tipo sigmoidal, resultado de una unión cooperativa de estos ligandos. Cinética sigmoidal Alosterismo Cooperatividad De unión Cinética Enzimas oligoméricas
133 Ecuación de Arrhenius k(t): constante cinética (dependiente de la temperatura) A: factor preexponencial o factor de frecuencia. Refleja la frecuencia de las colisiones. Ea: energía de activación, expresada en kj/mol. R: constante universal de los gases. Su valor es 8,3143 J K-1 mol-1 T: temperatura absoluta [K]
134 Importancia fisiológica de las enzimas alostéricas con cooperatividad positiva de unión Pueden ser reguladas por compuestos no análogos del sustrato (retroinhibición y retroactivación). La cooperatividad positiva de unión, tanto del sustrato como de inhibidores o activadores, les permite responder a cambios pequeños en la concentración de sus ligandos con cambios grandes en la velocidad de la reacción catalizada (amplificación de la señal).
135 Significado del número de Hill (nh)
136 Especificidad vs afinidad Especificidad es la capacidad que tiene una enzima de discriminar entre posibles sustratos (sustratos alternos). Nos indica la velocidad relativa a la que se llevará a cabo la reacción catalizada con estos sustratos diferentes. Se mide por la constante de especificidad para cada sustrato. Los mejores sustratos, es decir aquellos que producen una reacción más rápida, son los que tienen una constante de especificidad mayor.
137 Especificidad vs afinidad Afinidad es la estabilidad del complejo ES. Nos indica la capacidad que tiene la enzima de formar un complejo con un determinado sustrato. Se mide por la constante de disociación (Kd) del complejo ES, que en ocasiones es igual a la Km. Los sustratos con mayor afinidad son los que tienen una menor Kd.
138
139 EFECTO DE LOS INHIBIDORES SOBRE LOS PARÁMETROS CINÉTICOS Tipo de inhibidor Vmax Km Competitivo Vmax akm Incompetitivo Vmax /a Km/a Mixto Vmax /a a Km/a No competitivo Vmax /a *Km *Si a = a a Km/a =Km
140 Patrones de inhibición
141
142 Ecuación de Hill
143 Parámetros cinéticos de la ecuación de Hill
144 Valores del número de Hill
145 Efecto del ph sobre los parámetros cinéticos
Enzimas. Por tanto aceleran en igual proporción la velocidad de la reacción en las dos direcciones. Rosario A. Muñoz-Clares
 Enzimas Las enzimas son catalizadores biológicos que disminuyen la energía de activación de las reacciones que catalizan, pero no modifican la constante de equilibrio. Por tanto aceleran en igual proporción
Enzimas Las enzimas son catalizadores biológicos que disminuyen la energía de activación de las reacciones que catalizan, pero no modifican la constante de equilibrio. Por tanto aceleran en igual proporción
Enzimas Departamento de Bioquímica Noviembre de 2005
 U.T.I. Biología Celular Enzimas Departamento de Bioquímica Noviembre de 2005 Enzimas A. Propiedades generales de las enzimas B. Principios fundamentales de su acción catalítica C. Introducción a la cinética
U.T.I. Biología Celular Enzimas Departamento de Bioquímica Noviembre de 2005 Enzimas A. Propiedades generales de las enzimas B. Principios fundamentales de su acción catalítica C. Introducción a la cinética
ACTIVIDAD ENZIMÁTICA. Dra. Lilian González Segura Departamento de Bioquímica Facultad de Química
 ACTIVIDAD ENZIMÁTICA Dra. Lilian González Segura Departamento de Bioquímica Facultad de Química Porqué la gran mayoría de las reacciones en los seres vivos necesitan ser catalizadas para que ocurran a
ACTIVIDAD ENZIMÁTICA Dra. Lilian González Segura Departamento de Bioquímica Facultad de Química Porqué la gran mayoría de las reacciones en los seres vivos necesitan ser catalizadas para que ocurran a
A B Ej. Cinética de primer orden
 Cinética enzimática A B Ej. Cinética de primer orden Concentración de A o B tiempo Reactivo Producto -da/dt = v = k [A] A=A 0 e- kt db/dt = v = k [A 0 ]-[B] B=A 0 + e kt Concentración en función del tiempo
Cinética enzimática A B Ej. Cinética de primer orden Concentración de A o B tiempo Reactivo Producto -da/dt = v = k [A] A=A 0 e- kt db/dt = v = k [A 0 ]-[B] B=A 0 + e kt Concentración en función del tiempo
Concentración en función del tiempo
 Cinética enzimática Act A B Concentración de A o B tiempo Reactivo -da/dt = v = k [A] Producto db/dt = v = k [A 0 ]-[B] Concentración en función del tiempo velocidad tiempo Reactivo v = A 0 exp(-kt) Producto
Cinética enzimática Act A B Concentración de A o B tiempo Reactivo -da/dt = v = k [A] Producto db/dt = v = k [A 0 ]-[B] Concentración en función del tiempo velocidad tiempo Reactivo v = A 0 exp(-kt) Producto
Definiciones. Ecuación Expresión Función Constante Parámetro Variable. Rosario A. Muñoz-Clares
 Definiciones Ecuación Expresión Función Constante Parámetro Variable Definiciones Energía libre Energía de activación Constante de velocidad Constante de equilibrio Constante de afinidad Constante de disociación
Definiciones Ecuación Expresión Función Constante Parámetro Variable Definiciones Energía libre Energía de activación Constante de velocidad Constante de equilibrio Constante de afinidad Constante de disociación
Energía y enzimas: bioenergética. n Los organismos obtienen su energía de la luz o de compuestos químicos y la conservan en forma de ATP.
 Enzimas y catálisis Patricio Muñoz Torres patricio.munozt@gmail.com Energía y enzimas: bioenergética n Los organismos obtienen su energía de la luz o de compuestos químicos y la conservan en forma de ATP.
Enzimas y catálisis Patricio Muñoz Torres patricio.munozt@gmail.com Energía y enzimas: bioenergética n Los organismos obtienen su energía de la luz o de compuestos químicos y la conservan en forma de ATP.
Tema 6. Cinética Enzimática TEMA 7 CINÉTICA ENZIMÁTICA 3. INHIBICIONES EN REACCIONES ENZIMÁTICAS INHIBICIÓN COMPETITIVA Y NO COMPETITIVA
 Tema 6 Cinética Enzimática 1 TEMA 7 CINÉTICA ENZIMÁTICA 1. DEFINICIONES CÓMO ACTÚAN LOS ENZIMAS? 2. CINÉTICA ENZIMÁTICA MODELO DE MICHAELIS-MENTEN REPRESENTACIONES 3. INHIBICIONES EN REACCIONES ENZIMÁTICAS
Tema 6 Cinética Enzimática 1 TEMA 7 CINÉTICA ENZIMÁTICA 1. DEFINICIONES CÓMO ACTÚAN LOS ENZIMAS? 2. CINÉTICA ENZIMÁTICA MODELO DE MICHAELIS-MENTEN REPRESENTACIONES 3. INHIBICIONES EN REACCIONES ENZIMÁTICAS
ACTIVIDAD ENZIMÁTICA. Curvas temporales de la actividad enzimática de la lactato deshidrogenasa de músculo esquelético de pollo.
 ACTIVIDAD ENZIMÁTICA Curvas temporales de la actividad enzimática de la lactato deshidrogenasa de músculo esquelético de pollo. Monitoreo de la purificación de la lactato deshidrogenasa SDS PAGE Actividad
ACTIVIDAD ENZIMÁTICA Curvas temporales de la actividad enzimática de la lactato deshidrogenasa de músculo esquelético de pollo. Monitoreo de la purificación de la lactato deshidrogenasa SDS PAGE Actividad
ENZIMAS. Kuhne en el año de 1876 les llamó enzima a los catalizadores que producían
 ENZIMAS Dr. Santiago René Anzaldúa Arce. Kuhne en el año de 1876 les llamó enzima a los catalizadores que producían fermentaciones de diversos compuestos, La palabra enzima significa en la levadura, pues
ENZIMAS Dr. Santiago René Anzaldúa Arce. Kuhne en el año de 1876 les llamó enzima a los catalizadores que producían fermentaciones de diversos compuestos, La palabra enzima significa en la levadura, pues
1. Características generales
 1. Características generales Los enzimas son proteínas que catalizan reacciones químicas en los seres vivos. Los enzimas son catalizadores, es decir, sustancias que, sin consumirse en una reacción, aumentan
1. Características generales Los enzimas son proteínas que catalizan reacciones químicas en los seres vivos. Los enzimas son catalizadores, es decir, sustancias que, sin consumirse en una reacción, aumentan
CARACTERÍSTICAS DE LAS ENZIMAS
 BIOQUÍMICA I CARACTERÍSTICAS DE LAS ENZIMAS 1. Son los catalizadores de las reacciones químicas de los sistemas biológicos. 2. Tienen gran poder catalítico. 3. Poseen un elevado grado de especificidad
BIOQUÍMICA I CARACTERÍSTICAS DE LAS ENZIMAS 1. Son los catalizadores de las reacciones químicas de los sistemas biológicos. 2. Tienen gran poder catalítico. 3. Poseen un elevado grado de especificidad
CINETICA ENZIMATICA ESTUDIA LA VELOCIDAD DE LAS REACCIONES BIOQUÍMICAS
 CINETICA ENZIMATICA ESTUDIA LA VELOCIDAD DE LAS REACCIONES BIOQUÍMICAS Es la medida de la formación de producto o la desapariciónde sustrato por unidad de tiempo. E S P Velocidad de una reacción se muestra
CINETICA ENZIMATICA ESTUDIA LA VELOCIDAD DE LAS REACCIONES BIOQUÍMICAS Es la medida de la formación de producto o la desapariciónde sustrato por unidad de tiempo. E S P Velocidad de una reacción se muestra
CATALISIS ENZIMATICA
 UNIVERSIDAD DE CHILE FACULTAD DE CIENCIAS QUIMICAS Y FARMACEUTICAS DEPARTAMENTO DE BIOQUÍMICA Y BIOLOGÍA MOLECULAR CATALISIS ENZIMATICA María Antonieta Valenzuela P 2013 Historia sobre conocimiento de
UNIVERSIDAD DE CHILE FACULTAD DE CIENCIAS QUIMICAS Y FARMACEUTICAS DEPARTAMENTO DE BIOQUÍMICA Y BIOLOGÍA MOLECULAR CATALISIS ENZIMATICA María Antonieta Valenzuela P 2013 Historia sobre conocimiento de
ENZIMAS: CONCEPTOS BÁSICOS Y CINÉTICA
 ENZIMAS: CONCEPTOS BÁSICOS Y CINÉTICA Enzimas: catalizadores de naturaleza proteica Seis clases de enzimas Clase 1. Oxidoreductasas 2. Transferasas 3. Hidrolasas 4. Liasas 5. Isomerasas 6. Ligasas Tipo
ENZIMAS: CONCEPTOS BÁSICOS Y CINÉTICA Enzimas: catalizadores de naturaleza proteica Seis clases de enzimas Clase 1. Oxidoreductasas 2. Transferasas 3. Hidrolasas 4. Liasas 5. Isomerasas 6. Ligasas Tipo
DEPARTAMENTO DE BIOQUÍMICA ESFUNO EUTM E N Z I M A S
 DEPARTAMENTO DE BIOQUÍMICA ESFUNO EUTM E N Z I M A S Enzimas A. Propiedades generales B. Principios fundamentales de su acción catalítica C. Introducción a la cinética enzimática D. Regulación de la actividad
DEPARTAMENTO DE BIOQUÍMICA ESFUNO EUTM E N Z I M A S Enzimas A. Propiedades generales B. Principios fundamentales de su acción catalítica C. Introducción a la cinética enzimática D. Regulación de la actividad
CINÉTICA ENZIMÁTICA. Ecuación de Michaelis-Menten Efecto de inhibidores
 CINÉTICA ENZIMÁTICA Ecuación de Michaelis-Menten Efecto de inhibidores Producto [P] CINÉTICA ENZIMÁTICA La cinética enzimática estudia la velocidad de las reacciones catalizadas por enzimas. Proporciona
CINÉTICA ENZIMÁTICA Ecuación de Michaelis-Menten Efecto de inhibidores Producto [P] CINÉTICA ENZIMÁTICA La cinética enzimática estudia la velocidad de las reacciones catalizadas por enzimas. Proporciona
NOCIONES BÁSICAS DE ENERGÍA
 NOCIONES BÁSICAS DE ENERGÍA Esta obra está bajo una licencia Attribution-NonCommercial-ShareAlike 3.0 Unported de Creative Commons. Para ver una copia de esta licencia, visite http://creativecommons.org/licenses/by-nc-sa/3.0/
NOCIONES BÁSICAS DE ENERGÍA Esta obra está bajo una licencia Attribution-NonCommercial-ShareAlike 3.0 Unported de Creative Commons. Para ver una copia de esta licencia, visite http://creativecommons.org/licenses/by-nc-sa/3.0/
TEMA 5 ENZIMAS. Cualquier complejidad intelectual puede ser transmitida en el lenguaje corriente «Brontosaurus» y la nalga del ministro S.J.
 TEMA 5 ENZIMAS Cualquier complejidad intelectual puede ser transmitida en el lenguaje corriente «Brontosaurus» y la nalga del ministro S.J.Gould BIOLOGÍA 2º BACHILLERATO Enzimas Concepto Biocatalizador
TEMA 5 ENZIMAS Cualquier complejidad intelectual puede ser transmitida en el lenguaje corriente «Brontosaurus» y la nalga del ministro S.J.Gould BIOLOGÍA 2º BACHILLERATO Enzimas Concepto Biocatalizador
ENZIMAS SE TRATA DE PROTEÍNAS ESPECIALES QUE EJERCEN SU ACCIÓN UNIÉNDOSE SELECTIVAMENTE A OTRAS MOLÉCULAS DENOMINADAS SUSTRATOS.
 ENZIMAS SE TRATA DE PROTEÍNAS ESPECIALES QUE EJERCEN SU ACCIÓN UNIÉNDOSE SELECTIVAMENTE A OTRAS MOLÉCULAS DENOMINADAS SUSTRATOS. INDUCEN MODIFICACIONES QUÍMICAS EN LOS SUSTRATOS A LOS QUE SE UNEN POR:
ENZIMAS SE TRATA DE PROTEÍNAS ESPECIALES QUE EJERCEN SU ACCIÓN UNIÉNDOSE SELECTIVAMENTE A OTRAS MOLÉCULAS DENOMINADAS SUSTRATOS. INDUCEN MODIFICACIONES QUÍMICAS EN LOS SUSTRATOS A LOS QUE SE UNEN POR:
Concepto de velocidad inicial [ ] d[ ] v =, t -> 0 dt
![Concepto de velocidad inicial [ ] d[ ] v =, t -> 0 dt Concepto de velocidad inicial [ ] d[ ] v =, t -> 0 dt](/thumbs/70/63569259.jpg) VARIABLES QUE INFLUYEN EN LA VELOCIDAD DE UNA REACIÓN ENZIMÁTICA Concepto de velocidad inicial [ ] d[ ] v =, t -> 0 dt p s t VARIABLES QUE INFLUYEN EN LA VELOCIDAD DE UNA REACIÓN ENZIMÁTICA Concentración
VARIABLES QUE INFLUYEN EN LA VELOCIDAD DE UNA REACIÓN ENZIMÁTICA Concepto de velocidad inicial [ ] d[ ] v =, t -> 0 dt p s t VARIABLES QUE INFLUYEN EN LA VELOCIDAD DE UNA REACIÓN ENZIMÁTICA Concentración
ENZIMAS Catalizadores biológicos
 ENZIMAS Catalizadores biológicos Las enzimas están en el centro de cada proceso bioquímico. Son el origen de la compleja sinfonía altamente regulada que denominamos vida. ENDOCELULARES EXOCELULARES Citosol
ENZIMAS Catalizadores biológicos Las enzimas están en el centro de cada proceso bioquímico. Son el origen de la compleja sinfonía altamente regulada que denominamos vida. ENDOCELULARES EXOCELULARES Citosol
ESTUDIOS CINÉTICOS SE MIDE LA VELOCIDAD DE LA REACCIÓN CATALIZADA. La velocidad de reacciones químicas: Para una reacción:
 ESTUDIOS CINÉTICOS SE MIDE LA VELOCIDAD DE LA REACCIÓN CATALIZADA La velocidad de reacciones químicas: Para una reacción: A B La velocidad depende de la concentración del reactante: v = k[a] k = constante
ESTUDIOS CINÉTICOS SE MIDE LA VELOCIDAD DE LA REACCIÓN CATALIZADA La velocidad de reacciones químicas: Para una reacción: A B La velocidad depende de la concentración del reactante: v = k[a] k = constante
Cinética Enzimática. Enrique Rivera González
 Cinética Enzimática Enrique Rivera González Importancia Las enzimas son proteínas capaces de catalizar específicamente reacciones bioquímicas. La actividad catalítica de las enzimas depende de su estructura.
Cinética Enzimática Enrique Rivera González Importancia Las enzimas son proteínas capaces de catalizar específicamente reacciones bioquímicas. La actividad catalítica de las enzimas depende de su estructura.
ENZIMAS SON BIOCATALIZADORES AUMENTAN LA VELOCIDAD DE REACCIÓN NO SE GASTAN EN CANTIDADES MUY PEQUEÑAS
 ENZIMAS SON BIOCATALIZADORES AUMENTAN LA VELOCIDAD DE REACCIÓN NO SE GASTAN EN CANTIDADES MUY PEQUEÑAS ENZIMAS: CATALIZADORES BIOLOGICOS ACELERAN LA VELOCIDAD DE LA REACCIÓN SON PROTEÍNAS GLOBULARES NO
ENZIMAS SON BIOCATALIZADORES AUMENTAN LA VELOCIDAD DE REACCIÓN NO SE GASTAN EN CANTIDADES MUY PEQUEÑAS ENZIMAS: CATALIZADORES BIOLOGICOS ACELERAN LA VELOCIDAD DE LA REACCIÓN SON PROTEÍNAS GLOBULARES NO
endoenzimas exoenzimas:
 Enzimas Enzimas:son proteínas altamente especializadas que tienen como función la catálisis o regulación de la velocidad de las reacciones químicas que se llevan a cabo en los seres vivos. Son macromoléculas
Enzimas Enzimas:son proteínas altamente especializadas que tienen como función la catálisis o regulación de la velocidad de las reacciones químicas que se llevan a cabo en los seres vivos. Son macromoléculas
PROPEDÉUTICO DE ODONTOLOGÍA BIOQUÍMICA BÁSICA
 PROPEDÉUTICO DE ODONTOLOGÍA BIOQUÍMICA BÁSICA 2012 Dagmar Stojanovic de Malpica Ph D Escuela de Biología, Facultad de Ciencias, U.C.V. UNIDAD IV. ENZIMAS Relación entre el G o y la K eq en una reacción
PROPEDÉUTICO DE ODONTOLOGÍA BIOQUÍMICA BÁSICA 2012 Dagmar Stojanovic de Malpica Ph D Escuela de Biología, Facultad de Ciencias, U.C.V. UNIDAD IV. ENZIMAS Relación entre el G o y la K eq en una reacción
ESTRUCTURA DE LA TRIOSAFOSFATO ISOMERASA esta proteína es una eficiente enzima involucrada en la vía glucolítica.
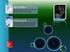 ESTRUCTURA DE LA TRIOSAFOSFATO ISOMERASA esta proteína es una eficiente enzima involucrada en la vía glucolítica. Características generales Cinética química Nomenclatura Centro activo Cofactores Factores
ESTRUCTURA DE LA TRIOSAFOSFATO ISOMERASA esta proteína es una eficiente enzima involucrada en la vía glucolítica. Características generales Cinética química Nomenclatura Centro activo Cofactores Factores
TEMA 13. LAS REACCIONES METABÓLICAS. LA IMPORTANCIA DE LAS ENZIMAS.
 TEMA 13. LAS REACCIONES METABÓLICAS. LA IMPORTANCIA DE LAS ENZIMAS. 1.-Características de las reacciones metabólicas. 2.- Enzimas y reacciones enzimáticas. 2.1. Mecanismo de las reacciones enzimáticas.
TEMA 13. LAS REACCIONES METABÓLICAS. LA IMPORTANCIA DE LAS ENZIMAS. 1.-Características de las reacciones metabólicas. 2.- Enzimas y reacciones enzimáticas. 2.1. Mecanismo de las reacciones enzimáticas.
Universidad Nacional de Tucumán ENZIMAS
 ENZIMAS INTRODUCIÓN Las reacciones químicas en sistemas biológicos raramente ocurren en ausencia de un catalizador. Estos catalizadores se denominan enzimas y son casi en su totalidad de naturaleza proteica,
ENZIMAS INTRODUCIÓN Las reacciones químicas en sistemas biológicos raramente ocurren en ausencia de un catalizador. Estos catalizadores se denominan enzimas y son casi en su totalidad de naturaleza proteica,
Página 1 clases83.jimdo.com PRIMERA CLASE DE ENZIMAS DEFINICION ENERGIA DE ACTIVACION CONCENTRACION EN FUNCION DE TIEMPO
 Página 1 clases83.jimdo.com 096437814 PRIMERA CLASE DE ENZIMAS DEFINICION ENERGIA DE ACTIVACION CONCENTRACION EN FUNCION DE TIEMPO Página 2 clases83.jimdo.com 096437814 Página 3 clases83.jimdo.com 096437814
Página 1 clases83.jimdo.com 096437814 PRIMERA CLASE DE ENZIMAS DEFINICION ENERGIA DE ACTIVACION CONCENTRACION EN FUNCION DE TIEMPO Página 2 clases83.jimdo.com 096437814 Página 3 clases83.jimdo.com 096437814
Enzimas. Determinación de su actividad catalítica en distintos materiales biológicos
 Enzimas Determinación de su actividad catalítica en distintos materiales biológicos Qué son? La mayoría son proteínas ( existe ARN catalítico ). que función cumplen? Catalizadores biológicos Sus propiedades
Enzimas Determinación de su actividad catalítica en distintos materiales biológicos Qué son? La mayoría son proteínas ( existe ARN catalítico ). que función cumplen? Catalizadores biológicos Sus propiedades
ENZIMAS-2005 CINÉTICA ENZIMÁTICA
 ENZIMAS-00 Las enzimas son catalizadores biológicos en su mayoría de naturaleza proteica (99,99%) y las ribosimas (fragmentos de RNA) (0,%). Las enzimas tienen tres propiedades bien definidas e inigualables
ENZIMAS-00 Las enzimas son catalizadores biológicos en su mayoría de naturaleza proteica (99,99%) y las ribosimas (fragmentos de RNA) (0,%). Las enzimas tienen tres propiedades bien definidas e inigualables
QUÍMICA BIOLÓGICA. Enzimas Cinética Enzimática
 QUÍMICA BIOLÓGICA Enzimas Cinética Enzimática 2017 INTRODUCCIÓN Proteínas (única excepción: RNAs catalíticos o ribozimas) Holoenzima (complejo catalíticamente activo) Apoenzima (inactiva) Cofactor (coenzimas,
QUÍMICA BIOLÓGICA Enzimas Cinética Enzimática 2017 INTRODUCCIÓN Proteínas (única excepción: RNAs catalíticos o ribozimas) Holoenzima (complejo catalíticamente activo) Apoenzima (inactiva) Cofactor (coenzimas,
Reacciones enzimáticas Sergio Huerta Ochoa UAM-Iztapalapa
 Reacciones enzimáticas Sergio Huerta Ochoa UAM-Iztapalapa aturaleza Planta Piloto de Fermentaciones Síntesis de compuestos orgánicos Industria química La naturaleza de las enzimas 1) La reacción química
Reacciones enzimáticas Sergio Huerta Ochoa UAM-Iztapalapa aturaleza Planta Piloto de Fermentaciones Síntesis de compuestos orgánicos Industria química La naturaleza de las enzimas 1) La reacción química
UNIDAD 12. METABOLISMO Y ENZIMAS.
 UNIDAD 12. METABOLISMO Y ENZIMAS. 1.- REACCIONES METABÓLICAS. Reacción metabólica. Cualquier reacción entre biomoléculas que ocurre en los seres vivos. Características de las reacciones metabólicas: -
UNIDAD 12. METABOLISMO Y ENZIMAS. 1.- REACCIONES METABÓLICAS. Reacción metabólica. Cualquier reacción entre biomoléculas que ocurre en los seres vivos. Características de las reacciones metabólicas: -
Proteínas como blancos farmacológicos. Dra. Jenny Fiedler.
 Proteínas como blancos farmacológicos. Enzimas Dra. Jenny Fiedler. Estructura de proteínas Estructura primaria Secuencia de aminoácidos en una proteína 1 2 3 4 5 126 127 128 129 Lys-Val-Phe-Gly-Arg...Gly-Cys-Arg-Leu
Proteínas como blancos farmacológicos. Enzimas Dra. Jenny Fiedler. Estructura de proteínas Estructura primaria Secuencia de aminoácidos en una proteína 1 2 3 4 5 126 127 128 129 Lys-Val-Phe-Gly-Arg...Gly-Cys-Arg-Leu
EL CONTROL DE LAS ACTIVIDADES CELULARES
 EL CONTROL DE LAS ACTIVIDADES CELULARES LAS REACCIONES CELULARES BÁSICAS Todas las células llevan a cabo funciones vitales: Ingestión de nutrientes Eliminación de desperdicios Crecimiento Reproducción
EL CONTROL DE LAS ACTIVIDADES CELULARES LAS REACCIONES CELULARES BÁSICAS Todas las células llevan a cabo funciones vitales: Ingestión de nutrientes Eliminación de desperdicios Crecimiento Reproducción
1.- Explica cuáles son los principales factores que afectan a la actividad enzimática.
 PREGUNTAS RESUELTAS. LOS ENZIMAS 1.- Explica cuáles son los principales factores que afectan a la actividad enzimática. 2.- Qué es un inhibidor y de cuántos tipos puede ser la acción que realizan? 3.-
PREGUNTAS RESUELTAS. LOS ENZIMAS 1.- Explica cuáles son los principales factores que afectan a la actividad enzimática. 2.- Qué es un inhibidor y de cuántos tipos puede ser la acción que realizan? 3.-
Enzimas Catalizadores bioquímicos. Rogelio Valadez Blanco
 Enzimas Catalizadores bioquímicos Rogelio Valadez Blanco COFACTORES Algunas enzimas tienen necesidad de cofactores para realizar su actividad catalítica Una proteína inactiva por sí sola se llama apoenzima
Enzimas Catalizadores bioquímicos Rogelio Valadez Blanco COFACTORES Algunas enzimas tienen necesidad de cofactores para realizar su actividad catalítica Una proteína inactiva por sí sola se llama apoenzima
ENZIMAS Las enzimas son proteínas
 ENZIMAS Las enzimas son proteínas Actúan como catalizadores de las reacciones químicas necesarias para la supervivencia celular Que es un catalizador??? Es una sustancia que acelera la velocidad de la
ENZIMAS Las enzimas son proteínas Actúan como catalizadores de las reacciones químicas necesarias para la supervivencia celular Que es un catalizador??? Es una sustancia que acelera la velocidad de la
TEMA 5:BIOCATALIZADORES: ENZIMAS, VITAMINAS Y HORMONAS
 TEMA 5:BIOCATALIZADORES: ENZIMAS, VITAMINAS Y HORMONAS INDICE 1. BIOCATALIZADORES 2. ENZIMAS 2.1. CONCEPTO, PROPIEDADES Y COMPOSICIÓN QUÍMICA 2.2. MECANISMOS DE ACCIÓN 2.3. ESPECIFICIDAD ENZIMÁTICA 2.4.
TEMA 5:BIOCATALIZADORES: ENZIMAS, VITAMINAS Y HORMONAS INDICE 1. BIOCATALIZADORES 2. ENZIMAS 2.1. CONCEPTO, PROPIEDADES Y COMPOSICIÓN QUÍMICA 2.2. MECANISMOS DE ACCIÓN 2.3. ESPECIFICIDAD ENZIMÁTICA 2.4.
Son proteínas globulares altamente especializadas que provocan o aceleran una reacción bioquímica.
 1.7.- Enzimas Las reacciones precisan de una cierta cantidad de energía para iniciarse. Esta energía, denominada energía de activación, permite romper los enlaces de las moléculas que están reaccionando
1.7.- Enzimas Las reacciones precisan de una cierta cantidad de energía para iniciarse. Esta energía, denominada energía de activación, permite romper los enlaces de las moléculas que están reaccionando
ENZIMAS. 3)- La mayor parte de las rutas metabólicas son comunes a todos los seres vivos.
 ENZIMAS Son sustancias encargadas de facilitar las reacciones químicas (reacciones metabólicas), son catalizadores de las reacciones son biocatalizadores. Las enzimas tienen una naturaleza proteica (salvo
ENZIMAS Son sustancias encargadas de facilitar las reacciones químicas (reacciones metabólicas), son catalizadores de las reacciones son biocatalizadores. Las enzimas tienen una naturaleza proteica (salvo
METABOLISMO. Contenidos trabajados en clase.
 METABOLISMO Contenidos trabajados en clase. Qué son? Donde actúan? Como actúan? Propiedades o características Toda reacción exergónica necesita calor (energía )para comenzar Ej La combustión de la madera
METABOLISMO Contenidos trabajados en clase. Qué son? Donde actúan? Como actúan? Propiedades o características Toda reacción exergónica necesita calor (energía )para comenzar Ej La combustión de la madera
Factores que afectan la velocidad de una reacción catalizada por enzimas
 Factores que afectan la velocidad de una reacción catalizada por enzimas Concentración de sustrato o sustratos (cofactores) Concentración de enzima Inhibidores Activadores ph Temperatura Regulación de
Factores que afectan la velocidad de una reacción catalizada por enzimas Concentración de sustrato o sustratos (cofactores) Concentración de enzima Inhibidores Activadores ph Temperatura Regulación de
El metabolismo es un conjunto de reacciones químicas que tienen lugar en las células del cuerpo
 METABOLISMO El metabolismo es un conjunto de reacciones químicas que tienen lugar en las células del cuerpo El metabolismo transforma la energía que contienen los alimentos que ingerimos en el combustible
METABOLISMO El metabolismo es un conjunto de reacciones químicas que tienen lugar en las células del cuerpo El metabolismo transforma la energía que contienen los alimentos que ingerimos en el combustible
FACULTAD DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA. CURSO DE BIOQUÍMICA (CLAVE 1508) Licenciaturas de QFB y QA
 FACULTAD DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA CURSO DE BIOQUÍMICA (CLAVE 1508) Licenciaturas de QFB y QA Prof. Laura Carmona Salazar Grupos: 03 Semestre: 13-I Este material es exclusivamente para uso
FACULTAD DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA CURSO DE BIOQUÍMICA (CLAVE 1508) Licenciaturas de QFB y QA Prof. Laura Carmona Salazar Grupos: 03 Semestre: 13-I Este material es exclusivamente para uso
REPARTIDO DE PRÁCTICO DE ACTIVIDAD ENZIMATICA
 REPARTIDO DE PRÁCTICO DE ACTIVIDAD EZIMATICA Las enzimas son macromoléculas biológicas que aceleran la velocidad de una reacción hasta lograr el equilibrio. La enorme mayoría de las enzimas conocidas son
REPARTIDO DE PRÁCTICO DE ACTIVIDAD EZIMATICA Las enzimas son macromoléculas biológicas que aceleran la velocidad de una reacción hasta lograr el equilibrio. La enorme mayoría de las enzimas conocidas son
Cuestiones de Bioquímica
 1º de Química, gr. D http://www.uv.es/bbm Tema 4 Cuestiones de Bioquímica 1) Una reacción enzimática puede escribirse como dos reacciones sucesivas, donde el complejo ES es el intermediario en la conversión
1º de Química, gr. D http://www.uv.es/bbm Tema 4 Cuestiones de Bioquímica 1) Una reacción enzimática puede escribirse como dos reacciones sucesivas, donde el complejo ES es el intermediario en la conversión
03/08/2009 DESORDEN ENERGÍA DISIPADA ENERGÍA CONVERTIDA EN: -SÍNTESIS -MOVIMIENTO -REPRODUCCIÓN -PENSAMIENTO
 Enzimas, vitaminas y nutrientes INTRODUCCIÓN VIDA organización ió estructuras simple complejo Leyes universales: Orden desorden La energía se disipa Caos, aleatoriedad: Flecha del tiempo ENERGÍA 1 Fuente
Enzimas, vitaminas y nutrientes INTRODUCCIÓN VIDA organización ió estructuras simple complejo Leyes universales: Orden desorden La energía se disipa Caos, aleatoriedad: Flecha del tiempo ENERGÍA 1 Fuente
INTITUCIÓN EDUCATIVA COLEGIO ARTISTICO RAFAEL CONTRERAS NAVARRO GUIA DE APRENDIZAJE METABOLISMO CELULAR
 INTITUCIÓN EDUCATIVA COLEGIO ARTISTICO RAFAEL CONTRERAS NAVARRO GUIA DE APRENDIZAJE METABOLISMO CELULAR PROFESOR: Jesús Alonso Paba León GRADO: Undecimo GUÍA DE ESTUDIO METABOLISMO CELULAR La vida de cualquier
INTITUCIÓN EDUCATIVA COLEGIO ARTISTICO RAFAEL CONTRERAS NAVARRO GUIA DE APRENDIZAJE METABOLISMO CELULAR PROFESOR: Jesús Alonso Paba León GRADO: Undecimo GUÍA DE ESTUDIO METABOLISMO CELULAR La vida de cualquier
UAM Química Física. Cinética-2
 4. Cinética química Velocidad de reacción Mecanismos de reacción Catálisis Teorías cinéticas Reacciones en disolución UAM 2010-11. Química Física. Cinética-2 1 Catálisis Catalizador Mecanismo de reacciones
4. Cinética química Velocidad de reacción Mecanismos de reacción Catálisis Teorías cinéticas Reacciones en disolución UAM 2010-11. Química Física. Cinética-2 1 Catálisis Catalizador Mecanismo de reacciones
Rosario A. Muñoz Clares
 Rosario A. Muñoz Clares TAREAS 1.- En la reacción de primer orden A B la concentración de A en el tiempo cero es de 0.5 mm. Al cabo de 2 s es de 0.25 mm. Cuál será al cabo de 5 s? 2.- A) Cuál será la constante
Rosario A. Muñoz Clares TAREAS 1.- En la reacción de primer orden A B la concentración de A en el tiempo cero es de 0.5 mm. Al cabo de 2 s es de 0.25 mm. Cuál será al cabo de 5 s? 2.- A) Cuál será la constante
Factores que afectan la velocidad de una reacción catalizada por enzimas
 Factores que afectan la velocidad de una reacción catalizada por enzimas Concentración de sustrato o sustratos (cofactores) Concentración de enzima Inhibidores Activadores ph Temperatura Regulación de
Factores que afectan la velocidad de una reacción catalizada por enzimas Concentración de sustrato o sustratos (cofactores) Concentración de enzima Inhibidores Activadores ph Temperatura Regulación de
SERIE Nº 6. Enzimas y Coenzimas
 SERIE Nº 6. Enzimas Las reacciones químicas que ocurren en los organismos vivos presentan casi siempre una energía de activación tan elevada, que en condiciones compatibles con la vida ocurrirían a velocidades
SERIE Nº 6. Enzimas Las reacciones químicas que ocurren en los organismos vivos presentan casi siempre una energía de activación tan elevada, que en condiciones compatibles con la vida ocurrirían a velocidades
QUÍMICA BIOLÓGICA. Trabajo Práctico Nº2: Cinética Enzimática. Estudio cinético de la Glucosa-6-fosfato deshidrogenasa
 QUÍMICA BIOLÓGICA Trabajo Práctico Nº2: Cinética Enzimática Estudio cinético de la Glucosa-6-fosfato deshidrogenasa Las enzimas son catalizadores biológicos, en la mayoría de los casos de naturaleza proteica.
QUÍMICA BIOLÓGICA Trabajo Práctico Nº2: Cinética Enzimática Estudio cinético de la Glucosa-6-fosfato deshidrogenasa Las enzimas son catalizadores biológicos, en la mayoría de los casos de naturaleza proteica.
METABOLISMO Y ENZIMAS
 Guía de Actividades N 7 METABOLISMO Y ENZIMAS SECTOR EJE 1 UNIDAD 1 : CIENCIAS NATURALES - BIOLOGÍA : ESTRUCTURA Y FUNCIÓN DE LOS SERES VIVOS : ESTRUCTURA Y FUNCIÓN DE LA CÉLULA ESTUDIANTE : PROFESOR :
Guía de Actividades N 7 METABOLISMO Y ENZIMAS SECTOR EJE 1 UNIDAD 1 : CIENCIAS NATURALES - BIOLOGÍA : ESTRUCTURA Y FUNCIÓN DE LOS SERES VIVOS : ESTRUCTURA Y FUNCIÓN DE LA CÉLULA ESTUDIANTE : PROFESOR :
Es la capacidad de realizar un trabajo. A pesar que existen varias formas de energía: química, luminosa, mecánica, etc., solo hay dos tipos básicos:
 Es la capacidad de realizar un trabajo. A pesar que existen varias formas de energía: química, luminosa, mecánica, etc., solo hay dos tipos básicos: Potencial: es la capacidad de realizar trabajo como
Es la capacidad de realizar un trabajo. A pesar que existen varias formas de energía: química, luminosa, mecánica, etc., solo hay dos tipos básicos: Potencial: es la capacidad de realizar trabajo como
Contenidos teóricos. Unidad temática 1. Diseño molecular de vida. Tema 1. El agua como disolvente
 Contenidos teóricos Unidad temática 1. Diseño molecular de vida. Tema 1. El agua como disolvente Tema 2. Principales biomoléculas presentes en los seres vivos y su relación estructurafunción: proteínas,
Contenidos teóricos Unidad temática 1. Diseño molecular de vida. Tema 1. El agua como disolvente Tema 2. Principales biomoléculas presentes en los seres vivos y su relación estructurafunción: proteínas,
METABOLISMO Y ENZIMAS
 DESAFÍO Nº 12 Profesora Verónica Abasto Córdova Biología 1 Medio Nombre del Estudiante : Curso : METABOLISMO Y ENZIMAS TIMBRE METABOLISMO En las clases anteriores, estudiamos los principios de la teoría
DESAFÍO Nº 12 Profesora Verónica Abasto Córdova Biología 1 Medio Nombre del Estudiante : Curso : METABOLISMO Y ENZIMAS TIMBRE METABOLISMO En las clases anteriores, estudiamos los principios de la teoría
ENZIMAS GENERALIDADES DE LAS ENZIMAS. Material extraído de:
 ENZIMAS GENERALIDADES DE LAS ENZIMAS Material extraído de: Bioquimica y Biologia molecular para ciencias de la salud. José A. Lozano. Pags 133-157 McKee, T. y McKeeJ. R. (2003). Bioquímica. La base molecular
ENZIMAS GENERALIDADES DE LAS ENZIMAS Material extraído de: Bioquimica y Biologia molecular para ciencias de la salud. José A. Lozano. Pags 133-157 McKee, T. y McKeeJ. R. (2003). Bioquímica. La base molecular
PROTEINAS COMO CATALIZADORES ENZIMAS
 PROTEINAS COMO CATALIZADORES ENZIMAS ENZIMAS son proteínas que catalizan reacciones químicas en los seres vivos. son catalizadores: sustancias que, sin consumirse en una reacción, aumentan notablemente
PROTEINAS COMO CATALIZADORES ENZIMAS ENZIMAS son proteínas que catalizan reacciones químicas en los seres vivos. son catalizadores: sustancias que, sin consumirse en una reacción, aumentan notablemente
Generalidades de ENZIMAS
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,009 Generalidades de ENZIMAS Dr. Mynor Leiva Desde los nutrientes
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,009 Generalidades de ENZIMAS Dr. Mynor Leiva Desde los nutrientes
LAS ENZIMAS ENZIMAS CLASIFICACIÓN ESTRUCTURA FUNCIÓN. Biocatalizadores. proteica. velocidad reacción. Energía activación. Inorgánica.
 LAS ENZIMAS ENZIMAS ESTRUCTURA puede ser FUNCIÓN CLASIFICACIÓN Holoenzima formada Estrictamente proteica Biocatalizadores actúan Ligasas Isomerasas Liasas Hidrolasas Transferasas Oxidorreductasas de naturaleza
LAS ENZIMAS ENZIMAS ESTRUCTURA puede ser FUNCIÓN CLASIFICACIÓN Holoenzima formada Estrictamente proteica Biocatalizadores actúan Ligasas Isomerasas Liasas Hidrolasas Transferasas Oxidorreductasas de naturaleza
Las Proteínas BIOLOGÍA 2º BACHILLERATO TEMA 4: Actividades: 1º DÍA Los aminoácidos. Pg
 BIOLOGÍA 2º BACHILLERATO TEMA 4: Las Proteínas Actividades: 1º DÍA Los aminoácidos Pg 58-59-60 1. Define el concepto de aminoácido. Escribe su fórmula general explicando su estructura molecular. 2. a)
BIOLOGÍA 2º BACHILLERATO TEMA 4: Las Proteínas Actividades: 1º DÍA Los aminoácidos Pg 58-59-60 1. Define el concepto de aminoácido. Escribe su fórmula general explicando su estructura molecular. 2. a)
GUIA DE APRENDIZAJE METABOLISMO CELULAR
 LICEO de Música Depto. BIOLOGIA GUIA DE APRENDIZAJE METABOLISMO CELULAR SECTOR: Biología NIVEL: Cuarto Año Medio Profesora : Ingrid Alamos CONTENIDO: Metabolismo Celular OBJETIVO DE APRENDIZAJE: Reconocer
LICEO de Música Depto. BIOLOGIA GUIA DE APRENDIZAJE METABOLISMO CELULAR SECTOR: Biología NIVEL: Cuarto Año Medio Profesora : Ingrid Alamos CONTENIDO: Metabolismo Celular OBJETIVO DE APRENDIZAJE: Reconocer
Tema 7. Actividad enzimática
 Tema 7. Actividad enzimática Definición, clasificación y nomenclatura de las enzimas Coenzimas y cofactores Mecanismos de la catálisis enzimática Centro activo y especificidad Tipos de catálisis Generalidades
Tema 7. Actividad enzimática Definición, clasificación y nomenclatura de las enzimas Coenzimas y cofactores Mecanismos de la catálisis enzimática Centro activo y especificidad Tipos de catálisis Generalidades
Bioquímica Estructural y Metabólica. TEMA 5. Enzimología
 TEMA 5. Enzimas. Clasificación. Principios de la catálisis enzimá6ca. Energía de ac6vación. Velocidad de reacción y equilibrio de reacción. Ciné6ca enzimá6ca: ecuación de Michaelis- Menten. Ecuación de
TEMA 5. Enzimas. Clasificación. Principios de la catálisis enzimá6ca. Energía de ac6vación. Velocidad de reacción y equilibrio de reacción. Ciné6ca enzimá6ca: ecuación de Michaelis- Menten. Ecuación de
Enzimas Regulatorias. Enzimas Alostéricas. Enzimas modificadas covalentemente. Activación proteolítica de pro-enzimas
 Enzimas Regulatorias Enzimas Alostéricas Enzimas modificadas covalentemente Activación proteolítica de pro-enzimas La inhibición por retroalimentación se refiere a la inhibición de una de las primeras
Enzimas Regulatorias Enzimas Alostéricas Enzimas modificadas covalentemente Activación proteolítica de pro-enzimas La inhibición por retroalimentación se refiere a la inhibición de una de las primeras
CURSO BIOQUÍMICA Y FITOQUÍMICA. FACULTAD DE CIENCIAS AGRARIAS Y FORESTALES UNLP. Primer cuatrimestre 2011 UNIDAD Nº 3
 CURSO BIOQUÍMICA Y FITOQUÍMICA. FACULTAD DE CIENCIAS AGRARIAS Y FORESTALES UNLP. Primer cuatrimestre 2011 UNIDAD Nº 3 FACTORES QUE INCIDEN EN LA ACTIVIDAD ENZIMÁTICA: PRESENCIA DE INHIBIDORES. Dentro de
CURSO BIOQUÍMICA Y FITOQUÍMICA. FACULTAD DE CIENCIAS AGRARIAS Y FORESTALES UNLP. Primer cuatrimestre 2011 UNIDAD Nº 3 FACTORES QUE INCIDEN EN LA ACTIVIDAD ENZIMÁTICA: PRESENCIA DE INHIBIDORES. Dentro de
Tema 10. Regulación de la actividad enzimática
 Tema 10. Regulación de la actividad enzimática Control de la actividad enzimática Regulación por cambios en la concentración de enzima Regulación alostérica Modificaciones covalentes reversibles Activación
Tema 10. Regulación de la actividad enzimática Control de la actividad enzimática Regulación por cambios en la concentración de enzima Regulación alostérica Modificaciones covalentes reversibles Activación
TEMA 11.- CINÉTICA ENZIMÁTICA
 TEMA 11.- CINÉTICA ENZIMÁTICA Introducción: Cinética enzimática. Ecuación de Michaelis-Menten. Ecuación de Lineweaver-Burk. Reacciones con múltiples substratos. Inhibición enzimática: - Reversible Competitiva.
TEMA 11.- CINÉTICA ENZIMÁTICA Introducción: Cinética enzimática. Ecuación de Michaelis-Menten. Ecuación de Lineweaver-Burk. Reacciones con múltiples substratos. Inhibición enzimática: - Reversible Competitiva.
6. Enzimas - Actividades
 I.E.S. Flavio Irnitano El Saucejo (Sevilla) Curso 2.015 2.016 Departamento de Biología y Geología NIVEL: 2º Bachillerato MATERIA: BIOLOGÍA 6.1. Concepto y estructura. BLOQUE I. CUÁL ES LA COMPOSICIÓN DE
I.E.S. Flavio Irnitano El Saucejo (Sevilla) Curso 2.015 2.016 Departamento de Biología y Geología NIVEL: 2º Bachillerato MATERIA: BIOLOGÍA 6.1. Concepto y estructura. BLOQUE I. CUÁL ES LA COMPOSICIÓN DE
Cinética de Reacciones Catalizadas por Enzimas
 Cinética de Reacciones Catalizadas por Enzimas Las enzimas son biomoleculas que se comportan como catalizadores muy potentes y eficaces de las reacciones químicas en los sistemas biológicos. Una enzima
Cinética de Reacciones Catalizadas por Enzimas Las enzimas son biomoleculas que se comportan como catalizadores muy potentes y eficaces de las reacciones químicas en los sistemas biológicos. Una enzima
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA. FACULTAD DE AGRONOMÍA. ÁREA DE CIENCIAS. SUBÁREA DE CIENCIAS QUÍMICAS. BIOQUÍMICA DICIEMBRE 2015.
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA. FACULTAD DE AGRONOMÍA. ÁREA DE CIENCIAS. SUBÁREA DE CIENCIAS QUÍMICAS. BIOQUÍMICA DICIEMBRE 2015. GUÍA DE ESTUDIO EXAMEN PARCIAL 1 Serie 1 Responder a los siguientes
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA. FACULTAD DE AGRONOMÍA. ÁREA DE CIENCIAS. SUBÁREA DE CIENCIAS QUÍMICAS. BIOQUÍMICA DICIEMBRE 2015. GUÍA DE ESTUDIO EXAMEN PARCIAL 1 Serie 1 Responder a los siguientes
Es la capacidad de realizar un trabajo. En términos bioquímicos: representa la capacidad de cambio, ya que la vida depende de que la energía pueda
 Es la capacidad de realizar un trabajo. En términos bioquímicos: representa la capacidad de cambio, ya que la vida depende de que la energía pueda ser transformada de una forma a otra, cuyo estudio es
Es la capacidad de realizar un trabajo. En términos bioquímicos: representa la capacidad de cambio, ya que la vida depende de que la energía pueda ser transformada de una forma a otra, cuyo estudio es
PRACTICO Nº 3 ENZIMOLOGÍA II
 PRACTICO Nº 3 ENZIMOLOGÍA II I. - INTRODUCCIÓN FACTORES QUE AFECTAN LA ACTIVIDAD ENZIMATICA Para definir la actividad de una preparación enzimática se utiliza en la práctica distintas expresiones. La cantidad
PRACTICO Nº 3 ENZIMOLOGÍA II I. - INTRODUCCIÓN FACTORES QUE AFECTAN LA ACTIVIDAD ENZIMATICA Para definir la actividad de una preparación enzimática se utiliza en la práctica distintas expresiones. La cantidad
BLOQUE I: LAS MOLÉCULAS DE LA VIDA ENZIMAS. 2. Mecanismo de acción y cinética enzimática.
 ENZIMAS 1. Concepto y estructura. 2. Mecanismo de acción y cinética enzimática. 3. Regulación de la actividad enzimática: temperatura, ph, inhibidores. 4. Bibliografía. 5. Preguntas selectividad. Imagen
ENZIMAS 1. Concepto y estructura. 2. Mecanismo de acción y cinética enzimática. 3. Regulación de la actividad enzimática: temperatura, ph, inhibidores. 4. Bibliografía. 5. Preguntas selectividad. Imagen
Cap. 6 Introducción al metabolismo
 Metabolismo = todas las reacciones químicas que ocurren en un organismo. Maneja los recursos de materiales (moléculas) y de energía según las necesidades del organismo. Incluye: Catabolismo = degradación
Metabolismo = todas las reacciones químicas que ocurren en un organismo. Maneja los recursos de materiales (moléculas) y de energía según las necesidades del organismo. Incluye: Catabolismo = degradación
PROTEÍNAS. https://www.youtube.com/watch?v=ff4wchvlw9u
 PROTEÍNAS https://www.youtube.com/watch?v=ff4wchvlw9u QUÉ SON LAS PROTEÍNAS? Son biomóleculas formadas básicamente por carbono, hidrógeno, oxígeno y nitrógeno polímeros lineales construidos a partir de
PROTEÍNAS https://www.youtube.com/watch?v=ff4wchvlw9u QUÉ SON LAS PROTEÍNAS? Son biomóleculas formadas básicamente por carbono, hidrógeno, oxígeno y nitrógeno polímeros lineales construidos a partir de
Cinética enzimática. La velocidad enzimática sigue una curva denominada hipérbola descripta por la Ecuación de Michaelis y Menten:
 Cinética enzimática Hemos visto que la concentración de sustrato es uno de los factores más importantes que determinan la velocidad de una reacción enzimática. La velocidad enzimática sigue una curva denominada
Cinética enzimática Hemos visto que la concentración de sustrato es uno de los factores más importantes que determinan la velocidad de una reacción enzimática. La velocidad enzimática sigue una curva denominada
ENZIMAS. Las enzimas son proteínas con función catalítica
 ENZIMAS Las enzimas son proteínas con función catalítica Las enzimas son catalizadores biológicos que permiten que las reacciones metabólicas ocurran a gran velocidad en condiciones compatibles con la
ENZIMAS Las enzimas son proteínas con función catalítica Las enzimas son catalizadores biológicos que permiten que las reacciones metabólicas ocurran a gran velocidad en condiciones compatibles con la
Catálisis enzimática. Tema 8 (cont)
 Tema 8 (cont) Catálisis enzimática 1 Para entender las enzimas necesitamos dos propiedades termodinámicas de la reacción 1. Diferencia de E libre (ΔG) entre productos y reactantes. Se relaciona con la
Tema 8 (cont) Catálisis enzimática 1 Para entender las enzimas necesitamos dos propiedades termodinámicas de la reacción 1. Diferencia de E libre (ΔG) entre productos y reactantes. Se relaciona con la
Problema 1: Características de las reacciones enzimáticas. Problema 2: Cinética de una enzima alostérica.
 Problema 1: Características de las reacciones enzimáticas Cuál de los siguientes enunciados, acerca de las reacciones catalizadas por enzimas, NO es cierto? A. Las enzimas forman complejos con sus sustratos.
Problema 1: Características de las reacciones enzimáticas Cuál de los siguientes enunciados, acerca de las reacciones catalizadas por enzimas, NO es cierto? A. Las enzimas forman complejos con sus sustratos.
Metabolismo celular I. Reacciones enzimáticas
 Metabolismo celular I Reacciones enzimáticas Reacciones químicas: Son transformaciones, por medio de las cuales unas sustancias se convierten en otras. Podemos distinguir dos grupos: 1) reacciones químicas
Metabolismo celular I Reacciones enzimáticas Reacciones químicas: Son transformaciones, por medio de las cuales unas sustancias se convierten en otras. Podemos distinguir dos grupos: 1) reacciones químicas
TEMA 8. ENZIMAS II. 1. Cinética enzimática 2. Inhibición enzimática 3. Reacciones multisustrato 4. Regulación enzimática. 1. Cinética enzimática.
 TEMA 8. ENZIMAS II 1. Cinética enzimática 2. Inhibición enzimática 3. Reacciones multisustrato 4. Regulación enzimática 1. Cinética enzimática. Los principios generales de la cinética de las reacciones
TEMA 8. ENZIMAS II 1. Cinética enzimática 2. Inhibición enzimática 3. Reacciones multisustrato 4. Regulación enzimática 1. Cinética enzimática. Los principios generales de la cinética de las reacciones
Licenciatura Ingeniería Bioquímica Industrial MANUAL DE PRÁCTICAS DEL LABORATORIO DE INGENIERÍA ENZIMÁTICA
 División de Ciencias Biológicas y de la Salud Departamento de Biotecnología Licenciatura Ingeniería Bioquímica Industrial MANUAL DE PRÁCTICAS DEL LABORATORIO DE INGENIERÍA ENZIMÁTICA Dr. Sergio Huerta
División de Ciencias Biológicas y de la Salud Departamento de Biotecnología Licenciatura Ingeniería Bioquímica Industrial MANUAL DE PRÁCTICAS DEL LABORATORIO DE INGENIERÍA ENZIMÁTICA Dr. Sergio Huerta
PRINCIPIOS DE CINÉTICA ENZIMÁTICA. Dra. Lilian González Segura Departamento de Bioquímica Facultad de Química
 PRINCIPIOS DE CINÉTICA ENZIMÁTICA Dra. Lilian González Segura Departamento de Bioquímica Facultad de Química CINÉTICA Es el estudio de las velocidades de las reacciones, aporta las bases para el entendimiento
PRINCIPIOS DE CINÉTICA ENZIMÁTICA Dra. Lilian González Segura Departamento de Bioquímica Facultad de Química CINÉTICA Es el estudio de las velocidades de las reacciones, aporta las bases para el entendimiento
UNIVERSIDAD PERUANA CAYETANO HEREDIA CENTRO FORMATIVO PREUNIVERSITARIO BIOLOGÍA METABOLISMO
 UNIVERSIDAD PERUANA CAYETANO HEREDIA CENTRO FORMATIVO PREUNIVERSITARIO BIOLOGÍA METABOLISMO METABOLISMO Ciclo interdependendiente, intercambio de E y materia. AUTOTROFOS FOTOSINTETICOS HETEROTROFOS Procesos
UNIVERSIDAD PERUANA CAYETANO HEREDIA CENTRO FORMATIVO PREUNIVERSITARIO BIOLOGÍA METABOLISMO METABOLISMO Ciclo interdependendiente, intercambio de E y materia. AUTOTROFOS FOTOSINTETICOS HETEROTROFOS Procesos
Metabolismo. Catabolismo. Oxidación-reducción 30/09/2009. Clase 5. Energética celular: nutrición y metabolismo
 Clase 5. Energética celular: nutrición y metabolismo Qué permite a los seres vivos tener conductas? 1. Los organismos vivos: Estructura y función. 2. Metabolismo 1. Oxidación reducción. 2. Energía libre.
Clase 5. Energética celular: nutrición y metabolismo Qué permite a los seres vivos tener conductas? 1. Los organismos vivos: Estructura y función. 2. Metabolismo 1. Oxidación reducción. 2. Energía libre.
1.- CONCEPTO DE ENZIMA
 ENZIMAS 1.- CONCEPTO DE ENZIMA Los enzimas son catalizadores muy potentes y eficaces, Químicamente son proteínas Actúan en pequeña cantidad y se recuperan indefinidamente No llevan a cabo reacciones energéticamente
ENZIMAS 1.- CONCEPTO DE ENZIMA Los enzimas son catalizadores muy potentes y eficaces, Químicamente son proteínas Actúan en pequeña cantidad y se recuperan indefinidamente No llevan a cabo reacciones energéticamente
QUE SON? Biocatalizadoras. ENZIMA: griego zymos (fermento)
 Enzimas QUE SON? Biocatalizadoras. ENZIMA: griego zymos (fermento) CATALIZADOR: Sustancia que aumenta la velocidad de una reacción, sin alterarse en el proceso. NATURALEZA QUIMICA: proteica PROPIEDADES
Enzimas QUE SON? Biocatalizadoras. ENZIMA: griego zymos (fermento) CATALIZADOR: Sustancia que aumenta la velocidad de una reacción, sin alterarse en el proceso. NATURALEZA QUIMICA: proteica PROPIEDADES
Generalidades de ENZIMAS
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,007 Generalidades de ENZIMAS Dr. Mynor Leiva 1 ENZIMAS Proteínas
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS FASE I, Unidad Didáctica: BIOQUÍMICA MÉDICA 2º AÑO CICLO ACADÉMICO 2,007 Generalidades de ENZIMAS Dr. Mynor Leiva 1 ENZIMAS Proteínas
Catálisis Enzimática MODELO DE MICHAELIS- MENTEN
 Catálisis Enzimática MODELO DE MICHAELIS- MENTEN Enzima - Sustrato La enzima dihidrofolato reductasa de E. coli con sus dos sustratos, dihidrofolato (derecha) y NADPH (izquierda), unidos al sitio activo.
Catálisis Enzimática MODELO DE MICHAELIS- MENTEN Enzima - Sustrato La enzima dihidrofolato reductasa de E. coli con sus dos sustratos, dihidrofolato (derecha) y NADPH (izquierda), unidos al sitio activo.
Biopolímero s (4831)
 Biopolímero s (4831) 4.3. Conceptos de catálisis química. 4.3.3. Ejemplos de tipos de catálisis. Aplicación a la catálisis enzimática Los iones metálicos como catalizadores Como se dijo anteriormente los
Biopolímero s (4831) 4.3. Conceptos de catálisis química. 4.3.3. Ejemplos de tipos de catálisis. Aplicación a la catálisis enzimática Los iones metálicos como catalizadores Como se dijo anteriormente los
UNIDAD 11. METABOLISMO CELULAR Y DEL SER VIVO
 UNIDAD 11. METABOLISMO CELULAR Y DEL SER VIVO Índice: 1. Las enzimas Definición Influencia de ph y temperatura Cofactores enzimáticos Clasificación de las enzimas 2. La reacción enzimática Complejo enzima-sustrato
UNIDAD 11. METABOLISMO CELULAR Y DEL SER VIVO Índice: 1. Las enzimas Definición Influencia de ph y temperatura Cofactores enzimáticos Clasificación de las enzimas 2. La reacción enzimática Complejo enzima-sustrato
IES Francisco Pacheco
 6. ENZIMAS. 6.1. Concepto y estructura. 6.2. Mecanismo de acción enzimática. 6.3. Cinética enzimática. 6.4. Regulación de la actividad enzimática: temperatura, ph, inhibidores. 6.5. Nomenclatura y clasificación
6. ENZIMAS. 6.1. Concepto y estructura. 6.2. Mecanismo de acción enzimática. 6.3. Cinética enzimática. 6.4. Regulación de la actividad enzimática: temperatura, ph, inhibidores. 6.5. Nomenclatura y clasificación
FISIOLOGÍA GENERAL Jesús Merino Pérez y María José Noriega Borge
 ENZIMAS INTRODUCCIÓN Las enzimas son el grupo más variado y especializado de las proteínas, su función es actuar como catalizadores, permitiendo que las reacciones que transcurren en los seres vivos puedan
ENZIMAS INTRODUCCIÓN Las enzimas son el grupo más variado y especializado de las proteínas, su función es actuar como catalizadores, permitiendo que las reacciones que transcurren en los seres vivos puedan
LA ENERGÍA EN LAS REACCIONES METABÓLICAS
 LA ENERGÍA EN LAS REACCIONES METABÓLICAS ENERGIA DE ACTIVACIÓN. CATALIZADORES ENERGIA DE ACTIVACIÓN. CATALIZADORES REACTIVOS PRODUCTOS ENERGIA DE ACTIVACIÓN. ENZIMAS Las ENZIMAS son proteínas que ACTÚAN
LA ENERGÍA EN LAS REACCIONES METABÓLICAS ENERGIA DE ACTIVACIÓN. CATALIZADORES ENERGIA DE ACTIVACIÓN. CATALIZADORES REACTIVOS PRODUCTOS ENERGIA DE ACTIVACIÓN. ENZIMAS Las ENZIMAS son proteínas que ACTÚAN
