Espectroscopía Infraroja OBJETIVOS * 30/09/2010 * 1
|
|
|
- Lorenzo Velázquez Correa
- hace 5 años
- Vistas:
Transcripción
1 Espectroscopía Infraroja Carolina Jullian M. OBJETIVOS Adquirir principios y conceptos para la correcta formación de una base espectroscópica. Interpretación t adecuada d de los espectros para la obtención de información estructural. A través de la interpretación inicial de compuestos modelos, se finalizará con la elucidación estructural de compuestos desconocidos. La luz es una forma de energía, la cual se propaga en forma de onda La distancia entre cada una de las ondas se le llama longitud de onda * 1
2 La velocidad de propagación de la luz en el espacio es constante para todas las zonas del espectro electromagnético y tiene un valor de 3x10 8 ms -1. La velocidad de la luz c, es el producto de la longitud de onda, por la frecuencia c En general en espectroscopía se utiliza la longitud de onda y sus unidades son: 1Å = m 1nm = 10-9 m 1 m = 10-6 m En IR se utiliza número de onda: 1 1 cm c La energía de la luz, E, se relaciona con la frecuencia por medio de la constante de Planck h, donde E = h Con h = 6.23x10-24 Js m c x s m Hertz( Hz) La frecuencia de la energía absorbida, se relaciona con la energía de transición entre un estado inicial y uno final. E = h E f E i Por lo tanto para que exista una transición, la frecuencia debe corresponder exactamente a la diferencia de energía entre los dos niveles. * 2
3 Si suponemos los movimientos vibracionales de un enlace como un oscilador armónico (resorte) B A La frecuencia de vibración, osc en un sistema A-B, en el cual la masa A es mucho mayor que la masa B, estará dada por la siguiente ecuación: osc = ½ K/m Donde K es la constante de fuerza Cuando la masa A y B son comparables, se utiliza la siguiente ecuación, = (m A xm B / m A + m B ) donde es la masa reducida del sistema, y la frecuencia de oscilación quedará: osc = ½ K/ A medida que aumenta el número de enlaces, aumenta K, causando que la frecuencia de oscilación osc también aumente, C-C < C=C < C C Tipo de enlace Constante de fuerza (g/seg 2 ) calculada (cm -1 ) observada (cm -1 ) h ( m m k m m 1 1 2) 2 C-H 5.0x C-D 5.0x C-C 4.5x C=C 9.7x C C 15.6x C=O 12.1x C-O 5.0x C-N 4.9x O-H 7.0x obs C C > C=C > C-C * 3
4 Si pensamos en la vibración de un enlace C-H como en un resorte, éste se estirará y se contraerá con una cierta frecuencia, describiendo una onda. Este tipo de enlace tiene una frecuencia de 9 x seg -1 Una onda de radiación electromagnética puede transferir su energía a la onda vibracional del enlace C-H, sólo si la frecuencia de la onda electromagnética es igual a la frecuencia vibracional. h La radiación electromagnética deberá tener entonces una longitud de onda: = c / = 3x10 8 ms -1 9x10 13 s -1 Que se traduce a número de onda, (cm -1 ) =[ 1/ ( m)] x =3.33x10-6 m = 3.33 m (cm -1 ) =[ 1/3.33 ( m)] x = 3003 cm -1 * 4
5 Cuando la radiación de ésta frecuencia interactúa con la vibración del enlace C-H, la energía es absorbida y la intensidad de la vibración del enlace aumenta. Luego, después de absorber la energía, el enlace vibra con la misma frecuencia, pero con mayor amplitud, dando entonces las señales en el espectro de IR Una molécula compuesta por n-átomos, tiene 3n grados de libertad, seis de los cuales son de traslación y rotación de la molécula. Nos deja entonces 3n-6 grados de vibración Pero no todos éstos modos de vibración absorben en la zona del infrarrojo. Para que absorban, el enlace debe poseer un momento dipolar diferente en magnitud respecto del estado vibracional excitado. Las vibraciones involucran ya sea un cambio en el largo del enlace, que se conoce como tensión. O un cambio en el ángulo del enlace que se conoce como torsión * 5
6 Los modos vibracionales, tienen nombres descriptivos, como ser de tensión (stretching) simétricas y antisimétricas Los modos vibracionales, tienen nombres descriptivos, como ser de tensión (stretching) simétricas y antisimétricas de torsión (bending) en el plano, tijera (scissoring) rocking Los modos vibracionales, tienen nombres descriptivos, como ser de tensión (stretching) simétricas y antisimétricas de torsión (bending) en el plano, tijera (scissoring) rocking de torsión (bending) fuera del plano, twisting y wagging * 6
7 El formaldehído, molécula de 4 átomos, presentará seis vibraciones fundamentales (12 6 ), las cuales hemos asignado en el espectro. Espectro infrarojo del formaldehido en estado gaseoso, H 2 C=O ip bend. Scissoring str. sim cm str. asim cm cm -1 oop twisting 1150 cm-1 ip bend. Rocking 720 cm -1 Tipo de vibración Frecuencia (cm -1 ) Intensidad C-H alcanos (stretch) s -CH 3 (bend) 1450 y 1375 m -CH 2 (bend) 1465 m alquenos (stretch) m (bend) s aromáticos (stretch) s (fuera del plano) s alquino (stretch) 3300 s aldehído w w * 7
8 C-H rock metilo C-H rock C-H scissoring C-H stret. Tipo de vibración Frecuencia (cm -1 ) Intensidad C=C alqueno m-w aromáticos m-w C C alquino m-w C=O cetona (acíclica) s aldehído s ac. carboxílico s ester s amida s anhídrido 1810 s N=O nitro (R-NO 2 ) s s Tipo de vibración Frecuencia (cm -1 ) Intensidad C-O alcohol,eter m Ester, ac. Carb. O-H alcohol,fenol libre m H-unido m ac. carboxílico m N-H amina primaria y secundaria 3500 m C N nitrilo m * 8
9 En la siguiente carta observamos en las zonas en que aparecen las diferentes bandas de absorción. La sección en azul nos indica las vibraciones stretching, las verdes nos estarían indicando las correspondientes a las vibraciones bending. En los alquenos se observa claramente la separación entre la tensión C-H sp 2 y sp 3. Las absorciones de tensión se observan en azul, las de torsión en verde y los sobretonos en naranja. sustitución tensión rango(cm -1 ) asignación torsión rango(cm -1 ) asignación R-CH=CH =CH2 (2 bandas) C=C =C-H bending R-CH=CHR (cis) =C-H C=C =C-H bending R-CH=CHR =C-H =C-H (trans) 1675 C=C bending =C-H =C-H R 2 C=CH C=C bending R 2 C=CHR =C-H C=C =C-H bending * 9
10 -C C- stret. C-H stret. C-H stret. En bencenos sustituidos es claramente evidente la separación entre los stretching C-H sp 2 y sp 3 C-H stretch (aromatics) In-plane C-H bending C-C stret. Ar. ring Algunas señales angostas y débiles se observan en el rango de 950 a 1250cm -1 que son debidas a vibraciones de torsión en el plano. Sobretonos y combinación de tonos débiles se observan entre cm -1 Sustitucion Ar rango(cm -1 ) asignación Mono-alquil R-C 6 H & =C-H bending oop Di-alquil R 2 -C 6 H 4 Orto Meta Para Para & & C-H bending Oop & ring torsion Tri-alquil R 3 -C 6 H 3 1,2,3-1,2,4 1,3, & & & C-H bending Oop & ring torsion Tetra-alquil R 4 -C 6 H 2 1,2,3,4 1,2,3, =C-H bending oop * 10
11 Di-alquil R 2 -C 6 H 4 Orto Meta Para & & C-H bending Oop & ring torsion C-H stretch (aromatics) C-C stret. Ar. ring Di-alquil R 2 -C 6 H 4 Orto Meta Para & & C-H bending Oop & ring torsion Di-alquil R 2 -C 6 H 4 Orto Meta Para & & C-H bending Oop & ring torsion * 11
12 ALCOHOLES Los alcoholes tienen una señal muy característica entre cm -1. Es una señal ancha e intensa. La absorción mas importante aquí es una señal ancha del OH alrededor de 3350 cm -1 Los alcoholes además tienen una absorción de tensión C-O entre cm -1. AMINAS La señal de tensión del N-H es menos sensitiva que la del O-H En soluciones gaseosas y en soluciones diluidas la absorción del N-H libre se observa entre 3400 a 3500 cm -1 * 12
13 Aminas alifáticas primarias, muestran dos picos bien definidos debido a la tensión simétrica y antisimétrica, separadas alrededor de 80 a 100 cm -1. Aminas secundarias exhiben solo una absorción cercana a los 3420 cm -1. La absorción C-N se encuentra en el mismo rango, 1200 a 1350 cm -1 (aromáticos) y 1000 a 1250 cm -1 (alifáticos) que para las aminas primarias. En las aminas terciarias no se observan las absorciones N-H. Sólo se observan las absorciones C-N, al igual que para las aminas primarias y secundarias. * 13
14 Para las Cetonas la vibración de tensión del grupo carbonilo da una señal intensa entre los 1710 y 1740 cm -1. El momento dipolar de esta función se ve aumentada con la vibración stretching. Por otra parte los sustituyentes alquilo estabilizan el carácter del carbocatión. O CH 3 C CH 3 Una cetona típica muestra una absorción importante C=O a 1715 cm -1 y otra de C-O entre cm -1 C-O ALDEHIDOS C-H stret. aldehido C-H stret. alcano C=O stret. * 14
15 ESTERES Los esteres presentan absorciones del C=O mayores que para cetonas simples. Las absorciones características de los esteres son: C=O 1735 cm -1, C-O 1250 cm -1 y 1050 cm -1 Acidos Carboxílicos Los ácidos carboxílicos existen predominantemente como dímeros formando enlaces por puente de hidrogeno. La absorción stretching del O-H para estos dímeros es muy fuerte y ancha, extendiéndose desde 2500 a 3300 cm -1 La señal ancha bending a 935 cm -1 es típica de especies dimericas Derivados de ácidos carboxílicos Existe una relación entre la reactividad de los derivados y la frecuencia del stretching del carbonilo. Los anhídridos y los haluros de acilo absorben a frecuencias mas altas que las cetonas, mientras que las amidas, relativamente menos reactivas absorben a frecuencias menores. * 15
16 Aquí observamos el efecto inductivo del sustituyente sobre la frecuencia de tensión del carbonilo En el caso de los anhidridos, se observan dos absorciones correspondientes a la tensión simétrica y antisimétrica del C=O. La absorción asimétrica es mas intensa en el caso de anhídridos acíclicos. * 16
17 Las AMIDAS presentan absorciones intensas del C=O a menor frecuencia que en cetonas, debido a la conjugación pi-pi con la amida. En la región del C=O aparecen dos bandas intensas, donde la de mayor frecuencia (banda I de la amida) es esencialmente stretching del C=O, la señal de menor frecuencia (amida II) es básicamente bending N-H. Las amidas secundarias presentan solo una absorción N-H y las absorciones de la amida I&II aparecen a frecuencias levemente menores. Las amidas terciarias no presentan la absorción debida al N-H, y sólo se observa la señal de la amida I del carbonilo. * 17
18 Analizando un espectro IR Paso 1 Espectrosopía Infrarroja Chequear por la presencia del grupo carbonilo a 1715 cm -1 Si la molécula esta conjugada, la señal del carbonilo se desplazará 30 cm -1 a menor energía. Si se encuentra presente la absorción del carbonilo: Acidos carboxílicos -chequear por grupo OH. (absorción ancha alrededor cm -1 ) Amidas -chequear por grupo NH. (una o dos absorciones alrededor de 3500 cm -1 ) Analizando un espectro IR Espectrosopía Infrarroja Esteres anhídridos aldehídos cetonas -chequear por C-O. (absorciones medias alrededor cm -1 ) -chequear por dos señales C=O alrededor 1810 y 1760 cm -1 -chequear señales C-H del aldehido (absorciones alrededor de 2850 y 2750 cm -1 ) -cuando todos los grupos anteriores han sido eliminados C 4 H 8 O 2 Dimetil OH Stretch C=O Stretch C-O Stretch * 18
19 Analizando un espectro IR Paso 2 Espectrosopía Infrarroja Si el grupo carbonilo esta ausente, chequear por alcohol, amina o eter. Alcohol & fenol -chequear por grupo OH absorción ancha entre cm -1 (se confirma con banda C-O alrededor cm -1. Aminas -chequear por tensión N-H cercano a 3500 cm -1 N-H scissoring cm -1 N-H bending 800 cm -1 eter -chequear por C-O cm -1 C 4 H 11 N NH 2 Stretch N-H Si Scissor CH 3 CH 2 C-N Stretch Aliphatic -C-H N-H OOP Bending Espectrosopía Infrarroja Analizando un espectro IR Paso 3. Refinar la estructura buscando dobles, triples enlaces y nitro. Si el grupo carbonilo esta ausente, chequear por alcohol, amina o eter. Doble enlace -C=C, y C C se observan > 3000 cm -1 alqueno C=C banda débil 1650 cm -1 aromático C=CC cm -1 Triple enlace -C N, banda angosta a 2250 cm -1 R-C C-R, debil angosta 2150 cm -1 R-C C-H cm -1 terminal 3300 cm -1 nitro -dos absorciones intensas cm -1 y cm -1. * 19
20 C 3 H 4 O Acetylene C C Aliphatic -C-H OH Bonded Terminal Alkyne C-H C-O Stretch HC CCH 2 OH C 7 H 5 N Aromatic Overtones Unsat (=C) Nitrile (C N) Aromatic (C=C) Aromatic Monsubstitution Analizando un espectro IR Paso 4. Espectrosopía Infrarroja Si ninguna de las señales anteriores se encuentra, entonces el compuesto es un hidrocarburo. hidrocarburos -absorciones cercanas a 3000 cm -1 * 20
21 EJERCICIOS C 10 H 12 O d 5 3 m 1 m 2 m C 9 H 9 N * 21
22 C 6 H 10 O s d d t m Este compuesto, presenta las siguientes absorciones características en el IR. Una intensa a los 1725 cm -1 y una menos intensa a los 1640 cm -1. Además de un par de señales a 2760 y 2850 cm -1 * 22
Espectro Electromagnético
 Espectro Electromagnético En las moléculas orgánicas se observan vibraciones moleculares con energías que corresponden a la porción del infrarrojo del espectro electromagnético. Describiendo de la forma
Espectro Electromagnético En las moléculas orgánicas se observan vibraciones moleculares con energías que corresponden a la porción del infrarrojo del espectro electromagnético. Describiendo de la forma
ANÁLISIS DE ESPECTROS
 EFECTOS DE CONJUGACIÓN Y TAMAÑO DE ANILLO EN C=O ALQUENOS Y AROMÁTICOS ( ESTIRAMIENTO C=C ) O-H 3600 N-H 3400 C-H 3000 C=N = 2250 C=C = 2150 C=O 1715 C=C 1650 C-O 1100 ANÁLISIS DE ESPECTROS CONJUGACIÓN
EFECTOS DE CONJUGACIÓN Y TAMAÑO DE ANILLO EN C=O ALQUENOS Y AROMÁTICOS ( ESTIRAMIENTO C=C ) O-H 3600 N-H 3400 C-H 3000 C=N = 2250 C=C = 2150 C=O 1715 C=C 1650 C-O 1100 ANÁLISIS DE ESPECTROS CONJUGACIÓN
INSPECCIÓN DEL ESPECTRO
 IDROCARBUROS (ABSORCIONES C- ) ALCOOLES ÁCIDOS (ABSORCIONES O- ) AMINAS (ABSORCIONES N- ) O- 3600 N- 3400 C- 3000 C=N = 2250 C=C = 2150 C=O 1715 C=C 1650 C-O 1100 INSPECCIÓN DEL ESPECTRO Regiones Típicas
IDROCARBUROS (ABSORCIONES C- ) ALCOOLES ÁCIDOS (ABSORCIONES O- ) AMINAS (ABSORCIONES N- ) O- 3600 N- 3400 C- 3000 C=N = 2250 C=C = 2150 C=O 1715 C=C 1650 C-O 1100 INSPECCIÓN DEL ESPECTRO Regiones Típicas
VIBRACIONES CARACTERÍSTICAS DE ALGUNAS DE LAS FUNCIONES QUÍMICA-ORGÁNICAS MÁS IMPORTANTES.
 VIBRACIONES CARACTERÍSTICAS DE ALGUNAS DE LAS FUNCIONES QUÍMICA-ORGÁNICAS MÁS IMPORTANTES. ALCANOS NORMALES (LINEALES) En todos los alcanos normales o ramificados se espera encontrar solo estiramientos
VIBRACIONES CARACTERÍSTICAS DE ALGUNAS DE LAS FUNCIONES QUÍMICA-ORGÁNICAS MÁS IMPORTANTES. ALCANOS NORMALES (LINEALES) En todos los alcanos normales o ramificados se espera encontrar solo estiramientos
ESPECTROSCOPIA INFRARROJA. Prof. Dr. Alberto Postigo
 ESPECTROSCOPIA INFRARROJA Prof. Dr. Alberto Postigo 1 2 Transición energética en el IR 3 A.-TEORIA DE LA ESPECTROSCOPIA IR (cm 1 ) = 1 (cm) (z) = c (cm) = c (cm/sec) (cm) cm 1 = 1 ( ) x 10,000 and = 1-1
ESPECTROSCOPIA INFRARROJA Prof. Dr. Alberto Postigo 1 2 Transición energética en el IR 3 A.-TEORIA DE LA ESPECTROSCOPIA IR (cm 1 ) = 1 (cm) (z) = c (cm) = c (cm/sec) (cm) cm 1 = 1 ( ) x 10,000 and = 1-1
Tema 7: Espectroscopia Vibracional (IR)
 Tabla 1. El espectro electromagnético Región Longitud de onda Energía de excitación Tipo de excitación Rayos x, rayos cósmicos 286 (Kcal/mol) Ultravioleta Visible Infrarrojo próximo Infrarrojo
Tabla 1. El espectro electromagnético Región Longitud de onda Energía de excitación Tipo de excitación Rayos x, rayos cósmicos 286 (Kcal/mol) Ultravioleta Visible Infrarrojo próximo Infrarrojo
Espectroscopía IR Parte II. Química Orgánica III Primer Semestre 2016 Facultad de CCQQ y Farmacia USAC
 Espectroscopía IR Parte II Química Orgánica III Primer Semestre 2016 Facultad de CCQQ y Farmacia USAC Grupos funcionales que presentan absorción en la región 4000-3000 cm En esta región se encuentran las
Espectroscopía IR Parte II Química Orgánica III Primer Semestre 2016 Facultad de CCQQ y Farmacia USAC Grupos funcionales que presentan absorción en la región 4000-3000 cm En esta región se encuentran las
ESPECTROSCOPíA INFRARROJA
 ESPECTROSCOPíA INFRARROJA Química Orgánica 1 Facultad de Farmacia y Bioquímica UBA 2016 Autor: Dra. Isabel Perillo 1 Espectro electromagnético Unidades de l usadas: para UV-visible: nm (mm): 10-9 m para
ESPECTROSCOPíA INFRARROJA Química Orgánica 1 Facultad de Farmacia y Bioquímica UBA 2016 Autor: Dra. Isabel Perillo 1 Espectro electromagnético Unidades de l usadas: para UV-visible: nm (mm): 10-9 m para
ESPECTROSCOPIA ULTRAVIOLETA CONTINUACIÓN. Prof. Dr. Alberto Postigo
 ESPETROSOPIA ULTRAVIOLETA ONTINUAIÓN Prof. Dr. Alberto Postigo Fuerza de dipolo y momento de transición dipolar eléctrico La magnitud de una banda de absorción se caracteriza por max a una longitudde onda
ESPETROSOPIA ULTRAVIOLETA ONTINUAIÓN Prof. Dr. Alberto Postigo Fuerza de dipolo y momento de transición dipolar eléctrico La magnitud de una banda de absorción se caracteriza por max a una longitudde onda
TALLER DE ESPECTROSCOPIA
 TALLER DE ESPECTROSCOPIA I. OBJETIVOS a) Conocer los principios fundamentales que rigen la interacción energía-materia (radiación electromagnética-moléculas) en uno de los métodos espectroscópicos más
TALLER DE ESPECTROSCOPIA I. OBJETIVOS a) Conocer los principios fundamentales que rigen la interacción energía-materia (radiación electromagnética-moléculas) en uno de los métodos espectroscópicos más
Unidad II: Espectrometría IR
 Unidad II: Espectrometría IR Primera parte Química Orgánica III Primer Semestre 2016 Facultad de CC.QQ. y Farmacia, USAC Radiación Infrarroja Este tipo de radiación se presenta en un intervalo de longitud
Unidad II: Espectrometría IR Primera parte Química Orgánica III Primer Semestre 2016 Facultad de CC.QQ. y Farmacia, USAC Radiación Infrarroja Este tipo de radiación se presenta en un intervalo de longitud
Espectro Electromagnético
 1 Espectro Electromagnético La luz es radiación electromagnética y está compuesta por una parte eléctrica y otra magnética. Las particulas subatómicas, electrones y fotones, tienen propiedades de partículas
1 Espectro Electromagnético La luz es radiación electromagnética y está compuesta por una parte eléctrica y otra magnética. Las particulas subatómicas, electrones y fotones, tienen propiedades de partículas
ESPECTROSCOPÍA INFRARROJA
 MÉTODOS 2: ESPECTROSCOPÍA INFRARROJA Universidad Pedagógica Nacional Facultad de Ciencia y Tecnología Departamento de Química Julie Benavides Melo 2 CONTENIDOS 3 CONTENIDOS 4 CONTENIDOS ÁREAS TEMÁTICAS
MÉTODOS 2: ESPECTROSCOPÍA INFRARROJA Universidad Pedagógica Nacional Facultad de Ciencia y Tecnología Departamento de Química Julie Benavides Melo 2 CONTENIDOS 3 CONTENIDOS 4 CONTENIDOS ÁREAS TEMÁTICAS
Grupos funcionales Series homólogas
 Grupos funcionales Series homólogas Grupo funcional: Es un átomo o grupo de átomos unidos de manera característica y que determinan, preferentemente, las propiedades del compuesto en que están presentes.
Grupos funcionales Series homólogas Grupo funcional: Es un átomo o grupo de átomos unidos de manera característica y que determinan, preferentemente, las propiedades del compuesto en que están presentes.
Práctica 4. Espectroscopia IR y Análisis elemental
 Laboratorio de Química de Coordinación Práctica 4. Espectroscopia IR y Análisis elemental Parte II: Las técnicas Tarea previa 1. Leer los fundamentos teóricos de la práctica 2. La molécula de agua (H2O)
Laboratorio de Química de Coordinación Práctica 4. Espectroscopia IR y Análisis elemental Parte II: Las técnicas Tarea previa 1. Leer los fundamentos teóricos de la práctica 2. La molécula de agua (H2O)
SEGUNDO DE BACHILLERATO QUÍMICA. Simple C-C sp 3. Doble C=C sp 2. Triple C C
 TEMA 10. QUÍMICA ORGÁNICA PROPIEDADES GENERALES - Solubilidad: se disuelven generalmente en otros compuestos orgánicos, como éter, cloroformo o benceno - Estabilidad: suelen descomponerse a temperaturas
TEMA 10. QUÍMICA ORGÁNICA PROPIEDADES GENERALES - Solubilidad: se disuelven generalmente en otros compuestos orgánicos, como éter, cloroformo o benceno - Estabilidad: suelen descomponerse a temperaturas
La Mecánica Cuántica. La Espectroscopia Infrarroja
 La Mecánica Cuántica. La Espectroscopia Infrarroja 1. La Espectroscopia Infrarroja La luz que ven nuestros ojos no es más que una parte del espectro electromagnético. La luz se puede considerar como un
La Mecánica Cuántica. La Espectroscopia Infrarroja 1. La Espectroscopia Infrarroja La luz que ven nuestros ojos no es más que una parte del espectro electromagnético. La luz se puede considerar como un
Unidad I: Diversidad de compuestos orgánicos, isomería y reactividad.
 Unidad I: Diversidad de compuestos orgánicos, isomería y reactividad. GRUPOS FUNCIONALES El átomo, o grupos de ellos, que confiere a un compuesto propiedades particulares se denomina grupo funcional.
Unidad I: Diversidad de compuestos orgánicos, isomería y reactividad. GRUPOS FUNCIONALES El átomo, o grupos de ellos, que confiere a un compuesto propiedades particulares se denomina grupo funcional.
ESPECTROSCOPÍA INTERACCIÓN RADIACIÓN-MATERIA. Es el laboratorio de la química cuántica
 ESPECTROSCOPÍA INTERACCIÓN RADIACIÓN-MATERIA Es el laboratorio de la química cuántica RADIACIÓN ELECTROMAGNÉTICA E = h n c = nl La energía aumenta Cómo interactúa con la materia la radiación según su energía
ESPECTROSCOPÍA INTERACCIÓN RADIACIÓN-MATERIA Es el laboratorio de la química cuántica RADIACIÓN ELECTROMAGNÉTICA E = h n c = nl La energía aumenta Cómo interactúa con la materia la radiación según su energía
Práctica 6 IDENTIFICACIÓN DE CONTAMINANTES MEDIANTE ESPECTROSCOPÍA INFRARROJA
 Práctica 6 IDENTIFICACIÓN DE CONTAMINANTES MEDIANTE ESPECTROSCOPÍA INFRARROJA 1. Objetivo Familiarizarse con los fundamentos de la identificación de moléculas a partir de su espectro de absorción infrarrojo.
Práctica 6 IDENTIFICACIÓN DE CONTAMINANTES MEDIANTE ESPECTROSCOPÍA INFRARROJA 1. Objetivo Familiarizarse con los fundamentos de la identificación de moléculas a partir de su espectro de absorción infrarrojo.
Haluro de alcanoilo. Síntesis
 DERIVADOS DE LOS ÁCIDOS CARBOXÍLICOS: HALUROS DE ALCANOIDES Y ANHÍDRIDOS Los acidos carboxilicos son compuestos orgánicos que contienen uno, dos o mas grupos carboxílico, R-COOH Haluro de alcanoilo Anhídridos
DERIVADOS DE LOS ÁCIDOS CARBOXÍLICOS: HALUROS DE ALCANOIDES Y ANHÍDRIDOS Los acidos carboxilicos son compuestos orgánicos que contienen uno, dos o mas grupos carboxílico, R-COOH Haluro de alcanoilo Anhídridos
INDICE DE DEFICIENCIA DE HIDRÓGENO TEORIA BÁSICA DE ESPECTROSCOPÍA INFRAROJA
 INDIE DE DEFIIENIA DE HIDRÓGENO Y TEORIA BÁSIA DE ESPETROSOPÍA INFRAROJA QUE SE PUEDE SABER DE UNA FÓRMULA MÍNIMA DE UN OMPUESTO? SE PUEDE DETERMINAR EL NUMERO DE ANILLOS Y DOBLES ENLAES. Hidrucarburos
INDIE DE DEFIIENIA DE HIDRÓGENO Y TEORIA BÁSIA DE ESPETROSOPÍA INFRAROJA QUE SE PUEDE SABER DE UNA FÓRMULA MÍNIMA DE UN OMPUESTO? SE PUEDE DETERMINAR EL NUMERO DE ANILLOS Y DOBLES ENLAES. Hidrucarburos
TABLA IR-I ALCANOS. ν CH δ CH
 Grupo º de onda (cm -1 ) Intensidad 1 1 mol l cm c TABLA I-I ALAOS h Origen otas 2970~2950 ch 70 ν as - 3 (1) - 3 2730 2820 (ε 15 21) en -Me, ausente en -Et. 2880~2860 m 30 ν s - 3 2830 2815 (ε 35 75)
Grupo º de onda (cm -1 ) Intensidad 1 1 mol l cm c TABLA I-I ALAOS h Origen otas 2970~2950 ch 70 ν as - 3 (1) - 3 2730 2820 (ε 15 21) en -Me, ausente en -Et. 2880~2860 m 30 ν s - 3 2830 2815 (ε 35 75)
Contenidos. Características del carbono Tipos de hibridación y enlace Formulación y nomenclatura de compuestos orgánicos
 QUIMICA ORGANICA Contenidos Características del carbono Tipos de hibridación y enlace Formulación y nomenclatura de compuestos orgánicos Características del Carbono Electronegatividad Enlace covalente
QUIMICA ORGANICA Contenidos Características del carbono Tipos de hibridación y enlace Formulación y nomenclatura de compuestos orgánicos Características del Carbono Electronegatividad Enlace covalente
Sencillo C C Doble C = C Triple C C
 FORMULACIÓN ORGÁNICA Existe un nº inmenso de compuestos del carbono, por lo que se impone una clasificación y sistematización para su estudio. Las causas de tan amplia variedad De compuestos la encontramos
FORMULACIÓN ORGÁNICA Existe un nº inmenso de compuestos del carbono, por lo que se impone una clasificación y sistematización para su estudio. Las causas de tan amplia variedad De compuestos la encontramos
Resumen de la clase anterior
 Grupos Funcionales Resumen de la clase anterior sp 3 sp 2 sp Elemento de baja electronegatividad Capaz de hibridar electrones Carbono Hidrógeno Hidrocarburos Alifáticos Alicíclicos Aromáticos Alcanos Alquenos
Grupos Funcionales Resumen de la clase anterior sp 3 sp 2 sp Elemento de baja electronegatividad Capaz de hibridar electrones Carbono Hidrógeno Hidrocarburos Alifáticos Alicíclicos Aromáticos Alcanos Alquenos
QUIMICA ORGANICA DE BIOPROCESOS. CEBI_A3_ 4: Espectroscopía (1º parte)
 CARRERA DE ESPECIALIZACION EN BIOTECNOLOGIA INDUSTRIAL FCEyN-INTI Materia de Articulación CEBI_A3 QUIMICA ORGANICA DE BIOPROCESOS Docente a cargo: Dra. Silvia Flores CEBI_A3_ 4: Espectroscopía (1º parte)
CARRERA DE ESPECIALIZACION EN BIOTECNOLOGIA INDUSTRIAL FCEyN-INTI Materia de Articulación CEBI_A3 QUIMICA ORGANICA DE BIOPROCESOS Docente a cargo: Dra. Silvia Flores CEBI_A3_ 4: Espectroscopía (1º parte)
UNIVERSIDAD DE PUERTO RICO RECINTO DE RÍO PIEDRAS DEPARTAMENTO DE QUÍMICA QUÍMICA ORGÁNICA II (QUIM 3032)
 QUÍMICA RGÁNICA II (QUIM 3032) PRIMER EXAMEN PARCIAL UNIVERSIDAD DE PUERT RIC RECINT DE RÍ PIEDRAS DEPARTAMENT DE QUÍMICA 25 DE FEBRER DE 2016 SECCIÓN: NMBRE: NÚM. DE ESTUDIANTE: El examen consta de 13
QUÍMICA RGÁNICA II (QUIM 3032) PRIMER EXAMEN PARCIAL UNIVERSIDAD DE PUERT RIC RECINT DE RÍ PIEDRAS DEPARTAMENT DE QUÍMICA 25 DE FEBRER DE 2016 SECCIÓN: NMBRE: NÚM. DE ESTUDIANTE: El examen consta de 13
QUIMICA ORGANICA I GUIA DE NOMENCLATURA
 UNIVERSIDAD NACIONAL DE SAN LUIS Facultad de Química, Bioquímica y Farmacia Área de Química Orgánica Dr. Antonio T. D Arcangelo QUIMICA ORGANICA I GUIA DE NOMENCLATURA FARMACIA EQUIPO DOCENTE Profesor
UNIVERSIDAD NACIONAL DE SAN LUIS Facultad de Química, Bioquímica y Farmacia Área de Química Orgánica Dr. Antonio T. D Arcangelo QUIMICA ORGANICA I GUIA DE NOMENCLATURA FARMACIA EQUIPO DOCENTE Profesor
Química. Hibridación de Orbitales Atómicos en el Carbono
 Química Hibridación de Orbitales Atómicos en el Carbono La estructura electrónica de los átomos que constituyen una molécula orgánica determina la estructura tridimensional de ésta y sus propiedades. sp
Química Hibridación de Orbitales Atómicos en el Carbono La estructura electrónica de los átomos que constituyen una molécula orgánica determina la estructura tridimensional de ésta y sus propiedades. sp
La Espectroscopía de Infrarrojo. Infrarrojo. Los enlaces y el infrarrojo. Espectroscopia de Infrarrojo. Espectroscopia de Infrarrojo
 Los enlaces y el infrarrojo La Espectroscopía de Infrarrojo hν IR d1 d2 Baja energía Alta energía María Font.. Dpto. Química Orgánica y Farmacéutica. Universidad de Navarra 1 María Font.. Dpto. Química
Los enlaces y el infrarrojo La Espectroscopía de Infrarrojo hν IR d1 d2 Baja energía Alta energía María Font.. Dpto. Química Orgánica y Farmacéutica. Universidad de Navarra 1 María Font.. Dpto. Química
FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS ORGÁNICOS
 FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS ORGÁNICOS.Índice 1. Generalidades 2. Hidrocarburos: 2.1 Alcanos 2.2 Alquenos 2.3 Alquinos 2.4 Radicales 2.5 Hidrocarburos ramificados 2.6 Hidrocarburos cíclicos
FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS ORGÁNICOS.Índice 1. Generalidades 2. Hidrocarburos: 2.1 Alcanos 2.2 Alquenos 2.3 Alquinos 2.4 Radicales 2.5 Hidrocarburos ramificados 2.6 Hidrocarburos cíclicos
2ª Parte: Estructura y reactividad de
 2ª Parte: Estructura y reactividad de los compuestos CMPUESTS orgánicos. CARBNÍLICS 2.- Principales familias de compuestos orgánicos: - Hidrocarburos alifáticos: alcanos, alquenos y alquinos. - Hidrocarburos
2ª Parte: Estructura y reactividad de los compuestos CMPUESTS orgánicos. CARBNÍLICS 2.- Principales familias de compuestos orgánicos: - Hidrocarburos alifáticos: alcanos, alquenos y alquinos. - Hidrocarburos
ESPECTROSCOPÍA EJEMPLOS DE ELUCIDACION ESTRUCTURAL DE COMPUESTOS. Elucidación estructural: Ejemplo 1 Dados los siguientes espectros:
 ESPECTROSCOPÍA EJEMPLOS DE ELUCIDACION ESTRUCTURAL DE COMPUESTOS Elucidación estructural: Ejemplo 1 Dados los siguientes espectros: 1) Empezaremos por encontrar la formula molecular, pues no la tenemos.
ESPECTROSCOPÍA EJEMPLOS DE ELUCIDACION ESTRUCTURAL DE COMPUESTOS Elucidación estructural: Ejemplo 1 Dados los siguientes espectros: 1) Empezaremos por encontrar la formula molecular, pues no la tenemos.
INTRODUCCION A LA NOMENCLATURA E ISOMERIA DE LOS COMPUESTOS ORGANICOS
 INTRODUCCION A LA NOMENCLATURA E ISOMERIA DE LOS COMPUESTOS ORGANICOS Extractado de la Guía de Problemas de Química Orgánica I por la Dra. Diana Bekerman Fórmulas y representación de estructuras químicas
INTRODUCCION A LA NOMENCLATURA E ISOMERIA DE LOS COMPUESTOS ORGANICOS Extractado de la Guía de Problemas de Química Orgánica I por la Dra. Diana Bekerman Fórmulas y representación de estructuras químicas
(( )) Tema 5: Técnicas espectroscópicas: Espectrofotometría. visible Infrarrojo. Ultravioleta. Espectro de emisión de los cuerpos en equilibrio
 Tema 5: Técnicas espectroscópicas: Espectrofotometría 0 22 Hz Frecuencia 0 4 Hz 0 3 Hz γ X UV IR micro radio Rayos γ (gamma) λ < pm Rayos X pm-0nm Visible 400-800nm Ultravioleta 0-400 nm Longitud de onda
Tema 5: Técnicas espectroscópicas: Espectrofotometría 0 22 Hz Frecuencia 0 4 Hz 0 3 Hz γ X UV IR micro radio Rayos γ (gamma) λ < pm Rayos X pm-0nm Visible 400-800nm Ultravioleta 0-400 nm Longitud de onda
Química Orgánica Grupos funcionales con oxígeno o nitrógeno
 Química rgánica Grupos funcionales con oxígeno o nitrógeno IES La Magdalena. Avilés. Asturias La parte carbonada constituye el esqueleto fundamental de las moléculas orgánicas. En esta estructura básica
Química rgánica Grupos funcionales con oxígeno o nitrógeno IES La Magdalena. Avilés. Asturias La parte carbonada constituye el esqueleto fundamental de las moléculas orgánicas. En esta estructura básica
Tablas de Espectroscopía Infrarroja. Elaboradas por: Francisco Rojo Callejas
 Tablas de Espectroscopía Infrarroja Elaboradas por: Francisco ojo allejas Figura I-1 egiones básicas de un espectro de Infrarrojo 4000 3000 2000 1500 0 (cm -1 ) 500 y >N y N N * * * y y N, * * de> y -
Tablas de Espectroscopía Infrarroja Elaboradas por: Francisco ojo allejas Figura I-1 egiones básicas de un espectro de Infrarrojo 4000 3000 2000 1500 0 (cm -1 ) 500 y >N y N N * * * y y N, * * de> y -
1 ANÁLISIS DE COMPUESTOS ORGÁNICOS
 1 ANÁLISIS DE COMPUESTOS ORGÁNICOS 1.1. EL ANÁLISIS DE COMPUESTOS ORGÁNICOS Una de las actividades más apasionantes que realiza el químico, es cuando se encuentra con una sustancia desconocida; inmediatamente
1 ANÁLISIS DE COMPUESTOS ORGÁNICOS 1.1. EL ANÁLISIS DE COMPUESTOS ORGÁNICOS Una de las actividades más apasionantes que realiza el químico, es cuando se encuentra con una sustancia desconocida; inmediatamente
Tabla de Preferencia de Grupos Funcionales de Química Orgánica
 Tabla de Preferencia de Grupos Funcionales de Química Orgánica Función Química Ácido Carboxílico Éster Amida Aldehído Cetona Alcohol Amina Fórmula Grupo General Funcional O - COOH R C OH O -COO- R C O
Tabla de Preferencia de Grupos Funcionales de Química Orgánica Función Química Ácido Carboxílico Éster Amida Aldehído Cetona Alcohol Amina Fórmula Grupo General Funcional O - COOH R C OH O -COO- R C O
TEMA 3. Grupos funcionales con enlaces múltiples.
 TEMA 3. Grupos funcionales con enlaces múltiples. Alquenos. Alquinos. Compuestos aromáticos. El grupo carbonilo. Aldehídos. Cetonas. Ácidos carboxílicos. Ésteres. Anhídridos. Amidas Tioésteres, Fosfoésteres,
TEMA 3. Grupos funcionales con enlaces múltiples. Alquenos. Alquinos. Compuestos aromáticos. El grupo carbonilo. Aldehídos. Cetonas. Ácidos carboxílicos. Ésteres. Anhídridos. Amidas Tioésteres, Fosfoésteres,
NOMENCLATURA Y FORMULACION
 NOMENCLATURA Y FORMULACION RESUMEN NORMAS IUPAC La nomenclatura de compuestos orgánicos puede llegar a ser extraordinariamente compleja. En este seminario sólo se pretende dar unas nociones muy elementales
NOMENCLATURA Y FORMULACION RESUMEN NORMAS IUPAC La nomenclatura de compuestos orgánicos puede llegar a ser extraordinariamente compleja. En este seminario sólo se pretende dar unas nociones muy elementales
COLEGIO SAN JOSÉ - Hijas de María Auxiliadora C/ Emilio Ferrari, 87 - Madrid Departamento de Ciencias Naturales
 TEMA 3. FORMULACIÓN ORGÁNICA EJERCICIOS 3. Grupos funcionales 1. Se dan las siguientes moléculas utilizando su fórmula semidesarrollada. Indica a qué familia pertenecen y escribe la fórmula desarrollada
TEMA 3. FORMULACIÓN ORGÁNICA EJERCICIOS 3. Grupos funcionales 1. Se dan las siguientes moléculas utilizando su fórmula semidesarrollada. Indica a qué familia pertenecen y escribe la fórmula desarrollada
ESPECTROSCOPÍA MOLECULAR
 ESPECTROSCOPÍA MOLECULAR INTERACCIÓN RADIACIÓN-MATERIA Es el laboratorio de la química cuántica RADIACIÓN ELECTROMAGNÉTICA E = h n c = nl La energía aumenta Nota: ṽ = 1/l E = hcṽ ṽ es proporcional a la
ESPECTROSCOPÍA MOLECULAR INTERACCIÓN RADIACIÓN-MATERIA Es el laboratorio de la química cuántica RADIACIÓN ELECTROMAGNÉTICA E = h n c = nl La energía aumenta Nota: ṽ = 1/l E = hcṽ ṽ es proporcional a la
Tema 1 Introducción. Universidad San Pablo CEU 1
 Tema 1 Introducción Revisión de nomenclatura de hidrocarburos. Estructura y nomenclatura de grupos funcionales. Principales tipos de reacciones orgánicas. Mecanismos de reacción. Rupturas homolíticas yheterolíticas.
Tema 1 Introducción Revisión de nomenclatura de hidrocarburos. Estructura y nomenclatura de grupos funcionales. Principales tipos de reacciones orgánicas. Mecanismos de reacción. Rupturas homolíticas yheterolíticas.
MATERIAL 09 TEMA: ESPECTROSCOPÍA DE ABSORCION MOLECULAR EN EL ULTRAVIOLETA
 MATERIAL 09 TEMA: ESPECTROSCOPÍA DE ABSORCION MOLECULAR EN EL ULTRAVIOLETA y EL VISIBLE La espectroscopia de absorción molecular en el ultravioleta y visible se emplea en el análisis cuantitativo y es
MATERIAL 09 TEMA: ESPECTROSCOPÍA DE ABSORCION MOLECULAR EN EL ULTRAVIOLETA y EL VISIBLE La espectroscopia de absorción molecular en el ultravioleta y visible se emplea en el análisis cuantitativo y es
QUÍMICA ORGÁNICA.QUÍMICA DEL CARBONO
 QUÍMICA ORGÁNICA.QUÍMICA DEL CARBONO ENLACES DEL CARBONO ENLACE SIMPLE C-C ENLACE DOBLE C=C ENLACE TRIPLE C C TIPO DE ORBITAL sp 3 sp 2 sp Nº DE ORBITALES HÍBRIDOS ORBITALES P SIN HIBRIDAR GEOMETRÍA DE
QUÍMICA ORGÁNICA.QUÍMICA DEL CARBONO ENLACES DEL CARBONO ENLACE SIMPLE C-C ENLACE DOBLE C=C ENLACE TRIPLE C C TIPO DE ORBITAL sp 3 sp 2 sp Nº DE ORBITALES HÍBRIDOS ORBITALES P SIN HIBRIDAR GEOMETRÍA DE
Elucidación estructural: Resolución de problemas
 Objetivos: Elucidación estructural: Resolución de problemas Composición: átomos presentes y su proporción en la molécula, lo que se traduce en la obtención de una formula molecular. Composición elemental
Objetivos: Elucidación estructural: Resolución de problemas Composición: átomos presentes y su proporción en la molécula, lo que se traduce en la obtención de una formula molecular. Composición elemental
FORMULACIÓN DE QUÍMICA ORGÁNICA 1- HIDROCARBUROS DE CADENA ABIERTA A) ALCANOS
 FORMULACIÓN DE QUÍMICA ORGÁNICA 1- HIDROCARBUROS DE CADENA ABIERTA A) ALCANOS Fórmula molecular C n H 2n+2 Sufijo ANO. Para los alcanos de cadena lineal, si tienen 1 C se utiliza el prefijo met-; 2 C et-;
FORMULACIÓN DE QUÍMICA ORGÁNICA 1- HIDROCARBUROS DE CADENA ABIERTA A) ALCANOS Fórmula molecular C n H 2n+2 Sufijo ANO. Para los alcanos de cadena lineal, si tienen 1 C se utiliza el prefijo met-; 2 C et-;
Espectrometría de masas. Complemento
 Espectrometría de masas Complemento Alcanos Se observan los iones moleculares, aunque con baja intensidad El patrónde fragmentación presenta picos que difieren en 14 unidades de masa (pérdida de CH 2
Espectrometría de masas Complemento Alcanos Se observan los iones moleculares, aunque con baja intensidad El patrónde fragmentación presenta picos que difieren en 14 unidades de masa (pérdida de CH 2
CUESTIONES DE ORGÁNICA
 CUESTIONES DE ORGÁNICA 1.- Escriba la fórmula desarrollada de cada uno de los siguientes compuestos y nombre el grupo funcional que presentan. a) CH 3 CH 2 CHO b) CH 3 CH 2 CONH 2 c) CH 3 CH 2 COOCH 2
CUESTIONES DE ORGÁNICA 1.- Escriba la fórmula desarrollada de cada uno de los siguientes compuestos y nombre el grupo funcional que presentan. a) CH 3 CH 2 CHO b) CH 3 CH 2 CONH 2 c) CH 3 CH 2 COOCH 2
c = λν λ: cm; ν: ciclos/seg E = hν c: velocidad de la luz (en el vacío: 3 x 1010 cm/seg) E = hc/ν h: cte. de Planck (6.62 x 1027 erg/seg) Y
 Espectroscopía Espectroscopía ultravioleta-visible visible Espectroscopía infrarroja Espectroscopía de resonancia magnética nuclear Espectrometría de masas Pincipisd Principios de la Espectroscopía Molecular:
Espectroscopía Espectroscopía ultravioleta-visible visible Espectroscopía infrarroja Espectroscopía de resonancia magnética nuclear Espectrometría de masas Pincipisd Principios de la Espectroscopía Molecular:
QUÍMICA DEL CARBONO 1. El carbono. 2. Grupos funcionales. 3. Isomería. 4. Compuestos orgánicos.
 QUÍMICA DEL CARBONO 1. El carbono. 2. Grupos funcionales. 3. Isomería. 4. Compuestos orgánicos. Química 1º bachillerato Química del carbono 1 1. EL CARBONO El carbono es una molécula muy especial capaz
QUÍMICA DEL CARBONO 1. El carbono. 2. Grupos funcionales. 3. Isomería. 4. Compuestos orgánicos. Química 1º bachillerato Química del carbono 1 1. EL CARBONO El carbono es una molécula muy especial capaz
Problemas de Química Física II. 3º de Químicas. RAMAN y POLIATOMICAS
 Problemas de Química Física II. 3º de Químicas RAMAN y POLIATOMICAS 1. Las primeras frecuencias del espectro Raman del N 2 son 19.908, 27.857, 35.812, 43.762, 51.721 y 59.622 cm -1. Sabiendo que estas
Problemas de Química Física II. 3º de Químicas RAMAN y POLIATOMICAS 1. Las primeras frecuencias del espectro Raman del N 2 son 19.908, 27.857, 35.812, 43.762, 51.721 y 59.622 cm -1. Sabiendo que estas
PROBLEMAS DE SELECTIVIDAD. QUÍMICA ORGÁNICA
 PROBLEMAS DE SELECTIVIDAD. QUÍMICA ORGÁNICA 2017 1) Dado el siguiente compuesto CH 3 CH 2 CHOHCH 3 a) Justifique si presenta o no isomería óptica. b) Escriba la estructura de un isómero de posición y otro
PROBLEMAS DE SELECTIVIDAD. QUÍMICA ORGÁNICA 2017 1) Dado el siguiente compuesto CH 3 CH 2 CHOHCH 3 a) Justifique si presenta o no isomería óptica. b) Escriba la estructura de un isómero de posición y otro
Maestría en Química Bioorgánica Preguntas Modelo Química. Marque la respuesta correcta en cada uno de los siguientes planteamientos.
 Maestría en Química Bioorgánica Preguntas Modelo Química Marque la respuesta correcta en cada uno de los siguientes planteamientos. 1. Cuando un átomo pasa de un estado atómico de energía mayor a uno de
Maestría en Química Bioorgánica Preguntas Modelo Química Marque la respuesta correcta en cada uno de los siguientes planteamientos. 1. Cuando un átomo pasa de un estado atómico de energía mayor a uno de
CONTENIDOS MÍNIMOS septiembre
 DEPARTAMENTO DE FÍSICA Y QUÍMICA CONTENIDOS MÍNIMOS septiembre CONTENIDOS MÍNIMOS curso 2015/16 1º BACHILLERATO-FÍSICA Y QUÍMICA QUÍMICA ESTRUCTURA ATÓMICA -Partículas subatómicas. -Modelo atómico de Thompson.
DEPARTAMENTO DE FÍSICA Y QUÍMICA CONTENIDOS MÍNIMOS septiembre CONTENIDOS MÍNIMOS curso 2015/16 1º BACHILLERATO-FÍSICA Y QUÍMICA QUÍMICA ESTRUCTURA ATÓMICA -Partículas subatómicas. -Modelo atómico de Thompson.
Química Analítica Orgánica
 Curso de especialización en procesos farmacéuticos y biotecnológicos Química Analítica Orgánica Dra. Victoria Cavaliere 2013 Objetivos de la materia Lograr que el alumno conozca los fundamentos teóricoexperimentales
Curso de especialización en procesos farmacéuticos y biotecnológicos Química Analítica Orgánica Dra. Victoria Cavaliere 2013 Objetivos de la materia Lograr que el alumno conozca los fundamentos teóricoexperimentales
PROBLEMAS DE SELECTIVIDAD. TEMA 7: QUÍMICA ORGÁNICA
 PROBLEMAS DE SELECTIVIDAD. TEMA 7: QUÍMICA ORGÁNICA 2015 1) Dados los compuestos CH 3 CH 2 CH 2 Br y CH 3 CH 2 CH = CH 2, indica, escribiendo la reacción correspondiente: a) El que reacciona con H 2 O/H
PROBLEMAS DE SELECTIVIDAD. TEMA 7: QUÍMICA ORGÁNICA 2015 1) Dados los compuestos CH 3 CH 2 CH 2 Br y CH 3 CH 2 CH = CH 2, indica, escribiendo la reacción correspondiente: a) El que reacciona con H 2 O/H
TEMA 3. Grupos funcionales con enlaces múltiples.
 TEMA 3. Grupos funcionales con enlaces múltiples. Alquenos. Alquinos. Compuestos aromáticos. El grupo carbonilo. Aldehídos. Cetonas. Ácidos carboxílicos. Ésteres. Anhídridos. Amidas Tioésteres, Fosfoésteres,
TEMA 3. Grupos funcionales con enlaces múltiples. Alquenos. Alquinos. Compuestos aromáticos. El grupo carbonilo. Aldehídos. Cetonas. Ácidos carboxílicos. Ésteres. Anhídridos. Amidas Tioésteres, Fosfoésteres,
QUÍMICA ORGÁNICA PÁGS LIBRO
 QUÍMICA ORGÁNICA PÁGS. 335-357 LIBRO Química del carbono Química del carbono; aquella que estudia los compuestos que tienen C Química del carbono HIDROCARBUROS Formados por C e H. Tipos: De cadena abierta
QUÍMICA ORGÁNICA PÁGS. 335-357 LIBRO Química del carbono Química del carbono; aquella que estudia los compuestos que tienen C Química del carbono HIDROCARBUROS Formados por C e H. Tipos: De cadena abierta
QUÍMICA ORGÁNICA PÁGS LIBRO
 QUÍMICA ORGÁNICA PÁGS. 335-357 LIBRO Química del carbono Química del carbono; aquella que estudia los compuestos que tienen C Química del carbono HIDROCARBUROS Formados por C e H. Tipos: De cadena abierta
QUÍMICA ORGÁNICA PÁGS. 335-357 LIBRO Química del carbono Química del carbono; aquella que estudia los compuestos que tienen C Química del carbono HIDROCARBUROS Formados por C e H. Tipos: De cadena abierta
FORMULACIÓN. Clasificación de los compuestos orgánicos. Hidrocarburos. Alcoholes y fenoles Éteres Aldehídos y cetonas Ácidos carboxílicos Esteres
 FORMULACIÓN Clasificación de los compuestos orgánicos Hidrocarburos. Alcoholes y fenoles Éteres Aldehídos y cetonas Ácidos carboxílicos Esteres CLASIFICACIÓN DE LOS COMPUESTOS ORGÁNICOS Clasificación de
FORMULACIÓN Clasificación de los compuestos orgánicos Hidrocarburos. Alcoholes y fenoles Éteres Aldehídos y cetonas Ácidos carboxílicos Esteres CLASIFICACIÓN DE LOS COMPUESTOS ORGÁNICOS Clasificación de
Experimentos cuánticos I. Curso 2011
 Experimentos cuánticos I. Curso 2011 Laboratorio 1: Absorción en Yodo gaseoso: transiciones electrónicas (entre niveles vibracionales) en moléculas diatómicas homonucleares. Regiones del espectro EM en
Experimentos cuánticos I. Curso 2011 Laboratorio 1: Absorción en Yodo gaseoso: transiciones electrónicas (entre niveles vibracionales) en moléculas diatómicas homonucleares. Regiones del espectro EM en
QUÍMICA ORGÁNICA PÁGS LIBRO
 QUÍMICA ORGÁNICA PÁGS. 335-357 LIBRO Química del carbono Química del carbono; aquella que estudia los compuestos que tienen C Química del carbono HIDROCARBUROS Formados por C e H. Tipos: De cadena abierta
QUÍMICA ORGÁNICA PÁGS. 335-357 LIBRO Química del carbono Química del carbono; aquella que estudia los compuestos que tienen C Química del carbono HIDROCARBUROS Formados por C e H. Tipos: De cadena abierta
Nombre: Curso: Fecha:
 GUÍA ESTUDIO Nº1 PROPIEDADES DE HIDROCARBUROS Y FUNCIONES ORGÁNICAS PROPIEDADES DE LOS HIDROCARBUROS Propiedades de alcanos Subsector Profesor Química Paulina Gómez a) Propiedades físicas: Son menos densos
GUÍA ESTUDIO Nº1 PROPIEDADES DE HIDROCARBUROS Y FUNCIONES ORGÁNICAS PROPIEDADES DE LOS HIDROCARBUROS Propiedades de alcanos Subsector Profesor Química Paulina Gómez a) Propiedades físicas: Son menos densos
RESUMEN DE FORMULACIÓN DE QUÍMICA ORGÁNICA
 RESUMEN DE FRMULACIÓN DE QUÍMICA RGÁNICA 1. HIDRCARBURS SATURADS (ALCANS) a) Los cuatro primeros tienen por nombres: CH 4 metano; - etano; - CH 2 - propano; - CH 2 - CH 2 - butano. El resto se nombra mediante
RESUMEN DE FRMULACIÓN DE QUÍMICA RGÁNICA 1. HIDRCARBURS SATURADS (ALCANS) a) Los cuatro primeros tienen por nombres: CH 4 metano; - etano; - CH 2 - propano; - CH 2 - CH 2 - butano. El resto se nombra mediante
QUÍMICA DEL CARBONO. Una instauración es un enlace múltiple (doble o triple) entre dos carbonos.
 QUÍMICA DEL CARBONO Conceptos básicos Los carbonos, según la posición que ocupan en la cadena, pueden ser carbonos primarios (están unidos a un único átomo de carbono), carbonos secundarios (están unidos
QUÍMICA DEL CARBONO Conceptos básicos Los carbonos, según la posición que ocupan en la cadena, pueden ser carbonos primarios (están unidos a un único átomo de carbono), carbonos secundarios (están unidos
EJERCICIOS DE INTERPRETACIÓN PARTE 2
 EJERCICIOS DE INTERPRETACIÓN PARTE 2 7 Ácido -Bromobutírico NMR 09 CH 3 CH 2 CH O C OH 3 1 Br 1 2 8 Feniletil Acetato NMR 14 5 O CH 2 CH 2 O C CH 3 3 2 2 9 Etil Succinato NMR 18 O O CH 3 CH 2 O C CH 2
EJERCICIOS DE INTERPRETACIÓN PARTE 2 7 Ácido -Bromobutírico NMR 09 CH 3 CH 2 CH O C OH 3 1 Br 1 2 8 Feniletil Acetato NMR 14 5 O CH 2 CH 2 O C CH 3 3 2 2 9 Etil Succinato NMR 18 O O CH 3 CH 2 O C CH 2
Química del Carbono, Curso /05/2014. Tema 9. Química del Carbono. El carbono: Z=6 A=12. C =1s 2 2s 2 p 2
 Tema 9 Química del Carbono El carbono: Z=6 A=12 C =1s 2 2s 2 p 2 C 1 Se puede representar como En el espacio, la segunda capa: 2 Orbitales del carbono en conjunto ORBITALES QUE EL CARBONO EMPLEA EN SUS
Tema 9 Química del Carbono El carbono: Z=6 A=12 C =1s 2 2s 2 p 2 C 1 Se puede representar como En el espacio, la segunda capa: 2 Orbitales del carbono en conjunto ORBITALES QUE EL CARBONO EMPLEA EN SUS
MATERIAL 06. TEMA: MÉTODOS ESPECTROSCÓPICOS DE ANÁLISIS
 MATERIAL 06. TEMA: MÉTODOS ESPECTROSCÓPICOS DE ANÁLISIS La espectroscopia es el estudio de las interacciones de las radiaciones electromagnéticas con la materia (átomos y moléculas). Los métodos analíticos
MATERIAL 06. TEMA: MÉTODOS ESPECTROSCÓPICOS DE ANÁLISIS La espectroscopia es el estudio de las interacciones de las radiaciones electromagnéticas con la materia (átomos y moléculas). Los métodos analíticos
Química Orgánica Grupos funcionales con oxígeno o nitrógeno
 Química rgánica Grupos funcionales con oxígeno o nitrógeno IES La Magdalena. Avilés. Asturias La parte carbonada constituye el esqueleto fundamental de las moléculas orgánicas. En esta estructura básica
Química rgánica Grupos funcionales con oxígeno o nitrógeno IES La Magdalena. Avilés. Asturias La parte carbonada constituye el esqueleto fundamental de las moléculas orgánicas. En esta estructura básica
ANARMONICIDAD Y RESONANCIA EN VIBRACIONES DE MOLÉCULAS
 ANARMONICIDAD Y RESONANCIA EN VIBRACIONES DE MOLÉCULAS PRESENTADO POR: ADRIANA LISSETH LUQUE DIAZ JORGE ENRIQUE JURADO TASCO MARCO ANTONIO HUERTA ORTIZ PABLO LABRA VÁZQUEZ MAESTRÍA EN CIENCIAS QUÍMICAS
ANARMONICIDAD Y RESONANCIA EN VIBRACIONES DE MOLÉCULAS PRESENTADO POR: ADRIANA LISSETH LUQUE DIAZ JORGE ENRIQUE JURADO TASCO MARCO ANTONIO HUERTA ORTIZ PABLO LABRA VÁZQUEZ MAESTRÍA EN CIENCIAS QUÍMICAS
HIDROCARBUROS AROMATICOS. Dr. Alberto Postigo
 HIDROCARBUROS AROMATICOS Dr. Alberto Postigo 1 1.-Nomenclatura. Fuentes naturales. Espectroscopia IR 2.-Reacciones de sustitución aromática electrofílica 3.-Hidrocarburos aromáticos polinucleares 4.- Reacciones
HIDROCARBUROS AROMATICOS Dr. Alberto Postigo 1 1.-Nomenclatura. Fuentes naturales. Espectroscopia IR 2.-Reacciones de sustitución aromática electrofílica 3.-Hidrocarburos aromáticos polinucleares 4.- Reacciones
QUÍMICA DEL CARBONO 1. El enlace de carbono. 2. Grupos funcionales. 3. Isomería.
 QUÍMICA DEL CARBONO 1. El enlace de carbono. 2. Grupos funcionales. 3. Isomería. Química 2º bachillerato Química del carbono 1 0. CONOCIMIENTOS PREVIOS Los conocimientos previos que son necesarios dominar
QUÍMICA DEL CARBONO 1. El enlace de carbono. 2. Grupos funcionales. 3. Isomería. Química 2º bachillerato Química del carbono 1 0. CONOCIMIENTOS PREVIOS Los conocimientos previos que son necesarios dominar
TEMARIO DE LOS EXÁMENES DE ADMISIÓN PARA INGRESO AL PROGRAMA DE MAESTRÍA EN CIENCIA DE MATERIALES DE LA UNIVERSIDAD DE SONORA
 TEMARIO DE LOS EXÁMENES DE ADMISIÓN PARA INGRESO AL PROGRAMA DE MAESTRÍA EN CIENCIA DE MATERIALES DE LA UNIVERSIDAD DE SONORA Examen de Química Química Orgánica Orbitales híbridos. Propiedades de los enlaces
TEMARIO DE LOS EXÁMENES DE ADMISIÓN PARA INGRESO AL PROGRAMA DE MAESTRÍA EN CIENCIA DE MATERIALES DE LA UNIVERSIDAD DE SONORA Examen de Química Química Orgánica Orbitales híbridos. Propiedades de los enlaces
Formulación Química Orgánica
 Formulación Química rgánica Hidrocarburos Compuestos que solamente tiene H y C. Pueden presentar insaturaciones. Se nombran a partir del número de carbonos: C met- 2 C et- 3 C prop- 4 C but- 5 C pent-
Formulación Química rgánica Hidrocarburos Compuestos que solamente tiene H y C. Pueden presentar insaturaciones. Se nombran a partir del número de carbonos: C met- 2 C et- 3 C prop- 4 C but- 5 C pent-
Tema 7. Espectroscopia para el estudio de la materia. 1. Introducción. 1. Introducción. 1. Introducción
 1 Tema 7. Espectroscopia para el estudio de la materia 1801: Thomas Young. Naturaleza dual de la radiación y la materia. Interacción Radiación-materia. Ley de Lambert-Beer 3. Espectroscopía InfraRojos
1 Tema 7. Espectroscopia para el estudio de la materia 1801: Thomas Young. Naturaleza dual de la radiación y la materia. Interacción Radiación-materia. Ley de Lambert-Beer 3. Espectroscopía InfraRojos
Espectroscopía IR. de compuestos de
 Espectroscopía IR de compuestos de coordinación C. Kremer Facultad de Química Contenido 1 Compuestos de coordinación simples 2 Grupos funcionales típicos 3 Ejemplos de biomoléculas 1 Qué esperamos ver
Espectroscopía IR de compuestos de coordinación C. Kremer Facultad de Química Contenido 1 Compuestos de coordinación simples 2 Grupos funcionales típicos 3 Ejemplos de biomoléculas 1 Qué esperamos ver
RESUMEN DE FORMULACIÓN DE QUÍMICA ORGÁNICA
 RGÁNICA RESUMEN DE FRMULACIÓN DE QUÍMICA RGÁNICA 1. HIDRCARBURS SATURADS (ALCANS) a) Los cuatro primeros tienen por nombres: CH 4 metano; - etano; - CH 2 - propano; - CH 2 - CH 2 - butano. El resto se
RGÁNICA RESUMEN DE FRMULACIÓN DE QUÍMICA RGÁNICA 1. HIDRCARBURS SATURADS (ALCANS) a) Los cuatro primeros tienen por nombres: CH 4 metano; - etano; - CH 2 - propano; - CH 2 - CH 2 - butano. El resto se
UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE ESTUDIOS SUPERIORES CUAUTITLÁN
 UNIVERSIDAD NACIONAL AUTÓNOMA MÉXICO FACULTAD ESTUDIOS SUPERIORES CUAUTITLÁN LICENCIATURA EN QUÍMICA FARMACEUTICA BIOLOGICA Tercer semestre ASIGNATURA: Química Orgánica I NÚMERO HORAS / SEMANA 13 / SEMESTRE
UNIVERSIDAD NACIONAL AUTÓNOMA MÉXICO FACULTAD ESTUDIOS SUPERIORES CUAUTITLÁN LICENCIATURA EN QUÍMICA FARMACEUTICA BIOLOGICA Tercer semestre ASIGNATURA: Química Orgánica I NÚMERO HORAS / SEMANA 13 / SEMESTRE
TEMA 9. DETERMINACIÓN DE ESTRUCTURAS MEDIANTE MÉTODOS FÍSICOS
 TEMA 9. DETERMINACIÓN DE ESTRUCTURAS MEDIANTE MÉTODOS FÍSICOS 1. Interacción de la energía radiante y la materia orgánica. 2. Fundamentos de la espectroscopia infrarroja: regiones del IR y modos fundamentales
TEMA 9. DETERMINACIÓN DE ESTRUCTURAS MEDIANTE MÉTODOS FÍSICOS 1. Interacción de la energía radiante y la materia orgánica. 2. Fundamentos de la espectroscopia infrarroja: regiones del IR y modos fundamentales
Química Orgánica I-Plan Temario 2º parcial promocional. TEORÍA ÁCIDO BASE. Expresión constante de acidez y basicidad. Ácidos y bases de Lewis.
 Temario 2º parcial promocional 1) ACIDEZ Y BASICIDAD TEORÍA ÁCIDO BASE. Expresión constante de acidez y basicidad. Ácidos y bases de Lewis. Acidez de compuestos orgánicos. Acidez de alcoholes. Acidez de
Temario 2º parcial promocional 1) ACIDEZ Y BASICIDAD TEORÍA ÁCIDO BASE. Expresión constante de acidez y basicidad. Ácidos y bases de Lewis. Acidez de compuestos orgánicos. Acidez de alcoholes. Acidez de
ANARMONICIDAD Y RESONANCIA EN VIBRACIONES DE MOLÉCULAS
 ANARMONICIDAD Y RESONANCIA EN VIBRACIONES DE MOLÉCULAS Jiménez Bárcenas Nadia Rosalina López Salazar Fátima Mendoza Pérez Bernardo Monzón González César Raúl Equipo 3: Principios de estructura de la materia
ANARMONICIDAD Y RESONANCIA EN VIBRACIONES DE MOLÉCULAS Jiménez Bárcenas Nadia Rosalina López Salazar Fátima Mendoza Pérez Bernardo Monzón González César Raúl Equipo 3: Principios de estructura de la materia
Departamento de Ciencias Profesores: Sergio Andrés Magdalena Loyola Curso: IIIº Medio QUÍMICA ORGÁNICA
 FUNDACIÓN EDUCACIONAL COLEGIO DE LOS SS.CC. Manquehue Departamento de Ciencias Profesores: Sergio Andrés Magdalena Loyola Curso: IIIº Medio Nombre: Curso: QUÍMICA ORGÁNICA CICLOALCANOS CnH2n Son cadenas
FUNDACIÓN EDUCACIONAL COLEGIO DE LOS SS.CC. Manquehue Departamento de Ciencias Profesores: Sergio Andrés Magdalena Loyola Curso: IIIº Medio Nombre: Curso: QUÍMICA ORGÁNICA CICLOALCANOS CnH2n Son cadenas
Royal American School QUIMICA 2º MEDIO Profesora: Jimena Hurtado Pereira GUÍA DE TRABAJO Nº1 QUIMICA ORGÁNICA NOMBRE: CURSO:
 Royal American School QUIMICA 2º MEDIO Profesora: Jimena Hurtado Pereira GUÍA DE TRABAJO Nº1 QUIMICA ORGÁNICA NOMBRE: CURSO: AE: Crear modelos del carbono y explicar sus propiedades como base para la formación
Royal American School QUIMICA 2º MEDIO Profesora: Jimena Hurtado Pereira GUÍA DE TRABAJO Nº1 QUIMICA ORGÁNICA NOMBRE: CURSO: AE: Crear modelos del carbono y explicar sus propiedades como base para la formación
M. En C. José Antonio González Moreno Tecnologías Químicas Octubre del 2017
 M. En C. José Antonio González Moreno Tecnologías Químicas Octubre del 2017 La siguiente información no pretende ser una materia, sino una herramienta y guía básica en la cual el alumnado pueda recordar
M. En C. José Antonio González Moreno Tecnologías Químicas Octubre del 2017 La siguiente información no pretende ser una materia, sino una herramienta y guía básica en la cual el alumnado pueda recordar
Fundamentos de Espectroscopía UV-Visible
 Fundamentos de Espectroscopía UV-Visible Cátedra de Química Orgánica I Facultad de Farmacia y Bioquímica UBA 2016 Teórico dictado por Dra. Isabel Perillo 1 Especto electromagnético Unidades de l usadas:
Fundamentos de Espectroscopía UV-Visible Cátedra de Química Orgánica I Facultad de Farmacia y Bioquímica UBA 2016 Teórico dictado por Dra. Isabel Perillo 1 Especto electromagnético Unidades de l usadas:
NOMENCLATURA DE GRUPOS FUNCIONALES
 Química IIº Medio Prof. Juan Pastrián / Sofía Ponce de León MECLATUA DE GUPS FUCIALES ALCLES Los alcoholes se caracterizan por poseer el grupo funcional hidroxilo ( ) en su estructura, el que se encuentra
Química IIº Medio Prof. Juan Pastrián / Sofía Ponce de León MECLATUA DE GUPS FUCIALES ALCLES Los alcoholes se caracterizan por poseer el grupo funcional hidroxilo ( ) en su estructura, el que se encuentra
3.1 EL ATOMO DE CARBONO
 3.1 EL ATOMO DE CARBONO La química orgánica es la química de los compuestos del carbono El nombre engañoso orgánica es una reliquia de los tiempos en que los compuestos químicos se dividían según su origen,
3.1 EL ATOMO DE CARBONO La química orgánica es la química de los compuestos del carbono El nombre engañoso orgánica es una reliquia de los tiempos en que los compuestos químicos se dividían según su origen,
Formulación orgánica. Gloria Almonacid Caballer IES Juan García Valdemora Curso 2017/2018
 Formulación orgánica Gloria Almonacid Caballer IES Juan García Valdemora Curso 2017/2018 Compuestos orgánicos INTRDUCCIÓN -formados por C principalmente. También H,, N, S, P y halógenos. Propiedades Generales
Formulación orgánica Gloria Almonacid Caballer IES Juan García Valdemora Curso 2017/2018 Compuestos orgánicos INTRDUCCIÓN -formados por C principalmente. También H,, N, S, P y halógenos. Propiedades Generales
Teoría Estructural 25/06/2012
 La Química Orgánica está a punto de enloquecerme. Se me figura como un bosque tropical primigenio, lleno de las cosas más notables, una selva infinita y terrible en la que uno no se atreve a penetrar porque
La Química Orgánica está a punto de enloquecerme. Se me figura como un bosque tropical primigenio, lleno de las cosas más notables, una selva infinita y terrible en la que uno no se atreve a penetrar porque
Medicina Veterinaria. Parte I
 Medicina Veterinaria QUÍMICA ORGÁNICA Parte I Moléculas Polares y No Polares Moléculas No Polares: Los electrones están distribuidos simétricamente en la molécula y el centro de las cargas eléctricas coincide
Medicina Veterinaria QUÍMICA ORGÁNICA Parte I Moléculas Polares y No Polares Moléculas No Polares: Los electrones están distribuidos simétricamente en la molécula y el centro de las cargas eléctricas coincide
OXIDACIÓN Y REDUCCIÓN DE COMPUESTOS ORGÁNICOS
 OXIDACIÓN Y REDUCCIÓN DE COMPUESTOS ORGÁNICOS O OXIDACIÓN: Aumento de átomos de oxígeno o pérdida de átomos de hidrógeno en un compuesto orgánico. O REDUCCIÓN: Aumento de átomos de hidrógeno o pérdida
OXIDACIÓN Y REDUCCIÓN DE COMPUESTOS ORGÁNICOS O OXIDACIÓN: Aumento de átomos de oxígeno o pérdida de átomos de hidrógeno en un compuesto orgánico. O REDUCCIÓN: Aumento de átomos de hidrógeno o pérdida
Desplazamiento Químico. Dr. Jorge A. Palermo
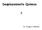 Desplazamiento Químico δ Dr. Jorge A. Palermo ν 0 = γ B 0 / 2π ECUACIÓN DE LARMOR E aumenta con B 0 Núcleo 1 2.35 Tesla 100 Mz 17.63 Tesla 750 Mz ν 0 aumenta con B 0 2 13 C 31 P 15.35 Mz 25.1 Mz 40.5 Mz
Desplazamiento Químico δ Dr. Jorge A. Palermo ν 0 = γ B 0 / 2π ECUACIÓN DE LARMOR E aumenta con B 0 Núcleo 1 2.35 Tesla 100 Mz 17.63 Tesla 750 Mz ν 0 aumenta con B 0 2 13 C 31 P 15.35 Mz 25.1 Mz 40.5 Mz
FORMULACIÓN BÁSICA QUÍMICA ORGÁNICA
 FORMULACIÓN BÁSICA QUÍMICA ORGÁNICA La fórmula empírica indica los elementos que forman la molécula y la proporción relativa de los mismos. CH (escasa información) La fórmula molecular indica el número
FORMULACIÓN BÁSICA QUÍMICA ORGÁNICA La fórmula empírica indica los elementos que forman la molécula y la proporción relativa de los mismos. CH (escasa información) La fórmula molecular indica el número
clubdelquimico.blogspot.com
 clubdelquimico.blogspot.com Dadas las fórmulas siguientes: CH3OH, CH3CH2COOH, CH3COOCH3 y CH3CONH2 a. Diga cuál es el nombre del grupo funcional presente en cada una de las moléculas y nombre todos los
clubdelquimico.blogspot.com Dadas las fórmulas siguientes: CH3OH, CH3CH2COOH, CH3COOCH3 y CH3CONH2 a. Diga cuál es el nombre del grupo funcional presente en cada una de las moléculas y nombre todos los
