Tablas de Espectroscopía Infrarroja. Elaboradas por: Francisco Rojo Callejas
|
|
|
- Ana Belén Santos Padilla
- hace 7 años
- Vistas:
Transcripción
1 Tablas de Espectroscopía Infrarroja Elaboradas por: Francisco ojo allejas
2 Figura I-1 egiones básicas de un espectro de Infrarrojo (cm -1 ) 500 y >N y N N * * * y y N, * * de> y > (cm -1 )
3 Figura I-2 Algoritmo general de interpretación de espectros de I T5 y T7 3200~3650? Agua en la muestra, alcoholes o aminas. Usar las tablas 5 y7. T1 2800~3000? cuantas señales? solo dos tres o más 2 Ó? 3 2 Y? ~1445? ierto, y/o ~1365? ~710? adenas de -( )- 2 n con n 4 T2 y T3 3000~3? Insaturaciones: alque ó aromático dos señales: 14~1550 y 1550~1610? Aromático 0~650? Alque, die, polie 1600~1680? 1750~1860? >= 2 El número, forma y posición, junto con sus pequeños sobretos en 2000~1650 caracterizan las posiciones sustituídas del anillo bencénico T4 1950~2300? Triple enlace o dobles geminales: Acetile: - - Nitrilo: - N Diazo: -(N N) +, >=N= + N- Ales: >==< Tiocinanato y sim.: -S- N, -N==S, -N== etes y sim.: >==, >==N Analizar usando el diagrama de flujo de la figura I-4 T6 1540~1850? arbonilo. Analizar usando el diagrama de flujo de la figura I (cm -1 )
4 Grupo Nº de onda (cm -1 ) Intensidad 1 1 mol l cm c TABLA I-I ALANS h rigen Notas 2970~2950 ch 70 ν as - 3 (1) (ε 15 21) en -NMe, ausente en -NEt. 2880~2860 m 30 ν s (ε 35 75) en -Me, ausente en -Et en metilendioxi. 1470~1450 m < 15 δ as ~1365 ch 15 δ s - 3 Doblete en gem-dimetilos (ver (5)-(7)). Junto a carbonilos ver (11)-(13). 2935~2915 ch 75 ν as ~2845 ch 45 ν s ~1445 m 8 tijera en ciclopentas, 1450 en ciclohexas. Se desplaza por hiperconjugación (ver (14)-(16)). (2) ch 3 rocking -( 2 ) n - Presente cuando n 4. casionalmente como doblete en sólidos. Mas alto a mer n. Propilo ; Etilo El también tiene bandas de flexión en 1300 (ε 1). Los espectros de sólidos con cadenas largas y grupos polares terminales (ácidos, ésteres, amidas) muestran una serie de bandas regulares entre (3) débil débil ν δ sin uso práctico sin uso práctico (4) -( 2 ) rocking de corresponde a la banda en 720 de (2). (5) 1170 ch, mas débil que esqueleto Un doblete en 1380 sugiere grupos gem-dimetilo; 3 el doblete de 1380 la confirmación se realiza por la vibración del 3 (ε 15). esqueleto (5)-(7). 3 (6) 3 3 (7) cuaternario 3 3 (8) 2 (9) ver tabla XI () N ch " " ombro en 1145 de la de ch " " Posición mas estable que la de la banda en ch " ch " ch " m m " " " ν as 2 esqueleto 3050 ν as 2 ν meti ν as 2 metile También absorbe en De estas dos la de 1195 es mas estable, la señal en 1215 es un hombro de la primera. Ausente en anillos sin Normalmente obstruido por señales fuertes de otro tipo. Se desplaza hasta al incrementar la tensión del grupo epoxi, p. ej. unido a ciclopentas. 10) (11) aracterizado por su alta intensidad. Al acetilar la banda en 1380 se vuelve mas intensa que la de Lo mismo ocurre con acetatos de el y fel. casionalmente se vuelve doblete. (12) Se desplaza a frecuencias meres que la flexión usual de 3 (1380). Señal aguda e intensa. La flexión asimétrica permanece en su posición usual (1460), pero se desplaza en los terpes ( ). (13) δ as - 3. También con bandas en 1135, 1155, δ s - 3 (14) La flexión de todos los metiles activos se observa como una serie de bandas intensas y agudas entre las bandas comunes de 1465 a Lo mismo ocurre con - 2 -S 2 - y otros. La integración de la intensidad pudiera proporcionar el número de metiles activos. (15) - 2 -= No es muy intensa. Los dobles enlaces pudieran ser de aromáticos. La intensidad disminuye aún mas si el está entre dos enlaces múltiples (dobles o triples). (16) - 2 -N El adyacente al N + también se desplaza como los dos anteriores. Si aparecen nuevas bandas al convertir la amina en sal, entonces se sabe que hay grupos - 2 -N-.
5 TABLA I-II ALQUENS 1. Frecuencias de estiramiento - (ε entre paréntesis). A) = insaturados =- (alques, aromáticos). La banda de , m(30) 3000~2975, m ν as 2 ν s 2 Las bandas por encima de 3000 sugieren la presencia de 2975 se traslapa con los alcas. B) 3020, m ν - 2. Señales de estiramiento = y de flexión =-, afectadas por el tipo de sustituyente Tipo ν = Sobreto de la Flexión en el pla flexión fuera del δ. pla δ. Flexión fuera del pla δ. ) vinilo terminal -=2 D) metile terminal ~1620 m (40) 1665~1645 m (35) E) cis, disustituído 1660~1620 m (10) 1 2 F) trans, disustituído 2 1 G) trisustituído ) tetrasustituído ~1660 ancho (2) 1680~1660 ancho~m 1680~1660 ancho, intenso cuando está unido directamente a ó N. 1860~1800 m (30) 1800~1750 m (30) 1420, m (10~20). Se encima con las señales de 2 de alcas, (14)-(16) 1300, m~ancho 1415, m (10~20). Misma región de tabla I, (14)-(16). 1415, m (10~20) 9, ch (50) y 910 ch (110); Incluye las flexiones simétrica y asimétrica de los 3. 8, ch (~150). Flexión asimétrica. 730~675, m (40). casionalmente dudoso. En cíclicos aparecen varias bandas semejantes entre 800~650 (ε 50 ), difícil asignarlas. 965, ch (). Flexión asimétrica de los. 840~800, ch (40). Los cíclicos dan dos señales entre 850~7. No hay, pero los 2 contiguos (>=- 2 ) se pueden detectar por su flexión (Tabla I, (15)). 3. Dobles enlaces conjugados Grupo ν = δ - (fuera del pla) La conjugación influye poco. En ocasiones la I) Die 1650 y 1600 banda trans de 965 sube a 9. La banda cis aparece en 720, a veces como un prupo. J) Trie 1650 y 1600; en ocasiones solo una banda y en otras la de 1600 aparece como un hombro de K) Polie Banda ancha en 1650~1580
6 TABLA I-III AMÁTIS Posición Intensidad ε rigen Notas 1) 3~3000 Mes de 60 Estiram - y En algus aromáticos la banda principal combinaciones está debajo de 3000 cm -1 2) 2000~1660, Baja, ~5 Sobreto de las Grupo de 2 a 6 bandas pequeñas, varias bandas, flexiones fuera característico del patrón de sustitución, ver figura I-1 del campo - y comparar con fig. I-3, si necesita combinaciones ampliar concentre la muestra. Los 3) 1600~ ~14 Variable, mes de. La señal de 1600 en ocasiones es mas intensa que la correspondiente ( ) de alques carbonilos ocultan estas señales. Nucleo bencénico Usualmente 1500 es mas intensa que onjugado con dies da otra señal en Los sistemas condensados absorben en y dos bandas en Flexiones fuera del pla (debajo de 0 cm -1 ) Bandas muy intensas, ε a 500. El número, forma e intensidad relativa depende de los hidróges libres, como lo muestra la fig. I-3. Para piridinas y similares se usa la misma tabla, el heteroátomo se considera entonces un sustituyente. Flexiones en el pla (1225~950 cm -1 ) Estas señales son solo complementarias, pues los estiramientos -, -N y - caen en la misma región. Aparecen varias señales en función del número de hidróges. Señales débiles, pero agudas, que pueden aumentar significativamente en presencia de grupos polares. Sustituyentes en: ~1125, 1110~1070, 1070~0 1:2-1225~1175, 1070~0 (doblete), 0~960 1:3-1175~1125, 1110~1070, 1070~0 1:4-1225~1175, 1070~0 (doblete) 1:2:3-1175~1125, 1110~1070, 1070~0, 0~960 1:2:4-1225~1175, 1175~1125, 1070~0 (doblete), 0~960 1:3:5-1175~1125, 1070~0
7 Figura I-5 Señales aracterísticas de Sustituciones en Aromáticos No hay señal
8 TABLA I-IV: ENLAES X Y, X=Y=Z. Grupo Posición (cm-1) ε Notas Acetile terminal, - Estir. - -: 2230~ Estir. -: 3320~3280 La señal en ~3300 es muy aguda.también hay una flexión del enlace - en 700~600 y ocasionalmente el sobreto en 1300~1200 Acetile central, ~ Desaparece si la simetría es alta 1335~1325 Nitrilo - N Aislado: 2260~2240 onjugado: 2240~2210 ~1330 causado por flex ~150 Las cianamidas (=N- N) dan igual que los conjugados. Los cianuros alcalis (NaN, KN) producen una señal intensa del carbanión en 2~2050. Sales de diazonio, -(N N) ~2240 Medio La posición depende del contraión Diazo -=N + =N ~2035 >=N + =N ~2000 Diazocetonas--N 2 2~20 Ales >==< --N ~2060 En aromáticos el estiram. del carbonilo se desplaza a 1645, en alifáticos a 1630~ Se divide si el ale es terminal y tiene grupos electroatrayentes (e.g. acidos, cetonas). 850 (solo si el ale es terminal, flexión -) 850 mas intensa que 1950, sobreto en Isocianato -N== 2275~ ~2000 Muy intensa, le afecta conjugación arbodiimida, -N==N- Alifática: 2140~ ~1580 Mas intensa que carbonilo. Aromática: ~1680 Los aromáticos dan este doblete ~1560 asimétrico. Azida, -N ~2095 intensa Estiram. asim., en aromáticos se divide 1340~1180 débil Estiram. sim Tiocianato, -S- N Alifático 2140 Aromático 2175~2160 Isotiocianato, -N==S Alifático 2140~19 y 10 Aromático 2130~2040, 1250 y 930 ete, >== ~2150 etenimina, >==N ~2000 Bióxido de carbo, ==, Mas intensas que isocianatos intensa 2 un poco ancha, dividida o con hombros. Estiram. antisim., estruct. Fina Las tres son señales finas, usadas en la calibración del equipo.
9 -1 Fig. I-4 Algoritmo para la interpretación de señales en la zona cm 2300~2240? intensa? isocianato -N== nitrilo aislado - N ó sales de diazonio -(N N) + 3 (cont.) 2240~2210? 3320~3280, chica, pero aguda? acetile terminal -, comprobar con 700~ ~1325? acetile central nitrilo conjugado >=- N ó cianamida =N- N ó acetile central - -' 2180~2160? intensa? aromático? tiocianato aromático -S- N 2160~1980? intensa? ancha, con hombros o doblete ancho? isotiocianato -N==S doblete asimétrico? carbodiimida aromática -N==N- carbodiimida alifática -N==N-' (2140~2130) ó tiocianato alifático -S- N (2150~2130) ó azida -N ( buscar señal en 1340~1180) ~1940? 2160~2140? cete >== ale >==< hay carbonilo? (punto 5) diazocetona 2110~2080? 2075~2060? --N 2 diazocetona --N ~2035? grupo diazo: + - -=N =N 2030~1980? + - grupo diazo '=N =N ( 2030~2000) ó cetenimina >==N (2010~1980) (cm -1 )
10 TABLA I-V: ALLES Y FENLES. Tabla 5.a: Vibraciones de estiramiento del enlace -: Estado del alcohol Posición, cm -1 oeficiente ε Forma Notas 1) Libre, sin asociar: Agudo Medido en fase vapor o en disolventes Primario, polares, pero si estos están Secundario, húmedos, también aparece la señal del agua en ' Terciario, ' '' Feles, φ ) idroperóxido: Puentes de hidróge: 3) Dímero 3600~3500 Agudo No se observa rmalmente, por ocultarlo la banda polimérica. También aquí aparecen otros puentes de 4) Polimérico hidróge con éteres, cetonas y aminas 3400~3200 Grande Ancho También aquí aparecen las aminas (3500~3200) y la pequeña señal de sobreto del carbonilo. En muestras húmedas aparece la señal de estiramiento -- (3600~3), en cuyo caso también se observa la flexión en 1640~1615. Puentes intramoleculares: 5) Alcoholes polivalentes 3600~ Agudo 6) puentes π ) Puente intramolec. con carbonilos, nitro, etc. 3200~2500 Ancho Generalmente se pierde bajo la señal de los estiramientos - Tabla 5.b: Vibraciones de estiramiento del enlace -: α β α α Tipo de alcohol Posición, cm -1 Desplazamientos, cm -1 Notas Primario 1050 (1075~1025) Secundario 1 (1150~1) Terciario 1125 (1200~1) Feles 1200 (1250~1150) amificación en α: -15 Insaturación en α: -30 Anillo en α-α': -50 Insaturación en α y anillo α-α': - Die conjugado en α: -140 Tabla 5.c: Vibraciones de torsión del enlace -: Posición (cm -1 ) Forma Notas 660 ± 50 Ancha No es muy útil Las insaturaciones pueden ser alques o aromáticos. Sobre β y mas lejos influyen en la posición. Si tanto en α como en α' y α'' hay ramificaciones, descuente otros 15 cm -1.
11 TABLA I-VI: GUP ABNIL. ÁIDS ABXÍLIS, ÉSTEES, ANIDIDS, ALDEÍDS Y ETNAS GUP Frecuencia (cm -1 ) NTAS IGEN Ácidos carboxílicos Ésteres Anhidridos Aldehídos etonas Señal intensa, característica del grupo carbonilo Señal ancha por puentes de hidróge, con patrón de sobretos de la torsión entre Dos señales, una ancha en , otra más débil en Ancha, mediana Señal intensa, característica del grupo carbonilo Dos bandas, una de mayor intensidad: Formiato Acetato Alquil ester Doble banda de carbonilo Normalmente el simétrico (mayor ν) es mas intenso que el antisimétrico, excepto en anhidridos cíclicos U o dos bandas intensas Señal intensa, característica del grupo carbonilo Estiramiento del carbonilo Estiramiento del Torsón/estiramiento del carboxilo Torsión fuera del pla del dímero del carboxilo Estiramiento del carbonilo 2 Estiramientos simétrico y asimétrico. Mayor ν e intensidad: mer ν: Estiramiento simétrico de los carbonilos: Estiramiento antisimétrico de los carbonilos: Estiramientos simétrico y asimétrico de los enlaces ---- Estiramiento del carbonilo Dos señales, la primera puede estar muy y cerca de metilos y metiles esonancia de Fermi Torsión de los - Estiramiento del carbonilo Señal intensa, característica del grupo carbonilo 2 1 y 1300 Señales pequeñas en alifáticos, más intensas y finas en aromáticos 2 Torsión del carbonilo 2 2
12 Fig. I-6 Algoritmo para la interpretación de señales en cm ~1540, INTENSA? si ABNIL Anhidrido si 1 o 2 bandas intensas y anchas en 1310~1020? si Doble en ? Dos carbonilos diferentes? Ácido si Señales en 1420~1200? si Bandas anchas en 3000~2200? Ester si Dos bandas intensas, en ? Aldehído si Señales en ? etona
13 TABLA I-VII: AMINAS Y SALES DE AMNI. Tabla 7.a: Vibraciones de estiramiento del enlace N-: Tipo de amina Posición, cm -1 oeficiente ε Notas Libre: 1) Primaria: -N 2 y φ-n 2 ~3500 (estiram. asim.) ~3400 (estiram. sim.) Ancha en primarias ε ~30 en φ-n 2 La presencia de estas dos señales es característica de aminas prim. 2) Secundaria: -N-' 3350~3310 ancha Muy pequeña en N-heterociclos como la piperidina φ-n- y φ-n-φ' 3450 ε ~30 a 40 Pirroles, indoles, etc. 34 ε ~150 a 300 aracterísticos, ver tabla 10-2 N >=N 3400~3300 También estiramiento =N en 16~1640 cm -1. Asociada: El desplazamiento desde la posición libre es inferior a cm-1, aunque puede llegar hasta 3 cm-1. En general son mas pequeñas, agudas y mes sensibles a los cambios en concentración que las bandas de alcoholes -. Tabla 7.b: Vibraciones de flexión del enlace N-: -N 2 Tipo Posición, cm -1 Intensidad Notas Primarias, 1640~1560 hica a mediana Flexión de tijera, tanto en aminas alifáticas como aromáticas. Muy característica, corresponde a la torsión, } 0~650 Mediana, ancha presente solo en aminas 1 as y 2 as, en 3 as. Secundarias, -N- 1580~14 ancha No es útil por su difícil detección Tabla 7.c: Vibraciones de estiramiento del enlace -N: Si bien la posición es casi igual al estiramiento -, la intensidad es mucho mayor, debido a al polaridad del enlace -N. Tipo de enlace -N Posición (cm -1 ) Intensidad Notas N () () N () 1230~1030 mediana Dos señales en terciarias, en aminas cíclicas la posición esta a mer número de onda. 1360~1250 hica Estiramiento φ-n. Se desplaza por el incremento en el carácter del doble enlace. 1280~1180 mediana Estiramiento del enlace alifático -N
14 Tabla 7.d: Sales de aminas iónicas: Grupo Posición (cm -1 ) Forma y tamaño Notas + N ~3030 Ancho y chico ~3000 Ancho Los estiram. asim. y sim. de N- se traslapan sobre la banda -, se le llama banda de amonio. Amina primaria, ~2500 Varias, medianas Tos combinados y sobretos, siempre aparecen. + -N 3 ~2000 mediana Tos combinados y sobretos, siempre aparecen. Amina Secundaria, + >N 2 Amina Terciaria, N + Ión Amonio cuaternario >N + < Aminas insaturadas, (aromáticas): N+ Guanidinio: Estiram. -N de las guanidinas libres en clorhidratos: Mo-substituídas Di-substituídas Tri-substituídas N N N +
TABLA IR-I ALCANOS. ν CH δ CH
 Grupo º de onda (cm -1 ) Intensidad 1 1 mol l cm c TABLA I-I ALAOS h Origen otas 2970~2950 ch 70 ν as - 3 (1) - 3 2730 2820 (ε 15 21) en -Me, ausente en -Et. 2880~2860 m 30 ν s - 3 2830 2815 (ε 35 75)
Grupo º de onda (cm -1 ) Intensidad 1 1 mol l cm c TABLA I-I ALAOS h Origen otas 2970~2950 ch 70 ν as - 3 (1) - 3 2730 2820 (ε 15 21) en -Me, ausente en -Et. 2880~2860 m 30 ν s - 3 2830 2815 (ε 35 75)
VIBRACIONES CARACTERÍSTICAS DE ALGUNAS DE LAS FUNCIONES QUÍMICA-ORGÁNICAS MÁS IMPORTANTES.
 VIBRACIONES CARACTERÍSTICAS DE ALGUNAS DE LAS FUNCIONES QUÍMICA-ORGÁNICAS MÁS IMPORTANTES. ALCANOS NORMALES (LINEALES) En todos los alcanos normales o ramificados se espera encontrar solo estiramientos
VIBRACIONES CARACTERÍSTICAS DE ALGUNAS DE LAS FUNCIONES QUÍMICA-ORGÁNICAS MÁS IMPORTANTES. ALCANOS NORMALES (LINEALES) En todos los alcanos normales o ramificados se espera encontrar solo estiramientos
Espectro Electromagnético
 Espectro Electromagnético En las moléculas orgánicas se observan vibraciones moleculares con energías que corresponden a la porción del infrarrojo del espectro electromagnético. Describiendo de la forma
Espectro Electromagnético En las moléculas orgánicas se observan vibraciones moleculares con energías que corresponden a la porción del infrarrojo del espectro electromagnético. Describiendo de la forma
ESPECTROSCOPIA INFRARROJA. Prof. Dr. Alberto Postigo
 ESPECTROSCOPIA INFRARROJA Prof. Dr. Alberto Postigo 1 2 Transición energética en el IR 3 A.-TEORIA DE LA ESPECTROSCOPIA IR (cm 1 ) = 1 (cm) (z) = c (cm) = c (cm/sec) (cm) cm 1 = 1 ( ) x 10,000 and = 1-1
ESPECTROSCOPIA INFRARROJA Prof. Dr. Alberto Postigo 1 2 Transición energética en el IR 3 A.-TEORIA DE LA ESPECTROSCOPIA IR (cm 1 ) = 1 (cm) (z) = c (cm) = c (cm/sec) (cm) cm 1 = 1 ( ) x 10,000 and = 1-1
TABLA 1- Desplazamientos químicos (δ) de protones de metilos, metilenos y metinos de alcanos monosustituidos con sustituyentes x en posición α
 TABLA 1- Desplazamientos químicos (δ) de protones de metilos, metilenos y metinos de alcanos monosustituidos con sustituyentes x en posición α alógeno N S --N X 3 X 2 X - 3,- 2-0,86 0,91 1,25 1,33 1,50
TABLA 1- Desplazamientos químicos (δ) de protones de metilos, metilenos y metinos de alcanos monosustituidos con sustituyentes x en posición α alógeno N S --N X 3 X 2 X - 3,- 2-0,86 0,91 1,25 1,33 1,50
Espectroscopía IR. de compuestos de
 Espectroscopía IR de compuestos de coordinación C. Kremer Facultad de Química Contenido 1 Compuestos de coordinación simples 2 Grupos funcionales típicos 3 Ejemplos de biomoléculas 1 Qué esperamos ver
Espectroscopía IR de compuestos de coordinación C. Kremer Facultad de Química Contenido 1 Compuestos de coordinación simples 2 Grupos funcionales típicos 3 Ejemplos de biomoléculas 1 Qué esperamos ver
Tema 7: Espectroscopia Vibracional (IR)
 Tabla 1. El espectro electromagnético Región Longitud de onda Energía de excitación Tipo de excitación Rayos x, rayos cósmicos 286 (Kcal/mol) Ultravioleta Visible Infrarrojo próximo Infrarrojo
Tabla 1. El espectro electromagnético Región Longitud de onda Energía de excitación Tipo de excitación Rayos x, rayos cósmicos 286 (Kcal/mol) Ultravioleta Visible Infrarrojo próximo Infrarrojo
TALLER DE ESPECTROSCOPIA
 TALLER DE ESPECTROSCOPIA I. OBJETIVOS a) Conocer los principios fundamentales que rigen la interacción energía-materia (radiación electromagnética-moléculas) en uno de los métodos espectroscópicos más
TALLER DE ESPECTROSCOPIA I. OBJETIVOS a) Conocer los principios fundamentales que rigen la interacción energía-materia (radiación electromagnética-moléculas) en uno de los métodos espectroscópicos más
EJERCICIOS DE INTERPRETACIÓN PARTE 2
 EJERCICIOS DE INTERPRETACIÓN PARTE 2 7 Ácido -Bromobutírico NMR 09 CH 3 CH 2 CH O C OH 3 1 Br 1 2 8 Feniletil Acetato NMR 14 5 O CH 2 CH 2 O C CH 3 3 2 2 9 Etil Succinato NMR 18 O O CH 3 CH 2 O C CH 2
EJERCICIOS DE INTERPRETACIÓN PARTE 2 7 Ácido -Bromobutírico NMR 09 CH 3 CH 2 CH O C OH 3 1 Br 1 2 8 Feniletil Acetato NMR 14 5 O CH 2 CH 2 O C CH 3 3 2 2 9 Etil Succinato NMR 18 O O CH 3 CH 2 O C CH 2
INTRODUCCION A LA NOMENCLATURA E ISOMERIA DE LOS COMPUESTOS ORGANICOS
 INTRODUCCION A LA NOMENCLATURA E ISOMERIA DE LOS COMPUESTOS ORGANICOS Extractado de la Guía de Problemas de Química Orgánica I por la Dra. Diana Bekerman Fórmulas y representación de estructuras químicas
INTRODUCCION A LA NOMENCLATURA E ISOMERIA DE LOS COMPUESTOS ORGANICOS Extractado de la Guía de Problemas de Química Orgánica I por la Dra. Diana Bekerman Fórmulas y representación de estructuras químicas
UNIVERSIDAD DE PUERTO RICO RECINTO DE RÍO PIEDRAS DEPARTAMENTO DE QUÍMICA QUÍMICA ORGÁNICA II (QUIM 3032)
 QUÍMICA RGÁNICA II (QUIM 3032) PRIMER EXAMEN PARCIAL UNIVERSIDAD DE PUERT RIC RECINT DE RÍ PIEDRAS DEPARTAMENT DE QUÍMICA 25 DE FEBRER DE 2016 SECCIÓN: NMBRE: NÚM. DE ESTUDIANTE: El examen consta de 13
QUÍMICA RGÁNICA II (QUIM 3032) PRIMER EXAMEN PARCIAL UNIVERSIDAD DE PUERT RIC RECINT DE RÍ PIEDRAS DEPARTAMENT DE QUÍMICA 25 DE FEBRER DE 2016 SECCIÓN: NMBRE: NÚM. DE ESTUDIANTE: El examen consta de 13
OpenCourseWare UAM Química Orgánica I Invierno 2009 Dra. Alicia Lara Lemus
 AMINAS Clasificación Amoniaco Su fórmula general es: RNH2, R2NH o R3N, donde R es un grupo alquilo o arilo. Primaria (1 ) Secundaria (2 ) Terciaria (3 ) Según el número de grupos que se unen al nitrógeno
AMINAS Clasificación Amoniaco Su fórmula general es: RNH2, R2NH o R3N, donde R es un grupo alquilo o arilo. Primaria (1 ) Secundaria (2 ) Terciaria (3 ) Según el número de grupos que se unen al nitrógeno
HIDROCARBUROS AROMATICOS. Dr. Alberto Postigo
 HIDROCARBUROS AROMATICOS Dr. Alberto Postigo 1 1.-Nomenclatura. Fuentes naturales. Espectroscopia IR 2.-Reacciones de sustitución aromática electrofílica 3.-Hidrocarburos aromáticos polinucleares 4.- Reacciones
HIDROCARBUROS AROMATICOS Dr. Alberto Postigo 1 1.-Nomenclatura. Fuentes naturales. Espectroscopia IR 2.-Reacciones de sustitución aromática electrofílica 3.-Hidrocarburos aromáticos polinucleares 4.- Reacciones
DETERMINACIÓN ESTRUCTURAL (Teoría) CURSO , GRUP A 9 de febrero Apellidos... Nombre...
 DETERMINAIÓN ESTRUTURAL (Teoría) URS 2003-2004, GRUP A 9 de febrero 2004 Apellidos... Nombre... 1.- Que diferencias espera encontrar entre el 3 - y el 3 -D. a) en sus espectros de masas. El ión molecular
DETERMINAIÓN ESTRUTURAL (Teoría) URS 2003-2004, GRUP A 9 de febrero 2004 Apellidos... Nombre... 1.- Que diferencias espera encontrar entre el 3 - y el 3 -D. a) en sus espectros de masas. El ión molecular
Química Orgánica Grupos funcionales con oxígeno o nitrógeno
 Química rgánica Grupos funcionales con oxígeno o nitrógeno IES La Magdalena. Avilés. Asturias La parte carbonada constituye el esqueleto fundamental de las moléculas orgánicas. En esta estructura básica
Química rgánica Grupos funcionales con oxígeno o nitrógeno IES La Magdalena. Avilés. Asturias La parte carbonada constituye el esqueleto fundamental de las moléculas orgánicas. En esta estructura básica
Química Orgánica Grupos funcionales con oxígeno o nitrógeno
 Química rgánica Grupos funcionales con oxígeno o nitrógeno IES La Magdalena. Avilés. Asturias La parte carbonada constituye el esqueleto fundamental de las moléculas orgánicas. En esta estructura básica
Química rgánica Grupos funcionales con oxígeno o nitrógeno IES La Magdalena. Avilés. Asturias La parte carbonada constituye el esqueleto fundamental de las moléculas orgánicas. En esta estructura básica
Aldehídos y Cetonas: Compuestos carbonílicos
 Aldehídos y etonas: ompuestos carbonílicos Grupo arbonilo: plano, 120 o, polar, hibridación sp 2 carga parcial negativa : : : : :.. : carga parcial positiva esonancia Aldehído arbonilo etona - - - = alquil.
Aldehídos y etonas: ompuestos carbonílicos Grupo arbonilo: plano, 120 o, polar, hibridación sp 2 carga parcial negativa : : : : :.. : carga parcial positiva esonancia Aldehído arbonilo etona - - - = alquil.
ESPECTROSCOPÍA EJEMPLOS DE ELUCIDACION ESTRUCTURAL DE COMPUESTOS. Elucidación estructural: Ejemplo 1 Dados los siguientes espectros:
 ESPECTROSCOPÍA EJEMPLOS DE ELUCIDACION ESTRUCTURAL DE COMPUESTOS Elucidación estructural: Ejemplo 1 Dados los siguientes espectros: 1) Empezaremos por encontrar la formula molecular, pues no la tenemos.
ESPECTROSCOPÍA EJEMPLOS DE ELUCIDACION ESTRUCTURAL DE COMPUESTOS Elucidación estructural: Ejemplo 1 Dados los siguientes espectros: 1) Empezaremos por encontrar la formula molecular, pues no la tenemos.
Prelim. nomenclatura:prelim. nomenclatura 14/10/08 18:31 Página 1 NOMENCLATURA DE QUÍMICA ORGÁNICA
 Prelim. nomenclatura:prelim. nomenclatura 14/10/08 18:31 Página 1 NOMENCLATURA DE QUÍMICA ORGÁNICA Prelim. nomenclatura:prelim. nomenclatura 14/10/08 18:31 Página 2 PROYECTO EDITORIAL BIBLIOTECA DE QUÍMICAS
Prelim. nomenclatura:prelim. nomenclatura 14/10/08 18:31 Página 1 NOMENCLATURA DE QUÍMICA ORGÁNICA Prelim. nomenclatura:prelim. nomenclatura 14/10/08 18:31 Página 2 PROYECTO EDITORIAL BIBLIOTECA DE QUÍMICAS
Desplazamiento Químico. Dr. Jorge A. Palermo
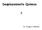 Desplazamiento Químico δ Dr. Jorge A. Palermo ν 0 = γ B 0 / 2π ECUACIÓN DE LARMOR E aumenta con B 0 Núcleo 1 2.35 Tesla 100 Mz 17.63 Tesla 750 Mz ν 0 aumenta con B 0 2 13 C 31 P 15.35 Mz 25.1 Mz 40.5 Mz
Desplazamiento Químico δ Dr. Jorge A. Palermo ν 0 = γ B 0 / 2π ECUACIÓN DE LARMOR E aumenta con B 0 Núcleo 1 2.35 Tesla 100 Mz 17.63 Tesla 750 Mz ν 0 aumenta con B 0 2 13 C 31 P 15.35 Mz 25.1 Mz 40.5 Mz
Sencillo C C Doble C = C Triple C C
 FORMULACIÓN ORGÁNICA Existe un nº inmenso de compuestos del carbono, por lo que se impone una clasificación y sistematización para su estudio. Las causas de tan amplia variedad De compuestos la encontramos
FORMULACIÓN ORGÁNICA Existe un nº inmenso de compuestos del carbono, por lo que se impone una clasificación y sistematización para su estudio. Las causas de tan amplia variedad De compuestos la encontramos
QUÍMICA DEL CARBONO 1. El carbono. 2. Grupos funcionales. 3. Isomería. 4. Compuestos orgánicos.
 QUÍMICA DEL CARBONO 1. El carbono. 2. Grupos funcionales. 3. Isomería. 4. Compuestos orgánicos. Química 1º bachillerato Química del carbono 1 1. EL CARBONO El carbono es una molécula muy especial capaz
QUÍMICA DEL CARBONO 1. El carbono. 2. Grupos funcionales. 3. Isomería. 4. Compuestos orgánicos. Química 1º bachillerato Química del carbono 1 1. EL CARBONO El carbono es una molécula muy especial capaz
QUÍMICA ORGÁNICA PÁGS LIBRO
 QUÍMICA ORGÁNICA PÁGS. 335-357 LIBRO Química del carbono Química del carbono; aquella que estudia los compuestos que tienen C Química del carbono HIDROCARBUROS Formados por C e H. Tipos: De cadena abierta
QUÍMICA ORGÁNICA PÁGS. 335-357 LIBRO Química del carbono Química del carbono; aquella que estudia los compuestos que tienen C Química del carbono HIDROCARBUROS Formados por C e H. Tipos: De cadena abierta
ESTRUCTURAS DE RESONANCIA
 1 ESTRUCTURAS DE RESONANCIA HIBRIDOS DE RESONANCIA CUANDO SON POSIBLES DOS O MÁS ESTRUCTURAS PARA REPRESENTAR LOS ENLACES DE UNA MOLÉCULA Y SÓLO DIFIENREN EN LA COLOCACIÓN DE LOS ELECTRONES LA MOLÉCULA
1 ESTRUCTURAS DE RESONANCIA HIBRIDOS DE RESONANCIA CUANDO SON POSIBLES DOS O MÁS ESTRUCTURAS PARA REPRESENTAR LOS ENLACES DE UNA MOLÉCULA Y SÓLO DIFIENREN EN LA COLOCACIÓN DE LOS ELECTRONES LA MOLÉCULA
UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUIMICAS QUÍMICA ORGÁNICA III ACIDOS CARBOXILICOS
 Nombre: Mayra Morales Carrera: Bioquímica y Farmacia ACIDEZ UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUIMICAS QUÍMICA ORGÁNICA III ACIDOS CARBOXILICOS Los ácidos carboxílicos son compuestos
Nombre: Mayra Morales Carrera: Bioquímica y Farmacia ACIDEZ UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUIMICAS QUÍMICA ORGÁNICA III ACIDOS CARBOXILICOS Los ácidos carboxílicos son compuestos
2. Describa la clasificación de las aminas, puede ver la página 644 capítulo 18 de su libro de Timberlake
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS, CUM UNIDAD DIDÁCTICA DE QUÍMICA, PRIMER AÑO GUÍA DE ESTUDIO 2015 SEMANA 23 AMINAS Elaborado por: Lic. Fernando Andrade Barrios 1. Defina
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS, CUM UNIDAD DIDÁCTICA DE QUÍMICA, PRIMER AÑO GUÍA DE ESTUDIO 2015 SEMANA 23 AMINAS Elaborado por: Lic. Fernando Andrade Barrios 1. Defina
Nombre: Curso: Fecha:
 GUÍA ESTUDIO Nº1 PROPIEDADES DE HIDROCARBUROS Y FUNCIONES ORGÁNICAS PROPIEDADES DE LOS HIDROCARBUROS Propiedades de alcanos Subsector Profesor Química Paulina Gómez a) Propiedades físicas: Son menos densos
GUÍA ESTUDIO Nº1 PROPIEDADES DE HIDROCARBUROS Y FUNCIONES ORGÁNICAS PROPIEDADES DE LOS HIDROCARBUROS Propiedades de alcanos Subsector Profesor Química Paulina Gómez a) Propiedades físicas: Son menos densos
1. Si las aminas son compuestos nitrogenados de dónde derivan?
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS, CUM UNIDAD DIDÁCTICA DE QUÍMICA, PRIMER AÑO GUÍA DE ESTUDIO 2016 SEMANA 23 AMINAS Elaborado por: Licda. Edda García 1. Si las aminas
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS, CUM UNIDAD DIDÁCTICA DE QUÍMICA, PRIMER AÑO GUÍA DE ESTUDIO 2016 SEMANA 23 AMINAS Elaborado por: Licda. Edda García 1. Si las aminas
FORMULACIÓN. Clasificación de los compuestos orgánicos. Hidrocarburos. Alcoholes y fenoles Éteres Aldehídos y cetonas Ácidos carboxílicos Esteres
 FORMULACIÓN Clasificación de los compuestos orgánicos Hidrocarburos. Alcoholes y fenoles Éteres Aldehídos y cetonas Ácidos carboxílicos Esteres CLASIFICACIÓN DE LOS COMPUESTOS ORGÁNICOS Clasificación de
FORMULACIÓN Clasificación de los compuestos orgánicos Hidrocarburos. Alcoholes y fenoles Éteres Aldehídos y cetonas Ácidos carboxílicos Esteres CLASIFICACIÓN DE LOS COMPUESTOS ORGÁNICOS Clasificación de
ESPECTROSCOPíA INFRARROJA
 ESPECTROSCOPíA INFRARROJA Química Orgánica 1 Facultad de Farmacia y Bioquímica UBA 2016 Autor: Dra. Isabel Perillo 1 Espectro electromagnético Unidades de l usadas: para UV-visible: nm (mm): 10-9 m para
ESPECTROSCOPíA INFRARROJA Química Orgánica 1 Facultad de Farmacia y Bioquímica UBA 2016 Autor: Dra. Isabel Perillo 1 Espectro electromagnético Unidades de l usadas: para UV-visible: nm (mm): 10-9 m para
UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUIMICAS QUIMICA DE ALIMENTOS. Factores que afectan la acidez de los ácidos carboxílicos.
 NOMBRE: Diana Jiménez UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUIMICAS QUIMICA DE ALIMENTOS ACIDOS CARBOXILICOS. Acidez de los ácidos carboxílicos Factores que afectan la acidez de los ácidos
NOMBRE: Diana Jiménez UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUIMICAS QUIMICA DE ALIMENTOS ACIDOS CARBOXILICOS. Acidez de los ácidos carboxílicos Factores que afectan la acidez de los ácidos
TEMA 1 NOMENCLATURA QUÍMICA ORGÁNICA (II). GRUPOS FUNCIONALES
 TEMA 1 NMENLATURA QUÍMIA RGÁNIA (II). GRUPS FUNINALES ÍNDIE 1. onceptos generales 2. Derivados halogenados 3. Alcoholes y fenoles 4. Éteres 5. Aldehídos y cetonas 6. Ácidos carboxílicos 7. Ésteres 8. Aminas
TEMA 1 NMENLATURA QUÍMIA RGÁNIA (II). GRUPS FUNINALES ÍNDIE 1. onceptos generales 2. Derivados halogenados 3. Alcoholes y fenoles 4. Éteres 5. Aldehídos y cetonas 6. Ácidos carboxílicos 7. Ésteres 8. Aminas
Espectro Electromagnético
 1 Espectro Electromagnético La luz es radiación electromagnética y está compuesta por una parte eléctrica y otra magnética. Las particulas subatómicas, electrones y fotones, tienen propiedades de partículas
1 Espectro Electromagnético La luz es radiación electromagnética y está compuesta por una parte eléctrica y otra magnética. Las particulas subatómicas, electrones y fotones, tienen propiedades de partículas
Haluro de alcanoilo. Síntesis
 DERIVADOS DE LOS ÁCIDOS CARBOXÍLICOS: HALUROS DE ALCANOIDES Y ANHÍDRIDOS Los acidos carboxilicos son compuestos orgánicos que contienen uno, dos o mas grupos carboxílico, R-COOH Haluro de alcanoilo Anhídridos
DERIVADOS DE LOS ÁCIDOS CARBOXÍLICOS: HALUROS DE ALCANOIDES Y ANHÍDRIDOS Los acidos carboxilicos son compuestos orgánicos que contienen uno, dos o mas grupos carboxílico, R-COOH Haluro de alcanoilo Anhídridos
FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS ORGÁNICOS
 FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS ORGÁNICOS.Índice 1. Generalidades 2. Hidrocarburos: 2.1 Alcanos 2.2 Alquenos 2.3 Alquinos 2.4 Radicales 2.5 Hidrocarburos ramificados 2.6 Hidrocarburos cíclicos
FORMULACIÓN Y NOMENCLATURA DE COMPUESTOS ORGÁNICOS.Índice 1. Generalidades 2. Hidrocarburos: 2.1 Alcanos 2.2 Alquenos 2.3 Alquinos 2.4 Radicales 2.5 Hidrocarburos ramificados 2.6 Hidrocarburos cíclicos
Teoría Estructural 25/06/2012
 La Química Orgánica está a punto de enloquecerme. Se me figura como un bosque tropical primigenio, lleno de las cosas más notables, una selva infinita y terrible en la que uno no se atreve a penetrar porque
La Química Orgánica está a punto de enloquecerme. Se me figura como un bosque tropical primigenio, lleno de las cosas más notables, una selva infinita y terrible en la que uno no se atreve a penetrar porque
RESUMEN DE FORMULACIÓN DE QUÍMICA ORGÁNICA
 RESUMEN DE FRMULACIÓN DE QUÍMICA RGÁNICA 1. HIDRCARBURS SATURADS (ALCANS) a) Los cuatro primeros tienen por nombres: CH 4 metano; - etano; - CH 2 - propano; - CH 2 - CH 2 - butano. El resto se nombra mediante
RESUMEN DE FRMULACIÓN DE QUÍMICA RGÁNICA 1. HIDRCARBURS SATURADS (ALCANS) a) Los cuatro primeros tienen por nombres: CH 4 metano; - etano; - CH 2 - propano; - CH 2 - CH 2 - butano. El resto se nombra mediante
COMPUESTOS ORGÁNICOS: FORMULACIÓN, ESTRUCTURA, PROPIEDADES,
 COMPUESTOS ORGÁNICOS: FORMULACIÓN, ESTRUCTURA, PROPIEDADES, Un libro que pretende ser útil a todos aquellos estudiantes que deseen iniciarse en el tema de la formulación orgánica y comprender, al mismo
COMPUESTOS ORGÁNICOS: FORMULACIÓN, ESTRUCTURA, PROPIEDADES, Un libro que pretende ser útil a todos aquellos estudiantes que deseen iniciarse en el tema de la formulación orgánica y comprender, al mismo
Práctica 6 IDENTIFICACIÓN DE CONTAMINANTES MEDIANTE ESPECTROSCOPÍA INFRARROJA
 Práctica 6 IDENTIFICACIÓN DE CONTAMINANTES MEDIANTE ESPECTROSCOPÍA INFRARROJA 1. Objetivo Familiarizarse con los fundamentos de la identificación de moléculas a partir de su espectro de absorción infrarrojo.
Práctica 6 IDENTIFICACIÓN DE CONTAMINANTES MEDIANTE ESPECTROSCOPÍA INFRARROJA 1. Objetivo Familiarizarse con los fundamentos de la identificación de moléculas a partir de su espectro de absorción infrarrojo.
Nomenclatura empírica o común de los ácidos carboxílicos. Nomenclatura IUPAC de los ácidos carboxílicos
 Nomenclatura empírica o común de los ácidos carboxílicos Poseen nombres derivados de su fuente original: Ácido fórmico (HCOOH) segregado por las hormigas Ácido acético (CH 3 COOH) contenido e integrante
Nomenclatura empírica o común de los ácidos carboxílicos Poseen nombres derivados de su fuente original: Ácido fórmico (HCOOH) segregado por las hormigas Ácido acético (CH 3 COOH) contenido e integrante
Conceptos basicos (III)
 erramientas de la Química rgánica erramientas de la Química rgánica ompuestos carbonílicos onceptos basicos (III) δ δ plano 120 º = polar sp 2 Z Z Z Z = ó Ar Z = ó Ar aldehídos cetonas María Font. Dpto.
erramientas de la Química rgánica erramientas de la Química rgánica ompuestos carbonílicos onceptos basicos (III) δ δ plano 120 º = polar sp 2 Z Z Z Z = ó Ar Z = ó Ar aldehídos cetonas María Font. Dpto.
TABLAS DE ESPECTROSCOPIA INFRARROJA
 Michelle Alvarez 4to Bioquímica línica TABLAS DE ESPETRSPIA INFRARRJA ALANS Forma sp3-h 2850-3000 intensa estrecha Tijera H2 y -H2 con 1450-1470 media Estrecha H3 Balanceo de H3 Balanceo de cadena de al
Michelle Alvarez 4to Bioquímica línica TABLAS DE ESPETRSPIA INFRARRJA ALANS Forma sp3-h 2850-3000 intensa estrecha Tijera H2 y -H2 con 1450-1470 media Estrecha H3 Balanceo de H3 Balanceo de cadena de al
QUÍMICA ORGÁNICA BÁSICA
 QUÍMICA ORGÁNICA BÁSICA 1. INTRODUCCIÓN: NATURALEZA DE LA QUÍMICA ORGÁNICA Panorama histórico y situación actual El carácter químico especial del carbono Fuentes y transformaciones de los compuestos orgánicos.
QUÍMICA ORGÁNICA BÁSICA 1. INTRODUCCIÓN: NATURALEZA DE LA QUÍMICA ORGÁNICA Panorama histórico y situación actual El carácter químico especial del carbono Fuentes y transformaciones de los compuestos orgánicos.
TEMA 9. DETERMINACIÓN DE ESTRUCTURAS MEDIANTE MÉTODOS FÍSICOS
 TEMA 9. DETERMINACIÓN DE ESTRUCTURAS MEDIANTE MÉTODOS FÍSICOS 1. Interacción de la energía radiante y la materia orgánica. 2. Fundamentos de la espectroscopia infrarroja: regiones del IR y modos fundamentales
TEMA 9. DETERMINACIÓN DE ESTRUCTURAS MEDIANTE MÉTODOS FÍSICOS 1. Interacción de la energía radiante y la materia orgánica. 2. Fundamentos de la espectroscopia infrarroja: regiones del IR y modos fundamentales
Reacciones de adición
 erramientas de la Química rgánica erramientas de la Química rgánica eacciones de adición en los alquenos : adición polar (I) eacciones de adición + + - δ+ δ- - 1 2 erramientas de la Química rgánica eacciones
erramientas de la Química rgánica erramientas de la Química rgánica eacciones de adición en los alquenos : adición polar (I) eacciones de adición + + - δ+ δ- - 1 2 erramientas de la Química rgánica eacciones
2ª Parte: Estructura y reactividad de
 2ª Parte: Estructura y reactividad de los compuestos CMPUESTS orgánicos. CARBNÍLICS 2.- Principales familias de compuestos orgánicos: - Hidrocarburos alifáticos: alcanos, alquenos y alquinos. - Hidrocarburos
2ª Parte: Estructura y reactividad de los compuestos CMPUESTS orgánicos. CARBNÍLICS 2.- Principales familias de compuestos orgánicos: - Hidrocarburos alifáticos: alcanos, alquenos y alquinos. - Hidrocarburos
Ejercicios de Espectroscopía Infrarroja para el curso de Química analítica IV
 Ejercicios de Espectroscopía Infrarroja para el curso de Química analítica IV Fernando de J. Amézquita L. Diana Mendoza O. Universidad de Guanajuato En esta presentación encontrarás once espectros de compuestos
Ejercicios de Espectroscopía Infrarroja para el curso de Química analítica IV Fernando de J. Amézquita L. Diana Mendoza O. Universidad de Guanajuato En esta presentación encontrarás once espectros de compuestos
Programa de Acceso Inclusivo, Equidad y Permanencia PAIEP U. de Santiago. Química
 GRUPOS FUNCIONALES Se denomina función a un átomo, o grupo de átomos, que reemplaza uno o varios átomos de hidrógeno en la molécula de un hidrocarburo, confiriendo a la sustancia resultante propiedades
GRUPOS FUNCIONALES Se denomina función a un átomo, o grupo de átomos, que reemplaza uno o varios átomos de hidrógeno en la molécula de un hidrocarburo, confiriendo a la sustancia resultante propiedades
QUIMICA ORGÁNICA II TALLER ESPCTROSCOPIA UV-VISIBLE- IR TALLER DE ESPECTROSCOPIA IR
 TALLER DE ESPECTROSCOPIA IR Nomenclatura de los sistemas dieno: Dieno homoanular No sos dienos homoanular Dieno heteroanular No es dieno heteroanular Endo Exo Sistema cruzado no se aplica Wodward Fieser
TALLER DE ESPECTROSCOPIA IR Nomenclatura de los sistemas dieno: Dieno homoanular No sos dienos homoanular Dieno heteroanular No es dieno heteroanular Endo Exo Sistema cruzado no se aplica Wodward Fieser
UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUIMICAS QUIMICA ORGANICA
 UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUIMICAS QUIMICA ORGANICA TANIA POZO CARRERA DE QUIMICA FARMACEUTICA ACIDEZ DE LOS ACIDOS CARBOXILICOS Los ácidos carboxílicos contienen el grupo carboxilo
UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUIMICAS QUIMICA ORGANICA TANIA POZO CARRERA DE QUIMICA FARMACEUTICA ACIDEZ DE LOS ACIDOS CARBOXILICOS Los ácidos carboxílicos contienen el grupo carboxilo
UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD CIENCIAS QUIMICAS ESCUELA DE QUIMICA FARMACEUTICA QUIMICA ORGANICA III
 UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD CIENCIAS QUIMICAS ESCUELA DE QUIMICA FARMACEUTICA QUIMICA ORGANICA III Nombre: Mayra Vallejo Palacios Curso: 5 semestre Farmacia ACIDEZ DE LOS ACIDOS CARBOXILICOS
UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD CIENCIAS QUIMICAS ESCUELA DE QUIMICA FARMACEUTICA QUIMICA ORGANICA III Nombre: Mayra Vallejo Palacios Curso: 5 semestre Farmacia ACIDEZ DE LOS ACIDOS CARBOXILICOS
NOMENCLATURA DE GRUPOS FUNCIONALES
 Química IIº Medio Prof. Juan Pastrián / Sofía Ponce de León MECLATUA DE GUPS FUCIALES ALCLES Los alcoholes se caracterizan por poseer el grupo funcional hidroxilo ( ) en su estructura, el que se encuentra
Química IIº Medio Prof. Juan Pastrián / Sofía Ponce de León MECLATUA DE GUPS FUCIALES ALCLES Los alcoholes se caracterizan por poseer el grupo funcional hidroxilo ( ) en su estructura, el que se encuentra
NOMENCLATURA Y FORMULACION
 NOMENCLATURA Y FORMULACION RESUMEN NORMAS IUPAC La nomenclatura de compuestos orgánicos puede llegar a ser extraordinariamente compleja. En este seminario sólo se pretende dar unas nociones muy elementales
NOMENCLATURA Y FORMULACION RESUMEN NORMAS IUPAC La nomenclatura de compuestos orgánicos puede llegar a ser extraordinariamente compleja. En este seminario sólo se pretende dar unas nociones muy elementales
COMPUESTOS NITROGENADOS
 IQ3204 QUÍMICA ORGÁNICA Profesores: Raúl Quijada, Teresa Velilla Otoño 2013 Auxiliar: Moisés Gómez COMPUESTOS NITROGENADOS 1. GENERALIDADES 1.1 Nomenclatura AMINAS R NH 2 R 2 NH R 3 N Amina Primaria Amina
IQ3204 QUÍMICA ORGÁNICA Profesores: Raúl Quijada, Teresa Velilla Otoño 2013 Auxiliar: Moisés Gómez COMPUESTOS NITROGENADOS 1. GENERALIDADES 1.1 Nomenclatura AMINAS R NH 2 R 2 NH R 3 N Amina Primaria Amina
Química del Carbono, Curso /05/2014. Tema 9. Química del Carbono. El carbono: Z=6 A=12. C =1s 2 2s 2 p 2
 Tema 9 Química del Carbono El carbono: Z=6 A=12 C =1s 2 2s 2 p 2 C 1 Se puede representar como En el espacio, la segunda capa: 2 Orbitales del carbono en conjunto ORBITALES QUE EL CARBONO EMPLEA EN SUS
Tema 9 Química del Carbono El carbono: Z=6 A=12 C =1s 2 2s 2 p 2 C 1 Se puede representar como En el espacio, la segunda capa: 2 Orbitales del carbono en conjunto ORBITALES QUE EL CARBONO EMPLEA EN SUS
GLÚCIDOS Y LÍPIDOS 4/6/15 GLÚCIDOS. (CH 2 O)n n 3. Biomoléculas DEPARTAMENTO DE BIOQUÍMICA ESFUNO E.U.T.M. Grupos funcionales. Esqueleto carbonado
 DEPARTAMENTO DE BIOQUÍMICA ESFUNO E.U.T.M Biomoléculas Las moléculas de los sistemas biológicos estan compuestas principalmente de carbono, hidrógeno, oxígeno, nitrógeno, azufre y fósforo. GLÚCIDOS Y LÍPIDOS
DEPARTAMENTO DE BIOQUÍMICA ESFUNO E.U.T.M Biomoléculas Las moléculas de los sistemas biológicos estan compuestas principalmente de carbono, hidrógeno, oxígeno, nitrógeno, azufre y fósforo. GLÚCIDOS Y LÍPIDOS
CROMATOGRAFÍA LÍQUIDA DE ALTA RESOLUCIÓN
 CROMATOGRAFÍA LÍQUIDA DE ALTA RESOLUCIÓN Curso: Química Analítica II Loreto Ascar 2012 Esquema de las bases de la separación en cromatografía de: (a)absorción, (b) partición, (c) Intercambio iónico y (d)
CROMATOGRAFÍA LÍQUIDA DE ALTA RESOLUCIÓN Curso: Química Analítica II Loreto Ascar 2012 Esquema de las bases de la separación en cromatografía de: (a)absorción, (b) partición, (c) Intercambio iónico y (d)
Proteínas Polímeros de aminoácidos ( resíduos) PM aa aprox 110 PM prot
 Proteínas Polímeros de aminoácidos (50-2000 resíduos) PM aa aprox 110 PM prot 5000-200000 DiversasFunciones Estructurales (rígidas), Enzimas (más flexibles) Estructuras: primaria, secundaria, terciaria,
Proteínas Polímeros de aminoácidos (50-2000 resíduos) PM aa aprox 110 PM prot 5000-200000 DiversasFunciones Estructurales (rígidas), Enzimas (más flexibles) Estructuras: primaria, secundaria, terciaria,
QUÍMICA ORGÁNICA I (1345) CUADERNO ELECTRÓNICO DE APUNTES
 UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO Facultad de Química QUÍMICA ORGÁNICA I (1345) CUADERNO ELECTRÓNICO DE APUNTES José Luis Medina Franco Semestre 2002-2 Presentación del cuaderno electrónico Bienvenido
UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO Facultad de Química QUÍMICA ORGÁNICA I (1345) CUADERNO ELECTRÓNICO DE APUNTES José Luis Medina Franco Semestre 2002-2 Presentación del cuaderno electrónico Bienvenido
AMINAS. Dra. Ana M. Bruno 2016
 Dra. Ana M. Bruno 2016 Algunas aminas biológicamente activas Muchas drogas de adicción son alcaloides Estructura de las aminas El amoniaco tiene una estructura tetraédrica algo distorsionada, con una de
Dra. Ana M. Bruno 2016 Algunas aminas biológicamente activas Muchas drogas de adicción son alcaloides Estructura de las aminas El amoniaco tiene una estructura tetraédrica algo distorsionada, con una de
Ejercicios variados resueltos
 Ejercicios variados resueltos Programa de Acceso Inclusivo, Equidad y Permanencia 1. Cuál de los siguientes compuestos es isómero del CH 3 CH 2 COOH? a) CH 3 CO CH 2 OH b) CH 3 CH 2 CHO c) CH 2 =CH COOH
Ejercicios variados resueltos Programa de Acceso Inclusivo, Equidad y Permanencia 1. Cuál de los siguientes compuestos es isómero del CH 3 CH 2 COOH? a) CH 3 CO CH 2 OH b) CH 3 CH 2 CHO c) CH 2 =CH COOH
FORMULACIÓN DE QUÍMICA ORGÁNICA 1- HIDROCARBUROS DE CADENA ABIERTA A) ALCANOS
 FORMULACIÓN DE QUÍMICA ORGÁNICA 1- HIDROCARBUROS DE CADENA ABIERTA A) ALCANOS Fórmula molecular C n H 2n+2 Sufijo ANO. Para los alcanos de cadena lineal, si tienen 1 C se utiliza el prefijo met-; 2 C et-;
FORMULACIÓN DE QUÍMICA ORGÁNICA 1- HIDROCARBUROS DE CADENA ABIERTA A) ALCANOS Fórmula molecular C n H 2n+2 Sufijo ANO. Para los alcanos de cadena lineal, si tienen 1 C se utiliza el prefijo met-; 2 C et-;
COMPLEMENTO CLASE AUXILIAR N 1: NOMENCLATURA IUPAC
 IQ3204 QUÍMICA RGÁNICA toño 2010 Profesores: Raúl Quijada, Teresa Velilla Auxiliar: Óscar Arias CMPLEMENT CLASE AUXILIAR N 1: NMENCLATURA IUPAC Dependiendo de los grupos funcionales presentes, las sustancias
IQ3204 QUÍMICA RGÁNICA toño 2010 Profesores: Raúl Quijada, Teresa Velilla Auxiliar: Óscar Arias CMPLEMENT CLASE AUXILIAR N 1: NMENCLATURA IUPAC Dependiendo de los grupos funcionales presentes, las sustancias
Criterio para aromaticidad
 Química Orgánica Paula Yurkanis Bruice Capítulos 14 y 15 Reacciones de SEA en el benceno Criterio para aromaticidad 1. Un compuesto debe tener una nube cíclica ininterrumpida de electrones π por arriba
Química Orgánica Paula Yurkanis Bruice Capítulos 14 y 15 Reacciones de SEA en el benceno Criterio para aromaticidad 1. Un compuesto debe tener una nube cíclica ininterrumpida de electrones π por arriba
Nomenclatura Grupos Funcionales
 IQ3204 Química Orgánica Semestre Otoño 2014 Clase Auxiliar Nº1 Nomenclatura Grupos Funcionales Profesores: Raúl Quijada, Teresa Velilla Profesor Auxiliar: Moisés Gómez Clasificación de los Hidrocarburos:
IQ3204 Química Orgánica Semestre Otoño 2014 Clase Auxiliar Nº1 Nomenclatura Grupos Funcionales Profesores: Raúl Quijada, Teresa Velilla Profesor Auxiliar: Moisés Gómez Clasificación de los Hidrocarburos:
TEMA 2. CLASIFICACION Y NOMECLATURA DE LOS COMPUESTOS ORGANICOS.
 TEMA 2. LASIFIAIN Y NMELATURA DE LS MPUESTS RGANIS. 1. oncepto de radical y grupo funcional. Series homólogas. 2. Principales tipos de compuestos orgánicos. Formulación y nomenclatura. 2 Tema 2 TEMA 2.
TEMA 2. LASIFIAIN Y NMELATURA DE LS MPUESTS RGANIS. 1. oncepto de radical y grupo funcional. Series homólogas. 2. Principales tipos de compuestos orgánicos. Formulación y nomenclatura. 2 Tema 2 TEMA 2.
Resonancia Magnética Nuclear
 Clase 4 152.952 147.290 123.188 117.525 114.209 113.216 76.850 55.678 48.146 41.562 40.012 33.361 32.113 23.659 20.654 19.816 19.720 190 180 170 160 150 140 130 120 110 100 90 80 70 60 50 40 30 20 10 ppm
Clase 4 152.952 147.290 123.188 117.525 114.209 113.216 76.850 55.678 48.146 41.562 40.012 33.361 32.113 23.659 20.654 19.816 19.720 190 180 170 160 150 140 130 120 110 100 90 80 70 60 50 40 30 20 10 ppm
GUÍA DE GRUPOS FUNCIONALES
 GUÍA DE GRUPOS FUNCIONALES Área Química Resultados de aprendizaje Conocer el concepto de disolución y calcular la concentración de esta en ejercicios, de forma lógica. Contenidos 1. Alcoholes simples y
GUÍA DE GRUPOS FUNCIONALES Área Química Resultados de aprendizaje Conocer el concepto de disolución y calcular la concentración de esta en ejercicios, de forma lógica. Contenidos 1. Alcoholes simples y
La Espectroscopía de Infrarrojo. Infrarrojo. Los enlaces y el infrarrojo. Espectroscopia de Infrarrojo. Espectroscopia de Infrarrojo
 Los enlaces y el infrarrojo La Espectroscopía de Infrarrojo hν IR d1 d2 Baja energía Alta energía María Font.. Dpto. Química Orgánica y Farmacéutica. Universidad de Navarra 1 María Font.. Dpto. Química
Los enlaces y el infrarrojo La Espectroscopía de Infrarrojo hν IR d1 d2 Baja energía Alta energía María Font.. Dpto. Química Orgánica y Farmacéutica. Universidad de Navarra 1 María Font.. Dpto. Química
HIDROCARBUROS AROMÁTICOS
 HIDROCARBUROS AROMÁTICOS Los hidrocarburos aromáticos son compuestos insaturados de un tipo especial. Originalmente recibieron el nombre de aromáticos debido al aroma que algunos poseen. Sin embargo no
HIDROCARBUROS AROMÁTICOS Los hidrocarburos aromáticos son compuestos insaturados de un tipo especial. Originalmente recibieron el nombre de aromáticos debido al aroma que algunos poseen. Sin embargo no
3.1 EL ATOMO DE CARBONO
 3.1 EL ATOMO DE CARBONO La química orgánica es la química de los compuestos del carbono El nombre engañoso orgánica es una reliquia de los tiempos en que los compuestos químicos se dividían según su origen,
3.1 EL ATOMO DE CARBONO La química orgánica es la química de los compuestos del carbono El nombre engañoso orgánica es una reliquia de los tiempos en que los compuestos químicos se dividían según su origen,
Química Analítica Orgánica
 Curso de especialización en procesos farmacéuticos y biotecnológicos Química Analítica Orgánica Dra. Victoria Cavaliere 2013 Objetivos de la materia Lograr que el alumno conozca los fundamentos teóricoexperimentales
Curso de especialización en procesos farmacéuticos y biotecnológicos Química Analítica Orgánica Dra. Victoria Cavaliere 2013 Objetivos de la materia Lograr que el alumno conozca los fundamentos teóricoexperimentales
Tema 9. Química Orgánica
 Tema 9. Química Orgánica ÍNDICE 1. Enlace covalente en las moléculas orgánicas 1.1. ibridaciones del carbono 1.2. Resonancia 1.3. Polaridad de enlace 2. Representación de moléculas orgánicas 3. idrocarburos
Tema 9. Química Orgánica ÍNDICE 1. Enlace covalente en las moléculas orgánicas 1.1. ibridaciones del carbono 1.2. Resonancia 1.3. Polaridad de enlace 2. Representación de moléculas orgánicas 3. idrocarburos
Química Orgánica. por átomos de carbono. A diferencia de otros
 Química Orgánica La definición moderna de la química orgánica es el estudio de los compuestos que se componen por átomos de carbono. A diferencia de otros elementos, el carbono crea enlaces muy fuertes
Química Orgánica La definición moderna de la química orgánica es el estudio de los compuestos que se componen por átomos de carbono. A diferencia de otros elementos, el carbono crea enlaces muy fuertes
Facultad de Farmacia. Departamento de Química Física. Universidad de Granada. OBTENCIÓN N DEL ESPECTRO IR del Ácido acetilsalicílico.
 Facultad de Farmacia Universidad de Granada PRÁCTICA Nº N 4 Departamento de Química Física OBTENCIÓN N DEL ESPECTRO IR del Ácido acetilsalicílico lico OBJETIVO: Obtener el espectro IR del ácido acetilsalicílico
Facultad de Farmacia Universidad de Granada PRÁCTICA Nº N 4 Departamento de Química Física OBTENCIÓN N DEL ESPECTRO IR del Ácido acetilsalicílico lico OBJETIVO: Obtener el espectro IR del ácido acetilsalicílico
MATERIAL 09 TEMA: ESPECTROSCOPÍA DE ABSORCION MOLECULAR EN EL ULTRAVIOLETA
 MATERIAL 09 TEMA: ESPECTROSCOPÍA DE ABSORCION MOLECULAR EN EL ULTRAVIOLETA y EL VISIBLE La espectroscopia de absorción molecular en el ultravioleta y visible se emplea en el análisis cuantitativo y es
MATERIAL 09 TEMA: ESPECTROSCOPÍA DE ABSORCION MOLECULAR EN EL ULTRAVIOLETA y EL VISIBLE La espectroscopia de absorción molecular en el ultravioleta y visible se emplea en el análisis cuantitativo y es
REACTIVIDAD DE LOS COMPUESTOS ORGÁNICOS
 REATIVIDAD DE LS MPUESTS RGÁNIS 1. Reacciones inorgánicas / Reacciones orgánicas 2. Representación general de una reacción orgánica 3. Algunos aspectos a tener en cuenta en las reacciones orgánicas 4.
REATIVIDAD DE LS MPUESTS RGÁNIS 1. Reacciones inorgánicas / Reacciones orgánicas 2. Representación general de una reacción orgánica 3. Algunos aspectos a tener en cuenta en las reacciones orgánicas 4.
Química. Hibridación de Orbitales Atómicos en el Carbono
 Química Hibridación de Orbitales Atómicos en el Carbono La estructura electrónica de los átomos que constituyen una molécula orgánica determina la estructura tridimensional de ésta y sus propiedades. sp
Química Hibridación de Orbitales Atómicos en el Carbono La estructura electrónica de los átomos que constituyen una molécula orgánica determina la estructura tridimensional de ésta y sus propiedades. sp
QUÍMICA DEL CARBONO. Elaborado por Carlos García. CSCJ Salesianas 0
 QUÍMICA DEL CARBONO Elaborado por Carlos García. CSCJ Salesianas 0 EL ÁTOMO DE CARBONO El átomo de carbono tiene una covalencia de 4. El átomo de carbono puede formar enlaces covalentes (s y p) con otros
QUÍMICA DEL CARBONO Elaborado por Carlos García. CSCJ Salesianas 0 EL ÁTOMO DE CARBONO El átomo de carbono tiene una covalencia de 4. El átomo de carbono puede formar enlaces covalentes (s y p) con otros
QUÍMICA // 2º BACHILLERATO.
 QUÍMICA // 2º BACHILLERATO. FORMULACIÓN Y NOMENCLATURA QUÍMICA ORGANICA. TEMA 2 TEMARIO QUÍMICA.. I.E.S. FERNANDO DE LOS RÍOS (QUINTANAR DEL REY) Temario Química. Tema 2. 2 Índice de Contenido. 1. INTRODUCCIÓN....
QUÍMICA // 2º BACHILLERATO. FORMULACIÓN Y NOMENCLATURA QUÍMICA ORGANICA. TEMA 2 TEMARIO QUÍMICA.. I.E.S. FERNANDO DE LOS RÍOS (QUINTANAR DEL REY) Temario Química. Tema 2. 2 Índice de Contenido. 1. INTRODUCCIÓN....
Espectroscopía de Infrarrojo (IR) y espectrometría de masas (MS)
 Espectroscopía de Infrarrojo (IR) y espectrometría de masas (MS) Elucidación Estructural de Compuestos Orgánicos Resonancia Magnética Nuclear (RMN) Espectrometría de Masa (MS) Espectroscopía de Infrarojo
Espectroscopía de Infrarrojo (IR) y espectrometría de masas (MS) Elucidación Estructural de Compuestos Orgánicos Resonancia Magnética Nuclear (RMN) Espectrometría de Masa (MS) Espectroscopía de Infrarojo
c = λν λ: cm; ν: ciclos/seg E = hν c: velocidad de la luz (en el vacío: 3 x 1010 cm/seg) E = hc/ν h: cte. de Planck (6.62 x 1027 erg/seg) Y
 Espectroscopía Espectroscopía ultravioleta-visible visible Espectroscopía infrarroja Espectroscopía de resonancia magnética nuclear Espectrometría de masas Pincipisd Principios de la Espectroscopía Molecular:
Espectroscopía Espectroscopía ultravioleta-visible visible Espectroscopía infrarroja Espectroscopía de resonancia magnética nuclear Espectrometría de masas Pincipisd Principios de la Espectroscopía Molecular:
Reacciones Ácido-Base 25/06/2012
 Básicas ITESM, campus qro. 1 Gran número de reacciones orgánicas son del tipo ácido- base. Diferenciar entre un ácido y una base usando las definiciones : 1. Bronsted-Lowry 2. Lewis. Factores que afectan
Básicas ITESM, campus qro. 1 Gran número de reacciones orgánicas son del tipo ácido- base. Diferenciar entre un ácido y una base usando las definiciones : 1. Bronsted-Lowry 2. Lewis. Factores que afectan
Química Orgánica y Biológica Apunte
 FUERZAS INTERMOLECULARES El enlace covalente es la unión que explica el mantenimiento de la unidad estructural de un compuesto orgánico. Además de este enlace intramolecular se pueden dar interacciones
FUERZAS INTERMOLECULARES El enlace covalente es la unión que explica el mantenimiento de la unidad estructural de un compuesto orgánico. Además de este enlace intramolecular se pueden dar interacciones
FORMULACIÓN BÁSICA QUÍMICA ORGÁNICA
 FORMULACIÓN BÁSICA QUÍMICA ORGÁNICA La fórmula empírica indica los elementos que forman la molécula y la proporción relativa de los mismos. CH (escasa información) La fórmula molecular indica el número
FORMULACIÓN BÁSICA QUÍMICA ORGÁNICA La fórmula empírica indica los elementos que forman la molécula y la proporción relativa de los mismos. CH (escasa información) La fórmula molecular indica el número
TEMA 2 CLASIFICACION Y NOMECLATURA DE LOS COMPUESTOS ORGANICOS
 TEMA LASIFIAIN Y NMELATURA DE LS MPUESTS RGANIS. oncepto de radical y grupo funcional. Series homólogas.. Principales tipos de compuestos orgánicos. Formulación y nomenclatura. Fundamentos de Química rgánica
TEMA LASIFIAIN Y NMELATURA DE LS MPUESTS RGANIS. oncepto de radical y grupo funcional. Series homólogas.. Principales tipos de compuestos orgánicos. Formulación y nomenclatura. Fundamentos de Química rgánica
FACTORES QUE AFECTAN AL DESPLAZAMIENTO QUIMICO (δ) EN RMN PROTÓNICA. Los principales factores que afectan al desplazamiento químico son:
 Elucidación estructural: Resonancia Magnética Nuclear (desplazamiento de 1 H) FACTORES QUE AFECTAN AL DESPLAZAMIENTO QUIMICO (δ) EN RMN PROTÓNICA Los principales factores que afectan al desplazamiento
Elucidación estructural: Resonancia Magnética Nuclear (desplazamiento de 1 H) FACTORES QUE AFECTAN AL DESPLAZAMIENTO QUIMICO (δ) EN RMN PROTÓNICA Los principales factores que afectan al desplazamiento
Tabla de Preferencia de Grupos Funcionales de Química Orgánica
 Tabla de Preferencia de Grupos Funcionales de Química Orgánica Función Química Ácido Carboxílico Éster Amida Aldehído Cetona Alcohol Amina Fórmula Grupo General Funcional O - COOH R C OH O -COO- R C O
Tabla de Preferencia de Grupos Funcionales de Química Orgánica Función Química Ácido Carboxílico Éster Amida Aldehído Cetona Alcohol Amina Fórmula Grupo General Funcional O - COOH R C OH O -COO- R C O
ACIDEZ DE LOS ÁCIDOS CARBOXÍLICOS
 UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUIMICAS TRABAJO DE QUIMICA ORGANICA III Nombre: Kerly Ochoa Romero Carrera: Quimica Semestre: Quinto 1.- Estructura ACIDEZ DE LOS ÁCIDOS CARBOXÍLICOS
UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUIMICAS TRABAJO DE QUIMICA ORGANICA III Nombre: Kerly Ochoa Romero Carrera: Quimica Semestre: Quinto 1.- Estructura ACIDEZ DE LOS ÁCIDOS CARBOXÍLICOS
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS, CUM UNIDAD DIDÁCTICA QUÍMICA, PRIMER AÑO. Guías de Estudio Química 2010
 HIDROCARBUROS AROMÁTICOS Y COMPUESTOS ORGÁNICOS HALOGENADOS ELABORADO POR: LICDA. VIVIAN MARGARITA SANCHEZ GARRIDO. HIDROCARBUROS AROMATICOS (contienen anillos bencénicos) Benceno y sus derivados Hidrocarburos
HIDROCARBUROS AROMÁTICOS Y COMPUESTOS ORGÁNICOS HALOGENADOS ELABORADO POR: LICDA. VIVIAN MARGARITA SANCHEZ GARRIDO. HIDROCARBUROS AROMATICOS (contienen anillos bencénicos) Benceno y sus derivados Hidrocarburos
Espectrometría de Masa
 Espectrometría de Masa La espectrometría de masa crea partículas cargadas (iones). Luego estos iones se analizan y pueden entregar información sobre el peso molecular de la molécula y acerca de su estructura
Espectrometría de Masa La espectrometría de masa crea partículas cargadas (iones). Luego estos iones se analizan y pueden entregar información sobre el peso molecular de la molécula y acerca de su estructura
REACTIVIDAD DE LOS COMPUESTOS ORGÁNICOS
 REACTIVIDAD DE LOS COMPUESTOS ORGÁNICOS Reacciones Inorgánicas En general son rápidas y sencillas, especialmente las iónicas en solución acuosa porque los reactivos ya están listos para reaccionar. Reacciones
REACTIVIDAD DE LOS COMPUESTOS ORGÁNICOS Reacciones Inorgánicas En general son rápidas y sencillas, especialmente las iónicas en solución acuosa porque los reactivos ya están listos para reaccionar. Reacciones
QUÍMICA ORGÁNICA. Física y Química CH 3 CH CH CH 2 CH 3 CH 3 CH 2 CH 2 C CH
 1 QUÍMIA GÁNIA Física y Química 2 La química del carbono o química orgánica, estudia todas aquellas sustancias en cuyas moléculas toma parte el carbono Los átomos de carbono, tienen mucha facilidad para
1 QUÍMIA GÁNIA Física y Química 2 La química del carbono o química orgánica, estudia todas aquellas sustancias en cuyas moléculas toma parte el carbono Los átomos de carbono, tienen mucha facilidad para
QUÍMICA. 2º Bachilerrato orgánica Estereoisomería:
 TEMA 10: QUÍMICA ORÁNICA. 1.- Isomerías. En química orgánica es usual encontrar compuestos químicos diferentes que poseen igual fórmula molecular. Estos compuestos se denominan isómeros. 1.1. Isómeros
TEMA 10: QUÍMICA ORÁNICA. 1.- Isomerías. En química orgánica es usual encontrar compuestos químicos diferentes que poseen igual fórmula molecular. Estos compuestos se denominan isómeros. 1.1. Isómeros
TEMA 3. Grupos funcionales con enlaces múltiples.
 TEMA 3. Grupos funcionales con enlaces múltiples. Alquenos. Alquinos. Compuestos aromáticos. El grupo carbonilo. Aldehídos. Cetonas. Ácidos carboxílicos. Ésteres. Anhídridos. Amidas Tioésteres, Fosfoésteres,
TEMA 3. Grupos funcionales con enlaces múltiples. Alquenos. Alquinos. Compuestos aromáticos. El grupo carbonilo. Aldehídos. Cetonas. Ácidos carboxílicos. Ésteres. Anhídridos. Amidas Tioésteres, Fosfoésteres,
AMINOÁCIDOS Y PROTEÍNAS
 4/6/15 DEPARTAMENTO DE BIOQUÍMICA ESFUNO EUTM AMINOÁCIDOS Y PROTEÍNAS ESTRUCTURA DE LOS AMINOÁCIDOS Grupo carboxilo Grupo amino Carbono α Cadena Lateral Ión dipolar o zwitterión Las proteínas tienen L-aminoácidos
4/6/15 DEPARTAMENTO DE BIOQUÍMICA ESFUNO EUTM AMINOÁCIDOS Y PROTEÍNAS ESTRUCTURA DE LOS AMINOÁCIDOS Grupo carboxilo Grupo amino Carbono α Cadena Lateral Ión dipolar o zwitterión Las proteínas tienen L-aminoácidos
CONJUGACIÓN, RESONANCIA Y ESTABILIDAD DE ALQUENOS
 CONJUGACIÓN, RESONANCIA Y ESTABILIDAD DE ALQUENOS Universidad de San Carlos de Guatemala Facultad de Ciencias Químicas y Farmacia Departamento de Química Orgánica Sistemas Conjugados Los sistemas insaturados
CONJUGACIÓN, RESONANCIA Y ESTABILIDAD DE ALQUENOS Universidad de San Carlos de Guatemala Facultad de Ciencias Químicas y Farmacia Departamento de Química Orgánica Sistemas Conjugados Los sistemas insaturados
Los principales grupos funcionales son los siguientes:
 GRUPOS FUNCIONALES Qué es un grupo funcional? Hemos visto que los hidrógenos de los hidrocarburos pueden ser sustituidos por átomos de otro metal o por un agrupamiento de átomos para obtener compuestos
GRUPOS FUNCIONALES Qué es un grupo funcional? Hemos visto que los hidrógenos de los hidrocarburos pueden ser sustituidos por átomos de otro metal o por un agrupamiento de átomos para obtener compuestos
Unidad 1.3.4: Conjugación y resonancia en alquenos. Química Orgánica I Facultad de CC.QQ. Y Farmacia USAC Primer semestre 2017
 Unidad 1.3.4: Conjugación y resonancia en alquenos Química Orgánica I Facultad de CC.QQ. Y Farmacia USAC Primer semestre 2017 Dienos conjugados Son compuestos que presentan dos enlaces dobles C-C, separados
Unidad 1.3.4: Conjugación y resonancia en alquenos Química Orgánica I Facultad de CC.QQ. Y Farmacia USAC Primer semestre 2017 Dienos conjugados Son compuestos que presentan dos enlaces dobles C-C, separados
UNIDAD 14. NOMENCLATURA QUÍMICA ORGÁNICA Cómo se nombran los compuestos orgánicos?
 P á g i n a 157 UNIDAD 14. NOMENCLATURA QUÍMICA ORGÁNICA Cómo se nombran los compuestos orgánicos? Desempeño Esperado. El estudiante reconoce los grupos funcionales de la química orgánica, identifica por
P á g i n a 157 UNIDAD 14. NOMENCLATURA QUÍMICA ORGÁNICA Cómo se nombran los compuestos orgánicos? Desempeño Esperado. El estudiante reconoce los grupos funcionales de la química orgánica, identifica por
