María Cristina Caterina Gisela Ortiz Ariadna Tomeo
|
|
|
- Samuel Quintero Guzmán
- hace 6 años
- Vistas:
Transcripción
1 María Cristina Caterina Gisela Ortiz Ariadna Tomeo 1
2 Punto de fusión Definición: Temperatura del cambio de estado sólido-líquido a 1 atmósfera de presión. 2
3 Punto de fusión En un sólido cristalino, las moléculas están unidas por fuerzas de cohesión formando el retículo cristalino. El aumento de la temperatura provoca aumento de la energía cinética del sistema lo que lleva a vencer las fuerzas intermoleculares y el sólido funde 3
4 Punto de fusión Hay diferencias entre las uniones intermoleculares de sólidos orgánicos e inorgánicos? En los compuestos orgánicos predominan las fuerzas de Van der Waals. También las uniones puente de hidrógeno y las atracciones dipolo-dipolo. En los compuestos inorgánicos tienen mucha importancia las uniones iónicas. 4
5 Punto de fusión La presión externa tiene influencia en la temperatura de fusión? A diferencia del punto de ebullición, el punto de fusión de una sustancia es poco afectado por la presión. 5
6 Punto de fusión En las sustancias puras, el proceso de fusión ocurre a una temperatura definida, o con un intervalo muy pequeño. En cambio, si hay impurezas, éstas provocan que la temperatura de fusión disminuya y el intervalo en que se observa el cambio de estado se amplíe. 6
7 P unto de fus ión pres enc ia de impurezas 75
8 Punto de fusión Cómo podemos verificar la presencia de impurezas en un sólido? -determinando la temperatura de fusión -realizando una cromatografía analítica Llenado de capilares para determinar la temperatura de fusión 8
9 Punto de fusión Cómo se determina la temperatura de fusión? Distintos aparatos empleados 9
10 Punto de fusión Cómo se determina la temperatura de fusión? Distintos aparatos electrónicos empleados 10
11 Punto de fusión Es criterio de pureza? -No, existen mezclas que se comportan como sólidos puros: son conocidas como eutécticas: funden a temperatura constante. -Algunos tipos de impurezas no deprimen la temperatura de fusión. Es criterio de identidad? No, varios sólidos pueden tener temperaturas de fusión iguales o muy similares. 11
12 Punto de fusión Pero hay alguna forma de emplear el PF en la identificación de un compuesto? Por ejemplo: tenemos un sólido (X) que suponemos es ácido benzoico y contamos con un testigo (T) del mismo. Si al tomar el punto de fusión de una mezcla (X+T) el valor obtenido es igual al de X purificado, puedo asegurar que X=T. Si el valor disminuye y aumenta el rango, uno de los sólidos está actuando como impureza. A este ensayo se lo conoce como PF mezcla 12
13 Purificación de sólidos Los métodos empleados para la purificación de sólidos son: recristalización sublimación cromatografía preparativa 13
14 Siempre es necesario purificar un sólido antes de emplearlo? Algunos sólidos se van contaminando con el tiempo, por ejemplo por reacciones de degradación. Ej: Aspirina ( por acción de la humedad) Enalapril ( por acción de la luz) 14
15 Cuando se aislan sólidos a partir de procesos de extracción (por ejemplo a partir de materiales de origen vegetal) suelen contener impurezas. Los productos sólidos que se obtienen en una síntesis, suelen estar acompañados de pequeñas cantidades de reactivos y de subproductos. 15
16 El método más empleado para la eliminación de las impurezas de un sólido recibe el nombre de RECRISTALIZACIÓN Consiste en sucesivas cristalizaciones, empleando un disolvente puro, o una mezcla de disolventes, y se basa en la diferencia de solubilidades en frío y en caliente. 16
17 En qué consiste? En disolver el sólido a purificar en un solvente en caliente (obtención de una solución saturada en caliente) y dejarlo que cristalice al disminuir la temperatura (porque la solución estará sobresaturada y el exceso de sólido que no llegue a solubilizarse a esa menor temperatura se separará en forma de cristales, dejando fuera de la red cristalina a las impurezas). 17
18 Podemos esquematizarla así: se calienta se enfría se coloca el sólido con unos ml del solvente en el que la muestra es insoluble en frío se obtiene una solución saturada a la temperatura de ebullición del solvente al enfriarse la solución se sobresatura y el exceso de sólido se separa como cristales. Las impurezas quedan solubilizadas 18
19 Técnica general 1- Selección del solvente adecuado (puro o mezcla) 2- Disolución en caliente de la sustancia impura en el solvente elegido. 3- Si la solución es coloreada, se trata con carbón activado. 4- Si existe material insoluble o se agregó carbón activado, filtración de la solución en caliente. 5- Enfriamiento de la solución. 6- Separación de los cristales de las aguas madres por filtración al vacío en frío. Lavado de los cristales. 7- Secado del sólido. Posteriormente se controla la pureza (a través de la temperatura de fusión y/o cromatografía) 19
20 Condiciones del solvente para recristalizar: -no debe solubilizar al sólido en frío -debe solubilizarlo en caliente -al enfriarse, el sólido debe cristalizar -no debe reaccionar con el sólido a purificar -de ser posible no debe ser tóxico ni inflamable -para favorecer el secado, debe ser volátil -de ser posible, su punto de ebullición debe ser menor que el punto de fusión del sólido 20
21 Selección del solvente adecuado para recristalizar: Realizar las pruebas en tubos de ensayo con poca cantidad de sólido (punta de espátula) probando primero con el solvente en frío (el sólido no se debe solubilizar) y luego en caliente (se tiene que solubilizar todo el sólido para que el solvente sea elegido) y comprobando que los cristales reaparecen al enfriar. Solvente Solvente Solubilidad en frío Solubilidad en caliente Es solvente de elección? A Si Si NO B No No NO C No Si Si 21
22 Disolución del sólido en caliente (en solventes poco volátiles) Coloque el sólido en el erlenmeyer y agregue solvente hasta cubrirlo; agregue un trozo de piedra porosa; caliente hasta temperatura de ebullición del solvente. Si es necesario para que toda la muestra se solubilice en caliente, agregue más solvente. 22
23 Disolución del sólido en caliente Aparato para calentamiento a reflujo Si se emplea un solvente volátil se emplea la misma técnica con un aparato de calentamiento a reflujo, que consiste en balón con boca esmerilada adosado a un refrigerante, para que los vapores del solvente condensen y vuelvan al balón. 23
24 Se emplea la mínima cantidad de solvente necesaria para solubilizar todo el sólido en caliente para recuperar la mayor cantidad de muestra, pero se debe agregar una pequeña cantidad extra de solvente para evitar la precipitación del sólido durante la filtración en caliente. 24
25 Cómo se eliminan las impurezas insolubles en caliente? Se realiza una filtración por gravedad empleando embudo de vidrio con papel plegado, sobre un erlenmeyer. De ser posible el embudo se calienta para evitar la precipitación del sólido al disminuir la temperatura. Plegado del papel de filtro 25
26 Cuando todo el sólido cristalizó lentamente y se encuentra a temperatura ambiente, se filtra a presión reducida utilizando un embudo de porcelana y un kitasato. Los cristales se lavan con unos mililitros del solvente en el que es insoluble en frío y se vuelve a eliminar el solvente. 26
27 Para secar la muestra, pasar el sólido a un vidrio de reloj o placa de Petri (cuidar que quede bien repartido para favorecer el secado) y dejarlo cerca de una fuente de calor o colocar en estufa (si la muestra lo permite). Una vez seco cargar capilares y tomar la temperatura de fusión. 27
28 Objetivos del Trabajo Práctico: Purificar una muestra sólida por el método de recristalización. 28
29 Materiales necesarios: tubos de ensayo pinza de madera gradilla erlenmeyer placa calefactora capilares varilla de vidrio agarraderas doblenueces vaso de precipitados aro metálico embudo de vidrio papel de filtro embudo Hirsch kitasato vidrio de reloj aparato para medir punto de fusión 29
30 Informe Título del trabajo práctico Objetivos Datos bibliográficos de los compuestos Equipos empleados: esquemas Resultados obtenidos, y condiciones de trabajo: solvente/s empleado/s. rangos de temperaturas de fusión de la muestra cruda. Conclusiones: deben referirse claramente a los objetivos propuestos. Bibliografía empleada. 30
31 Recristalización en mezcla de solventes Cuándo se usa? Cuando no se cuenta con un solvente en el que la muestra sea insoluble en frío y soluble en caliente. Se usan combinados dos solventes: -en uno la muestra es soluble en frío y en caliente, -en el otro es insoluble en frío y en caliente. 31
32 Recristalización en mezcla de Condiciones: solventes -Los solventes deben ser totalmente miscibles. -Deben tener puntos de ebullición cercanos. Ejemplos: Etanol-agua Acetona-etanol 32
33 BIBLIOGRAFÍA RECOMENDADA MARTÍNEZ GRAU Y y CSÁKY, Técnicas Experimentales en Síntesis Orgánica. VOGEL, Practical Organic Chemistry GALAGOVSKY KURMAN, Fundamentos teórico-prácticos del Laboratorio. 33
CRISTALIZACIÓN: PURIFICACIÓN DEL ÁCIDO BENZOICO. Purificar un compuesto orgánico mediante cristalización y determinar su punto de fusión
 EXPERIMENTO 1 CRISTALIZACIÓN: PURIFICACIÓN DEL ÁCIDO BENZOICO Objetivo general Purificar un compuesto orgánico mediante cristalización y determinar su punto de fusión Objetivos específicos 1.- Determinar
EXPERIMENTO 1 CRISTALIZACIÓN: PURIFICACIÓN DEL ÁCIDO BENZOICO Objetivo general Purificar un compuesto orgánico mediante cristalización y determinar su punto de fusión Objetivos específicos 1.- Determinar
Aprender mediante clase expositiva las diferentes técnicas de separación de mezclas CONTENIDOS. Destilación Cristalización Filtración
 Aprender mediante clase expositiva las diferentes técnicas de separación de mezclas CONTENIDOS Destilación Cristalización Filtración La destilación es un método comúnmente utilizado para la purificación
Aprender mediante clase expositiva las diferentes técnicas de separación de mezclas CONTENIDOS Destilación Cristalización Filtración La destilación es un método comúnmente utilizado para la purificación
LABORATORIO DE QUÍMICA ORGANICA GUÍA No 3: SOLUBILIDAD Y RECRISTALIZACIÓN
 LABORATORIO DE QUÍMICA ORGANICA 502502 GUÍA No 3: SOLUBILIDAD Y RECRISTALIZACIÓN I. EL PROBLEMA Hacer uso del concepto de solubilidad en función de la temperatura para obtener un compuesto puro por recristalización
LABORATORIO DE QUÍMICA ORGANICA 502502 GUÍA No 3: SOLUBILIDAD Y RECRISTALIZACIÓN I. EL PROBLEMA Hacer uso del concepto de solubilidad en función de la temperatura para obtener un compuesto puro por recristalización
Universidad Iberoamericana
 Universidad Iberoamericana Ingeniería Química Laboratorio de Química General Grupo R Equipo 1 : Extracción y Cristalización por Francisco José Guerra Millán Prof. Celia Margarita del Valle Méndez I Extracción
Universidad Iberoamericana Ingeniería Química Laboratorio de Química General Grupo R Equipo 1 : Extracción y Cristalización por Francisco José Guerra Millán Prof. Celia Margarita del Valle Méndez I Extracción
LABORATORIO DE QUÍMICA FACULTAD DE FARMACIA CRISTALIZACIÓN.
 CRISTALIZACIÓN. Un compuesto orgánico cristalino está constituido por un empaquetamiento tridimensional de moléculas unidas principalmente por fuerzas de Van der Waals, que originan atracciones intermoleculares
CRISTALIZACIÓN. Un compuesto orgánico cristalino está constituido por un empaquetamiento tridimensional de moléculas unidas principalmente por fuerzas de Van der Waals, que originan atracciones intermoleculares
SEPARACIÓN DE LOS COMPONENTES DE UNA MEZCLA
 PRÁCTICA Nº 3 SEPARACIÓN DE LOS COMPONENTES DE UNA MEZCLA OBJETIVOS: Establecer los fundamentos teóricos de los proceso de separación. Separar los componentes de diversas muestras problema. I. FUNDAMENTOS
PRÁCTICA Nº 3 SEPARACIÓN DE LOS COMPONENTES DE UNA MEZCLA OBJETIVOS: Establecer los fundamentos teóricos de los proceso de separación. Separar los componentes de diversas muestras problema. I. FUNDAMENTOS
UNAM- Facultad de Química Prof. Mario Alfredo García Carrillo
 GUIA DE ESTUDIOS PARA EL PRIMER EXAMEN. 1. El punto de fusión del ácido benzoico puro y del 2-naftol puro son 122.5 C y 123 C respectivamente. Se tiene una muestra que no se sabe si es ácido benzoico o
GUIA DE ESTUDIOS PARA EL PRIMER EXAMEN. 1. El punto de fusión del ácido benzoico puro y del 2-naftol puro son 122.5 C y 123 C respectivamente. Se tiene una muestra que no se sabe si es ácido benzoico o
TÉCNICAS DE MUESTREO, ANÁLISIS E INTERPRETACIÓN. Ingeniería Ambiental
 TÉCNICAS DE MUESTREO, ANÁLISIS E INTERPRETACIÓN Ingeniería Ambiental Problema Elección del método analítico Toma de muestra Tratamiento de la muestra Proceso de medida Tratamiento de los datos Valoración
TÉCNICAS DE MUESTREO, ANÁLISIS E INTERPRETACIÓN Ingeniería Ambiental Problema Elección del método analítico Toma de muestra Tratamiento de la muestra Proceso de medida Tratamiento de los datos Valoración
11 Reacción del Haloformo sobre la Acetofenona. Obtención de Ácido Benzoico.
 PRÁCTICA 11 Reacción del Haloformo sobre la Acetofenona. Obtención de Ácido Benzoico. I. OBJETIVOS. a) Efectuar la síntesis del ácido benzoico a partir de la acetofenona por medio de la reacción del haloformo.
PRÁCTICA 11 Reacción del Haloformo sobre la Acetofenona. Obtención de Ácido Benzoico. I. OBJETIVOS. a) Efectuar la síntesis del ácido benzoico a partir de la acetofenona por medio de la reacción del haloformo.
PRUEBAS DE SOLUBILIDAD EN DISOLVENTES ORGÁNICOS: CRISTALIZACIÓN CON PAR DE DISOLVENTES
 PRUEBAS DE SOLUBILIDAD EN DISOLVENTES ORGÁNICOS: CRISTALIZACIÓN CON PAR DE DISOLVENTES OBJETIVOS a) Realizar pruebas de solubilidad a un compuesto sólido para encontrar el par de disolventes adecuados
PRUEBAS DE SOLUBILIDAD EN DISOLVENTES ORGÁNICOS: CRISTALIZACIÓN CON PAR DE DISOLVENTES OBJETIVOS a) Realizar pruebas de solubilidad a un compuesto sólido para encontrar el par de disolventes adecuados
PRÁCTICA 2. PURIFICACIÓN DEL CLORURO DE SODIO (NaCl), POR EFECTO DEL ION COMÚN
 11 PRÁCTICA 2 PURIFICACIÓN DEL CLORURO DE SODIO (NaCl), POR EFECTO DEL ION COMÚN PROPÓSITO GENERAL I. El propósito general de esta práctica es ampliar en el estudiante sus conocimientos acerca de algunos
11 PRÁCTICA 2 PURIFICACIÓN DEL CLORURO DE SODIO (NaCl), POR EFECTO DEL ION COMÚN PROPÓSITO GENERAL I. El propósito general de esta práctica es ampliar en el estudiante sus conocimientos acerca de algunos
Disoluciones. Química General II 2011
 Disoluciones Química General II 2011 Disolución Es una mezcla homogénea de dos o mas sustancias. Componentes: Soluto: Sustancia (s) presente (s) en menor cantidad en una disolución, son las sustancias
Disoluciones Química General II 2011 Disolución Es una mezcla homogénea de dos o mas sustancias. Componentes: Soluto: Sustancia (s) presente (s) en menor cantidad en una disolución, son las sustancias
PROBLEMA EXPERIMENTAL Nº 2
 PRBLEMA EXPERIMENTAL Nº 2 (30 puntos) SÍNTESIS DEL ÁCID VINILBENZIC Realización de la práctica Br H Ph 3 P= CH 2 Br + Ph 3 P P H CH 2 PPh 3 1. NaH, CH 2 2. HCl sal de fosfonio CH=CH 2 H ácido vinilbenzoico
PRBLEMA EXPERIMENTAL Nº 2 (30 puntos) SÍNTESIS DEL ÁCID VINILBENZIC Realización de la práctica Br H Ph 3 P= CH 2 Br + Ph 3 P P H CH 2 PPh 3 1. NaH, CH 2 2. HCl sal de fosfonio CH=CH 2 H ácido vinilbenzoico
1.5 Métodos de separación de mezclas Decantación, filtración, extracción, cristalización, destilación, cromatografía.
 1.5 Métodos de separación de mezclas Decantación, filtración, extracción, cristalización, destilación, cromatografía. 1 Para tomar apuntes MÉTODO DE SEPARACIÓN PROPIEDAD(ES) EN LAS QUE SE BASA MEZCLAS
1.5 Métodos de separación de mezclas Decantación, filtración, extracción, cristalización, destilación, cromatografía. 1 Para tomar apuntes MÉTODO DE SEPARACIÓN PROPIEDAD(ES) EN LAS QUE SE BASA MEZCLAS
Informe del trabajo práctico nº1
 Informe del trabajo práctico nº1 Profesora : Lic. Graciela Lic. Mariana Alumnas: Romina María Luján Graciela Mariana Curso: Química orgánica 63.14 turno 1 OBJETIVOS: Determinar el punto de fusión de una
Informe del trabajo práctico nº1 Profesora : Lic. Graciela Lic. Mariana Alumnas: Romina María Luján Graciela Mariana Curso: Química orgánica 63.14 turno 1 OBJETIVOS: Determinar el punto de fusión de una
MÉTODOS FÍSICOS DE SEPARACIÓN Y PURIFICACIÓN. 1. Destilación. 2. Extracción. 3. Sublimación. 4. Cristalización. 5. Cromatografía.
 MÉTODOS FÍSICOS DE SEPARACIÓN Y PURIFICACIÓN. 1. Destilación. 2. Extracción. 3. Sublimación. 4. Cristalización. 5. Cromatografía. 1. Destilación. La separación y purificación de líquidos por destilación
MÉTODOS FÍSICOS DE SEPARACIÓN Y PURIFICACIÓN. 1. Destilación. 2. Extracción. 3. Sublimación. 4. Cristalización. 5. Cromatografía. 1. Destilación. La separación y purificación de líquidos por destilación
EXPERIMENTO 6: SÍNTESIS, PURIFICACIÓN Y ANÁLISIS DEL ÁCIDO ACETIL SALICÍCLICO (aspirina).
 EXPERIMENT 6: SÍNTESIS, PURIFIAIÓN Y ANÁLISIS DEL ÁID AETIL SALIÍLI (aspirina). BJETIV: Sintetizar ácido acetilsalicílico a partir de la reacción de esterificación del grupo hidroxílico del ácido salicílico
EXPERIMENT 6: SÍNTESIS, PURIFIAIÓN Y ANÁLISIS DEL ÁID AETIL SALIÍLI (aspirina). BJETIV: Sintetizar ácido acetilsalicílico a partir de la reacción de esterificación del grupo hidroxílico del ácido salicílico
Se tiene programado ejecutarse la séptima y octava semana de clase.
 PRÁCTICA No 3. ENLACES QUÍMICOS INTRODUCCIÓN Los enlaces químicos son las fuerzas de atracción que mantienen los átomos unidos. Los enlaces químicos se producen cuando los núcleos y los electrones de átomos
PRÁCTICA No 3. ENLACES QUÍMICOS INTRODUCCIÓN Los enlaces químicos son las fuerzas de atracción que mantienen los átomos unidos. Los enlaces químicos se producen cuando los núcleos y los electrones de átomos
4A Reacciones de Sustitución Electrofílica Aromática. Obtención de p-yodoanilina.
 PRÁCTICA 4A Reacciones de Sustitución Electrofílica Aromática. Obtención de p-yodoanilina. I. OBJETIVOS. a) Conocer una reacción de sustitución electrofílica aromática. b) Efectuar una reacción que permita
PRÁCTICA 4A Reacciones de Sustitución Electrofílica Aromática. Obtención de p-yodoanilina. I. OBJETIVOS. a) Conocer una reacción de sustitución electrofílica aromática. b) Efectuar una reacción que permita
FACULTAD DE CIENCIAS NATURALES EXACTAS Y DE LA EDUCACIÓN DEPARTAMENTO DE QUÍMICA ÁREA QUÍMICA ORGANICA
 FACULTAD DE CIENCIAS NATURALES EXACTAS Y DE LA EDUCACIÓN DEPARTAMENTO DE QUÍMICA ÁREA QUÍMICA ORGANICA PRUEBAS DE CARACTERIZACION DE COMPUESTOS ORGANICOS Guía No: 01 Páginas: 1 a 7 1. INTRODUCCIÓN La materia
FACULTAD DE CIENCIAS NATURALES EXACTAS Y DE LA EDUCACIÓN DEPARTAMENTO DE QUÍMICA ÁREA QUÍMICA ORGANICA PRUEBAS DE CARACTERIZACION DE COMPUESTOS ORGANICOS Guía No: 01 Páginas: 1 a 7 1. INTRODUCCIÓN La materia
PRÁCTICA REACCION DEL HALOFORMO SOBRE LA ACETOFENONA OBTENCIÓN DEL ÁCIDO BENZOICO I. OBJETIVOS REACCIÓN
 PRÁCTICA REACCION DEL HALOFORMO SOBRE LA ACETOFENONA OBTENCIÓN DEL ÁCIDO BENZOICO 12 I. OBJETIVOS b) Efectuar la síntesis del ácido benzoico a partir de la acetofenona por medio de la reacción del haloformo.
PRÁCTICA REACCION DEL HALOFORMO SOBRE LA ACETOFENONA OBTENCIÓN DEL ÁCIDO BENZOICO 12 I. OBJETIVOS b) Efectuar la síntesis del ácido benzoico a partir de la acetofenona por medio de la reacción del haloformo.
DESTILACIÓN. Curso 2016
 DESTILACIÓN Curso 2016 Farmacéutica Ana María REVERDITO Farmacéutica y Bioquímica Amalia FIGUEROA Bioquímico Marcelo AGMAN Doctora María Gabriela LORENZO Cátedra: QUÍMICA ORGÁNICA I 1 CONTENIDOS Fundamentos
DESTILACIÓN Curso 2016 Farmacéutica Ana María REVERDITO Farmacéutica y Bioquímica Amalia FIGUEROA Bioquímico Marcelo AGMAN Doctora María Gabriela LORENZO Cátedra: QUÍMICA ORGÁNICA I 1 CONTENIDOS Fundamentos
ANÁLISIS DE PROPIEDADES FÍSICAS DE SUSTANCIAS ORGÁNICAS
 OBJETIVOS PRÁCTICA #1 ANÁLISIS DE PROPIEDADES FÍSICAS DE SUSTANCIAS ORGÁNICAS Comparar el comportamiento al calor de sustancias alifáticas, aromáticas y iónicas. Comparar la solubilidad de sustancias polares,
OBJETIVOS PRÁCTICA #1 ANÁLISIS DE PROPIEDADES FÍSICAS DE SUSTANCIAS ORGÁNICAS Comparar el comportamiento al calor de sustancias alifáticas, aromáticas y iónicas. Comparar la solubilidad de sustancias polares,
Práctica nº 1. Reconocimiento del material. Objetivo: conocer todo el material que puede haber en un laboratorio.
 Práctica nº 1. Reconocimiento del material. Objetivo: conocer todo el material que puede haber en un laboratorio. Matraz aforado: tiene forma de pera con fondo plano o curvo (finalidad calentar el contenido),
Práctica nº 1. Reconocimiento del material. Objetivo: conocer todo el material que puede haber en un laboratorio. Matraz aforado: tiene forma de pera con fondo plano o curvo (finalidad calentar el contenido),
CONOCIMIENTO DEL EQUIPO DE LABORATORIO Y USO DEL MECHERO ESTUDIO DE LA LLAMA. OBJETIVOS.
 EXPERIMENTO I CONOCIMIENTO DEL EQUIPO DE LABORATORIO Y USO DEL MECHERO ESTUDIO DE LA LLAMA. OBJETIVOS. a) Identificar los diferentes equipos y materiales utilizados en el laboratorio de química. b) Utilizar
EXPERIMENTO I CONOCIMIENTO DEL EQUIPO DE LABORATORIO Y USO DEL MECHERO ESTUDIO DE LA LLAMA. OBJETIVOS. a) Identificar los diferentes equipos y materiales utilizados en el laboratorio de química. b) Utilizar
9 Condensación de Claisen-Schmidt. Obtención de Dibenzalacetona.
 PRÁCTICA 9 Condensación de Claisen-Schmidt. Obtención de Dibenzalacetona. I. OBJETIVOS. a) Efectuar una condensación aldólica cruzada dirigida. b) Obtener un producto de uso comercial. REACCIÓN: H O O
PRÁCTICA 9 Condensación de Claisen-Schmidt. Obtención de Dibenzalacetona. I. OBJETIVOS. a) Efectuar una condensación aldólica cruzada dirigida. b) Obtener un producto de uso comercial. REACCIÓN: H O O
Material de uso frecuente en el laboratorio de química. Figura Nombre Uso / Características. Crisol. Espátula de porcelana. Capsula de porcelana
 Material de uso frecuente en el laboratorio de química. En un Laboratorio de Química se utiliza una amplia variedad de instrumentos o herramientas que, en su conjunto, se denominan material de laboratorio.
Material de uso frecuente en el laboratorio de química. En un Laboratorio de Química se utiliza una amplia variedad de instrumentos o herramientas que, en su conjunto, se denominan material de laboratorio.
Reacciones de Sustitución Electrofílica Aromática. Obtención de p-yodoanilina
 PRÁCTICA 2 Reacciones de Sustitución Electrofílica Aromática. Obtención de p-yodoanilina I. OBJETIVOS Conocer una reacción de sustitución electrofílica aromática. Efectuar una reacción que permita obtener
PRÁCTICA 2 Reacciones de Sustitución Electrofílica Aromática. Obtención de p-yodoanilina I. OBJETIVOS Conocer una reacción de sustitución electrofílica aromática. Efectuar una reacción que permita obtener
3016 Oxidación de ácido ricinoleico (de aceite de castor) con KMnO 4 para obtener ácido azelaico
 6 Oxidación de ácido ricinoleico (de aceite de castor) con KMnO 4 para obtener ácido azelaico CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.) C H 6 O 4 (.) Clasificación
6 Oxidación de ácido ricinoleico (de aceite de castor) con KMnO 4 para obtener ácido azelaico CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.) C H 6 O 4 (.) Clasificación
PRÁCTICA 4 SOLUBILIDAD Y CRISTALIZACIÓN
 PRÁCTICA 4 SOLUBILIDAD Y CRISTALIZACIÓN OBJETIVOS Estudiar cómo varía la solubilidad de un compuesto químico con la temperatura y, a partir de los datos obtenidos, representar la curva de solubilidad de
PRÁCTICA 4 SOLUBILIDAD Y CRISTALIZACIÓN OBJETIVOS Estudiar cómo varía la solubilidad de un compuesto químico con la temperatura y, a partir de los datos obtenidos, representar la curva de solubilidad de
7 Reducción del Grupo Nitro. Obtención de m-nitroanilina a partir de m-dinitrobenceno.
 PRÁCTICA 7 Reducción del Grupo Nitro. Obtención de m-nitroanilina a partir de m-dinitrobenceno. I. OBJETIVOS. a) Efectuar una reducción selectiva de un grupo nitro del m-dinitrobenceno, para obtener la
PRÁCTICA 7 Reducción del Grupo Nitro. Obtención de m-nitroanilina a partir de m-dinitrobenceno. I. OBJETIVOS. a) Efectuar una reducción selectiva de un grupo nitro del m-dinitrobenceno, para obtener la
TÉCNICAS EXPERIMENTALES EN SÍNTESIS ORGÁNICA
 TÉCNICAS EXPERIMENTALES EN SÍNTESIS ORGÁNICA PROYECTO EDITORIAL BIBLIOTECA DE QUÍMICAS Director: Carlos Seoane Prado Catedrático de Química Orgánica Universidad Complutense de Madrid COLECCIÓN: Química
TÉCNICAS EXPERIMENTALES EN SÍNTESIS ORGÁNICA PROYECTO EDITORIAL BIBLIOTECA DE QUÍMICAS Director: Carlos Seoane Prado Catedrático de Química Orgánica Universidad Complutense de Madrid COLECCIÓN: Química
Reglamento. 1. Dentro del laboratorio es obligatorio el uso de la bata de algodón, perfectamente cerrada.
 Reglamento 1. Dentro del laboratorio es obligatorio el uso de la bata de algodón, perfectamente cerrada. 2. Todos los alumnos, durante la sesión de laboratorio, deberán usar zapato cerrado con un tacón
Reglamento 1. Dentro del laboratorio es obligatorio el uso de la bata de algodón, perfectamente cerrada. 2. Todos los alumnos, durante la sesión de laboratorio, deberán usar zapato cerrado con un tacón
12 Reacción de Schotten-Baumann. Obtención de Benzoato de Fenilo.
 PRÁCTICA 12 Reacción de Schotten-Baumann. Obtención de Benzoato de Fenilo. I. OBJETIVO. Efectuar una esterificación del fenol como ejemplo de la reacción de Schotten-Baumann. REACCIÓN: OH O O + Cl NaOH
PRÁCTICA 12 Reacción de Schotten-Baumann. Obtención de Benzoato de Fenilo. I. OBJETIVO. Efectuar una esterificación del fenol como ejemplo de la reacción de Schotten-Baumann. REACCIÓN: OH O O + Cl NaOH
DIFERENCIA ENTRE COMPUESTOS ORGÁNICOS E INORGÁNICOS
 DIFERENCIA ENTRE COMPUESTOS ORGÁNICOS E INORGÁNICOS 1. Objetivos Demostrar experimentalmente algunas de las diferencias entre los compuestos orgánicos e inorgánicos. 2. Fundamento teórico Entre las diferencias
DIFERENCIA ENTRE COMPUESTOS ORGÁNICOS E INORGÁNICOS 1. Objetivos Demostrar experimentalmente algunas de las diferencias entre los compuestos orgánicos e inorgánicos. 2. Fundamento teórico Entre las diferencias
COLEGIO DE BACHILLERES DEL ESTADO DE TLAXCALA DIRECCIÓN ACADÉMICA CAPACITACIÓN. TECNOLOGÍA DE LABORATORIO I.
 r COLEGIO DE BACHILLERES DEL ESTADO DE TLAXCALA DIRECCIÓN ACADÉMICA DEPARTAMENTO DE BIBLIOTECAS Y LABORATORIOS. MANUAL DE ACTIVIDADES EXPERIMENTALES DE: CAPACITACIÓN. TECNOLOGÍA DE LABORATORIO I. 1. METODOS
r COLEGIO DE BACHILLERES DEL ESTADO DE TLAXCALA DIRECCIÓN ACADÉMICA DEPARTAMENTO DE BIBLIOTECAS Y LABORATORIOS. MANUAL DE ACTIVIDADES EXPERIMENTALES DE: CAPACITACIÓN. TECNOLOGÍA DE LABORATORIO I. 1. METODOS
TEMA 5: LABORATORIO PIPETA GRADUADA ÉMBOLO PARA PIPETAS PERILLA DE GOMA PIPETA AFORADA MATRAZ DE FONDO PLANO MATRAZ DE FONDO REDONDO MATRAZ AFORADO
 TEMA 5: LABORATORIO PIPETA GRADUADA PIPETA AFORADA ÉMBOLO PARA PIPETAS PERILLA DE GOMA BURETA DE FONDO REDONDO DE FONDO PLANO AFORADO DE DESTILACIÓN ERLENMEYER PROBETA FRASCO TRANSPARENTE FRASCOS TOPACIO
TEMA 5: LABORATORIO PIPETA GRADUADA PIPETA AFORADA ÉMBOLO PARA PIPETAS PERILLA DE GOMA BURETA DE FONDO REDONDO DE FONDO PLANO AFORADO DE DESTILACIÓN ERLENMEYER PROBETA FRASCO TRANSPARENTE FRASCOS TOPACIO
Técnicas de Cristalización 1/8
 Técnicas de Cristalización 1/8 Técnicas de Cristalización. Tipos de cristalización. Cristalización por evaporación del disolvente, por adición de otro disolvente, por variación de la temperatura y por
Técnicas de Cristalización 1/8 Técnicas de Cristalización. Tipos de cristalización. Cristalización por evaporación del disolvente, por adición de otro disolvente, por variación de la temperatura y por
Informe del trabajo práctico nº6
 Informe del trabajo práctico nº6 Profesora : Lic. Graciela. Lic. Mariana. Alumnas: Romina. María Luján. Graciela. Mariana. Curso: Química orgánica 63.14 turno 1 OBJETIVOS Obtención de ácido pícrico y determinación
Informe del trabajo práctico nº6 Profesora : Lic. Graciela. Lic. Mariana. Alumnas: Romina. María Luján. Graciela. Mariana. Curso: Química orgánica 63.14 turno 1 OBJETIVOS Obtención de ácido pícrico y determinación
 TRABAJO PRÁCTICO N 2 CAMBIOS DE ESTADO SÓLIDO LÍQUIDO GASEOSO Manteniendo constante la presión, a baja temperatura los cuerpos se presentan en forma sólida tal que los átomos se encuentran entrelazados
TRABAJO PRÁCTICO N 2 CAMBIOS DE ESTADO SÓLIDO LÍQUIDO GASEOSO Manteniendo constante la presión, a baja temperatura los cuerpos se presentan en forma sólida tal que los átomos se encuentran entrelazados
CROMATOGRAFIA. Dra. María del Rosario Torviso Química Orgánica I FFyB-UBA
 CROMATOGRAFIA Dra. María del Rosario Torviso Química Orgánica I FFyB-UBA 1 CROMATOGRAFIA Se basa en el principio general de distribución de un compuesto entre dos fases, una fija o estacionaria (FE) y
CROMATOGRAFIA Dra. María del Rosario Torviso Química Orgánica I FFyB-UBA 1 CROMATOGRAFIA Se basa en el principio general de distribución de un compuesto entre dos fases, una fija o estacionaria (FE) y
Informe del trabajo práctico nº9
 Informe del trabajo práctico nº9 Profesora : Lic. Graciela. Lic. Mariana. Alumnas: Romina. María Luján. Graciela. Mariana. Curso: Química orgánica 63.14 turno 1 OBJETIVOS Sintetizar y purificar por recristalizacion
Informe del trabajo práctico nº9 Profesora : Lic. Graciela. Lic. Mariana. Alumnas: Romina. María Luján. Graciela. Mariana. Curso: Química orgánica 63.14 turno 1 OBJETIVOS Sintetizar y purificar por recristalizacion
OBTENCIÓN DE INDICADORES DEL TIPO DE LAS FTALEÍNAS FENOLFTALEÍNA Y FLUORESCEINA
 EXPERIMENT No. 8 BTENCIÓN DE INDICADRES DEL TIP DE LAS FTALEÍNAS FENLFTALEÍNA Y FLURESCEINA BJETIVS a) El alumno aprenda los métodos de síntesis de colorantes del tipo de las ftaleínas, por condensación
EXPERIMENT No. 8 BTENCIÓN DE INDICADRES DEL TIP DE LAS FTALEÍNAS FENLFTALEÍNA Y FLURESCEINA BJETIVS a) El alumno aprenda los métodos de síntesis de colorantes del tipo de las ftaleínas, por condensación
Contextualización Aprendizaje básico del trabajo en un laboratorio químico.
 OPERACIONES BÁSICAS DE LABORATORIO I Grado en Química: 1º Curso, 1º cuatrimestre FICHA TÉCNICA DE LA ASIGNATURA Situación / Sentido de la asignatura Contextualización Aprendizaje básico del trabajo en
OPERACIONES BÁSICAS DE LABORATORIO I Grado en Química: 1º Curso, 1º cuatrimestre FICHA TÉCNICA DE LA ASIGNATURA Situación / Sentido de la asignatura Contextualización Aprendizaje básico del trabajo en
EXPERIMENTO No. 6, 7
 EXPERIMENTO No. 6, 7 SÍNTESIS DE SULFANILAMIDA OBJETIVOS a) Efectuar la síntesis de intermediarios necesarios en la industria farmacéutica. b) Adiestrarse en el manejo de reactivos irritantes como el ácido
EXPERIMENTO No. 6, 7 SÍNTESIS DE SULFANILAMIDA OBJETIVOS a) Efectuar la síntesis de intermediarios necesarios en la industria farmacéutica. b) Adiestrarse en el manejo de reactivos irritantes como el ácido
5007 Reacción de anhidrido ftálico con resorcina para obtener fluoresceina
 57 Reacción de anhidrido ftálico con resorcina para obtener fluoresceina CH H H + 2 + 2 H 2 H C 8 H 4 3 C 6 H 6 2 C 2 H 12 5 (148.1) (11.1) (332.3) Clasificación Tipos de reacción y clases de productos
57 Reacción de anhidrido ftálico con resorcina para obtener fluoresceina CH H H + 2 + 2 H 2 H C 8 H 4 3 C 6 H 6 2 C 2 H 12 5 (148.1) (11.1) (332.3) Clasificación Tipos de reacción y clases de productos
Cristales. Empaquetamiento de Esferas
 Cristales Un cristal es una disposición simétrica de átomos, iones o moléculas dispuestos en un modelo tridimensional repetitivo. Sí los centros de las unidades materiales se reemplazan por puntos, el
Cristales Un cristal es una disposición simétrica de átomos, iones o moléculas dispuestos en un modelo tridimensional repetitivo. Sí los centros de las unidades materiales se reemplazan por puntos, el
4008 Síntesis del hidrocloruro de 2-dimetilaminometilciclohexanona
 4008 Síntesis del hidrocloruro de 2-dimetilaminometilciclohexanona + + H 2 N(CH 3 H H EtH, H NH(CH 3 C 6 H 10 CH 2 C 2 H 8 N C 9 H 18 N (98.2) (30.0) (81.6) (191.7) asificación Tipos de reacción y clases
4008 Síntesis del hidrocloruro de 2-dimetilaminometilciclohexanona + + H 2 N(CH 3 H H EtH, H NH(CH 3 C 6 H 10 CH 2 C 2 H 8 N C 9 H 18 N (98.2) (30.0) (81.6) (191.7) asificación Tipos de reacción y clases
Métodos de separación de sistemas materiales sencillos
 Métodos de separación de sistemas materiales sencillos SISTEMAS MATERIALES Mezclas Separación física Sustancias Puras no Son uniformes? si si Pueden descomponerse por reacciones químicas? no Mezclas heterogéneas
Métodos de separación de sistemas materiales sencillos SISTEMAS MATERIALES Mezclas Separación física Sustancias Puras no Son uniformes? si si Pueden descomponerse por reacciones químicas? no Mezclas heterogéneas
PRÁCTICAS TÉCNICAS DE SEPARACIÓN Y PREPARACIÓN DE DISOLUCIONES FÍSICA Y QUÍMICA 2º
 PRÁCTICAS TÉCNICAS DE SEPARACIÓN Y PREPARACIÓN DE DISOLUCIONES FÍSICA Y QUÍMICA 2º CURSO: NOMBRE: COMPAÑEROS QUE FORMAN TU GRUPO: 1 FILTRACIÓN DE AGUA Y ARENA La filtración es la separación de las partículas
PRÁCTICAS TÉCNICAS DE SEPARACIÓN Y PREPARACIÓN DE DISOLUCIONES FÍSICA Y QUÍMICA 2º CURSO: NOMBRE: COMPAÑEROS QUE FORMAN TU GRUPO: 1 FILTRACIÓN DE AGUA Y ARENA La filtración es la separación de las partículas
Departamento Ciencias. Física y Química MATERIA. se clasifica en. SUSTANCIAS PURAS pueden ser. por métodos. físicos originan. Compuestos.
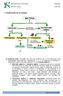 1. Clasificación de la materia MATERIA se clasifica en MEZCLAS pueden ser por métodos físicos originan SUSTANCIAS PURAS pueden ser Heterogéneas Homogéneas Compuestos como las Disoluciones formados por
1. Clasificación de la materia MATERIA se clasifica en MEZCLAS pueden ser por métodos físicos originan SUSTANCIAS PURAS pueden ser Heterogéneas Homogéneas Compuestos como las Disoluciones formados por
En términos de fuerzas intermoleculares, cuándo es posible disolver una sustancia en otra?
 Práctica 5 Fuerzas intermoleculares y solubilidad Pregunta a responder al final de la sesión: En términos de fuerzas intermoleculares, cuándo es posible disolver una sustancia en otra? Introducción Los
Práctica 5 Fuerzas intermoleculares y solubilidad Pregunta a responder al final de la sesión: En términos de fuerzas intermoleculares, cuándo es posible disolver una sustancia en otra? Introducción Los
SÍNTESIS EN MICROESCALA DE ÁCIDO ACETILSALICÍLICO
 Páina: 1/4 DEPARTAMENT ESTRELLA CAMPS PRÁCTIC 5: SÍNTESIS EN MICRESCALA DE ÁCID ACETILSALICÍLIC Bibliorafía: Química, La Ciencia Central, T.L. Brown, H.E.LeMay, Jr., B.Bursten; Ed. Prentice-Hall, Hispanoamérica,
Páina: 1/4 DEPARTAMENT ESTRELLA CAMPS PRÁCTIC 5: SÍNTESIS EN MICRESCALA DE ÁCID ACETILSALICÍLIC Bibliorafía: Química, La Ciencia Central, T.L. Brown, H.E.LeMay, Jr., B.Bursten; Ed. Prentice-Hall, Hispanoamérica,
LA DIVERSIDAD DE LA MATERIA
 Tema 3 LA DIVERSIDAD DE LA MATERIA 1 Clasificación de la materia Un sistema material es una porción de materia que se separa para realizar un estudio experimental. Es aquella parte del universo que se
Tema 3 LA DIVERSIDAD DE LA MATERIA 1 Clasificación de la materia Un sistema material es una porción de materia que se separa para realizar un estudio experimental. Es aquella parte del universo que se
 TRABAJO PRÁCTICO Nº 3 SISTEMAS MATERIALES - Materia Es todo lo que posee masa, y ocupa un lugar en el espacio. - Sistema Material Porción de materia que se aisla para su estudio. - Sustancia Pura - Sistema
TRABAJO PRÁCTICO Nº 3 SISTEMAS MATERIALES - Materia Es todo lo que posee masa, y ocupa un lugar en el espacio. - Sistema Material Porción de materia que se aisla para su estudio. - Sustancia Pura - Sistema
Nombres de los integrantes: Práctica 6 Propiedades Físicas y Enlace Químico en Sólidos
 1 Nombres de los integrantes: Universidad Nacional Autónoma de México Facultad de Química Laboratorio de Química General I Grupo Equipo Práctica 6 Propiedades Físicas y Enlace Químico en Sólidos Problema
1 Nombres de los integrantes: Universidad Nacional Autónoma de México Facultad de Química Laboratorio de Química General I Grupo Equipo Práctica 6 Propiedades Físicas y Enlace Químico en Sólidos Problema
PRÁCTICA AROMÁTICA: NITRACIÓN DE CLOROBENCENO I. OBJETIVOS II. REACCIÓN
 PRÁCTICA SUSTITUCIÓN AROMÁTICA: 3 ELECTROFÍLICA NITRACIÓN DE CLOROBENCENO I. OBJETIVOS II. REACCIÓN a) Conocer una reacción de sustitución electrofílica aromática y aplicar los conceptos de la sustitución
PRÁCTICA SUSTITUCIÓN AROMÁTICA: 3 ELECTROFÍLICA NITRACIÓN DE CLOROBENCENO I. OBJETIVOS II. REACCIÓN a) Conocer una reacción de sustitución electrofílica aromática y aplicar los conceptos de la sustitución
PRÁCTICA 1 SUSTITUCIÓN ELECTROFÍLICA AROMÁTICA: NITRACIÓN DE BENCENO
 FACULTAD DE QUÍMICA DPTO. DE QUÍMICA ORGÁNICA LABORATORIO DE QUÍMICA ORGÁNICA II (1413) PRÁCTICA 1 SUSTITUCIÓN ELECTROFÍLICA AROMÁTICA: NITRACIÓN DE BENCENO OBJETIVO. Conocer una reacción de sustitución
FACULTAD DE QUÍMICA DPTO. DE QUÍMICA ORGÁNICA LABORATORIO DE QUÍMICA ORGÁNICA II (1413) PRÁCTICA 1 SUSTITUCIÓN ELECTROFÍLICA AROMÁTICA: NITRACIÓN DE BENCENO OBJETIVO. Conocer una reacción de sustitución
3011 Síntesis de ácido eritro-9,10-dihidroxiesteárico a partir de ácido oleico
 311 Síntesis de ácido eritro-9,1-dihidroxiesteárico a partir de ácido oleico COOH KMnO 4 /NaOH HO HO COOH C 18 H 34 O 2 (282.5) KMnO 4 (158.) NaOH (4.) C 18 H 36 O 4 (316.5) Literatura A. Lapworth und
311 Síntesis de ácido eritro-9,1-dihidroxiesteárico a partir de ácido oleico COOH KMnO 4 /NaOH HO HO COOH C 18 H 34 O 2 (282.5) KMnO 4 (158.) NaOH (4.) C 18 H 36 O 4 (316.5) Literatura A. Lapworth und
PRÁCTICA # 01 PREPARACIÓN DE DISOLUCIONES
 REPÚBLICA BOLIVARIANA DE VENEZUELA MINISTERIO DEL PODER POPULAR PARA LA DEFENSA AVIACIÓN MILITAR VENEZOLANA U.E.A.M LIBERTADOR ASIGNATURA: QUÍMICA PROF(A): ANGÉLICA RODRÍGUEZ MARBELIS MELENDEZ CURSO: 4to
REPÚBLICA BOLIVARIANA DE VENEZUELA MINISTERIO DEL PODER POPULAR PARA LA DEFENSA AVIACIÓN MILITAR VENEZOLANA U.E.A.M LIBERTADOR ASIGNATURA: QUÍMICA PROF(A): ANGÉLICA RODRÍGUEZ MARBELIS MELENDEZ CURSO: 4to
OBTENCIÓN DE ACETATO DE ETILO POR UNA METODOLOGÍA CONVENCIONAL
 ISSN 2007-957 OBTENCIÓN DE ACETATO DE ETILO POR UNA METODOLOGÍA CONVENCIONAL Jorge Rivera Elorza Escuela Superior de Ingeniería Química e Industrias Extractivas, IPN riej23204@yahoo.com.mx Ivonne Yesenia
ISSN 2007-957 OBTENCIÓN DE ACETATO DE ETILO POR UNA METODOLOGÍA CONVENCIONAL Jorge Rivera Elorza Escuela Superior de Ingeniería Química e Industrias Extractivas, IPN riej23204@yahoo.com.mx Ivonne Yesenia
PRUEBAS DE SOLUBILIDAD EN DISOLVENTES ORGÁNICOS Y CRISTALIZACIÓN SIMPLE Y CON CARBÓN ACTIVADO
 PRUEBAS DE SOLUBILIDAD EN DISOLVENTES ORGÁNICOS Y CRISTALIZACIÓN SIMPLE Y CON CARBÓN ACTIVADO I. OBJETIVOS. Realizar pruebas de solubilidad para encontrar un disolvente ideal para efectuar una cristalización.
PRUEBAS DE SOLUBILIDAD EN DISOLVENTES ORGÁNICOS Y CRISTALIZACIÓN SIMPLE Y CON CARBÓN ACTIVADO I. OBJETIVOS. Realizar pruebas de solubilidad para encontrar un disolvente ideal para efectuar una cristalización.
CRISTALIZACION SIMPLE Y CON CARBON ACTIVADO
 PRACTICA VI CRISTALIZACION SIMPLE Y CON CARBON ACTIVADO I. OBJETIVO a) Utilizar la técnica de cristalización, como una de las más importantes técnicas usadas para la purificación de compuestos sólidos.
PRACTICA VI CRISTALIZACION SIMPLE Y CON CARBON ACTIVADO I. OBJETIVO a) Utilizar la técnica de cristalización, como una de las más importantes técnicas usadas para la purificación de compuestos sólidos.
Materia. Mezclas Son aquellas que están formados por 2 o más sustancias.
 Qué es la materia? Materia Sustancias Puras Son aquellas que tienen una composición y propiedades DEFINIDAS. Mezclas Son aquellas que están formados por 2 o más sustancias. Elementos No se pueden separar
Qué es la materia? Materia Sustancias Puras Son aquellas que tienen una composición y propiedades DEFINIDAS. Mezclas Son aquellas que están formados por 2 o más sustancias. Elementos No se pueden separar
EXPERIMENTO No. 7 OBJETIVOS ANTECEDENTES
 EXPERIMENTO No. 7 a) SÍNTESIS DE INDOLES DE FISCHER: OBTENCIÓN DE 1,2,3,4-TETRAHIDROCARBAZOL b) SÍNTESIS DE ÍNDIGO*: 2-(1,3-Dihidro-3-oxo-2H-indol-2- ilid-eno)-1,2-dihidro-3h-indol-3-ona OBJETIVOS a) Preparar
EXPERIMENTO No. 7 a) SÍNTESIS DE INDOLES DE FISCHER: OBTENCIÓN DE 1,2,3,4-TETRAHIDROCARBAZOL b) SÍNTESIS DE ÍNDIGO*: 2-(1,3-Dihidro-3-oxo-2H-indol-2- ilid-eno)-1,2-dihidro-3h-indol-3-ona OBJETIVOS a) Preparar
Práctica 4 AISLAMIENTO DE CAFEINA A PARTIR DEL TÉ Y/O COCA COLA
 Práctica 4 AISLAMIENTO DE CAFEINA A PARTIR DEL TÉ Y/O COCA COLA OBJETIVO: 1. El alumno aislará la cafeína a partir del té y/o Coca Cola usando una disolución de carbonato de sodio, neutralización y extracción
Práctica 4 AISLAMIENTO DE CAFEINA A PARTIR DEL TÉ Y/O COCA COLA OBJETIVO: 1. El alumno aislará la cafeína a partir del té y/o Coca Cola usando una disolución de carbonato de sodio, neutralización y extracción
OXIDACION DE n-butanol A. a) Ejemplificar un método para obtener aldehídos alifáticos mediante la oxidación de alcoholes.
 PRÁCTICA OXIDACION DE n-butanol A n-butiraldehído I. OBJETIVOS a) Ejemplificar un método para obtener aldehídos alifáticos mediante la oxidación de alcoholes. b) Formar un derivado sencillo del aldehído
PRÁCTICA OXIDACION DE n-butanol A n-butiraldehído I. OBJETIVOS a) Ejemplificar un método para obtener aldehídos alifáticos mediante la oxidación de alcoholes. b) Formar un derivado sencillo del aldehído
ACIDOS CARBOXILICOS Y ESTERES. ELABORADO POR: Lic. Raúl Hernández Mazariegos
 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS, CUM UNIDAD DIDÁCTICA QUÍMICA, PRIMER AÑO PRACTICAS DE LABORATORIO QUIMICA 2010 ACIDOS CARBOXILICOS Y ESTERES ELABORADO POR: Lic. Raúl
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA FACULTAD DE CIENCIAS MÉDICAS, CUM UNIDAD DIDÁCTICA QUÍMICA, PRIMER AÑO PRACTICAS DE LABORATORIO QUIMICA 2010 ACIDOS CARBOXILICOS Y ESTERES ELABORADO POR: Lic. Raúl
Propiedades Físicas y Enlace Químico en Sólidos
 Propiedades Físicas y Enlace Químico en Sólidos Las propiedades físicas de sólidos dependen de los enlaces químicos que mantienen unidas a las entidades que los forman. La cantidad, intensidad y naturaleza
Propiedades Físicas y Enlace Químico en Sólidos Las propiedades físicas de sólidos dependen de los enlaces químicos que mantienen unidas a las entidades que los forman. La cantidad, intensidad y naturaleza
OBTENCION DE LA meta-nitroanilina
 PRÁCTICA OBTENCION DE LA meta-nitroanilina I. OBJETIVOS: 1. Efectuar una reducción selectiva de un grupo nitro del metadinitrobenceno, para obtener la meta-nitroanilina. 2. Realizar la separación y la
PRÁCTICA OBTENCION DE LA meta-nitroanilina I. OBJETIVOS: 1. Efectuar una reducción selectiva de un grupo nitro del metadinitrobenceno, para obtener la meta-nitroanilina. 2. Realizar la separación y la
Tarea Previa 1. Qué es un enlace químico? 2. Investiga las características de los siguientes tipos de enlace químico: Iónico. Covalente molecular
 Equipo: Nombre: Nombre: Nombre: Práctica 6: Propiedades Físicas y Enlace Químico en Sólidos Problema 1 Cómo son los puntos de fusión y la solubilidad de sustancias cuya estructura se mantiene por diferentes
Equipo: Nombre: Nombre: Nombre: Práctica 6: Propiedades Físicas y Enlace Químico en Sólidos Problema 1 Cómo son los puntos de fusión y la solubilidad de sustancias cuya estructura se mantiene por diferentes
CLASIFICACIÓN DE LA MATERIA
 1. Clasificación de la materia por su aspecto CLASIFICACIÓN DE LA MATERIA La materia homogénea es la que presenta un aspecto uniforme, en la cual no se pueden distinguir a simple vista sus componentes.
1. Clasificación de la materia por su aspecto CLASIFICACIÓN DE LA MATERIA La materia homogénea es la que presenta un aspecto uniforme, en la cual no se pueden distinguir a simple vista sus componentes.
filosofiatotal.blogspot.com depcienat1.blogspot.com
 www.alambiques.info filosofiatotal.blogspot.com depcienat1.blogspot.com www.panreac.es Ahhhh! Un vaso de limonada helada es muy refrescante en un día caluroso. La limonada es una combinación de jugo de
www.alambiques.info filosofiatotal.blogspot.com depcienat1.blogspot.com www.panreac.es Ahhhh! Un vaso de limonada helada es muy refrescante en un día caluroso. La limonada es una combinación de jugo de
SAPONIFICACIÓN: SÍNTESIS DE JABÓN
 SAPONIFICACIÓN: SÍNTESIS DE JABÓN Objetivos: 1. Preparar jabón a partir de aceite vegetal 2. Observar las propiedades del jabón al someterlo a distintas pruebas. Introducción: Las propiedades de las grasas
SAPONIFICACIÓN: SÍNTESIS DE JABÓN Objetivos: 1. Preparar jabón a partir de aceite vegetal 2. Observar las propiedades del jabón al someterlo a distintas pruebas. Introducción: Las propiedades de las grasas
CORPORACION MUNICIPAL DE DESARROLLO SOCIAL LICEO INDUSTRIAL EULOGIO GORDO MONEO ANTOFAGASTA FONO FAX:
 CORPORACION MUNICIPAL DE DESARROLLO SOCIAL LICEO INDUSTRIAL EULOGIO GORDO MONEO ANTOFAGASTA FONO FAX:55-2231189 WWW.LICEOINDUSTRIALEGM.CL GUÍA DE APRENDIZAJE Profesor Asignatura Objetivo de Aprendizaje
CORPORACION MUNICIPAL DE DESARROLLO SOCIAL LICEO INDUSTRIAL EULOGIO GORDO MONEO ANTOFAGASTA FONO FAX:55-2231189 WWW.LICEOINDUSTRIALEGM.CL GUÍA DE APRENDIZAJE Profesor Asignatura Objetivo de Aprendizaje
Revista de Química. Vol. VII. Nº 2. Diciembre de 1993 OBTENCION DEL OXIDO DE MAGNESIO A PARTIR DE LA DOLOMITA RESUMEN
 Revista de Química. Vol. VII. Nº 2. Diciembre de 1993 OBTENCION DEL OXIDO DE MAGNESIO A PARTIR DE LA DOLOMITA Juan Huamayalli L. y Rómulo Ochoa L.* RESUMEN El presente trabajo de investigación muestra
Revista de Química. Vol. VII. Nº 2. Diciembre de 1993 OBTENCION DEL OXIDO DE MAGNESIO A PARTIR DE LA DOLOMITA Juan Huamayalli L. y Rómulo Ochoa L.* RESUMEN El presente trabajo de investigación muestra
DESTILACION FRACCIONADA
 I Rev. 2 Hoja 1 de 7 1. INTRODUCCION. Como se mencionó en la práctica anterior (destilación simple), la destilación es un método de purificación ampliamente usado. Es una de las operaciones básicas más
I Rev. 2 Hoja 1 de 7 1. INTRODUCCION. Como se mencionó en la práctica anterior (destilación simple), la destilación es un método de purificación ampliamente usado. Es una de las operaciones básicas más
4B Reacciones de Sustitución Electrofílica Aromática. Yodación de la Vainillina.
 PRÁCTICA 4B Reacciones de Sustitución Electrofílica Aromática. Yodación de la Vainillina. I. OBJETIVOS. a) Llevar a cabo la yodación de la vainillina para ejemplificar una reacción de sustitución electrofílica
PRÁCTICA 4B Reacciones de Sustitución Electrofílica Aromática. Yodación de la Vainillina. I. OBJETIVOS. a) Llevar a cabo la yodación de la vainillina para ejemplificar una reacción de sustitución electrofílica
EXTRACCION SIMPLE Y MULTIPLE Y DEL PRINCIPIO ACTIVO DEL CLORASEPTIC
 PRACTICA X EXTRACCION SIMPLE Y MULTIPLE Y DEL PRINCIPIO ACTIVO DEL CLORASEPTIC I. OBJETIVOS II MATERIAL a) Conocer la técnica de extracción como método de separación y purificación de las sustancias integrantes
PRACTICA X EXTRACCION SIMPLE Y MULTIPLE Y DEL PRINCIPIO ACTIVO DEL CLORASEPTIC I. OBJETIVOS II MATERIAL a) Conocer la técnica de extracción como método de separación y purificación de las sustancias integrantes
Escuela del Petróleo - Química
 Escuela del Petróleo - Química 2012 1 Unidad 2 1) Sistema Materiales 2) Materiales Homogéneos y Heterogéneos. a. Separación de las fases b. Sustancia Pura 3) extensivas e intensivas 4) Sistemas dispersos
Escuela del Petróleo - Química 2012 1 Unidad 2 1) Sistema Materiales 2) Materiales Homogéneos y Heterogéneos. a. Separación de las fases b. Sustancia Pura 3) extensivas e intensivas 4) Sistemas dispersos
Extracción líquido-líquido
 Extracción líquido-líquido: ExtracciónDecantación 1/5 Extracción líquido-líquido Coeficiente de reparto. ExtracciónDecantación. Secado de disoluciones y recuperación de producto. Fundamento teórico. Procedimiento
Extracción líquido-líquido: ExtracciónDecantación 1/5 Extracción líquido-líquido Coeficiente de reparto. ExtracciónDecantación. Secado de disoluciones y recuperación de producto. Fundamento teórico. Procedimiento
Métodos para la determinación de grasas
 Practica 4 Métodos para la determinación de grasas Antecedentes Los lípidos se encuentran ampliamente distribuidos en animales y vegetales, formado parte fundamental de membranas celulares. En los alimentos
Practica 4 Métodos para la determinación de grasas Antecedentes Los lípidos se encuentran ampliamente distribuidos en animales y vegetales, formado parte fundamental de membranas celulares. En los alimentos
SEPARACIÓN DE LOS COMPONENTES DE UNA MEZCLA OBJETIVOS: Establecer los fundamentos teóricos de los proceso de separación.
 PRÁCTICA Nº 2 SEPARACIÓN DE LOS COMPONENTES DE UNA MEZCLA OBJETIVOS: Establecer los fundamentos teóricos de los proceso de separación. Separar los componentes de una muestra problema. Realizar la destilación
PRÁCTICA Nº 2 SEPARACIÓN DE LOS COMPONENTES DE UNA MEZCLA OBJETIVOS: Establecer los fundamentos teóricos de los proceso de separación. Separar los componentes de una muestra problema. Realizar la destilación
LA MATERIA. - Masa - Volumen -Energía - Carga eléctrica. Propiedades generales
 TEMA 2 La Materia LA MATERIA Propiedades generales - Masa - Volumen -Energía - Carga eléctrica Propiedades características - Densidad - Punto de fusión - Punto de ebullición -Conductividad eléctrica -
TEMA 2 La Materia LA MATERIA Propiedades generales - Masa - Volumen -Energía - Carga eléctrica Propiedades características - Densidad - Punto de fusión - Punto de ebullición -Conductividad eléctrica -
OBTENCIÓN DE ACETATO DE ISOAMILO. a) Preparar un éster a partir de un alcohol y un ácido carboxílico.
 PRÁCTICA 11 OBTENCIÓN DE ACETATO DE ISOAMILO (ACEITE DE PLATANO) I. OBJETIVO a) Preparar un éster a partir de un alcohol y un ácido carboxílico. b) Aplicar algunas técnicas de laboratorio ya conocidas
PRÁCTICA 11 OBTENCIÓN DE ACETATO DE ISOAMILO (ACEITE DE PLATANO) I. OBJETIVO a) Preparar un éster a partir de un alcohol y un ácido carboxílico. b) Aplicar algunas técnicas de laboratorio ya conocidas
INSTRUMENTOS BÁSICOS DE UN LABORATORIO
 INSTRUMENTOS BÁSICOS DE UN LABORATORIO Trasfondo y Contenido En un laboratorio se utiliza una amplia variedad de instrumentos o herramientas que, en su conjunto, se denominan material de laboratorio. Pueden
INSTRUMENTOS BÁSICOS DE UN LABORATORIO Trasfondo y Contenido En un laboratorio se utiliza una amplia variedad de instrumentos o herramientas que, en su conjunto, se denominan material de laboratorio. Pueden
OBTENCION DEL ACIDO BENZOICO
 I. OBJETIVOS PRACTICA XI OBTENCION DEL ACIDO BENZOICO a) Ilustrar un método de obtención de ácidos carboxílicos. b) Preparar ácido benzóico mediante la reacción del haloformo. c) Demostrar que mediante
I. OBJETIVOS PRACTICA XI OBTENCION DEL ACIDO BENZOICO a) Ilustrar un método de obtención de ácidos carboxílicos. b) Preparar ácido benzóico mediante la reacción del haloformo. c) Demostrar que mediante
5012 Síntesis de ácido acetilsalicílico (aspirina) a partir de ácido salicílico y anhidrido acético
 NP 5012 Síntesis de ácido acetilsalicílico (aspirina) a partir de ácido salicílico y anhidrido acético CH CH + H H 2 S 4 + CH 3 CH C 4 H 6 3 C 7 H 6 3 C 9 H 8 4 C 2 H 4 2 (120.1) (138.1) (98.1) (180.2)
NP 5012 Síntesis de ácido acetilsalicílico (aspirina) a partir de ácido salicílico y anhidrido acético CH CH + H H 2 S 4 + CH 3 CH C 4 H 6 3 C 7 H 6 3 C 9 H 8 4 C 2 H 4 2 (120.1) (138.1) (98.1) (180.2)
1001 Nitración de tolueno a 4-nitrotolueno, 2-nitrotolueno y 2,4- dinitrotolueno
 1001 Nitración de tolueno a 4-nitrotolueno, 2-nitrotolueno y 2,4- dinitrotolueno CH 3 CH 3 CH 3 NO 2 CH 3 NO 2 HNO 3 /H 2 SO 4 + + + subproductos NO 2 NO 2 C 7 H 8 HNO 3 (63.0) C 7 H 7 NO 2 C 7 H 6 N 2
1001 Nitración de tolueno a 4-nitrotolueno, 2-nitrotolueno y 2,4- dinitrotolueno CH 3 CH 3 CH 3 NO 2 CH 3 NO 2 HNO 3 /H 2 SO 4 + + + subproductos NO 2 NO 2 C 7 H 8 HNO 3 (63.0) C 7 H 7 NO 2 C 7 H 6 N 2
PURIFICACIÓN DE ÁCIDO BENZOICO POR RECRISTALIZACIÓN Y SUBLIMACIÓN Y DETERMINACIÓN DEL PUNTO DE FUSIÓN
 PURIFICACIÓN DE ÁCIDO BENZOICO POR RECRISTALIZACIÓN Y SUBLIMACIÓN Y DETERMINACIÓN DEL PUNTO DE FUSIÓN Isabella Orozco 11200001, David Colorado 10120042 Universidad Icesi Facultad de Ciencias Naturales
PURIFICACIÓN DE ÁCIDO BENZOICO POR RECRISTALIZACIÓN Y SUBLIMACIÓN Y DETERMINACIÓN DEL PUNTO DE FUSIÓN Isabella Orozco 11200001, David Colorado 10120042 Universidad Icesi Facultad de Ciencias Naturales
Práctica 6. Propiedades físicas y enlace químico
 Práctica 6. Propiedades físicas y enlace químico Revisaron: M. en C. Martha Magdalena Flores Leonar Dr. Víctor Manuel Ugalde Saldívar PREGUNTA A RESPONDER AL FINAL DE LA PRÁCTICA Qué tipo de enlace predomina
Práctica 6. Propiedades físicas y enlace químico Revisaron: M. en C. Martha Magdalena Flores Leonar Dr. Víctor Manuel Ugalde Saldívar PREGUNTA A RESPONDER AL FINAL DE LA PRÁCTICA Qué tipo de enlace predomina
PRÁCTICA Nº 2 OPERACIONES COMUNES EN UN LABORATORIO
 PRÁCTICA Nº 2 OPERACIONES COMUNES EN UN LABORATORIO OBJETIVO Utilizar el material de laboratorio en las operaciones más comunes realizadas en un laboratorio de química. I. ASPECTOS TEÓRICOS Una vez conocido
PRÁCTICA Nº 2 OPERACIONES COMUNES EN UN LABORATORIO OBJETIVO Utilizar el material de laboratorio en las operaciones más comunes realizadas en un laboratorio de química. I. ASPECTOS TEÓRICOS Una vez conocido
PRÁCTICA Nº 4 GRAVIMETRÍA. OBJETIVOS. Determinar el porcentaje de humedad y cenizas en alimentos y suelo. I. FUNDAMENTO TEÓRICO.
 PRÁCTICA Nº 4 GRAVIMETRÍA OBJETIVOS. Determinar el porcentaje de humedad y cenizas en alimentos y suelo. I. FUNDAMENTO TEÓRICO. El término Gravimetría (del lat. gravis, pesado, y metría, medida), se refiere
PRÁCTICA Nº 4 GRAVIMETRÍA OBJETIVOS. Determinar el porcentaje de humedad y cenizas en alimentos y suelo. I. FUNDAMENTO TEÓRICO. El término Gravimetría (del lat. gravis, pesado, y metría, medida), se refiere
Práctica 3. Solubilidad
 Práctica 3. Solubilidad PREGUNTS RESPONDER L FINL DE L PRÁTI La concentración es una propiedad intensiva o extensiva? Por qué? Por qué al aumentar la temperatura aumenta la solubilidad de una disolución
Práctica 3. Solubilidad PREGUNTS RESPONDER L FINL DE L PRÁTI La concentración es una propiedad intensiva o extensiva? Por qué? Por qué al aumentar la temperatura aumenta la solubilidad de una disolución
Laboratorio De Química TRABAJO PRÁCTICO Nº 3 SISTEMAS MATERIALES
 TRABAJO PRÁCTICO Nº 3 SISTEMAS MATERIALES - Materia Es todo lo que posee masa, y ocupa un lugar en el espacio. - Sistema Materi al Porción de materia que se aisla para su estudio. - Sistema Homogéneo Es
TRABAJO PRÁCTICO Nº 3 SISTEMAS MATERIALES - Materia Es todo lo que posee masa, y ocupa un lugar en el espacio. - Sistema Materi al Porción de materia que se aisla para su estudio. - Sistema Homogéneo Es
LOS ESTADOS DE LA MATERIA
 LOS ESTADOS DE LA MATERIA Como ya hemos estudiado, la materia se presenta en cuatro estados físicos: sólido, líquido, gas y plasma. El plasma es el estado de la materia en las estrellas. Una sustancia,
LOS ESTADOS DE LA MATERIA Como ya hemos estudiado, la materia se presenta en cuatro estados físicos: sólido, líquido, gas y plasma. El plasma es el estado de la materia en las estrellas. Una sustancia,
FILTRACIÓN Y DECANTACIÓN
 Universidad Tecnológica de Pereira Facultad de Tecnología Programa de Química Química I FILTRACIÓN Y DECANTACIÓN Objetivos Aplicar adecuadamente las técnicas de filtración por gravedad y al vacío. Separar
Universidad Tecnológica de Pereira Facultad de Tecnología Programa de Química Química I FILTRACIÓN Y DECANTACIÓN Objetivos Aplicar adecuadamente las técnicas de filtración por gravedad y al vacío. Separar
Aplicación y control de procesos químicos de purificación Siglema: AQPU-02
 PRACTICA: 1 Método de purificación de líquidos Objetivos Reconocer las diferentes técnicas de destilación, métodos ampliamente utilizados en laboratorio de química orgánica para la purificación de sustancias
PRACTICA: 1 Método de purificación de líquidos Objetivos Reconocer las diferentes técnicas de destilación, métodos ampliamente utilizados en laboratorio de química orgánica para la purificación de sustancias
PRÁCTICA 1. IDENTIFICACIÓN Y MANEJO DE MATERIAL DE LABORATORIO: PREPARACIÓN DE DISOLUCIONES Y MEDIDA DE DENSIDADES
 PRÁCTICA 1. IDENTIFICACIÓN Y MANEJO DE MATERIAL DE LABORATORIO: PREPARACIÓN DE DISOLUCIONES Y MEDIDA DE DENSIDADES OBJETIVOS ESPECÍFICOS 1) Identificar y manejar el material básico de laboratorio. 2) Preparar
PRÁCTICA 1. IDENTIFICACIÓN Y MANEJO DE MATERIAL DE LABORATORIO: PREPARACIÓN DE DISOLUCIONES Y MEDIDA DE DENSIDADES OBJETIVOS ESPECÍFICOS 1) Identificar y manejar el material básico de laboratorio. 2) Preparar
TRABAJO PRÁCTICO Nº2 SOLUBILIDAD DE COMPUESTOS ORGÁNICOS
 1. Introducción TRABAJO PRÁCTICO Nº2 SOLUBILIDAD DE COMPUESTOS ORGÁNICOS En este práctico observaremos algunas características físicas de los compuestos orgánicos. Entre las propiedades físicas más fáciles
1. Introducción TRABAJO PRÁCTICO Nº2 SOLUBILIDAD DE COMPUESTOS ORGÁNICOS En este práctico observaremos algunas características físicas de los compuestos orgánicos. Entre las propiedades físicas más fáciles
