RESONANCIA MAGNÉTICA NUCLEAR
|
|
|
- Emilia Quintana Camacho
- hace 7 años
- Vistas:
Transcripción
1 RESONANIA MAGNÉTIA NULEAR
2 SPIN DEL NULEO El nucleo de algunos átomos poseen SPIN. Estos núcleos se comportan como si estuvieran girando... no sabemos si realmente giran! Es como la propiedad de un electrón, que puede poser dos spins: +1/2 y -1/2. ada núcleo de spin-activo tiene un número de spins definido por su número cuántico de spin, I. los números cuánticos de spin de algunos núcleos comunes..
3 Números cuánticos de spin de algunos núcleos Los isótopos más abundantes de y O no tienen espín. Elemento N 16 O 17 O 19 F spin Nuclear No uántico 1/ / /2 1/2 ( I ) No. Estados de spin Elementos con masa impar y/o número atómico impar Tienen la propiedad de spin nuclear. El número de estados de spin es 2I + 1, donde I es el número cuántico de spin.
4 EL PROTÓN Aunque está aumentando el interés en otros núcleos, particularmente -13, el núcleo de hidrógeno (protones) se estudia con más frecuencia, y dedicaremos nuestra atención a ello.
5 ESTADOS DE SPIN NULEAR - IDRÓGENO El giro del núcleo cargado positivamente genera un vector momento magnético, /2-1/2 DOS ESTADOS DE SPIN Los dos estados son equivalentes en energía en ausencia de un campo magnético o uno eléctrico.
6 EL FENÓMENO DE RESONANIA absorción de energía por el núcleo en movimiento (spinning)
7 NIVELES DE ENERGÍA DE SPIN NULEAR N En un campo magnético fuerte (Bo) el spin de los dos estados difieren en energía. -1/2 sin alinear +1/2 B o S alineado
8 Absorción de Energía cuantizada opuesto -1/2-1/2 E = h Radiofrecuencia E +1/2 +1/2 ampo aplicado B o alineado
9 LA SEPARAIÓN DE E DEPENDE DE B o -1/2 degenerado a B o = 0 E = kb o = h + 1/2 B o fuerza del campo magnético
10 EL EFETO SEUNDARIO DE UN AMPO MAGNÉTIO FUERTE UANDO SE OLOA UN ÁTOMO DE IDRÓGENO ON UN SPIN-ATIVO EN UN AMPO MAGNÉTIO FUERTE.. OMIENZA A PREESAR
11 N RADIOFREQUENIA Mz h Si = entonces la energía será absorbida y el spin se invierte. S El nucleo precesa con una frecuencia al colocarlo en un campo magnético fuerte. RESONANIA MAGNETIA NULEAR RMN
12 La ecuación de Larmor E = kb o = h se transforma en frecuencia de la radiación entrante que provocara una transición B 0 B o propiedad giromagnética Fuerza del campo magnético es una constante que es diferente para cada nucleo (,, N, etc)
13 Frecuencias de Resonancia Isótopo Abundancia B o (Tesla) Frecuencia(Mz) (radians/tesla) % % : % F 100.0%
14 POBLAIÓN E INTENSIDAD DE SEÑAL La intensidad de la señal en RMN depende de la Diferencia de Poblaciones de los dos estados de spin La radiación induce transiciones hacia abajo o hacia arriba. resonancia Emisión decaemiento inducido Para una señal positiva neta debe haber un exceso de spins en el estado de baja energía. Saturación = poblaciones iguales = no hay señal población en exceso
15 INSTRUMENTAIÓN LÁSIA ANTES DE 1960 SE BARRÍA EL AMPO
16 Un espectrómetro simple de 60 Mz RF (60 Mz) Oscilador Transmisor h Señal de absorción RF Detector Receptor Registrador MAGNETO N MAGNETO S ~ 1.41 Tesla (+/-) unos pocos ppm Sonda
17 Afortunadamente, los diferentes tipos de protones precesionan a diferentes valores. N B o = 1.41 Tesla EJEMPLO: h 60 Mz Mz 2 S O Mz Mz Para provocar la absorción de la energía a 60 Mz la intensidad de campo magnético, Bo, debe aumentarse a un valor diferente para cada tipo de protones. Las diferencias son muy pequeñas, en el intervalo de partes por millón.
18 EN LA RMN LÁSIA EL INSTRUMENTO BARRE DE "AMPO BAJO" A "AMPO ALTO" AMPO BAJO ESALA DE RMN AMPO ALTO AMPO BAJO BARRIDO AMPO ALTO
19 Espectro de Fenilacetona O 2 3 NOTE QUE ADA TIPO DIFERENTE DE PROTON APAREE EN UN LUGAR DIFERENTE - PUEDE INDIAR UÁNTOS TIPOS DIFERENTES DE IDRÓGENO AY???
20 INSTRUMENTAIÓN MODERNA TENOLOGÍA DE TRANSFORMADA DE FOURIER PULSADA FT-RMN Requiere de una computadora
21
22 EXITAIÓN PULSADA N PULSO DE RF DE BANDA ANA ontiene varias radiofrecuencias 1... n 2 1 O Todos los tipos de hidrógeno son excitados simultáneamente con el pulso de RF. S
23 DEAIMIENTO INDUIDO LIBRE FID ( relajación ) 1 O , 2, 3 tienen diferentes vidas media
24 FID OMPUESTO espectro dominio tiempo tiempo
25 TRANSFORMADA DE FOURIER Una técnica matemática que resuelve una señal FID compleja en las frecuencias individuales que se sumaron para generarla. DOMINIO TIEMPO FID convertida a DOMINIO FREUENIA ESPETRO RMN DOMINIO TÉRMINO MATEMÁTIO SEÑAL FT-RMN computadora OMPLEJA Transformada fourier una mezcla de frecuencias decayendo (en tiempo) frecuenciasl individuales onvertidas en espectro
26 El FID compuesto se transforma en un espectro de RMN clásico: O PROTONES 2 PROTONES PROTONES Group n Shift Error ESPETRO EN DOMINIO DE FREUENIAS
27 El FID compuesto se transforma en un espectro de RMN clásico: 2 O 3 espectro dominio frecuencia
28 OMPARIÓN DE TENIAS O Y FT
29 MÉTODO ONDA ONTINUA (O) EL VIEJO MÉTODO LÁSIO El campo magnético se BARRE" de campo bajo a campo alto mientras que un haz constante de radiofrecuencia (onda continua) irradía con una frecuencia fija (decir 100 Mz). Este método requiere de varios minutos para graficar en espectro de RMN. LENTO, MUO RUIDO
30 METODO DE TRANSFORMADA DE FOURIER PULSADA (FT) EL NUEVO MÉTODO FT - OMPUTADORA Muchos protones se relajan (decaen) de sus estados excitados rápidamente (segundos). El pulso de excitación, la colección de datos (FID), y la operación de FT (computadora) toma unos cuantos segundos. El pulso y la colección de datos se puede ciclar y repetirse cada pocos segundos RÁPIDA BAJO RUIDO Se pueden hacer muchas repeticiones en muy poco tiempo, llevando a mejorar la señal..
31 MEJORA LA RELAIÓN SEÑAL-RUIDO Sumando las señales de muchos impulsos, se puede aumentar la intensidad de la señal por encima del nivel de ruido. ruido señal señal mejorada 1er pulso 2 pulso pulso n etc. sumando muchos pulsos el ruido es aleatorio y se cancela
32 INTEGRAIÓN
33 NMR Espectro de Fenilacetona O 2 3 ada tipo de proton ocurre en diferentes lugares. Se puede saber cuantos tipos distintos de protones contiene la molécula.
34 INTEGRAIÓN DE UN PIO No sólo cada tipo diferente de hidrógeno da un pico distinto en el espectro NMR, pero también podemos determinar la cantidad relativa de cada tipo de hidrógeno mediante un proceso llamado integración. Integración = determinación del área bajo un pico El área bajo un pico es proporcional al número de átomos de hidrógeno que generan el pico.
35 AETATO DE BENILO La línea integral sube una cantidad proporcional al número de en cada pico linea integración MÉTODO 1 Linea integración 55 : 22 : 33 = 5 : 2 : 3 Relación simple de las alturas
36 Acetato de Bencilo(FT-NMR) Real : / 11.3 = / 11.3 = / 11.3 = O O 3 MÉTODO 2 Integración digital asume que / 3 = 11.3 Integrales son buenas con una precisión de cerca 10%. Los instrumentos modernos informan integral como un número.
37 NMR Espectro de Fenilacetona O PROTONES PROTONES 2 PROTONES Group n Shift Error
38 ANISOTROPÍA DIAMAGNÉTIA EFETO DE SIELDING POR ELETRONES DE VALENIA
39 Anisotropía Diamagnética El campo aplicado induce la circulación de los electrones de valencia, esto genera un campo magnético que se opone al campo aplicado. Los electrones de valencia protegen el núcleo del efecto de campo aplicado Líneas del campo magnético B o aplicado B inducido (opone a B o ) Los campos se contrarrestan en el nucleo
40 PROTONES DIFIEREN EN SU SIELDING Todos los diferentes tipos de protones en una molécula tienen un diferentes efecto de shielding. Todos responden diferente al campo magnético aplicado y aparecen en lugares diferentes en el espectro. Esto es por lo qué un espectro NMR contiene información útil (diferentes tipos de protones aparecen en lugares predecibles). AMPO BAJO Protones menos protegidos. espectro AMPO ALTO Protones más protegidos.. un mayor campo para producir resonancia.
41 DESPLAZAMIENTO QUÍMIO
42 PIOS SE MIDEN EN RELAIÓN A TMS Más bien que medir la posición exacta de resonancia de un pico, medimos cuánto se desplaza de la señal de TMS. 3 3 Si 3 3 ompuesto de referencia tetrametilsilano TMS Protones muy protegidos aparecen a campo alto. TMS desplazamiento en z n campo bajo 0 originalmente se pensaba que no habría ningún otro compuesto en un mayor campo que TMS.
43 De la discusión teórica frecuencia Fuerza del campo ampos magnéticos fuertes (B o ) causan que el instrumento opere a mayores frecuencias ( ). h = B 2 o = ( K) B o constantes Fuerza del campo NMR 1.41 T 2.35 T 7.05 T 1 Frecuencia de operación 60 Mhz 100 Mz 300 Mz
44 FREUENIAS ALTAS DAN MÁS SIELDING El cambio observado para un determinado protón en z también depende de la frecuencia del instrumento utilizado. a frecuencias más altas = desplazamientos más grandes en z. desplazamiento en z campo bajo n 0 TMS
45 DESPLAZAMIENTO QUÍMIO Los desplazamientos de TMS en z son mayores en los instrumentos de campo altos (300 Mz, 500 Mz) que en los instrumentos de campo menores (100 Mz, 60 Mz). Podemos ajustar el desplazamiento a un valor independiente del campo, de la siguiente manera: partes por millón desplaza miento = = cambio en z frecuencia del equipo en Mz = ppm Esta división da un número independiente del instrumento utilizado. Un proton en una molécula determinada ocurrirá siempre al mismo desplazamiento químico (valor constante).
46 EQUIVALENIA en z de 1 PPM Qué representa una ppm? 1 frecuencia de operación z equivalente de 1 ppm 60 Mhz 60 z 100 Mz 100 z 300 Mz 300 z 1 parte por millón de n Mz es n z 1 n Mz ( ) = n z ppm ada unidad ppm representa ya sea un cambio de 1 ppm en Bo (intensidad de campo magnético, Tesla) o 1 ppm de cambio en la frecuencia precesional (Mz).
47 Tabla de correlación NMR AMPO BAJO DESPROTEGIDA l 3, -O -N AMPO ALTO PROTEGIDA TMS (ppm) ROO RO = 2 F 2 l 2 Br 2 I 2 O 2 NO 2 2 Ar 2 NR 2 2 S - = O Se pueden definir intervalos para diferentes tipos de protones. Esta tabla es general, la siguiente diapositiva es mas clara.
48 DESPLAZAMIENTOS QUÍMIOS APORX (ppm) PARA PROTONES ESPEÍFIOS R R-N R-=- R- -R R-S R I R-= Br O R l O O RO R--N RO O O O O R-- O R--O N O O 2 N R--O- R F R R-N Ar-N R-S- R-O Ar-O
49 NO NEESITA MEMORIZAR LA TABLA ANTERIOR NORMALMENTE ES SUFIIENTE ON SABER QUÉ TIPOS DE ÁTOMOS DE IDRÓGENO APAREEN EN LAS ÁREAS DE LA TABLA DE RMN ácido OO aldéhido O benceno alqueno =- - donde en unido a un átomo cercano a electronegativo enlaces pi X-- X=-- alifático LA MAYORÍA DE ESPETROS PUEDEN INTERPRETARSE ON LOS DATOS QUE SE MUESTRAN AQUÍ
50 DESPROTEIÓN Y ANISOTROPÍA Son tres factores los principales para fijar las posiciones de resonancia (en la escala de ppm) de la mayoría de los protones. 1. Desprotección por elementos electronegativos. 2. ampo anisotrópico usualmente debido a electrones en la molécula. 3. Desprotección debida a puentes de hidrógeno. Vamos a discutir estos factores en las secciones siguientes.
51 DESIELDING POR ELEMENTOS ELETRONEGATIVOS
52 DESIELDING POR UN ELEMENTO ELETRONEGATIVO - l Elemento electronegativo - El loro desprotege" al protón, es decir, quita densidad de electrones de valencia del carbono, el que a su vez gana más densidad del hidrógeno. ESALA NMR protones desprotegidos" aparecen en el campo bajo protones altamente protegidos aparecen en campo alto desprotección mueve la resonancia del protón a campo bajo
53 Relación Electronegatividad- Desplazamiento Químico Dependencia del Desplazamiento Químico de 3 X con el elemento X ompuesto 3 X 3 F 3 O 3 l 3 Br 3 I 4 ( 3 ) 4 Si Elemento X Electronegatividad de X Desplazamiento F O l Br I Si mas desprotegidos desprotección aumenta con la electronegatividad del átomo x TMS
54 Efecto de sustituyentes en el desplazamiento químico mas protegidos l 3 2 l 2 3 l ppm El efecto aumenta con un mayor número de átomos electronegativos. menos protegidos - 2 -Br Br Br ppm El efecto disminuye con la distancia.
55 AMPOS ANISOTROPIOS DEBIDO A LA PRESENIA DE ENLAES La presencia de enlaces o un sistema cercano afecta enormemente el desplazamiento químico. Anillos de benceno tienen el mayor efecto.
56 orriente del Anillo en Benceno electrones circulando Desprotegido los campos se suman B o ampo magnético secundario generado por electrones electrones desprotegen protones aromáticos
57 AMPO ANISOTROPIO EN UN ALQUENO desprotegido los campos se suman = protones desprotegidos Desplazado a campo bajo Líneas de campo magnético (anisotropicas) B o
58 AMPO ANISOTRÓPIO PARA UN ALQUINO B o protegidos los campos se restan protones protegidos Líneas de campo magnético (anisotropicas)
59 PUENTES DE IDRÓGENO
60 PUENTES DE IDRÓGENO DESPROTEGEN AL PROTÓN R O O R O R El desplazamiento químico depende de la cantidad de puentes de hidrógeno que se den. alcoholes varían en desplazamiento químico de 0,5 ppm (O libre) a unos 5.0 ppm (muchos puentes de ). Los puentes de hidrógeno alargan el enlace O- y reduce la densidad de electrones de valencia alrededor del protón - es desprotegido y desplazado a campo bajo en el espectro NMR.
61 EJEMPLOS EXTREMOS R O O O O R Los ácidos carboxílicos forman puentes de hidrógeno fuertes - forman dímeros. 3 O O O con los ácidos carboxílicos las absorciones del O- se encuentran entre 10 y 12 ppm muy lejos a campo bajo. en el salicilato de metilo, que tiene fuerte puentes de hidrógeno internos, la absorción de NMR del O- es aproximadamente 14 ppm, a muy, muy campo bajo. nótese que se forma un anillo de 6 miembros.
62 SPIN-SPIN SPLITTING
63 SPIN-SPIN SPLITTING A menudo, un grupo de átomos de hidrógeno aparecerá como un multiplete en lugar de un solo pico. Los multipletes se denominan como sigue: Singulete Doblete Triplete uarteto Quinteto Septeto Octeto etc. Esto ocurre debido a la interacción con hidrógenos vecinos y se llama SPIN-SPIN SPLITTING.
64 1,1,2-Tricloroetano Los dos tipos de átomos de hidrógeno no aparecen como picos únicos, más bien hay un "triplete" y un "doblete". integral = 2 l l integral = 1 l triplete doblete Los subpicos son debido a spinspin splitting y se predicen con la regla n + 1.
65 Regla n + 1
66 1,1,2-Tricloroetano integral = 2 l l integral = 1 l De dónde vienen estos multipletes?... interacción con los vecinos
67 la señal de este hidrógeno está dividida por sus dos vecinos dos vecinos n+1 = 3 triplete estos átomos de hidrógeno están divididos por su único vecino Un vecino n+1 = 2 doblete MULTIPLETES singulete doublete triplete cuarteto quinteto sexteto septeto
68 EXLUSIONES DE LA REGLA N+1 IMPORTANTE! 1) Protones que son equivalentes por simetría generalmente no se dividen entre sí X Y X 2 2 Y no hay splitting si x=y no hay splitting si x=y 2) Protones en el mismo grupo generalmente no se dividen entre sí or mas detalles después
69 EXLUSIONES DE LA REGLA N+1 3) la regla N + 1 regla se aplica principalmente a los protones en cadenas alifáticas (saturadas) o anillos saturados o SI SI pero no se aplica (en la forma simple que se muestra aquí) a protones en dobles enlaces o anillos de aromáticos. 3 3 NO NO
70 ALGUNOS PATRONES OMUNES
71 ALGUNOS PATRONES OMUNES DE SPLITTING X Y 3 ( x = y ) X 2 2 ( x = y ) Y 3 3
72 EJEMPLOS DE ESPETROS ON SPLITTING
73 Espectro de Bromoetano Br 2 3
74 Espectro de 2-Nitropropano 3 3 O N + O - 1:6:15:20:16:6:1 en multipletes mayores las señales exteriores se pierden en la línea de base
75 Espectro de Acetaldehido 3 O offset = 2.0 ppm
76 INTENSIDADES DE SEÑALES EN MULTIPLETES TRIÁNGULO DE PASAL
77 TRIÁNGULO DE PASAL Intensidades de multipletes 1 singulete Los valores al centro son las sumas de los dos números inmediatamente anteriores doblete triplete cuarteto quinteto sexteto septeto octeto
78 EL ORIGEN DEL SPIN-SPIN SPLITTING OMO OURRE
79 EL DESPLAZAMIENTO QUÍMIO DEL PROTÓN A ES AFETADO POR EL SPIN DE SUS VEINOS Alineado con B o Opuesto ab o 50 % de +1/2-1/2 las moléculas A A 50 % de las moléculas B o campo bajo vecino alineado campo alto vecino opuesto En un momento dado alrededor de la mitad de las moléculas en solución tendrá spin + 1/2 y la otra mitad tendrá spin -1/2.
80 ARREGLOS DE SPIN UN VEINO n+1 = 2 doblete UN VEINO n+1 = 2 doblete spins azules spins verdes Las posiciones de resonancia (splitting) de un determinado hidrógeno se ve afectada por el posible spin de su vecino.
81 ARREGLOS DE SPIN dos vecinos n+1 = 3 triplete un vecino n+1 = 2 doblete spin de metilenos spin de metinos
82 ARREGLOS DE SPIN tres vecinos n+1 = 4 cuarteto dos vecinos n+1 = 3 triplete spin de metilos spin de metilenos
83 LA ONSTANTE DE AOPLAMIENTO
84 LA ONSTANTE DE AOPLAMIENTO J J J J J J La constante de acoplamiento J es la distancia (medida en z) entre los picos de un multiplete. J es una medida de la cantidad de interacción entre los dos conjuntos de átomos de hidrógeno que generan el multiplete.
85 100 Mz OMPARAIÓN DE AMPO 200 z Las constantes de acoplamiento son constantes - no cambian a intensidades de campo diferentes J = 7.5 z 7.5 z 100 z Mz Mayor separación 400 z 200 z El valor de es dependiente del campo J = 7.5 z 7.5 z ppm
86 100 Mz 200 z J = 7.5 z J = 7.5 z 100 z Mz Vea la compresión del multiplete en espectro de 200 Mz cuando se traza en la misma escala que el espectro de 100 Mz en lugar de en un gráfico que sea dos veces más amplio. Mayor separación J = 7.5 z 400 z 200 z ppm
87 50 Mz Por qué comprar un instrumento de campo mayor? J = 7.5 z!se simplifican los espectros Mz J = 7.5 z 2 1 Se resuelven los multipletes Mz Los efectos de segundo orden se minimizan J = 7.5 z 3 2 1
88 NOMENLATURA DE J El tipo más común de acoplamiento es entre átomos de hidrógeno en átomos de carbono adyacentes. 3 J A veces esto se llama acoplamiento vicinal. Es designado 3 J ya que participan 3 enlaces entre los dos átomos de hidrógeno. Otro tipo de acoplamiento que también puede ocurrir en casos especiales 2 J o acoplamiento geminal ( a menudo 2 J = 0 ) El acoplamiento geminal no ocurre cuando los dos átomos de hidrógeno son equivalentes debido a las rotaciones alrededor de los otros dos enlaces. 2 J
89 AOPLAMIENTO A DISTANIA Acoplamientos más grandes que 2 J o 3 J también existen, pero funcionan sólo en situaciones especiales. 4 J, por ejemplo, se produce principalmente cuando los átomos de hidrógeno se ven obligados a adoptar esta conformación «W» (como en los compuestos bicíclicos). Acoplamientos más grandes que 3 J (p. ej., 4 J, 5 J, etc.) suelen llamarse "acoplamiento a larga distancia".
90 ONSTANTES DE AOPLAMIENTO OMUNES vicinal trans 6 a 8 z 11 a 18 z tres enlaces tres enlaces 3 J 3 J cis geminal 6 a 15 z 0 a 5 z tres enlaces dos enlaces 3 J 2 J ax ax,ax = 8 a 14 eq ax,eq = 0 a 7 tres enlaces 3 J eq ax eq,eq = 0 a 5
91 cis trans 6 a 12 z 4 a 8 z tres enlaces 3 J 4 a 10 z tres enlaces 3 J 0 a 3 z cuatro enlaces 4 J 0 a 3 z cuatro enlaces 4 J Acoplamientos que ocurren a distancias mayores a tres enlaces son acoplamientos a larga distancia y son generalmente pequeños (< 3 z) y frecuentemente inexistentes (0 z).
92 RESUMEN
93 INFORMAIÓN DE LOS ESPETROS DE NMR 1. ada tipo de hidrógeno da un pico o un grupo de picos (multiplete). 2. El desplazamiento químico ( en ppm) permite definir el tipo de hidrógeno que genera la señal (alcano, alqueno, benceno, aldehido, etc.) 3. La integración define el número de cada tipo de hidrógeno. 4. Spin-spin splitting informa sobre el número de hidrógenos en carbones adiacentes 5. La constante de acoplamiento J da información sobre el arreglo de los átomos involucrados
94 ESPETROSOPÍA ERRAMIENTA PODEROSA En general, con sólo cuatro tipos de datos 1) Fórmula mínima (o % composición) 2) Espectro de infrarojo 3) Espectro de NMR 4) Espectro de masas un químico a menudo puede asignar la estructura completa de una molécula desconocida.
95 EJERIIOS DE INTERPRETAIÓN PARTE 1
96 1 Metil Etil etona (MEK) NMR 07 O
97
98 2 Acetato de Etilo NMR 08 omparar el cambio de desplazamiento del metileno al de metil etil cetona (diapositiva anterior). O 3 O
99 3 Ácido a-loropropiónico NMR O O 3 l 1
100 4 t-butil Metil etona (3,3-dimetil-2-butanona) NMR 03 O
101 5 1-Nitropropano NMR 05 + O N O
102 6 1,3-Dicloropropano NMR 17 l l 2 4
RESONANCIA MAGNÉTICA NUCLEAR
 RESONANCIA MAGNÉTICA NUCLEAR SPIN DEL NUCLEO El nucleo de algunos átomos poseen SPIN. Estos núcleos se comportan como si estuvieran girando... no sabemos si realmente giran! Es como la propiedad de un
RESONANCIA MAGNÉTICA NUCLEAR SPIN DEL NUCLEO El nucleo de algunos átomos poseen SPIN. Estos núcleos se comportan como si estuvieran girando... no sabemos si realmente giran! Es como la propiedad de un
ESPECTROSCOPÍA DE RESONANCIA MAGNÉTICA NUCLEAR DE PROTONES
 ESPETROSOPÍA DE RESONANIA MAGNÉTIA NULEAR DE PROTONES La resonancia magnética nuclear es posible porque los núcleos de ciertos átomos, aquellos que tienen número de espín diferente de cero, (I ) se comportan
ESPETROSOPÍA DE RESONANIA MAGNÉTIA NULEAR DE PROTONES La resonancia magnética nuclear es posible porque los núcleos de ciertos átomos, aquellos que tienen número de espín diferente de cero, (I ) se comportan
EJERCICIOS DE INTERPRETACIÓN PARTE 2
 EJERCICIOS DE INTERPRETACIÓN PARTE 2 7 Ácido -Bromobutírico NMR 09 CH 3 CH 2 CH O C OH 3 1 Br 1 2 8 Feniletil Acetato NMR 14 5 O CH 2 CH 2 O C CH 3 3 2 2 9 Etil Succinato NMR 18 O O CH 3 CH 2 O C CH 2
EJERCICIOS DE INTERPRETACIÓN PARTE 2 7 Ácido -Bromobutírico NMR 09 CH 3 CH 2 CH O C OH 3 1 Br 1 2 8 Feniletil Acetato NMR 14 5 O CH 2 CH 2 O C CH 3 3 2 2 9 Etil Succinato NMR 18 O O CH 3 CH 2 O C CH 2
Introducción Espectroscopía RMN
 Introducción Espectroscopía RMN +½ -½ +½ -½ Espín Nuclear + + +1/2 1/2 Un núcleo se comporta como un imán diminuto En ausencia de Mext: distribución al azar + + + + + Un campo o externo provoca momentos
Introducción Espectroscopía RMN +½ -½ +½ -½ Espín Nuclear + + +1/2 1/2 Un núcleo se comporta como un imán diminuto En ausencia de Mext: distribución al azar + + + + + Un campo o externo provoca momentos
ESPECTROCOPIA DE RESONANCIA MAGNETICA NUCLEAR
 ESPECTROCOPIA DE RESONANCIA MAGNETICA NUCLEAR La Espectroscopía de Resonancia Magnética Nuclear (RMN) es la herramienta de determinación estructural más potente del químico orgánico. Mediante el RMN podemos
ESPECTROCOPIA DE RESONANCIA MAGNETICA NUCLEAR La Espectroscopía de Resonancia Magnética Nuclear (RMN) es la herramienta de determinación estructural más potente del químico orgánico. Mediante el RMN podemos
Instrumentación en Resonancia Magnética Nuclear: el espectrómetro
 Instrumentación en Resonancia Magnética Nuclear: el espectrómetro Un imán que genere un campo magnético fijo y estable. Generalmente se identifica cada espectrómetro por la frecuencia de resonancia del
Instrumentación en Resonancia Magnética Nuclear: el espectrómetro Un imán que genere un campo magnético fijo y estable. Generalmente se identifica cada espectrómetro por la frecuencia de resonancia del
Resonancia Magnética Nuclear RMN
 Resonancia Magnética Nuclear RMN María Font.. Dpto. Química Orgánica y Farmacéutica. Sección n de Modelización Molecular. Universidad de Navarra 1 María Font.. Dpto. Química Orgánica y Farmacéutica. Sección
Resonancia Magnética Nuclear RMN María Font.. Dpto. Química Orgánica y Farmacéutica. Sección n de Modelización Molecular. Universidad de Navarra 1 María Font.. Dpto. Química Orgánica y Farmacéutica. Sección
TEMA 10. ESPECTROSCOPIA DE RESONANCIA MAGNÉTICA NUCLEAR
 TEMA 10. ESPETROSOPIA DE RESONANIA MAGNÉTIA NULEAR 1. Fundamentos físicos de la espectroscopia de RMN. 2. El espectrómetro de resonancia magnética nuclear. 3. Resonancia magnética nuclear de 1. Apantallamiento
TEMA 10. ESPETROSOPIA DE RESONANIA MAGNÉTIA NULEAR 1. Fundamentos físicos de la espectroscopia de RMN. 2. El espectrómetro de resonancia magnética nuclear. 3. Resonancia magnética nuclear de 1. Apantallamiento
Resonancia Magnética Nuclear. Algunos núcleos atómicos, como por ejemplo el hidrógeno, tienen una propiedad denominada momento magnético
 Resonancia Magnética Nuclear Algunos núcleos atómicos, como por ejemplo el hidrógeno, tienen una propiedad denominada momento magnético Los hidrógenos de un compuesto se comportan como minúsculos imanes
Resonancia Magnética Nuclear Algunos núcleos atómicos, como por ejemplo el hidrógeno, tienen una propiedad denominada momento magnético Los hidrógenos de un compuesto se comportan como minúsculos imanes
Desplazamiento Químico. Dr. Jorge A. Palermo
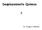 Desplazamiento Químico δ Dr. Jorge A. Palermo ν 0 = γ B 0 / 2π ECUACIÓN DE LARMOR E aumenta con B 0 Núcleo 1 2.35 Tesla 100 Mz 17.63 Tesla 750 Mz ν 0 aumenta con B 0 2 13 C 31 P 15.35 Mz 25.1 Mz 40.5 Mz
Desplazamiento Químico δ Dr. Jorge A. Palermo ν 0 = γ B 0 / 2π ECUACIÓN DE LARMOR E aumenta con B 0 Núcleo 1 2.35 Tesla 100 Mz 17.63 Tesla 750 Mz ν 0 aumenta con B 0 2 13 C 31 P 15.35 Mz 25.1 Mz 40.5 Mz
Resonancia Magnética Nuclear
 Resonancia Magnética Nuclear Química Orgánica I 2013 1H 4.29 4.28 4.28 4.27 4.26 4.26 4.25 4.24 4.23 4.22 4.22 4.21 4.20 4.18 4.18 4.16 4.16 4.14 3.85 3.80 3.75 2.82 2.81 2.80 2.77 2.76 2.75 2.72 2.71
Resonancia Magnética Nuclear Química Orgánica I 2013 1H 4.29 4.28 4.28 4.27 4.26 4.26 4.25 4.24 4.23 4.22 4.22 4.21 4.20 4.18 4.18 4.16 4.16 4.14 3.85 3.80 3.75 2.82 2.81 2.80 2.77 2.76 2.75 2.72 2.71
Resonancia Magnética Nuclear
 Clase 4 152.952 147.290 123.188 117.525 114.209 113.216 76.850 55.678 48.146 41.562 40.012 33.361 32.113 23.659 20.654 19.816 19.720 190 180 170 160 150 140 130 120 110 100 90 80 70 60 50 40 30 20 10 ppm
Clase 4 152.952 147.290 123.188 117.525 114.209 113.216 76.850 55.678 48.146 41.562 40.012 33.361 32.113 23.659 20.654 19.816 19.720 190 180 170 160 150 140 130 120 110 100 90 80 70 60 50 40 30 20 10 ppm
Momento angular de espín
 Momento angular de espín 14 Ene 04 Reson 1 Estado de espín de un electrón: Ŝ 2 χ(σ) = s(s + 1) 2 χ(σ) Ŝ z χ(σ) = m s χ(σ) Donde s = 1/2 y hay dos orientaciones: m s = 1/2, 1/2 Estado de espín de un núcleo:
Momento angular de espín 14 Ene 04 Reson 1 Estado de espín de un electrón: Ŝ 2 χ(σ) = s(s + 1) 2 χ(σ) Ŝ z χ(σ) = m s χ(σ) Donde s = 1/2 y hay dos orientaciones: m s = 1/2, 1/2 Estado de espín de un núcleo:
J H,H pequeño. Equivalencia química y equivalencia magnética
 La magnitud de J para 1 H, 1 H varía entre -20 y 20 Hz J a 2 enlaces 2 J H,H 10-15 Hz J a 3 enlaces 3 J H,H 3-10 Hz J a larga distancia H-C-C-C-H 4 J H,H pequeño Los J heteronucleares son mas grandes,
La magnitud de J para 1 H, 1 H varía entre -20 y 20 Hz J a 2 enlaces 2 J H,H 10-15 Hz J a 3 enlaces 3 J H,H 3-10 Hz J a larga distancia H-C-C-C-H 4 J H,H pequeño Los J heteronucleares son mas grandes,
TEMA 2: Resonancia Magnética Nuclear RMN-1H y 13C Fundamentos
 Fundamentos La Resonancia Magnética Nuclear (RMN) es la técnica que mayor información estructural proporciona. Ello se debe a que se observan los núcleos de los átomos y se puede conocer la influencia
Fundamentos La Resonancia Magnética Nuclear (RMN) es la técnica que mayor información estructural proporciona. Ello se debe a que se observan los núcleos de los átomos y se puede conocer la influencia
E = h = h B 0. Un núcleo con numero atómico impar o numero másico impar tiene spin nuclear.
 ESPETRSPIA 1 -RMN Un núcleo con numero atómico impar o numero másico impar tiene spin nuclear. La carga del núcleo al girar genera un campo magnético uando se aplica un campo magnético externo La carga
ESPETRSPIA 1 -RMN Un núcleo con numero atómico impar o numero másico impar tiene spin nuclear. La carga del núcleo al girar genera un campo magnético uando se aplica un campo magnético externo La carga
Introducción a la Resonancia Magnética Nuclear. Química Orgánica III Primer Semestre 2014
 Introducción a la Resonancia Magnética Nuclear Química Orgánica III Primer Semestre 2014 Referencias empleadas en esta presentación: McMurry, John. Química Orgánica. 8ª. Edición. CENGAGE. Wade, L.J. Química
Introducción a la Resonancia Magnética Nuclear Química Orgánica III Primer Semestre 2014 Referencias empleadas en esta presentación: McMurry, John. Química Orgánica. 8ª. Edición. CENGAGE. Wade, L.J. Química
ANÁLISIS INSTRUMENTAL_UII_PARTE DOS. Propiedades magnéticas de cuatro importantes núcleos que tienen un número cuántico de espín de ½
 RESONANCIA MAGNÉTICA NUCLEAR ANÁLISIS INSTRUMENTAL_UII_PARTE DOS Propiedades magnéticas de cuatro importantes núcleos que tienen un número cuántico de espín de ½ Desplazamiento químico Desdoblamiento spin-
RESONANCIA MAGNÉTICA NUCLEAR ANÁLISIS INSTRUMENTAL_UII_PARTE DOS Propiedades magnéticas de cuatro importantes núcleos que tienen un número cuántico de espín de ½ Desplazamiento químico Desdoblamiento spin-
(( )) Tema 5: Técnicas espectroscópicas: Espectrofotometría. visible Infrarrojo. Ultravioleta. Espectro de emisión de los cuerpos en equilibrio
 Tema 5: Técnicas espectroscópicas: Espectrofotometría 0 22 Hz Frecuencia 0 4 Hz 0 3 Hz γ X UV IR micro radio Rayos γ (gamma) λ < pm Rayos X pm-0nm Visible 400-800nm Ultravioleta 0-400 nm Longitud de onda
Tema 5: Técnicas espectroscópicas: Espectrofotometría 0 22 Hz Frecuencia 0 4 Hz 0 3 Hz γ X UV IR micro radio Rayos γ (gamma) λ < pm Rayos X pm-0nm Visible 400-800nm Ultravioleta 0-400 nm Longitud de onda
SISTEMAS PROTÓNICOS EN RESONANCIA MAGNÉTICO NUCLEAR DE 1 H. Fernando de J. Amézquita L. Diana Mendoza O. Universidad de Guanajuato
 SISTEMAS PROTÓNICOS EN RESONANCIA MAGNÉTICO NUCLEAR DE 1 H Fernando de J. Amézquita L. Diana Mendoza O. Universidad de Guanajuato Clasificación de los sistemas protónicos Sistema A2 Sistema AX Sistema
SISTEMAS PROTÓNICOS EN RESONANCIA MAGNÉTICO NUCLEAR DE 1 H Fernando de J. Amézquita L. Diana Mendoza O. Universidad de Guanajuato Clasificación de los sistemas protónicos Sistema A2 Sistema AX Sistema
Elucidación estructural: Resonancia Magnética Nuclear (Introducción)
 Elucidación estructural: Resonancia Magnética Nuclear (Introducción) Antes de comenzar a entender el fenómeno de la Resonancia magnética debemos considerar cuales son las propiedades que poseen los núcleos
Elucidación estructural: Resonancia Magnética Nuclear (Introducción) Antes de comenzar a entender el fenómeno de la Resonancia magnética debemos considerar cuales son las propiedades que poseen los núcleos
ESPECTROSCOPIA INFRARROJA INTERPRETACIÓN BÁSICA Y TABLAS
 ESPECTROSCOPIA INFRARROJA INTERPRETACIÓN BÁSICA Y TABLAS RESONANCIA MAGNÉTICA PROTÓNICA REGLAS BÁSICAS DE INTERPRETACIÓN Y TABLAS REGLAS BÁSICAS DE INTERPRETACIÓN DE RESONANCIA MAGNÉTICA PROTÓNICA
ESPECTROSCOPIA INFRARROJA INTERPRETACIÓN BÁSICA Y TABLAS RESONANCIA MAGNÉTICA PROTÓNICA REGLAS BÁSICAS DE INTERPRETACIÓN Y TABLAS REGLAS BÁSICAS DE INTERPRETACIÓN DE RESONANCIA MAGNÉTICA PROTÓNICA
PRÁCTICA DE ESPECTROSCOPIA INFRARROJA
 PRÁCTICA DE ESPECTROSCOPIA INFRARROJA PREPARACIÓN DE MUESTRAS Tu profesor te enseñará el manejo del equipo de infrarrojo y las técnicas de preparación de muestra: disolución, película, pastilla, y suspensión.
PRÁCTICA DE ESPECTROSCOPIA INFRARROJA PREPARACIÓN DE MUESTRAS Tu profesor te enseñará el manejo del equipo de infrarrojo y las técnicas de preparación de muestra: disolución, película, pastilla, y suspensión.
Resonancia Magnética Nuclear
 RMN 01 MÉTODOS ESPECTROSCÓPICOS APLICADOS A DETERMINACIÓN DE ESTRUCTURAS MOLECULARES Resonancia Magnética Nuclear Resonancia Magnética Nuclear Espectroscopía de RMN es una forma de espectroscopia de Absorción.
RMN 01 MÉTODOS ESPECTROSCÓPICOS APLICADOS A DETERMINACIÓN DE ESTRUCTURAS MOLECULARES Resonancia Magnética Nuclear Resonancia Magnética Nuclear Espectroscopía de RMN es una forma de espectroscopia de Absorción.
Resonancia Magnética Nuclear
 Resonancia Magnética Nuclear Por qué algunas señales aparecen como señales múltiples (multipletes)? Dos átomos que se encuentren contiguos interaccionan modificándose mutuamente. La forma de la señal depende
Resonancia Magnética Nuclear Por qué algunas señales aparecen como señales múltiples (multipletes)? Dos átomos que se encuentren contiguos interaccionan modificándose mutuamente. La forma de la señal depende
Temario: Temario: SEMINARIO1 hora lectiva (2 grupos) martes y jueves. SEMINARIO1 hora lectiva (2 grupos) martes y jueves
 PROFESORES PARTICIPANTES: DRA. CAROLINA JULLIAN M. DR. ERNAN PESSOA M. COORDINADOR CATEDRA 2 horas lectivas SEMINARIO1 hora lectiva (2 grupos) martes y jueves Temario: ESPECTROSCOPIA NOMENCLATURA ESTRUCTURA
PROFESORES PARTICIPANTES: DRA. CAROLINA JULLIAN M. DR. ERNAN PESSOA M. COORDINADOR CATEDRA 2 horas lectivas SEMINARIO1 hora lectiva (2 grupos) martes y jueves Temario: ESPECTROSCOPIA NOMENCLATURA ESTRUCTURA
DETERMINACIÓN ESTRUCTURAL (Teoría) CURSO , GRUP A 9 de febrero Apellidos... Nombre...
 DETERMINAIÓN ESTRUTURAL (Teoría) URS 2003-2004, GRUP A 9 de febrero 2004 Apellidos... Nombre... 1.- Que diferencias espera encontrar entre el 3 - y el 3 -D. a) en sus espectros de masas. El ión molecular
DETERMINAIÓN ESTRUTURAL (Teoría) URS 2003-2004, GRUP A 9 de febrero 2004 Apellidos... Nombre... 1.- Que diferencias espera encontrar entre el 3 - y el 3 -D. a) en sus espectros de masas. El ión molecular
VIBRACIONES CARACTERÍSTICAS DE ALGUNAS DE LAS FUNCIONES QUÍMICA-ORGÁNICAS MÁS IMPORTANTES.
 VIBRACIONES CARACTERÍSTICAS DE ALGUNAS DE LAS FUNCIONES QUÍMICA-ORGÁNICAS MÁS IMPORTANTES. ALCANOS NORMALES (LINEALES) En todos los alcanos normales o ramificados se espera encontrar solo estiramientos
VIBRACIONES CARACTERÍSTICAS DE ALGUNAS DE LAS FUNCIONES QUÍMICA-ORGÁNICAS MÁS IMPORTANTES. ALCANOS NORMALES (LINEALES) En todos los alcanos normales o ramificados se espera encontrar solo estiramientos
Espectrometría de Masa
 Espectrometría de Masa La espectrometría de masa crea partículas cargadas (iones). Luego estos iones se analizan y pueden entregar información sobre el peso molecular de la molécula y acerca de su estructura
Espectrometría de Masa La espectrometría de masa crea partículas cargadas (iones). Luego estos iones se analizan y pueden entregar información sobre el peso molecular de la molécula y acerca de su estructura
Constantes de Acoplamiento
 Metodologías para la determinación estructural de fármacos y el estudio de fenómenos de reconocimiento molecular Programa de doctorado en Química Médica Constantes de Acoplamiento Ana Ramos Acoplamiento
Metodologías para la determinación estructural de fármacos y el estudio de fenómenos de reconocimiento molecular Programa de doctorado en Química Médica Constantes de Acoplamiento Ana Ramos Acoplamiento
Trabajo Practico nº2
 Trabajo Practico nº2 Espectroscopía de Resonancia Paramagnética Electrónica (RPE). Introducción La Resonancia Paramagnética Electrónica (RPE, en inglés EPR: Electron Paramagnetic Resonance) es una técnica
Trabajo Practico nº2 Espectroscopía de Resonancia Paramagnética Electrónica (RPE). Introducción La Resonancia Paramagnética Electrónica (RPE, en inglés EPR: Electron Paramagnetic Resonance) es una técnica
ESPECTROSCOPÍA EJEMPLOS DE ELUCIDACION ESTRUCTURAL DE COMPUESTOS. Elucidación estructural: Ejemplo 1 Dados los siguientes espectros:
 ESPECTROSCOPÍA EJEMPLOS DE ELUCIDACION ESTRUCTURAL DE COMPUESTOS Elucidación estructural: Ejemplo 1 Dados los siguientes espectros: 1) Empezaremos por encontrar la formula molecular, pues no la tenemos.
ESPECTROSCOPÍA EJEMPLOS DE ELUCIDACION ESTRUCTURAL DE COMPUESTOS Elucidación estructural: Ejemplo 1 Dados los siguientes espectros: 1) Empezaremos por encontrar la formula molecular, pues no la tenemos.
TALLER DE ESPECTROSCOPIA
 TALLER DE ESPECTROSCOPIA I. OBJETIVOS a) Conocer los principios fundamentales que rigen la interacción energía-materia (radiación electromagnética-moléculas) en uno de los métodos espectroscópicos más
TALLER DE ESPECTROSCOPIA I. OBJETIVOS a) Conocer los principios fundamentales que rigen la interacción energía-materia (radiación electromagnética-moléculas) en uno de los métodos espectroscópicos más
CALCULO DEL INDICE DE DEFICIENCIA DE HIDRÓGENOS IDH.
 Pag:1 CALCULO DEL INDICE DE DEFICIENCIA DE HIDRÓGENOS IDH. En química orgánica, el índice de deficiencia de hidrógeno (IDH) es utilizado para ayudar a dibujar estructuras químicas. La fórmula permite determinar
Pag:1 CALCULO DEL INDICE DE DEFICIENCIA DE HIDRÓGENOS IDH. En química orgánica, el índice de deficiencia de hidrógeno (IDH) es utilizado para ayudar a dibujar estructuras químicas. La fórmula permite determinar
Espectro Electromagnético
 Espectro Electromagnético En las moléculas orgánicas se observan vibraciones moleculares con energías que corresponden a la porción del infrarrojo del espectro electromagnético. Describiendo de la forma
Espectro Electromagnético En las moléculas orgánicas se observan vibraciones moleculares con energías que corresponden a la porción del infrarrojo del espectro electromagnético. Describiendo de la forma
Espectrometría de luminiscencia molecular Cap.15
 Espectrometría de luminiscencia molecular Cap.15 Luz cuyo origen no radica exclusivamente en las altas temperaturas Se da en sustancias que pueden absorber energía, excitándose a niveles mayores y emitirla
Espectrometría de luminiscencia molecular Cap.15 Luz cuyo origen no radica exclusivamente en las altas temperaturas Se da en sustancias que pueden absorber energía, excitándose a niveles mayores y emitirla
Espectro Electromagnético
 1 Espectro Electromagnético La luz es radiación electromagnética y está compuesta por una parte eléctrica y otra magnética. Las particulas subatómicas, electrones y fotones, tienen propiedades de partículas
1 Espectro Electromagnético La luz es radiación electromagnética y está compuesta por una parte eléctrica y otra magnética. Las particulas subatómicas, electrones y fotones, tienen propiedades de partículas
CALCULO DEL INDICE DE DEFICIENCIA DE HIDRÓGENOS IDH.
 Pag:1 Ya hemos visto cómo podemos averiguar la fórmula empírica y molecular de un compuesto. En este tema conoceremos varias técnicas analíticas que combinadas nos podrán ayudar a identificar la fórmula
Pag:1 Ya hemos visto cómo podemos averiguar la fórmula empírica y molecular de un compuesto. En este tema conoceremos varias técnicas analíticas que combinadas nos podrán ayudar a identificar la fórmula
Estructura y reactividad
 Universidad Nacional de uyo QUÍMIA OGÁNIA Estructura y reactividad Efectos sobre la reactividad (Efectos inductivos, estéricos y de resonancia) Análisis de efectos sobre las estructuras de compuestos orgánicos.
Universidad Nacional de uyo QUÍMIA OGÁNIA Estructura y reactividad Efectos sobre la reactividad (Efectos inductivos, estéricos y de resonancia) Análisis de efectos sobre las estructuras de compuestos orgánicos.
Práctica 5 APLICACIONES DE LA ESPECTROSCOPÍA DE RESONANCIA MAGNÉTICA NUCLEAR
 Práctica 5 APLICACIONES DE LA ESPECTROSCOPÍA DE RESONANCIA MAGNÉTICA NUCLEAR 1. Objetivo El objetivo de la presente práctica es la identificación cualitativa de compuestos orgánicos mediante la técnica
Práctica 5 APLICACIONES DE LA ESPECTROSCOPÍA DE RESONANCIA MAGNÉTICA NUCLEAR 1. Objetivo El objetivo de la presente práctica es la identificación cualitativa de compuestos orgánicos mediante la técnica
TABLA 1- Desplazamientos químicos (δ) de protones de metilos, metilenos y metinos de alcanos monosustituidos con sustituyentes x en posición α
 TABLA 1- Desplazamientos químicos (δ) de protones de metilos, metilenos y metinos de alcanos monosustituidos con sustituyentes x en posición α alógeno N S --N X 3 X 2 X - 3,- 2-0,86 0,91 1,25 1,33 1,50
TABLA 1- Desplazamientos químicos (δ) de protones de metilos, metilenos y metinos de alcanos monosustituidos con sustituyentes x en posición α alógeno N S --N X 3 X 2 X - 3,- 2-0,86 0,91 1,25 1,33 1,50
Práctica 6 IDENTIFICACIÓN DE CONTAMINANTES MEDIANTE ESPECTROSCOPÍA INFRARROJA
 Práctica 6 IDENTIFICACIÓN DE CONTAMINANTES MEDIANTE ESPECTROSCOPÍA INFRARROJA 1. Objetivo Familiarizarse con los fundamentos de la identificación de moléculas a partir de su espectro de absorción infrarrojo.
Práctica 6 IDENTIFICACIÓN DE CONTAMINANTES MEDIANTE ESPECTROSCOPÍA INFRARROJA 1. Objetivo Familiarizarse con los fundamentos de la identificación de moléculas a partir de su espectro de absorción infrarrojo.
ESTRUCTURA DE LA MATERIA
 ESTRUCTURA DE LA MATERIA 1. Naturaleza de la materia (el átomo). 2. Modelos atómicos clásicos. 3. Modelo mecánico cuántico. 4. Mecánica ondulatoria de Schrödinger. 5. Números cuánticos. 6. Orbitales atómicos.
ESTRUCTURA DE LA MATERIA 1. Naturaleza de la materia (el átomo). 2. Modelos atómicos clásicos. 3. Modelo mecánico cuántico. 4. Mecánica ondulatoria de Schrödinger. 5. Números cuánticos. 6. Orbitales atómicos.
Problemas. Módulo 2. Espectroscopía de IR y RMN
 Problemas. Módulo 2. Espectroscopía de IR y RMN 1. Dadas las estructuras de cinco isómeros de fórmula molecular C 4 H 8 Oy los espectros IR identificados como A, B, C, D y E, indique de manera razonada
Problemas. Módulo 2. Espectroscopía de IR y RMN 1. Dadas las estructuras de cinco isómeros de fórmula molecular C 4 H 8 Oy los espectros IR identificados como A, B, C, D y E, indique de manera razonada
Interacción materia-radiación
 Interacción materia-radiación 1. Indicar en qué zona del espectro electromagnético aparece cada uno de los tránsitos siguientes: a) 3000 cm -1 ; b) 100 Kcal/mol; c) 3.3 10-1 ergios y d) 6 10 9 sg 1.. ierto
Interacción materia-radiación 1. Indicar en qué zona del espectro electromagnético aparece cada uno de los tránsitos siguientes: a) 3000 cm -1 ; b) 100 Kcal/mol; c) 3.3 10-1 ergios y d) 6 10 9 sg 1.. ierto
ESPECTROMETRIA DE MASAS
 ESPECTROMETRIA DE MASAS Utilizando la espectrometría de masas (EM) podemos conocer la masa de una molécula. Ademas podemos obtener información sobre esa misma molécula utilizando una muestra mínima. Aunque
ESPECTROMETRIA DE MASAS Utilizando la espectrometría de masas (EM) podemos conocer la masa de una molécula. Ademas podemos obtener información sobre esa misma molécula utilizando una muestra mínima. Aunque
FACTORES QUE AFECTAN AL DESPLAZAMIENTO QUIMICO (δ) EN RMN PROTÓNICA. Los principales factores que afectan al desplazamiento químico son:
 Elucidación estructural: Resonancia Magnética Nuclear (desplazamiento de 1 H) FACTORES QUE AFECTAN AL DESPLAZAMIENTO QUIMICO (δ) EN RMN PROTÓNICA Los principales factores que afectan al desplazamiento
Elucidación estructural: Resonancia Magnética Nuclear (desplazamiento de 1 H) FACTORES QUE AFECTAN AL DESPLAZAMIENTO QUIMICO (δ) EN RMN PROTÓNICA Los principales factores que afectan al desplazamiento
PARTÍCULAS FUNDAMENTALES. NÚMEROS CUÁNTICOS. PROPIEDADES PERIÓDICAS.
 PARTÍCULAS FUNDAMENTALES. NÚMEROS CUÁNTICOS. PROPIEDADES PERIÓDICAS. PARTÍCULAS FUNDAMENTALES. CONCEPTOS PREVIOS De acuerdo con lo anterior, en un átomo hay tres partículas fundamentales: protones y neutrones,
PARTÍCULAS FUNDAMENTALES. NÚMEROS CUÁNTICOS. PROPIEDADES PERIÓDICAS. PARTÍCULAS FUNDAMENTALES. CONCEPTOS PREVIOS De acuerdo con lo anterior, en un átomo hay tres partículas fundamentales: protones y neutrones,
La espectroscopia de resonanc resonan ia magnética nuclear (RMN) es un fenóme fenóm no
 Resonancia Magnética Nuclear de Sólidos y su aplicación ala caracterización de polímeros Carlos García Aparicio Madrid, 2012 La espectroscopia de resonancia magnética nuclear (RMN) es un fenómeno que ocurre
Resonancia Magnética Nuclear de Sólidos y su aplicación ala caracterización de polímeros Carlos García Aparicio Madrid, 2012 La espectroscopia de resonancia magnética nuclear (RMN) es un fenómeno que ocurre
Los átomos constituyen la unidad básica de todos los materiales de ingeniería. La estructura de los átomos Están constituidos por las siguientes partí
 Capítulo 2: Estructura atómica Los átomos constituyen la unidad básica de todos los materiales de ingeniería. La estructura de los átomos Están constituidos por las siguientes partículas subatómicas: Protones
Capítulo 2: Estructura atómica Los átomos constituyen la unidad básica de todos los materiales de ingeniería. La estructura de los átomos Están constituidos por las siguientes partículas subatómicas: Protones
UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUÍMICAS
 UNIVERSIDAD CENTRAL DEL ECUADR FACULTAD DE CIENCIAS QUÍMICAS ÉTERES Y EPÓXIDS Cazar Irina Lenin Lombeida 12 de Julio del 2011 QUIMICA RGANICA II TEMA: QUIMICA RGANICA FRANCIS CAREY: EJERCICIS DE ÉTERES
UNIVERSIDAD CENTRAL DEL ECUADR FACULTAD DE CIENCIAS QUÍMICAS ÉTERES Y EPÓXIDS Cazar Irina Lenin Lombeida 12 de Julio del 2011 QUIMICA RGANICA II TEMA: QUIMICA RGANICA FRANCIS CAREY: EJERCICIS DE ÉTERES
Los compuestos del Carbono
 Los compuestos del Carbono Segunda fila de la Tabla Periódica El átomo de carbono está en el medio de la fila y en realidad no cede ni acepta electrones. Comparte sus electrones con otros carbonos al igual
Los compuestos del Carbono Segunda fila de la Tabla Periódica El átomo de carbono está en el medio de la fila y en realidad no cede ni acepta electrones. Comparte sus electrones con otros carbonos al igual
Tema 6. Espectroscopia para el estudio de la materia
 Tema 6. Espectroscopia para el estudio de la materia 1. Introducción. Naturaleza dual de la radiación y la materia 2. Interacción Radiación-materia. Ley de Lambert-Beer 3. Espectroscopía InfraRojo 4. Espectroscopía
Tema 6. Espectroscopia para el estudio de la materia 1. Introducción. Naturaleza dual de la radiación y la materia 2. Interacción Radiación-materia. Ley de Lambert-Beer 3. Espectroscopía InfraRojo 4. Espectroscopía
TUTORIAL PARA LA INTERPRETACIÓN DE ESPECTROS DE RESONANCIA MAGNÉTICA NUCLEAR DE PROTÓN.
 9 8 7 6 5 4 3 1 0 TUTRIAL PARA LA INTERPRETACIÓN DE ESPECTRS DE RESNANCIA MAGNÉTICA NUCLEAR DE PRTÓN. Juan A. Palop Tutorial para la interpretación de espectros de Resonancia Magnética Nuclear de protón
9 8 7 6 5 4 3 1 0 TUTRIAL PARA LA INTERPRETACIÓN DE ESPECTRS DE RESNANCIA MAGNÉTICA NUCLEAR DE PRTÓN. Juan A. Palop Tutorial para la interpretación de espectros de Resonancia Magnética Nuclear de protón
Tema 14 11/02/2005. Tema 8. Mecánica Cuántica. 8.1 Fundamentos de la mecánica cuántica
 Tema 14 11/0/005 Tema 8 Mecánica Cuántica 8.1 Fundamentos de la mecánica cuántica 8. La ecuación de Schrödinger 8.3 Significado físico de la función de onda 8.4 Soluciones de la ecuación de Schrödinger
Tema 14 11/0/005 Tema 8 Mecánica Cuántica 8.1 Fundamentos de la mecánica cuántica 8. La ecuación de Schrödinger 8.3 Significado físico de la función de onda 8.4 Soluciones de la ecuación de Schrödinger
El electrón. Naturaleza. Distribución de los electrones en el átomo. Química General I
 El electrón. Naturaleza. Distribución de los electrones en el átomo. Química General I Atención Leer del libro Química de Chang 10ma edición. Capítulo 7, págs 288 a 294. Ojo, la lectura es para ubicarse
El electrón. Naturaleza. Distribución de los electrones en el átomo. Química General I Atención Leer del libro Química de Chang 10ma edición. Capítulo 7, págs 288 a 294. Ojo, la lectura es para ubicarse
Los reactivos pueden clasificarse por sus características y formas de reaccionar:
 La Reacción Química En Química Orgánica El objetivo de esta guía es enseñarte a comprender las reacciones químicas estudiadas desde el punto de vista de la química orgánica. Este enfoque es diferente a
La Reacción Química En Química Orgánica El objetivo de esta guía es enseñarte a comprender las reacciones químicas estudiadas desde el punto de vista de la química orgánica. Este enfoque es diferente a
Tema 7: Espectroscopia Vibracional (IR)
 Tabla 1. El espectro electromagnético Región Longitud de onda Energía de excitación Tipo de excitación Rayos x, rayos cósmicos 286 (Kcal/mol) Ultravioleta Visible Infrarrojo próximo Infrarrojo
Tabla 1. El espectro electromagnético Región Longitud de onda Energía de excitación Tipo de excitación Rayos x, rayos cósmicos 286 (Kcal/mol) Ultravioleta Visible Infrarrojo próximo Infrarrojo
El electrón. Naturaleza. Distribución de los electrones en el átomo. Química General I 2012
 El electrón. Naturaleza. Distribución de los electrones en el átomo. Química General I 2012 Atención Leer del libro Química de Chang 10ma edición. Capítulo 7, págs 288 a 294. Ojo, la lectura es para ubicarse
El electrón. Naturaleza. Distribución de los electrones en el átomo. Química General I 2012 Atención Leer del libro Química de Chang 10ma edición. Capítulo 7, págs 288 a 294. Ojo, la lectura es para ubicarse
ESPECTROSCOPIA DE RESONANCIA MAGNÉTICA NUCLEAR
 ESPECTROSCOPIA DE RESONANCIA MAGNÉTICA NUCLEAR La espectroscopia de resonancia magnética nuclear (RMN) se basa en la medida de la absorción de la radiación electromagnética en la región de las radiofrecuencias
ESPECTROSCOPIA DE RESONANCIA MAGNÉTICA NUCLEAR La espectroscopia de resonancia magnética nuclear (RMN) se basa en la medida de la absorción de la radiación electromagnética en la región de las radiofrecuencias
Materiales. Eléctricos. Materiales. Magneticos
 Materiales Eléctricos Materiales Magneticos Propiedades Magnéticas de los Materiales Materiales Eléctricos El magnetismo se manifiesta por la fuerza que se ejerce sobre un conductor con corriente eléctrica
Materiales Eléctricos Materiales Magneticos Propiedades Magnéticas de los Materiales Materiales Eléctricos El magnetismo se manifiesta por la fuerza que se ejerce sobre un conductor con corriente eléctrica
1.- Fundamentos básicos
 1.- Fundamentos básicos - Algunos núcleos tienen espín: La circulación de carga genera un campo magnético a lo largo del eje de giro ( 1 H, 7 Li, 11 B, 13 C, 14 N, 19 F, 23 Na, 27 Al, 29 Si, 31 P, 33 S,
1.- Fundamentos básicos - Algunos núcleos tienen espín: La circulación de carga genera un campo magnético a lo largo del eje de giro ( 1 H, 7 Li, 11 B, 13 C, 14 N, 19 F, 23 Na, 27 Al, 29 Si, 31 P, 33 S,
Teoría del Enlace de Orbitales Moleculares (TOM)
 Teoría del Enlace de Orbitales Moleculares (TOM) Conceptos Fundamentales: Combinación Lineal de Orbitales Atómicos: CLOA Moléculas diatómicas sencillas homonucleares: OM enlazantes y antienlazantes. OM
Teoría del Enlace de Orbitales Moleculares (TOM) Conceptos Fundamentales: Combinación Lineal de Orbitales Atómicos: CLOA Moléculas diatómicas sencillas homonucleares: OM enlazantes y antienlazantes. OM
UNIVERSIDAD NACIONAL DEL SUR 1
 UNIVERSIDAD NACIONAL DEL SUR 1 PROGRAMA DE: CODIGO: 393 H O R A S D E C L A S E P R O F E S O R R E S P O N S A B L E T E O R I C A S P R A C T I C A S Dra. Alicia B. Chopa Por semana Por cuatrimestre
UNIVERSIDAD NACIONAL DEL SUR 1 PROGRAMA DE: CODIGO: 393 H O R A S D E C L A S E P R O F E S O R R E S P O N S A B L E T E O R I C A S P R A C T I C A S Dra. Alicia B. Chopa Por semana Por cuatrimestre
UNIVERSIDAD DE PUERTO RICO RECINTO DE RÍO PIEDRAS DEPARTAMENTO DE QUÍMICA QUÍMICA ORGÁNICA II (QUIM 3032)
 QUÍMICA RGÁNICA II (QUIM 3032) PRIMER EXAMEN PARCIAL UNIVERSIDAD DE PUERT RIC RECINT DE RÍ PIEDRAS DEPARTAMENT DE QUÍMICA 25 DE FEBRER DE 2016 SECCIÓN: NMBRE: NÚM. DE ESTUDIANTE: El examen consta de 13
QUÍMICA RGÁNICA II (QUIM 3032) PRIMER EXAMEN PARCIAL UNIVERSIDAD DE PUERT RIC RECINT DE RÍ PIEDRAS DEPARTAMENT DE QUÍMICA 25 DE FEBRER DE 2016 SECCIÓN: NMBRE: NÚM. DE ESTUDIANTE: El examen consta de 13
Resonancia Magnética Nuclear
 Víctor Moreno de la Cita Jesús J. Fernández Romero 25 de mayo de 2010 1 Base teórica 2 Medicina Química y análisis no destructivo Computación cuántica 3 4 Notación que emplea Kittel: µ = Momento magnético
Víctor Moreno de la Cita Jesús J. Fernández Romero 25 de mayo de 2010 1 Base teórica 2 Medicina Química y análisis no destructivo Computación cuántica 3 4 Notación que emplea Kittel: µ = Momento magnético
ESPECTROSCOPIA INFRARROJA. Prof. Dr. Alberto Postigo
 ESPECTROSCOPIA INFRARROJA Prof. Dr. Alberto Postigo 1 2 Transición energética en el IR 3 A.-TEORIA DE LA ESPECTROSCOPIA IR (cm 1 ) = 1 (cm) (z) = c (cm) = c (cm/sec) (cm) cm 1 = 1 ( ) x 10,000 and = 1-1
ESPECTROSCOPIA INFRARROJA Prof. Dr. Alberto Postigo 1 2 Transición energética en el IR 3 A.-TEORIA DE LA ESPECTROSCOPIA IR (cm 1 ) = 1 (cm) (z) = c (cm) = c (cm/sec) (cm) cm 1 = 1 ( ) x 10,000 and = 1-1
BIOLOGIA. Unidad 0.- Conceptos básicos de química para biología. - Los átomos constituyen la unidad más pequeña de la materia ( aprox cm).
 .- Conceptos básicos de química para biología. 1. Los átomos. - Los átomos constituyen la unidad más pequeña de la materia ( aprox. 10-8 cm). - Los átomos están formados por partículas sub-atómicas denominadas
.- Conceptos básicos de química para biología. 1. Los átomos. - Los átomos constituyen la unidad más pequeña de la materia ( aprox. 10-8 cm). - Los átomos están formados por partículas sub-atómicas denominadas
NOMENCLATURA PARA LA CARACTERIZACIÓN EN R.M.N.
 NOMENLATURA PARA LA ARATERIZAIÓN EN R.M.N. El número de señales que va a aparecer en un espectro de resonancia magnética nuclear va a depender de la simetría de la molécula que estemos investigando. Equivalencia
NOMENLATURA PARA LA ARATERIZAIÓN EN R.M.N. El número de señales que va a aparecer en un espectro de resonancia magnética nuclear va a depender de la simetría de la molécula que estemos investigando. Equivalencia
UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUIMICAS QUÍMICA ORGÁNICA III ACIDOS CARBOXILICOS
 Nombre: Mayra Morales Carrera: Bioquímica y Farmacia ACIDEZ UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUIMICAS QUÍMICA ORGÁNICA III ACIDOS CARBOXILICOS Los ácidos carboxílicos son compuestos
Nombre: Mayra Morales Carrera: Bioquímica y Farmacia ACIDEZ UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUIMICAS QUÍMICA ORGÁNICA III ACIDOS CARBOXILICOS Los ácidos carboxílicos son compuestos
Prefacio... ix COMO UTILIZAR ESTE LIBRO... 1 QUE ES LA QUIMICA... 2 EL METODO CIENTIFICO... 3 LAS RAMAS DE LA QUIMICA... 3
 ÍNDICE Prefacio... ix 1 introducción a la química... 1 COMO UTILIZAR ESTE LIBRO... 1 QUE ES LA QUIMICA... 2 EL METODO CIENTIFICO... 3 LAS RAMAS DE LA QUIMICA... 3 2 el sistema métrico y la medición científica...
ÍNDICE Prefacio... ix 1 introducción a la química... 1 COMO UTILIZAR ESTE LIBRO... 1 QUE ES LA QUIMICA... 2 EL METODO CIENTIFICO... 3 LAS RAMAS DE LA QUIMICA... 3 2 el sistema métrico y la medición científica...
QUÍMICA ORGÁNICA SERIE DE EJERCICIOS Nº3 HALUROS DE ALQUILO,MÉTODOS DE ESTUDIO MOLÉCULAS, COMPUESTOS AROMÁTICOS
 QUÍMICA ORGÁNICA SERIE DE EJERCICIOS Nº3 HALUROS DE ALQUILO,MÉTODOS DE ESTUDIO MOLÉCULAS, COMPUESTOS AROMÁTICOS 1. Considerando que la reacción de 1-yodo-2-metilbutano cn CN - es de tipo SN2, indicar cómo
QUÍMICA ORGÁNICA SERIE DE EJERCICIOS Nº3 HALUROS DE ALQUILO,MÉTODOS DE ESTUDIO MOLÉCULAS, COMPUESTOS AROMÁTICOS 1. Considerando que la reacción de 1-yodo-2-metilbutano cn CN - es de tipo SN2, indicar cómo
Enlace Covalente: Contenidos
 Introducción Teoría de Lewis. Regla del cteto Estrategia para la formulación de estructuras de Lewis. Carga formal sobre un átomo. Concepto de resonancia. Excepciones a la regla del octeto. Geometría molecular
Introducción Teoría de Lewis. Regla del cteto Estrategia para la formulación de estructuras de Lewis. Carga formal sobre un átomo. Concepto de resonancia. Excepciones a la regla del octeto. Geometría molecular
Movimiento vibracional
 ESPECTROSCOPÍA Movimiento vibracional El oscilador armónico como modelo de la vibración molecular Los sistemas que vibran a nivel molecular incluyen las vibraciones internas de una molécula y las vibraciones
ESPECTROSCOPÍA Movimiento vibracional El oscilador armónico como modelo de la vibración molecular Los sistemas que vibran a nivel molecular incluyen las vibraciones internas de una molécula y las vibraciones
QUÍMICA DEL CARBONO 1. El carbono. 2. Grupos funcionales. 3. Isomería. 4. Compuestos orgánicos.
 QUÍMICA DEL CARBONO 1. El carbono. 2. Grupos funcionales. 3. Isomería. 4. Compuestos orgánicos. Química 1º bachillerato Química del carbono 1 1. EL CARBONO El carbono es una molécula muy especial capaz
QUÍMICA DEL CARBONO 1. El carbono. 2. Grupos funcionales. 3. Isomería. 4. Compuestos orgánicos. Química 1º bachillerato Química del carbono 1 1. EL CARBONO El carbono es una molécula muy especial capaz
TEMA 5 ESPECTROSCOPÍA Y ESTRUCTURA
 Tema 5. Espectroscopía y estructura TEMA 5 ESPECTROSCOPÍA Y ESTRUCTURA 1. Definición de espectroscopía. 2. Espectroscopía de infrarrojo. 3. Resonancia magnética nuclear. 4. Resonancia magnética nuclear
Tema 5. Espectroscopía y estructura TEMA 5 ESPECTROSCOPÍA Y ESTRUCTURA 1. Definición de espectroscopía. 2. Espectroscopía de infrarrojo. 3. Resonancia magnética nuclear. 4. Resonancia magnética nuclear
Tema 11. CONCEPTOS FUNDAMENTALES EN QUÍMICA ORGÁNICA
 Tema 11. EPTS FUDAMETALES E QUÍMIA RGÁIA o metales con electronegatividad similar (,,, ). Uniones covalentes debilmente polares o apolares Reactividad: interacciones entre áreas o zonas de las moléculas
Tema 11. EPTS FUDAMETALES E QUÍMIA RGÁIA o metales con electronegatividad similar (,,, ). Uniones covalentes debilmente polares o apolares Reactividad: interacciones entre áreas o zonas de las moléculas
Tema 9. Química Orgánica
 Tema 9. Química Orgánica ÍNDICE 1. Enlace covalente en las moléculas orgánicas 1.1. ibridaciones del carbono 1.2. Resonancia 1.3. Polaridad de enlace 2. Representación de moléculas orgánicas 3. idrocarburos
Tema 9. Química Orgánica ÍNDICE 1. Enlace covalente en las moléculas orgánicas 1.1. ibridaciones del carbono 1.2. Resonancia 1.3. Polaridad de enlace 2. Representación de moléculas orgánicas 3. idrocarburos
γ 13 C = C RMN H = ν = H o H 0 (T) ν 1 H RMN (MHz)* ν 13 C RMN (MHz)
 RMN I = 0 No observable en RMN I = ½ BSERVABLE EN RMN Abundancia natural del =.% Sensibilidad INTENSIDAD DE LAS SEÑALES RMN se basa en los mismos principios que RMN: utilizando una RF adecuada (o un pulso
RMN I = 0 No observable en RMN I = ½ BSERVABLE EN RMN Abundancia natural del =.% Sensibilidad INTENSIDAD DE LAS SEÑALES RMN se basa en los mismos principios que RMN: utilizando una RF adecuada (o un pulso
Diasterómeros ó diasteroisómeros
 Diasterómeros ó diasteroisómeros Estereoisómeros que no son imágenes especulares Isomería cis-trans en dobles enlaces -Isómeros cis-trans -ompuestos con dos ó más centros quirales No son imágenes especulares
Diasterómeros ó diasteroisómeros Estereoisómeros que no son imágenes especulares Isomería cis-trans en dobles enlaces -Isómeros cis-trans -ompuestos con dos ó más centros quirales No son imágenes especulares
UNIVERSIDA CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUIMCAS CARRERA DE QUIMICA FARMACEUTICA QUIMICA ORGANICA III
 Nombre: Laura Cadena Fecha: 26 de junio del 2011 Tema: UNIVERSIDA CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUIMCAS CARRERA DE QUIMICA FARMACEUTICA QUIMICA ORGANICA III FACOTRES QUE AFECTAN LA ACIDEZ DE
Nombre: Laura Cadena Fecha: 26 de junio del 2011 Tema: UNIVERSIDA CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUIMCAS CARRERA DE QUIMICA FARMACEUTICA QUIMICA ORGANICA III FACOTRES QUE AFECTAN LA ACIDEZ DE
DETERMINACIÓN ESTRUCTURAL GUÍA DOCENTE CURSO
 Curso 204-5 DETERMINACIÓN ESTRUCTURAL GUÍA DOCENTE CURSO 204-5 Titulación: 703G Asignatura: Determinación estructural 542 Materia: Determinación estructural Módulo: Intensificación en química enológica
Curso 204-5 DETERMINACIÓN ESTRUCTURAL GUÍA DOCENTE CURSO 204-5 Titulación: 703G Asignatura: Determinación estructural 542 Materia: Determinación estructural Módulo: Intensificación en química enológica
Asignaturas antecedentes y subsecuentes
 PROGRAMA DE ESTUDIOS Elucidación de Estructuras Moleculares Área a la que pertenece: AREA DE FORMACIÓN INTEGRAL PROFESIONAL Horas teóricas: 3 Horas practicas: 4 Créditos: 10 Clave: F0232 Ninguna. Asignaturas
PROGRAMA DE ESTUDIOS Elucidación de Estructuras Moleculares Área a la que pertenece: AREA DE FORMACIÓN INTEGRAL PROFESIONAL Horas teóricas: 3 Horas practicas: 4 Créditos: 10 Clave: F0232 Ninguna. Asignaturas
Medicina Veterinaria. Parte I
 Medicina Veterinaria QUÍMICA ORGÁNICA Parte I Moléculas Polares y No Polares Moléculas No Polares: Los electrones están distribuidos simétricamente en la molécula y el centro de las cargas eléctricas coincide
Medicina Veterinaria QUÍMICA ORGÁNICA Parte I Moléculas Polares y No Polares Moléculas No Polares: Los electrones están distribuidos simétricamente en la molécula y el centro de las cargas eléctricas coincide
HIDROCARBUROS AROMÁTICOS
 HIDROCARBUROS AROMÁTICOS Los hidrocarburos aromáticos son compuestos insaturados de un tipo especial. Originalmente recibieron el nombre de aromáticos debido al aroma que algunos poseen. Sin embargo no
HIDROCARBUROS AROMÁTICOS Los hidrocarburos aromáticos son compuestos insaturados de un tipo especial. Originalmente recibieron el nombre de aromáticos debido al aroma que algunos poseen. Sin embargo no
Espectroscopía de Masas (MS) M +. Espectrometría de masas (MS) Esquema general y concepto (1) Esquema general y concepto (3)
 Espectrometría de masas (MS) Espectroscopía de Masas (MS) * Es una técnica analítica basada en la posibilidad de separar especies moleculares (y atómicas) según su masa * Es aplicable para el análisis
Espectrometría de masas (MS) Espectroscopía de Masas (MS) * Es una técnica analítica basada en la posibilidad de separar especies moleculares (y atómicas) según su masa * Es aplicable para el análisis
ESTRUCTURAS DE RESONANCIA
 1 ESTRUCTURAS DE RESONANCIA HIBRIDOS DE RESONANCIA CUANDO SON POSIBLES DOS O MÁS ESTRUCTURAS PARA REPRESENTAR LOS ENLACES DE UNA MOLÉCULA Y SÓLO DIFIENREN EN LA COLOCACIÓN DE LOS ELECTRONES LA MOLÉCULA
1 ESTRUCTURAS DE RESONANCIA HIBRIDOS DE RESONANCIA CUANDO SON POSIBLES DOS O MÁS ESTRUCTURAS PARA REPRESENTAR LOS ENLACES DE UNA MOLÉCULA Y SÓLO DIFIENREN EN LA COLOCACIÓN DE LOS ELECTRONES LA MOLÉCULA
UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUIMICAS QUIMICA DE ALIMENTOS. Factores que afectan la acidez de los ácidos carboxílicos.
 NOMBRE: Diana Jiménez UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUIMICAS QUIMICA DE ALIMENTOS ACIDOS CARBOXILICOS. Acidez de los ácidos carboxílicos Factores que afectan la acidez de los ácidos
NOMBRE: Diana Jiménez UNIVERSIDAD CENTRAL DEL ECUADOR FACULTAD DE CIENCIAS QUIMICAS QUIMICA DE ALIMENTOS ACIDOS CARBOXILICOS. Acidez de los ácidos carboxílicos Factores que afectan la acidez de los ácidos
1/27/2013. Átomos con un solo electrón: La energía depende solamente del número cuántico principal (n) n=4 Orbitales degenerados (igual energía) n=3
 ESTRUCTURA ELECTRÓNICA Espín y configuraciones electrónicas Número y masa atómicos (isótopos) Tabla periódica y configuraciones electrónicas Átomos con un solo electrón: La energía depende solamente del
ESTRUCTURA ELECTRÓNICA Espín y configuraciones electrónicas Número y masa atómicos (isótopos) Tabla periódica y configuraciones electrónicas Átomos con un solo electrón: La energía depende solamente del
Átomos polielectrónicos Espín y configuraciones electrónicas Número y masa atómicos (isótopos) Tabla periódica y configuraciones electrónicas
 ESTRUCTURA ELECTRÓNICA Espín y configuraciones electrónicas Número y masa atómicos (isótopos) Tabla periódica y configuraciones electrónicas Átomos con un solo electrón: La energía depende solamente del
ESTRUCTURA ELECTRÓNICA Espín y configuraciones electrónicas Número y masa atómicos (isótopos) Tabla periódica y configuraciones electrónicas Átomos con un solo electrón: La energía depende solamente del
Planificación didáctica de PRUEBA DE ACCESO A: GRADO SUPERIOR
 Planificación didáctica de PRUEBA DE ACCESO A: GRADO SUPERIOR PARTE ESPECÍFICA: OPCIÓN C, QUÍMICA Julio de 2016 Rev.: 0 Índice 1.- CONTENIDOS... 1 1.1.- Teoría atómico-molecular.... 1 1.2.- Modelos atómicos....
Planificación didáctica de PRUEBA DE ACCESO A: GRADO SUPERIOR PARTE ESPECÍFICA: OPCIÓN C, QUÍMICA Julio de 2016 Rev.: 0 Índice 1.- CONTENIDOS... 1 1.1.- Teoría atómico-molecular.... 1 1.2.- Modelos atómicos....
CONTENIDOS MÍNIMOS septiembre
 DEPARTAMENTO DE FÍSICA Y QUÍMICA CONTENIDOS MÍNIMOS septiembre CONTENIDOS MÍNIMOS curso 2015/16 1º BACHILLERATO-FÍSICA Y QUÍMICA QUÍMICA ESTRUCTURA ATÓMICA -Partículas subatómicas. -Modelo atómico de Thompson.
DEPARTAMENTO DE FÍSICA Y QUÍMICA CONTENIDOS MÍNIMOS septiembre CONTENIDOS MÍNIMOS curso 2015/16 1º BACHILLERATO-FÍSICA Y QUÍMICA QUÍMICA ESTRUCTURA ATÓMICA -Partículas subatómicas. -Modelo atómico de Thompson.
ESTRUCTURA ATÓMICA Y PROPIEDADES PERIÓDICAS
 ESTRUCTURA ATÓMICA Y PROPIEDADES PERIÓDICAS 1.- Escriba la configuración electrónica de los siguientes iones o elementos: 8 O -2, 9 F - y 10 Ne, e indique el período y grupo de los elementos correspondientes.
ESTRUCTURA ATÓMICA Y PROPIEDADES PERIÓDICAS 1.- Escriba la configuración electrónica de los siguientes iones o elementos: 8 O -2, 9 F - y 10 Ne, e indique el período y grupo de los elementos correspondientes.
Química Orgánica I. Clase 2.
 Química Orgánica I Clase 2. Enlace Quimico. Teoria de Enlace de Valencia F 2 Enlace Covalente Polar: Enlace donde la densidad electronica esta polarizada hacia uno de los dos atomos. Electronegatividad
Química Orgánica I Clase 2. Enlace Quimico. Teoria de Enlace de Valencia F 2 Enlace Covalente Polar: Enlace donde la densidad electronica esta polarizada hacia uno de los dos atomos. Electronegatividad
ÍNDICE
 ÍNDICE 1 Radiación térmica y el postulado de Planck... 17 1-1 Introducción... 19 1-2 Radiación térmica... 19 1-3 Teoría clásica de la cavidad radiante... 24 1-4 Teoría de Planck de la cavidad radiante...
ÍNDICE 1 Radiación térmica y el postulado de Planck... 17 1-1 Introducción... 19 1-2 Radiación térmica... 19 1-3 Teoría clásica de la cavidad radiante... 24 1-4 Teoría de Planck de la cavidad radiante...
Tema 1 Átomos y Tabla Periódica
 Tema Átomos y Tabla Periódica Tres partículas subatómicas: el protón (carga +), el neutrón (carga = ) y el electrón (carga -) : son las partículas principales que afectan el comportamiento químico de los
Tema Átomos y Tabla Periódica Tres partículas subatómicas: el protón (carga +), el neutrón (carga = ) y el electrón (carga -) : son las partículas principales que afectan el comportamiento químico de los
Química Orgánica y Biológica Apunte
 FUERZAS INTERMOLECULARES El enlace covalente es la unión que explica el mantenimiento de la unidad estructural de un compuesto orgánico. Además de este enlace intramolecular se pueden dar interacciones
FUERZAS INTERMOLECULARES El enlace covalente es la unión que explica el mantenimiento de la unidad estructural de un compuesto orgánico. Además de este enlace intramolecular se pueden dar interacciones
Teoría Básica de RMN. La RMN es otro tipo de Espectroscopía de Absorción
 Teoría Básica de RMN La RMN es otro tipo de Espectroscopía de Absorción Base de la RMN: Absorción de energía por un núcleo atómico que provoca transiciones entre niveles de energía nucleares (o entre distintos
Teoría Básica de RMN La RMN es otro tipo de Espectroscopía de Absorción Base de la RMN: Absorción de energía por un núcleo atómico que provoca transiciones entre niveles de energía nucleares (o entre distintos
SELECCION DE PREGUNTAS REPRESENTATIVAS SOBRE TEMAS DEL MODULO DE
 SELECCION DE PREGUNTAS REPRESENTATIVAS SOBRE TEMAS DEL MODULO DE ESTRUCTURA Y PROPIEDADES MOLECULARES Temas de Mecánica Cuántica y Estructura atómica 1) Cuál es el operador asociado al observable energía,
SELECCION DE PREGUNTAS REPRESENTATIVAS SOBRE TEMAS DEL MODULO DE ESTRUCTURA Y PROPIEDADES MOLECULARES Temas de Mecánica Cuántica y Estructura atómica 1) Cuál es el operador asociado al observable energía,
Espectroscopía Clase integradora
 Espectroscopía Clase integradora Qué es la espectroscopía? La espectroscopia es el estudio de la INTERACCIÓN entre la materia y energía radiante, por ejemplo, radiación electromagnética. Busca relacionar
Espectroscopía Clase integradora Qué es la espectroscopía? La espectroscopia es el estudio de la INTERACCIÓN entre la materia y energía radiante, por ejemplo, radiación electromagnética. Busca relacionar
