CORIFOLITROPINA ALFA (ELONVA / MSD)
|
|
|
- José Ignacio Maestre Correa
- hace 8 años
- Vistas:
Transcripción
1 Presentación CN Jer precargada 100mcg E/1 PVL= 530,41 CN Jer precargada 150mcg E/1 PVL= 530,41 DH/ DISPENSACIÓN HOSPITALARIA. Excipientes Citrato de sodio, sacarosa, polisorbato 20, Metionina, hidróxido de sodio (ajuste ph), ácido clorhídrico (ajuste ph), API CORIFOLITROPINA ALFA (ELONVA / MSD) G03GA Grupo terapéutico GONADOTROFINAS Naturaleza del recipiente Jeringas precargadas de vidrio hidrolítico tipo I, cerradas con un émbolo de elastómero de bromobutilo y una cápsula de cierre. Período de validez Estabilidad 3 años. T 2-8ºC Conservar a una temperatura igual o inferior a 25 C durante un periodo no superior a 1 mes. Solicitado por Dr. Rubio Rubio (Jefe Sección Ginecología Obstetricia) Fecha solicitud 18/05/2011 Fecha autorización en España 18/03/2010 Intercambio terapéutico por/de Folitropina beta Estructura y mecanismo de acción Corifolitropina alfa es una glicoproteína producida en células de ovario de hámster chino (CHO) mediante tecnología DNA recombinante. En este proceso se ha desarrollado una molécula que permite prolongar la acción estimulante folicular (FSH), lo que se ha conseguido añadiendo el 7 péptido carboxi-terminal de la subunidad β de la gonadotropina coriónica humana (hcg) a la cadena β de la FSH Humana. Corifolitropina alfa no presenta ninguna actividad LH/hCG intrínseca 1-4. Página 1 de 8
2 Indicaciones y posología Corifolitropina alfa está indicado para la estimulación ovárica controlada en combinación con un antagonista de la GnRH, para el desarrollo de folículos múltiples en mujeres que participan en un programa de Técnicas de Reproducción Asistida. La dosis usual es de 100mcg y 150 mcg /semana para mujeres con peso corporal 60 y > 60 Kg, respectivamente. La acción sostenida permite la administración de una única inyección subcutánea, que sustituye a las primeras 7 inyecciones de otras preparaciones de FSH administradas diariamente. El tratamiento se inicia durante la fase folicular inicial del ciclo menstrual. El día 5 ó 6 de estimulación se combina con un antagonista GnRH y el día 8 se puede continuar con inyecciones diarias de FSH (recombinante) hasta desencadenar la maduración final de los ovocitos. Se aconseja una dosis de FSH de 150 UI, aunque depende de la respuesta ovárica. En general, se logra un desarrollo folicular adecuado el día 9 de tratamiento como promedio (entre 6-18 días) 1,2. Insuficiencia renal y/o hepática: No se han realizado estudios en pacientes con insuficiencia renal, pero como la excreción de corifolitropina alfa puede resultar afectada, no se recomienda su uso en esta situación. Aunque tampoco hay estudios en insuficiencia hepática, su escasa eliminación por esta vía hace poco probable la afectación en estos casos 1,2. Farmacocinética Tras la administración subcutánea presenta una absorción y eliminación lentas. La biodisponibilidad absoluta es del 58%, con unas concentraciones independientes de la dosis, alcanzándose la máxima a las 44h. El volumen de distribución es de 9,2L, localizándose principalmente en ovarios y riñones. El aclaramiento es de 0,13 L/h y puesto que su eliminación es fundamentalmente vía renal, puede verse afectada por alteraciones en el funcionamiento normal del riñón. La vida media es de 70h (60-110), por lo que las concentraciones activas se mantienen durante una semana 1-4. Efectos adversos La reacciones adversas comunicadas con mayor frecuencia son: síndrome de hiperestimulación ovárica (SHO) (5,2%), dolor pélvico (4,1% ) y molestias pélvicas (5,5%), cefalea (3,2%), náuseas (1,7%), fatiga (1,4%) y molestias en las mamas (como dolor a la palpación) (1,2%) 1-4. Análisis de la evidencia disponible La corifolitropina alfa es la primera molécula con acción prolongada y su aparición en el mercado se ha basado en dos ensayos pivotales en Fase III, dobleciego, aleatorizados, con control activo, que determinan la eficacia y seguridad tras su administración semanal frente a la FSH recombinante (rfsh) diaria (Puregon ), utilizando diferente dosis en función del peso corporal. De hecho, los criterios de inclusión son: - Ensayo ENGAGE (38819) de no inferioridad 5 : mujeres 18 y 36 años con indicación de estimulación ovárica controlada para un proceso de FIV o ICSI (microinyección intracitoplasmática de espermatozoides), ciclo menstrual normal entre días y peso corporal > 60Kg y 90 Kg, IMC Kg/m 2. - Ensayo ENSURE (107012) de equivalencia 6 : 396 con idénticas características, excepto peso corporal 60 Kg, IMC Kg/m 2. La pauta de administración de ambas gonadotrofinas en el ensayo ENGAGE se muestra en las siguientes figuras, de modo que en el grupo de investigación se administra una dosis de corifolitropina alfa (150 mcg) seguida de 6 días de placebo y Página 2 de 8
3 en el grupo control se administra rfsh durante 7 días (200 UI). A partir del día 8 se inicia en ambos grupos la administración diaria de rfsh 5 : En la siguiente tabla aparecen los principales resultados, que también se muestran en la tabla 1: Página 3 de 8
4 La variable principal (exigida por la FDA), la tasa de embarazo en curso alcanzada, definida como presencia de al menos un feto con latido cardíaco a las 10 semanas tras la transferencia del embrión, o un nacimiento confirmado por ciclo iniciado o por transferencia embrionario, mostró unos resultados acordes con la no inferioridad, con una diferencia de 0,9 ( 3,9-5,7) favorable a corifolitropina. La variable coprincipal (exigida por la EMA), definida como el número de ovocitos recuperados por ciclo iniciado, resultó significativa a favor de corifolitropina alfa. En ambos casos se consiguieron diferencias que no sobrepasaban el límite de no inferioridad establecido previamente. No se observaron diferencias clínicamente relevantes entre ambos grupos en lo referente a otras variables secundarias: número de ovocitos en metafase II, tasa de fertilización, número medio de embriones transferidos de buena calidad, tasa media de implantación. El perfil de seguridad no mostró diferencias relevantes entre los grupos, siendo el SHO el efecto adverso más frecuente, con una incidencia de 4,1% y 2,7% para corifolitropina y rfsh, respectivamente (p=0,15), aunque en los casos más graves motivó la suspensión del tratamiento en una proporción mayor para el grupo de tratamiento (2,1% vs 0,4%). En el otro ensayo fase III (ENSURE) para pacientes con peso 60 Kg, en el que se compara 150mcg de corifolitropina alfa frente a 150 UI de rfsh, se consiguió un número de ovocitos recuperados (variable principal) acorde con la equivalencia: 13,3 vs 10,6. Sin embargo, la tasa de embarazo en curso no alcanzó una diferencia favorable a corifolitropina alfa: 9,2% ( 18,9-0,5%). Aunque se observaron diferencias entre los grupos en cuanto a la historia y características basales de los pacientes, los procedimientos de estimulación y fertilización y la transferencia embrionaria, ninguno de estos factores podía explicar dicha diferencia 6. En el informe EPAR se indica la conveniencia de haber incluido este parámetro en la variable principal, pero eso habría requerido incluir un número de pacientes de 3 a 4 veces mayor, y quizá este podría ser el motivo de no haberlo llevado a cabo. La incidencia global de efectos adversos fue comparable entre ambos grupos y de igual forma, el SHO fue mayor en el grupo de tratamiento: 3,0% vs 1,6%. En la figura se incluyen los efectos adversos de ambos ensayos 3 : Para minimizar el riesgo de SHO, el informe EPAR resalta el hecho de considerar las contraindicaciones y precauciones reflejadas en la ficha técnica: historia previa de SHO, ciclo previo de Página 4 de 8
5 Estimulación Ovárica Controlada con resultado de más de 30 folículos 11 mm medidos por ecografía, no combinar con un agonista de la GnRH por favorecer una respuesta ovárica superior 2. Estudio económico En la siguiente tabla se muestra el cálculo de los costes comparativos respecto a las alternativas disponibles en el hospital, considerando como referencia los datos utilizados en el ensayo ENGAGE: periodo de estimulación de 9 días y una dosis inicial de rfsh de 200 UI. Puesto que los ensayos han demostrado la equivalencia de eficacia entre las alternativas, no es necesario relacionarla con su coste, es decir, nos basamos en una minimización de costes: Origen PVL Unitario Pauta posológica Coste total /ciclo /paciente Coste /incremental /ciclo/paciente Corifolitropina alfa (ELONVA ) Jer precargada 100 mcg 150 mcg REC 530,41 60 Kg: 100 mcg x 7 días UI Puregon x 2 días > 60 Kg: 150 mcg x 7 días UI Puregon x 2 días 647,07 Folitropina beta (PUREGON ) Vial 100 UI/0,5ml Vial 200 UI /0,5ml Cartucho 600 UI /0,72ml Cartucho 900 UI /1,08ml REC 29,234 * 58,334 * 177,88 * 272,26 * 200 UI x 9 días = UI 544,52 102,55 Folitropina alfa (GONAL ) Vial 1050 UI (77 mcg) REC 357,33 * 200 UI x 9 días = UI 714,66 +67,59 Urofolitropina (FOSTIPUR ) Amp polvo + disolvente 75 UI/ml Amp polvo + disolvente 150 UI/ml Humano (FSH purificada de orina) 18,39 * 27,22 * UI x 9 días = UI (max. 450 UI/día) 244,98 353,86 402,09-293,21 * Con descuento del 7,5% Cabe destacar, tal como se refleja en la tabla, la notable diferencia de precio respecto a la gonadotrofina de origen urinario. A pesar de que las recombinantes aparecieron con ventajas relativas a la tolerancia y seguridad, incluso se asociaron inicialmente a una mayor eficacia clínica, lo cierto es que una reciente revisión de la Cochrane, compara la efectividad de rfsh con tres de los principales tipos de gonadotrofinas urinarias. A partir de 42 ensayos incluidos, la comparación no puso de manifiesto diferencias estadísticamente significativas en la tasa de nacimientos (OR 0,97; IC 95% 0,87 a 1,08), lo que supone que para un grupo con un 25% de nacimientos tras el uso de FSH urinaria, la proporción estaría entre el 22,5% y 26,5% utilizando rfsh. Tampoco hubo diferencia en la incidencia de SHO (OR 1,18; IC 95% 0,86 a 1,61), lo que significa que un 2% de riesgo de SHO usando FSH urinaria equivaldría a un riesgo entre 1,7% y 3,2% al utilizar rfsh. Los autores concluyen que la elección de una gonadotrofina debería depender de la disponibilidad, la conveniencia de usar una u otra y el coste 7. Página 5 de 8
6 El importe económico de estas tres gonadotrofinas desde enero de 2011 hasta la actualidad ha sido de: Fostipur (843 ampollas), Gonal (794 viales) y Puregon 900 (694 cartuchos). Si se hiciera una sustitución total por ejemplo de Puregon 900, supondría un incremento de aproximadamente para ese periodo de tiempo. Sin embargo, si se restringe su uso en favor de la urofolitropina se conseguiría ajustar el coste. Nivel y grado de la evidencia Fuentes de evidencia sobre tratamiento: MEDLINE. Estrategia de búsqueda: filtros metodológicos o Libre: coriofollitropin alfa o Limits: Meta-Analysis, Randomized Controlled Trial, Review. Nivel evidencia: I Grado de recomendación: A Conclusiones Corifolitropina alfa es una proteína de fusión obtenida por tecnología DNA recombinante con actividad estimulante folicular prolongada. La ventaja clara respecto a las alternativas disponibles es precisamente su acción prolongada, que permite su administración semanal en lugar de diaria como hasta ahora. Aunque es cierto que el cumplimiento a priori es elevado en este tipo de pacientes, es importante incluir mejoras que faciliten un proceso altamente estresante que puede llevar al abandono en algunos casos. números absolutos es pequeña y la incidencia baja. No obstante, es importante considerar que esta administración única también presenta la desventaja de no poder revertir un SHO en caso de que se produzca, cosa que con la rfsh si es posible. Por ello, es recomendable seleccionar previamente a las pacientes candidatas a la corifolitropina alfa, sobre todo en función de contraindicaciones y precauciones relacionadas con antecedentes de SHO y mayor riesgo de su aparición. En cuanto al impacto económico, supone un coste incremental de por ciclo y paciente respecto a Puregon, lo que implica un notable aumento si se incluyen a todas las pacientes (en la solicitud no se indica las pacientes por año que se estima tratar con Elonva ). Por ello, y teniendo en cuenta el menor coste de la gonadotrofina de origen urinario, sería conveniente establecer unos criterios de uso para cada una de ellas. En definitiva, se recomienda la inclusión de corifolitropina alfa en la GFT del Hospital, delimitando claramente las condiciones de uso en lo referente a las contraindicaciones y precauciones del medicamento, para seleccionar de forma adecuada las pacientes candidatas a su utilización, reducir el riesgo de SHO y ajustar el coste. Grado Recomendación del CIM: B Se incluye en la GFT con recomendaciones específicas La evidencia muestra una eficacia comparable (no inferioridad) al comparador activo: folitropina beta (Puregon ), y un perfil de seguridad similar a excepción de una incidencia ligeramente superior de síndrome de hiperestimulación ovárica en el caso de corifolitropina alfa. Sin embargo, se considera dentro del límite aceptable teniendo en cuenta que la diferencia en Página 6 de 8
7 BIBLIOGRAFIA 1. Elonva. BOT: Base de datos del Medicamento. Consejo General de Colegios Oficiales de Farmacéuticos. Disponible en: (2011) 2. Elonva. Informe EPAR de la European Medicines Agency. En: 3. Croxtall JD, McKeage K. Corifollitropin alfa: a review of its use in controlled ovarian stimulation for assisted reproduction. BioDrugs 2011;25: De Lartigue J. Corfollitropin alfa: a new option to treat female infertility. Drugs Today (Barc) 2011; 47: Devroey P, Boostanfar R, Koper NP et al. A double-blind, non-inferiority RCT comparing corifollitropin alfa and recombinant FSH during the first seven days of ovarian stimulation using a GnRH antagonist protocol. Human Reprod 2009;24: Mannaerts B. The corifollitropin alfa Ensure study group. Corifollitropin alfa for ovarian stimulation in IVF: a randomized trial in lower-body-weight women. Reproduct BioMed Online 2010;21: Van Wely M, Kwan I, Burt AL et al. Recombinant versus urinary gonadotrophin for ovarian stimulation in assisted reprodctive technology cycles (review). The Cochrane Collaboration. Cochrane Database Syst Rev 2011 Feb 16;(2):CD AUTORA: Dra. E. Romá Sánchez TIEMPO: 22 h Nº REGISTRO:08/11 Página 7 de 8
8 Tabla 1: Resultados de los ensayos de corifolitropina alfa en comparación con rfsh. ESTUDIO, AUTOR, Escala Tratamiento AÑO Jadad Ensayo ENGAGE Devroey P et al, Fase III Pacientes candidatas a FIV o ICSI con peso corporal > 60Kg A, DC, C, MC, no inferioridad 4 Pauta tratamiento Pauta control Variable principal de resultado 150mcg Corifolitropina alfa (Elonva ) N= UI folitropina beta (Puregon ) N=750 PACIENTES por intención de tratar Tasa embarazo en curso Por ciclo iniciado Por embrión transferido Nº ovocitos recuperado (media) Por ciclo iniciado Por ovocito recuperado Grupo Tratamiento (IC 95%) 38,9% 43,8% 13,7 14,1 RESULTADOS Grupo control (IC 95%) 38,1% 40,6% 12,5 12,7 Diferencia (IC 95%; p) +0,9% (-3,9-5,7; 0,71) 3,1 (-2,0-8,2; 0,24) +1,2 (0,5-1,9; 0,001) +1,6 (0,8-2,3; <0,001) No inferioridad demostrada Complicaciones/ reacciones adversas más frecuentes % ELON. vs % PUR - SHO 1,9 vs 1,2 - Embarazo ectópico 0,9 vs 1,2 - Dolor en el proceso 22,3 vs 20,1 - Aborto 13,8 vs 11,2 - Molestias pélvicas 12,1 vs 12,3 - Cefalea 10,5 vs 15,2 Ensayo ENSURE Mannaerts B, Pacientes candidatas a FIV o ICSI con peso corporal 60Kg A, DC, C, MC, equivalencia 4 100mcg Corifolitropina alfa (Elonva ) N= UI folitropina beta (Puregon ) N=128 PACIENTES por intención de tratar Nº ovocitos recuperado (media) Por ciclo iniciado 13,3 10,6 +2,5 (1,2-3,9; ) Equivalencia establecida Variable secundaria Tasa embarazo en curso Por ciclo iniciado 25,4% 34,4% 9,2% ( 18,9-0,5%) - SHO 3,0 vs 1,6 - Embarazo ectópico 3,0 vs 3,1 - Molestias pélvicas 10,1 vs 14,7 - Dolor pélvico 10,4 vs 10,9 - Hemorragia antepartum 6,0 vs 12,4 - Cefalea 8,2 vs 8,5 A: aleatorizado; DC: doble-ciego; C: controlado; MC: multicéntrico; SHO: síndrome hiperestimulación ovárica. Página 8 de 8
CORIFOLITROPINA ALFA para la estimulación ovárica en reproducción asisitida Informe preliminar de la Comisión de Farmacia HOSPITAL REINA SOFÍA CÓRDOBA
 CORIFOLITROPINA ALFA para la estimulación ovárica en reproducción asisitida Informe preliminar de la Comisión de Farmacia HOSPITAL REINA SOFÍA CÓRDOBA 1.- Identificación del fármaco: Nombre Comercial:
CORIFOLITROPINA ALFA para la estimulación ovárica en reproducción asisitida Informe preliminar de la Comisión de Farmacia HOSPITAL REINA SOFÍA CÓRDOBA 1.- Identificación del fármaco: Nombre Comercial:
Cada jeringa precargada contiene 100 microgramos de corifolitropina alfa en 0,5 ml de solución inyectable.
 1. NOMBRE DEL MEDICAMENTO Elonva 100 microgramos solución inyectable. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada jeringa precargada contiene 100 microgramos de corifolitropina alfa en 0,5 ml de solución
1. NOMBRE DEL MEDICAMENTO Elonva 100 microgramos solución inyectable. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada jeringa precargada contiene 100 microgramos de corifolitropina alfa en 0,5 ml de solución
INFORMACIÓN PARA EL PRESCRIPTOR ELONVA Corifolitropina alfa 100 mcg/0,5 ml mcg/0,5 ml Solución Inyectable - Vía subcutánea VENTA BAJO RECETA
 INFORMACIÓN PARA EL PRESCRIPTOR ELONVA Corifolitropina alfa 100 mcg/0,5 ml - 150 mcg/0,5 ml Solución Inyectable - Vía subcutánea VENTA BAJO RECETA FORMULA: Cada jeringa prellenada de ELONVA 100 mcg/0,5
INFORMACIÓN PARA EL PRESCRIPTOR ELONVA Corifolitropina alfa 100 mcg/0,5 ml - 150 mcg/0,5 ml Solución Inyectable - Vía subcutánea VENTA BAJO RECETA FORMULA: Cada jeringa prellenada de ELONVA 100 mcg/0,5
MARCO GARNIQUE MONCADA Máster en Reproducción Humana Ginecólogo del Servicio de Medicina Reproductiva del INMP Ginecólogo de CREA, Centro de
 MARCO GARNIQUE MONCADA Máster en Reproducción Humana Ginecólogo del Servicio de Medicina Reproductiva del INMP Ginecólogo de CREA, Centro de Reproducción Asistida Retraso en la edad del primer embarazo
MARCO GARNIQUE MONCADA Máster en Reproducción Humana Ginecólogo del Servicio de Medicina Reproductiva del INMP Ginecólogo de CREA, Centro de Reproducción Asistida Retraso en la edad del primer embarazo
INFERTILIDAD TRATAMIENTO DE LA INFERTILIDAD. Infertilidad. Etiología
 TRATAMIENTO DE LA INFERTILIDAD INFERTILIDAD Inhabilidad de las parejas para concebir (o embarazarse) después de 1 año sin control de natalidad. Fecundidad probabilidad de concebir por mes de esfuerzo Usado
TRATAMIENTO DE LA INFERTILIDAD INFERTILIDAD Inhabilidad de las parejas para concebir (o embarazarse) después de 1 año sin control de natalidad. Fecundidad probabilidad de concebir por mes de esfuerzo Usado
NOMBRE DEL FÁRMACO e indicación clínica (Informe para la Comisión de Farmacia y Terapéutica del Hospital xxxxxxxxxx) Fecha xx/xx/xx
 NOMBRE DEL FÁRMACO e indicación clínica (Informe para la Comisión de Farmacia y Terapéutica del Hospital xxxxxxxxxx) Fecha xx/xx/xx 1.- IDENTIFICACIÓN DEL FÁRMACO Y AUTORES DEL INFORME Fármaco: Indicación
NOMBRE DEL FÁRMACO e indicación clínica (Informe para la Comisión de Farmacia y Terapéutica del Hospital xxxxxxxxxx) Fecha xx/xx/xx 1.- IDENTIFICACIÓN DEL FÁRMACO Y AUTORES DEL INFORME Fármaco: Indicación
CORIFOLITROPINA ALFA
 CORIFOLITROPINA ALFA ELONVA? (Schering Plough) ESTIMULACIÓN OVÁRICA CONTROLADA La función ovárica es controlada por un conjunto de hormonas, genéricamente conocido como gonadotropinas, entre las que se
CORIFOLITROPINA ALFA ELONVA? (Schering Plough) ESTIMULACIÓN OVÁRICA CONTROLADA La función ovárica es controlada por un conjunto de hormonas, genéricamente conocido como gonadotropinas, entre las que se
Prevención primaria SHO. S. González Núñez
 Hospital Universitari Sant Joan de Déu (Barcelona) SERVEI DE GINECOLOGIA I OBSTETRICIA S. González Núñez 1. Identificación de factores de riesgo conocidos para implementar estrategias preventivas específicas.
Hospital Universitari Sant Joan de Déu (Barcelona) SERVEI DE GINECOLOGIA I OBSTETRICIA S. González Núñez 1. Identificación de factores de riesgo conocidos para implementar estrategias preventivas específicas.
GONAL-f 75 UI (5,5 microgramos) polvo y disolvente para solución inyectable.
 1. DENOMINACIÓN DEL MEDICAMENTO GONAL-f 75 UI (5,5 microgramos) polvo y disolvente para solución inyectable. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un vial contiene 6 microgramos de folitropina alfa,
1. DENOMINACIÓN DEL MEDICAMENTO GONAL-f 75 UI (5,5 microgramos) polvo y disolvente para solución inyectable. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un vial contiene 6 microgramos de folitropina alfa,
Volumen a inyectar (ml) 75 0,13 150 0,25
 DENOMINACIÓN DEL MEDICAMENTO. GONAL-f 75 UI (5,5 microgramos) polvo y disolvente para solución inyectable. GONAL-f 1050 UI/1,75 ml (77 microgramos/1,75 ml) polvo y disolvente para solución inyectable.
DENOMINACIÓN DEL MEDICAMENTO. GONAL-f 75 UI (5,5 microgramos) polvo y disolvente para solución inyectable. GONAL-f 1050 UI/1,75 ml (77 microgramos/1,75 ml) polvo y disolvente para solución inyectable.
MADURACIÓN OVOCITARIA EN TRAAC
 MADURACIÓN OVOCITARIA EN TRAAC Dr. Marco Garnique Moncada Jefe del Servicio de Medicina Reproductiva del INMP Ginecólogo Obstetra Máster en Reproducción Humana IVI - España La EOC produce múltiples folículos
MADURACIÓN OVOCITARIA EN TRAAC Dr. Marco Garnique Moncada Jefe del Servicio de Medicina Reproductiva del INMP Ginecólogo Obstetra Máster en Reproducción Humana IVI - España La EOC produce múltiples folículos
Qué hay de nuevo en Es1mulación Ovárica?
 Dra. Marcela IRIGOYEN Médica Especialista en Medicina Reproduc3va Fer3lidad San Isidro Ex directora del Curso Superior de Medicina Reproduc3va de la SAMeR Qué hay de nuevo en Es1mulación Ovárica? INDUCCIÓN
Dra. Marcela IRIGOYEN Médica Especialista en Medicina Reproduc3va Fer3lidad San Isidro Ex directora del Curso Superior de Medicina Reproduc3va de la SAMeR Qué hay de nuevo en Es1mulación Ovárica? INDUCCIÓN
A. DESCRIPCIÓN DEL MEDICAMENTO Y SU INDICACIÓN
 17 INSULINA GLARGINA A. DESCRIPCIÓN DEL MEDICAMENTO Y SU INDICACIÓN 1. Denominación común internacional (DCI), denominación oficial española (DOE) o nombre genérico del principio activo. glargina (Lantus
17 INSULINA GLARGINA A. DESCRIPCIÓN DEL MEDICAMENTO Y SU INDICACIÓN 1. Denominación común internacional (DCI), denominación oficial española (DOE) o nombre genérico del principio activo. glargina (Lantus
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 INDOMETACINA 25 mg COMPRIMIDOS RECUBIERTOS ANTIINFLAMATORIO ANTIRREUMÁTICO Página 1 INDOMETACINA 25 mg Comprimidos
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 INDOMETACINA 25 mg COMPRIMIDOS RECUBIERTOS ANTIINFLAMATORIO ANTIRREUMÁTICO Página 1 INDOMETACINA 25 mg Comprimidos
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Mupirocina ISDIN 20 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene 20 mg de mupirocina. Para consultar
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. NOMBRE DEL MEDICAMENTO Mupirocina ISDIN 20 mg/g pomada 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada gramo de pomada contiene 20 mg de mupirocina. Para consultar
PROCEDIMIENTO ESPECÍFICO ESTIMULACION OVARICA PARA FIV/ ICSI COD. PE-OBS-08
 PROCEDIMIENTO ESPECÍFICO ESTIMULACION OVARICA PARA FIV/ ICSI COD. PE-OBS-08 Elaborado por: Emilia Ocón Moraleda Área de Obstetricia y Ginecología Fecha 20/01/2009 Revisado por: Juan Manuel Marín García.
PROCEDIMIENTO ESPECÍFICO ESTIMULACION OVARICA PARA FIV/ ICSI COD. PE-OBS-08 Elaborado por: Emilia Ocón Moraleda Área de Obstetricia y Ginecología Fecha 20/01/2009 Revisado por: Juan Manuel Marín García.
RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO
 DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO PG 600 MONODOSIS 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Vial con el polvo:
DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO PG 600 MONODOSIS 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Vial con el polvo:
FOLITROPINA DELTA ( REKOVELLE, FERRING) EN ESTIMULACIÓN OVÁRICA EN REPRODUCCIÓN ASISTIDA
 FOLITROPINA DELTA ( REKOVELLE, FERRING) EN ESTIMULACIÓN OVÁRICA EN REPRODUCCIÓN ASISTIDA Santiago Cuéllar Rodríguez RESUMEN La folitropina delta es un análogo recombinante de la hormona foliculoestimulante
FOLITROPINA DELTA ( REKOVELLE, FERRING) EN ESTIMULACIÓN OVÁRICA EN REPRODUCCIÓN ASISTIDA Santiago Cuéllar Rodríguez RESUMEN La folitropina delta es un análogo recombinante de la hormona foliculoestimulante
SITUACIÓN ACTUAL DE LA FIV/ICSI EN ANDALUCÍA. REGISTRO SEF.
 SITUACIÓN ACTUAL DE LA FIV/ICSI EN ANDALUCÍA. REGISTRO SEF. Sandra Zamora López, Mar Salas Martínez y Luis Martínez Granados. Banco semen CEIFER, Granada; Roquetas FIV, Almería; Unidad de Reproducción
SITUACIÓN ACTUAL DE LA FIV/ICSI EN ANDALUCÍA. REGISTRO SEF. Sandra Zamora López, Mar Salas Martínez y Luis Martínez Granados. Banco semen CEIFER, Granada; Roquetas FIV, Almería; Unidad de Reproducción
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Elonva 100 microgramos solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada jeringa precargada
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Elonva 100 microgramos solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada jeringa precargada
A. DESCRIPCIÓN DEL MEDICAMENTO Y SU INDICACIÓN
 6 CARMUSTINA EN IMPLANTES A. DESCRIPCIÓN DEL MEDICAMENTO Y SU INDICACIÓN 1. Denominación común internacional (DCI), denominación oficial española (DOE) o nombre genérico del principio activo. CARMUSTINA
6 CARMUSTINA EN IMPLANTES A. DESCRIPCIÓN DEL MEDICAMENTO Y SU INDICACIÓN 1. Denominación común internacional (DCI), denominación oficial española (DOE) o nombre genérico del principio activo. CARMUSTINA
PROFILAXIS DE LA ETV EN LA FERTILIZACIÓN IN VITRO. Ángeles Blanco
 PROFILAXIS DE LA ETV EN LA FERTILIZACIÓN IN VITRO Ángeles Blanco ETV y Técnicas de reproducción asistida (TRA) La FIV y otras TRA se usan para resolver la infertilidad de las parejas. 1.5 millones de ciclos
PROFILAXIS DE LA ETV EN LA FERTILIZACIÓN IN VITRO Ángeles Blanco ETV y Técnicas de reproducción asistida (TRA) La FIV y otras TRA se usan para resolver la infertilidad de las parejas. 1.5 millones de ciclos
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1/7 1. DENOMINACIÓN DEL MEDICAMENTO Ovitrelle 250 microgramos polvo y disolvente para solución inyectable. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Para asegurar
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1/7 1. DENOMINACIÓN DEL MEDICAMENTO Ovitrelle 250 microgramos polvo y disolvente para solución inyectable. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Para asegurar
CENAVUL Suspensión inyectable
 Camí Pedra Estela s/n 43205 Reus Telf. 977 75 72 73 Fax. 977 75 13 98 www.cenavisa.com E-mail: cenavisa@cenavisa.com FICHA TÉCNICA: CENAVUL Suspensión inyectable Reg. nº: 2145 ESP FICHA TÉCNICA (RESUMEN
Camí Pedra Estela s/n 43205 Reus Telf. 977 75 72 73 Fax. 977 75 13 98 www.cenavisa.com E-mail: cenavisa@cenavisa.com FICHA TÉCNICA: CENAVUL Suspensión inyectable Reg. nº: 2145 ESP FICHA TÉCNICA (RESUMEN
PROSPECTO: INFORMACIÓN PARA EL USUARIO. BRAVELLE 75 Unidades Internacionales polvo y disolvente para solución inyectable Urofolitropina
 PROSPECTO: INFORMACIÓN PARA EL USUARIO BRAVELLE 75 Unidades Internacionales polvo y disolvente para solución inyectable Urofolitropina Lea todo el prospecto detenidamente antes de empezar a usar el medicamento.
PROSPECTO: INFORMACIÓN PARA EL USUARIO BRAVELLE 75 Unidades Internacionales polvo y disolvente para solución inyectable Urofolitropina Lea todo el prospecto detenidamente antes de empezar a usar el medicamento.
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Elonva 100 microgramos solución inyectable. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada jeringa precargada
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Elonva 100 microgramos solución inyectable. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada jeringa precargada
ARIPIPRAZOL En adolescentes contrastorno Bipolar I
 ARIPIPRAZOL En adolescentes contrastorno Bipolar I Información para profesionales sanitarios Preguntas frecuentes Disponible en la web de la AEMPS www.aemps.gob.es Información sobre prevención de riesgos
ARIPIPRAZOL En adolescentes contrastorno Bipolar I Información para profesionales sanitarios Preguntas frecuentes Disponible en la web de la AEMPS www.aemps.gob.es Información sobre prevención de riesgos
Grupo de estudio internacional del cáncer de mama (IBCSG) 23-01
 Grupo de estudio internacional del cáncer de mama (IBCSG) 23-01 Disección axilar vs. no disección axilar en cáncer de mama con axila clínicamente negativa y micrometástasis en ganglio centinela Viviana
Grupo de estudio internacional del cáncer de mama (IBCSG) 23-01 Disección axilar vs. no disección axilar en cáncer de mama con axila clínicamente negativa y micrometástasis en ganglio centinela Viviana
Uso de Gonadotropinas en Estimulación Ovárica Controlada en técnicas de reproducción asistida
 Uso de Gonadotropinas en Estimulación Ovárica Controlada en técnicas de reproducción asistida Informe para la Guía Farmacoterapéutica de Hospitales de Andalucía 03/05/2012 Tabla de contenido (control +
Uso de Gonadotropinas en Estimulación Ovárica Controlada en técnicas de reproducción asistida Informe para la Guía Farmacoterapéutica de Hospitales de Andalucía 03/05/2012 Tabla de contenido (control +
DELOS OTIC CIPROFLOXACINA CLORHIDRATO - HIDROCORTISONA. Gotas Óticas. Hidrocortisona 1,00 g. Ciprofloxacina Clorhidrato 0,20 g.
 DELOS OTIC CIPROFLOXACINA CLORHIDRATO - HIDROCORTISONA Gotas Óticas Industria Argentina Venta bajo receta FORMULA Cada 100 ml contienen: Hidrocortisona 1,00 g. Ciprofloxacina Clorhidrato 0,20 g. Excipientes:
DELOS OTIC CIPROFLOXACINA CLORHIDRATO - HIDROCORTISONA Gotas Óticas Industria Argentina Venta bajo receta FORMULA Cada 100 ml contienen: Hidrocortisona 1,00 g. Ciprofloxacina Clorhidrato 0,20 g. Excipientes:
TADALAFILO (ADCIRCA / ELI LILLY)
 Presentación CN 664452 Comp recub 20mg E/56 PVL= 520 (ADCIRCA / ELI LILLY) Excipientes Núcleo del comprimido: lactosa monohidrato, croscarmelosa sódica, hidroxipropilcelulosa, celulosa microcristalina,
Presentación CN 664452 Comp recub 20mg E/56 PVL= 520 (ADCIRCA / ELI LILLY) Excipientes Núcleo del comprimido: lactosa monohidrato, croscarmelosa sódica, hidroxipropilcelulosa, celulosa microcristalina,
FÁRMACOS EN ESTERILIDAD II. COMO ACTÚAN. BLOQUEO DE HIPÓFISIS: AGONISTAS Y ANTAGONISTAS Gn RH. SOPORTE FASE LÚTEA: PROGESTERONA
 FÁRMACOS EN ESTERILIDAD II. COMO ACTÚAN. BLOQUEO DE HIPÓFISIS: AGONISTAS Y ANTAGONISTAS Gn RH. SOPORTE FASE LÚTEA: PROGESTERONA MARINA ALFONSO BALAGUER DUE FIVV VALENCIA 2012 Comienza en el cerebro (Hipotálamo)
FÁRMACOS EN ESTERILIDAD II. COMO ACTÚAN. BLOQUEO DE HIPÓFISIS: AGONISTAS Y ANTAGONISTAS Gn RH. SOPORTE FASE LÚTEA: PROGESTERONA MARINA ALFONSO BALAGUER DUE FIVV VALENCIA 2012 Comienza en el cerebro (Hipotálamo)
VACUNACIÓN FRENTE A MENINGOCOCO B (BEXSERO ) Tatiana Amil Pena MIR-4 Pediatría
 VACUNACIÓN FRENTE A MENINGOCOCO B (BEXSERO ) Tatiana Amil Pena MIR-4 Pediatría ÍNDICE Introducción: el meningococo y la enfermedad meningocócica Vacunación frente al meningococo B: Vacuna frente a meningococo
VACUNACIÓN FRENTE A MENINGOCOCO B (BEXSERO ) Tatiana Amil Pena MIR-4 Pediatría ÍNDICE Introducción: el meningococo y la enfermedad meningocócica Vacunación frente al meningococo B: Vacuna frente a meningococo
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1/18
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1/18 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Oncept IL-2 liofilizado y disolvente para suspensión inyectable para gatos. 2. COMPOSICIÓN
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1/18 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO Oncept IL-2 liofilizado y disolvente para suspensión inyectable para gatos. 2. COMPOSICIÓN
Capítulo 2. Fertilización in vitro/ Inyección Intracitoplasmática de Espermatozoides
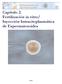 Capítulo 2. Fertilización in vitro/ Inyección Intracitoplasmática de Espermatozoides 24/75 Resumen FIV/ICSI La tabla que sigue muestra el resumen de los ciclos de FIV/ICSI. Como se ve, de los 25,736 ciclos
Capítulo 2. Fertilización in vitro/ Inyección Intracitoplasmática de Espermatozoides 24/75 Resumen FIV/ICSI La tabla que sigue muestra el resumen de los ciclos de FIV/ICSI. Como se ve, de los 25,736 ciclos
La Plata,. de... de 20. CONSENTIMIENTO INFORMADO: CRIOPRESERVACION Y ALMACENAMIENTO DE EMBRIONES. PERSONA SOLA.
 Consentimiento nº:.. La Plata,. de... de 20. CONSENTIMIENTO INFORMADO: CRIOPRESERVACION Y ALMACENAMIENTO DE EMBRIONES. PERSONA SOLA. Este consentimiento informado corresponde a:. (Historia Clínica Nº )
Consentimiento nº:.. La Plata,. de... de 20. CONSENTIMIENTO INFORMADO: CRIOPRESERVACION Y ALMACENAMIENTO DE EMBRIONES. PERSONA SOLA. Este consentimiento informado corresponde a:. (Historia Clínica Nº )
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1/72 1. NOMBRE DEL MEDICAMENTO Puregon 50 U.I. polvo y disolvente para solución inyectable 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Puregon 50 U.I. consiste
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1/72 1. NOMBRE DEL MEDICAMENTO Puregon 50 U.I. polvo y disolvente para solución inyectable 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Puregon 50 U.I. consiste
FICHA TÉCNICA (RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO)
 FICHA TÉCNICA (RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO) 1 DENOMINACIÓN DEL MEDICAMENTO SERIGAN 1000 UI/4 ml 2 COMPOSICIÓN CUALITATIVA Y CUANTITATIVA EN TÉRMINOS DE PRINCIPIOS ACTIVOS Y COMPONENTES DEL
FICHA TÉCNICA (RESUMEN DE CARACTERÍSTICAS DEL PRODUCTO) 1 DENOMINACIÓN DEL MEDICAMENTO SERIGAN 1000 UI/4 ml 2 COMPOSICIÓN CUALITATIVA Y CUANTITATIVA EN TÉRMINOS DE PRINCIPIOS ACTIVOS Y COMPONENTES DEL
FICHA TECNICA. ACT-HIB Vacuna de polisacárido de Haemophilus influenzae tipo b conjugado a proteína del tétanos
 FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO. ACT-HIB Vacuna de polisacárido de Haemophilus influenzae tipo b conjugado a proteína del tétanos 2. COMPOSICION CUALITATIVA Y CUANTITATIVA. Liofilizado (para una
FICHA TECNICA 1. NOMBRE DEL MEDICAMENTO. ACT-HIB Vacuna de polisacárido de Haemophilus influenzae tipo b conjugado a proteína del tétanos 2. COMPOSICION CUALITATIVA Y CUANTITATIVA. Liofilizado (para una
Resultados perinatales de los recién nacidos obtenidos a partir de FIV con transferencia de embriones congelados. Estudio de la cohorte española.
 Resultados perinatales de los recién nacidos obtenidos a partir de FIV con transferencia de embriones congelados. Estudio de la cohorte española. Dres. Jose Antonio Moreno - Miguel Angel Checa INTRODUCCION
Resultados perinatales de los recién nacidos obtenidos a partir de FIV con transferencia de embriones congelados. Estudio de la cohorte española. Dres. Jose Antonio Moreno - Miguel Angel Checa INTRODUCCION
INDUCTORES DE LA OVULACIÓN BAJA COMPLEJIDAD
 Puerto la Cruz INDUCTORES DE LA OVULACIÓN BAJA COMPLEJIDAD *Coordinador Jefe Postgrado Ginecología y Obstetricia Universidad de Oriente -Ciudad Hospitalaria Dr. Luís Razetti -Barcelona *Director fundador
Puerto la Cruz INDUCTORES DE LA OVULACIÓN BAJA COMPLEJIDAD *Coordinador Jefe Postgrado Ginecología y Obstetricia Universidad de Oriente -Ciudad Hospitalaria Dr. Luís Razetti -Barcelona *Director fundador
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 Este medicamento está sujeto a seguimiento adicional, lo que agilizará la detección de nueva información sobre su seguridad. Se invita
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 Este medicamento está sujeto a seguimiento adicional, lo que agilizará la detección de nueva información sobre su seguridad. Se invita
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Elonva 100 microgramos solución inyectable Elonva 150 microgramos solución inyectable 2. COMPOSICIÓN CUALITATIVA
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Elonva 100 microgramos solución inyectable Elonva 150 microgramos solución inyectable 2. COMPOSICIÓN CUALITATIVA
Fase lútea: Qué debo tratar? Con qué? Hasta cuándo? 22/04/2010 Dr. Miguel Dolz
 Fase lútea: Qué debo tratar? Con qué? Hasta cuándo? 22/04/2010 Dr. Miguel Dolz Aspectos fisiológicos del cuerpo lúteo: antes de la implantación LH Esteroides(E,P) Factores crecimiento Interleukinas 17/12/09
Fase lútea: Qué debo tratar? Con qué? Hasta cuándo? 22/04/2010 Dr. Miguel Dolz Aspectos fisiológicos del cuerpo lúteo: antes de la implantación LH Esteroides(E,P) Factores crecimiento Interleukinas 17/12/09
FICHA TÉCNICA. La cantidad de principios activos presentes en 1 ml de ADDAMEL es de:
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO ADDAMEL concentrado para solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 ml de ADDAMEL contiene: Principio activo Cantidad Cloruro de cromo,
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO ADDAMEL concentrado para solución para perfusión 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA 1 ml de ADDAMEL contiene: Principio activo Cantidad Cloruro de cromo,
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Elonva 100 microgramos solución inyectable Elonva 150 microgramos solución inyectable 2. COMPOSICIÓN CUALITATIVA
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Elonva 100 microgramos solución inyectable Elonva 150 microgramos solución inyectable 2. COMPOSICIÓN CUALITATIVA
TERCERA SECCION CONSEJO DE SALUBRIDAD GENERAL
 TERCERA SECCION CONSEJO DE SALUBRIDAD GENERAL DÉCIMO Segunda Actualización de la Edición 2016 del Cuadro Básico y Catálogo de Medicamentos. Al margen un sello con el Escudo Nacional, que dice: Estados
TERCERA SECCION CONSEJO DE SALUBRIDAD GENERAL DÉCIMO Segunda Actualización de la Edición 2016 del Cuadro Básico y Catálogo de Medicamentos. Al margen un sello con el Escudo Nacional, que dice: Estados
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión
 FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 ACICLOVIR 5% Crema CREMA ANTIVIRAL Página 1 ACICLOVIR 5% Crema Crema Principio Activo Aciclovir Excipientes necesarios
FICHA TECNICA LABORATORIO QUÍMICO FARMACÉUTICO INDUSTRIAL DELTA S.A. versión - 1.0. 2013 ACICLOVIR 5% Crema CREMA ANTIVIRAL Página 1 ACICLOVIR 5% Crema Crema Principio Activo Aciclovir Excipientes necesarios
Un vial contiene 75 UI de hormona estimulante del folículo recombinante (FSH) en 0,5 ml de solución
 1. NOMBRE DEL MEDICAMENTO Puregon 50 UI/0,5 ml solución inyectable Puregon 75 UI/0,5 ml solución inyectable Puregon 100 UI/0,5 ml solución inyectable Puregon 150 UI/0,5 ml solución inyectable Puregon 200
1. NOMBRE DEL MEDICAMENTO Puregon 50 UI/0,5 ml solución inyectable Puregon 75 UI/0,5 ml solución inyectable Puregon 100 UI/0,5 ml solución inyectable Puregon 150 UI/0,5 ml solución inyectable Puregon 200
ANEXO I RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 4 1. NOMBRE DEL MEDICAMENTO Puregon 50 U.I. 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Puregon consiste en un polvo liofilizado con disolvente para reconstitución.
ANEXO I RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 4 1. NOMBRE DEL MEDICAMENTO Puregon 50 U.I. 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Puregon consiste en un polvo liofilizado con disolvente para reconstitución.
FICHA TÉCNICA. Una vez reconstituido, 1 ml de la solución contiene 100 UI de gonadotropina coriónica y 200 UI de gonadotropina sérica.
 FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO OVUCEL PORCINO LIOFILIZADO 5 DOSIS 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Vial con el liofilizado: Sustancias activas: Vial con polvo liofilizado:
FICHA TÉCNICA 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO OVUCEL PORCINO LIOFILIZADO 5 DOSIS 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Vial con el liofilizado: Sustancias activas: Vial con polvo liofilizado:
Inhibidores de neuraminidasa para la prevención y el tratamiento de la influenza en adultos y niños sanos
 Artículo de revisión REVISION COCHRANE Inhibidores de neuraminidasa para la prevención y el tratamiento de la influenza en adultos y niños sanos Jefferson T, Jones M, Doshi P, Del Mar C, Hama R, Thompson
Artículo de revisión REVISION COCHRANE Inhibidores de neuraminidasa para la prevención y el tratamiento de la influenza en adultos y niños sanos Jefferson T, Jones M, Doshi P, Del Mar C, Hama R, Thompson
Resumen de las características del producto. 1 ml. Para consultar la lista completa de excipientes, ver sección 6.1.
 Resumen de las características del producto 1. NOMBRE DEL MEDICAMENTO Agua para preparaciones inyectables B.Braun Disolvente para uso parenteral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio Activo
Resumen de las características del producto 1. NOMBRE DEL MEDICAMENTO Agua para preparaciones inyectables B.Braun Disolvente para uso parenteral 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio Activo
RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO. GESTAVET HCG 200/PMSG 400 Liofilizado y disolvente para solución inyectable para porcino.
 RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO GESTAVET HCG 200/PMSG 400 Liofilizado y disolvente para solución inyectable para porcino. 2. COMPOSICIÓN CUALITATIVA
RESUMEN DE LAS CARACTERISTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO GESTAVET HCG 200/PMSG 400 Liofilizado y disolvente para solución inyectable para porcino. 2. COMPOSICIÓN CUALITATIVA
Gonadotropina sérica equina (PMSG) Gonadotropina coriónica (HCG)
 FERTIPIG liofilizado y disolvente para solución inyectable para cerdos 1. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA El vial de liofilizado contiene: El vial de solvente contiene: 2 000 UI 1 000 UI 375 mg
FERTIPIG liofilizado y disolvente para solución inyectable para cerdos 1. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA El vial de liofilizado contiene: El vial de solvente contiene: 2 000 UI 1 000 UI 375 mg
Utilidad de un esquema combinado de FSH + LH recombinantes versus FSH recombinante sola en ciclos de fertilización in vitro
 Artículo original Ginecol Obstet Mex. 2017 noviembre;85(11):727-734. Utilidad de un esquema combinado de FSH + LH recombinantes versus FSH recombinante sola en ciclos de fertilización in vitro Kably-Ambe
Artículo original Ginecol Obstet Mex. 2017 noviembre;85(11):727-734. Utilidad de un esquema combinado de FSH + LH recombinantes versus FSH recombinante sola en ciclos de fertilización in vitro Kably-Ambe
1. NOMBRE DEL MEDICAMENTO
 1. NOMBRE DEL MEDICAMENTO Puregon 150 UI/0,18 ml solución inyectable Puregon 300 UI/0,36 ml solución inyectable Puregon 600 UI/0,72 ml solución inyectable Puregon 900 UI/1,08 ml solución inyectable 2.
1. NOMBRE DEL MEDICAMENTO Puregon 150 UI/0,18 ml solución inyectable Puregon 300 UI/0,36 ml solución inyectable Puregon 600 UI/0,72 ml solución inyectable Puregon 900 UI/1,08 ml solución inyectable 2.
Un vial contiene 75 UI de hormona estimulante del folículo recombinante (FSH) en 0,5 ml de solución
 1. NOMBRE DEL MEDICAMENTO Puregon 50 UI/0,5 ml solución inyectable Puregon 75 UI/0,5 ml solución inyectable Puregon 100 UI/0,5 ml solución inyectable Puregon 150 UI/0,5 ml solución inyectable Puregon 200
1. NOMBRE DEL MEDICAMENTO Puregon 50 UI/0,5 ml solución inyectable Puregon 75 UI/0,5 ml solución inyectable Puregon 100 UI/0,5 ml solución inyectable Puregon 150 UI/0,5 ml solución inyectable Puregon 200
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. Menopur 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Menopur 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principios activos: 1 Ampolla con la sustancia seca contiene Menotropina (Gonadotropina menopáusica humana, hmg)
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO Menopur 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principios activos: 1 Ampolla con la sustancia seca contiene Menotropina (Gonadotropina menopáusica humana, hmg)
SOLUCIÓN ORAL DE SACAROSA (24%) PRESENTADA EN VIALES UNIDOSIS DE 1.5 ML PARA LA PREVENCIÓN DEL DOLOR EN NEONATOS
 SUCROSE 24% EPMC PHARMA SOLUCIÓN ORAL DE SACAROSA (24%) PRESENTADA EN VIALES UNIDOSIS DE 1.5 ML PARA LA PREVENCIÓN DEL DOLOR EN NEONATOS El uso de sacarosa por vía oral, para el tratamiento del dolor neonatal,
SUCROSE 24% EPMC PHARMA SOLUCIÓN ORAL DE SACAROSA (24%) PRESENTADA EN VIALES UNIDOSIS DE 1.5 ML PARA LA PREVENCIÓN DEL DOLOR EN NEONATOS El uso de sacarosa por vía oral, para el tratamiento del dolor neonatal,
PUREGON Folitropina Beta Solución (Inyectable)
 1. NOMBRE COMERCIAL: PUREGON 2. NOMBRE GENERICO: Folitropina beta PUREGON Folitropina Beta Solución (Inyectable) 3. FORMA FARMACEUTICA Y FORMULACION: Solución inyectable El cartucho contiene: Folitropina
1. NOMBRE COMERCIAL: PUREGON 2. NOMBRE GENERICO: Folitropina beta PUREGON Folitropina Beta Solución (Inyectable) 3. FORMA FARMACEUTICA Y FORMULACION: Solución inyectable El cartucho contiene: Folitropina
MINOXIDIL AL 2%, SOLUCIÓN DE. Excipientes: Propilenglicol Agua purificada Etanol 96 %
 FN/2006/PO/039 1. NOMBRE: Solución de minoxidil 2. SINÓNIMOS Minoxidil en solución hidroalcohólica MINOXIDIL AL 2%, SOLUCIÓN DE 3. COMPOSICIÓN 3.1. FÓRMULA PATRÓN ( 2 % ) Minoxidil Excipientes: Propilenglicol
FN/2006/PO/039 1. NOMBRE: Solución de minoxidil 2. SINÓNIMOS Minoxidil en solución hidroalcohólica MINOXIDIL AL 2%, SOLUCIÓN DE 3. COMPOSICIÓN 3.1. FÓRMULA PATRÓN ( 2 % ) Minoxidil Excipientes: Propilenglicol
FICHA TÉCNICA. Menopur 600 UI: Cada vial de polvo contiene menotropina equivalente a 600 UI de actividad FSH y 600 UI de actividad LH.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO MENOPUR 600 UI polvo y disolvente para solución inyectable. MENOPUR 1200 UI polvo y disolvente para solución inyectable. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO MENOPUR 600 UI polvo y disolvente para solución inyectable. MENOPUR 1200 UI polvo y disolvente para solución inyectable. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
Vacuna frente al papilomavirus humano. (Comentarios a las fichas técnicas)
 Vacuna frente al papilomavirus humano (Comentarios a las fichas técnicas) Prof. Ángel Gil de Miguel, Catedrático de Medicina Preventiva y Salud Pública, Universidad Rey Juan Carlos, Comunidad de Madrid
Vacuna frente al papilomavirus humano (Comentarios a las fichas técnicas) Prof. Ángel Gil de Miguel, Catedrático de Medicina Preventiva y Salud Pública, Universidad Rey Juan Carlos, Comunidad de Madrid
INFORMACIÓN PARA EL PRESCRIPTOR PUREGON Folitropina beta 300 UI/0,36 ml 600 UI/0,72 ml Solución inyectable - Vía subcutánea VENTA BAJO RECETA
 INFORMACIÓN PARA EL PRESCRIPTOR PUREGON Folitropina beta 300 UI/0,36 ml 600 UI/0,72 ml Solución inyectable - Vía subcutánea VENTA BAJO RECETA Exclusivamente diseñado para ser utilizado en combinación con
INFORMACIÓN PARA EL PRESCRIPTOR PUREGON Folitropina beta 300 UI/0,36 ml 600 UI/0,72 ml Solución inyectable - Vía subcutánea VENTA BAJO RECETA Exclusivamente diseñado para ser utilizado en combinación con
Lea todo el prospecto antes de empezar a usar el medicamento.
 Lea todo el prospecto antes de empezar a usar el medicamento. - Conserve este prospecto. Puede tener que volver a leerlo. - Si tiene alguna duda, consulte a su médico o farmacéutico. - Este medicamento
Lea todo el prospecto antes de empezar a usar el medicamento. - Conserve este prospecto. Puede tener que volver a leerlo. - Si tiene alguna duda, consulte a su médico o farmacéutico. - Este medicamento
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Puregon 50 UI/0,5 ml solución inyectable Puregon 75 UI/0,5 ml solución inyectable Puregon 100 UI/0,5 ml solución
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Puregon 50 UI/0,5 ml solución inyectable Puregon 75 UI/0,5 ml solución inyectable Puregon 100 UI/0,5 ml solución
Informe Público de Evaluación
 REF. PTE. AUTORIZACIÓN Informe Público de Evaluación SULFATO DE MAGNESIO GENFARMA 150 mg/ml Solución inyectable y para perfusión Este documento resume cómo ha evaluado la Productos Sanitarios (AEMPS) los
REF. PTE. AUTORIZACIÓN Informe Público de Evaluación SULFATO DE MAGNESIO GENFARMA 150 mg/ml Solución inyectable y para perfusión Este documento resume cómo ha evaluado la Productos Sanitarios (AEMPS) los
momento en que nosotros lo consideremos necesario (día de la inseminación). El día de la inseminación, el marido entregará en el laboratorio una
 INSEMINACIOŃ INTRAUTERINA (IIU) La inseminación intrauterina es un procedimiento que se realiza desde tiempos tan remotos como el siglo III y que tiene como finalidad ayudar a las parejas a obtener un
INSEMINACIOŃ INTRAUTERINA (IIU) La inseminación intrauterina es un procedimiento que se realiza desde tiempos tan remotos como el siglo III y que tiene como finalidad ayudar a las parejas a obtener un
1 HORMONA FOLICULOEsTIMULANTE
 1 HORMONA FOLICULOEsTIMULANTE J. Herrero, A. Bernabeu y A. Voskuilen Puntos clave La hormona foliculoestimulante (FSH) es una gonadotropina de origen hipofisario que actúa sobre las células de la granulosa
1 HORMONA FOLICULOEsTIMULANTE J. Herrero, A. Bernabeu y A. Voskuilen Puntos clave La hormona foliculoestimulante (FSH) es una gonadotropina de origen hipofisario que actúa sobre las células de la granulosa
ANEXO 1 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO 1 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Ovitrelle 250 microgramos polvo y disolvente para solución inyectable. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
ANEXO 1 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Ovitrelle 250 microgramos polvo y disolvente para solución inyectable. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
Estimulación ideal en donantes de ovocitos. Dra. Mónica Álvarez Grupo de Interés de Endocrinología
 Estimulación ideal en donantes de ovocitos Dra. Mónica Álvarez Grupo de Interés de Endocrinología Introducción Incremento de la demanda de donación de ovocitos. Edad media al nacimiento del primer hijo
Estimulación ideal en donantes de ovocitos Dra. Mónica Álvarez Grupo de Interés de Endocrinología Introducción Incremento de la demanda de donación de ovocitos. Edad media al nacimiento del primer hijo
Registro FIV-ICSI de la Sociedad Española de Fertilidad. Año 2008
 Registro SEF Registro FIV-ICSI de la Sociedad Española de Fertilidad. Año 2008 Informe estadístico final Abril 2010 2 Análisis estadístico final INDICE 1 Introducción 5 2 Número de ciclos 5 3 Ciclos de
Registro SEF Registro FIV-ICSI de la Sociedad Española de Fertilidad. Año 2008 Informe estadístico final Abril 2010 2 Análisis estadístico final INDICE 1 Introducción 5 2 Número de ciclos 5 3 Ciclos de
ANEXO I RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. DENOMINACIÓN DEL MEDICAMENTO Luveris 75 UI, polvo y disolvente para solución inyectable. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un vial contiene
ANEXO I RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. DENOMINACIÓN DEL MEDICAMENTO Luveris 75 UI, polvo y disolvente para solución inyectable. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Un vial contiene
LA IMPORTANCIA DE LOS COMPLEJOS POLIVITAMINICOS. Esfuerzos intelectuales o de concentración mental. Dietas alimenticias para la reducción de peso
 X albintil jarabe LA IMPORTANCIA DE LOS COMPLEJOS POLIVITAMINICOS Las vitaminas son sustancias orgánicas no energéticas que nuestro organismo necesita para el normal desarrollo de su metabolismo. Debido
X albintil jarabe LA IMPORTANCIA DE LOS COMPLEJOS POLIVITAMINICOS Las vitaminas son sustancias orgánicas no energéticas que nuestro organismo necesita para el normal desarrollo de su metabolismo. Debido
REVISIÓN DE LOS ESTÁNDARES EN LA ATENCIÓN MÉDICA EN DIABETES 2013 POR LA ADA EN RELACIÓN A LAS 2012.
 REVISIÓN DE LOS ESTÁNDARES EN LA ATENCIÓN MÉDICA EN DIABETES 2013 POR LA ADA EN RELACIÓN A LAS 2012. Además de pequeños cambios relacionados a las nuevas evidencias, y para aclarar las recomendaciones,
REVISIÓN DE LOS ESTÁNDARES EN LA ATENCIÓN MÉDICA EN DIABETES 2013 POR LA ADA EN RELACIÓN A LAS 2012. Además de pequeños cambios relacionados a las nuevas evidencias, y para aclarar las recomendaciones,
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO. CUNISER 500 Gonadotropina sérica equina (PMSG), en polvo y disolvente para solución inyectable.
 RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO CUNISER 500 Gonadotropina sérica equina (PMSG), en polvo y disolvente para solución inyectable. 2. COMPOSICIÓN CUALITATIVA
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO CUNISER 500 Gonadotropina sérica equina (PMSG), en polvo y disolvente para solución inyectable. 2. COMPOSICIÓN CUALITATIVA
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 Este medicamento está sujeto a seguimiento adicional, lo que agilizará la detección de nueva información sobre su seguridad. Se invita
ANEXO I FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 Este medicamento está sujeto a seguimiento adicional, lo que agilizará la detección de nueva información sobre su seguridad. Se invita
INFORME A LA COMISIÓN DE FARMACIA Y TERAPÉUTICA ( 06/ 10/ 2008) INSULINAS
 Centro de Información de Medicamentos. Servicio de Farmacia. INFORME A LA COMISIÓN DE FARMACIA Y TERAPÉUTICA ( 06/ 10/ 2008) Datos del solicitante INSULINAS Dr. Pedro José Pines Corrales, FEA del servicio
Centro de Información de Medicamentos. Servicio de Farmacia. INFORME A LA COMISIÓN DE FARMACIA Y TERAPÉUTICA ( 06/ 10/ 2008) Datos del solicitante INSULINAS Dr. Pedro José Pines Corrales, FEA del servicio
FICHA TÉCNICA. MENCEVAX AC es una preparación liofilizada de polisacáridos purificados de Neisseria meningitidis (meningococo) de los grupos A y C.
 FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. MENCEVAX AC Vacuna de polisacáridos meningocócicos, grupos A y C. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA. MENCEVAX AC es una preparación liofilizada de polisacáridos
FICHA TÉCNICA 1. NOMBRE DEL MEDICAMENTO. MENCEVAX AC Vacuna de polisacáridos meningocócicos, grupos A y C. 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA. MENCEVAX AC es una preparación liofilizada de polisacáridos
Hipersensibilidad conocida a penciclovir, famciclovir o a los otros componentes de la formulación, por ejemplo propilenglicol.
 1. NOMBRE DEL MEDICAMENTO Penciclovir Beecham bomba dosificadora Penciclovir Beecham crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio activo: Penciclovir al 1% DCI: penciclovir 3. FORMA FARMACÉUTICA
1. NOMBRE DEL MEDICAMENTO Penciclovir Beecham bomba dosificadora Penciclovir Beecham crema 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Principio activo: Penciclovir al 1% DCI: penciclovir 3. FORMA FARMACÉUTICA
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO. VETERIN ANESTRO 100 UI - 50 UI/ml POLVO Y DISOLVENTE PARA SOLUCIÓN INYECTABLE
 DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO VETERIN ANESTRO 100 UI - 50 UI/ml POLVO Y DISOLVENTE PARA
DEPARTAMENTO DE MEDICAMENTOS VETERINARIOS FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1. DENOMINACIÓN DEL MEDICAMENTO VETERINARIO VETERIN ANESTRO 100 UI - 50 UI/ml POLVO Y DISOLVENTE PARA
POSICIONAMIENTO TERAPÉUTICO EN GUÍAS Y PROTOCOLOS CLÍNICOS
 POSICIONAMIENTO TERAPÉUTICO EN GUÍAS Y PROTOCOLOS CLÍNICOS Agradecimientos: F. Puigventos B. Calderón Javier Bautista Paloma Jefe de Servicio de Farmacia Hospital U. Virgen del Rocío DEFINICIÓN: El posicionamiento
POSICIONAMIENTO TERAPÉUTICO EN GUÍAS Y PROTOCOLOS CLÍNICOS Agradecimientos: F. Puigventos B. Calderón Javier Bautista Paloma Jefe de Servicio de Farmacia Hospital U. Virgen del Rocío DEFINICIÓN: El posicionamiento
Denominación (de fantasía) Mifepriston Linepharma. Mifepristone Linepharma. Mifepristone Linepharma 200 mg comprimé
 Anexo I Lista de las denominaciones (de fantasía), forma farmacéutica, dosis de los medicamentos, forma de administración, solicitantes/titulares de la autorización de comercialización en los Estados Miembros
Anexo I Lista de las denominaciones (de fantasía), forma farmacéutica, dosis de los medicamentos, forma de administración, solicitantes/titulares de la autorización de comercialización en los Estados Miembros
ANEXO 1 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
 ANEXO 1 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Ovitrelle 250 microgramos/0,5 ml, solución inyectable en jeringa precargada. 2. COMPOSICIÓN CUALITATIVA Y
ANEXO 1 FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO 1 1. NOMBRE DEL MEDICAMENTO Ovitrelle 250 microgramos/0,5 ml, solución inyectable en jeringa precargada. 2. COMPOSICIÓN CUALITATIVA Y
FICHA TÉCNICA PREÑATEC
 FICHA TÉCNICA PREÑATEC USO VETERINARIO 1. GENERALIDADES: a) Nombre comercial : PREÑATEC b) Clase de uso : Suplemento vitamínico y mineral c) Formulación : Solución inyectable d) Composición química : Cada
FICHA TÉCNICA PREÑATEC USO VETERINARIO 1. GENERALIDADES: a) Nombre comercial : PREÑATEC b) Clase de uso : Suplemento vitamínico y mineral c) Formulación : Solución inyectable d) Composición química : Cada
CABATINA Inyectable. Ficha Técnica
 CABATINA Inyectable ANTIHEMORRÁGICO. CABATINA INYECTABLE está indicada para el tratamiento inicial de emergencia de intoxicaciones agudas y sobreagudas generadas por rodenticidas anticoagulantes. Ficha
CABATINA Inyectable ANTIHEMORRÁGICO. CABATINA INYECTABLE está indicada para el tratamiento inicial de emergencia de intoxicaciones agudas y sobreagudas generadas por rodenticidas anticoagulantes. Ficha
LABORATORIOS NORMON, S.A. AMBROXOL NORMON 15 mg/5 ml Jarabe EFG
 1. NOMBRE DEL MEDICAMENTO 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada 5 ml de jarabe contienen: AMBROXOL (D.C.I.) hidrocloruro 15 mg Excipientes, ver apartado 6.1. 3. FORMA FARMACEUTICA Jarabe. 4. DATOS
1. NOMBRE DEL MEDICAMENTO 2. COMPOSICION CUALITATIVA Y CUANTITATIVA Cada 5 ml de jarabe contienen: AMBROXOL (D.C.I.) hidrocloruro 15 mg Excipientes, ver apartado 6.1. 3. FORMA FARMACEUTICA Jarabe. 4. DATOS
Orgalutran sólo debe ser recetado por un especialista con experiencia en el tratamiento de la esterilidad.
 1. NOMBRE DEL MEDICAMENTO Orgalutran 0,25 mg/0,5 ml solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada jeringa precargada contiene 0,25 mg de ganirelix en 0,5 ml de solución acuosa. El
1. NOMBRE DEL MEDICAMENTO Orgalutran 0,25 mg/0,5 ml solución inyectable 2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA Cada jeringa precargada contiene 0,25 mg de ganirelix en 0,5 ml de solución acuosa. El
Dr. MARCO GARNIQUE MONCADA. Jefe del Servicio de Medicina Reproductiva del INMP Ginecólogo Obstetra Máster en Reproducción Humana
 Dr. MARCO GARNIQUE MONCADA Jefe del Servicio de Medicina Reproductiva del INMP Ginecólogo Obstetra Máster en Reproducción Humana Folículo Estimulante. Desencadenan la Maduración final de los Ovocitos.
Dr. MARCO GARNIQUE MONCADA Jefe del Servicio de Medicina Reproductiva del INMP Ginecólogo Obstetra Máster en Reproducción Humana Folículo Estimulante. Desencadenan la Maduración final de los Ovocitos.
