Licenciatura en Química 1-7 Curso
|
|
|
- Eduardo Saavedra Quintero
- hace 7 años
- Vistas:
Transcripción
1 Licenciatura en Química 1-7 CÓDIGO: B053/99/7432 CURSO: Carga docente: 10 créditos (8 teóricos + 2 prácticos) Curso: 2º, Troncal Anual Departamento: Química Inorgánica Profesor/es: GA- Diego Cazorla Amorós - GB- Javier Narciso Romero OBJETIVOS 1. Presentar y discutir la química de los elementos que configuran la Tabla Periódica, en función de su posición en la misma, así como la de sus compuestos. 2. Integrar los hechos experimentales sobre propiedades de elementos y compuestos con conceptos introducidos en el curso anterior (p.ej. teorías de enlace) 3. Analizar y criticar distintos modelos utilizados para explicar las propiedades de los elementos químicos y sus compuestos. 4. Describir aplicaciones de los elementos químicos y sus compuestos, relacionándolas con sus propiedades químicas y físicas. PROGRAMA Teoría 1. Introducción. Introducción al curso. Contenidos de la Química Inorgánica. Evolución histórica. Campos de actividad en la actualidad. 2. Hidrógeno. Introducción. Estado natural. Isótopos. Propiedades físicas. Propiedades químicas. Reacciones. Métodos de preparación. Aplicaciones. 3. Elementos del Grupo 17. Halógenos. Introducción. Estado natural. Propiedades físicas. Propiedades químicas. Reacciones. Métodos de preparación. Aplicaciones. 4. Elementos del Grupo 16:(i) Oxígeno. Introducción. Estado natural. Propiedades físicas. Propiedades químicas. Reacciones. Métodos de preparación. Aplicaciones.Ozono. 5. Elementos del Grupo 16: (i)azufre, Selenio, Teluro y Polonio. Introducción. Estado natural. Formas moleculares y formas alotrópicas. Propiedades físicas. Propiedades químicas. Reactividad. Métodos de obtención. Aplicaciones 6. Elementos del Grupo 18: Gases nobles. Introducción. Estado natural. Propiedades físicas. Propiedades químicas. Separación. Aplicaciones. Compuestos de los gases nobles. 7. Elementos del Grupo 15:(i) Nitrógeno. Introducción. Estado natural. Propiedades físicas. Propiedades químicas. Reacciones. Métodos de obtención. Aplicaciones. 8. Elementos del Grupo 15:(ii) Fósforo, Arsénico, Antimonio y bismuto. Introducción. Estado natural. Propiedades físicas. Formas alotrópicas del arsénico, antimonio y bismuto.propiedades químicas y reacciones. Métodos de preparación. Aplicaciones 9. Elementos del Grupo 14:Carbono, Silicio,Germanio, Estaño y Plomo. Introducción. Estado natural. Formas alotrópicas del carbono. Formas de baja cristalinidad. Formas alotrópicas del silicio, germanio y estaño. Propiedades químicas. Métodos de obtención. Aplicaciones 10. Elementos del Grupo 13:Boro, Aluminio, Galio, Indio y Talio. Introducción. Estado natural. Formas alotrópicas del boro. Estructuras de los restantes elementos. Propiedades físicas. Propiedades químicas: tendencias en el grupo. Métodos de preparación. Aplicaciones 11. Hidruros moleculares. Características generales. Introducción. Naturaleza del enlace. Propiedades físicas. Enlace de hidrógeno. Propiedades químicas.
2 Licenciatura en Química Haluros de hidrógeno. Introducción. Propiedades físicas. Propiedades químicas. Métodos de preparación. Aplicaciones. 13. Combinaciones hidrogenadas de los elementos del Grupo 16: Agua y Peróxido de Hidrógeno. Introducción. Agua: enlace, propiedades físicas y químicas, diagramas de Latimer y Frost. Peróxido de hidrógeno:enlace, propiedades físicas y químicas, preparación y aplicaciones. Sulfuro de hidrógeno y polisulfanos. 14. Combinaciones hidrogenadas de los elementos del Grupo 15. Amoniaco, hidracina e hidroxilamina. Introducción. Hidruros mono- y polinucleares. Amoniaco. Hidracina. Hidroxilamina. 15. Hidruros del grupo 13. Hidruros de boro: Introducción. Clasificación y nomenclatura. Reglas de Wade. Hidruros de boro neutros (boranos). Hidruros aniónicos. Carboranos. 16. Combinaciones halogenadas de los elementos del Bloque p. Introducción. Combinaciones interhalógeno. Combinaciones halogenadas de los elementos del grupo Compuestos oxigenados de los halógenos..introducción. Óxidos: estructura, enlace y propiedades. Oxoácidos y oxosales: estructura, enlace propiedades químicas, métodos de obtención y aplicaciones. 18. Compuestos oxigenados de los elementos del Grupo 16. Introducción. Óxidos de azufre: estructura, enlace, propiedades, preparación y aplicaciones. Oxoácidos y oxosales de azufre: estructura, enlace, propiedades, preparación y aplicaciones 19. Compuestos oxigenados del nitrógeno. Introducción. Óxidos: estructura, enlace, propiedades, preparación y aplicaciones. Oxoácidos y oxosales: estructura, enlace, propiedades, preparación y aplicaciones. 20. Compuestos oxigenados del fósforo. Introducción. Óxidos: estructura y propiedades. Oxoácidos y oxosales: estructura y propiedades. Ácido fosfórico y fosfatos: obtención y aplicaciones. 21. Compuestos oxigenados de los elementos del Grupo 14.Introducción Óxidos de carbono: estructura, enlace, propiedades y aplicaciones. Ácido carbónico y carbonatos: propiedades ácido-bae, obtención y aplicaciones. 22. Metales. Estado natural y distribución de los metales: obtención y purificación de metales. 23. Metales alcalinos (Grupo 1). Introducción. Estado natural.propiedades físicas. Propiedades químicas. Reacciones. Métodos de preparación. Aplicaciones. 24. Metales alcalinotérreos (Grupo 2). Introducción. Estado natural.propiedades físicas. Propiedades químicas. Reacciones. Métodos de preparación. Aplicaciones. 25. Metales del Grupo 12. Introducción. Estado natural. Propiedades químicas. Métodos de obtención y aplicaciones. 26. Metales de transición de la primera serie (3d).Introducción. Estado natural. Propiedades químicas. Métodos de obtención y purificación. Aplicaciones. 27. Metales de transición de la segunda y tercera series (4d y 5d).Introducción.Estado natural. Propiedades químicas. Aplicaciones. 28. Metales del Grupo 3 y Lantánidos. Introducción. Estado natural. Propiedades químicas. Métodos de obtención. Aplicaciones. 29. Actínidos. Introducción. Estado natural. Propiedades químicas. Estudio específico de torio, uranio y plutonio. Seminarios: Química Inorgánica Industrial.Visionado de vídeos y discusión. Aplicaciones industriales de la sal: Industria cloro-álcali. Procesos de obtención de metales:hierro, acero, alumnio y titanio. Prácticas:
3 Licenciatura en Química Diagramas de Latimer y Frost. 2. Elaboración de un tema monográfico mediante consulta de páginas web. 3. Diagramas de Ellingham. 4. Preparación de cromo mediante reducción del óxido de cromo (III). Construir un diagrama de Ellingham para los pares C/CO, Al/Al2O3 y Cr/Cr2O3. Deducir las condiciones en las que la reducción de un óxido metálico a metal son espontáneas (termodinámicamente favorables). Obtener cromo por reducción del Cr2O3 con alumnio. 5. Química de los elementos metálicos. Química del hierro. Química del cobre. Química del níquel. OBSERVACIONES Evaluación: Un examen escrito conteniendo entre 10 y 15 preguntas relativamente breves en las que el alumno debe demostrar el conocimiento de los principios básicos aprendidos a lo largo del curso. Se valorará el informe de las prácticas realizadas. BIBLIOGRAFIA Basic Inorganic chemistry, Cotton, F.A., Wilkinson, G.y Gaus, P.L (2ª ed.) John Wiley and Sons Química Inorgánica. Gutierrez Rios, E. (2ª ed.) Ed. Reverté The Metallic elements, Parish, R.V. Longman Química Inorgánica. Introducción a la química de Coordinación, del Estado Sólido y Descriptiva, McGraw-Hill.1995 Industrial Inorganic Chemistry, Büchner, W., Schliebs, R. Winter, G. y Büchel, K. H.. Verlag Chemie Concepts and Models of Inorganic Chemistry. Douglas, B.E., McDaniel,D.H. y Alexander, J.J. (3ª ed.) John Wiley & sons.1994 Inorganic Chemistry.Shriver, D.F., Atkins, P.W. y Langford C.H..(2ª ed) Oxford University Press Chemistry of the Elements Greeenwood, N.N., y Earnshaw A. Pergamon Press Advanced Inorganic chemistry. Cotton,F.A. y Wilkinson G. (5ª ed.) John Wiley & Sons
4 Licenciatura en Química 4-7 QUIMICA INORGANICA CÓDIGO: 7432 CURSO: Carga docente: 10 créditos (8 teóricos + 2 prácticos) (anual) Departamento: Química Inorgánica Profesor/es: GA- Diego Cazorla Amorós - GB- Javier Narciso Romero OBJETIVOS 1. Presentar y discutir la química de los elementos que configuran la Tabla Periódica, en función de su posición en la misma, así como la de sus compuestos. 2. Integrar los hechos experimentales sobre propiedades de elementos y compuestos con conceptos introducidos en el curso anterior (p.ej. teorías de enlace) 3. Analizar y criticar distintos modelos utilizados para explicar las propiedades de los elementos químicos y sus compuestos. 4. Describir aplicaciones de los elementos químicos y sus compuestos, relacionándolas con sus propiedades químicas y físicas PROGRAMA Teoría 1. Introducción.. 2. Hidrógeno. 3. Elementos del Grupo 17. Halógenos.. 4. Elementos del Grupo 16:(i) Oxígeno. 5. Elementos del Grupo 16: (i)azufre, Selenio, Teluro y Polonio. 6. Elementos del Grupo 18: Gases nobles.. 7. Elementos del Grupo 15:(i) Nitrógeno. 8. Elementos del Grupo 15:(ii) Fósforo, Arsénico, Antimonio y bismuto. 9. Elementos del Grupo 14:Carbono, Silicio,Germanio, Estaño y Plomo. 10. Elementos del Grupo 13:Boro, Aluminio, Galio, Indio y Talio. 11. Hidruros moleculares. Características generales. 12. Haluros de hidrógeno Combinaciones hidrogenadas de los elementos del Grupo 16: Agua y Peróxido de Hidrógeno Combinaciones hidrogenadas de los elementos del Grupo 15. Amoniaco, hidracina e hidroxilamina. 15. Hidruros del grupo Combinaciones halogenadas de los elementos del Bloque p Compuestos oxigenados de los halógenos Compuestos oxigenados de los elementos del Grupo Compuestos oxigenados del nitrógeno. 20. Compuestos oxigenados del fósforo Compuestos oxigenados de los elementos del Grupo Metales. Estado natural y distribución de los metales: obtención y purificación de metales. 23. Metales alcalinas (Grupo 1). 24. Metales alcalinotérreos (Grupo 2). 25. Metales del Grupo Metales de transición de la primera serie (3d) Metales de transición de la segunda y tercera series (4d y 5d). 28. Metales del Grupo 3 y Lantánidos Actínidos. Seminarios: 1. Química Inorgánica Industrial.. Prácticas: 1. Diagramas de Latimer y Frost 2. Elaboración de un tema monográfico mediante consulta de páginas web. 3. Diagramas de Ellingham 4. Preparación de cromo mediante reducción del óxido de cromo (III). 5. Química de los elementos metálicos. OBSERVACIONES Evaluación: Un examen escrito conteniendo entre 10 y 15 preguntas relativamente breves en las que el alumno debe demostrar el conocimiento de los principios básicos aprendidos a lo largo del curso. Se valorará el informe de las prácticas realizadas. BIBLIOGRAFIA Basic Inorganic chemistry, Cotton, F.A., Wilkinson, G.y Gaus, P.L (2ª ed.) John Wiley and Sons Química Inorgánica. Gutierrez Rios, E. (2ª ed.) Ed. Reverté The Metallic elements, Parish, R.V. Longman. 1997
5 Licenciatura en Química 5-7 Química Inorgánica. Introducción a la química de Coordinación, del Estado Sólido y Descriptiva, McGraw-Hill.1995 Industrial Inorganic Chemistry, Büchner, W., Schliebs, R. Winter, G. y Büchel, K. H.. Verlag Chemie Concepts and Models of Inorganic Chemistry. Douglas, B.E., McDaniel,D.H. y Alexander, J.J. (3ª ed.) John Wiley & sons.1994 Inorganic Chemistry.Shriver, D.F., Atkins, P.W. y Langford C.H..(2ª ed) Oxford University Press Chemistry of the Elements Greeenwood, N.N., y Earnshaw A. Pergamon Press Advanced Inorganic chemistry. Cotton,F.A. y Wilkinson G. (5ª ed.) John Wiley & Sons
6 Licenciatura en Química 6-7 INORGANIC CHEMISTRY CODE: 7432 ACADEMIC YEAR: Credits: 10 credits (8 theoretical + 2 practical) Department: Inorganic Chemistry Lecturer/s: GA- Diego Cazorla Amorós - GB- Javier Narciso Romero OBJECTIVES 1. Introduction and discussion of the chemistry of the elements in the Periodic Table, as a function of the position. The chemistry of the compounds is included. 2. To relate the experimental facts on properties of elements and compunds with the properties of the elements and their compounds. 3. To make a critical analysis of the different models used to explain the properties of the elements and their compounds. 4. To describe the main applications of the elemensts and their compounds, and relating them to their physical and chemical properties. PROGRAMME Theory 1. Introduction to Inorganic Chemistry. 2. Hydrogen. 3. Group 17: Halogens 4. Group 16:(i) Oxygen 5. Group 16:(ii) S, Se, Te, Po. 6. Group 18: Noble gases 7. Group 15:(i) Nitrogen 8. Group 15:(ii) P, As, Sb, Bi. 9. Group 14: C, Si, Ge, Sn, Pb. 10. Group 13: B, Al, Ga, In, Tl. 11. Covalent hydrides. General concepts. 12. Hydrogen halides. 13. Hydrides of elements of group 16: Water and Hydrogen Peroxide. 14. Hydrides of elements of group 15: Ammnonia, hydrazine, hydroxylaminne. 15. Hydrides of elements of group Halides of elements of block p. 17. Oxygen compounds of the halogens 18. Oxygen compounds of elements of group Oxygen compounds of nitrogen. 20. Oxygen compounds of phosphorous 21. Oxygen compounds of elements of group Metals. 23. Alkaline metals. 24. Alkaline-earth metals. 25. Group 12 metals. 26. First transition metals (3d). 27. Second and third transition series (4d and 4d) 28. Group 3 and lantanides. 29. Actinides. Seminars 1. Industrial Inorganic Chemistry. Experimentation 1. Latimer and Frost diagrams. 2. Preparation of a monograph using web pages. 3. Ellingham diagrams. 4. Synthesis of chromium by reduction of Cr(III). 5. Chemistry of the metallic alements. OBSERVATIONS
7 Licenciatura en Química 7-7 Previous knowledge: Chemical nomenclature, Periodic Table and those acquired in 24/ and 24/ Evaluation: Written examination containing a minimum of 10 and a maximum of 15 brief questions where their answers had to be justified by using the basic principles explained during the course. The report of the experimentation part will also be evaluated. BIBLIOGRAPHY Basic Inorganic chemistry, Cotton, F.A., Wilkinson, G.y Gaus, P.L (2ª ed.) John Wiley and Sons Química Inorgánica. Gutierrez Rios, E. (2ª ed.) Ed. Reverté The Metallic elements, Parish, R.V. Longman Química Inorgánica. Introducción a la química de Coordinación, del Estado Sólido y Descriptiva, McGraw-Hill.1995 Industrial Inorganic Chemistry, Büchner, W., Schliebs, R. Winter, G. y Büchel, K. H.. Verlag Chemie Concepts and Models of Inorganic Chemistry. Douglas, B.E., McDaniel,D.H. y Alexander, J.J. (3ª ed.) John Wiley & sons.1994 Inorganic Chemistry.Shriver, D.F., Atkins, P.W. y Langford C.H..(2ª ed) Oxford University Press Chemistry of the Elements Greeenwood, N.N., y Earnshaw A. Pergamon Press Advanced Inorganic chemistry. Cotton,F.A. y Wilkinson G. (5ª ed.) John Wiley & Sons
Licenciado en Química 1 de 7 QUÍMICA INORGÁNICA
 Licenciado en Química 1 de 7 CÓDIGO: 24/93-0204 CURSO: 1999-2000 Carga docente: 9.5 créditos (7,5 teóricos + 2 prácticos) (primer cuatrimestre) Departamento: Química Inorgánica Profesor/es: GA- Mª José
Licenciado en Química 1 de 7 CÓDIGO: 24/93-0204 CURSO: 1999-2000 Carga docente: 9.5 créditos (7,5 teóricos + 2 prácticos) (primer cuatrimestre) Departamento: Química Inorgánica Profesor/es: GA- Mª José
ESTRUCTURA Y PROPIEDADES DE LA MATERIA
 Ingeniería Química 1-5 CÓDIGO: 19/96/3018 CURSO: 2000-2001 B052/99/7345 CURSO: 2000-2001 Carga docente: 7 créditos (4,5 teóricos + 2,5prácticos) Curso. 1º Primer cuatrimestre Departamento: Química Inorgánica
Ingeniería Química 1-5 CÓDIGO: 19/96/3018 CURSO: 2000-2001 B052/99/7345 CURSO: 2000-2001 Carga docente: 7 créditos (4,5 teóricos + 2,5prácticos) Curso. 1º Primer cuatrimestre Departamento: Química Inorgánica
3. Estudiar la química de los elementos de transición, con especial énfasis en la
 Ingeniería Química 1-5 CÓDIGO: B052/99/7345 CURSO: 2003-2004 Carga docente: 7 créditos (4,5 teóricos + 2,5prácticos) Curso: 1º, Obligatoria Primer cuatrimestre Departamento: Química Inorgánica Profesor/es:
Ingeniería Química 1-5 CÓDIGO: B052/99/7345 CURSO: 2003-2004 Carga docente: 7 créditos (4,5 teóricos + 2,5prácticos) Curso: 1º, Obligatoria Primer cuatrimestre Departamento: Química Inorgánica Profesor/es:
QUIMICA APLICADA EN LA INGENIERIA GEOLOGICA
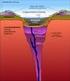 Ingeniería Geológica 1-5 CÓDIGO: B051/99/7491 CURSO: 2002-2003 Carga docente: 6 créditos (4,5 teóricos + 1,5 prácticos) Curso: 1º, Troncal Segundo cuatrimestre Departamento: Química Inorgánica Profesor/es:
Ingeniería Geológica 1-5 CÓDIGO: B051/99/7491 CURSO: 2002-2003 Carga docente: 6 créditos (4,5 teóricos + 1,5 prácticos) Curso: 1º, Troncal Segundo cuatrimestre Departamento: Química Inorgánica Profesor/es:
Programa de la asignatura Curso: 2007 / 2008 QUÍMICA INORGÁNICA (1229)
 Programa de la asignatura Curso: 2007 / 2008 QUÍMICA INORGÁNICA (1229) PROFESORADO Profesor/es: JOSE VICENTE CUEVAS VICARIO - correo-e: jvcv@ubu.es JAVIER GARCIA TOJAL - correo-e: qipgatoj@ubu.es FICHA
Programa de la asignatura Curso: 2007 / 2008 QUÍMICA INORGÁNICA (1229) PROFESORADO Profesor/es: JOSE VICENTE CUEVAS VICARIO - correo-e: jvcv@ubu.es JAVIER GARCIA TOJAL - correo-e: qipgatoj@ubu.es FICHA
ASIGNATURA: QUÍMICA INORGÁNICA
 Página 1 de 6 CARACTERÍSTICAS GENERALES* Tipo: DESCRIPCIÓN Formación básica, Obligatoria, Optativa Trabajo de fin de grado, Prácticas externas Duración: Anual Semestre/s: 3 y 4 Número de créditos ECTS:
Página 1 de 6 CARACTERÍSTICAS GENERALES* Tipo: DESCRIPCIÓN Formación básica, Obligatoria, Optativa Trabajo de fin de grado, Prácticas externas Duración: Anual Semestre/s: 3 y 4 Número de créditos ECTS:
Ejercicios y respuestas del apartado: Tabla periódica. Grupos y períodos. Metales, no metales y gases nobles
 Ejercicios y respuestas del apartado: Tabla periódica. Grupos y períodos. Metales, no metales y gases nobles Elementos de la tabla periódica (1) 1. Grupo de los halógenos: ---------> Símbolos: (1), (2),
Ejercicios y respuestas del apartado: Tabla periódica. Grupos y períodos. Metales, no metales y gases nobles Elementos de la tabla periódica (1) 1. Grupo de los halógenos: ---------> Símbolos: (1), (2),
DATOS BÁSICOS DE LA ASIGNATURA DATOS BÁSICOS DE LOS PROFESORES DATOS ESPECÍFICOS DE LA ASIGNATURA
 DATOS BÁSICOS DE LA ASIGNATURA #$%&'( )* +$(, $( -.$*/-#*0,1* $0( '2*,$0(,, /'1 3 ",0 " 1'0$( 1-,' %0,'( /$( DATOS BÁSICOS DE LOS PROFESORES #$%&'( #,'$4*-',-%#,$( 5'-( #**0-6$(!%- /( 1'/8&(,/27$#$(! DATOS
DATOS BÁSICOS DE LA ASIGNATURA #$%&'( )* +$(, $( -.$*/-#*0,1* $0( '2*,$0(,, /'1 3 ",0 " 1'0$( 1-,' %0,'( /$( DATOS BÁSICOS DE LOS PROFESORES #$%&'( #,'$4*-',-%#,$( 5'-( #**0-6$(!%- /( 1'/8&(,/27$#$(! DATOS
ASIGNATURA: QUÍMICA INORGÁNICA
 Página 1 de 7 CARACTERÍSTICAS GENERALES* Tipo: Formación básica, Obligatoria, Optativa Trabajo de fin de grado, Prácticas externas Duración: Anual Semestre/s: 3 y 4 Número de créditos ECTS: 12 Idioma/s:
Página 1 de 7 CARACTERÍSTICAS GENERALES* Tipo: Formación básica, Obligatoria, Optativa Trabajo de fin de grado, Prácticas externas Duración: Anual Semestre/s: 3 y 4 Número de créditos ECTS: 12 Idioma/s:
GUÍA DOCENTE DE ASIGNATURA CURSO 2008/2009
 GUÍA DOCENTE DE ASIGNATURA CURSO 2008/2009 1. DATOS BÁSICOS DE LA ASIGNATURA 1.1.Nombre Química Inorgánica 1.3. Código 5002104 1.4.Plan 2000 1.7. Curso de la Titulación 1.11. Créditos ECTS Organización
GUÍA DOCENTE DE ASIGNATURA CURSO 2008/2009 1. DATOS BÁSICOS DE LA ASIGNATURA 1.1.Nombre Química Inorgánica 1.3. Código 5002104 1.4.Plan 2000 1.7. Curso de la Titulación 1.11. Créditos ECTS Organización
Química Inorgánica I
 GUÍA DOCENTE 2010-2011 Química Inorgánica I 1. Denominación de la asignatura: Química Inorgánica I Código 2. Materia o módulo a la que pertenece la asignatura: Química Inorgánica 3. Departamento(s) responsable(s)
GUÍA DOCENTE 2010-2011 Química Inorgánica I 1. Denominación de la asignatura: Química Inorgánica I Código 2. Materia o módulo a la que pertenece la asignatura: Química Inorgánica 3. Departamento(s) responsable(s)
1. ASIGNATURA / COURSE
 1. ASIGNATURA / COURSE 1.1. Nombre / Course Title QUÍMICA INORGÁNICA / INORGANIC CHEMISTRY 1.2. Código / Course Code 12693 1.3. Tipo / Type of course Troncal/Compulsory 1.4. Nivel / Level of course Grado
1. ASIGNATURA / COURSE 1.1. Nombre / Course Title QUÍMICA INORGÁNICA / INORGANIC CHEMISTRY 1.2. Código / Course Code 12693 1.3. Tipo / Type of course Troncal/Compulsory 1.4. Nivel / Level of course Grado
QUÍMICA DE LOS ELEMENTOS NO METÁLICOS
 ASIGNATURA DE GRADO: QUÍMICA DE LOS ELEMENTOS NO METÁLICOS Curso 2015/2016 (Código:61032043) 1.PRESENTACIÓN DE LA ASIGNATURA La asignatura que nos ocupa Química de los elementos no metálicos es de carácter
ASIGNATURA DE GRADO: QUÍMICA DE LOS ELEMENTOS NO METÁLICOS Curso 2015/2016 (Código:61032043) 1.PRESENTACIÓN DE LA ASIGNATURA La asignatura que nos ocupa Química de los elementos no metálicos es de carácter
UNIVERSIDAD DE LOS ANDES Departamento de Química
 UNIVERSIDAD DE LOS ANDES Departamento de Química QUIMICA INORGANICA I - TEORIA - Código: QUIM 1201. Créditos: 3. Horario: Martes, Miércoles, Jueves y Viernes de 10:00 a.m. 10:50 a.m. en el salón AU-310
UNIVERSIDAD DE LOS ANDES Departamento de Química QUIMICA INORGANICA I - TEORIA - Código: QUIM 1201. Créditos: 3. Horario: Martes, Miércoles, Jueves y Viernes de 10:00 a.m. 10:50 a.m. en el salón AU-310
TITULACIÓN: GRADO EN QUÍMICA CENTRO: FACULTAD DE CIENCIAS EXPERIMENTALES CURSO ACADÉMICO: GUÍA DOCENTE
 TITULACIÓN: GRADO EN QUÍMICA CENTRO: FACULTAD DE CIENCIAS EXPERIMENTALES CURSO ACADÉMICO: 2011-2012 GUÍA DOCENTE 1. DATOS BÁSICOS DE LA ASIGNATURA NOMBRE: Química Inorgánica I CÓDIGO: 10312009 CURSO ACADÉMICO:
TITULACIÓN: GRADO EN QUÍMICA CENTRO: FACULTAD DE CIENCIAS EXPERIMENTALES CURSO ACADÉMICO: 2011-2012 GUÍA DOCENTE 1. DATOS BÁSICOS DE LA ASIGNATURA NOMBRE: Química Inorgánica I CÓDIGO: 10312009 CURSO ACADÉMICO:
TIPO: T CURSO: 2º SEMESTRE:1º y 2º CRÉDITOS (horas/semana): 9.0 CRÉDITOS ECTS: 7.5 PROFESOR: Dr. Jordi Abellà Iglesias IDIOMA: Castellano / Català
 22015 QUÍMICA INORGÁNICA Pág 1 de 7 ASIGNATURA: Química Inorgánica ESTUDIOS: INGENIERÍA QUÍMICA (1 er Ciclo) CÓDIGO: 22015 TIPO: T CURSO: 2º SEMESTRE:1º y 2º CRÉDITOS (horas/semana): 9.0 CRÉDITOS ECTS:
22015 QUÍMICA INORGÁNICA Pág 1 de 7 ASIGNATURA: Química Inorgánica ESTUDIOS: INGENIERÍA QUÍMICA (1 er Ciclo) CÓDIGO: 22015 TIPO: T CURSO: 2º SEMESTRE:1º y 2º CRÉDITOS (horas/semana): 9.0 CRÉDITOS ECTS:
Guía docente de la asignatura Química Inorgánica
 Guía docente de la asignatura Química Inorgánica Titulación: Grado en Ingeniería Química Industrial Curso 2010/2011 Guía Docente 1. Datos de la asignatura Nombre Materia Módulo Química Inorgánica Química
Guía docente de la asignatura Química Inorgánica Titulación: Grado en Ingeniería Química Industrial Curso 2010/2011 Guía Docente 1. Datos de la asignatura Nombre Materia Módulo Química Inorgánica Química
GUÍA DOCENTE Química Inorgánica I
 GUÍA DOCENTE 2015-2016 Química Inorgánica I 1. Denominación de la asignatura: Química Inorgánica I Titulación Grado en Química Código 5273 2. Materia o módulo a la que pertenece la asignatura: Química
GUÍA DOCENTE 2015-2016 Química Inorgánica I 1. Denominación de la asignatura: Química Inorgánica I Titulación Grado en Química Código 5273 2. Materia o módulo a la que pertenece la asignatura: Química
PONTIFICIA UNIVERSIDAD CATOLICA DEL ECUADOR FACULTAD DE CIENCIAS EXACTAS Y NATURALES ESCUELA DE CIENCIAS QUÍMICAS
 PONTIFICIA UNIVERSIDAD CATOLICA DEL ECUADOR FACULTAD DE CIENCIAS EXACTAS Y NATURALES ESCUELA DE CIENCIAS QUÍMICAS 1.- DATOS INFORMATIVOS: Materia: Química Inorgánica Carrera: Química Analítica Nivel: Segundo
PONTIFICIA UNIVERSIDAD CATOLICA DEL ECUADOR FACULTAD DE CIENCIAS EXACTAS Y NATURALES ESCUELA DE CIENCIAS QUÍMICAS 1.- DATOS INFORMATIVOS: Materia: Química Inorgánica Carrera: Química Analítica Nivel: Segundo
Denominación: QUIMICA INORGANICA Código: 57206
 L ICENCIADO EN Q UÍMICAS. C URSO 2007-08. DATOS DE LA ASIGNATURA Denominación: QUIMICA INORGANICA Código: 57206 Clase: TRONCAL Curso: 2 Carácter: ANUAL Cuatrimestre: 2 Créditos LRU: 12 Teóricos: 10 Prácticos:
L ICENCIADO EN Q UÍMICAS. C URSO 2007-08. DATOS DE LA ASIGNATURA Denominación: QUIMICA INORGANICA Código: 57206 Clase: TRONCAL Curso: 2 Carácter: ANUAL Cuatrimestre: 2 Créditos LRU: 12 Teóricos: 10 Prácticos:
GUIA DOCENTE DE LA ASIGNATURA DESCRIPTION OF INDIVIDUAL COURSE UNIT. Complemento de Química Inorgánica. Grado. Licenciatura en Química.
 GUIA DOCENTE DE LA ASIGNATURA DESCRIPTION OF INDIVIDUAL COURSE UNIT Nombre de la asignatura/módulo/unidad y código Course title and code Nivel (Grado/Postgrado) Level of course (Undergraduate/ Postgraduate)
GUIA DOCENTE DE LA ASIGNATURA DESCRIPTION OF INDIVIDUAL COURSE UNIT Nombre de la asignatura/módulo/unidad y código Course title and code Nivel (Grado/Postgrado) Level of course (Undergraduate/ Postgraduate)
PONTIFICIA UNIVERSIDAD CATOLICA DEL ECUADOR FACULTAD DE CIENCIAS EXACTAS Y NATURALES ESCUELA DE CIENCIAS QUÍMICAS
 PONTIFICIA UNIVERSIDAD CATOLICA DEL ECUADOR FACULTAD DE CIENCIAS EXACTAS Y NATURALES ESCUELA DE CIENCIAS QUÍMICAS 1.- DATOS INFORMATIVOS: MATERIA: Química Inorgánica, T y L CÓDIGO: 12799 CARRERA: Ciencias
PONTIFICIA UNIVERSIDAD CATOLICA DEL ECUADOR FACULTAD DE CIENCIAS EXACTAS Y NATURALES ESCUELA DE CIENCIAS QUÍMICAS 1.- DATOS INFORMATIVOS: MATERIA: Química Inorgánica, T y L CÓDIGO: 12799 CARRERA: Ciencias
CIENCIA DE LOS MATERIALES DE CARBÓN
 Licenciatura en Química 1-7 CÓDIGO: B053/99/7465 CURSO: 2002-2003 Carga docente: 6 créditos (3 teóricos + 3 prácticos) Curso: Optativa Segundo cuatrimestre Departamento: Química Inorgánica Profesor/es:
Licenciatura en Química 1-7 CÓDIGO: B053/99/7465 CURSO: 2002-2003 Carga docente: 6 créditos (3 teóricos + 3 prácticos) Curso: Optativa Segundo cuatrimestre Departamento: Química Inorgánica Profesor/es:
QUIMICA 1RO INGENIERIA INDUSTRIAL Y DE SISTEMAS EJECUTIVO PLUS INGENIERIO: LEONOR BARRAZA MARCELA RAMIREZ SANCHEZ TEMA: TABLA PERIODICA Y SUS
 QUIMICA 1RO INGENIERIA INDUSTRIAL Y DE SISTEMAS EJECUTIVO PLUS INGENIERIO: LEONOR BARRAZA MARCELA RAMIREZ SANCHEZ TEMA: TABLA PERIODICA Y SUS CARACTERISTICAS LOS ALCALINOS Explica que son aquellos metales
QUIMICA 1RO INGENIERIA INDUSTRIAL Y DE SISTEMAS EJECUTIVO PLUS INGENIERIO: LEONOR BARRAZA MARCELA RAMIREZ SANCHEZ TEMA: TABLA PERIODICA Y SUS CARACTERISTICAS LOS ALCALINOS Explica que son aquellos metales
DISTRIBUCIÓN HORARIA DE LA ASIGNATURA SEGÚN NORMATIVA
 GUÍA DOCENTE CURSO: 2016-17 DATOS BÁSICOS DE LA ASIGNATURA Asignatura: Química Inorgánica I Código de asignatura: 50902207 Plan: Grado en Química (Plan 2009) Año académico: 2016-17 Ciclo formativo: Grado
GUÍA DOCENTE CURSO: 2016-17 DATOS BÁSICOS DE LA ASIGNATURA Asignatura: Química Inorgánica I Código de asignatura: 50902207 Plan: Grado en Química (Plan 2009) Año académico: 2016-17 Ciclo formativo: Grado
Plan Piloto de 2º Curso (EEES) Facultad de Ciencias Químicas UCLM Curso 2010/11 DATOS DE LA ASIGNATURA
 DATOS DE LA ASIGNATURA Denominación: QUIMICA INORGANICA Código: 57206 Clase: TRONCAL Curso: 2 Carácter: ANUAL Cuatrimestre: 2 Créditos LRU: 12 Teóricos: 10 Prácticos: 2 Créditos ECTS: 11.33 Horas totales
DATOS DE LA ASIGNATURA Denominación: QUIMICA INORGANICA Código: 57206 Clase: TRONCAL Curso: 2 Carácter: ANUAL Cuatrimestre: 2 Créditos LRU: 12 Teóricos: 10 Prácticos: 2 Créditos ECTS: 11.33 Horas totales
PONTIFICIA UNIVERSIDAD CATOLICA DEL ECUADOR FACULTAD DE CIENCIAS EXACTAS Y NATURALES ESCUELA DE CIENCIAS QUÍMICAS
 PONTIFICIA UNIVERSIDAD CATOLICA DEL ECUADOR FACULTAD DE CIENCIAS EXACTAS Y NATURALES ESCUELA DE CIENCIAS QUÍMICAS 1.- DATOS INFORMATIVOS: Materia: Química Inorgánica Carrera: Química Analítica Nivel: Segundo
PONTIFICIA UNIVERSIDAD CATOLICA DEL ECUADOR FACULTAD DE CIENCIAS EXACTAS Y NATURALES ESCUELA DE CIENCIAS QUÍMICAS 1.- DATOS INFORMATIVOS: Materia: Química Inorgánica Carrera: Química Analítica Nivel: Segundo
TITULACIÓN: LICENCIATURA EN QUÍMICA CURSO ACADÉMICO: GUÍA DOCENTE de QUIMICA INORGÁNICA
 TITULACIÓN: LICENCIATURA EN QUÍMICA CURSO ACADÉMICO: 2011-2012 GUÍA DOCENTE de QUIMICA INORGÁNICA DATOS BÁSICOS DE LA ASIGNATURA NOMBRE: QUÍMICA INORGÁNICA CÓDIGO: 3165 AÑO DE PLAN DE ESTUDIOS: 1995 adap.
TITULACIÓN: LICENCIATURA EN QUÍMICA CURSO ACADÉMICO: 2011-2012 GUÍA DOCENTE de QUIMICA INORGÁNICA DATOS BÁSICOS DE LA ASIGNATURA NOMBRE: QUÍMICA INORGÁNICA CÓDIGO: 3165 AÑO DE PLAN DE ESTUDIOS: 1995 adap.
QUIMICA INORGÁNICA I. Grupo A: Juan Manuel Salas Peregrín. Agustín Francisco Pérez Cadenas. Grupo B: José Rivera Utrilla
 GUIA DOCENTE DE LA ASIGNATURA: QUIMICA INORGÁNICA I MÓDULO MATERIA CURSO SEMESTRE CRÉDITOS TIPO Química Inorgánica PROFESOR(ES) Química Inorgánica I 2º 1º 6 Troncal DIRECCIÓN COMPLETA DE CONTACTO PARA
GUIA DOCENTE DE LA ASIGNATURA: QUIMICA INORGÁNICA I MÓDULO MATERIA CURSO SEMESTRE CRÉDITOS TIPO Química Inorgánica PROFESOR(ES) Química Inorgánica I 2º 1º 6 Troncal DIRECCIÓN COMPLETA DE CONTACTO PARA
EL SISTEMA PERIÓDICO
 EL SISTEMA PERIÓDICO CONTENIDOS. 1.- Primeras clasificaciones de los elementos químicos. 2.- Clasificaciones de Meyer y Mendeleiev. 3.- Clasificación actual de los elementos químicos. 4.- Tabla periódica
EL SISTEMA PERIÓDICO CONTENIDOS. 1.- Primeras clasificaciones de los elementos químicos. 2.- Clasificaciones de Meyer y Mendeleiev. 3.- Clasificación actual de los elementos químicos. 4.- Tabla periódica
1. Introducción 2. Configuración electrónica y clasificación periódica 3. Propiedades periódicas Cuestionario de orientación y problemas
 PRÓLOGO A LA PRIMERA EDICIÓN 13 PRÓLOGO A LA TERCERA EDICIÓN 15 CAPÍTULO 1 Estructura atómica 17 1. Introducción 2. Principales experimentos que contribuyeron al conocimiento de la estructura atómica 3.
PRÓLOGO A LA PRIMERA EDICIÓN 13 PRÓLOGO A LA TERCERA EDICIÓN 15 CAPÍTULO 1 Estructura atómica 17 1. Introducción 2. Principales experimentos que contribuyeron al conocimiento de la estructura atómica 3.
SEMEST RE MÓDULO MATERIA CURSO. Química Inorgánica I. 2º 1º 6 Troncal
 GUIA DOCENTE DE LA ASIGNATURA QUIMICA INORGÁNICA I Curso 2017-2018 (Fecha última actualización 07/06/2017) (Fecha de aprobación en Consejo de Departamento: 13/06/2017) MÓDULO MATERIA CURSO SEMEST RE CRÉDITOS
GUIA DOCENTE DE LA ASIGNATURA QUIMICA INORGÁNICA I Curso 2017-2018 (Fecha última actualización 07/06/2017) (Fecha de aprobación en Consejo de Departamento: 13/06/2017) MÓDULO MATERIA CURSO SEMEST RE CRÉDITOS
GUÍA DOCENTE QUÍMICA INORGÁNICA. Curso Miguel Julve Olcina Carlos J. Gómez García. Departament de Química Inorgànica Universitat de València
 GUÍA DOCENTE QUÍMICA INORGÁNICA Curso 2008-2009 Miguel Julve Olcina Carlos J. Gómez García Departament de Química Inorgànica Universitat de València I. Datos iniciales Nombre de la asignatura: Química
GUÍA DOCENTE QUÍMICA INORGÁNICA Curso 2008-2009 Miguel Julve Olcina Carlos J. Gómez García Departament de Química Inorgànica Universitat de València I. Datos iniciales Nombre de la asignatura: Química
UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE QUÍMICA
 Asignatura QUIMICA INORGÁNICA I UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE QUÍMICA Ciclo TRONCO COMÚN PROGRAMAS DE ESTUDIO TERCER SEMESTRE Área QUÍMICA Departamento QUÍMICA INORGÁNICA Y NUCLEAR
Asignatura QUIMICA INORGÁNICA I UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO FACULTAD DE QUÍMICA Ciclo TRONCO COMÚN PROGRAMAS DE ESTUDIO TERCER SEMESTRE Área QUÍMICA Departamento QUÍMICA INORGÁNICA Y NUCLEAR
ENLACE QUIMICO Y ESTRUCTURA DE LA MATERIA
 Licenciatura en Química 1-5 CÓDIGO: B053/99/7424 CURSO 2002-2003 Carga docente: 7 créditos (5 teóricos + 2 prácticos) Curso: 1º, Troncal Primer cuatrimestre Departamento: Química Inorgánica Profesor/es:
Licenciatura en Química 1-5 CÓDIGO: B053/99/7424 CURSO 2002-2003 Carga docente: 7 créditos (5 teóricos + 2 prácticos) Curso: 1º, Troncal Primer cuatrimestre Departamento: Química Inorgánica Profesor/es:
Descriptores Creditos ECTS Carácter Curso Cuatrimestre. 9 OB 2 2c Castellano
 Guía Materia 2017 / 2018 DATOS IDENTIFICATIVOS Química inorgánica I Asignatura Código Titulacion Química inorgánica I V11G200V01404 Grado en Química Descriptores Creditos ECTS Carácter Curso Cuatrimestre
Guía Materia 2017 / 2018 DATOS IDENTIFICATIVOS Química inorgánica I Asignatura Código Titulacion Química inorgánica I V11G200V01404 Grado en Química Descriptores Creditos ECTS Carácter Curso Cuatrimestre
Grado de Química Curso
 DATOS DE LA ASIGNATURA Asignatura: Química Inorgánica Descriptiva Código (uhu): 757509202 Módulo: Fundamental Materia: Química Créditos ECTS 9 Teóricos: 6 Prácticos: 3 Departamento/s: Química y CCMM Prof.
DATOS DE LA ASIGNATURA Asignatura: Química Inorgánica Descriptiva Código (uhu): 757509202 Módulo: Fundamental Materia: Química Créditos ECTS 9 Teóricos: 6 Prácticos: 3 Departamento/s: Química y CCMM Prof.
EXPERIENCIA PILOTO DE IMPLANTACIÓN DEL SISTEMA ECTS. Facultad de Ciencias Químicas GUÍA DOCENTE. Química Inorgánica
 EXPERIENCIA PILOTO DE IMPLANTACIÓN DEL SISTEMA ECTS GUÍA DOCENTE Química Inorgánica I.- Identificación Nombre de la asignatura: Carácter: Titulación: Ciclo: Semestre/Cuatrimestre: Departamento: Profesores
EXPERIENCIA PILOTO DE IMPLANTACIÓN DEL SISTEMA ECTS GUÍA DOCENTE Química Inorgánica I.- Identificación Nombre de la asignatura: Carácter: Titulación: Ciclo: Semestre/Cuatrimestre: Departamento: Profesores
TIPO: T CURSO: 4º SEMESTRE:1º y 2º CRÉDITOS (horas/semana): 9 CRÉDITOS ECTS: 7.5 PROFESOR: Dr. Jordi Abellà Iglesias IDIOMA: Castellano / Catalán
 33030 QUÍMICA INORGÁNICA AVANZADA Pág 1 de 5 ASIGNATURA: QUÍMICA INORGÁNICA AVANZADA ESTUDIOS: LICENCIATURA EN QUÍMICA (2º Ciclo) CÓDIGO: 33030 TIPO: T CURSO: 4º SEMESTRE:1º y 2º CRÉDITOS (horas/semana):
33030 QUÍMICA INORGÁNICA AVANZADA Pág 1 de 5 ASIGNATURA: QUÍMICA INORGÁNICA AVANZADA ESTUDIOS: LICENCIATURA EN QUÍMICA (2º Ciclo) CÓDIGO: 33030 TIPO: T CURSO: 4º SEMESTRE:1º y 2º CRÉDITOS (horas/semana):
Se recomienda haber cursado las asignaturas de Química del primer curso de Grado y la asignatura de Química Inorgánica I.
 GUIA DOCENTE DE LA ASIGNATURA QUÍMICA INORGÁNICA II MÓDULO MATERIA CURSO SEMESTRE CRÉDITOS TIPO Química Inorgánica Química Inorgánica II 2 2 6 Teórica PROFESORES DIRECCIÓN COMPLETA DE CONTACTO PARA TUTORÍAS
GUIA DOCENTE DE LA ASIGNATURA QUÍMICA INORGÁNICA II MÓDULO MATERIA CURSO SEMESTRE CRÉDITOS TIPO Química Inorgánica Química Inorgánica II 2 2 6 Teórica PROFESORES DIRECCIÓN COMPLETA DE CONTACTO PARA TUTORÍAS
Guía docente de la asignatura
 Guía docente de la asignatura Asignatura Materia Química Inorgánica I Química Inorgánica Módulo Titulación Grado en Química Plan 472 Código 45948 Periodo de impartición 2º curso, Primer cuatrimestre Tipo/Carácter
Guía docente de la asignatura Asignatura Materia Química Inorgánica I Química Inorgánica Módulo Titulación Grado en Química Plan 472 Código 45948 Periodo de impartición 2º curso, Primer cuatrimestre Tipo/Carácter
FORMULACIÓN QUÍMICA INORGÁNICA FORMULACIÓN QUÍMICA INORGÁNICA. Son aquellas sustancias que están formadas por átomos de la misma clase.
 FORMULACIÓN QUÍMICA INORGÁNICA FORMULACIÓN QUÍMICA INORGÁNICA Elementos químicos Son aquellas sustancias que están formadas por átomos de la misma clase. Símbolos Dalton se inventó una serie de símbolos
FORMULACIÓN QUÍMICA INORGÁNICA FORMULACIÓN QUÍMICA INORGÁNICA Elementos químicos Son aquellas sustancias que están formadas por átomos de la misma clase. Símbolos Dalton se inventó una serie de símbolos
Estructura Atómica y Tabla Periódica
 Estructura Atómica y Tabla Periódica Átomos y Elementos Estructura Atómica y Tabla Periódica Átomo Tabla Periódica Núcleo Electrones Grupos Períodos Protones Neutrones Arreglo de electrones Número atómico
Estructura Atómica y Tabla Periódica Átomos y Elementos Estructura Atómica y Tabla Periódica Átomo Tabla Periódica Núcleo Electrones Grupos Períodos Protones Neutrones Arreglo de electrones Número atómico
Ficha 1. CONCEPTOS BÁSICOS
 Ficha 1. CONCEPTOS BÁSICOS 1 4 LA TABLA PERIÓDICA Ejercicio 1. Las cosas están formadas a partir de: Protones Moléculas Elementos químicos Ejercicio 2. Los elementos químicos se representan ordenados en:
Ficha 1. CONCEPTOS BÁSICOS 1 4 LA TABLA PERIÓDICA Ejercicio 1. Las cosas están formadas a partir de: Protones Moléculas Elementos químicos Ejercicio 2. Los elementos químicos se representan ordenados en:
FORMULACIÓN Y NOMENCLATURA
 FORMULACIÓN Y NOMENCLATURA 0. Introducción. Existen tres tipos de nomenclaturas que nos permiten nombrar los compuestos químicos inorgánicos: A. Nomenclatura Sistemática (normas propuestas por la Unión
FORMULACIÓN Y NOMENCLATURA 0. Introducción. Existen tres tipos de nomenclaturas que nos permiten nombrar los compuestos químicos inorgánicos: A. Nomenclatura Sistemática (normas propuestas por la Unión
EJERCICIOS DE FORMULACIÓN QUÍMICA INORGÁNICA
 EJERCICIOS DE FORMULACIÓN QUÍMICA INORGÁNICA COMPUESTOS BINARIOS DEL OXÍGENO 1.- Cl 2 O 7 2.- FeO 3.- N 2 O 4.- SO 3 1.- NOMBRA LOS SIGUIENTES COMPUESTOS: 6.- Br 2 O 7.- P 2 O 5 8.- CO 2 9.- I 2 O 5 5.-
EJERCICIOS DE FORMULACIÓN QUÍMICA INORGÁNICA COMPUESTOS BINARIOS DEL OXÍGENO 1.- Cl 2 O 7 2.- FeO 3.- N 2 O 4.- SO 3 1.- NOMBRA LOS SIGUIENTES COMPUESTOS: 6.- Br 2 O 7.- P 2 O 5 8.- CO 2 9.- I 2 O 5 5.-
UNIVERSIDAD NACIONAL DEL SUR 1
 UNIVERSIDAD NACIONAL DEL SUR 1 H O R A S D E C L A S E P R O F E S O R R E S P O N S A B L E T E O R I C A S P R A C T I C A S Por semana Por cuatrimestre Por semana Por cuatrimestre Dra. Aurora E. Sagua
UNIVERSIDAD NACIONAL DEL SUR 1 H O R A S D E C L A S E P R O F E S O R R E S P O N S A B L E T E O R I C A S P R A C T I C A S Por semana Por cuatrimestre Por semana Por cuatrimestre Dra. Aurora E. Sagua
QUÍMICA INORGÁNICA AVANZADA
 Licenciatura en Química 1-7 CÓDIGO: B053/99/7443 CURSO: 2002-2003 Carga docente: 8 créditos (6 teóricos + 2 prácticos) Curso: 4º, Troncal Segundo cuatrimestre Departamento: Química Inorgánica Profesor/es:
Licenciatura en Química 1-7 CÓDIGO: B053/99/7443 CURSO: 2002-2003 Carga docente: 8 créditos (6 teóricos + 2 prácticos) Curso: 4º, Troncal Segundo cuatrimestre Departamento: Química Inorgánica Profesor/es:
Ley Periódica. Química General I 2013
 Ley Periódica Química General I 2013 Ley Periódica Mendeleev estudió las configuraciones electrónicas y descubrió la periodicidad cuando estas eran similares. Configuración electrónica similar Propiedades
Ley Periódica Química General I 2013 Ley Periódica Mendeleev estudió las configuraciones electrónicas y descubrió la periodicidad cuando estas eran similares. Configuración electrónica similar Propiedades
GUÍA DOCENTE Química Inorgánica I
 GUÍA DOCENTE 2017-2018 Química Inorgánica I 1. Denominación de la asignatura: Química Inorgánica I Titulación Grado en Química Código 5273 2. Materia o módulo a la que pertenece la asignatura: Química
GUÍA DOCENTE 2017-2018 Química Inorgánica I 1. Denominación de la asignatura: Química Inorgánica I Titulación Grado en Química Código 5273 2. Materia o módulo a la que pertenece la asignatura: Química
EJERCICIOS DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA 3º ESO
 EJERCICIOS DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA 3º ESO 1 COMPUESTOS BINARIOS 1.1 CON OXÍGENO 1.1.1 Y UN METAL (ÓXIDOS METÁLICOS) 1 BaO Monóxido de bario Óxido de bario 2 Na 2 O Monóxido
EJERCICIOS DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA 3º ESO 1 COMPUESTOS BINARIOS 1.1 CON OXÍGENO 1.1.1 Y UN METAL (ÓXIDOS METÁLICOS) 1 BaO Monóxido de bario Óxido de bario 2 Na 2 O Monóxido
19.1 Propiedades generales 19.1.1 Propiedades físicas. Tema 19: Estudio general de los elementos. II. No metales. 19.1.2 Propiedades químicas
 : Estudio general de los elementos. II. No metales 19.1 Propiedades generales (físicas y químicas) 19.2 Gases nobles 19.3 Halógenos 19.4 Familia del oxígeno 19.5 Familia del nitrógeno 19.6 Familia del
: Estudio general de los elementos. II. No metales 19.1 Propiedades generales (físicas y químicas) 19.2 Gases nobles 19.3 Halógenos 19.4 Familia del oxígeno 19.5 Familia del nitrógeno 19.6 Familia del
DATOS DE LA ASIGNATURA
 DATOS DE LA ASIGNATURA Denominación: QUÍMICA INORGÁNICA Código: 57607 Clase: TRONCAL Curso: 1º Carácter: CUATRIMESTRAL Cuatrimestre: 1º Créditos LRU: 7.5 Teóricos: 3 Prácticos: 2 Créditos ECTS: 6.8 Horas
DATOS DE LA ASIGNATURA Denominación: QUÍMICA INORGÁNICA Código: 57607 Clase: TRONCAL Curso: 1º Carácter: CUATRIMESTRAL Cuatrimestre: 1º Créditos LRU: 7.5 Teóricos: 3 Prácticos: 2 Créditos ECTS: 6.8 Horas
Ley Periódica. Química General I 2012
 Ley Periódica Química General I 2012 Ley Periódica Mendeleev estudió las configuraciones electrónicas y descubrió la periodicidad cuando estas eran similares. Configuración electrónica similar Propiedades
Ley Periódica Química General I 2012 Ley Periódica Mendeleev estudió las configuraciones electrónicas y descubrió la periodicidad cuando estas eran similares. Configuración electrónica similar Propiedades
- Nomenclatura tradicional. Hoy está totalmente en desuso, pero es necesario conocerla para poder formular oxiácidos. La posibilidad de que un mismo
 NORMAS BÁSICAS SOBRE FORMULACIÓN - Se escribe siempre en primer lugar el símbolo del elemento (o grupo) que actúa con número de oxidación positivo, generalmente un metal y a continuación el símbolo del
NORMAS BÁSICAS SOBRE FORMULACIÓN - Se escribe siempre en primer lugar el símbolo del elemento (o grupo) que actúa con número de oxidación positivo, generalmente un metal y a continuación el símbolo del
Tema 4. Propiedades generales. Propiedades generales de los elementos no metálicos. Propiedades generales de los óxidos y de los haluros a lo largo
 Tema 4. Propiedades generales. Propiedades generales de los elementos no metálicos. Propiedades generales de los óxidos y de los haluros a lo largo del sistema periódico. Variación del carácter iónicocovalente.
Tema 4. Propiedades generales. Propiedades generales de los elementos no metálicos. Propiedades generales de los óxidos y de los haluros a lo largo del sistema periódico. Variación del carácter iónicocovalente.
QUÍMICA INORGÁNICA I - Licenciatura en Química QUÍMICA INORGÁNICA - Químico Analista y Profesorado en Química
 QUÍMICA INORGÁNICA I - Licenciatura en Química QUÍMICA INORGÁNICA - Químico Analista y Profesorado en Química Carácter: Obligatoria Carga horaria: 9 horas semanales, 135 horas totales (15 semanas de cursado)
QUÍMICA INORGÁNICA I - Licenciatura en Química QUÍMICA INORGÁNICA - Químico Analista y Profesorado en Química Carácter: Obligatoria Carga horaria: 9 horas semanales, 135 horas totales (15 semanas de cursado)
FACULTAD DE CIENCIAS GRADO DE QUÍMICA. Curso 2016/17. Asignatura: EXPERIMENTACIÓN EN QUÍMICA INORGÁNICA DATOS DE LA ASIGNATURA
 FACULTAD DE CIENCIAS GRADO DE QUÍMICA Asignatura: DATOS DE LA ASIGNATURA Denominación: Código: 100456 Plan de estudios: GRADO DE QUÍMICA Curso: 2 Denominación del módulo al que pertenece: FUNDAMENTAL Materia:
FACULTAD DE CIENCIAS GRADO DE QUÍMICA Asignatura: DATOS DE LA ASIGNATURA Denominación: Código: 100456 Plan de estudios: GRADO DE QUÍMICA Curso: 2 Denominación del módulo al que pertenece: FUNDAMENTAL Materia:
FORMULACIÓN INORGÁNICA. CURSO 2014-2015 COMPUESTOS BINARIOS.
 FORMULACIÓN INORGÁNICA. CURSO 2014-2015 COMPUESTOS BINARIOS. 1. ÓXIDOS. Son compuestos, formados por la unión del oxígeno y cualquier otro elemento de la tabla periódica (excepto los gases nobles que jamás
FORMULACIÓN INORGÁNICA. CURSO 2014-2015 COMPUESTOS BINARIOS. 1. ÓXIDOS. Son compuestos, formados por la unión del oxígeno y cualquier otro elemento de la tabla periódica (excepto los gases nobles que jamás
PROGRAMA QUÍMICA INORGÁNICA
 PROGRAMA QUÍMICA INORGÁNICA Objetivo de Estudio de la Disciplina El objetivo de la Química es el conocimiento de las especies químicas elementos y compuestos sus propiedades, reacciones químicas, los métodos
PROGRAMA QUÍMICA INORGÁNICA Objetivo de Estudio de la Disciplina El objetivo de la Química es el conocimiento de las especies químicas elementos y compuestos sus propiedades, reacciones químicas, los métodos
Licenciado en Química 1-8 Curso QUÍMICA FÍSICA I
 Licenciado en Química 1-8 CÓDIGO: B053/99/7430 CURSO: 2003-2004 Carga docente: 7 créditos totales (5 teóricos + 2 prácticos) Curso: 1º, troncal 1er Cuatrimestre Grupos: 3 Departamento: Química Física Profesor/es:
Licenciado en Química 1-8 CÓDIGO: B053/99/7430 CURSO: 2003-2004 Carga docente: 7 créditos totales (5 teóricos + 2 prácticos) Curso: 1º, troncal 1er Cuatrimestre Grupos: 3 Departamento: Química Física Profesor/es:
VERSIÓN CERO NOMBRE:.PARALELO: 1. Seleccione entre los siguientes enunciados la alternativa incorrecta:
 ESCUELA SUPERIOR POLITÉCNICA DEL LITORAL INSTITUTO DE CIENCIAS QUÍMICAS Y AMBIENTALES OFICINA DE ADMISIONES CURSO DE NIVEL CERO A, INVIERNO 2012 PRIMERA EVALUACIÓN DE QUÍMICA, MARZO 08 DEL 2012 VERSIÓN
ESCUELA SUPERIOR POLITÉCNICA DEL LITORAL INSTITUTO DE CIENCIAS QUÍMICAS Y AMBIENTALES OFICINA DE ADMISIONES CURSO DE NIVEL CERO A, INVIERNO 2012 PRIMERA EVALUACIÓN DE QUÍMICA, MARZO 08 DEL 2012 VERSIÓN
PROGRAMA DE ASIGNATURA
 REPÚBLICA BOLIVARIANA DE VENEZUELA UNIVERSIDAD NACIONAL EXPERIMENTAL RAFAEL MARÍA BARALT PROGRAMA EDUCACIÓN PROYECTO BIOLOGIA Y QUIMICA PROGRAMA DE ASIGNATURA NOMBRE DE LA ASIGNATURA CODI G MENC SEMESTRE
REPÚBLICA BOLIVARIANA DE VENEZUELA UNIVERSIDAD NACIONAL EXPERIMENTAL RAFAEL MARÍA BARALT PROGRAMA EDUCACIÓN PROYECTO BIOLOGIA Y QUIMICA PROGRAMA DE ASIGNATURA NOMBRE DE LA ASIGNATURA CODI G MENC SEMESTRE
Química de los Elementos. Código: Créditos ECTS: 12. Titulación Tipo Curso Semestre. Uso de idiomas
 2018/2019 Química de los Elementos Código: 102505 Créditos ECTS: 12 Titulación Tipo Curso Semestre 2502444 Química OB 2 A Contacto Nombre: Juli Real Obradors Correo electrónico: Juli.Real@uab.cat Equipo
2018/2019 Química de los Elementos Código: 102505 Créditos ECTS: 12 Titulación Tipo Curso Semestre 2502444 Química OB 2 A Contacto Nombre: Juli Real Obradors Correo electrónico: Juli.Real@uab.cat Equipo
DISTRIBUCIÓN HORARIA DE LA ASIGNATURA SEGÚN NORMATIVA
 GUÍA DOCENTE CURSO: 2017-18 DATOS BÁSICOS DE LA ASIGNATURA Asignatura: Química Inorgánica II Código de asignatura: 50903216 Plan: Grado en Química (Plan 2009) Año académico: 2017-18 Ciclo formativo: Grado
GUÍA DOCENTE CURSO: 2017-18 DATOS BÁSICOS DE LA ASIGNATURA Asignatura: Química Inorgánica II Código de asignatura: 50903216 Plan: Grado en Química (Plan 2009) Año académico: 2017-18 Ciclo formativo: Grado
uco.es/grados GUÍA DOCENTE DENOMINACIÓN DE LA ASIGNATURA DATOS DEL PROFESORADO REQUISITOS Y RECOMENDACIONES COMPETENCIAS
 Curso 27/8 DENOMINACIÓN DE LA ASIGNATURA Denominación: EXPERIMENTACIÓN EN QUÍMICA INORGÁNICA Código: 45 Plan de estudios: GRADO DE QUÍMICA Curso: 2 Denominación del módulo al que pertenece: FUNDAMENTAL
Curso 27/8 DENOMINACIÓN DE LA ASIGNATURA Denominación: EXPERIMENTACIÓN EN QUÍMICA INORGÁNICA Código: 45 Plan de estudios: GRADO DE QUÍMICA Curso: 2 Denominación del módulo al que pertenece: FUNDAMENTAL
Español. Se emplea también Inglés en material docente / In addition to Spanish, English is also extensively used in teaching material
 ASIGNATURA / COURSE TITLE QUIMICA INORGÁNICA / INORGANIC CHEMISTRY 1.1. Código / Course number 16357 1.2. Materia / Content area QUIMICA INORGÁNICA / INORGANIC CHEMISTRY 1.3. Tipo / Course type Formación
ASIGNATURA / COURSE TITLE QUIMICA INORGÁNICA / INORGANIC CHEMISTRY 1.1. Código / Course number 16357 1.2. Materia / Content area QUIMICA INORGÁNICA / INORGANIC CHEMISTRY 1.3. Tipo / Course type Formación
MÓDULO MATERIA CURSO SEMESTRE CRÉDITOS TIPO. Química Inorgánica Química Inorgánica II 2º 4º 6 Obligatoria
 GUIA DOCENTE DE LA ASIGNATURA ( ) QUÍMICA INORGÁNICA II Curso 2017-2018 (Fecha última actualización: 12/06/2017) (Fecha de aprobación en Consejo de Departamento: 13/06/2017) MÓDULO MATERIA CURSO SEMESTRE
GUIA DOCENTE DE LA ASIGNATURA ( ) QUÍMICA INORGÁNICA II Curso 2017-2018 (Fecha última actualización: 12/06/2017) (Fecha de aprobación en Consejo de Departamento: 13/06/2017) MÓDULO MATERIA CURSO SEMESTRE
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA. Nivel: Educación Secundaria Obligatoria
 NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA Nivel: Educación Secundaria Obligatoria Conceptos básicos Los elementos químicos se representan mediante símbolos, que consisten en una o dos letras que
NOMENCLATURA y FORMULACIÓN en QUÍMICA INORGÁNICA Nivel: Educación Secundaria Obligatoria Conceptos básicos Los elementos químicos se representan mediante símbolos, que consisten en una o dos letras que
Idioma en que se imparte: ECTS: Horas/ECTS: Volumen de trabajo del alumno: Castellano Inglés
 Guía Docente Asignatura: Química Inorgánica Módulo (según el plan de estudios): Materias específicas Titulación: Grado en Ingeniería Química Industrial Código: 509101008 Plan de Estudios: Plan 5091. Decreto
Guía Docente Asignatura: Química Inorgánica Módulo (según el plan de estudios): Materias específicas Titulación: Grado en Ingeniería Química Industrial Código: 509101008 Plan de Estudios: Plan 5091. Decreto
6. ELEMENTOS Y COMPUESTOS
 6. ELEMENTOS Y COMPUESTOS 1. Cuáles son metales y cuáles no metales de los siguientes elementos: carbono, azufre, cobre y aluminio? Por qué? Son metales el cobre y el aluminio, y son no metales el carbono
6. ELEMENTOS Y COMPUESTOS 1. Cuáles son metales y cuáles no metales de los siguientes elementos: carbono, azufre, cobre y aluminio? Por qué? Son metales el cobre y el aluminio, y son no metales el carbono
Titulación(es) Titulación Centro Curso Periodo Grado de Química FACULTAT DE QUÍMICA 2 Primer cuatrimestre
 FICHA IDENTIFICATIVA Datos de la Asignatura Código 34198 Nombre Química Inorgánica I Ciclo Grado Créditos ECTS 4.5 Curso académico 2016-2017 Titulación(es) Titulación Centro Curso Periodo 1108 - Grado
FICHA IDENTIFICATIVA Datos de la Asignatura Código 34198 Nombre Química Inorgánica I Ciclo Grado Créditos ECTS 4.5 Curso académico 2016-2017 Titulación(es) Titulación Centro Curso Periodo 1108 - Grado
Compuestos Binarios- Óxidos-Hidruros-Hidrácidos-Sales Binarias. ÓXIDOS ( Metal/No Metal + O )
 Alcalinos + O Alcalino-Térreos + O Metales de Transición + O Térreos + O Carbonoideos + O ÓXIDOS ( Metal/No Metal + O ) Li 2 O monóxido de dilitio óxido de litio (I) Na 2 O monóxido de disodio óxido de
Alcalinos + O Alcalino-Térreos + O Metales de Transición + O Térreos + O Carbonoideos + O ÓXIDOS ( Metal/No Metal + O ) Li 2 O monóxido de dilitio óxido de litio (I) Na 2 O monóxido de disodio óxido de
Licenciatura en Química 1-6 Curso EXPERIMENTACION QUÍMICA INORGÁNICA
 Licenciatura en Química 1-6 CÓDIGO: B053/99/7439 CURSO: 2002-2003 Carga docente: 5 créditos prácticos Curso: 4º, Troncal Primer cuatrimestre Departamento: Química Inorgánica Profesor/es: Mª Salvadora Sánchez
Licenciatura en Química 1-6 CÓDIGO: B053/99/7439 CURSO: 2002-2003 Carga docente: 5 créditos prácticos Curso: 4º, Troncal Primer cuatrimestre Departamento: Química Inorgánica Profesor/es: Mª Salvadora Sánchez
ASIGNATURA: QUÍMICA INORGÁNICA
 ASIGNATURA: QUÍMICA INORGÁNICA Código:43-205 Régimen: cuatrimestral Horas reloj semanales: 8 Horas Teoricas:80 Horas Practicas: 18 Horas Laboratorio:30 Horas Totales:128 Escuela/s: Química, Farmacia y
ASIGNATURA: QUÍMICA INORGÁNICA Código:43-205 Régimen: cuatrimestral Horas reloj semanales: 8 Horas Teoricas:80 Horas Practicas: 18 Horas Laboratorio:30 Horas Totales:128 Escuela/s: Química, Farmacia y
GUÍA DOCENTE DE ASIGNATURA CURSO 2010/2011
 GUÍA DOCENTE DE ASIGNATURA CURSO 200/20. DATOS BÁSICOS DE LA ASIGNATURA..Nombre.3. Código de la asignatura Experimentación en Síntesis Inorgánica 500303.4.Plan 2000.2. Código UNESCO.5.Curso académico 200-
GUÍA DOCENTE DE ASIGNATURA CURSO 200/20. DATOS BÁSICOS DE LA ASIGNATURA..Nombre.3. Código de la asignatura Experimentación en Síntesis Inorgánica 500303.4.Plan 2000.2. Código UNESCO.5.Curso académico 200-
1. ASIGNATURA / COURSE
 1. ASIGNATURA / COURSE 1.1. Nombre / Course Title ORIGEN Y EVOLUCIÓN CELULAR / CELL ORIGIN AND EVOLUTION 1.2. Código / Course Code 13810 1.3. Tipo / Type of course OPTATIVA / OPTIONAL 1.4. Nivel / Level
1. ASIGNATURA / COURSE 1.1. Nombre / Course Title ORIGEN Y EVOLUCIÓN CELULAR / CELL ORIGIN AND EVOLUTION 1.2. Código / Course Code 13810 1.3. Tipo / Type of course OPTATIVA / OPTIONAL 1.4. Nivel / Level
QUÍMICA INORGÁNICA AVANZADA
 Licenciatura en Química 1-7 CÓDIGO: B053/99/7443 CURSO: 2000-2001 Carga docente: 9 créditos Curso: 4º Segundo cuatrimestre Departamento: Química Inorgánica Profesor/es: GA- Rosa Torregrosa Maciá GB- Miguel
Licenciatura en Química 1-7 CÓDIGO: B053/99/7443 CURSO: 2000-2001 Carga docente: 9 créditos Curso: 4º Segundo cuatrimestre Departamento: Química Inorgánica Profesor/es: GA- Rosa Torregrosa Maciá GB- Miguel
UNIVERSIDAD DE LOS ANDES DEPARTAMENTO DE QUÍMICA QUÍMICA INORGÁNICA II - TEORIA
 UNIVERSIDAD DE LOS ANDES DEPARTAMENTO DE QUÍMICA QUÍMICA INORGÁNICA II - TEORIA Código: QUIM 1212 Horario: lunes, 11:00-11:50 a.m. Martes, jueves y viernes 10:00 a.m. 10:50 a.m. Profesor: Andreas Reiber,
UNIVERSIDAD DE LOS ANDES DEPARTAMENTO DE QUÍMICA QUÍMICA INORGÁNICA II - TEORIA Código: QUIM 1212 Horario: lunes, 11:00-11:50 a.m. Martes, jueves y viernes 10:00 a.m. 10:50 a.m. Profesor: Andreas Reiber,
Plan Código Tipo Curso Créditos Periodos de (Teóricos+Prácticos) docencia Cuarto Cuarto 7,5(5,5T + 1,5P) 1C
 Asignatura: QUÍMICA INORGÁNICA AVANZADA Plan Código Tipo Curso Créditos Periodos de (Teóricos+Prácticos) docencia 6 57230 Cuarto Cuarto 7,5(5,5T + 1,5P) 1C Equipo docente Prof. Teoría: Antonio F. Antiñolo
Asignatura: QUÍMICA INORGÁNICA AVANZADA Plan Código Tipo Curso Créditos Periodos de (Teóricos+Prácticos) docencia 6 57230 Cuarto Cuarto 7,5(5,5T + 1,5P) 1C Equipo docente Prof. Teoría: Antonio F. Antiñolo
EJERCICIOS DE REPASO DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS
 EJERCICIOS DE REPASO DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS No hace falta hacerlos todos, ya os habréis dado cuenta de que si entendéis la lógica que hay detrás de la formulación
EJERCICIOS DE REPASO DE FORMULACIÓN Y NOMENCLATURA DE QUÍMICA INORGÁNICA COMPUESTOS BINARIOS No hace falta hacerlos todos, ya os habréis dado cuenta de que si entendéis la lógica que hay detrás de la formulación
Primer Apellido Segundo Apellido Primer nombre Segundo nombre PREGUNTAS:
 ESPOL - INSTITUTO DE CIENCIAS QUÍMICAS Y AMBIENTALES - OFICINA DE ADMISIONES Examen de Ubicación de QUÍMICA- NIVEL CERO - 2009.12.29 Nombres y apellidos del aspirante: Primer Apellido Segundo Apellido
ESPOL - INSTITUTO DE CIENCIAS QUÍMICAS Y AMBIENTALES - OFICINA DE ADMISIONES Examen de Ubicación de QUÍMICA- NIVEL CERO - 2009.12.29 Nombres y apellidos del aspirante: Primer Apellido Segundo Apellido
16 32 16 16 16 neutro 14 30 16 14 15 anión Fe +3 26 56 30 26 23 catión = 100
 I.E.. Al-Ándalus. Dpto. ísica y Química. Q 4º E. Ejercicios Tema. - 1 - BRE PARTÍCULA DEL ÁTM Y MAA ATÓMICA. 1. Completar la siguiente tabla: Z A º p + º e - Tipo ión 15 8 8 15 7 8 10 anión Ca + 0 41 1
I.E.. Al-Ándalus. Dpto. ísica y Química. Q 4º E. Ejercicios Tema. - 1 - BRE PARTÍCULA DEL ÁTM Y MAA ATÓMICA. 1. Completar la siguiente tabla: Z A º p + º e - Tipo ión 15 8 8 15 7 8 10 anión Ca + 0 41 1
Titulación(es) Titulación Centro Curso Periodo Grado de Química FACULTAT DE QUÍMICA 2 Segundo cuatrimestre
 FICHA IDENTIFICATIVA Datos de la Asignatura Código 34199 Nombre Química Inorgánica II Ciclo Grado Créditos ECTS 4.5 Curso académico 2016-2017 Titulación(es) Titulación Centro Curso Periodo 1108 - Grado
FICHA IDENTIFICATIVA Datos de la Asignatura Código 34199 Nombre Química Inorgánica II Ciclo Grado Créditos ECTS 4.5 Curso académico 2016-2017 Titulación(es) Titulación Centro Curso Periodo 1108 - Grado
GUÍA DOCENTE DE ASIGNATURA
 GUÍA DOCENTE DE ASIGNATURA 1. DATOS DE LA ASIGNATURA 1.1. Nombre Química Inorgánica 1.2. Código 005002104 1..Plan 2000 1.4.Ciclo 1º 1.5. Curso 2º 1.6. Tipo Troncal 1.7. Cuatrimestre Anual 1.8. Créditos
GUÍA DOCENTE DE ASIGNATURA 1. DATOS DE LA ASIGNATURA 1.1. Nombre Química Inorgánica 1.2. Código 005002104 1..Plan 2000 1.4.Ciclo 1º 1.5. Curso 2º 1.6. Tipo Troncal 1.7. Cuatrimestre Anual 1.8. Créditos
FORMULACIÓN Y NOMENCLATURA
 FORMULACIÓN Y NOMENCLATURA.- Formulación: Es la representación escrita de una molécula que se rige por unas normas universales establecidas por acuerdo de la comunidad científica..- Nomenclatura: Es el
FORMULACIÓN Y NOMENCLATURA.- Formulación: Es la representación escrita de una molécula que se rige por unas normas universales establecidas por acuerdo de la comunidad científica..- Nomenclatura: Es el
Pontificia Universidad Católica del Ecuador
 1. DATOS INFORMATIVOS: MATERIA O MÓDULO: Química Inorgánica, T y L CÓDIGO: 13895 CARRERA: NIVEL: Licenciatura en Ciencias Químicas, con mención en Química Analítica Segundo Nivel No. CRÉDITOS: 7 CRÉDITOS
1. DATOS INFORMATIVOS: MATERIA O MÓDULO: Química Inorgánica, T y L CÓDIGO: 13895 CARRERA: NIVEL: Licenciatura en Ciencias Químicas, con mención en Química Analítica Segundo Nivel No. CRÉDITOS: 7 CRÉDITOS
OCEANOGRAFÍA QUÍMICA Y CONTAMINACIÓN MARINA Licenciado en Biología -1
 Licenciado en Biología -1 CÓDIGO: 20/93-0948 CURSO: 1998-99 Carga docente: 6 créditos (3 teóricos + 3 prácticos) (segundo cuatrimestre) Departamentos: Química-Física e Ingeniería Química Profesor/es: Enrique
Licenciado en Biología -1 CÓDIGO: 20/93-0948 CURSO: 1998-99 Carga docente: 6 créditos (3 teóricos + 3 prácticos) (segundo cuatrimestre) Departamentos: Química-Física e Ingeniería Química Profesor/es: Enrique
REPASO DE FORMULACIÓN INORGÁNICA
 REPASO DE FORMULACIÓN INORGÁNICA 1. Cl 2 O 7 2. FeO 3. N 2 O 4. SO 3 5. Cr 2 O 3 6. Br 2 O 7. P 2 O 5 8. CO 2 9. I 2 O 5 10. MnO 2 11. Trióxido de dicromo 12. Óxido de nitrógeno (V) 13. Heptaóxido de dicloro
REPASO DE FORMULACIÓN INORGÁNICA 1. Cl 2 O 7 2. FeO 3. N 2 O 4. SO 3 5. Cr 2 O 3 6. Br 2 O 7. P 2 O 5 8. CO 2 9. I 2 O 5 10. MnO 2 11. Trióxido de dicromo 12. Óxido de nitrógeno (V) 13. Heptaóxido de dicloro
1. Temas a desarrollar en la Unidad I.
 Secretaria de educación Pública Subsecretaría de Educación Media Superior Dirección General de Educación Tecnológica Industrial Centro de Estudios Tecnológicos Industrial y de Servicios No. 5 Gertrudis
Secretaria de educación Pública Subsecretaría de Educación Media Superior Dirección General de Educación Tecnológica Industrial Centro de Estudios Tecnológicos Industrial y de Servicios No. 5 Gertrudis
Universidad Central del Este U C E Facultad de Ciencias de las Ingenierías y Recursos Naturales Escuela de Ingeniería Industrial
 Universidad Central del Este U C E Facultad de Ciencias de las Ingenierías y Recursos Naturales Escuela de Ingeniería Industrial Programa de la asignatura: (QUI-012) Química Inorgánica I Total de Créditos:
Universidad Central del Este U C E Facultad de Ciencias de las Ingenierías y Recursos Naturales Escuela de Ingeniería Industrial Programa de la asignatura: (QUI-012) Química Inorgánica I Total de Créditos:
PROGRAMA QUÍMICA 2015-2016
 PROGRAMA QUÍMICA 2015-2016 1. Conceptos comunes. Transformaciones físicas y químicas. Leyes ponderales de la química. Masas atómicas y masas moleculares. Número de Avogadro. Mol. Fórmula empírica y fórmula
PROGRAMA QUÍMICA 2015-2016 1. Conceptos comunes. Transformaciones físicas y químicas. Leyes ponderales de la química. Masas atómicas y masas moleculares. Número de Avogadro. Mol. Fórmula empírica y fórmula
Titulación(es) Titulación Centro Curso Periodo Grado de Química FACULTAT DE QUÍMICA 2 Primer cuatrimestre
 FICHA IDENTIFICATIVA Datos de la Asignatura Código 34198 Nombre Química Inorgánica I Ciclo Grado Créditos ECTS 4.5 Curso académico 2014-2015 Titulación(es) Titulación Centro Curso Periodo 1108 - Grado
FICHA IDENTIFICATIVA Datos de la Asignatura Código 34198 Nombre Química Inorgánica I Ciclo Grado Créditos ECTS 4.5 Curso académico 2014-2015 Titulación(es) Titulación Centro Curso Periodo 1108 - Grado
1. ASIGNATURA / COURSE
 1. ASIGNATURA / COURSE 1.1. Nombre / Course Title COMPUESTOS INORGÁNICOS / INORGANIC COMPOUNDS 1.2. Código / Course Code 12706 1.3. Tipo / Type of course Troncal / Compulsory 1.4. Nivel / Level of course
1. ASIGNATURA / COURSE 1.1. Nombre / Course Title COMPUESTOS INORGÁNICOS / INORGANIC COMPOUNDS 1.2. Código / Course Code 12706 1.3. Tipo / Type of course Troncal / Compulsory 1.4. Nivel / Level of course
Trióxido de dihierro
 OXIDOS = Elemento - Oxígeno No metal (1) + Oxígeno = Óxido no metálico CO 2 ; SO 3 ; N 2 O 5 ; CO ; SO 2 ; NO 2 (1) excepto halógenos X no m Metal + Oxígeno = Óxido metálico Fe 2 O 3 ; Li 2 O ; CaO ; Ag
OXIDOS = Elemento - Oxígeno No metal (1) + Oxígeno = Óxido no metálico CO 2 ; SO 3 ; N 2 O 5 ; CO ; SO 2 ; NO 2 (1) excepto halógenos X no m Metal + Oxígeno = Óxido metálico Fe 2 O 3 ; Li 2 O ; CaO ; Ag
