Bloque I.- Defectos Defectos en Cerámicos
|
|
|
- María Victoria Bustamante Ortiz de Zárate
- hace 6 años
- Vistas:
Transcripción
1 Defecto en Cerámico Solid State Chemitry (A.R. Wet) (Tema 9.- Crytal defect and Non-toichiometry) Química del Etado Sólido: una introducción (L: Smart-E. Moore) (Ed. Addion-Weley Iberoamericana) 1
2 Defecto Prop. Sólido Imperfeccione o Defecto G crital Creación defecto: H > 0 (endot) y S > 0 (S: entropía configuracional) S = k ln W (W: toda la poible manera de ditribuir n defecto entre la N poible poicione al azar W ) G= H - T S o al [ ] W S H puede er S G>0 o [ ] óptima (en eq.) todo Xtale preentan defecto o al T [defecto] 2
3 Tipo de Defecto Claificación egún COMPOSICIÓN o Etequiométrico o intríneco: lo defecto no modifican la compoición o Schottky: vacante de la red o Frenkel: un átm e tralada a una poición interticial creando una vacante o No-etequiométrico o extríneco: cambio en la compoición aparición de defecto o e crean cuando un atm. extraño e inerta dentro de la red Ej.- NaCl: dopado con CaCl 2: : cada Ca 2+ reemplazará do Na + 3
4 Puntuale Claificación egún DIMENSIÓN o Schottky o Frenkel o Deorden Antietructural o Centro de Color Un olo átomo o una poición de red (vacante o interticiale) o Arita Superficie Lineale o Hélice Borde de grano o Mixta o Etructurale Plano de macla Falta de apilamiento Complejo o Cluter Frontera antifae o Exteno o planare o Compoicionale Plano Cizalladura critaligráfica Plano macla química 4
5 Defecto puntuale (I) Defecto FRENKEL Defecto intríneco: n iempre Balance de Carga: ELECTRONEUTRALIDAD Vacante + Catión Interticial* Sin Modificación ρ Ione peq. (H y Li) Ej: haluro de plata (Ag + h.o. h.t.) *: Poición normalmente no ocupada Defecto SCHOTTKY (Iónico) Vacante Anión y Catión Modificación ρ [ ] σ iónica Ej: haluro alcalino (1:1) 5
6 Defecto v.. Etructura Crital Haluro alcalino (no C) Etructura tipo NaCl Defecto predominante Schottky Óxido alcalino-terreo AgCl, Ag Br NaCl NaCl Schottky Cation Frenkel Haluro de C, TiCl CCl Schottky BeO Fluoruro de alcalinoterreo, CeO 2, ThO 2 Wurzita, ZnS Fluorita, CaF 2 Schottky Anión Frenkel (meno frecuente) 6
7 Concentración de defecto H Nº defecto Schottky n = N exp 2kT nº por m 3 1 F Nº defecto Frenkel n = ( N N ) 2 F i exp H 2kT H : Eg creación de defecto Schottky H F : Eg creación de defecto Frenkel N: nº poicione reticulare (catiónica y aniónica) N i : nº poicione interticiale En un xtal: H H F e formara el defecto con H 7
8 Deducción de la expreión nº defecto Schottky Formación defecto: proceo endotérmico, H>0, pero S En el equil.: G = 0, G = H - T S Crital MX: n = n c = n a n : nº defecto Schottky por m 3 n a : nº defecto aniónico por m 3 n c : nº defecto catiónico por m 3 N: nº poicione catiónica poible por m 3 Formula de Boltzman: S = k Ln W W: nº de forma de ditribuir n defecto entre N poible poicione al azar 8
9 Deducción de la expreión nº defecto Schottky La teoría de la probabilidad W = N!! ( N n), n! iendo N! = N ( N -1)( N 2)( N 3 )... 1 Nº de forma de ditribuir la vacante catiónica: W c = N! ( N n )! n! Nº de forma de ditribuir la vacante aniónica: El nº total de forma de ditribuir eto defecto e: W = W W c a = W ( N n ) N!! n a = ( N n )! n!! 2 N! 9
10 Deducción de la expreión nº defecto Schottky N! S = k ln W = k ln = 2k ln coniderando la implificación de STIRLING : ln N! S = 2k N lnn - N, ( N - n )!n ( N - n ) { N ln N - (N - n ) ln (N - n ) - n ln n } 2 N!!n, Si para creación defecto, la entalpía e: H Para creación n defecto, la entalpía e: n H El cambio en la Eg libre de Gibb: G = n H 2kT{N lnn-(n-n ) ln(n-n ) n ln n } 10
11 Deducción de la expreión nº defecto Schottky Equilibrio el cambio en la Eg libre de Gibb = 0: d G dn = 0 H 2kT d {N lnn-(n-n ) ln(n-n ) n ln n } dn Operando, H 2kT [ln(n-n ) +1-ln n 1] H n = = 2kT ln ( N n ) n H, 2kT ( N n ) exp, como N >>> n n = N exp H 2kT 11
12 Solucione ólida: Interticiale y utitucionale La mayoría de lo materiale preentan impureza en porcentaje muy bajo (incluo ppm) etán formando S.S. (Sutit. o Intert.) dependiendo del tamaño de la impureza y de lo radio iónico de la red hueped 12
13 o Cuerpo: V : vacante o ión Mg Notación Kröger-Vink o Subíndice: o poición que ocupa en la red huéped el defecto (M x ) o poición interticial: M i o X i o Superíndice: Carga efectiva repecto anfitrión V Mg : V: Vacante Mg: Sutitución defecto en de poición Fe por Mg 2+ en MgO : carga e 2(-) : carga efectiva (+) : carga efectiva (-) X : carga efectiva neutra Al i : Fe x Mg: Fe ocupa poic. de Mg y e neutro (Fe 2+ ) Fe Al: cation Al Mg: Fe ocupa poic. de Mg y tiene exceo carga (+): (Fe 3+ ) i: defecto ocupa poición intert. : carga e 3(+) 13
14 Aociación de defecto Eliminar Na + de NaCl: eliminación de Na + y e deja e - (e ) en u poición Eliminar Cl - de NaCl: eliminación de Cl - y e - : hueco elect. poitivo (h )en u poición vacante: V Cl (V Na -V Cl): Vacante de Na con carga neg. y vacante Cl con carga poit (Al Mg- V Mg ) :Al en poición de Mg con ecao de carga (+) + vacante Mg con carga 2(-) DIMERO (Al Mg- V Mg Al Mg ) x : TRIMERO o cluter de 3 defecto 14
15 Ejemplo de creación de defecto en S.S. KCl (1:1): nº = poic aniónica = nº poicione catiónica Introducir CaCl 2 S.S 1.- Sutitución Atómica: CaCl Ca k + V K +2 Cl Cl 2.- Sutitución Atómica + fuerte ionización: CaCl Ca k + V K +2 Cl Cl 3.- Poicione Interticiale + fuerte ionización: CaCl Ca i + 2V K +2 Cl Cl 15
16 Tabla de aociación de Energía 16
17 Deorden anti-etructural: orden-deorden Intercambio de átm. entre diferente poicione en la etructura H, pero S : T 450ºC Latón-β Latón- β (ordenada deordenada) T ordenada mientra T deordenada Aleacione Metálica Latón- β : Cu: centro cubo Zn: equina cubo Cúbica imple CCl Latón- β: Cu y Zn: ditribución aleat Cúbica centrada cuerpo 17
18 Deorden anti-etructural: Orden-Deorden AuCu 3 Átm Au Átm Cu Átm Au-Cu Li 2 Fe 2 O 4 y Li 2 TiO 3 : etruc. Tipo NaCl, con ditrib. aleatoria de catione en poicione octaédrica Epinela: [A] t [B] o O 4 [B] t [AB] o O 4 (normal, T invera, T) (intercambio Retic.) poic. 18
19 Deorden anti-etructural: Orden-Deorden Ag 2 HgI 4 ordenada : poicione no ocupada T: ¾ poic. Ocupada de manera ordenada por Ag + y Hg T (>500ºC): Ag y Hg dipueto al azar en cualquiera de lo 4 poicione catiónica poible Grado de deorden en función de la Temp. deorden total e alcanzado al uperra cierta temp crítica (Tc) 19
20 Centro de Color e - no apareado atrapado en poicione aniónica vacante de la red o irradiación de luz muy intena (Rayo-X, UV, neutrone, ) o calentamiento en el vapor del metal NaCl anaranjado amarillento KCl violeta KBr azul verdoo Na Cl Na Cl Cl Na Cl Na Na e - Na Cl Cl Na Cl Na Na Cl Na Cl Átom del vapor difunden dentro del Xtal y e itúan en poicione catiónica; al mimo tiempo e crea un nº equiv de poicione vacante aniónica y la ionización produce un catión de metal alcalino con un e - atrapado en la vacante aniónica e - atrapado e comporta como una part. en una caja de potencial, con ólo cierto nivele poible de Eg, cuya diferencia de Eg etá en la parte viible del epct. Electromg (Centro F o Farbenzentre ) 20
21 Centro de color: Láer de Rubí MonoCrital de Al 2 O 3 : dopado con peq. cantidad de Cr 3+ (0.05% en peo) Cr Alx : átm de Cr = poic. átm de Al (h.o. deordenada etruc. Corindon ) Cr 3+ d 3 ( 5 orb. degenerado): Dedoblamiento por entorno octaed. tranicione entre nivele Al 2 O 3 + Cr 2 O 3 : color blanco color rojo Al 2 O 3 + Cr 2 O 3 : color blanco color verde 21
22 Láer de Rubí Energía (10 3 cm -1 ) 4 T 1 Tranición No-radiativa (calor) 4 T 2 Tiempo de vida : población ( Fluorecencia) Aborción 4 A 2 Etado fundamental Emiión láer (6934 A) Intena, coherente 22
23 Defecto Lineale: Dilocacione Originan una ditorión en la etructura xtalina alrededor de una línea Formación: o durante la olidificación, enfriamiento o por deformación plática o permanente del Xtal. o por condenación de vacante o por deajute atómico en la S.S. Tipo: o dilocación de arita, bode, cuña o de Taylor o dilocación de hélice, tornillo o de Burger o dilocacione mixta ARISTA HÉLICE MIXTA 24
24 Dilocacione Vector de Burger (b): ditancia de deplazamiento de lo átom. en torno a una dilocación A) ARISTA: plano atómico adicional magnitud: ditancia 1-5 b a la dirección de la dilocación b a dirección mov b 25
25 Ej: Dilocación en Arita 26
26 Dilocacione B) Hélice: debida efuerzo de cizalladura ditorión en forma de epiral Magnitud y ditancia: 1-5 b a la línea de dilocación b a dirección mov. 27
27 Dilocacione Mixta C) Mixta: combinanción anteriore b ni e ni B ni e finalizan en la uperf., jamá dentro del xtal 28
28 Dilocacione y Etructura Critalina Etructura Iónica: má complicada Plano extra metal NaCl Eg (deform) = α G b 2 G: mod. Cizalla elático b: v. Burger α: cte. (0.5-1) 2 plano extra b (Burger) e MAYOR No toda lo mov. on favorable (pto electrotático): FRÁGILES (poca diloc.) 30
29 Movimiento de la dilocacione en Cerámico Delizamiento: deplazamiento ecuencial de plano en la dirección de b al uperar la tenión crítica (deplz. de cizalla) σ > σ peierl 31
30 Movimiento de la dilocacione en Cerámico Trepado: Controlado por la difuión Temp. (má lento que deplazamiento) 32
31 Crecimiento de la dilocacione Xtale cuidadoamente preparado apena tienen dilocacione (10 2 línea de dilocacione/cm 2 ) Deformación plática Nº dilocacione : ( /cm 2 para alguno metale altamente deform. Fuente Frank-Read: Mecanimo multiplicación dilocacione de de 33
32 Defecto planare Imperfeccione bidimenionale Tipo: o Borde o Frontera o Límite de grano o Superficie o Falta de Apilamiento o Plano de Macla o Plano de Cizalladura Critaligráfica (CS) 34
33 Borde de Grano Interfae entre do critale con orientación, dicontinuidade en la orientación atómica. Epeo =f (Temp. Sinterización, tiempo, atmofera, mobilidad atómica, ) Formación: durante el proceo de olidificación: critale formado a partir de núcleo que crecen imultáneamente Claificación de borde de grano: o Borde de ángulo grande (diferencia de orientación mayor de 15-20º) o Borde de ángulo pequeño. 35
34 Borde de Grano de Ángulo Grande Modelo de borde de grano Situación má favorable Eg: eparación entre la dilocacione (defecto) e uniforme y periódica Modelo de átomo coincidente Aquello donde lo Xtale coinciden y poicione reticulare on ocupada por atm. que podrían pertenecer a cualquiera de lo xtale. 36
35 Borde de Grano de Ángulo Pequeño Modelo de dilocacione Sitema de dilocacione periódica eparada por regione deformada eláticamente, libre de defecto 37
36 Plano de Macla Plano que epara do parte de un grano con una pequeña diferencia de orientación de u plano ( macla = plano de reflexión) Formación: térmico. durante proceo de deformación o en tratamiento 38
37 Plano Critalográfico de Cizalladura (CS) Ej: TiO 2, WO 3, ReO 3, MoO 2, ReO 3 etá formado por octaedro ReO 6 que comparten vértice con 6 octaedro Plano CS Octaedro ReO 6 comparten lado 39
38 Compueto No Etequiométrico No tienen una relación atómica fija entre lo contituyente Ej: UO 2 poibilidade: (UO UO 2.25 ) Intervalo de compoición Ej: FeO : %O 50%; (51 %O 53) Fe 1-x O 3 Fe2+ < > 2 Fe
Tema 3.- Defectos-Imperfecciones
 BLOQUE II.- ESTRUCTURA Tema 3.- Defectos-Imperfecciones * James F. Shackerlford Introducción a la Ciencia de Materiales para Ingenieros. Cuarta edición. Ed. Prentice Hall (1998) 1 Objetivos Comprender
BLOQUE II.- ESTRUCTURA Tema 3.- Defectos-Imperfecciones * James F. Shackerlford Introducción a la Ciencia de Materiales para Ingenieros. Cuarta edición. Ed. Prentice Hall (1998) 1 Objetivos Comprender
Estructuras Cristalinas
 Estructuras Cristalinas Bibliografía: Solid State Chemistry: An introduction, L. Smart and E. Moore. 1992 Solid State Chemistry and its applications, A.R. West. 1984 1 Enlace en Cerámicos Iónico Mezcla
Estructuras Cristalinas Bibliografía: Solid State Chemistry: An introduction, L. Smart and E. Moore. 1992 Solid State Chemistry and its applications, A.R. West. 1984 1 Enlace en Cerámicos Iónico Mezcla
Tema 3. Solidificación, defectos y difusión en sólidos
 Tema 3. Solidificación, defectos y difusión en sólidos 2. Defectos a) Defectos puntuales b) Dislocaciones c) Defectos superficiales 3. Difusión en sólidos a) Generalidades b) Mecanismos de difusión c)
Tema 3. Solidificación, defectos y difusión en sólidos 2. Defectos a) Defectos puntuales b) Dislocaciones c) Defectos superficiales 3. Difusión en sólidos a) Generalidades b) Mecanismos de difusión c)
11. DEFECTOS CRISTALINOS Y NO-ESTEQUIOMETRÍA
 Tema 11. DEFECTOS CRISTALINOS Y NO-ESTEQUIOMETRÍA Cristales perfectos e imperfectos Tipos de defectos Defectos puntuales Defectos Schottky Defectos Frenkel Centros de color Cristales no-estequiométricos
Tema 11. DEFECTOS CRISTALINOS Y NO-ESTEQUIOMETRÍA Cristales perfectos e imperfectos Tipos de defectos Defectos puntuales Defectos Schottky Defectos Frenkel Centros de color Cristales no-estequiométricos
Conductores Iónicos. BLOQUE IV: CERAMICAS DE ALTAS PRESTACIONES Cerámicas Funcionales
 BLOQUE IV: CERAMICAS DE ALTAS PRESTACIONES Cerámicas Funcionales Conductores Iónicos Bibliografía: Solid State Chemistry: An introduction, L. Smart and E. Moore. 1992 (Cap. 3) Solid State Chemistry and
BLOQUE IV: CERAMICAS DE ALTAS PRESTACIONES Cerámicas Funcionales Conductores Iónicos Bibliografía: Solid State Chemistry: An introduction, L. Smart and E. Moore. 1992 (Cap. 3) Solid State Chemistry and
IMPERFECCIONES CRISTALINAS
 IMPERFECCIONES CRISTALINAS LOS DEFECTOS O IMPERFECCIONES AFECTAN LAS PROPIEDADES FISICAS Y MECANICAS: AFECTAN LA CAPACIDAD DE FORMACION DE ALEACIONES EN FRIO. CONDUCTIVIDAD ELECTRICA DE SEMICONDUCTORES
IMPERFECCIONES CRISTALINAS LOS DEFECTOS O IMPERFECCIONES AFECTAN LAS PROPIEDADES FISICAS Y MECANICAS: AFECTAN LA CAPACIDAD DE FORMACION DE ALEACIONES EN FRIO. CONDUCTIVIDAD ELECTRICA DE SEMICONDUCTORES
Universidad Técnica Nacional
 Universidad Técnica Nacional Química I-CB005 Unidad II Átomos Moléculas e Iones Teoría atómica de Dalton Postulados de la teoría atómica de Dalton: Los elementos están formados por partículas extremadamente
Universidad Técnica Nacional Química I-CB005 Unidad II Átomos Moléculas e Iones Teoría atómica de Dalton Postulados de la teoría atómica de Dalton: Los elementos están formados por partículas extremadamente
Estructuras Cristalinas. Julio Alberto Aguilar Schafer
 Estructuras Cristalinas Julio Alberto Aguilar Schafer Modelo del estado líquido los metales Modelo del paso del estado líquido al estado sólido de los metales Equilibrio líquido-vapor Presión de vapor
Estructuras Cristalinas Julio Alberto Aguilar Schafer Modelo del estado líquido los metales Modelo del paso del estado líquido al estado sólido de los metales Equilibrio líquido-vapor Presión de vapor
Objetivos de aprendizaje
 Objetivos de aprendizaje Conocer y describir las propiedades periódicas y su variación a través de grupos y periodos. Interpretar datos relacionados con las propiedades periódicas de los elementos. Propiedades
Objetivos de aprendizaje Conocer y describir las propiedades periódicas y su variación a través de grupos y periodos. Interpretar datos relacionados con las propiedades periódicas de los elementos. Propiedades
Los sólidos iónicos. Estructuras características de los sólidos iónicos
 Los sólidos iónicos Los compuestos iónicos suelen presentar una serie de características físicas que los distinguen de los covalentes. Así, los sólidos iónicos como el cloruro sódico y el nitrato de potasio
Los sólidos iónicos Los compuestos iónicos suelen presentar una serie de características físicas que los distinguen de los covalentes. Así, los sólidos iónicos como el cloruro sódico y el nitrato de potasio
Universidad Central de Venezuela Facultad de Ciencias Escuela de Química Unidad Docente de Principios de Química Principios de Química I
 Tema VI: Tabla periódica Universidad Central de Venezuela Facultad de Ciencias Escuela de Química Unidad Docente de Principios de Química Principios de Química I Guía de Problemas 1) Defina potencial de
Tema VI: Tabla periódica Universidad Central de Venezuela Facultad de Ciencias Escuela de Química Unidad Docente de Principios de Química Principios de Química I Guía de Problemas 1) Defina potencial de
Defectos cristalinos. Introducción a la Ciencia de Materiales. M. Bizarro
 Defectos cristalinos Monocristal Cuando el arreglo de un sólido cristalino es perfecto o se extiende completamente a lo largo del sólido sin interrupción, se dice que es un monocristal. Todas las celdas
Defectos cristalinos Monocristal Cuando el arreglo de un sólido cristalino es perfecto o se extiende completamente a lo largo del sólido sin interrupción, se dice que es un monocristal. Todas las celdas
SOLUCIONES BLOQUE 2. EL ÁTOMO: MODELOS, TABLA PERIÓDICA Y ENLACE QUÍMICO.
 SOLUCIONES BLOQUE 2. EL ÁTOMO: MODELOS, TABLA PERIÓDICA Y ENLACE QUÍMICO. Modelos Atómicos 1. Solución: Descubrimiento de los dos «tipos» de electricidad. Siglo XVIII. Descubrimiento del electrón. 1897.
SOLUCIONES BLOQUE 2. EL ÁTOMO: MODELOS, TABLA PERIÓDICA Y ENLACE QUÍMICO. Modelos Atómicos 1. Solución: Descubrimiento de los dos «tipos» de electricidad. Siglo XVIII. Descubrimiento del electrón. 1897.
TEMA 4. IMPERFECIONES EN SÓLIDOS
 TEMA 4. IMPERFECIONES EN SÓLIDOS En el Tema 3 se ha descrito el SÓLIDO CRISTALINO mediante la aproximación del CRISTAL IDEAL, que tomamos como modelo de perfección cristalina Los sólidos cristalinos reales
TEMA 4. IMPERFECIONES EN SÓLIDOS En el Tema 3 se ha descrito el SÓLIDO CRISTALINO mediante la aproximación del CRISTAL IDEAL, que tomamos como modelo de perfección cristalina Los sólidos cristalinos reales
I.E.S. Grande Covián Física y Química 4º ESO ACTIVIDADES SOBRE ÁTOMO, SISTEMA PERIÓDICO Y ENLACES QUÍMICOS
 I.E.S. Grande Covián Física y Química 4º ESO ACTIVIDADES SOBRE ÁTOMO, SISTEMA PERIÓDICO Y ENLACES QUÍMICOS Nombre:. Apellidos: Grupo: Fecha:. 1º) Escribe la diferencia fundamental entre el modelo atómico
I.E.S. Grande Covián Física y Química 4º ESO ACTIVIDADES SOBRE ÁTOMO, SISTEMA PERIÓDICO Y ENLACES QUÍMICOS Nombre:. Apellidos: Grupo: Fecha:. 1º) Escribe la diferencia fundamental entre el modelo atómico
Tema 3. El cristal real
 3.1. Imperfecciones en los sólidos 3.1.1. Defectos puntuales: vacantes, intersticiales e impurezas 3.1.2. Defectos lineales: dislocaciones 3.1.3. Defectos superficiales 3.1.4. Influencia de las dislocaciones
3.1. Imperfecciones en los sólidos 3.1.1. Defectos puntuales: vacantes, intersticiales e impurezas 3.1.2. Defectos lineales: dislocaciones 3.1.3. Defectos superficiales 3.1.4. Influencia de las dislocaciones
EJERCICIOS RESUELTOS DE ENLACE QUIMICO
 EJERCICIOS RESUELTOS DE ENLACE QUIMICO 1. a) Qué tipo de enlace presenta el compuesto formado por F y Ca? b) Formule dicho compuesto a) Considerando los números atómicos del F (Z=9) y el Ca (Z=20) se desarrollan
EJERCICIOS RESUELTOS DE ENLACE QUIMICO 1. a) Qué tipo de enlace presenta el compuesto formado por F y Ca? b) Formule dicho compuesto a) Considerando los números atómicos del F (Z=9) y el Ca (Z=20) se desarrollan
Ejercicios y respuestas del apartado: Enlaces (covalente, iónico, metálico): Definición, propiedades, estructura de Lewis, ejercicios de predicción
 Ejercicios y respuestas del apartado: Enlaces (covalente, iónico, metálico): Definición, propiedades, estructura de Lewis, ejercicios de predicción de enlace 2 de 12 Qué es el enlace químico?, iguales
Ejercicios y respuestas del apartado: Enlaces (covalente, iónico, metálico): Definición, propiedades, estructura de Lewis, ejercicios de predicción de enlace 2 de 12 Qué es el enlace químico?, iguales
Tema 2.- Estructura de la Materia
 BLOQUE II.- ESTRUCTURA Estructura de la Materia * James F. Shackerlford Introducción a la Ciencia de Materiales para Ingenieros. Cuarta edición. Ed. Prentice Hall (1998) * Pat L. Mangonon Ciencia de Materiales:
BLOQUE II.- ESTRUCTURA Estructura de la Materia * James F. Shackerlford Introducción a la Ciencia de Materiales para Ingenieros. Cuarta edición. Ed. Prentice Hall (1998) * Pat L. Mangonon Ciencia de Materiales:
Unidad 1: Estructura atómica de la materia
 ACTIVIDADES Unidad 1: Estructura atómica de la materia Para a realización de ditas actividades recoméndase seguir a seguinte páxina de internet do Ministerio de Educación e ciencia na cal se explica de
ACTIVIDADES Unidad 1: Estructura atómica de la materia Para a realización de ditas actividades recoméndase seguir a seguinte páxina de internet do Ministerio de Educación e ciencia na cal se explica de
ENLACE QUÍMICO UNIDADES ESTRUCTURALES DE LAS SUSTANCIAS IONES ÁTOMOS MOLÉCULAS ENLACE IÓNICO ENLACE METÁLICO ENLACE COVALENTE ENLACE COVALENTE
 ENLACE QUÍMICO Y TIPOS ENLACE QUÍMICO Enlace químico es la fuerza responsable de la unión entre las unidades estructurales ( iones, átomos o moléculas) que forman la materia. UNIDADES ESTRUCTURALES DE
ENLACE QUÍMICO Y TIPOS ENLACE QUÍMICO Enlace químico es la fuerza responsable de la unión entre las unidades estructurales ( iones, átomos o moléculas) que forman la materia. UNIDADES ESTRUCTURALES DE
Empaquetamiento compacto
 Empaquetamiento compacto Energía y empaquetamiento No denso, empaquetamiento aleatorio Energy Distancia del enlace energía de enlace Denso, empaquetamiento ordenado Energy distancia del enlace r Energía
Empaquetamiento compacto Energía y empaquetamiento No denso, empaquetamiento aleatorio Energy Distancia del enlace energía de enlace Denso, empaquetamiento ordenado Energy distancia del enlace r Energía
Estructura de sólidos
 Estructura de sólidos Química Inorgánica - 2006 Tipos de estructuras cristalinas cristal enlace características molecular covalente-baja energía cristales blandos, bajo p.f. red covalente covalente cristales
Estructura de sólidos Química Inorgánica - 2006 Tipos de estructuras cristalinas cristal enlace características molecular covalente-baja energía cristales blandos, bajo p.f. red covalente covalente cristales
IMPERFECCIONES EN SÓLIDOSS
 IMPERFECCIONES EN SÓLIDOSS UN ORDENAMIENTO PERFECTO DE LOS ÁTOMOS EN LOS MATERIALES CRISTALINOS SOLAMENTE PUEDE OCURRIR A UNA TEMPERATURA DE 0 K. TAL SÓLIDO IDEAL NO EXISTE: TODOS TIENEN GRAN NÚMERO DE
IMPERFECCIONES EN SÓLIDOSS UN ORDENAMIENTO PERFECTO DE LOS ÁTOMOS EN LOS MATERIALES CRISTALINOS SOLAMENTE PUEDE OCURRIR A UNA TEMPERATURA DE 0 K. TAL SÓLIDO IDEAL NO EXISTE: TODOS TIENEN GRAN NÚMERO DE
EJERCICIO DE EXAMEN DE QUÍMICA INORGÁNICA
 EJERCICIO DE EXAMEN DE QUÍMICA INORGÁNICA Las 6 preguntas siguientes se refieren a la tabla periódica que se presenta. Los símbolos han sido asignados arbitrariamente. D H B A E M G J L R X Y N P Q Z T
EJERCICIO DE EXAMEN DE QUÍMICA INORGÁNICA Las 6 preguntas siguientes se refieren a la tabla periódica que se presenta. Los símbolos han sido asignados arbitrariamente. D H B A E M G J L R X Y N P Q Z T
FÍSICA Y QUÍMICA 3º ESO ACTIVIDADES DE RECUPERACIÓN
 FÍSICA Y QUÍMICA 3º ESO ACTIVIDADES DE RECUPERACIÓN (PARTE 2) CURSO 2012/13 Nombre y apellidos: 1 LA CIENCIA Y SU MÉTODO. MEDIDA DE MAGNITUDES LOS ÁTOMOS Y SU COMPLEJIDAD 1. Qué explica el modelo atómico
FÍSICA Y QUÍMICA 3º ESO ACTIVIDADES DE RECUPERACIÓN (PARTE 2) CURSO 2012/13 Nombre y apellidos: 1 LA CIENCIA Y SU MÉTODO. MEDIDA DE MAGNITUDES LOS ÁTOMOS Y SU COMPLEJIDAD 1. Qué explica el modelo atómico
MODIFICACIÓN DE LAS PROPIEDADES DE LOS METALES CONTENIDOS
 MODIFICACIÓN DE LAS PROPIEDADES DE LOS METALES CONTENIDOS Generalidades Estructura interna de los metales. Defectos en la estructura cristalina Soluciones sólidas Mecanismos de endurecimiento de los metales
MODIFICACIÓN DE LAS PROPIEDADES DE LOS METALES CONTENIDOS Generalidades Estructura interna de los metales. Defectos en la estructura cristalina Soluciones sólidas Mecanismos de endurecimiento de los metales
ENLACE IÓNICO O ELECTROVALENTE
 ENLACE IÓNICO O ELECTROVALENTE Servicios Educativos Integrales Caracterizado por: o Cesión de electrones por parte de un metal a un no metal o Formación de iones de carga contraria, metal (+) y no metal
ENLACE IÓNICO O ELECTROVALENTE Servicios Educativos Integrales Caracterizado por: o Cesión de electrones por parte de un metal a un no metal o Formación de iones de carga contraria, metal (+) y no metal
Sistema Periódico de los elementos. 2º Bachillerato
 Sistema Periódico de los elementos 2º Bachillerato Índice 1. Clasificación de los elementos 2. Núcleo atómico 3. Configuración electrónica 4. La tabla periódica 5. Propiedades periódicas Tamaño y radio
Sistema Periódico de los elementos 2º Bachillerato Índice 1. Clasificación de los elementos 2. Núcleo atómico 3. Configuración electrónica 4. La tabla periódica 5. Propiedades periódicas Tamaño y radio
Estructura Cristalina de Sólidos
 Estructura Cristalina de Sólidos Relación entre estructura periódica y propiedades Bibliografía: 1. Solid State Physics. Ashcroft and Mermin. 2. Solid State Chemistry. West. 3. Química del Estado Sólido.
Estructura Cristalina de Sólidos Relación entre estructura periódica y propiedades Bibliografía: 1. Solid State Physics. Ashcroft and Mermin. 2. Solid State Chemistry. West. 3. Química del Estado Sólido.
INSTITUTO POLITECNICO NACIONAL
 INSTITUTO POLITECNICO NACIONAL CECYT NO. 1 GONZALO VÁZQUEZ VELA GUÍA DE QUÍMICA I PERIÓDO ESCOLAR 2015-2016 ACADEMIA DE QUÍMICA TURNO VESPERTINO 1 Materia y Energía 1.- Calcula la energía, en Joules y
INSTITUTO POLITECNICO NACIONAL CECYT NO. 1 GONZALO VÁZQUEZ VELA GUÍA DE QUÍMICA I PERIÓDO ESCOLAR 2015-2016 ACADEMIA DE QUÍMICA TURNO VESPERTINO 1 Materia y Energía 1.- Calcula la energía, en Joules y
29/09/2010 TEMA 2. CONTENIDO. Continuación Tema 2. Configuración electrónica de cationes y aniones. de elementos representativos.
 2 Continuación Tema 2 Prof(a): María Angélica Sánchez Palacios TEMA 2. CONTENIDO Introducción a la forma y características de la tabla periódica. Introducción a los modelos atómicos. El Método Científico.
2 Continuación Tema 2 Prof(a): María Angélica Sánchez Palacios TEMA 2. CONTENIDO Introducción a la forma y características de la tabla periódica. Introducción a los modelos atómicos. El Método Científico.
2x = x = M. 100 = α = % NOCl eq K C =
 1 Universidad de Castilla la Mancha Selectividad Septiembre.013 Opción A SEPTIEMBRE 013 1.- El cloruro de nitrosilo es un gas utilizado en la síntesis de productos farmacéuticos. Se descompone a altas
1 Universidad de Castilla la Mancha Selectividad Septiembre.013 Opción A SEPTIEMBRE 013 1.- El cloruro de nitrosilo es un gas utilizado en la síntesis de productos farmacéuticos. Se descompone a altas
2/15/2013. Estructura ENLACE QUIMICO Y MOLÉCULAS. Tipos de enlace Enlace iónico Enlace metálico Enlace covalente CH 4 CH 3 OH.
 ENLACE QUIMICO Y MOLÉCULAS Tipos de enlace Enlace iónico Enlace metálico Enlace covalente Símbolos de Lewis y regla dl del octeto Compuestos químicos: Representaciones Metano CH 4 Etanol CH 3 OH Ácido
ENLACE QUIMICO Y MOLÉCULAS Tipos de enlace Enlace iónico Enlace metálico Enlace covalente Símbolos de Lewis y regla dl del octeto Compuestos químicos: Representaciones Metano CH 4 Etanol CH 3 OH Ácido
UNIDAD EDUCATIVA COLEGIO SAN ANTONIO DEL TUY OCUMARE DEL TUY, ESTADO MIRANDA ASIGNATURA: QUÍMICA
 UNIDAD EDUCATIVA COLEGIO SAN ANTONIO DEL TUY OCUMARE DEL TUY, ESTADO MIRANDA ASIGNATURA: QUÍMICA GUÍA DE ESTUDIO DE PROBLEMAS Y CUESTIONARIO PARA EL EXAMEN DE LAPSO DE 3ER AÑO Profesor: Carlos M. Landaeta
UNIDAD EDUCATIVA COLEGIO SAN ANTONIO DEL TUY OCUMARE DEL TUY, ESTADO MIRANDA ASIGNATURA: QUÍMICA GUÍA DE ESTUDIO DE PROBLEMAS Y CUESTIONARIO PARA EL EXAMEN DE LAPSO DE 3ER AÑO Profesor: Carlos M. Landaeta
EL ÁTOMO. Estructura del átomo. Núcleo. Envoltura. La materia esta constituida por pequeñas partículas llamadas átomos
 ESTRUCTURA ATOMICA EL ÁTOMO La materia esta constituida por pequeñas partículas llamadas átomos Estructura del átomo Envoltura Núcleo ESTRUCTURA Y CONSTITUCIÓN DEL ÁTOMO electrones protones neutrones CARACTERÍSTICAS
ESTRUCTURA ATOMICA EL ÁTOMO La materia esta constituida por pequeñas partículas llamadas átomos Estructura del átomo Envoltura Núcleo ESTRUCTURA Y CONSTITUCIÓN DEL ÁTOMO electrones protones neutrones CARACTERÍSTICAS
EL SISTEMA PERIÓDICO
 EL SISTEMA PERIÓDICO CONTENIDOS. 1.- Primeras clasificaciones de los elementos químicos. 2.- Clasificaciones de Meyer y Mendeleiev. 3.- Clasificación actual de los elementos químicos. 4.- Tabla periódica
EL SISTEMA PERIÓDICO CONTENIDOS. 1.- Primeras clasificaciones de los elementos químicos. 2.- Clasificaciones de Meyer y Mendeleiev. 3.- Clasificación actual de los elementos químicos. 4.- Tabla periódica
UNIVERSIDAD NACIONAL AGRARIA LA MOLINA CENTRO DE ESTUDIOS PREUNIVERSITARIOS SEGUNDO SEMINARIO DE QUIMICA
 UNIVERSIDAD NACIONAL AGRARIA LA MOLINA CENTRO DE ESTUDIOS PREUNIVERSITARIOS SEGUNDO SEMINARIO DE QUIMICA 1. La configuración electrónica del átomo del elemento E es: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 1
UNIVERSIDAD NACIONAL AGRARIA LA MOLINA CENTRO DE ESTUDIOS PREUNIVERSITARIOS SEGUNDO SEMINARIO DE QUIMICA 1. La configuración electrónica del átomo del elemento E es: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 1
Introducción a la Formulación y Nomenclatura de las Sustancias Inorgánicas
 D EPA R T A M ENTO D E FÍSICA Y Q UÍM ICA Introducción a la Formulación y Nomenclatura de las Sustancias Inorgánicas José Manuel Ramírez Fernández Valencias y estados, grados o números de oxidación Con
D EPA R T A M ENTO D E FÍSICA Y Q UÍM ICA Introducción a la Formulación y Nomenclatura de las Sustancias Inorgánicas José Manuel Ramírez Fernández Valencias y estados, grados o números de oxidación Con
Tipos de Reacciones Químicas.
 Tipos de Reacciones Químicas. Reacción Química Proceso durante el cual una sustancia (o sustancias) cambia para formar una o más sustancias nuevas. Reactivos: Sustancias de las que se parte en una reacción
Tipos de Reacciones Químicas. Reacción Química Proceso durante el cual una sustancia (o sustancias) cambia para formar una o más sustancias nuevas. Reactivos: Sustancias de las que se parte en una reacción
ALEACIONES 1. INTRODUCCION 2. CLASIFICACION 3. SOLUCIONES SÓLIDAS 4. FASES INTERMEDIAS 5. SOLUCIONES SÓLIDAS ORDENADAS M.V.M.G ALEACIONES 1
 ALEACIONES 1. INTRODUCCION 2. CLASIFICACION 3. SOLUCIONES SÓLIDAS 4. FASES INTERMEDIAS 5. SOLUCIONES SÓLIDAS ORDENADAS 2007-08 ALEACIONES 1 INTRODUCCIÓN Una aleación es la combinación de dos o más metales,
ALEACIONES 1. INTRODUCCION 2. CLASIFICACION 3. SOLUCIONES SÓLIDAS 4. FASES INTERMEDIAS 5. SOLUCIONES SÓLIDAS ORDENADAS 2007-08 ALEACIONES 1 INTRODUCCIÓN Una aleación es la combinación de dos o más metales,
ORGANIZACIÓN DE LOS ELEMENTOS EN LA TABLA PERIÓICA PROPIEDADES PERIÓDICAS
 Nombre del estudiante: Grado: Asignatura: Química Tema: Organización de los elementos en la tabla periódica. Propiedades periódicas. Indicador de logro: Ubico un determinado elemento en la tabla periódica
Nombre del estudiante: Grado: Asignatura: Química Tema: Organización de los elementos en la tabla periódica. Propiedades periódicas. Indicador de logro: Ubico un determinado elemento en la tabla periódica
CAPITULO 2 LA TABLA PERIODICA
 1.0079 1 H HIDROGENO 6.941 3 Li LITIO 22.989 11 Na SODIO 30.098 19 K POTASIO CAPITULO 2 LA TABLA PERIODICA ORDENAMIENTO ACTUAL GRUPOS Y PERIODOS PROPIEDADES PERIODICAS TAMAÑO POTENCIAL DE IONIZACION AFINIDAD
1.0079 1 H HIDROGENO 6.941 3 Li LITIO 22.989 11 Na SODIO 30.098 19 K POTASIO CAPITULO 2 LA TABLA PERIODICA ORDENAMIENTO ACTUAL GRUPOS Y PERIODOS PROPIEDADES PERIODICAS TAMAÑO POTENCIAL DE IONIZACION AFINIDAD
Física del Estado Sólido REDES CRISTALINAS. Dr. Andrés Ozols. Facultad de Ingeniería Universidad de Buenos Aires. Dr. A. Ozols 1
 Física del Estado Sólido REDES CRISTALINAS Dr. Andrés Ozols Facultad de Ingeniería Universidad de Buenos Aires 2009 Dr. A. Ozols 1 ÁTOMOS EN SÓLIDOS Dr. A. Ozols 2 ORDEN CRISTALINO y FORMA René Just Hauy
Física del Estado Sólido REDES CRISTALINAS Dr. Andrés Ozols Facultad de Ingeniería Universidad de Buenos Aires 2009 Dr. A. Ozols 1 ÁTOMOS EN SÓLIDOS Dr. A. Ozols 2 ORDEN CRISTALINO y FORMA René Just Hauy
Consideraciones sobre estructuras representativas
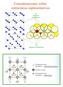 Consideraciones sobre estructuras representativas CONSIDERACIONES SOBRE ESTRUCTURAS REPRESENTATIVAS: En el empacamiento compacto hcp y ccp el número de coordinación es 12 Los elementos metálicos son los
Consideraciones sobre estructuras representativas CONSIDERACIONES SOBRE ESTRUCTURAS REPRESENTATIVAS: En el empacamiento compacto hcp y ccp el número de coordinación es 12 Los elementos metálicos son los
Tema 3: Técnicas de dopado
 Tema 3: Técnica de dopado Bibliografía divera Varia técnica: Durante el crecimiento Difuión Implantación iónica Etudiaremo: Aplicacione itema/método/tecnología Teoría Ejemplo Tema 3: Técnica de dopado
Tema 3: Técnica de dopado Bibliografía divera Varia técnica: Durante el crecimiento Difuión Implantación iónica Etudiaremo: Aplicacione itema/método/tecnología Teoría Ejemplo Tema 3: Técnica de dopado
Colección de problemas Unidad 2
 Facultad de Química, UNAM Curso: Química General I Colección de problemas Unidad 2 1. Describe una contribución importante a la ciencia hecha por cada uno de los científicos siguientes: Dalton, Thomson,
Facultad de Química, UNAM Curso: Química General I Colección de problemas Unidad 2 1. Describe una contribución importante a la ciencia hecha por cada uno de los científicos siguientes: Dalton, Thomson,
TEMA 1: ESTRUCTURA INTERNA DE LOS MATERIALES
 PERIODO Departamento de Tecnología. IES Nuestra Señora de la Almudena Mª Jesús Saiz TEMA 1: ESTRUCTURA INTERNA DE LOS MATERIALES El átomo: Toda la materia está compuesta por átomos y éstos por partículas
PERIODO Departamento de Tecnología. IES Nuestra Señora de la Almudena Mª Jesús Saiz TEMA 1: ESTRUCTURA INTERNA DE LOS MATERIALES El átomo: Toda la materia está compuesta por átomos y éstos por partículas
INTRODUCCIÓN A LA QUÍMICA
 INTRODUCCIÓN A LA QUÍMICA TRABAJO PRÁCTICO N 1 4 Año A, B, C, D 2.015 Prof. María Laura Sepúlveda Broky INTRODUCCIÓN A LA QUÍMICA Prof. María Laura Sepúlveda Broky 1)A- Realizar un esquema de la Tabla
INTRODUCCIÓN A LA QUÍMICA TRABAJO PRÁCTICO N 1 4 Año A, B, C, D 2.015 Prof. María Laura Sepúlveda Broky INTRODUCCIÓN A LA QUÍMICA Prof. María Laura Sepúlveda Broky 1)A- Realizar un esquema de la Tabla
LA TABLA PERIÓDICA. 1
 LA TABLA PERIÓDICA. 1 Clasificación de Mendeleiev Clasificó lo 63 elementos conocidos utilizando el criterio de masa atómica creciente, ya que no se conocía el concepto de número atómico puesto que no
LA TABLA PERIÓDICA. 1 Clasificación de Mendeleiev Clasificó lo 63 elementos conocidos utilizando el criterio de masa atómica creciente, ya que no se conocía el concepto de número atómico puesto que no
1. Estructura atómica y clasificación periódica
 Química 1. Estructura atómica y clasificación periódica Para comenzar. Para afianzar los contenidos teóricos correspondientes a este capítulo, les proponemos una serie de actividades que es conveniente
Química 1. Estructura atómica y clasificación periódica Para comenzar. Para afianzar los contenidos teóricos correspondientes a este capítulo, les proponemos una serie de actividades que es conveniente
EJERCICIOS DE SELECTIVIDAD DE QUÍMICA. TEMAS 1 Y 2
 EJERCICIOS DE SELECTIVIDAD DE QUÍMICA. TEMAS 1 Y 2 1.- a) Razone si una molécula de fórmula AB 2 debe ser siempre lineal. b) Justifique quién debe tener un punto de fusión mayor, el CsI o el CaO. c) Ponga
EJERCICIOS DE SELECTIVIDAD DE QUÍMICA. TEMAS 1 Y 2 1.- a) Razone si una molécula de fórmula AB 2 debe ser siempre lineal. b) Justifique quién debe tener un punto de fusión mayor, el CsI o el CaO. c) Ponga
Prueba objetiva. Física y Química. Bloque III.
 Prueba objetiva. Física y Química. Bloque III. 1) Explicar el significado de los siguientes conceptos: 1.- Potencial de ionización: 2.- Criterios de ordenación de los elementos dentro de la Tabla Periódica:
Prueba objetiva. Física y Química. Bloque III. 1) Explicar el significado de los siguientes conceptos: 1.- Potencial de ionización: 2.- Criterios de ordenación de los elementos dentro de la Tabla Periódica:
1. Sistemas materiales: propiedades 2. Estados de agregación g de los sistemas materiales 3. Teoría cinético molecular
 UNIDAD 1: DIVERSIDAD Y UNIDAD DE ESTRUCTURA DE LA MATERIA 1. Sistemas materiales: propiedades 2. Estados de agregación g de los sistemas materiales 3. Teoría cinético molecular 4. Sustanciaspuras puras,
UNIDAD 1: DIVERSIDAD Y UNIDAD DE ESTRUCTURA DE LA MATERIA 1. Sistemas materiales: propiedades 2. Estados de agregación g de los sistemas materiales 3. Teoría cinético molecular 4. Sustanciaspuras puras,
Tema 6. Equilibrios de precipitación
 Tema 6. Equilibrios de precipitación 1. Introducción. 2. Solubilidad y Constante de solubilidad. 3. Sales poco solubles. 4. Factores que afectan a la solubilidad. 5. Predicción de las reacciones de precipitación.
Tema 6. Equilibrios de precipitación 1. Introducción. 2. Solubilidad y Constante de solubilidad. 3. Sales poco solubles. 4. Factores que afectan a la solubilidad. 5. Predicción de las reacciones de precipitación.
Enlace Químico. Química General I 2012
 Enlace Químico Química General I 2012 Los electrones de valencia son los electrones del último orbital en un átomo, son los causantes de los enlaces químicos. Grupo e - configuración # de valencia 1A ns
Enlace Químico Química General I 2012 Los electrones de valencia son los electrones del último orbital en un átomo, son los causantes de los enlaces químicos. Grupo e - configuración # de valencia 1A ns
ANEXOS. Química Física I Termodinámica. Área de Química Física Departamento de Química F.Q.B.F. U.N.S.L.
 ANEXOS Química Física I Termodinámica Área de Química Física Departamento de Química F.Q.B.F. U.N.S.L. Contenido Tabla Periódica de los Elementos... 2 Constantes Fundamentales y Datos Generales... 3 Ajuste
ANEXOS Química Física I Termodinámica Área de Química Física Departamento de Química F.Q.B.F. U.N.S.L. Contenido Tabla Periódica de los Elementos... 2 Constantes Fundamentales y Datos Generales... 3 Ajuste
Tema 4: Propiedades periódicas de los elementos - 1 -
 Tema 4: Propiedades periódicas de los - - BIBLIOGRAFÍA: * Estructura atómica y enlace químico J. Casabó i Gispert * Química. Curso Universitario B.M. Mahan y R.J. Myers * Química General R.H. Petrucci,
Tema 4: Propiedades periódicas de los - - BIBLIOGRAFÍA: * Estructura atómica y enlace químico J. Casabó i Gispert * Química. Curso Universitario B.M. Mahan y R.J. Myers * Química General R.H. Petrucci,
Equilibrio sólido- líquido en sistemas de dos componentes
 Equilibrio sólido- líquido en sistemas de dos componentes Miscibilidad en fase líquida e inmiscibilidad en fase sólida: sean C y B dos sustancias miscibles en todas las proporciones en la fase líquida
Equilibrio sólido- líquido en sistemas de dos componentes Miscibilidad en fase líquida e inmiscibilidad en fase sólida: sean C y B dos sustancias miscibles en todas las proporciones en la fase líquida
FÍSICA Y QUÍMICA 1º Bachillerato Ejercicios: El átomo y sus enlaces
 1(9) Ejercicio nº 1 Calcula el número atómico y el número másico, así como el número de protones, neutrones y electrones de los siguientes aniones: 35 1 80 1 1 31 3 17 Cl ; Br ; O ; P 35 8 15 Ejercicio
1(9) Ejercicio nº 1 Calcula el número atómico y el número másico, así como el número de protones, neutrones y electrones de los siguientes aniones: 35 1 80 1 1 31 3 17 Cl ; Br ; O ; P 35 8 15 Ejercicio
QUÍMICA GENERAL E INORGÁNICA QUÍMICA GENERAL REACCIONES QUÍMICAS Y ESTEQUIOMETRÍA
 QUÍMICA GENERAL E INORGÁNICA QUÍMICA GENERAL REACCIONES QUÍMICAS Y ESTEQUIOMETRÍA 2016 Equipo docente: Profesora Titular: Dra. Graciela Valente Profesora Adjunta: Dra. Cecilia Medaura Jefes de Trabajos
QUÍMICA GENERAL E INORGÁNICA QUÍMICA GENERAL REACCIONES QUÍMICAS Y ESTEQUIOMETRÍA 2016 Equipo docente: Profesora Titular: Dra. Graciela Valente Profesora Adjunta: Dra. Cecilia Medaura Jefes de Trabajos
DEFECTOS E IMPERFECCIONES CRISTALINAS
 DEFECTOS E IMPERFECCIONES CRISTALINAS Realmente no existen cristales perfectos sino que contienen varios tipos de imperfecciones y defectos, que afectan a muchas de sus propiedades físicas y mecánicas
DEFECTOS E IMPERFECCIONES CRISTALINAS Realmente no existen cristales perfectos sino que contienen varios tipos de imperfecciones y defectos, que afectan a muchas de sus propiedades físicas y mecánicas
Ejercicios UD. 4 Elementos y Compuestos Física y Química CEPA COSLADA
 1.- En qué consistía la ley de las triadas? Quién la propuso? 2.- Por qué la tabla donde se ordenan los elementos químicos se llama tabla periódica? Los elementos están ordenados en la tabla periódica
1.- En qué consistía la ley de las triadas? Quién la propuso? 2.- Por qué la tabla donde se ordenan los elementos químicos se llama tabla periódica? Los elementos están ordenados en la tabla periódica
b) La zona externa del átomo se llama CORTEZA. y ahí es donde se mueven los ELECTRONES
 PREGUNTAS DE RESPUESTA BREVE 1. Completa las siguientes frases relativas a los átomos de los elementos: a) La parte del átomo en donde se puede considerar que se concentra toda su masa es el NÚCLEO y ahí
PREGUNTAS DE RESPUESTA BREVE 1. Completa las siguientes frases relativas a los átomos de los elementos: a) La parte del átomo en donde se puede considerar que se concentra toda su masa es el NÚCLEO y ahí
TEMA 3. DIAGRAMAS DE FASES BINARIOS
 TEMA 3. DIAGRAMAS DE FASES BINARIOS 3.1. INTRODUCCIÓN 3.2. SOLUCIONES SÓLIDAS 3.3. SOLUBILIDAD TOTAL 3.4. REACCIONES INVARIANTES 3.5. EJEMPLOS Tema 3. Diagramas de fases binarios 1 3.1. INTRODUCCIÓN MICROESTRUCTURA
TEMA 3. DIAGRAMAS DE FASES BINARIOS 3.1. INTRODUCCIÓN 3.2. SOLUCIONES SÓLIDAS 3.3. SOLUBILIDAD TOTAL 3.4. REACCIONES INVARIANTES 3.5. EJEMPLOS Tema 3. Diagramas de fases binarios 1 3.1. INTRODUCCIÓN MICROESTRUCTURA
Actividad: Cómo son las configuraciones electrónicas?
 Cómo son las configuraciones electrónicas de los elementos que forman una familia? Nivel: 2º Medio Subsector: Ciencias químicas Unidad temática: Actividad: Cómo son las configuraciones electrónicas? En
Cómo son las configuraciones electrónicas de los elementos que forman una familia? Nivel: 2º Medio Subsector: Ciencias químicas Unidad temática: Actividad: Cómo son las configuraciones electrónicas? En
GUIA DE REPASO 1º MEDIO PREPARACION EXAMEN. Subsector: QUÍMICA Docente: Liduvina Campos A. Nombre alumno: Curso: Fecha:
 Liceo Polivalente Juan Antonio Ríos Quinta Normal GUIA DE REPASO 1º MEDIO PREPARACION EXAMEN Unidad temática: Ejercicios de contenidos Guías 0 a 6 Objetivo General: Repaso de contenidos guías 0 a 6 Contenidos:
Liceo Polivalente Juan Antonio Ríos Quinta Normal GUIA DE REPASO 1º MEDIO PREPARACION EXAMEN Unidad temática: Ejercicios de contenidos Guías 0 a 6 Objetivo General: Repaso de contenidos guías 0 a 6 Contenidos:
Contenido. 3.- Carga nuclear efectiva y reactividad. 4.- Propiedades periódicas:
 LA TABLA PERIÓDICA Contenido Primeras clasificaciones periódicas. 1.1. Sistema periódico de Mendeleiev. 2.- La tabla periódica. 2.1. Ley de Moseley. 3.- Carga nuclear efectiva y reactividad. 4.- Propiedades
LA TABLA PERIÓDICA Contenido Primeras clasificaciones periódicas. 1.1. Sistema periódico de Mendeleiev. 2.- La tabla periódica. 2.1. Ley de Moseley. 3.- Carga nuclear efectiva y reactividad. 4.- Propiedades
El resultado es el Sistema Periódico. -En el sistema periódico los elementos están colocados por orden creciente de su número atómico (Z).
 Tema 2. La Tabla periódica -Desde hace tiempo los químicos han intentado ordenar los elementos de forma que queden agrupados aquellos que tienen propiedades químicas similares El resultado es el Sistema
Tema 2. La Tabla periódica -Desde hace tiempo los químicos han intentado ordenar los elementos de forma que queden agrupados aquellos que tienen propiedades químicas similares El resultado es el Sistema
Celdas Galvánicas y Electrolíticas
 Celdas Galvánicas y Electrolíticas Reacciones de óxido-reducción Reacciones en las cuales una o más de las sustancias intervinientes modifica su estado de oxidación. Znº (s) + Cu +2 (ac) Zn 2+ (ac) + Cuº
Celdas Galvánicas y Electrolíticas Reacciones de óxido-reducción Reacciones en las cuales una o más de las sustancias intervinientes modifica su estado de oxidación. Znº (s) + Cu +2 (ac) Zn 2+ (ac) + Cuº
TEMA 2 TEMA PROPIEDADES PERIÓDICAS DE LOS PROPIEDADES PERIÓDICAS DE ELEMENT LOS
 Tema 2 La Tabla Periódica TEMA 2 PROPIEDADES PERIÓDICAS DE LOS ELEMENTOS 1. Períodos y grupos. La clasificación de Mendeléev. 2. Periodicidad de las estructuras electrónicas. 3. Periodicidad de las propiedades
Tema 2 La Tabla Periódica TEMA 2 PROPIEDADES PERIÓDICAS DE LOS ELEMENTOS 1. Períodos y grupos. La clasificación de Mendeléev. 2. Periodicidad de las estructuras electrónicas. 3. Periodicidad de las propiedades
COLEGIO SAN JOSÉ - Hijas de María Auxiliadora C/ Emilio Ferrari, 87 - Madrid Departamento de Ciencias Naturales
 TEMA 1. ELEMENTOS Y COMPUESTOS EJERCICIOS 5. El enlace químico 1. Explica el proceso de formación del enlace iónico en el cloruro de aluminio (AlCl 3 ). a) Escribe las configuraciones electrónicas del
TEMA 1. ELEMENTOS Y COMPUESTOS EJERCICIOS 5. El enlace químico 1. Explica el proceso de formación del enlace iónico en el cloruro de aluminio (AlCl 3 ). a) Escribe las configuraciones electrónicas del
(ii) explique por qué la primera energía de ionización del magnesio es mayor que el de sodio.
 TABLA PERIÓDICA 1. Qué propiedad generalmente disminuye a lo largo del período 3? A. número atómico B. electronegatividad C. radio atómico D. primera energía de ionización 2. Qué propiedad aumenta hacia
TABLA PERIÓDICA 1. Qué propiedad generalmente disminuye a lo largo del período 3? A. número atómico B. electronegatividad C. radio atómico D. primera energía de ionización 2. Qué propiedad aumenta hacia
PAU Química. Septiembre 2008 PRIMERA PARTE
 1 PAU Química. Septiembre 2008 PRIMERA PARTE Cuestión 1. A las siguientes especies: X, Y y Z +, les corresponden los números atómicos 17, 18 y 19, respectivamente. a) Escriba la configuración electrónica
1 PAU Química. Septiembre 2008 PRIMERA PARTE Cuestión 1. A las siguientes especies: X, Y y Z +, les corresponden los números atómicos 17, 18 y 19, respectivamente. a) Escriba la configuración electrónica
Unidad 7 LA TABLA PERIÓDICA.
 Unidad 7 LA TABLA PERIÓDICA. Primeras clasificaciones REPASO periódicas. Cuando a principios del siglo XIX se midieron las masas atómicas de una gran cantidad de elementos, se observó que ciertas propiedades
Unidad 7 LA TABLA PERIÓDICA. Primeras clasificaciones REPASO periódicas. Cuando a principios del siglo XIX se midieron las masas atómicas de una gran cantidad de elementos, se observó que ciertas propiedades
Esquema del tema. Tema 4: Enlace iónico. Un poco de empirismo
 Esquema del tema Modelo iónico Características de los compuestos iónicos Corrigiendo el modelo iónico: Polarización y Módulo 12555- Química Inorgánica Título: Ingeniería Química Responsable: Juan José
Esquema del tema Modelo iónico Características de los compuestos iónicos Corrigiendo el modelo iónico: Polarización y Módulo 12555- Química Inorgánica Título: Ingeniería Química Responsable: Juan José
PROPIEDADES PERIÓDICAS Y CONFIGURACIÓN ELECTRÓNICA
 PROPIEDADES PERIÓDICAS Y CONFIGURACIÓN ELECTRÓNICA Se conocen con el nombre de propiedades periódicas a aquellas propiedades relacionadas con la actividad química de los elementos y que varían de forma
PROPIEDADES PERIÓDICAS Y CONFIGURACIÓN ELECTRÓNICA Se conocen con el nombre de propiedades periódicas a aquellas propiedades relacionadas con la actividad química de los elementos y que varían de forma
3.- Calcular y compar ar las densidades at ómicas lineales de las dir ecciones : [1,0,0], [1,1,0] y [1,1,1] en la red FCC y en la red BCC.
![3.- Calcular y compar ar las densidades at ómicas lineales de las dir ecciones : [1,0,0], [1,1,0] y [1,1,1] en la red FCC y en la red BCC. 3.- Calcular y compar ar las densidades at ómicas lineales de las dir ecciones : [1,0,0], [1,1,0] y [1,1,1] en la red FCC y en la red BCC.](/thumbs/58/41894864.jpg) GEOMETRÍA CRISTALINA: 1.- Determinar los índices de Miller de una cara del cubo. 2.- Repr esent ar en el espacio del sist ema cúbico, los planos cuyos índices de Miller son (1,0,3), (1,1,1) y (1,0,1) y
GEOMETRÍA CRISTALINA: 1.- Determinar los índices de Miller de una cara del cubo. 2.- Repr esent ar en el espacio del sist ema cúbico, los planos cuyos índices de Miller son (1,0,3), (1,1,1) y (1,0,1) y
QUÍMICA FUNDAMENTAL. Tabla Periódica
 QUÍMICA FUNDAMENTAL Tabla Periódica 1 TEMAS DE ESTUDIO Construcción de la Tabla Periódica con base en la configuración electrónica Propiedades periódicas de los elementos 2 ANTECEDENTES HISTÓRICOS: ELEMENTOS
QUÍMICA FUNDAMENTAL Tabla Periódica 1 TEMAS DE ESTUDIO Construcción de la Tabla Periódica con base en la configuración electrónica Propiedades periódicas de los elementos 2 ANTECEDENTES HISTÓRICOS: ELEMENTOS
Colección de ejercicios UNIDAD 2
 Facultad de Química, UNAM Curso: Química General I Colección de ejercicios UNIDAD 2 1. Describe cuál fue la contribución al conocimiento de la estructura atómica hecha por cada uno de los siguientes científicos:
Facultad de Química, UNAM Curso: Química General I Colección de ejercicios UNIDAD 2 1. Describe cuál fue la contribución al conocimiento de la estructura atómica hecha por cada uno de los siguientes científicos:
Tema 2: Estructura de la Materia.
 Tema 2: Estructura de la Materia. 1. Microestuctura de los materiales. 2. Escalas de observación: tecnológica, microestructural y atómica. 3. Enlaces interatómicos primarios y secundarios. 4. Microestructuras
Tema 2: Estructura de la Materia. 1. Microestuctura de los materiales. 2. Escalas de observación: tecnológica, microestructural y atómica. 3. Enlaces interatómicos primarios y secundarios. 4. Microestructuras
Reacción y Ecuación Química. SEMANA 04 Licda. Lilian Judith Guzmán Melgar
 Reacción y Ecuación Química SEMANA 04 Licda. Lilian Judith Guzmán Melgar REACCION QUIMICA Proceso mediante el cual tiene lugar un cambio químico. Cambio químico: Cambio durante el cual la sustancia original
Reacción y Ecuación Química SEMANA 04 Licda. Lilian Judith Guzmán Melgar REACCION QUIMICA Proceso mediante el cual tiene lugar un cambio químico. Cambio químico: Cambio durante el cual la sustancia original
ESTRUCTURA ATÓMICA DE LA MATERIA. SISTEMA PERIÓDICO ESTRUCTURA ATÓMICA DE LA MATERIA
 ESTRUCTURA ATÓMICA DE LA MATERIA. SISTEMA PERIÓDICO ESTRUCTURA ATÓMICA DE LA MATERIA La teoría atómica de Dalton se mantuvo con éxito durante casi un siglo pero tuvo que ser abandonada a partir del descubrimiento
ESTRUCTURA ATÓMICA DE LA MATERIA. SISTEMA PERIÓDICO ESTRUCTURA ATÓMICA DE LA MATERIA La teoría atómica de Dalton se mantuvo con éxito durante casi un siglo pero tuvo que ser abandonada a partir del descubrimiento
I.E.S. Al-Ándalus. Dpto. Física y Química. 1º Bachillerato. Tema 3. Enlace Químico - 1 -
 I.E.S. Al-Ándalu. Dto. íica y Química. 1º Bachillerato. Tema 3. Enlace Químico - 1 - ALGUS EJEMPLS DE ELACES IÓIC Y CVALETE., Tenemo un enlace entre do elemento de electronegatividade muy diferente. El
I.E.S. Al-Ándalu. Dto. íica y Química. 1º Bachillerato. Tema 3. Enlace Químico - 1 - ALGUS EJEMPLS DE ELACES IÓIC Y CVALETE., Tenemo un enlace entre do elemento de electronegatividade muy diferente. El
Unidad II Química I PERIODICIDAD QUÍMICA Y TABLA PERIÓDICA
 Unidad II Química I PERIODICIDAD QUÍMICA Y TABLA PERIÓDICA Gloria Angélica Fuentes Zenteno 1 Índice 2.3.1 Antecedentes 2.3.2 Componentes de la Tabla Periódica Nombre Símbolo Número y Masa atómica Estructura
Unidad II Química I PERIODICIDAD QUÍMICA Y TABLA PERIÓDICA Gloria Angélica Fuentes Zenteno 1 Índice 2.3.1 Antecedentes 2.3.2 Componentes de la Tabla Periódica Nombre Símbolo Número y Masa atómica Estructura
PROPIEDADES PERIÓDICAS DE LOS ELEMENTOS - (2015)
 PROPIEDADES PERIÓDICAS DE LOS ELEMENTOS - (2015) Serie A - RADIOS ATOMICOS, VOLUMENES ATÓMICOS, PROPIEDADES GENERALES Serie B - ENERGÍA DE IONIZACIÓN, AFINIDAD ELECTRÓNICA y ELECTRONEGATIVIDAD: Serie A:
PROPIEDADES PERIÓDICAS DE LOS ELEMENTOS - (2015) Serie A - RADIOS ATOMICOS, VOLUMENES ATÓMICOS, PROPIEDADES GENERALES Serie B - ENERGÍA DE IONIZACIÓN, AFINIDAD ELECTRÓNICA y ELECTRONEGATIVIDAD: Serie A:
Química Inorgánica Bloque d 1. BLOQUE d
 Química Inorgánica Bloque d 1 BLOQUE d Los elementos del bloque d están ubicados entre los grupos 2 y 13 de la tabla periódica y se los suele llamar metales de transición. elemento de transición: es un
Química Inorgánica Bloque d 1 BLOQUE d Los elementos del bloque d están ubicados entre los grupos 2 y 13 de la tabla periódica y se los suele llamar metales de transición. elemento de transición: es un
ELECTROQUÍMICA. 1. Procesos electroquímicos (pila). 2. Potenciales normales de electrodo. 3. Ecuación de Nernst. 4. Electrolisis. 5. Leyes de Faraday.
 ELECTROQUÍMICA 1. Procesos electroquímicos (pila). 2. Potenciales normales de electrodo. 3. Ecuación de Nernst. 4. Electrolisis. 5. Leyes de Faraday. Química 2º bachillerato Electroquímica 1 0. CONOCIMIENTOS
ELECTROQUÍMICA 1. Procesos electroquímicos (pila). 2. Potenciales normales de electrodo. 3. Ecuación de Nernst. 4. Electrolisis. 5. Leyes de Faraday. Química 2º bachillerato Electroquímica 1 0. CONOCIMIENTOS
METALES. 1.- Materiales CRISTALINOS y la deformación plástica
 METALES 1.- Materiales CRISTALINOS y la deformación plástica esfuerzo El ensayo de tracción s = F/A 0 s f, resistencia a la fluencia s T, resistencia a la tracción s T, resistencia a la ruptura s= Ke n
METALES 1.- Materiales CRISTALINOS y la deformación plástica esfuerzo El ensayo de tracción s = F/A 0 s f, resistencia a la fluencia s T, resistencia a la tracción s T, resistencia a la ruptura s= Ke n
EJERCICIOS PROPUESTOS EN PRUEBAS PAU DE ASTURIAS
 Modelo 010 1.- A) La tabla adjunta muestra las temperaturas de ebullición de algunos hidrocarburos y alcoholes. Explicar de forma razonada los valores anormalmente elevados de las temperaturas de ebullición
Modelo 010 1.- A) La tabla adjunta muestra las temperaturas de ebullición de algunos hidrocarburos y alcoholes. Explicar de forma razonada los valores anormalmente elevados de las temperaturas de ebullición
ENLACE QUÍMICO Y ESTRUCTURA DE LA MATERIA
 PROBLEMAS DE LA ASIGNATURA: ENLACE QUÍMICO Y ESTRUCTURA DE LA MATERIA ÁREA DE QUÍMICA INORGÁNICA 1º CURSO. LICENCIATURA EN CIENCIAS QUÍMICAS CURSO 2006/2007 PROFESOR RESPONSABLE: - Dr. Luis Sánchez Granados
PROBLEMAS DE LA ASIGNATURA: ENLACE QUÍMICO Y ESTRUCTURA DE LA MATERIA ÁREA DE QUÍMICA INORGÁNICA 1º CURSO. LICENCIATURA EN CIENCIAS QUÍMICAS CURSO 2006/2007 PROFESOR RESPONSABLE: - Dr. Luis Sánchez Granados
Enlaces y Propiedades de Cristales con esos Enlaces
 Enlaces y Propiedades de Cristales con esos Enlaces Enlaces Enlaces Primarios, participan directamente los electrones de valencia. El rol de estos electrones (ser cedidos, compartidos o captados) depende
Enlaces y Propiedades de Cristales con esos Enlaces Enlaces Enlaces Primarios, participan directamente los electrones de valencia. El rol de estos electrones (ser cedidos, compartidos o captados) depende
LECCIÓN Nº 03 TABLA PERIÓDICA
 LECCIÓN Nº 03 TABLA PERIÓDICA OBJETIVO ESPECÍFICO: Conocer las características estructurales y propiedades de las partículas subatómicas(electrón, protón y neutrón), modelos Reconocer Número atómico y
LECCIÓN Nº 03 TABLA PERIÓDICA OBJETIVO ESPECÍFICO: Conocer las características estructurales y propiedades de las partículas subatómicas(electrón, protón y neutrón), modelos Reconocer Número atómico y
Bloque II: Silicatos BLOQUE III: CERAMICAS TRADICIONALES SILICATOS. Bibliografía Química Inorgánica, Enrique Gutierrez Rios
 BLOQUE III: CERAMICAS TRADICIONALES SILICATOS Bibliografía Química Inorgánica, Enrique Gutierrez Rios 1 Características generales Estructuras tridimensionales: XRD Эn sólo Estado Sólido Aplicación industriales
BLOQUE III: CERAMICAS TRADICIONALES SILICATOS Bibliografía Química Inorgánica, Enrique Gutierrez Rios 1 Características generales Estructuras tridimensionales: XRD Эn sólo Estado Sólido Aplicación industriales
Elementos y compuestos químicos
 5 Elementos y compuestos químicos PARA EMPEZAR Esquema de contenidos Los elementos químicos Clasificación de los elementos La tabla periódica Bioelementos Oligoelementos Agrupación de elementos Moléculas
5 Elementos y compuestos químicos PARA EMPEZAR Esquema de contenidos Los elementos químicos Clasificación de los elementos La tabla periódica Bioelementos Oligoelementos Agrupación de elementos Moléculas
Las que tienen relación con el de tamaño: LAS PROPIEDADES PERIÓDICAS. Se pueden separar en dos grupos: PERIODICIDAD
 LAS PROPIEDADES PERIÓDICAS Se pueden separar en dos grupos: 1- Las que tienen relación con el de tamaño: Los radios atómicos y los radios iónicos o cristalinos. La densidad. (ρ) El punto de fusión y ebullición.
LAS PROPIEDADES PERIÓDICAS Se pueden separar en dos grupos: 1- Las que tienen relación con el de tamaño: Los radios atómicos y los radios iónicos o cristalinos. La densidad. (ρ) El punto de fusión y ebullición.
LA TABLA PERIÓDICA. Cuestiones generales. Propiedades periódicas
 Cuestiones generales. LA TABLA PERIÓDICA. 1.- Indica el nombre, símbolo, nombre del grupo a que pertenece y periodo de los elementos de números atómicos 3, 9, 16, 19, 38 y 51. 2.- a) Indica el nombre,
Cuestiones generales. LA TABLA PERIÓDICA. 1.- Indica el nombre, símbolo, nombre del grupo a que pertenece y periodo de los elementos de números atómicos 3, 9, 16, 19, 38 y 51. 2.- a) Indica el nombre,
SOLUCIONARIO Guía Técnico Profesional
 SOLUCIONARIO Guía Técnico Profesional Teoría atómica III: tabla periódica y propiedades periódicas SGUICTC003TC33-A16V1 Ítem Alternativa Habilidad 1 D Reconocimiento 2 E Reconocimiento 3 B Reconocimiento
SOLUCIONARIO Guía Técnico Profesional Teoría atómica III: tabla periódica y propiedades periódicas SGUICTC003TC33-A16V1 Ítem Alternativa Habilidad 1 D Reconocimiento 2 E Reconocimiento 3 B Reconocimiento
Capítulo 2 La estructura de los sólidos cristalinos
 Capítulo 2 La estructura de los sólidos cristalinos TEMA 2: La estructura de los sólidos cristalinos 1. Los enlaces interatómicos 2. La estructura cristalina 3. Estructuras de empaquetamiento compacto
Capítulo 2 La estructura de los sólidos cristalinos TEMA 2: La estructura de los sólidos cristalinos 1. Los enlaces interatómicos 2. La estructura cristalina 3. Estructuras de empaquetamiento compacto
